Соединения и композиции в качестве ингибиторов с-kit киназы
Номер патента: 24293
Опубликовано: 30.09.2016
Авторы: Лю Сяодон, Набакка Джульет, Мольтени Валентина, Петрасси Ханк Майкл Джеймс, Ех Винс, Ли Сяолинь, Нгуйен Бао, Лорен Джон
Формула / Реферат
1. Соединение формулы (Ia) или формулы (IIa) или его фармацевтически приемлемая соль
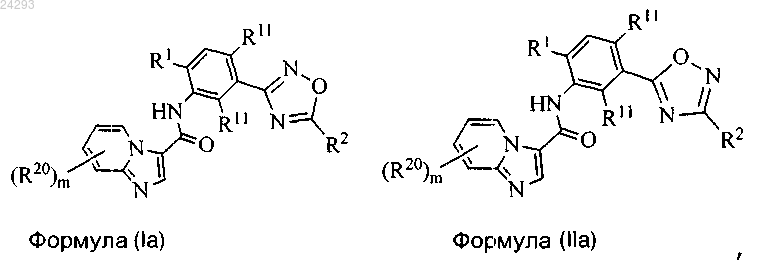
где m=1 и R20 выбран из Н, галогена, С1-С6алкила, С1-С6галогеналкила, С1-С6галогеналкокси, дейтерия, дейтерированного C1-С6алкила, -CN, -(CR92)nOR4, -C(O)R4, R10, -(CR92)nR10, -((CR92)nO)tR4, -(CR92)nO(CR92)nR7, -(CR92)nC(=O)R4, -C(=O)N(R4)2, -OR4 и -(CR92)nCN;
или m=4 и R20 обозначает дейтерий;
R1 выбран из С1-С6алкила и галогена;
каждый R11 независимо выбран из Н, галогена и С1-С6алкила;
L2 обозначает -(CR92)n-, -CHR6-, -(CR92)nO-, -NH-, -(CR92)nC(=O)-, -C(=O)O(CR92)n-, -(CR92)nOC(=O))NR4-, -(CR92)nNR4C(=O)(CR92)n-, -(CR92)nNR4C(=O)- или -(CR92)nNR4C(=O)О-;
R2 обозначает R3 или L2R3;
R3 выбран из незамещенного С3-С8циклоалкила, циклобутанона, циклопентанона и замещенного С3-С8циклоалкила,
причем замещенный С3-С8циклоалкил R3 замещен 1-4 заместителями, независимо выбранными из С1-С6алкила, галогена, С1-С6галогеналкила, -OR4, -CN, -C(=O)OR4, -C(=O)R4, -C(=O)R7, -C(=O)OR5, -(CR92)nOR4, -C(=O)O(CR92)nOR4, -N(R4)2, =N-OR4, =N-O-(CR92)nR5, -C(=O)NR42, -NR4C(=O)OR4, -NR4C(=O)(CR92)nOR4, -NR4(CR92)nOR4, -NR4S(=O)2R4, -N(C(=O)OR4)2, =CH2, =CH(CR92)nOR4, R8, -(CR92)nR8, дейтерированного С1-С6алкокси, -S(=O)2R4, -S(=O)2R7, -S(=O)2R8, -S(=O)2N(R4)2, -S(=O)2NHC(=O)OR4, -S(=O)2(CR92)nC(=O)OR4, -S(=O)2(CR92)nOR4, спиро-присоединенного диоксолана, спиро-присоединенного диоксолана, который замещен С1-С6алкилом, спиро-присоединенного диоксана, спиро-присоединенного тетрагидрофуранила, спиро-присоединенного оксетана, спиро-присоединенного циклобутанона, спиро-присоединенного циклобутанола, незамещенного 5-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О и S, 5-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О и S, замещенного 1-3 заместителями, независимо выбранными из С1-С6алкила, галогена, С1-С6галогеналкила, С1-С6галогеналкокси, -OR4 и R8;
каждый R4 независимо выбран из Н и С1-С6алкила;
R5 обозначает незамещенный С3-С8циклоалкил, незамещенный 5-6-членный гетероциклоалкил с 1-2 гетероатомами, независимо выбранными из N или О, или С3-С8циклоалкил, замещенный 1-3 заместителями, независимо выбранными из С1-С6алкила;
каждый R6 независимо выбран из -NHC(O)OR4, -OR4 и -(CR92)nOR4;
каждый R7 независимо выбран из С1-С6галогеналкила;
R8 выбран из незамещенного фенила, незамещенного 5-6-членного гетероарила с 1-3 гетероатомами, независимо выбранными из N, О или S, тетразолила, незамещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, незамещенного С3-С8циклоалкила, замещенного 5-6-членного гетероарила с 1-3 гетероатомами, независимо выбранными из N, О или S, замещенного фенила, замещенного 5-членного гетероарила с 1-4 гетероатомами, выбранными из N, замещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, замещенного С3-С8циклоалкила, оксазолидин-2-она, пирролидинона и пирролидин-2-она,
причем замещенный фенил, замещенный 5-6-членный гетероарил с 1-3 гетероатомами, независимо выбранными из N, О или S, замещенный 5-членный гетероарил с 1-4 гетероатомами, выбранными из N, замещенный С3-С8циклоалкил и замещенный 4-6-членный гетероциклоалкил R8 замещены 1-3 заместителями, независимо выбранными из С1-С6алкила, -(С(R9)2)nOR4, -(С(R9)2)nR5, -(C(R9)2)nC(O)OR4, -C(O)OR4 и -S(O)2R4;
каждый R9 независимо выбран из Н и С1-С6алкила;
R10 выбран из незамещенного фенила, незамещенного 5-6-членного гетероарила с 1-2 гетероатомами, независимо выбранными из N, О или S, незамещенного триазолила, незамещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, незамещенного С3-С8циклоалкила, замещенного 5-6-членного гетероарила с 1-2 гетероатомами, независимо выбранными из N, О или S, замещенного фенила, замещенного триазолила, замещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, замещенного С3-С8циклоалкила, оксазолидин-2-она, пирролидинона и пирролидин-2-она,
причем замещенный фенил, замещенный 5-6-членный гетероарил с 1-2 гетероатомами, независимо выбранными из N, О или S, замещенный 5-членный гетероарил с 1-4 гетероатомами, выбранными из N, замещенный С3-С8циклоалкил и замещенный 4-6-членный гетероциклоалкил R10 замещены 1-3 заместителями, независимо выбранными из С1-С6алкила, -(С(R9)2)nOR4, -(С(R9)2)nR5, -(C(R9)2)nC(O)OR4 и -S(O)2R4;
t=1, 2 или 3, и
каждый n независимо выбран из 1, 2, 3 и 4.
2. Соединение по п.1, в котором R1 выбран из -СН3 и F.
3. Соединение по любому из пп.1-2, в котором R1 обозначает -СН3.
4. Соединение по любому из пп.1-3, в котором каждый R11 независимо выбран из Н, F и -СН3.
5. Соединение по любому из пп.1-4, в котором каждый R11 обозначает Н.
6. Соединение по любому из пп.1-5, в котором R3 выбран из незамещенного С3-С8циклоалкила, циклобутанона, циклопентанона и замещенного С3-С8циклоалкила,
причем замещенный С3-С8циклоалкил R3 замещен 1-4 заместителями, независимо выбранными из С1-С6алкила, галогена, С1-С6галогеналкила, -OR4, -(CR92)nOR4, -N(R4)2, =N-OR4, =N-O-(CR92)nR5, -NR4C(=O)OR4, -NR4C(=O)(CR92)nOR4, -NR4(CR92)nOR4, -NR4S(=O)2R4, -N(C(=O)OR4)2, =CH2, =CH(CR92)nOR4, R8, дейтерированного С1-С6алкокси, спиро-присоединенного диоксолана, спиро-присоединенного диоксолана, который замещен С1-С6алкилом, спиро-присоединенного диоксана, спиро-присоединенного тетрагидрофуранила, спиро-присоединенного циклобутанона, спиро-присоединенного циклобутанола, незамещенного 5-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N и О, и 5-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N и О, замещенного 1-3 заместителями, независимо выбранными из С1-С6алкила.
7. Соединение по любому из пп.1-6, в котором каждый R4 независимо выбран из Н, метила, этила, пропила, бутила, изопропила и трет-бутила.
8. Соединение по любому из пп.1-7, в котором R5 независимо выбран из циклопропила или морфолинила.
9. Соединение по любому из пп.1-8, в котором каждый R7 независимо выбран из CH2F, -CHF2, -CH2CHF2, -CH2CF3 и -CF3.
10. Соединение по любому из пп.1-9, в котором каждый R9 независимо выбран из Н, метила и этила.
11. Соединение по любому из пп.1-10, в котором R8 выбран из незамещенного С3-С8циклоалкила и незамещенного 5-членного гетероарила с 1-4 гетероатомами, выбранными из N.
12. Соединение по любому из пп.1-11, в котором
R3 выбран из циклопропила, циклобутила, циклопентила и циклогексила, каждый из которых незамещен или каждый из которых замещен 1-4 заместителями, независимо выбранными из -F, -СН3, -СН2СН3, -CF3, -ОН, -OCH3, -СН2ОСН3, -NH2, -N(CH3)2, =N-OCH3, =N-OCH2CH3, =N-OCH(CH3)2, =N-OH, =N-O-CH2R5, =N-O-CH2CH2R5, -NHC(=O)OC(CH3)3, -NHC(=O)OCH3, -NHC(=O)CH2OCH3, -NHCH2CH2OCH3, -NHCH2CH2OH, -NHS(=O)2CH3, -N(C(=O)OCH3)2, =CH2, =CHCH2CH2OH, -OCD3, циклопропила, триазолила, пиразолила, спиро-присоединенного диоксолана, спиро-присоединенного диоксолана, который замещен -CH3, спиро-присоединенного диоксана, спиро-присоединенного тетрагидрофуранила, спиро-присоединенного циклобутанона, спиро-присоединенного циклобутанола, пиперидинила и пилеразинила, замещенного -СН3,
или R3 обозначает циклобутанон или циклопентанон.
13. Соединение по любому из пп.1-12, в котором R3 обозначает циклопропил, замещенный 1 или 2 F, или R3 обозначает циклобутил, замещенный 2 F.
14. Соединение по любому из пп.1-13, в котором m=1 и R20 выбран из Н, галогена, С1-С6алкила, С1-С6галогеналкила, C1-С6галогеналкокси, дейтерированного С1-С6алкила, -CN, -(CR92)nOR4, R10, -(CR92)nR10, -((CR92)nO)tR4, -(CR92)nO(CR92)nR7, -(CR92)nC(=O)R4 и -C(=O)N(R4)2.
15. Соединение по любому из пп.1-14, в котором m=1 и R20 выбран из Н, -F, -СН3, -CF3, -CD3, -CN, -OCHF2, -C(CH3)OH, -CH2OCH2CH2OH, -CH2OCH2CF3, -C(=O)NH2, -CH2CH2C(CH3)2OH, -СН2ОСН2СН2ОСН3, -CH2OCH2CH2F, -СН2СН2С(=O)СН3, -CH2OH и -СН2СН3.
16. Соединение по любому из пп.1-15, в котором m=1 и R20 обозначает -СН3.
17. Соединение по любому из пп.1-16, в котором m=1 и R20 обозначает Н.
18. Соединение по любому из пп.1-17, в котором
R10 выбран из морфолинила, пиперидинила, пиперидин-1-ила, пиперидин-2-ила, пиперидин-3-ила, пиперидин-4-ила, пиперазинила, пиперазин-1-ила, пиразолила, пиразол-1-ила, пиразол-3-ила, пиразол-4-ила, триазолила, 1Н-1,2,3-триазол-4-ила, 4Н-1,2,4-триазол-3-ила, 1Н-1,2,4-триазол-5-ила, тиазолила, тиазол-4-ила, тиазол-5-ила, имидазолила, имидазол-1-ила, имидазол-2-ила, каждый из которых незамещен или каждый из которых замещен 1-3 заместителями, независимо выбранными из С1-С6алкила, -(CR92)nOR4, -(C(R9)2)nC(O)OR4, -(C(R9)2)nR5 и -S(=O)2R4,
или R10 выбран из оксазолидин-2-она и пирролидин-2-она.
19. Соединение по любому из пп.1-18, в котором
R10 выбран из морфолинила, пиперидинила, пиперидин-1-ила, пиперидин-2-ила, пиперидин-3-ила, пиперидин-4-ила, пиперазинила, пиперазин-1-ила, пиразолила, пиразол-1-ила, пиразол-3-ила, пиразол-4-ила, триазолила, 1Н-1,2,3-триазол-4-ила, 4Н-1,2,4-триазол-3-ила, 1Н-1,2,4-триазол-5-ила, тиазолила, тиазол-4-ила, тиазол-5-ила, имидазолила, имидазол-1-ила, имидазол-2-ила, каждый из которых незамещен или каждый из которых замещен 1-3 заместителями, независимо выбранными из -СН3, -СН2СН2ОН, -СН2С(O)ОН, -СН2СН2ОН, -СН2С(СН3)2ОН, -S(O)2CH3 и -CH2CH2-R5.
20. Соединение по любому из пп.1-13, в котором m=4 и R20 обозначает дейтерий.
21. Соединение по п.1, выбранное из
N-{5-[3-(3,3-дифторциклобутил)-1,2,4-оксадиазол-5-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{2-метил-5-[5-(3-оксоциклопентил)-1,2,4-оксадиазол-3-ил]фенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-гидрокси-3-метилциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[3-(гидроксиимино)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(4,4-дифторциклогексил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-гидрокси-3-метилциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[3-(метоксиимино)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-{5,8-диоксаспиро[3.4]октан-2-ил}-1,2,4-оксадиазол-3-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-(2-метил-5-{5-[(6R)-6-метил-5,8-диоксаспиро[3.4]октан-2-ил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-{5,9-диоксаспиро[3.5]нонан-2-ил}-1,2,4-оксадиазол-3-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{2-метил-5-[5-(3-оксоциклобутил)-1,2,4-оксадиазол-3-ил]фенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(2-метил-5-{5-[(6S)-6-метил-5,8-диоксаспиро[3.4]октан-2-ил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[3-(этоксиимино)циклобутил]-1,2,4-оксадиазол-3-ил}2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-{3-[(циклопропилметокси)имино]циклобутил}-1,2,4-оксадиазол-3-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-[2-метил-5-(5-{3-[(пропан-2-илокси)имино]циклобутил}-1,2,4-оксадиазол-3-ил)фенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-аминоциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-метоксициклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[1-(метоксиметил)циклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{1-[3-(3-{имидазо[1,2-а]пиридин-3-амидо}-4-метилфенил)-1,2,4-оксадиазол-5-ил]циклопропил}трет-бутилкарбамата;
N-{5-[5-(1-метансульфонамидоциклопропил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{1-[3-(3-{имидазо[1,2-а]пиридин-3-амидо}-4-метилфенил)-1,2,4-оксадиазол-5-ил]циклопропил}-N-(метоксикарбонил)метилкарбамата;
N-{1-[3-(3-{имидазо[1,2-а]пиридин-3-амидо}-4-метилфенил)-1,2,4-оксадиазол-5-ил]циклопропил}метилкарбамата;
N-(5-{5-[3-гидрокси-3-(трифторметил)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{[3-(3-{имидазо[1,2-а]пиридин-3-амидо}-4-метилфенил)-1,2,4-оксадиазол-5-ил]метил}-1-метилциклопропилкарбамата;
N-{1-[3-(3-{имидазо[1,2-а]пиридин-3-амидо}-4-метилфенил)-1,2,4-оксадиазол-5-ил]циклобутил}метилкарбамата;
N-{5-[5-(1-метансульфонамидоциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[1-(диметиламино)циклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{2-метил-5-[5-(3-метилиденциклобутил)-1,2,4-оксадиазол-3-ил]фенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-циклопропил-3-гидроксициклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[3-(3-гидроксипропилиден)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-[2-метил-5-(5-{5-оксаспиро[3.4]октан-2-ил}-1,2,4-оксадиазол-3-ил)фенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-(2-метил-5-{5-[(2,2,3,3-тетрафторциклобутокси)метил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-фторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(гидроксиметил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(2-гидроксиэтокси)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(метоксиметил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(1Н-пиразол-4-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[1-(2-гидроксиэтил)-1Н-пиразол-4-ил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(1-метил-1Н-пиразол-4-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(1-метил-1Н-пиразол-3-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[1-(2-гидрокси-2-метилпропил)-1Н-пиразол-4-ил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-(2-метил-5-{5-[3-(1Н-пиразол-1-ил)циклобутил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(1,3-тиазол-4-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-фторфенил}-6-(1-метил-1Н-пиразол-4-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-фторфенил}-6-[1-(2-гидрокси-2-метилпропил)-1Н-пиразол-4-ил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-(1-метансульфонилпиперидин-4-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-{1-[2-(морфолин-4-ил)этил]-1Н-пиразол-4-ил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-фторфенил}-6-{1-[2-(морфолин-4-ил)этил]-1Н-пиразол-4-ил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(2,2,2-трифторэтокси)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(3-оксобутил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(3-гидрокси-3-метилбутил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[2-(1-гидроксициклопропил)этил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[2-(морфолин-4-ил)этил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-циклобутил-1,2,4-оксадиазол-3-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-диметилциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-(морфолин-4-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
6-циано-N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-фторфенил}-6-(5-метил-4Н-1,2,4-триазол-3-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
3-N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3,6-дикарбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[2-(4-метилпиперазин-1-ил)этил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(2,2-дифторциклопропил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-(1Н-1,2,3-триазол-4-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-[1-(2-гидроксиэтил)-1Н-1,2,3-триазол-4-ил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2,4-диметилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-ме:тилфенил}-7-(2-оксо-1,3-оксазолидин-3-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-метилимидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-мэтилимидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-фторимидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-фторимидазо[1,2-а]пиридин-3-карбоксамида;
7-циано-N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-циклопентил-1,2,4-оксадиазол-3-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-[2-метил-5-(5-{6-оксоспиро[3.3]гептан-2-ил}-1,2,4-оксадиазол-3-ил)фенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-(2-оксопирролидин-1-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(2,2-дифторэтокси)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-этилциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(5-метил-4Н-1,2,4-триазол-3-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-метилимидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(морфолин-4-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(1Н-имидазол-1-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(2-фторэтокси)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[3-(метоксиметил)-1Н-1,2,4-триазол-5-ил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(2,2-дифторциклопропил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(2,2,2-трифторэтокси)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-циклобутил-1,2,4-оксадиазол-3-ил)-2-метилфенил]-6-[(2,2,2-трифторэтокси)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1R)-2,2-дифторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1S)-2,2-дифторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[3-гидрокси-3-(трифторметил)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)-7-метилимидазо[1,2-а]пиридин-3-карбоксамида;
6-фтор-N-(5-{5-[3-гидрокси-3-(трифторметил)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1R,2S)-2-фторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-5,6,7,8-тетрадейтероимидазо[1,2-а]пиридин-3-карбоксамида;
7-фтор-N-(5-{5-[3-гидрокси-3-(трифторметил)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(4-метил-1Н-имидазол-1-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(2R,6S)-2,6-диметилморфолин-4-ил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[3-метокси-3-(трифторметил)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
6-фтор-N-(5-{5-[1-(метоксиметил)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[1-(2-метоксиэтил)-5-метил-1Н-1,2,4-триазол-3-ил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-{6-гидроксиспиро[3.3]гептан-2-ил}-1,2,4-оксадиазол-3-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1S,2S)-2-фторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
7-метил-N-(2-метил-5-{5-[(2,2,3,3-тетрафторциклобутокси)метил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
6-метил-N-(2-метил-5-{5-[(2,2,3,3-тетрафторциклобутокси)метил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-циклопропил-1,2,4-оксадиазол-3-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(циклопропилметил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1R,2S)-2-фторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)-7-метилимидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1S,2R)-2-фторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)-7-метилимидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1R)-2,2-дифторциклопропил]-1,2,4-оксадиазол-3-ил}-2,4-диметилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1S)-2,2-дифторциклопропил]-1,2,4-оксадиазол-3-ил}-2,4-диметилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1R,2S)-2-фторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-фторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-метилимидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-фторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-метилимидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1S,2R)-2-фторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{3,3-дифтор-1-[3-(3-{имидазо[1,2-а]пиридин-3-амидо}-4-метилфенил)-1,2,4-оксадиазол-5-ил]циклобутил}метилкарбамата;
N-{3,3-дифтор-1-[3-(4-метил-3-{7-метилимидазо[1,2-а]пиридин-3-амидо}фенил)-1,2,4-оксадиазол-5-ил]циклобутил}метилкарбамата;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(2-фторэтокси)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(3-циклопропил-1,2,4-оксадиазол-5-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,3,4-оксадиазол-2-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-гидрокси-3-метилциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(3Z)-3-(метоксиимино)циклопентил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(3Z)-3-(гидроксиимино)циклопентил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(2-метил-5-{5-[1-(трифторметил)циклопропил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-гидрокси-3-метилциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{2-метил-5-[5-(3-оксоциклобутил)-1,2,4-оксадиазол-3-ил]фенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-гидроксициклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(2-метил-5-{5-[3-(пиперидин-1-ил)циклобутил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(2-метил-5-{5-[3-(морфолин-4-ил)циклобутил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(2-метил-5-{5-[3-(4-метилпиперазин-1-ил)циклобутил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{2-метил-5-[5-(3-{[2-(морфолин-4-ил)этокси]имино}циклобутил)-1,2,4-оксадиазол-3-ил]фенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{3-[3-(3-{имидазо[1,2-а]пиридин-3-амидо}-4-метилфенил)-1,2,4-оксадиазол-5-ил]циклобутил}трет-бутилкарбамат;
N-{5-[5-(3-аминоциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3-метансульфонамидоциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
1-метилциклопропил N-{2-[3-(3-{имидазо[1,2-а]пиридин-3-амидо}-4-метилфенил)-1,2,4-оксадиазол-5-ил]этил}карбамата;
N-{5-[5-(1-аминоциклопропил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[1-(2-метоксиацетамидо)циклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-{3-[(2-метоксиэтил)амино]циклобутил}-1,2,4-оксадиазол-3-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-фторфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[3-метокси-3-(трифторметил)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)-N-метилимидазо[1,2-а]пиридин-3-карбоксамида;
N-{1-[3-(3-{имидазо[1,2-а]пиридин-3-амидо}-4-метилфенил)-1,2,4-оксадиазол-5-ил]циклобутил}трет-бутилкарбамат;
N-{5-[5-(1-аминоциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{2-фтор-5-[5-(3-метилиденциклобутил)-1,2,4-оксадиазол-3-ил]фенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[1-(гидроксиметил)циклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-{[(2,2-дифторциклопропил)формамидо]метил}-1,2,4-оксадиазол-3-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
1-метилциклопропил N-[(3-{4-метил-3-[7-(трифторметил)имидазо[1,2-а]пиридин-3-амидо]фенил}-1,2,4-оксадиазол-5-ил)метил]карбамата;
метил N-{3-[3-(3-{имидазо[1,2-а]пиридин-3-амидо}-4-метилфенил)-1,2,4-оксадиазол-5-ил]циклобутил}карбамата;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(4-метилпиперазин-1-ил)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-{[4-(2-гидроксиэтил)пиперазин-1-ил]метил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(2-метоксиэтокси)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
2-{4-[3-({5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}карбамоил)имидазо[1,2-а]пиридин-6-ил]-1Н-пиразол-1-ил}уксусной кислоты;
N-{5-[5-(1-гидроксициклопропил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-(дифторметокси)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(2-метил-5-{5-[3-(1Н-1,2,4-триазол-1-ил)циклобутил]-1,2,4-оксадиазол-3-ил}фенил)имидазо[1,2-а]пиридин-3-карбоксамида;
6-фтор-N-{5-[5-(3-гидроксициклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-циклобутил-1,2,4-оксадиазол-3-ил)-2-фторфенил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(2-гидрокси-2-метилпропил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(2-оксо-1,3-оксазолидин-3-ил)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-(2-гидрокси-2-метилпропил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-диметилциклобутил)-1,2,4-оксадиазол-3-ил]-2-фторфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-фторфенил}-6-(5-метил-4Н-1,2,4-триазол-3-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
6-фтор-N-{5-[5-(3-гидрокси-3-метилциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(2-гидроксициклопропил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{3-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2,6-диметилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
7-циано-N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(1-гидроксиэтил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-(5-метил-1Н-имидазол-1-ил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-[(2-метоксиэтокси)метил]имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1S)-2,2-дифторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)-7-метилимидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(1-фторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(1-гидроксициклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-{5-[5-(1-карбамоилциклопропил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-6-фторимидазо[1,2-а]пиридин-3-карбоксамида и
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}-7-(пиперидин-4-ил)имидазо[1,2-а]пиридин-3-карбоксамида.
22. Соединение по п.1, выбранное из
N-{5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1R)-2,2-дифторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1S)-2,2-дифторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-(5-{5-[(1S,2R)-2-фторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида и
N-(5-{5-[(1R,2S)-2-фторциклопропил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида.
23. Фармацевтическая композиция, обладающая свойствами ингибитора c-kit киназ, содержащая терапевтически эффективное количество соединения по любому из пп.1-22 и фармацевтически приемлемый носитель.
24. Лекарственное средство для лечения у пациента заболевания, опосредуемого киназой, где лекарственное средство содержит терапевтически эффективное количество соединения по любому из пп.1-22, киназа выбрана из рецептор фактора стволовых клеток (c-kit), α-рецептора к фактору роста, выделенному из тромбоцитов (PDGFRα), и β-рецептора к фактору роста, выделенному из тромбоцитов (PDGFRβ), и заболевание представляет собой заболевание, связанное с тучными клетками, респираторное заболевание, воспалительное нарушение, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), аутоиммунное нарушение, метаболическое нарушение, фиброзное заболевание, дерматологическое заболевание, легочную артериальную гипертензию (РАН) или первичную легочную гипертензию (РРН).
25. Лекарственное средство по п.24, где заболевание представляет собой астму, аллергический ринит, легочную артериальную гипертензию (РАН), легочный фиброз, печеночный фиброз, кардиальный фиброз, склеродермию, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), крапивницу, дерматоз, аллергический дерматит, аллергический контактный дерматит, ревматоидный артрит, множественный склероз, меланому, желудочно-кишечную стромальную опухоль, опухоль тучных клеток, мастоцитоз, анафилактический синдром, болезнь Крона, диабет типа I или диабет типа II.
26. Применение соединения по любому из пп.1-22 для получения лекарственного средства для лечения у пациента заболевания или нарушения, где участвует модуляция киназы, причем киназа выбрана из c-kit, PDGFRα и PDGFRβ.
27. Способ лечения заболевания или нарушения, где участвует модуляция киназы, включающий введение в систему или пациенту, которому требуется такое лечение, эффективного количества соединения по любому из пп.1-22, причем киназа выбрана из с-kit, PDGFRα и PDGFRβ.
28. Способ по п.27, в котором заболевание представляет собой заболевание, связанное с тучными клетками, респираторное заболевание, воспалительное нарушение, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), аутоиммунное нарушение, метаболическое нарушение, фиброзное заболевание, дерматологическое заболевание, легочную артериальную гипертензию (РАН) или первичную легочную гипертензию (РРН).
29. Способ по п.28, в котором заболевание представляет собой астму, аллергический ринит, легочную артериальную гипертензию (РАН), легочный фиброз, печеночный фиброз, кардиальный фиброз, склеродермию, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), крапивницу, дерматоз, аллергический дерматит, аллергический контактный дерматит, ревматоидный артрит, множественный склероз, меланому, желудочно-кишечную стромальную опухоль, опухоль тучных клеток, мастоцитоз, анафилактический синдром, болезнь Крона, диабет типа I или диабет типа II.
30. Способ модуляции активности киназы, включающий введение в систему или пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения по любому из пп.1-22 или его фармацевтически приемлемых солей, причем киназа представляет собой c-kit, PDGFRα и PDGFRβ.
31. Применение соединения по любому из пп.1-22 для лечения заболевания, опосредуемого c-kit, PDGFRα, PDGFRβ или их комбинацией, причем заболевание выбрано из заболевания, связанного с тучными клетками, респираторного заболевания, воспалительного нарушения, синдрома раздраженного кишечника (IBS), воспалительного заболевания кишечника (IBD), аутоиммунного нарушения, метаболического нарушения, фиброзного заболевания, дерматологического заболевания, легочной артериальной гипертензии (РАН) и первичной легочной гипертензии (РРН).
32. Применение по п.31, где заболевание представляет собой астму, аллергический ринит, легочную артериальную гипертензию (РАН), легочный фиброз, печеночный фиброз, кардиальный фиброз, склеродермию, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), крапивницу, дерматоз, диабет типа I или диабет типа II.
33. Соединение, выбранное из
N-(5-{5-[3-(2-метоксиэтокси)циклобутил]-1,2,4-оксадиазол-3-ил}-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамида;
N-[5-(5-{[(3,3-дифторциклобутил)амино]метил}-1,2,4-оксадиазол-3-ил)-2-метилфенил]имидазо[1,2-а]пиридин-3-карбоксамида и
N-{5-[(3,3-дифторциклобутил)карбамоил]-2-метилфенил}имидазо[1,2-а]пиридин-3-карбоксамида.
Текст
Ех Винс, Ли Сяолинь, Лю Сяодон, Лорен Джон, Мольтени Валентина, Набакка Джульет, Нгуйен Бао, Петрасси Ханк Майкл Джеймс (US) Представитель: Медведев В.Н. (RU) Изобретение относится к соединениям формулы (Ia) и (IIa), где значения радикалов определены в формуле изобретения, и их фармацевтическим композициям, которые могут быть использованы в качестве ингибиторов протеинкиназы, а также к способам применения таких соединений для лечения, облегчения или профилактики состояния, связанного с патологической или разрегулированной активностью киназы. В некоторых вариантах осуществления изобретение относится к способам применения таких соединений для лечения, облегчения или профилактики заболеваний или нарушений, которые включают патологическую активацию c-kit или c-kit и Область изобретения Изобретение относится к ингибиторам PDGFR и/или с-kit киназ и к способам использования таких соединений. Уровень техники Протеинкиназы (PK) составляют большую группу структурно родственных фосфорилтрансфераз,имеющих высококонсервативные структуры и каталитические функции. Протеинкиназы являются ферментными компонентами путей трансдукции сигналов, которые катализируют перенос концевого фосфата от АТФ к гидроксильной группе остатков тирозина, серина и/или треонина белков и поэтому распределяются по семействам на основании субстратов, которые они фосфорилируют: ПротеинТирозинКиназы (PTK) и Протеин Серин/Треонин Киназы. Протеинкиназы играют критическую роль в контроле роста и дифференцировки клеток и ответственны за контроль различных клеточных процессов трансдукции сигнала, причем протеинкиназы являются ключевыми медиаторами клеточных сигналов, приводящих к продукции факторов роста и цитокинов. Сверхэкспрессия или патологическая экспрессия нормальных или мутантных протеинкиназ играет значительную роль в развитии многих заболеваний и нарушений, включая нарушения центральной нервной системы, такие как болезнь Альцгеймера, воспалительные нарушения, такие как артрит, заболевания костей, такие как остеопороз, метаболические нарушения, такие как диабет, нарушения пролиферации кровеносных сосудов, такие как ангиогенез, аутоиммунные заболевания, такие как ревматоидный артрит,глазные заболевания, сердечно-сосудистое заболевание, атеросклероз, рак, тромбоз, псориаз, рестеноз,шизофрению, болевые ощущения, отторжение трансплантата и инфекционные болезни, такие как вирусные и грибковые инфекции. Резюме изобретения Изобретение относится к соединениям и к их фармацевтически приемлемым солям, фармацевтически приемлемым сольватам (например, гидратам), N-оксидным производным, защищенным производным, индивидуальным изомерам и смеси изомеров, которые являются ингибиторами с-kit киназы или ингибиторами c-kit и PDGFR (PDGFR и PDGFR) киназы. В одном аспекте изобретение относится к таким соединениям и к их фармацевтически приемлемым солям, фармацевтически приемлемым сольватам (например, гидратам), N-оксидным производным, защищенным производным, индивидуальным изомерам и смеси изомеров, имеющим структуру согласно формуле (Ia) или (IIa)R1 выбран из С 1-С 6 алкила и галогена; каждый R11 независимо выбран из Н, галогена и C1-С 6 алкила;R3 выбран из незамещенного С 3-С 8 циклоалкила, циклобутанона, циклопентанона и замещенного С 3 С 8 циклоалкила,причем замещенный С 3-С 8 циклоалкил R3 замещен 1-4 заместителями, независимо выбранными из С 1-С 6 алкила, галогена, C1-С 6 галогеналкила, -OR4, -CN, -C(=O)OR4, -C(=O)R4, -C(=O)R7, -C(=O)OR5,-(CR92)nOR4, -C(=O)O(CR92)nOR4, -N(R4)2, =N-OR4, =N-O-(CR92)nR5, -C(=O)NR42, -NR4C(=O)OR4,-NR4C(=O)(CR92)nOR4, NR4(CR92)nOR4, -NR4S(=O)2R4, -N(C(=O)OR4)2, =CH2, =CH(CR92)nOR4, R8,-(CR92)nR8, дейтерированного С 1-С 6 алкокси, -S(=O)2R4, -S(=O)2R7, -S(=O)2R8, -S(=O)2N(R4)2,-S(=O)2NHC(=O)OR4, -S(=O)2(CR92)nC(=O)OR4, -S(=O)2(CR92)nOR4, спиро-присоединенного диоксолана,спиро-присоединенного диоксолана, который замещен С 1-С 6 алкилом, спиро-присоединенного диоксана,спиро-присоединенного тетрагидрофуранила, спиро-присоединенного оксетана, спиро-присоединенного циклобутанона, спиро-присоединенного циклобутанола, незамещенного 5-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О и S, 5-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О и S, замещенного 1-3 заместителями, независимо выбранными из С 1-С 6 алкила, галогена, C1-С 6 галогеналкила, С 1-С 6 галогеналкокси, -OR4 и R8;-1 024293 каждый R4 независимо выбран из Н и С 1-С 6 алкила;R5 обозначает незамещенный С 3-С 8 циклоалкил, незамещенный 5-6-членный гетероциклоалкил с 1-2 гетероатомами, независимо выбранными из N или О, или С 3-С 8 циклоалкил, замещенный 1-3 заместителями, независимо выбранными из С 1-С 6 алкила; каждый R6 независимо выбран из -NHC(O)OR4, -OR4 и -(CR92)nOR4; каждый R7 независимо выбран из С 1-С 6 галогеналкила;R8 выбран из незамещенного фенила, незамещенного 5-6-членного гетероарила с 1-3 гетероатомами, независимо выбранными из N, О или S, тетразолила, незамещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, незамещенного С 3-С 8 циклоалкила, замещенного 5-6-членного гетероарила с 1-3 гетероатомами, независимо выбранными из N, О или S, замещенного фенила, замещенного 5-членного гетероарила с 1-4 гетероатомами, выбранными из N, замещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, замещенного С 3-С 8 циклоалкила, оксазолидин-2-она, пирролидинона и пирролидин-2-она,причем замещенный фенил, замещенный 5-6-членный гетероарил с 1-3 гетероатомами, независимо выбранными из N, О или S, замещенный 5-членный гетероарил с 1-4 гетероатомами, выбранными из N,замещенный С 3-С 8 циклоалкил и замещенный 4-6-членный гетероциклоалкил R8 замещены 1-3 заместителями, независимо выбранными из С 1-С 6 алкила, -(С(R9)2)nOR4, -(С(R9)2)nR5, (C(R9)2)nC(O)OR4, -С(О)OR4 и -S(O)2R4; каждый R9 независимо выбран из Н и С 1-С 6 алкила;R10 выбран из незамещенного фенила, незамещенного 5-6-членного гетероарила с 1-2 гетероатомами, независимо выбранными из N, О или S, незамещенного триазолила, незамещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, незамещенного С 3 С 8 циклоалкила, замещенного 5-6-членного гетероарила с 1-2 гетероатомами, независимо выбранными изN, О или S, замещенного фенила, замещенного триазолила, замещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, замещенного С 3-С 8 циклоалкила, оксазолидин-2-она, пирролидинона и пирролидин-2-она,причем замещенный фенил, замещенный 5-6-членный гетероарил с 1-2 гетероатомами, независимо выбранными из N, О или S, замещенный 5-членный гетероарил с 1-4 гетероатомами, выбранными из N,замещенный С 3-С 8 циклоалкил и замещенный 4-6-членный гетероциклоалкил R10 замещены 1-3 заместителями, независимо выбранными из С 1-С 6 алкила, -(С(R9)2)nOR4, -(С(R9)2)nR5, -(C(R9)2)nC(O)OR4 иt=1, 2 или 3, и каждый n независимо выбран из 1, 2, 3 и 4. В некоторых вариантах осуществления в любом из вышеупомянутых соединений формулы (Ia),формулы (IIa), формулы (Ib), формулы (IIb), формулы (Ic), формулы (IIe), формулы (Id), формулы (IId),формулы (Ie), формулы (IIe), формулы (If) или формулы (IIf) R1 выбран из -СН 3 и F. В некоторых вариантах осуществления R1 обозначает -СН 3. В некоторых вариантах осуществления R11 независимо выбран из Н, F и -СН 3. В некоторых вариантах осуществления каждый R11 обозначает Н. В некоторых вариантах осуществления R3 выбран из незамещенного С 3-С 8 циклоалкила, циклобутанона, циклопентанона и замещенного С 3-С 8 циклоалкила, причем замещенный С 3-С 8 циклоалкил R3 замещен 1-4 заместителями, независимо выбранными из С 1-С 6 алкила, галогена, С 1-С 6 галогеналкила, -OR4,-(CR92)nOR4, -O(CR92)nOR4, -N(R4)2, =N-OR4, =N-O-(CR92)nR5, -NR4C(=O)OR4, -NR4C(=O)(CR92)nOR4,-NR4(CR92)nOR4, -NR4S(=O)2R4, -N(C(=O)OR4)2, =CH2, =CH(CR92)nOR4, R8, дейтерированного С 1 С 6 алкокси, спиро-присоединенного диоксолана, спиро-присоединенного диоксолана, который замещен С 1-С 6 алкилом, спиро-присоединенного диоксана, спиро-присоединенного тетрагидрофуранила, спироприсоединенного циклобутанона, спиро-присоединенного циклобутанола, незамещенного 5-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N и О, и 5-6-членнсго гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N и О, замещенного 1-3 заместителями, независимо выбранными из С 1-С 6 алкила . В некоторых вариантах осуществления каждый R4 независимо выбран из Н, метила, этила, пропила,бутила, изопропила и трет-бутила. В некоторых вариантах осуществления каждый R5 независимо выбран из циклопропила или морфолинила. В некоторых вариантах осуществления каждый R7 независимо выбран из CH2F, -CHF2, -CH2CHF2,-CH2CF3 и -CF3. В некоторых вариантах осуществления каждый R9 независимо выбран из Н, метила и этила. В некоторых вариантах осуществления R8 выбран из незамещенного С 3-С 8 циклоалкила и незамещенного 5-членного гетероарила с 1-4 гетероатомами, выбранными из N. В некоторых вариантах осуществления R3 выбран из циклопропила, циклобутила, циклопентила и циклогексила, каждый из которых незамещен или каждый из которых замещен 1-4 заместителями, независимо выбранными из -F, -CH3, -CH2CH3, -CF3, -ОН, -OCH3, -СН 2 ОСН 3, -NH2, -N(CH3)2,-2 024293-ОСН 2 СН 2 ОСН 3, =N-OCH3, =N-ОСН 2 СН 3, =N-OCH(CH3)2, =N-OH, =N-O-CH2R5, =N-O-CH2CH2R5,NHC(=O)OC(CH3)3,-NHC(=O)OCH3,-NHC(=O)CH2OCH3,-NHCH2CH2OCH3,-NHCH2CH2OH,-NHS(=O)2CH3, -N(C(=O)OCH3)2, =CH2, =CHCH2CH2OH, OCD3, циклопропила, триазолила, пиразолила,спиро-присоединенного диоксолана, спиро-присоединенного диоксолана, который замещен -СН 3, спироприсоединенного диоксана, спиро-присоединенного тетрагидрофуранила, спиро-присоединенного циклобутанона, спиро-присоединенного циклобутанола, пиперидинила и пиперазинила, замещенного -СН 3,или R3 обозначает циклобутанон или циклопентанон. В некоторых вариантах осуществления R3 обозначает циклопропил, замещенный 1 или 2 F, или R3 обозначает циклобутил, замещенный 2. В некоторых вариантах осуществления m=1 и R20 выбран из Н, галогена, С 1-С 6 алкила, С 1 С 6 галогеналкила,С 1-С 6 галогеналкокси,дейтерированного С 1-С 6 алкила,-CN,-(CR92)nOR4,9 4 10 9 10 9 4 9 9 7 9 4-(CR 2)nC(=O)OR , R , -(CR 2)nR , -CR 2)nO)tR , -(CR 2)nO(CR 2)nR , -(CR 2)nC(=O)R и -C(=O)N(R4)2. В некоторых вариантах осуществления m=1 и R20 выбран из Н, -F, -СН 3, -CF3, -CD3, -CN, -OCHF2,-C(CH3)OH, -CH2CH2C(=O)OC(CH3)3, -СН 2 ОСН 2 СН 2 ОН, -CH2OCH2CF3, -C(=O)NH2, -СН 2 СН 2 С(СН 3)2 ОН,-СН 2 ОСН 2 СН 2 ОСН 3, -CH2OCH2CH2F, -CH2CH2C(=O)CH3, -CH2OH и -СН 2 ОСН 3. В некоторых вариантах осуществления m=1 и R20 обозначает -СН 3. В некоторых вариантах осуществления m=1 и R20 обозначает Н. В некоторых вариантах осуществления R10 выбран из морфолинила, пиперидинила, пиперидин-1 ила, пиперидин-2-ила, пиперидин-3-ила, пиперидин-4-ила, пиперазинила, пиперазин-1-ила, пиразолила,пиразол-1-ила, пиразол-3-ила, пиразол-4-ила, триазолила, 1 Н-1,2,3-триазол-4-ила, 4 Н-1,2,4-триазол-3 ила, 1 Н-1,2,4-триазол-5-ила, тиазолила, тиазол-4-ила, тиазол-5-ила, имидазолила, имидазол-1-ила, имидазол-2-ила, каждый из которых незамещен или каждый из которых замещен 1-3 заместителями, независимо выбранными из С 1-С 6 алкила, -(CR92)nOR4, -(C(R9)2)nC(O)OR4, -(C(R9)2)nR5 и -S(=O)2R4, или R10 выбран из оксазолидин-2-она и пирролидин-2-она. В некоторых вариантах осуществления R10 выбран из морфолинила, пиперидинила, пиперидин-1 ила, пиперидин-2-ила, пилеридин-3-ила, пиперидин-4-ила, пиперазинила, пиперазин-1-ила, пиразолила,пиразол-1-ила, пиразол-3-ила, пиразол-4-ила, триазолила, 1 Н-1,2,3-триазол-4-ила, 4 Н-1,2,4-триазол-3 ила, 1 Н-1,2,4-триазол-5-ила, тиазолила, тиазол-4-ила, тиазол-5-ила, имидазолила, имидазол-1-ила, имидазол-2-ила, каждый из которых незамещен или каждый из которых замещен 1-3 заместителями, независимо выбранными из -СН 3, -СН 2 СН 2 ОН, -СН 2 С(O)ОН, -СН 2 СН 2 ОН, -СН 2 С(СН 3)2 ОН, -S(O)2CH3 и -CH2CH2R5. В некоторых вариантах осуществления m=4 и R20 обозначает дейтерий. В некоторых вариантах осуществления соединения формулы (Ia) или формулы (IIa) выбраны из следующих:N-5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил-6-[(2-фторэтокси)метил]имидазо[1,2-а]пиридин-3-карбоксамид. В других предпочтительных вариантах осуществления соединения формулы (Ia) или формулы (IIa) выбраны из следующих:N-(5-5-[(1R,2S)-2-фторциклопропил]-1,2,4-оксадиазол-3-ил-2-метилфенил)имидазо[1,2-а]пиридин-3-карбоксамид. В некоторых вариантах осуществления соединения формулы (Ia) или формулы (IIa) выбраны из следующих:N-5-[5-(3,3-дифторциклобутил)-1,2,4-оксадиазол-3-ил]-2-метилфенил-7-(пиперидин-4-ил)имидазо[1,2-а]пиридин-3-карбоксамид. В другом аспекте изобретение относится к фармацевтическим композициям, которые включают терапевтически эффективное количество соединения формулы (Ia) или формулы (IIa) и фармацевтически приемлемый носитель. В некоторых вариантах таких фармацевтических композиций, фармацевтическую композицию составляют для внутривенного введения, интравитреального введения, внутримышечного введения, перорального введения, ректального введения, чрескожного введения, легочного введения,введения ингаляцией, назального введения, топического введения, глазного введения или ушного введения. В других вариантах осуществления такие фармацевтические композиции находятся в форме таблетки, пилюли, капсулы, жидкости, ингаляционного препарата, раствора назального спрея, суппозитория,раствора, эмульсии, мази, глазных капель или ушных капель. В других вариантах осуществления такие фармацевтические композиции составляют для перорального введения, и они находятся в форме таблетки, пилюли, капсулы, жидкости, раствора или эмульсии. В других вариантах осуществления такие фармацевтические композиции составляют для перорального введения, и они находятся в форме таблетки,пилюли или капсулы. В других вариантах осуществления такие фармацевтические композиции дополнительно включают одно или более дополнительных терапевтических средств. В других вариантах осуществления такие вышеописанные фармацевтические композиции дополнительно включают одно или более дополнительных терапевтических средств. В другом аспекте изобретение относится к лекарственным средствам для лечения пациента с заболеванием или нарушением, связанным с с-kit или PDGFR киназной активностью, или c-kit и PDGFR киназной активностью, и такие лекарственные средства включают терапевтически эффективное количество соединения формулы (Ia) или формулы (IIa). В некоторых вариантах осуществления этого аспекта заболевание представляет собой заболевание, связанное с тучными клетками, респираторное заболевание,воспалительное нарушение, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), аутоиммунное нарушение, метаболическое нарушение, фиброзное заболевание, дерматологическое заболевание, легочная артериальная гипертензия (РАН) или первичная легочная гипертензия(РРН). В других вариантах осуществления этого аспекта, заболевание представляет собой астму, аллергический ринит, легочную артериальную гипертензию (РАН), легочный фиброз, печеночный фиброз,кардиальный фиброз, склеродермию, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), крапивницу, дерматоз, диабет типа I или диабет типа II. В другом аспекте изобретение относится к лекарственным средствам для лечения заболевания, опосредуемого с-kit или PDGFR киназной активностью, или с-kit и PDGFR киназной активностью, у пациента, и такие лекарственные средства включают терапевтически эффективное количество соединения формулы (Ia) или формулы (IIa), и заболевание представляет собой заболевание, связанное с тучными клетками, респираторное заболевание, воспалительное нарушение, синдром раздраженного кишечника (IBS),воспалительное заболевание кишечника (IBD), аутоиммунное нарушение, метаболическое нарушение,фиброзное заболевание, дерматологическое заболевание, легочную артериальную гипертензию (РАН) или первичную легочную гипертензию (РРН). В некоторых вариантах осуществления этого аспекта, заболевание представляет собой астму, аллергический ринит, легочную артериальную гипертензию (РАН), легочный фиброз, печеночный фиброз,кардиальный фиброз, склеродермию, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), крапивницу, дерматоз, диабет типа I или диабет типа II. В другом аспекте изобретение относится к применению соединения формулы (Ia) или формулы(IIa) в получении лекарственного средства для лечения заболевания или нарушения у пациента, в котором участвует с-kit или PDGFR киназная активность, или с-kit и PDGFR киназная активность. Другой аспект изобретения включает способы лечения заболевания или нарушения, в котором участвует с-kit или PDGFR киназная активность или с-kit и PDGFR киназная активность, причем способ включает введение в систему или пациенту, которому требуется такое лечение, эффективного количества соединения формулы (Ia) или формулы (IIa) или его фармацевтически приемлемых солей или фармацевтических композиций, с осуществлением, таким образом, лечения заболевания или нарушения. В некоторых вариантах осуществления таких способов способы включают введение соединения в клетку или систему ткани, или пациенту, представляющему собой животное или человека. В некоторых вариантах осуществления таких способов заболевания или состояния представляют собой метаболическое нарушение, фиброзное заболевание, респираторное заболевание, воспалительное заболевание или нарушение,дерматологическое заболевание или аутоиммунное заболевание. В некоторых вариантах осуществления таких способов, заболевания или состояния представляют собой астму, аллергический ринит, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), легочную артериальную гипертензию (РАН), легочный фиброз, фиброз печени, кардиальный фиброз, склеродермию, крапивницу,дерматозы, аллергический дерматит, диабет типа I или диабет типа II. В другом аспекте изобретение относится к соединению формулы (Ia) или формулы (IIa) для применения в лечении заболевания, опосредуемого c-kit, PDGFR, PDGFR или их комбинацией, причем заболевание выбрано из заболевания, связанного с тучными клетками, респираторного заболевания, воспалительного нарушения, синдрома раздраженного кишечника (IBS), воспалительного заболевания кишечника (IBD), аутоиммунного нарушения, метаболического нарушения, фиброзного заболевания, дерматологического заболевания, легочной артериальной гипертензии (РАН) и первичной легочной артериальной гипертензии (РРН). В некоторых вариантах осуществления этого аспекта заболевание выбрано из заболевания, связанного с тучными клетками, респираторного заболевания, воспалительного нарушения,синдрома раздраженного кишечника (IBS), воспалительного заболевания кишечника (IBD), аутоиммунного нарушения, метаболического нарушения, фиброзного заболевания, дерматологического заболевания, легочной артериальной гипертензии (РАН) и первичной легочной гипертензии (РРН). В других вариантах осуществления заболевание представляет собой астму, аллергический ринит, легочную артериальную гипертензию (РАН), легочный фиброз, печеночный фиброз, кардиальный фиброз, склеродермию,синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), крапивницу,дерматоз, диабет типа I или диабет типа II. Подробное описание изобретения Определения Термин "алкил" в рамках изобретения относится к насыщенному углеводороду с прямой или разветвленной цепью. В некоторых вариантах осуществления такие алкильные группы могут быть замещены. В рамках изобретения термины "С 1-С 3 алкил", "С 1-С 4 алкил", "С 1-С 5 алкил", "С 1-С 6 алкил", "С 1 С 7 алкил" и "С 1-С 8 алкил" относятся к алкильной группе, содержащей по меньшей мере 1 и самое большее 3, 4, 5, 6, 7 или 8 атомов углерода соответственно. Если не указано иное, алкильная группа обычно представляет собой С 1-С 6 алкил. Неограничивающие примеры алкильных групп в рамках изобретения включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил,гексил, гептил, октил, нонил, децил и т.п. Термин "алкокси" в рамках изобретения относится к группе -ORa, где Ra обозначает алкильную группу, определенную здесь. В рамках изобретения термины "С 1-С 3 алкокси", "С 1-С 4 алкокси", "C1 С 5 алкокси", "С 1-С 6 алкокси", "С 1-С 7 алкокси" и "С 1-С 8 алкокси" относятся к алкоксигруппе, в которой алкильная часть содержит по меньшей мере 1, и самое большее 3, 4, 5, 6, 7 или 8 атомов углерода. Неограничивающие примеры алкоксигрупп в рамках изобретения включают метокси, этокси, н-пропокси, изопропокси, н-бутилокси, трет-бутилокси, пентилокси, гексилокси, гептилокси, октилокси, нонилокси, децилокси и т.п. Термин "циклоалкил" в рамках изобретения относится к насыщенной моноциклической, конденсированной бициклической, конденсированной трициклической, спироциклической или соединенной мостиковой связью полициклической кольцевой системе. В рамках изобретения термины "С 3 С 5 циклоалкил", "С 3-С 6 циклоалкил ", "С 3-С 7 циклоалкил", "С 3-С 8 циклоалкил", "С 3-С 9 циклоалкил" и "С 3 С 10 циклоалкил" относятся к циклоалкильной группе, причем: насыщенная моноциклическая, конденсированная бициклическая или соединенная мостиковой связью полициклическая кольцевая система содержит по меньшей мере 3, и самое большее 5, 6, 7, 8, 9 или 10 атомов углерода. Неограничивающие примеры циклоалкильных групп в рамках изобретения включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононил, циклодецил и т.п. Термин "галоген" в рамках изобретения относится к фтору (F), хлору (Cl), брому (Br) или йоду (I). Термины "галогеналкил" или "замещенный галогеналкил" в рамках изобретения относятся к алкильной группе, определенной здесь, замещенной одной или более группами галогена как определено здесь. Группы галогена могут быть одинаковыми или разными. Галогеналкил может представлять собой моногалогеналкил, дигалогеналкил или полигалогеналкил, включая пергалогеналкил. Пергалогеналкил относится к алкилу, в котором все атомы водорода заменены атомами галогена. Моногалогеналкил может иметь один йод, бром, хлор или фтор в алкильной группе. Дигалогеналкильные и полигалогеналкильные группы могут иметь два или более одних и тех же атомов галогена или комбинации разных групп галогена в составе алкила. Такие галогеналкильные группы также указаны здесь как "С 1 С 3 галогеналкил", "C1-С 4 галогеналкил", "С 1-С 5 галогеналкил", "С 1-С 6 галогеналкил", "C1-С 7 галогеналкил" и"С 1-С 8 галогеналкил", причем алкильная группа содержит по меньшей мере 1 и самое большее 3, 4, 5, 6, 7 или 8 атомов углерода соответственно. Неограничивающие примеры таких галогеналкильных групп с разветвленной или прямой цепью в рамках изобретения включают фторметил, дифторметил, трифторме- 10024293 тил, хлорметил, дихлорметил, трихлорметил, пентафторэтил, гептафторпропил, дифторхлорметил, дихлорфторметил, дифторэтил, дифторпропил, дихлорэтил и дихлорпропил. В некоторых вариантах осуществления галогеналкильная группа представляет собой трифторметил. Термин "гетероарил" в рамках изобретения относится к 5-6-членному гетероароматическому моноциклическому кольцу, имеющему от 1 до 4 гетероатомов, независимо выбранных из азота, кислорода и серы, 8-10-членному конденсированному бициклическому кольцу, имеющему от 1 до 4 гетероатомов,независимо выбранных из азота, кислорода и серы, и где по меньшей мере одно из колец является ароматическим, или 12-14-членному конденсированному трициклическому кольцу, имеющему от 1 до 4 гетероатомов, независимо выбранных из азота, кислорода и серы, и где по меньшей мере одно из колец является ароматическим. Системы таких конденсированных бициклических и трициклических колец могут быть конденсированы с одним или более арильными, циклоалкильными или гетероциклоалкильными кольцами. Неограничивающие примеры гетероарильных групп в рамках изобретения включают 2- или 3 фурил; 1-, 2-, 4- или 5-имидазолил; 3-, 4- или 5-изотиазолил; 3-, 4- или 5-изоксазолил; 2-, 4- или 5 оксазолил; 4- или 5-1,2,3-оксадиазолил; 2- или 3-пиразинил; 1-, 3-, 4- или 5-пиразолил; 3-, 4-, 5- или 6 пиридазинил; 2-, 3- или 4-пиридил; 2-, 4-, 5- или 6-пиримидинил; 1-, 2- или 3-пирролил; 1- или 5 тетразолил; 2- или 5-1,3,4-тиадиазолил; 2-, 4- или 5-тиазолил; 2- или 3-тиенил; 2-, 4- или 6-1,3,5 триазинил; 1-, 3- или 5-1,2,4-триазолил; 1-, 4- или 5-1,2,3-триазолил; 1-, 2-, 3-, 4-, 5-, 6-, 7-, 8- или 9 акридинил; 1-, 3-, 4-, 5-, 6-, 7-, 8-, 9- или 10-бензо[g]изохинолин; 2-, 4-, 5-, 6- или 7-бензоксазолил; 1-, 2-,4-, 5-, 6- или 7-бензимидазолил; 2-, 4-, 5-, 6- или 7-бензотиазолил; 2-, 3-, 4-, 5-, 6-, 7-бензо[b]тиенил; 2-, 3, 4-, 5-, 6-, 7-, 8-, 9-бензо[b]оксепин; 2-, 4-, 5-, 6-, 7- или 8-бензоксазинил; 1-, 2-, 3-, 4-, 5-, 6-, 7-, 8 или 9 карбазолил; 3-, 4-, 5-, 6-, 7- или 8-циннолинил; 2-, 4- или 5-4 Н-имидазо[4,5-d]тиазолил; 2-, 3-, 5- или 6 имидазо[2,1-b]тиазолил; 2-, 3-, 6- или 7-имидазо[1,2-b][1,2,4]триазинил; 1-, 3-, 4-, 5-, 6- или 7-индазолил ; 1-, 2-, 3-, 5-, 6-, 7- или 8-индолизинил; 1-, 2-, 3-, 4-, 5-, 6- или 7-индолил; 1-, 2-, 3-, 4-, 5-, 6- или 7 изоиндолил; 1-, 3-, 4-, 5-, 6-, 7- или 8-изохинолинил; 2-, 3-, 4-, 5-, 6- или 7-нафтиридинил; 1-, 2-, 4-, 5-, 6-,7-, 8- или 9-пиримидинил; 1-, 2-, 3-, 4-, 6-, 7-, 8-, 9- или 10-фенантридинил; 1-, 2-, 3-, 4-, 5-, 6-, 7-, 8-, 9 или 10-фенантролинил; 1-, 2-, 3-, 4-, 6-, 7-, 8- или 9-феназинил; 1-, 2-, 3-, 4-, 6-, 7-, 8-, 9- или 10 фенотиазинил; 1-, 2-, 3-, 4-, 6-, 7-, 8-, 9- или 10-феноксазинил; 1-, 4-, 5-, 6-, 7- или 8-фталазинил; 2-, 4-, 6 или 7-птеридинил; 2-, 6-, 7- или 3-пуринил; 2-, 3-, 5-, 6-, 7-, 8-, 9-, 10- или 11-7 Н-пиразино[2,3c]карбазолил; 2-, 3-, 5-, 6- или 7-фуро[2-b]пиранил; 1-, 3- или 5-1 Н-пиразоло[4,3-d]оксазолил; 2-, 3-, 5 или 8-пиразино[2,3-d]пиридазинил; 1-, 2-, 3-, 4-, 5- или 8-5 Н-пиридо[2,3-d]-о-оксазинил; 1-, 2-, 3-, 4-, 6-,7-, 8- или 9-хинолизинил; 2-, 3-, 4-, 5-, 6-, 7- или 8-хинолинил; 2-, 3-, 4-, 5-, 6-, 7- или 8-хиназолинил; 2-,3-, 4- или 5-тиено[2,3-b]фуранил и 1-, 3-, 6-, 7-, 8- или 9-фуро[3,4-с]циннолинил. Термин "гетероатомы" в рамках изобретения относится к атомам азота (N), кислорода (О) или серы(S). Термин "гетероциклоалкил" в рамках изобретения относится к насыщенной 3-6-членной моноциклической кольцевой углеводородной структуре, насыщенной 6-9-членной конденсированной бициклической кольцевой углеводородной структуре или насыщенной 10-14-членной конденсированной трициклической кольцевой углеводородной структуре, в которых от одного до четырех кольцевых атомов углерода кольцевой углеводородной структуры заменен одной-четырьмя группами, независимо выбранными из-О-, -NR- или -S-, причем R обозначает водород, С 1-С 4 алкил или защитную группу аминогруппы. Неограничивающие примеры гетероциклоалкильных групп в рамках изобретения включают азиридинил, азиридин-1-ил, азиридин-2-ил, азиридин-3-ил, оксиранил, оксиран-2-ил, оксиран-3-ил, тииранил,тииран-2-ил, тииран-3-ил, азетадинил, азетадин-1-ил, азетадин-2-ил, азетадин-3-ил, оксетанил, оксетан-2 ил, оксетан-3-ил, оксетан-4-ил, тиетанил, тиетан-2-ил, тиетан-3-ил, тиетан-4-ил, пирролидинил, пирролидин-1-ил, пирролидин-2-ил, пирролидин-3-ил, пирролидин-4-ил, пирролидин-5-ил, тетрагидрофуранил,тетрагидрофуран-2-ил, тетрагидрофуран-3-ил, тетрагидрофуран-4-ил, тетрагидрофуран-5-ил, тетрагидротиенил, тетрагидротиен-2-ил, тетрагидротиен-3-ил, тетрагидротиен-4-ил, тетрагидротиен-5-ил, пиперидинил, пиперидин-1-ил, пиперидин-2-ил, пиперидин-3-ил, пиперидин-4-ил, пиперидин-5-ил, пиперидин 6-ил, тетрагидропиранил, тетрагидропиран-2-ил, тетрагидропиран-3-ил, тетрагидропиран-4-ил, тетрагидрояиран-5-ил, тетрагидропиран-6-ил, тетрагидротиопиранил, тетрагидротиопиран-2-ил, тетрагидротиопиран-3-ил, тетрагидротиопиран-4-ил, тетрагидротиопиран-5-ил, тетрагидротиопиран-6-ил, пиперазинил,пиперазин-1-ил, липеразин-2-ил, пиперазин-3-ил, пиперазин-4-ил, пиперазин-5-ил, пиперазин-6-ил, морфолинил, морфолин-2-ил, морфолин-3-ил, морфолин-4-ил, морфолин-5-ил, морфслин-6-ил, тиоморфолинил, тиоморфолин-2-ил, тиоморфолин-3-ил, тиоморфолин-4-ил, тиоморфолин-5-ил, тиоморфолин-6-ил,оксатианил, оксатиан-2-ил, оксатиан-3-ил, оксатиан-5-ил, оксатиан-6-ил, дитианил, дитиан-2-ил, дитиан 3-ил, дитиан-5-ил, дитиан-6-ил, азепанил, азепан-1-ил, азепан-2-ил, азепан-3-ил, азепан-4-ил, азепан-5-ил,азепан-6-ил, азепан-7-ил, оксепанил, оксепан-2-ил, оксепан-3-ил, оксепан-4-ил, оксепан-5-ил, оксепан-6 ил, оксепан-7-ил, тиепанил, тиепан-2-ил, тиепан-3-ил, тиепан-4-ил, тиепан-5-ил, тиепан-6-ил, тиепан-7 ил, диоксоланил, диоксолан-2-ил, диоксолан-4-ил, диоксолан-5-ил, тиоксанил, тиоксан-2-ил, тиоксан-3 ил, тиоксан-4-ил, тиоксан-5-ил, дитиоланил, дитиолан-2-ил, дитиолан-4-ил, дитиолан-5-ил, пирролинил,пирролин-1-ил, пирролин-2-ил, пирролин-3-ил, пирролин-4-ил, пирролин-5-ил, имидазолинил, имидазолин-1-ил, имидазолин-3-ил, имидазолин-4-ил, имидазолин-5-ил, имидазолидинил, имидазолидин-1-ил,- 11024293 имидазолидин-2-ил, имидазолидин-3-ил, имидазолидин-4-ил, имидазолидин-4-ил, пиразолинил, пиразолин-1-ил, пиразолин-3-ил, пир 1 азолин-4-ил, пиразолин-5-ил, пиразолидинил, пиразолидин-1-ил, пиразолидин-2-ил, пиразолидин-3-ил, пиразолидин-4-ил, пиразолидин-5-ил, гексагидро-1,4-диазепинил, дигидрофуранилдигидропиранил, 1,2,3,6-тетрагидропиридинил, 2 Н-пиранил, 4 Н-пиранил, дигидропиранил,дигидротиенил, дигидрофуранил, 3-азабицикло[3.1.0]гексанил, 3-азабицикло[4.1.0]гептанил, пирролидинил-2-он, пиперидинил-3-он, пиперидинил-2-он, пиперидинил-4-он и 2 Н-пирролил. Термин "приемлемый" относительно соединения, состава, композиции или ингредиента в рамках изобретения означает не имеющий никакого постоянного вредного эффекта на общее здоровье получающего лечение пациента. Термин "введение" упоминаемого соединения означает обеспечение получения пациентом, нуждающимся в лечении, соединения формулы (Ia) или формулы (IIa), его фармацевтически приемлемой соли, фармацевтически приемлемого сольвата или сольвата. Термин "аутоиммунное заболевание" или "аутоиммунное нарушение" в рамках изобретения относится к заболеванию, в котором клетки неконтролируемо атакуют собственные ткани тела и органы (аутоиммунитет), вызывая воспалительные реакции и другие серьезные симптомы и заболевания. Неограничивающие примеры аутоиммунных заболеваний включают идиопатическую тромбоцитопеническую пурпуру, гемолитическую анемию, системную красную волчанку, ревматоидный артрит (FA), рассеянный склероз (MS), иммунно-опосредованный или типа 1 сахарный диабет, иммунно-опосредованный гломерулонефрит, склеродермию, пернициозную анемию, алопецию, пузырчатку, пузырчатку обыкновенную, миастению гравис, воспалительные заболевания кишечника, болезнь Крона, псориаз, аутоиммунные заболевания щитовидной железы и болезнь Хасимото, тиреоидит Хасимото, дерматомиозит,синдром Гудпасчера, псевдопаралитическую миастению гравис, ophtalmia sympatica, факогенный увеит,хронический агрессивный гепатит, первичный биллиарный цирроз, аутоиммунную гемолитическую анемию, болезнь Верлофа, витилиго вульгарное, болезнь Бехчета, коллагеноз, увеит, синдром Сьогрена, аутоиммунный миокардит, аутоиммунные заболевания печени, аутоиммунный гастрит, пузырчатка, синдром Гийена-Барре и HTLV-1-ассоциированную миелопатию. Термин "носитель" в рамках изобретения относится к химическим соединениям или средствам, которые облегчают включение соединения, описанного здесь, в клетки или ткани. Термины "совместное введение" или "комбинированное введение", или подобное, в рамках изобретения охватывают введение выбранных терапевтических средств отдельному пациенту и включает режимы лечения, в которых средства не обязательно вводят одним и тем же путем введения или в одно и то же; время. Термин "дерматологическое заболевание" или "дерматологическое нарушение" в рамках изобретения относится к кожному нарушению. Такие дерматологические нарушения включают, но не ограничены ими, пролиферативные или воспалительные нарушения, такие как аллергический дерматит кожи, буллезные нарушения, коллагенозы, контактная дерматитная экзема, болезнь Кавасаки, розацеа, синдром Сьогрена-Ларссо, актинический кератоз, базально-клеточный рак и крапивница. Термин "разбавитель" в рамках изобретения относится к химическим соединениям, которые используются для разбавления соединения, описанного здесь, перед доставкой. Разбавители могут также использоваться для стабилизации соединений, описанных здесь. Термины "эффективное количество" или "терапевтически эффективное количество" в рамках изобретения относятся к достаточному количеству соединения, описанного здесь, которое при введении до некоторой степени снимает один или более симптомов подвергаемого лечению заболевания или состояния. Результат может представлять собой уменьшение и/или облегчение признаков, симптомов или причин заболевания, или любую другую желательную альтерацию биологической системы. Например, "эффективное количество" для терапевтических применений представляет собой количество композиции,включающей соединение, как раскрыто здесь, которое требуется, чтобы обеспечить клинически значимое уменьшение симптомов заболевания. Подходящее "эффективное" количество в любом индивидуальном случае может быть определено с использованием таких методик, как исследование увеличения дозы. Термин "усиление" в рамках изобретения означает увеличение или продление либо потенциала, либо продолжительности желаемого эффекта. Таким образом, в отношении усиления эффекта терапевтических средств, термин "усиление" относится к способности увеличивать или продлевать либо потенциал,либо продолжительность эффекта других терапевтических средств в системе. "Эффективное в отношении усиления количество" в рамках изобретения относится к количеству, подходящему для того, чтобы усилить эффект другого терапевтического средства в желаемой системе. Термины "фиброз" или "фиброзное заболевание" в рамках изобретения относятся к состояниям, которые следуют за острым или хроническим: воспалением и связаны с патологическим накоплением клеток и/или коллагена и включают, но не ограничены им, фиброз индивидуальных органов или тканей,таких как сердце, почка, сустав, легкое или кожа, и включают такие нарушения как идиопатический легочный фиброз и криптогенный фиброзирующий альвеолит. Термин "воспалительное заболевание или нарушения" в рамках изобретения относится к заболеваниям или состояниям, которые характеризуются одним или более признаками боли (dolor, от генерации вредных веществ и возбуждения нервов), высокой температуры (calor, от вазодилатации), красноты (rubor, от вазодилатации и увеличенного кровотока), отека (tumor, от чрезмерного притока или ограниченного оттока жидкости) и потери функции (functio laesa, которая может быть частичной или полной, временной или постоянной). Воспаление принимает множество форм и включает, но не ограничено ими,воспаление, которое является одним или более из следующих: острое, адгезивное, атрофическое, катаральное, хроническое, цирротическое, диффузное, диссеминированное, экссудативное, фибринозное,фиброзирующее, центральное, гранулематозное, гиперпластическое, гипертрофическое, интерстициальное, метастатическое, некротическое, облитеративное, паренхиматозное, пластическое, продуктивное,пролиферирующее, псевдомембранозное, гнойное, склерозирующее, серозно-фибринозное, серозное,простое, специфическое, подострое, гнойное, токсическое, травматическое и/или язвенное. Воспалительные нарушения далее включают, не будучи ограниченными ими, такие, которые воздействуют на кровеносные сосуды (полиартериит, височный артериит); сустав (артрит: кристаллический,остео-, псориатический, реактивный, ревматоидный, Рейтера); желудочно-кишечный тракт (заболевание); кожа (дерматит); или множественные органы и ткани (системная красная волчанка). В рамках изобретения термин "ингибирует" или "ингибирование" относится к сокращению или подавлению данного состояния, симптома или нарушения, или заболевания, или значительному уменьшению в базовой активности биологической активности или процесса. Термин "фармацевтически приемлемый" в рамках изобретения относится к материалу, такому как носитель или разбавитель, который не снижает биологическую активность или свойства соединений,описанных здесь. Такие материалы вводятся индивидууму, не вызывая нежелательные биологические действия или вредные взаимодействия с любым из компонентов композиции, в которой они содержатся. Термин "фармацевтически приемлемый носитель" в рамках изобретения включает любые и все растворители, дисперсионные среды, покрытия, поверхностно-активные вещества, антиоксиданты, консерванты (например, антибактериальные агенты, противогрибковые агенты), изотонические средства, средства, задерживающие поглощение, соли, консерванты, стабилизаторы лекарственного средства, связующие, эксципиенты, разрыхлители, лубриканты, подсластители, ароматизаторы, красители и т.п. и их комбинации, известные специалисту (см., например, Remington's Pharmaceutical Sciences, 18th Ed. MackPrinting Company, 1990, pp. 1289-1329). Кроме того, за исключением случаев, когда какой-либо обычный носитель является несовместимым с активным ингредиентом, его использование в терапевтических или фармацевтических композициях также может быть рассмотрено. Термин "фармацевтически приемлемая соль" в рамках изобретения относится к составу соединения, который не вызывает значительного раздражения организма, которому его вводят, и не приводит к исчезновению биологической активности и свойств соединений, описанных здесь. Термины "комбинация" или "фармацевтическая комбинация" в рамках изобретения означают продукт, который является результатом смешивания или комбинирования более чем одного активного ингредиента, и включают как фиксированные, так и нефиксированные комбинации активных ингредиентов. Термин "фиксированная комбинация" означает, что активные ингредиенты, например, соединение формулы (Ia) или формулы (IIa) и дополнительное терапевтическое средство, оба вводят пациенту одновременно в форме единственного объекта или лекарственной формы. Термин "нефиксированная комбинация" означает, что активные ингредиенты, например, соединение формулы (Ia) или формулы (IIa) и дополнительное терапевтическое средство, оба вводят пациенту как отдельные объекты одновременно,конкурентно или последовательно без определенных сроков, причем такое введение обеспечивает терапевтически эффективные уровни 2 соединений в организме пациента. Последнее также относится к коктейльной терапии, например, введению 3 или более активных ингредиентов. Термины "композиция" или "фармацевтическая композиция" в рамках изобретения относятся к смеси по меньшей мере одного соединения, такого как соединения формулы (Ia) или формулы (IIa), по меньшей мере с одним и в случае необходимости более чем одним другим фармацевтически приемлемым химическим компонентом, таким как носители, стабилизаторы, разбавители, диспергирующие агенты, суспендирующие агенты, загустители и/или эксципиенты. Термин "респираторное заболевание" в рамках изобретения относится к заболеваниям, затрагивающим органы, участвующие в дыхании, такие как нос, глотка, гортань, трахея, бронхи и легкие. Респираторные заболевания включают, но не ограничены ими, астму, респираторный дистресс-синдром взрослых и аллергическую (экзогенную) астму, неаллергическую (эндогенную) астму, острую тяжелую астму, хроническую астму, клиническую астму, ночную астму, индуцированную аллергеном астму,чувствительную к аспирину астму, астму физического усилия, изокапническую гипервентиляцию,детскую астму, астму зрелого возраста, кашлевую астму, профессиональную астму, стероидрезистентную астму, сезонную астму, сезонный аллергический ринит, хронический аллергический ринит, хроническое обструктивное заболевание легких, включая хронический бронхит или эмфизему,легочную гипертензию, интерстициальный фиброз легкого и/или воспаление дыхательных путей и муковисцидоз, и гипоксию. Термин "пациент" в рамках изобретения охватывает млекопитающих и не млекопитающих. Примеры млекопитающих включают, но не ограничены ими, человека, шимпанзе, человекообразных обезьян,нечеловекообразных обезьян, рогатый скот, лошадей, овец, коз, свиней; кроликов, собак, кошек, крыс,- 13024293 мышей, морских свинок и т.п. Примеры не млекопитающих включают, но не ограничены ими, птиц, рыб и т.п. Часто пациентом является человек, и может представлять собой человека, у которого была диагностирована необходимость лечения заболевания или нарушения, раскрытого здесь. В рамках изобретения для пациента существует "необходимость"' лечения, если такой пациент получил бы от такого лечения выгоду с биологической, с медицинской точки зрения или в отношении качества жизни. Термин "ингибитор с-kit" в рамках изобретения относится к соединению, которое ингибирует с-kit киназу. Термин "заболевание или нарушение, связанное с активностью с-kit" в рамках изобретения относится к любому болезненному состоянию, связанному с с-kit киназой. Такие заболевания или нарушения включают, но не ограничены ими, заболевание, связанное с тучными клетками, воспалительные заболевания, респираторные заболевания, фиброзные заболевания, дерматологическое заболевание, метаболические нарушения и аутоиммунные заболевания, такие как, только в качестве примера, астма, дерматит,аллергический ринит, легочный фиброз, печеночный фиброз, кардиальный фиброз, склеродермия, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), крапивница, ревматоидный артрит, рассеянный склероз, крапивница, легочная артериальная гипертензия (РАН), первичная легочная гипертензия (РРН), дерматоз, диабет, диабет типа I и диабет типа II. Термин "ингибитор PDGFR" в рамках изобретения относится к соединению, которое ингибирует киназу PDGFR. Термин "заболевание или нарушение, связанное с активностью PDGFR" в рамках изобретения относится к любому болезненному состоянию, связанному с киназой PDGFR. Такие заболевания или нарушения включают, но не ограничены ими, воспалительные заболевания, респираторные заболевания,фиброзные заболевания, метаболические нарушения и аутоиммунные заболевания, такие как, только в качестве примера, астма, дерматит, аллергический ринит, склеродермия, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), крапивница, ревматоидный артрит, рассеянный склероз, легочная артериальная гипертензия и диабет. Термин "оптический изомер" или "стереоизомер" в рамках изобретения относится к любой из различных стереоизомерных конфигураций, которые могут существовать для данного соединения согласно настоящему изобретению и включает геометрические изомеры. Следует понимать, что заместитель может быть присоединен в хиральном центре атома углерода. Термин "хиральный" относится к молекулам,которые имеют свойство не накладываться друг на друга на их партнере зеркального отображения, в то время как термин "ахиральный" относится к молекулам, которые накладываются друг на друга на их партнере зеркального отображения. Поэтому изобретение включает энантиомеры, диастереомеры или рацематы соединения."Энантиомеры" представляют собой пару стереоизомеров, которые не накладываются: друг на друга на зеркальных отображениях друг друга. 1:1 смесь пары энантиомеров представляет собой "рацемическую" смесь. Этот термин используется для определения рацемической смеси, где необходимо. "Диастереоизомеры" являются стереоизомерами, которые имеют по меньшей мере два асимметрических атома,но которые не являются зеркальными отображениями друг друга. Абсолютная стереохимия определяется согласно Cahn-lngold-Prelog R-S системе. Когда соединение является чистым энантиомером, стереохимия в каждом хиральном углероде может быть определена или как R, или как S. Разделенные соединения,абсолютная конфигурация которых неизвестна, могут определяться как (+) или как (-) в зависимости от направления (право- или левовращающий), в котором они отклоняют плоскость поляризованного света при длине волны D линии натрия. Некоторые соединения, описанные здесь, содержат один или более центров или осей асимметрии и могут, таким образом, давать начало энантиомерам, диастереомерам и другим стереоизомерным формам, которые могут быть определены, в терминах абсолютной стереохимии, как (R)- или (S)-. Термин "терапевтически эффективное количество" соединения согласно настоящему изобретению в рамках изобретения относится к количеству соединения согласно настоящему изобретению, которое вызывает биологический или медицинский ответ пациента, например, уменьшение или ингибирование активности фермента или белка или облегчение симптомов, облегчение состояния, замедляет или отдаляет прогрессию заболевания или предотвращает заболевание и т.д. В одном неограничивающем варианте осуществления термин "терапевтически эффективное количество" относится к количеству соединения согласно настоящему изобретению, которое, при введении пациенту, является эффективным для (1) по меньшей мере частичного облегчения, ингибирования, предотвращения и/или улучшения состояния, или нарушения или заболевания (Ia) опосредуемого киназой с-kit или киназами с-kit и PDGFR, или (IIa) связанного с активностью киназы с-kit или киназы с-kit и PDGFR, или (iii) характеризующегося активностью (нормальной или патологической) киназы с-kit или киназ с-kit и PDGFR; или (2) уменьшения или ингибирования активности киназы с-kit или киназ с-kit и PDGFR; или (3) снижения или ингибирования экспрессии киназы с-kit или киназ с-kit и PDGFR. В другом неограничивающем варианте осуществления термин "терапевтически эффективное количество" относится к количеству соединения согласно настоящему изобретению, которое, при введении в клетку или ткань, или в неклеточный биологический мате- 14024293 риал, или в среду, является эффективным для по меньшей мере частичного уменьшения или ингибирования активности киназы с-kit или киназ c-kit и PDGFR; или по меньшей мере частичного снижения или ингибирования экспрессии киназы с-kit или киназ с-kit и PDGFR. Термин "лечение" в рамках изобретения относится к способам облегчения, уменьшения или улучшения симптомов заболевания или состояния, предотвращения дополнительных симптомов, улучшения или предотвращения основных метаболических причин симптомов, ингибирования заболевания или состояния, остановки развития заболевания или состояния, устранения заболевания или состояния, индукции регрессии заболевания или состояния, устранения состояния, вызванного заболеванием или состоянием, или остановки симптомов заболевания или состояния профилактическим и/или терапевтическим образом. Кроме того, в рамках изобретения термин "лечение" любого заболевания или нарушения относится,в одном варианте осуществления, к облегчению заболевания или нарушения (то есть, замедлению или остановке или ослаблению развития заболевания или по меньшей мере одного из его клинических симптомов). В другом варианте осуществления "лечение" относится к облегчению или улучшению по меньшей мере одного физического параметра, включая такие, которые могут не чувствоваться пациентом. В еще одном варианте осуществления "лечение" относится к коррекции заболевания или нарушения, в физическом (например, стабилизация различимого симптома), физиологическом (например, стабилизация физического параметра) отношении или в обоих отношениях. В еще одном варианте осуществления "лечение" относится к предотвращению или задержке начала или развития или прогрессии заболевания или нарушения. Названия соединений по изобретению получали, используя ChemDraw Ultra 10,0 (CambridgeSoft) или JChem version 5.3.1 (ChemAxon). Если не указано иное, термин "соединения согласно настоящему изобретению" или "соединения по изобретению" относится к соединениям формулы (Ia) и формулы (IIa) и к их фармацевтически приемлемым солям, гидратам или сольватам, стереоизомерам (включая диастереоизомеры и энантиомеры), таутомерам и изотопно-меченым соединениям (включая замещения дейтерием). В рамках изобретения термины, используемые в единственном числе в контексте настоящего изобретения (особенно в контексте формулы изобретения), должны рассматриваться как охватывающие как единственное, так и множественное число, если не указано иное или если это явно не противоречит контексту. Все способы, описанные здесь, могут быть выполнены в любом подходящем порядке, если не указано иное или если это явно не противоречит контексту. Использование любого и всех примеров или иллюстративной терминологии (например, "такой как") предназначено только для лучшего освещения изобретения и не вводит ограничения в отношении объема заявленного изобретения. Здесь описаны различные перечисленные варианты осуществления изобретения. Понятно, что признаки, определенные в каждом варианте осуществления, могут быть скомбинированы с другими указанными признаками с получением дополнительных вариантов осуществления настоящего изобретения. Описание предпочтительных вариантов осуществления Изобретение относится к соединениям, их фармацевтически приемлемым солям, которые являются ингибиторами с-kit киназы или киназ с-kit и PDGFR. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit (IC50PDGFR/IC50 c-kit) в диапазоне от 750 до 1000. Некоторые варианты соединений по изобретению имеютIC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit (IC50 PDGFR/IC50 c-kit) в диапазоне от 500 до 750. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit (IC50 PDGFR/IC50 c-kit) в диапазоне от 250 до 500. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибированияPDGFR к IC50 в отношении ингибирования c-kit (IC50 PDGFR/IC50 c-kit) в диапазоне от 100 до 250. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit (IC50 PDGFR/IC50 c-kit) в диапазоне от 75 до 100. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit (IC50 PDGFR/IC50 c-kit) в диапазоне от 50 до 75. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit (IC50PDGFR/IC50 с-kit) в диапазоне от 25 до 50. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit (IC50 PDGFR/IC50 c-kit) в диапазоне от 10 до 25. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit (IC50 PDGFR/IC50 с-kit) в диапазоне от 7,5 до 10. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибирования PDGFR кIC50 в отношении ингибирования c-kit (IC50 PDGFR/IC50 c-kit) в диапазоне от 5 до 7,5. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit (IC50 PDGFR/IC50 c-kit) в диапазоне от 2,5 до 5. Некоторые варианты соединений по изобретению имеют IC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit(IC50 PDGFR/IC50 с-kit) в диапазоне от 1 до 2,5. Некоторые варианты соединений по изобретению имеютIC50 в отношении ингибирования PDGFR к IC50 в отношении ингибирования c-kit (IC50 PDGFR/IC50 c-kit) в диапазоне от 0,95 до 2,5. Также изобретение относится к фармацевтическим композициям, которые включают такие соединения. Изобретение также относится: к способам лечения заболеваний и/или нарушений, связанных с киназой c-kit или киназами c-kit и PDGFR, с использованием таких соединений и фармацевтических композиций. Ингибиторы киназы c-kit или киназы c-kit и PDGFR согласно настоящему изобретению представляют собой соединения, имеющие структуру формулы (Ia) или формулы (IIa), и их фармацевтически приемлемые солиR1 выбран из С 1-С 6 алкила и галогена; каждый R11 независимо выбран из Н, галогена и С 1-С 6 алкила;R3 выбран из незамещенного С 3-С 8 циклоалкила, циклобутанона, циклопентанона и замещенного С 3 С 8 циклоалкила,причем замещенный С 3-С 8 циклоалкил R3 замещен 1-4 заместителями, независимо выбранными из С 1-С 6 алкила, галогена, C1-С 6 галогеналкила, -OR4, -CN, -C(=O)OR4, -C(=O)R4, -C(=O)R7, -C(-O)OR5,-(CR92)nOR4, -C(=O)O(CR92)nOR4, -N(R4)2, =N-OR4, =N-O-(CR92)nR5, -C(=O)NR42, -NR4C(=O)OR4,-NR4C(=O) (CR92)nOR4, -NR4(CR92)nOR4, -NR4S(=O)2R4, -N(C(=O)OR4)2, =CH2, =CH(CR92)nOR4, R8,-(CR92)nR8, дейтерированного С 1-С 6 алкокси, -S(=O)2R4, -S(=O)2R7, -S(=O)2R8, -S(=O), N(R4)2,-S(=O)2NHC(=O)OR4, -S(=O)2(CR92)nC(=O)OR4, -S(=O)2(CR92)nOR4, спиро-присоединенного диоксолана,спиро-присоединенного диоксолана, который замешен С 1-С 6 алкилом, спиро-присоединенного диоксана,спиро-присоединенного тетрагидрофуранила, спиро-присоединенного оксетана, спиро-присоединенного циклобутанона, спиро-присоединенного циклобутанола, незамещенного 5-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О и S, 5-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О и S, замещенного 1-3 заместителями, независимо выбранными из С 1-С 6 алкила, галогена, C1-С 6 галогеналкила, С 1-С 6 галогеналкокси, -OR4 и R8; каждый R4 независимо выбран из Н и С 1-С 6 алкила;R5 обозначает незамещенный С 3-С 8 циклоалкил, незамещенный 5-6-членный гетероциклоалкил с 1-2 гетероатомами, независимо выбранными из N или О, или С 3-С 8 циклоалкил, замещенный 1-3 заместителями, независимо выбранными из С 1-С 6 алкила; каждый R6 независимо выбран из -NHC(O)OR4, -OR4 и (CR92)nOR4; каждый R7 независимо выбран из C1-С 6 галогеналкила;R8 выбран из незамещенного фенила, незамещенного 5-6-членного гетероарила с 1-3 гетероатомами, независимо выбранными из N, О или S, тетразолила, незамещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, незамещенного С 3-С 8 циклоалкила, замещенного 5-6-членного гетероарила с 1-3 гетероатомами, независимо выбранными из N, О или S, замещенного фенила, замещенного 5-членного гетероарила с 1-4 гетероатомами, выбранными из N, замещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, замещенного С 3-С 8 циклоалкила, оксазолидин-2-она, пирролидинона и пирролидин-2-она,причем замещенный фенил, замещенный 5-6-членный гетероарил с 1-3 гетероатомами, независимо выбранными из N, О или S, замещенный 5-членный гетероарил с 1-4 гетероатомами, выбранными из N,замещенный С 3-С 8 циклоалкил и замещенный 4-6-членный гетероциклоалкил R8 замещены 1-3 заместителями, независимо выбранными из С 1-С 6 алкила, -(С(R9)2)nOR4, -(С(R9)2)nR5, -(C(R9)2)nC(O)OR4,-C(O)OR4 и -S(O)2R4; каждый R9 независимо выбран из Н и С 1-С 6 алкила;R10 выбран из незамещенного фенила, незамещенного 5-6-членного гетероарила с 1-2 гетероатома- 16024293 ми, независимо выбранными из N, О или S, незамещенного триазолила, незамещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, незамещенного С 3 С 8 циклоалкила, замещенного 5-6-членного гетероарила с 1-2 гетероатомами, независимо выбранными изN, О или S, замещенного фенила, замещенного триазолила, замещенного 4-6-членного гетероциклоалкила с 1-2 гетероатомами, независимо выбранными из N, О или S, замещенного С 3-С 8 циклоалкила, оксазолидин-2-она, пирролидинона и пирролидин-2-она,причем замещенный фенил, замещенный 5-6-членный гетероарил с 1-2 гетероатомами, независимо выбранными из N, О или 3, замещенный 5-членный гетероарил с 1-4 гетероатомами, выбранными из N,замещенный С 3-С 8 циклоалкил и замещенный 4-6-членный гетероциклоалкил R10 замещены 1-3 заместителями, независимо выбранными из С 1-С 6 алкила, -(С(R9)2)nOR4, -(С(R9)2)nR5, -(C(R9)2)nC(O)OR4 иt=1, 2 или 3, и каждый n независимо выбран из 1, 2, 3 и 4. Соединения формулы (Ia) или формулы (IIa), их фармацевтически приемлемые соли и фармацевтические композиции по изобретению также включают все подходящие изотопные вариации таких соединений и их фармацевтически приемлемых солей, сольватов, N-оксидов и изомеров и фармацевтических композиций. Поэтому любая формула, данная здесь, также обозначает немеченые формы, а также изотопно-меченые формы соединений. Изотопно-меченые соединения имеют структуры, изображенные формулами, данными здесь, за исключением того, что один или более атомов заменены атомом, имеющим выбранную атомную массу или массовое число. Примеры изотопов, которые могут быть включены в соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора (3),фтора и хлора, такие как 2 Н, 3 Н, 11 С, 13 С, 14 С, 15N, 18F, 31P, 32P, 35S, 36Cl, 125I соответственно. Изобретение включает различные изотопно-меченые соединения, как определено здесь, например, такие, в которых присутствуют радиоактивные изотопы, такие как 3 Н и 14 С, или такие, в которых присутствуют нерадиоактивные изотопы, такие как 2 Н и 13 С. Такие изотопно-меченые соединения могут быть использованы в метаболических исследованиях (с 14 С), исследованиях кинетических реакций (с, например, 2 Н или 3 Н),методиках детекции или отображения, таких как позитронная эмиссионная томография (PET) или однофотонная эмиссионная компьютерная томография (SPECT), включая тесты распределения в ткани лекарственного средства или субстрата, или в радиоактивном лечении пациентов. В частности, 18F или меченое соединение может быть особенно желательным для исследований SPECT или PET. Изотопномеченые соединения формулы (Ia) могут в целом быть получены обычными методиками, известными специалисту, или способами, аналогичными описанным в сопутствующих Примерах и Примерах получения, с использованием подходящих изотопно-меченых реактивов вместо немеченого реактива, используемого ранее. Далее, замещение более тяжелыми изотопами, особенно дейтерием (то есть, 2 Н или D), может предоставить определенные терапевтические преимущества, являющиеся следствием большей метаболической стабильности, например, увеличенный период полужизни in vivo или сниженные требования к дозировке, или улучшение терапевтического индекса. Следует понимать, что дейтерий в этом контексте расценивают как заместитель соединения формулы (Ia). Концентрация такого более тяжелого изотопа, в частности, дейтерия, может быть определена изотопным коэффициентом обогащения. Термин "изотопный коэффициент обогащения" в рамках изобретения означает отношение между распространенностью изотопа и естественной распространенностью указанного изотопа. Если заместитель в соединении по изобретению обозначен как дейтерий, такое соединение имеет изотопный коэффициент обогащения для каждого определяемого атома дейтерия по меньшей мере 3500 (включение дейтерия на 52,5% в каждом определяемом атоме дейтерия), по меньшей мере 4000 (60%-ое включение дейтерия), по меньшей мере 4500 (включение дейтерия на 67,5%), по меньшей мере 5000 (75%-ое включение дейтерия), по меньшей мере 5500 (включение дейтерия на 82,5%), по меньшей мере 6000 (90%-ое включение дейтерия), по меньшей мере 6333,3 (95%-ое включение дейтерия), по меньшей мере 6466,7 (97%-ое включение дейтерия), по меньшей мере 6600 (99%-ое включение дейтерия) или по меньшей мере 6633,3 (включение дейтерия на 99,5%). Фармацевтически приемлемые сольваты в соответствии с изобретением включают такие, в которых растворитель кристаллизации может быть изотопно замещен, например, D2O, d6-ацетон, d6-ДМСО. Соединения по изобретению, то есть соединения формулы (Ia) и формулы (IIa), которые содержат группы, способные действовать как доноры и/или акцепторы для водородных связей, могут быть способны образовывать сокристаллам с подходящими сокристаллическими формами. Эти сокристаллы могут быть получены из соединений формулы (Ia) известными процедурами формирования сокристаллов. Такие процедуры включают размол, нагревание, совозгонку, соплавление или контактирование в соединениях раствора формулы (Ia) с сокристаллической формой в условиях кристаллизации и выделения сформированных таким образом сокристаллов. Подходящие сокристаллические формы включают описанные в WO 2004/078163. Следовательно, изобретение также относится к сокристаллам, включающим соединение формулы (Ia) и формулы (IIa). Способы получения соединений формулы (Ia) или формулы (IIa) Общие процедуры получения соединений формулы (Ia) или формулы (Ia) описаны в примерах,приведенных ниже. В описанных реакциях реактивные функциональные группы, например, гидрокси,амино, имино, тио или карбоксильные группы, когда они желательны в конечном продукте, могут быть защищены во избежание их нежелательного участия в реакциях. Обычные защитные группы могут использоваться в соответствии с обычной практикой (см., например, T.W. Greene and P. G. M. Wuts in "Protective Groups in Organic Chemistry, John Wiley and Sons, 19S1). В некоторых вариантах осуществления соединения формулы (Ia) или формулы (IIa) по изобретению получают в форме соли присоединения с фармацевтически приемлемой кислотой, вводя в реакцию форму свободного основания соединения формулы (Ia) или формулы (IIa) со стехиометрическим количеством подходящей фармацевтически приемлемой органической кислоты или неорганической кислоты или подходящего реактива анионного обмена. В других вариантах осуществления фармацевтически приемлемую соль присоединения с основанием соединений формулы (Ia) или формулы (IIa) получают, вводя в реакцию форму свободной кислоты соединения формулы (Ia) или формулы (IIa) со стехиометрическим количеством подходящего фармацевтически приемлемого органического основания или неорганического основания или подходящего реактива ионного обмена. Такие реакции обычно осуществляют в воде или в органическом растворителе, или в их смеси. Вообще, использование неводной среды, такой как простой эфир, этилацетат, этанол, изопропанол или ацетонитрил, желательно, если оно реально. Альтернативно, формы соли соединений формулы (Ia) или формулы (IIa) получают, используя соли исходных материалов или промежуточных соединений. В некоторых вариантах осуществления соединения формулы (Ia) или формулы (IIa) находятся в форме других солей, включая, но не ограничиваясь ими,оксалаты и трифторацетаты. В некоторых вариантах осуществления формируют полусоли кислот и оснований, например, гемисульфат и соли гемикальция. Такие фармацевтически приемлемые соли присоединения с кислотой соединений формулы (Ia) или формулы (IIa) включают, но не ограничены ими, гидробромид, гидрохлорид, сульфат, нитрат, сукцинат,малеат, формиат, ацетат, адипат, безилат, бикарбонат/карбонат, пропионат, фумарат, цитрат, тартрат,лактат, бензоат, салицилат, глутамат, аспартат, п-толуолсульфонат, бензолсульфонат, метансульфонат,этансульфонат, этандисульфонат, камфорсульфонат, хлортеофиллонат, нафталинсульфонат (например. 2-нафталинсульфонат), гексаноатную соль, бисульфат/сульфат, борат, камсилат, цикламат, эдисилат,эзилат, глюцептат, глюконат, глюкуронат, гексафторфосфат, гибензат, гиппурат, гидрохлорид/хлорид,гидробромид/бромид, гидройодид/йодид, изетионат, лактобионат, лаурилсульфат, малат, малонат, манделат, мезилат, метилсульфат, нафтоат, напсилат, нафтилат, 2-напсилат, никотинат, октадеканоат, олеат,оротат, оксалат, пальмитат, памоат, фосфат/гидрофосфат/дигидрофосфат, полигалактуронат, пироглутамат, сахарат, стеарат, сульфосалицилат, таннат, тозилат, трифторацетат и ксинофоат. Органическая кислота или неорганические кислоты, используемые для формирования некоторых фармацевтически приемлемых солей присоединения с кислотой соединений формулы (Ia) или формулы(IIa), включают, но не ограничены ими, бромисто-водородную кислоту, соляную кислоту, серную кислоту, азотную кислоту, фосфорную кислоту, янтарную кислоту, малеиновую кислоту, малоновую кислоту,миндальную кислоту, муравьиную кислоту, уксусную кислоту, пропионовую кислоту, гликолевую кислоту, щавелевую кислоту, фумаровую кислоту, лимонную кислоту, винную кислоту, молочную кислоту,бензойную кислоту, салициловую кислоту, глутаминовую кислоту, аспарагиновую кислоту, толуолсульфоновую кислоту, сульфосалициловую кислоту, бензолсульфоновую кислоту, метансульфоновую кислоту, этансульфоновую кислоту, нафталинсульфоновую кислоту, такую как 2-нафталинсульфоновая кислота, или гексановую кислоту. Такая фармацевтически приемлемая соль присоединения с основанием соединений формулы (Ia) или формулы (IIa) включает, но не ограничена ими, соли аммония, алюминия, аргинина, бензатина,кальция, холина, меди, диэтиламина, диоламина, глицина, изопропиламина, холината, диэтаноламина,пиперазина, железа, лизина, магния, меглумина, оламина, калия, серебра, натрия, трометамина и цинка. Органические или неорганические основания, используемые для формирования некоторых фармацевтически приемлемых солей присоединения с основанием соединений формулы (Ia) или формулы(IIa), включают, но не ограничены ими, соли, полученные из солей аммония и металлов из столбцов I-XII периодической таблицы, или соли, полученные из первичных, вторичных и третичных аминов, замещенных аминов, включая натуральные замещенные амины, циклических аминов, катионообменных смол и т.п. В некоторых вариантах осуществления формы свободной кислоты или свободного основания соединений формулы (Ia) или формулы (IIa) по изобретению получают из соответствующей соли присоединения с основанием или соли присоединения с кислотой, соответственно. Например, соединение формулы (Ia) в форме соли присоединения с кислотой превращают в соответствующее свободное основание,обрабатывая подходящим основанием (только в качестве примера, раствором гидроксида аммония, гидроксида натрия и т.п.). Например, соединение формулы (Ia) в форме соли присоединения с основанием превращают в соответствующую свободную кислоту, обрабатывая подходящей кислотой (только в качестве примера, соляной кислотой). Списки дополнительных подходящих солей могут быть найдены, например, в "Remington's Pharmaceutical Sciences", 20th ed., Mack Publishing Company, Easton, Pa., (1985); и в "Handbook of PharmaceuticalSalts: Properties, Selection, and Use", Stahl and Wermuth (Wiley-VCH, Weinheim, Германия, 2002. В некоторых вариантах осуществления соединения формулы (Ia) или формулы (IIa) в неокисленной форме получают из N-оксидов соединений формулы (Ia) или формулы (IIa), обрабатывая восстановителем (только в качестве примера, серой, диоксидом серы, трифенилфосфином, боргидридом лития, боргидридом натрия, тркхлоридом, трибромидом фосфора и т.п.) в подходящем инертном органическом растворителе (только в качестве примера, ацетонитриле, этаноле, водном растворе диоксана и т.п.) при температуре от 0 до 80 С. В некоторых вариантах осуществления соединения формулы (Ia) или формулы (IIa) получают как защищенные производные, используя способы, известные специалисту. Подробное описание методик,которые могут быть использованы для получения защитных групп и их удаления, может быть найдено в Т. W. Greene, "Protecting Groups in Organic Chemistry," 3rd edition, John Wiley and Sons, Inc., 1999. В некоторых вариантах осуществления соединения формулы (Ia) или формулы (IIa) получают или формируют в форме сольватов (например, гидратов). В некоторых вариантах осуществления гидраты соединений формулы (Ia) или формулы (IIa) получают перекристаллизацией из смеси вода/органический растворитель, используя органические растворители, такие как диоксин, тетрагидрофуран или метанол. Кроме того, соединения согласно настоящему изобретению, включая их соли, могут также быть получены в форме их гидратов или включать другие растворители, используемые для их кристаллизации. Соединения согласно настоящему изобретению могут образовывать сольваты с фармацевтически приемлемыми растворителями (включая воду); поэтому изобретение охватывает как сольватированные, так и несольватированные формы. Термин "сольват" относится к молекулярному комплексу соединения согласно настоящему изобретению (включая его фармацевтически приемлемые соли) с одной или более молекулами растворителя. Такие молекулы растворителя являются обычно используемыми в области фармации, о которых известно, что они являются безвредными для реципиента, как, например, вода, этанол и т.п. Термин "гидрат" относится к комплексу, где молекулой растворителя является вода. Соединения согласно настоящему изобретению, включая их соли, гидраты и сольваты, могут образовывать полиморфы. Любой асимметрический атом (например, углерода и т.п.) соединения(й) согласно настоящему изобретению может присутствовать в рацемической или энантиомерно обогащенной, например, (R)-, (S)или (R,S)-конфигурации. В некоторых вариантах осуществления каждый асимметрический атом имеет по меньшей мере 50%-ый энантиомерный избыток, по меньшей мере 60%-ый энантиомерный избыток,по меньшей мере 70%-ый энантиомерный избыток, по меньшей мере 80%-ый энантиомерный избыток,по меньшей мере 90%-ый энантиомерный избыток, по меньшей мере 95%-ый энантиомерный избыток или по меньшей мере 99%-ый энантиомерный избыток в (R)- или (S)-конфигурации. Заместители на атомах с ненасыщенными двойными связями могут, если возможно, присутствовать в цис-(Z)- или транс(Е)-форме. Соответственно, в рамках изобретения соединение согласно настоящему изобретению может быть в форме одного из возможных изомеров, ротамеров, атропизомеров, таутомеров или их смесей, например,как в основном чистые геометрические (цис или транс) изомеры, диастереомеры, оптические изомеры(антиподы), рацематы или их смеси. Любые полученные смеси изомеров могут быть разделены на основе физико-химических различий компонентов на чистые или в основном чистые геометрические или оптические изомеры, диастереомеры, рацематы, например, хроматографией и/или фракционной кристаллизацией. Любые полученные рацематы конечных продуктов или промежуточных соединений могут быть разделены на оптические антиподы известными способами, например, разделением их диастереомерных солей, полученных с оптически активной кислотой или основанием, и выделением в свободном состоянии оптически активного кислотного или основного соединения. В частности, основная группа может таким образом использоваться для разделения соединений согласно настоящему изобретению на их оптические антиподы, например, фракционной кристаллизацией соли, образующейся с оптически активной кислотой, например, винной кислотой, дибензоилвинной кислотой, диацетилвинной кислотой, ди-О,О'-птолуоил винной кислотой, миндальной кислотой, яблочной кислотой или камфор-10-сульфоновой кислотой. Рацемические продукты могут также быть разделены хиральной хроматографией, например, высокоэффективной жидкостной хроматографией (ВЭЖХ), с использованием хирального адсорбента. В некоторых вариантах осуществления соединения формулы (Ia) или формулы (IIa) получают в форме их индивидуальных стереоизомеров. В других вариантах осуществления соединения формулы (Ia) или формулы (IIa) по изобретению получают в форме их индивидуальных стереоизомеров, вводя в реакцию рацемическую смесь соединения с оптически активным разделяющим агентом, чтобы сформировать пару диастереоизомерных соединений, разделяя диастереомеры и рекуперируя оптически чистые энантиомеры. В некоторых вариантах осуществления разделение энантиомеров осуществляют, используя ковалентные диастереомерные производные соединений формулы (Ia) или формулы (IIa) или используя диссоциируемые комплексы (например, кристаллические диастереомерные соли). Диастереомеры имеют различные физические свойства (например, температуры плавления, температуры кипения, растворимость, реакционную способность и т.д.) и их легко разделяют, используя эти различия. В некоторых вариантах осуществления диастереомеры разделяют хроматографией, или методиками разделения, основанными на различиях в растворимости. Оптически чистый энантиомер затем рекуперируют, наряду с разделяющим агентом, любыми практическими средствами, которые не приводят к рацемизации. Более подробное описание методик, которые могут быть использованы для разделения стереоизомеров соединений из их рацемической смеси, может быть найдено в Jean Jacques, Andre Collet, Samuel H. Wilen, "Enantiomers, Racemates and Resolutions," John Wiley And Sons, Inc., 1981. Смеси изомеров, доступных согласно изобретению, могут быть разделены способом, известным специалисту, на индивидуальные изомеры; диастереоизомеры могут быть разделены, например, разделением между полифазными смесями растворителей, перекристаллизацией и/или хроматографическим разделением, например, на силикагеле, или, например, жидкостной хроматографией среднего давления на колонке с обратной фазой, и рацематы могут быть разделены, например, формированием солей с оптически чистыми солеобразующими реактивами и разделением смеси полученных таким образом диастереоизомеров, например, посредством фракционной кристаллизации или хроматографией на колонке с оптически активными материалами. В зависимости от выбора исходных материалов и процедур, некоторые варианты осуществления соединений согласно настоящему изобретению присутствуют в форме одного из возможных изомеров или их смесей, например, как чистые оптические изомеры или как смеси изомеров, такие как рацематы и смеси диастереоизомеров, в зависимости от количества асимметрических атомов углерода. Настоящее изобретение включает все такие возможные изомеры, включая рацемические смеси, диастереомерные смеси и оптически чистые формы. Оптически активные (R)- и (S)-изомеры могут быть получены с использованием хиральных синтонов или хиральных реактивов, или разделены с использованием обычных методик. Если соединение содержит двойную связь, заместитель может быть в конфигурации Е или Z. Если соединение содержит двузамещенный циклоалкил, заместитель циклоалкила может иметь цис- или транс-конфигурацию. Все таутомерные формы также включены в рамки изобретения. Соединения формулы (Ia) или формулы (IIa) получают способами, описанными здесь и проиллюстрированными в примерах. Промежуточные соединения и конечные продукты могут быть обработаны и/или очищены согласно стандартным методам, например, с использованием хроматографических способов, способов распределения, (пере)кристаллизации и т.п. Изобретение относится также к таким формам процесса, в которых соединение, которое может быть получено в качестве промежуточного соединения на любой стадии способа, используют как исходный материал, и осуществляют оставшиеся стадии способа, или в которых исходный материал формируется в условиях реакции или используется в форме производного, например, в защищенной форме или в форме соли, или соединение, которое может быть получено способом согласно изобретению, получают в условиях способа и обрабатывают далее in situ. Все исходные материалы, строительные блоки, реактивы, кислоты, основания, осушители, растворители и катализаторы, используемые для синтеза соединений согласно настоящему изобретению, либо являются коммерчески доступными, либо могут быть получены способами органического синтеза, известными специалисту. Неограничивающие примеры схем синтеза, используемых для получения соединений по изобретению, иллюстрируются в реакционных схемах (I)-(IV). Группы R1, R20, R11 и R2 имеют определенные здесь значения. Схема (I) иллюстрирует синтез соединений формулы (Ia) путем сочетания амина с карбоновой кислотой в присутствии основания и реагента сочетания. Только в качестве примера, реагент сочетания представляет собой HATU, и основание представляет собой диизопропилэтиламин. Схема (I) Схема (II) иллюстрирует синтез соединений формулы (IIa) путем сочетания амина с карбоновой кислотой в присутствии основания и реагента сочетания. Только в качестве примера, реагент сочетания представляет собой HATU, и основание представляет собой диизопропилэтиламин. Схема (II) Схема (III) иллюстрирует синтез соединений формулы (Ia) путем формирования оксадиазола из со- 20024293 Схема (IV) иллюстрирует синтез соединений формулы (IIa) путем формирования оксадиазола из соответствующего N'-гидроксиформимидамида и карбоновой кислоты. Схема (IV) Приведенные здесь примеры предлагаются для того, чтобы проиллюстрировать, но не ограничить,соединения формулы (Ia) или формулы (IIa), приведенной здесь, и получение таких соединений. Фармакология и применимость Протеинтирозинкиназы (РТК) играют центральную роль в регуляции разнообразных клеточных процессов и поддержании контроля над клеточной функцией. Протеинкиназы катализируют и регулируют процесс фосфорилирования, в котором ковалентные киназы присоединяют фосфатные группы к белковым или липидным мишеням в ответ на различные внеклеточные сигналы. Примеры таких стимулов включают гормоны, нейромедиаторы, факторы роста и дифференцировки, события клеточного цикла,экологические стрессы и пищевые стрессы. Внеклеточный стимул может воздействовать на одну или более клеточных реакций, связанных с ростом, миграцией, дифференцировкой клеток, секрецией гормонов, активацией факторов транскрипции, сокращением мышц, метаболизмом глюкозы, контролем синтеза белка и регуляцией клеточного цикла. Многие заболевания связаны с патологическими клеточными реакциями, запускаемыми опосредованными протеинкиназой событиями. Эти заболевания включают, но не ограничены ими, аутоиммунные заболевания, воспалительные заболевания, заболевания костей, метаболические нарушения, неврологические и нейродегенеративные заболевания, рак, сердечно-сосудистые заболевания, респираторные заболевания, аллергии и астму, болезнь Альцгеймера и связанные с гормонами заболевания. Примеры протеинтирозинкиназ включают, но не ограничены ими,(а) тирозинкиназы, такие как Irk, IGFR-1, Zap-70, Bmx, Btk, CHK (Csk гомологичная киназа), CSK(b) и серин/треонин киназы, такие как Aurora, c-RAF, SGK, MAP киназы (например, МКК 4, МКК 6 и т.д.), SAPK2, SAPK2, Ark, ATM (1-3), CamK (1-IV), CamKK, Chk1 и 2 (киназы контрольной точки),CKI, CK2, Erk, IKK-I (также IKK- или CHUK), IKK-2 (также IKK-P), Ilk, Jnk (1-3), LimK (1 и 2),MLK3Raf (А, В и С), CDK (1-10), РКС (включая все подтипы РКС), Plk (1-3), NIK, Рак (1-3), PDK1, PKR,RhoK, RIP, RIP-2, GSK3 ( и ), РКА, Р 38, Erk (1-3), PKB (включая все подтипы РКВ) (также AKT-1,AKT-2, АКТ-3 или AKT3-1), IRAKI, FRK, SGK, TAK1 и Tp1-2 (также СОТ). Фосфорилирсвание модулирует или регулирует различные клеточные процессы, такие как пролиферация, рост, дифференцировка, метаболизм, апоптоз, подвижность, транскрипция, трансляция и дру- 21024293 гие процессы трансдукции сигналов. Аберрантная или избыточная активность РТК наблюдалась во многих болезненных состояниях, включая, но не ограничиваясь ими, доброкачественные и злокачественные пролиферативные нарушения, заболевания, возникающие вследствие патологической активации иммунной системы, и заболевания, возникающие вследствие патологической активации нервных систем. Конкретные заболевания и болезненные состояния включают, но не ограничены ими, аутоиммунные нарушения, отторжение аллотрансплантата, заболевание трансплантат против хозяина, диабетическую ретинопатию, хориоидальную неоваскуляризацию вследствие возрастной дегенерации желтого пятна, псориаз, артрит, остеоартрит, ревматоидный артрит, инвазию синовиального паннуса при артрите, рассеянный склероз, миастению гравис, сахарный диабет, диабетическую ангиопатию, ретинопатию недоношенных, инфантильные гемангиомы, немелкоклеточный рак легкого, мочевого пузыря и головы и шеи,рака предстательной железы, рак молочной железы, рак яичника, рак желудка и поджелудочной железы,псориаз, фиброз, ревматоидный артрит, атеросклероз, рестеноз, аутоиммунное заболевание, аллергию,респираторные заболевания, астму, отторжение трансплантата, воспаление, тромбоз, пролиферацию сосудов сетчатки, воспалительное заболевание кишечника, болезнь Крона, неспецифический язвенный колит, заболевания костей, отторжение трансплантата кости или костного мозга, волчанку, хронический панкреатит, кахексию, септический шок, фибропролиферативные и дифференцировочные кожные заболевания или нарушения, заболевания центральной нервной системы, нейродегенеративные заболевания,нарушения или состояния, связанные с повреждением нервов и дегенерации аксонов вследствие повреждения головного или спинного мозга, острый или хронический рак, глазные заболевания, вирусные инфекции, заболевание сердца, заболевания легких или заболевания почек и бронхит. Тирозинкиназы могут быть широко классифицированы как протеинтирозинкиназы рецепторного типа (имеющие внеклеточные, трансмембранные и внутриклеточные домены) или нерецепторного типа(являющиеся полностью внутриклеточными). Тирозинкиназы переносят концевой фосфат АТФ к остаткам тирозина белков, таким образом активируя или инактивируя пути трансдукции сигналов. Патологическая или неконтролируемая активация многих из этих киназ (аберрантная активность протеинтирозинкиназы) в результате, например, сверхэкспрессии или мутации приводит к неконтролируемому росту клеток. Было обнаружено, что многие из протеинтирозинкиназ, будь то рецепторные или нерецепторные тирозинкиназы, участвуют в клеточных путях трансдукции сигналов, участвующих в многочисленных патогенных состояниях, включая, но не ограничиваясь ими, иммуномодуляцию, воспаление или пролиферативные нарушения, такие как рак.c-kit Тучные клетки являются элементами ткани, происходящими из специфической субпопуляции гематопоэтических стволовых клеток, которые экспрессируют антигены CD34, c-kit и CD13. Тучные клетки характеризуются их гетерогенностью не только в отношении тканевой локализации и структуры, но также и на функциональном и гистохимическом уровнях. Незрелые клетки-предшественники тучных клеток циркулируют в кровотоке и дифференцируются в различные ткани. Эти процессы дифференцировки и пролиферации находятся под влиянием цитокинов, одним важным из которых является фактор стволовых клеток (SCF), который также называют лигандом с-kit, стальным фактором или фактором роста тучных клеток. Рецептор фактора стволовых клеток кодируется протоонкогеном, с-kit, который экспрессируется в клетках-предшественниках гематопоэтических клеток, тучных клетках, зародышевых клетках,интерстициальных клетках Cajal (ICC) и некоторых человеческих опухолях, и также экспрессируется негематопоэтическими клетками. Фактор стволовых клеток (SCF), также известный как лиганд c-kit, является первичным регулирующим фактором для роста и функционирования человеческих тучных клеток. Рецептор SCF, рецепторc-kit, является трансмембранной протеинтирозинкиназой рецепторного типа, которая инициирует рост клеток и каскады трансдукции сигналов пролиферации в ответ на связывание SCF. Цитирование рецептора c-kit, опосредуемое SCF, вызывает его димеризацию, сопровождаемую его трансфорилированием,приводя к рекрутированию и активации различных интрацитоплазматических субстратов. Эти активированные субстраты индуцируют множество внутриклеточных путей трансдукции сигналов, ответственных за пролиферацию и активацию клеток. Известно, что эти белки участвуют во многих клеточных механизмах, которые, в случае разрушения, приводят к таким нарушениям, как патологическая пролиферация и миграция клеток, а также воспаление. Связь между тучными клетками, SCF и рецептором c-kit обсуждается в следующих источниках:factor for human mast cells", J. Immunol., 153, 3717-3723, 1994; Meininger, C.J. et al., "The c-kit receptor ligand functions as a mast cell chemoattractant", Blood, 79, 958-963, 1992, и Kinashi, T. et al., "Steel factor and ckit regulate cell-matrix adhesion", Blood, 83, 1033-1038, 1994. В следующих ссылках обсуждается сигнальный путь c-kit и его связь с различными даунстримпутями и связь с заболеваниями, связанными с тучными клетками: Thommes, K. et al., "Identification ofand cell migration", Blood, 99, 3342-3349, 2002. Тучные клетки являются первичными эффекторными клетками в аллергическом воспалении. Тучные клетки также участвуют в других патогенных процессах, таких как острое воспаление и фиброз. Тучные клетки, присутствующие в тканях пациентов, участвуют в генезе или способствуют генезу таких заболеваний, как аутоиммунные заболевания (рассеянный склероз, ревматоидный артрит, воспалительные заболевания кишечника (IBD, аллергические заболевания (аллергический ринит, аллергический синусит, анафилактический синдром, крапивница, болезнь Квинке, аллергический дерматит, аллергический контактный дерматит, узелковая эритема, мультиформная эритема, кожный некротический венулит и воспаление кожи после укуса насекомого, и бронхиальная астма), ангиогенез опухоли, опухоли зародышевых клеток, опухоли тучных клеток, желудочно-кишечные стромальные опухоли, мелкоклеточный рак легкого, меланома, рак молочной железы, острый миелогенный лейкоз, глиобластома, нейробластома и мастоцитоз, воспалительные заболевания, диабет, диабет типа I, диабет типа II, синдром раздраженного кишечника (IBS), нарушения ЦНС и интерстициальный цистит. В этих заболеваниях тучные клетки участвуют в деструкции тканей, высвобождая коктейль различных протеаз и медиаторов, категоризирующихся на три группы: предварительно сформированные гранулоассоциированные медиаторы (гистамин, протеогликаны и нейтральные протеазы), медиаторы-производные липидов (простагландины, тромбоксаны и лейкотриены) и различные цитокины (IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, TNF-, GM-CSF,MIP-L, MIP-1, MIP-2 и IFN-). Высвобождение активированными тучными клетками медиаторов(TNF-, гистамина, лейкотриенов, простагландинов и т.д.), а также протеаз может i) индуцировать воспаление и вазодилатацию и ii) участвовать в процессе деструкции ткани. Кроме того, активация тучных клеток индуцирует разнообразные эффекторные ответы, такие как секреция аллергических медиаторов, протеаз, хемокинов, таких как МСР-1 и RANTES, лейкотриенов,простагландинов и нейротрофинов; и индукция транскрипции генов цитокинов (IL-4, IL-5, IL-6, IL-13,TNF- и GM-CSF). Эти медиаторы способствуют созданию астматического фенотипа за счет своего действия на эндотелиальные клетки, гладкомышечные клетки и фибробласты и на внеклеточную матрицу, и за счет рекрутирования других воспалительных клеток. Астма характеризуется обструкцией воздушного потока, бронхиальной гиперчувствительностью и воспалением дыхательных путей. Воспаление дыхательных путей является ведущим фактором в развитии и укоренении астмы. При аллергической астме аллергены, как считается, инициируют воспалительный процесс, вызывая опосредуемую Т-лимфоцитами реакцию (ТН 2), которая приводит к продукции специфического для аллергена IgE. IgE связывается с его высокоаффинным рецептором FcRI на тучных клетках легких, запуская непосредственную аллергическую реакцию типа 1 (IgE-опосредованную). Таким образом, тучные клетки играют роль в механизме астмы. Активация тучных клеток различными стимулами, такими как стресс, травма, инфекция и нейромедиаторы, также участвует в обострении химического дисбаланса, вызывающего нарушения ЦНС. Более конкретно, дегранулирование тучных клеток стимулируется общими нейромедиаторами, такими как нейротензин, соматостатин, вещество Р и ацетилхолин, факторами роста или выживания, особенно такими как NGF. Тучные клетки, участвующие в ответе на такой стимул, могут быть тучными клетками головного мозга, но также и другими тучными клетками, высвобождающими в кровоток содержимое их гранул, которое, в конечном счете, достигает сенсорных, моторных или мозговых нейронов. После активации тучных клеток, высвобожденные гранулы высвобождают различные факторы, способные к модуляции и изменению нейротрансмиссии и выживанию нейронов. Среди таких факторов важным является серотонин, поскольку увеличение уровня свободного серотонина наблюдалось у пациентов с депрессией. Альтернативно, внезапный выброс серотонина может сопровождаться периодом нехватки серотонина,приводя к боли и мигрени. Как следствие, считается, что тучные клетки усиливают аутокринным или паракринным образом дерегуляцию нейротрансмиссии. Например, индуцированное тревогой или стрессом высвобождение нейромедиаторов, таких как серотонин, активирует тучные клетки, которые, в свою очередь, высвобождают содержимое их гранул, дополнительно способствуя химическому дисбалансу в мозге, приводящему к нарушениям ЦНС. Другие медиаторы, высвобождаемые тучными клетками, могут быть категоризированы на вазоактивные, ноцицептивные, провоспалительные и другие нейромедиаторы. Все вместе, эти факторы могут индуцировать нарушения активности нейронов, вне зависимости от того, являются ли они сенсорными,моторными или нейронами ЦНС. Кроме того, пациенты, страдающие мастоцитозом, более склонны к нарушениям ЦНС, чем нормальная популяция. Это можно объяснить наличием активирующих мутаций в рецепторе с-kit, которые вызывают дегранулирование тучных клеток и выброс факторов, способствующих химическому дисбалансу и изменению нейротрансмиссии. Активация тучных клеток различными лекарственными средствами, включая, но не ограничиваясь ими, производные салициловой кислоты, производные морфина, опиоиды, героин, амфетамины, алкоголь, никотин, анальгетики, анестетики и анксиолитики, приводит к дегранулированию тучных клеток,что участвует в обострении химического дисбаланса, ответственного за привыкание к лекарственному средству и абстиненции. После активации тучных клеток, высвобожденные гранулы высвобождают различные факторы, способные к модуляции и изменению нейротрансмиссии. Среди таких факторов морфин, который связывается или запасается в гранулах тучных клеток. Табачный дым также вызывает высвобождение медиаторов из тучных клеток собаки и модулирует продукцию простагландина, приводящую к астме. Кроме того, пациенты, страдающие мастоцитозом, более склонны к развитию нарушений,связанных с использованием некоторых субстанций, чем нормальная популяция. Это можно объяснить наличием активирующих мутаций в рецепторе c-kit, которые вызывают дегранулирование тучных клеток и выброс факторов, способствующих химическому дисбалансу и изменению нейротрансмиссии. Тучные клетки были также идентифицированы как участвующие в развитии, или способствующие развитию, зависимости от лекарственного средства и абстиненции. Связь между тучными клетками, SCF' и киназой c-kit в различных заболеваниях обсуждается в следующих ссылках: Oliveira et al., "Stem Cell Factor: A Hemopoietic Cytokine with Important Targets in Asthma", Current Drug Targets, 2:313-318, 2003; Puxeddu et al., "Mast cells in allergy and beyond", The International Journal of BiochemistryCell Biology, 35:1601-1607, 2003; Rottem et al., "Mast cells and autoimmunity", Autoimmunity Reviews, 4:21-27, 2005; Woolley, D.E. et al., "The mast cell in inflammatory arthritis", N. нормальных клетках, и нормальная функциональная активность этого продукта гена с-kit важна для поддержания нормального гематопоэза, меланогенеза, генетогенеза и роста и дифференцировки тучных клеток. Ингибирование активности с-kit киназы уменьшает рост и дифференцировку тучных клеток и таким образом опосредует заболевания и/или состояния, связанные с тучными клетками, такие как аутоиммунные заболевания, рассеянный склероз, ревматоидный артрит, воспалительные заболевания кишечника(IBD), респираторные заболевания, аллергические заболевания, аллергический ринит, аллергический синусит, анафилактический синдром, крапивница, болезнь Квинке, аллергический дерматит, аллергический контактный дерматит, узелковая эритема, мультиформная эритема, кожный некротический венулит и воспаление кожи после укуса насекомого, и бронхиальная астма, ангиогенез опухоли, опухоли зародышевых клеток, опухоли тучных клеток, желудочно-кишечные стромальные опухоли, мелкоклеточный рак легкого, мланома, рак молочной железы, острый миелогенный лейкоз, глиобластома, нейробластома и мастоцитоз, воспалительные заболевания, диабет, диабет типа I, диабет типа II, синдром раздраженного кишечника (IBS), нарушения ЦНС и интерстициальный цистит. В добавление к ее важности для нормальной физиологической активности клеток, киназа c-kit играет роль в биологических аспектах некоторых форм человеческого рака, и нерегулируемая активность сkit киназы участвует в патогенезе человеческого рака и в некоторых типах опухолей. Пролиферация роста опухолевых клеток, опосредуемая с-kit, может быть вызвана специфической мутацией полипептида сkit, которая приводит к лиганднезависимой активации или аутокринной стимуляции рецептора. В первом случае мутации, которые вызывают конститутивную активацию активности с-kit киназы в отсутствие связывания SCF, участвуют в злокачественных случаях человеческого рака, включая опухоли зародышевых клеток, опухоли тучных клеток, желудочно-кишечные стромальные опухоли, мелкоклеточный рак легкого, меланому, рак молочной железы, острый миелогенный лейкоз, глиобластому, нейробластому и мастоцитоз. Тест пролиферации для оценки эффективности ингибиторов с-kit и ингибиторов PDGFR описан вleukemia blasts", Blood, 97 (5): 1413-1421, 2001. В этом тесте используют клетки MO7e, которые являются человеческой промегакариоцитарной линией клеток лейкоза, которые зависят от SCF для пролиферации. Эти ссылки в комбинации с Berlin et al., Ekland et al., и Miyachi et al. (процитированными выше) показывают, что было обнаружено, что ингибитор c-kit киназы, скринированный с помощью этого теста пролиферации, может лечить ревматоидный артрит и астму. Кроме того, позже было обнаружено, что соединение, которое было первоначально оценено на его эффективность как ингибитора c-kit с использованием теста пролиферации, основанного на клеткахBa/F3 и производных от клеток Ba/F3 (см. WO 2004/01903), является эффективным в лечении опухолей тучных клеток и астмы (см. Bellamy F. et al., "Pharmacokinetics of masitinib in cats", Vet. Res. Commun.,June 16 (epub) 2009; Hahn K.A. et al., "Mastinib is safe and effective for treatment of canine mact cell tumours',J. Vet. Intern. Med., 22, 1301-1309, 2008 и Humbert M. et al., "Mastinib, a c-kit/PDGF receptor tyrosine kinaseinhibitor, improves disease control in severe corticosteroid-dependent asthmatics", 64, 1194-1201, 2009). Рецептор c-kit имеет существенную гомологию с рецептором PDGF и рецептором CSF-1 (c-Fms). Семейство рецепторов тромбоцитарного фактора роста (PDGF)PDGF (Тромбоцитарный Фактор роста) представляет собой распространенный фактор роста, который играет важную роль как в нормальном росте, так и в патологической пролиферации клеток. Например, это наблюдается при онкогенезе и при заболеваниях гладкомышечных клеток кровеносных сосудов,например, при атеросклерозе и тромбозе. Семейство фактора роста PDGF состоит из PDGF-A, PDGF-B,PDGF-C и PDGF-D, которые образуют либо гомо-, либо гетеродимеры (АА, АВ, ВВ, СС, DD), которые связываются с рецепторами протеинтирозинкиназы PDGFR- и PDGFR-. Димеризация факторов роста является предпосылкой для активации киназы, поскольку мономерные формы неактивны. Обе изоформы рецептора димеризуются после связывания, приводя к трем возможным комбинациям рецептора,PDGFR-, PDGFR- и PDGFR-. Фактор роста АА связывается только с -, фактор роста ВВ может связываться с -, - и -, факторы роста СС и АВ специфически взаимодействуют с - и -, и фактор роста DD связывается с -. PDGF-рецептор играет важную роль в поддержании, росте и развитии гематопоэтических и негематопоэтических клеток. Ключевыми даунстрим-медиаторами трансдукции сигналов PDGFR являются пути Ras/митогенактивируемой протеинкиназы (МАРК), PI-3 киназы и фосфолипазы- (PLCg). Члены семейства МАРК регулируют различные биологические функции путем фосфорилирования целевых молекул (факторы транскрипции и другие киназы) и таким образом вносят свой вклад в регуляцию клеточных процессов,- 25024293 таких как пролиферация, дифференцировка, апоптоз и иммунный ответ. Активация PI-3 киназы генерирует PIP3, который функционирует как вторичный мессенджер, активирующий даунстримтирозинкиназы Btk и Itk, киназы Ser/Thr PDK1 и Akt (PKB). Активация Akt участвует в выживании, пролиферации и росте клеток. После активации PLC гидролизует свой субстрат, PtdIns(4,5)P2, и образует два вторичных мессенджера, диацилглицерол и Ins(1,4,5)Р 3, который стимулирует внутриклеточные процессы, такие как пролиферация, ангиогенез и подвижность клеток.PDGFR экспрессируется на ранних стволовых клетках, тучных клетках, миелоидных клетках, мезенхимальных клетках и гладкомышечных. клетках. Только PDGFR- участвует в миелоидных лейкозах обычно как партнер транслокации с Tel, белком HIP1 (Huntingtin interacting protein) или Rabaptin5. Активирующие мутации в киназном домене PDGFR- связаны с желудочно-кишечными стромальными опухолями (GIST). Некоторые варианты соединений формулы (Ia) и формулы (IIa) по изобретению ингибируют активность рецептора PDGF (PDGFR и PDGFR) и активность с-kit киназы и могут быть использованы для лечения заболеваний, которые отвечают на ингибирование киназы рецептора PDGF. Поэтому некоторые соединения формулы (Ia) и формулы (IIa) по изобретению могут быть использованы для лечения опухолевых заболеваний, таких как глиомы, саркомы, опухоли предстательной железы, мелкоклеточный рак. легкого и опухоли толстого кишечника, молочной железы и яичника. Кроме того, некоторые варианты соединений формулы (Ia) и формулы (IIa) по изобретению могут быть использованы для лечения таких нарушений, как тромбоз, псориаз, склеродермия, фиброз, астма, метаболические нарушения и гиперэозинофилия. Соединения формулы (Ia) и формулы (IIa) по изобретению также эффективны против заболеваний, связанных с миграцией и пролиферацией гладкомышечных клеток сосудов, таких как рестеноз и атеросклероз. Пациенты со облитеративным бронхиолитом (ОВ), хроническим отторжением аллогенных трансплантатов легкого, часто демонстрируют повышенную концентрацию PDGF в жидкостях бронхоальвеолярного лаважа. В некоторых вариантах осуществления соединения формулы (Ia) и формулы (IIa) по изобретению демонстрируют полезные эффекты в лечении нарушений, возникающих в результате трансплантации, например, аллогенной трансплантации, особенно отторжения ткани, таких как облитеративный бронхиолит (ОВ). В некоторых вариантах осуществления соединения формулы (Ia) и формулы (IIa) по изобретению могут быть использованы для защиты стволовых клеток, например, для борьбы с гемотоксическим эффектом химиотерапевтических средств, таких как 5-фторурацил. Соединения формулы (Ia) и формулы (IIa) по изобретению и их фармацевтически приемлемые соли,фармацевтически приемлемые сольваты (например, гидраты), N-оксидные производные, защищенные производные, индивидуальные изомеры и смесь изомеров являются ингибиторами активности с-kit киназы или ингибиторами активности с-kit киназы и PDGFR ( и ) киназы. В некоторых вариантах осуществления соединения формулы (Ia) и формулы (IIa) по изобретению и их фармацевтически приемлемые соли, фармацевтически приемлемые сольваты (например, гидраты), N-оксидные производные, защищенные производные, индивидуальные изомеры и смесь изомеров являются ингибиторами активности c-kit киназы и активности PDGFR ( и ) киназы. В других вариантах осуществления соединения формулы(Ia) и формулы (IIa) по изобретению и их фармацевтически приемлемые соли, фармацевтически приемлемые сольваты (например, гидраты), N-оксидные производные, защищенные производные, индивидуальные изомеры и смесь изомеров являются ингибиторами любой активности c-kit киназы. Такие соединения формулы (Ia) и формулы (IIa) по изобретению и их фармацевтически приемлемые соли, фармацевтически приемлемые сольваты (например, гидраты), N-оксидные производные, защищенные производные, индивидуальные изомеры и смесь изомеров могут быть использованы для лечения заболеваний или нарушений, в которых киназа c-kit, или киназа c-kit и PDGFR ( и/или ), участвует в патологии и/или симптоматологии заболевания или нарушения. Такие заболевания или нарушения включают, но не ограничены ими, заболевание, связанное с тучными клетками, воспалительные заболевания, респираторные заболевания, аллергические нарушения, фиброзные заболевания, метаболические нарушения, аутоиммунные заболевания, нарушение ЦНС, нейродегенеративное нарушение, неврологические заболевания,дерматологические заболевания, реакция "трансплантант против хозяина", болевое состояние, опухолевое нарушение, сердечно-сосудистое заболевание и рак. Неограничивающие примеры таких заболеваний включают астму, аллергический ринит, аллергический синусит, бронхиальную астму, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), легочную артериальную гипертензию (РАН), идиопатическую артериальную гипертензию (IPAH), первичную легочную гипертензию (РРН), легочный фиброз, фиброз печени, кардиальный фиброз, склеродермию, крапивницу, дерматозы, аллергический дерматит, аллергический контактный дерматит, диабет, диабет типа I, диабет типа II, ревматоидный артрит, множественный склероз,цитопении (только в качестве примера, анемию, лейкопению, нейтропению, тромбоцитопению, гранулоктопению, pancytoia и идиопатическую тромбоцитопеническую пурпуру), системную красную волчанку, хроническое обструктивное заболевание легких (COPD), респираторный дистресс-синдром взрослых(РДСВ), неспецифический язвенный колит, болезнь Крона, псориаз, лимфомы (только в качестве примера, В- и Т-клеточные лимфомы), миелодиспластический синдром, рак молочной железы, рак поджелудочной железы, сосочковый рак щитовидной железы, рак яичника, аденокистозную карциному человека,немелкоклеточный рак легкого, секреторный рак молочной железы, врожденную фибросаркому, врожденную аденомиосаркому, острый миелогенный лейкоз, метастаз хронического миелоидного лейкоза,связанную с раком боль, нейробластому, остеосаркому, меланому, костные метастазы, опухоль молочной железы, почек, легкого, предстательной железы, поджелудочной железы, толстого кишечника, яичника,щитовидной железы, колоректальные опухоли, нейронные опухоли, опухоли матки, желудочнокишечные стромальные опухоли (GIST), глиомы, саркомы, ангиогенез опухоли, опухоли зародышевых клеток, опухоли тучных клеток, глиобластому, нейробластому, мастоцитоз, остеопороз, гиперэозинофилию, рестеноз, атеросклероз, анафилактический синдром, болезнь Квинке, узелковую эритему, мультиформную эритему, кожный некротический венулит, воспаление кожи после укуса насекомого, нарушения ЦНС и интерстициальный цистит. В некоторых вариантах осуществления соединения формулы (Ia) и формулы (IIa) по изобретению и их фармацевтически приемлемые соли, фармацевтически приемлемые сольваты (например, гидраты), Nоксидные производные, защищенные производные, индивидуальные изомеры и смесь изомеров могут быть использованы для лечения заболеваний или нарушений, в которых киназа c-kit участвует в патологии и/или симптоматологии заболевания или нарушения. Неограничивающие примеры таких заболеваний включают астму, аллергический ринит, аллергический синусит, бронхиальную астму, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника (IBD), легочную артериальную гипертензию (РАН), идиопатическую артериальную гипертензию (IPAH), первичную легочную гипертензию (РРН), легочный фиброз, фиброз печени, кардиальный фиброз, склеродермию, крапивницу, дерматозы, аллергический дерматит, аллергический контактный дерматит, диабет, диабет типа I, диабет типа II, ревматоидный артрит, множественный склероз, цитопении (только в качестве примера, анемию,лейкопению, нейтропению, тромбоцитопению, гранулоктопению, pancytoia и идиопатическую тромбоцитопеническую пурпуру), системную красную волчанку, хроническое обструктивное заболевание легких (COPD), респираторный дистресс-синдром взрослых (РДСВ), неспецифический язвенный колит, болезнь Крона, псориаз, лимфомы (только в качестве примера, В- и Т-клеточные лимфомы), миелодиспластический синдром, рак молочной железы, рак поджелудочной железы, сосочковый рак щитовидной железы, рак яичника, аденокистозную карциному человека, немелкоклеточный рак легкого, секреторный рак молочной железы, врожденную фибросаркому, врожденную аденомиосаркому, острый миелогенный лейкоз, метастаз хронического миелоидного лейкоза, связанную с раком боль, нейробластому, остеосаркому, меланому, костные метастазы, опухоль молочной железы, почек, легкого, предстательной железы,поджелудочной железы, толстого кишечника, яичника, щитовидной железы, колоректальные опухоли,нейронные опухоли, опухоли матки, желудочно-кишечные стромальные опухоли (GIST), глиомы, саркомы, ангиогенез опухоли, опухоли зародышевых клеток, опухоли тучных клеток, глиобластому, нейробластому, мастоцитоз, остеопороз, гиперэозинофилию, рестеноз, атеросклероз, анафилактический синдром, болезнь Квинке, узелковую эритему, мультиформную эритему, кожный некротический венулит,воспаление кожи после укуса насекомого, нарушения ЦНС и интерстициальный цистит. В некоторых вариантах осуществления соединения формулы (Ia) и формулы (IIa) по изобретению и их фармацевтически приемлемые соли, фармацевтически приемлемые сольваты (например, гидраты), Nоксидные производные, защищенные производные, индивидуальные изомеры и смесь изомеров могут быть использованы для лечения заболеваний или нарушений, в которых киназа c-kit и киназа PDGFR ( и/или ) участвуют в патологии и/или симптоматологии заболевания или нарушения. Неограничивающие примеры таких заболеваний включают астму, аллергический ринит, аллергический синусит, бронхиальную астму, синдром раздраженного кишечника (IBS), воспалительное заболевание кишечника(IBD), легочную артериальную гипертензию (РАН), идиопатическую артериальную гипертензию (IPAH),первичную легочную гипертензию (РРН), легочный фиброз, фиброз печени, кардиальный фиброз, склеродермию, крапивницу, дерматозы, аллергический дерматит, аллергический контактный дерматит, диабет, диабет типа I, диабет типа II, ревматоидный артрит, множественный склероз, цитопении (только в качестве примера, анемию, лейкопению, нейтропению, тромбоцитопению, гранулоктопению, pancytoia и идиопатическую тромбоцитопеническую пурпуру), системную красную волчанку, хроническое обструктивное заболевание легких (COPD), респираторный дистресс-синдром взрослых (РДСВ), неспецифический язвенный колит, болезнь Крона, псориаз, лимфомы (только в качестве примера, В- и Т-клеточные лимфомы), миелодиспластический синдром, рак молочной железы, рак поджелудочной железы, сосочковый рак щитовидной железы, рак яичника, аденокистозную карциному человека, немелкоклеточный рак легкого, секреторный рак молочной железы, врожденную фибросаркому, врожденную аденомиосаркому,острый миелогенный лейкоз, метастаз хронического миелоидного лейкоза, связанную с раком боль, нейробластому, остеосаркому, меланому, костные метастазы, опухоль молочной железы, почек, легкого,предстательной железы, поджелудочной железы, толстого кишечника, яичника, щитовидной железы,колоректальные опухоли, нейронные опухоли, опухоли матки, желудочно-кишечные стромальные опу- 27024293 холи (GIST), глиомы, саркомы, ангиогенез опухоли, опухоли зародышевых клеток, опухоли тучных клеток, глиобластому, нейробластому, мастоцитоз, остеопороз, гиперэозинофилию, рестеноз, атеросклероз,анафилактический синдром, болезнь Квинке, узелковую эритему, мультиформную эритему, кожный некротический венулит, воспаление кожи после укуса насекомого, нарушения ЦНС и интерстициальный цистит. Другой аспект изобретения включает способы лечения пролиферативно-клеточных заболеваний,включающие введение в систему или з организм пациента, для которых существует необходимость такого лечения, эффективного количества соединения формулы (Ia) и формулы (IIa) или их фармацевтически приемлемых солей или фармацевтических композиций; причем пролиферативно-клеточное заболевание представляет собой лимфому, остеосаркому, меланому или опухоль молочной железы, почки, предстательной железы, колоректальную опухоль, опухоль щитовидной железы, яичника, поджелудочной железы, нейронов, легкого, матки или желудочно-кишечную опухоль. В некоторых вариантах осуществления соединения формулы (Ia) и формулы (IIa), их фармацевтически приемлемые соли, сольваты, N-оксиды и изомеры, фармацевтические композиции и/или комбинации по изобретению используются в лечении заболеваний и/или нарушений, включая, но не ограничиваясь ими, астму, бронхиальную астму, аллергическую астму, эндогенную астму, экзогенную астму, астму физического усилия, лекарственную астму (включая аспирин и NSAID-индуцированную) и индуцированную пылью астму, хроническое обструктивное заболевание легких (COPD); бронхит, включая инфекционный и эозинофильный бронхит; эмфизему; бронхоэктаз; муковисцидоз; саркоидоз; легкое фермера и родственные заболевания; гиперсенситивный пневмонит; фиброз легкого, включая криптогенный фиброзирующий альвеолит, идиопатические интерстициальные пневмонии, фиброз, усложняющий противоопухолевую терапию и хроническую инфекцию, включая туберкулез и аспергиллез и другие микозы; осложнения после трансплантации легкого; васкулитические и тромбические нарушения сосудистой сети легкого и легочную гипертензию; противокашлевую активность, включая лечение хронического кашля,ассоциированного с воспалительными и секреторными состояниями дыхательных путей, и ятрогенного кашля; острый и хронический ринит, включая медикаментозный ринит и вазомоторный ринит; хронический и сезонный аллергический ринит, включая вазомоторный ринит (поллиноз); носовой полипоз; острую вирусную инфекцию, включая насморк, и инфекции, вызванные респираторным синцитиальным вирусом, вирусом гриппа, коронавирусом (включая атипичную пневмонию) и аденовирусом. В некоторых вариантах осуществления соединения формулы (Ia) и формулы (IIa), их фармацевтически приемлемые соли, сольваты, N-оксиды и изомеры, фармацевтические композиции и/или комбинации по изобретению используются в лечении дерматологическое нарушений, включая, но не ограничиваясь ими, псориаз, аллергический дерматит, контактный дерматит или другие экзематозные дерматозы и реакции гиперчувствительности замедленного типа; фито- и фотодерматит; себорейный дерматит, герпетиформный дерматит, плоский лишай, склерозирующий и атрофический лишай, гангренозную пиодермию, саркоид кожи, базальноклеточный рак, актинический кератоз, дисковидную красную волчанку,пузырчатку, пемфигоид, буллезный эпидермолиз, крапивницу, болезнь Квинке, васкулит, токсические эритемы, кожные эозинофилии, очаговую алопецию, алопецию по мужскому типу, синдром Свита, синдром Вебера-Крисчена, мультиформную эритему; целлюлит, как инфекционный, так и неинфекционный; панникулит; кожные лимфомы, немеланомный рак кожи и другие диспластические поражения; лекарственные нарушения, включая фиксированные лекарственные сыпи. В некоторых вариантах осуществления соединения формулы (Ia) и формулы (IIa), их фармацевтически приемлемые соли, сольваты, N-оксиды и изомеры, фармацевтические композиции и/или комбинации по изобретению используются в лечении ревматоидного артрита, синдрома раздраженного кишечника, системной красной волчанки, рассеянного склероза, тиреоидита Хашимото, болезни Крона, воспалительного заболевания кишечника (IBD), болезнь Грейвса (диффузный токсический зоб), Аддисоновой болезни, сахарного диабета, идиопатической тромбоцитопенической пурпуры, эозинофильного фасциита, синдрома гипер-IgE, антифосфолипидного синдрома и синдрома Сезари. В некоторых вариантах осуществления соединения формулы (Ia) и формулы (IIa), их фармацевтически приемлемые соли, сольваты, N-оксиды и изомеры, фармацевтические композиции и/или комбинации по изобретению используются в лечении рака, включая, но не ограничиваясь ими, опухоли предстательной железы, молочной железы, легкого, яичника, поджелудочной железы, кишечника и толстого кишечника, желудка, кожи и головного мозга и злокачественные процессы, поражающие костный мозг(включая лейкоз) и лимфопролиферативные системы, лимфомы, такие как ходжкинские и неходжкинские; включая профилактику и лечение метастатического заболевания и рецидивов опухоли и паранеопластических синдромов. Изобретение относится к соединениям формулы (Ia) и формулы (IIa), их фармацевтически приемлемым солям, фармацевтически приемлемым сольватам (например, гидратам), N-оксидным производным, защищенным производным, индивидуальным изомерам и смеси изомеров, и к фармацевтическим композициям, содержащим по меньшей мере одно соединение формулы (Ia) или формулы (IIa) или их фармацевтически приемлемые соли, фармацевтически приемлемые сольваты (например, гидраты), Nоксидные производные, защищенные производные, индивидуальные изомеры или смесь изомеров, для применения в формировании активности c-kit киназы, или киназы c-kit и PDGFR (активность киназыи/или ), и таким образом используются в профилактике или лечении заболеваний и/или нарушений,связанных с активностью c-kit киназы, или киназы c-kit и PDGFR (активность киназыи/или ). Также изобретение относится к способам лечения пациента, страдающего заболеванием и/или нарушением, связанным с активностью c-kit киназы, причем способ включает введение пациенту эффективного количества соединения формулы (Ia) или формулы (IIa) или их фармацевтически приемлемых солей, фармацевтически приемлемых сольватов (например, гидратов), N-оксидных производных, защищенных производных, индивидуальных изомеров или смеси изомеров, либо индивидуально, либо как часть фармацевтической композиции, как описано здесь. Также изобретение относится к способам лечения пациента, страдающего заболеванием и/или нарушением, связанным с активностью киназы c-kit и PDGFR (активность киназыи/или ), причем способ включает введение пациенту эффективного количества соединения формулы (Ia) или формулы (IIa) или их фармацевтически приемлемых солей, фармацевтически приемлемых сольватов (например, гидратов), N-оксидных производных, защищенных производных, индивидуальных изомеров или смеси изомеров, либо индивидуально, либо как часть фармацевтической композиции, как описано здесь. Изобретение относится к применению соединения формулы (Ia) или формулы (IIa) или их фармацевтически приемлемых солей, фармацевтически приемлемых сольватов (например, гидратов), Nоксидных производных, защищенных производных, индивидуальных изомеров или смеси изомеров в получении лекарственного средства для лечения заболевания или нарушения, связанного с активностьюc-kit киназы. Также изобретение относится к применению соединения формулы (Ia) или формулы (IIa),или их фармацевтически приемлемых солей, фармацевтически приемлемых сольватов (например, гидратов), N-оксидных производных, защищенных производных, индивидуальных изомеров или смеси изомеров в получении лекарственного средства для лечения заболевания или нарушения, связанного с активностью киназы с-kit и PDGFR (активность киназыи/или ). Кроме того, изобретение относится к применению соединения, имеющего формулу (Ia) или формулу (IIa), или их фармацевтически приемлемых солей или фармацевтических композиций, и в случае необходимости в комбинации с терапевтически эффективным количеством второго средства, в получении лекарственного средства для лечения заболевания или состояния, модулируемого активностью киназы,особенно c-kit или c-kit и PDGFR ( и ). В соответствии с предшествующим, настоящее изобретение также относится к способу для профилактики или лечения любого из заболеваний или нарушений, описанных выше, у пациента, включающему введение указанному пациенту терапевтически эффективного количества соединения формулы (Ia) или формулы (IIa) или его фармацевтически приемлемей соли. Для любого из вышеупомянутых применений необходимая дозировка варьирует в зависимости от способа введения, конкретного состояния,подлежащего лечению, и желаемого эффекта (см. "Введение и фармацевтические композиции", ниже). Введение и фармацевтические композиции Для терапевтических применений соединений формулы (Ia) и формулы (IIa) или их фармацевтически приемлемых солей, описанных здесь, такие соединения вводят в терапевтически эффективных количествах индивидуально или в составе фармацевтической композиции. Соответственно, изобретение относится к фармацевтическим композициям, которые включают по меньшей мере одно соединение формулы (Ia) или формулы (IIa) или их фармацевтически приемлемые сольваты соли, и один или более фармацевтически приемлемых носителей, разбавителей или эксципиентов. Кроме того, такие соединения и композиции вводят отдельно или в комбинации с одним или более дополнительными терапевтическими средствами. Способ введения таких соединений и композиций включает, но не ограничен ими, пероральное введение, ректальное введение, чрескожное введение, парентеральное, внутривенное введение, интравитреальное введение, внутримышечное введение, легочное введение, введение ингаляцией, внутриносовое введение, топическое введение, глазное введение или ушное введение. В некоторых вариантах осуществления способ введения таких соединений и композиций представляет собой пероральное введение. В других вариантах осуществления способ введения таких соединений и композиций представляет собой легочное введение, введение ингаляцией или внутриносовое введение. Терапевтически эффективное количество варьирует в зависимости от, среди прочего, показанного заболевания, серьезности заболевания, возраста и относительного состояния здоровья пациента, потенциала вводимого соединения, способа введения и желательного лечения. В некоторых вариантах осуществления суточная доза соединения формулы (Ia) и формулы (IIa), удовлетворительные результаты были получены системно при суточных дозах от приблизительно 0,03 до 2,5 мг/кг массы тела. В некоторых вариантах осуществления суточная доза соединения формулы (Ia) и формулы (IIa), вводимого ингаляцией, находится в диапазоне от 0,05 микрограммов на килограмм массы тела (мкг/кг) до 100 микрограммов на килограмм массы тела (мкг/кг). В других вариантах осуществления суточная доза соединения формулы (Ia) и формулы (IIa), вводимого перорально, находится в диапазоне от 0,01 микрограммов на килограмм массы тела (мкг/кг) до 100 миллиграммов на килограмм массы тела (мг/кг). Обозначенная суточная доза для крупного млекопитающего, например, человека, находится в диапазоне от приблизительно
МПК / Метки
МПК: A61K 31/437, A61P 29/00, A61P 11/00, A61P 17/00, C07D 471/04, A61P 3/00
Метки: с-kit, композиции, соединения, качестве, ингибиторов, киназы
Код ссылки
<a href="https://eas.patents.su/30-24293-soedineniya-i-kompozicii-v-kachestve-ingibitorov-s-kit-kinazy.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения и композиции в качестве ингибиторов с-kit киназы</a>
Предыдущий патент: Новое антитело против ngf человека
Следующий патент: Способ выщелачивания металлсодержащего сульфидного концентрата
Случайный патент: Нить, стойкая к порезам












