Двузамещенные октагидропиррол[3,4-c]пирролы в качестве модуляторов орексиновых рецепторов
Номер патента: 22766
Опубликовано: 29.02.2016
Авторы: Чай Венин, Свенсон Девин М., Шайрман Брок Т., Стокинг Эмили М., Савалль Брэд М., Ли Киев С., Шах Чандравадан Р., Сойод-Джонсон Акинола, Стротер Кэтлин К., Пиппел Дэниел Дж., Рудольф Дейл А., Летавич Майкл А.
Формула / Реферат
1. Соединение формулы (I)
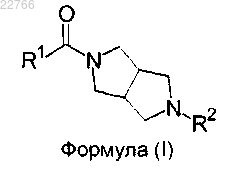
где R1 выбран из группы, состоящей из:
A) фенила, возможно замещенного одним или двумя заместителями Ra и замещенного Rb в орто-позиции;
Ra независимо выбран из галогена, -С1-4алкила, -С1-4алкокси и -NO2, где два соседних Ra заместителя могут объединяться и формировать шестичленное ароматическое кольцо;
Rb выбран из группы, состоящей из:
a) галогена, -С1-4алкокси, -С1-4алкила, -CF3, -OCF3 или -CN;
b) 5-членного гетероарильного кольца, содержащего один атом кислорода или один атом серы;
c) 5-6-членного гетероарильного кольца, содержащего один, два или три атома азота, и, возможно, содержащего один атом кислорода, где кольцо возможно замещено галогеном или -C1-4алкилом; и
d) фенила, возможно замещенного галогеном, -СН3 или -CF3,
B) пиридина, возможно замещенного одним или двумя заместителями Rc и замещенного Rd, где Rd расположен рядом с местом присоединения R1;
Rc является С1-4алкилом;
Rd выбран из группы, состоящей из:
a) 5-6-членного гетероарильного кольца, выбранного из 1Н-1,2,3-триазол-1-ила, 2Н-1,2,3-триазол-2-ила, 1Н-пиразол-5-ила, 3-метил-1,2,4-оксадиазол-5-ила, пиридинила, 3-метилпиридин-2-ила; 1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ила, фенила и пиримидин-2-ила; и
b) -CF3, -Br и -С1-4алкокси;
C) 5-членного гетероарильного кольца, выбранного из группы, состоящей из 2-метил-1,3-тиазолила, 1Н-пиразол-5-ила, оксазолила, изоксазолила, тиофен-2-ила и фуран-2-ила, каждый из которых замещен фенилом, который возможно замещен -F; и
D) 5-13-членного арильного или гетероарильного кольца, выбранного из 3-метилфуран-2-ила, 9Н-флуоренила, хинолинила, циннолинила; 3-(1Н-пиррол-1-ил)тиофен-2-ила, 8-[1,2,3]-триазол-2-ил-нафталин-1-ила, 2,3-дигидро-1,4-бензодиоксин-5-ила, 1Н-индол-7-ила, 4-фторнафталин-1-ила и нафталин-1-ила;
R2 выбран из группы, состоящей из:
A) 6-членного гетероарильного кольца, содержащего два атома азота, замещенных одним или несколькими заместителями, независимо выбранными из галогена, -С1-4алкила, -CD3, -D, -C1-4алкокси, циклопропила, морфолин-4-ила, -СО2С1-4алкила, -СО2Н, -СН2ОН, -С(O)N(С1-4алкила)2, -CF3, -CN, -ОН, -NO2, -N(С1-4алкила)2, фенила, фуран-2-ила, тиофен-2-ила, 1Н-пиразол-4-ила и пирролидин-1-ила;
B) пиридина, замещенного одним или двумя заместителями, независимо выбранными из галогена, -С1-4алкила, -С1-4алкокси и -CF3;
C) 9-членного гетероарильного кольца, выбранного из бензоксазол-2-ила, 6-фтор-1,3-бензотиазолила, 1,3-бензотиазолила, 6-метокси-1,3-бензотиазолила, 6-метил-1,3-бензотиазолила, 6-хлор-бензотиазол-2-ила и 4-метил-6,7-дигидро-5Н-циклопента[d]пиримидинила;
D) 10-членного гетероарильного кольца, выбранного из хиноксалин-2-ила, 3-метилхиноксалин-2-ила, 6,7-дифторхиноксалин-2-ила, 3-(трифторметил)хиноксалинила, хинолинила, 4-метилхинолинила и 6-фторхиназолин-2-ила; и
E) 4-метил-1,3,5-триазин-2-ила или 2-метилпиримидин-4(3Н)-онила;
или его фармацевтически приемлемая соль.
2. Соединение формулы (II)
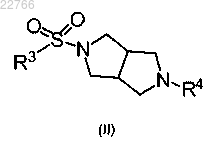
где R3 является фенилом, возможно замещенным -С1-4алкокси или фенилом; и
R4 выбран из (5-трифторметил)пиридин-2-ила, (5-трифторметил)пиримидин-2-ила, 4,6-диметилпиримидин-2-ила и хиноксалин-2-ила;
или его фармацевтически приемлемая соль.
3. Соединение по п.1, где R1 представляет собой фенил, где Ra независимо выбран из -F, -I, -Cl, -ОСН3, -ОСН2, СН3, -СН3-СН(СН3)2, -С(СН3)3 и -NO2.
4. Соединение по п.1, где R1 представляет собой фенил, а Rb выбран из -Br, -F, -I, -С1-4алкила, -ОСН3,
-ОСН2СН3, -CN, -CF3 и OCF3.
5. Соединение по п.1, где R1 представляет собой фенил, где Ra выбран из -F, -Cl, -СН3, -С(СН3)3, -ОСН3 и -ОСН2СН3, a Rb выбран из -Br, -F, -I, -С1-4алкила, -ОСН3, -ОСН2СН3, -CN, -CF3 и OCF3.
6. Соединение по п.1, где R1 представляет собой фенил, где Rb представляет собой 2-тиофен-2-ил или 2-фуран-2-ил.
7. Соединение по п.1, где R1 представляет собой фенил, где Rb выбран из фенила, 3-хлорфенила, 4-фторфенила, 3-фторфенила, 4-метилфенила и 4-трифторметилфенила.
8. Соединение по п.1, где R1 представляет собой фенил, где Rb выбран из 1Н-пиррол-1-ила, 1Н-пиразол-1-ила, 1Н-пиразол-5-ила, 1Н-имидазол-2-ила, 1-метил-1Н-имидазол-2-ила, 1Н-1,2,3-триазол-1-ила, 2Н-1,2,3-триазол-2-ила, 2Н-1,2,3-триазол-1-ила, 1Н-1,2,4-триазол-5-ила, 2Н-1,2,4-триазол-1-ила, 2Н-1,2,4-триазол-3-ила, 4Н-1,2,4-триазол-3-ила, 4Н-1,2,4-триазол-4-ила, 1-метил-1Н-1,2,4-триазол-3-ила, 1-метил-1Н-1,2,4-триазол-5-ила и 1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ила.
9. Соединение по п.1, где R1 представляет собой фенил, где Rb выбран из пиридин-2-ила, 3-хлорпиридин-2-ила, 3-фторпиридин-2-ила, 3-метилпиридин-2-ила, 4-метилпиридин-2-ила, 5-метилпиридин-2-ила, 6-метилпиридин-2-ила, 2-пиридин-3-ила и 2-пиримидин-2-ила.
10. Соединение по п.1, где R1 представляет собой фенил, где Rb выбран из 3-метил-1,2,4-оксадиазол-5-ила и оксазол-2-ила.
11. Соединение по п.1, где R1 представляет собой фенил, где Ra представляет собой галоген, -С1-4алкил или -С1-4алкокси, a Rb представляет собой триазол или пиримидин, замещенный или незамещенный галогеном или -С1-4алкилом.
12. Соединение по п.1, где R1 представляет собой
(1-метилэтил)-2-(2Н-1,2,3-триазол-2-ил)фенил, 2-(1Н-1,2,3-триазол-1-ил)фенил, 2-(2Н-1,2,3-триазол-2-ил)фенил, 2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил, 2-метил-6-(2Н-1,2,3-триазол-2-ил)фенил, 3-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил, 3-фтор-2-(1Н-1,2,3-триазол-1-ил)фенил, 3-метокси-2-(1Н-1,2,3-триазол-1-ил)фенил, 3-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил, 3-метил-2-(2Н-1,2,3-триазол-2-ил)фенил, 3-метил-2-(1Н-1,2,3-триазол-1-ил)фенил, 4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил, 4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил, 4-метокси-2-(1Н-1,2,3-триазол-2-ил)фенил, 4,5-диметокси-2-[1,2,3]триазол-1-илфенил, 4,5-диметокси-2-[1,2,3]триазол-2-ил-фенил, 5-[1,2,3]триазол-2-ил-бензо[1,3]диоксол-4-ил, 5-хлор-2-(2Н-1,2,3-триазол-2-ил)фенил, 5-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил, 5-иод-2-(2Н-1,2,3-триазол-2-ил)фенил, 5-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил, 5-метил-2-(2Н-1,2,3-триазол-2-ил)фенил, 1-[1,2,3]триазол-2-илнафталин-2-ил, 2-(1Н-1,2,4-триазол-1-ил)фенил, 2-(1Н-1,2,4-триазол-5-ил)фенил, 2-(1-метил-1Н-1,2,4-триазол-5-ил)фенил, 2-(1-метил-1Н-1,2,4-триазол-3-ил)фенил, 2-(4Н-1,2,4-триазол-3-ил)фенил, 2-(4Н-1,2,4-триазол-4-ил)фенил, 2-(3-метил-1,2,4-оксадиазол-5-ил)фенил, 3-фтор-2-(3-метил-1,2,4-оксадиазол-5-ил)фенил, 2-фтор-6-(3-метил-1,2,4-оксадиазол-5-ил)фенил, 4,5-дифтор-2-(4Н-1,2,4-триазол-4-ил)фенил, 2-фтор-6-пиримидин-2-илфенил, 2-(пиримидин-2-ил)пиридин-3-ил, 3-фтор-2-пиримидин-2-илфенил, 4-фтор-2-(пиримидин-2-ил)фенил, 4-метокси-2-(пиримидин-2-ил)фенил, 5-фтор-2-пиримидин-2-илфенил и 5-метил-2-пиримидин-2-илфенил.
13. Соединение по п.1, где R1 представляет собой пиридинил, где Rd выбран из -CF3, -Br и -ОСН2СН2СН3.
14. Соединение по п.1, где R1 представляет собой пиридинил, где Rd выбран из 1Н-пиразол-5-ила, 2Н-1,2,3-триазол-1-ила, 2Н-1,2,3-триазол-2-ила, 4Н-1,2,3-триазол-1-ила, 1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ила, 3-метилпиридин-2-ила и 3-метил-1,2,4-оксадиазол-5-ила.
15. Соединение по п.1, где R1 представляет собой пиридинил, где Rd выбран из 1Н-пиразол-5-ила, 2Н-1,2,3-триазол-1-ила и 2Н-1,2,3-триазол-2-ила.
16. Соединение по п.1, где R1 представляет собой 1-фенил-1Н-пиразол-5-ил, 3-фенилтиофен-2-ил, 3-фенилфуран-2-ил, 5-фенил-1,3-оксазол-4-ил, 5-фенилизоксазол-4-ил, 5-(2-фторфенил)-2-метил-1,3-тиазол-4-ил, 2-метил-5-фенилтиазол-4-ил или 5-(4-фторфенил)-2-метил-1,3-тиазол-4-ил.
17. Соединение по п.1, где R1 выбран из 3-метилфуран-2-ила, 9Н-флуоренила, хинолинила, циннолинила; 3-(1Н-пиррол-1-ил)тиофен-2-ила, 8-[1,2,3]-триазол-2-ил-нафталин-1-ила, 2,3-дигидро-1,4-бензодиоксин-5-ила, 1Н-индол-7-ила, 4-фторнафталин-1-ила и нафталин-1-ила, a R2 выбран из 4,6-диметилпиримидин-2-ила, 4-фенилпиримидин-2-ила, хиноксалинила и 4-метоксипиримидин-2-ила.
18. Соединение по п.1, где R2 представляет собой пиримидинил, замещенный одним или несколькими заместителями, независимо выбранными из -F, -Cl, -D, -CD3, -CH3, этила, изопропила, пропила, трет-бутила, -CF3, -OCH3, -N(CH3)2, -CN, -ОН, -СН2ОН, -NO2, -CO2CH3, -CO2H, C(O)N(CH3)2, фенила, фуран-2-ила, тиофен-2-ила, 1Н-пиразол-4-ила, циклопропила, пирролидин-1-ила и морфолин-4-ила.
19. Соединение по п.1, где R2 представляет собой 4,6-диметилпиримидин-2-ил, 4,5-диметилпиримидин-2-ил, 4,6-диметоксипиримидин-2-ил, 4-фенилпиримидин-2-ил, 4-фуран-2-илпиримидин-2-ил, 4-метилпиримидин-2-ил, 4-метоксипиримидин-2-ил, 4-тиофен-2-илпиримидин-2-ил, N,N,6-триметилпиримидин-4-амин, 4-(трифторметил)пиримидин-2-ил, 4,5,6-триметилпиримидин-2-ил, 4-(трифторметил)пиримидин-5-карбоновую кислоту, 4-(трифторметил)пиримидин-5-карбоновую кислоту, 5-нитропиримидин-2-ил, 6-метилпиримидин-4-карбоновую кислоту, N,N-диметил-4-(трифторметил)пиримидин-5-карбоновую кислоту, N,N,6-триметилпиримидин-карбоновую кислоту, 6-метилпиримидин-4-карбонитрил, 4,6-бис(трифторметил)пиримидин-2-ил, 6-метилпиримидин-4-ол, 4-(фуран-2-ил)-6-метилпиримидин-2-ил, 5-фтор-4-метилпиримидин-2-ил, 5-фторпиримидин-2-ил, 4-метокси-6-метилпиримидин-2-ил, 4-этил-6-метилпиримидин-2-ил, 4-изопропил-6-метилпиримидин-2-ил, 4-трет-бутил-6-метилпиримидин-2-ил, 4-циклопропил-6-метилпиримидин-2-ил, 4-метил-6-морфолин-4-илпиримидин-2-ил, 5-хлор-4-метилпиримидин-2-ил, 5-хлор-4,6-диметилпиримидин-2-ил, 5-фтор-4,6-диметилпиримидин-2-ил, 5-трифторметилпиримидин-2-ил, 4,6-бис[(2Н3)метил](2Н)пиримидин-2-ил и 5-этил-4,6-диметилпиримидин-2-ил.
20. Соединение по п.1, где R2 представляет собой пиримидинил, замещенный одним или несколькими заместителями, независимо выбранными из -Cl, -F, -CH3, -CF3, -N(CH3)2, -D и -CD3.
21. Соединение по п.1, где R2 представляет собой 4,6-диметилпиримидин-2-ил, 4,5-диметилпиримидин-2-ил, 4,6-диметоксипиримидин-2-ил, 4-метилпиримидин-2-ил, 4-метоксипиримидин-2-ил, N,N,6-триметилпиримидин-4-амин, 4-(трифторметил)пиримидин-2-ил, 4,5,6-триметилпиримидин-2-ил, 4,6-бис(трифторметил)пиримидин-2-ил, 6-метилпиримидин-4-ол, 5-фтор-4-метилпиримидин-2-ил, 5-фторпиримидин-2-ил, 4-метокси-6-метилпиримидин-2-ил, 5-хлор-4-метилпиримидин-2-ил, 5-хлор-4,6-диметилпиримидин-2-ил, 5-фтор-4,6-диметилпиримидин-2-ил, 5-трифторметилпиримидин-2-ил и 4,6-бис [(2Н3)метил](2Н)пиримидин-2-ил.
22. Соединение по п.1, где R2 представляет собой пиразинил или триазинил, замещенный одним или более -СН3.
23. Соединение по п.1, где R2 представляет собой пиридинил, замещенный одним или несколькими заместителями, независимо выбранными из -F, -ОСН3, -ОСН2СН3, -СН3 и -CF3.
24. Соединение по п.1, где R2 выбран из бензооксазол-2-ила, 2-метилпиримидин-4(3Н)-она и 4-метил-6,7-дигидро-5Н-циклопент[d]пиримидинила, a R1 представляет собой фенил, замещенный в орто-позиции Rb, где Rb представляет собой 2Н-1,2,3-триазол-2-ил, 2Н-1,2,3-триазол-1-ил, 3-метил-1,2,4-оксадиазол-5-ил или 2-пиримидин-2-ил.
25. Соединение по п.1, где R2 выбран из хиноксалин-2-ила, 3-метилхиноксалин-2-ила, 6,7-дифторхиноксалин-2-ила, 3-(трифторметил)хиноксалина, 4-метилхинолинила и 6-фторхиназолин-2-ила, a R1 представляет собой фенил, замещенный в орто-позиции Rb, где Rb представляет собой 2Н-1,2,3-триазол-2-ил, 2Н-1,2,3-триазол-1-ил, 3-метил-1,2,4-оксадиазол-5-ил или 2-пиримидин-2-ил.
26. Соединение по п.2, где R3 представляет собой бифенил или 2-метоксифенил, a R4 представляет собой (5-трифторметил)пиридин-2-ил, (5-трифторметил)пиримидин-2-ил, 4,6-диметилпиримидин-2-ил или хиноксалин-2-ил.
27. Соединение по п.1, где R1 выбран из 2-(1Н-1,2,3-триазол-1-ил)фенила, 2-(2Н-1,2,3-триазол-2-ил)фенила, 2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенила, 2-метил-6-(2Н-1,2,3-триазол-2-ил)фенила, 3-фтор-2-(2Н-1,2,3-триазол-2-ил)фенила, 3-фтор-2-(1Н-1,2,3-триазол-1-ил)фенила, 3-метокси-2-(1Н-1,2,3-триазол-1-ил)фенила, 3-метокси-2-(2Н-1,2,3-триазол-2-ил)фенила, 3-метил-2-(2Н-1,2,3-триазол-2-ил)фенила, 3-метил-2-(1Н-1,2,3-триазол-1-ил)фенила, 4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенила, 4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенила, 4-метокси-2-(1Н-1,2,3-триазол-2-ил)фенила, 4,5-диметокси-2-[1,2,3]триазол-1-ил-фенила, 4,5-диметокси-2-[1,2,3]триазол-2-ил-фенила, 5-хлор-2-(2Н-1,2,3-триазол-2-ил)фенила, 5-фтор-2-(2Н-1,2,3-триазол-2-ил)фенила, 5-метокси-2-(2Н-1,2,3-триазол-2-ил)фенила, 5-метил-2-(2Н-1,2,3-триазол-2-ил)фенила, 2-(1Н-1,2,4-триазол-1-ил)фенила, 2-(1Н-1,2,4-триазол-5-ил)фенила, 2-(1-метил-1Н-1,2,4-триазол-5-ил)фенила, 2-(1-метил-1Н-1,2,4-триазол-3-ил)фенила, 2-(4Н-1,2,4-триазол-3-ил)фенила, 2-(4Н-1,2,4-триазол-4-ил)фенила, 2-(3-метил-1,2,4-оксадиазол-5-ил)фенила, 3-фтор-2-(3-метил-1,2,4-оксадиазол-5-ил)фенила, 2-фтор-6-(3-метил-1,2,4-оксадиазол-5-ил)фенила, 4,5-дифтор-2-(4Н-1,2,4-триазол-4-ил)фенила, 2-фтор-6-пиримидин-2-илфенила, 2-(пиримидин-2-ил)пиридин-3-ила, 3-фтор-2-пиримидин-2-илфенила, 4-фтор-2-(пиримидин-2-ил)фенила, 4-метокси-2-(пиримидин-2-ил)фенила, 5-фтор-2-пиримидин-2-илфенила и 5-метил-2-пиримидин-2-илфенила, a R2 выбран из группы, состоящей из 4,6-диметилпиримидин-2-ила, 4,5-диметилпиримидин-2-ила, 4,6-диметоксипиримидин-2-ила, 4-метилпиримидин-2-ила, 4-метоксипиримидин-2-ила, N,N,6-триметилпиримидин-4-амина, 4-(трифторметил)пиримидин-2-ила, 4,5,6-триметилпиримидин-2-ила, 4,6-бис(трифторметил)пиримидин-2-ила, 6-метилпиримидин-4-ола, 5-фтор-4-метилпиримидин-2-ила, 5-фторпиримидин-2-ила, 4-метокси-6-метилпиримидин-2-ила, 5-хлор-4-метилпиримидин-2-ила, 5-хлор-4,6-диметилпиримидин-2-ила, 5-фтор-4,6-диметилпиримидин-2-ила, 5-трифторметилпиримидин-2-ила и 4,6-бис[(2Н3)метил](2Н)пиримидин-2-ила.
28. Соединение по п.1, где R1 выбран из 3-фтор-2-(3-метил-1,2,4-оксадиазол-5-ил)фенила, 6-фтор-2-(2Н-1,2,3-триазол-2-ил)фенила, 4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенила и 3-[1,2,3]триазол-2-ил-пиридин-2-ила, a R2 выбран из 4,6-диметилпиримидин-2-ила, 5-фтор-4,6-диметилпиримидин-2-ила и 5-фтор-4-метилпиримидин-2-ила.
29. Соединение, выбранное из
4-[5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-6-метокси-N,N-диметилпиримидин-2-амина;
N,N-диметил-6-[5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-2-(трифторметил)пиримидин-4-амина;
6-[5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-N,N-диметил-2-(трифторметил)пиримидин-4-амина;
4-[5-{[5-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-6-метокси-N,N-диметилпиримидин-2-амина;
4-метокси-N,N-диметил-6-[5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропирроло[3,4-с]пиррол-2(1Н)-ил]пиримидин-2-амина;
6-[5-{[4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-N,N-диметил-2-(трифторметил)пиримидин-4-амина;
4-[5-{[4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-6-метокси-N,N-диметилпиримидин-2-амина;
2-(4,6-диметилпиримидин-2-ил)-5-{[3-(1Н-пиррол-1-ил)тиофен-2-ил]карбонил}октагидропиррол[3,4-с]пиррола;
6-[5-{[5-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-N,N-диметил-2-(трифторметил)пиримидин-4-амина;
2-(4,6-диметилпиримидин-2-ил)-5-[(1-фенил-1Н-пиразол-5-ил)карбонил]октагидропиррол[3,4-с]пиррола;
8-{[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]карбонил}хинолина;
2-(4,6-диметилпиримидин-2-ил)-5-[(3-фенилтиофен-2-ил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(3-фенилфуран-2-ил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[2-(1Н-1,2,4-триазол-5-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[3-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{5-[(2,4-диметоксифенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-6-фтор-1,3-бензотиазола;
2-{5-[(2,4-диметоксифенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-1,3-бензотиазола;
2-[5-{[2-(1Н-пиразол-1-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]хиноксалина;
2-{5-[(2-тиофен-2-илфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-{5-[(2-метилнафталин-1-ил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-(2,3-дигидро-1,4-бензодиоксин-5-илкарбонил)-5-(4-фенилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4-фенилпиримидин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4-фенилпиримидин-2-ил)-5-{[2-(1Н-пиразол-1-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4-фенилпиримидин-2-ил)-5-{[2-(1Н-пиррол-1-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-[(2-метилнафталин-1-ил)карбонил]-5-(4-фенилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(5-хиноксалин-2-ил-гексагидропиррол[3,4-с]пиррол-2-карбонил)бензонитрила;
2-[5-{[2-(1Н-пиррол-1-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]хиноксалина;
2-{5-[(4'-фторбифенил-2-ил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-{5-[(3'-фторбифенил-2-ил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-{5-[(2-метилфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-(бифенил-2-илкарбонил)-5-(4-фуран-2-илпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4-метилпиримидин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-{5-[(2-тиофен-2-илфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хинолина;
2-(4-фуран-2-илпиримидин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-{5-[(2-этилфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-[5-(1Н-индол-7-илкарбонил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]хиноксалина;
2-[(2-тиофен-2-илфенил)карбонил]-5-(4-тиофен-2-илпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(бифенил-2-илкарбонил)-5-(4-тиофен-2-илпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-[2-(1-метил-1Н-имидазол-2-ил)фенил]метанона;
2-[(2-бромофенил)карбонил]-5-(4-фенилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-{5-[(3'-хлорбифенил-2-ил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-{5-[(2-бромофенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-(4,6-диметилпиримидин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(бифенил-2-илкарбонил)-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4-метоксипиримидин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
6-фтор-2-{5-[(2-тиофен-2-илфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-1,3-бензотиазола;
2-(4,6-диметилпиримидин-2-ил)-5-[(2-метилнафталин-1-ил)карбонил]октагидропиррол[3,4-с]пиррола;
2-[(3'-фторбифенил-2-ил)карбонил]-5-(4-метилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4-метоксипиримидин-2-ил)-5-[(2-метилнафталин-1-ил)карбонил]октагидропиррол[3,4-с]пиррола;
2-[(2-метилнафталин-1-ил)карбонил]-5-(4-метилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(3'-фторбифенил-2-ил)карбонил]-5-(4-метоксипиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(3'-фторбифенил-2-ил)карбонил]октагидропиррол[3,4-с]пиррола;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-фторфенил)метанона;
2-(4-метоксипиримидин-2-ил)-5-[(4'-метилбифенил-2-ил)карбонил]октагидропиррол[3,4-с]пиррола;
2-[(3'-хлорбифенил-2-ил)карбонил]-5-(4-метоксипиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(2-этоксинафталин-1-ил)карбонил]-5-(4-метоксипиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(4-фторнафталин-1-ил)карбонил]-5-(4-метоксипиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4-метоксипиримидин-2-ил)-5-(нафталин-1-илкарбонил)октагидропиррол[3,4-с]пиррола;
2-[(2-этоксифенил)карбонил]-5-(4-метоксипиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(2-метоксинафталин-1-ил)карбонил]-5-(4-метоксипиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(бифенил-2-илкарбонил)-5-[4-(1Н-пиразол-4-ил)пиримидин-2-ил]октагидропиррол[3,4-с]пиррола;
2-[4-(1Н-пиразол-4-ил)пиримидин-2-ил]-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(3,6-диметилпиразин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(бифенил-2-илкарбонил)-5-(3,5-диметилпиразин-2-ил)октагидропиррол[3,4-с]пиррола;
2-метил-3-{5-[(2-тиофен-2-илфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-[5-(бифенил-2-илкарбонил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-3-метилхиноксалина;
2-(4,6-диметилпиримидин-2-ил)-5-{[2-(1Н-пиразол-1-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметоксипиримидин-2-ил)-5-[(2-фтор-6-пиримидин-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(2-пиридин-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметоксипиримидин-2-ил)-5-[(2-пиридин-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметоксипиримидин-2-ил)-5-[(5-фтор-2-пиримидин-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметоксипиримидин-2-ил)-5-{[5-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(2-фтор-6-пиримидин-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(5-фтор-2-пиримидин-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[5-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(2-этилфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(2-этоксинафталин-1-ил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметоксипиримидин-2-ил)-5-{[2-(1Н-пиразол-1-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(5-фенил-1,3-оксазол-4-ил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(5-фенилизоксазол-4-ил)карбонил]октагидропиррол[3,4-с]пиррола;
[5-(2-изопропил-6-метилпиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-[1,2,3]триазол-2-илфенил)метанона;
2-[(2-бромофенил)карбонил]-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметоксипиримидин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-[5-{[2-(4Н-1,2,4-триазол-3-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]хиноксалина;
2-[5-{[2-(4Н-1,2,4-триазол-3-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-1,3-бензоксазола;
2-(4-метилпиримидин-2-ил)-5-{[2-(4Н-1,2,4-триазол-3-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(2-этоксифенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[4-фтор-2-(трифторметил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(4-фторнафталин-1-ил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[2-(1-метилэтил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(3-метокси-2-метилфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-(нафталин-1-илкарбонил)октагидропиррол[3,4-с]пиррола;
2-[5-{[2-(4Н-1,2,4-триазол-3-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-3-(трифторметил)хиноксалина;
2-метил-3-[5-{[2-(4Н-1,2,4-триазол-3-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]хиноксалина;
2-[6-метил-2-(трифторметил)пиримидин-4-ил]-5-{[2-(4Н-1,2,4-триазол-3-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-[6-метил-2-(трифторметил)пиримидин-4-ил]-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-[6-метил-2-(трифторметил)пиримидин-4-ил]октагидропиррол[3,4-с]пиррола;
2-{[4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-[6-метил-2-(трифторметил)пиримидин-4-ил]октагидропиррол[3,4-с]пиррола;
2-(6-метилпиразин-2-ил)-5-{[5-метил-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(3,6-диметилпиразин-2-ил)-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(5-метил-2-пиримидин-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(3,6-диметилпиразин-2-ил)-5-[(5-метил-2-пиримидин-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(3,6-диметилпиразин-2-ил)-5-{[4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[5-иодо-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
4-[5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-N,N-диметил-6-(трифторметил)пиримидин-2-амина;
2-(4,6-диметилпиримидин-2-ил)-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенила]карбонил}октагидропиррол[3,4-с]пиррола;
N,N-диметил-4-{5-[(5-метил-2-пиримидин-2-илфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-6-(трифторметил)пиримидин-2-амина;
4-{5-[(5-фтор-2-пиримидин-2-илфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-N,N-диметил-6-(трифторметил)пиримидин-2-амина;
4-[5-{[5-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-N,N-диметил-6-(трифторметил)пиримидин-2-амина;
4-[5-{[4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-N,N-диметил-6-(трифторметил)пиримидин-2-амина;
2-[(5-метил-2-пиримидин-2-илфенил)карбонил]-5-[6-метил-2-(трифторметил)пиримидин-4-ил]октагидропиррол[3,4-с]пиррола;
2-[(5-фтор-2-пиримидин-2-илфенил)карбонил]-5-(4-фенилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-{[5-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-[6-метил-2-(трифторметил)пиримидин-4-ил]октагидропиррол[3,4-с]пиррола;
[5-(2,6-диметилпиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(5-фтор-2-[1,2,3]триазол-2-илфенил)метанона;
4-{5-[(2-фтор-6-пиримидин-2-илфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-N,N-диметил-6-(трифторметил)пиримидин-2-амина;
2-[(2-фтор-6-пиримидин-2-илфенил)карбонил]-5-[6-метил-2-(трифторметил)пиримидин-4-ил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
N,N,6-триметил-2-[5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]пиримидин-4-амина;
N,N,4-триметил-6-[5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]пиримидин-2-амина;
N,N-диметил-4-[5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-6-(трифторметил)пиримидин-2-амина;
2-(2,6-диметилпиримидин-4-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
[5-(3,6-диметилпиразин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(5-метил-2-[1,2,3]триазол-2-илфенил)метанона;
2-[5-{[5-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-N,N,6-триметилпиримидин-4-амина;
2-(5-метоксипиридин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-[(2-этоксинафталин-1-ил)карбонил]-5-(4-фенилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-{[5-метил-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-(4-фенилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
(4-хлор-2-[1,2,3]триазол-2-ил-фенил)-[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
2-(4,6-диметоксипиримидин-2-ил)-5-{[5-метил-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[5-метил-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4-фенилпиримидин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[5-(2-фторфенил)-2-метил-1,3-тиазол-4-ил]карбонил}октагидропиррол[3,4-с]пиррола;
2-[(2-тиофен-2-илфенил)карбонил]-5-[6-(трифторметил)пиридин-2-ил]октагидропиррол[3,4-с]пиррола;
2-(6-метилпиридин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4-метилпиримидин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4-метилпиридин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(6-метоксипиридин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметоксипиримидин-2-ил)-5-[(2-тиофен-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-{5-[(2-тиофен-2-илфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-1,3-бензоксазола;
2-[(2-тиофен-2-илфенил)карбонил]-5-[3-(трифторметил)пиридин-2-ил]октагидропиррол[3,4-с]пиррола;
[5-(4-фенилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-[2-(4Н-[1,2,4]триазол-3-ил)фенил]метанона;
2-(4,6-диметоксипиримидин-2-ил)-5-{[5-(2-фторфенил)-2-метил-1,3-тиазол-4-ил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4-тиофен-2-илпиримидин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-[5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-1,3-бензоксазола;
2-{5-[(2-этоксинафталин-1-ил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-{5-[(5-фтор-2-пиримидин-2-илфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-(6-этоксипиридин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-[(5-фтор-2-пиримидин-2-илфенил)карбонил]-5-[4-(трифторметил)пиримидин-2-ил]октагидропиррол[3,4-с]пиррола;
2-[5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]хиноксалина;
2-[(5-фтор-2-пиримидин-2-илфенил)карбонил]-5-(4-метоксипиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4-фуран-2-илпиримидин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-фторпиридин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-[4-(трифторметил)пиримидин-2-ил]октагидропиррол[3,4-с]пиррола;
2-(4-метоксипиримидин-2-ил)-5-{[2-(1Н-1,2,4-триазол-5-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(3,6-диметилпиразин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4-метоксипиримидин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[5-хлор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-{[4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-(6-метилпиразин-2-ил)октагидропиррол[3,4-с]пиррола;
2-{[4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-(4-метоксипиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4,6-диметоксипиримидин-2-ил)-5-{[4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(5-метокси-2-[1,2,3]триазол-2-илфенил)метанона;
(2-фтор-6-[1,2,3]триазол-2-илфенил)-[5-(4-метоксипиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
6-хлор-2-{5-[(2,4-диметоксифенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-1,3-бензотиазола;
2-(бифенил-2-илкарбонил)-5-(4-фенилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-{5-[(2,6-диметоксифенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}хиноксалина;
2-[(2,6-диметоксифенил)карбонил]-5-(4-фенилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(2,4-диметоксифенил)карбонил]-5-(4-фенилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[5-(бифенил-2-илкарбонил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]хиноксалина;
2-[5-(бифенил-2-илкарбонил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-1,3-бензотиазола;
2-{5-[(2,4-диметоксифенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-4-метилхинолина;
2-{5-[(2,4-диметоксифенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-6-метокси-1,3-бензотиазола;
2-{5-[(2,4-диметоксифенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-6-метил-1,3-бензотиазола;
2-(бифенил-2-илкарбонил)-5-(6-метилпиридин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(бифенил-2-илкарбонил)-5-(4-метилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[5-(бифенил-2-илкарбонил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]хинолина;
2-[5-(бифенил-2-илкарбонил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-6-фтор-1,3-бензотиазола;
2-(бифенил-2-илкарбонил)-5-(4-метоксипиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[5-(бифенил-2-илкарбонил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-4-метилхинолина;
(2,4-диметоксифенил)-[5-(4-метоксипиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
(5-бензооксазол-2-илгексагидропиррол[3,4-с]пиррол-2-ил)-(2-метоксифенил)метанона;
(2-пиридин-3-илфенил)-(5-хиноксалин-2-илгексагидропиррол[3,4-с]пиррол-2-ил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-[2-(1Н-имидазол-2-ил)фенил]метанона;
(5-бензооксазол-2-илгексагидропиррол[3,4-с]пиррол-2-ил)-(2,4-диметоксифенил)метанона;
(5-бензооксазол-2-илгексагидропиррол[3,4-с]пиррол-2-ил)бифенил-2-илметанона;
(2,4-диметоксифенил)-[5-(6-метилпиридин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
(2,4-диметоксифенил)-[5-(4-метилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
бифенил-2-ил-[5-(6-метоксибензотиазол-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
бифенил-2-ил-[5-(6-метилбензотиазол-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
[5-(6-хлорбензотиазол-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2,6-диметоксифенил)метанона;
бифенил-2-ил-[5-(6-хлорбензотиазол-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
(2,4-диметоксифенил)-(5-хиноксапин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил)метанона;
(5-бензооксазол-2-илгексагидропиррол[3,4-с]пиррол-2-ил)-(2,6-диметоксифенил)метанона;
(4'-метилбифенил-2-ил)-(5-хиноксалин-2-ил-гексагидропиррол[3,4-с]пиррол-2-ил)метанона;
(5-хиноксалин-2-илгексагидропиррол[3,4-с]пиррол-2-ил)-(4'-трифторметилбифенил-2-ил)метанона;
(4'-метилбифенил-2-ил)-[5-(4-фенилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
[5-(4-фенилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(4'-трифторметилбифенил-2-ил)метанона;
(4-метокси-2-метилфенил)-(5-хиноксалин-2-илгексагидропиррол[3,4-с]пиррол-2-ил)метанона;
(3'-хлорбифенил-2-ил)-[5-(4-фенилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
(2-метоксифенил)-[5-(4-метоксипиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
(2-метоксифенил)-[5-(4-метилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-метоксифенил)метанона;
2-[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-карбонил]бензонитрила;
циннолин-4-ил-[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
(5-фтор-2-пиримидин-2-илфенил)-[5-(6-метил-2-трифторметилпиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-[1,2,3]триазол-1-илфенил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-[1,2,4]триазол-1-илфенил)метанона;
[5-(4,6-диметоксипиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(3-фенилпиридин-2-ил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(3-фенилпиридин-2-ил)метанона;
[5-(6-метил-2-пропилпиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-[1,2,3]триазол-2-илфенил)метанона;
[5-(2-метилпиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-[1,2,3]триазол-2-илфенил)метанона;
[5-(6-метилпиразин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-[1,2,3]триазол-2-илфенил)метанона;
[5-(3,6-диметилпиразин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(5-фтор-2-пиримидин-2-илфенил)метанона;
[5-(3,6-диметилпиразин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-[2-(2Н-[1,2,4]триазол-3-ил)фенил]метанона;
[5-(2-пирролидин-1-ил-6-трифторметилпиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-[1,2,3]триазол-2-илфенил)метанона;
2-(2,6-диметилпиримидин-4-ил)-5-{[5-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-нитро-6-[1,2,3]триазол-2-илфенил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-фуран-2-илфенил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-метил-5-фенилтиазол-4-ил)метанона;
2-[(2,3-диметилфенил)карбонил]-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(3-фтор-2-метилфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[5-фтор-2-(трифторметил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-[(4-хлор-2-метоксифенил)карбонил]-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(5-хлор-2-метилфенил)карбонил]-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(2,5-диметилфенил)карбонил]-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(2,6-диметилфенил)карбонил]-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-[(5-фтор-2-метилфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-[(2,4-диметилфенил)карбонил]-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(2,5-диэтоксифенил)карбонил]-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(2,6-диэтоксифенил)карбонил]-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-[(2-хлор-6-метилфенил)карбонил]-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-фтор-2-(пиримидин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-йодофенил)метанона;
2-(4,6-диметилпиримидин-2-ил)-5-{[2-(трифторметил)пиридин-3-ил]карбонил}октагидропиррол[3,4-с]пиррола;
(2-бромопиридин-3-ил)(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(2-(пиримидин-2-ил)пиридин-3-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(2-(1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ил)пиридин-3-ил)метанона;
(2-(1Н-пиразол-5-ил)пиридин-3-ил)(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(2-(2Н-1,2,3-триазол-2-ил)пиридин-3-ил)(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(3-фтор-2-(пиримидин-2-ил)фенил)(5-(4,5,6-триметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(3-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил)(5-(4,5,6-триметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил)(5-(4,5,6-триметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(3-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил)(5-(6-фторхиназолин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(3-фтор-2-(пиримидин-2-ил)фенил)(5-(6-фторхиназолин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(6,7-дифторхиноксалин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил)метанона;
(5-(6,7-дифторхиноксалин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(5-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил)метанона;
(5-(6,7-дифторхиноксалин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил)метанона;
(2-бром-3-фторфенил)(5-(6-фторхиназолин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-фтор-2-(5-метилпиридин-2-ил)фенил)метанона;
(2-бромопиридин-3-ил)(5-(4,5,6-триметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(2-(1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ил)пиридин-3-ил)(5-(4,5,6-триметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(2-(1Н-пиразол-5-ил)пиридин-3-ил)(5-(4,5,6-триметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
6-[5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-2-метилпиримидин-4(3Н)-она;
2-(2,6-диметилпиримидин-4-ил)-5-{[5-(4-фторфенил)-2-метил-1,3-тиазол-4-ил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[5-(4-фторфенил)-2-метил-1,3-тиазол-4-ил]карбонил}октагидропиррол[3,4-с]пиррола;
6-[5-{[5-(4-фторфенил)-2-метил-1,3-тиазол-4-ил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-2-метилпиримидин-4(3Н)-она;
6-{5-[(5-фтор-2-пиримидин-2-илфенил)карбонил]гексагидропиррол[3,4-с]пиррол-2(1Н)-ил}-2-метилпиримидин-4(3Н)-она;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-фтор-2-(2Н-1,2,3-триазол-2-ил)фенил)метанона;
(5-(4,6-диметоксипиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(2-метил-6-(2Н-1,2,3-триазол-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-метил-2-(2Н-1,2,3-триазол-2-ил)фенил)метанона;
(2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил)(5-(5-нитропиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
метил 2-(5-(2-фтор-6-(2Н-1,2,3-триазол-2-ил)бензоил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)-4-(трифторметил)пиримидин-5-карбоксилата;
2-(5-(2-фтор-6-(2Н-1,2,3-триазол-2-ил)бензоил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)-4-(трифторметил)пиримидин-5-карбоновой кислоты;
(2-(4Н-1,2,4-триазол-4-ил)фенил)(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
2-(5-(2-фтор-6-(2Н-1,2,3-триазол-2-ил)бензоил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)-6-метилпиримидин-4-карбоновой кислоты;
(4,5-дифтор-2-(4Н-1,2,4-триазол-4-ил)фенил)(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-метил-2-(1Н-1,2,3-триазол-1-ил)фенил)метанона;
2-(5-(2-фтор-6-(2Н-1,2,3-триазол-2-ил)бензоил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)-N,N,6-триметилпиримидин-4-карбоксамида;
2-(5-(2-фтор-6-(2Н-1,2,3-триазол-2-ил)бензоил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)-N,N-диметил-4-(трифторметил)пиримидин-5-карбоксамида;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(мезитил)метанона;
(2,3-дифторфенил)(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-метокси-2-(пиримидин-2-ил)фенил)метанона;
(2,3-диметоксифенил)(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(2-(трифторметокси)фенил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(6-метил-2-[1,2,3]триазол-2-илпиридин-3-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(2-метокси-4-метилфенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-метокси-2-метилфенил)метанона;
(2,6-дифторфенил)(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
2-[5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-6-метилпиримидин-4-карбонитрила;
2-[4,6-бис(трифторметил)пиримидин-2-ил]-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-[5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-6-метилпиримидин-4-ола;
(2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил)(5-(4-(фуран-2-ил)-6-метилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
2-(4,6-диметилпиримидин-2-ил)-5-[(3-фтор-2-пиримидин-2-илфенил)карбонил]октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[3-фтор-2-(1Н-пиразол-5-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[3-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[3-метокси-2-(1Н-1,2,3-триазол-1-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[3-фтор-2-(1Н-1,2,3-триазол-1-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[4-метокси-2-(1Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-фтор-4-метилпиримидин-2-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(2-хлор-5-фторпиримидин-4-ил)-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-фторпиримидин-2-ил)-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-фтор-4-метилпиримидин-2-ил)-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-(4,5,6-триметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4,5-диметилпиримидин-2-ил)-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-(4-метокси-6-метилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4-этил-6-метилпиримидин-2-ил)-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-[4-метил-6-(1-метилэтил)пиримидин-2-ил]октагидропиррол[3,4-с]пиррола;
2-[4-метил-6-(1-метилэтил)пиримидин-2-ил]-5-{[2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[5-(1-метилэтил)-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-[4-метил-6-(1-метилэтил)пиримидин-2-ил]октагидропиррол[3,4-с]пиррола;
2-(4-трет-бутил-6-метилпиримидин-2-ил)-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4-циклопропил-6-метилпиримидин-2-ил)-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-(4-метил-1,3,5-триазин-2-ил)октагидропиррол[3,4-с]пиррола;
2-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}-5-(4-метил-6-морфолин-4-илпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-{[2-(4Н-1,2,4-триазол-3-ил)фенил]карбонил}-5-(4,5,6-триметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[2-(3-метил-1,2,4-оксадиазол-5-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[2-(1-метил-1Н-1,2,4-триазол-5-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[2-(1-метил-1Н-1,2,4-триазол-3-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[2-(3-метил-1,2,4-оксадиазол-5-ил)фенил]карбонил}-5-(4,5,6-триметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(5-фтор-4-метилпиримидин-2-ил)-5-{[2-(3-метил-1,2,4-оксадиазол-5-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[2-(1-метил-1Н-1,2,4-триазол-3-ил)фенил]карбонил}-5-(4,5,6-триметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(5-фтор-4-метилпиримидин-2-ил)-5-{[2-(1-метил-1Н-1,2,4-триазол-3-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-[5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-4-метил-6,7-дигидро-5Н-циклопентал[d]пиримидина;
2-(4,6-диметилпиримидин-2-ил)-5-{[3-фтор-2-(3-метил-1,2,4-оксадиазол-5-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[2-фтор-6-(3-метил-1,2,4-оксадиазол-5-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-хлор-4-метилпиримидин-2-ил)-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-хлор-4,6-диметилпиримидин-2-ил)-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-хлор-4,6-диметилпиримидин-2-ил)-5-{[2-(3-метил-1,2,4-оксадиазол-5-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
4-метил-2-[5-{[2-(3-метил-1,2,4-оксадиазол-5-ил)фенил]карбонил}гексагидропиррол[3,4-с]пиррол-2(1Н)-ил]-6,7-дигидро-5Н-циклопентал[d]пиримидина;
2-(5-хлор-4,6-диметилпиримидин-2-ил)-5-{[2-(1-метил-1Н-1,2,4-триазол-3-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-хлор-4-метилпиримидин-2-ил)-5-{[2-(1-метил-1Н-1,2,4-триазол-3-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-этил-4,6-диметилпиримидин-2-ил)-5-{[2-(1-метил-1Н-1,2,4-триазол-3-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{[3-(2Н-1,2,3-триазол-2-ил)пиридин-2-ил]карбонил}-5-(4,5,6-триметилпиримидин-2-ил)октагицропиррол[3,4-с]пиррола;
2-(5-хлор-4,6-диметилпиримидин-2-ил)-5-{[3-(2Н-1,2,3-триазол-2-ил)пиридин-2-ил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-фтор-4,6-диметилпиримидин-2-ил)-5-{[3-(2Н-1,2,3-триазол-2-ил)пиридин-2-ил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-(9Н-флуорен-4-илкарбонил)октагидропиррол[3,4-с]пиррола;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(5-[1,2,3]триазол-2-илбензо [1,3]диоксол-4-ил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(8-[1,2,3]триазол-2-илнафталин-1-ил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(4-[1,2,3]триазол-1-илпиридин-3-ил)метанона;
(5-трет-бутил-2-метоксифенил)-[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(1-[1,2,3]триазол-2-илнафталин-2-ил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(3-[1,2,3]триазол-2-илпиридин-2-ил)метанона;
(2-бром-4,5-диметоксифенил)-[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
(3,4-дигидро-2Н-бензо[b][1,4]диоксепин-6-ил)-[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-фтор-2-(6-метилпиридин-2-ил)фенил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(6-метил-2-[1,2,3]триазол-1-илпиридин-3-ил)метанона;
(1-бромнафталин-2-ил)-[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(3-метоксинафталин-2-ил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(8-[1,2,3]триазол-2-илнафталин-1-ил)метанона;
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(1-метоксинафталин-2-ил)метанона;
(4,5-диметокси-2-[1,2,3]триазол-1-илфенил)-[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
(4,5-диметокси-2-[1,2,3]триазол-2-илфенил)-[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-фтор-2-(4-метилпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-пропоксипиридин-2-ил)метанона;
(3-пропоксипиридин-2-ил)(5-(5-(трифторметил)пиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-фтор-2-(3-фторпиридин-2-ил)фенил)метанона;
(3-пропоксипиридин-2-ил)(5-(хиноксалин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
2-(5-([1,1'-бифенил]-2-илсульфонил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)хиноксалина;
2-[(2,6-диметоксифенил)карбонил]-5-[5-(трифторметил)пиридин-2-ил]октагидропиррол[3,4-с]пиррола;
(2,6-диметоксифенил)(5-(5-(трифторметил)пиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(2,6-диметоксифенил)(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-метилфуран-2-ил)метанона;
2-[(3-метилфуран-2-ил)карбонил]-5-[5-(трифторметил)пиридин-2-ил]октагидропиррол[3,4-с]пиррола;
(3-метилфуран-2-ил)(5-(5-(трифторметил)пиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(3-метилфуран-2-ил)(5-(хиноксалин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
2-([1,1'-бифенил]-2-илсульфонил)-5-(5-(трифторметил)пиридин-2-ил)октагидропиррол[3,4-с]пиррола;
2-([1,1'-бифенил]-2-илсульфонил)-5-(5-(трифторметил)пиримидин-2-ил)октагидрспиррол[3,4-с]пиррола;
2-([1,1'-бифенил]-2-илсульфонил)-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-((2-метоксифенил)сульфонил)октагидропиррол[3,4-с]пиррола;
2-((2-метоксифенил)сульфонил)-5-(5-(трифторметил)пиримидин-2-ил)октагидропиррол[3,4-с]пиррола;
2-((2-метоксифенил)сульфонил)-5-(5-(трифторметил)пиридин-2-ил)октагидропиррол[3,4-с]пиррола;
2-(5-((2-метоксифенил)сульфонил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)хиноксалина;
(3,6'-диметил-[2,3'-бипиридин]-2'-ил)(5-(хиноксалин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(3,6'-диметил-[2,3'-бипиридин]-2'-ил)(5-(5-(трифторметил)пиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(3,6'-диметил-[2,3'-бипиридин]-2'-ил)(5-(5-(трифторметил)пиридин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-фтор-2-(пиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(пиридин-2-ил)фенил)метанона;
[2,3'-бипиридин]-2'-ил(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-фтор-2-(оксазол-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(6-метилпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(3-метилпиридин-2-ил)фенил)метанона;
(2-(3-хлорпиридин-2-ил)-3-фторфенил)(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(4-метилпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(5-метилпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(3-фторпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(оксазол-2-ил)фенил)метанона;
2-(5-фтор-4-метилпиримидин-2-ил)-5-{[4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-хлор-4-метилпиримидин-2-ил)-5-{[4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-фтор-4,6-диметилпиримидин-2-ил)-5-{[4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,5-диметилпиримидин-2-ил)-5-{[4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-[(3-пропоксипиридин-2-ил)карбонил]-5-[5-(трифторметил)пиридин-2-ил]октагидропиррол[3,4-с]пиррола;
2-{4,6-бис[(2Н3)метил](2Н)пиримидин-2-ил}-5-{[2-фтор-6-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{4,6-бис[(2Н3)метил](2Н)пиримидин-2-ил}-5-{[3-фтор-2-(3-метил-1,2,4-оксадиазол-5-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-{4,6-бис[(2Н3)метил](2Н)пиримидин-2-ил}-5-{[4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(5-этил-4,6-диметилпиримидин-2-ил)-5-{[3-(2Н-1,2,3-триазол-2-ил)пиридин-2-ил]карбонил}октагидропиррол[3,4-с]пиррола;
2-(4,6-диметилпиримидин-2-ил)-5-{[3-(3-метил-1,2,4-оксадиазол-5-ил)пиридин-2-ил]карбонил}октагидропиррол[3,4-с]пиррола;
(5-(6,7-дифторхиноксалин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(пиримидин-2-ил)фенил)метанона;
(5-(6,7-дифторхиноксалин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(пиримидин-2-ил)фенил)метанона;
(5-(6,7-дифторхиноксалин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил)метанона;
(5-(6-(диметиламино)пиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил)метанона;
(5-(6-(диметиламино)-2-метилпиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-метокси-2-(2Н-1,2,3-триазол-2-ил)фенил)метанона;
(5-(6-(диметиламино)-2-метилпиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(пиримидин-2-ил)фенил)метанона;
(5-(6-(диметиламино)пиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(пиримидин-2-ил)фенил)метанона;
(3-фтор-2-(пиримидин-2-ил)фенил)(5-(5-фтор-4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(5-хлор-4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(пиримидин-2-ил)фенил)метанона;
(5-(5-хлор-4-метилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(пиримидин-2-ил)фенил)метанона;
(3-фтор-2-(пиримидин-2-ил)фенил)(5-(5-фтор-4-метилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона;
(5-(4,5-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(3-фтор-2-(пиримидин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(5-фтор-2-(6-метилпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидрогпиррол[3,4-с]пиррол-2(1Н)-ил)(5-фтор-2-(4-метилпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(5-фтор-2-(5-метилпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(5-фтор-2-(3-фторпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(5-фтор-2-(пиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(4-фтор-2-(оксазол-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(6-фтор-2-(6-метилпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(6-фтор-2-(4-метилпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(6-фтор-2-(5-метилпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(6-фтор-2-(3-фторпиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(6-фтор-2-(пиридин-2-ил)фенил)метанона;
(5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)(6-фтор-2-(оксазол-2-ил)фенил)метанона;
(3,6'-диметил-[2,3'-бипиридин]-2'-ил)(5-(хиноксалин-2-ил)гексагидропиррол[3,4-с]пиррол-2(1Н)-ил)метанона и
[5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-ил]-(2-фтор-6-[1,2,3]триазол-2-илфенил)метанона×HCl×1,65Н2О.
30. Фармацевтическая композиция для лечения заболевания, расстройства или состояния, обусловленного активностью орексиновых рецепторов, включающая:
(а) эффективное количество по меньшей мере одного соединения, выбранного из соединений формулы (I)
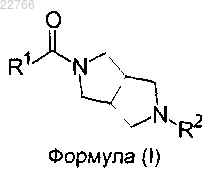
где R1 выбран из группы, состоящей из:
A) фенила, возможно замещенного одним или двумя заместителями Ra и замещенного Rb в орто-позиции;
Ra независимо выбран из галогена, -С1-4алкила, -С1-4алкокси и -NO2, где два соседних Ra заместителя могут вместе формировать шестичленное ароматическое кольцо;
Rb выбран из группы, состоящей из
a) галогена, -С1-4алкокси, -С1-4алкила, -CF3, -OCF3 или -CN;
b) 5-членного гетероарильного кольца, содержащего один атом кислорода или один атом серы;
c) 5-6-членного гетероарильного кольца, содержащего один, два или три атома азота, возможно, содержащего один атом кислорода, где кольцо возможно замещено галогеном или -C1-4алкилом; и
d) фенила, возможно замещенного галогеном, -СН3 или -CF3,
B) пиридина, возможно замещенного одним или двумя заместителями Rc и замещенного Rd, где Rd расположен рядом с местом присоединения R1;
Rc является С1-4алкилом;
Rd выбран из группы, состоящей из:
a) 5-6-членного гетероарильного кольца, выбранного из группы, состоящей из 1Н-1,2,3-триазол-1-ила, 2Н-1,2,3-триазол-2-ила, 1Н-пиразол-5-ила, 3-метил-1,2,4-оксадиазол-5-ила, пиридинила, 3-метилпиридин-2-ила; 1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ила, фенила и пиримидин-2-ила; и
b) -CF3, -Br и -С1-4алкокси;
C) 5-членного гетероарильного кольца, выбранного из 2-метил-1,3-тиазолила, 1Н-пиразол-5-ила, оксазолила, изоксазолила, тиофен-2-ила и фуран-2-ила, каждый из которых замещен фенилом, возможно замещен -F; и
D) 5-13-членного арильного или гетероарильного кольца, выбранного из 3-метилфуран-2-ила, 9Н-флуоренила, хинолинила, циннолинила; 3-(1Н-пиррол-1-ил)тиофен-2-ила, 8-[1,2,3]-триазол-2-илнафталин-1-ила, 2,3-дигидро-1,4-бензодиоксин-5-ила, 1Н-индол-7-ила, 4-фторнафталин-1-ила и нафталин-1-ила;
R2 выбран из группы, состоящей из:
A) 6-членного гетероарильного кольца, содержащего два атома азота, замещенных одним или несколькими заместителями, независимо выбранными из галогена, -С1-4алкила, -CD3, -D, -С1-4алкокси, циклопропила, морфолин-4-ила, -СО2С1-4алкила, -СО2Н, -СН2ОН, -С(O)N(С1-4алкил)2, -CF3, -CN, -ОН, -NO2, -N(С1-4алкил)2, фенила, фуран-2-ила, тиофен-2-ила, 1Н-пиразол-4-ила и пирролидин-1-ила;
B) пиридина, замещенного одним или двумя заместителями, независимо выбранными из галогена, -С1-4алкила, -С1-4алкокси и -CF3;
C) 9-членного гетероарильного кольца, выбранного из бензоксазол-2-ила, 2-метилпиримидин-4(3Н)-онила, 6-фтор-1,3-бензотиазолила, 1,3-бензотиазолила, 6-метокси-1,3-бензотиазолила, 6-метил-1,3-бензотиазолила, 6-хлорбензотиазол-2-ила и 4-метил-6,7-дигидро-5Н-циклопента[d]пиримидинила;
D) 10-членного гетероарильного кольца, выбранного из хиноксалин-2-ила, 3-метилхиноксалин-2-ила, 6,7-дифторхиноксалин-2-ила, 3-(трифторметил)хиноксалинила, хинолина, 4-метилхинолина и 6-фторхиназолин-2-ила; и
E) 4-метил-1,3,5-триазин-2-ила;
и фармацевтически приемлемых солей соединений формулы (I); и
(b) по меньшей мере один фармацевтически приемлемый эксципиент.
31. Фармацевтическая композиция, включающая эффективное количество по меньшей мере одного соединения по п.29 и по меньшей мере один фармацевтически приемлемый эксципиент.
32. Способ лечения заболевания, расстройства или состояния, обусловленного активностью орексиновых рецепторов, заключающийся во введении пациенту эффективного количества по меньшей мере одного соединения формулы (I)

где R1 выбран из группы, состоящей из:
A) фенила, возможно замещенного одним или двумя заместителями Ra и замещенного Rb в орто-позиции;
Ra независимо выбран из галогена, -С1-4алкила, -С1-4алкокси и -NO2, где два соседних Ra заместителя могут вместе формировать 6-членное ароматическое кольцо;
Rb выбран из группы, состоящей из:
a) галогена, -С1-4алкокси, -С1-4алкила, -CF3, -OCF3 или -CN;
b) 5-членного гетероарильного кольца, содержащего один атом кислорода или один атом серы;
c) 5-6-членного гетероарильного кольца, содержащего один, два или три атома азота, возможно содержащего один атом кислорода, где кольцо возможно замещено галогеном или -C1-4алкилом; и
d) фенила, возможно замещенного галогеном, -СН3 или -CF3,
B) пиридина, возможно замещенного одним или двумя заместителями Rc и замещенного Rd, где Rd расположен рядом с местом присоединения R1;
Rc является C1-4алкилом;
Rd выбран из группы, состоящей из:
a) 5-6-членного гетероарильного кольца, выбранного из 1Н-1,2,3-триазол-1-ила, 2Н-1,2,3-триазол-2-ила, 1Н-пиразол-5-ила, 3-метил-1,2,4-оксадиазол-5-ила, пиридинила, 3-метилпиридин-2-ила; 1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразол-5-ила, фенила и пиримидин-2-ила; и
b) -CF3, -Br и -С1-4алкокси;
C) 5-членного гетероарильного кольца, выбранного из 2-метил-1,3-тиазолила, 1Н-пиразол-5-ила, оксазолила, изоксазолила, тиофен-2-ила и фуран-2-ила, каждый из которых замещен фенилом, возможно замещен -F; и
D) 5-13-членного арильного или гетероарильного кольца, выбранного из 3-метилфуран-2-ила, 9Н-флуоренила, хинолинила, циннолинила; 3-(1Н-пиррол-1-ил)тиофен-2-ила, 8-[1,2,3]-триазол-2-ил-нафталин-1-ила, 2,3-дигидро-1,4-бензодиоксин-5-ила, 1Н-индол-7-ила, 4-фторнафталин-1-ила и нафталин-1-ила;
R2 выбран из группы, состоящей из:
A) 6-членного гетероарильного кольца, содержащего два атома азота, замещенных одним или несколькими заместителями, независимо выбранными из галогена, -С1-4алкила, -CD3, -D, -С1-4алкокси, циклопропила, морфолин-4-ила, -СО2С1-4алкила, -СО2Н, -СН2ОН, -С(О)N(С1-4алкил)2, -CF3, -CN, -ОН, -NO2, -N(С1-4алкил)2, фенила, фуран-2-ила, тиофен-2-ила, 1Н-пиразол-4-ила и пирролидин-1-ила;
B) пиридина, замещенного одним или двумя заместителями, независимо выбранными из галогена, -С1-4алкила, -С1-4алкокси и -CF3;
C) 9-членного гетероарильного кольца, выбранного из бензоксазол-2-ила, 2-метилпиримидин-4(3Н)-онила, 6-фтор-1,3-бензотиазолила, 1,3-бензотиазолила, 6-метокси-1,3-бензотиазолила, 6-метил-1,3-бензотиазолила, 6-хлор-бензотиазол-2-ила и 4-метил-6,7-дигидро-5Н-циклопента[d]пиримидинила;
D) 10-членного гетероарильного кольца, выбранного из хиноксалин-2-ила, 3-метилхиноксалин-2-ила, 6,7-дифторхиноксалин-2-ила, 3-(трифторметил)хиноксалинила, хинолина, 4-метилхинолина и 6-фторхиназолин-2-ила; и
E) 4-метил-1,3,5-триазин-2-ила;
или его фармацевтически приемлемой соли и по меньшей мере одного фармацевтически приемлемого эксципиента.
33. Способ по п.32, где заболевание, расстройство или состояние выбрано из нарушений сна, болезни Паркинсона, синдрома Туретта, кататонии, тревожности, бреда, деменции, избыточного веса или ожирения, или условий, связанных с избыточной массой тела или ожирением, инсулинорезистентности, сахарного диабета II типа, гиперлипидемии, желчно-каменной болезни, стенокардии, гипертонии, одышки, тахикардии, бесплодия, апноэ во сне, болей в спине и суставах, варикозного расширения вен, остеоартроза, гипертонии, тахикардии, аритмии, стенокардии, острой сердечной недостаточности, язвенной болезни, синдрома раздраженного кишечника, диареи и желудочно-пищеводного рефлюкса.
34. Способ по п.32, где заболевание, расстройство или состояние представляет собой бессонницу.
35. Способ по п.33, где нарушение сна вызвано расстройствами цикла сна-бодрствования, такими как нарушение суточного ритма, бессонница, синдром беспокойных ног или нарушений сна, вторичных по отношению к неврологическому расстройству, такому как мании, депрессии, маниакально-депрессивные психозы, шизофрения, болевые синдромы, фибромиалгии или невропатическая боль.
Текст
ДВУЗАМЕЩЕННЫЕ ОКТАГИДРОПИРРОЛ[3,4-с]ПИРРОЛЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ ОРЕКСИНОВЫХ РЕЦЕПТОРОВ Описаны дизамещенные соединения октагидропиррол[3,4-с]пиррола, используемые в качестве модуляторов рецепторов орексина. Такие соединения могут использоваться в фармацевтических средствах и способах лечения заболеваний, расстройств и болезней, на которые влияет деятельность орексина, как, например, бессонница.(71)(73) Заявитель и патентовладелец: ЯНССЕН ФАРМАЦЕВТИКА НВ (BE) 022766 Настоящая заявка истребует приоритет по предварительной заявке на патент США за номером 61/151429, поданной 10 февраля 2009 года. Область применения изобретения Изобретение относится к определенным двузамещенным соединениям октаногидропиррол[3,4 с]пиррола, содержащим его лекарственным препаратам, методам его получения и использования для модуляции орексиновых рецепторов и лечения болезненных состояний, расстройств и заболеваний, обусловленных активностью орексиновых рецепторов. Предпосылки создания изобретения Сигнальная активность орексина (или гипокретина) осуществляется при помощи двух рецепторов и двух пептидных агонистов. Два пептида орексина (орексин А и орексин В), называемые далее в тексте орексинами, связываются с двумя высокоаффинными рецепторами, названными орексиновыми рецепторами 1 и 2 типа. Орексиновый рецептор 1 типа селективен к орексину А, в то время как орексиновый рецептор 2 типа способен связывать с одинаковой афинностью оба вида орексинов. Орексины являются продуктами расщепления производного одного гена, препроорексина В центральной нервной системе нейроны, экспрессирующие препроорексин - предшественник, из которого образуется орексин, были обнаружены в перифорникальном ядре и области дорсального и латерального гипоталамуса (С. Peyron etal., J. Neurosci., 1998, 18(23), 9996-10015). Орексинергические клетки данного ядра проникают во многие области мозга, распространяясь рострально до обонятельных луковиц и каудально до спинного мозга(van den Pol, A.N. et al., J. Neuroscience., 1999, 19(8), 3171-3182). Широкое распространение в ЦНС орексинергических проекционных путей и нейронов, экспрессирующих орексиновые рецепторы, может свидетельствовать об участии орексина в ряде физиологических функций, включая процессы питания, питья, возбуждения, стресса, вознаграждения, обмена веществ и размножения (Т. Sakurai, Nature Reviews Neuroscience, 2007, 8 (3), 171-181). Индуцированный некроз клеток, экспрессирующих препроорексин, позволил предположить, что наиболее физиологически значимую роль орексины играют в регуляции процессов возбуждения, питания и обмена веществ (J. Нага et al., Neuron, 2001, 30, 345-354). Главный орексинергический проекционный путь, представленный блуждающим нервом, вероятно, обуславливает центральные влияния орексина на деятельность сердца (W.K. Samson et al., Brain Res., 1999, 831, 248-253; Т. Shirasaka et al., Am. J.Physiol., 1999, 277, R1780-R1785; C.-T. Chen et al., Am. J. Physiol., 2000, 278, R692-R697), секрецию желудочного сока и моторику желудка (A.L. Kirchgessner and M.-Т. Liu, Neuron, 1999, 24, 941-951; N. Takahashi et al., Biochem. Biophys. Res. Commun., 1999, 254, 623-627). Некоторые данные указывают на то, что орексиновая система является важным регулятором процессов возбуждения. Грызуны, которым была проведена интрацеребровентрикулярная инъекция орексина, проводили больше времени в состоянии бодрствования (Piper et al., J. Neurosci. 2000, 12, 726-730). Влияние орексина на процессы возбуждения были связаны с орексинергическими проекционными путями, ведущими к гистаминергическим нейронам в туберомамиллярном ядре (ТМЯ) (Yamanaka et al., Biochem. Biophys. Res. Comm. 2002, 290, 1237-1245). Нейроны ТМЯ в первую очередь экспрессируют орексиновые рецепторы 2 типа, в меньшей степени экспрессируются орексиновые рецепторы 1 типа. У грызунов, у которых ген препроорексина был инактивирован или орексинергические нейроны были повреждены, наблюдался измененный цикл сна-бодрствования, схожий с нарколепсией (Chemelli et al., Cell 1999, 98, 437-451; Hara et al., 2001, supra). Модели нарколепсии у собак показали, что у исследуемых животных имелись мутантные или нефункциональные орексиновые рецепторы 2 типа (Lin et al., Cell 1999,98, 365-37 6). Нарколепсия у людей, по-видимому, связана с недостаточностью орексиновой сигнальной активности, которая может быть связана с иммунной абляцией орексинергических нейронов в латеральной области гипоталамуса (Mignot et al., Am.J. Hum. Genet. 2001, 68: 686-699; MinotThorsby, New England J. Med. 2001, 344, 692), или, в редких случаях, с мутациями в гене орексина-2 (Peyron et al., NatureMed. 2000, б, 991-997). В публикации было показано, что у крыс, собак и людей, прошедших лечение двойным антагонистом орексиновых рецепторов 1 и 2 типа, АСТ-078573 (Brisbare-Roch et al., NatureMedicine, 2007, 13, 150-155), наблюдается снижение продолжительности бодрствования в сочетании с характерными клиническими и ЭЭГ (электроэнцефалографическими) признаками сна, что представляет доказательства в пользу роли орексиновой системы в регуляции состояния возбуждения, сна и бодрствования. ЭЭГ данные указывают на то, что орексин-2 может играть более важную роль, чем орексин-1, в модуляции цикла сна-бодрствования (P. Malherbe et al., Molecular Pharmacology (2009) 76(3): 618-31; СDugovic et al., J. Pharmacol. Exp. Ther., 2009, 330(1), 142-151). Поэтому расстройства цикла снабодрствования являются наиболее вероятными мишенями для терапии антагонистами орексиновых рецепторов 2 типа. Примерами таких расстройств могут служить нарушения перехода сон-бодрствование,инсомния, синдром беспокойных ног, нарушение суточного ритма организма, нарушения сна и вторичные нарушения сна, возникающие на фоне неврологических расстройств (например, маний, депрессий,биполярного расстройства, шизофрении) и болевых синдромов (например, фибромиалгии, нейропатической боли). Орексиновая система также взаимодействует с дофаминовой системой мозга. Интрацеребровентрикулярные инъекции орексинов у мышей повышали их двигательную активность, частоту груминга и сте-1 022766 реотипии; эти поведенческие эффекты изменялись в противоположном направлении при введении антагонистов D2 дофаминовых рецепторов (Nakamura et al., Brain Research, 873(1), 181-7). Поэтому модуляторы орексина-2 могут найти применение в лечении различных неврологических расстройств; например,агонисты или активаторы могут применяться для лечения кататонии, антагонисты или ингибиторы - для лечения болезни Паркинсона, синдрома Туретта, тревожности, делирия и деменций. Последние данные свидетельствуют о роли орексина в патогенезе болезни Альцгеймера (Kang et al,Science Express, 2009, 1-10). Было показано, что содержание бета-амилоида в интерстициальной жидкости мозга подвержено суточным колебаниям у людей и грызунов, которые были подвергнуты депривации сна, причем у грызунов было отмечено достоверное повышение содержания бета-амилоида в интерстициальной жидкости мозга. Инфузия двойного антагониста орексина вызвала у грызунов снижение содержания бета-амилоида в инстерстициальной жидкости и ликвидировала его естественные суточные колебания. Снижение содержания бета-амилоида в интерстициальной жидкости коррелирует со снижением образования амилоидных бляшек, которые являются отличительным признаком болезни Альцгеймера, следовательно, регулирование времени сна потенциально может подавлять агрегацию бетаамилоида и замедлять прогрессирование болезни Альцгеймера. Орексинергические проекционные нейроны связаны со многими областями мозга, которые отвечают за процессы вознаграждения (Т. Sakurai, supra), исследования с использованием экспериментальных моделей приема веществ, вызывающих наркотическую зависимость, удовлетворенность, и восстановления на животных позволили расширить понимание связи между орексиновой системой и развитием зависимости. Исчерпывающий набор данных указывает на то, что вещества, вызывающие наркотическую зависимость, активируют орексиновую систему, которая, в свою очередь, усиливает вознаграждение при приеме наркотика или стимулирует потребность в его поиске (G. Aston-Jones et al., Neuropharmacology,2009, 56 (Suppl 1) 112-121. Было показано такое взаимодействие орексиновой системы с никотином (J. К.Kane et al., Endocrinology, 2000, 141(10), 3623-3629; J. К. Kane et al., Neurosci. Lett., 2001, 298(1), 1-4),морфином (D.Georgescu, et al, J.Neurosci., 2003, 23(8), 3106-3111) и амфетамином (С. J. Winrow et al.,Neuropharmacology, 2010, 58(1), 185-94) Проведенные в ряде лабораторий дополнительные исследования показали важную связь между орексиновой системой и потреблением этанола. Например, было показано,что потребление этанола предпочитающими алкоголь крысами положительно регулирует содержание мРНК в латеральной области гипоталамуса и что антагонист орексиновых рецепторов 1 типа снижает оперантную реакцию в ответ на этанол (Lawrence, et. al., Br. J. Pharmacol., 2006, 148, 752-759). Также было показано, что лечение антагонистом орексиновых рецепторов 1 типа снижает оперантную реакцию в ответ на этанол (Richards, et. al., Psychopharmacology, 2008, 199 (1), 109-117). В рамках других исследований было показано повышение активации Fos белка в орексинергических нейронах после восстановления ситуационного поиска алкоголя (Dayas, et. al., Biol. Psychiatry, 2008, 63 (2), 152-157 and Hamlin, et. al.,Neuroscience, 2007, 146, 525-536). Исследования также показали повышение потребления алкоголя после инфузии орексина в паравентрикулярное ядро гипоталамуса или в латеральную область гипоталамуса(Schneider, et. al., Alcohol. Clin. Exp. Res., 2007, 31(11), 1858-1865). Эти исследования свидетельствуют о том, что функционирование орексиновой системы влияет на пристрастие к алкоголю, и поэтому антагонисты орексиновых рецепторов потенциально могут быть использованы для лечения алкоголизма. Орексины и их рецепторы были обнаружены в миэнтерическом и подслизистом сплетении энтеральной нервной системы, и было показано, что орексины in vitro повышают моторику (KirchgessnerLiu, Neuron 1999, 24, 941-951) и стимулируют in vitro секрецию желудочного сока (Takahashi et al., Biochem. Biophys. Res. Comm. 1999, 254, 623-627). Влияние орексина на пищеварительную систему может реализоваться за счет проекционных путей в составе блуждающего нерва (van den Pol, 1999, supra), так как ваготомия или введение атропина предотвращает проявление эффектов от интрацеребровентрикулярной инъекции орексина на секрецию желудочного сока (Takahashi et al., 1999, supra). Поэтому антагонисты орексиновых рецепторов или другие ингибиторы орексиновой системы являются потенциальными лекарствами для лечения язв, синдрома раздраженной кишки, диареи и гастроэзофагеального рефлюкса. Масса тела также может регулироваться орексиновой системой за счет ее влияния на аппетит и обмен веществ. (Т. Sakurai et al., Cell, 1998, 92(4), 573-585; Т. Sakurai, Reg. Pept., 1999, 85(1), 25-30). Некоторые эффекты орексина на обмен веществ и аппетит могут реализоваться в желудочно-кишечном тракте, где, предположительно, орексины изменяют моторику желудка и секрецию желудочного сока. Поэтому антагонисты орексиновых рецепторов могут найти применение в лечении избыточного веса или ожирения и состояний, связанных с избыточным весом и ожирением, таких как резистентность к инсулину, диабет II типа, гиперлипидемия, желчно-каменная болезнь, стенокардия, артериальная гипертензия, одышка, тахикардия, бесплодие, апноэ во сне, боль в спине и суставах, варикозное расширение вен и остеоартрит. Напротив, агонисты орексиновых рецепторов могут быть использованы при лечении недостаточной массы тела и связанных с ней состояний, таких как гипотензия, брадикардия, аменорея и связанное с ней бесплодие, и таких расстройств питания, как анорексия и булимия. Показано, что интрацеребровентрикулярное введение орексинов повышает среднее артериальное давление и частоту сердечных сокращений как у свободно движущихся животных (во время бодрствования) (Samson et al., Brain Res. 1999, 831, 248-253; Shirasaka et al., Am. J. Physiol. 1999, 277, R1780-R1785)-2 022766 и животных, анестезированных уретаном, (Chen et al., Am. J. Physiol. 2000, 278, R692-R697), со сходными результатами. Поэтому агонисты орексиновых рецепторов могут быть возможными средствами для лечения гипотензии, брадикардии и связанной с ними сердечной недостаточности, в то время как антагонисты орексиновых рецепторов могут применяться для лечения артериальной гипертензии, тахикардии и других аритмий, стенокардии и острой сердечной недостаточности. Из вышеизложенного видно, что идентификация модуляторов орексиновых рецепторов, и как один из вариантов осуществления изобретения - модулятора орексинового рецептора 2 типа, может предоставить большое преимущество при разработке терапевтических средств для лечения широкого спектра заболеваний, которые могут регулироваться посредством воздействия на рецепторы данной системы. Цитирование в качестве ссылки не может рассматриваться как признание того, что такая ссылка является известным уровнем техники для настоящего изобретения. Все издания, упомянутые в настоящем документе, полностью включены в него посредством ссылки. Были зарегистрированы различные низкомолекулярные модуляторы орексиновых рецепторов, например производные N-ароилциклических аминов (международная публикацияWO 2003002561, 9 января 2003 г.), производные этилендиамина (международная публикация . WO 2003051872, 26 июня 2003 г.), производные сульфониламиноуксусной кислоты (международная публикацияWO 2004033418, 22 апреля 2004 г.), производные N-арилацетилциклических аминов (международная публикацияWO 2004041791, 21 мая 2004 г.), производные диазепана (международная публикацияWO 2007126935, 8 ноября 2007 г.), производные амидоэтилтиоэфира (международная публикацияWO 2007126934, 8 ноября 2007 г.), производные двузамещенного пролина бис-амида (международная публикацияWO 2008008551, 17 января 2 008 г.), мостиковые производные диазепана (международная публикацияWO 2008008517, 17 января 2 008 г.), замещенные производные диазепана (международная публикацияWO 2008008518, 17 января 2008 г.; US 20080132490, WO 2009058238), производные диазепана с кислородным мостиком (международная публикацияWO 2008143856, 27 ноября 2008 г.),производные 1,2-диамидоэтилена (международная публикацияWO 2009022311, 19 февраля 2 009 г.),гетероарильные производные (международная публикацияWO 20090163485, 25 июня 2009 г.), метилзамещенные производные пиперидина (международная публикацияWO 2009124956, 15 октября 2009 г.), двузамещенное производное N,N-1,4-диазепана (Сох et al., BioorganicMedicinal Chemistry Letters,2009, 19 (11), 2997-3001), лиганды орексиновых/гипокретиновых рецепторов (Boss, et al., Journal of Medicinal Chemistry, 2009, 52(4), 891-903) 3,9-диазобицикло[4.2.1]нонаны (Coleman et al, BioorganicMedicinal Chemistry Letters, 2010, 20(14), 4201-4205), двойной антагонист орексиновых рецепторов, [(7R)-4(5-хлоро-1,3-бензоксазол-2-ил)-7-метил-1,4-диазепан-1-ил][5-метил-2-(2 Н-1,2,3-триазол-2 ил)фенил]метанон, (Сох, et. al., Journal of Medicinal Chemistry, 2010 53(14) 5320-5332), производные пиридазина карбоксамида (международная публикацияWO 2010051238), 2,5-двузамещенные производные бензамида (международная публикацияWO 2010051237, 6 мая 2 010 г.), изоникотинамиды (Международная публикацияWO 2010051236), производные гетероциклилбензоилпиперазинов (Международная публикацияWO 201048012), замещенные производные диазепана (международная публикацияWO 2010048017), замещенные производные пирролидина (международная публикацияWO 2010048014), производные триазолилбензоилпиперидина (международная публикацияWO 2010048010), производные триазолилбензоилморфолина (WO 2010048013), конформационно-ограниченные производные двузамещенного N,N-1,4-диазепана (Coleman et al., BioorganicMedicinal Chemistry Letters, 2010, 20(7), 2311-2315), производные трипиридилкарбоксамида (международная публикацияWO 2010017260), производные замещенного имидазопиридилметилпиперидина (международная публикацияWO 2010072722), производные замещенного имидазопиразинпиперидина (US 2010160344, 24 июня 2010; US 20100160345, 24 июня 2010; международная публикацияWO 2010060472, 3 июня 2010 г.),производныеN-[(1R,4S,6R)-3-(2-пиридинилкарбонил)-3-азобицикло[4.1.0]гепт-4-ил]метил-2 гетероариламина (международная публикацияWO 2010063663), производные N-[(lS,4S,6S)-3-(2 пиридинилкарбонил)-3-азобицикло[4.1.0]гепт-4-ил]метил-2-гетероариламина (международная публикацияWO 2010063662), производные имидазопиримидина (международная публикацияWO 2010060471) и производные имидазопиразина (международная публикацияWO 2010060470). Однако остается потребность в мощных модуляторах орексиновых рецепторов с требуемыми фармацевтическими свойствами. Замещенные диазобициклические соединения были зарегистрированы как активные вещества, которые оказывают воздействие на центральную нервную систему (международная публикацияWO 2001081347, 1 ноября 2001 г.; US 2002/0019388, 14 февраля 2002 г.), модуляторы 7 ацетилхолиновых рецепторов (US 2005/101602, 12 мая 2005 г.; US 2005/0065178, 24 марта 2005 г. и Frost et al, Journal ofMedicinal Chemistry, 2006, 49(26), 7843-7853), ингибиторы переносчика пролина для лечения когнитивных нарушений (WO 2008067121, 5 июня 2008 г.) и улучшения когнитивных функций (WO 2006124897,23 ноября 2006 г. и US 20060258672, 16 ноября 2006 г.), как лиганд андрогенового рецептора для лечения состояний, связанных с функционированием андрогенового рецептора, включая рак (WO 2009081197, 2 июля 2009 г.), и как гистон диацетилазных ингибиторов для лечения рака, нейродегенеративных и аутоиммунных заболеваний (WO 20060123121, 23 ноября 2006 г.). Краткое описание изобретения У некоторых двузамещенных производных октаногидропиррол[3,4-с]пиррола была обнаружена орексинмодулирующая активность. Таким образом, данное изобретение описывает общий и предпочтительные варианты осуществления изобретения, определяемые, соответственно, независимыми и зависимыми пунктами формулы изобретения, которые прилагаются к настоящему документу и включены в него путем ссылки. В общем аспекте изобретение сводится к химическому соединению формулы (I) где R1 - радикал, выбранный из группы, состоящей из: А) бензольного кольца, замещенного или незамещенного одним или двумя радикалами Ra, и замещенного в орто-положении радикалом Rb;Ra выбирается независимым образом из группы, состоящей из: -Н, галогена, -С 1-4 алкила, -С 1-4 алкоксила и -NO2, где два смежных радикала Ra должны соединяться друг с другом с образованием шестичленного ароматического кольца;b) 5-членного гетероарильного кольца, содержащего один атом кислорода или серы;c) 5-6-членного гетероарильного кольца, содержащего один, два или три атома азота, которое может добавочно содержать один атом кислорода, и которое может быть замещено или не замещено галогеном или -С 1-4 алкилом; иd) фенила, замещенного или не замещенного галогеном, -СН 3 или -CF3;B) пиридина, замещенного или не замещенного одним или двумя радикалами Rc, и замещенного Rd,d где R находится у смежного атома, к которому присоединяется заместитель R1;C) 5-членного гетероарильного кольца, выбранного из группы, состоящей из 2-метил-1,3 триазолила, 1 Н-пиразол-5-ила, оксазола, изоксазолила, тиофен-2-ила и фуран-2-ила, каждый из которых замещен фенилом, который может быть замещен или не замещен -F; иD) 5-13-членного арильного или гетероарильного кольца, выбранного из группы, состоящей из 3 метилфуран-2-ила, 9 Н-флуорена, хинолина, циннолина; 3-(1 Н-пиррол-1-ил)тиофен-2-ила, 8-[1,2,3]триазол-2-ил-нафталин-1-ила, 2,3-дигидро-1,4-бензодиоксин-5-ила, 1 Н-индол-7-ила, 4-фторонафталин-1 ила и нафталин-1-ила;A) 6-членного гетероарильного кольца, содержащего два атома азота, и замещенного одним или более радикалом, выбранным независимым образом из группы, состоящей из галогена, -C1-4 алкила, -CD3,-D, -C1-4 алкоксила, циклопропила, морфолин-2-ила, -СО 2 С 1-4 алкила, -СО 2 Н, -СН 2 ОН, -С(О)NB) пиридина, замещенного одним или двумя радикалами, выбранными независимым образом из группы, состоящей из галогена, -С 1-4 алкила, -С 1-4 алкоксила и -CF3;E) 4-метил-1,3,5-триазин-2-ила или 2-метилпиримидин-4(3 Н)-она. В другом общем аспекте изобретение сводится к химическому соединению формулы (II) где R3 - бензольное кольцо, замещенное или не замещенное радикалами, которые были выбраны не-4 022766 зависимым образом из группы, состоящей из -С 1-4 алкоксила и фенила; иR4 - радикал, выбранный из группы, состоящей из (5-трифторметил)пиридин-2-ила, (5-трифторметил)пиримидин-2-ила, 4,6-диметилпиримидин-2-ила и хиноксалин-2-ила. Дальнейшие варианты осуществления настоящего изобретения представляют собой фармацевтически приемлемые соли соединений формулы (I) или формулы (II), фармацевтически приемлемые пролекарства соединений формулы (I) или формулы (II) и фармацевтически активные метаболиты соединений формулы (I) или формулы (II). В некоторых вариантах осуществления настоящего изобретения соединение формулы (I) или формулы (II) является соединением, которое было выбрано из списка соединений, которые были приведены выше в качестве примеров или подробно описываются ниже. В еще одном аспекте изобретение относится к лекарственным препаратам для лечения заболеваний,расстройств или состояний, обусловленных активностью орексиновых рецепторов, которые содержат эффективное количество по меньшей мере одного химического соединения, выбранного из соединений формулы (I) или формулы (II), фармацевтически приемлемых солей соединений формулы (I) или формулы (II), фармацевтически приемлемых пролекарств соединений формулы (I) или формулы (II) и фармацевтически приемлемых активных метаболитов соединения формулы (I) или формулы (II). Фармацевтические композиции по изобретению могут иметь в своем составе одно или несколько фармацевтически приемлемых вспомогательных веществ. В другом аспекте, вариант осуществления настоящего изобретения в области химии может использоваться в качестве модулятора орексиновых рецепторов. Таким образом, изобретение относится к способу модуляции активности орексиновых рецепторов, включая случаи, когда эти рецепторы находятся в организме пациента, что подразумевает воздействие на орексиновые рецепторы эффективного количества по меньшей мере одного химического соединения, выбранного из соединений формулы (I) или формулы (II), фармацевтически приемлемых солей соединений формулы (I) или формулы (II), фармацевтически приемлемых пролекарств соединений формулы (I) или формулы (II) и фармацевтически приемлемых активных метаболитов соединения формулы (I) или формулы (II). В другом аспекте изобретение относится к способу лечения пациента, которому был поставлен диагноз заболевания, расстройства или медицинского состояния, обусловленного активностью орексиновых рецепторов, которое требует введения пациенту, нуждающемуся в таком лечении, эффективного количества по меньшей мере одного химического соединения, выбранного из соединений формулы (I) или формулы (II), фармацевтически приемлемых солей соединений формулы (I) или формулы (II), фармацевтически приемлемых пролекарств соединений формулы (I) или формулы (II) и фармацевтически приемлемых активных метаболитов соединения формулы (I) или формулы (II). Дополнительные варианты осуществления настоящего изобретения, относящегося к способу лечения, изложены в подробном описании. В другом аспекте, методика изучения изотопных индикаторов в метаболических исследованиях(преимущественно с 14 С), исследованиях кинетических реакций (с использованием, например, 2 Н или 3 Н), регистрации или получения изображений [при помощи таких способов, как позитронно-эмиссионная томография (ПЭТ) или однофотонная эмиссионная компьютерная томография (ОФЭКТ)] содержала исследования препарата или ткани субстрата, либо исследование проводилось при облучении пациентов. Например, соединения, меченные 18F или 11 С, предпочтительно исследовать при помощи ПЭТ, в то время как соединения, меченные I123, лучше исследовать при помощи ОФЭКТ. Целью настоящего изобретения является преодоление или смягчение по меньшей мере одного из недостатков стандартных методик и/или известных способов, либо предоставление пригодных альтернатив для последних. Дополнительные варианты реализации, особенности и достоинства изобретения будут очевидны из следующего подробного описания и практического осуществления изобретения. Краткое описание чертежей Фиг. 1 является дифракцией рентгеновских лучей на порошке образца соединения X. Подробное описание изобретения Изобретение может быть более полно оценено из нижеследующего описания, включающего глоссарий терминов и заключительные примеры. Для краткости цитируемые публикации, включая патенты,включены в настоящее описание посредством ссылки. Термины "включающий", "содержащий", "состоящий" используются в настоящем документе в их открытом неограниченном значении. Термин "алкил" относится к алкильной группе с прямой или разветвленной цепью, содержащей от 1 до 12 атомов углерода. Примеры алкильных групп содержат метил (Me, который также может быть структурно обозначен символом "/"), этил (Et), н-пропил, изопропил, бутил, изобутил, втор-бутил, третбутил (tBu), фенил, изофенил, трет-фенил, гексил, изогексил, и группы, которые в свете общепринятых знаний и учений, представленных здесь, будут считаться эквивалентными одному из вышеприведенных примеров. Термин "алкокси" включает алкильную группу с прямой или разветвленной цепью и конечным атомом кислорода, который связан с алкильной группой остальной части молекулы. Алкоксигруппы со-5 022766 держат метокси, этокси, изопропокси, бутокси, трет-бутокси, пентоксигруппы и т.п. Термины "аминоалкил", "тиоалкил" и "сульфонилалкил" обозначают аналоги алкоксигрупп, в которых концевой атом кислорода замещен, соответственно, NH (или NR), S и SO2. Термин "циано" обозначает -CN группу. Используемый в настоящей заявке термин "циклоалкил" означает насыщенный или частично насыщенный моноциклический, конденсированный полициклический или спирополициклический карбоцикл, содержащий от 3 до 12 кольцевых атомов на карбоцикл. Типовые примеры циклоалкильных групп содержат следующие фрагменты в виде соответствующим образом связанных фрагментов:"Гетероциклоалкил" означает насыщенную или частично насыщенную моноциклическую кольцевую структуру, содержащую от 4 до 7 атомов в структуре кольца, выбранных из атомов углерода, и до двух гетероатомов, выбранных из азота, кислорода и серы. Структура кольца может необязательно содержать до двух оксогрупп, присоединенных к гетероатомам серы. Показательные структуры, в форме соответствующим образом связанных составляющих, содержат: Термин "арил" относится к моноциклическим, конденсированным или полициклическим соединениям, кольца которых имеют один общий атом, углеродным ароматическим кольцам (кольцевые соединения, в которых все атомы кольца представлены углеродом), содержащим в кольце от 3 до 12 атомов.(Атомы углерода в ароматических группах находятся в состоянии sp2 гибридизации). Показательным примером ароматических групп могут служить следующие фрагменты молекул: Используемый в настоящей заявке термин "гетероарил" означает моноциклический, конденсированный бициклический или конденсированный полициклический ароматический гетероцикл(кольцевую структуру, имеющую в кольце атомы, выбираемые из атомов углерода и до четырех гетероатомов, выбираемых из азота, кислорода и серы), содержащий от 3 до 12 кольцевых атомов на гетероцикл. Показательные примеры гетероарильных групп содержат следующие объекты в форме соответствующим образом связанных составляющих: Специалистам в данной области будет понятно, что список перечисленных и приведенных выше видов гетероарильных, циклоалкильных, арильных или гетероциклоалкильных групп не является исчерпывающим, и поэтому в рамках этих терминов могут быть выбраны дополнительные виды этих соединений. Термином "галоген" обозначается хлор, фтор, бром или йод. Термин "гало" означает хлор, фтор,бром и йод.-6 022766 Термин "замещенный" означает, что указанная функциональная группа или составляющая имеет один или несколько заместителей. Термин "незамещенный" означает, что указанная группа не имеет заместителей. Используемый в настоящей заявке термин "возможно замещенный" означает, что указанная группа либо не имеет заместителей, либо несет один или более заместителей. Если термин "замещенный" используется для описания структурной системы, это значит, что замещение происходит на любой позиции системы, где это допускается валентностью. В тех случаях, когда для определенной составляющей или группы явно не указано, что она является необязательно замещенной или замещенной любым определенным заместителем, предполагается, что такая составляющая или группа является незамещенной. Термины "пара", "мета" и "орто" имеют общепринятое значение в рамках данной отрасли. Таким образом, например, полностью замещенная фенильная группа имеет заместители в обоих "орто" (о) положениях относительно точки их присоединения к бензольному кольцу, в обоих "мета" (м) положениях и в одном "пара" (п) положении напротив точки присоединения фенильной группы показанным ниже образом. Для большей сжатости описания ряд приводимых в настоящей заявке количественных выражений дается без модификатора "приблизительно". Подразумевается, что независимо от того, указывается ли модификатор "приблизительно" явным образом или нет, каждое приводимое в настоящей заявке численное значение относится к конкретному приведенному значению, а также к приближению к данному приведенному значению, которое может быть разумным образом оценено любым специалистом, включая эквиваленты и приближения, связанные с условиями проведения эксперимента и/или измерения для подобного приведенного значения. При указании выхода соединения в процентах приводимый выход относится к массе структурной единицы, для которой указывается выход, по отношению к максимально достижимому количеству данной структурной единицы в конкретных стехиометрических условиях. Если не указано иное, приводимые в процентах концентрации относятся к массовым соотношениям. Термины "буферный" раствор или "буфер" здесь являются взаимозаменяемыми в соответствии со своим стандартным значением. Буферные растворы используются для контроля рН среды, и их выбор,использование и функция известны специалистам в данной области. См., например, G.D. Considine, ed.,"Van Nostrand's Encyclopedia of Chemistry", стр. 261, 5-e издание (2005), в котором, в частности, описываются буферные растворы и то, каким образом компоненты буферного раствора влияют на его рН. См. также "Handbook of Chemistry and Physics", 84 ред., стр. 8-37 до 8-44. Например, буферный раствор, полученный добавлением MgSO4 и NaHCO3 к раствору в соотношении 10:1 вес/вес, может поддерживать рН раствора около 7,5. Каждая из приведенных в настоящей заявке формул представляет как соединения со структурами,иллюстрируемыми данной структурной формулой, так и некоторые вариации или формы подобных структур. В частности, соединения любой приведенной в настоящем документе формулы могут иметь асимметричные центры и, следовательно, существовать в различных энантиомерных формах. Все оптические изомеры и стереоизомеры соединений общей формулы, а также смеси таковых рассматриваются в рамках данной формулы. Таким образом, любая приведенная здесь формула предназначена для обозначения рацемата, одной или более энантиомерных форм, одной или более диастереомерных форм, одной или более атропизомерных форм и смесей упомянутого. Кроме того, некоторые структуры могут существовать в форме геометрических изомеров (например, цис- и транс-изомеров), таутомеров или атропизомеров. и используются для обозначения аналогичного пространственного расСимволы положения химических структур, которые были приведены в данном документе. По аналогии символы и используются для обозначения аналогичного пространственного расположения химических структур, которые были приведены в данном документе. Кроме того, каждая приведенная в настоящей заявке формула помимо собственно соединений также включает их гидраты, сольваты и полиморфы, а также их смеси, даже если такие формы не указаны явно. Некоторые соединения формулы (I) или формулы (II), или фармацевтически приемлемые соли соединений формулы (I) или формулы (II),также могут быть получены в виде сольватов. Сольваты содержат формы, образуемые в результате взаимодействия или комплексообразования соединений, составляющих предмет настоящего изобретения, с одним или более растворителем и получаемые либо в виде раствора, либо в виде твердой или кристаллической формы. В ряде вариантов осуществления упомянутый растворитель представляет собой воду, а сольваты являются гидратами. Кроме того, некоторые кристаллические формы соединений формулы (I) или формулы (II), или фармацевтически приемлемые соли соединений формулы (I) или формулы (II),могут быть получены в виде сокристаллов. В некоторых вариантах осуществления настоящего изобретения соединения формулы (I) или формулы (II) могут быть получены в кристаллической форме. В других вариантах осуществления настоящего изобретения кристаллическая форма соединения формулы (I) или-7 022766 формулы (II) имела вид кубических кристаллов. В других вариантах осуществления настоящего изобретения фармацевтически приемлемые соли соединений формулы (I) или формулы (II) были получены в кристаллической форме. В других вариантах осуществления настоящего изобретения соединения формулы (I) или формулы (II) были получены в одной из нескольких полиморфных форм, в виде смеси кристаллических форм, в виде полиморфной или некристаллической формы. В других вариантах осуществления настоящего изобретения соединения формулы (I) или формулы (II) в растворе были конвертированы в пределах одной или нескольких кристаллических и/или полиморфных форм. Упоминание приведенного здесь химического соединения является случаем, когда: (а) фактически упоминается это химическое соединение, и (b) соединение упоминается в том случае, когда подразумевается любая из форм этого химического соединения в определенной среде. Например, упоминание в настоящей заявке такого соединения, как R-COOH, содержит отсылку к любой, например, из следующих форм: R-COOH(s), R-COOH(sol) и R-COO-(sol). Например, R-COOH(s) является твердым веществом и может содержаться, например, в таблетке или любой другой твердой фармацевтической форме лекарственного или фармацевтического препарата; R-COOH(sol) является недиссоциированной формой соединения в растворителе; и R-COC-(sol) является диссоциированной формой соединения в растворителе, такой как диссоциированная форма соединения в водной среде, где эта диссоциированная форма образуется из RCOOH, из ее соли и любого другого соединения, которое при диссоциации в рассмотренной среде даетR-СОС-. В другом примере такое выражение, как "действие на структурную единицу соединением формулы R-COOH" означает действие на упомянутую структурную единицу формой или формами соединения R-COOH, которая существует или которые существуют в той среде, где осуществляется описываемое воздействие. В еще одном примере такое выражение, как "введение структурной единицы в реакцию с соединением по формуле R-COOH", относится к реакции (а) подобной структурной единицы в соответствующей химической форме или формах, которая существует или которые существуют в той среде, где осуществляется описываемая реакция, с (б) соответствующей химической формой или формами соединения R-СООН, которая существует или которые существуют в той среде, где осуществляется описываемая реакция. В этой связи, если подобная структурная единица находится, например, в водной среде,подразумевается, что упомянутое соединение R-COOH находится в той же среде, и поэтому на упомянутую структурную единицу действуют такие реагенты, как R-COOH(aq) и/или R-COO-(aq), где нижний индекс "(aq)" означает "водный" в соответствии с его общепринятым значением в химии и биохимии. В этих номенклатурных примерах была выбрана карбоксильная функциональная группа; этот выбор был сделан непреднамеренно и был ограниченным, однако это всего лишь пример. Подразумевается, что аналогичные примеры могут быть приведены и для иных функциональных групп, включая, помимо прочего, такие группы, как гидроксильная группа, азотная основная группа, например, в аминах, а также любые другие группы, которые известным образом взаимодействуют или перестраиваются в содержащей данное соединение среде. Подобные взаимодействия и перестройки содержат, помимо прочего, диссоциацию, ассоциацию, таутомеризм, сольволиз, включая гидролиз, сольватацию, включая гидратацию, протонирование и депротонирование. В настоящей заявке не приводится дальнейших примеров в этой связи, поскольку возможные взаимодействия и перестройки в каждой конкретной среде хорошо известны специалистам в данной области. В другом примере цвиттерионное соединение в настоящей заявке включается путем отсылки к соединению, которое может образовывать цвиттерион, даже если оно явно не упоминается в своей цвиттерионной форме. Термины "цвиттерион","цвиттерионы", а также их синонимы "цвиттерионное соединение" и "цвиттерионные соединения" являются стандартными рекомендованными IUPAC терминами, которые хорошо известны и входят в стандартный набор определенных научных терминов. В этой связи термину "цвиттерион" присвоен уникальный идентификатор CHEBI:27369 в Словаре химических объектов биологического интереса (ChEBI). Как в целом хорошо известно, цвиттерион или цвиттерионное соединение представляет собой в целом нейтральное соединение, имеющее формальные единичные заряды противоположных знаков. Иногда к подобным соединениям также применяется термин "внутренние соли". В ряде источников такие соединения называются "диполярными ионами", хотя в других источниках последний термин считается неправильным. В качестве конкретного примера, аминоэтановая кислота (аминокислота глицин) имеет формулу H2NCH2COOH и в ряде сред (в данном случае в нейтральной среде) существует в форме цвиттериона +H3NCH2COO-. Цвиттерионы, цвиттерионные соединения, внутренние соли и диполярные ионы в известных и хорошо обоснованных значениях перечисленных терминов относятся к сфере действия настоящего изобретения, как без труда определят специалисты. Поскольку нет необходимости называть каждый отдельный вариант осуществления настоящего изобретения, который может определить специалист, в настоящей заявке не приводятся явно структуры цвиттерионных соединений, родственных соединениям, составляющим предмет настоящего изобретения. Тем не менее, все такие структуры являются частью вариантов осуществления настоящего изобретения. В настоящей заявке не приводятся дальнейшие примеры в этой связи, поскольку возможные взаимодействия и перестройки в каждой конкретной среде, приводящие к различным формам каждого конкретного соединения, хорошо известны специалистам. Каждая из приведенных в настоящей заявке формул также представляет как немеченные, так и изо-8 022766 топно-меченые формы соответствующих соединений. Изотопно-меченые соединения имеют структуры,соответствующие представленным в настоящей заявке формулам, за исключением того, что один или более атомов в них заменены атомом, имеющим определенную атомную массу или массовое число. Примерами изотопов, которые могут быть включеныв соединения, относящиеся к настоящему изобретению, могут служить следующие изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора: 2 Н, 3 Н, 11 С, 13 С, 14 С, 15N, 18O, 17O, 31 Р, 32 Р, 35S, 18F, 36Cl, 125I соответственно. Такие меченные изотопами соединения пригодны для исследований метаболизма (предпочтительно с 14 С), исследований кинетики реакций (например, с 2 Н или 3 Н), в методиках обнаружения или получения изображений [таких как томография, основанная на методе позитронной эмиссии (PET), или однофотонная эмиссионная компьютерная томография (SPECT)], включая количественные анализы лекарства или субстрата тканей, или при радиационной терапии пациентов. В частности, для исследования соединений, меченных 18F или 11 С,предпочтительно использовать ПЭТ, в то время как соединения, меченные 123I, лучше исследовать при помощи ОФЭКТ. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий (т.е. 2 Н), может дать определенные терапевтические преимущества вследствие большей метаболической стабильности соединений, например, увеличенного периода полувыведения in vivo или снижения необходимой дозировки. Соединения настоящего изобретения, меченные изотопами, и пролекарства таковых могут, в целом, быть приготовлены путем осуществления процедур согласно схемам или примерам и способам приготовления, описанным ниже, путем замены реагента, не содержащего меченых атомов, на легкодоступный реагент с мечеными атомами. При обсуждении любой приведенной в настоящей заявке формулы выбор конкретного фрагмента из списка возможных вариантов для конкретной химической переменной не означает фиксирование такого выбора фрагмента для данной переменной в других формулах. Другими словами, если некоторая химическая переменная присутствует в формуле более чем в одном месте, выбор варианта для нее из списка возможных в одном месте не зависит от выбора варианта для той же переменной в другом месте формулы, если не указано иное. В качестве первого примера по используемой для обозначения заместителей терминологии, если заместитель S1 пример представляет собой один из S1 и S2, и заместитель S2 пример представляет собой один из S3 и S4, то указанные варианты обозначения заместителей содержат варианты осуществления настоящего изобретения в соответствии со следующими наборами: S1 пример является S1 и S2 пример представляет собой S3; S1 пример является S1 и S2 пример представляет собой S4; S1 пример является S2 и S2 пример представляет собой S3; S1 пример представляет собой S2 и S2 пример представляет собой S4; и их любых эквивалентов в каждом из таких выборов. Поэтому для краткости изложения без ограничения общности в настоящей заявке используется сокращенная терминология: "S1 пример представляет собой один из S1 и S2, a S2 пример представляет собой один из S3 и S4". Приведенный выше первый пример по используемой для обозначения заместителей терминологии, данный в общих терминах, иллюстрирует различные варианты обозначения заместителей, описанные в настоящей заявке. Установленные выше правила распространяются, когда это возможно, на такие радикалы, как R1, R2, R3, R4, A, Ra, Rb, Rc, Rd, Re, Rf, Rg, Rh, RI, RJ, Rk и любые другие использованные родовые обозначения заместителей. Кроме того, если для любого участника химической структуры или заместителя приводится более чем один вариант, варианты осуществления настоящего изобретения содержат различные сочетания вариантов из списков возможных заместителей, а также их эквиваленты. В качестве второго примера по используемой для обозначения заместителей терминологии, если они были описаны, заместитель S пример представляет собой один из S1, S2, и S3, и этот список относится к вариантам осуществления настоящего изобретения, для которых S пример представляет собой S1; S пример представляет S2; S пример представляет S3;S пример представляет собой один из S1 и S2; S пример представляет собой один из S1 и S3; S пример представляет собой один из S2 и S3; S пример представляет собой один из S1, S2 и S3; и S пример представляет собой любой эквивалент в каждом из таких наборов. Поэтому для краткости изложения без ограничения общности в настоящей заявке используется сокращенная терминология: "S пример представляет собой один из S1,S2 и S3". Приведенный выше второй пример по используемой для обозначения заместителей терминологии, данный в общих терминах, иллюстрирует различные варианты обозначения заместителей, описанные в настоящей заявке. Установленные выше правила распространяются, когда это возможно, на такие радикалы, как R1, R2, R3, R4, A, Ra, Rb, Rc, Rd, Re, Rf, Rg, Rh, RI, RJ и Rk, и любые другие использованные родовые обозначения заместителей. Номенклатура "C1-J" где ji, используемая в настоящей заявке для обозначения класса заместителей,включает варианты осуществления настоящего изобретения, для которых индивидуально реализовано каждое и все возможные количества атомов углерода от i до j, включая i и j. В качестве примера, терминC1-3 относится независимо к вариантам осуществления, в которых имеется один атом углерода (C1), вариантам осуществления, в которых имеются два атома углерода (С 2), и вариантам осуществления, в которых имеются три атома углерода (С 3). Используемый в настоящей заявке термин Cn-m алкил означает линейную или разветвленную алифатическую цепь с полным количеством N углеродных центров в цепи, удовлетворяющим условиюn Nm, где mn. Любое упоминание в настоящей заявке дивалентного заместителя включает различные-9 022766 варианты присоединения упомянутого заместителя, если имеется более одной такой возможности. Например, упоминание дивалентного заместителя -А-В-, где АВ, в настоящей заявке относится к таким дивалентным заместителям -А-В-, где фрагмент А присоединяется к первому замещаемому центру и фрагмент В присоединяется ко второму замещаемому центру, а также к таким дивалентным заместителям -А-В-, где фрагмент А присоединяется ко второму замещаемому центру и фрагмент В присоединяется к первому замещаемому центру. В соответствии с приведенными выше соображениями по обозначению заместителей и используемой номенклатуре подразумевается, что в настоящей заявке явное упоминание некоторого набора возможностей означает, при наличии химического смысла и если не указано иное, независимую отсылку ко всем возможным вариантам осуществления данного набора, а также отсылку ко всем и каждому возможному варианту осуществления подмножеств явно указанного набора возможных вариантов. Некоторые варианты осуществления настоящего изобретения представлены соединениями формулы (I), где R1 - фенил, замещенный Ra, где Ra представлен -F, -I, -Cl, -ОСН 3, -ОСН 2 СН 3, -СН 3, -СН(СН 3)2,-С(СН 3)3 или -NO2. В некоторых вариантах осуществления настоящего изобретения R1 является замещенным фенилом,в котором Rb представлен -Br, -F, -I, -С 1-4 алкилом, -ОСН 3, -ОСН 2 СН 3, -CN, -CF3 или -OCF3. В некоторых вариантах осуществления настоящего изобретения R1 - фенил, замещенный Ra, в котором Ra представлен -Н, -F, -Cl, -СН 3, -С(СН 3)3, -ОСН 3 или -ОСН 2 СН 3, и Rb представлен -Br, -F, -I, -С 1-4 алкилом, -ОСН 3, -ОСН 2 СН 3, -CN, -CF3 или -OCF3. В некоторых вариантах осуществления настоящего изобретения R1 является замещенным фенилом,в котором Rb является 2-тиофен-2-илом или 2-фуран-2-илом. В некоторых вариантах осуществления настоящего изобретения R1 является замещенным фенилом,в котором Rb является фенилом, 3-хлорфенилом, 4-фторфенилом, 3-фторфенилом, 4-метилфенилом или 4-трифторметилфенилом. В некоторых вариантах осуществления настоящего изобретения R1 является замещенным фенилом,в котором Rb является 1 Н-пиррол-1-илом, 1 Н-пиразол-1-илом, 1 Н-пиразол-5-илом, 1 Н-имидазол-2-илом,1-метил-1 Н-имидазол-2-илом, 1 Н-1,2,3-триазол-1-илом, 2 Н-1,2,3-триазол-2-илом, 2 Н-1,2,3-триазол-1 илом, 1 Н-1,2,4-триазол-5-илом, 2 Н-1,2,4-триазол-1-илом, 2 Н-1,2,4-триазол-3-илом, 4 Н-1,2,4-триазол-3 илом, 4 Н-1,2,4-триазол-4-илом, 1-метил-1 Н-1,2,4-триазол-3-илом, 1-метил-1 Н-1,2,4-триазол-5-илом или 1-(тетрагидро-2 Н-пиран-2-ил)-1 Н-пиразол-5-илом. В некоторых вариантах осуществления настоящего изобретения R1 является замещенным фенилом,в котором Rb является пиридин-2-илом, 3-хлорпиридин-2-илом, 3-фторпиридин-2-илом, 3 метилпиридин-2-илом, 4-метилпиридин-2-илом, 5-метилпиридин-2-илом, 6-метилпиридин-2-илом, 2 пиридин-3-илом или 2-пиримидин-2-илом. В некоторых вариантах осуществления настоящего изобретения R1 является замещенным фенилом,в котором Rb является 3-метил-1,2,4-оксадиазол-5-илом или оксазол-2-илом. В некоторых вариантах осуществления настоящего изобретения R1 является фенилом, замещеннымR , где Ra является галогеном, -С 1-4 алкилом или -С 1-4 алкоксилом, и Rb является триазолом или пиримидином, замещенным или незамещенным галогеном или -C1-4 алкилом. В некоторых вариантах осуществления настоящего изобретения R1 является (1-метилэтил)-2-(2 Н 1,2,3-триазол-2-ил)фенилом, 2-(1 Н-1,2,3-триазол-1-ил)фенилом, 2-(2 Н-1,2,3-триазол-2-ил)фенилом, 2 фтор-6-(2 Н-1,2,3-триазол-2-ил)фенилом, 2-метил-6-(2 Н-1,2,3-триазол-2-ил)фенилом, 3-фтор-2-(2 Н-1,2,3 триазол-2-ил)фенилом,3-фтор-2-(1 Н-1,2,3-триазол-1-ил)фенилом,3-метокси-2-(1 Н-1,2,3-триазол-1 ил)фенилом, 3-метокси-2-(2 Н-1,2,3-триазол-2-ил)фенилом, 3-метил-2-(2 Н-1,2,3-триазол-2-ил)фенилом, 3 метил-2-(1 Н-1,2,3-триазол-1-ил)фенилом, 4-фтор-2-(2 Н-1,2,3-триазол-2-ил)фенилом, 4-метокси-2-(2 Н 1,2,3-триазол-2-ил)фенилом, 4-метокси-2-(1 Н-1,2,3-триазол-2-ил)фенилом, 4,5-диметокси-2-[1,2,3]триазол-1-илфенилом, 4,5-диметокси-2-[1,2,3]триазол-2-илфенилом, 5-[1,2,3]триазол-2-илбензо[1,3]диоксол 4-илом, 5-хлор-2-(2 Н-1,2,3-триазол-2-ил)фенилом, 5-фтор-2-(2 Н-1,2,3-триазол-2-ил)фенилом, 5-йод-2(2 Н-1,2,3-триазол-2-ил)фенилом, 5-метокси-2-(2 Н-1,2,3-триазол-2-ил) фенилом, 5-метил-2-(2 Н-1,2,3 триазол-2-ил)фенилом, 1-[1,2,3]триазол-2-ил-нафталин-2-илом, 2-(1 Н-1,2,4-триазол-1-ил)фенилом, 2-(1 Н 1,2,4-триазол-5-ил)фенилом, 2-(1-метил-1 Н-1,2,4-триазол-5-ил)фенилом, 2-(1-метил-1 Н-1,2,4-триазол-3 ил)фенилом, 2-(4 Н-1,2,4-триазол-3-ил)фенилом, 2-(4 Н-1,2,4-триазол-4-ил)фенилом, 2-(3-метил-1,2,4 оксадиазол-5-ил)фенилом,3-фтор-2-(3-метил-1,2,4-оксадиазол-5-ил)фенилом,2-фтор-6-(3-метил-1,2,4 оксадиазол-5-ил)фенилом, 4,5-дифтор-2-(4 Н-1,2,4-триазол-4-ил)фенилом), 2-фтор-6-пиримидин-2-илфенилом, 2-(пиримидин-2-ил)пиридин-3-илом, 3-фтор-2-пиримидин-2-илфенилом, 4-фтор-2-(пиримидин-2 ил)фенилом, 4-метокси-2-(пиримидин-2-ил)фенилом, 5-фтор-2-пиримидин-2-илфенилом или 5-метил-2 пиримидин-2-илфенилом. Некоторые варианты осуществления настоящего изобретения представлены соединениями формулы (I), где R1 является замещенным пиридином, в котором Rd представлен -CF3, -Br или -ОСН 2 СН 2 СН 3. В некоторых вариантах осуществления настоящего изобретения R1 представлен замещенным пиридином, Rd является 1 Н-пиразол-5-илом, 2 Н-1,2,3-триазол-1-илом, 2 Н-1,2,3-триазол-2-илом, 4 Н-1,2,3 триазол-1-илом, 1-(тетрагидро-2 Н-пиран-2-ил)-1 Н-пиразол-5-илом, 3-метилпиридин-2-илом или 3-метил- 10022766 1,2,4-оксадиазол-5-илом. В некоторых вариантах осуществления настоящего изобретения R1 представлен замещенным пиридином, Rd является 1 Н-пиразол-5-илом, 2 Н-1,2,3-триазол-1-илом или 2 Н-1,2,3-триазол-2-илом. В некоторых вариантах осуществления настоящего изобретения R1 является 1-фенил-1 Н-пиразол-5 илом, 3-фенилтиофен-2-илом, 3-фенилфуран-2-илом, 5-фенил-1,3-оксазол-4-илом, 5-фенилизоксазол-4 илом, 5-(2-фторфенил)-2-метил-1,3-тиазол-4-илом, 2-метил-5-фенил-тиазол-4-илом или 5-(4-фторфенил)2-метил-1,3-тиазол-4-илом. Некоторые варианты осуществления настоящего изобретения представлены соединениями формулы (I), в которых R1 является 3-метилфуран-2-илом, 9 Н-флуореном, хинолином, циннолином; 3-(1 Нпиррол-1-ил)тиофен-2-илом, 8-[1,2,3]-триазол-2-илнафталин-1-илом, 2,3-дигидро-1,4-бензодиоксин-5 илом, 1 Н-индол-7-илом, 4-фторнафталин-1-илом и нафталин-1-илом, и R2 выбирается из группы, состоящей из 4,6-диметилпиримидин-2-ила, 4-фенилпиримидин-2-ила, хиноксалина или 4 метоксопиримидин-2-ила. Некоторые варианты осуществления настоящего изобретения представлены соединениями формулы (I), где R2 является пиримидином, замещенным -F, -Cl, -D, -CD3, -СН 3, этилом, изопропилом, пропилом, трет-бутилом, -CF3, -ОСН 3, -N(CH3)2, -CN, -ОН, -СН 2 ОН, -NO2, -СО 2 СН 3, -СО 2 Н, -С(O)N(CH3)2, фенилом, фуран-2-илом, тиофен-2-илом, 1 Н-пиразол-4-илом, циклопропилом, пирролидин-1-илом или морфолин-4-илом. В некоторых вариантах осуществления настоящего изобретения R2 является 4,6 диметилпиримидин-2-илом, 4,5-диметилпиримидин-2-илом, 4,6-диметоксипиримидин-2-илом, 4-фенилпиримидин-2-илом, 4-фуран-2-илпиримидин-2-илом, 4-диметилпиримидин-2-илом, 4-метоксипиримидин-2-илом, 4-тиофен-2-илпиримидин-2-илом, N,N,6-триметилпиримидин-4-амином, 4-(трифторметил)пиримидин-2-илом, 4,5,6-триметилпиримидин-2-илом, 4-(трифторметил)пиримидин-5-карбоксилатом, 4-(трифторметил)пиримидин-5-карбоновой кислотой, 5-нитропиримидин-2-илом, 6-метилпиримидин-4-карбоновой кислотой, N,N-диметил-4-(трифторметил)пиримидин-5-карбоксамидом, N,N,6 триметилпиримидинкарбоксамидом, 6-метилпиримидин-4-карбонитрилом, 4,6-бис(трифторметил)пиримидин-2-илом, 5-метилпиримидин-4-олом, 4-(фуран-2-ил)-6-метилпиримидин-2-илом, 5-фтор-4-метилпиримидин-2-илом, 5-фтопиримидин-2-илом, 4-метокси-6-метилпиримидин-2-илом, 4-этил-6-метилпиримидин-2-илом, 4-изопропил-6-метилпиримидин-2-илом, 4-трет-бутил-6-метилпиримидин-2-илом, 4 циклопропил-6-метилпиримидин-2-илом,4-метил-6-морфолин-4-илпиримидин-2-илом,5-хлор-4 метилпиримидин-2-илом, 5-хлор-4,6-диметилпиримидин-2-илом, 5-фтор-4,6-диметилпиримидин-2-илом,5-трифторметилпиримидин-2-илом, 4,6-бис[(2 Н 3)метил](2 Н)пиримидин-2-илом или 5-этил-4,6-диметилпиримидин-2-илом. В некоторых вариантах осуществления настоящего изобретения R2 является пиримидином, замещенным одним или более -Cl, -F, -СН 3, -CF3, -N(CH3)2, -D или -CD3. В некоторых вариантах осуществления настоящего изобретения R2 является 4,6-диметилпиримидин-2-илом, 4,5-диметилпипимидином-2-илом, 4,6-диметоксипиримидин-2-илом, 4-метилпиримидин-2-илом, 4-метоксипиримидин-2-илом, N,N,6-триметилпиримидин-4-амином, 4-(трифторметил) пиримидин-2-илом, 4,5,6-триметилпиримидин-2-илом, 4,6-бис(трифторметил)пиримидин-2-илом, 6-метилпиримидин-4-олом, 5-фтор-4-метилпиримидин-2-илом, 5-фторпиримидин-2-илом, 4-метокси-6-метилпиримидин-2-илом, 5-хлор-4-метилпиримидин-2-илом, 5-хлор-4,6-диметилпиримидин-2-илом, 5 фтор-4,6-диметилпиримидин-2-илом, 5-трифторметилпиримидин-2-илом или 4,6-бис[(2 Н 3)метил](2 Н) пиримидин-2-илом. Некоторые варианты осуществления настоящего изобретения представлены соединениями формулы (I), где R2 является пиразином или триазином, которые были замещены одним или более -СН 3. Некоторые варианты осуществления настоящего изобретения представлены соединениями формулы (I), где R2 является пиридином, замещенным одним или более -F, -ОСН 3, -ОСН 2 СН 3, -СН 3 или -CF3. В некоторых вариантах осуществления настоящего изобретения R2 является бензооксазол-2-илом,2-метилпиримидин-4(3 Н)-оном и 4-метил-6,7-дигидро-5 Н-циклопента[d]пиримидином, и R1 представлен фенилом, замещенным в орто-положении Rb, где Rb является 2 Н-1,2,3-триазол-2-илом, 2 Н-1,2,3-триазол 1-илом, 3-метил-1,2,4-оксадиазол-5-илом или 2-пиримидин-2-илом. Некоторые варианты осуществления настоящего изобретения представлены соединениями формулы (I), где R2 является хиноксалин-2-илом, 3-метилхиноксалин-2-илом, 6,7-дифторхиноксалин-2-илом, 3(трифторметил)хиноксалином, 4-метилхинолином или 6-фторхиназолин-2-илом, и R1 представлен фенилом, замещенным в орто-положении Rb, где Rb является 2 Н-1,2,3-триазол-2-илом, 2 Н-1,2,3-триазол-1 илом, 3-метил-1,2,4-оксадиазол-5-илом или 2-пиримидин-2-илом. Некоторые варианты осуществления настоящего изобретения представлены соединениями формулы (II), где R3 является бифенилом или 2-метоксифенилом, и R4 представлен (5-трифторметил)пиридин 2-илом, (5-трифторметил)пиримидин-2-илом, 4,6-диметилпиримидин-2-илом или хиноксалин-2-илом. Некоторые варианты осуществления настоящего изобретения представлены соединениями формулы (I), где R1 является 2-(1 Н-1,2,3-триазол-1-ил)фенилом, 2-(2 Н-1,2,3-триазол-2-ил)фенилом, 2-фтор-6(2 Н-1,2,3-триазол-2-ил)фенилом, 2-метил-6-(2 Н-1,2,3-триазол-2-ил)фенилом, 3-фтор-2-(2 Н-1,2,3-триазол- 11022766 2-ил)фенилом, 3-фтор-2-(1 Н-1,2,3-триазол-1-ил)фенилом, 3-метокси-2-(1 Н-1,2,3-триазол-1-ил)фенилом,3-метокси-2-(2 Н-1,2,3-триазол-2-ил)фенилом, 3-метил-2-(2 Н-1,2,3-триазол-2-ил)фенилом, 3-метил-2-(1 Н 1,2,3-триазол-1-ил)фенилом, 4-фтор-2-(2 Н-1,2,3-триазол-2-ил)фенилом, 4-метокси-2-(2 Н-1,2,3-триазол-2 ил)фенилом, 4-метокси-2-(1 Н-1,2,3-триазол-2-ил)фенилом, 4,5-диметокси-2-[1,2,3]триазол-1-илфенилом,4,5-диметокси-2-[1,2,3]триазол-2-илфенилом, 5-хлор-2-(2 Н-1,2,3-триазол-2-ил)фенилом, 5-фтор-2-(2 Н 1,2,3-триазол-2-ил)фенилом, 5-метокси-2-(2 Н-1,2,3-триазол-2-ил) фенилом, 5-метил-2-(2 Н-1,2,3-триазол 2-ил)фенилом, 2-(1 Н-1,2,4-триазол-1-ил)фенилом, 2-(1 Н-1,2,4-триазол-5-ил)фенилом, 2- (1-метил-1 Н 1,2,4-триазол-5-ил)фенилом, 2-(1-метил-1 Н-1,2,4-триазол-3-ил)фенилом, 2-(4 Н-1,2,4-триазол-3-ил)фенилом, 2-(4 Н-1,2,4-триазол-4-ил)фенилом, 2-(3-метил-1,2,4-оксадиазол-5-ил)фенилом, 3-фтор-2-(3-метил 1,2,4-оксадиазол-5-ил)фенилом, 2-фтор-6-(3-метил-1,2,4-оксадиазол-5-ил)фенилом, 4,5-дифтор-2-(4 Н 1,2,4-триазол-4-ил)фенилом), 2-фтор-6-пиримидин-2-илфенил, 2-(пиримидин-2-ил)пиридин-3-илом, 3 фтор-2-пиримидин-2-илфенил, 4-фтор-2-(пиримидин-2-ил)фенилом, 4-метокси-2-(пиримидин-2-ил)фенилом, 5-фтор-2-пиримидин-2-илфенилом или 5-метил-2-пиримидин-2-илфенилом, и R2 является 4,6 диметилпиримидин-2-илом, 4,5-диметилпиримидин-2-илом,4,6-диметоксипиримидин-2-илом, 4-метилпиримидин-2-илом, 4-метоксипиримидин-2-илом, N,N,6-триметилпиримидин-4-амином, 4-(трифторметил)пиримидин-2-илом, 4,5,6-триметилпиримидин-2-илом, 4,6-бис(трифторметил)пиримидин-2-илом,6-метилпиримидин-4-олом, 5-фтор-4-метилпиримидин-2-илом, 5-фторпиримидин-2-илом, 4-метокси-6 метилпиримидин-2-илом, 5-хлор-4-метилпиримидин-2-илом, 5-хлор-4,6-диметилпиримидин-2-илом, 5 фтор-4,6-диметилпиримидин-2-илом, 5-трифторметилпиримидин-2-илом или 4,6-бис[(2 Н 3)метил](2 Н) пиримидин-2-илом. Некоторые варианты осуществления настоящего изобретения представлены соединениями формулы (I), где R1 является 3-фтор-2-(3-метил-1,2,4-оксадиазол-5-ил)фенилом, 6-фтор-2-(2 Н-1,2,3-триазол-2 ил)фенилом, 4-метокси-2-(2 Н-1,2,3-триазол-2-ил)фенилом или 3-[1,2,3]триазол-2-илпиридин-2-илом, иR2 является 4,6-диметилпиримидин-2-илом, 5-фтор-4,6-диметилпиримидин-2-илом или 5-фтор-4-метилпиримидин-2-илом. Для создания лекарственных препаратов используются соединения формулы (I), формулы (II) и их фармацевтически приемлемые соли, самостоятельно или в сочетании с одним или более дополнительным активным компонентом. Поэтому лекарственный препарат должен содержать эффективное количество по меньшей мере одного соединения формулы (I) и формулы (II) или их фармацевтически приемлемых солей. Изобретение также включает фармацевтически приемлемые соли соединений формулы (I) и формулы (II), которые, были описаны выше, и специфические соединения, которые были приведены в виде примера, а также методы лечения такими солями. Термин "фармацевтически приемлемая соль" обозначает соль свободной кислоты или основания соединения формулы (I) и формулы (II), которая является нетоксичной, биологически переносимой или иным образом биологически допустимой для назначения пациенту. См., в основном, G.S. Paulekuhn, et(Дж.С. Полекун и др. "Тенденции в выборе активных фармацевтических ингредиентов солей на основании анализа базы данных "Оранжевой книги"), J. Med. Chem., 2007, 50:6665-72, S.M. Berge, et al., "Pharmaceutical Salts" (СМ. Берг и др. "Фармацевтические соли"), J Pharm Sci., 1977, 66:1-19, и "Handbook ofPharmaceutical Salts, Properties, Selection, and Use" Stahl and Wermuth, Eds., Wiley-VCH and VHCA, Zurich,2002 ("Справочник фармацевтических солей, свойства, выбор и применение" Шталь и Вермут, ред.,Wiley-VCH and VHCA, Цюрих, 2002). Примерами фармацевтически приемлемых солей являются те, которые имеют фармакологический эффект и допустимы для контакта с тканями пациентов без чрезмерной раздражающей, токсической или аллергической реакции. Соединения формулы (I) и формулы (II) могут иметь в своем составе достаточно кислую группу, достаточно основную группу или оба вида функциональных групп, и, соответственно, реагировать со множеством неорганических и органических оснований, неорганических и органических кислот с образованием фармацевтически приемлемых солей. Примеры фармацевтически приемлемых солей содержат сульфаты, пиросульфаты, бисульфаты,сульфиты, бисульфиты, фосфаты, моногидрофосфаты, дигидрофосфаты, метафосфаты, пирофосфаты,хлориды, бромиды, йодиды, ацетаты, пропионаты, деканоаты, каприлаты, акрилаты, формиаты, изобутираты, капроаты, гептаноаты, пропиолаты, оксалаты, малонаты, сукцинаты, субераты, себакаты, фумараты, малеаты, бутин-1,4-диоаты, гексин-1,6-диоаты, бензоаты, хлорбензоаты, метилбензоаты, динитробензоаты, гидроксибензоаты, метоксибензоаты, фталаты, сульфонаты, ксиленсульфонаты, фенилацетаты,фенилпропионаты, фенилбутираты, цитраты, лактаты, -гидроксибутираты, гликоляты, тартраты, метансульфонаты, пропансульфонаты, нафталин-1-сульфонаты, нафталин-2-сульфонаты и манделаты. Если соединение формулы (I) или формулы (II) является азотным основанием, то желательная фармацевтически приемлемая соль может быть получена при помощи любого подходящего способа, доступного в данной области, например, в результате обработки данного свободного основания неорганической кислотой, такой как хлороводородная кислота, бромоводородная кислота, серная кислота, аминосульфоновая кислота, азотная кислота, борная кислота, фосфорная кислота и т.д., или органической кислотой, такой как уксусная кислота, фенилуксусная кислота, пропионовая кислота, стеариновая кислота,- 12022766 молочная кислота, аскорбиновая кислота, малеиновая кислота, гидроксималеиновая кислота, изэтиновая кислота, сукцинатная кислота, валериановая кислота, фумаровая кислота, малоновая кислота, пируватная кислота, щавелевая кислота, гликолевая кислота, салициловая кислота, олеиновая кислота, пальмитиновая кислота, лауриновая кислота, пиранозидиловая кислота, такая как глюкуроновая кислота или галактуроновая кислоты, альфа-гидроксильная кислота, такая как миндальная кислота, лимонная кислота,винная кислота, аминокислота, такая как аспарагиновая кислота, глутаровая кислота или глутаминовая кислота, ароматическая кислота, такая как бензойная кислота, ацетилсалициловая кислота, нафтойная кислота, или коричная кислота, сульфоновая кислота, такая как лаурилсульфоновая кислота, птолуолсульфоновая кислота, метансульфоновая кислота, этансульфоновая кислота, любые совместимые смеси кислот, которые были приведены выше, и любых других кислот и их смесей, которые рассматриваются как эквиваленты и допустимые заменители с учетом среднего уровня компетенции в данной технологии. Если соединение формулы (I) или формулы (II) является кислотой (такой как карбоновая или сульфоновая кислоты), то желательная фармацевтически приемлемая соль может быть получена при помощи любого подходящего способа, например, в результате обработки данной свободной кислоты неорганическими или органическими основаниями, такими как амины (первичные, вторичные и третичные), щелочные гидроксиды металлов, гидроксидами щелочно-земельных металлов, любыми совместимыми смесями оснований, которые были приведены выше в виде примеров, и любыми другими основаниями и их смесями, которые рассматриваются как эквиваленты и допустимые заменители с учетом среднего уровня компетенции в данной технологии. Показательные примеры допустимых солей содержат органические соли, полученные из аминокислот, таких как N-метил-D-глюкамин, лизин, холин, глицин и аргинин, аммониевые соли, карбонаты, бикарбонаты, первичные, вторичные и третичные амины и циклические амины, такие как трометамин, бензиламины, пирролидины, пиперидин, морфолин и пиперазин, и неорганические соли, производные натрия, кальция, калия, магния, марганца, железа, меди, цинка, алюминия и лития. Изобретение также относится к фармацевтически приемлемым пролекарствам соединений формулы (I) и формулы (II), и методикам лечения, в которых используются эти фармацевтически приемлемые пролекарства. Термин "пролекарство" означает, что при приеме пациентом предшественник разработанного соединения превратится в необходимое соединение in vivo при помощи таких химических и физических процессов, как сольволиз или ферментитивное расщепление, либо под действием физиологических условий (например, пролекарство при попадании в условия физиологического рН превращается в соединение формулы (I) или формулы (II. "Фармацевтически приемлемое пролекарство" означает пролекарство, которое является нетоксичным, биологически переносимым и иным образом биологически допустимым для назначения пациенту. Показательные методики выбора и приготовления подходящих производных пролекарств описаны, например, в "Design of Prodrugs", ed. H. Bundgaard, Elsevier, 1985. Примеры пролекарств содержат соединения, имеющие в своем составе аминокислотный остаток,полипептидную цепь из двух или более (например, двух, трех или четырех) аминокислотных остатков,ковалентно связанных амидной или эфирной связью со свободной амино-, гидрокси- или карбоксильной группой соединения формулы (I) или формулы (II). Примеры аминокислотных остатков содержат двадцать существующих в природе аминокислот, которые обычно обозначаются тремя буквами, а также 4 гидроксипролин, гидроксилизин, демозин, изодемозин, 3-метилгистидин, норвалин, бета-аланин, гаммааминомасляная кислота, цитруллин гомоцистеин, гомосерин, орнитин и метионинсульфон. Дополнительные виды пролекарств могут быть получены, например, путем функционализации свободных карбоксильных групп соединений формулы (I) или формулы (II) с получением амидов или алкильных эфиров. Примеры амидов содержат производные аммония, первичных C1-6 алкиламинов и вторичных ди(C1-6 алкил) аминов. Вторичные амины содержат 5- или 6-членные составляющие гетероциклоалкильного или гетероарильного кольца. Примеры амидов содержат производные аммония, первичныхC1-3 алкиламинов и ди (C1-2 алкил)аминов. Примеры эфиров изобретения содержат C1-7 алкил, С 5-7 циклоалкил, фенил и фенил(C1-6 алкил)эфиры. Предпочтительные эфиры содержат метиловые эфиры. Пролекарства также могут быть получены функционализацией свободных гидроксильных групп для получения замещенных производных, включая гемисукцинаты, фосфатные эфиры, диметиламиноацетаты и фосфорилоксиметилоксикарбонилы, следуя процедурам, описанным в Fleisher et al., Adv. Drug Delivery Rev. 1996, 19, 115-130. Для получения пролекарств могут также использоваться карбаматные производные гидроксильных и аминогрупп. Карбонатные производные, сульфонатные эфиры и сульфатные эфиры гидроксигрупп могут также давать пролекарства. Также для получения пролекарств возможно использование гидроксигрупп, таких как (ацилокси)метил- и (ацилокси)этил эфиры, где ацильная группа может быть алкилэфиром, возможно несущим в качестве заместителей одну или более эфирных, амино или карбоксильных функциональных групп, или где упомянутая ацильная группа представляет собой эфир аминокислоты, как описано выше. Пролекарства этого типа могут быть получены по методике, описанной Robinson et al., J Med Chem. 1996, 39(1), 10-18. Свободные амины также могут быть функционализированы как амиды, сульфонамиды или фосфонамиды. Все перечисленные фрагменты пролекарств могут иметь в своей структуре дополнительные функциональные группы, такие как эфирные, амино и карбок- 13022766 сильные группы. Настоящее изобретение также относится к фармацевтически активным метаболитам соединений формулы (I) или формулы (II), которые также могут использоваться в методиках изобретения. Термин"фармацевтически активный метаболит" обозначает фармацевтически активный продукт метаболизма соединения формулы (I), формулы (II) или их солей в организме. Пролекарства и активные метаболиты соединения могут быть определены с помощью обычных способов, известных и доступных специалистам в данной области. См., например, Bertolini, et al., J Med Chem. 1997, 40, 2011-2016; Shan, et al., JPharm Sci. 1997, 86 (7), 765-767; Bagshawe, Drug Dev Res. 1995, 34, 220-230; Bodor, Adv Drug Res. 1984,13, 224-331; Bundgaard, Design of Prodrugs (Elsevier Press, 1985); и "Larsen, Design and Application of Prodrugs, Drug Design and Development" (Krogsgaard-Larsen, et al., eds., Harwood Academic Publishers, 1991). В рамках методики изобретения соединения формулы (I) или формулы (II) и их фармацевтически приемлемые соли, фармацевтически приемлемые пролекарства и фармацевтически активные метаболиты данного изобретения используются в качестве модуляторов орексиновых рецепторов. Будучи модуляторами, эти соединения могут выступать в роли антагонистов, агонистов или обратных агонистов. Термин"модуляторы" включает как ингибиторы, так и активаторы, где термин "ингибиторы" относится к соединениям, которые уменьшают, предотвращают, инактивируют, уменьшают восприимчивость или подавляют экспрессию или активность орексиновых рецепторов, в то время как "активаторы" являются соединениями, которые повышают, активируют, облегчают, увеличивают восприимчивость или осуществляют положительную регуляцию экспрессии и активности орексиновых рецепторов. Используемые здесь термины "проводить лечение" или "лечение" используются для обозначения приема пациентом активного вещества или их сочетания в изобретении с целью достижения терапевтического или профилактического воздействия посредством модуляции активностиорексиновых рецепторов. Лечение включает обратное развитие, улучшение, подавление прогрессирования, уменьшение тяжести или профилактику заболевания, расстройства или состояния, одного и более симптома такого заболевания, расстройства или состояния, которое обусловлено модуляцией активности орексиновых рецепторов. Термин "пациент" относится к млекопитающему пациенту, нуждающемуся в таком лечении, например, к человеку. Соответственно, изобретение относится к способам использования описанных соединений для лечения пациентов, страдающих или имеющих диагностированные заболевания, расстройства или состояния, обусловленные активностью орексиновых рецепторов, таких как расстройства цикла снабодрствования, метаболические нарушения, неврологические и другие расстройства (например, нарушения процессов питания, питья, возбуждения, стресса, зависимости, расстройства метаболизма и репродукции). Симптомы или болезненные состояния также охвачены терминами "медицинские состояния,расстройства или заболевания". Расстройства сна содержат, но не ограничиваются этим, расстройства перехода сон-бодрствование,инсомнию, синдром беспокойных ног, нарушения суточного ритма организма, нарушения сна, в том числе вторичные, которые возникли на почве неврологических расстройств (например, маний, депрессий, биполярного расстройства, шизофрении и болевых синдромов (например, фибромиалгии и невропатических болей. Метаболические нарушения содержат, без ограничений, избыточный вес или ожирение, а также состояния, связанные с избыточным весом или ожирением, например, резистентность к инсулину, диабет II типа, гиперлипидемия, желчно-каменная болезнь, стенокардия, гипертензия, одышка, тахикардия, бесплодие, апноэ во сне, боли в спине и суставах, варикозное расширение вен и остеоартрит. Неврологические расстройства содержат, без ограничений, болезнь Паркинсона, болезнь Альцгеймера, синдром Туретта, кататонию, тревожность, делирий и слабоумие. Прочие расстройства содержат, без ограничений, язвы, синдром раздраженного кишечника, диарею и желудочно-пищеводный рефлюкс. В способах лечения в соответствии с данным изобретением эффективное количество фармацевтического агента в соответствии с изобретением назначается пациенту с имеющимся или диагностированным заболеванием, расстройством или состоянием. "Эффективное количество" означает количество или дозировку, достаточную для достижения в общем желательного терапевтического или профилактического эффекта для пациента, нуждающегося в таком лечении при указанном заболевании, расстройстве или состоянии. Эффективные количества или дозы соединений настоящего изобретения могут быть оценены обычными способами, такими как моделирование, исследования с увеличением дозы или клинические исследования, а также с учетом обычных факторов, таких как режим или способ применения или доставки лекарства, фармакокинетика соединения, тяжесть и течение заболевания, расстройства или состояния,предыдущее или текущее лечение пациента, состояние здоровья и ответная реакция организма пациента на лекарство, а также оценка лечащего терапевта. Пример дозы находится в интервале от около 0,001 до около 200 мг соединения на 1 кг массы тела пациента в сутки, предпочтительно от около 0,05 до 100 мг/кг/сут, или от около 1 до 35 мг/кг/сут, единичной или дробной дозы (например, два раза в день, три раза в день, четыре раза в сутки). Для человека с массой тела 70 кг иллюстративный интервал допустимой дозировки составляет от около 0,05 до около 7 г/сут, или от около 0,2 до около 2,5 г/сут.- 14022766 После улучшения состояния пациента облегчения симптомов заболевания или расстройства дозировка может быть скорректирована для профилактического или поддерживающего лечения. Например,дозировка, частота введения или и то и другое могут быть снижены в зависимости от симптомов до уровня, при котором поддерживается желательный терапевтический или профилактический эффект от приема препарата. Разумеется, если симптомы облегчены до приемлемого уровня, лечение можно прекратить. Однако при наличии рецидивов симптомов пациенту может потребоваться долговременное периодическое лечение. Кроме того, активные агенты в соответствии с настоящим изобретением могут применяться в сочетании с дополнительными активными компонентами для лечения перечисленных выше состояний. Дополнительные действующие вещества могут вводиться совместно с действующим веществом соединений формул I и II или формул 1 и 2 или входить в состав фармацевтической композиции в соответствии с изобретением. В примерном варианте осуществления изобретения дополнительные действующие вещества представляют собой вещества с известной или обнаруженной эффективностью при лечении состояний, расстройств или заболеваний, опосредованных активностью орексина, например, другой модулятор орексина или соединение, активное в отношении другой мишени, связанной с конкретным состоянием,расстройством или заболеванием. Такая комбинация может служить для повышения эффективности (например, путем включения в комбинацию соединения, потенцирующего силу действия или эффективность действующего вещества в соответствии с изобретением), снижения одного или нескольких побочных явлений или снижения требуемой дозы действующего вещества настоящего изобретения. Активные агенты настоящего изобретения используются самостоятельно или в сочетании с одним или более дополнительным активным компонентом для приготовления фармацевтических композиций,соответствующих целям настоящего изобретения. Фармацевтическая композиция настоящего изобретения включает: (а) эффективное количество, по меньшей мере, одного действующего вещества настоящего изобретения; и (b) фармацевтически приемлемое вспомогательное вещество. Термин "фармацевтически приемлемый эксципиент" означает нетоксичное, биологически переносимое и по остальным параметрам биологически допустимое для введения пациенту вещество, такое как инертное вещество, добавляемое в фармакологическую композицию или иным образом используемое в качестве средства доставки, носителя или разбавителя для облегчения введения агента и совместимое с последним. Примеры наполнителей содержат карбонат кальция, фосфат кальция, различные сахара и типы крахмалов, производные целлюлозы, желатин, растительные масла и полиэтиленгликоли. Формы доставки фармацевтических композиций, содержащих одну или более единиц дозирования активных агентов, могут быть приготовлены с использованием соответствующих фармацевтических наполнителей и способов приготовления, известных сегодня или доступных в будущем специалистам. Описываемые композиции могут в соответствии с целями настоящего изобретения вводиться любым соответствующим путем, например, перорально, парентерально, ректально, местно, в глаза либо через ингалятор. Препарат может быть в форме таблеток, капсул, саше, драже, порошков, гранул, пастилок, порошков для восстановления, жидких препаратов или суппозиториев. Предпочтительно композиции сформулированы для внутривенного вливания, местного применения или перорального введения. Для перорального введения соединения изобретения могут быть представлены в форме таблеток или капсул, либо в виде раствора, эмульсии или суспензии. Для приготовления композиций для перорального введения соединения могут быть сформулированы так, чтобы давать определенную дозу, например от около 0,05 до около 100 мг/кг в сутки, или от около 0,05 до около 35 мг/кг в сутки, или от около 0,1 до около 10 мг/кг в сутки. Например, общую суточную дозу приблизительно 5 мг - 5 г в сутки можно вводить один, два, три или четыре раза в сутки. Таблетки для перорального введения могут включать соединение в соответствии с изобретением,смешанные с фармацевтически приемлемыми наполнителями, такими как инертные разбавители, вещества для улучшения распадаемости таблеток, связывающие агенты, смазывающие вещества, подсластители, вкусовые добавки, красители и консерванты. Соответствующие инертные наполнители содержат карбонаты натрия и кальция, фосфаты натрия и кальция, лактозу, крахмал, сахар, глюкозу, метилцеллюлозу, стеарат магния, маннит, сорбит и т.п. Примеры жидких наполнителей для орального введения содержат этанол, глицерин, воду и т.п. Крахмал, поливинилпирролидон (PVP), натрий гликолят крахмала,микрокристаллическая целлюлоза и альгиновая кислота являются допустимыми веществами для улучшения распадаемости таблеток. Связывающие агенты могут включать крахмал и желатин. Смазывающим агентом, при его наличии, может быть стеарат магния, стеариновая кислота или тальк. При необходимости таблетки могут быть покрыты таким материалом, как глицерилмоностеарат или глицерилдистеарат, для замедления всасывания в желудочно-кишечном тракте, или могут иметь энтеросолюбельную оболочку. Капсулы для орального применения могут быть твердыми и мягкими желатиновыми. Для приготовления твердых желатиновых капсул соединения изобретения могут быть смешаны с твердым, полужидким или жидким разбавителем. Мягкие желатиновые капсулы могут быть приготовлены путем смешивания соединения изобретения с водой или маслом, таким как арахисовое масло или оливковое масло,- 15022766 с жидким парафином, смесью моно- и диглицеридов жирных кислот с короткой цепью, полиэтиленгликолем 400 или пропиленгликолем. Возможные жидкости для перорального применения содержат суспензии, растворы, эмульсии или сиропы, либо могут быть лиофилизованы и поставляться в сухом виде для восстановления водой или иным соответствующим носителем перед использованием. Такие жидкие композиции по желанию могут содержать фармацевтически приемлемые вспомогательные вещества, например, суспендирующие добавки (например, сорбит, метилцеллюлоза, натрия альгинат, желатин, гидроксиэтилцеллюлоза, карбоксиметилцеллюлоза, гель алюминия стеарата и т.п.); Неводный носитель, например, масло (например,миндальное масло или фракционированное кокосовое масло), полипропиленгликоль, этиловый спирт или воду; консерванты (например, метил или пропил п-гидроксибензоат или сорбиновую кислоту); Смачивающие добавки, например, лецитин; и, если нужно, ароматизаторы или красители. Активные агенты, составляющие предмет настоящего изобретения, могут также вводиться пациенту парентеральными путями. Например, соединения могут быть сформулированы для ректального применения в виде суппозиториев. Для парентерального введения, включая внутривенное, внутримышечное,внутрибрюшинное или подкожное, соединения изобретения могут быть представлены в виде стерильных водных растворов или суспензий, буферных с адекватным рН и изотоничностью или в парентерально приемлемом масле. Соответствующие жидкие носители содержат раствор Рингера и изотонический раствор хлорида натрия. Такие формы будут представлены в форме стандартной дозировки, такой как ампулы или одноразовые приспособления для инъекций, в форме нескольких доз, таких как колбы, из которых может быть отобрана адекватная доза, или в твердой форме или в форме первичного концентрата,который может быть использован для приготовления соединений, пригодных для введения. Иллюстративные дозировки для вливания могут варьировать от около 1 до 1000 мкг/кг/мин соединения, перемешанного с фармакологическим носителем за время от нескольких мин до нескольких суток. Для местного введения соединения могут быть смешаны с фармацевтическим носителем в концентрации от около 0,1% до около 10% лекарства в носителе. В другом способе введения соединения настоящего изобретения могут использоваться в виде пластыря для трансдермальной доставки. Соединения изобретения могут альтернативно вводиться в способах настоящего изобретения путем ингаляции, через нос или рот, например, в виде спрея, содержащего также допустимый носитель. Ниже описаны примеры соединений, пригодных для применения в способах настоящего изобретения путем ссылок на иллюстративные схемы синтеза для их общего приготовления, а также с последующими конкретными примерами. Как станет ясно специалистам в области, для получения различных соединений исходные материалы могут быть выбраны соответствующим образом, так чтобы желаемые заместители сохранялись в соответствии со схемой реакции при наличии или отсутствии защиты, в зависимости от ситуации, и давали желаемый продукт. В качестве альтернативы может быть необходимо или желательно ввести вместо желаемого заместителя соответствующую группу, которая может быть проведена через схему реакции и затем заменена соответствующим образом на требуемый заместитель. Если не указано иное, переменные соответствуют определениям выше в отношении формулы (I). Реакции могут проводиться в промежутке между температурой плавления и температурой флегмы растворителя и предпочтительно между 0 С и температурой флегмы растворителя. Реакционные смеси можно нагревать традиционным способом или в микроволновой печи. Реакции также могут проводиться в герметичном сосуде под давлением выше температуры кипения растворителя. В настоящем документе используются следующие сокращения: Промежуточные соединения формул (VIa) и (VIb) легко получить как показано на схеме А из имеющихся в продаже и синтезированных соединений формулы (IV). Соединения формулы (VIa) получают путем реакции соединения формулы (IV), где Ra2 представляет собой -Н, галоген, -С 1-4 алкил, -С 1-4 алкокси, -NO2, -NHCOCH3, либо два члена Ra2 могут соединяться с образованием 6-членного ароматического кольца, где X представляет собой С или N (при условии, что только один член X может быть N), с имеющимися в продаже соединениями НЕТ формулы (V), где НЕТ - 5-6-членный гетероарил, содержащий от одного до трех атомов азота, в присутствии йодида ртути (I), CS2CO3 и N,N'-диметилциклогексан-1,2-диамина; в растворителе, например, ДМФ или диоксане, при температуре от 60 до 100 С (при нагреве традиционными способами или в микроволновой печи). Специалистам в данной области известно, что 1,2,3-триазол может существовать в двух таутомерных формах, обозначаемых как 2 Н-[1,2,3]триазол и 1 Н-[1,2,3]триазол, что обусловливает формирование двух региоизомеров. Альтернативно, соединения формулы (VIb) можно получить путем реакции галогенпроизводных бензонитрильных соединений формулы (VII) с НЕТ, где НЕТ представляет собой 5-членный гетероарил,выбранный из группы, состоящей из триазола или пиразола, в растворителе, например, ДМФ и т.п., в присутствии неорганического основания, например, K2CO3 и т.п., при температуре от 100 до 130 С. Последующий гидролиз нитрила основанием, например, водным раствором NaOH и т.п., в растворителе,например метаноле, дает соединения формулы (VIb). Соединения формулы (VIb) можно также получить путем реакции галогенпроизводных бензонитрильных соединений формулы (VII) с HET-Sn(алкил)3, где HET-Sn(алкил)3 представляет собой имеющийся в продаже или синтезированный приемлемыми методами триалкилолово-гетероарил в растворителе, например, диметиловом эфире, в присутствии палладиевого катализатора, например, Pd(PPh3)4, в присутствии или отсутствие каталитического количества йодида меди, при температурах от 100 до 160 С, с нагревом традиционным способом или в микроволновой печи. Последующий гидролиз нитрила- 17022766 основанием, например, водным раствором NaOH и т.п., в растворителе, например, метаноле, дает соединения формулы (VIb). Соединения формулы (VIb) можно также получить путем реакции галогенопроизводных бензонитрильных соединений формулы (VII) с НЕТ-бороновой кислотой, где НЕТ-бороновая кислота представляет собой имеющуюся в продаже или полученную приемлемым синтетическим путем бороновую кислоту,в растворителе, например, ДМФ, в присутствии основания, например, NaHCO3, палладиевого катализатора, например, Pd(PPh3)4, при температуре от 80 С до температуры кипения растворителя. Последующий гидролиз нитрила основанием, например, водным раствором NaOH и т.п., в растворителе, например,метаноле, дает соединения формулы (VIb). Соединения формулы (I), где Rb2 представляет собой -I, далее превращаются в соединения формулы(I), где Rb2 представляет собой НЕТ, где НЕТ представляет собой 5-6-членный гетероарил, содержащий от одного до трех атомов азота и могущий содержать один атом кислорода. При реакции соединения формулы (I), где Rb2 представляет собой HET-Sn(алкил)3, где НЕТ-Sn(алкил)3 представляет собой имеющийся в продаже или синтезированный приемлемым способом триалкилолово-гетероарил в растворителе, например диметиловом эфире, в присутствии палладиевого катализатора, например, Pd(PPh3)4, в присутствии или отсутствие каталитического количества йодида меди при температурах от 100 до 160 С с нагревом традиционным способом или в микроволновой печи, образуются соединения формулы (I). Схема В В соответствии со схемой В соединения формулы (VIc) получают из соединений формулы (IV),сначала путем превращения имеющегося в продаже или полученного приемлемым синтетическим путем соединения формулы (IV), где Ra2 представляет собой -Н, галоген, -С 1-4 алкил, -С 1-4 алкокси, -CF3 или-NO2, и где X представляет собой С или N (при условии, что только один член X может быть N) в соединение формулы (IX) в условиях этерификации, например, путем обработки спиртового раствора соединения (IV) кислотой. В предпочтительном варианте осуществления изобретения соединение формулы(IV) растворяют в растворителе, например МеОН, и обрабатывают H2SO4 для получения соединения формулы (IX). Соединение формулы (X) получают путем реакции подходящего соединения формулы(IX) с пинаколбораном в присутствии фосфина и палладиевого катализатора в присутствии основного амина в растворителе, например ТГФ, при температурах от комнатной до 70 С. В предпочтительном варианте осуществления фосфин представляет собой три(о-толил)фосфин, палладиевый катализатор-Pd(OAc)2, а основной амин триэтиламин. Соединение формулы (VIc) получают путем реакции соединения формулы (X) с соединением Rb2Cl, где Rb2-Cl представляет собой подходящий готовый или синтезированный 6-членный хлорзамещенный гетероарил, в присутствии палладиевого катализатора, основания, например Na2CO3, и т.п., в растворителе, например, 2-метилтетрагидрофуране (2-метил-ТГФ) и т.п., при температурах от комнатной до 80 С. В предпочтительном варианте осуществления изобретения палладиевый катализатор представляет собой продукт присоединения PdCl2 (dppf) -ДХМ, основание представляет собой Na2CO3 и растворитель представляет собой 2-метил-ТГФ. Соединение формулы (VIc) получают из соединения формулы (XI) путем гидролиза эфира. В предпочтительном способе гидролиза соединение формулы (XI) в метил-ТГФ обрабатывают водным раствором NaOH для получения соединения формулы (VIc). Схема С- 18022766 В соответствии со схемой С, замещенные гетероарилы R2Cl формулы (XIVa) и (XVIb) получают из готовых или синтезированных соединений формулы (XIIIa) или (XIIIb). Используют готовые пиримидолы формулы (XIIIa) или формулы (XIIIb), либо получают их путем реакции замещенных алкилмалонатов формулы (XII), где Re представляет собой галоген, с мочевиной в присутствии основания, например, натрия этоксида и т.п.; В подходящем растворителе, например, этаноле, при температурах от комнатной до температуры кипения растворителя. Хлорирование готовых пиримидинолов формулы (XIIIb) или полученных синтетическим путем соединений формулы (XIIIa) производят с помощью хлорирующего агента,например оксалилхлорида и т.п.; в растворителе, например CH2Cl2, в присутствии основания, напримерN,N-диметиланилина и т.п.; при температурах от комнатной до температуры кипения растворителя для получения хлорпиримидинов формулы (XIVa) или (XIVb). Кроме того, хлорпиримидины формулыFe(acac)3, в растворителе, например Et2O, при 0 С с получением алкилхлорпиримидинов формулы (XVIa) или (XVIb). Схема D В соответствии со схемой D соединения формулы (XX) получают из синтезированного или готового 2-бензилоктагидропиррол[3,4-с]пиррола сначала путем защиты вторичного атома азота группы 2 бензилоктагидропиррол[3,4-с]пиррола с помощью карбаматной группы. В предпочтительном варианте осуществления изобретения карбамат представляет собой трет-бутилкарбамат (boc), который получают путем обработки 2-бензилоктагидропиррол[3,4-с]пиррола ди-трет-бутилдикарбонатом в растворителе,например ДХМ, для получения соединения (XVII). Соединение (XVIII) получают путем обработки соединения (XVII) газообразным водородом в присутствии катализатора. В особенно предпочтительном варианте осуществления катализатор представляет собой Pd на углероде, в растворителе, например МеОН, в присутствии АсОН. Соединение формулы (XIX) получают путем обработки соединения (XVIII) соединением формулы R2Cl, где R2 - то же, что в формуле (I). Готовые или полученные путем синтеза соответствующие гетероарилы формулы R2Cl вступают в реакцию с соединением (XVIII) в присутствии подходящего третичного органического основания, например CS2CO3, Na2CO3, ТЭА и т.п. В растворителе, таком как ДМФ, дихлорметан, ТГФ, н-бутанол и т.п.; при температуре от комнатной до температуры кипения растворителя с использованием традиционного или микроволнового нагрева для получения соединений формулы (XIX). В предпочтительном варианте осуществления основание представляет собойCS2CO3 и растворитель представляет собой ДМФ. Удаление группы трет-бутилкарбамата (boc) в соединениях формулы (XIX) достигается методами,известными специалистам, например обработкой HCl, ТФК или п-толуолсульфоновой кислотой, в растворителе, например СН 3 ОН, диоксане или CH2Cl2. В предпочтительном варианте осуществления изобретения соединение формулы (XIX) обрабатывается ТФК и ДХМ или HCl для получения соединения формулы (XX). Соединения формулы (XX) также могут быть получены из 2-бензилоктагидропиррол[3,4-с]пиррола. В соответствии со схемой D, 2-бензилоктагидропиррол[3,4-с]пиррол обрабатывается R2Cl, где R2 - то же,что в формуле (I). Готовый или синтезированный соответствующим образом замещенный гетероарил формулы R2Cl реагирует с соединением 2-бензилоктагидропиррол[3,4-с]пиррол в присутствии третичного органического или неорганического основания, например, CS2CO3, NarCO3, ТЭА и т.п.; В растворителе, таком как ДМФ, дихлорметан, ТГФ и т.п.; при температуре от комнатной до температуры кипения растворителя; для получения соединения формулы (XXI). В предпочтительном варианте осуществления изобретения основание представляет собой CS2CO3 и растворитель представляет собой ДМФ. Соединение формулы (XX) получают путем обработки соединения формулы (XXI) газообразным водородом в присутствии катализатора в растворителе, например АсОН. В предпочтительном варианте осуществления катализатор представляет собой Pd на углероде. В соответствии со схемой Е, соединение формулы (I) получают из соединения формулы (XIX),(XX) или (XXI) путем реакции соединения формулы (XIX), (XX) или (XXI) с соединением формулыR1CO2H в условиях, благоприятных для образования амида. Соединения формулы R1CO2H, где R1 - то же, что в формуле (I), готовые или полученные путем синтеза, соответствующим образом замещенные гетероарил- или арилкарбоновые кислоты. В предпочтительном варианте осуществления соединение формулы (XIX), (XX) или (XXI) в форме свободного основания или соли кислоты вступает в реакцию с соединением формулы R1CO2H в присутствии обезвоживающего агента, например HOBt/EDAC, CDI,HATU, НОАТ; подходящего основания, например ДИПЭА, ТЭА и т.п.; в органическом растворителе или смеси растворителей, например толуоле, ацетонитриле, уксусноэтиловом эфире, ДМФ, ТГФ, метиленхлориде и т.п.; для получения соединения формулы (XXII), (XXIII) или (I). В особенно предпочтительном варианте осуществления изобретения обезвоживающий агент представляет собой HATU, а основание представляет собой ДИПЭА. В альтернативном варианте осуществления изобретения соединение формулы R1CO2H (как описано выше) может быть сначала превращено в соединение формулы R1COCl, или соединение формулыR1COCl представляет собой готовый замещенный ароматический сульфонилхлорид. В предпочтительном варианте осуществления изобретения соединение формулы R1CO2H обрабатывается тионилхлоридом в растворителе, например толуоле, для получения соединения формулы R1COCl. Соединение формулы (I) получают путем обработки соединения формулы R1COCl соединением формулы (XIX), (XX) или (XXI), подходящим третичным органическим основанием, например ТЭА и т.п., в растворителе, например дихлорметане, ТГФ и т.п., при температуре от комнатной до температуры кипения растворителя. Соединение формулы (II) получают путем обработки соединения формулы R1SO2Cl соединением формулы (XIX), (XXI) или (XXV), где R4 представляет собой (5-трифторметил)пиридин-2-ил, (5 трифторметил)пиримидин-2-ил, 4,6-диметилпиримидин-2-ил или хиноксалин-2-ил; в подходящем третичном органическом основании, например ТЭА и т.п., в растворителе, например дихлорметане, ТГФ и т.п., при температуре от комнатной до температуры кипения растворителя. Что касается схемы Е, специалисту в данной области известно, что последовательность превращений, показанная на схемах D и Е, может быть другой, например, формирование амидной связи может быть первой реакцией получения соединений формул (XXII) и (XXIII). После удаления группы Nбензила из соединения формулы (XXII) или удаление карбамата из соединения формулы (XXIII) соединение вступает в реакцию с соединением формулы R2Cl, где R2Cl - то же, что в формуле (I). Схема F 3-фтор-2-(3-метил-1,2,4-оксадиазол-5-ил)бензойная кислота и 2-фтор-6-(3-метил-1,2,4-оксадиазол 5-ил)бензойная кислота образуются по схеме Н. 3-фторфталевый ангидрид растворяли в растворителе,например МеОН, при температуре от комнатной до температуры кипения растворителя для получения сложных эфиров кислот (XXVIIa) и (XXIIb). Превращение кислоты в хлорангидрид производится в стандартных условиях хлорирования. В предпочтительном способе осуществления кислота обрабатывается оксалилхлоридом в растворителе, например ДХМ. При последующей реакции хлорангидрида с Nгидроксиацетамидом в растворителе, например CH2Cl2, образуется смесь эфиров (XXVIIIa) и (XXVIIIb). В конечном итоге эфиры (XXVIIIa) и (XXVIIIb) превращаются в смесь эфиров (XXIXa) и (XXIXb) и ки- 20022766 слот (ХХХа) и (XXXb) путем обработки основанием, предпочтительно ацетатом натрия, в присутствии растворителя, предпочтительно t-BuOH. Альтернативно, кислоту (ХХХа) получают путем превращения 2-фтор-6-йодбензойной кислоты в хлорангидрид путем реакции с хлорирующим агентом, например, оксалилхлоридом, в растворителе, например, ДХМ, с каталитическим количеством ДМФ, при температуре 0 С. Последующая реакция хлорангидрида с N-гидроксиацетамидом в растворителе, например, CH2Cl2, дает (Z)-N'-2-фтор-6 йодбензоил)окси)ацетимидамид. 5-(2-фтор-6-йодфенил)-3-метил-1,2,4-оксадиазол получают путем реакции (Z)-N'-2-фтор-6-йодбензоил)окси)ацетимидамида с ацетатом натрия в растворителе, например третбутаноле, при температуре от 100 до 110 С. 3-Фтор-2-(3-метил-1,2,4-оксадиазол-5-ил)бензойную кислоту(ХХХа) получают путем реакции 5-(2-фтор-6-йодфенил)-3-метил-1,2,4-оксадиазола с реактивом Гриньяна, например, i-PrMgCl, в подходящем растворителе, например ТГФ и т.п., при температуре -78 С. При последующем добавлении газообразного СО 2 при температуре-78 С образуется 3-фтор-2-(3-метил-1,2,4 оксадиазол-5-ил)бензойная кислота (ХХХа). Схема Н Дейтерированные пиримидиновые соединения формулы (XXXII) получают в соответствии со схемой Н. Ацетилацетон вступает в реакцию с неорганическим основанием, например K2CO3 в дейтерированной воде, при температуре от 100 до 120 С, для получения 1,1,1,3,3,3,5,5-октадейтеропентан-2,4 диона. 1,1,1,3,3,3,5,5-октадейтеропентан-2,4-дион затем вступает в реакцию с дейтерированной мочевиной,в растворителе, например дейтерированном этаноле, 35 мас.% DCl в D2O, при температуре от 90 до 100 С для получения дейтерированных пиримидинолов формулы (XXXI). При хлорировании в стандартных условиях образуются хлордейтерированные пиримидиновые соединения формулы (XXXII). Соединения формулы (I) могут быть переведены в соответствующие соли с применением способов,известных специалистам в данной области. Например, амины формулы (I) могут обрабатываться трифторуксусной кислотой (ТФК), HCl, малеиновой кислотой или лимонной кислотой в растворителе, например (Et2O), CH2Cl2, тетрагидрофуране (ТГФ), или метаноле (МеОН) для получения соответствующих солей. В особенно предпочтительном варианте осуществления кислота представляет собой HCl и растворитель представляет собой изопропанол. Соединения, приготовленные в соответствии со схемами, описанными выше, могут быть получены как отдельно взятые энантиомеры, диастереомеры или региоизомеры путем энантио-, диастерео- или региоспецифичного синтеза или путем разделения. Соединения, приготовленные в соответствии со схемами, описанными выше, альтернативно могут быть получены как рацемические (1:1) или нерацемические (не 1:1) смеси или как смеси диастереомеров или региоизомеров. В том случае, если получают рацемические и нерацемические смеси энантиомеров, отдельно взятые энантиомеры могут быть выделены с помощью традиционных способов разделения, известных специалистам в данной области, таких как хиральная хроматография, перекристаллизация, образование диастереомерной соли, превращение в диастереомерные аддукты, биотрансформация или ферментная трансформация. В том случае, если получают региоизомерные или диастереомерные смеси, отдельно взятые изомеры могут быть приготовлены традиционными способами, такими как хроматография или кристаллизация. В следующих примерах более подробно проиллюстрировано настоящее изобретение и предпочтительные варианты его осуществления. Примеры Химия. Если не указано иное, для получения описанных в приведенных ниже примерах соединений и соответствующих аналитических данных использовались следующие экспериментальные и аналитические процедуры. Если иное не оговорено особо, реакционные смеси перемешивали на магнитной мешалке при комнатной температуре в атмосфере азота. Если растворы были "осушены", то, как правило, для этого использовали осушающий агент, такой как Na2SO4 или MgSO4. Если смеси, растворы и экстракты были"концентрированы", то обычно их концентрировали на роторном испарителе при пониженном давлении. Реакции в условиях микроволнового излучения проводили в инициаторе Biotage или приборе СЕМ Discover. Для колоночной хроматографии на нормальной фазе использовали силикагель (SiO2) в виде готовых патронов, элюирование проводили указанными растворителями. Препаративную обращенно-фазную высокоэффективную жидкостную хроматографию (ВЭЖХ) проводили с помощью системы Gilson с колонкой Xterra Prep RP18 или XBridge C18 OBD (5 мкм, 30100 мм или 50150 мм), с градиентом ацето- 21022766 нитрил/вода 10-99% (20 мМ NH4OH) в течение 12-18 мин, при скорости протекания 30 мл/мин. Если не указано иное, масс-спектры (МС) получали на анализаторе Agilent серии 1100 MSD при ионизации методом электрораспыления (ИЭР) в позитивном режиме. Рассчитанная масса соответствует точно массе соединения. Спектры ЯМР (NMR) были получены на спектрометрах Bruker, модель DRX. Формат данных 1 Н ЯМР: химический сдвиг в промилле, слабопольный сдвиг относительно эталонного соединения тетраметилсилана (мультиплетность, константа взаимодействия J в Гц, интеграция). Химические названия генерировались с помощью ChemDraw Ultra 6.0.2 (CambridgeSoft Corp., Cambridge, MA) или ACD/Name в. 9 (Advanced Chemistry Development, Торонто, Онтарио, Канада). Промежуточный продукт: 5-фтор-2-[1,2,3]триазол-2-ил-бензойная кислота 5-Фтор-2-[1,2,3]триазол-2-ил-бензойная кислота. К раствору 5-фтор-2-йодбензойной кислоты (3,86 г, 14,65 ммоль) в сосуде для микроволновой печи добавляли 2 Н-[1,2,3]триазол (2,5 г, 36,2 ммоль),CS2CO3 (8,62 г, 24,5 ммоль), транс-N,N'-диметилциклогексан-1,2-диамин (0,4 мл), Cul (244 мг) и ДМФEtOAc. Водный слой подкисляли и экстрагировали EtOAc. Органический слой высушивали над Na2SO4 и концентрировали. После хроматографии (ДХМ до 10% МеОН/1% НОАс/ДХМ) получали продукт в виде белого порошка (2,14 г, 71%). 1H ЯМР (400 МГц, CD3OD): 7,91 (с, 2 Н), 7,76 (дд, J=8,9, 4,8 Гц, 1 Н), 7,59(дд, J=8,5, 2,9 Гц, 1 Н), 7,49-7,42 (м, 1 Н). Промежуточные продукты 2-12 готовили аналогично промежуточному продукту 1. Промежуточный продукт 2: 2-[1,2,3]триазол-2-ил-бензойная кислота Указанное в заголовке соединение получали аналогично промежуточному продукту 1, но вместо 5 фтор-2-йодбензойной кислоты использовали 2-йодбензойную кислоту. В результате этой реакции образовалось 2 продукта, 2-[1,2,3]триазол-2-ил-бензойная кислота и 2-[1,2,3]триазол-1-ил-бензойная кислота,что обусловлено наличием таутомерных форм 1,2,3-триазола. 1 Н ЯМР (400 МГц, CD3OD): 7,91 (с, 2 Н),7,85-7,82 (м, 1 Н), 7,75 (дд, J=8,1, 1,0 Гц, 1 Н), 7,69 (тд, J=7,7, 1,5 Гц, 1 Н), 7,60-7,55 (м, 1 Н). Промежуточный продукт 3: 2-[1,2,3]триазол-1-ил-бензойная кислота Указанное в заголовке соединение выделяли из продуктов синтеза промежуточного продукта 2. 1 Н ЯМР (400 МГц, CD3OD): 6,70 (д, J=0,9 Гц, 1 Н), 6,50 (дд, J=7,7, 1,5 Гц, 1 Н), 6,30 (д, J=1,0 Гц, 1 Н),6,24,6,18 (м, 1 Н), 6,17-6,11 (м, 1 Н), 6,01 (дд, J=7,8, 1,0 Гц, 1 Н). Промежуточный продукт 4: 4-фтор-2-[1,2,3]триазол-2-ил-бензойная кислота Указанное в заголовке соединение получали аналогично промежуточному продукту 1, но вместо 5 фтор-2-йодбензойной кислоты использовали 4-фтор-2-йодбензойную кислоту на стадии А. 1 Указанное в заголовке соединение получали аналогично промежуточному продукту 1, но вместо 5 фтор-2-йодбензойной кислоты использовали 3-фтор-2-йодбензойную кислоту на стадии А. 1H ЯМР (400 МГц, CD3OD): 7,93 (с, 2 Н), 7,81 (д, J=8,3 Гц, 1 Н), 7,63-7,58 (м, 1 Н), 7,29 (тд, J=8,9, 0,9 Гц, 1 Н). Промежуточный продукт 6: 4-хлор-2-[1,2,3]триазол-2-ил-бензойная кислота Указанное в заголовке соединение получали аналогично промежуточному продукту 1, но вместо 5 фтор-2-йодбензойной кислоты использовали 4-хлор-2-йодбензойную кислоту на стадии А. 1 Указанное в заголовке соединение получали аналогично промежуточному продукту 1, но вместо 5 фтор-2-йодбензойной кислоты использовали 2-бром-5-йодбензойную кислоту на стадии А. 1H ЯМР (400 МГц, CD3OD): 8,09 (д, J=2,0, 1 Н), 8,03-7,97 (м, 1 Н), 7,95-7,86 (м, 3 Н), 7,53 (д, J=8,4, 1H). Промежуточный продукт 8: 5-метил-2-[1,2,3]триазол-2-ил-бензойная кислота Указанное в заголовке соединение получали аналогично промежуточному продукту 1, но вместо 5 фтор-2-йодбензойной кислоты использовали 2-йод-5-метилбензойную кислоту на стадии А. 1H ЯМР (400 МГц, CD3OD): 7,87 (с, 2 Н), 7,66 (д, J=1,3 Гц, 1 Н), 7,59 (д, J=8,2 Гц, 1 Н), 7,53-7,46 (м, 1 Н), 2,45 (с, 3 Н). Промежуточный продукт 9: 5-хлор-2-[1,2,3]триазол-2-ил-бензойная кислота Указанное в заголовке соединение получали аналогично промежуточному продукту 1, но вместо 5 фтор-2-йодбензойной кислоты использовали 5-хлор-2-йодбензойную кислоту на стадии А. 1H ЯМР (400 МГц, CD3OD): 7,91 (с, 2 Н), 7,82-7,74 (м, 2 Н), 7,71-7,66 (м, 1 Н). Промежуточный продукт 10: 5-метокси-2-[1,2,3]триазол-2-ил-бензойная кислота Указанное в заголовке соединение получали аналогично промежуточному продукту 1, но вместо 5 фтор-2-йодбензойной кислоты использовали 2-йод-5-метоксибензойную кислоту на стадии А. 1H ЯМР Указанное в заголовке соединение получали аналогично промежуточному продукту 1, но вместо 5 фтор-2-йодбензойной кислоты использовали 2-йод-6-метилбензойную кислоту на стадии А. 1H ЯМР (400 МГц, CD3OD): 7,89 (с, 2 Н), 7,72 (д, J=8,1 Гц, 1 Н), 7,48 (т, J=7,9 Гц, 1 Н), 7,36 (д, J=7,7 Гц, 1 Н), 2,46 (с, 3 Н). Промежуточный продукт 12: 2-фтор-6-[1,2,3]триазол-2-ил-бензойная кислота Способ А. Указанное в заголовке соединение получали аналогично промежуточному продукту 1, но вместо 5-фтор-2-йодбензойной кислоты использовали 2-фтор-6-йодбензойную кислоту. 1H ЯМР (400- 23022766 МГц, CD3OD): 7,96 (с, 2 Н), 7,87-7,82 (м, 1 Н), 7,70 (тд, J=8,1, 5,1 Гц, 1 Н), 7,59 (ддд, J=9,7, 8,4, 1,4 Гц, 1 Н). Способ В. 2-Фтор-6-[1,2,3]триазол-2-ил-бензойная кислота. В двухлитровую трехгорлую круглодонную колбу, снабженную навесной механической мешалкой, термопарой, колбонагревателем, обратным холодильником и отверстием для подачи азота, вносили 2-фтор-6-йодбензойную кислоту (127 г, 480 ммоль), йодид меди (4,57 г, 24 ммоль) и CS2CO3 (312,6 г, 965 ммоль). К этим твердым веществам добавляли диоксан (640 мл), затем воду (2,6 мл, 144 ммоль), затем 1 Н-1,2,3-триазол (55,6 мл, 959 ммоль), и,наконец, транс-1,2-диметилциклогексан-1,2-диамин (15,1 мл, 96 ммоль). После этого смесь нагревали до 60 С в течение 30 мин, затем до 83 С в течение 30 мин и, наконец, до 100 С в течение 3 ч. Через 3 ч выдержки при 100 С смесь охлаждали и добавляли 1 л МТБЭ и 1 л воды. После энергичного встряхивания слои разделяли и донный слой подкисляли до рН 1,72 добавлением примерно 148 мл концентрированной хлористо-водородной кислоты. После этого водный раствор дважды экстрагировали EtOAc. Комбинированный органический слой высушивали над Na2SO4, фильтровали и концентрировали до получения темного маслянистого вещества. Маслянистое вещество перемешивали в течение ночи с EtOAc (450 мл) и отфильтровывали образующийся осадок. Материнские жидкости концентрировали до получения твердого вещества коричневого цвета (106,21 г, 75 мас.% по данным количественной ВЭЖХ, 79,7 г, 80%). 1H ЯМР (400 МГц, ДМСО-d6): 8,22-8,13 (шир. с, 2 Н), 7,84-7,80 (м, 1 Н), 7,74-7,65 (м, 1 Н), 7,50-7,41 (м, 1 Н). Промежуточный продукт 13: 5-фтор-2-пиримидин-2-ил-бензойная кислота Стадия А. 5-Фтор-2-йодбензойной кислоты метиловый эфир. В круглодонную колбу объемом 500 мл вносили 5-фтор-2-йодбензойную кислоту (23 г, 86,5 ммоль) в метаноле (230 мл). К полученному раствору добавляли конц. серную кислоту (2,3 мл, 43,2 ммоль). Полученную реакционную смесь нагревали до температуры 65 С и перемешивали ее в течение 15 ч. Полученную смесь концентрировали под пониженным давлением для получения неочищенного продукта, который затем разделяли между EtOAc (250 мл) и полунасыщенным раствором Na2CO3(aq) (250 мл). Слои тщательно перемешивали и разделяли. Органический слой высушивали над сульфатом магния, фильтровали и концентрировали под пониженным давлением для получения желтого маслянистого вещества (23 г, выход 95%). 1 Н ЯМР (400 МГц, CDCl3): 7,94 (дд, J=8,7, 5,4 Гц, 1 Н), 7,54 (дд, J=9,0, 3,1 Гц, 1 Н), 6,93 (м, 1 Н), 3, 94 (с, 3 Н). Стадия В. 5-Фтор-2-(4,4,5,5-тетраметил-[1,3,2]диоксаборолан-2-ил)бензойной кислоты метиловый эфир. В круглодонную колбу объемом 1 л с обратным холодильником, температурным датчиком и подключением к источнику азота вносили 5-фтор-2-йодбензойной кислоты метиловый эфир (23 г, 82 ммоль) в безводном ТГФ (250 мл). Добавляли безводный триэтиамин (34 мг, 246,4 ммоль) и дегазировали полученную смесь путем барботирования азота в течение 5 мин. К смеси добавляли пинаколборан (179 мл,123,2 ммоль) и дегазировали еще 5 мин. И наконец, добавляли три(о-толил)фосфин (1,25 г, 4,1 ммоль) и ацетат палладия (461 мг, 2,053 ммоль). Реакционную смесь снова дегазировали путем барботирования азота. Смесь нагревали до 65 С и перемешивали в течение часа. После охлаждения до комнатной температуры реакцию останавливали полунасыщенной солью хлорида аммония и разделяли получившиеся слои. Водный раствор дополнительно экстрагировали уксусноэтиловым эфиром (250 мл) и высушивали общий органический слой над сульфатом магния. После фильтрации и концентрации получался неочищенный продукт в форме желтого маслянистого вещества (23 г). Этот неочищенный продукт перемешивали в 25% EtOAc/гексана (250 мл). Полученные твердые продукты являлись нежелательными, поэтому их удаляли путем фильтрации. Полученный раствор концентрировали до желтого маслянистого вещества (21 г, 75 мас.% желаемый выход, 16,1 г фактический продукт, выход 70%), которое использовали на следующей стадии без дальнейшей очистки. 1 Н ЯМР-исследование показало, что неочищенный продукт содержит 14 мас.% пинакола, 6,5 мас.% лиганда и 4 мас.% исходного материала. 1 Н ЯМР (400 МГц,CDCl3): 7,61 (дд, J=9,5, 2,5 Гц, 1 Н), 7,52-7,45 (м, 1 Н), 7,21 (тд, J=8,3, 2,5 Гц, 1 Н), 3,91 (с, ЗН), 1,41 (с,12 Н). Стадия С. 5-Фтор-2-пиримидин-2-ил-бензойной кислоты метиловый эфир. В круглодонную колбу объемом 250 мл вносили 5-фтор-2-(4,4,5,5-тетраметил-[1,3,2]диоксаборолан-2-ил)бензойной кислоты метиловый эфир (5,9 г, 21,06 ммоль) в 2-метил-ТГФ (50 мл). К полученному раствору добавляли 2 хлорпиримидин (2,9 г, 2 5,28 ммоль), карбонат натрия (6,7 г 63,19 ммоль) и воду (17 мл). Смесь дегазировали 30 мин. Продукт присоединения PdCl2(dppf)-ДХМ (CAS72287-26-4) (0,688 г, 0,843 ммоль) добавляли к реакционной смеси и дегазировали ее еще 30 мин. Полученную реакционную смесь нагревали до температуры 74 С и перемешивали ее в течение ночи. К полученному раствору добавляли диэтиловый эфир (100 мл) и воду (100 мл). Слои тщательно перемешивали и разделяли. Водный слой дополнительно экстрагировали диэтиловым эфиром (100 мл). Комбинированный органический слой высушивали над сульфатом магния, фильтровали и концентрировали под пониженным давлением для получения коричневого неочищенного материала (5,85 г, желаемое количество 49%, фактический продукт 2,87). Не- 24022766 очищенный продукт очищали путем перекристаллизации в 10% EtOAc/гексане. Смесь нагревали до 70 С и медленно охлаждали до комнатной температуры. После фильтрования получался желаемый продукт в виде твердого вещества коричневого цвета (1,72 г фактического продукта, выход после перекристаллизации 35%.) 1 Н ЯМР (400 МГц, CDCl3): 8,78 (д, J=4,9 Гц, 2 Н), 8,09 (дд, J=8,7, 5,5 Гц, 1 Н), 7,39 (дд, J=8,6,2,7 Гц, 1 Н), 7,30-7,20 (м, 2 Н), 3,77 (с, ЗН). Стадия D. 5-Фтор-2-пиримидин-2-ил-бензойная кислота. К раствору 5-фтор-2-пиримидин-2 илбензойной кислоты метилового эфира (1,72 г, 7,407 ммоль) в 2-метил-ТГФ (20 мл) добавляли гидроксид натрия (0,74 г, 18517 ммоль) и воду (20 мл). Смесь нагревали до 72 С и перемешивали в течение 2 ч. Слои разделяли и водный слой дополнительно экстрагировали МТБЭ. Затем в водный слой по каплям добавляли 50% HCl(aq) до достижения рН 1. Полученные твердые вещества фильтровали для получения желаемого продукта в форме беловатого твердого вещества (1,34 г, выход 83%). 1H ЯМР (400 МГц,CD3OD): 8,82 (д, J=5,0 Гц, 2 Н), 7,89 (дд, J=8,6, 5,4 Гц, 1 Н), 7,53 (дд, J=9,0, 2,7 Гц, 1 Н), 7,39 (м, 2 Н). Промежуточный продукт 14: 2-фтор-6-пиримидин-2-ил-бензойная кислота Стадия А. 2-Фтор-6-йодбензойной кислоты метиловый эфир. В круглодонную колбу объемом 200 мл вносили 2-фтор-6-йодбензойную кислоту (7,5 г, 28,2 ммоль), LiOHH2O (1,42 г, 33,8 ммоль и ТГФ (100 мл). Полученную реакционную смесь нагревали до температуры 50 С и перемешивали ее в течение 2 ч. Затем добавляли диметилсульфат (4,03 мл, 42,3 ммоль) 65 С и нагревали смесь до температуры 65C. Через 2 ч смесь охлаждали до комнатной температуры и добавляли NH4Cl(aq) (50 л, 13 мас.% раствор). Два образовавшихся слоя тщательно перемешивали, а затем разделяли. Органический слой высушивали над MgSO4, фильтровали и концентрировали под пониженным давлением для получения светлокоричневого маслянистого вещества (7,79 г, выход 99%). 1H ЯМР (400 МГц, CDCl3): 7,68-7,60 (м, 1 Н),7,15-7,06 (м, 2 Н), 3,98 (с, 3 Н). Стадия В. 2-Фтор-6-(4,4,5,5-тетраметил-[1,3,2]диоксаборолан-2-ил)бензойной кислоты метиловый эфир. В круглодонную колбу объемом 500 мл вносили 2-фтор-6-йодбензойной кислоты метиловый эфир(7,29, 26,0 ммоль и безводный ТГФ (150 мл). Эту смесь нагревали до 0 С и добавляли по каплям iPrMgCl (13,7 мл, 2MB ТГФ, 27,3 ммоль. Через 10 мин добавляли 2-изопропокси-4,4,5,5-тетраметил-1,3,2 диоксаборолан (5,58 мл, 27,3 ммоль). Смеси давали нагреться до комнатной температуры и через 30 мин добавляли раствор NH4Cl(aq) (150 мл, 13 мас.%). Слои смешивали и затем разделяли и водный слой экстрагировали 100 мл МТБЭ. Комбинированный органический слой высушивали над Na2SO4, фильтровали и концентрировали до конечной массы 6,07 г (90 мас.%, выход 75%). 1H ЯМР (400 МГц, CDCl3): 7,477,38 (м, 2 Н), 7,17-7,11 (м, 1 Н), 3,92 (с, 3 Н), 1,36 (с, 12 Н). Стадия С. 2-Фтор-6-пиримидин-2-ил-бензойной кислоты метиловый эфир. В круглодонную колбу объемом 250 мл под слоем азота вносили 2-фтор-6-(4,4,5,5-тетраметил-[1,3,2]диоксаборолан-2-ил)бензойной кислоты метиловый эфир (5,46 г, 19,5 ммоль) в 2-метил-ТГФ (50 мл), 2-хлорпиримидин (2,68 г, 23,4 ммоль и карбонате натрия (6,2 г, 58,5 ммоль в воде (17 мл). Затем добавляли продукт присоединения PdCl2 (dppf)-ДХМ (CAS72287-26-4) (1,27 г, 1,56 ммоль) и нагревали реакционную смесь до 74 С при перемешивании в течение 2,5 ч. После охлаждения смесь разводили МТБЭ (50 мл) и водой (80 мл). Слои тщательно перемешивали и разделяли. Водный слой дополнительно экстрагировали МТБЭ (100 мл). Комбинированный органический слой высушивали над сульфатом магния, фильтровали, концентрировали и очищали методом флеш-хроматографии (0-25% уксусноэтиловый эфир/гексан для получения указанного в заголовке соединения (1,72 г, 72 мас.%, 30% выход). 1 Н ЯМР (400 МГц, CDCl3): 8,79 (д,J=4,9 Гц, 2 Н), 8,15 (д, J=7,9 Гц, 1 Н), 7,51 (тд, J=8,1, 5,6 Гц, 1 Н), 7,28-7,20 (м, 2 Н), 3,92 (с, 3 Н). Стадия D. 2-Фтор-6-пиримидин-2-ил-бензойная кислота. К раствору 2-фтор-6-пиримидин-2-илбензойной кислоты метилового эфира (1,36 г, 5,85 ммоль) в 2-метил-ТГФ (20 мл) добавляли раствор гидроксида натрия (2MB воде, 9,3 мл, 18,6 ммоль). Смесь нагревали до 72 С и перемешивали в течение 9 ч. Слои разделяли и водный слой подкисляли до рН 2 путем добавления 50% HCl(aq) (3,1 мл) по каплям. Полученное твердое вещество перемешивали в течение часа, фильтровали, промывали водой, МТБЭ и гептаном, а затем высушивали для получения желаемого продукта в форме белого твердого вещества(6,16 г, 28,2 ммоль). Реакционную смесь перемешивали в течение 24 ч при 23 С. Растворитель удаляли под вакуумом, полученный продукт был готов к следующей стадии без дальнейшей очистки. МС (электрораспылительная ионизация): расчетная масса для C18H26N2O2, 302,41; m/z по результатам анализа,303,2 [М+Н]+. 1 Н ЯМР (400 МГц, CDCl3): 7,36-7,20 (м, 5 Н), 3,61-3,46 (м, 4 Н), 3,24 (шир. с, 2 Н), 2,85-2,72(200 мл), НОАс (3 мл) и 10% Pd/C типа Дегусса (400 мг) загружали во флакон для встряхивания Parr и встряхивали 3 дня при давлении газообразного водорода 482,6 кПа (70 psi). Полученный материал фильтровали через Celite и концентрировали. Неочищенную смесь очищали путем колоночной флешхроматографии, ДХМ до 10% МеОН/ДХМ с 1% NH4OH, в результате чего получали желаемый продукт. МС (электрораспылительная ионизация): расчетная масса для C11H20N2O2, 212,29; m/z по результатам анализа, 213,2 [М+Н]+. 1 ЯМР (400 МГц, CDCl3): 3,60-3,55 (м, 2 Н), 3,38-3,25 (м, 4 Н), 2,95-2,86 (м, 4 Н),1,47 (с, 9 Н). Промежуточный продукт 16: (2-фтор-6-[1,2,3]триазол-2-илфенил)-(гексагидропиррол[3,4-с]пиррол 2-ил)метанон Способ А. Стадия А. 5-(2-фтор-6-[1,2,3]триазол-2-ил-бензоил)гексагидропиррол[3,4-с]пиррол-2-карбоновой кислоты трет-бутиловый эфир. В трехгорлую круглодонную колбу объемом 100 мл вносили толуол (8,5 мл), водный карбонат натрия (1,42 г в 10,7 мл воды) и промежуточный продукт 15 (0,905 мг, 4,26 ммоль). Двухфазную смесь охлаждали до 0 С. После охлаждения до 0 С 2-фтор-6-[1,2,3]триазол-2-илбензоилхлорид приливали к двухфазной смеси амина и водного карбоната натрия при перемешивании. Наблюдали экзотермическую реакцию. Смеси давали нагреться до комнатной температуры. Через час образец органического слоя добавляли к метанолу и определяли небольшое оставшееся количество хлорангидрида (в форме метилового эфира). Добавляли дополнительное количество амина (50 мг) и смесь перемешивали в течение ночи при комнатной температуре. В конце этого периода слои разделяли и добавляли к органическому слою 100 мл метанола. Органический слой концентрировали и очищали методом флеш-хроматографии, градиент 5-50% раствора 10% МеОН, 0,1% NH4OH в ДХМ/ДХМ Желаемые фракции комбинировали и концентрировали для получения белого пенистого твердого вещества (1,327 г,76,8%). Масс-спектрометрия (электрораспылительная ионизация): расчетная масса для C20H24FN5O3,401,44, m/z по результатам анализа 346,2 [М+Н-56]+. 1H ЯМР (400 МГц, CDCl3): 7,91-7,73 (м, 3 Н), 7,537,39 (м, 1 Н), 7,18-7,06 (м, 1 Н), 4,00-2,76 (м, 10 Н), 1,52-1,33 (м, 9 Н). Стадия В. (2-Фтор-6-[1,2,3]триазол-2-илфенил)-(гексагидропиррол[3,4-с]пиррол-2-ил)метанон. 5-(2 фтор-6-[1,2,3]триазол-2-ил-бензоил)гексагидропиррол[3,4-с]пиррол-2-карбоновой кислоты трет-бутиловый эфир (1,3 г, 3,21 ммоль) поглощали ДХМ (6,0 мл) и добавляли ТФК (3,0 мл). Смесь перемешивали в течение часа. Растворитель удаляли, затем смесь снова растворяли в ДХМ и подщелачивали 1 Н. водн.NaOH. Слои разделяли. Водный слой экстрагировали еще 2 раза ДХМ (и небольшим количеством МеОН). Органический слой комбинировали, высушивали (Na2SO4), фильтровали и концентрировали для получения желаемого продукта в форме свободного основания, (2-фтор-6-[1,2,3]триазол-2 илфенил)(гексагидропиррол[3,4-с]пиррол-2-ил)метанона, так как вязкий/пенистый осадок оказался очень гигроскопичным (950,6 мг, 93,3%). Масс-спектрометрия (электрораспылительная ионизация): расчетная масса для C15H16FN5O, 301,32, m/z по результатам анализа 302,2 [М+Н]+. 1H ЯМР (400 МГц, CDCl3): 7,907,73 (м, 3 Н), 7,54-7,42 (м, 1 Н), 7,19-7,10 (м, 1 Н), 3,85-2,65 (м, 10 Н). Способ В. Стадия А. 2-Фтор-6-[1,2,3]триазол-2-ил-бензойная кислота (0,97 г, 4,71 ммоль), гексагидропиррол[3,4-с]пиррол-2-карбоновой кислоты трет-бутиловый эфир (промежуточный продукт 15, 1,0 г,4,71 ммоль), HATU (2,68 г, 7,06 ммоль), в ДМФ (18,8 мл) добавляли к ДИЭА (2,43 мл, 14,13 ммоль). Смесь перемешивали в течение часа. Затем смесь разводили EtOAc и промывали водой. Водный слой экстрагировали EtOAc, органические слои комбинировали, высушивали (Na2SO4), фильтровали и концентрировали для получения неочищенного продукта. После очистки методом флеш-хроматографии (550% раствора 10% МеОН, 0,1% NH4OH в ДХМ/EtOAc в течение 25 мин и 50-100% с 25-35 мин) был получен 5-(2-фтор-6-[1,2,3]триазол-2-ил-бензоил)гексагидропиррол[3,4-с]пиррол-2-карбоновой кислоты трет-бутиловый эфир (0,376 г, 19,5%). Стадия В. (2-Фтор-6-[1,2,3]триазол-2-илфенил)-(гексагидропиррол[3,4-с]пиррол-2-ил)метанон. Указанное в заголовке соединение получали аналогично промежуточному продукту 16, метод А, стадия В. Промежуточный продукт 17: бифенил-2-ил-(гексагидропиррол[3,4-с]пиррол-2-ил)метанон Указанное в заголовке соединение получали аналогично промежуточному продукту 16, метод В,используя бифенил-2-карбоновую кислоту вместо 2-фтор-6-[1,2,3]триазол-2-ил-бензойной кислоты на стадии А. Промежуточный продукт 18: [5-(2-фторфенил)-2-метилтиазол-4-ил]-(гексагидропиррол[3,4-с]пиррол-2-ил)метанон Указанное в заголовке соединение получали аналогично промежуточному продукту 16, метод В,используя 5-(2-фторфенил)-2-метилтиазол-4-карбоновую кислоту вместо 2-фтор-6-[1,2,3]триазол-2 илбензойной кислоты на стадии А. Масс-спектрометрия (электрораспылительная ионизация): расчетная масса для C17H18FN3OS, 331,41, m/z по результатам анализа 332,1 [М+1]+. 1H ЯМР (400 МГц, CDCl3): 7,54-7,45 (м, 1 Н), 7,40-7,32 (м, 1 Н), 7,21-7,10 (м, 2 Н), 3,79-3,70 (м, 1 Н), 3,61-3,50 (м, 2 Н), 3,22-3,13 (м,1 Н), 3,12-3,05 (м, 1 Н), 3,03-2,94 (м, 1 Н), 2,85-2,45 (м, 8 Н). Промежуточный продукт 19: (Гексагидропиррол[3,4-с]пиррол-2-ил)-(5-метил-2-[1,2,3]триазол-2 илфенил)метанон Указанное в заголовке соединение получали аналогично промежуточному продукту 16, метод В,используя 5-метил-[1,2,3]триазол-2-ил-бензойную кислоту вместо 2-фтор-6-[1,2,3]триазол-2-илбензойной кислоты на стадии А. Масс-спектрометрия (электрораспылительная ионизация): расчетная масса для C17H19N5O, 297,36, m/z по результатам анализа 298,2 [М+1]+. 1H ЯМР (400 МГц, CDCl3): 7,887,76 (м, 3 Н), 7,36-7,29 (м, 1 Н), 7,22-7,18 (м, 1 Н), 3,81-2,59 (м, 10 Н), 2,42 (с, 3 Н). Промежуточный продукт 20: 2-(гексагидропиррол[3,4-с]пиррол-2-ил)-(2-[1,2,3]триазол-2-илфенил) метанон Указанное в заголовке соединение получали аналогично промежуточному продукту 16, метод В,используя 2-[1,2,3]триазол-2-ил-бензойную кислоту вместо 2-фтор-6-[1,2,3]триазол-2-ил-бензойной кислоты на стадии А. Масс-спектрометрия (электрораспылительная ионизация): расчетная масса дляC15H17N5O, 283,33, m/z по результатам анализа 284,1 [М+1]+. 1H ЯМР (400 МГц, CDCl3): 7,99 (д, J=8,2,1H), 7,55-7,51 (м, 1 Н), 7,48-7,36 (м, 2 Н), 3,99-2,42 (м, 11 Н). Промежуточный продукт 21: (5-фтор-2-[1,2,3]триазол-2-илфенил)-(гексагидропиррол[3,4-с]пиррол 2-ил)метанон Указанное в заголовке соединение получали аналогично промежуточному продукту 16, метод В,используя 5-фтор-2-[1,2,3]триазол-2-ил-бензойную кислоту (промежуточный продукт 97) вместо 2-фтор 6-[1,2,3]триазол-2-ил-бензойной кислоты на стадии А. Масс-спектрометрия (электрораспылительная ионизация): расчетная масса для C15H16FN5O, 301,32, m/z по результатам анализа 302,0 [М+1]+. 1H ЯМР- 27022766 Указанное в заголовке соединение получали аналогично промежуточному продукту 16, метод В,используя 4-фтор-2-[1,2,3]триазол-2-ил-бензойную кислоту вместо 2-фтор-6-[1,2,3]триазол-2-ил-бензойной кислоты на стадии А. Масс-спектрометрия (электрораспылительная ионизация): расчетная масса дляC15H16FN5O, 301,32, m/z по результатам анализа 302,0 [М+1]+. 1H ЯМР (400 МГц, CDCl3): 7,90-7,72 (м,3 Н), 7,43-7,35 (м, 1 Н), 7,17-7,08 (м, 1 Н), 3,81-3,62 (м, 2 Н), 3,39-2,56 (м, 8 Н). Промежуточный продукт 23: 2-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррол Способ А. Стадия А. 5-(4,6-Диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-карбоновой кислоты трет-бутиловый эфир. Гексагидропиррол[3,4-с]пиррол-2-карбоновой кислоты трет-бутиловый эфир (1,20 г, 5,6 ммоль), 2-хлор-4,6-диметилпиримидин (1,03 г, 7,2 ммоль), Cs2CO3 (2,12 г, 6,5 ммоль) и ДМФ (15 мл) смешивали и нагревали до 100 С в течение 24 ч. Затем реакционной смеси давали остыть, а затем добавляли EtOAc и воду. Продукты экстрагировали в EtOAc, высушивали над Na2SO4 и концентрировали. Полученную неочищенную смесь очищали методом флеш-хроматографии на колонке(EA/hex) для получения указанного в заголовке соединения (1,27 г, 71%). МС (электрораспылительная ионизация): расчетная масса для C17H26N4O2, 318,42; m/z по результатам анализа 319,2 [М+Н]+. 1 Н ЯМР(400 МГц, CDCl3): 6,25 (с, 1 Н), 3,85-3,75 (м, 2 Н), 3,69-3,46 (м, 4 Н), 3,38-3,20 (м, 2 Н), 2,94 (шир. с, 2 Н),2,29 (с, 6 Н), 1,44 (с, 9 Н). Стадия В. 2-(4,6-Диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррол. 5-(4,6-диметилпиримидин-2-ил)гексагидропиррол[3,4-с]пиррол-2-карбоновой кислоты трет-бутиловый эфир (0,92 г, 2,9 ммоль),ДХМ (10 мл) и ТФК (5 мл) перемешивали при 23 С в течение 2 ч. Смесь концентрировали для удаления летучих веществ, разводили EtOAc и 1 Н. водн. NaOH, a затем экстрагировали EtOAc (3). Органические фракции высушивали и концентрировали для получения указанного в заголовке соединения (0,61 г,96%), содержащего небольшое количество ДХМ и использующееся непосредственно в таком виде. Расчетная масса при МС (электрораспылительная ионизация) для C12H18N4, 218,30; m/z по результатам анализа, 219,2 [М+Н]+. 1 Н ЯМР (400 МГц, CDCl3): 6,27 (с, 1 Н), 3,81-3,70 (м, 2 Н), 3,55-3,48 (м, 2 Н), 3,16-3,07(м, 2 Н), 2,94-2,78 (м, 4 Н), 2,29 (с, 6 Н). Способ В. Стадия А. 2-Бензил-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррол. В трехлитровую трехгорлую колбу с механической мешалкой, обратным холодильником, датчиком температуры и отверстием для подачи азота вносили 2-бензилоктагидропиррол[3,4-с]пиррол (109 г, 538,8 ммоль) в ДМФ (1,6 л). К полученному раствору добавляли 2-хлор-4,6-метилпиримидин (76,8 г, 538,8 ммоль) и CS2CO3 (351,1 г, 1,08 моль). Неоднородную смесь нагревали до 100 С и перемешивали в течение 15 ч. После охлаждения до комнатной температуры смесь разводили уксусноэтиловым эфиром (1,5 л) и водой (1,5 л). Слои тщательно перемешивали и разделяли. Водный слой дополнительно экстрагировали уксусноэтиловым эфиром (1,5 л). Комбинированный органический слой высушивали над сульфатом натрия, фильтровали и концентрировали под пониженным давлением (160 г, 96% выход). МС (электрораспылительная ионизация): расчетная масса для C19H24N4, 308,20; m/z по результатам анализа 309[М+Н]+. 1H ЯМР (500 МГц, CDCl3): 7,32-7,26 (м, 4 Н), 7,25-7,20 (м, 1 Н), 6,27 (с, 1 Н), 3,81-3,73 (м, 2 Н),3,58 (с, 2 Н), 3,54 (дд, J=ll,4, 3,5 Гц, 2 Н), 2,95-2,86 (м, 2 Н), 2,80-2,68 (м, 2 Н), 2,47-2,40 (м, 2 Н), 2,35-2,24 (с,6 Н). Стадия В. 2-(4,6-Диметилпиримидин-2-ил)октагидропиррол[3,4-с]пирролНОАс. В 4-литровый автоклав, снабженный механической мешалкой, температурным датчиком, нагревательной рубашкой и портом для подачи газа вносили 5% Pd/C (66,9 г, Johnson Matthey 5R338, 56,8% Н 2 О, 3,45 мол.%) и раствор 2-бензил-5-(4,6-диметилпиримидин-2-ил)октагидропиррол[3,4-с]пиррола (160 г, 519 ммоль) и уксусной кислоты (30 мл, 519 ммоль) в этаноле (3,2 л). Смесь перемешивали при 50 С под давлением Н 2(г) 344,7 кПа (50 psi) в течение 4 ч. Катализатор удаляли и полученный раствор концентрировали при пониженном давлении для получения желаемого продукта в форме белого порошка (144 г, количественный выход) в виде соли НОАс. Масс-спектрометрия (электрораспылительная ионизация): расчетная масса для C12H18N4, 218,15; m/z по результатам анализа 219 [М+Н]+. 1H ЯМР (CDCl3, 400 МГц): 6,30 (с, 1 Н),3,79-3,59 (м, 4 Н), 3,39 (м, 2 Н), 3,09-2,88 (м, 4 Н), 2,29 (с, 6 Н), 1,93 (с, 3 Н). Промежуточный продукт 24: [4-(гксагидропиррол[3,4-с]пиррол-2-ил)-6-метоксипиримидин-2-ил] диметиламин Стадия А. Промежуточный продукт 24 получали аналогично промежуточному продукту 23 способ А, используя (4-хлор-6-метоксипиримидин-2-ил)диметиламин вместо 2-хлор-4,6-диметилпиримидина на стадии А для получения 5-(2-диметиламин-6-метоксипиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2- 28022766 карбоновой кислоты трет-бутилового эфира. Стадия В.[4-(Гексагидропиррол[3,4-с]пиррол-2-ил)-6-метоксипиримидин-2-ил]диметиламин. Смесь 5-(2-диметиламин-6-метоксипиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2-карбоновой кислоты трет-бутилового эфира (700 мг) и ТФК (10 мл) перемешивали в диоксане (30 мл) при комнатной температуре в течение 18 ч. После удаления кислоты и растворителей получалась неочищенная соль трифторуксусной кислоты указанного в заголовке соединения (1,3 г). Ее очищали методом флешхроматографии с использованием 0-10% МеОН (2 М NH3) и ДХМ (градиент) для получения чистого указанного в заголовке соединения (155 мг, 30,4%). МС (электрораспылительная ионизация): результаты вычисления массы для C13H21N5O, 263,34; m/z по результатам анализа 264,1 [М+Н]+. Промежуточный продукт использовали без дальнейшей очистки. Промежуточный продукт 25: [6-(Гексагидропиррол[3,4-с]пиррол-2-ил)-2-трифторметилпиримидин 4-ил]диметиламин Стадия А. Указанное в заголовке соединение получали аналогично промежуточному продукту 23,Способ А, заменив (6-хлор-2-трифторметилпиримидин-4-ил)диметиламин на 2-хлор-4,6-диметилпиримидин на стадии А для получения 5-(6-диметиламин-2-трифторметилпиримидин-4 ил)гексагидропиррол[3,4-с]пиррол-2-карбоновой кислоты трет-бутилового эфира. Стадия В. [6-(Гексагидропиррол[3,4-с]пиррол-2-ил)-2-трифторметилпиримидин-4-ил]диметиламин. Смесь 5-(6-диметиламин-2-трифторметилпиримидин-4-ил)гексагидропиррол[3,4-с]пиррол-2-карбоновой кислоты трет-бетилового эфира (600 мг) и ТФК (10,0 мл) перемешивали в диоксане (30,0 мл) при комнатной температуре в течение 18 ч. После удаления кислоты и растворителей получалась неочищенная соль трифторуксусной кислоты указанного в заголовке соединения (800 г, 165%) Неочищенный продукт очищали на колонке для флеш-хроматографии с использованием 0-10% МеОН (2 М NH3) и ДХМ (градиент) для получения чистого указанного в заголовке соединения (250 мг, 53,5%). МС (электрораспылительная ионизация), расчетная масса для С 13 Н 18 F3N5, 301,32; m/z по результатам анализа 302,2 [М+Н]+. Промежуточный продукт использовался непосредственно для последующих реакций. Промежуточный продукт 26: 2-(4-Фенилпиримидин-2-ил)октагидропиррол[3,4-с]пиррол Указанное в заголовке соединение получали аналогично промежуточному продукту 23, способ А,используя 2-хлор-4-фенилпиримидин вместо 2-хлор-4,6-диметилпиримидина на стадии А. МС (электрораспылительная ионизация): расчетная масса для C29H26N4O, 266,35; m/z по результатам анализа, 267,2 Указанное в заголовке соединение получали аналогично промежуточному продукту 23, Способ А,используя 2-хлор-4-метил-пиримидин вместо 2-хлор-4,6-диметилпиримидина на стадии А. МС (электрораспылительная ионизация), расчетная масса для CnH16N4, 204,28; m/z по результатам анализа, 205,2 Указанное в заголовке соединение получали аналогично промежуточному продукту 23, способ А,используя 2-хлорбензооксазол вместо 2-хлор-4,6-диметилпиримидина на стадии А. МС (электрораспылительная ионизация): расчетная масса для C11H16N4, 229,28; m/z по результатам анализа, 230,15 [М+Н]+. 1 Н ЯМР (400 МГц, CDCl3): 7,43-7,33 (м, 1 Н), 7,29-7,22 (м, 1 Н), 7, 120-7, 13 (м, 1 Н), 7,05-6,98 (м, 1 Н), 3,893,77 (м, 2 Н), 3,55 (дд, J=10,9, 3,2 Гц, 2 Н), 3,25-3,15(м, 2 Н), 3,02-2,90 (м, 2 Н), 2,88-2,79 (м, 2 Н). Промежуточный продукт 29: 2-(гексагидропиррол[3,4-с]пиррол-2-ил)-3-метилхиноксалин
МПК / Метки
МПК: A61K 31/407, A61P 25/00, C07D 487/04
Метки: октагидропиррол[3,4-c]пирролы, рецепторов, орексиновых, модуляторов, качестве, двузамещенные
Код ссылки
<a href="https://eas.patents.su/30-22766-dvuzameshhennye-oktagidropirrol34-cpirroly-v-kachestve-modulyatorov-oreksinovyh-receptorov.html" rel="bookmark" title="База патентов Евразийского Союза">Двузамещенные октагидропиррол[3,4-c]пирролы в качестве модуляторов орексиновых рецепторов</a>
Предыдущий патент: Фармацевтическая композиция
Следующий патент: Способ получения катализатора полимеризации олефинов и катализаторы, полученные данным способом
Случайный патент: Расширяемые трубные изделия для использования в геологических структурах, способы расширения трубных изделий и способы их изготовления


































