Соединения в качестве ингибиторов plk, фармацевтические композиции, их содержащие, и их применение
Номер патента: 19487
Опубликовано: 30.04.2014
Авторы: Не Чжэ, Феер Виктория, Итикава Такаси, Кэлдор Стефен У., Макбрайд Кристофер, Лэм Бетти, Джоунз Бенджамин, Цао Шелдон Кс., Лю Янь, Стэффорд Джеффри А., Кирянов Андре А., Натала Сриниваса Редди
Формула / Реферат
1. Соединение формулы
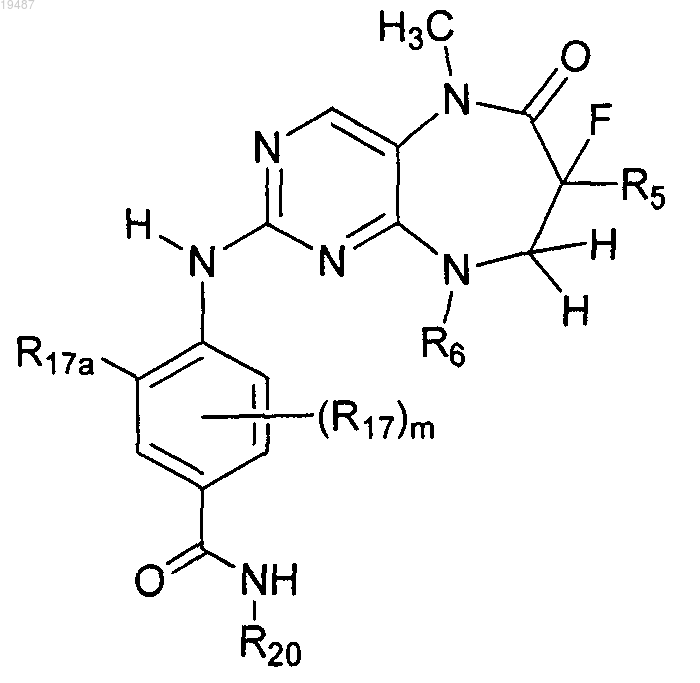
и фармацевтически приемлемые соли указанного соединения, где
R5 выбирают из группы, включающей водород, галоген, (С1-3)алкил и (С2-3)алкенил;
R6 выбирают из группы, включающей (С1-10)алкил и (С3-12)циклоалкил;
m выбирают из группы, включающей 0 и 1; и
R17a независимо выбирают из группы, состоящей из водорода, фтора, хлора, метила, этила, CF3, трифторметокси, метокси и этокси;
R17 независимо выбирают из группы, состоящей из фтора, хлора, метила и метокси;
R20 выбран из группы, состоящей из
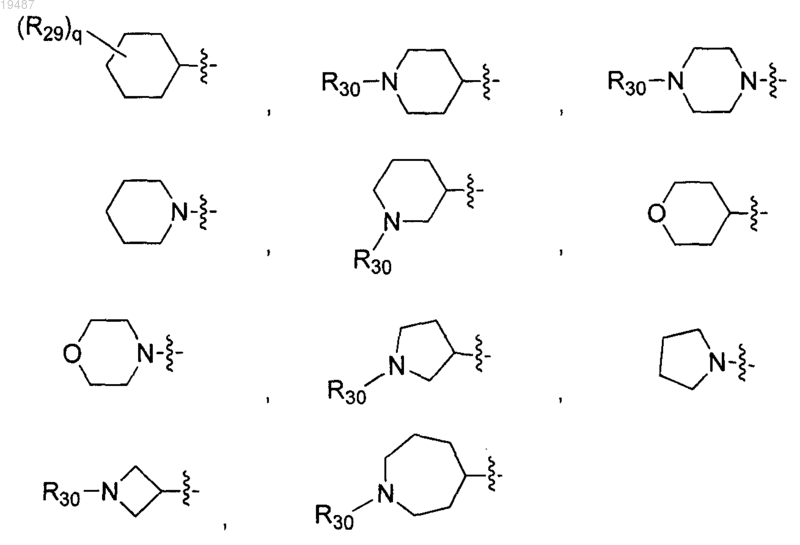
q выбран из группы, состоящей из 0 и 1;
R29 выбирают из группы, состоящей из гидрокси и N,N-диметиламино;
R30 выбирают из группы, состоящей из водорода, метила, этила, 2,2,2-трифторэтила, 2-гидроксиэтила, циклопропилметила, изопропила и циклопентила;
за исключением 4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамида и 4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамида.
2. Соединение по п.1, отличающееся тем, что R5 представляет собой фтор.
3. Соединение по любому из пп.1 или 2, отличающееся тем, что R6 выбирают из группы, состоящей из изопропила, циклопропила, циклопентила и циклогексила.
4. Соединение по любому из пп.1-3, отличающееся тем, что R17a представляет собой метокси.
5. Соединение по любому из пп.1-4, отличающееся тем, что R17 представляет собой фтор.
6. Соединение по п.1, выбранное из группы, включающей
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилазетидин-3-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(2-гидроксиэтил)пиперидин-4-ил)-3-метоксибензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-этилпиперидин-4-ил)-3-метоксибензамид;
(R)-4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиперидин-3-ил)бензамид;
(S)-4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиперидин-3-ил)бензамида;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиперидин-4-ил)бензамид;
N-(азепан-4-ил)-4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилазепан-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-фтор-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-метилпиперидин-4-ил)бензамид;
3-хлор-4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-метилпиперидин-4-ил)-3-(трифторметокси)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метил-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-этил-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-фтор-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-этокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-метилпиперидин-4-ил)-3-(трифторметил)бензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилазетидин-3-ил)бензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-этилпиперидин-4-ил)-3-метоксибензамид;
(S)-4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиперидин-3-ил)бензамид;
(R)-4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиперидин-3-ил)бензамид;
(R)-4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпирролидин-3-ил)бензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((1R,4R)-4-гидроксициклогексил)-3-метоксибензамид;
N-(азепан-4-ил)-4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид;
N-(азетидин-3-ил)-4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(2-гидроксиэтил)пиперидин-4-ил)-3-метоксибензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((цис)-2-гидроксициклогексил)-3-метоксибензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((транс)-2-гидроксициклогексил)-3-метоксибензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(4-(диметиламино)циклогексил)-3-метоксибензамид;
N-(азетидин-3-ил)-4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(тетрагидро-2Н-пиран-4-ил)бензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиперидин-4-ил)бензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(2-(диметиламино)-2-оксоэтил)пиперидин-4-ил)-3-метоксибензамид;
(S)-4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пирролидин-3-ил)бензамид;
(R)-4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-3-ил)бензамид;
(S)-4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-3-ил)бензамид;
(R)-4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пирролидин-3-ил)бензамид;
4-(9-циклопентил-7-фтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7-фтор-5,7-диметил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7-фтор-5,7-диметил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилазетидин-3-ил)бензамид;
4-(9-циклогексил-7-фтор-5,7-диметил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилазетидин-3-ил)бензамид;
(R)-4-(9-циклопентил-7-этил-7-фтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7-этил-7-фтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
(S)-4-(9-циклопентил-7-этил-7-фтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7-этил-7-фтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилазетидин-3-ил)бензамид;
4-(9-циклогексил-7-этил-7-фтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7-фтор-5-метил-6-оксо-7-винил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклогексил-7-этил-7-фтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилазетидин-3-ил)бензамид;
4-(9-циклопентил-7-фтор-5-метил-6-оксо-7-винил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилазетидин-3-ил)бензамид;
4-(9-циклопентил-7-фтор-5-метил-6-оксо-7-винил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-((R)-пиперидин-3-ил)бензамид;
(R)-4-(9-циклопентил-7-фтор-5-метил-6-оксо-7-винил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
(S)-4-(9-циклопентил-7-фтор-5-метил-6-оксо-7-винил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
(R)-4-(9-циклопентил-7-фтор-5-метил-6-оксо-7-винил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-этилпиперидин-4-ил)-3-метоксибензамид;
(R)-4-(9-циклопентил-7-фтор-5-метил-6-оксо-7-винил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(2-гидроксиэтил)пиперидин-4-ил)-3-метоксибензамид;
4-((R)-9-циклопентил-7-фтор-5-метил-6-оксо-7-винил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-((R)-пиперидин-3-ил)бензамид;
(R)-4-(9-циклопентил-7-фтор-5-метил-6-оксо-7-винил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-фтор-5-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(2-(диметиламино)ацетил)пиперидин-4-ил)-2-фтор-5-метоксибензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-фтор-N-(1-(2-гидроксиэтил)пиперидин-4-ил)-5-метоксибензамид;
(R)-4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-фтор-5-метокси-N-(пиперидин-3-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-6-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-фтор-5-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-фтор-3-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-фтор-5-метокси-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-изопропилазетидин-3-ил)-3-метоксибензамид;
4-(9-циклогексил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-этилазетидин-3-ил)-3-метоксибензамид;
N-(азетидин-3-ил)-4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-фтор-5-метоксибензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-этилазетидин-3-ил)-3-метоксибензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-изопропилазетидин-3-ил)-3-метоксибензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-этилазетидин-3-ил)-2-фтор-5-метоксибензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-фтор-N-(1-изопропилазетидин-3-ил)-5-метоксибензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-циклопентилазетидин-3-ил)-2-фтор-5-метоксибензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-метил-N-(1-метилпиперидин-4-ил)бензамид;
4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-метокси-N-(1-метилпиперидин-4-ил)бензамид;
N-(азетидин-3-ил)-4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид;
и фармацевтически приемлемые соли указанных соединений.
7. Соединение по п.1, представляющее собой 4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-фтор-5-метокси-N-(1-метилпиперидин-4-ил)бензамид и фармацевтически приемлемые соли указанного соединения.
8. Фармацевтическая композиция, ингибирующая PLK активность, содержащая соединение по любому из пп.1-7 и фармацевтически приемлемый наполнитель.
9. Применение соединения по любому из пп.1-7 в качестве лекарственного средства для ингибирования PLK активности.
Текст
Предложены соединения, имеющие следующую формулу, для применения совместно с киназами в которой значения радикалов приведены в описании. Также предложены фармацевтические композиции, содержащие указанные соединения, применение указанных соединений в качестве лекарственного средства для ингибирования PLK активности.(71)(73) Заявитель и патентовладелец: ТАКЕДА ФАРМАСЬЮТИКАЛ КОМПАНИ ЛИМИТЕД (JP) Область изобретения Настоящее изобретение относится к соединениям, которые можно применять для ингибирования киназ, а также композициям, содержащим эти соединения. Изобретение также относится к применению данных соединений в качестве лекарственного средства для ингибирования активности поло-подобных киназ (PLK). Уровень техники Изобретение относится к ингибиторам ферментов, которые катализируют фосфорильный перенос и/или которые связывают нуклеотиды ATP/GTP, композициям, содержащим эти ингибиторы, и способам применения ингибиторов и композиций ингибиторов. Многие болезненные состояния характеризуются неконтролируемой пролиферацией и дифференциацией клеток. Эти болезненные состояния охватывают разнообразные клеточные типы и заболевания,такие как рак, атеросклероз, рестеноз и псориаз. Неконтролируемая передача сигнала, обусловленная нарушением регулирования фосфорилирования белка, приводила к ряду заболеваний и болезненных состояний, в том числе, например, воспалению, раку, аллергии/астме, заболеваниям и болезненным состояниям иммунной системы, заболеваниям и болезненным состояниям центральной нервной системы(ЦНС), сердечно-сосудистому заболеванию, дерматологическим заболеваниям и ангиогенезу. Ингибиторы и содержащие их композиции можно применять для лечения или модулирования заболевания, в котором могут участвовать фосфорилтрансферазы, в том числе киназы, при этом симптомы такого заболевания, или воздействие других физиологических процессов, могут быть обусловлены фосфорилтрансферазами, в том числе киназами. В изобретении также предложены способы получения соединений ингибиторов и способы лечения заболеваний, в которых проявляется активность одной или более фосфорилтрансферазы, в том числе киназы. Фосфорилтрансферазы представляют собой большое семейство ферментов, которые переносят фосфорсодержащие группы от одного субстрата к другому. Согласно обозначениям, установленным комитетом по номенклатуре Международного союза по биохимии и молекулярной биологии (IUBMB),ферменты этого типа имеют классификационные номера (ЕС), начинающиеся от 2,7 (см. Bairoch A., TheENZYME database in Nucleic Acids Res. 28:204-305 (2000. Киназы представляют собой класс ферментов,которые действуют при катализе фосфорильного переноса. Протеинкиназы составляют самое большое подсемейство структурно-родственных фосфорилтрансфераз и отвечают за регулирование разнообразных процессов сигнальной трансдукции в клетке (см. Hardie, G. и Hanks, S. (1995). The Protein KinaseFacts Book, I и II, Academic Press, San Diego, CA). Как полагают, протеинкиназы образовались из общего предкового гена благодаря сохранению их структуры и каталитической функции. Почти все киназы содержат сходный каталитический домен 250-300 аминокислот. Протеинкиназы можно классифицировать на семейства в зависимости от субстратов, которые они фосфорилируют (например, протеин-тирозин,протеин-серин/треонин, гистидин и т.д.). Были идентифицированы фрагменты последовательности протеинкиназ, которые, в общем, соответствуют каждому из этих семейств киназ (см., например, Hanks,S.K.; Hunter, Т., FASEB J. 9:576-596 (1995); Kinghton et al., Science, 253:407-414 (1991); Hiles et al., Cell 70:419-429 (1992); Kunz et al., Cell, 73:585-596 (1993); Garcia-Bustos et al., EMBO J., 13:2352-2361 (1994. Липидные киназы (например, PI3K) составляют отдельную группу киназ, имеющих структурное сходство с протеинкиназами. Протеинкиназы и липидные киназы регулируют многие различные клеточные процессы, в том числе, помимо прочего, пролиферацию, рост, дифференциацию, метаболизм, процессы клеточного цикла,апоптоз, подвижность, транскрипцию, трансляцию и другие сигнальные процессы, путем добавления фосфатных групп к мишеням, таким как белки или липиды. Процессы фосфорилирования, катализируемые киназами, действуют в качестве молекулярных включателей/выключателей, которые могут модулировать или регулировать биологическое функционирование белка-мишени. Фосфорилирование белковмишеней происходит в ответ на разнообразные внеклеточные сигналы (гормоны, нейромедиаторы, факторы роста и дифференциации и т.д.), процессы клеточного цикла, стрессы, связанные с окружающей средой или питанием и т.д. Протеинкиназы и липидные киназы могут функционировать в сигнальных путях, активируя или инактивируя, или модулируя активность (прямо или косвенно) мишеней. Эти мишени могут включать, например, метаболические ферменты, регуляторные белки, рецепторы, белки цитоскелета, ионные каналы или насосы или транскрипционные факторы. Первоначальный интерес к протеинкиназам как фармакологическим мишеням был вызван полученными данными, что многие вирусные онкогены кодируют структурно модифицированные клеточные протеинкиназы посредством конститутивной ферментной активности. Эти данные указывали на потенциальное участие протеинкиназ, связанных с онкогенами, в пролиферативных заболеваниях человека. Впоследствии дерегулирующая активность протеинкиназ, возникающая в результате различных более тонких механизмов, участвовала в патофизиологии целого ряда важных заболеваний человека, в том числе, например, рака, состояний ЦНС и иммуногенных родственных заболеваний. Поэтому разработка селективных ингибиторов протеинкиназ,которые могут блокировать патологию и/или симптомы заболеваний, возникающие в результате нарушения активности протеинкиназы, вызвала большой интерес. Рак возникает в результате разрегулирования нормальных процессов, которые контролируют кле-1 019487 точное деление, дифференциацию и апоптический некроз клеток. Протеинкиназы играют решающую роль в этом регуляторном процессе. Неполный неограничивающий перечень таких киназ включает ab1,Aurora-A, Aurora-B, Aurora-C, Akt, bcr-abl, Blk, Brk, Btk, c-Kit, c-Met, c-Src, CDK1, CDK2, CDK4, CDK6,cRaf1, CSF1R, CSK, EGFR, ErbB2, ErbB4, ERK, Fak, fes, FGFR1, FGFR2, FGFR3, FGFR4, FGFR5, Fgr, Flt4, Flt-1, FER, Frk, Fyn, Hck, IGF-1R, INS-R, Jak, KDR, Lck, Lyn, MEK, p38, PDGFR, PIK, PKC, PLK,PYK2, Ros, Tie1, Tie2, Trk, Yes и Zap70. В биологии млекопитающих такие протеинкиназы включают сигнальные пути митоген-активируемой протеинкиназы (MAPK). Сигнальные пути MAPK несоответственно активируются посредством различных общих механизмов, связанных с заболеваниями, таких как мутация ras генов и разрегулирования рецепторов фактора роста (Magnuson et al., Seminars in Pak Biology 5:247-252 (1994. Соответственно, ингибирование протеинкиназ является целью настоящего изобретения. Поло-подобные киназы (PLK, в том числе PLK1, PLK2, PLK3 и PLK4) представляют собой сериновые/треониновые протеинкиназы, которые участвовали в развитии рака у человека, такого как опухоли толстой кишки, груди и другие солидные опухоли. Как полагают, поло-подобные киназы (также называемые PLK) участвуют в процессах фосфорилирования белков, которые регулируют клеточный цикл. В частности, PLK1 может играть важную роль в регулировании точного расщепления хромосом во время митоза. Неправильное регулирование клеточного цикла может привести к клеточной пролиферации и другим нарушениям. Как было обнаружено, в раковой ткани толстой кишки человека PLK находятся в состоянии повышенной экспрессии (см. Barr et al. в Nat. Rev. Mol. Cell Biol. 5: 429 (2004); van Vugt et al. вOcogene, 24: 2844 (2005. PLK1 недавно была описана в качестве перспективной молекулы-кандидата для прицельной опухолевой терапии (см. Takai et al. в Oncogene, 24:287 (2005); McInnes et al. в CurrentTopics in Med. Chem., 5:181 (2005. Существует постоянная потребность в обнаружении новых терапевтических средств для лечения заболеваний человека. Протеинкиназы, в частности, помимо прочего, поло-подобная киназа (PLK), представляют собой особенно перспективные цели для открытия новых терапевтических препаратов благодаря их важной роли в гиперпролиферативных заболеваниях; раке (например, солидных опухолях, лейкемиях, лимфомах, немелкоклеточном раке легкого и раке пищевода); воспалительных и аутоиммунных заболеваниях (например, псориазе, алопеции; рассеянном склерозе; колите, артрите, болезни Альцгеймера, гломерулонефрите и заживлении ран); алопеции и воспалении слизистой оболочки, вызванных химиотерапевтическими препаратами; сердечно-сосудистых заболеваниях (например, стенозах, артериосклерозах, рестенозах и гипертрофии); вирусных, бактериальных, грибковых и/или паразитических инфекционных заболеваниях (например, цитомегалических инфекциях, герпесе, гепатитах В и С, саркоме Капоши, ВИЧ заболеваниях); нефрологических заболеваниях (например, гломерулонефрите); хронических и острых нейродегенеративных заболеваниях (например, болезни Гентингтона, боковом амиотрофическом склерозе, болезни Паркинсона, СПИДе, слабоумии, болезни Альцгеймера, ишемии мозга и травмах нерва); кожных заболеваниях (например, псориазе); заболеваниях костей; защите пролиферирующих клеток (например, клеток волос, кишечника, крови и клеток-предшественников) от повреждения ДНК, вызванного радиацией, УФ-лечением и/или цитостатическим лечением; и других заболеваниях. Некоторые ингибиторы PLK описаны в WO 2007/095188. В настоящем изобретении предложены ингибиторы PLK, в том числе ингибиторы, имеющие пониженную чувствительность к множественной лекарственной устойчивости. Краткое описание изобретения Настоящее изобретение относится к соединениям, которые проявляют активность в ингибировании киназ. В настоящем изобретении также предложены композиции, содержащие эти соединения. Согласно одному варианту реализации предложена фармацевтическая композиция, которая в качестве активного ингредиента содержит ингибитор киназы согласно настоящему изобретению. Фармацевтические композиции согласно изобретению могут содержать 0,001-100% одного или более ингибиторов согласно этому изобретению. Эти фармацевтические композиции можно принимать совместно или по отдельности разнообразными способами, в том числе, например, перорально, парентерально, внутрибрюшинно, внутривенно, внутриартериально, трансдермально, подъязычно, внутримышечно, ректально,трансбуккально, интраназально, через липосомы, посредством ингаляции, вагинально, посредством внутриглазного введения, локально (например, с помощью катетера или стента), подкожным путем, через жировую ткань, внутрисуставным или интратекальным путями. Композиции также можно принимать совместно или по отдельности в дозируемых лекарственных формах с медленным высвобождением. Также предложены способы применения соединений согласно настоящему изобретению. Согласно одному варианту реализации изобретения соединения и композиции применяют для ингибирования киназ. В частности, соединения и композиции можно применять для ингибирования PLK. Согласно еще одному варианту реализации изобретения соединения и композиции применяют для лечения болезненного состояния, при котором киназы обладают активностью, которая содействует патологии и/или симптоматологии болезненного состояния. Согласно еще одному варианту реализации изобретения соединения вводят субъекту, при этом активность киназы в организме субъекта изменяется, предпочтительно уменьшается.-2 019487 Согласно еще одному варианту реализации изобретения предложен способ применения соединения согласно настоящему изобретению в качестве лекарства для применения при лечении болезненного состояния, о котором известно, что оно обусловлено киназами, или о котором известно, что оно лечится ингибиторами киназы. Следует отметить в отношении всех вышеописанных вариантов реализации изобретения, что настоящее изобретение охватывает все фармацевтически приемлемые соли соединения, как хорошо известно в настоящей области, для введения фармацевтических веществ в ионизированной форме. Также следует отметить, что, если не указана конкретная стереохимия, перечисленные соединения включают все возможные стереоизомеры (например, энантиомеры или диастереомеры, в зависимости от количества хиральных центров, и геометрические изомеры), независимо от того, присутствует ли соединение в виде индивидуального стереоизомера или смеси стереоизомеров. Кроме того, если не указано иначе, перечисленные соединения включают все возможные резонансные формы и таутомеры. Что касается формулы изобретения, формулировка "соединение, включающее формулу", "соединение, имеющее формулу" и "соединение формулы" охватывает это соединение и все фармацевтически приемлемые ионизированные формы, все возможные стереоизомеры и все возможные резонансные формы и таутомеры, если в конкретном параграфе формулы изобретения специально не указано иное. Краткое описание чертежей На фиг. 1 А-1 С показаны последовательности SEQ ID No. 1-6, рассматриваемые в этом изобретении. Определения Если не указано иначе, для целей настоящего патента нижеприведенные термины, применяемые при описании изобретения и формулы изобретения, имеют следующие значения. Следует отметить, что применяемые при описании изобретения и прилагаемой формулы формы единственного числа включают объекты во множественном числе, если содержание четко не указывает на другое. Кроме того, определения стандартных химических терминов можно найти в справочниках, в том числе Carey и Sundberg "Advanced Organic Chemistry 4th Ed.", vol. A (2000) и В (2001), Plenum Press,New York. Также, если не указано иное, применяют обычные способы масс-спектроскопии, ЯМР, ВЭЖХ,белковой химии, биохимии, методы рекомбинантной ДНК и фармакологии, в пределах компетентности в данной области. Термин "алкил", сам по себе, означает прямой или разветвленный, насыщенный или ненасыщенный алифатический радикал, содержащий цепь из углеродных атомов. Согласно конкретному варианту реализации изобретения "алкил", один или вместе с другим радикалом, может представлять собой(С 1-20)алкил, (С 1-15)алкил, (С 1-10)алкил, (С 1-5)алкил, (С 1-4)алкил или (С 1-3)алкил. Альтернативным образом,"алкил", один или вместе с другим радикалом, может представлять собой (С 1)алкил, (С 2)алкил или(С 3)алкил. Термин "амино" означает азотсодержащую группировку, содержащую два дополнительных заместителя, в которых, например, атом водорода или углерода присоединен к азоту. Например, типичной аминогруппой является -NHCH3. Термин "животное" включает людей, млекопитающих, не относящихся к человеку (например, собак, кошек, кроликов, крупный рогатый скот, лошадей, овец, коз, свиней,оленей и т.п.) и не млекопитающих (например, птиц и т.п.). Термин "циклоалкил" означает не ароматический, насыщенный или частично ненасыщенный, моноциклический, бициклический или полициклический ансамбль колец. Как правило, применяют обозначения (Сх)циклоалкил и (Сх-y)циклоалкил, где X и Y указывают количество углеродных атомов в ансамбле колец. Например, (С 3-10)циклоалкил включает циклопропил, циклобутил, циклопентил, циклогексил. Согласно отдельному варианту реализации изобретения "циклоалкил", один или вместе с другим радикалом, может представлять собой (С 3-14)циклоалкил, (С 3-10)циклоалкил, (С 3-7)циклоалкил, (С 8-10)циклоалкил или (С 5-7)циклоалкил. Альтернативным образом, "циклоалкил", один или вместе с другим радикалом,может представлять собой (С 5)циклоалкил, (С 6)циклоалкил, (С 7)циклоалкил, (С 8)циклоалкил,(С 9)циклоалкил или (С 10)циклоалкил. Термины "заболевание", "болезнь" и "состояние", в частности,включают любое болезненное состояние животного или органа животного и включают болезненное состояние, которое может быть вызвано медицинской или ветеринарной терапией, применяемой для лечения этого животного, или свойственна этой терапии, т.е. представляют собой "побочные эффекты" такой терапии. Термин "гало" означает фтор, хлор, бром или йод. Термин "гидрокси" означает радикал -ОН."IC50" означает молярную концентрацию ингибитора, которая вызывает 50% ингибирование фермента-мишени. Термин "фармацевтически приемлемый" означает, что соединение можно применять для получения фармацевтической композиции, которая в общем является безопасной, нетоксичной и биологически или иным образом приемлемой в применяемых количествах, и включает соединение, которое является подходящим для ветеринарного использования, также фармацевтического применения при лечении людей. Термин "фармацевтически приемлемые соли" означает соли соединений согласно настоящему изобретению, которые являются фармацевтически приемлемыми. Такие соли включают соли присоединения кислоты, образованные с неорганическими кислотами, такими как соляная, бромисто-водородная, сер-3 019487 ная, азотная, фосфорная кислоты и т.п.; или с органическими кислотами, такими как уксусная, пропионовая, капроевая, гептановая, циклопентанпропионовая, гликолевая, пировиноградная, молочная, малоновая, янтарная, яблочная, малеиновая, фумаровая, винно-каменная, лимонная, бензойная, о-(4 гидроксибензоил)бензойная, коричная, миндальная, метансульфоновая, этансульфоновая, 1,2 этандисульфоновая, 2-гидроксиэтансульфоновая, бензолсульфоновая, п-хлорбензолсульфоновая, 2 нафталинсульфоновая, п-толуолсульфоновая, камфорасульфоновая, 4-метилбицикло[2.2.2]окт-2-ен-1 карбоновая, глюкогептоновая, 4,4'-метиленбис-3-гидрокси-2-ен-1-карбоновая, 3-фенилпропионовая,триметилуксусная, третичная бутилуксусная, лаурил серная, глюконовая, глутаминовая, гидроксинафтойная, салициловая, стеариновая, муконовая кислоты и т.п. Фармацевтически приемлемые соли также включают соли присоединения основания, которые можно получить, если присутствующие протоны кислоты способны реагировать с неорганическими или органическими основаниями. Приемлемые неорганические основания включают гидроксид натрия, карбонат натрия, гидроксид калия, гидроксид алюминия и гидроксид кальция. Приемлемые органические основания включают этаноламин, диэтаноламин, триэтаноламин, трометамин, N-метилглюкамин и т.п. Термины "субъект" и "пациент" включают людей, млекопитающих, не относящихся к человеку (например, собак, кошек, кроликов, крупный рогатый скот, лошадей, овец, коз, свиней, оленей и т.п.) и не млекопитающих (например, птиц и т.п.). Конкретный субъект или пациент представляет собой человека. В отношении всех определений, представленных в настоящем документе, следует отметить, что эти определения не являются окончательными в том смысле, что, помимо уже определенных заместителей,возможно включение и других заместителей. Поэтому (С 1)алкил указывает, что имеется один атом углерода, но не указывает, какие заместители содержит атом углерода. Поэтому (С 1)алкил включает метил(т.е. -СН 3), а также -CRR'R", где каждый R, R' и R" независимо представляет собой водород или дополнительный заместитель, в котором атом, присоединенный к углероду, представляет собой гетероатом или циано. Поэтому, например, все CF3, СН 2 ОН и CH2CN представляют собой (С 1)алкилы. Аналогичным образом, такие термины, как алкиламино и т.п., включают диалкиламино и т.п. Подробное описание изобретения Настоящее изобретение относится к соединениям, которые могут быть использованы для ингибирования киназ и, в частности, для ингибирования Polo-подобных киназ (Polo-like kinases, называемых в настоящем описании PLK). Настоящее изобретение также относится к фармацевтическим композициям,включающим такие соединения. Кроме того, настоящее изобретение относится к способам применения указанных соединений. Следует отметить, что соединения согласно настоящему изобретению также могут проявлять активность по отношению к другим членам того же семейства белков и, таким образом,могут быть использованы в лечении заболеваний, связанных с этими другими членами того же семейства белков. Нарушение регулирования PLK приводит к развитию таких нарушений, как гиперпролиферативные нарушения; раковые заболевания (например, солидные опухоли, лейкемии, лимфомы, различные виды немелкоклеточного рака легких и карцином пищевода); воспалительные и аутоиммунные заболевания(например, псориаз, алопеция (облысение; рассеянный склероз; колит, артрит, болезнь Альцгеймера,гломерулонефрит и нарушение заживления ран); вызванная химиотерапевтическим воздействием алопеция и мукозит (воспаление слизистой оболочки); сердечно-сосудистые заболевания (например, стенозы,артериосклерозы, рестенозы и гипертрофия); вирусные, бактериальные, грибковые и/или паразитарные инфекционные заболевания (например, цитомегалические инфекции, герпес, гепатит В и С, саркома Капоши, ВИЧ-заболевания); нефрологические заболевания (например, гломерулонефрит); хронические и острые нейродегенеративные заболевания (например, болезнь Гентингтона, боковой амиотрофический склероз, болезнь Паркинсона, слабоумие, вызванное СПИД, болезнь Альцгеймера, ишемии мозга и травмы нервной системы); заболевания кожных покровов (например, псориаз); заболевания костной ткани; регулирование PLK также важно для защиты пролиферирующих клеток (например, волос, кишечника,крови и клеток-предшественников) от повреждения ДНК, вызываемого лучевой терапией, УФ-терапией и/или цитостатической терапией. Следует отметить, что соединения согласно настоящему изобретению также могут проявлять ингибирующую активность по отношению к другим членам того же семейства белковых кеназ и, таким образом, могут быть использованы в лечении заболеваний, связанных с этими другими членами того же семейства белков. Ингибиторы polo-подобных киназ В одном варианте реализации ингибиторы PLK, предлагаемые согласно настоящему изобретению,включают и фармацевтически приемлемые соли указанного соединения, гдеR17a независимо выбирают из группы, состоящей из водорода, фтора, хлора, метила, этила, CF3,трифторметокси, метокси и этокси;R17 независимо выбирают из группы, состоящей из фтора, хлора, метила и метокси;R29 выбирают из группы, состоящей из гидрокси и N,N-диметиламино;R30 выбирают из группы, состоящей из водорода, метила, этила, 2,2,2-трифторэтила, 2 гидроксиэтила, циклопропилметила, изопропила и циклопентила; за исключением 4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5 Н-пиримидо[4,5b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамида и 4-(9-циклогексил-7,7 дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5 Н-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1 метилпиперидин-4-ил)бензамида. В одном варианте реализации изобретения предлагаются соединения указанной выше структурной формулы, где R5 представляет собой фтор. В другом варианте соединение R6 выбирают из группы, состоящей из изопропила, циклопропила,циклопентила и циклогексила. Кроме того, в частном случае в соединении по изобретению по меньшей мере один из R17a представляет собой метокси. В другом частном случае по меньшей мере один из R17 представляет собой фтор. Конкретные неограничивающие примеры соединений, предлагаемых согласно настоящему изобретению, включают 4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5 Н-пиримидо[4,5-b][1,4]диазепин 2-иламино)-3-метокси-N-(1-метилазетидин-3-ил)бензамид; 4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5 Н-пиримидо[4,5-b][1,4]диазепин 2-иламино)-N-(1-(2-гидроксиэтил)пиперидин-4-ил)-3-метоксибензамид; 4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5 Н-пиримидо[4,5-b][1,4]диазепин 2-иламино)-N-(1-этилпиперидин-4-ил)-3-метоксибензамид;N-(азетидин-3-ил)-4-(9-циклопентил-7,7-дифтор-5-метил-6-оксо-6,7,8,9-тетрагидро-5 Нпиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид; и фармацевтически приемлемые соли указанных соединений. Соединения настоящего изобретения получают согласно следующим этапам: обработка соединения, соответствующего формуле в условиях, в которых происходит образование первого продукта реакции, соответствующего формуле обработка первого продукта реакции в условиях, в которых происходит образование второго продукта реакции, соответствующего формуле обработка второго продукта реакции в условиях, в которых происходит образование третьего продукта реакции, соответствующего формуле реакция третьего продукта реакции с соединением, соответствующим формуле в условиях, в которых происходит образование четвертого продукта реакции, соответствующего формуле обработка четвертого продукта реакции в условиях, в которых происходит образование пятого продукта реакции, соответствующего формуле обработка пятого продукта реакции в условиях, в которых происходит образование шестого продукта реакции, соответствующего формуле обработка шестого продукта реакции в условиях, в которых происходит образование седьмого про-8 019487 дукта реакции, соответствующего формуле реакция седьмого продукта реакции с соединением, соответствующим формуле в условиях, в которых происходит образование восьмого продукта реакции, соответствующего формуле обработка восьмого продукта реакции в условиях, в которых происходит образование девятого продукта реакции, соответствующего формуле реакция девятого продукта реакции с соединением, соответствующим формуле в условиях, в которых происходит образование десятого продукта реакции, соответствующего формуле реакция десятого продукта реакции с соединением, соответствующим формуле в условиях, в которых происходит образование одиннадцатого продукта реакции, соответствующего формуле реакция одиннадцатого продукта реакции с соединением, соответствующим формуле в условиях, в которых происходит образование двенадцатого продукта реакции, соответствующего формулеm выбирают из группы, включающей 2 или 3; каждый R17 независимо выбирают из группы, включающей фтор, хлор, метил и метокси;R17a выбирают из группы, включающей водород, фтор, хлор, метил, этил, CF3, трифторметокси, метокси и этокси; каждый из R19 и R20 независимо выбирают из группы, включающей водород;R29 выбирают из группы, состоящей из гидрокси и N,N-диметиламино;Z5 представляет собой уходящую группу. В еще одном варианте каждого из вышеуказанных примеров реализации и вариантов реализации Z1 представляет собой атом галогена. В еще одном варианте каждого из вышеуказанных примеров реализации и вариантов реализации Z2 представляет собой атом галогена. В другом варианте каждого из вышеуказанных примеров реализации и вариантов реализации Z3 представляет собой атом галогена. И в другом варианте каждого из вышеуказанных примеров реализации и вариантов реализации Z4 представляет собой атом галогена. В другом варианте каждого из вышеуказанных примеров реализации и вариантов реализации Z5 представляет собой атом галогена. Следует отметить, что соединения, предлагаемые согласно настоящему изобретению, могут находиться в виде фармацевтически приемлемой соли. Настоящее изобретение также относится к применению в качестве медикамента соединения, включаемого в любой из указанных выше примеров и вариантов реализации. Соединения настоящего изобретения могут быть использованы для лечения гиперпролиферативных нарушений; раковых заболеваний; воспалительных заболеваний; аутоиммунных заболеваний; вызванной химиотерапевтическим воздействием алопеции и мукозита; сердечно-сосудистых заболеваний; вирусных, бактериальных, грибковых и/или паразитарных инфекционных заболеваний; нефрологических заболеваний; хронических и острых нейродегенеративных заболеваний; заболеваний кожных покровов;- 10019487 заболеваний костной ткани и защиты пролиферирующих клеток. Настоящее изобретение также относится к фармацевтической композиции, включающей в качестве активного ингредиента соединение, включаемое в любой из указанных выше примеров и вариантов реализации. В одном из конкретных вариантов композиция представляет собой твердый препарат, пригодный для перорального введения. В другом конкретном варианте композиция представляет собой жидкий препарат, пригодный для перорального введения. В другом конкретном варианте композиция представляет собой таблетку. В еще одном из конкретных вариантов композиция представляет собой жидкий препарат, пригодный для парентерального введения. Другой аспект изобретения относится к фармацевтической композиции, включающей соединение,включаемое в любой из указанных выше примеров и вариантов осуществления, при этом указанная композиция пригодна для введения способом, выбираемым из группы, состоящей из перорального, парентерального, интраперитонеального (внутрибрюшного), внутривенного, внутриартериального, трансдермального, сублингвального (подъязычного), внутримышечного, перректального, трансбуккального, интраназального введения, введения при помощи липосом, введения посредством ингаляции, способа первагинального введения, интраокулярного введения, местного введения (например, при помощи катетера или стента), способа подкожного введения, введения внутрь жировой ткани, способа внутрисуставного введения и интратекального (подоболочечного) введения. Другой аспект изобретения относится к набору, включающему соединение, включаемое в любой из указанных выше примеров и вариантов реализации; и инструкции, которые включают один или несколько информационных листов, выбираемых из группы, состоящей из описания заболевания, для лечения которого вводят композицию, информации по хранению композиции, информации по дозированию и инструкции, касающейся способа введения композиции. В одном из конкретных вариантов набор включает соединение в виде многократной дозировки лекарственной формы. Соли ингибиторов киназы. Следует иметь в виду, что соединения согласно настоящему изобретению могут присутствовать и быть введены в форме солей. Например, в объем притязаний настоящего изобретения входит превращение соединений согласно настоящему изобретению в их фармацевтически приемлемые соли, образующиеся из различных органических и неорганических кислот и оснований и применение этих соединений в форме их солей в соответствии с методиками, хорошо известными в данной области. Если соединения согласно настоящему изобретению имеют форму свободного основания, эти соединения можно получить в виде фармацевтически приемлемой соли присоединения кислоты с помощь реакции этого соединения в форме свободного основания с фармацевтически приемлемой неорганической или органической кислотой, например в виде гидрогалогенидов, таких как гидрохлорид, гидробромид, гидроиодид; других минеральных кислот и их соответствующих солей, таких как сульфат, нитрат, фосфат и т.д.; и алкила и моноарилсульфонатов, таких как этансульфонат, толуолсульфонат и бензолсульфонат; и других органических кислот и их соответствующих солей, таких как ацетат, тартрат, малеат, сукцинат, цитрат, бензоат,салицилат и аскорбат. Другие соли присоединения кислоты согласно настоящему изобретению включают, помимо прочего, адипат, альгинат, аргинат, аспартат, бисульфат, бисульфит, бромид, бутират, камфорат, камфорасульфонат, каприлат, хлорид, хлорбензоат, циклопентанпропионат, диглюконат, дигидрогенфосфат, динитробензоат, додецилсульфат, фумарат, галактерат (из муциновой кислоты), галактуронат, глюкогептонат, глюконат, глютамат, глицерофосфат, хемисукцинат, хемисульфат, гептаноат, гексаноат, гиппурат, гидрохлорид, гидробромид, гидроиодид, 2-гидроксиэтансульфонат, иодид, изетионат,изо-бутират, лактат, лактобионат, малат, малонат, манделат, метафосфат, метансульфонат, метилбензоат,моноводородфосфат, 2-нафталинсульфонат, никотинат, нитрат, оксалат, олеат, памоат, пектинат, персульфат, фенилацетат, 3-фенилпропионат, фосфат, фосфонат и фталат. Следует иметь в виду, что формы свободного основания будут, как правило, несколько отличаться от их соответствующих солевых форм по физическим свойствам, таким как растворимость в полярных растворителях, но в других отношениях,для целей настоящего изобретения эти соли эквиваленты их соответствующим формам свободного основания. Если соединения согласно настоящему изобретению имеют форму свободной кислоты, фармацевтически приемлемую соль присоединения основания можно получить с помощью реакции соединения в форме свободной кислоты с фармацевтически приемлемым неорганическим или органическим основанием. Примерами таких оснований являются гидроксиды щелочных металлов, в том числе гидроксиды калия, натрия и лития; гидроксиды щелочно-земельных металлов, такие как гидроксиды бария и кальция; алкоксиды щелочных металлов, например этанолат калия и пропанолат натрия; и различные органические основания, такие как гидроксид аммония, пиперидин, диэтаноламин и N-метилглютамин. В изобретение также включены алюминиевые соли соединений согласно настоящему изобретению. Дополнительные соли основания согласно настоящему изобретению включают, помимо прочего, соли меди,трехвалентного железа, двухвалентного железа, лития, магния, марганца, двухвалентного марганца, калия, натрия и цинка. Соли органических оснований включают, помимо прочего, соли первичных, вторичных и третичных аминов, замещенные амины, в том числе природные замещенные амины, циклические амины и основные ионообменные смолы, например аргинин, бетаин, кофеин, хлорпрокаин, холин,- 11019487N,N'-дибензилэтилендиамин (бензатин), дициклогексиламин, диэтаноламин, 2-диэтиламиноэтанол, 2 диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изо-пропиламин, лидокаин, лизин, меглумин, N-метил-D-глюкамин,морфолин, пиперазин, пиперидин, полиаминовые смолы, прокаин, пурины, теобромин, триэтаноламин,триэтиламин, триметиламин, трипропиламин и трис-(гидроксиметил)метиламин (трометамин). Следует иметь в виду, что формы свободной кислоты будут, как правило, несколько отличаться от их соответствующих солевых форм по физическим свойствам, таким как растворимость в полярных растворителях,но в других отношениях для целей настоящего изобретения эти соли эквиваленты их соответствующим формам свободной кислоты. Можно также получить защищенные производные соединений согласно настоящему изобретению. Примеры способов, применимых для получения и удаления защитных групп, можно найти в T.W.Greene, Protecting Groups in Organic Synthesis, 3rd edition, John WileySons, Inc. 1999. Композиции, содержащие ингибиторы киназы. В сочетании с соединениями согласно настоящему изобретению можно применять разнообразные композиции и способы введения. Такие композиции могут включать, помимо соединений согласно настоящему изобретению, обычные фармацевтические наполнители и другие обычные фармацевтически неактивные вещества. Кроме того, в добавление к соединениям согласно настоящему изобретению композиции могут включать активные вещества. Эти дополнительные активные вещества могут включать дополнительные соединения согласно изобретению и/или одно или более других фармацевтически активных веществ. Композиции могут находиться в газообразной, жидкой, полужидкой или твердой форме, приготовленной способом, подходящим для пути введения, который предполагают применить. Для перорального введения, как правило, применяют капсулы и таблетки. Для парентерального введения обычно применяют восстановление влагосодержания лиофилизированного порошка, полученного согласно настоящему описанию. Композиции, содержащие соединения согласно настоящему изобретению, могут быть введены вместе или по отдельности перорально, парентерально, внутрибрюшинно, внутривенно, внутриартериально,трансдермально, сублингвально, внутримышечно, ректально, трансбуккально, интраназально, через липосомы, с помощью ингаляции, вагинальным, внутриглазным путями, локально (например, с помощью катетера или стента), подкожно, через жировую ткань, внутрисуставным или интратекальным путями. Соединения и/или композиции согласно изобретению также могут быть введены совместно или по отдельности в лекарственных формах с медленным высвобождением. Ингибиторы киназы и содержащие их композиции могут быть введены совместно или по отдельности в любой обычной лекарственной форме. Совместное введение в контексте этого изобретения означает введение более чем одного терапевтического препарата, один из которых включает ингибитор киназы,в ходе координированного лечения с целью достижения улучшения клинического результата. Такое совместное введение также может иметь одинаковую протяженность по времени, т.е. происходить в течение частично совпадающих периодов времени. Растворы или суспензии, применяемые для парентерального, интрадермального, подкожного или топического введения, могут включать один или более из следующих компонентов: стерильный разбавитель, такой как вода для инъекции, солевой раствор, нелетучее масло, полиэтиленгликоль, глицерин,пропиленгликоль или другой синтетический растворитель; противомикробные средства, такие как бензиловый спирт и метилпарабены; антиоксиданты, такие как аскорбиновая кислота и бисульфит натрия; хелатирующие агенты, такие как этилендиаминтетрауксусная кислота (EDTA); буферные вещества, такие как ацетаты, цитраты и фосфаты; вещества для регулирования тоничности, такие как хлорид натрия или декстроза, и вещества для регулирования кислотности или щлочности композиции, такие как щелочные реагенты или реагенты, повышающие кислотность, или буферные вещества, такие как карбонаты, бикарбонаты, фосфаты, соляная кислота, и органические кислоты, такие как уксусная и лимонная кислоты. Парентеральные препараты могут быть заключены в ампулы, одноразовые шприцы или флаконы с однократной или многократными дозами, сделанные из стекла, пластмассы или другого подходящего материала. Если соединения согласно настоящему изобретению проявляют недостаточную растворимость,можно применять способы солюбилизирования соединений. Такие способы известны специалистам в данной области и включают, помимо прочего, применение сорастворителей, таких как диметилсульфоксид (ДМСО), применение поверхностно-активных веществ, таких как твин (tween), или растворение в водном бикарбонате натрия. Производные соединений, такие как пролекарства соединений, также можно применять при приготовлении эффективных фармацевтических композиций. После смешивания или добавления соединений согласно настоящему изобретению к композиции,можно получить раствор, суспензию, эмульсию или т.п. Форма образовавшейся композиции будет зависеть от ряда факторов, в том числе предполагаемого способа введения и растворимости соединения в выбранном носителе или среде. Эффективную концентрацию, необходимую для облегчения заболевания,подвергаемого лечению, можно определить эмпирически.- 12019487 Композиции согласно настоящему изобретению можно использовать для введения людям и животным в стандартных лекарственных формах, таких как таблетки, капсулы, пилюли, порошки, сухие порошки для ингаляторов, гранулы, стерильные парентеральные растворы или суспензии и пероральные растворы или суспензии, и эмульсии масло-вода, содержащие подходящие количества соединений, в частности их фармацевтически приемлемых солей, предпочтительно солей натрия. Фармацевтически терапевтически активные соединения и их производные обычно приготавливают и вводят в виде стандартных лекарственных форм или в виде лекарственных форм для многократного приема. В настоящем изобретении стандартные лекарственные формы относятся к физически дискретным единицам дозирования,подходящим для людей и животных и упакованным по отдельности, как известно в данной области. Каждая стандартная лекарственная доза содержит предварительно установленное количество терапевтически активного соединения, достаточное для обеспечения необходимого терапевтического эффекта, совместно с требуемым фармацевтическим носителем, средой или разбавителем. Примеры стандартных лекарственных форм включают ампулы и шприцы, отдельно упакованную таблетку или капсулу. Стандартные лекарственные формы можно вводить частями или многократно. Лекарственная форма для многократного приема представляет собой несколько идентичных стандартных лекарственных форм, помещенных в одну упаковку, с целью введения в форме отдельной стандартной дозы. Примеры лекарственных форм для многократного введения включают флаконы, склянки с таблетками или капсулами или склянки объемом в пинту или галлоны. Соответственно, лекарственная форма для многократного введения представляет собой несколько стандартных доз, которые не разделяют при упаковке. Помимо одного или более соединений согласно настоящему изобретению композиции могут включать разбавитель, такой как лактоза, сахароза, дикальция фосфат или карбоксиметилцеллюлоза; смазывающее вещество, такое как стеарат магния, стеарат кальция и тальк; и связующее вещество, такое как крахмал, природные камеди, такие как гуммиарабик, желатин, глюкоза, меласса, поливинилпирролидин,целлюлозы и их производные, повидон, кросповидоны и другие такого рода связующие вещества, известные специалисту, опытному в данной области. Жидкие фармацевтически вводимые композиции можно, например, приготовить путем растворения, диспергирования или иным образом смешивания активного соединения, которое описано выше, и возможных фармацевтических вспомогательных веществ в носителе, таком как, например, вода, солевой раствор, водная декстроза, глицерин, гликоли, этанол и т.п., с получением раствора или суспензии. При необходимости, вводимые фармацевтические композиции могут также содержать незначительные количества вспомогательных веществ, таких как увлажняющие вещества, эмульгирующие вещества или солюбилизирующие вещества, буферные вещества и т.п.,например ацетат, цитрат натрия, производные циклодекстрина, сорбитанмонолаурат, триэтаноламинацетат натрия, триэтаноламин олеат и другие такие вещества. Фактические способы получения указанных лекарственных форм известны или будут очевидны специалистам, опытным в этой области техники; например, см. Remington's Pharmaceutical Sciences, Mack Publishing Company, Easton, Pa., 15th Edition, 1975. В любом случае, вводимая композиция или состав будут содержать достаточное количество ингибитора согласно настоящему изобретению для снижения активности киназы in vivo, и, тем самым, лечения болезненного состояния субъекта. Лекарственные формы или композиции могут включать одно или более соединений согласно настоящему изобретению в диапазоне от 0,005 до 100% (по массе) с учетом содержания дополнительных веществ, таких как вещества, описанные в настоящем документе. Для перорального введения фармацевтически приемлемая композиция может включать любой один или более обычно применяемых наполнителей, таких как, например, фармацевтического качества маннитол, лактоза, крахмал, стеарат магния,тальк, производные целлюлозы, кросскармеллоза натрия, глюкоза, сахароза, карбонат магния, сахарин натрия, тальк. Указанные композиции включают растворы, суспензии, таблетки, капсулы, порошки, сухие порошки для ингаляторов и составы с замедленным высвобождением, такие как, помимо прочего,имплантаты и микроинкапсулированные системы доставки, и биодеградируемые, биосовместимые полимеры, такие как коллаген, этиленвинилацетат, полиангидриды, полигликолевая кислота, полиортоэфиры, полимолочная кислота и другие. Специалисту, опытному в данной области техники, известны способы получения этих составов. Композиции могут содержать 0,01-100% (по массе) одного или более ингибиторов киназы, возможно 0,1-95%, и возможно 1-95%. Соли, предпочтительно натриевые соли, ингибиторов можно смешивать с носителями, которые препятствуют быстрому выведению соединения из организма, такими как составы или покрытия замедленного действия. Составы могут дополнительно включать другие активные соединения для достижения необходимых сочетаний свойств. Составы для перорального введения. Пероральные фармацевтические лекарственные формы могут быть представлены в виде твердого вещества, геля или жидкости. Примеры твердых лекарственных форм включают, помимо прочего, таблетки, капсулы, гранулы и нерасфасованные порошки. Более конкретные примеры пероральных таблеток включают спрессованные таблетки, жевательные пастилки и таблетки, которые могут иметь энтеросолюбильное покрытие, сахарное покрытие или покрытие в виде пленки. Примеры капсул включают твердые или мягкие желатиновые капсулы. Гранулы и порошки можно получить в нешипучих или шипучих- 13019487 формах. Каждый ингредиент можно комбинировать с другими ингредиентами, известными специалисту,опытному в данной области. В некоторых вариантах реализации соединения согласно настоящему изобретению предложены в виде твердых лекарственных форм, предпочтительно капсул или таблеток. Таблетки, пилюли, капсулы,пастилки и т.п. могут содержать один или более из следующих ингредиентов или соединений аналогичной природы: связующее вещество; разбавитель; дезинтегрирующее вещество; лубрикант; вещество,способствующее скольжению; подсластитель и ароматизирующее вещество. Примеры связующих веществ, которые можно применять в настоящем изобретении, включают, помимо прочего, микрокристаллическую целлюлозу, трагакантовую камедь, раствор глюкозы, камедь акации, раствор желатина, сахарозу и крахмальную пасту. Примеры смазывающих веществ, которые можно применять в настоящем изобретении, включают,помимо прочего, тальк, крахмал, стеарат магния или кальция, ликоподий и стеариновую кислоту. Примеры разбавителей, которые можно применять в настоящем изобретении, включают, помимо прочего, лактозу, сахарозу, крахмал, каолин, соль, маннитол и дикальция фосфат. Примеры веществ, способствующих скольжению, которые можно применять в настоящем изобретении, включают, помимо прочего, коллоидный диоксид кремния. Примеры дезинтегрирующих веществ, которые можно применять в настоящем изобретении, включают, помимо прочего, кросскармеллозу натрия, крахмал гликолат натрия, альгиновую кислоту, кукурузный крахмал, картофельный крахмал, бентонит, метилцеллюлозу, агар и карбоксиметилцеллюлозу. Примеры окрашивающих веществ, которые можно применять в настоящем изобретении, включают,помимо прочего, любые одобренные сертифицированные водорастворимые красители FD и С, их смеси; и водонерастворимые красители FD и С, суспендированные в гидратированном оксиде алюминия. Примеры подсластителей, которые можно применять в настоящем изобретении, включают, помимо прочего, сахарозу, лактозу, маннитол и искусственные подсластители, такие как цикламат натрия и сахарин, и любое количество ароматических добавок, высушенных распылением. Примеры ароматизирующих веществ, которые можно применять в настоящем изобретении, включают, помимо прочего, природные ароматические добавки, выделенные из растений, таких как фрукты, и синтетические смеси соединений, которые создают приятное ощущение, такие как, помимо прочего, мята перечная и метилсалицилат. Примеры увлажняющих веществ, которые можно применять в настоящем изобретении, включают,помимо прочего, моностеарат пропиленгликоля, сорбитмоноолеат, монолаурат диэтиленгликоля и лауриловый эфир полиоксиэтилена. Примеры противорвотных покрытий, которые можно применять в настоящем изобретении, включают, помимо прочего, жирные кислоты, жиры, воски, шеллак, аммонизированный шеллак и ацетатфталаты целлюлозы. Примеры пленочных покрытий, которые можно применять в настоящем изобретении, включают,помимо прочего, гидроксиэтилцеллюлозу, натрия карбоксиметилцеллюлозу, полиэтиленгликоль 4000 и ацетатфталат целлюлозы. При необходимости перорального введения в композиции можно применять соль соединения, которая защищает ее от кислотной среды желудка. Например, композицию можно приготовить в энтеросолюбильном покрытии, которое сохраняет свою целостность в желудке и высвобождает активное соединение в кишечнике. Композицию также можно приготовить в комбинации с антацидом или другим подобным ингредиентом. Если стандартная лекарственная форма представляет собой капсулу, она может дополнительно содержать жидкий носитель, такой как жирное масло. Кроме того, стандартные лекарственные формы могут дополнительно содержать разные другие вещества, которые модифицируют физическую форму единицы дозирования, например, покрытия из сахара и другие растворимые в кишечнике вещества. Соединения согласно настоящему изобретению можно также вводить в виде компонента эликсира,суспензии, сиропа, вафли, карамельной крошки, жевательной резинки или т.п. Помимо активных соединений сироп может включать сахарозу в качестве подсластителя и несколько консервантов, красителей и красящих веществ и ароматических добавок. Соединения согласно настоящему изобретению можно также смешивать с другими активными препаратами, которые не ослабляют требуемое действия, или с препаратами, которые дополняют требуемое действие, такими как антациды, Н 2 блокаторы и диуретики. Например, если соединение применяют для лечения астмы или гипертензии, его можно применять с другими бронходилататорами и антигипертензивными средствами соответственно. Примеры фармацевтически приемлемых носителей, которые могут быть включены в таблетки, содержащие соединения согласно настоящему изобретению, включают, помимо прочего, связующие вещества, смазывающие вещества, разбавители, дезинтегрирующие вещества, окрашивающие вещества, ароматизирующие вещества и увлажняющие вещества. Таблетки с энтеросолюбильным покрытием, благодаря энтеросолюбильному покрытию, сопротивляются действию кислоты в желудке и растворяются или распадаются в нейтральной или щелочной среде кишечника. Таблетки с сахарным покрытием могут- 14019487 представлять собой спрессованные таблетки, на которые нанесены различные слои фармацевтически приемлемых веществ. Таблетки с пленочным покрытием могут представлять собой спрессованные таблетки, которые были покрыты полимерами или другим подходящим покрытием. Многослойные спрессованные таблетки могут представлять собой спрессованные таблетки, сделанные с помощью более чем одного цикла сжатия с применением фармацевтически приемлемых веществ, описанных ранее. В изготовлении таблеток также можно применять окрашивающие вещества. В изготовлении таблеток можно применять ароматизирующие и подсластители, которые особенно успешно применяются при получении жевательных таблеток и пастилок. Примеры жидких пероральных лекарственных форм, которые можно применять в настоящем изобретении, включают, помимо прочего, водные растворы, эмульсии, суспензии, растворы и/или суспензии, восстановленные из нешипучих гранул, и шипучие препараты, восстановленные из шипучих гранул. Примеры водных растворов, которые можно применять в настоящем изобретении, включают, помимо прочего, эликсиры и сиропы. В настоящем документе эликсиры относятся к прозрачным, подслащнным, водно-спиртовым препаратам. Примеры фармацевтически приемлемых носителей, которые можно применять в эликсирах, включают, помимо прочего, растворители. Конкретные примеры растворителей, которые можно применять в настоящем изобретении, включают глицерин, сорбит, этиловый спирт и сироп. В настоящем документе сиропы относятся к концентрированным водным растворам сахара, например сахарозы. Сиропы также могут включать консервант. Эмульсии относятся к двухфазным системам, в которых одна жидкость диспергируется в форме маленьких капелек в другой жидкости. Эмульсии могут представлять собой эмульсии масло-в-воде или вода-в-масле. Примеры фармацевтически приемлемых носителей, которые можно применять в эмульсиях, включают, помимо прочего, неводные жидкости, эмульгирующие вещества и консерванты. Примеры фармацевтически приемлемых веществ, которые можно применять в нешипучих гранулах, восстанавливаемых в жидкую пероральную лекарственную форму, включают разбавители, подсластители и увлажняющие вещества. Примеры фармацевтически приемлемых веществ, которые можно применять в шипучих гранулах,восстанавливаемых в жидкую пероральную лекарственную форму, включают органические кислоты и источник диоксида углерода. Красящие и ароматизирующие вещества можно применять во всех вышеуказанных лекарственных формах. Конкретные примеры консервантов, которые можно применять в настоящем изобретении, включают глицерин, метил- и пропилпарабен, бензойную кислоту, бензоат натрия и спирт. Конкретные примеры неводных жидкостей, которые можно применять в эмульсиях, включают минеральное масло и хлопковое масло. Конкретные примеры эмульгирующих веществ, которые можно применять в настоящем изобретении, включают желатин, гуммиарабик, трагакант, бентонит и поверхностно-активные вещества, такие как полиоксиэтилен сорбит моноолеат. Конкретные примеры суспендирующих веществ, которые можно применять в настоящем изобретении, включают натрий карбоксиметилцеллюлозу, пектин, трагакант, вигум и гуммиарабик. Разбавители включают лактозу и сахарозу. Подслащивающие вещества включают сахарозу, сиропы, глицерин и искусственные подслащивающие вещества, такие как цикламат натрия и сахарин. Конкретные примеры увлажняющих веществ, которые можно применять в настоящем изобретении,включают моностеарат пропиленгликоля, моноолеат сорбита, монолаурат диэтиленгликоля и лауриловый эфир полиоксиэтилена. Конкретные примеры органических кислот, которые можно применять в настоящем изобретении,включают лимонную и винно-каменную кислоту. Источники диоксида углерода, которые можно применять в шипучих композициях, включают бикарбонат натрия и карбонат натрия. Окрашивающие вещества включают любые одобренные сертифицированные водорастворимые красители FD и С и их смеси. Конкретные примеры ароматизирующих веществ, которые можно применять в настоящем изобретении, включают природные ароматические добавки, выделенные из растений, таких как фрукты, и синтетические смеси соединений, которые создают приятное вкусовое ощущение. Для твердой лекарственной формы раствор или суспензию, например, в пропиленкарбонате, растительных маслах или триглицеридах предпочтительно инкапсулировать в желатиновой капсуле. Такие растворы и их приготовление и инкапсулирование описаны в патентах США 4328245; 4409239 и 4410545. Для жидкой лекарственной формы, раствор, например в полиэтиленгликоле, можно разбавить достаточным количеством фармацевтически приемлемого жидкого носителя, например воды, которое можно легко измерить при введении. Альтернативным образом, жидкие или полутвердые пероральные составы можно приготовить путем растворения или диспергирования активного соединения или соли в растительных маслах, гликолях,триглицеридах, эфирах пропиленгликоля (например, пропиленкарбонате) и других подобных носителях,и инкапсулирования этих растворов или суспензий в оболочках твердых или мягких желатиновых кап- 15019487 сул. Другие применяемые составы включают составы, описанные в патентах СШАRe 28819 и 4358603. Инъецируемые препараты, растворы и эмульсии. Настоящее изобретение также направлено на композиции, разработанные для введения соединений согласно настоящему изобретению парентеральным путем, который, в общем, включает подкожную,внутримышечную или внутривенную инъекцию. Инъецируемые препараты можно приготовить в любой обычной форме, например в виде жидких растворов или суспензий, твердых форм, подходящих для приготовления раствора или суспензии в жидкости перед инъекцией, или в виде эмульсий. Примеры наполнителей, которые можно применять в сочетании с инъецируемыми препаратами согласно настоящему изобретению, включают, помимо прочего, воду, солевой раствор, декстрозу, глицерин или этанол. Инъецируемые композиции также могут содержать незначительные количества нетоксичных вспомогательных веществ, таких как увлажняющие или эмульгирующие вещества, буферные вещества, стабилизаторы, вещества, усиливающие растворимость и другие подобные вещества, такие как, например, ацетат натрия, сорбитанмонолаурат, триэтаноламин олеат и циклодекстрины. В настоящем документе также рассматривают имплантацию системы с медленным высвобождением или высвобождением с задержкой для поддержания постоянного уровня дозирования (см., например, патент США 3710795). Процентное содержание активного соединения, включенного в такие парентеральные композиции, существенно зависит от его конкретной природы, а также активности соединения и потребностей субъекта. Парентеральное введение составов включает внутривенное, подкожное и внутримышечное введение. Препараты для парентерального введения включают стерильные растворы, готовые для инъекции,стерильные сухие растворимые продукты, такие как лиофилизированные порошки, описанные в настоящем изобретении, которые смешивают с растворителем непосредственно перед применением, в том числе гиподермальные таблетки, стерильные суспензии, готовые для инъекции, стерильные сухие нерастворимые продукты, которые смешивают с наполнителем непосредственно перед применением, и стерильные эмульсии. Растворы могут быть водными или неводными. При внутривенном введении примеры подходящих носителей включают, помимо прочего, физиологический солевой раствор или фосфатно-солевой буферный раствор (PBS) и растворы, содержащие загустители и солюбилизирующие вещества, такие как глюкоза, полиэтиленгликоль и полипропиленгликоль и их смеси. Примеры фармацевтически приемлемых носителей, которые можно применять в парентеральных препаратах, включают, помимо прочего, водные среды, неводные среды, противомикробные средства,изотонические вещества, буферные вещества, антиоксиданты, местные анестезирующие средства, суспендирующие и диспергирующие вещества, эмульгирующие вещества, комплексообразующие или хелатирующие агенты и другие фармацевтически приемлемые вещества. Примеры водных сред, которые можно применять в настоящем изобретении, включают хлорид натрия для инъекций, раствор Рингера для инъекций, изотонический раствор декстрозы для инъекций, стерильную воду для инъекций, декстрозный и лактатный раствор Рингера для инъекций. Примеры неводных парентеральных сред, которые можно применять в настоящем изобретении,включают нелетучие масла растительного происхождения, хлопковое масло, кукурузное масло, кунжутное масло и арахисовое масло. К парентеральным препаратам можно добавлять противомикробные средства в бактериостатических или фунгистатических концентрациях, в частности, если препараты помещены в упаковки для многократного приема и, таким образом, предназначены для хранения и извлечения аликвот при многократном дозировании. Примеры противомикробных средств, которые можно применять в настоящем изобретении, включают фенолы или крезолы, ртутные препараты, бензиловый спирт, хлорбутанол, метиловые и пропиловый эфиры п-гидроксибензойной кислоты, тимерозал, бензалкониум хлорид и бензетониум хлорид. Примеры изотонических веществ, которые можно применять в настоящем изобретении, включают хлорид натрия и декстрозу. Примеры буферных веществ, которые можно применять в настоящем изобретении, включают фосфат и цитрат. Примеры антиоксидантов, которые можно применять в настоящем изобретении, включают бисульфат натрия. Примеры местных анестезирующих средств, которые можно применять в настоящем изобретении, включают прокаина гидрохлорид. Примеры суспендирующих и диспергирующих веществ, которые можно применять в настоящем изобретении, включают натрия карбоксиметилцеллюлозу, гидроксипропилметилцеллюлозу и поливинилпирролидон. Примеры эмульгирующих веществ, которые можно применять в настоящем изобретении, включают полисорбат 80 (твин 80). Комплексообразующие или хелатирующие агенты для ионов металлов включают EDTA. Фармацевтические носители также могут включать этиловый спирт, полиэтиленгликоль и пропиленгликоль для водных смешивающихся сред и гидроксид натрия, соляную кислоту, лимонную кислоту или молочную кислоту для регулирования рН. Концентрацию ингибитора в парентеральном составе можно регулировать таким образом, чтобы инъекция вводила фармацевтически эффективное количество, достаточное для оказания необходимого- 16019487 фармакологического эффекта. Как известно в данной области, точная концентрация ингибитора и/или дозировка, которую следует использовать, будет, в конечном счете, зависеть от возраста, массы и состояния пациента или животного. Парентеральные препараты в виде стандартной дозы можно поместить в ампулу, склянку или шприц с иглой. Как известно и практикуется в данной области, все препараты для парентерального введения должны быть стерильными. Можно приготовить инъецируемые препараты для местного и системного введения. Обычно терапевтически эффективную дозу для лечения ткани (тканей) приготавливают таким образом, что она содержит концентрацию ингибитора киназы по меньшей мере от примерно 0,1% по массе до примерно 90% по массе или более, предпочтительно более чем 1% по массе. Ингибитор можно ввести за один раз или можно разделить на несколько более мелких доз, которые вводят через определенные интервалы времени. Следует иметь в виду, что точная дозировка и продолжительность лечения будут зависеть от области тела, в которую парентерально вводится композиция, носителя и других возможных ингредиентов, которые можно определить эмпирически, используя известные протоколы проведения испытаний или путем экстраполяции результатов испытаний in vivo или in vitro. Следует отметить, что концентрации и дозировки могут также варьировать с возрастом подвергаемого лечению субъекта. Следует также иметь в виду, что для любого отдельного субъекта со временем может потребоваться корректировка конкретных режимов дозирования в соответствии с индивидуальной потребностью и профессиональным суждением лица, осуществляющего или надзирающего над введением составов. Поэтому предложенные в настоящем документе диапазоны концентраций являются иллюстративными и не предполагают ограничить объем или применение на практике описанных составов. Ингибитор киназы можно суспендировать в тонкоизмельченную или другую подходящую форму или синтезировать его производные для получения более растворимого активного продукта или пролекарства. Форма образующейся смеси зависит от ряда факторов, в том числе от предполагаемого пути введения и растворимости соединения в выбранном носителе или среде. Эффективная концентрация является достаточной для облегчения симптомов болезненного состояния и может быть определена эмпирически. Лиофилизированные порошки. Соединения согласно настоящему изобретению можно также приготовить в виде лиофилизированных порошков, которые можно восстановить для введения в виде растворов, эмульсий и других смесей. Лиофилизированные порошки можно также получить в виде твердых веществ или гелей. Стерильный, лиофилизированный порошок можно приготовить путем растворения соединения в фосфатно-солевом буферном растворе, содержащем декстрозу или другой подходящий наполнитель. Последующая стерильная фильтрация раствора, а затем лиофилизация при стандартных условиях, известных специалисту, опытному в данной области техники, позволяет получить требуемый состав. Короче, лиофилизированный порошок можно приготовить путем растворения декстрозы, сорбита, фруктозы,кукурузного сиропа, ксилитола, глицерина, глюкозы, сахарозы или другого подходящего вещества, примерно 1-20%, предпочтительно примерно 5-15%, в подходящем буферном веществе, таком как цитрат,фосфат натрия или калия или другом подобном буферном веществе, известном специалисту, опытному в данной области техники, обычно, при примерно нейтральном рН. Затем, к образовавшейся смеси добавляют ингибитор киназы предпочтительно при температуре выше комнатной, более предпочтительно примерно при 30-35 С и перемешивают до его растворения. Образовавшуюся смесь разбавляют до требуемой концентрации путем добавления дополнительного количества буферного вещества. Образовавшуюся смесь стерильно фильтруют или обрабатывают для удаления твердых частиц и обеспечения стерильности и распределяют по флаконам для лиофилизации. Каждый флакон может содержать одну дозу или многократные дозы ингибитора. Топическое введение. Соединения согласно настоящему изобретению можно также вводить в виде топических смесей. Топические смеси можно применять для местного и системного введения. Образовавшаяся смесь может представлять собой раствор, суспензию, эмульсии или т.п. и быть приготовленной в виде кремов, гелей,мазей, эмульсий, растворов, эликсиров, лосьонов, суспензий, настоек, паст, пен, аэрозолей, промываний,спреев, суппозиториев, повязок, дермальных пластырей или любых других составов, подходящих для топического введения. Ингибиторы киназы можно приготовить в виде аэрозолей для топического наложения, например, с помощью ингаляции (см. патент США 4044126, 4414209 и 4364923, в котором описаны аэрозоли для введения стероида, применяемого для лечения воспалительных заболеваний, в частности астмы). Эти составы для введения в дыхательные пути могут быть в форме аэрозоля или раствора для распылителя или в виде мелкозернистого порошка для инсуффляции, самостоятельно или в комбинации с инертным носителем, таким как лактоза. В таком случае частицы состава, как правило, будут иметь диаметр менее чем 50 мкм, предпочтительно менее чем 10 мкм. Ингибиторы также можно приготовить для местного или топического нанесения, например для топического нанесения на кожу и слизистые оболочки, например, в глазу, в форме гелей, кремов и лосьонов, и для нанесения в глаз или для интрацистернального или- 17019487 интраспинального нанесения. Топическое введение включает трансдермальную доставку и также введение в глаза или слизистую оболочку, или ингаляционные способы лечения. Можно также вводить назальные растворы ингибитора киназы отдельно или в комбинации с другими фармацевтически приемлемыми наполнителями. Составы для других способов введения. В зависимости от болезненного состояния, подвергаемого лечению, можно также применять другие пути введения, такие как топическое нанесение, трансдермальные пластыри и ректальное введение. Например, фармацевтические лекарственные формы для ректального введения представляют собой ректальные суппозитории, капсулы и таблетки для оказания системного эффекта. Ректальные суппозитории,применяемые в настоящем документе, представляют собой твердые объекты для помещения в прямую кишку, которые плавятся или размягчаются при температуре тела, высвобождая один или более фармакологически или терапевтически активных ингредиентов. Фармацевтически приемлемые вещества, применяемые в ректальных суппозиториях, представляют собой основы или среды и вещества, которые поднимают температуру плавления. Примеры основ включают масло какао (масло theobrom), глицеринжелатин, карбовакс, полиоксиэтиленгликоль и подходящие смеси моно-, ди- и триглицеридов жирных кислот. Можно применять комбинации различных основ. Вещества, которые поднимают температуру плавления суппозиториев, включают спермацет и воск. Ректальные суппозитории можно приготовить способом прессования или путем формования. Типичная масса ректального суппозитория составляет примерно от 2 до 3 г. Таблетки и капсулы для ректального введения можно изготавливать промышленным способом, применяя то же фармацевтически приемлемое вещество и такие же способы, как в случае составов для перорального введения. Примеры составов. Приведенные ниже составы представляют собой конкретные примеры пероральных, внутривенных и таблеточных составов, которые можно применять в сочетании с соединениями согласно настоящему изобретению. Следует отметить, что эти составы могут варьировать в зависимости от конкретного применяемого соединения и показания, для лечения которого собираются применять этот состав. Пероральный состав Дозировка, репициент и безопасность. Соединения согласно настоящему изобретению являются стабильными и могут применяться безопасно. В частности, соединения согласно настоящему изобретению можно применять в качестве ингибиторов PLK для лечения различных субъектов (например, людей, млекопитающих, не относящихся к че- 18019487 ловеку, и не млекопитающих). Оптимальная доза может варьировать в зависимости от таких условий,как, например, вид субъекта, масса тела субъекта, путь введения и конкретные свойства данного применяемого соединения. В целом, ежедневная доза для перорального введения взрослому (масса тела примерно 60 кг) составляет примерно от 1 до 1000 мг, примерно от 3 до 300 мг или примерно от 10 до 200 мг. Следует иметь в виду, что ежедневную дозу можно принимать в день при однократном введении или в виде многократных (например, 2 или 3) порций. Комбинированные способы лечения. Разнообразные терапевтические агенты могут иметь терапевтический аддитивный или синергический эффект с ингибиторами киназы согласно настоящему изобретению. Комбинированные способы лечения, которые включают одно или более соединений согласно настоящему изобретению с одним или более других терапевтических агентов, можно применять, например, для: 1) усиления терапевтического эффекта (эффектов) одного или более соединений согласно настоящему изобретению и/или одного или более других терапевтических агентов; 2) уменьшения побочных эффектов, проявляемых одним или более соединениями согласно настоящему изобретению и/или одним или более другими терапевтическими агентами; и/или 3) снижения эффективной дозы одного или более соединений согласно настоящему изобретению и/или одного или более других терапевтических агентов. Например, такие другие терапевтические агенты могут аддитивно или синергически сочетаться с ингибиторами киназы для ингибирования нежелательного клеточного роста, такого как неадекватный рост клеток, возникающий при нежелательных доброкачественных состояниях, или рост опухоли. Проводят обработку клеток соединением согласно настоящему изобретению в комбинации с антипролиферативным препаратом, при этом клетки обрабатывают соединением согласно настоящему изобретению до, одновременно и/или после обработки клеток противопролиферативным препаратом, называемым в настоящем документе комбинированной терапией. Следует отметить, что обработку одним препаратом перед другим называют в настоящем документе последовательной терапией, даже если препараты также вводят вместе. Следует отметить, что комбинированная терапия включает случай, когда препараты вводят до или друг за другом (последовательная терапия), а также когда вещества вводят одновременно. Примеры терапевтических агентов, которые можно применять в комбинации с ингибиторами киназы, включают, помимо прочего, противоопухолевые препараты, алкилирующие агенты, антибиотические препараты, антиметаболические агенты, гормональные препараты, вещества растительного происхождения и биологические агенты. Алкилирующие агенты представляют собой полифункциональные соединения, которые обладают способностью замещать ионы водорода алкильными группами. Примеры алкилирующих агентов включают, помимо прочего, бисхлорэтиламины (азотистые иприты, например хлорамбуцил, циклофосфамид,ифосфамид, мехлоретамин, мелфалан, упацилиприт), азиридины (например, тиотепа), алкил алкон сульфонаты (например, бусульфан), нитромочевины (например, кармустин, ломустин, стрептозоцин), неклассические алкилирующие агенты (алтретамин, дакарбазин, и прокарбазин), платиновые соединения (карбопластин и цисплатин). Эти соединения реагируют с фосфатными, амино, гидроксильными, сульфигидрильными, карбоксильными и имидазольными группами. При физиологических условиях эти лекарственные препараты ионизируются и образуют положительно заряженный ион, который присоединяется к восприимчивым нуклеиновым кислотам и белкам, что приводит к остановке клеточного цикла и/или некрозу клеток. Комбинированная терапия, в том числе ингибитор киназы и алкилирующий агент, может оказывать терапевтические синергические эффекты на рак и уменьшать побочные эффекты, связанные с этими химиотерапевтическими веществами. Антибиотические препараты представляют собой группу лекарств, которые создали способом, аналогичным антибиотикам, как модификацию природных продуктов. Примеры антибиотических препаратов включают, помимо прочего, антрациклины (например, доксорубицин, даунорубицин, эпирубицин,идарубицин и антраценедион), митомицин С, блеомицин, дактиномицин, пликатомицин. Эти антибиотические препараты препятствуют клеточному росту, направленно воздействуя на различные клеточные компоненты. Например, как предполагают, антрациклины, в общем, препятствуют действию топоизомеразы II ДНК на участках транскрипциально активной ДНК, что приводит к расщеплению нитей ДНК. Как полагают, блеомицин, в общем, хелатирует железо и образует активированный комплекс, который затем связывается с основаниями ДНК, вызывая расщепления нитей и некроз клеток. Комбинированная терапия, в том числе ингибитор киназы и антибиотический препарат, могут оказывать терапевтические синергические эффекты на рак и уменьшать побочные эффекты, связанные с этими химиотерапевтическими веществами. Антиметаболические средства представляют собой группу лекарств, которые препятствуют метаболическим процессам, жизненно важным для физиологии и пролиферации раковых клеток. Активно прилиферирующие раковые клетки требуют постоянного синтеза больших количеств нуклеиновых кислот, белков, липидов и других витальных клеточных составляющих. Многие из антиметаболитов ингибируют синтез пуриновых или пиримидиновых нуклеозидов или ингибируют ферменты репликации ДНК. Некоторые антиметаболиты также препятствуют синтезу рибонуклеозидов и РНК и/или метабо- 19019487 лизму аминокислот и также синтезу белка. Путем препятствия синтезу витальных клеточных составляющих антиметаболиты могут замедлить или остановить рост раковых клеток. Примеры антиметаболических препаратов включают, помимо прочего, фторурацил (5-FU), флоксуридин (5-FUdR), метотрексат,леуковорин, гидроксимочевину, тиогуанин (6-TG), меркаптопурин (6-МР), цитарабин, пентостатин, флударабина фосфат, кладрибин (2-CDA), аспарагиназу и гемцитабин. Комбинированная терапия, в том числе ингибитор киназы и антиметаболическое вещество, может оказывать терапевтические синергические эффекты на рак и уменьшать побочные эффекты, связанные с этими химиотерапевтическими веществами. Гормональные препараты представляют собой группу лекарств, которые регулируют рост и развитие органов, на которые направлено их действие. Большинство гормональных препаратов представляют собой половые стероиды и их производныеи аналоги, такие как эстрогены, андрогены и прогестины. Эти гормональные препараты могут служить в качестве антагонистов рецепторов для половых стероидов для регулирования с понижением экспрессии рецептора и транскрипции витальных генов. Примерами таких гормональных препаратов являются синтетические эстрогены (например, диэтилстибестрол), антиэстрогены (например, тамоксифен, торемифен, флуоксиместерол и ралоксифен), антиандрогены (бикалутамид,нилутамид, флутамид), ингибиторы ароматазы (например, аминоглутетимид, анастрозол и тетразол),кетоконазол, гозерелин ацетат, леупролид, мегестрола ацетат и мифепристон. Комбинированная терапия,в том числе ингибитор киназы и гормональный препарат, могут оказывать терапевтические синергические эффекты на рак и уменьшать побочные эффекты, связанные с этими химиотерапевтическими веществами. Препараты, полученные из растений, представляют собой группу лекарств, которые извлекают из растений или модифицируют на основе молекулярной структуры веществ. Примеры препаратов, получаемых из растений, включают, помимо прочего, алкалоиды барвинка (например, винкристин, винбластин, виндезин, винзолидин и винорелбин), подофиллотоксины (например, этопозид (VP-16) и тенипозид(VM-26, таксаны (например, паклитаксел и доцетаксел). Эти препараты, полученные из растений, в общем, действуют как антимитотические средства, которые связываются с тубулином и ингибируют митоз. Как полагают, подофиллотоксины, такие как этопозид, препятствуют синтезу ДНК путем взаимодействия с топоизомеразой II, что приводит к расщеплению нитей ДНК. Комбинированная терапия, в том числе ингибитор киназы и препарат, полученный из растений, может оказывать терапевтические синергические эффекты на рак и уменьшать побочные эффекты, связанные с этими химиотерапевтическими веществами. Биологические агенты представляют собой группу биомолекул, которые вызывают регрессию рака/опухоли, при самостоятельном применении или в комбинации с химиотерапией и/или радиотерапией. Примеры биологических агентов включают, помимо прочего, иммуномодулирующие белки, такие как цитокины, моноклональные антитела против опухолевых антигенов, подавляющие опухоль гены и вакцины против рака. Комбинированная терапия, в том числе ингибитор киназы и биологические агенты,может оказывать терапевтические синергические эффекты на рак, усиливать иммунные реакции пациента на онкогенные сигналы и уменьшать потенциальные побочные эффекты, связанные с этим химиотерапевтическим препаратом. Цитокины обладают сильным иммуномодулирующим действием. Некоторые цитокины, такие как интерлейкин-2 (IL-2, альдеслейкин) и интерферон, демонстрировали противоопухолевую активность и были одобрены для лечения пациентов с метастатическим почечно-клеточным раком и метастатической злокачественной меланомой. IL-2 представляет собой роста фактор Т-клеток, который является основным в Т-клеточно-опосредованных иммунных реакциях. Как полагают, селективное противоопухолевое воздействие IL-2 на некоторых пациентов является результатом клеточно-опосредованной иммунной реакции, которая распознает "свое" и "не свое". Примеры интерлейкинов, которые можно применять в сочетании с ингибитором киназы, включают, помимо прочего, интерлейкин 2 (IL-2), интерлейкин 4 (IL4), интерлейкин 12 (IL-12). Интерфероны включают более чем 23 родственных подтипа с перекрывающимися активностями,при этом все из подтипов IFN включены в объем настоящего изобретения. IFN демонстрирует активность против многих твердых и гематологических злокачественных опухолей, при этом последние, повидимому, являются особенно чувствительными. Другие цитокины, которые можно применять в сочетании с ингибитором киназы, включают те цитокины, которые оказывают сильные эффекты на гемопоэз и иммунные функции. Примеры указанных цитокинов включают, помимо прочего, эритропоиетин, гранулоцит-CSF (филграстин) и гранулоцит,макрофаг-CSF (сарграмостим). Эти цитокины можно применять в сочетании с ингибитором киназы для снижения миелопоэзной токсичности, вызванной химиотерапией. Другие иммуномодулирующие препараты, отличные от цитокинов, также можно применять в сочетании с ингибитором киназы для ингибирования аномального клеточного роста. Примеры таких иммуномодулирующих препаратов включают, помимо прочего, палочку Calmette-Guerin, левамизол и остреотид, октапептид длительного действия, который имитирует эффекты природного гормона соматостатина. Моноклональные антитела против опухолевых антигенов представляют собой антитела, вызванные- 20019487 против антигенов, экспрессируемых опухолями, предпочтительно опухолеспецифических антигенов. Например, моноклональное антитело HERCEPTIN (траструзумаб) применяют против рецептора 2 эпидермального фактора роста (HER2) человека, который избыточно экспрессируется в некоторых опухолях молочной железы, в том числе при метастатическом раке груди. Избыточная экспрессия белка HER2 связана в клинической практике с более агрессивным заболеванием и более неблагоприятным прогнозом.HERCEPTIN применяют в качестве единственного средства для лечения пациентов с метастатическим раком груди, опухоли которого избыточно экспрессируют белок HER2. Комбинированная терапия, в том числе ингибитор киназы и HERCEPTIN, может оказывать терапевтические синергические эффекты на опухоли, особенно на метастатические раки. Еще одним примером моноклональных антител против опухолевых антигенов является RITUXAN(ритуксимаб), который применяют против CD20 в клетках лимфомы и который селективно разрушает нормальные и злокачественные CD20+ pre-B и зрелые В клетки. RITUXAN применяют в качестве единственного средства для лечения пациентов с повторной или стойкой малоразвитой или фолликулярной,CD20+, В клеточной не-ходжкинской лимфомой. Комбинированная терапия, в том числе ингибитор киназы и RITUXAN, может оказывать терапевтические синергические эффекты не только на лимфому, но также на другие формы или типы злокачественных опухолей. Гены, подавляющие опухоль, представляют собой гены, которые функционируют для ингибирования клеточного роста и циклов деления, таким образом, предотвращая развитие неоплазии. Мутации в генах, подавляющих опухоль, заставляют клетку игнорировать один или более из компонентов сети ингибирующих сигналов, что позволяет преодолеть контрольные точки клеточного цикла и приводит к более высокой степени контролирования клеточный рост-рак. Примеры генов, подавляющих опухоль, включают, помимо прочего, DPC-4, NF-1, NF-2, RB,p53, WT1, BRCA1 и BRCA2.DPC-4 связан с раком поджелудочной железы и принимает участие в цитоплазматическом пути, который ингибирует клеточное деление. NF-1 несет информацию о белке, который ингибирует Ras, цитоплазматическом ингибирующем белке. NF-1 связан с нейрофибромой и феохромоцитомами нервной системы и миелоидной лейкемией. NF-2 кодирует ядерный белок, который связан с менингиомой, шванномой и эпендимомой нервной системы. RB несет информацию о белке pRB, ядерном белке, который является главным ингибитором клеточного цикла. RB связан с ретинобластомой, а также раком костей, мочевого пузыря, мелкоклеточным раком лгкого и раком молочной железы. р 53 несет информацию о белке р 53, который регулирует клеточное деление и может вызвать апоптоз. Мутацию и/или неактивность р 53 обнаруживают при самых различных заболеваниях ракаом. WT1 связан с опухолью Вильмса почек.BRCA1 связан с раком груди и яичников, и BRCA2 связан с раком груди. Ген, подавляющий опухоль,можно перенести в опухолевые клетки, где он проявляет свои подавляющие опухоль функции. Комбинированная терапия, в том числе ингибитор киназы и ген, подавляющий опухоль, может оказывать терапевтические синергические эффекты на пациентов, страдающих от различных форм раковых заболеваний. Противораковые вакцины представляют собой группу препаратов, которые вызывают в организме специфическую иммунную реакцию на опухоли. Большинство противораковых вакцин, находящихся на стадии исследований и разработки и клинических испытаний, представляют собой опухолеспецифические антигены (ТАА). ТАА являются структурами (т.е. белками, ферментами или карбогидратами), которые присутствуют в опухолевых клетках и соответственно отсутствуют или присутствуют в незначительных количествах в нормальных клетках. Имея преимущество быть в некоторой степени уникальными для опухолевой клетки, антигены ТАА обеспечивают мишени для иммунной системы, которые должны быть распознаны, и вызывают их разрушение. Примеры антигенов ТАА включают, помимо прочего,ганглиозиды (GM2), простатический специфический антиген (PSA), альфа-фетопротеин (AFP), карциноэмбриональный антиген (СЕА) (вызванный раком толстой кишки и другими аденокарциномами, например, раком груди, легких, желудка и поджелудочной железы), антигены, связанные с меланомой (MART1, gp100, MAGE 1,3 тирозиназа), фрагменты папилломавируса Е 6 и Е 7, целые клетки или части/лизаты аутологических опухолевых клеток и аллогенных опухолевых клеток. Для усиления иммунной реакции на ТАА можно применять вспомогательные вещества. Примеры вспомогательных веществ включают, помимо прочего, бациллу Calmette-Guerin (BCG), эндотоксин липополисахариды, гемоцианин лимфы улитки (GKLH), интерлейкин-2 (IL-2), гранулоцитарномоноцитарный колониестимулирующий фактор, (GM-CSF) и цитоксан, химиотерапевтический препарат,который, как полагают, снижает вызванную опухолью супрессию при приеме в низких дозах. Примеры Получение ингибиторов киназ. Можно разработать различные способы для синтезирования соединений согласно настоящему изобретению. Типичные способы синтезирования этих соединений приведены в примерах. Стоит заметить,тем не менее, что соединения согласно настоящему изобретению также можно синтезировать с помощью других синтетических подходов, которые могут быть разработаны в дальнейшем. Должно быть очевидно, что некоторые соединения согласно настоящему изобретению включают- 21019487 атомы, которые образуют связи с другими атомами, которые придают определенную стереохимию соединению (например, хиральные центры). Должно быть очевидно, что синтез соединений согласно настоящему изобретению может привести к созданию смеси различных стереоизомеров (т.е. энантиомеров и диастереомеров). Если не указана конкретная стереохимия, в объем понимания соединения предполагают входящими все различные возможные стереоизомеры. В данной области известны различные способы разделения смесей различных стереоизомеров. Например, рацемическую смесь соединения можно привести во взаимодействие с оптически активным расщепляющим агентом с получением пары диастереоизомерных соединений. Диастереомеры затем можно разделить для того, чтобы получить оптически чистые энантиомеры. Диссоциируемые комплексы также можно применять для расщепления энантиомеров (например, кристаллических диастереоизомерных солей). Диастереомеры обычно имеют достаточно различные физические свойства (например, температуры плавления, температуры кипения, растворимость, реакционную способность и т.д.) и их можно легко разделить, пользуясь преимуществом этих различий. Например, диастереомеры обычно можно разделить с помощью хроматографии или с помощью методик разделения/расщепления, основанных на различиях в растворимости. Более подробное описание методик, которые можно применять для расщепления рацемической смеси с получением стереоизомеров соединений, можно найти в Jean Jacques AndreCollet, Samuel H. Wilen, Enantiomers, Racemates and Resolutions, John WileySons, Inc. (1981). Соединения согласно настоящему изобретению также можно получить в виде фармацевтически приемлемой соли присоединения кислоты путем приведения во взаимодействие формы свободного основания соединения с фармацевтически приемлемой неорганической или органической кислотой. В качестве альтернативы, фармацевтически приемлемые соли присоединения основания указанного соединения можно получить путем приведения во взаимодействие формы свободной кислоты соединения с фармацевтически приемлемым неорганическим или органическим основанием. Неорганические и органические кислоты и основания, подходящие для получения фармацевтически приемлемых солей соединений,описаны в разделе определений в настоящем изобретении. В качестве альтернативы, солевые формы указанных соединений можно получить, используя соли исходных веществ или промежуточных продуктов. Формы свободной кислоты или свободного основания соединений можно получить из соответствующей формы соли присоединения основания или соли присоединения кислоты. Например, соединение в форме соли присоединения кислоты можно превратить в соответствующее свободное основание путем обработки подходящим основанием (например, раствором гидроксида аммония, гидроксидом натрия, и тому подобными). Соединение в форме соли присоединения основания можно превратить в соответствующую свободную кислоту путем обработки подходящей кислотой (например, соляной кислотой и т.д.).N-оксиды соединений согласно настоящему изобретению можно получить с помощью способов,известных среднему специалисту в данной области. Например, N-оксиды можно получить путем обработки неокисленной формы соединения окисляющим агентом (например, трифторперуксусной кислотой,пермалеиновой кислотой, пербензойной кислотой, перуксусной кислотой, мета-хлорпероксибензойной кислотой, или тому подобными) в подходящем инертном органическом растворителе (например, галогенированном углеводороде, таком как дихлорметан) при приблизительно 0 С. В качестве альтернативы,N-оксиды указанных соединений можно получить из N-оксида подходящего исходного материала. Соединения в неокисленной форме можно получить из N-оксидов соединений путем обработки восстанавливающим агентом (например, серой, диоксидом серы, трифенилфосфином, борогидридом лития, борогидридом натрия, треххлористым фосфором, трибромидом, или тому подобными) в подходящем инертном органическом растворителе (например, ацетонитриле, этаноле, водном диоксане или т.п.) при температуре от 0 до 80 С. Производные соединений в виде пролекарств можно получить с помощью способов, известных среднему специалисту в данной области (например, дополнительное описание см. у Saulnier и др. (1994),Bioorganic and Medicinal Chemistry Letters, том 4, с. 1985). Например, подходящие пролекарства можно получить путем приведения во взаимодействие исходного соединения с подходящим карбамилирующим агентом (например, 1,1-ацилоксиалкилкарбонхлоридатом, пара-нитрофенилкарбонатом или т.п.). Защищенные производные указанных соединений можно получить с помощью способов, известных среднему специалисту в данной области. Подробное описание методик, применимых для получения защитных групп и их удаления можно найти у T.W. Greene, Protective Groups in Organic Synthesis, 3-е издание, John WileySons, Inc. 1999. Соединения согласно настоящему изобретению можно легко получить, или они могут быть получены во время процесса согласно настоящему изобретению, в виде сольватов (например, гидратов). Гидраты соединений согласно настоящему изобретению можно легко получить путем перекристаллизации из смеси водного/органического растворителей, применяя органические растворители, такие как диоксин,тетрагидрофуран или метанол. Соединения согласно настоящему изобретению также можно получить в виде отдельных стереоизомеров путем приведения во взаимодействие рацемической смеси соединения с оптически активным расщепляющим агентом с получением пары диастереоизомерных соединений, разделения диастереоме- 22019487 ров и получения оптически чистого энантиомера. Несмотря на то что расщепление энантиомеров можно осуществить, используя ковалентные диастереомерные производные соединений, диссоциируемые комплексы являются предпочтительными (например, кристаллические диастереоизомерные соли). Диастереомеры имеют различные физические свойства (например, температуры плавления, температуры кипения, растворимость, реакционную способность и т.д.) и их можно легко разделить, пользуясь преимущетвом этих различий. Диастереомеры можно разделить с помощью хроматографии или предпочтительно с помощью методик разделения/расщепления, основанных на различиях в растворимости. Оптически чистый энантиомер затем получают, наряду с расщепляющим агентом, с помощью любых целесообразных средств, которые не приведут к рацемизации. Более подробное описание методик, применимых для расщепления стереоизомеров соединений из их рацемической смеси, можно найти в Jean Jacques AndreCollet, Samuel H. Wilen, Enantiomers, Racemates and Resolutions, John WileySons, Inc. (1981). Используемые в данном патенте символы и условные обозначения, применяемые в описанных процессах, схемах и примерах, идентичны с применяемыми в современной научной литературе, например вJournal of the American Chemical Society или в Journal of Biological Chemistry. Стандартные однобуквенные или трехбуквенные сокращения, как правило, применяют для обозначения аминокислотных остатков, которые предполагают находящимися в L-конфигурации, если не указано иначе. Если не указано иначе, все исходные вещества были получены из коммерческих источников и использовались без дополнительной очистки. В частности, в примерах и на всем протяжении настоящего описания могут использоваться следующие сокращения: Все ссылки на эфир или Et2O относятся к диэтиловому эфиру; солевой раствор относится к насыщенному водному раствору NaCl. Если не указано иначе, все температуры выражены в С (градусы по Цельсию). Все реакции ведут в инертной атмосфере при комнатной температуре, если не указано иначе. 1 Н ЯМР спектры регистрировали на Bruker Avance 400. Химические сдвиги выражали в частях на миллион (ppm). Константы взаимодействия выражали в единицах герц (Гц). Варианты расщепления описывают видимую мультиплетность и обозначены как s (синглет), d (дублет), t (триплет), q (квартет), m(мультиплет), br (широкий). Масс-спектры с низким разрешением (МС) и данные по чистоте соединений собирали на одноквадрупольной системе ЖХ/МС Waters ZQ, оборудованной источником с ионизацией электрораспылением (ИЭР), УФ-детектором (220 и 254 нм) и испарительным светорассеивающим детектором (ELSD). Тонкослойную хроматографию выполняли на 0,25-мм пластинах силикагеля E.Merck(60F-254), визуализировали с помощью УФ-света, 5% этанольной фосфорномолибденовой кислоты, нингидрина или раствора пара-анисальдегида. Колоночную флэш-хроматографию выполняли на силикагеле(230-400 меш, Merck). Исходные вещества и реагенты, применяемые для получения этих соединений, либо доступны из коммерческих источников, таких как Aldrich Chemical Company (Милуоки, Висконсин), Bachem (Торранс, Калифорния), Sigma (Сент-Луис, Миссури), либо их можно получить способами, хорошо известными среднему специалисту в данной области, следуя методикам, описанным в таких обычных источниках, как Fieser и Fieser's Reagents for Organic Synthesis, тома 1-17, John Wiley and Sons, Нью-Йорк, НьюЙорк, 1991; Rodd's Chemistry of Carbon Compounds, тома 1-5 и доп., Elsevier Science Publishers, 1989; Organic Reactions, тома 1-40, John Wiley and Sons, Нью-Йорк, Нью-Йорк, 1991; March J.: Advanced OrganicChemistry, 4-e изд., John Wiley и Sons, Нью-Йорк, Нью-Йорк; и Larock: Comprehensive Organic Transformations, VCH Publishers, New York, 1989. Полные содержания всех документов, цитированных в настоящем изобретении, включены в данный патент посредством ссылки. Схемы синтеза соединений согласно настоящему изобретению. Соединения согласно настоящему изобретению можно синтезировать согласно схемам реакций,представленным ниже. Другие схемы реакций смогут легко разработать специалисты в данной области. Также должно быть очевидно, что множество различных растворителей, температур и других условий реакций можно изменять для оптимизирования выхода реакций. В реакциях, описанных далее, может потребоваться защита реакционноспособных функциональных групп, например гидрокси, амино, имино, тио или карбоксигрупп, если их присутствие желательно в конечном продукте, чтобы избежать их нежелательного участия в реакциях. Типичные защитные группы можно применять в соответствии со стандартной практикой, например, см. T.W. Greene и P.G.M. Wuts"Protective Groups in Organic Chemistry", John Wiley and Sons, 1991. Основные синтетические подходы для получения соединений согласно настоящему изобретению представлены на следующих схемах. Схема 1- 24019487 Как показано на схеме 1, соединение С получают путем восстановительного аминирования соединения 1 В соединением 1 А, применяя, например, триацетоксиборогидрид натрия или цианборогидрид натрия. В особых вариантах реализации Z1 представляет собой Me или Et; R6 представляет собой циклопентил, изопропил или 2-6-членный алкильный мостик, соединенный с R2 или R3 в Y; R2 и R3 в Y, каждый независимо, представляют собой Н, Me, Et или 2-6-членный алкильный мостик. В других особых вариантах реализации соединение 1 В представляет собой циклопентанон, циклогексанон или кетон. Схема 2 Как показано на схеме 2, соединение С получают путем присоединения по Михаэлю соединения 2 А(т.е. этилакрилата) к соединению 2 В (т.е. циклопропиламину или циклопентиламину) с последующим алкилированием посредством R5-Z3. Схема 3 Как показано на схеме 3, соединение 3 А превращают в соединение С, применяя соединение 3 В (т.е. циклопропиламин или циклопентиламин) в присутствии основания (т.е. K2CO3) и йодида натрия. Схема 4 Как показано на схеме 4, соединение С обрабатывают соединением 4 А в присутствии основания(т.е. K2CO3 или диизопропилэтиламин) с получением соединения 4 В. Соединение 4 В превращают путем восстановления, применяя восстановленное железо и последующую реакцию циклизации, с получением соединения 4 С. Соединение 4 Е получают путем N-алкилирования соединения 4 С соединением 4D (например, алкилгалогенидом (например, иодметаном. Соединение 4 Е обрабатывают соединением 4F в присутствии каталитического количества кислоты (т.е. конц. HCl или пиридинийхлорида) (приблизительно от 0,1 до 10 экв.) с получением соединения 4G. Соединение 4F представляет собой такое соединение, которое либо включает R7, если он желателен в конечном продукте, либо приводит к образованиюR7, если он желателен в конечном продукте. Как показано на схеме 5, соединение С обрабатывают соединением 5 А в присутствии основания(т.е. K2CO3 или диизопропилэтиламина) с получением соединения 5 В. Соединение 5 В превращают путем восстановления, применяя восстановленное железо и последующую реакцию циклизации, с получением соединения 5 С. Соединение 5 Е получают путем IV-алкилирования соединения 5 С алкилгалогенидом 5D(т.е. иодметаном). Соединение 5 Е обрабатывают анилином или бензиламином (соединение 5F, L =CHR14) в присутствии каталитического количества кислоты (т.е. конц. HCl или пиридинийхлорида) с получением соединения 5G. Схема 6 Реакцию сочетания соединения 6 А с амином (соединением 6 В, т.е. метиламином или 1 метилпиперидин-4-амином), с применением подходящих реагентов сочетания (т.е. HATU, TBTU и т.д.),осуществляют с получением соединения 6 С. Как показано на схеме 7, соединение 7 А обрабатывают дибензиламином (7 В) в этаноле с получением 7 С. Проводят реакцию Реформатского этилбромацетата (7D) с 7 С в присутствии цинковой пыли,триметилсилилхлорида с получением соединения 7 Е, которое подвергают гидрогенизации в присутствии палладиевого катализатора (т.е. Pd(OH)2 на углероде) с получением 7F. Восстановительное аминирование соединения 7F альдегидом или кетоном (т.е. циклопентаноном или циклогексаноном) в присутствии триацетоксиборогидрида натрия и ацетата натрия с получением 7G. Соединение 7G подвергают реакции нуклеофильного ароматического замещения (SNAr) с содержащим заместители пиримидином 7 Н (т.е. 2,4-дихлор-5-нитропиримидином) в присутствии основания (т.е. K2CO3) с получением соединения 7I,которое при восстановительной циклизации с применением металл-кислотного катализатора (т.е. Fe/HCl или Sn/HCl), позволяет получить соединение 7J. Соединение 7J кипятят с обратным холодильником вместе с соединением 7K (т.е. 4-амино-3-метоксибензойной кислотой), в присутствии кислотного катализатора (т.е. конц. HCl или TsOH), с получением соединения 7L, которое подвергают реакции сочетания с амином (т.е. метиламином или 1-метилпиперидин-4-амином) с получением соединения 7 М. Соединение 7N подвергают N-алкилированию, применяя алкилирующий агент (т.е. метилйодид), с- 27019487 получением соединения 7O. Соединение 7O кипятят с обратным холодильником вместе с соединением 7 Р (т.е. 4-амино-3-метоксибензойной кислотой), в присутствии кислотного катализатора (т.е. конц. HCl или TsOH), с получением соединения 7Q, которое подвергают воздействию амина (т.е. метиламина или 1-метилпиперидин-4-амина), применяя подходящие реагенты сочетания (т.е. HATU, TBTU и т.д.), с получением соединения 7R. Схема 8 Как показано на схеме 8, соединение 8 А обрабатывают основанием (т.е. метоксидом натрия) в метаноле с получением соединения 8 В, которое гидрогенируют в присутствии катализатора (т.е. Pd/C) с получением соединения 8 С. Соединение 8D кипятят с обратным холодильником вместе с соединением 8 С в присутствии кислотного катализатора (т.е. конц. HCl или TsOH), с получением соединения 8 Е. Соединение 8 Е подвергают конденсации с амином (т.е. метиламином или 1-метилпиперидин-4-амином),применяя подходящие реагенты сочетания (т.е. HATU, TBTU и т.д.), с получением соединения 8F. Схема 9 Как показано на схеме 9, соединение 9 А обрабатывают окисляющим агентом (например, перборатом натрия в уксусной кислоте) с получением соединения 9 В, которое превращают в его метиловый эфир, применяя основание (т.е. NaOMe) в метаноле с получением соединения 9 С. Соединение 9 С подвергают реакции нуклеофильного замещения в присутствии CuCN с получением соединения 9D, которое гидролизуют с получением кислоты 9 Е в присутствии сильной кислоты (т.е. конц. HCl). Соединение 9 Е- 28019487 гидрогенируют в присутствии катализатора (т.е. Pd/C) и уксусной кислоты в спирте, таком как метанол, с получением соединения 9F. Соединение 9F кипятят с обратным холодильником вместе с соединением 9G в присутствии кислотного катализатора (т.е. конц. HCl или TsOH), с получением соединения 9 Н. Соединение 9 Н обрабатывают амином (т.е. метиламином или 1-метилпиперидин-4-амином), применяя подходящие реагенты сочетания (т.е. HATU, TBTU и т.д.), с получением соединения 9I. Схема 10 Как показано на схеме 10, соединение 10 А подвергают реакции сочетания с производным пиперазина (т.е. бензил-4-аминопиперазин-1-карбоксилатом), применяя подходящие реагенты сочетания (т.е.HATU, TBTU и т.д.), с получением соединения 10 В. Соединение 10 В подвергают гидрогенизации для снятия защитной группы Cbz в присутствии катализатора (т.е. Pd-C) в спирте с получением соединения 10 С. Соединение 10 С алкилируют, применяя алкилгалогенид (т.е. этилбромид или изопропилбромид), в присутствии основания, такого как диизопропилэтиламид, с получением соединения 10D. Схема 11 Как показано на схеме 11, соединение 7 М подвергают О-алкилированию, применяя алкилирующий агент (т.е. метилйодид), с получением соединения 11 А.
МПК / Метки
МПК: C07D 487/04, C07D 487/14, A61P 11/00, A61P 37/08, A61K 31/4545
Метки: соединения, содержащие, фармацевтические, качестве, ингибиторов, композиции, применение
Код ссылки
<a href="https://eas.patents.su/30-19487-soedineniya-v-kachestve-ingibitorov-plk-farmacevticheskie-kompozicii-ih-soderzhashhie-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения в качестве ингибиторов plk, фармацевтические композиции, их содержащие, и их применение</a>
Предыдущий патент: Производные индол-2-она, двузамещенные в положении 3, их получение и их применение в терапии
Следующий патент: Ингибиторы limk2 и способы их применения
Случайный патент: Устройство и способ прессования упаковки