N-гидрокси-2-(алкил-, арил- или гетероарилсульфанил, -сульфинил или -сульфонил)-3-замещенные алкилов, арилов или гетероариламидов в качестве ингибиторов матриксных металлопротеиназ
Номер патента: 1742
Опубликовано: 27.08.2001
Авторы: Бэйкер Жанни Леа, Гросу Джордж Теодор, Венкатесан Аранапакам Мудумбай, Дэвис Жами Мари
Формула / Реферат
1. Соединения формулы I
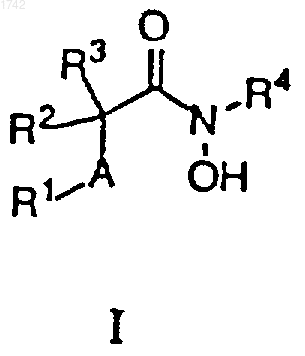
в которой
R1 представляет собой алкил из 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арил, содержащий 6-10 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
циклоалкил, содержащий 3-8 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный 5-10-членный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
или гетероарил-(СН2)0-6, в котором данная гетероарильная группа является 5-6-членной с одним или двумя гетероатомами, независимо выбранными из О, S и N, и необязательно может быть замещена одной или двумя группами, независимо выбранными из R5;
А представляет собой -S-, -SO- или SO2-;
R2 и R3, взятые с углеродным атомом, к которому они присоединены, образуют 5-7-членное гетероциклическое кольцо, содержащее О, S или N-R7, необязательно имеющее одну или две двойные связи;
R4 представляет собой водород,
алкил, содержащий 1-6 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
фенил или нафтил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
C3-С8циклоалкил или бициклоалкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный 5-10-членный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
R5 представляет собой С7-С11ароил, C2-C6алканоил, C1-C12алкил, C2-C12алкенил, C2-C12алкинил, F, Cl, Br, I, CN, СНО, C1-C6алкокси, арилокси, гетероарилокси, C3-С6алкенилокси, C3-С6алкинилокси, C1-С6алкоксиарил, C1-С6алкоксигетероарил, C1-C6-алкиламино-C1-C6
алкокси, C1-C2алкилендиокси, арилокси-C1-C6алкиламин, C1-C12перфторалкил, S(O)n-C1-C6алкил, S(O)n-арил, где n равно 0, 1 или 2; ОСОО-C1-C6алкил, ОСООарил, OCONR6, СООН, COO-C1-C6алкил, СООарил, CONR6R6, CONHOH, NR6R6, SO2NR6R6, NR6SO2арил, NR6CONR6R6, NHSO2CF3, SO2NH гетероарил, SО2NНСОарил, CONHSO2-C1-C6алкил, СОNНSO2арил, SO2NHCOapил, CONHSO2-C1-C6алкил, CONHSO2арил, NH2, ОН, арил, гетероарил, C3-С8циклоалкил, или насыщенный или ненасыщенный 5-10-членнный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7; где C1-C6алкил является линейным или разветвленным, гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу, имеющую 1-3 гетероатома, независимо выбранными из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, независимо выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси;
R6 представляет собой Н, C1-C18алкил, необязательно замещенный на ОН; C3-С6алкенил, C3-С6алкинил, C1-C6перфторалкил, S(O)n-C1-C6алкил, S(O)nарил, где n равно 0, 1 или 2; или СОгетероарил;
в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу, имеющую 1-3 гетероатома, независимо выбранных из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси; а
R7 представляет собой С7-С11ароил, C2-С6алканоил, C1-C12перфторалкил, S(O)n-C1-C6алкил, S(O)n-арил, где n равно 0, 1 или 2; COO-C1-C6алкил, СООарил, CONHR6, CONR6R6, CONHOH, SO2NR6R6, SO2CF3, SO2NHгетероарил, SO2NHCOapил, CONHSO-C1-C6алкил, СОNНSО2арил, арил или гетероарил; в котором арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси; а гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу, имеющую 1-3 гетероатома, независимо выбранных из О, S или N-C1-C6алкила;
алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арилалкил, содержащий 7-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5;
бифенилалкил, содержащий 13-18 углеродных атомов, в котором бифенил необязательно замещен одной или двумя группами, независимо выбранными из R5;
арилалкенил, содержащий 8-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5;
циклоалкилалкил или бициклоалкилалкил, содержащий 4-12 углеродных атомов, в котором циклоалкил или бициклоалкил, необязательно замещен одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или N-C1-C6алкила, необязательно замещенный одной или двумя группами, независимо выбранными из R5; или
R8R9N-С1-C6-алкоксиарил-С1-C6-алкил, где R8 и R9 независимо выбраны из C1-C6алкила или R8 и R9 вместе с азотюь образует 5-7-членное насыщенное гетероциклическое кольцо, необязательно содержащее атом кислорода, в котором данная арильная группа представляет собой фенил или нафтил;
или его фармацевтически приемлемую соль.
2. Соединение по п.1, где
R1 представляет собой алкил из 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арил, содержащий 6-10 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
циклоалкил, содержащий 3-8 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный моно- или бициклический 5-10-членный гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5; или
гетероарил-(СН2)0-6, в котором данная гетероарильная группа является 5-6-членной с одним или двумя гетероатомами, независимо выбранными из О, S и N, может быть необязательно замещена одной или двумя группами, независимо выбранными из R5;
А представляет собой -S-, -SO- или SO2-;
R2 и R3, взятые с углеродным атомом, к которому они присоединены, образуют 5-7-членное гетероциклическое кольцо, содержащее О, S или NR7, необязательно с одной или двумя двойными связями;
R4 представляет собой водород,
алкил, содержащий 1-6 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
фенил или нафтил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
C3-С8циклоалкил или бициклоалкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
R5 представляет собой Н, F, Cl, Br, I, CN, СНО, С7-С11ароил, C2-C6алканоил, C1-C12алкил, C2-C12алкенил, C2-C12алкинил, C1-C6алкокси, арилокси, гетероарилокси, C3-C6алкенилокси, C3-С6алкинилокси, C1-C6алкоксиарил, C1-C6алкоксигетероарил, С1-C6-алкиламино-С1-C6алкокси, C1-C2алкилендиокси, арилокси-С1-С6алкиламин, C1-C12перфторалкил, S(O)n-C1-C6алкил, S(O)n-арил, где n равно 0, 1 или 2; ОСОО-C1-C6алкил, ОСООарил, OCONR6, COOH, COO-C1-C6алкил, СООарил, CONR6R6, CONHOH, NR6R6, SO2NR6R6, NR6SO2apил, NR6CONR6R6, NНSО2СF3, SО2NНгетероарил, SО2NНСОарил, CONHSO2-C1-C6алкил, СОNНSО2арил, SO2NHCOapил, CONHSO2-C1-C6алкил, СОNНSО2арил, NH2, ОН, арил, гетероарил, C3-С8циклоалкил, или насыщенный или ненасыщенный 5-10-членнный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, независимо выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси;
R6 представляет собой Н, C1-C18алкил, необязательно замещенный на ОН; C3-С6алкенил, C3-C6алкинил, C1-C6перфторалкил, S(O)nалкил или арил, где n равно 0, 1 или 2; или СОгетероарил;
в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранную из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси; a
R7 представляет собой С7-С11ароил, C2-C6алканоил, C1-C12перфторалкил, S(O)n-алкил, S(O)n-арил, где n равно 0, 1 или 2; СОО-алкил, СООарил, CONHR6, CONR6R6, CONHOH, SО2NR6R6, SO2CF3, SO2NНгетероарил, SО2NНСОарил, СОNНSО2алкил, СОNНSО2 арил, арил или гетероарил; где C1-C6алкил является линейным или разветвленным, гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранных из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, С1-C6алкила, C1-C6алкокси или гидрокси;
алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арилалкил, содержащий 7-16 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
бифенилалкил, содержащий 13-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арилалкенил, содержащий 8-16 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
циклоалкилалкил или бициклоалкилалкил, содержащий 4-12 углеродных атомов, где циклоалкил или бициклоалкил, необязательно замещен одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или N-C1-C6алкила, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
R8R9N-C1-С6-алкоксиарил-С1-C6-алкил, где R8 и R9 независимо выбраны из C1-C6алкила или R8 и R9 вместе с азотом образует 5-7-членное насыщенное гетероциклическое кольцо, необязательно содержащее атом кислорода, в котором данная арильная группа представляет собой фенил или нафтил;
или его фармацевтически приемлемые соли.
3. Соединение по п.2, в котором
R1 представляет собой фенил, нафтил, алкшы, содержащий 1-18 углеродных атомов или гетероарил, такой как пиридил, тиенил, имидазолил или фуранил, необязательно замещенный C1-C6алкилом, C1-C6алкокси, С6-С10арилокси, гетероарилокси, C3-С6алкенилокси, C3-С6алкинилокси, галогеном; или S(O)n-С1-С6алкил C1-C6алкоксиарилом или C1-C6алкоксигетероарилом;
А представляет собой -S-, -SO- или SO2-;
R2 и R3, взятые с углеродным атомом, к которому они присоединены, образуют 5-7-членное гетероциклическое кольцо, содержащее О, S или N-R7, необязательно с одной или двумя двойными связями;
R4 представляет собой водород,
алкил, содержащий 1-6 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
фенил или нафтил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
C3-С8циклоалкил или бициклоалкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
R5 представляет собой Н, С7-С11ароил, С2-C6алканоил, C1-C12алкил, C2-C12алкенил, C2-C12алкинил, F, Cl, Br, I, CN, СНО, C1-C6алкокси, арилокси, гетероарилокси, C3-C6 алкенилокси, C3-С6алкинилокси, С1-C6-алкиламино-С1-С6алкокси, C1-С2-алкилендиокси, арилокси-C1-C6алкиламин, C1-C12перфторалкил, S(O)n-C1-C6алкил, S(O)n-арил, где n равно 0, 1 или 2; ОСОО-C1-C6алкил, ОСООарил, OCONR6, СООН, COO-C1-C6алкил, СООарил, CONR6R6, CONHOH, NR6R6, SO2NR6R6, NR6SO2арил, NR6CОNR6R6, NНSО2СF3, SО2NНгетероарил, SО2NНСОарил, CONHSO2-C1-C6алкил, СОNНSО2арил, SО2NНСОарил, CONHSO2-C1-C6алкил, СОNНSО2арил, NH2, ОН, арил, гетероарил, C3-С8циклоалкил; насыщенный или ненасыщенный 5-10-членный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, в котором C1-C6алкил является линейным или разветвленным, гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси;
R6 представляет собой Н, С1-С18алкил, необязательно замещенный на ОН; C3-С6алкенил, C3-C6алкинил, C1-C6перфторалкил, S(O)nалкил или арил, где n равно 0, 1 или 2; или СОгетероарил; в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранную из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси; а
R7 представляет собой С7-С11ароил, С2-C6алканоил, C1-C12перфторалкил, S(O)n-алкил, S(O)n-арил, где n равно 0, 1 или 2; СООалкил, СООарил, CONHR6, CONR6R6, CONHOH, SO2NR6R6, SО2СF3, SО2NНгетероарил, SО2NНСОарил, СОNНSО2алкил, СОNНSO2арил, арил, или гетероарил; где арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, независимо выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-С6алкокси или гидрокси; а гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранных из О, S или N-C1-C6 алкила;
алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арилалкил, содержащий 7-16 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
бифенилалкил, содержащий 13-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арилалкенил, содержащий 8-16 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
циклоалкилалкил или бициклоалкилалкил, содержащий 4-12 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR-C1-C6алкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
R8R9N-С1-C6-алкоксиарил-С1-C6-алкил, где R8 и R9 независимо выбраны из C1-C6алкила или R8 и R9 вместе с азотом образует 5-7-членное насыщенное гетероциклическое кольцо, необязательно содержащее атом кислорода, в котором данная арильная группа представляет собой фенил или нафтил;
и его фармацевтически приемлемые соли.
4. Соединение по п.1, которое представляет гидроксиамид 1-бензил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты или его фармацевтически приемлемую соль.
5. Соединение по п.1, которое представляет гидроксиамид 4-(4-метоксибензолсульфонил)-1-(3-метоксибензил)пиперидин-4-карбоновой кислоты или его фармацевтически приемлемую соль.
6. Соединение по п.1, которое представляет гидроксиамид 1-(3,4-дихлорбензил)-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты или его фармацевтически приемлемую соль.
7. Соединение по п.1, которое представляет гидроксиамид 4-(4-метоксибензолсульфонил)-1-(4-метилбензил)пиперидин-4-карбоновой кислоты или его фармацевтически приемлемую соль.
8. Соединение по п.1, которое представляет гидроксиамид 4-(4-метоксибензолсульфонил)-1-нафталин-2-илметилпиперидин-4-карбоновой кислоты или его фармацевтически приемлемую соль.
9. Соединение по п.1, которое представляет гидроксиамид 1-бифенил-4-илметил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты или его фармацевтически приемлемую соль.
10. Соединение по п.1, которое представляет гидроксиамид 4-(4-метоксибензолсульфонил)-1-(3-метилбут-2-енил)пиперидин-4-карбоновой кислоты или его фармацевтически приемлемую соль.
11. Соединение по п.1, которое представляет гидроксиамид 1-(4-бромобензил)-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты или его фармацевтически приемлемую соль.
12. Соединение по п.1, которое представляет гидроксиамид 4-(4-метоксибензолсульфонил)-1-[4-(2-пиперидин-1-ил-этокси)бензил]пиперидин-4-карбоновой кислоты или его фармацевтически приемлемую соль.
13. Соединение по п.1 или его фармацевтически приемлемая соль, которое представляет выбранное из группы соединений, состоящей из
гидроксиамид 4-(4-метокси-1-бензолсульфонил)-1-(3-фенилпропил)пиперидин-4-карбоновой кислоты,
гидроксиамид 1-трет-бутил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,
гидроксиамид 1-бутил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,
гидроксиамид 1-циклооктил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,
гидроксиамид 1-этил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,
гидроксиамид 1-изопропил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,
гидроксиамид 1-метил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,
гидроксиамид 1-бензил-4-(4-бутоксибензолсульфонил)пиперидин-4-карбоновой кислоты,
гидроксиамид 1-(4-фтор-бензил)-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,
гидроксиамид 1-(4-фтор-бензил)-4-(4-бутоксибензолсульфонил)пиперидин-4-карбоновой кислоты,
гидроксиамид 4-(4-метоксибензолсульфонил)-1-(4-метоксибензил)пиперидин-4-карбоновой кислоты,
гидроксиамид 4-(4-метоксибензолсульфонил)-1-[2-(4-метоксифенил)этил]пиперидин-4-карбоновой кислоты,
гидроксиамид 4-(4-метоксибензолсульфонил)-1-(2-фенилэтил)пиперидин-4-карбоновой кислоты,
гидроксиамид 4-(4-n-бутоксибензолсульфонил)-1-(4-метоксибензил)этил]пиперидин-4-карбоновой кислоты,
гидроксиамид 4-(4-метоксибензолсульфонил)-1-(3-феноксипропил)пиперидин-4-карбоновой кислоты,
гидроксиамид 4-(4-н-бутоксибензолсульфонил)-1-(3-феноксипропил)пиперидин-4-карбоновой кислоты,
гидроксиамид 4-(4-метоксибензолсульфонил)-1-(2-феноксиэтил)пиперидин-4-карбоновой кислоты,
гидроксиамид 4-(4-n-бутоксибензолсульфонил)-1-(2-феноксиэтил)пиперидин-4-карбоновой кислоты,
гидроксиамид 4-(4-метоксибензолсульфонил)-1-[4-(2-1-ил-этокси)бензил]пиперидин-4-карбоновой кислоты.
14. Способ ингибирования патологических изменений, опосредованных матриксными металлопротеиназами у млекопитающих, который включает введение млекопитающему необходимое ему терапевтически эффективное количество ингибирующего матриксную металлопротеиназу соединения формулы

в которой
R1 представляет собой алкил из 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арил, содержащий 6-10 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
циклоалкил, содержащий 3-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный моно- или бициклический 5-10-членный гетероцикл, содержащий один гетероатом, выбранный из O, S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5; или
гетероарил-(СН2)0-6, в котором данная гетероарильная группа является 5-6-членной с одним или двумя гетероатомами, независимо выбранными из О, S и N, может быть необязательно замещена одной или двумя группами, независимо выбранными из R5;
А представляет собой -S-, -SO- или SO2-;
R2 и R3, взятые с углеродным атомом, к которому они присоединены, образуют 5-7-членное гетероциклическое кольцо, содержащее О, S или N-R7, необязательно с одной или двумя двойными связями;
R4 представляет собой водород,
алкил, содержащий 1-6 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
фенил или нафтил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
C3-С8циклоалкил или бициклоалкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный моно- или бициклический 5-10-членный гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
R5 представляет собой Н, C7-C11ароил, С2-С6алканоил, C1-C12алкил, C2-C12алкенил, C2-C12алкинил, F, Cl, Br, I, CN, СНО, C1-C6алкокси, арилокси, гетероарилокси, C3-С6алкенилокси, C3-С6алкинилокси, C1-C6алкоксиарил, C1-C6алкоксигетероарил, C1-C6-алкиламино-C1-C6алкокси, C1-C2алкилендиокси, арилокси-С1-C6алкиламин, C1-C12перфторалкил, S(O)n-C1-C6алкил, S(O)n-арил, где n равно 0, 1 или 2; ОСОО-C1-C6алкил, ОСООарил, OCONR6, СООН, COO-C1-C6алкил, СООарил, CONR6R6, CONHOH, NR6R6, SO2NR6R6, NR6SO2apил, NR6CONR6R6, NHSO2CF3, SО2NНгетероарил, SО2NНСОарил, CONHSO2C1-C6алкил, СОNНSО2арил, SО2NНСОарил, CONHSO2-C1-C6алкил, СОNНSО2арил, NH2, ОН, арил, гетероарил, C3-С8циклоалкил, или насыщенный или ненасыщенный 5-10-членный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7; где C1-С6алкил является линейным или разветвленным, гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, независимо выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси;
R6 представляет собой Н, C1-C18алкил, необязательно замещенный на ОН; C3-C6алкенил, C3-С6алкинил, C1-C6перфторалкил, S(O)n-C1-C6алкил, S(O)nарил, где n равно 0, 1 или 2; или СОгетероарил;
в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранную из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси; а
R7 представляет сосющ С7-С11ароил, C2-C6алканоил, C1-C12перфторалкил, S(O)n-C1-C6алкил, S(O)n-арил, где n равен 0, 1 или 2; COO-C1-C6алкил, СООарил, CONHR6, CONR6R6, CONHOH, SO2NR6R6, SО2СF3, SO2NHгетероарил, SO2NHCOapил, CONHSO-C1-C6алкил, CONHSO2apил, арил или гетероарил; в котором арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси; а гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S, N-C1-C6алкила;
алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арилалкил, содержащий 7-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5;
бифенилалкил, содержащий 13-18 углеродных атомов, в котором бифенил необязательно замещен одной или двумя группами, независимо выбранными из R5;
арилалкенил, содержащий 8-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5;
циклоалкилалкил или бициклоалкилалкил, содержащий 4-12 углеродных атомов, в котором циклоалкил или бициклоалкил, необязательно замещен одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или N-C1-C6алкила, необязательно замещенный одной или двумя группами, независимо выбранными из R5; или
R8R9N-С1-С6-алкоксиарил-С1-C6-алкил, где R8 и R9 независимо выбраны из C1-C6алкила или R8 и R9 вместе с азотом образует 5-7-членное насыщенное гетероциклическое кольцо, необязательно содержащее атом кислорода, в котором данная арильная группа представляет собой фенил или нафтил;
и его фармацевтически приемлемую соль.
15. Способ по п.14, в котором заболевание, которое лечат, представляет собой атеросклероз, образование атеросклеротической бляшки, уменьшение коронарного тромбоза от разрыва атеросклеротической бляшки, рестеноз, опосредуемое ММР нарушение остеогенеза, воспалительные заболевания центральной нервной системы, старение кожи, рост злокачественной опухоли, остеоартрит, ревматоидный артрит, септический артрит, изъязвление роговицы, аномальное раневое заживление, костное заболевание, протеинурию, заболевание аневризма аорты, утрату перерожденного хряща после повреждения сустава, демиелинизирующие заболевания нервной системы, цирроз печени, гломерулярное заболевание почек, преждевременное разрушение плодных оболочек, заболевание воспаление пищеварительного тракта или периодонтальное заболевание.
16. Способ по п.14, в котором заболевание, которое лечат, представляет собой связанную с возрастом дегенерацию желтого пятна, диабетическую ретинопатию, пролиферативную витреоретинопатию, раннюю ретинопатию, глазное воспаление, кератоконус, Sjogren's синдром,миопию, злокачественные опухоли глаза, ангиогенез/реваскуляризацию сосудов глаза и отторжение роговичного имплантата.
17. Способ подавления патологических изменений, опосредованных ФНО-a превращающим ферментом (ФАПФ) млекопитающих, который включает введение млекопитающему, нуждающемуся в нем, терапевтически эффективного количества соединения ингибирующего ФАПР указанной формулы
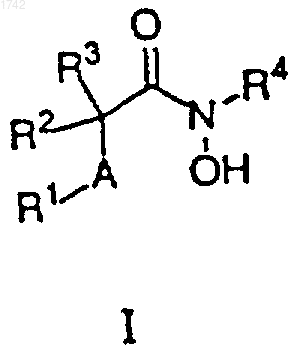
где R1 представляет собой алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арил, содержащий 6-10 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
циклоалкил, содержащий 3-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный 5-10 членный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5; или
гетероарил-(СН2)0-6, в котором данная гетероарильная группа является 5-6-членной гетероарильной группой с одним или двумя гетероатомами, независимо выбранными из О, S и N, который может быть необязательно замещен одной или двумя группами, независимо выбранными из R5;
А представляет собой -S-, -SO- или SO2-;
R2 и R3, взятые с углеродным атомом, к которому они присоединены, образуют 5-7-членное гетероциклическое кольцо, содержащее О, S или N-R7, необязательно имеющее одну или две двойные связи;
R4 представляет собой водород,
алкил, содержащий 1-6 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
фенил или нафтил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
C3-С8циклоалкил или бициклоалкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный 5-10-членный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
R5 представляет собой Н, С7-С11ароил, С2-С6алканоил, C1-C12алкил, C2-C12алкенил, С2-С12алкинил, F, Cl, Br, I, CN, СНО, C1-C6алкокси, арилокси, гетероарилокси, C3-С6алкенилокси, C3-С6алкинилокси, C1-C6алкоксиарил, C1-C6алкоксигетероарил, С1-C6алкиламино-C1-С6алкокси, C1-C2алкилендиокси, арилокси-C1-C6алкиламин, C1-C12перфторалкил, S(O)n-C1-C6алкил, S(O)n-арил, где n равно 0, 1 или 2; ОСОО-C1-C6алкил, ОСООарил, OCONR6, COOH, COO-C1-C6алкил, СООарил, CONR6R6, CONHOH, NR6R6, SO2NR6R6, NR6SO2apил, NR6CONR6R6, NHSO2CF3, SО2NНгетероарил, SО2NНСОарил, CONHSO2-C1-C6алкил, СОNНSО2арил, SО2NНСОарил, CONHSO2-C1-C6алкил, СОNНSО2арил, NH2, ОН, арил, гетероарил, C3-С8циклоалкил, или насыщенный или ненасыщенный 5-10-членнный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7; где C1-C6алкил является линейным и разветвленным, гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, независимо выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси;
R6 представляет собой Н, C1-C18алкил, необязательно замещенный на ОН; C3-С6алкенил, C3-С6алкинил, C1-С6перфторалкил, S(O)n-C1-С6алкил, S(O)nарил, где n равно 0, 1 или 2; или СОгетероарил; в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранную из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси; а
R7 представляет собой С7-С11ароил, C2-C6алканоил, C1-C12перфторалкил, S(O)n-C1-C6алкил, S(O)n-арил, где n равен 0, 1 или 2; COO-C1-C6алкил, СООарил, CONHR6, CONR6R6, CONHOH, SO2NR6R6, SO2CF3, SО2NНгетероарил, SO2NНСОарил, CONHSO-C1-C6алкил, СОNНSО2арил, арил или гетероарил; в котором арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, независимо выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси; а гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S, N-C1-C6алкила;
алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арилалкил, содержащий 7-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5;
бифенилалкил, содержащий 13-18 углеродных атомов, в котором бифенил необязательно замещен одной или двумя группами, независимо выбранными из R5;
арилалкенил, содержащий 8-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5;
циклоалкилалкил или бициклоалкилалкил, содержащий 4-12 углеродных атомов, в котором циклоалкил или бициклоалкил необязательно замещен одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или N-C1-C6алкила, необязательно замещенный одной или двумя группами, независимо выбранными из R5; или
R8R9N-С1-C6-алкоксиарил-C1-C6-алкил, где R8 и R9 независимо выбраны из C1-C6алкила или R8 и R9 вместе с азотом образует 5-7-членное насыщенное гетероциклическое кольцо, необязательно содержащее атом кислорода, в котором арильная группа представляет собой фенил или нафтил;
и его фармацевтически приемлемую соль.
18. Способ по п.14, а котором заболевание, которое лечат, представляет собой ревматоидные артриты, отторжение трансплантанта, кахексию, анорексию, воспаление, лихорадку, устойчивость к инсулину, септический шок, застойную сердечную недостаточность, воспалительное заболевание центральной нервной системы, воспалительное заболевание пищеварительного тракта или ВИЧ инфекцию.
19. Фармацевтическая композиция, включающая фармацевтический носитель и терапевтически эффективное количество ингибирующего матриксную металлопротеиназу или ФАПФ соединения формулы
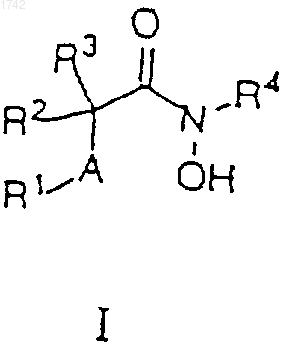
в которой
R1 представляет собой алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арил, содержащий 6-10 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
циклоалкил, содержащий 3-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный 5-10-членный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
или гетероарил-(СН2)0-6, в котором данная гетероарильная группа является 5-6-членной с одним или двумя гетероатомами, независимо выбранными из О, S и N, который может быть необязательно замещен одной или двумя группами, независимо выбранными из R5;
А представляет собой -S-, -SO- или SO2-;
R2 и R3, взятые с углеродным атомом, к которому они присоединены, образуют 5-7-членное гетероциклическое кольцо, содержащее О, S или N-R7, необязательно с одной или двумя двойными связями;
R4 представляет собой водород,
алкил, содержащий 1-6 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
фенил или нафтил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
C3-С8циклоалкил или бициклоалкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный 5-10-членный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
R5 представляет собой Н, С7-С11ароил, С2-С6алканоил, C1-C12алкил, C2-C12алкенил, C2-C12алкинил, F, Cl, Br, I, CN, СНО, C1-C6алкокси, арилокси, гетероарилокси, C3-С6алкенилокёш, C3-С6алкинилокси, C1-C6алкоксиарил, C1-C6алкоксигетероарил, C1-С6-алкиламино-C1-С6алкокси, C1-C2алкилендиокси, арилокси-C1-C6алкиламин, C1-C12перфторалкил, S(O)n-C1-C6алкил, S(O)n-арил, где n равно 0, 1 или 2; ОСОО-C1-C6алкил, ОСООарил, OCONR6, COOH, COO-C1-C6алкил, СООарил, CONR6R6, CONHOH, NR6R6, SO2NR6R6, NR6SО2арил, NR6CONR6R6, NHSO2CF3, SO2NHгетероарил, SО2NНСОарил, CONHSO2-C1-C6алкил, СОNНSО2арил, SО2NНСОарил, CONHSO2-C1-C6алкил, CONHSO2арил, NH2, ОН, арил, гетероарил, C3-С8циклоалкил, или насыщенный или ненасыщенный 5-10-членнный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7; в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, независимо выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси;
R6 представляет собой Н, C1-C18алкил, необязательно замещенный на ОН; C3-C6алкенил, C3-C6алкинил, C1-C6перфторалкил, S(O)n-C1-C6алкил-S(O)nарил, где n равно 0, 1 или 2; или СОгетероарил; в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранную из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси; a
R7 представляет собой С7-С11ароил, C2-C6алканоил, C1-C12перфторалкил, S(O)n-C1-C6алкил, S(O)n-арил, где n равно 0, 1 или 2; COO-C1-C6алкил, СООарил, CONHR6, CONR6R6, CONHOH, SO2NR6R6, SO2CF3, SО2NHгетероарил, SО2NНСОарил, CONHSO-C1-C6алкил, СОNНSО2арил, арил или гетероарил; в котором арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6алкила, C1-C6алкокси или гидрокси; а гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S или N-C1-C6алкила;
алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5;
арилалкил, содержащий 7-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5;
бифенилалкил, содержащий 13-18 углеродных атомов, в котором бифенил необязательно замещен одной или двумя группами, независимо выбранными из R5;
арилалкенил, содержащий 8-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5;
циклоалкилалкил или бициклоалкилалкил, содержащий 4-12 углеродных атомов, в котором циклоалкил или бициклоалкил, необязательно замещен одной или двумя группами, независимо выбранными из R5;
насыщенный или ненасыщенный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или N-C1-C6алкила, необязательно замещенный одной или двумя группами, независимо выбранными из R5; или
R8R9N-С1-C6-алкоксиарил-С1-C6-алкил, где R8 и R9 независимо выбраны из C1-C6алкила или R8 и R9 вместе с азотом образует 5-7-членное насыщенное гетероциклическое кольцо, необязательно содержащее атом кислорода, в котором данная арильная группа представляет собой фенил или нафтил;
и его фармацевтически приемлемую соль.
Текст
1 Матриксные металлопротеиназы (MMPs) представляют собой группу ферментов, которые вовлечены в патологическое разрушение соединительной ткани и базальных мембран. Эти содержащие цинк эндопептидазы состоят из нескольких подгрупп ферментов, включающих коллагеназы, стромелизины и желатиназы. Было показано, что среди этих видов желатиназы более всего вовлечены в рост и распространение злокачественных опухолей. Известно, что уровень экспрессии желатиназы повышается со злокачественностью и что желатиназа может разрушать базальную мембрану, что ведет к метастазам опухоли. Недавно было показано,что ангиогенез, необходимый для роста солидных опухолей, обладает желатиназным компонентом в своей патологии. Более того, существует доказательство, которое предполагает, что желатиназа участвует в разрыве бляшки, ассоциированной с атеросклерозом. Другие состояния, опосредуемые MMPs, представляют собой рестеноз, опосредуемое ММР нарушение остеогенеза, воспалительные заболевания центральной нервной системы, старение кожи, рост злокачественной опухоли, остеоартрит, ревматоидный артрит, септический артрит, изъязвление роговицы, аномальное раневое заживление, костное заболевание, протеинурия, заболевание аневризма аорты, утрата перерожденного хряща после повреждения сустава, демиелинизирующие заболевания нервной системы, цирроз печени, гломерулярное заболевание почек, преждевременное разрушение плодных оболочек,заболевание воспаление пищеварительного тракта, периодонтальное заболевание, связанная с возрастом дегенерация желтого пятна, диабетическая ретинопатия, пролиферативная витреоретинопатия, ранняя ретинопатия, глазное воспаление, кератоконус, Sjogren's синдром, миопия, злокачественные опухоли глаза, ангиогенез/реваскуляризация сосудов глаза и отторжение роговичного имплантата. Что касается последних обзоров, см.: (1) Recent Advances inTNF-, связанного с мембраной. TNF- представляет собой провоспалительный цитокин,который, как полагают, выполняет свою функцию при ревматоидном артрите, септическом шоке, отторжении имплантата, кахексии, анорексии, воспалении, застойной сердечной недостаточности, воспалительном заболевании 2 центральной нервной системы, воспалительном заболевании пищеварительного тракта, инсулиновой резистентности и HIV-инфекции, помимо его собственных хорошо освещенных противоопухолевых свойств. Например, изучение антител к TNFантителам и трансгенных животных показало, что блокирование образованияTNF- подавляет развитие артрита. Данное наблюдение недавно было распространено также и на людей. Предполагается, что небольшие молекулы ингибиторов MMPs и ТАСЕ обладают, по этой причине, возможностью для лечения ряда болезненных состояний. Хотя был идентифицирован и описан в литературе ряд ингибиторов ММР и ТАСЕ, большинство этих молекул представляют собой пептидные и пептидоподобные соединения, которые, как и следовало ожидать,биодоступны и обладают фармакокинетическими затруднениями, обычными для таких соединений, которые ограничивают их клиническую эффективность. Низкомолекулярные, сильные,длительного действия, перорально биодоступные ингибиторы MMPs и/или ТАСЕ являются,следовательно, очень желательными для потенциального постоянного лечения вышеупомянутых болезненных состояний. В последнее время появились две ссылки(Патент США 5455258 и Европейская патентная заявка 606046), которые описывают арилсульфонамидозамещенные гидроксамовые кислоты. В данных документах рассматриваются соединения, проиллюстрированные на примере CGS 27023A. В них представлены только ингибиторы непептидноматричных металлопротеиназ,описанных к настоящему времени.Salah с соавт., Liebigs Ann. Chem. 195,(1973) описали некоторые производные арилзамещенных тио- и арилзамещенных сульфонильных ацетогидроксамовой кислоты общей формулы 1. Данные соединения были получены для изучения реакции Манниха. Впоследствии они были протестированы на их фунгицидную активность. 3 Некоторые сульфонкарбоновые кислоты описаны в патенте США 4933367. Было показано, что эти соединения проявляют гипогликемическую активность. Настоящее изобретение относится к новым, низкомолекулярным, непептидным ингибиторам матричных металлопротеиназ (MMPs) и TNFпревращающего фермента (ТАСЕ),предназначенных для лечения артрита, опухолевых метастазов, тканевого изъязвления, аномального раневого заживления, периодонтального заболевания, костного заболевания, диабетов (инсулиновая резистентность) и HIVинфекции. В соответствии с настоящим изобретением предлагается группа соединений общей формулы I где R1 представляет собой алкил, содержащий 118 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; арил, содержащий 6-10 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; циклоалкил, содержащий 3-8 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; насыщенный или ненасыщенный 5-10 членный моно- или бициклический гетероцикл,содержащий один гетероатом, выбранный из О,S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5; или гетероарил-(СН 2)0-6-, в котором гетероарильная группа является 5-6-членной с одним или двумя гетероатомами, независимо выбранными из О, S и N, и необязательно может быть замещена одной или двумя группами, независимо выбранными из R5; А представляет собой -S-, -SO- или -SO2-;R2 и R3, взятые с углеродным атомом, к которому они присоединены, образуют 5-7 членное гетероциклическое кольцо, содержащее О, S или NR7, необязательно с одной или двумя двойными связями; 4 алкил, содержащий 1-6 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; фенил или нафтил, необязательно замещенный одной или двумя группами, независимо выбранными из R5; С 3-С 8 циклоалкил или бициклоалкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5; насыщенный или ненасыщенный 5-10 членный моно- или бициклический гетероцикл,содержащий один гетероатом, выбранный из О,S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5;C1-C6 алкил, СООарил, CONR6R6, CONHOH,NR6R6, SO2NR6R6, NR6SO2apил, -NR6CONR6R6,NHSO2CF3, SO2NНгетероарил, SO2NHCOapил,CONHSO2apил,CON-HSO2-C1-C6 алкил,SO2NНСОарил, CONHSO2-C1-C6-алкил, CONHSO2aрил, NH2, ОН, арил, гетероарил, C3C8 циклоалкил; или насыщенный или ненасыщенный 5-10-членный моно- или бициклический гетероцикл, содержащий один гетероатом,выбранный из О, S или NR7, в котором C1-C6 алкил является линейным или разветвленным,гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6 алкил, C1C6 алкокси, или гидрокси;R6 представляет собой Н, C1-C18 алкил, необязательно замещенный на ОН; C3-C6 алкенил,C3-С 6 алкинил, C1-C6 перфторалкил, S(O)n-C1-C6 алкил S(O)nарил, где n равно 0, 1 или 2; или СОгетероарил, в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами,независимо выбранными из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбран 5 ными из галогена, циано, амино, нитро, C1C6 алкила, C1-C6 алкокси, или гидрокси; а R7 представляет собой С 7-С 11 ароил, С 2-C6 алканоил, C1-C12 перфторалкил, S(О)n-C1-C6 алкил, S(O)nарил, где n равно 0, 1 или 2; COOC1-C6 алкил, СООарил, CONHR6, CONR6R6,CONHOH, SO2NR6R6, SO2 СF3, SO2NHгетероарил, SO2NHCOapил, CONHSO-C1-C6 арил,CONHSO2apил или гетероарил, где арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, независимо выбранными из галогена, циано, амино, нитро,C1-C6 алкила, C1-C6 алкокси, или гидрокси; а гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу,обладающую 1-3 гетероатомами, независимо выбранными из О, S или N-C1-C6 алкила; алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; арилалкил, содержащий 7-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5; бифенилалкил, содержащий 13-18 углеродных атомов, в котором бифенил необязательно замещен одной или двумя группами, независимо выбранными из R5; арилалкенил, содержащий 8-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5; циклоалкилалкил или бициклоалкилалкил,содержащий 4-12 углеродных атомов, в котором циклоалкильная или бициклоалкильная группа необязательно замещена одной или двумя группами, независимо выбранными из R5; насыщенный или ненасыщенный моноили бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или N-C1C6 алкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5; илиR и R9 независимо выбраны из C1-C6 алкила илиR8 и R9 вместе с азотом образуют 5-7-членное насыщенное гетероциклическое кольцо, необязательно содержащее атом кислорода, в котором данная арильная группа представляет собой фенил или нафтил; и его фармацевтически приемлемые соли. Более предпочтительными соединениями настоящего изобретения является группа соединений общей формулы (Iа)R1 представляет собой алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; арил, содержащий 6-10 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; циклоалкил, содержащий 3-8 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; насыщенный или ненасыщенный моноили бициклический 5-10 членный гетероцикл,содержащий один гетероатом, выбранный из О,S или NR7, необязательно замещенный одной или двумя группами, независимо выбранными из R5; или гетероарил-(СН 2)0-6, в котором данная гетероарильная группа является 5-6-членной с одним или двумя гетероатомами, независимо выбранными из О, S и N, может быть необязательно замещена одной или двумя группами,независимо выбранными из R5; А представляет собой -S-, -SO- или SO2-;R2 и R3, взятые с углеродным атомом, к которому они присоединены, образуют 5-7 членное гетероциклическое кольцо, содержащее О, S или N-R7, необязательно имеющее одну или две двойные связи;R4 представляет собой водород,алкил, содержащий 1-6 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; фенил или нафтил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;C3-С 8 циклоалкил или бициклоалкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;C2-C12 алкенил, C2-C12 алкинил, C1-C6 алкокси,арилокси, гетероарилокси, C3-C6 алкенилокси,C3-С 6 алкинилокси, C1-C6 алкоксиарил, C1-C6 алкоксигетероарил, С 1-C6-алкиламино-С 1-C6 алкокси, C1-С 2-алкилендиокси, арилокси-С 1-C6 алкиламин, C1-C12 перфторалкил, S(O)n-C1-C6 алкил, S(O)n-арил, где n равно 0, 1 или 2; OCOOC1-C6 алкил, ОСООарил, OCONR6, COOH, COOC1-C6 алкил, СООарил, CONR6R6, CONHOH,NR6R6, SO2NR6R6, NR6SO2apил, NR6CONR6R6,NHSO2CF3, SО 2NНгетероарил, SO2NНСОарил,CONHSO2-C1-C6 алкил,СОNНSО 2 арил,SО 2NНСОарил,CONHSO2-C1-C6 алкил,СОNНSО 2 арил, NH2, ОН, арил, гетероарил, C3 С 8 циклоалкил; или насыщенный или ненасыщенный 5-10-членный моно- или бициклический гетероцикл, содержащий один гетероатом,выбранный из О, S или NR7; в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, независимо выбранными из галогена,циано, амино, нитро, C1-C6 алкила, C1-C6 алкокси,или гидрокси;R6 представляет собой Н, C1-C18 алкил, необязательно замещенный на ОН; C3-C6 алкенил,C3-C6 алкинил, C1-C6 перфторалкил, S(O)nалкил или арил, где n равно 0, 1 или 2; или СОгетероарил; в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранную из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6 алкила, C1-C6 алкокси или гидрокси; аR7 представляет собой С 7-С 11 ароил, С 2C6 алканоил, C1-C12 перфторалкил, S(O)n-алкил,S(O)n-арил, где n равен 0, 1 или 2; СООалкил,СООарил, CONHR6, CONR6R6, CONHOH,SO2NR6R6,SO2 СF3,SO2NHгетероарил,SO2NHСОарил, СОNНSО 2 алкил, СONНSO2 арил, гетероарил; в котором C1-C6 алкил является линейным или разветвленным, гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранную из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано,амино, нитро, C1-C6 алкила, C1-C6 алкокси, или гидрокси; алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; 8 алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; арилалкил, содержащий 7-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5; бифенилалкил, содержащий 13-18 углеродных атомов, в котором бифенил необязательно замещен одной или двумя группами, независимо выбранными из R5; арилалкенил, содержащий 8-16 углеродных атомов, в котором арил необязательно замещен одной или двумя группами, независимо выбранными из R5; циклоалкилалкил или бициклоалкилалкил,содержащий 4-12 углеродных атомов, в котором циклоалкил или бициклоалкил необязательно замещен одной или двумя группами, независимо выбранными из R5; насыщенный или ненасыщенный моноили бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или N-C1C6 алкила, необязательно замещенный одной или двумя группами, независимо выбранными из R5;R и R9 независимо выбраны из C1-C6 алкила илиR8 и R9 вместе с азотом образует 5-7-членное насыщенное гетероциклическое кольцо, необязательно содержащее атом кислорода, в котором данная арильная группа представляет собой фенил или нафтил; и его фармацевтически приемлемую соль. Наиболее предпочтительной группой соединений являются соединения с нижеследующей формулой (Ib)R1 представляет собой фенил, нафтил, алкил, содержащий 1-18 углеродных атомов или гетероарил, такой как пиридил, тиенил, имидазолил или фуранил, необязательно замещенныйR2 и R3, взятые с углеродным атомом, к которому они присоединены, образуют 5-7 членное гетероциклическое кольцо, содержащее О, S или NR7, необязательно имеющее одну или две двойные связи;R4 представляет собой водород, 9 алкил, содержащий 1-6 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкенил, содержащий 3-18 углеродных атомов с 1-3 двойными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкинил, содержащий 3-18 углеродных атомов с 1-3 тройными связями, необязательно замещенный одной или двумя группами, независимо выбранными из R5; фенил или нафтил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;C3-C8 циклоалкил или бициклоалкил, необязательно замещенный одной или двумя группами, независимо выбранными из R5;C1-C6 алкил, СООарил, CONR6R6, CONHOH,NR6R6, SO2NR6R6, NR6SO2apил, -NR6 СONR6R6,NHSO2CF3, SO2NНгетероарил, SO2NHCOapил,CONHSO2-C1-C6 алкил,СОNНSO2 арил,CONHSO2-C1-C6 алкил,SO2NHCOapил,СОNНSO2 арил, NH2, ОН, арил, гетероарил, C3 С 8 циклоалкил; насыщенный или ненасыщенный 5-10-членный моно- или бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR7, в котором C1-C6 алкил является линейным или разветвленным, гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранными из О, S илиNR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино,нитро, C1-C6 алкила, C1-C6 алкокси; или гидрокси;R6 представляет собой Н, C1-C18 алкил, необязательно замещенный на ОН; C3-C6 алкенил,C3-C6 алкинил, C1-C6 перфторалкил, S(O)nалкил или арил, где n равно 0, 1 или 2; или СОгетероарил; в котором гетероарил представляет собой 5-10-членную моно- или бициклическую гетероарильную группу с 1-3 гетероатомами, независимо выбранную из О, S или NR7, а арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, выбранными из галогена, циано, амино, нитро, C1-C6 алкила, C1-C6 алкокси, или гидрокси; аSO2NНСОарил, СОNНSО 2 алкил, СОNНSО 2 арил, арил или гетероарил; где арил представляет собой фенил или нафтил, необязательно замещенный 1 или 2 группами, независимо выбранными из галогена, циано, амино, нитро, C1C6 алкила, C1-C6 алкокси, или гидрокси; а гетероарил представляет собой 5-10-членную моноили бициклическую гетероарильную группу с 13 гетероатомами, независимо выбранную из О,S или N-C1-C6 алкила; алкил, содержащий 1-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкенил, содержащий 3-18 углеродных атомов с 1-3 двойных связей, необязательно замещенный одной или двумя группами, независимо выбранными из R5; алкинил, содержащий 3-18 углеродных атомов с 1-3 тройных связей, необязательно замещенный одной или двумя группами, независимо выбранными из R5; арилалкил, содержащий 7-16 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; бифенилалкил, содержащий 13-18 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; арилалкенил, содержащий 8-16 углеродных атомов, необязательно замещенный одной или двумя группами, независимо выбранными из R5; циклоалкилалкил или бициклоалкилалкил,содержащий 4-12 углеродных атомов, необязательно замещенный одной или двумя группами,независимо выбранными из R5; насыщенный или ненасыщенный моноили бициклический гетероцикл, содержащий один гетероатом, выбранный из О, S или NR-C1C6 алкил, необязательно замещенный одним или двумя группами, независимо выбранными из R5;R и R9 независимо выбраны из C1-C6 алкила илиR8 и R9 вместе с азотом образует 5-7-членное насыщенное гетероциклическое кольцо, необязательно содержащее атом кислорода, в котором данная арильная группа представляет собой фенил или нафтил; и его фармацевтически приемлемые соли. Наиболее предпочтительные соединения настоящего изобретения, ингибирующие матриксную металлопротеиназу и ТАСЕ, представляют собой гидроксиамид 1-бензил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 4-(4-метоксибензолсульфонил)-1-(3-метоксибензил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-(3,4-дихлорбензил)-4-(4 метоксибензолсульфонил)пиперидин-4-карбоновой кислоты, 11 гидроксиамид 4-(4-метоксибензолсульфонил)-1-(4-метилбензил)пиперидин-4-карбоновой кислоты,гидроксиамид 4-(4-метоксибензолсульфонил)-1-нафталин-2-ил-метилпиперидин-4-карбоновой кислоты,гидроксиамид 1-бифенил-4-илметил-4-(4 метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 4-(4-метоксибензолсульфонил)-1-(3-метилбут-2-енил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-(4-бромобензил)-4-(4 метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 4-(4-метоксибензолсульфонил)-1-(3-фенилпропил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-трет-бутил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-бутил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-циклооктил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-этил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-изопропил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-метил-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-бензил-4-(4-бутоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-(4-фторобензил)-4-(4 метоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 1-(4-фторобензил)-4-(4 бутоксибензолсульфонил)пиперидин-4-карбоновой кислоты,гидроксиамид 4-(4-метоксибензолсульфонил)-1-(4-метоксибензил)пиперидин-4 карбоновой кислоты,гидроксиамид 4-(4-метоксибензолсульфонил)-1-[2-(4-метоксифенил)этил]пиперидин-4 карбоновой кислоты,гидроксиамид 4-(4-метоксибензолсульфонил)-1-(2-фенилэтил)пиперидин-4-карбоновой кислоты,гидроксиамид 4-(4-п-бутоксибензолсульфонил)-1-(4-метоксибензил)этил]пиперидин-4 карбоновой кислоты,гидроксиамид 4-(4-метоксибензолсульфонил)-1-(3-феноксипропил)пиперидин-4-карбоновой кислоты,гидроксиамид 4-(4-п-бутоксибензолсульфонил)-1-(3-феноксипропил)пиперидин-4 карбоновой кислоты, 001742 12 гидроксиамид 4-(4-метоксибензолсульфонил)-1-(2-феноксиэтил)пиперидин-4-карбоновой кислоты,гидроксиамид 4-(4-п-бутоксибензолсульфонил)-1-(2-феноксиэтил)пиперидин-4-карбоновой кислоты,гидроксиамид 4-(4-метоксибензолсульфонил)-1-[4-(2-пиперидин-1-ил-этокси)бензил]пиперидин-4-карбоновой кислоты. Необходимо иметь ввиду, что определение соединений формул I, If и Ib, когда R1, R2, R3 иR4 содержат асимметричные углероды, охватывают все возможные стереоизомеры и их смеси,которые обладают обсуждаемой ниже активностью. В частности, они охватывают рацемические модификации и любые оптические изомеры, которые обладают вышеуказанной активностью. Оптические изомеры могут быть получены в чистом виде с помощью стандартных методик разделения. Если не указано иначе, термин "алкил" относится к линейной или разветвленной алкильной группе C1-C6, арильная представляет собой фенил или нафтил. Фармацевтически приемлемые соли представляют собой соли, полученные с фармацевтически приемлемыми органическими и неорганическими кислотами, такими как молочная, лимонная, уксусная,винокаменная, янтарная, малеиновая, малоновая, хлористо-водородная, бромисто-водородная, фосфорная, азотная, серная, метансульфоновая, и известные аналогичные приемлемые кислоты. В соответствии с этим, в настоящем изобретении предлагается фармацевтическая композиция, которая включает соединение настоящего изобретения в сочетании или в ассоциации с фармацевтически приемлемым носителем. В частности, настоящее изобретение относится к фармацевтической композиции, которая включает эффективное количество соединения настоящего изобретения и фармацевтически приемлемый носитель. Созданные композиции предпочтительно адаптированы для перорального введения. Однако они могут быть приспособлены для других режимов введения, например, для парентерального введения пациентам. Для того чтобы достичь постоянства при введении, предпочтительно, чтобы любая композиция настоящего изобретения представляла собой форму единичной дозы. Соответствующие формы единичной дозы включают таблетки, капсулы и порошки в пакетах-саше и флаконах. Такие формы единичной дозы могут содержать от 0,1 до 100 мг любого соединения настоящего изобретения. Соединения настоящего изобретения могут быть введены перорально в дозе в интервале от 0,01 до 100 мг на кг. Такая композиция может быть введена от 1 до 6 раз в день, обычно 1-4 раза в день. Композиции в соответствии с изобретением могут быть приготовлены с обычными экс 13 ципиентами, такими как наполнители, дезинтеграторы, связующие агенты, лабриканты, вкусовые агенты и подобные. Они готовятся обычным образом. Настоящее изобретение также относится к способу получения соединений согласно изобретению. Способ согласно изобретению. Соединения согласно настоящему изобретению могут быть получены согласно одному из основных способов, данных ниже. Соответствующее замещенное производное меркантана алкилируют, используя или замещенным (схема 1), или незамещенным (схема 2) эфир -бромуксусной кислоты в кипящем ацетоне, используя К 2 СО 3 в количестве основания, полученное таким образом сульфидное производное окисляли м-хлорпербензойной кислотой в CH2Cl2 или используя Оксон в смеси метанол/вода. Сульфон, полученный вышеуказанным образом, далее может быть либо алкилирован, используя различные галоидные алкилы, с получением дизамещенных производных,либо он может быть гидролизован, используяNaOH/MeOH при комнатной температуре. Далее, полученную карбоновую кислоту превращают в производное гидроксамовой кислоты путем взаимодействия со смесью оксаленхлорид/ДМХ (каталитически). И гидроксиламин/триэтиламин. Схема 1 Синтез:f. (CDCl)2/CH2Cl2/Et3N/NH2OHCl. Как изложено вкратце на схеме 3, сульфидное производное может быть дополнительно алкилировано с использованием литийбис(триметилсилил)амида в ТГФ при 0 С. Данное алкилированное или монозамещенное соединение гидролизовали и преобразовывали в производное гидроксамовой кислоты. Сульфинильные производные получали путем окисления сульфидных производных гидроксамовой кислоты с помощью Н 2 О 2 в метанольном (МеОН)-растворе. Схема 3 Синтез: 15 Соответствующие гидроксиамиды: 1 замещенной-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты были получены, исходя из диэтаноламина и соответствующих замещенных алкильного или арильного галоидов (схема 4). Производные N-замещенного диэтаноламина были преобразованы в дихлорсоединения с использованием тионилхлорида. Соответствующие дихлориды реагировали с замещенными производными этилового эфира сульфонилуксусной кислоты в присутствии К 2 СО 3/18-Краун-6 в кипящем ацетоне. Полученные таким образом этиловые эфиры 1 замещенной-4-(4-метоксибензолсульфонил)пиперидин-4-карбоновой кислоты были преобразованы в гидроксиамид, как указано на схеме 4. В альтернативном случае эти классы соединений и другие гетероциклы могли быть получены, как указано на схемах 5 и 6. Схема 4 Альтернативно, на схемах 7-11 приведены способы получения соединений гидроксамовой кислоты с использованием твердофазного носителя (Р).(1:1); 25 С; 1 ч. 4-О-метилгидроксиламин-феноксиметилсополи(стирол-1%-дивинилбензол)-смола (гидроксиламиновая смола) может сочетаться с 2 галоидной кислотой с получением гидроксаматэфирной смолы. Данную реакцию сочетания осуществляли в присутствии карбодиимида,такого как DIC (диизопропилкарбодиимид), в инертном растворителе, таком как ДМФ, при комнатной температуре. Галоидная группа может быть замещена на тиол в присутствии основания, такого как DBU (1,5-диазабицикло[5.4.0]ундец-5-ен), в инертном растворителе,таком как ТГФ, при комнатной температуре. Сульфид может быть окислен до сульфоксида путем взаимодействия с окисляющим агентом,таким как трет-бутилгидроксипероксид в присутствии кислотного катализатора, такого как бензолсульфоновая кислота, в инертном растворителе, таком как DXM, при комнатной температуре. Альтернативно, данный сульфид может быть окислен до сульфона путем взаимодействия с окисляющим агентом, таким как метахлорпероксибензойная кислота, в инертном растворителе, таком как DXM, при комнатной температуре. Сульфид, сульфоксид или сульфон может быть обработан и кислотой, такой как трифторуксусная кислота, и в инертном растворителе, таком как DXM, до высвобождения свободной гидроксамовой кислоты. На схеме 8 показан способ получения гидроксамовых кислот, имеющих алкоксигруппы,присоединенные к ароматическому кольцу.d) 70%-ный трет-бутилгидропероксид (40 экв.); бензолсульфоновая кислота (2,0 экв); DXM; 25 С; 12-24 ч. е) mСРВА (5,0 экв.); DXM; 25 С 12-24 ч. f) ТФА:DXM (1:1); 25 С; 1 ч. Гидроксиламиновую смолу могут сочетать с 2-галоидной кислотой, а галоидная группа могла быть замещена на фторбензолтиол, как описано раньше. Затем группу фтора можно заместить на спирт в присутствии основания,такого как натрийгидрид, в инертном растворителе, таком как ДМФ при температуре около 80 С. Алкоксибензолсульфанильный эфир гидроксамовой кислоты может быть затем окислен либо до соответствующего сульфинильного,либо до сульфонильного эфира гидроксамовой кислоты, как описано раньше. Свободные гидроксамовые кислоты могут быть высвобождены,как описано раньше. На схеме 9 показан способ получения 2 бисарилсульфанил-, сульфинил- и сульфонилгидроксамовой кислот. Схема 9TFA:DXM (1:1); 25 С; 1 ч. Гидроксиламиновую смолу, можно сочетать с 2-галоидной кислотой, а галоидная группа может быть замещена бромбензолтиолом,как описано раньше. Затем бромбензолсульфаниловый эфир гидроксамовой кислоты можно окислить либо соответствующим сульфинильным, либо сульфонильным эфиром гидроксамовой кислоты, как описано раньше. Затем группу брома можно заместить на арильную группу путем взаимодействия с арилборной кислотой в присутствии катализатора, такого как тетракис(трифенилфосфин)палладий(0), и основания, такого как натрийкарбонат, в инертном растворителе, таком как DME (1,2 диметоксиэтан), при температуре около 80 С. Свободные гидроксамовые кислоты могут быть высвобождены, как описано раньше. На схеме 10 показан способ получения гидроксамовых кислот с аминогруппами, присоединенными к ароматическому кольцу. Схема 10DXM (1:1); 25 С; 1 ч. Гидроксиламиновая смола может сочетаться с 2-галоидной кислотой, а галоидная группа может быть замещена бромбензолтиолом, как описано раньше. Затем эту группу брома можно заместить на амин в присутствии(S)-BINAP, и основания, такого третбутоксиднатрий, в инертном растворителе, таком как диоксан при температуре около 80 С. Свободные гидроксамовые кислоты могут быть высвобождены, как описано раньше. На схеме 11 показан способ получения гидроксамовых кислот, имеющих сульфонатные группы, присоединенные к ароматическому кольцу. Схема 11TФA:DXM (1:1); 25 С; 1 ч. Гидроксиламиновая смола может сочетаться с 2-галоидной кислотой, а галоидная группа может быть замещена гидроксибензолтиолом, как описано раньше. Гидроксибензолсульфанильный эфир гидроксамовой кислоты может быть затем окислен либо до соответствующего сульфинильного, либо сульфонильного эфира гидроксамовой кислоты, как описано раньше. Гидроксигруппа может быть затем сульфонилирована в реакции с сульфонилхлоридом в присутствии основания, такого как триэтиламин, в инертном растворителе, таком какDXM, при комнатной температуре. Свободные гидроксамовые кислоты могут быть высвобождены, как описано раньше. Нижеследующие примеры иллюстрируют,а не ограничивают объем настоящего изобретения. HPLC-чистота соединений, полученных с помощью комбинированных методик, представ 001742 20 лена в виде области, выраженной в процентах,при заданной длине волны (%нм). Пример 1. N-Гидрокси-2-(4-метоксифенилсульфанил)-2-метил-3-фенилпропионамид. К перемешиваемому раствору 4-метоксибензолтиола (2,8 г, 20 ммолей) и безводного К 2 СО 3 (10 г, избыток) в безводном ацетоне (100 мл) в круглодонную колбу добавляли этиловый 2-бром-пропионат (3,6 г, 20 ммолей) и данную реакционную смесь нагревали до температуры кипения с обратным холодильником в течение 8 ч при хорошем перемешивании. По окончании данную реакцию охлаждали, отфильтровывали соли калия и данную реакционную смесь концентрировали. Полученный остаток экстрагировали хлороформом и промывали Н 2 О и раствором 0,5N NaOH. Органический слой далее тщательно промывали водой, обезвоживали надMgSO4, фильтровали и концентрировали, что дает этиловый эфир 2-(4-метоксифенилсульфанил)-пропионовой кислоты в виде светложелтого масла. Выход 4,5 г (94%); MS; 241(М+Н)+. К перемешиваемому раствору этилового эфира 2-(4-метоксифенилсульфанил)-пропионовой кислоты (2,44 г, 10 ммолей), в ТГФ (100 мл) при -4 С, медленно добавляли бис(триметилсилил)амид лития (1 М раствор, 15 мл, 15 ммолей). Полученную оранжевого цвета реакционную смесь перемешивали при комнатной температуре в течение 15 мин, а затем ее охлаждали до 0 С, при которых ее перемешивали в течение дополнительного часа. Температуру данной смеси вновь охлаждали к -40 С и по каплям добавляли бензилбромид (1,72 г, 10 ммолей) в ТГФ. Данную реакцию нагревали до комнатной температуры и перемешивали в течение ночи перед остановкой ее ледяной водой, экстрагировали хлороформом и промывали водой. Полученный органический слой обезвоживали над МgSO4, фильтровали и концентрировали и хроматографировали на колонке с силикагелем при помощи 10% этилацетата:гексана, что дает этиловый эфир 2-(4-метоксифенилсульфанил)-2 метил-3-фенилпропионовой кислоты в виде бесцветного масла. Выход: 860 мг, (26%); MS: 331 (М+Н)+. Этиловый эфир 2-(4-метоксифенилсульфанил)-2-метил-3-фенилпропионовой кислоты(4,12 г, 12 ммолей) растворяли в метаноле (50 мл) и добавляли 10N NaOH (20 мл). Эту реакцию оставляли перемешиваться в течение ночи при комнатной температуре. Полученную реакционную смесь концентрировали, разбавляли смесью 1:1 гексан:диэтиловый эфир и экстрагировали с Н 2 О. Водный слой охлаждали льдом и подкисляли до рН 3,0. Затем эту кислоту экстрагировали хлороформом, а органический слой обезвоживали над MgSO4, фильтровали и концентрировали, что дает 2-(4-метоксифенилсульфанил)-2-метил-3-фенилпропионовую ки 21 слоту в виде легкоплавкого твердого вещества. Выход 580 мг, 16%; MS: 303,2 (М+Н)+. К перемешиваемому раствору 2-(4 метоксифенилсульфанил)-2-метил-3-фенилпропионовой кислоты (0,5 г, 1,65 ммолей) и ДМФ(2 капли) в CH2Cl2 (100 мл) при 0 С капельным способом добавляли оксалилхлорид (1,0 г, 8 ммолей). После этого добавления полученную реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Одновременно в отдельной колбе в смеси ТГФ вода (5:1, 30 мл) при 0 С в течение 1 ч перемешивали смесь гидроксиламингидрохлорида (2,0 г, 29 ммолей) и триэтиламина (5 мл, избыток). По окончании 1 ч оксалилхлоридную реакционную смесь концентрировали, а полученный бледно-желтый остаток растворяли в 10 мл СН 2 Сl2 и медленно приливали к гидроксиламину при 0 С. Данную реакционную смесь перемешивали при комнатной температуре в течение 24 ч и концентрировали. Полученный остаток экстрагировали хлороформом и тщательно промывали водой. Полученный продукт выделяли очисткой с помощью колоночной хроматографии на силикагеле и элюировали этилацетатом. Выделяли Nгидрокси-2-(4-метоксифенилсульфанил)-2 метил-3-фенилпропионамид в виде бесцветного твердого вещества. Т. пл. 88 С; Выход, 300 мг,57%; MS: 318 (М+Н)+; 1H ЯМР (300 МГц, СDСl3):1,32 (с, 3 Н),3,07 (д, J=11 Гц, 1H), 3,23 (д, J=11 Гц, 1H), 3,79(n, 3 Н), 6,83-7,36 (м, 9 Н). Пример 2. N-Гидрокси-2-(4-метоксифенилсульфанил)-2-фенилацетамид. Этиловый эфир 2-(4-метоксифенилсульфанил)-фенилуксусной кислоты получали в соответствии с общим способом, как изложено в примере 1. Из исходного этилового бромфенилацетата (7,18 г, 31,4 ммоля) и 4 метокситиофенола (4,4 г, 31,4 ммоля) было выделено 8,5 г данного продукта в виде светложелтого масла. Выход 90%; MS: 303,1 (М+Н)+. Этиловый эфир 2-(4-метоксифенилсульфанил)-2-фенилуксусной кислоты получали из исходного этилового эфира 2-(4-метоксифенилсульфанил)-фенилуксусной кислоты (3,0 г, 10 ммолей), растворенного в метаноле (50 мл), и 10N NaOH (20 мл). Данную полученную реакционную смесь обрабатывали так же, как и в примере 1. Выход 1,9 г, 70%. Легкоплавкое твердое вещество. MS: 273 (M+H)+. Из исходной 2-(4-метоксифенилсульфанил)-фенилуксусной кислоты (1,05 г, 3,83 ммолей) и метода, который изложен в примере 1, выделяли 1,154 мг N-гидрокси-2-(4-метоксифенилсульфанил)-2-фенилацетамида в виде бесцветного твердого вещества. Т. пл. 155 С; Выход 14%; MS: 290 (M+H)+; 1 22 Пример 3. Гидроксамид 2-(4-метоксифенилсульфанил)-2,5-диметил-гекс-4-еновой кислоты. Этиловый эфир 2-(4-метоксифенилсульфанил)-2,5-диметил-гекс-4-еновой кислоты получали по методу из примера 1, второй параграф. Из исходного этилового эфира (4-метоксифенилсульфинил)-пропионовой кислоты (3,5 г,14,3 ммоля), и изопренилбромида (2,25 г, 15 ммолей) было выделено 2,2 г данного продукта в виде масла. Выход 50%; MS: 310 (M+H)+. 2-(4-Метоксифенилсульфанил)-2,5-диметил-гекс-4-еновую кислоту получали из исходного этилового эфира 2-(4-метоксифенилсульфанил)-2,5-диметил-гекс-4-еновой кислоты(2,0 г, 6,4 ммоля), растворенного в метаноле (50 мл), и 10N NaOH (20 мл). Полученную реакционную смесь обрабатывали, как изложено в примере 1. Выход составляет 1,9 г, 99% легкоплавкого твердого вещества. MS: 280 (M+H)+. Из исходной 2-(4-метоксифенилсульфанил)-2,5-диметил-гекс-4-еновой кислоты (1,67 г,5,8 ммолей) и по методу, как изложено в примере 1, было выделено 1,5 г гидроксиамида 2-(4 метоксифенилсульфанил)-2,5-диметил-гекс-4 еновой кислоты в виде бесцветного твердого вещества. Т. пл. 89 С; Выход 94%; MS: 296(с, 3 Н), 5,17 (т, J=7,5 Гц, 1 Н), 6,86 (д, J=12,4 Гц,2 Н), 7,35 (д, J=12,4 Гц, 2 Н). Пример 4. N-Гидрокси-2-(4-метоксифенилсульфанил)-3-метилбутирамид. Этиловый эфир 2-(4-метоксифенилсульфанил)-3-метилмасляной кислоты получали в соответствии с общим способом из примера 1. Из исходного этилового 2-бромо-3-метилбутаноата (20,9 г, 100 ммолей) и 4 метоксибензолтиола (14,0 г, 100 ммолей), было выделено 30 г данного продукта. Выход 99%; светло-желтое масло; MS: 271 (M+H)+. 2-(4-Метоксифенилсульфанил)-3-метилмасляную кислоту получали из исходного этилового эфира 2-(4-метоксифенилсульфанил)-3 метилмасляной кислоты (5,8 г, 21,6 ммолей),растворенного в метаноле (50 мл), и 10N NaOH(30 мл). Полученную реакционную смесь обрабатывали, как изложено в примере 1. Выход 5,0 г, 99%. Легкоплавкое твердое вещество. MS: 242 (М+Н)+. Из исходного 2-(4-метоксифенилсульфанил)-3-метилмасляной кислоты (4,39 г, 18,3 ммолей) и по методике, которая изложена в примере 1, в виде бесцветного твердого вещества выделяли 1,5 г N-гидрокси-2-(4-метоксифенилсульфанил)-3-метил-бутирамида. Т. пл. 119 С; выход 33%; MS: 256 (М+Н)+; 1(10 мл). Данную реакционную смесь перемешивали в течение 48 ч при комнатной температуре,время, в течение которого реакцию охлаждали до 0 С и останавливали с помощью раствора насыщенного Na2SO3 (20 мл). Данную реакционную смесь взбалтывали круговым движением. Ее перемешивали в течение 4 ч до концентрирования на водяной бане комнатной температуры,разбавляли водой, экстрагировали с помощью СНСl3 и промывали с помощью H2O2. Полученный органический слой обезвоживали надMgSO4, фильтровали и концентрировали. Названное соединение выделяли колоночной хроматографией на силикагеле и элюировали 75%ным этилацетат:гексаном. Легкоплавкое твердое вещество. Выход: 220 мг (52%); MS: 334,1H ЯМР (300 МГц, СDСl3): д 1,11 (с, 2 Н),1,22 (с, 3 Н), 3,84 (с, 3 Н), 7,00-7,61 (м, 9 Н). Пример 6. Гидроксиамид 2-(4-метоксибензолсульфинил)-2,5-диметил-гекс-4-еновой кислоты. Из исходного гидроксиамида 2-(4-метоксибензолсульфанил)-2,5-диметил-гекс-4-еновой кислоты (900 мг, 3,0 ммоля) (полученного в примере 3) и по методике, изложенной в примере 5, в виде бесцветного твердого вещества выделяли гидроксиамид 2-(4-метоксибензолсульфинил)-2,5-диметил-гекс-4-еновой кислоты. Выход: 104 мг (10%); т. пл. 108 С; MS: 312(д, J=9 Гц, 2 Н). Пример 7. М-Гидрокси-2-(4-метоксибензолсульфинил)-3-метилбутирамид. Из исходного 2-(4-метоксибензолсульфанил)-3-метилбутирамида (1 г, 3,9 ммоля), который получили в примере 4, и по методике из примера 5, в виде бесцветного твердого вещества выделяли N-гидрокси-2-(4-метоксибензолсульфинил)-3-метилбутирамид. Выход: 420 мгN-Гидрокси-2-(4-метоксибензолсульфинил)-2-фенилацетамид. Из исходного N-гидрокси-2-(4-метоксибензолсульфанил)-2-фенилацетамида (240 мг,0,83 ммолей), который получили в примере 2, и по методике изложенной в примере 5, в виде 24 бесцветного твердого вещества был выделен Nгидрокси-2-(4-метоксибензолсульфинил)-2 фенилацетамид. Выход: 100 мг (40%); т. пл. 135 С; MS 304 (M+H)+; 1H ЯМР (300 МГц, DMSO-d6):3,75 (с,3 Н), 4,38 (с, 1 Н), 6,92-7,69 (м, 9 Н). Пример 9. N-Гидрокси-2-(4-метоксибензолсульфонил)-2-фенилпропионамид. К перемешиваемому раствору из 4 метоксибензолтиола (2,8 г, 20 ммолей) и безводного К 2 СО 3 10 г, избыток) в безводном ацетоне (100 мл) в круглодонной колбе вносили бромэтилацетат (3,3 г, 20 ммолей) и данную реакционную смесь нагревали при температуре кипения с обратным холодильником в течение 8 ч при тщательном перемешивании. По окончании данную реакционную смесь оставляли охлаждаться, калийные соли отфильтровывали и полученную реакционную смесь концентрировали. Полученный остаток экстрагировали хлороформом и промывали с помощью H2O и 0,5N раствора NaOH. Органический слой дополнительно тщательно промывали водой, обезвоживали над МgSO4, фильтровали и концентрировали. Этиловый эфир (4-метоксифенилсульфанил)-уксусной кислоты выделяли в виде бледно-желтого масла. Выход: 4,4 г (100%); MS: 227 (М+Н)+. К перемешиваемому раствору 60%-ной 3 хлорпероксибензойной кислоты (14,0 г, 40 ммолей) в метиленхлориде (100 мл) при 0 С медленно добавляли этиловый эфир (4-метоксифенилсульфанил)-уксусной кислоты (4,4 г, 20 ммолей) в СН 2 Сl2 (15 мл). Данную реакционную смесь взмучивали круговым движением и перемешивали при комнатной температуре в течение 6 ч. Затем эту реакционную смесь разбавляли гексаном (300 мл) и перемешивали в течение 15 мин. Отфильтровывали частицы твердого вещества и добавляли раствор Na2SO3 к полученному органическому слою, который перемешивали в течение, по меньшей мере, 3 ч до того, как данную смесь экстрагировали с помощью СНСl3 и промывали с помощью Н 2O. Органический слой обезвоживали над MgSO4, фильтровали и концентрировали и выделяли в виде масла бесцветный этиловый эфир (4-метоксифенилсульфонил)-уксусной кислоты. Выход: 100%; MS: 259,1 (М+Н)+. К перемешиваемому раствору из этилового эфира(1,8 г, 10 ммолей) и 18-Крон-6 (500 мг) в ацетоне (250 мл) добавляли К 2 СО 3 (10 г, избыток) и данную смесь кипятили с обратным холодильником в течение 24 ч. По окончании эту реакционную смесь фильтровали, а полученный ацетоновый слой концентрировали. Полученный остаток экстрагировали хлороформом, тщательно промывали водой, обезвоживали над безводнымMgSO4, фильтровали и концентрировали. Полу 25 ченный продукт очищали с помощью силикагельной колоночной хроматографии, элюировали 30%-ным этилацетат:гексаном. Элюированный продукт, этиловый эфир 2-(4-метоксибензолсульфонил)-3-пропионовой кислоты, был выделен в виде легкоплавкого твердого вещества. Выход: 3,0 г, 86%; легкоплавкое твердое вещество; MS: 349 (М+Н)+. К перемешиваемому раствору этилового эфира 2-(4-метоксибензолсульфонил)-3-пропионовой кислоты (348 мг, 1 ммоль) в метаноле (25 мл) добавляли 10N NaOH (10 мл). Эту реакционную смесь перемешивали при комнатной температуре в течение 48 ч. По окончании, данную реакционную смесь концентрировали и осторожно нейтрализовали разбавленной НСl. Полученный остаток экстрагировали хлороформом, тщательно промывали водой, обезвоживали и концентрировали. Полученный продукт очищали силикагельной колоночной хроматографией путем элюцирования с помощью этилацетат:метанола (95:5), что дает 2-(4-метоксибензолсульфонил)-3-пропионовую кислоту в виде бесцветного масла. Выход: 250 мг, 89%;MS: 321 (M+H)+. Из исходной 2-(4-метоксибензолсульфонил)-3-пропионовой кислоты (200 мг, 0,625 ммоля) и по методике, изложенной в примере 1,выделяли в виде коричневого твердого вещества 150 мг N-гидрокси-2-(4-метоксибензолсульфонил)-3-фенилпропионамида. Выход: 71%; т. пл. 180 С; MS: 336 (М+Н)+; 1H ЯМР (300 МГц, СDСl3):3,2 (м, 1 Н),3,8 (с, 3 Н), 4,0-4,2 (м, 2 Н), 7,0-8,0 (м, 9 Н). Пример 10. Гидроксиамид 2-(4-метоксибензолсульфонил)-гексановой кислоты. Этиловый эфир 2-(4-метоксифенилсульфанил)-гексановой кислоты получали в соответствии с общим способом, который изложен в примере 1. Из исходного этилового 2 бромогексаноата (7 г, 32 ммоля) и 4-метоксибензолтиола (4,2 г, 30 ммолей), было выделено 8,3 г данного продукта. Выход 98%; светложелтое масло; MS: 283 (М+Н)+. Из исходного этилового эфира 2-(4 метоксифенилсульфанил)-гексановой кислоты(2,8 г, 10 ммолей) и по методике, которая изложена в примере 9, в виде бесцветного твердого вещества выделяли 9,3 г этилового эфира 2-(4 метоксифенилсульфонил)-гексановой кислоты. Выход: 95%; т. пл. 62 С; MS: 314 (М+Н)+. Из исходного этилового эфира 2-(4 метоксифенилсульфонил)-гексановой кислоты(2 г, 6,3 ммоля) по методике, которая изложена в примере 9, было выделено 1,5 г (83%) 2-(4 метоксифенилсульфонил)-гексановой кислоты в виде бесцветного твердого вещества. Т. пл. 116 С; MS: 287 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-гексановой кислоты и по методике, которая изложена в примере 1, в виде бесцветного твердого вещества было выделено 700 мг гид 001742H ЯМР (300 МГц, СОСl3):0,786 (т, J=7,2 Гц, 3 Н), 1,1-1,3 (м, 4 Н), 1,6-1,8 (м, 2 Н), 3,7 (м,1 Н), 3,9 (с, 3 Н), 7,2 (д, J=11 Гц, 2 Н), 7,8 (д, J=11 Гц, 2 Н), 9,3 (с, 1 Н), 10,9 (с, 1 Н). Пример 11. Гидроксиамид 2-(4-метоксибензолсульфонил)-тетрадекановой кислоты. Этиловый эфир 2-(4-метоксифенилсульфанил)-тетрадекановой кислоты получали в соответствии с общим способом, который изложен в примере 1. Из исходных соответствующих этил-2-бромомиристата (5,0 г, 14,9 ммолей) и 4 метокситиофенола (1,9 г, 13,4 ммолей) было выделено 5,0 г данного продукта. Выход 98%; светло-желтое масло; MS: 393 (М+Н)+. Из исходного этилового эфира 2-(4 метоксифенилсульфанил)-тетрадекановой кислоты (3,9 г, 10 ммолей) и по методике, которая изложена в примере 9, в виде бесцветного твердого вещества было выделено 3,2 г этилового эфира 2-(4-метоксибензолсульфонил)-тетрадекановой кислоты. Выход: 76%; масло; MS: 425(М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-тетрадекановой кислоты (2,5 г, 5,9 ммоля) в виде бесцветного твердого вещества по методике, которая изложена в примере 9, было выделено 2,0 г (85%) 2(4-метоксибензолсульфонил)-тетрадекановой кислоты. Т. пл. 82 С; MS: 397 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-тетрадекановой кислоты (1,14 г, 2,9 ммоля) и по методике, которая изложена в примере 1,было выделено 670 мг гидроксиамида 2-(4 метоксибензолсульфонил)-тетрадекановой кислоты, твердого вещества не совсем белого цвета. Выход: 57%; т. пл. 114 С; MS: 414 (М+Н)+; 1H ЯМР (300 МГц, DMSO-d6):0,85 (т, J=7 Гц, 3 Н), 1,16-1,27 (м, 20 Н), 1,66 (м, 2 Н), 3,623,70 (м, 1 Н), 3,87 (с, 3 Н), 7,12 (д, J=15 Гц, 2 Н),7,73 (д, J=15 Гц, 2 Н). Пример 12. N-Гидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-фенилпропионамид. К перемешиваемому раствору из этилового эфира 2-(4-метоксибензолсульфонил)-3-фенилпропионовой кислоты (1,0 г, 3 ммоля) (пример 9), метилиодида (1 мл, избыток) и 18-Крон-6(10 г, избыток) и данную реакционную смесь нагревали при температуре кипения с обратным холодильником в течение 24 ч. По окончании эту реакционную смесь фильтровали, а ацетоновый слой концентрировали. Полученный остаток экстрагировали хлороформом, тщательно промывали водой, обезвоживали над безводнымMgSO4, фильтровали и концентрировали. Полученный продукт очищали силикагелевой колоночной хроматографией путем элюирования его 27 с помощью 30%-ного этилацетат:гексана, что дает этиловый эфир 2-(4-метоксибензолсульфонил)-2-метил-3-фенилпропионовой кислоты в виде бесцветного масла. Выход 1,0 г, 98%; MS 349 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метил-3-фенилпропионовой кислоты (900 мг, 2,7 ммоля), по методике, которая изложена в примере 9, было выделено 850 мг (количественно) 2-(4-метоксибензолсульфонил)-2-метил-3-фенилпропионовой кислоты. Бесцветное масло, MS 335 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-3-фенилпропионовой кислоты(900 мг, 2,7 ммоля) и по методике, которая изложена в примере 1, было выделено 450 мг Nгидрокси-2-(4-метоксибензолсульфонил)-2 метил-3-фенилпропионамида в виде коричневого твердого вещества. Выход: 48%; т. пл. 58 С;(д, J=9 Гц, 1 Н), 3,6 (д, J=9 Гц, 1 Н), 3,9 (с, 3 Н),6,8-7,8 (м, 9 Н). Пример 13. Гидроксиамид 2-(4-метоксибензолсульфонил)-2,5-диметил-гекс-4-еновой кислоты. Из исходного этилового эфира 2-(4 метоксифенилсульфанил)-пропионовой кислоты(пример 1) (12 г; 50 ммолей) и по методике, которая изложена в примере 9, было выделено 12 г этилового эфира 2-(4-метоксифенилсульфонил)-пропионовой кислоты в виде полутвердого вещества. Выход 100%; MS: 256,1 (М+Н)+. По методике, которая изложена в примере 12, из исходного этилового эфира 2-(4-метоксибензилсульфонил) пропионовой кислоты и изопренилбромида (1,0 г, 6 ммолей) был получен этиловый эфир 2-(4-метоксибензолсульфонил)2,5-диметил-гекс-4-еновой кислоты (1 г, 3,6 ммоля). Выход 1,0 г, 81%; бесцветное масло;MS: 341 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2,5-диметил-гекс-4 еновой кислоты (900 мг, 2,6 ммоля) по методике, которая изложена в примере 9, было выделено 800 мг (96%) 2-(4-метоксибензолсульфонил)-2,5-диметил-гекс-4-еновой кислоты, MS: 313 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2,5-диметил-гекс-4-еновой кислоты (1,0 г,3,2 ммоля) и по методике, которая изложена в примере 1, было выделено 700 мг гидроксиамида 2-(4-метоксибензолсульфонил)-2,5 диметил-гекс-4-еновой кислоты в виде легкоплавкого твердого вещества. Выход: 67%; MS: 328 (М+Н)+; 1 28 Пример 14. 3-(Бифенил-4-ил)-N-гидрокси 2-(4-метоксибензолсульфонил)-2-метилпропионамид. По методике, которая изложена в примере 12, из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты (2,7 г,10 ммолей) и 4-(хлорметил) бифенила (2,5 г, 12 ммолей) был получен этиловый эфир 3(бифенил-4-ил)-2-(4-метоксибензолсульфонил)2-метилпропионовой кислоты. Выход 4,0 г,91%; бесцветное масло; MS: 438 (М+Н)+. Из исходного этилового эфира 3-(бифенил 4-ил)-2-(4-метоксибензолсульфонил)-2-метилпропионовой кислоты по методике, которая изложена в примере 9, было выделено 2,5 г (89%) 3-(бифенил-4-ил)-2-(4-метоксибензолсульфонил)-2-метилпропионовой кислоты в виде бесцветного твердого вещества. Т. пл. 161 С; MS: 411 (М+Н)+. Из исходной 3-(бифенил-4-ил)-2-(4 метоксибензолсульфонил)-2-метилпропионовой кислоты (2,0 г, 4,8 ммоля) и по методике, которая изложена в примере 1, было выделено 1,2 г 3-(бифенил-4-ил)-N-гидрокси-2-(4-метоксибензолсульфонил)-2-метилпропионамида в виде бесцветного твердого вещества. Выход: 58%; т. пл. 177 С; MS: 426 (М+Н)+; 1(д, J=9 Гц, 1 Н), 3,7 (д, J=9 Гц, 1 Н), 3,9 (с, 3 Н),7,0-7,8 (м, 13 Н), 9,7 (ушир. с, 1 Н). Пример 15. Гидроксиамид 1-(4-метоксибензолсульфонил)-2,5,9-триметил-дека-4,8-диеновой кислоты. По методике, которая изложена в примере 12, из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты (2,7 г,10 ммолей) и геранилбромида (3,0 г, 13 ммолей) был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2,5,9-триметил-дека-4,8-диеновой кислоты. Выход 4,0 г, 98%; бесцветное масло; MS: 409 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2,5,9-триметил-дека 4,8-диеновой кислоты было выделено 2,8 г 29 Пример 16. 3-Циклогексил-N-гидрокси-2(4-метоксибензолсульфонил)-2-метилпропионамид. По методике, которая изложена в примере 12, был получен этиловый эфир 3-циклогексил 2-(4-метоксибензолсульфонил)-2-метилпропионовой кислоты из исходного этилового эфира 2(4-метоксибензолсульфонил)-пропионовой кислоты и бромометилциклогексана (1,8 г, 10 ммолей). Выход 3,5 г, 95%; желтое масло; MS: 369 (М+Н)+. Из исходного этилового эфира 3 циклогексил-2-(4-метоксибензолсульфонил)-2 метилпропионовой кислоты было выделено 2,5 г (90%) 3-циклогексил-2-(4-метоксибензолсульфонил)-2-метилпропионовой кислоты по методике, которая изложена в примере 9. Т. пл. 116 С; MS: 341 (М+Н)+. Из исходной 3-циклогексил-2-(4-метоксибензолсульфонил)-2-метилпропионовой кислоты (2,0 г, 5,8 ммоля) и по методике, которая изложена в примере 1, было выделено 1,1 г 3 циклогексил-N-гидрокси-2-(4-метоксибензолсульфонил)-2-метилпропионамида в виде бесцветного твердого вещества. Выход: 55%; т. пл. 58 С; MS: 356 (М+Н)+; 1H ЯМР (300 МГц, CDCl3):1,4 (с, 3 Н),2,3-1,0 (м, 13 Н), 3,9 (с, 3 Н), 7,0 (д, 8,8 Гц, 2 Н),7,69 (д, 9,0 Гц, 2 Н). Пример 17. N-Гидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-пиперидин-1 ил-этокси)-фенил]-пропионамид. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-пиперидин-1 ил-этокси)-фенил]-пропионовой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты (2,7 г,10 ммолей) и 4-(2-пиперидин-1-ил-этокси)бензилхлорида (2,9 г, 10 ммолей). Выход 4,8 г,98%; коричневое масло; MS: 490 (M+S)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метил-3-[4-(2 пиперидин-1-ил-этокси)-фенил]-пропионовой кислоты (4,0 г, 7,9 ммолей) было выделено 3,5 г(выход: 94%) 2-(4-метоксибензолсульфонил)-2 метил-3-[4-(2-пиперидин-1-ил-этокси)фенил]пропионовой кислоты в виде бесцветных кристаллов по методике, которая изложена в примере 9. Т. пл. 106 С; MS: 462,5 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-пиперидин-1-илэтокси)-фенил]-пропионовой кислоты и по методике, которая изложена в примере 1, был выделен 1 г N-гидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-пиперидин-1-илэтокси)-фенил]-пропионамида в виде бесцветного твердого вещества. Выход: 1 г, 48%; т. пл. 98 С; MS: 477 (М+Н)+;(м, 8 Н), 10,8 (ушир. с, 1 Н). Пример 18. Гидроксиамид 2-[4-(2-азепан 1-ил-этокси)бензил]-2-(4-метоксибензолсульфонил)-пропионовой кислоты. По методике, которая изложена в примере 12, был получен этиловый эфир 2-[4-(2-азепан 1-ил-этокси)-бензил]-2-(4-метоксибензолсульфонил)-пропионовой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)пропионовой кислоты и 1-[2-(4-хлорометилфенокси)этил]-азепана (3,03 г, 10 ммолей). Выход 4,5 г, 90%; коричневое масло; MS: 504(М+Н)+. Из исходного этилового эфира 2-[4-(2 азепан-1-ил-этокси)бензил]-2-(4-метоксибензолсульфонил)-пропионовой кислоты было выделено 3,5 г (выход: 94%) 2-[4-(2-азепан-1-илэтокси)-бензил]-2-(4-метоксибензолсульфонил)пропионовой кислоты в виде полутвердого вещества по методике, которая изложена в примере 9. MS: 476 (М+Н)+. Из исходной 2-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-метоксибензолсульфонил)-пропионовой кислоты (2,0 г, 4,2 ммоля) и по методике, которая изложена в примере 1, был выделен 1 г гидроксиамида 2-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-метоксибензолсульфонил)-пропионовой кислоты в виде бесцветного твердого вещества. Выход: 1,8 г, 87%; т. пл. 68 С; MS: 477(м, 8 Н), 10,9 (ушир. с, 1 Н). Пример 19. Гидроксиамид 2-[4-(2-азепан 1-ил-этокси)-бензил]-2-(4-метоксибензолсульфонил)-пентановой кислоты. Этиловый эфир 2-[4-(2-азепан-1-илэтокси)-бензил]-2-(4-метоксибензолсульфонил)пентановой кислоты был получен в соответствии с общим способом, который изложен в примере 12. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-пентановой кислоты(3,5 г, 11,7 ммолей) и 1-[2-(4-хлорометилфенокси)-этил]-азепана (3,9 г, 12,8 ммолей). Выход 2,58% г (42%); коричневое масло; MS: 532,4 (М+Н)+. 2-[4-(2-Азепан-1-ил-этокси)бензил]-2-(4 метоксибензолсульфонил)-пентановая кислота была получена из исходного этилового эфира 2[4-(2-азепан-1-ил-этокси)-бензил]-2-(4-метоксибензолсульфонил)-пентановой кислоты (2 г,3,76 ммоля), растворенного в метаноле (300 мл),и 10N NaOH (15 мл). Полученную смесь обрабатывали так, как изложено в примере 1. Выход 830 мг (44%); коричневое твердое вещество; т. пл. 55 С; MS: 504,4 (М+Н)+. Из исходной 2-[4-(2-азепан-1-ил-этокси) бензил]-2-(4-метоксибензолсульфонил)-пентановой кислоты (690 мг, 1,37 ммоля) и по мето 1 31 дике, которая изложена в примере 1, было выделено 1,240 мг гидроксиамида 2-[4-(2-азепан-1 ил-этокси)бензил]-2-(4-метоксибензолсульфонил)-пентановой кислоты в виде желтого твердого вещества. Выход 34%; т. пл. 85 С; MS: 477H ЯМР (300 МГц, DMSO-d6):0,71 (т,J=7,3 Гц, 3 Н), 0,78-1,77 (м, 16 Н), 3,04-3,46 (м,4 Н), 3,87 (с, 3 Н), 4,26 (м, 2 Н), 6,87 (д, J=8,7 Гц,2 Н), 7,14 (м, 4 Н), 7,71 (д, J=9 Гц, 2 Н), 9,07 (с,1 Н), 10 (с, 1 Н). Пример 20. N-Гидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диизопропиламиноэтокси)фенил]пропионамид. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диизопропиламиноэтокси)фенил]-пропионовой кислоты из исходного этилового эфира 2-(4 метоксибензолсульфонил)-пропионовой кислоты (5,4 г, 20 ммолей) и 4-(2-N,N-диизопропиламиноэтокси)бензилхлорида (6,1 г, 20 ммолей). Выход 8,9 г, 88%; желтое масло; MS: 506,5(M+H)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метил-3-[4-(2-N,Nдиизопропиламиноэтокси)фенил]-пропионовой кислоты (4,0 г, 7,9 ммолей) было выделено 3,5 г(выход: 92%) 2-(4-метоксибензолсульфонил)-2 метил-3-[4-(2-N,N-диизопропиламиноэтокси)фенил]-пропионовой кислоты в виде бесцветных кристаллов по методике, которая изложена в примере 9. Т. пл. 68 С; MS: 478,6 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диизопропиламиноэтокси)фенил]-пропионовой кислоты (2,0 г, 4,1 ммоля) и по методике, которая изложена в примере 1, был выделен 1 г 2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диизопропиламиноэтокси)фенил]-пропионамида в виде бесцветного твердого вещества. Выход: 1 г,49%; т. пл. 98 С (HCl-соль); MS: 493 (M+H)+; 1(д, 6 Н), 1,4 (д, 6 Н), 3,5-1,5 (м, 6 Н), 3,9 (с, 3 Н),4,4 (с, 2 Н), 6,5-7,8 (м, 8 Н), 10,8 (ушир. с, 1 Н). Пример 21. N-Гидpoкcи-2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диэтиламиноэтокси)фенил]пропионамид. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диэтиламиноэтокси)фенил]-пропионовой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты (5,4 г,20 ммолей) и 4-(2-N,N-диэтиламиноэтокси)бензилхлорида (5,5 г, 20 ммолей). Выход 8,5 г,89%; коричневое масло; MS: 478,6 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метил-3-[4-(2-N,Nдиэтиламиноэтокси)-фенил]-пропионовой кислоты (3,5 г, 7,7 ммолей) было выделено 3,0 г(выход: 85%) 2-(4-метоксибензолсульфонил)-2 метил-3-[4-(2-N,N-диэтиламиноэтокси)фенил]пропионовой кислоты в виде бесцветных кристаллов по методике, которая изложена в примере 9. Т. пл. 96-98 С; MS: 450,5 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диэтиламиноэтокси)фенил]-пропионовой кислоты (2,0 г, 4,4 ммоля) и по методике, которая изложена в примере 1,был выделен 1 г 2-(4-метоксибензолсульфонил)2-метил-3-[4-(2-N,N-диэтиламиноэтокси)фенил]пропионамида в виде бесцветного твердого вещества. Выход: 1 г, 48%; т. пл. 56-59 С(с, 3 Н), 3,2-3,9 (м, 8 Н), 3,9 (с, 3 Н), 4,3 (с, 2 Н),6,5-7,8 (м, 8 Н), 10,8 (ушир. с, 1 Н). Пример 22. N-Гидpoкcи-2-(4-метоксибензолсульфонил)-2-метил-3-[3-(2-пиперидин-1-илэтокси)фенил]пропионамид. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2-метил-3-[3-(2-пиперидин-1 ил-этокси)фенил]-пропионовой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты (5,2 г, 20 ммолей) и 3-(2-пиперидин-1-ил-этокси)-бензилхлорида (6,0 г, 20 ммолей). Выход 8,2 г, 83%; коричневое масло; MS: 490 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метил-3-[3-(2-пиперидин-1-ил-этокси)фенил]-пропионовой кислоты (6,0 г, 12,2 ммоля) было выделено 4,9 г(выход: 79%) 2-(4-метоксибензолсульфонил)-2 метил-3-[3-(2-пиперидин-1-ил-этокси)фенил]пропионовой кислоты в виде бесцветных кристаллов по методике, которая изложена в примере 9. Т. пл. 112 С; MS: 462,5 (M+H)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-3-[3-(2-пиперидин-1-ил-этокси)фенил]-пропионовой кислоты (3,0 г, 6,5 ммоля) и по методике, которая изложена в примере 1, было выделено 1,8 г 2-(4-метоксибензолсульфонил)-2-метил-3-[3-(2-пиперидин-1 ил-этокси)фенил]-пропионамида в виде бесцветного твердого вещества. Выход: 1,8 г, 58%; т. пл. 74 С; MS: 477 (М+Н)+; 1H ЯМР (300 МГц, СDСl3):1,25 (с, 3 Н),1,6-1,8 (м, 6 Н), 2,5-3,7 (м, 8 Н), 3,9 (с, 3 Н), 4,4 (т,2 Н), 6,7-7,8 (м, 8 Н), 10,8 (ушир. с, 1 Н). Пример 23. 3-(4-3-[4-(3-Хлорофенил)пиперазин-1-ил]пропоксифенил-N-гидрокси-2(4-метоксибензолсульфонил)-2-метилпропионамид. По методике, которая изложена в примере 12, был получен этиловый эфир 3-(4-3-[4-(3 хлорофенил)пиперазин-1-ил]пропоксифенил-2(4-метоксибензолсульфонил)-2-метилпропионовой кислоты из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метилпропионовой кислоты (2,72 г, 10 ммолей) и 1-[2-(4 33 хлорометилфеноксиэтил]-4-(3-хлорофенил)пиперазина (4,2 г, 11 ммолей). Выход 5,5 г, 89%; коричневое масло; MS: 616 (М+Н)+. Из исходного этилового эфира 3-(4-3-[4(3-хлорофенил)пиперазин-1-ил]пропоксифенил-2-(4-метоксибензолсульфонил)-2-метилпропионовой кислоты (4,0 г, 6,5 ммоля) было выделено 3,0 г (выход: 78%) 3-(4-3-[4-(3-хлорофенил)пиперазин-1-ил]пропокси-фенил-2-(4 метоксибензолсульфонил)-2-метилпропионовой кислоты в виде бесцветных кристаллов по методике, которая изложена в примере 9. Т. пл. 196 С; MS: 588,1 (М+Н)+. Из исходной 3-(4-3-[4-(3-хлорофенил)пиперазин-1-ил]пропоксифенил-2-(4-метоксибензолсульфонил)-2-метилпропионовой кислоты (3,0 г, 5,1 ммоля) и по методике, которая изложена в примере 1, было выделено 1,8 г 3-(43-[4-(3-хлорофенил)пиперазин-1-ил]пропоксифенил-2-(4-метоксибензолсульфонил)-2 метилпропионамида в виде бледно-желтого твердого вещества. Выход: 1,8 г, 55%; т. пл. 122 С (HCl-соль); MS: 640 (М+Н)+; 1(м, 12 Н), 10,3 (ушир. с, 1 Н). Пример 24. Гидроксиамид 2-(4-метоксибензолсульфонил)-5-метил-2-[4-(2-морфолин-4 ил-этокси)бензил]-гекс-4-еновой кислоты. К перемешиваемому раствору из этилового эфира(3,0 г, 20 ммолей) и 18-Крон-6 (500 мг) в ацетоне (250 мл) был добавлен К 2 СО 3 (10 г, избыток) и смесь нагревали при температуре кипения с обратным холодильником в течение 24 ч. По окончании эту реакционную смесь фильтровали,а ацетоновый слой концентрировали. Полученный остаток экстрагировали хлороформом, тщательно промывали водой, обезвоживали над безводным МgSО 4, фильтровали и концентрировали. Полученный продукт очищали силикагелевой колоночной хроматографией, элюировали 30%-ным этилацетат:гексаном. В виде бесцветного масла был выделен продукт этиловый эфир 2-(4-метоксибензолсульфонил)-5-метилгекс-4-еновой кислоты. Выход: 3,0 г, 93%. По методике, которая изложена в примере 12, получали этиловый эфир 2-(4-метоксибензолсульфонил)-5-метил-2-[4-(2-морфолин-4 ил-этокси)бензил]-гекс-4-еновой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-5-метил-гекс-4-еновой кислоты (3,26 г, 10 ммолей) и 4-(2-морфолин-1-илэтокси)бензилхлорида (3,0 г, 11 ммолей). Выход 4,5 г, 82%; коричневое масло; MS: 546 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-5-метил-2-[4-(2-морфолин-4-ил-этокси)бензил]-гекс-4-еновой кислоты (3,0 г, 5,5 ммолей) было выделено 2,1 г 34 гекс-4-еновой кислоты в виде полутвердого вещества по методике, которая изложена в примере 9. MS: 518,6 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-5-метил-2-[4-(2-морфолин-4-ил-этокси)бензил]-гекс-4-еновой кислоты (1,0 г, 1,9 ммоля) и по методике, которая изложена в примере 1,было выделено 450 мг гидроксиамида 2-(4 метоксибензолсульфонил)-5-метил-2-[4-(2-морфолин-4-ил-этокси)бензил]-гекс-4-еновой кислоты в виде бледно-желтого твердого вещества. Выход: 450 мг, 45%; т. пл. 92 С (HCl-соль);H ЯМР (300 МГц, СDСl3):1,3 (д, 3 Н),1,65 (д, 2 Н), 3,5-1,8 (м, 14 Н), 3,9 (с, 3 Н), 4,5 (м,2 Н), 5,4 (м, 1 Н), 6,5-7,9 (м, 8 Н), 11,5 (ушир. с,1 Н). Пример 25. N-Гидрокси-2-(4-этоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диэтиламиноэтокси)фенил]-пропионамид. К перемешиваемому раствору из 4 гидрокситиофенола (12,6 г, 100 ммолей) и триэтиламина (15,0 г, 150 ммолей) в хлороформе(400 мл) по каплям приливали 2-бромоэтилпропионат (18,2 г, 100 ммолей). Данную реакционную смесь кипятили при температуре кипения с обратным холодильником в течение 1 ч и охлаждали до комнатной температуры. Охлажденную реакционную смесь промывали водой, обезвоживали и концентрировали. В виде бесцветного масла был выделен этиловый эфир 2-(4-гидроксифенилсульфанил)-пропионовой кислоты. Выход: 22,0 г, 99%, MS: 227 (М+Н)+. К перемешиваемому раствору из этилового эфира 2-(4-гидроксифенилсульфанил)-пропионовой кислоты (11,3 г, 50 ммолей) и К 2 СО 3(50 г, избыток) в ацетоне (300 мл, избыток) был добавлен этилиодид и нагрет при температуре кипения с обратным холодильником в течение 8 ч. По окончании нагревания реакционную смесь фильтровали и концентрировали. Полученный остаток экстрагировали хлороформом и тщательно промывали водой. Его обезводили и сконцентрировали. В виде бесцветного масла был выделен продукт этиловый эфир 2-(4 этоксифенилсульфанил)-пропионовой кислоты. Выход: 12,0 г, 98%; MS: 255 (М+Н)+. Этиловый эфир 2-(4-этоксифенилсульфанил)-пропионовой кислоты преобразовывали в этиловый эфир 2-(4-этоксифенилсульфонил)пропионовой кислоты, как описано в примере 9,параграф 2. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-этоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диэтиламиноэтокси)фенил]-пропионовой кислоты из исходного этилового эфира 2-(4-этоксибензолсульфонил)-пропионовой кислоты (3,5 г,12,2 ммоля) и (2-N,N-диэтиламиноэтокси)бензилхлорида (3,5 г, 12,2 ммоля). Выход 4,8 г,80%; коричневое масло; MS: 492,6 (М+Н)+. 35 Из исходного этилового эфира 2-(4-этоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диэтиламиноэтокси)фенил]-пропионовой кислоты(4,0 г, 8,1 ммоля) было выделено 3,2 г (выход: 80%) 2-(4-этоксибензолсульфонил)-2-метил-3[4-(2-N,N-диэтиламиноэтокси)фенил]-пропионовой кислоты в виде полутвердого вещества по методике, которая изложена в примере 9. MS: 464,5 (М+Н)+. Из исходной 2-(4-этоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диэтиламиноэтокси)фенил]-пропионовой кислоты (2,0 г, 4,3 ммоля) и по методике, которая изложена в примере 1,было выделено 1,2 г 2-(4-этоксибензолсульфонил)-2-метил-3-[4-(2-N,N-диэтиламиноэтокси)фенил]-пропионовой кислоты в виде бесцветного легкоплавкого твердого вещества. Выход: 1,2 г, 57%; (HCl-соль); MS: 640 (М+Н)+; 1(с, 2 Н), 6,5-7,8 (м, 8 Н), 10,8 (ушир. с, 1 Н). Пример 26. Гидроксиамид (4 Е)-2-(4 метоксибензолсульфонил)-5,9-диметил-2-[4-(2 морфолин-4-ил-этокси)бензил]-дека-4,8-диеновой кислоты. К перемешиваемому раствору из этилового эфира(4,2 г, 20 ммолей) и 18-Крон-6 (500 мг) в ацетоне (250 мг) добавляли К 2 СО 3 (10 г, избыток) и полученную смесь нагревали при температуре кипения с обратным холодильником в течение 24 ч. По окончании кипячения эту реакционную смесь фильтровали, а ее ацетоновый слой концентрировали. Полученный остаток экстрагировали хлороформом, тщательно промывали водой, обезвоживали над безводным MgSO4,фильтровали и концентрировали. Полученный продукт очищали силикагелевой колоночной хроматографией, элюировали 30%-ным этилацетат:гексаном. Данный продукт, этиловый эфир 2-(4-метоксибензолсульфонил)-5,9-диметилдека-4,8-диеновой кислоты, выделяли в виде бесцветного масла. Выход: 7,0 г, 89%. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-5,9-диметил-2-[4-(2-морфолин-4-ил-этокси)бензил]-дека-4,8-диеновой кислоты из исходного этилового эфира 2-(4 метоксибензолсульфонил)-5,9-диметил-2-[4-(2 морфолин-4-ил-этокси)бензил]-дека-4,8-диеновой кислоты и 4-(2-морфолин-1-ил-этокси)бензилхлорида (800 мг, 2,5 ммоля). Выход 1,2 г,76%; коричневое масло; MS: (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-5,9-диметил-2-[4-(2 морфолин-4-ил-этокси)бензил]-дека-4,8-диеновой кислоты было выделено 1,5 г (выход: 80%) 2-(4-метоксибензолсульфонил)-5,9-диметил-2[4-(2-морфолин-4-ил-этокси)бензил]-дека-4,8 диеновой кислоты в виде полутвердого вещест 001742(4 Е)-2-(4-метоксибензолсульфонил)-5,9 диметил-2-[4-(2-морфолин-4-ил-этокси)бензил]-дека-4,8-диеновой кислоты в виде бледножелтого твердого вещества. Выход: 550 мг,53%; т. пл. 61 С (HCl-соль); MS: 638 (М+Н)+. Пример 27. Гидроксиамид 2-[4-(2-диэтиламиноэтокси)бензил]-2-(4-метоксибензолсульфонил)-гексановой кислоты. Этиловый эфир 2-[4-(2-диэтиламиноэтокси)-бензил]-2-(4-метоксибензолсульфонил)гексановой кислоты был получен в соответствии с общим способом, который изложен в примере 12. Из исходного этилового эфира (4 метоксибензолсульфонил)-гексановой кислоты(4 г, 12,7 ммолей) и [2-(4-хлорометилфенокси)этил]диэтиламина (3,38 г, 14 ммолей). Выход 8,21 г неочищенного вещества (100%); коричневое масло; MS: 520,4 (M+H)+. 2-[4-(2-Диэтиламиноэтокси)-бензил]-2-(4 метоксибензолсульфонил)-гексановая кислота была получена из исходного этилового эфира 2[4-(2-диэтиламиноэтокси)бензил]-2-(4-метоксибензолсульфонил)-гексановой кислоты (8 г, 15,4 ммоля), растворенного в метаноле (200 мл) и 10N NaOH (30 мл). Полученную смесь обрабатывали, как изложено в примере 1. Выход 3,88 неочищенного вещества (51%); коричневое масло; MS: 492 (M+H)+. Из исходной 2-[4-(2-диэтиламиноэтокси)бензил]-2-(4-метоксибензолсульфонил)-гексановой кислоты (3,88 г, 7,89 ммолей) и по методике, которая изложена в примере 1, было выделено 1,800 мг гидроксиамида 2-[4-(2-диэтиламиноэтокси)бензил]-2-(4-метоксибензолсульфонил)-гексановой кислоты в виде желтого порошка. Выход 20%; т.пл. 67 С; MS: 507,4H ЯМР (300 МГц, DMSO-d6):0,75 (т,J=7, 1 Гц, 3 Н), 1,05 (м, 2 Н), 1,23 (т, J=7,2 Гц,6 Н), 1,37-1,91 (м, 2 Н), 3,13 (м, 4 Н), 3,38-3,51 (м,4 Н), 3,87 (с, 3 Н), 4,3 (т, J=4,8 Гц, 2 Н), 6,88 (д,J=8,7 Гц, 2 Н), 7,15 (м, 4 Н), 7,7 (д, J=9 Гц, 2 Н),9,07 (с, 1 Н), 10,1 (с, 1 Н). Пример 28. N-Гидрокси-2-(4-n-бутоксибензолсульфонил)-2-метил-3-[4-(2-пиперидин-1 ил-этокси)фенил]-пропионамид. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-n-бутоксибензолсульфонил)-2-метил-3-[4-(2-пиперидин-1 ил-этокси)фенил]-пропионовой кислоты из исходного этилового эфира 2-(4-n-бутоксибензолсульфонил)-пропионовой кислоты (3,1 г,10 ммолей). Из этилового эфира 2-(4-гидроксифенилсульфанил)-пропионовой кислоты и nбутилбромида по методике, которая изложена в(М+Н)+. Из исходного этилового эфира 2-(4-nбутоксибензолсульфонил)-2-метил-3-[4-(2-пиперидин-1-ил-этокси)фенил]-пропионовой кислоты было выделено 4,2 г (выход: 88%) 2-(4-nбутоксибензолсульфонил)-2-метил-3-[4-(2-пиперидин-1-ил-этокси)фенил]-пропионовой кислоты в виде бесцветного твердого вещества, по методике, которая изложена в примере 9. MS: 504,6 (M+H)+. Из исходной 2-(4-n-бутоксибензолсульфонил)-2-метил-3-[4-(2-пиперидин-1-ил-этокси)фенил]-пропионовой кислоты (3,0 г, 5,9 ммолей) и по методике, которая изложена в примере 1, было выделено 1,3 г 2-(4-n-бутоксибензолсульфонил)-2-метил-3-[4-(2-пиперидин-1 ил-этокси)фенил]-пропионамида в виде бесцветного твердого вещества. Т. пл. 65 С, выход: 1,3 г, 42% (НСl-соль); MS: 478,5 (М+Н)+; 1(м, 8 Н), 10,8 (ушир. с, 1 Н). Пример 29. N-Гидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-[3-(2-N,N-диэтиламиноэтокси)фенил]-пропионамид. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2-метил-3-[3-(2-N,N-диэтиламиноэтокси)фенил]-пропионовая кислота из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты (5,0 г,18 ммолей) и (2-N,N-диэтиламиноэтокси)бензилхлорида (4,9 г, 18 ммолей). Выход 8,1 г,93%; коричневое масло; MS: 478,1 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метил-3-[3-(2-N,Nдиэтиламиноэтокси)фенил]-пропионовой кислоты (8,1 г, 16,9 ммолей) было выделено по методике, которая изложена в примере 9, 6,7 г (выход: 88%) 2-(4-метоксибензолсульфонил)-2 метил-3-[3-(2-N,N-диэтиламиноэтокси)фенил]пропионовой кислоты в виде бесцветного полутвердого вещества. Т. пл. 78-81C; MS: 450,1(М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-3-[3-(2-N,N-диэтиламиноэтокси)фенил]-пропионовой кислоты (6,7 г, 15 ммолей) и по методике, которая изложена в примере 1,был выделен 2-(4-метоксибензолсульфонил)-2-метил-3-[3-(2-N,N-диэтиламиноэтокси)фенил]-пропионамид в виде бесцветного легкоплавкого твердого вещества. Выход: 1,5 г,21% (HCl-соль); MS: 450,5 (M+H)+; 1 38 Пример 30. N-Гидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-[2-морфолин-1-илэтокси)фенил]-пропионамид. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2-метил-3-[2-морфолин-1-илэтокси)фенил]-пропионовой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропиновой кислоты (5,2 г, 20 ммолей) и 3-(2-морфолин-1-ил-этокси)бензилхлорида (6,0 г, 20 ммолей). Выход 9,1 г, 93%; коричневое масло; MS 492 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метил-3-[2-морфолин-1-ил-этокси)фенил]-пропионовой кислоты(10,0 г, 20,3 ммоля) было выделено 8,0 г (выход: 86%) 2-(4-метоксибензолсульфонил)-2-метил-3[2-морфолин-1-ил-этокси)фенил]-пропионовой кислоты в виде бесцветных кристаллов, по методике, которая изложена в примере 9; MS: 464,4 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-3-[2-морфолин-1-ил-этокси)фенил]-пропионовой кислоты (4,55 г, 9,8 ммолей) и по методике, которая изложена в примере 1, было выделено 440 мг 2-(4-метоксибензолсульфонил)-2-метил-3-[2-морфолин-1-илэтокси)фенил]-пропионамида в виде бесцветного твердого вещества. Выход: 440 мг, 9%; т. пл. 63 С; MS: 479,5 (М+Н)+; 1H ЯМР (300 МГц, DMSO-d6):1,26 (с,3 Н), 3,18-3,8 (м, 12 Н), 3,9 (с, 3 Н), 4,4 (м, 2 Н),6,7-8,8 (м, 8 Н), 10,8 (ушир.с, 1 Н). Пример 31. Гидроксиамид 6-(1,3-диоксо 1,3-дигидроизоиндол-2-ил)-2-(4-метоксибензолсульфонил)-2-метилгексановая кислота. По методике, которая изложена в примере 9, был получен этиловый эфир 6-(1,3-диоксо 1,3-дигидроизоиндол-2-ил)-2-(4-метоксибензолсульфонил)-2-метилгексановой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-уксусной кислоты (5,0 г, 20 ммолей) и 4-фаталимидобромобутана (5,66 г, 20 ммолей). Выход 8,4 г, 97%; бесцветное масло;MS: 474 (М+Н). Из исходного этилового эфира 6-(1,3 диоксо-1,3-дигидроизоиндол-2-ил)-2-(4-метоксибензолсульфонил)-2-метилгексановой кислоты (8,4 г, 17,7 ммоля) было выделено по методике, которая изложена в примере 9, 6,95 гH ЯМР (300 МГц, DMSO-d6):1,44 (с,3 Н), 1,61-3,77 (м, 8 Н), 3,82 (с, ЗН), 6,92-8,21 (м,8 Н), 10,70 (ушир.с, 1 Н), 11,20 (ушир.с, 1 Н). Пример 32. 3-[4-(2-Диэтиламиноэтокси)фенил]-2-(4-фуран-2-ил-бензолсульфонил)-Nгидрокси-2-метилпропионамид. К перемешиваемому раствору из 4-бромотиофенола (19,0 г, 100 ммолей) и триэтиламина(15,0 г, 150 ммолей) в хлороформе (400 мл) по каплям добавляли 2-бромоэтилпропионат (18,2 г, 100 ммолей). Данную реакционную смесь нагревали при температуре кипения с обратным холодильником в течение 1 ч и охлаждали до комнатной температуры. Эту реакционную смесь промывали водой, обезвоживали и концентрировали. Был выделен этиловый эфир 2(4-бромофенилсульфанил)-пропионовой кислоты в виде бесцветного масла. Выход: 28,0 г,99%, MS: 290 (М+Н). Этиловый эфир 2-(4-бромофенилсульфанил)-пропионовой кислоты был преобразован в этиловый эфир 2-(4-бромофенилсульфонил)пропионовой кислоты по методике, которая описана в примере 9, параграф 2. Смесь из этилового эфира 2-(4-бромофенилсульфонил)-пропионовой кислоты (6,4 г,20 ммолей), 2-(трибутил)станнилфурана (7,5 г,21 ммоль) и (Рh3 Р)4Pd (500 мг) нагревали при температуре кипения с обратным холодильником в дегазированном толуоле (250 мл) в течение 8 ч. По окончании нагревания, данную реакционную смесь фильтровали через Целит и концентрировали. Отфильтрованный продукт очищали с помощью силикагелевой колоночной хроматографии путем элюирования 50%-ным этилацетат:гексаном. Бесцветное масло. Выход: 5,9 г, 95%, MS: 309 (М+Н)+. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-(2 фуранилбензолсульфонил)-2-метил-3-[4-(2-N,Nдиэтиламиноэтокси)-фенил]-пропионовой кислоты из исходного этилового эфира 2-(4-(2 фуранилбензолсульфонил)-пропионовой кислоты и 4-(2-N,N-диэтиламиноэтокси)-бензилхлорида (3,5 г, 12,2 ммоля). Выход 5,0 г, 97%; коричневое масло; MS: 514,6 (М+Н)+. Из исходного этилового эфира 2-(4-(2 фуранилбензолсульфонил)-2-метил-3-[4-(2-N,Nдиэтиламиноэтокси)фенил]-пропионовой кислоты (5,1 г, 10,0 ммолей) по методике, которая изложена в примере 9, было выделено 3,8 г (выход: 78%) 2-(4-(2-фуранилбензолсульфонил)-2 метил-3-[4-(2-N,N-диэтиламиноэтокси)-фенил]пропионовой кислоты. Т. пл.: 58 С, MS: 486,5 40 фуранилбензолсульфонил)-2-метил-3-[4-(2-N,Nдиэтиламиноэтокси)фенил]-пропионамида в виде бесцветного легкоплавкого твердого вещества. Выход: 3,2 г, 62% (HCl-соль); MS: 502H ЯМР (300 МГц, СDСl3):1,23 (т, 6 Н),1,4 (с, 2 Н), 2,8 (кв, 4 Н), 3,0 (т, 2 Н), 4,1 (т, 2 Н),6,5-8,0 (м, 7 Н). Пример 33. N-Гидрокси-2-(4-метоксибензолсульфонил)-2-[4-(2-морфолин-4-ил-этокси) бензил] бутирамид. Этиловый эфир 2-(4-метоксифенилсульфанил)-масляной кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового 2 бромбутирата (10,71 г, 55 ммолей) и 4 метокситиофенола (7 г, 50 ммолей) было получено 5,19 г (40%) данного продукта; прозрачное масло; MS: 255,2 (М+Н)+. Этиловый эфир 2-(4-метоксифенилсульфонил)-масляной кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового эфира 2-(4 метоксифенилсульфанил)-масляной кислоты(5 г, 20 ммолей). Выход 5,74 г (100%); прозрачное масло; MS: 287,1 (М+Н)+. По методике, которая изложена в примере 12, был получен 2-(4-метоксибензолсульфонил)2-[4-(2-морфолин-4-ил-этокси)бензил]-масляной кислоты из исходного этилового эфира 2-(4 метоксифенилсульфонил)-масляной кислоты(3,5 г, 12,2 ммоля) и 4-[2-(хлорометилфенокси)этил]-морфолина (2,34 г, 6,7 ммоля). Выход 5,7 г, 100%; коричневое масло; MS: 506,4 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-[4-(2-морфолин-4 ил-этокси)бензил]-масляной кислоты (5,54 г, 11 ммолей) было выделено 2,9 г (выход: 55%) 2-(4 метоксибензолсульфонил)-2-[4-(2-морфолин-4 ил-этокси)бензил]-масляной кислоты в виде бесцветного полутвердого вещества по методике, которая изложена в примере 9. MS: 478,3(М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-[4-(2-морфолин-4-ил-этокси)бензил]масляной кислоты и по методике, которая изложена в примере 1, было выделено 510 мг Nгидрокси-2-(4-метоксибензолсульфонил)-2-[4(2-морфолин-4-ил-этокси)бензил]-бутирамида в виде коричневого твердого вещества. Выход 2%; т. пл. 51 С; MS: 461,2 (М+Н)+; 1(с, 1 Н), 10,8 (с, 1 Н). Пример 34. N-Гидрокси-2-(4-метоксибензолсульфонил)-2-[4-(2-пиперидин-1-илэтокси)бензил]-бутирамид. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-метокси 41 бензолсульфонил)-2-[4-(2-пиперидин-1-илэтокси)бензил]-масляной кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-масляной кислоты и 1-[2-(4-хлорометилфенокси)этил]-пиперидина (0,85 г, 3,36 ммоля). Выход 1,07 г, 62%; коричневое масло; MS: 504,4(М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-[4-(2-пиперидин-1 ил-этокси)бензил]-масляной кислоты (3,7 г, 7,3 ммоля) было выделено 2,2 г (выход: 63%) 2-(4 метоксибензолсульфонил)-2-[4-(2-пиперидин-1 ил-этокси)бензил]-масляной кислоты в виде бесцветного полутвердого вещества по методике, которая изложена в примере 9. MS: 476(М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-[4-(2-пиперидин-1-ил-этокси)бензил]масляной кислоты и по методике, которая изложена в примере 1, было выделено 360 мг 2-(4 метоксибензолсульфонил)-2-[4-(2-пиперидин-1 ил-этокси)бензил]-бутирамида в виде коричневого твердого вещества. Выход 16%; т. пл. 75 С;H ЯМР (300 МГц, DMSO-d6):0,90 (т,J=7,1 Гц, 3 Н), 1,36-1,96 (м, 4 Н), 2,4-2,63 (м,14 Н), 3,87 (с, 3 Н), 4,01 (т, J=5,9 Гц, 2 Н), 6,8 (д,J=8,5 Гц, 2 Н), 7,11 (м, 4 Н), 7,71 (д, J=8,8 Гц, 2 Н),9,09 (с, 1 Н), 10,8 (с, 1 Н). Пример 35. Гидроксиамид 2-(4-метоксибензолсульфонил)-2-[4-(2-морфолин-4-илэтокси)бензил]-пентановой кислоты. Этиловый эфир 2-(4-метоксибензолсульфонил)-2-[4-(2-морфолин-4-ил-этокси)бензил]пентановой кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового 2 бромовалериата (8,23 г, 39,3 ммоля) и 4 метокситиофенола (5 г, 35,7 ммоля) было получено 10,46 г данного продукта (100%); прозрачное масло; MS: 269 (М+Н)+. Этиловый эфир 2-(4-метоксибензолсульфонил)-пентановой кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового эфира 2(4-метоксибензолсульфанил)-пентановой кислоты (6,9 г, 27,4 ммоля). Выход 7,07 г (86%); прозрачное масло; MS: 300,9 (M+H)+. По методике, которая изложена в примере 12, был получен этиловый эфир 2-(4-метоксибензолсульфанил)-пентановой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пентановой кислоты (3,0 г,10,8 ммолей) и 4-[2-(хлорометилфенокси)этил]морфолина (3,45 г, 11,9 ммолей). Выход 3,08 г,62%; коричневое масло; MS: 520,4 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-[4-(2-морфолин-4 ил-этокси)бензил]-пентановой кислоты (2,73 г,5,27 ммоля) было выделено по методике, которая изложена в примере 9, 1,45 г (выход: 56%) 2-(4-метоксибензолсульфонил)-2-[4-(2-морфо 001742 42 лин-4-ил-этокси)бензил]-пентановой кислоты в виде бесцветного полутвердого вещества. MS: 492,3 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-[4-(2-морфолин-4-ил-этокси)бензил]пентановой кислоты (1,01 г, 2,05 ммоля) и по методике, которая изложена в примере 1, было выделено 190 мг гидроксиамида 2-(4-метоксибензолсульфонил)-2-[4-(2-морфолин-4-илэтокси)бензил]-пентановой кислоты в виде коричневого твердого вещества. Выход 18%; т. пл. 101 С; MS: 507,4 (М+Н)+; 1H ЯМР (300 МГц, DMSO-d6):0,71 (т, J=7 Гц, 3 Н), 1,58-1,82 (м, 4 Н), 3,12-3,98 (м, 12 Н),3,87 (с, 3 Н), 4,35 (т, 2 Н), 6,89 (д, J=8,7 Гц, 2 Н),7,15 (м, 4 Н), 7,74 (д, J=8,9 Гц, 2 Н), 9,08 (с, 1 Н). Пример 36. Гидроксиамид 2-[4-(2-азепан 1-ил-этокси)бензил]-2-(4-метоксибензолсульфонил)-октановой кислоты. Этиловый эфир 2-[4-(2-азепан-1-илэтокси)бензил]-2-(4-метоксибензолсульфонил)октановой кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового эфира 2 бромооктаноата (11,8 г, 47,3 ммоля) и 4 метокситиофенола (6 г, 43 ммоля). Выход: 7,24 г(57%); прозрачное масло; MS: 312,2 (М+Н)+. Этиловый эфир 2-(4-метоксибензолсульфонил)-октановой кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного метилового эфира 2-(4-метоксибензолсульфанил)-октановой кислоты (4,0 г, 13,6 ммоля). Выход 3,7 г (83%); прозрачное масло; MS: 343,3 (М+Н)+. По методике, которая изложена в примере 12, из исходного этилового эфира 2-(4-метоксибензолсульфонил)-октановой кислоты (1,69 г,5,18 ммолей) и 1-[2-4-хлорометилфенокси)этил]-азепана (1,73 г, 6,0 ммолей) был получен этиловый эфир 2-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-метоксибензолсульфонил)-октановой кислоты. Выход 4,86 г, 99%; коричневое масло; MS: 574,5 (М+Н)+. Из исходного этилового эфира 2-[4-(2 азепан-1-ил-этокси)бензил]-2-(4-метоксибензолсульфонил)-октановой кислоты (4,8 г, 8,37 ммолей) по методике, которая изложена в примере 9, был выделен 1,55 г (выход: 34%) 2-[4-(2 азепан-1-ил-этокси)бензил]-2-(4-метоксибензолсульфонил)-октановой кислоты в виде бесцветного полутвердого вещества. MS: 551 (М+Н)+. Из исходной 2-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-метоксибензолсульфонил)-октановой кислоты и по методике, которая изложена в примере 1, было выделено 300 мг гидроксиамида 2-[4-(2-азепан-1-ил-этокси)бензил]-2-(4 метоксибензолсульфонил)-октановой кислоты. Выход 27%; т. пл. 65 С; MS: 561,6 (М+Н)+; 1H ЯМР (300 МГц, DMSO-d6):0,81 (т,J=6,6 Гц, 3 Н), 1,08-1,82 (м, 14 Н), 3,13-3,51 (м,12 Н), 3,87 (с, 3 Н), 4,33 (т, 2 Н), 6,88 (д, J=8,7 Гц, 43 2 Н), 7,14 (м, 4 Н), 7,7 (д, J=9 Гц, 2 Н), 9,06 (с, 1 Н),10,28 (с, 1 Н). Пример 37. Гидроксиамид 2-(4-метоксибензолсульфанил)-октановой кислоты. Этиловый эфир 2-(4-метоксибензолсульфанил)-октановой кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового 2 бромооктаноата (11,8 г, 47,3 ммоля) и 4 метокситиофенола (6 г, 43 ммоля). Выход: 7,24 г(57%); прозрачное масло; MS: 311,2 (M+H)+. Из исходного этилового эфира 2-(4 метоксибензолсульфанил)-октановой кислоты(3,1 г, 10 ммолей) и по методике, которая изложена в примере 9, было выделено 2,55 г (выход: 90%) 2-(4-метоксибензолсульфанил)-октановой кислоты в виде бесцветного полутвердого вещества. MS: 283 (М+Н)+. Из исходной 2-(4-метоксибензолсульфанил)-октановой кислоты (4,25 г, 16 ммолей) и по методике, которая изложена в примере 1,было выделено 3,64 г гидроксамида 2-(4 метоксибензолсульфанил)-октановой кислоты. Выход: 76%, Т. пл. 90 С; MS: 298,2 (М+Н)+. Пример 38. Гидроксиамид 2-(4-фторофенилсульфанил)-октановой кислоты. Этиловый эфир 2-(4-фторофенилсульфанил)-октановой кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового 2 бромооктаноата (6,47 г, 24,7 ммолей) и 4 фторотиофенола (3 г, 23,4 ммоля). Выход: 6,31 г(90%); прозрачное масло; MS: 299 (М+Н)+. Из исходного этилового эфира 2-(4-фторофенилсульфанил)-октановой кислоты (3,1 г, 10 ммолей) и по методике, которая изложена в примере 9, было выделено 2,89 г (выход: 100%) 2-(4-фторофенилсульфанил)-октановой кислоты в виде бесцветного полутвердого вещества. MS: 268,9 (М+Н)+. Из исходной 2-(4-фторофенилсульфанил)октановой кислоты (2,49 г, 9,2 ммоля) и по методике, которая изложена в примере 1, было выделено 2,72 г гидроксиамида 2-(4-фторофенилсульфанил)-октановой кислоты. Выход: 99%, Т. пл. 58 С; MS: 284 (М+Н)+. Пример 39. Гидроксиамид 2-(1-метил-1 Нимидазол-2-илсульфанил)-октановой кислоты. Этиловый эфир 2-(1-метил-1 Н-имидазол-2 илсульфанил)-октановой кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового 2 бромооктаноата (12,1 г, 48 ммолей) и 1-метил-2 меркаптоимидазола (5 г, 43,8 ммоля). Выход: 12 г (96%); прозрачное масло; MS: (M+H)+. Из исходного этилового эфира 2-(1-метил 1 Н-имидазол-2-илсульфанил)-октановой кислоты (12 г, 42,2 ммоля) и по методике, которая изложена в примере 9, было выделено 10,2 г 44 Из исходной 2-(1-метил-1 Н-имидазол-2 илсульфанил)-октановой кислоты (7,84 г, 30,6 ммоля) и по методике, которая изложена в примере 1, было выделено 2,77 г гидроксиамида 2(1-метил-1 Н-имидазол-2-илсульфанил)-октановой кислоты в виде бесцветного твердого вещества. Выход: 33%, Т. пл. 125 С; MS: 272,2(М+Н)+. Пример 40. N-Гидрокси-2-(4-метоксибензолсульфонил)-3-нафталин-2-ил-пропионамид. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-уксусной кислоты (5,0 г, 20 ммолей) и 2-бромометилнафталин (4,4 г, 20 ммолей). Выход 7,2 г, 91%; бесцветное масло;MS: 399 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-3-нафталин-2-илпропионовой кислоты (3,7 г, 9 ммолей) и по методике, которая изложена в примере 9, было выделено 23,3 г (96%) 2-(4-метоксибензолсульфонил)-3-нафталин-2-ил-пропионовой кислоты.(2,2 г, 5,9 ммолей) и по методике, которая изложена в примере 1, было выделено 820 мг Nгидрокси-2-(4-метоксибензолсульфонил)-3 нафталин-2-ил-пропионамида в виде светлокоричневого твердого вещества. Выход: 36%; т. пл. 161-163 С; MS: 502 (М+Н)+; 1(с, 1 Н), 6,92-7,89 (м, 11 Н). Пример 41. Гидроксиамид N-гидрокси-2(4-метоксифенилметансульфонил)-2-метил-3 фенилпропионовой кислоты. 4-Метоксибензилмеркаптан (7,0 г, 45 ммолей), этиловый 2-бромопропионат (8,2 г, 46 ммолей) и порошковый, высушенный в сушильном шкафу, калийкарбонат (10 г, 72 ммоля) в 150 мл ацетона нагревали при температуре кипения с обратным холодильником в течение 18 ч. Нагретую смесь охлаждали, фильтровали и фильтрат концентрировали. Полученный остаток поглощали 150 мл метиленхлорида, промывали водой (150 мл), обезвоживали над безводным натрийсульфатом и выпаривали с выходом 12 г (99%); бесцветная жидкость; MS: 255,1(М+Н)+. Данный продукт использовали без дальнейшей очистки. К ледяному (5 С) раствору этилового эфира 2-(4-метоксифенилметансульфонил)-пропионовой кислоты (5,7 г, 21 ммоль) в 100 мл CH2Cl2 порциями добавляли (7,2 г, 40 ммолей) nхлоробензойную кислоту и эту смесь мешали в течение 1 ч. Эту реакцию разбавляли гексаном(500 мл) и перемешивали при 25 С в течение 30 мин при комнатной температуре. Полученную смесь фильтровали, а органический слой обрабатывали насыщенным водным натрийбисульфитом (200 мл). Этот гексановый раствор, со 45 держащий указанный продукт промывали водой, обезвоживали (Na2SO4) и концентрировали. Выход 5,5 г (91%); бесцветное масло; MS 287,1(М+Н)+. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксифенилметансульфонил)-2-метил-3-фенилпропионовой кислоты из исходного этилового эфира 2-(4-метоксифенилметансульфонил)-пропионовой кислоты (2 г, 7 ммолей) и бензилбромида (1,3 г, 7,7 ммолей). Выход 3,0 г, 100%; легкоплавкое твердое вещество; MS: 377 (М+Н)+. 2-(4-Метоксифенилметансульфонил)-2 метил-3-фенилпропионовая кислота была получена из исходного этилового эфира 2-(4 метоксифенилметансульфонил)-2-метил-3 фенилпропионовой кислоты, растворенного в метаноле (50 мл) и 10N NaOH (30 мл). Полученную реакционную смесь обрабатывали, как изложено в примере 9. Выход 930 мг, 31%. Бесцветное твердое вещество, т. пл. 106-108 С; MS: 347 (М-Н)+. Из исходной 2-(4-метоксифенилметансульфонил)-2-метил-3-фенилпропионовой кислоты(2,7 г, 7,0 ммолей) и по методике, которая изложена в примере 1, было выделено 266 мг гидроксиамида N-гидрокси-2-(4-метоксифенилметансульфонил)-2-метил-3-фенилпропионовой кислоты в виде ахроматически белого твердого вещества. Выход: 10%; т. пл. 58-59 С; MS: 364,2(д, 1H), 4,69-4,74 (д, 1 Н), 6,94-6,98 (д, 2 Н), 7,297,33 (д, 4 Н), 9,24 (с, 1H), 10,88 (с, 1H). Пример 42. Гидроксиамид 5-метил-2-(3 метил-бут-2-енил)-2-(толуол-4-сульфонил)-гекс 4-еновой кислоты. Этиловый эфир 5-метил-2-(3-метил-бут-2 енил)-2-(толуол-4-сульфонил)-гекс-4-еновой кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового -(р-толуолсульфонил) ацетата (2,9 г, 10,9 ммолей) и 4-бромо-2 метилбутена (3,42 г, 23 ммоля). Выход 4,6 г; дубильное масло; MS: 379,2 (М+Н)+. 5-метил-2-(3-метил-бут-2-енил)-2-(толуол 4-сульфонил)-гекс-4-еновая кислота была получена в соответствии с общим способом, который изложен в примере 9. Из исходного этилового эфира 5-метил-2-(3-метил-бут-2-енил)-2-(толуол-4-сульфонил)-гекс-4-еновой кислоты (4,5 г,11 ммолей), этанола (15 мл) и 10N натрийгидроксида. Из исходной 5-метил-2-(3-метил-бут-2 енил)-2-(толуол-4-сульфонил)-гекс-4-еновой кислоты (4,1 г, 11 ммолей) и по методике, которая изложена в примере 1, было выделено 1,07 г гидроксиамида 5-метил-2-(3-метил-бут-2-енил)2-(толуол-4-сульфонил)-гекс-4-еновой кислоты 46 в виде бесцветного твердого вещества. Выход: 30%; т. пл. 108-110 С; MS: 366,2 (М+Н)+; 1 Н ЯМР (300 МГц, DMSO-d6):1,49 (с,6 Н), 1,62 (с, 6 Н), 2,41 (с, 3 Н), 2,53-2,63 (м, 4 Н),5,00-5,05 (т, 2 Н), 7,40-7,43 (д, 2 Н), 7,59-7,62 (д,2 Н), 9,04 (с, 1 Н), 10,80 (с, 1 Н). Пример 43. Гидроксиамид 2-метил-2-(2 метилфуран-3-сульфонил)-3-фенилпропионовой кислоты. Этиловый эфир 2-метил-2-(2-метилфуран 3-сульфонил)-3-фенилпропионовой кислоты(полученный из 3-меркапто-2-метилфурана) был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового эфира 2-метил-2-(2-метилфуран-3 сульфонил)-3-фенилпропионовой кислоты (2,9 г, 11,9 ммолей), бензилбромида (2,22 г, 13 ммолей) и калийкарбоната (10 г) в ацетоне (75 мл). Выход (99%); амбровое масло; MS: 337,1(М+Н)+. 2-Метил-2-(2-метилфуран-3-сульфонил)-3 фенилпропионовая кислота была получена в соответствии с общим способом, который изложен в примере 9. Из исходного этилового эфира 2-метил-2-(2-метилфуран-3-сульфонил)-3 фенилпропионовой кислоты (4,8 г, 14,3 ммоля),растворенного в этаноле (25 мл) и 10N натрийгидроксида (10 мл). Выход 3,7 г (84%), белое твердое вещество, MS: 307,4 (М+Н)+. Из исходной 2-метил-2-(2-метилфуран-3 сульфонил)-3-фенилпропионовой кислоты (3,58 г, 12 ммолей) и по методике, которая изложена в примере 1, было выделено 1,078 г гидроксиамида 2-метил-2-(2-метилфуран-3-сульфонил)-3 фенилпропионовой кислоты в виде оранжевого твердого вещества. Выход: 29%; т. пл. 68-70 С;H ЯМР (300 МГц, DMSO-d6):1,27 (с,3 Н), 2,81-2,86 (д, 1 Н), 3,33 (с, 3 Н), 3,61-3,66 (д,1 Н), 6,66 (с, 1 Н), 7,19-7,25 (м, 5 Н), 7,76 (с, 1 Н),9,09 (с, 1 Н), 10,81 (с, 1 Н). Пример 44. Гидроксиамид 2-метил-2-(2 метилфуран-3-сульфонил)-3-[4-(2-пиперидин-1 ил-этокси)фенил]-пропионовой кислоты. Этиловый эфир 2-метил-2-(2-метилфуран 3-сульфонил)-3-[4-(2-пиперидин-1-ил-этокси)фенил]-пропионовой кислоты был получен в соответствии с общим способом, который изложен в примере 9. Из исходного этилового эфира 2-(2-метилфуран-3-сульфонил)-пропионовой кислоты (2,4 г, 9,8 ммолей) и 1-[2-(4-хлорометилфенокси)этил]-пиперидина (2,96 г, 10,7 ммолей). Выход 2,4 г (92%); амбровое масло;MS: 464,2 (М+Н)+. 2-Метил-2-(2-метилфуран-3-сульфонил)-3[4-(2-пиперидин-1-ил-этокси)фенил]-пропионовая кислота была получена в соответствии с общим способом, который изложен в примере 1,из исходного этилового эфира 2-метил-2-(2 метилфуран-3-сульфонил)-3-[4-(2-пиперидин-1 ил-этокси)фенил]-пропионовой кислоты (2,01 г, 47 4,5 ммоля), растворенного в этаноле (20 мл) и 10N натрийгидроксида (10 мл). Полученную смесь обрабатывали, как изложено в примере 9. Выход 2,03 г; амбровые кристаллы, т. пл. 6668 С; MS: 434 (М+Н)+. Из исходной 2-метил-2-(2-метилфуран-3 сульфонил)-3-[4-(2-пиперидин-1-ил-этокси)фенил]-пропионовой кислоты (2,03 г, 6, ммолей) и по методике, которая изложена в примере 1,было выделено 1,36 г гидроксиамида 2-метил-2(2-метилфуран-3-сульфонил)-3-[4-(2-пиперидин-1-ил-этокси)фенил]-пропионовой кислоты в виде твердого вещества амбрового цвета. Выход: 32%; т. пл. 115-117 С; MS: 451,1 (М+Н)+; 1(м, 2 Н), 1,75 (с, 3 Н), 1,78 (с, 3 Н), 2,98-3,03 (м,2 Н), 3,42-3,47 (м, 2 Н), 3,5 (с, 3 Н), 6,65 (с, 1 Н),6,87-6,90 (д, 2 Н), 7,12-7,17 (д, 2 Н), 10,35 (с, 1 Н),10,60 (с, 1 Н), 11,70 (с, 1 Н). Пример 45. Гидроксиамид 2-метил-3-[4-(2 пиперидин-1-ил-этокси)фенил-2-(тиофен-2 сульфонил)-пропионовой кислоты. Этиловый эфир 2-метил-3-[4-(2-пиперидин-1-ил-этокси)фенил-2-(тиофен-2-сульфонил)-пропионовой кислоты был получен в соответствии с общим способом, который изложен в примере 9, из исходного этилового эфира 2 тиофен-2-сульфонил)-пропионовой кислоты(полученного из 2-меркаптотиофена и этилэфира 2-бромопропионовой кислоты) (4,4 г, 17,7 ммоля) и 1-[2-(4-хлорометилфенокси)этил] пиперидина (5,3 г, 19,5 ммолей). Выход (96%); полутвердое вещество; MS: 466. 2-Метил-3-[4-(2-пиперидин-1-ил-этокси)фенил-2-(тиофен-2-сульфонил)-пропионовая кислота была получена в соответствии с общим способом, который изложен в примере 9, из исходного этилового эфира 2-метил-3-[4-(2 пиперидин-1-ил-этокси)фенил-2-(тиофен-2 сульфонил)-пропионовой кислоты (9,8 г, 20 ммолей), растворенного в этаноле (20 мл) и 10N натрийгидроксида (20 мл). Полученную смесь обрабатывали, как изложено в примере 1. Выход 4,5 г (49%); белое твердое вещество с т. пл. 170172 С; MS: 436,3 (М-Н). Из исходной 2-метил-3-[4-(2-пиперидин-1 ил-этокси)фенил-2-(тиофен-2-сульфонил)-пропионовой кислоты (3,6 г, 8,0 ммолей) и по методике, которая изложена в примере 1, было выделено 345 мг гидроксиамида 2-метил-3-[4-(2 пиперидин-1-ил-этокси)-фенил-2-(тиофен-2 сульфонил)-пропионовой кислоты в виде ахроматически белого твердого вещества; выход: 10%; т. пл. 115-118 С; MS: 451,2 (M+Н)+; 1 48 Пример 46. Гидроксиамид 2-(октан-1 сульфонил)-3-[4-(2-пиперидин-ил-этокси)фенил]пропионовой кислоты. Этиловый эфир 2-(октан-1-сульфонил)-3[4-(2-пиперидин-ил-этокси)-фенил]-пропионовой кислоты был получен в соответствии с общим способом, который изложен в примере 9,из исходного этилового эфира 2-(октан-1 сульфонил)-пропионовой кислоты (5,0 г, 18 ммолей) и 1-[2-(4-хлорометилфенокси-этил]пиперидина (5,6 г, 19,7 ммоля). Выход 8,9 г(96%); амбровое масло; MS: 495. 2-(Октан-1-сульфонил)-3-[4-(2-пиперидинил-этокси)-фенил]-пропионовая кислота была получена в соответствии с общим способом,который изложен в примере 9, из исходного этилового эфира 2-(октан-1-сульфонил)-3-[4-(2 пиперидин-ил-этокси)-фенил]-пропионовой кислоты (8,9 г, 18 ммолей), этанола (25 мл) и 10N натрийгидроксида (25 мл). Выход 6,0 г (72%). Из исходной 2-(октан-1-сульфонил)-3-[4(2-пиперидин-ил-этокси)-фенил]-пропионовой кислоты (3,6 г, 7,7 ммолей) и по методике, которая изложена в примере 1, было выделено 3,3 г гидроксиамида 2-(октан-1-сульфонил)-3-[4-(2 пиперидин-ил-этокси)-фенил]-пропионовой кислоты в виде дубильного твердого вещества; выход: 89%; т. пл. 69-70 С; MS: 483,2 (М+Н)+; 1(д, 2 Н), 9,16 (с, 1 Н), 10,70 (с, 1 Н). Пример 47. Гидроксиамид 3-бифенил-4-ил 2-метил-2-(1-метил-1 Н-имидазол-2-сульфонил)пропионовой кислоты. Этиловый эфир 3-бифенил-4-ил-2-метил-2(1-метил-1 Н-имидазол-2-сульфонил)-пропионовой кислоты был получен в соответствии с общим способом, который изложен в примере 9,из исходного этилового эфира 2-метил-(1 метил-1 Н-имидазолсульфонил)-пропионовой кислоты (полученного из (1-метил-2-меркаптоимидазола и 2-бромоэтилпропионата) (3,0 г,12,2 ммоля) и 4-хлорометилбифенила (2,97 г, 15 ммолей). Выход 5,9 г (99%); легкоплавкое твердое вещество; MS: 413 (М+Н)+. 3-Бифенил-4-ил-2-метил-2-(1-метил-1 Нимидазол-2-сульфонил)-пропионовая кислота была получена в соответствии с общим способом, который изложен в примере 9. Из исходного этилового эфира 3-бифенил-4-ил-2-метил-2(1-метил-1 Н-имидазол-2-сульфонил)-пропионовой кислоты (5,0 г, 11,9 ммолей), этанола (15 мл) и 10N натрийгидроксида (10 мл). Выход 2,8 г (61%); коричневое твердое вещество с т. пл. 119-122 С; MS: 385,2 (М+Н). Из исходной 3-бифенил-4-ил-2-метил-2-(1 метил-1 Н-имидазол-2-сульфонил)-пропионовой кислоты (2,8 г, 7,0 ммолей) и по методике, которая изложена в примере 1, было выделено 112 мг гидроксиамида 3-бифенил-4-ил-2-метил-2-(1 метил-1 Н-имидазол-2-сульфонил)-пропионовой 49 кислоты в виде твердого вещества цвета танина; выход: 4%; т. пл. 112 С; MS: 451,2 (М+Н)+; 1H ЯМР (300 МГц, DMSO-d6):0,911 (с,3 Н), 3,3 (с, 3 Н), 3,5 (д, 1 Н), 6,8 (д, 1 Н), 6,9 (д,1 Н), 7,18-7,66 (м, 5 Н), 7,30-7,33 (д, 2 Н), 7,557,58 (д, 2 Н). Пример 48. Гидроксиамид 2-метил-3 фенил-2-(тиофен-2-сульфонил)-пропионовой кислоты. Этиловый эфир 2-метил-3-фенил-2(тиофен-2-сульфонил)-пропионовой кислоты был получен в соответствии с общим способом,который изложен в примере 9, из исходного этилового эфира 2-(тиофен-2-сульфонил)пропионовой кислоты (3,0 г, 12 ммолей) и бензилбромида (2,48 г, 15 ммолей). Выход 5,2 г(%); таниновое масло; MS: 339,1 (М+Н). 2-Метил-3-фенил-2-(тиофен-2-сульфонил)пропионовая кислота была получена в соответствии с общим способом, который изложен в примере 9, из исходного этилового эфира 2 метил-3-фенил-2-(тиофен-2-сульфонил)пропионовой кислоты (5,0 г, 15 ммолей), этанола (30 мл) и 10N натрийгидроксида (10 мл). Выход 5,6 г, MS: 310,0 (М+Н). Из исходной 2-метил-3-фенил-2-(тиофен 2-сульфонил)-пропионовой кислоты (5,0 г, 16 ммолей) и по методике, которая изложена в примере 1, было выделено 1,8 г гидроксиамида 2-метил-3-фенил-2-(тиофен-2-сульфонил)пропионовой кислоты в виде бесцветного твердого вещества; выход: 40%; т. пл. 116-117 С;H ЯМР (300 МГц, DMSO-d6):1,29 (с,3 Н), 3,33 (д, 1H), 3,69 (д, 1H), 7,18-7,30 (м, 5 Н),7,74 (м, 1 Н), 9,13 (с, 1H), 10,80 (с, 1H). Пример 49. Гидроксиамид 2-[8-(1 карбоксиэтансульфонил)-октан-1-сульфонил]пропионовой кислоты. Этиловый эфир 2-[8-(1-карбоксиэтансульфонил)-октан-1-сульфонил]-пропионовой кислоты был получен в соответствии с общим способом, который изложен в примере 9, из исходного этилового эфира 2-[8-(1-этоксикарбонилэтилсульфанил)-октилсульфанил]-пропионовой кислоты (10,2 г, 26 ммолей) и пероксимоноперсульфата натрия (64 г, 104 ммоля). Выход 9,87 г (86%); бесцветная жидкость; MS: 442,9 (М+Н). 2-[8-(1-Карбоксиэтансульфонил)-октан-1 сульфонил]-пропионовая кислота была получена в соответствии с общим способом, который изложен в примере 1. Из исходного этилового эфира 2-[8-(1-карбоксиэтансульфонил)-октан-1 сульфонил]-пропионовой кислоты (3,0 г, 6,8 ммолей), этанола (15 мл) и 10N натрийгидроксида (15 мл). Выход 2,7 г (98%); белое твердое вещество с т. пл. 99-102 С; MS: 387 (М+NН 3)+. Из исходной 2-[8-(1-карбоксиэтансульфонил)-октан-1-сульфонил]-пропионовой кислоты и по методике, которая изложена в примере 1, 001742 50 был выделен 641 мг гидроксиамида 2-[8-(1 карбоксиэтансульфонил)-октан-1-сульфонил]пропионовой кислоты в виде масла цвета амбры; выход: 23%; MS: 434,0 (М+Н)+; 1(м, 22 Н), 3,33 (м, 2 Н), 8,9 (с, 1H), 9,28 (с, 1H). Пример 50. Гидроксиамид 2-(4-бромобензолсульфонил)-2-метил-3-[4-(2-пиперидин-1 ил-этокси)-фенил]-пропионовой кислоты. Этиловый эфир 2-(4-бромобензолсульфонил)-2-метил-3-[4-(2-пиперидин-1-ил-этокси)фенил]-пропионовой кислоты был получен в соответствии с общим способом, который изложен в примере 9, из исходного этилового -(4 бромофенилсульфонил)ацетата (5,0 г, 16 ммолей) и 1-[2-(4-хлорометилфенокси)-этил]-пиперидина (4,97 г, 16 ммолей). Выход 6,1 г (71%); таниновое масло; MS: 541,1 (М+Н)+. 2-(4-Бромобензолсульфонил)-2-метил-3-[4(2-пиперидин-1-ил-этокси)-фенил]-пропионовая кислота была получена в соответствии с общим способом, который изложен в примере 9, из исходного этилового эфира 2-(4-бромобензолсульфонил)-2-метил-3-[4-(2-пиперидин-1-илэтокси)-фенил]-пропионовой кислоты (6,5 г, 20 ммолей), этанола (30 мл) и 10N натрийгидроксида (15 мл). Выход 6,3 г (100%); желтое твердое вещество с т. пл. 125-127 С; MS: 512,5(М+Н)+. Из исходной 2-(4-бромобензолсульфонил)2-метил-3-[4-(2-пиперидин-1-ил-этокси)-фенил]пропионовой кислоты и по методике, которая изложена в примере 1, было выделено 1,07 г гидроксиамида 2-(4-бромобензолсульфонил)-2 метил-3-[4-(2-пиперидин-1-ил-этокси)-фенил]пропионовой кислоты в виде желтого твердого вещества; выход: 17%; MS: 525,4 (М+Н)+. Пример 51. 3-(4-Бромофенил)-N-гидрокси 2-(4-метоксибензолсульфонил)-2-метилпропионамид. По методике, которая изложена в примере 9, был получен этиловый эфир 3-(4-бромофенил)-N-гидрокси-2-(4-метоксибензолсульфонил)-2-метилпропионовой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты (3,0 г, 11 ммолей) и 4-бромбензилбромида (3,0 г, 12 ммолей). Выход 4,67 г, 96%; бесцветное масло; MS: 441(М+Н)+. 3-(4-Бромофенил)-2-(4-метоксибензолсульфонил)-2-метилпропионовая кислота была получена из исходного этилового эфира 3-(4 бромофенил)-2-(4-метоксибензолсульфонил)-2 метилпропионовой кислоты (4,0 г, 9,0 ммолей),растворенного в метаноле (50 мл) и 10N NaOH(30 мл). Полученную реакционную смесь обрабатывали, как изложено в примере 9. Выход 3,0 г, 78%. Легкоплавкое твердое вещество. MS: 413 (M+H)+. Из исходной 3-(4-бромофенил)-2-(4 метоксибензолсульфонил)-2-метилпропионовой 51 кислоты (2,7 г, 6,5 ммолей) и по методике, которая изложена в примере 1, было выделено 2,26 г 3-(4-бромофенил)-N-гидрокси-2-(4-метоксибензолсульфонил)-2-метилпропионамида в виде ахроматически белого твердого вещества; выход: 81%; т. пл. 86-88 С; MS: 429,8 (М+Н)+; 1H ЯМР (300 МГц, CDCl3):1,42 (с, 3 Н),1,77 (ушир. с, 1 Н), 3,26 (д, J=7,0 Гц, 1 Н), 3,68 (д,J=7,0 Гц, 1 Н), 3,85 (с, 3 Н), 7,01-7,76 (м, 8 Н),9,71-9,88 (ушир. с, 1 Н). Пример 52. N-гидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-нафталин-2-ил-пропионамид. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2-метил-3-нафталин-2-илпропионовой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты и 2-бромометилнафталина (4,4 г,20 ммолей). Выход 8,0 г, 97%; бесцветные кристаллы, т. пл. 182-184 С; MS: 413 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метил-3-нафталин 2-ил-пропионовой кислоты (4,6 г, 11 ммолей) по методике, которая изложена в примере 9, было выделено 4,2 г (98%) 2-(4-метоксибензолсульфонил)-2-метил-3-нафталин-2-ил-пропионовой кислоты в виде бесцветных кристаллов. Т. пл. 144-146 С; MS: 384,9 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-3-нафталин-2-ил-пропионовой кислоты (2,4 г, 6,2 ммоля) и по методике, которая изложена в примере 1, было выделено 1,6 гN-гидрокси-2-(4-метоксибензолсульфонил)-2 метил-3-нафталин-2-ил-пропионамида в виде ахроматически белого твердого вещества; выход: 64%; т. пл. 185-187 С; MS: 400,2; 1 Н ЯМР (300 МГц, СDСl3):1,56 (с, 3 Н),3,28 (д, J=8,0 Гц, 1 Н), 3,81 (д, J=8 Гц, 1 Н), 3,93(с, 3 Н), 4,88 (ушир.с, 1 Н), 7,02-7,92 (м, 11 Н). Пример 53. N-Гидрокси-2-(4-метоксибензолсульфонил)-3-метил-бутирамид. Этиловый эфир 2-(4-метоксибензолсульфонил)-3-метил-бутирамида был получен в соответствии с общим способом, который изложен в примере 1. Из исходного этилового 2 бромо-3-метил-бутаноата (20,9 г, 100 ммолей) и 4-метоксибензолтиола (14,0 г, 100 ммолей) было выделено 30 г этилового эфира 2-(4-метоксифенилсульфанил)-3-метилмасляной кислоты. Выход 99%; светло-желтое масло; MS: 269(M+H)+. Из исходного этилового эфира 2-(4 метоксифенилсульфанил)-3-метилмасляной кислоты (2,68 г, 10 ммолей) и по методике, которая изложена в примере 9 для окисления, было выделено 3 г этилового эфира этилового эфира 2-(4-метоксифенилсульфанил)-3-метилмасляной кислоты в виде бесцветного твердого вещества. Выход: 99%; т. пл. 53 С; MS: 273 (M+H)+. 52 Из исходного этилового эфира 2-(4 метоксифенилсульфанил)-3-метилмасляной кислоты (3,0 г, 10 ммолей) по методике, которая изложена в примере 9, было выделено 2,7 г(96%) 2-(4-метоксифенилсульфанил)-3-метилмасляной кислоты в виде бесцветного твердого вещества. Т. пл. 96 С; MS: 273 (M+H)+. Из исходной 2-(4-метоксифенилсульфанил)-3-метилмасляной кислоты (2,0 г, 7,34 ммоля) и по методике, которая изложена в примере 9, было выделено 590 мг N-гидрокси-2-(4 метоксибензолсульфонил)-3-метил-бутирамида в виде бесцветного твердого вещества. Т. пл. 220 С; выход 28%; MS: 288 (M+H)+; 1(ушир.с, 1 Н), 3,53 (д, J=9, 1H), 7,12-7,17 (м, 2 Н),7,74-7,79 (м, 2 Н). Пример 54. Гидроксиамид 1-(4-метоксибензолсульфонил)-циклопентанкарбоновой кислоты. По методике, которая изложена в примере 9, был получен этиловый эфир 1-(4-метоксибензолсульфонил)-циклопентанкарбоновой кислоты из исходного этилового эфира 2-(4 метоксибензолсульфонил)-уксусной кислоты и 1,4-дибромбутана (2,4 г, 7,6 ммолей). Выход 2,4 г, 78%; бесцветное твердое вещество, т. пл. 86-88 С; MS: 313 (M+H)+. 1-(4-метоксибензолсульфонил)-циклопентанкарбоновая кислота была получена из исходного этилового эфира 1-(4-метоксибензолсульфонил)-циклопентанкарбоновой кислоты (2,2 г,7,0 ммолей), растворенного в метаноле (50 мл) и 10N NaOH (30 мл). Полученную реакционную смесь обрабатывали, как изложено в примере 9. Выход 1,66 г, 83%. Бесцветное твердое вещество; т. пл. 112-115 С; MS: 285 (М+Н)+. Из исходной 1-(4-метоксибензолсульфонил)-циклопентанкарбоновой кислоты (442 мг,1,5 ммоля) и по методике, которая изложена в примере 1, было выделено 410 мг гидроксиамида 1-(4-метоксибензолсульфонил)-циклопентанкарбоновой кислоты в виде бесцветного твердого вещества с т. пл. 89-91 С; выход 88%; MS: 400,2; 1(ушир.с, 1 Н). Пример 55. 3-(2-Бромофенил)-N-гидрокси 2-(4-метоксибензолсульфонил)-2-метилпропионамид. По методике, которая изложена в примере 9, был получен этиловый эфир 3-(2-бромофенил)-2-(4-метоксибензолсульфонил)-2-метилпропионовой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты (2,0 г, 7,3 ммоля) и 2(бромо)бензилбромида (2,0 г, 8 ммолей). Выход 3,1 г, 87%; бесцветное масло; MS; 441 (М+Н)+. 3-(2-Бромофенил)-2-(4-метоксибензолсульфонил)-2-метилпропионовая кислота была получена из исходного этилового эфира 3-(2 бромофенил)-2-(4-метоксибензолсульфонил)-2 метилпропионовой кислоты (3,0 г, 68 ммолей),растворенного в метаноле (50 мл) и 10N NaOH(30 мл). Полученную реакционную смесь обрабатывали, как изложено в примере 9. Выход 1,7 г, 63%. Воскообразное твердое вещество;MS: 414 (М+Н)+. Из исходной 3-(2-бромофенил)-2-(4 метоксибензолсульфонил)-2-метилпропионовой кислоты (470 мг, 1,1 ммоля) и по методике, которая изложена в примере 9, было выделено 380 мг 3-(2-бромофенил)-N-гидрокси-2-(4-метоксибензолсульфонил)-2-метилпропионовой кислоты в виде бесцветного твердого вещества. Т. пл. 93-96 С; выход 77%; MS: 400,2; 1(с, 3 Н), 6,92-7,89 (м, 8 Н). Пример 56. Гидроксиамид 2-(4-метоксибензолсульфонил)-2-метил-5-фенил-пент-4 еновой кислоты. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2-метил-5-фенил-пент-4 еновой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты и циннамилбромида (2,1 г, 11 ммолей). Выход 3,51 г, 82%; бесцветное масло; MS: 389(М+Н)+. 2-(4-Метоксибензолсульфонил)-2-метил-5 фенил-пент-4-еновая кислота была получена из исходного этилового эфира 2-(4-метоксибензолсульфонил)-2-метил-5-фенил-пент-4 еновой кислоты (3,0 г, 11 ммолей), растворенного в метаноле (50 мл) и 10N NaOH (30 мл). Полученную реакционную смесь обрабатывали,как изложено в примере 9. Выход 1,9 г, 68%; желтоватое масло; MS: 361 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-5-фенил-пент-4-еновой кислоты(440 мг, 1,2 ммоля) и по методике, которая изложена в примере 1, было выделено 420 мг гидроксиамида 2-(4-метоксибензолсульфонил)-2 метил-5-фенил-пент-4-еновой кислоты в виде бесцветного твердого вещества. Т. пл. 162164 С; выход 92%; MS: 376; 1H ЯМР (300 МГц, CDCl3):1,41 (с, 3 Н),3,0-3,16 (м, 1 Н), 3,30 (д, J=11 Гц, 2 Н), 3,92 (с,3 Н), 5,9-6,1 (м, 1 Н), 6,53 (д, J=11 Гц, 1 Н), 7,17,72 (м, 9 Н), 9,12 (ушир.с, 1 Н). Пример 57. Гидроксиамид 2-(4-метоксибензолсульфонил)-5-фенил-2-(3-фенил-пропил)пентановой кислоты. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-5-фенил-2-(3-фенил-пропил)пентановой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-уксусной 54 кислоты (4,0 г, 15,8 ммолей) и 3-бромопропилбензола (6,4 г, 32 ммоля). Выход 3,7 г, 47%; бесцветное масло; MS: 495 (М+Н)+. 2-(4-Метоксибензолсульфонил)-5-фенил-2(3-фенил-пропил)-пентановая кислота была получена из исходного этилового эфира 2-(4 метоксибензолсульфонил)-5-фенил-2-(3-фенилпропил)-пентановой кислоты (2,0 г, 4 ммоля),растворенного в метаноле (50 мл) и 10N NaOH(30 мл). Полученную реакционную смесь обрабатывали, как изложено в примере 9. Выход 1,18 г, 63%. Воскообразное твердое вещество;MS: 449,2 (М+Н-Н 2O)+. Из исходной 2-(4-метоксибензолсульфонил)-5-фенил-2-(3-фенил-пропил)-пентановой кислоты (600 мг, 1,2 ммоля) и по методике,которая изложена в примере 1, было выделено 420 мг гидроксиамида 2-(4-метоксибензолсульфонил)-5-фенил-2-(3-фенил-пропил)-пентановой кислоты в виде бесцветного твердого вещества. Т. пл. 118-120 С; выход 68%; MS: 482; 1H ЯМР (300 МГц, СDСl3):1,52-1,68 (м,2 Н), 1,74-1,92 (м, 2 Н), 1,98-2,20 (м, 4 Н), 2,582,72 (м, 4 Н), 3,86 (с, 3 Н), 6,93 (д, J=11 Гц, 2 Н),7,02-7,63 (м, 10 Н), 7,81 (д, J=11 Гц, 2 Н). Пример 58. Гидроксиамид 2-аллил-2-(4 метоксибензолсульфонил)-пент-4-еновой кислоты. По методике, которая изложена в примере 9, был получен этиловый эфир 2-аллил-2-(4 метоксибензолсульфонил)-пент-4-еновой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-уксусной кислоты (3,0 г, 11,6 ммоля) и аллилбромида (4 мл, избыток). Выход 3,6 г, 92%; желтое масло; MS: 338 (М+Н)+. 2-Аллил-2-(4-метоксибензолсульфонил)пент-4-еновая кислота была получена из исходного этилового эфира 2-аллил-2-(4-метоксибензолсульфонил)-пент-4-еновой кислоты (2,3 г,6,5 ммоля), растворенного в метаноле (50 мл) и 10N NaOH) (30 мл). Полученную реакционную смесь обрабатывали, как изложено в примере 9. Выход 1,76 г, 87%; желтоватое масло; MS: 311(M+H)+. Из исходной 2-аллил-2-(4-метоксибензолсульфонил)-пент-4-еновой кислоты (1,5 г, 4,8 ммоля) и по методике, которая изложена в примере 1, было выделено 1,5 г гидроксиамида 2 аллил-2-(4-метоксибензолсульфонил)-пент-4 еновой кислоты в виде бесцветного твердого вещества. Т. пл. 114-116 С; выход 99%; MS: 326; 1psi в течение 4 ч. По окончании гидрирования данная реакционная смесь была отфильтрована,а метанол удален. Полученное твердое вещество было кристаллизовано из метанола. Выход: 250 мг, 75%; MS: 326; 1(с, 3 Н), 6,04 (ушир.с, 1 Н), 6,97 (д, J=9 Гц, 2 Н),7,76 (д, J=9 Гц, 2 Н). Пример 60. 2-Бензил-N-гидрокси-2-(4 метоксибензолсульфонил)-3-фенилпропионамид. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-3-фенилпропионовой кислоты из исходного этилового эфира 2-(4 метоксибензолсульфонил)-уксусной кислоты(М+Н)+. 2-Бензил-2-(4-метоксибензолсульфонил)-3 фенилпропионовая кислота была получена из этилового эфира 2-бензил-2-(4-метоксибензолсульфонил)-3-фенилпропионовой кислоты(1,0 г, 2,2 ммоля), растворенного в метаноле (50 мл) и 10N NaOH (30 мл). Полученную реакционную смесь обрабатывали, как изложено в примере 9. Выход: 580 мг, 62%; воскообразное твердое вещество; MS: 409 (М-Н)-. Из исходной 2-бензил-2-(4-метоксибензолсульфонил)-3-фенилпропионовой кислоты 9410 мг, 1 ммоль и по методике, которая изложена в примере 1, было выделено 225 мг 2 бензил-N-гидрокси-2-(4-метоксибензолсульфонил)-3-фенилпропионамида в виде воскообразного твердого вещества. Выход 52%; MS: 426; 1H ЯМР (300 МГц, СDСl3):3,25 (д, J=14 Гц, 2 Н), 3,52 (д, J=14 Гц, 2 Н), 3,9 (с, 3 Н), 6,93 (д,J=8 Гц, 2 Н), 7,02-7,26 (м, 9 Н), 7,61 (д, J=8 Гц,2 Н), 7,87 (д, J=4 Гц, 1 Н), 9,58 (ушир.с, 1 Н). Пример 61. N-Гидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-пиридин-3-ил-пропионамид. К перемешиваемому раствору из этилового эфира 2-(4-метоксибензолсульфонил)пропионовой кислоты (2,7 г, 10 ммолей), 3 пиколилхлорид-гидрохлорида (3,2 г, 20 ммолей) и триэтиламмонийхлорида (1 г) в метиленхлориде (400 мл) было добавлено 10N NaOH (30 мл). Полученную реакцию продолжали выдерживать при комнатной температуре в течение 48 ч. По окончании выдерживания отделяли органический слой и тщательно промывали его водой. Отделенный органический слой обезвоживали, фильтровали и концентрировали. Полученный неочищенный продукт очищали с помощью силикагелевой колоночной хроматографии. Колонку элюировали с помощью 50%-ного этилацетат:гексана. Этиловый эфир 2-(4 001742 56 метоксибензолсульфонил)-2-метил-3-пиридин 3-ил-пропионовой кислоты был выделен в виде коричневого масла. Выход 3,0 г, 82%; коричневое масло; MS: 364 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метил-3-пиридин 3-ил-пропионовой кислоты (2,5 г, 6,8 ммоля) по методике, которая изложена в примере 9, было выделено 1,8 г (79%) 2-(4-метоксибензолсульфонил)-2-метил-3-пиридин-3-ил-пропионовой кислоты в виде бесцветного твердого вещества. Т. пл. 58 С; MS: 336 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-3-пиридин-3-ил-пропионовой кислоты (410 мг, 1 ммоль) и по методике, которая изложена в примере 1, было выделено 225 мг Nгидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-пиридин-3-ил-пропионамида в виде бесцветного твердого вещества. Выход 52%; т. пл. 98 С; MS: 351; 1(д, J=9,0, 1H), 3,65 (д, J=9,1, 1H), 3,9 (с, 3 Н), 78,5 (м, 8 Н). Пример 62. Гидроксиамид 2-(4-метоксибензолсульфонил)-2-пиридин-3-илметилдекановой кислоты. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-уксусной кислоты(7,5 г, 29 ммолей) и 1-бромооктана (6,7 г, 35 ммолей) и по методике, которая изложена в примере 9, было выделено 8 г монооктилового соединения, этилового эфира 2-(4-метоксибензолсульфонил)-декановой кислоты. Выход: 8,0 г 74%; MS: 370 (М+Н)+. По методике, которая изложена в примере 29, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2-пиридин-3-илметилдекановой кислоты из исходного этилового эфира 2-(4 метоксибензолсульфонил)-декановой кислоты(8,0 г, 21,6 ммолей) и 3-пиколилхлорид-гидрохлорид (4,1 г, 25 ммолей). Выход 6,5 г, 68%; коричневое масло; MS: (M+H)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-пиридин-3-илметилдекановой кислоты (5,0 г, 11 ммолей) по методике, которая изложена в примере 9, было выделено 4,5 г (91%) 2-(4-метоксибензолсульфонил)-2-пиридин-3-илметилдекановой кислоты. Т. пл. 159 С; MS: 434 (M+H)+. Из исходной 2-(4-метоксибензолсульфонил)-2-пиридин-3-илметилдекановой кислоты(2,5 г, 5,7 ммолей) и по методике, которая изложена в примере 1, было выделено 1,4 г гидроксиамида 2-(4-метоксибензолсульфонил)-2 пиридин-3-илметилдекановой кислоты в виде бесцветного твердого вещества. Выход: 50%; т. пл. 62 С; MS: 448; 1 57 Пример 63. Гидроксиамид 2-(4-метоксибензолсульфонил)-5-метил-2-пиридин-3-илметил-гекс-4-еновой кислоты. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-5-метил-гекс-4-еновой кислоты из исходного этилового эфира 2-(4 метоксибензолсульфонил)-уксусной кислотыMS: (М+Н)+. По методике, которая изложена в примере 29, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-5-метил-2-пиридин-3-илметил-гекс-4-еновой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-5 метил-гекс-4-еновой кислоты (4,0 г, 12,2 ммоля) и 3-пиколилхлорид-гидрохлорида (2,1 г, 13 ммолей). Выход 4,14 г, 81%; коричневое масло;MS: 418 (М+Н)+. 2-(4-Метоксибензолсульфонил)-5-метил-2 пиридин-3-илметил-гекс-4-еновая кислота была получена из исходного этилового эфира 2-(4 метоксибензолсульфонил)-5-метил-2-пиридин 3-илметил-гекс-4-еновой кислоты (4,0 г, 9,5 ммолей), растворенного в метаноле (50 мл) и 10N NaOH (30 мл). Полученную реакционную смесь обрабатывали, как изложено в примере 9. Выход 3,2 г, 87%; твердое вещество цвета слоновой кости; т. пл. 117-119 С; MS: 390 (М+Н)+. Из исходной 2-(4-метоксибензолсульфонил)-5-метил-2-пиридин-3-илметил-гекс-4-еновой кислоты (2,1 г, 5,4 ммоля) и по методике,которая изложена в примере 1, было выделено 1,82 г гидроксиамида 2-(4-метоксибензолсульфонил)-5-метил-2-пиридин-3-илметил-гекс-4 еновой кислоты в виде бесцветного твердого вещества. Выход: 82%; т. пл. 89-92 С; MS: 405; 1H ЯМР (300 МГц, CDCl3):1,63 (с, 3 Н),1,76 (с, 3 Н), 2,62-2,78 (м, 2 Н), 3,3 (д, J=4,0 Гц,1 Н), 3,63 (д, J=4,0 Гц, 1 Н), 3,82 (с, 3 Н), 5,26 (м,1 Н), 7,12-7,88 (м, 6 Н), 8,27-8,33 (м, 2 Н). Пример 64. 2-Бензил-4-диизопропиламиноN-гидрокси-2-(4-метоксибензолсульфонил)бутирамид. По методике, которая описана в примере 29, был получен этиловый эфир 2-бензил-4 диизопропиламино-2-(4-метоксибензолсульфонил)-масляной кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-3-фенилпропионовой кислоты (пример 9) и 2-диизопропиламиноэтилхлорид-гидрохлорида (4,0 г,20 ммолей). Выход 3,2 г, 79%; твердое вещество цвета слоновой кости, т. пл. 89-91 С; MS: 476,4(М+Н)+. Из исходного этилового эфира 2-бензил-4 диизопропиламино-2-(4-метоксибензолсульфонил)-масляной кислоты (3,53 г, 7,5 ммоля) по методике, которая изложена в примере 9, было выделено 2,8 г (86%) этиловый эфир 2-бензил-4 диизопропиламино-2-(4-метоксибензолсульфо 001742 58 нил)-масляной кислоты. Т. пл. 136-138 С; MS: 448,5 (М+Н)+. Из исходного этилового эфира 2-бензил-4 диизопропиламино-2-(4-метоксибензолсульфонил)-масляной кислоты (1,85 г, 4,1 ммоля) и по методике, которая изложена в примере 1, было выделено 1,3 г 2-бензил-4-диизопропиламиноN-гидрокси-2-(4-метоксибензолсульфонил)бутирамида в виде легкоплавкого воскообразного твердого вещества; Выход: 68%; MS: 463,3; 1(м, 2 Н), 2,71 (м, 2 Н), 3,18 (м, 1 Н), 3,48 (м, 1 Н),3,86 (с, 3 Н), 6,98 (д, J=8 Гц, 2 Н), 7,18-7,22 (м,5 Н), 7,92 (д, J=8 Гц, 2 Н), 8,12 (с, 1 Н). Пример 65. 3-Циклогексил-N-гидрокси-2(4-метоксибензолсульфонил)-2-пиридин-3-илметилпропионамид. По методике, которая изложена в примере 9, был получен этиловый эфир 3-циклогексил-2(4-метоксибензолсульфонил)-2-пиридин-3-илметилпропионовой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)уксусной кислоты (4,0 г, 15 ммолей) и 1 бромометилциклогексана (2,7 г, 15 ммолей). Выход 5,0 г, 94%; бесцветное масло; MS: 355(М+Н)+. По методике, которая изложена в примере 29, был получен этиловый эфир 3-циклогексил 2-(4-метоксибензолсульфонил)-2-пиридин-3 илметилпропионовой кислоты из исходного этилового эфира 3-циклогексил-2-(4-метоксибензолсульфонил)-пропионовой кислоты (1,5 г,4,2 ммоля) и 3-пиколилхлорида (1,0 г, 6 ммолей). Выход 1,0 г, 38%; бесцветное масло;MS: 446 (M+H)+. Из исходного этилового эфира 3 циклогексил-2-(4-метоксибензолсульфонил)-2 пиридин-3-илметилпропионовой кислоты (1,3 г,2,9 ммоля) по методике, которая изложена в примере 9, было выделено 1,0 г (83%) 3 циклогексил-2-(4-метоксибензолсульфонил)-2 пиридин-3-илметилпропионовой кислоты. Т. пл. 92 С; MS: 417,5 (M+H)+. Из исходной 3-циклогексил-2-(4-метоксибензолсульфонил)-2-пиридин-3-илметилпропионовой кислоты (1,0 г, 2,4 ммоля) и по методике,которая изложена в примере 1, было выделено 80 мг 3-циклогексил-N-гидрокси-2-(4-метоксибензолсульфонил)-2-пиридин-3-илметилпропионамида в виде бесцветной хлористо-водородной соли; выход: 71%; т. пл. 57-60 С; MS: 433; 1H ЯМР (300 МГц, СDСl3):0,8-2,08 (м,13 Н), 3,3 (д, J=14 Гц, 1 Н), 3,7 (д, J=14 Гц, 1 Н),3,9 (с, 3 Н), 7,0-8,5 (м, 8 Н). Пример 66. Гидроксиамид 2-(4-метоксибензолсульфонил)-4-метил-2-пиридин-3-илметилпентановой кислоты. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метокси 59 бензолсульфонил)-4-метилпентановой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-уксусной кислоты (5,0 г, 20 ммолей) и 1-бромо-2-метилпропана (2,6 г, 20 ммолей). Выход 6,0 г, 95%; бесцветное масло;MS: 315 (M+H)+. По методике, которая изложена в примере 29, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-4-метил-2-пиридин-3-илметилпентановой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-4-метилпентановой кислоты (3,1 г, 10 ммолей) и 3 пиколилхлорид-гидрохлорида (1,8 г, 11 ммолей). Выход 3,0 г, 75%; бесцветное масло; MS: 406 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-4-метил-2-пиридин 3-илметилпентановой кислоты (1,2 г, 2,9 ммоля) по методике, которая изложена в примере 9,было выделено 1,0 г 2-(4-метоксибензолсульфонил)-4-метил-2-пиридин-3-илметилпентановой кислоты в виде бесцветных кристаллов. Т. пл. 188-186 С; MS: 378 (M+H)+. Из исходной 2-(4-метоксибензолсульфонил)-4-метил-2-пиридин-3-илметилпентановой кислоты и по методике, которая изложена в примере 1, было выделено 180 мг гидроксиамида 2-(4-метоксибензолсульфонил)-4-метил 2-пиридин-3-илметилпентановой кислоты в виде бесцветного твердого вещества; выход: 21%; т. пл. 78 С; MS: 393,4; 1(м, 2 Н), 3,85 (с, 3 Н), 6,8-8,5 (м, 10 Н). Пример 67. N-Гидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-хинолин-6-ил-пропионамид. По методике, которая изложена в примере 29, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-2-метил-3-хинолин-6-илпропионовой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-пропионовой кислоты 95,2 г, 20 ммолей) и 7-бромометилхинолина (4,4 г, 20 ммолей). Выход 4,5 г,54%; бледно-желтое твердое вещество; т. пл. 86 С; MS: 414 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензолсульфонил)-2-метил-3-хинолин 6-ил-пропионовой кислоты по методике, которая изложена в примере 9, было выделено 2,5 г(90%) 2-(4-метоксибензолсульфонил)-2-метил 3-хинолин-6-ил-пропионовой кислоты в виде бесцветных кристаллов. Т. пл. 106-108 С; MS: 386,4 (M+H)+. Из исходной 2-(4-метоксибензолсульфонил)-2-метил-3-хинолин-6-ил-пропионовой кислоты (2,0 г, 5,2 ммоля) и по методике, которая изложена в примере 1, было выделено 1,2 г Nгидрокси-2-(4-метоксибензолсульфонил)-2-метил-3-хинолин-6-ил-пропионамида в виде бесцветного твердого вещества; выход: 57%; т. пл. 206 С; MS: 401,4 (М+Н)+;H ЯМР (300 МГц, СDСl3):1,4 (с, 3 Н),3,19 (м, 1 Н), 3,8-4,0 (м, 4 Н), 7,1-8,95 (м, 12 Н). Пример 68. Гидроксиамид 2-(4-метоксибензилсульфонил)-6-фенокси-2-пиридин-3-илметилгексановой кислоты. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксибензилсульфонил)-6-феноксигексановой кислоты (2,5 г, 10 ммолей) из исходного этилового эфира 2-(4-метоксибензолсульфонил)-уксусной кислоты и 1-бромо-4-феноксибутана (2,2 г, 10 ммолей). Выход 3,8 г, 93%; бесцветное масло;MS: 407 (М+Н)+. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксибензилсульфонил)-6-фенокси-2-пиридин-3 илметилгексановой кислоты из исходного этилового эфира 2-(4-метоксибензилсульфонил)-6 феноксигексановой кислоты и 3-пиколилхлорида (1,8 г, 11 ммолей). Выход 3,5 г, 71%; бесцветное масло; MS: 498 (М+Н)+. Из исходного этилового эфира 2-(4 метоксибензилсульфонил)-6-фенокси-2-пиридин-3-илметилгексановой кислоты (3,0 г, 6,0 ммолей) по методике, которая изложена в примере 9, было выделено 2,8 г (выход: количественно) 2-(4-метоксибензилсульфонил)-6-фенокси-2-пиридин-3-илметилгексановой кислоты в виде бесцветных кристаллов. Т. пл. 148-151 С;H ЯМР (300 МГц, СDСl3):1,5-2,5 (м,8 Н), 3,4 (ушир.с, 2 Н), 3,8 (с, 3 Н), 6,8-8,7 (м,13 Н). Пример 69. Гидроксиамид 2-(4-метоксибензолсульфонил)-5-метил-2-пиридин-3-илметилгексановой кислоты. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-5-гексановой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-уксусной кислоты (10,0 г, 39 ммолей) и 1-бромо-3-метилбутана (6,0 г, 40 ммолей). Выход 8,5 г, 62%; бесцветное масло; MS: 329 (M+H)+. По методике, которая изложена в примере 9, был получен этиловый эфир 2-(4-метоксибензолсульфонил)-5-метил-2-пиридин-3-илметилгексановой кислоты из исходного этилового эфира 2-(4-метоксибензолсульфонил)-5-гексановой кислоты (6,0 г, 18 ммолей) и пиколилхлорид-гидрохлорида (4,1 г, 25 ммолей). Выход 4,5 г, 60%; коричневое масло; MS: 420 (М+Н)+. 1
МПК / Метки
МПК: A61K 31/164, A61P 5/48, C07D 211/66
Метки: арилов, сульфонил)-3-замещенные, алкилов, сульфинил, матриксных, гетероарилсульфанил, ингибиторов, арил, n-гидрокси-2-(алкил, качестве, гетероариламидов, металлопротеиназ
Код ссылки
<a href="https://eas.patents.su/30-1742-n-gidroksi-2-alkil-aril-ili-geteroarilsulfanil-sulfinil-ili-sulfonil-3-zameshhennye-alkilov-arilov-ili-geteroarilamidov-v-kachestve-ingibitorov-matriksnyh-metalloproteinaz.html" rel="bookmark" title="База патентов Евразийского Союза">N-гидрокси-2-(алкил-, арил- или гетероарилсульфанил, -сульфинил или -сульфонил)-3-замещенные алкилов, арилов или гетероариламидов в качестве ингибиторов матриксных металлопротеиназ</a>
Предыдущий патент: Дерматологические и косметические композиции местного применения, содержащие сфингомиелиназу для повышения уровня церамидов в коже и слизистых оболочках
Следующий патент: Способ и устройство для изготовления пластмассовых фитингов, соединяемых с трубами электросваркой
Случайный патент: Способ получения агомелатина












