Применимые в качестве гербицидных соединений пиридопиразиновые производные
Номер патента: 15647
Опубликовано: 31.10.2011
Авторы: Тернбулл Майкл Драйсдейл, Картер Нейл Брайан, Кроули Патрик Джелф, Кордингли Мэттью Роберт
Формула / Реферат
1. Соединение формулы (I)
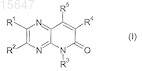
в которой R1 и R2независимо представляют собой водород, C1-C4-алкил или фенил;
R3 представляет собой C1-C4-галогеналкил или С2-С4-галогеналкенил;
R4 представляет собой фенил, замещенный 1-4 R8, которые могут быть одинаковыми или разными;
R5 представляет собой гидрокси, метилкарбонилокси-, этилкарбонилокси-, изопропилкарбонилокси-, н-пропилкарбонилокси-, бут-2-илкарбонилокси-, 2-метилпропилкарбонилокси-, трет-бутилкарбонилокси-;
каждый R8независимо представляет собой галоген, C1-C10-алкил, C1-C4-галогеналкил, C1-C10-алкокси или C1-С4-галогеналкокси;
или его соль или N-оксид.
2. Соединение по п.1, где R1 и R2, оба, представляют собой водород.
3. Соединение по п.1 или 2, где R3 представляет собой 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 3-хлорпропил, 3,3,3-трифторпропил, 4-хлорбутил, 4,4,4,3,3-пентафторбутил, 2-хлорпроп-2-ен-1-ил, 3,3-дихлорпроп-2-ен-1-ил, 2-фторпроп-2-ен-1-ил, 3,3-дифторпроп-2-ен-1-ил, 4,4-дифторбут-3-ен-1-ил или 3,4,4-трифтор-бут-3-ен-1-ил.
4. Соединение по любому из пп.1-3, где R3 представляет собой 2,2-дифторэтил.
5. Соединение по любому из пп.1-4, где R4 представляет собой 2,5-бис-(трифторметил)фенил, 3-бром-2-хлор-6-фторфенил, 2-хлор-3,6-дифторфенил, 2-хлор-4-фторфенил, 2-хлор-5-фторфенил, 2-хлорфенил, 2-хлор-3-трифторметилфенил, 2-хлор-5-трифторметилфенил, 2-хлор-6-трифторметилфенил, 2,3-дихлор-6-фторфенил, 2,4-дихлор-5-фторфенил, 3,5-дихлор-2-метоксифенил, 2,3-дихлорфенил, 2,4-дихлорфенил, 2,5-дихлорфенил, 2,6-дихлорфенил, 2,6-дихлор-4-трифторметоксифенил, 2,6-дихлор-4-трифторметилфенил, 2,6-диэтил-4-метилфенил, 2,3-диметоксифенил, 2-фторфенил, 2-метоксифенил, 2-метокси-5-трифторметоксифенил, 2,3,6-трихлорфенил, 2-трифторметоксифенил, 2-трифторметилфенил или 2,4,6-триметилфенил.
6. Способ борьбы с растениями, который включает нанесение на растение или в его локус гербицидно эффективного количества соединения формулы (I) по любому из пп.1-5.
7. Гербицидная композиция, которая содержит гербицидно эффективное количество соединения формулы (I) по любому из пп.1-5 в сочетании с адъювантами.
8. Гербицидная композиция, которая содержит гербицидно эффективное количество соединения формулы (I) по любому из пп.1-5, необязательно один или несколько других гербицидов и необязательно один или несколько антидотов.
Текст
ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ЕВРАЗИЙСКОМУ ПАТЕНТУ Дата публикации и выдачи патента ПРИМЕНИМЫЕ В КАЧЕСТВЕ ГЕРБИЦИДНЫХ СОЕДИНЕНИЙ ПИРИДОПИРАЗИНОВЫЕ ПРОИЗВОДНЫЕ Настоящее изобретение относится к соединениям формулы (I), в которой значения R1, R2, R3, R4 и R5 определены в п.1 формулы изобретения, или к их соли или N-оксиду. Кроме того, настоящее изобретение относится к способам получения соединений формулы (I), к способам борьбы с растениями и к композициям, содержащим соединения формулы (I). 015647 Настоящее изобретение относится к новым гербицидным 5-галогеналкил-5 Н-пиридо[2,3-b]пиразин 6-онам и 5-галогеналкенил-5 Н-пиридо[2,3-b]пиразин-6-онам, к способам их получения, к содержащим такие соединения композициям и к их использованию для борьбы с растениями или для ингибирования роста растений. Пиридо[2,3-b]пиразины были раскрыты в качестве промежуточных продуктов при синтезе фунгицидных соединений, например, в WO 04/056825, WO 05/123698 и WO 05/123733. Пиридо[2,3-b]пиразины были раскрыты в качестве фунгицидных соединений в WO 05/010000. Неожиданно было обнаружено, что некоторые 5-галогеналкил-5 Н-пиридо[2,3-b]пиразин-6-оны и 5-галогеналкенил-5 Н-пиридо[2,3-b]пиразин-6-оны являются отличными гербицидами и ингибиторами роста. Поэтому настоящее изобретение относится к соединению формулы (I) в которой R1 и R2 независимо представляют собой водород, C1-C4-алкил, C1-C4-галогеналкил, галоген, циано, гидрокси, C1-C4-алкокси, C1-C4-алкилтио, арил или арил, замещенный 1-5 R6, которые могут быть одинаковыми или разными, гетероарил или гетероарил, замещенный 1-5 R6, которые могут быть одинаковыми или разными;R4 представляет собой арил или арил, замещенный 1-5 R8, которые могут быть одинаковыми или разными, или гетероарил или гетероарил, замещенный 1-4 R8, которые могут быть одинаковыми или разными;R5 представляет собой гидрокси или группу, которая может быть метаболизирована до гидроксигруппы; каждый R6 и R8 независимо представляет собой галоген, циано, нитро, C1-C10-алкил,C1-C4-галогеналкил, C2-C10-алкенил, C2-C10-алкинил, гидрокси, C1-C10-алкокси, C1-C4-галогеналкокси,C1-C10-алкокси-C1-C4-алкил-, C3-C7-циклоалкил, C3-C7-циклоалкокси, C3-C7-циклоалкил-C1-C4-алкил-,C3-C7-циклоалкил-C1-C4-алкокси-, C1-C6-алкилкарбонил-, формил, C1-C4-алкоксикарбонил-, C1-C4-алкилкарбонилокси-, C1-C10-алкилтио-, C1-C4-галогеналкилтио-, C1-C10-алкилсульфинил-, C1-C4-галогеналкилсульфинил-, C1-C10-алкилсульфонил-, C1-C4-галогеналкилсульфонил-, амино, C1-C10-алкиламино-,ди-C1-C10-алкиламино-, C1-C10-алкилкарбониламино-, арил или арил, замещенный 1-3 R13, которые могут быть одинаковыми или разными, гетероарил или гетероарил, замещенный 1-3 R13, которые могут быть одинаковыми или разными, арил-C1-C4-алкил- или арил-C1-C4-алкил-, где арильный фрагмент замещен 1-3 R14, которые могут быть одинаковыми или разными, гетероарил-C1-C4-алкил- или гетероарил-C1-C4 алкил-, где гетероарильный фрагмент замещен 1-3 R13, которые могут быть одинаковыми или разными,арилокси- или арилокси-, замещенный 1-3 R13, которые могут быть одинаковыми или разными, гетероарилокси- или гетероарилокси-, замещенный 1-3 R13, которые могут быть одинаковыми или разными,арилтио- или арилтио-, замещенный 1-3 R13, которые могут быть одинаковыми или разными, или гетероарилтио- или гетероарилтио-, замещенный 1-3 R13, которые могут быть одинаковыми или разными; каждый R13 независимо представляет собой галоген, циано, нитро, C1-C6-алкил, C1-C6-галогеналкил или C1-C6-алкокси; или к его соли или N-оксиду. Соединения формулы (I) могут существовать в различных геометрически или оптически изомерных формах или таутомерных формах. Настоящее изобретение охватывает все такие изомеры и таутомеры и их смеси в любых пропорциях, а также изотопные формы, такие как дейтерированные соединения. Например, соединение формулы (Ia), т.е. соединение формулы (I), в которой значение R5 определено для соединений формулы (I) и отлично от гидрокси, может быть изображено только в одной таутомерной форме-1 015647 тогда как соединение формулы (Ib), т.е. соединение формулы (I), в которой R5 представляет собой гидрокси, может быть изображено в трех таутомерных формах: Каждый алкильный фрагмент (по отдельности или как часть большей группы, такой как алкокси,алкоксикарбонил, алкилкарбонил, алкиламинокарбонил, диалкиламинокарбонил) представляет собой неразветвленную или разветвленную цепь и представляет собой, например, метил, этил, н-пропил, нбутил, н-пентил, н-гексил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил или неопентил. Алкильные группы предпочтительно представляют собой C1-C6-алкильные группы, более предпочтительноC1-C4 и наиболее предпочтительно C1-C3-алкильные группы. Алкенильные или алкинильные фрагменты (по отдельности или как часть большей группы, такой как алкенилокси или алкинилокси) могут находиться в форме неразветвленных или разветвленных цепей, и алкенильные фрагменты, по необходимости, могут находиться в (Е)- или (Z)-конфигурации. Примерами являются винил, аллил, проп-2-енил и пропаргил. Алкенильные или алкинильные группы предпочтительно представляют собой C2-C6-алкенильные или алкинильные группы, более предпочтительноC2-C4 и наиболее предпочтительно C1-C3-алкенильные или алкинильные группы. Галоген представляет собой фтор, хлор, бром или йод. Галогеналкильные группы (по отдельности или как часть большей группы, такой как галогеналкокси или галогеналкилтио) представляют собой алкильные группы, которые замещены одним или несколькими одинаковыми или разными атомами галогена, и представляют собой, например, -CF3, -CF2Cl,-CHF2, -CH2CF3 или -CH2CHF2. Галогеналкенильные и галогеналкинильные группы (по отдельности или как часть большей группы, такой как галогеналкенилокси или галогеналкинилокси) представляют собой алкенильные или алкинильные группы соответственно, которые замещены одним или несколькими одинаковыми или разными атомами галогена, и представляют собой, например, -CH=CF2, -CCl=CClF или-CCCl. Циклоалкильные группы могут находиться в моно- или бициклической форме и могут быть необязательно замещены одной или несколькими метильными группами. Циклоалкильные группы предпочтительно содержат 3-8 атомов углерода, более предпочтительно 3-6 атомов углерода. Примерами моноциклических циклоалкильных групп являются циклопропил, 1-метилциклопропил, 2-метилциклопропил,циклобутил, циклопентил и циклогексил. В контексте описания настоящего изобретения термин "арил" относится к кольцевой системе, которая может быть моно-, би -или трициклической. Примеры таких колец включают фенил, нафталинил,антраценил, инденил или фенантренил. Предпочтительная арильная группа представляет собой фенил. Термин "гетероарил" относится к ароматической кольцевой системе, содержащей по крайней мере один гетероатом и состоящей либо из одного кольца, либо из двух или более конденсированных колец. Предпочтительно одиночные кольца могут содержать до трех, а бициклические системы до четырех гетероатомов, которые предпочтительно выбирают из атома азота, кислорода или серы. Примеры таких групп включают пиридил, пиридазинил, пиримидинил, пиразинил, триазинил, фуранил, тиофенил, оксазолил, изоксазолил, оксадиазолил, тиазолил, изотиазолил, тиадиазолил, пирролил, пиразолил, имидазолил, триазолил и тетразолил. Предпочтительная гетероарильная группа представляет собой пиридин. Примерами бициклических групп являются бензотиофенил, бензимидазолил, бензотиадиазолил, хинолинил, циннолинил, хиноксалинил и пиразоло[1,5-а]пиримидинил. Определение термина "гетероциклил" включает гетероарил и, кроме того, его ненасыщенные или частично ненасыщенные аналоги, такие как 4,5,6,7-тетрагидробензотиофенил, хромен-4-онил,9 Н-флуоренил, 3,4-дигидро-2 Н-бензо-1,4-диоксепинил, 2,3-дигидробензофуранил, пиперидинил,1,3-диоксоланил, 1,3-диоксанил, 4,5-дигидроизоксазолил, тетрагидрофуранил и морфолинил. Используемый в этом документе термин "гербицид" означает соединение, которое подавляет или модифицирует рост растений. Термин "гербицидно эффективное количество" означает количество соединения или сочетания таких соединений, которое способно вызывать эффект подавления или модификации роста растений. Эффекты подавления или модификации включают все отклонения от нормального развития, например уничтожение, замедление роста, ожог листьев, альбинизм, задержку развития и т.п. Термин "растения" относится ко всем физическим частям растения, включая семена, рассаду, саженцы, корни, клубни, стебли, черенки, листву и плоды. Предполагается, что термин "локус" включает почву, семена и рассаду, а также укоренившуюся растительность.-2 015647 Используемый в этом документе термин "метаболизм" означает преобразование или разложение вещества из одной формы в другую живым организмом, в частности растением (in planta). Предпочтительные (для любого сочетания) значения для R1, R2, R3, R4, R5, R6, R8, R9, R10, R11, R12,13R и R14 представлены ниже. Предпочтительно R1 представляет собой водород, C1-C4-алкил, C1-C4-галогеналкил, галоген, циано,гидрокси или C1-C4-алкокси. Более предпочтительно R1 представляет собой водород, C1-C4-алкил, галоген, циано или гидрокси. Еще более предпочтительно R1 представляет собой водород, метил, хлор или бром. Еще более предпочтительно R1 представляет собой водород или хлор. Наиболее предпочтительно R1 представляет собой водород. Предпочтительно R2 представляет собой водород, C1-C4-алкил, C1-C4-галогеналкил, галоген, циано,гидрокси или C1-C4-алкокси. Более предпочтительно R2 представляет собой водород, C1-C4-алкил, галоген, циано или гидрокси. Еще более предпочтительно R2 представляет собой водород, метил, хлор или бром. Еще более предпочтительно R2 представляет собой водород или хлор. Наиболее предпочтительно R2 представляет собой водород. Предпочтительно R3 представляет собой C1-C4-галогеналкил или C2-C4-галогеналкенил. Примерами таких предпочтительных групп для R3 являются 2-фторэтил, 2,2-дифторэтил,2,2,2-трифторэтил, 3-хлорпропил, 3,3,3-трифторпропил, 4-хлорбутил, 4,4,4,3,3-пентафторбутил,2-хлорпроп-2-ен-1-ил, 3,3-дихлорпроп-2-ен-1-ил, 2-фторпроп-2-ен-1-ил, 3,3-дифторпроп-2-ен-1-ил,4,4-дифторбут-3-ен-1-ил и 3,4,4-трифторбут-3-ен-1-ил. Более предпочтительно R3 представляет собой C1-C3-галогеналкил, в котором атомы галогена представляют собой, в частности, атом фтора. Примерами таких более предпочтительных групп для R3 являются 2-фторэтил, 2,2-дифторэтил,2,2,2-трифторэтил и 3,3,3-трифторпропил. Еще более предпочтительно R3 представляет собой C1-C2-галогеналкил, в котором атомы галогена представляют собой, в частности, атом фтора. Примерами таких еще более предпочтительных групп для R3 являются 2-фторэтил, 2,2-дифторэтил и 2,2,2-трифторэтил. Наиболее предпочтительно R3 представляет собой 2,2-дифторэтил. Предпочтительно R4 представляет собой арил или арил, замещенный 1-5 R8, которые могут быть одинаковыми или разными. Примерами таких более предпочтительных групп для R4 являются 2,5-бис-(трифторметил)фенил,3-бром-2-хлор-6-фторфенил, 2-бром-4-фторфенил, 5-бром-2-метоксифенил, 2-бромфенил, 2-бром-4 трифторметилфенил, 2-хлор-3,6-дифтор-5-нитрофенил, 2-хлор-3,6-дифторфенил, 2-хлор-4,5-дифторфенил, 2-хлор-6-фтор-3-метилфенил, 2-хлор-6-фтор-5-метилфенил, 2-хлор-6-фтор-3-нитрофенил, 2-хлор 4-фторфенил, 2-хлор-5-фторфенил, 2-хлор-6-фторфенил, 2-хлорфенил, 3-хлорфенил, 4-хлорфенил,2-хлор-3-трифторметилфенил, 2-хлор-5-трифторметилфенил, 5-хлор-2-трифторметилфенил, 2-хлор-6 трифторметилфенил, 2,3-дихлор-6-фторфенил, 2,4-дихлор-5-фторфенил, 3,5-дихлор-2-метоксифенил,2,3-дихлорфенил, 2,4-дихлорфенил, 2,5-дихлорфенил, 2,6-дихлорфенил, 3,4-дихлорфенил, 2,6-дихлор-4 трифторметоксифенил, 2,6-дихлор-4-трифторметилфенил, 2,6-диэтил-4-метилфенил, 2-дифторметоксифенил, 4,5-дифтор-2-метоксифенил, 2,3-диметоксифенил, 2,4-диметоксифенил, 2,5-диметилфенил,2-этилфенил, 2-фторфенил, 4-фтор-2-трифторметилфенил, 6-фтор-2-трифторметилфенил, 2-йодфенил, 2 метоксифенил, 2-метокси-5-трифторметоксифенил, 6-метил-2-нитрофенил, 2-метилфенил, нафт-2-ил,нафт-3-ил,фенил,2-нитро-4-трифторметилфенил,2,3,5-трихлорфенил,2,3,6-трихлорфенил,2-трифторметоксифенил, 2-трифторметилфенил, 2,3,6-трифторфенил и 2,4,6-триметилфенил. Более предпочтительно R4 представляет собой арил, замещенный 1-4 R8, которые могут быть одинаковыми или разными. Примерами таких более предпочтительных групп для R4 являются 2,5-бис-(трифторметил)фенил,3-бром-2-хлор-6-фторфенил, 2-хлор-3,6-дифторфенил, 2-хлор-4-фторфенил, 2-хлор-5-фторфенил,2-хлорфенил, 2-хлор-3-трифторметилфенил, 2-хлор-5-трифторметилфенил, 2-хлор-6-трифторметилфенил, 2,3-дихлор-6-фторфенил, 2,4-дихлор-5-фторфенил, 3,5-дихлор-2-метоксифенил, 2,3-дихлорфенил,2,4-дихлорфенил, 2,5-дихлорфенил, 2,6-дихлорфенил, 2,6-дихлор-4-трифторметоксифенил, 2,6-дихлор-4 трифторметилфенил, 2,6-диэтил-4-метилфенил, 2,3-диметоксифенил, 2-фторфенил, 2-метоксифенил,2-метокси-5-трифторметоксифенил, 2,3,6-трихлорфенил, 2-трифторметоксифенил, 2-трифторметилфенил и 2,4,6-триметилфенил. Наиболее предпочтительно R4 представляет собой арил, замещенный двумя или тремя R8, которые могут быть одинаковыми или разными. Примерами таких наиболее предпочтительных групп для R4 являются 2,5-бис-(трифторметил)фенил, 3-бром-2-хлор-6-фторфенил, 2-хлор-3,6-дифторфенил, 2-хлор-5-фторфенил, 2-хлор-5-трифторметилфенил, 2-хлор-6-трифторметилфенил, 2,3-дихлор-6-фторфенил, 2,6-дихлорфенил, 2,6-дихлор 4-трифторметоксифенил и 2,3,6-трихлорфенил.-3 015647 В одном предпочтительном варианте осуществления R4 представляет собой 2,5-бис(трифторметил)фенил. В одном предпочтительном варианте осуществления R4 представляет собой 3-бром-2-хлор-6 фторфенил. В одном предпочтительном варианте осуществления R4 представляет собой 2-хлор-3,6 дифторфенил. В одном предпочтительном варианте осуществления R4 представляет собой 2-хлор-5-фторфенил. В одном предпочтительном варианте осуществления R4 представляет собой 2-хлор-5 трифторметилфенил. В одном предпочтительном варианте осуществления R4 представляет собой 2-хлор-6 трифторметилфенил. В одном предпочтительном варианте осуществления R4 представляет собой 2,3-дихлор-6 фторфенил. В одном предпочтительном варианте осуществления R4 представляет собой 2,6-дихлорфенил. В одном предпочтительном варианте осуществления R4 представляет собой 2,6-дихлор-4 трифторметоксифенил. В одном предпочтительном варианте осуществления R4 представляет собой 2,3,6-трихлорфенил. Предпочтительно R5 представляет собой гидрокси, R9-окси-, R10-карбонилокси-, три-R11-силилоксиили R12-сульфонилокси-, гдеR9 представляет собой C1-C10-алкил, C2-C10-алкенил, C2-C10-алкинил или арил-C1-C4-алкил- или арил-C1-C4-алкил-, где арильный фрагмент замещен 1-5 заместителями, независимо выбранными из галогена, циано, нитро, C1-C6-алкила, C1-C6-галогеналкила или C1-C6-алкокси;R10 представляет собой C1-C10-алкил, C3-C10-циклоалкил, C3-C10-циклоалкил-C1-C10-алкил-,C1-C10-галогеналкил, C2-C10-алкенил, C2-C10-алкинил, C1-C4-алкокси-C1-C10-алкил-, C1-C4-алкилтио-C1-C4 алкил-, C1-C10-алкокси, C2-C10-алкенилокси, C2-C10-алкинилокси, C1-C10-алкилтио-, N-C1-C4-алкиламино-,N,N-ди(C1-C4-алкил)амино-, арил или арил, замещенный 1-3 R14, которые могут быть одинаковыми или разными, гетероарил или гетероарил, замещенный 1-3 R14, которые могут быть одинаковыми или разными, арил-C1-C4-алкил- или арил-C1-C4-алкил-, где арильный фрагмент замещен 1-3 R14, которые могут быть одинаковыми или разными, гетероарил-C1-C4-алкил- или гетероарил-C1-C4-алкил-, где гетероарильный фрагмент замещен 1-3 R14, которые могут быть одинаковыми или разными, арилокси- или арилокси-, замещенный 1-3 R14, которые могут быть одинаковыми или разными, гетероарилокси- или гетероарилокси-, замещенный 1-3 R14, которые могут быть одинаковыми или разными, арилтио- или арилтио-, замещенный 1-3 R14, которые могут быть одинаковыми или разными, или гетероарилтио- или гетероарилтио-, замещенный 1-3 R14, которые могут быть одинаковыми или разными; каждый R11 независимо представляет собой C1-C10-алкил или фенил или фенил, замещенный 1-5 заместителями, независимо выбранными из галогена, циано, нитро, C1-C6-алкила, C1-C6-галогеналкила илиR12 представляет собой C1-C10-алкил, C1-C10-галогеналкил или фенил или фенил, замещенный 1-5 заместителями, независимо выбранными из галогена, циано, нитро, C1-C6-алкила, C1-C6-галогеналкила или C1-C6-алкокси; и каждый R14 независимо представляет собой галоген, циано, нитро, C1-C10-алкил,C1-C4-галогеналкил, C1-C10-алкокси, C1-C4-алкоксикарбонил-, C1-C4-галогеналкокси, C1-C10-алкилтио-,C1-C4-галогеналкилтио-, C1-C10-алкилсульфинил-, C1-C4-галогеналкилсульфинил-, C1-C10-алкилсульфонил-, C1-C4-галогеналкилсульфонил-, арил или арил, замещенный 1-5 заместителями, независимо выбранными из галогена, циано, нитро, C1-C6-алкила, C1-C6-галогеналкила или C1-C6-алкокси, или гетероарил или гетероарил, замещенный 1-4 заместителями, независимо выбранными из галогена, циано, нитро,C1-C6-алкила, C1-C6-галогеналкила или C1-C6-алкокси. Более предпочтительно R5 представляет собой гидрокси, R9-окси- или R10-карбонилокси-. Еще более предпочтительно R5 представляет собой гидрокси, C1-C4-алкокси, C1-C4-алкилкарбонилокси-,C3-C6-циклоалкилкарбонилокси-,C3-C10-циклоалкил-C1-C10-алкилкарбонилокси-,C1-C4-галогеналкилкарбонилокси-, C2-C4-алкенилкарбонилокси-, C2-C4-алкинилкарбонилокси-, C1-C4 алкокси-C1-C4-алкилкарбонилокси-, C1-C4-алкилтио-C1-C4-алкилкарбонилокси-, C1-C4-алкоксикарбонилокси-, C2-C4-алкенилоксикарбонилокси-, C2-C4-алкинилоксикарбонилокси-, C1-C4-алкилтиокарбонилокси-, N-C1-C4-алкиламинокарбонилокси-, N,N-ди(C1-C4-алкил)аминокарбонилокси-, арилкарбонилоксиили арилкарбонилокси-, замещенный 1-3 R14, которые могут быть одинаковыми или разными,гетероарилкарбонилокси- или гетероарилкарбонилокси-, замещенный 1-3 R14, которые могут быть одинаковыми или разными, арил-C1-C4-алкилкарбонилокси- или арил-C1-C4-алкилкарбонилокси-, где арильный фрагмент замещен 1-3 R14, которые могут быть одинаковыми или разными, гетероарил-C1-C4 алкилкарбонилокси- или гетероарил-C1-C4-алкилкарбонилокси-, где гетероарильный фрагмент замещен 1-3 R14, которые могут быть одинаковыми или разными, арилоксикарбонилокси- или арилоксикарбонилокси-, замещенный 1-3 R14, которые могут быть одинаковыми или разными, гетероарилоксикарбонилокси- или гетероарилоксикарбонилокси-, замещенный 1-3 R14, которые могут быть одинаковыми или-4 015647 разными, арилтиокарбонилокси- или арилтиокарбонилокси-, замещенный 1-3 R14, которые могут быть одинаковыми или разными, или гетероарилтиокарбонилокси- или гетероарилтиокарбонилокси-, замещенный 1-3 R14, которые могут быть одинаковыми или разными. Примерами предпочтительных групп для R5 являются гидрокси, метокси, этокси, метилкарбонилокси-, этилкарбонилокси-, изопропилкарбонилокси-, н-пропилкарбонилокси-, бут-2-илкарбонилокси-,2-метилпропилкарбонилокси-, трет-бутилкарбонилокси-, циклопропилкарбонилокси-, циклопентилметилкарбонилокси-,хлорметилкарбонилокси-,трифторметилкарбонилокси-,аллилкарбонилокси-,(Е)-проп-1-ен-1-илкарбонилокси-, 2-метилпроп-1-ен-1-илкарбонилокси-, метоксиметилкарбонилокси-,этоксикарбонилокси-, трет-бутоксикарбонилокси-, бут-2-ин-1-илоксикарбонилокси-, этилтиокарбонилокси-, N,N-диэтиламинокарбонилокси-, фенилкарбонилокси-, 3-метоксифенилкарбонилокси-, 4-нитрофенилкарбонилокси-, бензилкарбонилокси-, фуран-2-илкарбонилокси-, 2,5-диметилфуран-3-илкарбонилокси-, тиофен-2-илкарбонилокси-, 3,5-диметилизоксазол-4-илкарбонилокси- и 1-фенилпроп-1-илкарбонилокси-. Еще более предпочтительно R5 представляет собой гидрокси, C1-C4-алкилкарбонилокси-,C3-C6-циклоалкилкарбонилокси-, C2-C4-алкенилкарбонилокси-, C2-C4-алкинилкарбонилокси-, C1-C4 алкоксикарбонилокси-, C2-C4-алкенилоксикарбонилокси-, C2-C4-алкинилоксикарбонилокси- или C1-C4 алкилтиокарбонилокси-. Примерами более предпочтительных групп для R5 являются гидрокси, метилкарбонилокси-,этилкарбонилокси-,изопропилкарбонилокси-,н-пропилкарбонилокси-,бут-2-илкарбонилокси-,2-метилпропилкарбонилокси-, трет-бутилкарбонилокси-, циклопропилкарбонилокси-, аллилкарбонилокси-, (Е)-проп-1-ен-1-илкарбонилокси-, 2-метилпроп-1-ен-1-илкарбонилокси-, этоксикарбонилокси-,трет-бутоксикарбонилокси-, бут-2-ин-1-илоксикарбонилокси- и этилтиокарбонилокси-. Наиболее предпочтительно R5 представляет собой гидрокси, C1-C4-алкилкарбонилокси-,C1-C4-алкоксикарбонилокси- или C1-C4-алкилтиокарбонилокси-. Примерами наиболее предпочтительных групп для R5 являются гидрокси, метилкарбонилокси-,этилкарбонилокси-, изопропилкарбонилокси-, н-пропилкарбонилокси-, бут-2-илкарбонилокси-, 2-метилпропилкарбонилокси-, трет-бутилкарбонилокси-, этоксикарбонилокси-, трет-бутоксикарбонилокси- и этилтиокарбонилокси-. В одном предпочтительном варианте осуществления R5 представляет собой гидрокси. В одном предпочтительном варианте осуществления R5 представляет собой R9-окси-, где R9 представляет собой C1-C10-алкил, C2-C10-алкенил, C2-C10-алкинил или арил-C1-C4-алкил- или арил-C1-C4 алкил-, где арильный фрагмент замещен 1-5 заместителями, независимо выбранными из галогена, циано,нитро, C1-C6-алкила, C1-C6-галогеналкила или C1-C6-алкокси. Такие R5 группы могут быть метаболизированы, предпочтительно in planta, с получением соответствующего соединения, в котором R5 представляет собой гидрокси. В одном предпочтительном варианте осуществления R5 представляет собой R10-карбонилокси-,где R10 представляет собой C1-C10-алкил, C3-C10-циклоалкил, C3-C10-циклоалкил-C1-C10-алкил-,C1-C10-галогеналкил, C2-C10-алкенил, C2-C10-алкинил, C1-C4-алкокси-C1-C10-алкил-, C1-C4-алкилтио-C1-C4 алкил-, C1-C10-алкокси, C2-C10-алкенилокси, C2-C10-алкинилокси, C1-C10-алкилтио-, N-C1-C4-алкиламино-,N,N-ди(C1-C4-алкил)амино-, арил или арил, замещенный 1-3 R14, которые могут быть одинаковыми или разными, гетероарил или гетероарил, замещенный 1-3 R14, которые могут быть одинаковыми или разными, арил-C1-C4-алкил- или арил-C1-C4-алкил-, где арильный фрагмент замещен 1-3 R14, которые могут быть одинаковыми или разными, гетероарил-C1-C4-алкил- или гетероарил-C1-C4-алкил-, где гетероарильный фрагмент замещен 1-3 R14, которые могут быть одинаковыми или разными, арилокси- или арилокси-, замещенный 1-3 R14, которые могут быть одинаковыми или разными, гетероарилокси- или гетероарилокси-, замещенный 1-3 R14, которые могут быть одинаковыми или разными, арилтио- или арилтио-, замещенный 1-3 R14, которые могут быть одинаковыми или разными, или гетероарилтио- или гетероарилтио-, замещенный 1-3 R14, которые могут быть одинаковыми или разными; и каждый R14 независимо представляет собой галоген, циано, нитро, C1-C10-алкил, C1-C4-галогеналкил, C1-C10-алкокси,C1-C4-алкоксикарбонил-, C1-C4-галогеналкокси, C1-C10-алкилтио-, C1-C4-галогеналкилтио-, C1-C10-алкилсульфинил-, C1-C4-галогеналкилсульфинил-, C1-C10-алкилсульфонил-, C1-C4-галогеналкилсульфонил-,арил или арил, замещенный 1-5 заместителями, независимо выбранными из галогена, циано, нитро,C1-C6-алкила, C1-C6-галогеналкила или C1-C6-алкокси, или гетероарил или гетероарил, замещенный 1-4 заместителями, независимо выбранными из галогена, циано, нитро, C1-C6-алкила, C1-C6-галогеналкила или C1-C6-алкокси. Такие R5 группы могут быть метаболизированы, предпочтительно in planta, с получением соответствующего соединения, в котором R5 представляет собой гидрокси. В одном предпочтительном варианте осуществления R5 представляет собой изопропилкарбонилокси- или трет-бутилкарбонилокси-. В одном предпочтительном варианте осуществления R5 представляет собой C1-C4-алкилсульфонилокси-. Примерами таких предпочтительных групп для R5 являются метилсульфонилокси- и изопропилсульфонилокси-.-5 015647 В одном предпочтительном варианте осуществления R5 представляет собой три(C1-C4 алкил)силилокси-. Примером предпочтительной группы для R5 является диметил-трет-бутилсилилокси-. Предпочтительно каждый R6 независимо представляет собой галоген, C1-C4-алкил,C1-C4-галогеналкил, C1-C4-алкокси или C1-C4-галогеналкокси. Примерами таких предпочтительных групп для R6 являются хлор, фтор, метил, этил, трифторметил, метокси или трифторметокси. Предпочтительно каждый R8 независимо представляет собой галоген, циано, нитро, C1-C10-алкил,C1-C4-галогеналкил, C1-C10-алкокси, C1-C4-алкоксикарбонил-, C1-C4-галогеналкокси, C1-C10-алкилтио-,C1-C4-галогеналкилтио-, C1-C10-алкилсульфинил-, C1-C4-галогеналкилсульфинил-, C1-C10-алкилсульфонил- или C1-C4-галогеналкилсульфонил-. Более предпочтительно каждый R8 независимо представляет собой галоген, циано, нитро, C1-C10 алкил, C1-C4-галогеналкил, C1-C10-алкокси, C1-C4-алкоксикарбонил-, C1-C4-галогеналкокси, C1-C10 алкилтио или C1-C4-галогеналкилтио. Примерами таких более предпочтительных групп для R8 являются йод, бром, хлор, фтор, циано, нитро, метил, этил, трифторметил, метокси, метоксикарбонил, трифторметокси или трифторметилтио. Наиболее предпочтительно каждый R8 независимо представляет собой галоген, C1-C10-алкил,C1-C4-галогеналкил, C1-C10-алкокси или C1-C4-галогеналкокси. Примерами таких наиболее предпочтительных групп для R8 являются бром, хлор, фтор, метил, этил, трифторметил, метокси или трифторметокси. В одном варианте осуществления R9 предпочтительно представляет собой C1-C10-алкил, более предпочтительно C1-C4-алкил, еще более предпочтительно метил или этил, наиболее предпочтительно метил. В другом варианте осуществления R9 предпочтительно представляет собой C2-C10-алкенил,C2-C10-алкинил, арил-C1-C4-алкил- или арил-C1-C4-алкил-, где арильный фрагмент замещен 1-3 R13, которые могут быть одинаковыми или разными, более предпочтительно C3-C4-алкенил, C3-C4-алкинил, бензил или бензил, в котором фенильный фрагмент замещен 1-3 R13, которые могут быть одинаковыми или разными, еще более предпочтительно аллил, пропаргил или бензил, наиболее предпочтительно R9 представляет собой аллил. Предпочтительно R10 представляет собой C1-C10-алкил, C3-C10-циклоалкил, C1-С 10-галогеналкил,C2-C10-алкенил, C2-C10-алкинил, C1-C4-алкокси-C1-C10-алкил-, C1-C4-алкилтио-C1-C4-алкил-, C1-С 10-алкокси,C1-C10-алкилтио-, N-C1-C4-алкиламино-, N,N-ди(С 1-С 4-алкил)амино-, фенил или фенил, замещенный 1-3R14, которые могут быть одинаковыми или разными, бензил или бензил, в котором фенильный фрагмент замещен 1-3 R14, которые могут быть одинаковыми или разными, тиенил или тиенил, замещенный 1-3R14, которые могут быть одинаковыми или разными, пиридил или пиридил, замещенный 1-3 R14, которые могут быть одинаковыми или разными, фенокси или фенокси, замещенный 1-3 R14, которые могут быть одинаковыми или разными, или фенилтио или фенилтио, замещенный 1-3 R14, которые могут быть одинаковыми или разными. Наиболее предпочтительно R10 представляет собой изопропил или трет-бутил. Предпочтительно каждый R11 независимо представляет собой C1-C4-алкил. Предпочтительно R12 представляет собой C1-C4-алкил или C1-C4-галогеналкил. Предпочтительно каждый R13 независимо представляет собой галоген, нитро, C1-C4-алкил,C1-C4-галогеналкил или C1-C4-алкокси. Примерами таких предпочтительных групп являются хлор, фтор,нитро, метил, этил, трифторметил и метокси. Предпочтительно каждый R14 независимо представляет собой галоген, нитро, C1-C4-алкил,C1-C4-галогеналкил, C1-C4-алкокси или C1-C4-галогеналкокси. Примерами таких предпочтительных групп являются хлор, фтор, нитро, метил, этил, трифторметил, метокси и трифторметокси. Более предпочтительно каждый R14 независимо представляет собой галоген, C1-C4-алкил,C1-C4-галогеналкил или C1-C4-алкокси. Соединения в представленных ниже табл. 1-27 иллюстрируют соединения по настоящему изобретению. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород, R4 представляет собой 2-хлор-4-фторфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 2,001-2,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2-хлорфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 3,001-3,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 3,5-дихлор-2-метоксифенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,0011,030, обозначены как соединения 4,001-4,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,3-дихлорфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 5,001-5,030 соответственно.-7 015647 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,4-дихлорфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 6,001-6,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,5-дихлорфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 7,001-7,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,6-дихлорфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 8,001-8,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,6-дихлор-4-трифторметилфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 9,001-9,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,6-диэтил-4-метилфенил, а R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,0011,030, обозначены как соединения 10,001-10,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2-фторфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 11,001-11,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2-метоксифенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 12,001-12,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2-трифторметоксифенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030,обозначены как соединения 13,001-13,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2-трифторметилфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030,обозначены как соединения 14,001-14,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 3-бром-2-хлор-6-фторфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,0011,030, обозначены как соединения 15,001-15,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,3-дихлор-6-фторфенил, а R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030,обозначены как соединения 16,001-16,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,6-дихлор-4-трифторметоксифенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 17,001-17,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2-хлор-6-трифторметилфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,0011,030, обозначены как соединения 18,001-18,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2-хлор-5-трифторметилфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,0011,030, обозначены как соединения 19,001-19,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2-хлор-5-фторфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 20,001-20,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,4-дихлор-5-фторфенил, а R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030,обозначены как соединения 21,001-21,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2-метокси-5-трифторметоксифенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 22,001-22,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,3-диметоксифенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 23,001-23,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2-хлор-3-трифторметилфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,0011,030, обозначены как соединения 24,001-24,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,4,6-триметилфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 25,001-25,030 соответственно.-8 015647 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,5-бис-(трифторметил)фенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,0011,030, обозначены как соединения 26,001-26,030 соответственно. 30 соединений формулы (I), где R1 и R2, оба, представляют собой водород; R4 представляет собой 2,3,6-трихлорфенил; R3 и R5 имеют значения, перечисленные в табл. 1 для соединений 1,001-1,030, обозначены как соединения 27,001-27,030 соответственно. Соединения по настоящему изобретению могут быть получены целым рядом способов, например способами, описанными на схемах 1-14. Схема 1 1) Соединения формулы (4), в которой значения R1, R2 и R4 определены для соединения формулы(I) и R16 представляет собой C1-C6-алкил, могут быть получены путем осуществления взаимодействия сложного аминопиразинового эфира формулы (2), в которой значения R1 и R2 определены для соединения формулы (I), и R16 представляет собой C1-C6-алкил, с производным кислоты формулы (3), в которой значение R4 определено для соединения формулы (I) и X представляет собой галоген или гидрокси,как представлено на схеме 1. Например, если (3) представляет собой хлорангидрид (т.е. где X представляет собой хлор), то взаимодействие может быть удобным образом осуществлено необязательно в присутствии основания, такого как триэтиламин или пиридин, в подходящем растворителе, таком как ацетонитрил или дихлорметан, необязательно с использованием микроволнового нагревания. В качестве альтернативы, если (3) представляет собой карбоновую кислоту (т.е. где X представляет собой гидрокси), то взаимодействие может быть удобным образом осуществлено методом амидного сочетания, например путем осуществления взаимодействия с конденсирующим агентом, таким как бис-(2-оксо-3-оксазолидинил)фосфинхлоридом, в присутствии основания, такого как триэтиламин, в подходящем растворителе, таком как дихлорметан, или другими методами амидной конденсации, обзор которых дан в Tetrahedron (2005), 61(46), 10827-10852. 2) Соединения формулы (5), в которой значения R1, R2 и R4 определены для соединения формулы(I), могут быть получены путем обработки соединения формулы (4), определение которого дано в п.1, с основанием в подходящем растворителе, таком как карбонат калия в N,N-диметилформамиде или гексаметилдисилазид лития в тетрагидрофуране, необязательно с использованием микроволнового нагревания. 3) Соединения формулы (6), в которой значения R1, R2, R4 и R10 определены для соединения формулы (I), могут быть получены путем осуществления взаимодействия соединения формулы (5), определение которого дано в п.2, с хлорангидридом формулы R10COCl или с ангидридом формулы (R10CO)2O, где значение R10 определено для соединения формулы (I), необязательно в присутствии основания, такого как триэтиламин или пиридин, необязательно в подходящем растворителе, таком как дихлорметан.-O-CO-R10, могут быть получены из соединения формулы (6), определение которого дано в п.3, путем осуществления взаимодействия с соединением формулы R3LG, в которой значение R3 определено для соединения формулы (I) и LG представляет собой уходящую группу, такую как галогенид, например бромид или йодид, или тозилат, мезилат или трифлат, в присутствии основания, такого как карбонат калия, необязательно в присутствии активатора/йодида, такого как йодид калия, в подходящем растворителе, таком как ацетонитрил или N,N-диметилформамид, необязательно с использованием микроволнового нагревания, как представлено на схеме 2. 5) Соединения формулы (Ib), т.е. соединение формулы (I), в которой R5 представляет собой гидрокси, могут быть получены путем обработки соединения формулы (Id), определение которого дано в п.4,основанием, таким как гидроксид натрия или карбонат калия, и водой в подходящем растворителе, таком как метанол или N,N-диметилформамид. 6) Соединения формулы (Ic), т.е. соединение формулы (I), в которой R5 представляет собой -O-R9,может быть получено из соединения формулы (Ib), определение которого дано в п.5, путем осуществления взаимодействия с соединением формулы R9LG, в которой значение R9 определено для соединения формулы (I) и LG представляет собой уходящую группу, такую как галогенид, например бромид или йодид, или тозилат, мезилат или трифлат, в присутствии основания, такого как карбонат калия, в подходящем растворителе, таком как N,N-диметилформамид. Схема 3- 10015647 7) Соединения формулы (Id), определение которых дано в п.4, могут быть, кроме того, получены укороченным путем непосредственно из соединения формулы (4), определение которого дано в п.1, путем осуществления взаимодействия с соединением формулы R3LG, определение которого дано в п.4, в присутствии основания, такого как гексаметилдисилазид натрия или калия, в подходящем растворителе,таком как тетрагидрофуран, необязательно с использованием микроволнового нагревания, с последующим осуществлением взаимодействия в том же реакторе с хлорангидридом формулы R10COCl или ангидридом формулы (R10CO)2O, определение которых дано в п.3, необязательно в присутствии основания,такого как триэтиламин, как представлено на схеме 3. 8) В качестве альтернативы соединения формулы (Id), определение которых дано в п.4, могут быть получены из соединения формулы (Ib), определение которого дано в п.5, путем осуществления взаимодействия с хлорангидридом формулы R10COCl или ангидридом формулы (R10CO)2O, определение которых дано в п.3, необязательно в присутствии основания, такого как триэтиламин, необязательно в подходящем растворителе, таком как дихлорметан. 9) Соединения формулы (Ib), определение которых дано в п.5, могут быть получены путем осуществления взаимодействия соединения формулы (4), определение которого дано в п.1, с соединением формулы R3LG, определение которого дано в п.4, в присутствии основания, такого как гексаметилдисилазид калия, в подходящем растворителе, таком как тетрагидрофуран, необязательно с использованием микроволнового нагревания (способ 1). 10) Соединения формулы (Ib), определение которых дано в п.5, могут быть также получены из соединения формулы (5), определение которого дано в п.2, путем осуществления взаимодействия с соединением формулы R3LG, определение которого дано в п.4, в присутствии основания, такого как гексаметилдисилазид калия, в подходящем растворителе, таком как тетрагидрофуран, необязательно с использованием микроволнового нагревания (способ 2). Синтез соединений формулы (5) был описан в п.2. 11) Соединения формулы (Ib), определение которых дано в п.5, могут быть также получены путем осуществления взаимодействия соединения формулы (4') с соединением формулы R3LG, определение которого дано в п.4, в присутствии основания, такого как гексаметилдисилазид натрия, в подходящем растворителе, таком как тетрагидрофуран, необязательно с использованием микроволнового нагревания(способ 3). Соединения формулы (4') могут быть также получены из соединения формулы (4) путем осуществления взаимодействия с основанием, таким как гексаметилдисилазид лития, в подходящем растворителе, таком как тетрагидрофуран или N,N-диметилформамид, необязательно с использованием микроволнового нагревания. Схема 4 12) Силильные соединения формулы (Ie), т.е. соединение формулы (I), в которой R5 представляет собой -O-Si(R11)3, могут быть получены из соединения формулы (Ib), определение которого дано в п.5,путем осуществления взаимодействия с триалкилсилилхлоридом формулы (R11)3SiCl в подходящем растворителе, таком как тетрагидрофуран или ацетонитрил, в присутствии основания, такого как триэтиламин, как представлено на схеме 4. Схема 5- 11015647 13) Сульфонильные соединения формулы (7), в которой значения R1, R2, R4 и R12 определены для соединения формулы (I), могут быть получены из соединения формулы (5), определение которого дано в п.2, путем осуществления взаимодействия с сульфонилхлоридом формулы R12SO2Cl, в которой значениеR12 определено для соединения формулы (I), в присутствии основания, такого как триэтиламин, в подходящем растворителе, таком как тетрагидрофуран или дихлорметан, как представлено на схеме 5. 14) Сульфонильные соединения формулы (If), т.е. соединение формулы (I), в которой R5 представляет собой -O-SO2-R12, могут быть получены путем осуществления взаимодействия соединения формулы(7), определение которого дано в п.13, с соединением формулы R3LG, определение которого дано в п.4, в присутствии основания, такого как гексаметилдисилазид натрия или калия, в подходящем растворителе,таком как тетрагидрофуран, необязательно с использованием микроволнового нагревания. 15) В качестве альтернативы соединения формулы (If), определение которых дано в п.14, могут быть получены путем осуществления взаимодействия соединения формулы (Ib), определение которого дано в п.5, с сульфонилхлоридом формулы R12SO2Cl, определение которого дано в п.13, в присутствии основания, такого как триэтиламин, в подходящем растворителе, таком как тетрагидрофуран или дихлорметан. Схема 6 16) Смесь N-оксидов формулы (Ig), т.е. соединение формулы (I), в которой атом азота в 5-положении окислен, и R5 представляет собой -О-CO-R10, и N-оксиды формулы (Ih), т.е. соединение формулы (I), в которой атом азота в 5-положении окислен, и R5 представляет собой гидрокси, могут быть получены путем осуществления взаимодействия соединения формулы (Id), определение которого дано в п.4, с окислителем, например с пероксикислотой, такой как перокситрифторуксусная кислота, полученная in situ, например, путем воздействия трифторуксусным ангидридом и пероксидом водорода на гранулы мочевины, в подходящем растворителе, таком как дихлорметан, как представлено на схеме 6. Схема 7 17) Соединения формулы (8), в которой значения R1 и R2 определены для соединения формулы (I) иR представляет собой C1-C6-алкил, могут быть получены путем осуществления взаимодействия сложного аминопиразинового эфира формулы (2), определение которого дано в п.1, с диалкилмалонатом формулы СН 2(CO2R17)2, в которой R17 представляет собой C1-C6-алкил, в присутствии основания, такого как метоксид натрия, в подходящем растворителе, таком как метанол, при температуре от 20 С до температуры возгонки, предпочтительно при нагревании с обратным холодильником, как представлено на схеме 7. 17- 12015647 18) Соединения формулы (9), в которой значения R1 и R2 определены для соединения формулы (I),могут быть получены путем гидролиза или декарбоксилирования соединения формулы (8), определение которого дано в п.17, путем обработки сильной водной кислотой, например концентрированной соляной кислотой, или, в качестве альтернативы, путем обработки разбавленной водной кислотой, например разбавленной соляной кислотой, и водой в подходящем растворителе, таком как этанол, необязательно с использованием микроволнового нагревания. 19) Соединения формулы (11), в которой значения R1, R2 и R8 определены для соединения формулы(I), могут быть получены путем осуществления взаимодействия соединения формулы (9), определение которого дано в п.18, с соединением олова формулы (10), в которой значение R8 определено для соединения формулы (I), в присутствии основания, такого как 4-диметиламинопиридин, и в подходящем растворителе, таком как диметилсульфоксид. Соединения олова (10) известны в литературе и могут быть получены способами, описанными в Aust. J. Chem., 1979, 32, 1561-6 и J. Chem. Soc. Perkin Trans. 1, 1990,3, 715-20. Схема 8 20) Нитросоединения формулы (13), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I), могут быть получены путем нитрования соединения формулы (12), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I), нитрующей смесью, например дымящей азотной кислотой или концентрированной серной кислотой, представленной на схеме 8. 21) Аминосоединения формулы (14), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I), могут быть получены путем восстановления соединения формулы (13), определение которого дано в п.20, с использованием стандартных условий восстановления, например железные опилки в водной соляной кислоте. 22) Ацилированные соединения формулы (15), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I) и значение R17 определено в п.17, могут быть получены путем ацилирования соединения формулы (14), определение которого дано в п.21, например путем осуществления взаимодействия с хлорангидридом формулы R17COCl или ангидридом (R17CO)2O, где значение R17 определено в п.17, в присутствии основания, такого как триэтиламин, в подходящем растворителе, таком как дихлорметан. 23) Алкилированные соединения формулы (16), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I) и R18 представляет собой C1-C6-алкил, могут быть получены путем алкилирования соединения формулы (14), определение которого дано в п.21, например путем осуществления взаимодействия с соединением формулы R18LG, в которой R18 представляет собой C1-C6-алкил и LG представляет собой уходящую группу, такую как галогенид, например бромид или йодид, или тозилат,мезилат или трифлат, необязательно в присутствии основания, такого как карбонат калия, в подходящем растворителе, таком как этанол или толуол.- 13015647 24) Соединения формулы (17), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I) и R19 представляет собой циано, C1-C4-алкилтио, галоген или гидрокси, могут быть получены путем диазотирования соединения формулы (14), определение которого дано в п.21, например путем осуществления взаимодействия с алкилнитритом, в присутствии подходящего нуклеофила, например цианида калия, в присутствии соли меди, например цианида меди, в подходящем растворителе, таком как ацетонитрил. Схема 9 25) Галогеналкильные соединения формулы (19), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I), X представляет собой галоген и n+m=3, могут быть получены путем осуществления взаимодействия соединения формулы (18) с галогенирующим агентом, таким как галоген формулы Х 2, в которой X представляет собой хлор или бром, в присутствии света, или N-галогенсукцинимид в которой X представляет собой хлор, бром или йод, в присутствии радикального иниформулы циатора, такого как бензоилпероксид, в подходящем растворителе, таком как тетрахлорид углерода, и необязательно в присутствии источника света, такого как ртутно-галогеновая лампа мощностью 500 Вт,при нагревании с обратным холодильником, как представлено на схеме 9. 26) Соединения формулы (20), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I) и R20 представляет собой C1-C8-алкокси, C1-C8-тиоалкокси, необязательно замещенный фенокси, необязательно замещенный тиофенокси, циано, гидрокси, C1-C4-алкиламино или ди(C1-C4 алкил)амино, могут быть получены путем осуществления взаимодействия соединения формулы (19),определение которого дано в п.25, где n=2 и m=1, с соединением формулы R20H, в которой R20 представляет собой C1-C8-алкокси, C1-C8-тиоалкокси, необязательно замещенный фенокси, необязательно замещенный тиофенокси, моно(C1-C4)алкиламино или ди(C1-C4-алкил)амино, в присутствии основания,такого как карбонат калия или гидрид натрия, в подходящем растворителе, таком как этанол илиN,N-диметилформамид, с соединением формулы R20M, в которой R20 представляет собой циано и М представляет собой металл, такой как натрий, или в которой R20 представляет собой гидрокси и М представляет собой металл, такой как натрий, в подходящем растворителе, таком как этанол или- 14015647 27) Альдегиды формулы (21), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I), могут быть получены из соединения формулы (19), определение которого дано в п.25, гдеn=1 и m=2, путем гидролиза кислотой, например водной серной кислотой, или из соединения формулы(19), определение которого дано в п.25, где n=2 и m=1, путем осуществления взаимодействия с диметилсульфоксидом в присутствии основания, такого как карбонат калия. 28) Соединения формулы (22), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I) и значение R17 определено в п.17, могут быть получены из соединения формулы (19), определение которого дано в п.25, где n=0 и m=3, путем гидролиза спиртом формулы R17OH, в которой значение R17 определено в п.17, необязательно в присутствии соли серебра, например нитрата серебра. 29) Соединения формулы (23), в которой значения R1, R2, R3, R8 и R10 определены для соединения формулы (I) и R21 представляет собой C1-C8-алкил или необязательно замещенный бензил, могут быть получены из альдегида формулы (21), определение которого дано в п.27, путем осуществления взаимодействия с гидроксиламином R21O-NH2 или с его солью, где R21 представляет собой C1-C8-алкил или необязательно замещенный бензил, например с гидрохлоридом, необязательно в присутствии основания,такого как ацетат натрия, в подходящем растворителе, таком как этанол. 30) Соединения формулы (24), в которой значения R1, R2, R3, R8, R10 определены для соединения формулы (I), могут быть получены из соединения формулы (23), определение которого дано в п.29, в конкретном случае, когда R21 представляет собой водород, путем осуществления взаимодействия с дегидратирующим агентом, таким как уксусный ангидрид. Схема 10 31) В некоторых случаях, когда арилуксусные кислоты не являются коммерчески доступными, их необходимо синтезировать. Типичный синтез представлен на схеме 10. Бензилгалогениды формулы (26),в которой значение R8 определено для соединения формулы (I) и X представляет собой галоген, могут быть получены путем осуществления взаимодействия замещенного толуола формулы (25), в которой значение R8 определено для соединения формулы (I), с галогенирующим агентом, таким как галоген формулы Х 2, в которой X представляет собой хлор или бром, в присутствии света, илиN-галогенсукцинимид формулы в которой X представляет собой хлор, бром или йод, в присутствии радикального инициатора, такого как бензоилпероксид, в подходящем растворителе, таком как тетрахлорид углерода, и необязательно в присутствии источника света, такого как ртутно-галогеновая лампа мощностью 500 Вт, при нагревании с обратным холодильником. 32) Бензилцианиды формулы (27), в которой значение R8 определено для соединения формулы (I),могут быть получены путем осуществления взаимодействия соединения формулы (26), определение которого дано в п.31, с цианидом металла, таким как цианид калия, в подходящем растворителе, таком как этанол, при нагревании с обратным холодильником. 33) Фенилуксусные кислоты формулы (28), в которой значение R8 определено для соединения формулы (I), могут быть получены путем гидролиза соединения формулы (27), определение которого дано в п.32, с использованием водной кислоты или щелочи, предпочтительно водной кислоты, такой как водная серная кислота, при нагревании с обратным холодильником. 34) Нитросоединения формулы (30), в которой значение R8 определено для соединения формулы (I) и значение R16 определено в п.1, могут быть получены путем нитрования соединения формулы (29), в которой значение R8 определено для соединения формулы (I) и значение R16 определено в п.1, нитрующей смесью, например дымящей азотной кислотой и концентрированной серной кислотой, как представлено на схеме 11. 35) Аминосоединения формулы (31), в которой значение R8 определено для соединения формулы(I) и значение R16 определено в п.1, могут быть получены путем восстановления соединения формулы(30), определение которого дано в п.34, с использованием стандартных условий восстановления, например железных опилок в водной соляной кислоте. 36) Соединения формулы (32), в которой значение R8 определено для соединения формулы (I), значение R16 определено в п.1, и R19 представляет собой циано, C1-C4-алкилтио, галоген или гидрокси, могут быть получены путем диазотирования соединения формулы (31), определение которого дано в п.35, например, путем осуществления взаимодействия с алкилнитритом, в присутствии подходящего нуклеофила, например цианида калия, в присутствии соли меди, например цианида меди, в подходящем растворителе, таком как ацетонитрил. Схема 12 37) Соединения формулы (36), в которой значения R1 и R2 определены для соединений формулы (I) и значение R16 определено в п.1, могут быть получены из соединения формулы (33), в которой X представляет собой галоген, такой как хлор, бром или йод, как представлено на схеме 12. Это может быть достигнуто сочетанием по Сузуки с использованием бороновой кислоты R1B(OH)2 или R2B(OH)2 в присутствии палладиевого катализатора, такого как ацетат палладия (II), в присутствии лиганда, такого как 2'-дициклогексилфосфино-2,6-диметокси-1,1'-бифенил, в присутствии основания, такого как фосфат калия, в подходящем растворителе, таком как смесь толуола и воды, при температуре от 50 до 150 С, предпочтительно от 100 до 120 С, необязательно с использованием микроволнового нагревания. В качестве альтернативы может применяться сочетание по Стилле оловосодержащего реагента R1Sn(R22)3 илиR2Sn(R22)3, где R22 представляет собой C1-C6-алкил, в присутствии палладиевого катализатора, такого как хлорид палладия (II), в присутствии лиганда, такого как три-трет-бутилфосфин, в подходящем растворителе, таком как N,N-диметилформамид или ацетонитрил, при температуре от 0 до 150 С, предпочтительно от 75 до 120 С.R определены для соединения формулы (I) и значение R16 определено в п.1, известны из литературы,например из J. Med. Chem. (1967), 10, 66; J. Med. Chem. (1967), 10, 899 и J, Med. Chem. (1967), 10, 598,существует потребность в получении указанных соединений в результате более коротких или более удобных методов синтеза. Например, соединения формулы (37), в которой значения R1 и R2 определены для соединения формулы (I), могут быть синтезированы путем конденсации диаминоурацила формулы(35) или его соли с дикетоном или кетоальдегидом формулы (36), в которой значения R1 и R2 определены для соединения формулы (I), в присутствии основания, такого как водный раствор аммиака. 39) Пиразинаминокислоты формулы (38), в которой значения R1 и R2 определены для соединения формулы (I), могут быть получены в результате раскрытия кольца соединения формулы (37), в которой значения R1 и R2 определены для соединения формулы (I), в присутствии основания, такого как гидроксид натрия, и воды, необязательно с использованием микроволнового нагревания. 40) Соединения формулы (39), в которой значения R1 и R2 определены для соединения формулы (I) и значение R16 определено в п.1, могут быть получены из соединения формулы (38), в которой значенияR1 и R2 определены для соединения формулы (I), например, путем этерификации спиртом формулыR16OH, в которой значение R16 определено в п.1, таким как метанол, в присутствии кислотного катализатора, такого как ацетилхлорид. Соединения формулы (I) по настоящему изобретению могут использоваться в качестве гербицидов в немодифицированной форме, как они были получены в результате синтеза, но, как правило, их включают в состав гербицидных композиций, используя различным путем адъюванты, такие как носители,растворители и поверхностно-активные вещества. Составы могут принимать различную физическую форму, например форму присыпок, гелей, смачивающих порошков, диспергируемых в воде гранул, диспергируемых в воде таблеток, шипучих гранул, эмульгируемых концентратов, микроэмульгируемых концентратов, эмульсий типа "масло-в-воде", жидких масляных смесей, дисперсий в воде, дисперсий в масле, суспоэмульсий, суспензий капсул, эмульгируемых гранул, растворимых жидкостей, растворимых в воде концентратов (водой или смешивающимся с водой органическим растворителем в качестве носителя), пропитанных полимерных пленок, или находиться в виде других форм, известных из Manual onDevelopment and Use of FAO Specifications for Plant Protection Products, 5th Edition, 1999. Такие составы могут использоваться сразу же или их разбавляют перед использованием. Разбавление может проводиться, например, водой, жидкими удобрениями, питательными микроэлементами, биологическими организмами, маслом или растворителями. Составы могут быть получены, например, путем смешивания активного ингредиента с адъювантами с целью получения композиций в форме мелкоизмельченных твердых веществ, гранул, растворов,дисперсий или эмульсий. Активные ингредиенты могут быть также включены в состав с другими адъювантами, такими как мелкоизмельченные твердые вещества, минеральные масла, масла растительного и животного происхождения, модифицированные масла растительного и животного происхождения, органические растворители, вода, поверхностно-активные вещества или их сочетания. Активные ингредиенты могут быть также заключены в очень мелкие микрокапсулы, состоящие из полимера. Микрокапсулы содержат активные ингредиенты в пористом носителе. Это делает возможным высвобождение регулируемых количеств активных ингредиентов в окружающую среду (например, замедленное высвобождение). Микрокапсулы обычно имеют в диаметре от 0,1 до 500 мкм. Они содержат активные ингредиенты в количестве приблизительно от 25 до 95 мас.% относительно массы капсулы. Активные ингредиенты могут находиться в форме монолитного твердого вещества, в форме мелких частиц в твердой или жидкой дисперсии или в форме подходящего раствора. Образующие капсулу мембраны содержат, например, натуральные или синтетические каучуки, целлюлозу, сополимеры стирола/бутадиена, полиакрилонитрил,полиакрилат, полиэфиры, полиамиды, полимочевины, полиуретан или химически модифицированные полимеры и ксантаты крахмала или другие полимеры, известные в этой связи специалисту в данной об 2- 17015647 ласти техники. В качестве альтернативы могут быть сформированы очень мелкие микрокапсулы, в которых активный ингредиент содержится в форме мелкоизмельченных частиц в твердой матрице из формирующего основу вещества, но микрокапсулы сами по себе не инкапсулированы. Адъюванты, которые подходят для приготовления композиций по настоящему изобретению, известны выше. В качестве жидких носителей могут быть использованы: вода, толуол, ксилол, петролейный эфир, растительные масла, ацетон, метилэтилкетон, циклогексанон, ангидриды кислот, ацетонитрил,ацетофенон, амилацетат, 2-бутанон, бутиленкарбонат, хлорбензол, циклогексан, циклогексанол, сложные алкиловые эфиры уксусной кислоты, диацетоновый спирт, 1,2-дихлорпропан, диэтаноламин, парадиэтилбензол, диэтиленгликоль, диэтиленгликоля абиетат, бутиловый эфир диэтиленгликоля, этиловый эфир диэтиленгликоля, метиловый эфир диэтиленгликоля, N,N-диметилформамид, диметилсульфоксид,1,4-диоксан, дипропиленгликоль, метиловый эфир дипропиленгликоля, дибензоат дипропиленгликоля,дипрокситол, алкилпирролидон, этилацетат, 2-этилгексанол, этиленкарбонат, 1,1,1-трихлорэтан,2-гептанон, -пинен, d-лимонен, этиллактат, этиленгликоль, бутиловый эфир этиленгликоля, метиловый эфир этиленгликоля, -бутиролактон, глицерин, глицерина ацетат, глицерина диацетат, глицерина триацетат, гексадекан, гексиленгликоль, изоамилацетат, изоборнилацетат, изооктан, изофорон, изопропилбензол, изопропилмиристат, молочная кислота, лауриламин, мезитилоксид, метоксипропанол,метилизоамилкетон, метилизобутилкетон, метиллаурат, метилоктаноат, метилолеат, хлористый метилен,м-ксилол, н-гексан, н-окстиламин, октадекановая кислота, октиламинацетат, олеиновая кислота,олеиламин, о-ксилол, фенол, полиэтиленгликоль (PEG400), пропионовая кислота, пропиллактат,пропиленкарбонат, пропиленгликоль, метиловый эфир пропиленгликоля, п-ксилол, толуол, триэтилфосфат, триэтиленгликоль, ксилолсульфоновая кислота, парафин, минеральное масло, трихлорэтилен, перхлорэтилен, этилацетат, амилацетат, бутилацетат, метиловый эфир пропиленгликоля, метиловый эфир диэтиленгликоля, метанол, этанол, изопропанол и другие спирты с большей молекулярной массой, такие как амиловый спирт, тетрагидрофурфуриловый спирт, гексанол, октанол, этиленгликоль, пропиленгликоль, глицерин, N-метил-2-пирролидон и т.п. Вода, как правило, является излюбленным носителем для разбавления концентратов. Подходящие твердые носители представляют собой, например, тальк, диоксидтитана, пирофиллитовую глину, двуокись кремния, аттапульгитовую глину, диатомовую землю, известняк, карбонат кальция, бентонит, монтмориллонит кальция, шелуху семян хлопчатника, пшеничную муку, соевую муку, пемзу, древесную муку, измельченную шелуху грецких орехов, лигнин и похожие вещества, как описано, например, в CFR 180.1001. (с)(d). Большое количество поверхностно-активных веществ может быть с успехом использовано в твердых и в жидких составах, в особенности в тех составах, которые могут быть разбавлены носителем перед применением. Поверхностно-активные вещества могут быть анионными, катионными, неионными или полимерными и могут использоваться в качестве эмульгаторов, увлажняющих средств или суспендирующих средств или для других целей. Обычные поверхностно-активные вещества включают, например,соли алкилсульфатов, такие как лаурилсульфат диэтаноламмония; соли алкиларилсульфонатов, такие как додецилбензолсульфонат кальция; продукты присоединения алкилфенола/алкиленоксида, такие как этоксилат нонилфенола; продукты присоединения спирта/алкиленоксида, такие как этоксилат тридецилового спирта; мыла, такие как стеарат натрия; соли алкилнафталинсульфонатов, такие как дибутилнафталинсульфонат натрия; сложные диалкиловые эфиры сульфосукцинатов, такие как ди(2 этилгексил)сульфосукцинат натрия; сложные эфиры сорбитола, такие как олеат сорбитола; четвертичные амины, такие как хлорид лаурилтриметиламмония, сложные жирнокислые эфиры полиэтиленгликоля,такие как стеарат полиэтиленгликоля; блок-сополимеры этиленоксида и пропиленоксида и соли моно- и диалкилфосфатных эфиров; а также дополнительные вещества, например, описанные в "McCutcheon'sDetergents and Emulsifiers Annual", MC Publishing Corp., Ridgewood, New Jersey, 1981. Дополнительные адъюванты, которые обычно могут быть использованы в пестицидных составах,включают ингибиторы кристаллизации, модификаторы вязкости, суспендирующие средства, красители,антиоксиданты, вспениватели, светопоглотители, вспомогательные вещества для смешивания, пеногасители, комплексообразующие средства, нейтрализующие или модифицирующие рН вещества и буферные смеси, ингибиторы коррозии, ароматизаторы, увлажняющие средства, усилители поглощения, питательные микроэлементы, пластификаторы, глиданты, смазки, диспергирующие вещества, загустители, антифризы, бактерицидные средства, а также жидкие и твердые удобрения. Композиции по настоящему изобретению могут дополнительно содержать добавку, включающую масло растительного или животного происхождения, минеральное масло, сложные алкиловые эфиры таких кислот или смеси таких кислот и производных кислот. Количество масляной добавки в композиции по настоящему изобретению, как правило, составляет от 0,01 до 10% от распыляемой смеси. Например, масляная добавка может быть добавлена в распылитель в желаемой концентрации после приготовления распыляемой смеси. Предпочтительные масляные добавки включают минеральные масла или масла растительного происхождения, например рапсовое масло, оливковое масло или подсолнечное масло,эмульгированные растительные масла, такие как AMIGO (Rhone-Poulenc Canada Inc.), сложные алкиловые эфиры масел растительного происхождения, например метиловые производные, или масло живот- 18015647 ного происхождения, такое как рыбий жир или говяжий жир. Предпочтительная масляная добавка, по существу, содержит, например, в качестве активных компонентов 80 мас.% сложных алкиловых эфиров рыбьего жира и 15 мас.% метилированного рапсового масла, а также 5 мас.% традиционных эмульгаторов и модификаторов рН. Особенно предпочтительные масляные добавки содержат сложные алкиловые эфиры C8-C22-жирных кислот, особенно метиловые производные C12-C18-жирных кислот, например сложные метиловые эфиры лауриновой кислоты, пальмитиновой кислоты и олеиновой кислоты, имеющие большое значение. Указанные сложные эфиры известны как метиллаурат (CAS-111-82-0),метилпальмитат (CAS-112-39-0) и метилолеат (CAS-112-62-9). Предпочтительное метилэфирное производное жирной кислоты представляет собой Emery 2230 и 2231 (Cognis GmbH). Указанные и другие масляные производные также известны из Compendium of Herbicide Adjuvants, 5th Edition, SouthernIllinois University, 2000. Применение и действие масляных добавок может быть дополнительно улучшено путем их сочетания с поверхностно-активными веществами, такими как неионные, анионные или катионные поверхностно-активные вещества. Примеры подходящих анионных, неионных и катионных поверхностноактивных веществ перечислены на с. 7 и 8 документа WO 97/34485. Предпочтительные поверхностноактивные вещества представляют собой анионные поверхностно-активные вещества додецилбензилсульфонатного типа, в особенности их соли кальция, а также неионные поверхностно-активные вещества типа этоксилатов жирных спиртов. Особое предпочтение отдается C12-C22-жирным спиртам со степенью этоксилирования от 5 до 40. Примерами коммерчески доступных поверхностно-активных веществ являются вещества Genapol (Clariant AG). Также предпочтительными являются силиконовые поверхностноактивные вещества, в особенности модифицированные полиалкилоксидом гептаметилтрилоксаны, которые являются коммерчески доступными, например, в виде Silwet L-77, а также перфорированные поверхностно-активные вещества. Концентрация поверхностно-активных веществ относительно общего содержания добавок составляет, как правило, от 1 до 30 мас.%. Примерами масляных добавок, состоящих из смесей масла или минеральных масел или их производных с поверхностно-активными веществами, являются Edenor ME SU, Turbocharge (Syngenta AG, CH) или ActipronC (BP Oil UK Limited, GB). При желании, также возможно использование в составах упомянутых поверхностно-активных веществ самих по себе, т.е. без масляных добавок. Кроме того, добавление органического растворителя к смеси масляной добавки и поверхностноактивного вещества может способствовать дополнительному усилению действия. Подходящими растворителями являются, например, Solvesso (ESSO) или Aromatic Solvent (Exxon Corporation). Концентрация таких растворителей может составлять от 10 до 80 мас.% относительно общей массы. Масляные добавки, которые присутствуют в смеси с растворителями, описаны, например, в US-А-4834908. Коммерчески доступная масляная добавка, раскрытая в указанном документе, известна под названием MERGE(BASF Corporation). Дополнительной масляной добавкой, которая является предпочтительной по настоящему изобретению, является SCORE (Syngenta Crop Protection Canada),В дополнение к перечисленным выше масляным добавкам, для целей усиления действия композиций по настоящему изобретению также возможно добавление в распыляемую смесь содержащих алкилпирролидоны составов (например, Agrimax). Также могут быть использованы составы синтетических кристаллических решеток, например полиакриламида, поливиниловых соединений или поли-1-п-ментена(например, Bond, Courier или Emerald). Также возможно добавление в распыляемую смесь растворов, содержащих пропионовую кислоту, например Eurogkem Pen-e-trate, в качестве усиливающего действие средства. Гербицидные композиции, как правило, содержат от 0,1 до 99 мас.%, в особенности от 0,1 до 95 мас.% соединений формулы (I) и от 1 до 99,9 мас.% адъюванта, которые предпочтительно содержат от 0 до 25 мас.% поверхностно-активного вещества. Хотя коммерческие продукты предпочтительно составлены в виде концентратов, конечный пользователь обычно использует разбавленные составы. Нормы внесения соединений формулы (I) могут варьировать в широком диапазоне и зависят от природы почвы; способа внесения (до появления или после появления всходов; протравливание семян; внесение в семенную борозду; беспахотное внесение и т.д.); сельскохозяйственной культуры; травы или сорняка, с которым подлежит бороться; преобладающих климатических условий и других факторов, определяемых способом внесения; времени внесения и сельскохозяйственной культуры-мишени. Соединения формулы (I) по настоящему изобретению, как правило, вносят в количестве от 10 до 2000 г/га, в особенности от 50 до 1000 г/га.- 19015647 Предпочтительные композиции, в частности, имеют следующие составы (% = мас.%): Эмульгируемые концентраты. Активный ингредиент: 1-95%, предпочтительно 60-90%. Поверхностно-активное вещество: 1-30%, предпочтительно 5-20%. Жидкий носитель: 1-80%, предпочтительно 1-35%. Присыпки. Активный ингредиент: 0,1-10%, предпочтительно 0,1-5%. Твердый носитель: 99,9-90%, предпочтительно 99,9-99%. Суспендируемые концентраты. Активный ингредиент: 5-75%, предпочтительно 10-50%. Вода: 94-24%, предпочтительно 88-30%. Поверхностно-активное вещество: 1-40%, предпочтительно 2-30%. Увлажняющие порошки. Активный ингредиент: 0,5-90%, предпочтительно 1-80%. Поверхностно-активное вещество: 0,5-20%, предпочтительно 1-15%. Твердый носитель: 5-95%, предпочтительно 15-90%. Гранулы. Активный ингредиент: 0,1-30%, предпочтительно 0,1-15%. Твердый носитель: 99,5-70%, предпочтительно 97-85%. Следующие примеры дополнительно иллюстрируют, но не ограничивают, настоящее изобретение. Примеры составов для гербицидов формулы (I) (% = мас.%) Эмульсии с любой желаемой концентрацией могут быть получены из таких концентратов путем разбавления водой. Растворы применимы для использования в форме микрокапель. Активный ингредиент тщательно смешивают с адъювантами, смесь тщательно измельчают в подходящей мельнице с получением увлажняющих порошков, которые могут быть разбавлены водой с получением суспензий с любой желаемой концентрацией. Активный ингредиент растворяют в хлористом метилене и наносят на носитель путем напыления, а затем выпаривают растворитель в вакууме. Мелкоизмельченный активный ингредиент равномерно наносят в миксере на носитель, смоченный полиэтиленгликолем. Таким способом получают не образующие пыли покрытые гранулы. Активный ингредиент смешивают и измельчают с адъювантами и смачивают смесь водой. Смесь спрессовывают, а затем сушат в струе воздуха. Готовые к применению присыпки получают путем смешивания активного ингредиента с носителями и измельчения смеси на подходящей мельнице. Мелкоизмельченный активный ингредиент тщательно смешивают с адъювантами с получением суспендируемого концентрата, из которого путем разбавления водой могут быть получены суспензии с любой желаемой концентрацией. Изобретение также относится к способу борьбы с растениями, который включает нанесение на растения или в их локус гербицидно эффективного количества соединения формулы (I). Изобретение также относится к способу ингибирования роста растений, который включает нанесение на растения или в их локус гербицидно эффективного количества соединения формулы (I).- 21015647 Изобретение также относится к способу селективной борьбы с травами и сорняками в полезных сельскохозяйственных культурах, который включает нанесение на полезные культуры или в их локус или на посевную площадь гербицидно эффективного количества соединения формулы (I). Полезные сельскохозяйственные культуры, в отношении которых может быть использована композиция по настоящему изобретению, включают многолетние культуры, такие как цитрусовые, культурный виноград, орехи, масличные пальмы, оливы, семечковые, косточковые и каучуконосы, и однолетние сельскохозяйственные культуры, такие как злаковые, например ячмень, пшеницу, хлопчатник, масличный рапс, кукурузу, рис, соевые бобы, сахарную свеклу, сахарный тростник, подсолнечник, декоративные растения и овощи, в особенности злаковые и кукурузу. Травы и сорняки, с которыми подлежит бороться, могут представлять собой однодольные, например Agrostis, Alopecurus, Avena, Bromus, Cyperus, Digitaria, Echinochloa, Lolium, Monochoria, Rottboellia,Sagittaria, Scirpus, Setaria, Sida и Sorghum, и двудольные, например Abutilon, Amaranthus, Chenopodium,Chrysanthemum, Galium, Ipomoea, Nasturtium, Sinapis, Solanum, Stellaria, Veronica, Viola и Xanthium. Следует понимать, что сельскохозяйственные культуры также включают такие сельскохозяйственные культуры, которые были наделены свойствами резистентности к гербицидам или классам гербицидов (например, ALS-, GS-, EPSPS-, РРО- и HPPD-ингибиторы) традиционными способами селекции или методами генной инженерии. Примером сельскохозяйственной культуры, которая была наделена резистентностью к имидазолинонам, например к имазамоксу, традиционными способами селекции, является сурепица Clearfield (канола). Примеры сельскохозяйственных культур, которые были наделены резистентностью к гербицидам методами генной инженерии, включают, например, глифозат- и глюфозинатрезистентные виды кукурузы, коммерчески доступные под торговыми названиями RoundupReady иLibertyLink. Следует понимать, что сельскохозяйственные культуры также включают такие культуры, которые были наделены свойствами резистентности к вредным насекомым методами генной инженерии, например кукуруза Bt (резистентная к огневке кукурузной), хлопчатник Bt (резистентный к долгоносику хлопковому), а также картофель Bt (резистентный к колорадскому жуку). Примерами кукурузы Bt являютсяBt 176 гибриды кукурузы NK (Syngenta Seeds). Токсин Bt представляет собой белок, который в природе синтезируется почвенными бактериями Bacillus thuringiensis. Примеры токсинов или способных синтезировать такие токсины трансгенных растений описаны в ЕР-А-451878, ЕР-А-374753, WO 93/07278,WO 95/34656, WO 03/052073 и ЕР-А-427529. Примерами трансгенных растений, содержащих один или несколько генов, кодирующих резистентность к насекомым, и экспрессирующих один или несколько токсинов, являются KnockOut (кукуруза), Yield Gard (кукуруза), NuCOTIN33B (хлопчатник), Bollgard (хлопчатник), NewLeaf (картофель), NatureGard и Protexcta. Возделываемые растения или их посевной материал могут быть резистентны и к гербицидам и в то же самое время к насекомым("stacked" transgenic events). Например, семена могут обладать способностью экспрессировать инсектицидный белок Cry3, будучи одновременно толерантной к глифозату. Также следует понимать, что сельскохозяйственными культурами являются такие культуры, которые были получены традиционными способами селекции или методами генной инженерии и содержат так называемые выходные характеристики (например, улучшенную стойкость при хранении, повышенную питательную ценность и улучшенный вкус). Посевные площади включают землю, на которой сельскохозяйственные культуры уже произрастают, и землю, предназначенную для культивирования таких сельскохозяйственных культур. Соединения формулы (I) по настоящему изобретению могут также использоваться в сочетании с одним или несколькими другими гербицидами. В частности, важными являются следующие смеси соединения формулы (I). Смеси соединения формулы (I) с синтетическим ауксином (например, соединение формулы (I) + клопиралид (162), соединение формулы (I) + 2,4-D (211), соединение формулы (I) + дикамба (228), соединение формулы (I) + МСРА (499), соединение формулы (I) + хинклорак (712) или соединение формулы (I) + аминопиралид (CAS RN 150114-71-9. Смеси соединения формулы (I) с дифлуфензопиром (252). Смеси соединения формулы (I) с ацетанилидом (например, соединение формулы (I) + ацетохлор (5),соединение формулы (I) + диметенамид (260), соединение формулы (I) + метолахлор (548), соединение формулы (I) + S-метолахлор (549) или соединение формулы (I) + претилахлор (656. Смеси соединения формулы (I) с флампроп-М (355). Смеси соединения формулы (I) с флуфенацетом (BAY FOE 5043) (369). Смеси соединения формулы (I) с пироксасульфоном (CAS RN 447399-55-5). Смеси соединения формулы (I) с триазином (например, соединение формулы (I) + атразин (37) или соединение формулы (I) + тербутилазин (775.(CAS RN 210631-68-8), соединение формулы (I) + 4-гидрокси-3-2-[(2-метоксиэтокси)метил]-6(трифторметил)-3-пиридинил]карбонил]бицикло[3.2.1]окт-3-ен-2-он (CAS RN 352010-68-5) или соединение формулы (I) + 4-гидрокси-3-2-(3-метоксипропил)-6-(дифторметил)-3-пиридинил]карбонил]бицикло[3.2.1]окт-3-ен-2-он). Смеси соединения формулы (I) с ингибитором HPPD и триазином. Смеси соединения формулы (I) с глифозатом (419). Смеси соединения формулы (I) с глифозатом и ингибитором HPPD (например, соединение формулы (I) + глифозат + изоксафлутол, соединение формулы (I) + глифозат + мезотрион, соединение формулы (I) + глифозат + пирасульфотол (CAS RN 365400-11-9), соединение формулы (I) + глифозат + сулькотрион, соединение формулы (I) + глифозат + темботрион, соединение формулы (I) + глифозат + топрамезон, соединение формулы (I) + глифозат + 4-гидрокси-3-2-[(2-метоксиэтокси)метил]-6(трифторметил)-3-пиридинил]карбонил]бицикло[3.2.1]окт-3-ен-2-он или соединение формулы (I) + глифозат + 4-гидрокси-3-2-(3-метоксипропил)-6-(дифторметил)-3-пиридинил]карбонил]бицикло[3.2.1]окт 3-ен-2-он). Смеси соединения формулы (I) с глюфозинатаммонием (418). Смеси соединения формулы (I) с глюфозинатаммонием и ингибитором HPPD (например,соединение формулы (I) + глюфозинатаммоний + изоксафлутол, соединение формулы (I) + глюфозинатаммоний + мезотрион, соединение формулы (I) + глюфозинатаммоний + пирасульфотол(CAS RN 365400-11-9), соединение формулы (I) + глюфозинатаммоний + сулькотрион, соединение формулы (I) + глюфозинатаммоний + темботрион, соединение формулы (I) + глюфозинатаммоний + топрамезон, соединение формулы (I) + глюфозинатаммоний + 4-гидрокси-3-2-[(2-метоксиэтокси)метил]-6(трифторметил)-3-пиридинил]карбонил]бицикло[3.2.1]окт-3-ен-2-он или соединение формулы (I) + глюфозинатаммоний+ 4-гидрокси-3-2-(3-метоксипропил)-6-(дифторметил)-3-пиридинил]карбонил]бицикло[3.2.1]окт-3-ен-2-он). Смеси соединения формулы (I) с ингибитором ALS или AHAS (например, соединение формулы (I) + бенсульфурон-метил (64), соединение формулы (I) + хлоримурон-этил (135), соединение формулы (I) + хлорансулам-метил (164), соединение формулы (I) + флорасулам (359), соединение формулы (I) + флукарбазон-натрий (364), соединение формулы (I) + имазамокс (451), соединение формулы (I) + имазапир (453), соединение формулы (I) + имазетапир (455), соединение формулы (I) + йодсульфурон-метил-натрий (466), соединение формулы (I) + мезосульфурон-метил (514), соединение формулы (I) + никосульфурон (577), соединение формулы (I) + пеноксулам (622), соединение формулы (I) + пироксулам (трифлосулам) (CAS RN 422556-08-9), соединение формулы (I) + тифенсульфурон-метил (тиаметурон-метил) (795), соединение формулы (I) + триасульфурон (817), соединение формулы (I) + трибенурон-метил (822), соединение формулы (I) + трифлоксисульфурон-натрий (833),соединение формулы (I) + тиенкарбазон (4-[(4,5-дигидро-3-метокси-4-метил-5-оксо-1 Н-1,2,4-триазол-1 ил)карбонилсульфамоил]-5-метилтиофен-3-карбоновая кислота,BAY636 или соединение формулы (I) + тиенкарбазон-метил (метил-4-[(4,5-дигидро-3-метокси-4-метил-5-оксо-1H-1,2,4-триазол-1 ил)карбонилсульфамоил]-5-метилтиофен-3-карбоксилат, CAS RN 317815-83-1, BAY636-метил. Смеси соединения формулы (I) с ингибитором РРО (например, соединение формулы (I) + бутафенацил (101), соединение формулы (I) + карфентразон-этил (121), соединение формулы (I) + цинидон-этил(152), соединение формулы (I) + флумиоксазин (376), соединение формулы (I) + фомезафен (401) или соединение формулы (I) + сложный этиловый эфир [3-[2-хлор-4-фтор-5-(1-метил-6-трифторметил-2,4 диоксо-1,2,3,4-тетрагидропиримидин-3-ил)фенокси]-2-пиридилокси]уксусной кислоты) (CAS RN 353292-31-6). Смеси соединения формулы (I) с ингибитором АССазы (например, соединение формулы (I) + бутроксидим (106), соединение формулы (I) + клетодим (155), соединение формулы (I) + клодинафоппропаргил (156), соединение формулы (I) + циклоксидим (190), соединение формулы (I) + цигалофопбутил (195), соединение формулы (I) + диклофоп-метил (238), соединение формулы (I) + феноксапроп-Рэтил (339), соединение формулы (I) + флуазифоп-бутил (361), соединение формулы (I) + флуазифоп-Рбутил (362), соединение формулы (I) + галоксифоп (427), соединение формулы (I) + галоксифоп-Р (428),соединение формулы (I) + пропаквизафоп (670), соединение формулы (I) + квизалофоп (717), соединение формулы (I) + квизалофоп-Р (718), соединение формулы (I) + сетоксидим (726), соединение формулы (I)+ тепралоксидим (771), соединение формулы (I) + тралкоксидим (811 или соединение формулы (I) + пиноксаден (CAS RN 243973-20-8). Смеси соединения формулы (I) с просульфокарбом (683) или соединения формулы (I) с триаллатом- 23015647 Смеси соединения формулы (I) с бромоксинилом (95), соединения формулы (I) с хлоридазоном(134), соединения формулы (I) с хлоротолуроном (143), соединения формулы (I) с диуроном (281) или соединения формулы (I) с метрибузином (554). Смеси соединения формулы (I) с кломазоном (159), соединения формулы (I) с дифлуфениканом(251), соединения формулы (I) с флуроклоридоном (389) или соединения формулы (I) с флуртамоном(392). Смеси соединения формулы (I) с пендиметалином (621) или соединения формулы (I) с трифлуралином (836). Смеси соединения формулы (I) с дифензокватметилсульфатом (248). Смеси соединения формулы (I) с дикватдибромидом (276). Смеси соединения формулы (I) с паракватдихлоридом (614). Компоненты смеси помимо соединения формулы (I) могут также находиться в форме сложных эфиров или солей, как указано, например, в The Pesticide Manual, 13th Edition (BCPC), 2003. Ссылка на глюфозинатаммоний также относится к глюфозинату, ссылка на хлорансулам-метил также относится к хлорансуламу, ссылка на диметенамид также относится к диметенамиду-Р, ссылка на флампроп-М также относится к флампропу и ссылка на пиритиобак-натрий также относится к пиритиобаку и т.д. Соотношение содержания соединения формулы (I) и другого компонента в смеси предпочтительно представляет собой от 1/100 до 1000/1. Смеси могут быть с успехом использованы в упомянутых выше составах (и в этом случае термин"активный ингредиент" относится к смеси соединения формулы (I) и другого компонента смеси). Кроме того, в сочетании с соединением формулы (I) по настоящему изобретению или в сочетании с описанной выше смесью могут быть использованы один или несколько из следующих гербицидов: ацифлуорфен-натрий (7), аклонифен (8), акролеин (10), алахлор (14), аллоксидим (18), аметрин (20), амикарбазон (21), амидосульфурон (22), амитрол (аминотриазол) (25), сульфамат аммония (26), анилофос(752), серная кислота (755), смоляные масла (758), ТСА-натрий (760), тебутам (CAS RN 35256-85-0), тебутиурон (765), тефурилтрион (CAS RN 473278-76-1), тербацил (772), тербуметон (774), тербутрин (776),тиенилхлор (789), тидиазимин (CAS RN 123249-43-4), тиазафлурон (CAS RN 25366-23-8), тиазопир (793),тиобенкарб (797), тиокарбазил (807), триазифлам (819), триклопир (827), триетазин (831), трифлусульфурон-метил (837), тригидрокситриазин (CAS RN 108-80-5), тринексапак-этил (CAS RN 95266-40-3) и тритосульфурон (843). Компоненты смеси помимо соединения формулы (I) могут также находиться в форме сложных эфиров или солей, как указано, например, в The Pesticide Manual, 13th Edition (BCPC), 2003. Ссылка на ацифлуорфен-натрий также относится к ацифлуорфену, и ссылка на бенсульфурон-метил также относится к бенсульфурону и т.д. Соотношение содержания соединения формулы (I) и другого компонента в смеси предпочтительно представляет собой от 1/100 до 1000/1. Смеси могут быть с успехом использованы в упомянутых выше составах (и в этом случае термин"активный ингредиент" относится к смеси соединения формулы (I) и другого компонента смеси). Соединения формулы (I) по настоящему изобретению могут также использоваться в сочетании с одним или несколькими антидотами. По аналогии, смеси соединения формулы (I) по настоящему изобретению с одним или несколькими дополнительными гербицидами могут также использоваться в сочетании с одним или несколькими антидотами. Антидоты могут представлять собой беноксакор (63), клоквинтоцет-мексил (163), циометринил (CAS RN 78370-21-5), ципросульфамид (CAS RN 221667-31-8), дихлормид (231), дициклонон (CAS RN 79260-71-2), фенхлоразол-этил (331), фенклорим (332), флуразол(386), флуксофеним (399), флурилазол (413) и соответствующий R-изомер, изоксадифен-этил (478), мефенпир-диэтил (506), нафтойный ангидрид (CAS RN 81-84-5) и оксабетринил (598). Особенно предпочтительными являются смеси соединения формулы (I) с беноксакором и соединения формулы (I) с клоквинтоцет-мексилом. Антидоты соединения формулы (I) могут также находиться в форме сложных эфиров или солей, как указано, например, в The Pesticide Manual, 13th Edition (BCPC), 2003. Ссылка на клоквинтоцет-мексил также относится к клоквинтоцету, и ссылка на фенхлоразол-этил также относится к фенхлоразолу и т.д. Предпочтительно соотношение содержания соединения формулы (I) и антидота в смеси составляет от 100/1 до 1/10, в особенности от 20/1 до 1/1. Смеси могут быть с успехом использованы в упомянутых выше составах (и в этом случае термин"активный ингредиент" относится к смеси соединения формулы (I) и антидота). Возможно, что антидот и соединение формулы (I) и один или несколько других гербицидов, если таковые имеются, вносятся одновременно. Например, антидот, соединение формулы (I) и один или несколько других гербицидов, если таковые имеются, могут вноситься в локус до появления всходов или могут вноситься в сельскохозяйственную культуру после появления всходов. Также возможно, что антидот и соединение формулы (I) и один или несколько других гербицидов, если таковые имеются, вносятся последовательно. Например,антидот может вноситься до посева семян путем обработки семян, а соединение формулы (I) и один или несколько других гербицидов, если таковые имеются, могут вноситься в локус до появления всходов или могут вноситься в сельскохозяйственную культуру после появления всходов. Предпочтительные смеси соединения формулы (I) с другими гербицидами и антидотами включают смеси соединения формулы (I) с триазином и антидотом; смеси соединения формулы (I) с глифозатом и антидотом; смеси соединения формулы (I) с глюфозинатом и антидотом; смеси соединения формулы (I) с изоксафлутолом и антидотом; смеси соединения формулы (I) с изоксафлутолом и триазином и антидотом; смеси соединения формулы (I) с изоксафлутолом и глифозатом и антидотом; смеси соединения формулы (I) с изоксафлутолом и глюфозинатом и антидотом; смеси соединения формулы (I) с мезотрионом и антидотом; смеси соединения формулы (I) с мезотрионом и триазином и антидотом; смеси соединения формулы (I) с мезотрионом и глифозатом и антидотом; смеси соединения формулы (I) с мезотрионом и глюфозинатом и антидотом; смеси соединения формулы (I) с сулькотрионом и антидотом; смеси соединения формулы (I) с сулькотрионом и триазином и антидотом; смеси соединения формулы (I) с сулькотрионом и глифозатом и антидотом; смеси соединения формулы (I) с сулькотрионом и глюфозинатом и антидотом.- 25015647 Последующие примеры дополнительно иллюстрируют, но не ограничивают, настоящее изобретение. Примеры получения 1. Реакции, охватываемые схемой 1. Пример 1.1. Получение метилового эфира 3-[2-(2-хлор-3,6-дифторфенил)ацетиламино]пиразин-2 карбоновой кислоты К раствору (2-хлор-3,6-дифторфенил)уксусной кислоты (3,151 г) в дихлорметане (20 мл) по каплям добавляли оксалилхлорид (1,30 мл) и добавляли каплю N,N-диметилформамида для инициации реакции. Реакционную смесь перемешивали при температуре окружающей среды в течение 1 ч. Растворитель выпаривали с получением бесцветного масла, которое растворяли в ацетонитриле (30 мл). Затем этот раствор делили на три порции и добавляли каждую порцию к суспензии метилового эфира 3-аминопиразин 2-карбоновой кислоты (0,76 г) в ацетонитриле (15 мл). Реакционные смеси нагревали в микроволновой печи при 130 С в течение 40 мин с получением темно-красных растворов, которые хранили при температуре окружающей среды в течение 16 ч. Образцы объединяли и концентрировали с получением метилового эфира 3-[2-(2-хлор-3,6-дифторфенил)ацетиламино]пиразин-2-карбоновой кислоты в виде темнооранжевого твердого вещества (4,15 г). 1 Н-ЯМР (400 МГц, CDCl3): 4,02 (с, 3 Н), 4,22 (с, 2 Н), 7,02-7,10 (м, 1 Н), 7,11-7,17 (м, 1 Н), 8,41 (д, 1 Н),8,61 (д, 1 Н), 10,8 (с, 1 Н) м.д. Пример 1.2. Получение 7-(2-хлор-3,6-дифторфенил)-8-гидрокси-5 Н-пиридо[2,3-b]пиразин-6-она(4,15 г) (пример 1.1) нагревали с карбонатом калия (1,67 г) в N,N-диметилформамиде (50 мл) при 110 С в течение 2 ч, а затем хранили при температуре окружающей среды в течение 16 ч. Добавляли воду и реакционную смесь подкисляли добавлением водной соляной кислоты (концентрированной). Формировался осадок, который выделяли путем фильтрации. Остаток последовательно промывали водой и гексаном с получением 7-(2-хлор-3,6-дифторфенил)-8-гидрокси-5 Н-пиридо[2,3-b]пиразин-6-она в виде коричневого твердого вещества (2,88 г). 1 Н-ЯМР (400 МГц, d6-ДМСО): 7,34-7,42 (м, 1 Н), 7,51-7,59 (м, 1 Н), 8,59 (д, 1 Н), 8,72 (д, 1 Н), 12,0 Смесь 7-(2-хлор-3,6-дифторфенил)-8-гидрокси-5 Н-пиридо[2,3-b]пиразин-6-она (0,20 г) (пример 1.2),триметилацетилхлорида (0,08 мл) и пиридина (0,05 мл) в дихлорметане (5 мл) перемешивали при температуре окружающей среды в течение 2 ч. Реакционную смесь разбавляли этилацетатом и водой. Разделяли фазы. Органическую фазу сушили над сульфатом магния и концентрировали с получением желтого полукристаллического масла. Это масло растирали с изогексаном с получением 7-(2-хлор-3,6 дифторфенил)-6-оксо-5,6-дигидропиридо[2,3-b]пиразин-8-илового эфира 2,2-диметилпропионовой кислоты в виде бледно-коричневого порошка (0,113 г). 1(0,053 г) в ацетонитриле (5 мл) добавляли 1-бром-2,2-дифторэтан (0,113 г). Реакционную смесь нагревали в микроволновой печи в течение 25 мин при 120 С. Реакционную смесь концентрировали и очищали остаток методом колоночной хроматографии на силикагеле (элюент:гексан/этилацетат, от 8/2 до 1/1) с получением соединения А 2 из таблицы А в виде желтого твердого вещества (0,083 г). Пример 2.2. Получение 7-(2-хлор-3,6-дифторфенил)-5-(2-фторэтил)-6-оксо-5,6-дигидропиридо[2,3b]пиразин-8-илового эфира 2,2-диметилпропионовой кислоты (соединение С 9 из таблицы С) К смеси 7-(2-хлор-3,6-дифторфенил)-6-оксо-5,6-дигидропиридо[2,3-b]пиразин-8-илового эфира 2,2-диметилпропионовой кислоты (пример 1.3) (0,20 г), карбоната калия (0,207 г) и йодида калия (каталитическое количество) в N,N-диметилформамиде (10 мл) добавляли 2-фторэтилбромид. Реакционную смесь нагревали в микроволновой печи в течение 20 мин при 120 С. Реакционную смесь концентрировали и очищали остаток методом колоночной хроматографии на силикагеле (элюент: этилацетат/гексан 1/1) с получением соединения С 9 из таблицы С в виде желтого твердого вещества (0,103 г). Пример 2.3. Получение 7-(2-хлор-3,6-дифторфенил)-5-(2,2,2-трифторэтил)-6-оксо-5,6 дигидропиридо[2,3-b]пиразин-8-илового эфира 2,2-диметилпропионовой кислоты (соединение С 8 из таблицы С) Смесь 7-(2-хлор-3,6-дифторфенил)-6-оксо-5,6-дигидропиридо[2,3-b]пиразин-8-илового эфира 2,2-диметилпропионовой кислоты (пример 1.3) (0,10 г), карбоната калия (0,053 г) и 2,2,2-трифторэтилтрифлата (0,130 г) нагревали в микроволновой печи при 150 С в течение 30 мин, а затем при 170 С в течение 30 мин. Реакционную смесь оставляли охлаждаться до температуры окружающей среды, а затем распределяли между дихлорметаном и водной соляной кислотой (2 М). Разделяли фазы. Органический слой сушили над сульфатом магния и концентрировали. Остаток растворяли в дихлорметане, обрабатывали триметилацетилхлоридом (0,063 мл) и пиридином (0,061 мл) и перемешивали при температуре окружающей среды. Реакционную смесь концентрировали и очищали остаток методом колоночной хроматографии на силикагеле (элюент: ацетон/изогексан от 0/10 до 1/9) с получением соединения С 8 из таблицы С в виде бежевого твердого вещества (0,049 г).(0,754 г). Реакционную смесь нагревали в микроволновой печи в течение 20 мин при 120 С. Реакционную смесь оставляли охлаждаться до температуры окружающей среды, после чего ее разбавляли водой и этилацетатом. Разделяли фазы. Органическую фазу промывали водой, сушили над сульфатом магния и концентрировали. Остаток растворяли в диэтиловом эфире и промывали раствор водой. Разделяли фазы и концентрировали органическую фазу с получением соединения В 2 из таблицы В в виде вязкого оранжевого масла (0,553 г). Соединения, упомянутые ниже в таблицах A-D, могут быть получены с использованием методов,аналогичных описанным в примерах 2.1-2.4. 3. Реакции, охватываемые схемой 3. Пример 3.1. Получение 3-[2-(2,3,6-трихлорфенил)ацетиламино]пиразин-2-карбоновой кислоты К раствору метилового эфира 3-[2-(2,3,6-трихлорфенил)ацетиламино]пиразин-2-карбоновой кислоты (0,373 г) (полученного, как описано в примере 1.1) в безводном тетрагидрофуране (10 мл) по каплям добавляли гексаметилдисилазид лития (LiHMDS) (1 М в ТГФ) (2 мл). Реакционную смесь перемешивали в течение 30 мин при температуре окружающей среды, а затем нагревали с обратным холодильником в течение 3 ч. Реакционную смесь оставляли охлаждаться до температуры окружающей среды и подкисляли добавлением водной соляной кислоты (1 М). Смесь концентрировали. Остаток растворяли в диэтиловом эфире и промывали водной соляной кислотой (1 М). Кислый раствор экстрагировали этилацетатом. Объединенные органические фракции сушили над сульфатом магния и концентрировали с получением 3-[2-(2,3,6-трихлорфенил)ацетиламино]пиразин-2-карбоновой кислоты (0,225 г), которую использовали на следующей стадии без дополнительной очистки. Пример 3.2. Альтернативный метод получения 5-(2,2-дифторэтил)-8-гидрокси-7-(2,3,6-трихлорфенил)-5 Н-пиридо[2,3-b]пиразин-6-она (соединение В 11 из таблицы В)(0,225 г) в безводном тетрагидрофуране (10 мл) в течение 10 мин по каплям добавляли гексаметилдисилазид натрия (NaHMDS) (1 М в ТГФ) (1,4 мл). Затем по каплям добавляли дифторэтилтрифлат(0,270 г) и оставляли реакционную смесь перемешиваться при температуре окружающей среды в течение 30 мин. Затем реакционную смесь нагревали с обратным холодильником в течение 6 ч. Реакционную смесь оставляли охлаждаться до температуры окружающей среды и подкисляли добавлением водной соляной кислоты (1 М). Смесь концентрировали. Остаток растворяли в диэтиловом эфире и промывали водной соляной кислотой (1 М). Кислый раствор экстрагировали этилацетатом. Объединенные органические фракции сушили над сульфатом магния и концентрировали. Остаток очищали по методу ВЭЖХ с обращенной фазой с получением соединения В 11 из таблицы В (0,034 г).(каталитическое количество) в тетрахлориде углерода (40 мл) нагревали с обратным холодильником. Для инициации реакции использовали ртутно-галогеновую лампу мощностью 500 Вт. Реакционную смесь нагревали с обратным холодильником и облучали в течение 30 мин. Реакционную смесь оставляли охлаждаться до температуры окружающей среды, а затем фильтровали. Фильтрат концентрировали с получением бесцветного масла, которое при отстаивании отверждалось с получением 1-бром-3-бромметил-2 хлор-4-фторбензола в виде не совсем белого твердого вещества (10,7 г). 1 К раствору цианида калия (2,38 г) в воде (2 мл) при нагревании в течение 30 мин по каплям добавляли раствор 1-бром-3-бромметил-2-хлор-4-фторбензола (9,945 г) (пример 4.2) в абсолютном этаноле(40 мл). Реакционную смесь нагревали с обратным холодильником в течение 7 ч. Реакционную смесь оставляли охлаждаться до температуры окружающей среды, а затем хранили при температуре окружающей среды в течение 16 ч. Смесь фильтровали и концентрировали фильтрат. Остаток растворяли в этилацетате, сушили над сульфатом магния и концентрировали с получением (3-бром-2-хлор-6 фторфенил)ацетонитрила в виде бледно-желтого масла (8,19 г). 1 Н-ЯМР (400 МГц, CDCl3): 3,89 (д, 2 Н), 7,00 (т, 1 Н), 7,64 (дд, 1 Н) м.д. Пример 4.3. Получение (3-бром-2-хлор-6-фторфенил)уксусной кислоты(3-Бром-2-хлор-6-фторфенил)ацетонитрил (8,15 г) (пример 4.3) растворяли в концентрированной серной кислоте (50 мас.% в воде) (90 мл). Реакционная смесь становилась очень горячей, а затем ее нагревали с обратным холодильником в течение 3 ч. Реакционную смесь оставляли охлаждаться до температуры окружающей среды и хранили при температуре окружающей среды в течение 16 ч. Смесь дважды экстрагировали дихлорметаном. Объединенные органические фазы сушили над сульфатом магния и концентрировали с получением (3-бром-2-хлор-6-фторфенил)уксусной кислоты в виде не совсем белого твердого вещества (8,3 г). 1H-ЯМР (400 МГц, CDCl3): 3,94 (д, 2 Н), 6,94 (т, 1 Н), 7,56 (дд, 1 Н) м.д. 5. Реакции, охватываемые схемой 12. Пример 5.1. Получение метилового эфира 3-амино-6-метилпиразин-2-карбоновой кислоты Метиловый эфир 3-амино-6-бромпиразин-2-карбоновой кислоты (1,0 г) (полученный в соответствии с J. Org. Chem. (1988), 59(9), 2052-5), ацетат палладия (II) (0,101 г) и 2'-дициклогексилфосфино-2,6 диметокси-1,1'-бифенил (S-Phos) помещали в колбу с толуолом (15 мл) и водой (3 капли). Добавляли метилбороновую кислоту (0,394 г) и фосфат калия (1,71 г) и нагревали реакционную смесь с обратным холодильником в течение 24 ч. После охлаждения реакционной смеси до температуры окружающей среды ее разбавляли водной соляной кислотой ( 1 М) и экстрагировали этилацетатом. Объединенные органические экстракты концентрировали и очищали остаток методом колоночной хроматографии на силикагеле(элюент: диэтиловый эфир) с получением метилового эфира 3-амино-6-метилпиразин-2-карбоновой кислоты в виде желтого твердого вещества (0,114 г). 1
МПК / Метки
МПК: A01P 13/00, C07D 471/04, A01N 43/90
Метки: производные, применимые, соединений, качестве, пиридопиразиновые, гербицидных
Код ссылки
<a href="https://eas.patents.su/30-15647-primenimye-v-kachestve-gerbicidnyh-soedinenijj-piridopirazinovye-proizvodnye.html" rel="bookmark" title="База патентов Евразийского Союза">Применимые в качестве гербицидных соединений пиридопиразиновые производные</a>
Предыдущий патент: Пневматическая шина для колеса тяжелого транспортного средства
Следующий патент: Сборки флаконов с множественными дозами и адаптеры для них
Случайный патент: Детектирование кавитации












