Производные феноксиуксусных кислот, применимые в качестве двойных агонистов активируемого пероксисомным пролифератором рецептора ( ppar )
Формула / Реферат
1. Соединение формулы (I)
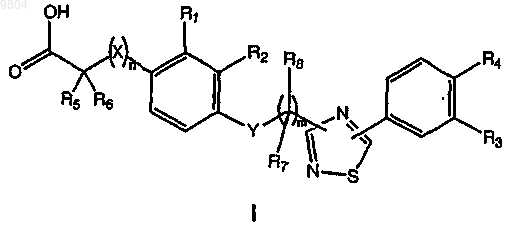
где m равно 1, 2 или 3;
n равно 0 или 1;
X означает S или О;
Y означает S, СН2 или О;
R1 и R2 независимо выбраны из Н, C1-4алкила, C1-3алкокси, галогена и -NRaRb, где каждый из Ra и Rb независимо выбран из Н и C1-4 алкила;
каждый из R3 и R4 независимо выбран из Н, галогена, циано, C1-4алкила, C1-3алкокси и NRcRd, где каждый из Rc и Rd независимо выбран из Н и C1-4алкила и где по меньшей мере один из R3 и R4 не Н; и
каждый из R5 и R6 независимо выбран из Н, C1-5алкила, C1-5алкокси, C3-5циклоалкила, (С3-5циклоалкил)C1-3алкила и NReRf, где каждый из Re и Rf независимо выбран из Н и C1-4алкила или R5 и R6 вместе образуют спиро C3-6циклоалкил или спиро 5- или 6-членный гетероциклил, имеющий 1-3 гетероатома, выбранных из О, S и N; и
каждый из R7 и R8 независимо выбран из Н, C1-5алкила и С3-5циклоалкила;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где m равно 1 или 2.
3. Соединение по п.1, где m равно 1.
4. Соединение по п.1, где n равно 1.
5. Соединение по п.1, где X означает О.
6. Соединение по п.1, где Y означает S или О.
7. Соединение по п.1, где Y означает S.
8. Соединение по п.1, где Y означает О.
9. Соединение по п.1, где R1 выбран из Н, C1-2алкила, C1-2алкокси и галогена.
10. Соединение по п.1, где R1 выбран из галогена, метила и метокси, и, в случае метила или метокси, R1 может быть замещенным или незамещенным.
11. Соединение по п.1, где R2 означает Н, галоген, метокси или метил.
12. Соединение по п.1, где R2 означает Н, фтор или хлор.
13. Соединение по п.1, где каждый из R3 и R4 независимо выбран из Н, галогена, C1-4алкила, C1-3алкокси и NRcRd.
14. Соединение по п.1, где каждый из R3 и R4 независимо выбран из Н, фтора, хлора, C1-2алкила и C1-2алкокси.
15. Соединение по п.1, где каждый из R3 и R4 независимо выбран из Н, фтора, хлора, метила, метокси, трифторметила, трифторметокси, дифторметила, дифторметокси, фторметила, фторметокси, трифторэтила и трифторэтокси.
16. Соединение по п.1, где каждый из R5 и R6 независимо выбран из Н, C1-3алкила и С1-3алкокси.
17. Соединение по п.1, где по меньшей мере один из R5 и R6 означает метил, метокси, этил и этокси и другой выбран из Н, метокси, метила, этила и этокси.
18. Соединение по п.1, где каждый из R7 и R8 независимо выбран из Н и C1-3алкила.
19. Соединение по п.1, где один из R7 и R8 означает Н и другой означает Н, метил или этил.
20. Соединение по п.1, где каждый из R7 и R8 означает Н.
21. Соединение по п.1, где X означает О; Y означает S или О; R1 выбран из Н, C1-2алкила, C1-2алкокси и галогена; каждый из R5 и R6 независимо выбран из Н, C1-3алкила и С1-3алкокси и каждый из R7 и R8 независимо выбран из Н и C1-3алкила.
22. Соединение по п.1, где m равно 1 или 2 и n равно 1.
23. Соединение по п.1, где каждый из R3 и R4 независимо выбран из Н, фтора, хлора, C1-2алкила и C1-2алкокси и R1 выбран из Н, C1-2алкила, C1-2алкокси и галогена.
24. Соединение по п.1, где каждый из R3 и R4 независимо выбран из Н, фтора, хлора, метила, метокси, трифторметила, трифторметокси, трифторэтила и трифторэтокси.
25. Соединение по п.1, где
m равно 1 или 2;
n равно 0 или 1;
X означает S или О;
Y означает S, СН2 или О;
R1 и R2 независимо выбраны из Н, C1-4алкила, C1-3алкокси, галогена и -NRaRb, где каждый из Ra и Rb независимо выбран из Н и C1-4алкила;
каждый из R3 и R4 независимо выбран из Н, галогена, циано, C1-4алкила, C1-3алкокси и NRcRd, где каждый из Rc и Rd независимо выбран из Н и C1-4алкила и где по меньшей мере один из R3 и R4 не является Н; и
каждый из R5 и R6 независимо выбран из Н, C1-5алкила, C1-5алкокси, C3-5циклоалкила, (С3-5циклоалкил)C1-3алкила и NReRf, где каждый из Re и Rf независимо выбран из Н и C1-4алкила, или R5 и R6 вместе образуют спиро C3-6циклоалкил; и
каждый из R7 и R8 независимо выбран из Н и C1-2алкила.
26. Соединение по п.1, где
m равно 1 или 2;
n равно 0 или 1;
X означает S или О;
Y означает S или О;
R1 и R2 независимо выбраны из Н, C1-2алкила, C1-2алкокси, галогена и -NRaRb, где каждый из Ra и Rb независимо выбран из Н и C1-4алкила;
каждый из R3 и R4 независимо выбран из Н, галогена, циано, C1-4алкила, C1-3алкокси и NRcRd, где каждый из Rc и Rd независимо выбран из Н и C1-4алкила и где по меньшей мере один из R3 и R4 не является Н;
каждый из R5 и R6 независимо выбран из Н, C1-3алкила, C1-2алкокси и
каждый из R7 и R8 означает Н.
27. Соединение по п.1, выбранное из таких, как
2-метил-2-{2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметокси]фенокси}пропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметокси]фенокси}пропионовая кислота,
2-метил-2-[2-метил-4-(3-п-толил-[1,2,4]тиадиазол-5-илметилсульфанил)фенокси]пропионовая кислота,
2-{4-[3-(4-трет-бутилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-{4-[3-(4-хлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-{4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-{4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-{4-[3-(2,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-{4-[3-(3,4-диметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-{4-[3-(3-хлор-4-метилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-{4-[3-(3-фтор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
1-{2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси}циклопентанкарбоновая кислота,
1-{4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}циклопентанкарбоновая кислота,
2-метил-2-{2-метил-4-[5-(4-трифторметилфенил)-[1,2,4]тиадиазол-3-илметилсульфанил]фенокси}
пропионовая кислота,
2-{4-[5-(4-хлорфенил)-[1,2,4]тиадиазол-3-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-{4-[5-(4-изопропилфенил)-[1,2,4]тиадиазол-3-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-метил-2-{2-метил-4-[5-(4-трифторметоксифенил)-[1,2,4]тиадиазол-3-илметилсульфанил]фенокси}
пропионовая кислота,
2-{4-[5-(4-трет-бутилфенил)-[1,2,4]тиадиазол-3-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси}
пропионовая кислота,
{2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси}уксусная кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси}
пропионовая кислота и
2-метил-2-{4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси}пропионовая кислота.
28. Соединение по п.1, выбранное из таких, как
2-метил-2-{2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси}
пропионовая кислота,
2-{4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметокси]фенокси}пропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметокси]фенокси}пропионовая кислота,
2-{4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенилсульфанил}пропионовая кислота,
2-{4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил}-2-метилпропионовая кислота,
2-{4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил}-2-метилпропионовая кислота,
2-{4-[3-(4-трет-бутилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил}-2-метилпропионовая кислота и
2-метил-2-(2-метил-4-{3-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]пропил}фенокси)пропионовая кислота.
29. Соединение по п.1, выбранное из таких, как
2-метил-2-{2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси}
пропионовая кислота,
2-метил-2-(2-метил-4-{2-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил]этил}фенокси)пропионовая кислота,
2-(4-{2-[3-(3-хлор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил]этил}-2-метилфенокси)-2-метилпропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметокси]фенокси}пропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметокси]фенокси}пропионовая кислота,
2-(4-{2-[3-(3-фтор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил]этил}-2-метилфенокси)-2-метилпропионовая кислота,
2-(4-{2-[3-(3-фтор-4-метилфенил)-[1,2,4]тиадиазол-5-ил]этил}-2-метилфенокси)-2-метилпропионовая кислота,
2-метил-2-(2-метил-4-{2-[3-(4-трифторметилфенил)-[1,2,4]-тиадиазол-5-ил]этилсульфанил}фенокси)пропионовая кислота,
2-(4-{2-[3-(3-хлор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил]этилсульфанил}-2-метилфенокси)-2-метилпропионовая кислота,
2-(4-{2-[3-(3-хлор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил]этилсульфанил}-2-метилфенокси)-2-метилпропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенилсульфанил}пропионовая кислота,
2-{4-[3-(3-хлор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил-метилсульфанил]-2-метилфенилсульфанил}-2-метилпропионовая кислота,
2-{4-[3-(3-фтор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил}-2-метилпропионовая кислота и
2-{4-[3-(3-фтор-4-метилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил}-2-метилпропионовая кислота.
30. Соединение по п.1, выбранное из таких, как
2-метил-2-{2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси)
пропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметокси]фенокси}пропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметокси]фенокси}пропионовая кислота,
2-{4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота и
2-{4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси}-2-метилпропионовая кислота.
31. Соединение по п.1, выбранное из таких, как
2-метил-2-{2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметокси]фенокси}пропионовая кислота,
2-метил-2-{2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметокси]фенокси}пропионовая кислота,
2-{4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметокси]-2-метилфенокси}-2-метилпропионовая кислота,
2-{4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметокси]-2-метилфенокси}-2-метилпропионовая кислота,
2-метил-2-(2-метил-4-{2-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этокси}фенокси)пропионовая кислота,
2-(4-{2-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-ил]этил}-2-метилфенокси)-2-метилпропионовая кислота,
2-метил-2-(2-метил-4-{2-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этил}фенокси)пропионовая кислота,
2-(4-{2-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этил}-2-метилфенокси)-2-метилпропионовая кислота,
2-(4-{2-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этокси}-2-метилфенокси)-2-метилпропионовая кислота,
2-(4-{2-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-ил]этокси}-2-метилфенокси)-2-метилпропионовая кислота,
2-метил-2-(2-метил-4-{2-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этокси}фенилсульфанил)пропионовая кислота,
2-(4-{2-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этокси}-2-метилфенилсульфанил)-2-метилпропионовая кислота,
2-(4-{2-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-ил]этокси}-2-метилфенилсульфанил)-2-метилпропионовая кислота,
2-метил-2-(2-метил-4-{2-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этилсульфанил}фенилсульфанил)пропионовая кислота,
2-(4-{2-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этилсульфанил}-2-метилфенилсульфанил)-2-метилпропионовая кислота и
2-(4-{2-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-ил]-этилсульфанил}-2-метилфенилсульфанил)-2-метилпропионовая кислота.
32. Фармацевтический состав, содержащий фармацевтически приемлемый носитель и соединение по п.1.
33. Фармацевтический состав, содержащий фармацевтически приемлемый носитель и соединение по п.21.
34. Фармацевтический состав, содержащий фармацевтически приемлемый носитель и соединение по п.23.
35. Фармацевтический состав, содержащий фармацевтически приемлемый носитель и соединение по п.25.
36. Фармацевтический состав, содержащий фармацевтически приемлемый носитель и соединение по п.26.
37. Фармацевтический состав, содержащий фармацевтически приемлемый носитель и соединение по п.27.
38. Фармацевтический состав, содержащий фармацевтически приемлемый носитель и соединение по п.28.
39. Фармацевтический состав, содержащий фармацевтически приемлемый носитель и соединение по п.29.
40. Фармацевтический состав, содержащий фармацевтически приемлемый носитель и соединение по п.30.
41. Способ лечения или подавления развития опосредуемого PPAR-дельта состояния или опосредуемого PPAR-альфа состояния или обоих, включающий введение пациенту при необходимости лечения фармацевтически эффективного количества состава по п.31.
42. Способ по п.41, где опосредуемое PPAR-дельта состояние выбрано из гиперлипидемии, атеросклероза, сердечно-сосудистой болезни, гиперхолестеринемии, диабета типа II, резистентности к инсулину, ухудшенной толерантности к глюкозе, дислипидемии, низкого-HDL-C, гипертриглицеридемии, и опосредуемое PPAR-альфа состояние выбрано из синдрома X (или метаболического синдрома), дислипидемии, высокого кровяного давления, ожирения и пониженного содержания глюкозы натощръ, резистентности к инсулину, диабета типа II, атеросклероза, гиперхолестеринемии, гипертриглицеридемии и низкого-HDL-C.
43. Способ лечения по меньшей мере одного опосредуемого PPAR-дельта состояния, включающий введение пациенту при необходимости лечения фармацевтически эффективного количества состава по п.32.
44. Способ по п.41, который дополнительно включает лечение по меньшей мере одного опосредуемого PPAR-гамма состояния.
45. Способ по п.43, который дополнительно включает лечение по меньшей мере одного опосредуемого PPAR-гамма состояния.
Текст
009804 Данная заявка претендует на приоритет по предварительной заявке Соединенных Штатов 60/516561,поданной 31 октября 2003 года. Исследование и разработка изобретения, описанного ниже, федерально не спонсированы. Изобретение относится к 4-феноксиалкил)тио)феноксиуксусным кислотам и аналогам, к содержащим их составам и способам их применения. Член семейства ядерных рецепторов, группы активируемых лигандом факторов транскрипции, активируемый пероксисомным пролифератором рецептор альфа (PPAR альфа или PPAR) является необходимым фактором транскрипции, регулирующим гены, относящиеся к метаболизму жирных кислот и инсулиновому действию. Рецепторы PPAR альфа находятся преимущественно в печени. Гены, регулируемые PPAR альфа,включают ферменты, вовлекаемые в бета-окисление жирных кислот, белка транспорта жирных кислот печени, и аро А 1, важного компонента липопротеинов высокой плотности (HDL). Селективные, обладающие высоким сродством агонисты PPAR альфа усиливают окисление жирных кислот печени, что, в свою очередь, снижает циркуляцию триглицеридов и свободных жирных кислот. Известные как средства для лечения гиперлипидемии, фибраты являются слабыми агонистами PPAR альфа. Примеры известных агонистов PPAR альфа, по-разному применимые при гиперлипидемии, диабете или атеросклерозе, включают фибраты, такие как фенофибрат (Fournier), гемифиброзил (ParkeDavis/Pfizer, Mylan, Watson), клофибрат (Wyeth-Ayerst, Novopharm), безафибрат и ципрофибрат, и уреидофибраты, такие как GW 7647, GW 9578 и GW 9820 (GlaxoSmithKline). Диабет является болезнью, которую вызывают или которой способствуют многие факторы и которая характеризуется гипергликемией, которая может быть связана с повышенной и преждевременной смертностью из-за повышенного риска микрососудистых и макрососудистых болезней, таких как нефропатия, нейропатия, ретинопатия, атеросклероз, синдром поликистоза яичников (PCOS), гипертензия,ишемия, удар и болезнь сердца. Диабет типа I (IDDM) является результатом генетической недостаточности инсулина, гормона, регулирующего метаболизм глюкозы. Диабет типа II известен как инсулиннезависимый сахарный диабет (NIDDM) и является следствием абсолютной резистентности к регулирующему воздействию инсулина на глюкозный и липидный метаболизм в основных чувствительных к инсулину тканях, например в мышцах, печени и жировой ткани. Эта резистентность к инсулину или пониженная чувствительность к инсулину имеет результатом недостаточную активацию инсулином усвоения, окисления и накопления глюкозы в мышцах и неадекватное подавление инсулином липолиза в жировой ткани, а также продуцирования и секреции глюкозы в печени. Многие, страдающие диабетом типа II, являются также тучными, и ожирение, по всей вероятности, вызывает и/или обостряет проблемы со здоровьем и социальные проблемы, такие как коронарная болезнь сердца, удар, обструктивное апноэ во сне, подагра, гиперлипидемия, остеоартрит, пониженная рождаемость и ослабленная физиологическая функция. Класс соединений, а именно тиазолидиндионы (глитазоны), как было подтверждено, способны облегчать многие симптомы NIDDM путем связывания с рецепторами семейства активируемого пероксисомным пролифератором рецептора (PPAR). Они усиливают чувствительность к инсулину в мышечной,печеночной и жировой тканях в различных животных моделях NIDDM, в результате корректируя повышенные уровни содержания в плазме глюкозы, триглицеридов и неэтерифицированных жирных кислот без какого-либо проявления гипогликемии. Однако нежелательные эффекты наблюдались при исследованиях на животных и/или людях, включая сердечную гипертрофию, разжижение крови и печеночную токсичность. Многие агонисты PPAR, находящиеся в настоящее время в стадии разработки, имеют кольцо тиазолидиндиона в качестве общего структурного элемента. Агонисты PPAR, как было продемонстрировано, чрезвычайно полезны для лечения NIDDM и других расстройств с участием резистентности к инсулину. Троглитазон, росиглитазон и пиоглитазон одобрены для лечения диабета типа II в Соединенных Штатах. Есть также некоторые показания, что бензимидазол содержащий производные тиазолидиндиона могут быть пригодны для лечения расстройства раздраженной толстой кишки (IBD), воспаления и катаракт (JP 10195057). Сердечно-сосудистая болезнь (CVD) является распространенной в мире и часто связана с другими болезненными состояниями, такими как диабет и ожирение. Многочисленные обследования населения делали попытки установить факторы риска для CVD, из них наиболее важными считаются высокие уровни содержания в плазме холестерина липопротеина низкой плотности (LDL-C), высокие уровни содержания в плазме триглицеридов (200 мг/дл) и низкие уровни содержания холестерина липопротеина высокой плотности (HDL-C). В настоящее время немногие методы лечения нацелены на низкие уровниHDL-C и триглицеридов. Активируемые пероксисомным пролифератором рецепторы (PPAR) являются метаболическими воспринимающими элементами, регулирующими экспрессию генов, вовлекаемых в глюкозный и липидный гомеостаз. Агонисты подтипа PPAR, такие как LOPID (гемфиброзил) и TRICOR (фенофибрат), и агонисты подтипа PPAR, такие как AVANDIA (малеат розиглитазона), применимы для лечения дислипидемии и диабета, соответственно. Другой член этого семейства ядерных рецепторов, активируемый-1 009804 пероксисомным пролифератором рецептор дельта (PPAR дельта или PPAR), является также необходимым фактором транскрипции, о котором есть сведения как о вовлекаемом в регулирующие гены, участвующие в липидном метаболизме и расходовании энергии. PPAR дельта, как было показано, действует как "шлюзовой" рецептор, модулирующий экспрессию других PPAR (Shi et al. , 2002, Proc. Natl. Acad.Sci. USA, 99 (5): 2613-2618). Каждый подтип рецепторов имеет отличающееся распределение в тканях: 1) PPAR показывает наивысшую экспрессию в печени, 2) PPAR появляется, главным образом, в жировой ткани, и 3) PPAR имеет самое широкое распространение - повсеместно у взрослой крысы (Braissantet al., 1996, Endocrinology 137 (1): 354-366) и во всех тканях человека, исследованных на данный момент,включая печень, почки, брюшную жировую ткань и скелетные мышцы (Auboeuf et al., 1997, Diabetes 46(8): 1319-1327). В последнее время опубликованы сообщения о сильных лигандах для PPAR, которые дают лучшее понимание их функции в липидном метаболизме. Основным действием, оказываемым указанными соединениями, у мышей db/db (Leibowitz et al., 2000, FEBS Lett. 473 (3): 333-336) и тучных обезьян резус(Oliver et al., 2001, Proc. Natl. Acad. Sci. USA 98 (9): 5306-5311) было увеличение содержания холестерина липопротеина высокой плотности (HDL-C) и снижение содержания триглицеридов с небольшим воздействием на глюкозу (хотя уровни содержания инсулина были пониженными у обезьян). HDL-C удаляет холестерин из периферических клеток через процесс, называемый обратным переносом холестерина. Первая и определяющая скорость стадия, перенос клеточного холестерина и фосфолипидов к компоненту аполипопротеина А-1 HDL, опосредуется связывающим АТР кассетным транспортером A1 (ABCA1)(Lawn et al., 1999, J. Clin. Investigation 104 (8): R25-R31). Было показано, что активация PPAR увеличивает уровень содержания HDL-C посредством транскрипционного регулирования АВСА 1 (Oliver et al.,2001, Proc. Natl. Acad. Sci. USA 98 (9): 5306-5311). Через индукцию экспрессии АВСА 1 mRNA в макрофагах агонисты PPAR могут повышать уровни содержания HDL-C у пациентов и удалять избыточный холестерин из нагруженных липидом макрофагов, ингибируя тем самым развитие атеросклеротических поражений. Существующая терапия гиперхолестеринемии включает лекарственные средства из группы статинов, которые снижают LDL-C, но оказывают небольшое воздействие на HDL-C, и фибраты, агонисты PPAR, которые имеют слабую активность и вызывают только умеренное повышение HDL-C. В дополнение, подобно фибратам, агонисты PPAR могут также снижать содержание триглицеридов, дополнительный фактор риска сердечно-сосудистой болезни и диабета. Повышенное содержание свободных жирных кислот, как было показано, вносит свой вклад в резистентность к инсулину и развитие диабета(3), 241-8). Примеры известных агонистов PPAR дельта, разнообразно применимых при гиперлипидемии, диабете или атеросклерозе, включают L-165041 (Leibowitz et al., 2000) и GW501516 (Oliver et al., Proceedingsof the National Academy of Sciences of the United States of America (2001), 98 (9), 5306-5311). Обработка дифференцированных моноцитов ТНР-1 веществом GW501516 вызывает экспрессию ABCA1 mRNA и улучшает отток холестерина из указанных клеток. Изобретение относится к соединениям формулы (I) нижеR1 и R2 независимо выбраны из Н, C1-4 алкила, C1-3 алкокси, галогена и -NRaRb, где каждый из Ra и Rb независимо выбран из Н и C1-4 алкила; каждый из R3 и R4 независимо выбран из Н, галогена, циано, C1-4 алкила, C1-3 алкокси и NRcRd, где каждый из Rc и Rd независимо выбран из Н и C1-4 алкила; и где по меньшей мере один из R3 и R4 не Н; и каждый из R5 и R6 независимо выбран из Н, C1-5 алкила, C1-5 алкокси, C3-5 циклоалкила, (С 3-5 циклоалкил)C1-3 алкила и NReRf, где каждый из Re и Rf независимо выбран из Н и C1-4 алкила, или R5 и R6 вместе образуют спиро C3-6 циклоалкил или спиро 5- или 6-членный гетероциклил, имеющий 1-3 гетероатома,выбранных из О, S и N; и каждый из R7 и R8 независимо выбран из Н, C1-5 алкила и С 3-5 циклоалкила; или их фармацевтически приемлемым солям. Изобретение также относится к составам, которые содержат одно или несколько соединений фор-2 009804 мулы (I) и фармацевтически приемлемый носитель или разбавитель. Эти составы и способы ниже могут еще содержать дополнительные фармацевтически активные агенты, такие как агенты, снижающие содержание липидов, или агенты, снижающие кровяное давление,или и те, и другие. В другом аспекте изобретение относится к способам применения указанных соединений или составов в различных способах лечения, предотвращения или подавления развития состояния, прямо или косвенно опосредуемого PPAR дельта. Указанное состояние включает, не ограничиваясь перечисленным,диабет, нефропатию, нейропатию, ретинопатию, синдром поликистоза яичников, гипертензию, ишемию,удар, расстройство раздраженной толстой кишки, воспаление, катаракту, сердечно-сосудистые болезни,метаболический синдром X, гипер-LDL-холестеринемию, дислипидемию (включая гипертриглицеридемию, гиперхолестеринемию, смешанную гиперлипидемию и гипо-HDL-холестеринемию), атеросклероз,ожирение и другие расстройства, относящиеся к липидному метаболизму и их осложнениям энергетического гомеостаза. Одним воплощением данного изобретения является способ лечения опосредуемого PPAR состояния, такого как опосредуемое PPAR дельта состояние и, необязательно, одно или несколько опосредуемых PPAR альфа или PPAR гамма состояний, причем опосредуемое PPAR альфа или PPAR гамма состояние (состояния) могут быть такими же, как указанное опосредуемое PPAR дельта состояние, или отличающимся от него, указанный способ содержит введение пациенту при необходимости лечения фармацевтически эффективного количества соединения или состава, описанного в данном описании. Другим воплощением данного изобретения является способ подавления начала и/или подавления развития опосредуемого PPAR дельта состояния, причем указанный способ включает введение пациенту при необходимости лечения фармацевтически эффективного количества соединения или состава, описанного в данном описании. Примеры состояний, которые можно лечить агонистом PPAR дельта, включают, не ограничиваясь перечисленным, диабет, сердечно-сосудистые болезни, метаболический синдром X, гипо-HDL-холестеринемию, гипер-LDL-холестеринемию, дислипидемию, атеросклероз и ожирение. Дислипидемия включает гипертриглицеридемию и смешанную гиперлипидемию. Например, дислипидемия (включая гиперлипидемию) может быть одним из следующих состояний: низкий HDL (35 или 40 мг/дл), высокий уровень триглицеридов (200 мг/дл) и высокий LDL (150 мг/дл). Примеры состояний, которые можно лечить агонистом PPAR альфа, включают синдром X (или метаболический синдром), дислипидемию, высокое кровяное давление, ожирение, пониженный уровень глюкозы натощак, резистентность к инсулину, диабет типа II, атеросклероз, гиперхолестеринемию, гипертриглицеридемию и неалкогольный стеатогепатит. Дополнительные характерные особенности и преимущества изобретения станут очевидными из подробного описания, примеров и формулы изобретения ниже. Подробное описание Изобретение относится к составам, содержащим соединения формулы (I), в кратком изложении выше и способы их применения. Предпочтительные соединения по изобретению являются агонистами PPAR дельта, которые имеют по меньшей мере одну и предпочтительно две или три из следующих характеристик, когда их вводят пациентам с гиперхолестеринемией, гипертриглицеридемией, низким HDL-C, ожирением, диабетом и/или метаболическим синдромом X: 1) повышение уровня содержания HDL-С, 2) снижение содержания триглицеридов, 3) снижение содержания свободных жирных кислот и 4) снижение уровней содержания инсулина. Улучшения в уровнях содержания HDL-C и триглицеридов полезно для сердечно-сосудистой системы. В дополнение, пониженный уровень содержания триглицеридов и свободных жирных кислот способствует уменьшению ожирения и облегчению или предотвращению диабета. Согласно одному аспекту изобретения соединения по изобретению являются соединениями двойных PPAR, иными словами, они являются и агонистами PPAR дельта и агонистами PPAR альфа, предпочтительно, когда активность ЕС 50 соединения, относящаяся к PPAR дельта, менее чем 0,2 мкМ и активность, относящаяся к PPAR альфа, менее чем 3 мкМ. Например, более предпочтительными двойными агонистами PPAR альфа-дельта являются такие соединения, имеющие активность ЕС 50, относящуюся кPPAR дельта, менее чем 0,03 мкМ и активность, относящуюся к PPAR альфа, менее чем 1 мкМ. Согласно другому аспекту изобретения соединения по изобретению являются агонистами panPPAR, а именно соединениями, имеющими активность агонистов PPAR альфа, PPAR дельта и PPAR гамма, предпочтительно, когда активность ЕС 50 Для PPAR дельта менее чем 0,2 мкМ, и активность дляPPAR альфа менее чем 3 мкМ, и активность для PPAR гамма менее чем 1 мкМ. Более предпочтительные агонисты pan-PPAR имеют активность EC50 для PPAR дельта, которая менее чем 0,03 мкМ, активность для PPAR альфа, которая менее чем 1 мкМ, и активность для PPAR гамма, которая менее чем 0,7 мкМ.PPAR дельта, будучи повсеместно экспрессированным, может действовать как шлюзовой (узловой) рецептор, который регулирует экспрессию/активность других ядерных рецепторов, таких как другиеPPAR. Например, PPAR дельта, как было показано, блокирует опосредуемый PPAR адипогенез и экспрессию ацил-СоА оксидазы, было также показано, что он объединяется с сорецепторами ядерного ре-3 009804 цептора SMRT (молчащий медиатор для ретиноидных и тироидных гормональных рецепторов), SHARP(SMART и связанный с гистондиацетилазой репрессорный белок) и HDAC (гистон диацетилаза). Таким образом, состояния, прямо опосредуемые указанными ядерными рецепторами, такие как ожирение и диабет типа II, могут быть косвенно опосредуемыми PPAR дельта (см., например, Shi et al., 2002, Proc.Natl. Acad. Sci. USA, 99 (5): 2613-2618). Некоторые аспекты изобретения относятся к лечению гипертриглицеридемии, повышению уровнейHDL, снижению уровней LDL и/или общему снижению холестерина. Предпочтительно способы лечения объединены с усовершенствованиями в отношении обширности, продолжительности или степени побочных эффектов, таких как отек, которые обычно связаны с другими существующими способами лечения. Изобретение дополнительно описано ниже. Подробное описание систематизировано следующим образом: А) термины, В) соединения, С) синтез, D) состав и введение, Е) применение, F) биологические примеры, G) другие воплощения и формула изобретения. А. Термины. Используемый в описании термин "субъект" относится к животному, предпочтительно млекопитающему, наиболее предпочтительно к человеку, являющемуся объектом лечения, наблюдения или эксперимента. Используемый в описании термин "терапевтически эффективное количество" означает такое количество активного соединения или фармацевтического агента, которое вызывает биологический или медицинский ответ в тканевой системе, в организме животного или человека, ожидаемый исследователем,ветеринаром, врачом или другим клиницистом, проявляющийся в облегчении, предотвращении, излечении или задержке начала или развития симтомов болезни или расстройства, подвергаемого лечению. Состояния, прямо и косвенно опосредуемые PPAR, включают, не ограничиваясь перечисленным,диабет, нефропатию, нейропатию, ретинопатию, синдром поликистоза яичников, гипертензию, ишемию,удар, расстройство раздраженной толстой кишки, воспаление, катаракту, сердечно-сосудистые болезни,метаболический синдром X, гипер-LDL-холестеринемию, дислипидемию (включая гипертриглицеридемию, гиперхолестеринемию, смешанную гиперлипидемию и гипо-HDL-холестеринемию), атеросклероз,ожирение и другие расстройства, относящиеся к липидному метаболизму и их осложнениям энергетического гомеостаза. Для терапевтических целей используемый в описании термин "совместно эффективное количество" означает такое количество каждого активного соединения или фармацевтического агента, одного или в сочетании, которое вызывает биологический или медицинский ответ в тканевой системе, в организме животного или человека, ожидаемый исследователем, ветеринаром, врачом или другим клиницистом,проявляющийся в облегчении симптомов болезни или расстройства, подвергаемого лечению. Для профилактических целей (т.е. ингибирования начала или развития расстройства) используемый в описании термин "совместно эффективное количество" относится к такому количеству каждого активного соединения или фармацевтического агента, одного или в сочетании, которое лечит или подавляет у субъекта начало или развитие расстройства, как ожидается исследователем, ветеринаром, врачом или другим клиницистом. Так, данное изобретение обеспечивает сочетания двух или более лекарственных средств, когда, например, (а) каждое лекарственное средство вводят в независимо терапевтически или профилактически эффективном количестве, (b) по меньшей мере одно лекарственное средство в сочетании вводят в количестве, которое ниже терапевтического или ниже профилактического, если его вводить одно, но является терапевтическим или профилактическим, когда его вводят в сочетании со вторым или дополнительными лекарственными средствами по изобретению, или (с) два (или более) лекарственных средств вводят в количестве, которое ниже терапевтического или ниже профилактического, если его вводить одно, но является терапевтическим или профилактическим, когда вводят вместе. Если не указано иначе, используемые в описании или отдельно, или как часть группы заместителя"алкил" и "алкокси" включают прямые или разветвленные цепи, имеющие 1-8 атомов углерода, такие какC1-6, C1-4, С 3-8, С 2-5 или какой-либо другой диапазон, и, если не указано иначе, включают как замещенные,так и незамещенные группы. Например, радикалы C1-6 алкил включают метил, этил, н-пропил, изопропил,н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, 3-(2-метил)бутил, 2-пентил, 2-метилбутил, неопентил, н-гексил, 2-гексил и 2-метилпентил. Алкоксирадикалы образованы из указанных выше алкильных групп с прямой или разветвленной цепью. "Алкил" и "алкокси" включают незамещенные или замещенные группы с одним или несколькими заместителями, такими как между 1 и 5, 1 и 3 или 2 и 4 заместителями. Заместители могут быть однаковыми (дигидрокси, диметил), подобными (хлор, фтор) или разными(хлорбензил- или аминометилзамещенными). Примеры замещенного алкила включают галогеналкил (такой, как фторметил, хлорметил, дифторметил, перхлорметил, 2-бромэтил, трифторметил и 3-йодциклопентил), гидроксиалкил (такой, как гидроксиметил, гидроксиэтил, 2-гидроксипропил), аминоалкил (такой, как аминометил, 2-аминоэтил, 3-аминопропил и 2-аминопропил), алкоксилалкил, нитроалкил, алкилалкил, цианоалкил, фенилалкил, гетероарилалкил, гетероциклилалкил, феноксиалкил, гетероарилоксиалкил (такой, как 2-пиридилоксиалкил), гетероциклилоксиалкил (такой, как 2-тетрагидропираноксиалкил), тиоалкилалкил (такой, как MeS-алкил), тиофенилалкил (такой, как phS-алкил), карбоксилалкил и т.д. Ди(С 1-3 алкил)аминогруппа включает независимо выбранные алкилгруппы для формирования, на-4 009804 пример, метилпропиламино и изопропилметиламино, в дополнение, диалкиламиногруппы, имеющие две одинаковые алкилгруппы, такие как диметиламино или диэтиламино. Термин "алкенил" включает необязательно замещенные углеводородные радикалы с прямой или разветвленной цепью, как указано выше, по меньшей мере с одной углерод-углеродной двойной связью(sp2). Алкенилы включают этенил (или винил), проп-1-енил, проп-2-енил (или аллил), изопропенил (или 1-метилвинил), бут-1-енил, бут-2-енил, бутадиенилы, пентенилы, гекса-2,4-диенил и т.д. Углеводородные радикалы, имеющие смесь двойных связей и тройных связей, такие как 2-пентен-4-инил, сгруппированы в описании как алкинилы. Алкенил включает циклоалкенил. Цис- и транс-формы или (Е)- и (Z)формы включены в изобретение. "Алкенил" может быть замещен одним или несколькими заместителями, включая, но без ограничения перечисленным, цианоалкенил и тиоалкенил. Термин "алкинил" включает необязательно замещенные углеводородные радикалы с прямой или разветвленной цеью, как выше, по меньшей мере с одной углерод-углеродной тройной связью (sp). Алкинилы включают этинил, пропинилы, бутинилы и пентинилы. Углеводородные радикалы, имеющие смесь двойных связей и тройных связей, такие как 2-пентен-4-инил, сгруппированы в описании как алкинилы. Алкинил не включает циклоалкинил. Используемый термин "Ас", один или как часть замещающей группы, означает ацетил (СН 3 СО-). Используемый термин "ацил" относится к заместителю, который имеет карбонилгруппу (С=O) и одну или несколько групп алкила или алкилена. Например, С 2-4 ацил включает, без ограничения, ацетил,СН 3 СН 2-(С=O)-СН 2- и СН 3 СН 2 СН 2(С=O)-. Термин "галоген" включает йод, бром, хлор и фтор. Термин "арил" или "Ar", используемый в описании, относится к незамещенной или замещенной ароматической углеводородной кольцевой системе, такой как фенил и нафтил. Когда Ar или арилгруппа является замещенной, она может иметь от одного до трех заместителей, которые независимо выбраны из С 1-С 8 алкила, C1-C8 алкокси, фторированного C1-C8 алкила (например, трифторметил), фторированного C1C8 алкокси (например, трифторметокси), галогена, циано, C1-C8 алкилкарбонила, такого как ацетил, карбоксила, гидрокси, амино, нитро, С 1-С 4 алкиламино (например, -NH-C1-C4 алкил), C1-C4 диалкиламино(например, -N-[C1-C4 алкил]2, где алкилгруппы могут быть одинаковыми или разными) или незамещенного, моно-, ди- или тризамещенного фенила, где заместители на фениле независимо выбраны из C1-C8 алкила, C1-C8 алкокси, фторированного C1-C8 алкила, фторированного C1-C8 алкокси, галогена, циано, ацетила, карбоксила, гидрокси, амино, нитро, алкиламино, диалкиламино или 5- или 6-членного гетероарила,имеющего 1-3 гетероатома, выбранных из N, О и S. Термин "гетероарил", используемый в описании, представляет стабильную незамещенную или замещенную 5- или 6-членную моноциклическую или бициклическую ароматическую кольцевую систему,которая состоит из атомов углерода и от 1 до 3 гетероатомов, выбранных из N, О и S. Гетероарилгруппа может быть присоединена при любом гетероатоме или атоме углерода, когда это имеет результатом создание стабильной структуры. Примеры гетероарилгрупп включают, не ограничиваясь указанным, бензимидазолил, бензизоксазолил, бензофуранил, бензопиразолил, бензотиадиазолил, бензотиазолил, бензотиенил, бензотриазолил, бензоксазолил, фуранил, фуразанил, фурил, имидазолил, индазолил, индолизинил, индолинил, индолил, изобензофуранил, изоиндолил, изотиазолил, изоксазолил, оксазолил, пуринил,пиразинил, пиразолил, пиридазинил, пиридинил, пиримидинил, пирролил, хинолинил, хинолил, тиадиазолил, тиазолил, тиофенил или триазолил. Когда гетероарилгруппа является замещенной, гетероарилгруппа может иметь от одного до трех заместителей, включая, не ограничиваясь указанными, C1-C8 алкил, галоген и арил. Термин "гетероциклил" включает необязательно замещенные неароматические кольца, имеющие атомы углерода и по меньшей мере 1 гетероатом (О, S, N) или группу гетероатомов (SO2, СО, CONN,COO) в кольце. Гетероциклил может быть насыщенным, частично насыщенным, неароматическим или конденсированным. Примеры гетероциклила включают циклогексилимино, имидазодинил, имидазолинил, морфолинил, пиперазинил, пиперидил, пиридил, пиранил, пиразолидинил, пиразолинил, пирролидинил, пирролинил и тиенил. Если не указано иначе, гетероарил и гетероциклил могут иметь валентность, присоединяющую их к остальной части молекулы через атом углерода, такой как 3-фурил или 2-имидазолил, или через гетероатом,такой как N-пиперидил или 1-пиразолил. Предпочтительно моноциклический гетероциклил имеет 5-7 атомов кольца или 5-6 атомов кольца; в кольце может быть 1-5 гетероатомов или групп гетероатомов и предпочтительно 1-3 или 1-2 гетероатома или группы гетероатомов. Гетероциклил и гетероарил также включают конденсированные, например бициклические, кольца,такие как кольца, необязательно конденсированные с необязательно замещенным карбоциклическим или гетероциклическим 5- или 6-членным ароматическим кольцом. Например, "гетероарил" включает необязательно замещенное 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота, конденсированное с необязательно замещенным 5- или 6-членным карбоциклическим или гетероциклическим ароматическим кольцом. Указанное гетероциклическое 5- или 6-членное ароматическое кольцо, конденсированное с указанным 5- или 6-членным ароматическим кольцом, может содержать 1, 2 или 3 атома-5 009804 азота, когда это 6-членное кольцо, или 1, 2 или 3 гетероатома, выбранных из кислорода, азота и серы,когда это 5-членное кольцо. Подразумевается, что определение какого-либо заместителя или замены при конкретном месте в молекуле является не зависимым от их определений где-либо еще в этой молекуле. Понятно, что заместители и схемы замещений на соединениях по данному изобретению могут быть выбраны специалистом в этой области так, чтобы получить химически стабильные соединения, которые легко могут быть синтезированы по технологиям, известным в технике, а также приведенными способами. Когда химические части молекул объединены так, как в этоксиметиле или фенилэтиле, термин описан в направлении от периферии к месту присоединения остальной части молекулы. Например, этоксиметил означает СН 3 СН 2 ОСН 2- и фенилэтил означает фенилгруппу, связанную посредством -СН 2 СН 2- с остальной частью молекулы (а не фенилгруппу, связанную с молекулой, с группой СН 3 СН 2 в качестве заместителя на фениле). Когда использованы скобки, они указывают периферийное замещение. Подразумевается, что используемый термин "состав" охватывает продукт, содержащий оговоренные ингредиенты в заданных количествах, а также любой продукт, который является результатом, непосредственно или косвенно, объединений оговоренных ингредиентов в заданных количествах. Соединения по изобретению дополнительно описаны в следующем разделе. В. Соединения. Данное изобретение относится к составам, содержащим соединения формулы (I), которые описаны выше, и способам их применения. Если не указано иначе, в формуле (I) каждый гидрокарбил (алкил, алкенил, алкинил, циклоалкил, цикловлкенил и т.д.) или гетерокарбил (гетероциклил, гетероарил, группа гетероатомов, такая как сульфонил, амино, амидо и т.д.) может быть замещенным или незамещенным,например "алкил" включает замещенный и незамещенный алкил, и "гетероциклил", и "арил", и "алкокси", и т.д. также могут быть замещенными или незамещенными. Например, когда R4 означает "метил или метокси", если не указано иначе, эти термины коллективно включают метил, метокси, трифторметил,трифторметокси, дифторметил, дифторметокси, фторметил, фторметокси, хлордифторметил, хлордифторметокси, дихлорфторметил и дихлорфторметокси и т.д. Примеры соединений по изобретению включают соединения формулы (I) где: (a) m равно 1 или 2;(b) m равно 1; (с) n равно 1; (d) X означает О; Y означает S или О; (е) Y означает S; (f) R1 выбран из Н,C1-2 алкила, C1-2 алкокси и галогена; (g) R1 выбран из галогена, метила и метокси и, если он метил или метокси, R1 может быть замещенным или незамещенным; (h) R2 означает Н, галоген, метокси или метил;(i) R2 означает Н, фтор или хлор; (j) каждый из R3 и R4 независимо выбран из Н, галогена, C1-4 алкила,C1-3 алкокси и NRcRd; (k) каждый из R3 и R4 независимо выбран из Н, фтора, хлора, C1-2 алкила и C1-2 алкокси; (l) каждый из R3 и R4 независимо выбран из Н, фтора, хлора, метила, метокси, трифторметила, трифторметокси, дифторметила, дифторметокси, фторметила, фторметокси, трифторэтила и трифторэтокси;(m) каждый из R5 и R6 независимо выбран из Н, C1-3 алкила и C1-3 алкокси; (n) по меньшей мере один из R5 и R6 означает метил, метокси, этил и этокси и другой выбран из Н, метокси, метила, этила и этокси; (о) каждый из R7 и R8 независимо выбран из Н и C1-3 алкила; (р) один из R7 и R8 означает Н и другой означает Н, метил или этил; (q) каждый из R7 и R8 означает Н; (r) X означает О; Y означает S или О; R1 выбран из Н, С 1-2 алкила, C1-2 алкокси и галогена; каждый из R5 и R6 независимо выбран из Н, C1-3 алкила и C1-3 алкокси и каждый из R7 и R8 независимо выбран из Н и C1-3 алкила; (s) m равно 1 или 2 и n равно 1; (t) каждый из R3 и R4 независимо выбран из Н, фтора, хлора, C1-2 алкила и C1-2 алкокси и R1 выбран из Н, C1-2 алкила,C1-2 алкокси и галогена; (u) каждый из R3 и R4 независимо выбран из Н, фтора, хлора, метила, метокси,трифторметила, трифторметокси, трифторэтила и трифторэтокси; или сочетания указанного выше. Примеры соединений формулы (I) также включают такие, где: (v) m равно 1 или 2; n равно 0 или 1;X означает S или О; Y означает S, CH2 или О; R1 и R2 независимо выбраны из Н, C1-4 алкила, C1-3 алкокси,галогена и -NRaRb, где каждый из Ra и Rb независимо выбран из Н и C1-4 алкила; каждый из R3 и R4 независимо выбран из Н, галогена, циано, C1-4 алкила, C1-3 алкокси и NRcRd, где каждый из Rc и Rd независимо выбран из Н и C1-4 алкила и где по меньшей мере один из R3 и R4 не Н; и каждый из R5 и R6 независимо выбран из Н, C1-5 алкила, C1-5 алкокси, С 3-5 циклоалкила, (C3-5 циклоалкил)C1-3 алкила и NReRf, где каждый из Re и Rf независимо выбран из Н и C1-4 алкила; или R5 и R6 вместе образуют спиро C3-6 циклоалкил; и каждый из R7 и R8 независимо выбран из Н и C1-2 алкила. Примеры соединений формулы (I) также включают такие соединения, где: (w) m равно 1 или 2; n равно 0 или 1; X означает S или О; Y означает S или О; R1 и R2 независимо выбраны из Н, C1-2 алкила,C1-2 алкокси, галогена и -NRaRb, где каждый из Ra и Rb независимо выбран из Н и C1-4 алкила; каждый изR3 и R4 независимо выбран из Н, галогена, циано, C1-4 алкила, C1-3 алкокси и NRcRd, где каждый из Rc и Rd независимо выбран из Н и C1-4 алкила и где по меньшей мере один из R3 и R4 не Н; и каждый из R5 и R6 независимо выбран из Н, C1-3 алкила, C1-2 алкокси; и каждый из R7 и R8 означает Н. Конкретные примеры соединений формулы (I) включают следующие соединения: 2-метил-2-[2-метил-4-(3-п-толил-[1,2,4]тиадиазол-5-илметилсульфанил)фенокси]пропионовая кислота; 2-метил-2-2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметокси]феноксипропионовая кислота; 2-4-[3-(4-трет-бутилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпро-6 009804 пионовая кислота; 2-4-[3-(4-хлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовая кислота; 2-4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси 2-метилпропионовая кислота; 2-4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовая кислота; 2-4-[3-(2,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовая кислота; 2-4-[3-(3,4-диметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовая кислота; 2-4-[3-(3-хлор-4-метилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовая кислота; 2-4-[3-(3-фтор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2 метилпропионовая кислота; 1-2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]феноксициклопентанкарбоновая кислота; 1-4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфеноксициклопентанкарбоновая кислота; 2-метил-2-2-метил-4-[5-(4-трифторметилфенил)-[1,2,4]тиадиазол-3-илметилсульфанил]фенокси пропионовая кислота; 2-4-[5-(4-хлорфенил)-[1,214]тиадиазол-3-илметилсульфанил]-2-метилфенокси-2-метилпропионовая кислота; 2-4-[5-(4-изопропилфенил)-[1,2,4]тиадиазол-3-илметилсульфанил]-2-метилфенокси-2-метилпропионовая кислота; 2-метил-2-2-метил-4-[5-(4-трифторметоксифенил)-[1,2,4]тиадиазол-3-илметилсульфанил]фенокси пропионовая кислота; 2-4-[5-(4-трет-бутилфенил)-[1,2,4]тиадиазол-3-илметилсульфанил]-2-метилфенокси-2-метилпропионовая кислота; 2-метил-2-2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси пропионовая кислота; 2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]феноксиуксусная кислота; 2-метил-2-2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси пропионовая кислота и 2-метил-2-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]феноксипропионовая кислота. Согласно одному аспекту к предпочтительным соединениям относятся 2-метил-2-2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметокси]феноксипропионовая кислота; 2-метил-2-2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси пропионовая кислота; 2-4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси 2-метилпропионовая кислота; 2-4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовая кислота; 2-метил-2-2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенилсульфанилпропионовая кислота; 2-4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил-2-метилпропионовая кислота; 2-4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил-2-метилпропионовая кислота; 2-4-[3-(4-трет-бутилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил-2-метилпропионовая кислота; 2-метил-2-(2-метил-4-3-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]пропилфенокси)пропионовая кислота. Согласно другому аспекту к предпочтительным соединениям относятся 2-метил-2-2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси пропионовая кислота; 2-метил-2-(2-метил-4-2-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил]этилфенокси)пропионовая кислота; 2-(4-2-[3-(3-хлор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил]этил-2-метилфенокси)-2-метилпропионовая кислота;-7 009804 2-(4-2-[3-(3-фтор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил]этил-2-метилфенокси)-2-метилпропионовая кислота; 2-(4-2-[3-(3-фтор-4-метилфенил)-[1,2,4]тиадиазол-5-ил]этил-2-метилфенокси)-2-метилпропионовая кислота; 2-метил-2-(2-метил-4-2-[3-(4-трифторметилфенил)-[1,2,4]-тиадиазол-5-ил]этилсульфанилфенокси)пропионовая кислота; 2-(4-2-[3-(3-хлор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил]этилсульфанил-2-метилфенокси)2-метилпропионовая кислота; 2-(4-2-[3-(3-хлор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-ил]этилсульфанил-2-метилфенокси)2-метилпропионовая кислота; 2-метил-2-2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенилсульфанилпропионовая кислота; 2-4-[3-(3-хлор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил-2-метилпропионовая кислота; 2-4-[3-(3-фтор-4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил-2-метилпропионовая кислота; 2-4-[3-(3-фтор-4-метилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенилсульфанил-2 метилпропионовая кислота. Примеры наиболее предпочтительных соединений включают следующие: 2-метил-2-2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметокси]феноксипропионовая кислота; 2-метил-2-2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметокси]феноксипропионовая кислота; 2-метил-2-2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси пропионовая кислота; 2-4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовая кислота и 2-4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси 2-метилпропионовая кислота. Дополнительные предпочтительные соединения включают следующие: 2-метил-2-2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметокси]феноксипропионовая кислота; 2-4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметокси]-2-метилфенокси-2-метилпропионовая кислота; 2-4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметокси]-2-метилфенокси-2-метилпропионовая кислота; 2-метил-2-(2-метил-4-2-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этоксифенокси)пропионовая кислота; 2-(4-2-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-ил]этил-2-метилфенокси)-2-метилпропионовая кислота; 2-метил-2-(2-метил-4-2-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этилфенокси)пропионовая кислота; 2-(4-2-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этил-2-метилфенокси)-2-метилпропионовая кислота; 2-(4-2-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этокси-2-метилфенокси)-2-метилпропионовая кислота; 2-(4-2-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-ил]этокси-2-метилфенокси)-2-метилпропионовая кислота; 2-метил-2-(2-метил-4-2-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этоксифенилсульфанил)пропионовая кислота; 2-(4-2-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этокси-2-метилфенилсульфанил)-2-метилпропионовая кислота; 2-(4-2-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-ил]этокси-2-метилфенилсульфанил)-2-метилпропионовая кислота; 2-метил-2-(2-метил-4-2-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этилсульфанилфенилсульфанил)пропионовая кислота; 2-(4-2-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]этилсульфанил-2-метилфенилсульфанил)-2-метилпропионовая кислота; 2-(4-2-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-ил]этилсульфанил-2-метилфенилсульфанил)-2-метилпропионовая кислота. Фармацевтический состав по изобретению представляет фармацевтический состав, содержащий фармацевтически приемлемый носитель и соединение по п.1, 20, 22, 24-27 или 28, как описано в прила-8 009804 гаемой формуле изобретения. Когда соединения по данному изобретению имеют по меньшей мере один хиральный центр, они,соответственно, могут существовать как энантиомеры. Когда соединения имеют два или более хиральных центров, они дополнительно могут существовать как диастереомеры. Следует понимать, что все такие изомеры и их смеси охвачены сферой действия данного изобретения. Более того, некоторые кристаллические формы соединений могут существовать как полиморфы и, как таковые, должны быть включены в данное изобретение. В дополнение, некоторые соединения могут образовывать сольваты с водой (т.е. гидраты) или общепринятыми органическими растворителями, и такие сольваты также должны находиться в сфере действия данного изобретения. Изобретение относится к раскрытым выше соединениям и близкородственным фармацевтически приемлемым формам раскрытых соединений, таким как соли, сложные эфиры, амиды, гидраты или их сольватированные формы, замаскированные или защищенные формы, и рацемическим смесям или энантиомерно или оптически чистым формам. Фармацевтически приемлемые соли, сложные эфиры и амиды включают соли карбоксилаты (например, C1-8 алкил, циклоалкил, арил, гетероарил или неароматические гетероциклические), аддитивные соли с аминокислотами, сложные эфиры и амиды, которые находятся в пределах разумного соотношения польза/риск, фармакологически эффективны и являются подходящими для контакта с тканями пациентов без чрезмерной токсичности, раздражения или аллергической реакции. Примеры солей включают гидробромид, гидрохлорид, сульфат, бисульфат, нитрат, ацетат, оксалат, валерат, олеат, пальмитат, стеарат,лаурат, борат, бензоат, лактат, фосфат, тозилат, цитрат, малеат, фумарат, сукцинат, тартрат, нафтилат,мезилат, глюкогептонат, лактиобионат и лаурилсульфонат. Они могут содержать катионы щелочных и щелочно-земельных металлов, таких как натрий, калий, кальций и магний, а также нетоксичные катионы аммония, четвертичного аммония и амина, такие как тетраметиламмоний, метиламин, триметиламин и этиламин. См., например, S.M. Berge, et al. "Pharmaceutical Salts", J. Pharm. Sci., 1977, 66: 1-19, эта публикация дана в качестве ссылки. Примеры фармацевтически приемлемых амидов по изобретению включают те, которые получены из аммония, первичных C1-6 алкиламинов и вторичных ди(С 1-6 алкил)аминов. Вторичные амины включают 5- или 6-членные гетероциклические или гетероароматические кольцевые части молекул, содержащие по меньшей мере 1 атом азота и необязательно 1-2 дополнительных гетероатома. Предпочтительные амиды получены из аммония, первичных C1-3 алкиламинов и ди(С 1-3 алкил)аминов. Примеры фармацевтически приемлемых сложных эфиров по изобретению включают сложные С 1-7 алкил,С 5-7 циклоалкил, фенил и фенил(C1-6)алкил эфиры. Предпочтительные сложные эфиры включают метиловые сложные эфиры. Изобретение также относится к соединениям, указанным выше, имеющим одну или несколько функциональных групп (например, амино или карбоксил), замаскированных защитной группой. Некоторые такие замаскированные или защищенные соединения являются фармацевтически приемлемыми,другие могут быть полезны в качестве промежуточных соединений. Раскрытые в описании синтетические промежуточные соединения и процессы и их незначительные модификации также включены в объем изобретения. Защитные группы для гидроксила Защита для гидроксильной группы включает метиловые простые эфиры, замещенные метиловые простые эфиры, замещенные этиловые простые эфиры, замещенные бензиловые простые эфиры и силиловые простые эфиры. Замещенные метиловые простые эфиры Примеры замещенных метиловых простых эфиров включают метилоксиметил, метилтиометил,трет-бутилтиометил, (фенилдиметилсилил)метоксиметил, бензилоксиметил, п-метоксибензилоксиметил,(4-метоксифенокси)метил, гваяколметил, трет-бутоксиметил, 4-пентенилоксиметил, силоксиметил, 2-метоксиэтоксиметил, 2,2,2-трихлорэтоксиметил, бис-(2-хлорэтокси)метил, 2-(триметилсилил)этоксиметил,тетрагидропиранил, 3-бромтетрагидропиранил, тетрагидротиопиранил, 1-метоксициклогексил, 4-метокситетрагидропиранил, 4-метокситетрагидротиопиранил, 4-метокситетрагидротиопиранил S,S-диоксидо,1-[(2-хлор-4-метил)фенил]-4-метоксипиперидин-4-ил, 1,4-диоксан-2-ил, тетрагидрофуранил, тетрагидротиофуранил и 2,3,3 а,4,5,6,7,7 а-октагидро-7,8,8-триметил-4,7-метанобензофуран-2-ил. Замещенные этиловые простые эфиры Примеры замещенных этиловых простых эфиров включают 1-этоксиэтил, 1-(2-хлорэтокси)этил, 1 метил-1-метоксиэтил, 1-метил-1-бензилоксиэтил, 1-метил-1-бензилокси-2-фторэтил, 2,2,2-трихлорэтил,2-триметилсилилэтил, 2-(фенилселенил)этил, трет-бутил, аллил, п-хлорфенил, п-метоксифенил, 2,4-динитрофенил и бензил. Замещенные бензиловые простые эфиры Примеры замещенных бензиловых простых эфиров включают п-метоксибензил, 3,4-диметоксибензил, о-нитробензил, п-нитробензил, п-галогенбензил, 2,6-дихлорбензил, п-цианобензил, п-фенилбензил,2- и 4-пиколил, 3-метил-2-пиколил N-оксидо, дифенилметил, п,п'-динитробензгидрил, 5-дибензосуберил,трифенилметил, -нафтилдифенилметил, п-метоксифенилдифенилметил, ди(п-метоксифенил)фенилметил, три(п-метоксифенил)метил, 4-(4'-бромфенацилокси)фенилдифенилметил, 4,4',4"-трис-(4,5-дихлор-9 009804 фталимидофенил) метил, 4,4',4"-трис-(левулиноилоксифенил)метил, 4,4',4"-трис-(бензоилоксифенил)метил, 3-(имидазол-1-илметил)-бис-(4',4"-диметоксифенил)метил, 1,1-бис-(4-метоксифенил)-1'-пиренилметил, 9-антрил, 9-(9-фенил)ксантенил, 9-(9-фенил-10-оксо)антрил, 1,3-бензодитиолан-2-ил и бензизотиазолил S,S-диоксидо. Силиловые простые эфиры Примеры силиловых простых эфиров включают триметилсилил, триэтилсилил, триизопропилсилил, диметилизопропилсилил, диэтилизопропилсилил, диметилгексилсилил, трет-бутилдиметилсилил,трет-бутилдифенилсилил, трибензилсилил, три-п-ксилилсилил, трифенилсилил, дифенилметилсилил и трет-бутилметоксифенилсилил. Сложные эфиры В дополнение к простым эфирам, гидроксильная группа может быть защищена как сложный эфир. Примеры сложных эфиров включают формиат, бензоилформиат, ацетат, хлорацетат, дихлорацетат, трихлорацетат, трифторацетат, метоксиацетат, трифенилметоксиацетат, феноксиацетат, п-хлорфеноксиацетат,п-Р-фенилацетат, 3-фенилпропионат, 4-оксопентаноат(левулинат), 4,4-(этилендитио)пентаноат, пивалоат, адамантоат, кротонат, 4-метоксикротонат, бензоат, п-фенилбензоат, 2,4,6-триметилбензоат(мезитоат). Карбонаты Примеры карбонатов включают метил, 9-флуоренилметил, этил, 2,2,2-трихлорэтил, 2-(триметилсилил)этил, 2-(фенилсульфонил)этил, 2-(трифенилфосфонио)этил, изобутил, винил, аллил, п-нитрофенил,бензил, п-метоксибензил, 3,4-диметоксибензил, о-нитробензил, п-нитробензил, S-бензилтиокарбонат, 4 этокси-1-нафтил и метилдитиокарбонат. Агенты вспомогательного расщепления Примеры агентов вспомогательного расщепления включают 2-йодбензоат, 4-азидобутират, 4-нитро 4-метилпентаноат, о-(дибромметил)бензоат, 2-формилбензолсульфонат, 2-(метилтиометокси)этилкарбонат, 4-(метилтиометокси)бутират и 2-(метилтиометоксиметил)бензоат. Разнообразные сложные эфиры Примеры разнообразных сложных эфиров включают 2,6-дихлор-4-метилфеноксиацетат, 2,6-дихлор 4-(1,1,3,3-тетраметилбутил)феноксиацетат, 2,4-бис-(1,1-диметилпропил)феноксиацетат, хлордифенилацетат, изобутират, моносукциноат, (Е)-2-метил-2-бутеноат(тиглоат), о-(метоксикарбонил)бензоат, п-Р-бензоат, -нафтоат, нитрат, алкил N,N,N',N'-тетраметилфосфородиамидат, N-фенилкарбамат, борат, диметилфосфинотиоил и 2,4-динитрофенилсульфенат. Сульфонаты Примеры сульфонатов включают сульфат, метансульфонат(мезилат), бензилсульфонат и тозилат. Аминозащитные группы Защита для аминогруппы включает карбаматы, амиды и специальные -NH защитные группы. Примеры карбаматов включают метил- и этилкарбаматы, замещенные этилкарбаматы, карбаматы вспомогательного расщепления, карбаматы фотолитического расщепления, производные типа мочевины и разнообразные карбаматы. Карбаматы Примеры метил- и этилкарбаматов включают метил и этил, 9-флуоренилметил, 9-(2-сульфо)флуоренилметил, 9-(2,7-дибром)флуоренилметил, 2,7-ди-трет-бутил-[9-(10,10-диоксо-10,10,10,10-тетрагидротиоксантил)]метил и 4-метоксифенацил. Замещенный этил Примеры замещенных этилкарбаматов включают 2,2,2-трихлорэтил, 2-триметилсилилэтил, 2-фенилэтил, 1-(1-адамантил)-1-метилэтил, 1,1-диметил-2-галогенэтил, 1,1-диметил-2,2-дибромэтил, 1,1-диметил-2,2,2-трихлорэтил, 1-метил-1-(4-бифенилил)этил, 1-(3,5-ди-трет-бутилфенил)-1-метилэтил, 2-(2'- и 4'-пиридил)этил, 2-(N,N-дициклогексилкарбоксамидо)этил, трет-бутил, 1-адамантил, винил, аллил, 1-изопропилаллил, циннамил, 4-нитроциннамил, 8-хинолил, N-гидроксипиперидинил, алкилдитио, бензил, пметоксибензил, п-нитробензил, п-бромбензил, п-хлорбензил, 2,4-дихлорбензил, 4-метилсульфинилбензил, 9-антрилметил и дифенилметил. Агенты вспомогательного расщепления Примеры агентов вспомогательного расщепления включают 2-метилтиоэтил, 2-метилсульфонилэтил, 2-(п-толуолсульфонил)этил, [2-(1,3-дитианил)]метил, 4-метилтиофенил, 2,4-диметилтиофенил, 2 фосфониоэтил, 2-трифенилфосфониоизопропил, 1,1-диметил-2-цианоэтил, м-хлор-п-ацилоксибензил, п(дигидроксиборил)бензил, 5-бензизоксазолилметил и 2-(трифторметил)-6-хромонилметил. Агенты фотолитического расщепления Примеры агентов фотолитического расщепления включают м-нитрофенил, 3,5-диметоксибензил, онитробензил, 3,4-диметокси-6-нитробензил и фенил(о-нитрофенил)метил. Производные типа мочевины Примеры производных типа мочевины включают фенотиазинил-(10)-карбонилпроизводное, N'-птолуолсульфониламинокарбонил и N'-фениламинотиокарбонил. Разнообразные карбаматы Примеры разнообразных карбаматов включают трет-амил, S-бензилтиокарбамат, п-цианобензил,- 10009804 циклобутил, циклогексил, циклопентил, циклопропилметил, п-децилоксибензил, диизопропилметил, 2,2 диметоксикарбонилвинил, o-(N,N-диметилкарбоксамидо)бензил, 1,1-диметил-3-(N,N-диметилкарбоксамидо)пропил, 1,1-диметилпропинил, ди(2-пиридил)метил, 2-фуранилметил, 2-йодэтил, изоборнил, изобутил, изоникотинил, п-(п'-метоксифенилазо)бензил, 1-метилциклобутил, 1-метилциклогексил, 1-метил-1 циклопропилметил, 1-метил-1-(3,5-диметоксифенил)этил, 1-метил-1-(п-фенилазофенил)этил, 1-метил-1 фенилэтил, 1-метил-1-(4-пиридил)этил, фенил, п-(фенилазо)бензил, 2,4,6-три-трет-бутилфенил, 4-(триметиламмоний)бензил и 2,4,6-триметилбензил. Примеры амидов включают следующие. АмидыN-Фталимид, N-дитиасукциноил, N-2,3-дифенилмалеоил, N-2,5-диметилпирролил, аддукт N-1,1,4,4 тетраметилдисилилазациклопентана, 5-замещенный 1,3-диметил-1,3,5-триазациклогексан-2-он, 5-замещенный 1,3-дибензил-1,3,5-триазациклогексан-2-он и 1-замещенный 3,5-динитро-4-пиридонил. Специальные -NH защитные группы Примеры специальных -NH защитных групп включают следующие.N-1,1-Диметилтиометилен, N-бензилиден, N-п-метоксибензилиден, N-дифенилметилен, N-[(2-пиридил)мезитил]метилен и N-(N',N'-диметиламинометилен). Защита карбоксильной группы Сложные эфиры Примеры сложных эфиров включают формиат, бензоилформиат, ацетат, трихлорацетат, трифторацетат, метоксиацетат, феноксиацетат, п-хлорфеноксиацетат, бензоат. Замещенные метиловые сложные эфиры Примеры замещенных метиловых сложных эфиров включают 9-флуоренилметил, метоксиметил,метилтиометил, тетрагидропиранил, тетрагидрофуранил, метоксиэтоксиметил, 2-(триметилсилил)этоксиметил, бензилоксиметил, фенацил, п-бромфенацил, -метилфенацил, п-метоксифенацил, карбоксамидометил и N-фталимидометил. 2-Замещенные этиловые сложные эфиры Примеры 2-замещенных этиловых сложных эфиров включают 2,2,2-трихлорэтил, 2-галогенэтил, хлоралкил, 2-(триметилсилил)этил, 2-метилтиоэтил, 1,3-дитианил-2-метил, 2-(п-нитрофенилсульфенил) этил, 2-(п-толуолсульфонил)этил, 2-(2'-пиридил)этил, 2-(дифенилфосфино)этил, 1-метил-1-фенилэтил,трет-бутил, циклопентил, циклогексил, аллил, 3-бутен-1-ил, 4-(триметилсилил)-2-бутен-1-ил, циннамил,-метилциннамил, фенил, п-(метилмеркапто)фенил и бензил. Замещенные бензиловые сложные эфиры Примеры замещенных бензиловых сложных эфиров включают трифенилметил, дифенилметил, бис(о-нитрофенил)метил, 9-антрилметил, 2-(9,10-диоксо)антрилметил, 5-дибензосуберил, 1-пиренилметил,2-(трифторметил)-6-хромилметил, 2,4,6-триметилбензил, п-бромбензил, о-нитробензил, п-нитробензил,п-метоксибензил, 2,6-диметоксибензил, 4-(метилсульфинил)бензил, 4-сульфобензил, пиперонил, 4-пиколил и п-Р-бензил. Силиловые сложные эфиры Примеры силиловых сложных эфиров включают триметилсилил, триэтилсилил, трет-бутилдиметилсилил, изопропилдиметилсилил, фенилдиметилсилил и ди-трет-бутилметилсилил. Активированные сложные эфиры Примеры активированных сложных эфиров включают тиолы. Разнообразные производные Примеры разнообразных производных включают оксазолы, 2-алкил-1,3-оксазолины, 4-алкил-5-оксо-1,3-оксазолидины, 5-алкил-4-оксо-1,3-диоксоланы, сложные ортоэфиры, фенилгруппу и комплекс- 11009804 пентааминокобальта(III). Станниловые сложные эфиры Примеры станниловых сложных эфиров включают триэтилстаннил и три-н-бутилстаннил. С. Синтез. Изобретение относится к способам получения раскрытых соединений согласно традиционным способам органического синтеза, а также матричным или комбинаторным способам синтеза. Схемы A-G описывают примерные пути синтеза. Используя указанные схемы, руководящие указания ниже и примеры соединений 1-28, специалист в этой области может разработать аналогичные или подобные способы для данного соединения, которые охватываются изобретением. Эти способы являются примерами предпочтительных схем синтеза, но не должны рассматриваться как ограничивающие объем изобретения. Специалист в этой области легко осознает, что синтез соединений по данному изобретению может быть осуществлен путем приобретения промежуточных или защищенных промежуточных соединений,описанных в какой-либо из схем, раскрытых в описании. Специалист в этой области дополнительно осознает, что во время какого-либо процесса получения соединений по данному изобретению может быть необходимо и/или желательно защищать чувствительные или реакционноспособные группы на каких-либо представляющих интерес молекулах. Это может быть достигнуто посредством традиционных защитных групп, таких как описанные в "Protective Groups in Organic Synthesis", John WileySons, 1991. Эти защитные группы могут быть удалены на подходящей стадии с использованием известных в технике способов. Когда при получении соединений по изобретению получают смесь стереоизомеров, эти изомеры могут быть разделены обычными техническими приемами, такими как препаративная хроматография. Соединения могут быть получены в рацемической форме, или отдельные энантиомеры могут быть получены энантиоспецифическим синтезом или разделением на изомеры. Эти соединения могут, например,быть разделены на их компоненты энантиомеры путем стандартных технологий, таких как формирование диастереомерных пар путем солеобразования. Соединения могут быть также разделены путем образования диастереомерных сложных эфиров или амидов с последующим хроматографическим разделением и удалением хирального вспомогательного агента. В качестве варианта соединения могут быть разделены с помощью колонки хиральной ВЭЖХ. Примеры схем синтеза представлены в примерах 1-38. Соединения, аналогичные целевым соединениям этих примеров, могут быть получены в соответствии с подобными путями. Раскрытые соединения применимы в фундаментальном исследовании и в качестве фармацевтических агентов, как описано в следующем разделе. Общие указания Схема 1. Синтез промежуточного соединения 1-D. Согласно схеме 1, где R1, R2, R5 и R6 имеют указанные выше значения (за исключением того, что R5 и R6 не образуют спиро C3-6 циклоалкила или спиро 5- или 6-членного гетероциклила), фенол 1-А, разновидности которого коммерчески доступны (такой, как 3-метилфенол, 2-этилфенол, 2-пропилфенол, 2,3 диметилфенол, 2-хлорфенол, 2,3-дихлорфенол, 2-бромфенол и 2-аминофенол), алкилируют до образования этилового сложного эфира феноксиуксусной кислоты 1-В с использованием подходящего сложного эфира галогенуксусной кислоты, такого как этиловый сложный эфир бромуксусной кислоты или этиловый сложный эфир 2-бром-2-метилпропионовой кислоты, в присутствии подходящего основания, такого как Cs2CO3, K2CO3 или NaH, в подходящем растворителе, таком как CH3CN или THF. Сульфирование этилового сложного эфира феноксиуксусной кислоты 1-В подходящим агентом сульфирования, таким как хлорсульфоновая кислота, происходит избирательно в пара-положении с образованием этилового сложного эфира 4-хлорсульфонилфеноксиуксусной кислоты 1-С. Превращение сульфонилхлорида 1-С в бензолтиол 1-D осуществляют, используя в качестве восстановителя металл, такой как олово или цинк, в кислотной среде, такой как этанол или диоксан. На схеме 2, где R1, R2, R3, R4, R5 и R6 имеют указанные выше значения (за исключением того, что R5 и R6 не образуют спиро С 3-6 циклоалкила или спиро 5- или 6-членного гетероциклила), фенилоксатиазолон 2-В получают при взаимодействии бензамида 2-А, разновидности которого коммерчески доступны(такие, как R3=CF3, или R4=OCF3, CF3, OCH3, Cl, Br или I, или R3=R4=Cl), с хлоркарбонилсульфенилхлоридом в подходящем растворителе, таком как толуол. Термолиз оксатиазолона 2-В и улавливание образующегося бензонитрилсульфида этилцианоформиатом в подходящем растворителе с высокой точкой кипения, таком как хлорбензол или 1,2-дихлорбензол, дает этиловые сложные эфиры фенил-[1,2,4]тиадиазол-5-карбоновой кислоты 2-С. Тиадиазоловый сложный эфир 2-С восстанавливают до соответствующего спирта 2-D, используя подходящий восстановитель, такой как боргидрид натрия, смешанный гидрид лития-алюминия или гидрид диизобутилалюминия. Этиловый сложный эфир феноксиуксусной кислоты 2-Е может быть получен в две стадии: (1) превращение спирта 2-D в мезилат в стандартных условиях с использованием метансульфонилхлорида и триэтиламина в подходящем растворителе, таком какCH2Cl2, или превращение спирта 2-D в бромид или хлорид в присутствии трифенилфосфина и тетрабромида углерода или тетрахлорида углерода, (2) алкилирование бензолтиола 1-D, полученного согласно схеме 1 выше, промежуточным соединением мезилатом, бромидом или хлоридом с использованием подходящего основания, такого как Cs2CO3, K2CO3 или NaH, в подходящем растворителе, таком как CH3CN,DMF или THF, в атмосфере азота. В качестве варианта синтез этиловых сложных эфиров феноксиуксусной кислоты 2-Е может быть осуществлен в одну стадию в стандартных условиях по Mitsunobu. Предпочтительные условия включают применение триарилфосфина, такого как трифенилфосфин, и азодикарбонильного реагента, такого как диэтилазодикарбоксилат, в подходящем растворителе, таком как THF. В стандартных условиях омыления этиловый сложный эфир феноксиуксусной кислоты 2-Е превращают в кислоту 2-F в атмосфере азота. Предпочтительные условия гидролиза включают применение NaOH в качестве основания в водно-спиртовой системе растворителей, такой как вода-метанол, или применениеLiOH в качестве основания в более мягкой системе вода-THF. Схема 3. Синтез соединения 2-F. В качестве варианта синтез [1,2,4]тиадиазолфеноксиуксусной кислоты 2-F может быть проведен,- 13009804 как показано на схеме 3, где R1, R2, R3, R4 R5 и R6 имеют указанные выше значения (за исключением того,что R5 и R6 не образуют спиро C3-6 циклоалкила или спиро 5- или 6-членного гетероциклила), путем инсталлирования боковой цепи замещенной уксусной кислоты на более поздней стадии синтеза. Соединение 3-В может быть получено в две стадии: (1) превращение спирта 2-D в мезилат в стандартных условиях с использованием метансульфонилхлорида и триэтиламина в подходящем растворителе, таком какCH2Cl2, (2) селективное алкилирование 4-меркаптофенола 3-А промежуточным соединением мезилатом с использованием подходящего основания, такого как Cs2CO3, K2CO3 или NaH, в подходящем растворителе, таком как CH3CN или THF, в атмосфере азота. В качестве варианта синтез соединения 3-В может быть осуществлен в одну стадию в стандартных условиях по Mitsunobu. Предпочтительные условия включают применение триарилфосфина, такого как трифенилфосфин, и азодикарбонильного реагента,такого как диэтилазодикарбоксилат, в подходящем растворителе, таком как THF. В присутствии подходящего основания, такого как Cs2CO3 или NaH, боковую цепь замещенной уксусной кислоты инсталлируют алкилированием фенолгруппы в 3-В с использованием подходящей замещенной галогенуксусной кислоты, такой как 2-бромизомасляная кислота, или сложного эфира галогенуксусной кислоты, такого как трет-бутил 2-бромизобутират, чтобы получить 3-С. Когда боковая цепь в 3-С представлена сложным эфиром уксусной кислоты, группа карбоновой кислоты может быть высвобождена путем использования обычных реакций, хорошо известных в области техники. Например, производное трет-бутилацетата 3-С превращают в кислоту 2-F, используя подходящую сильную кислоту, такую как трифторуксусная кислота, в подходящем растворителе, таком как дихлорметан. Схема 4. Синтез промежуточного соединения 4-F. Согласно схеме 4, где R1 и R2 имеют указанные выше в формуле (I) значения, метиловый сложный эфир 1-бромциклопентанкарбоновой кислоты 4-В получают бромированием циклопентанкарбоновой кислоты 4-А бромом в присутствии сильной кислоты, такой как хлорсульфоновая кислота, с последующим метилированием в метаноле при кипении с обратным холодильником. Алкилирование фенола 4-С метиловым сложным эфиром 1-бромциклопентанкарбоновой кислоты 4-В с использованием подходящего основания, такого как Cs2CO3, дает метиловый сложный эфир 1-феноксициклопентанкарбоновой кислоты 4-D. Ароматическое бромирование 4-D N-бромсукцинимидом в подходящем растворителе, таком как CH3CN, дает бромид 4-Е. Триизопропилсиланилсульфид 4-F получают при взаимодействии бромида 4-Е с триизопропилсилантиолом в присутствии подходящего основания, такого как NaH, и палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий. Схема 5. Синтез соединения 5-С. На схеме 5, где R1, R2, R3 и R4 имеют указанные в формуле (I) выше значения, спирт 2-D превращают в бромид 5-А в присутствии трифенилфосфина и тетрабромида углерода. Метиловый сложный эфир феноксициклопентанкарбоновой кислоты 5-В получают при взаимодействии бромида 5-А с триизопропилсиланилсульфидом 4-F, полученным согласно схеме 4 выше, с использованием подходящего основания, такого как Cs2CO3 или фторид тетрабутиламмония, в подходящем растворителе, таком как CH3CN,DMF или THF. В стандартных условиях омыления метиловый сложный эфир 5-В превращают в карбоновую кислоту 5-С в атмосфере азота. Предпочтительные условия гидролиза включают применение- 14009804 применение LiOH в качестве основания в более мягкой системе вода-THF. Схема 6. Синтез соединения 6-G. Согласно схеме 6, где R1, R2, R3, R4, R5 и R6 имеют указанные выше в формуле (I) значения, оксатиазолон 6-В получают при взаимодействии этилоксамата 6-А с хлоркарбонилсульфенилхлоридом в подходящем растворителе, таком как толуол. Термолиз оксатиазолона 6-В и улавливание образующегося нитрилсульфида бензонитрилом 6-С в подходящем растворителе с высокой точкой кипения, таком как хлорбензол или 1,2-дихлорбензол, дает этиловый сложный эфир фенил-[1,2,4]тиадиазол-3-карбоновой кислоты 6-D. Тиадиазол карбоновый сложный эфир 6-D восстанавливают до соответствующего спирта 6 Е, используя подходящий восстановитель, такой как боргидрид натрия, смешанный гидрид литияалюминия или гидрид диизобутилалюминия. Этиловый сложный эфир феноксиуксусной кислоты 6-F может быть получен в две стадии: (1) превращение спирта 6-Е в бромид или хлорид в присутствии трифенилфосфина и тетрабромида углерода или тетрахлорида углерода, (2) алкилирование бензолтиола 1-D,полученного согласно схеме 1 выше, промежуточным соединением бромидом или хлоридом с использованием подходящего основания, такого как Cs2CO3, K2CO3 или NaH, в подходящем растворителе, таком как CH3CN, DMF или THF, в атмосфере азота. В стандартных условиях омыления этиловый сложный эфир феноксиуксусной кислоты 6-F превращают в карбоновую кислоту 6-G. Предпочтительные условия гидролиза включают применение NaOH в качестве основания в водно-спиртовой системе растворителей, такой как вода-метанол-THF, или применение LiOH в качестве основания в более мягкой системе вода-THF. Схема 7. Синтез соединения 7-G. Согласно схеме 7, где R3 и R4 имеют указанные выше в формуле (I) значения, взаимодействие 7-А и 7-В дает 7-С, которое при окислении mCPBA дает 7-D. 7-D подвергают гидролизу, чтобы получить 7-Е. Обработка с соединениями, подобными D39, D44 и D34, ведет к 7-F, и дополнительный гидролиз дает соединения 7-G. Этиловый сложный эфир (4-хлорсульфонил-2-метилфенокси)уксусной кислоты. В колбу, содержащую хлорсульфоновую кислоту (15,0 мл, 226 ммоль), при 4 С медленно добавляют этил-(2-метилфенокси)ацетат A1a (10,0 г, 51,6 ммоль). Смесь перемешивают при 4 С в течение 30 мин и при комнатной температуре в течение 2 ч и затем выливают в воду со льдом. Осажденное белое твердое вещество фильтруют, промывают водой и сушат в вакууме в течение ночи, получая 14,0 г (93%) A1b в виде белого твердого вещества. 1 Н ЯМР (300 МГц, CDCl3)7,87-7,84 (м, 2 Н), 6,80 (д, J=9,5 Гц, 1 Н), 4,76 (с, 2 Н), 4,29 (кв, J=7,1 Гц,2 Н), 2,37 (с, 3H), 1,31 (т, J=7,1 Гц, 3H); МС (ES) m/z: 315 (M+Na+). Этиловый сложный эфир (4-меркапто-2-метилфенокси)уксусной кислоты. К раствору A1b (4,70 г, 16,1 ммоль) в EtOH (20 мл) добавляют 4,0 М HCl в диоксане (20 мл) с последующим добавлением порциями порошка олова с размером частиц 100 меш (9,80 г, 82,6 ммоль). Смесь кипятят с обратным холодильником в течение 2 ч, выливают в смесь CH2Cl2/лед (100 мл) и фильтруют. Фильтрат отделяют и водный слой экстрагируют CH2Cl2. Объединенные органические фазы промывают водой, сушат и концентрируют, получая 3,56 г (98%) A1c в виде желтого масла. 1 Н ЯМР (300 МГц, CDCl3)7,14-7,03 (м, 2 Н), 6,59 (д, J=8,4 Гц, 1 Н), 4,60 (с, 2 Н), 4,25 (кв, J=7,1 Гц,2 Н), 2,24 (с, 3H), 1,29 (т, J=7,1 Гц, 3H). Схема А 2- 16009804 5-(4-Трифторметилфенил)-[1,3,4]оксатиазол-2-он. Реакционную смесь 4-трифторметилбензамида А 2 а (2,57 г, 13,6 ммоль), хлоркарбонилсульфенилхлорида (3,57 г, 27,2 ммоль) в толуоле (35 мл) нагревают при 60 С в течение 15 ч и концентрируют. Добавляют CH2Cl2 и смесь фильтруют. Белое твердое вещество промывают CH2Cl2 и сушат в высоком вакууме, получая 922 мг (36%) 4-трифторметилбензамида А 2 а в качестве извлеченного исходного материала. Фильтрат концентрируют и подвергают колоночной хроматографии (EtOAc/гексан), получая 1,31 г Этиловый сложный эфир 3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-карбоновой кислоты. Реакционную смесь А 2b (448 мг, 1,81 ммоль) и этилцианоформиата (722 мг, 7,29 ммоль) в 1,2-дихлорбензоле (7 мл) нагревают при 160 С в течение 20 ч. После охлаждения до комнатной температуры реакционную смесь очищают колоночной хроматографией, получая 505 мг (92%) А 2 с в виде желтого твердого вещества. 1 Н ЯМР (300 МГц, CDCl3)8,50 (д, J=8,1 Гц, 2 Н), 7,76 (д, J=8,2 Гц, 2 Н), 4,57 (кв, J=7,1 Гц, 2 Н), 1,49[3-(4-Трифторметилфенил)-[1,2,4]тиадиазол-5-ил]метанол. К раствору А 2 с (200 мг, 0,662 ммоль) в EtOH (10 мл) при комнатной температуре добавляют NaBH4(64 мг, 1,7 ммоль). После перемешивания в течение 2 ч добавляют несколько капель воды, чтобы погасить избыток гидрида. EtOH выпаривают и остаток распределяют между CH2Cl2 и водой. Органическую фазу сушат и концентрируют, получая 167 мг (97%) A2d в виде не совсем белых кристаллов. 1 Н ЯМР (300 МГц, CDCl3)8,40 (д, J=8,1 Гц, 2 Н), 7,74 (д, J=8,2 Гц, 2 Н), 5,20 (с, 2 Н), 2,65 (ушир.с,1 Н); МС (ES) m/z: 261 (М+Н+). Этиловый сложный эфир 2-метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]феноксиуксусной кислоты. Смесь A2d (88 мг, 0,34 ммоль), метансульфонилхлорида (58 мг, 0,51 ммоль) и триэтиламина (70 мг,0,69 ммоль) в CH2Cl2 (3 мл) перемешивают при комнатной температуре в течение 1,5 ч. Смесь промывают водой и водную фазу подвергают обратной экстракции CH2Cl2. Объединенные органические слои сушат и концентрируют, получая 111 мг мезилата в виде желтого твердого вещества. Смесь сырого мезилата (111 мг) и этилового сложного эфира (4-меркапто-2-метилфенокси)уксусной кислоты A1c (111 мг, 0,491 ммоль) в CH3CN (4 мл) дегазируют в атмосфере N2 в течение около 15 мин. После добавления Cs2CO3 (214 мг, 0,656 ммоль) смесь перемешивают в течение ночи в атмосфере N2,концентрируют и очищают колоночной хроматографией (EtOAc/гексан), получая 102 мг (64%, 3 стадии) А 2 е в виде белого твердого вещества. 1 Н ЯМР (300 МГц, CDCl3)8,35 (д, J=8,1 Гц, 2 Н), 7,71 (д, J=8,2 Гц, 2 Н), 7,30 (д, J=1,7 Гц, 1 Н), 7,23- 17009804 атмосфере N2 в течение 30 мин и концентрируют. EtOAc и воду добавляют и смесь подкисляют концентрированной HCl. Органическую фазу отделяют и водную фазу экстрагируют EtOAc. Объединенные органические слои сушат и концентрируют, получая 70 мг (97%) целевого соединения, соединения 1, в виде не совсем белого твердого вещества. 1 Н ЯМР (300 МГц, МеОН-d4)8,37 (д, J=8,1 Гц, 2 Н), 7,78 (д, J=8,3 Гц, 2 Н), 7,28 (с, 1 Н), 7,26 (м, 1 Н),6,76 (д, J=8,3 Гц, 1 Н), 4,66 (с, 2 Н), 4,53 (с, 2 Н), 2,20 (с, 3H); МС (ES) m/z: 441 (М+Н+); FAB-HRMS (М+). Рассчитано 440,0476, найдено 440,0465. Пример 2.(518 мг, 4,52 ммоль) и триэтиламин (617 мг, 6,11 ммоль). Смесь перемешивают при комнатной температуре в течение 1 ч и затем распределяют между водой и CH2Cl2 (80 мл). Органический слой промывают насыщенным раствором соли, сушат, концентрируют и подвергают хроматографии на колонке(EtOAc/гексан), получая 859 мг (83%) мезилата в виде белого твердого вещества. Смесь мезилата (210 мг, 0,621 ммоль) и 4-меркаптофенола (113 мг, 0,897 ммоль) в CH3CN (8 мл) дегазируют в атмосфере N2 в течение около 10 мин. После добавления Cs2CO3 (242 мг, 0,742 ммоль) смесь перемешивают при комнатной температуре в течение 40 мин, концентрируют и очищают колоночной хроматографией (EtOAc/гексан), получая 228 мг (100%) В 1 в виде белого кристаллического твердого вещества. 1 Н ЯМР (300 МГц, CDCl3)8,35 (д, J=8,1 Гц, 2 Н), 7,71 (д, J=8,3 Гц, 2 Н), 7,36 (д, J=8,7 Гц, 2 Н), 6,78- 18009804 раствор В 1 (220 мг, 0,598 ммоль) в THF. К смеси при 40 С добавляют трет-бутил 2-бромизобутират (287 мг,1,29 ммоль). После нагревания при 70 С в течение 2 ч добавляют еще трет-бутил 2-бромизобутират (215 мг,0,970 ммоль) и нагревание продолжают в течение ночи. Смесь гасят водой (0,1 мл), концентрируют и подвергают хроматографии (EtOAc/гексан), получая 81 мг (27%) В 2. 1 Н ЯМР (300 МГц, CDCl3)8,35 (д, J=8,2 Гц, 2 Н), 7,71 (д, J=8,2 Гц, 2 Н), 7,34 (д, J=8,8 Гц, 2 Н), 6,78 2-Метил-2-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]феноксипропионовая кислота. Смесь В 2 (80 мг, 0,16 ммоль) в CH2Cl2 (1,5 мл) и трифторуксусной кислоты (0,5 мл) перемешивают при комнатной температуре в течение 1,5 ч, концентрируют и подвергают хроматографии на колонке дважды (EtOAc/гексан, CH2Cl2/МеОН), получая 40 мг (56%) целевого соединения, соединения 2, в виде светло-желтого твердого вещества. 1 Н ЯМР (300 МГц, CDCl3)8,34 (д, J=8,0 Гц, 2 Н), 7,71 (д, J=8,2 Гц, 2 Н), 7,37 (д, J=8,8 Гц, 2 Н), 6,87 2-Метил-4-[3-(4-трифторметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенол. Заменяя 4-меркаптофенол 4-меркапто-2-метилфенолом и следуя той же процедуре, как при получении В 1, получают С 1 (95%, белое кристаллическое твердое вещество). 1 Н ЯМР (300 МГц, CDCl3)8,35 (д, J=8,0 Гц, 2 Н), 7,71 (д, J=8,2 Гц, 2 Н), 7,26 (с, 1 Н), 7,20 (дд, J=8,0,2,1 Гц, 1 Н), 6,71 (д, J=8,2 Гц, 1 Н), 4,83 (с, 1 Н), 4,40 (с, 2 Н), 2,21 (с, 3H); МС (ES) m/z: 383 (М+Н+).- 19009804 пропионовая кислота. К раствору С 1 (39 мг, 0,10 ммоль) в THF (1 мл) добавляют NaH (20 мг, 0,50 ммоль; 60% в минеральном масле) и смесь нагревают при 60 С в течение 30 мин, в это время цвет раствора изменяется до синего, затем до коричневого. 2-Бромизомасляную кислоту (34 мг, 0,20 ммоль) добавляют и смесь нагревают при той же температуре в течение 1 ч, подкисляют 1 н. HCl и разбавляют CH2Cl2. Органическую фазу отделяют, промывают насыщенным раствором соли, сушат, концентрируют и подвергают хроматографии на колонке (EtOAc/гексан), изолируя 10 мг (21%) целевого соединения, соединения 3, в виде желтого масла. 1 Н ЯМР (300 МГц, CDCl3)8,35 (д, J=8,0 Гц, 2 Н), 7,71 (д, J=8,2 Гц, 2 Н), 7,28 (м, 1 Н), 7,18 (дд, J=8,4,2,4 Гц, 1 Н), 6,72 (д, J=8,5 Гц, 1 Н), 4,43 (с, 2 Н), 2,20 (с, 3H), 1,61 (с, 6 Н); МС (ES) m/z: 469 (М+Н+). Анал. рассч. для C21H19F3N2O3S2, 0,30 H2O: С, 53,22; Н, 4,17; N, 5,91. Найдено: С, 53,36; Н, 3,88; N, 5,62. Пример 4. Этиловый сложный эфир 2-метил-2-о-толилоксипропионовой кислоты. К смеси этилового сложного эфира 2-бром-2-метилпропионовой кислоты (8,27 мл, 64,0 ммоль) и 2 метилфенола (7,60 г, 70,2 ммоль) в диоксане (100 мл) добавляют Cs2CO3 (31,3 г, 96,0 ммоль). Затем смесь кипятят с обратным холодильником при 100 С в течение 4 ч и позволяют остыть до комнатной температуры, растворитель выпаривают при пониженном давлении. Остаток растворяют в Et2O, промывают 1 н. Этиловый сложный эфир 2-(4-хлорсульфонил-2-метилфенокси)-2-метилпропионовой кислоты. В колбу, содержащую D1a (11,3 г, 0,0510 моль), при 0 С медленно добавляют ClSO3H (15,2 мл,0,229 моль). Температуре позволяют подняться до комнатной температуры и раствор перемешивают в течение 1 ч. После перемешивания реакционную смесь выливают в лед. Твердое вещество фильтруют,промывают водой и сушат в вакууме, получая 7,7 г (47%) D1b. 1 Н ЯМР (300 МГц, CDCl3)7,82 (д, J=2,5 Гц, 1 Н), 7,75 (дд, J=8,9, 2,5 Гц, 1 Н), 6,67 (д, J=8,8 Гц, 1 Н),4,23 (кв, J=7,1 Гц, 2 Н), 2,31 (с, 3H), 1,70 (с, 6 Н), 1,22 (т, J=7,1 Гц); МС (ES) m/z: 343 (M+Na+). Этиловый сложный эфир 2-(4-меркапто-2-метилфенокси)-2-метилпропионовой кислоты. К раствору D1b (2,00 г, 6,25 ммоль) в EtOH (7,8 мл) добавляют HCl в диоксане (4,0 М, 7,8 мл, 31 ммоль) и порошок олова (3,70 г, 31,2 ммоль). Смесь кипятят с обратным холодильником в течение 3 ч, выливают в лед и экстрагируют CH2Cl2 (50 мл 3). Органические слои объединяют и сушат над Na2SO4. После фильтрования фильтрат концентрируют, получая 3,37 г (100%) D1c. 1 Н ЯМР (300 МГц, CDCl3)7,12 (д, J=2,0 Гц, 1 Н), 7,00 (дд, J=8,4, 2,4 Гц, 1 Н), 6,56 (д, J=8,4 Гц, 1 Н),4,23 (кв, J=7,1 Гц, 2 Н), 3,31 (с, 1 Н), 2,18 (с, 3H), 1,57 (с, 6 Н), 1,25 (т, J=7,1 Гц); МС (ES) m/z: 255 (М+Н+). Схема D2 Этиловый сложный эфир 3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-карбоновой кислоты. Следуя той же процедуре, как при получении А 2 с, получают D2b (белое твердое вещество, 97%). 1 Н ЯМР (300 МГц, CDCl3)8,42 (м, 2 Н), 7,33 (дд, J=8,9, 0,8 Гц, 2 Н), 4,56 (кв, J=7,1 Гц, 2 Н), 1,49 (т,J=7,1 Гц, 3H).[3-(4-Трифторметоксифенил)-[1,2,4]тиадиазол-5-ил]метанол. Следуя той же процедуре, как при получении A2d, получают D2c (белое твердое вещество, 70%). 1 Н ЯМР (300 МГц, CDCl3)8,32 (м, 2 Н), 7,31 (д, J=8,1 Гц, 2 Н), 5,17 (д, J=5,8 Гц, 2 Н), 1,26 (т, J=7,1 Гц,1 Н); МС (ES) m/z: 277 (М+Н+). 5-Бромметил-3-(4-трифторметоксифенил)-[1,2,4]тиадиазол. К раствору D2c (679 мг, 2,46 ммоль) в CH2Cl2 (10 мл) добавляют тетрабромид углерода (896 мг,- 21009804 2,70 ммоль) и трифенилфосфин (707 мг, 2,70 ммоль). Смесь перемешивают при 0 С в течение 1 ч и при комнатной температуре в течение 1 ч, концентрируют и очищают колоночной хроматографией, получая 678 мг (81%) D2d в виде белого твердого вещества. 1 Н ЯМР (300 МГц, CDCl3)8,32 (м, 2 Н), 7,31 (дд, J=8,9, 0,8 Гц, 2 Н), 4,82 (с, 2 Н); МС (ES) m/z: 339 Этиловый сложный эфир 2-метил-2-2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]феноксипропионовой кислоты. К смеси D2d (73 мг, 0,22 ммоль) и этилового сложного эфира 2-(4-меркапто-2-метилфенокси)-2 метилпропионовой кислоты D1c (52 мг, 0,21 ммоль) в CH3CN (1,5 мл) и DMF (0,1 мл) добавляют Cs2CO3(100 мг, 0,31 ммоль). После перемешивания при комнатной температуре в течение 15 мин смесь концентрируют. Остаток разбавляют EtOAc, промывают водой и насыщенным раствором соли, сушат, концентрируют и подвергают хроматографии на колонке, получая 82 мг (78%) D2e. 1 Н ЯМР (300 МГц, CDCl3)8,27 (д, J=8,9 Гц, 2 Н), 7,29 (дд, J=8,9, 0,9 Гц, 1 Н), 7,26 (м, 2 Н), 7,13 (дд,J=8,5, 2,4 Гц, 1 Н), 6,56 (д, J=8,5 Гц, 1 Н), 4,40 (с, 2 Н), 4,20 (кв, J=7,1 Гц, 2 Н), 2,18 (с, 3H), 1,58 (с, 6 Н), 1,20 2-Метил-2-2-метил-4-[3-(4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]фенокси пропионовая кислота. Раствор D2e (80 мг, 0,16 ммоль) в МеОН (1,0 мл) и THF (1,0 мл) обрабатывают 2 н. NaOH (1,0 мл,2,0 ммоль) в течение 4 ч и концентрируют. Остаток разбавляют EtOAc и водой и подкисляют концентрированной HCl. Органический слой отделяют и водный слой экстрагируют EtOAc. Объединенные органические фазы промывают насыщенным раствором соли, сушат, концентрируют и подвергают колоночной хроматографии, получая 71 мг (95%) соединения 4. 1 Н ЯМР (300 МГц, CDCl3)8,27 (д, J=8,8 Гц, 2 Н), 7,30-7,23 (м, 3H), 7,17 (д, J=8,4 Гц, 1 Н), 6,72 (д,J=8,4 Гц, 1 Н), 4,42 (с, 2 Н), 2,20 (с, 3H), 1,60 (с, 6 Н); МС (ES) m/z: 507 (M+Na+). Анал. рассч. для 5-п-Толил-[1,3,4]оксатиазол-2-он. Следуя той же процедуре, как при получении А 2b, получают D1. 1 Н ЯМР (300 МГц, CDCl3)7,86 (д, J=8,0 Гц, 2 Н), 7,29 (д, J=8,0 Гц, 2 Н), 2,43 (с, 3H). Этиловый сложный эфир 3-п-толил-[1,2,4]тиадиазол-5-карбоновой кислоты. Следуя той же процедуре, как при получении А 2 с, получают D2. 1 Н ЯМР (400 МГц, CDCl3)8,25 (д, J=8,2 Гц, 2 Н), 7,30 (д, J=8,0 Гц, 2 Н), 4,55 (кв, J=7,1 Гц, 2 Н), 2,42(3-п-Толил-[1,2,4]тиадиазол-5-ил)метанол. Следуя той же процедуре, как при получении A2d, получают D3. 1 Н ЯМР (300 МГц, CDCl3)8,16 (д, J=8,2 Гц, 2 Н), 7,28 (д, J=8,0 Гц, 2 Н), 5,16 (с, 2 Н), 2,69 (ушир.с,1 Н), 2,41 (с, 3H); МС (ES) m/z: 207 (М+Н+). 5-Бромметил-3-п-толил-[1,2,4]тиадиазол. Следуя той же процедуре, как при получении D2d, получают D4. 1 Н ЯМР (300 МГц, CDCl3)8,16 (д, J=8,2 Гц, 2 Н), 7,28 (д, J=8,1 Гц, 2 Н), 4,82 (с, 2 Н), 2,42 (с, 3H); МС (ES) m/z: 271 (М+Н+). Этиловый сложный эфир 2-метил-2-[2-метил-4-(3-п-толил-[1,2,4]тиадиазол-5-илметилсульфанил) фенокси]пропионовой кислоты. Следуя той же процедуре, как при получении D2e, получают D5. 1 Н ЯМР (300 МГц, CDCl3)8,12 (д, J=8,2 Гц, 2 Н), 7,27-7,24 (м, 3H), 7,14 (дд, J=8,5, 2,3 Гц, 1 Н), 6,56 2-Метил-2-[2-метил-4-(3-п-толил-[1,2,4]тиадиазол-5-илметилсульфанил)фенокси]пропионовая кислота. Следуя той же процедуре, как при получении соединения 4, получают соединение 5. 1 Н ЯМР (300 МГц, CDCl3)8,11 (д, J=8,2 Гц, 2 Н), 7,28-7,24 (м, 3H), 7,17 (дд, J=8,4, 2,2 Гц, 1 Н), 6,71 Этиловый сложный эфир 3-(4-трет-бутилфенил)-[1,2,4]тиадиазол-5-карбоновой кислоты. Этиловый сложный эфир 2-4-[3-(4-трет-бутилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовой кислоты. Этиловый сложный эфир 3-(4-хлорфенил)-[1,2,4]тиадиазол-5-карбоновой кислоты.D13 (не совсем белое твердое вещество, 87%). 1 Н ЯМР (300 МГц, CDCl3)8,22 (м, 2 Н), 7,45 (м, 2 Н), 5,17 (с, 2 Н); МС (ES) m/z: 227 (М+Н+). Этиловый сложный эфир 2-4-[3-(4-хлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовой кислоты. Этиловый сложный эфир 3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-карбоновой кислоты. Этиловый сложный эфир 2-4-[3-(3-хлор-4-трифторметоксифенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовой кислоты.D21 (не совсем белое твердое вещество, 94%). 1 Н ЯМР (300 МГц, CDCl3)8,07 (д, J=2,0 Гц, 1 Н), 7,80 (дд, J=8,4, 2,0 Гц, 1 Н), 7,58 (д, J=8,4 Гц, 1 Н). Этиловый сложный эфир 3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-карбоновой кислоты. Этиловый сложный эфир 2-4-[3-(3,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовой кислоты.D26 (не совсем белое твердое вещество, 54%). 1 Н ЯМР (300 МГц, CDCl3)7,81 (д, J=8,5 Гц, 1 Н), 7,56 (д, J=2,1 Гц, 1 Н), 7,39 (м, 1 Н). Этиловый сложный эфир 3-(2,4-дихлорфенил)-[1,2,4]тиадиазол-5-карбоновой кислоты. Этиловый сложный эфир 2-4-[3-(2,4-дихлорфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовой кислоты.- 28009804 Этиловый сложный эфир 3-(3,4-диметилфенил)-[1,2,4]тиадиазол-5-карбоновой кислоты. Этиловый сложный эфир 2-4-[3-(3,4-диметилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2-метилфенокси-2-метилпропионовой кислоты.- 29009804 Этиловый сложный эфир 3-(3-хлор-4-метилфенил)-[1,2,4]тиадиазол-5-карбоновой кислоты. Этиловый сложный эфир 2-4-[3-(3-хлор-4-метилфенил)-[1,2,4]тиадиазол-5-илметилсульфанил]-2 метилфенокси-2-метилпропионовой кислоты.D41 (не совсем белое твердое вещество, 96%). 1 Н ЯМР (400 МГц, CDCl3)7,87 (д, J=8,2 Гц, 1 Н), 7, 83 (д, J=10,6 Гц, 1 Н), 7,77 (м, 1 Н).
МПК / Метки
МПК: A61K 31/433, C07D 285/08, A61P 31/10
Метки: производные, рецептора, качестве, пролифератором, кислот, феноксиуксусных, применимые, агонистов, активируемого, двойных, пероксисомным
Код ссылки
<a href="https://eas.patents.su/30-9804-proizvodnye-fenoksiuksusnyh-kislot-primenimye-v-kachestve-dvojjnyh-agonistov-aktiviruemogo-peroksisomnym-proliferatorom-receptora-ppar.html" rel="bookmark" title="База патентов Евразийского Союза">Производные феноксиуксусных кислот, применимые в качестве двойных агонистов активируемого пероксисомным пролифератором рецептора ( ppar )</a>
Предыдущий патент: Система для маркировки и взятия проб биологического объекта
Следующий патент: Способ получения стабильного при хранении экстракта из листьев плюща, а также полученный этим способом экстракт
Случайный патент: Износостойкий узел












