Соединение бициклического циннамида
Номер патента: 14427
Опубликовано: 30.12.2010
Авторы: Кавано Коки, Миягава Такехико, Китазава Норитака, Такаиси Мамору, Кимура Тейдзи, Канеко Тосихико, Дои Эрико, Хагивара Хироаки, Сасаки Такео, Йосида Ю., Ито Коити
Формула / Реферат
1. Соединение, представленное формулой (I)
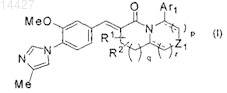
или его фармацевтически приемлемая соль,
где ![]() является одинарной связью или двойной связью; Ar1 является фенильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей А1, или пиридинильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей A1; R1 и R2 являются одинаковыми или разными и, каждый, являются группой, выбранной из группы заместителей А1; Z1 является метиленовой группой или виниленовой группой, которые могут быть замещены от 1 до 2 заместителями, выбранными из группы заместителей А1, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы заместителей А1; и р, q и r являются одинаковыми или разными и равны целому числу от 0 до 2;
является одинарной связью или двойной связью; Ar1 является фенильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей А1, или пиридинильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей A1; R1 и R2 являются одинаковыми или разными и, каждый, являются группой, выбранной из группы заместителей А1; Z1 является метиленовой группой или виниленовой группой, которые могут быть замещены от 1 до 2 заместителями, выбранными из группы заместителей А1, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы заместителей А1; и р, q и r являются одинаковыми или разными и равны целому числу от 0 до 2;
группа заместителей А1: (1) атом галогена, (2) гидроксильная группа, (3) цианогруппа, (4) С3-8 циклоалкильная группа, (5) С3-8 циклоалкоксигруппа, (6) С1-6 алкильная группа, где С1-6 алкильная группа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С3-8 циклоалкильную группу, С1-6 алкоксигруппу и С3-8 циклоалкоксигруппу, (7) С1-6 алкоксигруппа, где С1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С3-8 циклоалкильную группу и С3-8 циклоалкоксигруппу, (8) аминогруппа, которая может быть замещена одной или двумя С1-6 алкильными группами, где С1-6 алкильные группы могут быть замещены от 1 до 3 атомами галогена, (9) карбамоильная группа, которая может быть замещена одной или двумя С1-6 алкильными группами, где С1-6 алкильные группы могут быть замещены от 1 до 3 атомами галогена, (10) карбоксильная группа, (11) С1-6 алкоксикарбонильная группа, где С1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С3-8 циклоалкильную группу и С3-8 циклоалкоксигруппу, (12) С1-6 алкильная группа, (13) С1-6 алкилсульфонильная группа и (14) водород;
при условии, что соединение, где Z1 является метиленовой группой, Ar1 является фенильной группой, которая замещена одним атомом галогена, R1и R2, каждый, являются водородом, р и q, каждый, равен целому числу 1, r равен 0, и его фармацевтически приемлемые соли исключаются, и при условии, что когда q равно 0, тогда только один из R1и R2 может присутствовать в кольцевом фрагменте.
2. Соединение или его фармацевтически приемлемая соль по п.1, где соединение представлено формулой (II)
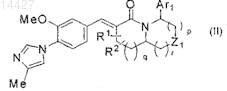
где Ar1является фенильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей А1, или пиридинильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей A1; R1 и R2 являются одинаковыми или разными и каждый является группой, выбранной из группы заместителей А1; Z1является метиленовой группой или виниленовой группой, которые могут быть замещены от 1 до 2 заместителями, выбранными из группы заместителей А1, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы заместителей А1; и р, q и r являются одинаковыми или разными и равны целому числу от 0 до 2;
группа заместителей А1: (1) атом галогена, (2) гидроксильная группа, (3) цианогруппа, (4) С3-8 циклоалкильная группа, (5) С3-8 циклоалкоксигруппа, (6) С1-6 алкильная группа, где С1-6 алкильная группа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С3-8 циклоалкильную группу, С1-6 алкоксигруппу и С3-8 циклоалкоксигруппу, (7) С1-6 алкоксигруппа, где С1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С3-8 циклоалкильную группу и С3-8 циклоалкоксигруппу, (8) аминогруппа, которая может быть замещена одной или двумя С1-6 алкильными группами, где С1-6 алкильные группы могут быть замещены от 1 до 3 атомами галогена, (9) карбамоильная группа, которая может быть замещена одной или двумя С1-6 алкильными группами, где С1-6 алкильные группы могут быть замещены от 1 до 3 атомами галогена, (10) карбоксильная группа, (11) С1-6 алкоксикарбонильная группа, где С1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С3-8 циклоалкильную группу и С3-8 циклоалкоксигруппу, (12) С1-6 алкильная группа, (13) С1-6 алкилсульфонильная группа и (14) водород.
3. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей C1-6 алкильную группу, гидроксильную группу и атом галогена.
4. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является метиленовой группой, которая может быть замещена 1 или 2 атомами галогена.
5. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу, гидроксильную группу и атом галогена; и р, q и r, каждый, равены 1.
6. Соединение или его фармацевтически приемлемая соль по п.5, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу и гидроксильную группу; и р, q и r, каждый, равны 1.
7. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу, гидроксильную группу и атом галогена; р и q, каждый, равны 1 и r равен 0.
8. Соединение или его фармацевтически приемлемая соль по п.7, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей
С1-6 алкильную группу и гидроксильную группу; р и q, каждый, равны 1 и r равен 0.
9. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является атомом кислорода и р, q и r, каждый, равны 1.
10. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу, атом галогена и гидроксильную группу; р равен 1 и q и r, каждый, равны 0.
11. Соединение или его фармацевтически приемлемая соль по п.10, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу и гидроксильную группу; р равен 1; и q и r, каждый, равны 0.
12. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу, атом галогена и гидроксильную группу; p и r, каждый, равны 1 и q равен 0.
13. Соединение или его фармацевтически приемлемая соль по п.12, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу и гидроксильную группу; p и r, каждый, равны 1; и q равен 0.
14. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу, атом галогена и гидроксильную группу; р равен 1; q равен 2 и r равен 0.
15. Соединение или его фармацевтически приемлемая соль по п.14, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу и гидроксильную группу; р равен 1; q равен 2 и r равен 0.
16. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу, атом галогена и гидроксильную группу; p и r, каждый, равны 1 и q равен 2.
17. Соединение или его фармацевтически приемлемая соль по п.16, где Z1является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С1-6 алкильную группу и гидроксильную группу; p и r, каждый, равны 1 и q равен 2.
18. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является виниленовой группой, где виниленовая группа может быть замещена одной или двумя С1-6 алкильными группами или атомами галогена; р равен 0 и q и r, каждый, равны 1.
19. Соединение или его фармацевтически приемлемая соль по п.18, где Z1является виниленовой группой, где виниленовая группа может быть замещена одной или двумя С1-6 алкильными группами; р равен 0 и q и r, каждый, равны 1.
20. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Z1является виниленовой группой, где виниленовая группа может быть замещена одной или двумя С1-6 алкильными группами или атомами галогена; р и q, каждый, равны 1 и r равен 0.
21. Соединение или его фармацевтически приемлемая соль по п.20, где Z1является виниленовой группой, где виниленовая группа может быть замещена одной или двумя С1-6 алкильными группами; р и q, каждый равны 1 и r равен 0.
22. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Ar1 является фенильной группой, замещенной от 1 до 3 атомами галогена.
23. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где Ar1является фенильной группой, замещенной от 1 до 3 атомами фтора или атомами хлора.
24. Соединение или его фармацевтически приемлемая соль по п.7 или 8, где Ar1является фенильной группой, замещенной 2 или 3 атомами галогена.
25. Соединение или его фармацевтически приемлемая соль по любому из пп.2, 22, 23 и 24, где Ar1 является фенильной группой, замещенной атомом фтора.
26. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где R1и R2 являются одинаковыми или разными и каждый является заместителем, выбранным из группы, включающей С1-6 алкильную группу, атом галогена, гидроксильную группу и водород.
27. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где соединение выбирают из следующей группы:
1) (E)-(3S)-(3,4,5-трифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(9R)-гексагидроиндолизин-5-он,
2) (E)-(3R)-(3,4,5-трифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(9R)-гексагидроиндолизин-5-он,
3) (E)-(3S)-(3,4,5-трифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(9S)-гексагидроиндолизин-5-он,
4) (Е)-(3R)-(3,4,5-трифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(9S)-гексагидроиндолизин-5-он,
5) (Е)-(3R)-(3,4-дифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(9R)-гексагидроиндолизин-5-он,
6) (E)-(3S)-(3,4-дифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(9S)-гексагидроиндолизин-5-он,
7) (Е)-(6R,9aS)-6-(4-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден)октагидрохинолизин-4-он,
8) (Е)-(6S,9aR)-6-(4-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
9) (Е)-(6S,8S,9aR)-6-фенил-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
10) (Е)-(6R,8R,9aS)-6-фенил-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
11) (Е)-(6S,8S,9aR)-6-(4-фторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
12) (Е)-(6R,8R,9aS)-6-(4-фторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
13) (Е)-(6S,9aS)-6-(3,4,5-трифторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
14) (Е)-(6R,9aR)-6-(3,4,5-трифторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
15) (Е)-(6S,8S,9aR)-6-(3,4,5-трифторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
16) (Е)-(6R,8R,9aS)-6-(3,4,5-трифторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
17) (Е)-(6S,8R,9aR)-6-(3,4,5-трифторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
18) (Е)-(6R,8S,9aS)-6-(3,4,5-трифторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
19) (Е)-(6S,9aS)-6-(4-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
20) (Е)-(6R,9aR)-6-(4-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
21) (Е)-(5S)-(4-фторфенил)-2-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(8aS)-гексагидроиндолизин-3-он,
22) (Е)-(5R)-(4-фторфенил)-2-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(8aR)-гексагидроиндолизин-3-он,
23) (Е)-(5S)-(3,4-дифторфенил)-2-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(8aS)-гексагидроиндолизин-3-он,
24) (Е)-(5R)-(3,4-дифторфенил)-2-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(8aR)-гексагидроиндолизин-3-он,
25) (Z)-(5S)-(3,4-дифторфенил)-2-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(8aS)-гексагидро-индолизин-3-он,
26) (Z)-(5R)-(3,4-дифторфенил)-2-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-(8aR)-гексагидроиндолизин-3-он,
27) (Е)-(5R,8aS)-5-(4-фторфенил)-2-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидроиндолизин-3-он,
28) (Е)-(5S,8aR)-5-(4-фторфенил)-2-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидроиндолизин-3-он,
29) (Е)-(6R,9aS)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(4-метоксифенил)октагидрохинолизин-4-он,
30) (Е)-(6S,9aR)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(4-метоксифенил)октагидрохинолизин-4-он,
31) (Е)-(4S,10aS)-4-(4-фторфенил)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидропиридо[1,2-а]азепин-6-он,
32) (Е)-(4R,10aR)-4-(4-фторфенил)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидропиридо[1,2-а]азепин-6-он,
33) (Е)-(5R,7aS)-5-(3,4-дифторфенил)-2-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидропирролидин-3-он,
34) (Е)-(3R,9aR)-3-(3,4-дифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидропирроло[1,2-а]азепин-5-он,
35) метил (Е)-4-{(4S*,9aR*)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-оксооктагидрохинолизин-4-ил}бензоат,
36) (Е)-(6S*,9aR*)-6-(4-гидроксиметилфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
37) (Е)-(6S*,9aR*)-6-(4-цианофенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
38) (Е)-4-{(4S*,9aR*)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-оксооктагидрохинолизин-4-ил}бензойная кислота,
39) (Е)-(6S*,9aR*)-6-(4-аминофенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
40) (Е)-4-{(4S*,9aR*)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-оксооктагидрохинолизин-4-ил}-N,N-диметилбензамид,
41) (Е)-(6S,9aR)-6-(3-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
42) (E)-(6R,9aS)-6-(3-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
43) (Е)-(6S,9aR)-6-(2-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
44) (Е)-(6R,9aS)-6-(2-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
45) (Е)-(6S,8R,9aR)-6-(4-фторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-8-метилоктагидрохинолизин-4-он,
46) (Е)-(6R,8S,9aS)-6-(4-фторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-8-метилоктагидрохинолизин-4-он,
47) (Е)-(6S,8R,9aR)-6-(4-фторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-8-метилоктагидрохинолизин-4-он,
48) (Е)-(6R,8S,9aS)-6-(4-фторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-8-метилоктагидрохинолизин-4-он,
49) (Е)-(6S,9aR)-6-(4-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-8-метил-1,2,3,6, 9,9а-гексагидрохинолизин-4-он,
50) (Е)-(6R,9aS)-6-(4-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-8-метил-1,2,3,6,9, 9а-гексагидрохинолизин-4-он,
51) (Е)-(6S,8S,9aR)-6-(4-фторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-8-метилоктагидрохинолизин-4-он,
52) (Е)-(6R,8R,9aS)-6-(4-фторфенил)-8-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-8-метилоктагидрохинолизин-4-он,
53) (E)-(4R,9aS)-7-[3-метокси-4-(4-метилимидазол-1-ил)бензилиден]-4-фенилгексагидропиридо[2,1-c][1,4] оксазин-6-он,
54) (Е)-(5S,7aR)-5-(3,4-дифторфенил)-2-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидропирролидин-3-он,
55) (Е)-(3S,9aS)-3-(3,4-дифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидропирроло[1,2-а]азепин-5-он,
56) (Е)-(3S,8aS)-3-(4-хлорфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидроиндолизин-5-он,
57) (Е)-(3S,8aS)-3-(2,4,5-трифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидроиндолизин-5-он,
58) (Е)-(3S,8aS)-3-(2,3,4-трифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидроиндолизин-5-он,
59) (Е)-(3S,8aS)-3-(2,5-дифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидроиндолизин-5-он,
61) (E)-(3S,8aS)-3-(2,6-дифторпиридин-3-ил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидроиндолизин-5-он,
62) (Е)-(3S,8aS)-3-(2,4-дифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидроиндолизин-5-он,
64) (Е)-(3S,8aS)-3-(3,5-дифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидроиндолизин-5-он,
65) (Е)-(6S,9aS)-6-(3,4-дифторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
66) (Е)-(6R,9aR)-6-(3,4-дифторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
67) (E)-(6S,9aS)-6-(4-хлорфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
68). (E)-(6R,9aR)-6-(4-хлорфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]октагидрохинолизин-4-он,
69) (Е)-(S)-6-(3,4,5-трифторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-1,2,3,8,9,9а-гексагидрохинолизин-4-он,
70) (Е)-(R)-6-(3,4,5-трифторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-1,2,3,8,9,9а-гексагидрохинолизин-4-он,
71) (Е)-(6S,8S,9aR)-8-фтор-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил) октагидрохинолизин-4-он,
72) (Е)-(6S,8R,9aR)-8-метокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)октагидрохинолизин-4-он,
73) (Е)-(R)-4-(4-фторфенил)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-3,4,8,9-тетрагидро-7Н-пиридо[2,1-с][1,4]оксазин-6-он,
74) (Е)-(S)-4-(4-фторфенил)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-3,4,8,9-тетрагидро-7H-пиридо[2,1-с][1,4]оксазин-6-он,
75) (Е)-(4R,9aR)-4-(4-фторфенил)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидропиридо [2,1-с][1,4]оксазин-6-он,
76) (Е)-(4S,9aS)-4-(4-фторфенил)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-с][1,4]оксазин-6-он,
77) (Е)-(6S,8R,9aR)-8-фтор-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил) октагидрохинолизин-4-он,
78) (Е)-(6S,9aR)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)-1,2,3,6,9, 9а-гексагидрохинолизин-4-он,
79) (Е)-(6S,9aR)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)-1,2,3,6,7, 9а-гексагидрохинолизин-4-он,
80) (Е)-(4R,9aR)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-4-(3,4,5-трифторфенил)гексагидропиридо[2,1-с][1,4]оксазин-6-он,
81) (Е)-(4S,9aS)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-4-(3,4,5-трифторфенил)гексагидропиридо[2,1-с][1,4]оксазин-6-он,
82) (Е)-(4S,9aR)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-4-(3,4,5-трифторфенил)гексагидропиридо[2,1-с][1,4]оксазин-6-он,
83) (Е)-(4R,9aS)-7-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-4-(3,4,5-трифторфенил)гексагидропиридо[2,1-с][1,4]оксазин-6-он,
84) (Е)-(6R,7S,9aR)-7-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)октагидрохинолизин-4-он,
85) (Е)-(6S,7R,9aS)-7-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)октагидрохинолизин-4-он,
86) (Е)-(6R,7R,9aR)-7-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)октагидрохинолизин-4-он,
87) (Е)-(6S,7S,9aS)-7-гидрокси-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)октагидрохинолизин-4-он,
88) (Е)-(6S,9aR)-6-(4-фторфенил)-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-1,2,3,6,9,9а-гексагидрохинолизин-4-он,
89) (3S,8aS)-6-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-3-(2,4,6-трифторфенил) гексагидроиндолизин-5-он,
90) (6S,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден} октагидрохинолизин-4-он,
91) (6S,9aR)-6-(3,4,5-трифторфенил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден} октагидрохинолизин-4-он,
92) (6S,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}октагидрохинолизин-4-он,
93) (Е)-(3S,8aS)-3-(2,3-дифторфенил)-6-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]гексагидроиндолизин-5-он,
94) (4R,9aS)-4-(4-фторфенил)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}гексагидропиридо[2,1-с][1,4]оксазин-6-он,
95) (4R,9aS)-4-(3,4-дифторфенил)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден} гексагидропиридо[2,1-c][1,4]оксазин-6-он,
96) (4R,9aS)-4-(4-хлорфенил)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}гексагидропиридо[2,1-с][1,4]оксазин-6-он,
97) метил (4S,9aR)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-6-оксо-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-2-карбоксилат,
98) метил (4R,9aS)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-6-оксо-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-2-карбоксилат,
99) метил (4R,9aR)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-6-оксо-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-2-карбоксилат,
100) метил (4S,9aS)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-6-оксо-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-2-карбоксилат,
101) (4R,9aS)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-4-(3,4,5-трифторфенил) октагидропиридо[1,2-а]пиразин-6-он,
102) (4S,9aR)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-4-(3,4,5-трифторфенил) октагидропиридо[1,2-а]пиразин-6-он,
103) (4S,9aS)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-4-(3,4,5-трифторфенил) октагидропиридо[1,2-а]пиразин-6-он,
104) (4R,9aR)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-4-(3,4,5-трифторфенил) октагидропиридо[1,2-а]пиразин-6-он,
105) (4S,9aR)-2-этил-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,
106) (4R,9aS)-2-этил-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,
107) (4R,9aR)-2-этил-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,
108) (4S,9aS)-2-этил-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,
109) (4S,9aR)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-2-метил-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,
110) (4R,9aS)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-2-метил-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,
111) (4S,9aR)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-2-пропил-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,
112) (4R,9aS)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-2-пропил-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,
113) (4R*,9aS*)-2-ацетил-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,
114) (4R*,9aS*)-2-метансульфонил-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он и
115) диметиламид (4R*,9aS*)-7-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}-6-оксо-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-2-карбоновой кислоты.
28. Лекарственное средство, содержащее соединение или его фармацевтически приемлемую соль по любому из пп.1-27 в качестве активного ингредиента.
29. Лекарственное средство по п.28, которое является профилактическим или терапевтическим агентом для заболевания, вызываемого амилоидом-b.
30. Лекарственное средство по п.29, где заболеванием, вызываемым амилоидом-b, является болезнь Альцгеймера, старческое слабоумие, синдром Дауна или амилоидоз.
Текст
Бициклическое соединение циннамида, представленное общей формулой (I) является одинарной или двойной связью; Ar1 является фенильной группой или пиригде динильной группой, необязательно замещенной от одного до трех заместителей; R1 и R2, каждый,являются С 1-6 алкильной группой, гидроксильной группой и т.д.; Z1 является необязательно замещенной метиленовой группой или виниленовой группой, атомом кислорода или иминогруппой, необязательно замещенной С 1-6 алкильной группой или С 1-6 ацильной группой; и р, q и r,каждый, равны целому числу от 0 до 2. Соединение действует на снижение А 40 и А 42. Поэтому соединение особенно полезно в качестве профилактического или лекарственного средства для нейродегенеративных заболеваний, причиной которых является А, таких как болезнь Альцгеймера или синдром Дауна.(71)(73) Заявитель и патентовладелец: ЭЙСАЙ Ар ЭНД Ди МЕНЕДЖМЕНТ КО.,ЛТД. (JP) 014427 Область техники Данное изобретение относится к соединению бициклического циннамида и к фармацевтическому агенту, содержащему соединение в качестве активного ингредиента. Более конкретно, данное изобретение относится к непептидному соединению бициклического циннамида и к ингибитору вырабатывания амилоида- (далее обозначен как А), который содержит соединение в качестве активного ингредиента и является особенно эффективным для лечения нейродегенеративного заболевания, вызванного А, такого как болезнь Альцгеймера или синдром Дауна. Уровень техники Болезнь Альцгеймера представляет собой заболевание, характеризуемое дегенерацией и потерей нейронов, а также образованием старческих бляшек и нейрофибриллярной дегенерацией. В настоящее время болезнь Альцгеймера лечат только симптоматическим лечением с применением агента, улучшающего симптомы, типичным представителем которого является ингибитор ацетилхолинестеразы, и фундаментальное лекарство для ингибирования прогресса заболевания до сих пор не разработано. Необходимо разработать способ контроля причины наступления патологии для создания фундаментального лекарства для болезни Альцгеймера. Полагают, что А-белки в качестве метаболитов белков предшественника амилоида (далее обозначен как БПА), в значительной степени вовлечены в дегенерацию и потерю нейронов и наступление симптомов слабоумия (см. непатентный документ 1 и непатентный документ 2, например). А-белок содержит в качестве основных компонентов A40, состоящий из 40 аминокислот, и A42, в котором количество аминокислот увеличено в С-концевой области. Известно, что А 40 и А 42 обладают высокой способностью к агрегации (см. непатентный документ 3, например) и являются основными компонентами старческих бляшек (см. непатентный документ 3, непатентный документ 4 и непатентный документ 5, например). Далее известно, что A40 и А 42 увеличиваются в результате мутации в генах БПА и пресенилина, которые обнаружены при наследственной болезни Альцгеймера (см. непатентный документ 6, непатентный документ 7 и непатентный документ 8, например). Следовательно, ожидается, что соединение, которое снижает образование А 40 и А 42, может являться ингибитором развития или агентом профилактики болезни Альцгеймера. А образуется при расщеплении БПА -секретазой и далее -секретазой. По этой причине были сделаны попытки создать ингибиторы -секретазы и -секретазы для снижения образования А. Многие из таких ингибиторов секретазы уже известны, например пептиды и пептидные миметики, такие какcerebrospinal fluid, and plasma in young (plaque-free) Tg2576 mice using the -secretase inhibitor N2-[(2S)-2(3,5-difluorophenyl)-2-hydroxyethanoyl]-N1-[(7S)-5-methyl-6-oxo-6,7-dihydro-5H-dibenzo[b,d]azepin-7-yl]-Lalaninamide (LY-411575), The journal of pharmacology and experimental therapeutics, 2004, Apr., 309(1),p. 49-55. Непатентный документ 12: Wong G.T., and twelve others, Chronic treatment with the -secretase inhibitor LY-411,575 inhibits -amyloid peptide production and alters lymphopoiesis and intestinal cell differentiation, The journal of biological chemistry, 2004, Mar. 26, 279(13), p. 12876-12882. Описание изобретения Проблемы, решаемые данным изобретением Как описано выше, ожидается, что соединение, которое ингибирует образование A40 и А 42 из БПА, может действовать как терапевтический или профилактический агент для заболевания, вызываемого А, представителем которого является болезнь Альцгеймера. Однако непептидное соединение,имеющее высокую эффективность, ингибирующее образование А 40 и А 42, до сих пор не известно. Следовательно, существует необходимость в новом соединении с низким молекулярным весом, которое ингибирует образование А 40 и А 42. Средства решения проблем В результате обширных исследований авторы данного изобретения впервые обнаружили непептидное соединение бициклического циннамида, которое ингибирует образование А 40 и А 42 из БПА, и,таким образом, нашли профилактический или терапевтический агент для заболеваний, вызванных А,типичным представителем которых является болезнь Альцгеймера. Это открытие легло в основу данного изобретения. Более конкретно, данное изобретение включает: 1) соединение, представленное формулой (I) или его фармацевтически приемлемую соль,где является одинарной связью или двойной связью; Ar1 является фенильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей А 1, или пиридинильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей A1; R1 и R2 являются одинаковыми или разными, и каждый является группой, выбранной из группы заместителей A1; Z1 является метиленовой группой или виниленовой группой, которые могут быть замещены от 1 до 2 заместителями, выбранными из группы заместителей А 1, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы заместителей А 1; и р,q и r являются одинаковыми или разными и равны целому числу от 0 до 2; группа заместителей А 1: (1) атом галогена, (2) гидроксильная группа, (3) цианогруппа, (4) С 3-8 циклоалкильная группа, (5) С 3-8 циклоалкоксигруппа, (6) С 1-6 алкильная группа, где С 1-6 алкильная группа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу, С 1-6 алкоксигруппу и С 3-8 циклоалкоксигруппу, (7) С 1-6 алкоксигруппа, где С 1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу и С 3-8 циклоалкоксигруппу, (8) аминогруппа, которая может быть замещена одной или двумя С 1-6 алкильными группами, где С 1-6 алкильные группы могут быть замещены от 1 до 3 атомами галогена, (9) карбамоильная группа, которая может быть замещена одной или двумя С 1-6 алкильными группами, где С 1-6 алкильные группы могут быть замещены от 1 до 3 атомами галогена, (10) карбоксильная группа, (11) С 1-6 алкоксикарбонильная группа, где С 1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу и С 3-8 циклоалкоксигруппу, (12) С 1-6 ацильная группа, (13) С 1-6 алкилсульфонильная группа и (14) водород; при условии, что соединение, где Z1 является метиленовой группой, Ar1 является фенильной группой, которая замещена одним атомом галогена, R1 и R2, каждый, являются водородом, р и q, каждый,равны целому числу 1, r равен 0, и его фармацевтически приемлемые соли исключаются и при условии,что когда q равно 0, тогда только один из R1 и R2 может присутствовать в кольцевом фрагменте;-2 014427 2) соединение или его фармацевтически приемлемую соль в соответствии с 1) выше, где соединение представлено формулой (II) где Ar1 является фенильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей А 1, или пиридинильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей A1; R1 и R2 являются одинаковыми или разными, и каждый является группой, выбранной из группы заместителей A1; Z1 является метиленовой группой или виниленовой группой, которые могут быть замещены от 1 до 2 заместителями, выбранными из группы заместителей А 1, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы заместителей А 1; и р, q и r являются одинаковыми или разными и равны целому числу от 0 до 2; группа заместителей А 1: (1) атом галогена, (2) гидроксильная группа, (3) цианогруппа, (4) С 3-8 циклоалкильная группа, (5) С 3-8 циклоалкоксигруппа, (6) С 1-6 алкильная группа, где С 1-6 алкильная группа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу, С 1-6 алкоксигруппу и С 3-8 циклоалкоксигруппу, (7) С 1-6 алкоксигруппа, где С 1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу и С 3-8 циклоалкоксигруппу, (8) аминогруппа, которая может быть замещена одной или двумя С 1-6 алкильными группами, где С 1-6 алкильные группы могут быть замещены от 1 до 3 атомами галогена, (9) карбамоильная группа, которая может быть замещена одной или двумя С 1-6 алкильными группами, где С 1-6 алкильные группы могут быть замещены от 1 до 3 атомами галогена, (10) карбоксильная группа, (11) С 1-6 алкоксикарбонильная группа, где С 1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу и С 3-8 циклоалкоксигруппу, (12) С 1-6 ацильная группа, (13) С 1-6 алкилсульфонильная группа и (14) водород; 3) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, гидроксильную группу и атом галогена; 4) соединение или его фармацевтически приемлемую соль в соответствии с 3) выше, где Z1 является метиленовой группой, которая может быть замещена 1 или 2 заместителями, выбранными из группы,включающей С 1-6 алкильную группу и гидроксильную группу; 5) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, гидроксильную группу и атом галогена; и р, q и r, каждый, равны 1; 6) соединение или его фармацевтически приемлемую соль в соответствии с 5) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С 1-6 алкильную группу и гидроксильную группу; и р, q и r, каждый, равен 1; 7) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, гидроксильную группу и атом галогена; р и q, каждый, равны 1 и r равен 0; 8) соединение или его фармацевтически приемлемую соль в соответствии с 7) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С 1-6 алкильную группу и гидроксильную группу; р и q, каждый, равны 1 и r равен 0; 9) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Z1 является атомом кислорода и р, q и r, каждый, равны 1; 10) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, атом галогена и гидроксильную группу; р равен 1 и q и r, каждый, равны 0; 11) соединение или его фармацевтически приемлемую соль в соответствии с 10) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С 1-6 алкильную группу и гидроксильную группу; р равен 1 и q и r,-3 014427 каждый, равны 0; 12) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, атом галогена и гидроксильную группу; p и r, каждый, равны 1 и q равен 0; 13) соединение или его фармацевтически приемлемую соль в соответствии с 12) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С 1-6 алкильную группу и гидроксильную группу; p и r, каждый, равны 1 и q равен 0; 14) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, атом галогена и гидроксильную группу; р равен 1; q равен 2 и r равен 0; 15) соединение или его фармацевтически приемлемую соль в соответствии с 14) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С 1-6 алкильную группу и гидроксильную группу; р равен 1; q равен 2 и r равен 0. 16) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, атом галогена и гидроксильную группу; p и r, каждый, равны 1 и q равен 2; 17) соединение или его фармацевтически приемлемую соль в соответствии с 16) выше, где Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С 1-6 алкильную группу и гидроксильную группу; p и r, каждый, равны 1 и q равен 2; 18) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Z1 является виниленовой группой, где виниленовая группа может быть замещена одной или двумя С 1-6 алкильными группами или атомами галогена; р равен 0 и q и r, каждый, равны 1; 19) соединение или его фармацевтически приемлемую соль в соответствии с 18), где Z1 является виниленовой группой, где виниленовая группа может быть замещена одной или двумя С 1-6 алкильными группами; р равен 0 и q и r, каждый, равны 1; 20) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Z1 является виниленовой группой, где виниленовая группа может быть замещена одной или двумя С 1-6 алкильными группами или атомами галогена; р и q, каждый, равны 1 и r равен 0; 21) соединение или его фармацевтически приемлемую соль в соответствии с 20), где Z1 является виниленовой группой, где виниленовая группа может быть замещена одной или двумя С 1-6 алкильными группами; р и q, каждый, равны 1 и r равен 0; 22) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где Ar1 является фенильной группой, замещенной от 1 до 3 атомами галогена; 23) соединение или его фармацевтически приемлемую соль в соответствии с 22) выше, где Ar1 является фенильной группой, замещенной от 1 до 3 атомами фтора или хлора; 24) соединение или его фармацевтически приемлемую соль в соответствии с 7) или 8) выше, где Ar1 является фенильной группой, замещенной от 2 или 3 атомами галогена; 25) соединение или его фармацевтически приемлемую соль в соответствии с любым из 2), 22), 23) и 24) выше, где Ar1 является фенильной группой, замещенной атомом фтора; 26) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где R1 2 и R являются одинаковыми или разными, и каждый является заместителем, выбранным из группы,включающей С 1-6 алкильную группу, атом галогена, гидроксильную группу и водород; 27) соединение или его фармацевтически приемлемую соль в соответствии с 1) или 2) выше, где соединение выбирают из следующей группы: 1)(4R,9aS)-2-метансульфонил-7-1-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)фенил]-(Е)-метилиден-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он и 115) диметиламид (4R,9aS)-7-1-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)фенил]-(Е)-метилиден-6-оксо-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-2-карбоновой кислоты; 28) лекарственное средство, содержащее соединение или его фармацевтически приемлемую соль в соответствии с любым из 1)-27) выше в качестве активного ингредиента; 29) лекарственное средство в соответствии с 28) выше, который является профилактическим или терапевтическим агентом для заболевания, вызываемого амилоидом-; 30) лекарственное средство в соответствии с 29) выше, где заболеванием, вызываемым амилоидом-,является болезнь Альцгеймера, старческое слабоумие, синдром Дауна или амилоидоз. Значения символов, терминов и подобных, применяемых в данном описании, объясняется ниже,также ниже представлено подробное описание данного изобретения. В данном описании структурная формула соединения может представлять определенный изомер для удобства. Однако данное изобретение включает все изомеры и изомерные смеси, такие как геометрические изомеры, которые могут быть получены из структуры соединения, оптические изомеры, основанные на асимметричном атоме углерода, стереоизомеры и таутомеры. Данное изобретение не ограничено описанием удобной химической формулы и может включать любые изомеры и их смеси. Следовательно, соединение в соответствии с данным изобретением может иметь асимметричный атом углерода в молекуле и существовать в виде оптически активного соединения или рацемата и данное изобретение включает каждое из оптически активных соединений и рацематов без ограничений. Хотя могут присутствовать кристаллические полиморфы соединения, соединение не ограничено ими и может присутствовать в виде смеси монокристаллических форм. Соединение может быть ангидридом или гидратом."Заболевание, вызванное А" относится к множеству заболеваний, таких как болезнь Альцгеймераamyloid gene in hereditary cerebral hemorrhage, Dutch type, Science, 1990, Jun. 1, 248(4959), p. 1124-1126,например), ухудшение познавательной способности (см. Laws S.M., and seven others, Association betweenacid isoform of human -amyloid precursor protein, Proceding National Academy of Science USA, 1995, June 6, 92(12), p. 5341-5345, например), амилоидоз, ишемия головного мозга (см. Laws S.M., and seven others,Association between the presenilin-1 mutation Glu318Gly and complaints of memory impairment, Neurobiologyjournal of Medical Genetics, 2002, Apr. 8, 114(3), p. 292-298, например), заболевание приона, наследственная амилоидная невропатия, повторное заболевание триплета (см. Kirkitadze M.D., and two others, Paradigm shifts in Alzheimer's disease and other neurodegenerative disorders: the emerging role of oligomeric assemblies, Journal of Neuroscience Research, 2002, Sep. 1, 69(5), p. 567-577; Evert B.O., and eight others, Inflammatory genes are unregulated in expanded ataxin-3-expressing cell lines and spinocerebellar ataxia type 3brains, The Journal of Neuroscience, 2001, Aug. 1, 21(15), p. 5389-5396; and Mann D.M., and one other, Deposition of amyloid(A4) protein within the brains of persons with dementing disorders other than Alzheimer's disease and Down's syndrome, Neuroscience Letters, 1990, Feb. 5, 109(1-2), p. 68-75, например), болезнь Пар-9 014427 кинсона (см. Primavera J., and four others, Brain accumulation of amyloid- in Non-Alzheimer Neurodegeneration, Journal of Alzheimer's Disease, 1999, Oct., 1(3), p. 183-193, например), деменция телец Леви (см. Giasson B.I., and two others, Interactions of amyloidogenic proteins. NeuroMolecular Medicine, 2003, 4(1-2), p. 4958; Masliah E., and six others, -amyloid peptides enhance -synuclein accumulation and neuronal deficits in acontaining the Kunitz protease inhibitor, Neurochemistry International, 2005, Feb., 46(3), p. 253-260 и Primavera J., and four others, Brain accumulation of amyloid- in Non-Alzheimer Neurodegeneration, Journal of Alzheimer's Disease, 1999, Oct, 1(3), p. 183-193, например), комплексное заболевание паркинсонизмомдеменцией (см. Schmidt M.L., and six others, Amyloid plaques in Guam amyotrophic lateral sclerosis/ parkinsonism-dementia complex contain species of A similar to those found in the amyloid plaques of Alzheimer'sdefects is associated with endosomal abnormalities, American Journal of Pathology, 2004, Mar., 164(3), p. 975985, например), боковой амиотрофический склероз (см. Sasaki S., and one other, Immunoreactivity of amyloid precursor protein in amyotropihic lateral sclerosis, Acta Neuropathologica (Berl.), 1999, May, 97(5),p. 463-468; Tamaoka A., and four others, Increased amyloidprotein in the skin of patients with amyotrophicMedicine, 1998, Apr.; 4(4), p. 452-455, например), прогрессирующий супрануклеарный паралич (см. Barrachina M., and six others, Amyloid- deposition in the cerebral cortex in Dementia with Lewy bodies is accompanied by a relative increase in APP mRNA isoforms containing the Kunitz protease inhibitor, Neurochemistrybearing the Thr113-114ins presenilin-1 mutation, Brain, 2000, Dec., 123(Pt12), p. 2467-2474, например), легкое ухудшение познавательной способности (см. Gattaz W.F., and four others, Platelet phospholipase A2"C1-6 Алкильная группа" в данном описании относится к линейной или разветвленной алкильной группе, содержащей от 1 до 6 атомов углерода. Предпочтительные примеры группы включают линейные или разветвленные алкильные группы, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутил,трет-бутил, н-пентил, изопентил, неопентил, н-гексил, 1-метилпропил, 1,2-диметилпропил, 1-этилпропил, 1-метил-2-этилпропил, 1-этил-2-метилпропил, 1,1,2-триметилпропил, 1-метилбутил, 2-метилбутил, 1,1-диметилбутил, 2,2-диметилбутил, 2-этилбутил, 1,3-диметилбутил, 2-метилпентил и 3-метилпентил."C1-6 Ацильная группа" относится к алкильной группе, содержащей от 1 до 6 атомов углерода, в которой один атом водорода замещен карбонильной группой. Предпочтительные примеры группы включают ацетил, пропионил и бутирил."Атом галогена" относится к атому фтора, атому хлора, атому брома, атому йода или подобным и предпочтительно является атомом фтора, атомом хлора или атомом брома."С 3-8 Циклоалкильная группа" относится к циклической алкильной группе, содержащей от 3 до 8 атомов углерода. Предпочтительные примеры группы включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил."С 3-8 Циклоалкоксигруппа" относится к циклической алкильной группе, содержащей от 3 до 8 атомов углерода, в которой один атом водорода замещен атомом кислорода. Предпочтительные примеры группы включают циклопропокси, циклобутокси, циклопентокси, циклогексокси, циклогептилокси и циклооктилокси."С 1-6 Алкоксигруппа" относится к алкильной группе, содержащей от 1 до 6 атомов углерода, в которой один атом водорода замещен атомом кислорода. Предпочтительные примеры группы включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, н-пентокси, изопентокси, втор-пентокси, трет-пентокси, н-гексокси, изо-гексокси, 1,2-диметилпропокси, 2-этилпропокси, 1-метил-2-этилпропокси, 1-этил-2-метилпропокси, 1,1,2-триметилпропокси, 1,1-диметилбутокси, 2,2-диметилбутокси, 2-этилбутокси, 1,3-диметилбутокси, 2-метилпентокси, 3-метилпентокси и гексилокси."С 1-6 Алкоксикарбонильная группа" относится к так называемой группе сложного эфира, в которой карбонильная группа связана с С 1-6 алкоксигруппой. Предпочтительные примеры группы включают метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил,изобутоксикарбонил, н-пентоксикарбонил и н-гексоксикарбонил."С 1-6 Алкилсульфонильная группа" относится к алкильной группе, содержащей от 1 до 6 атомов углерода, в которой один атом водорода замещен атомом серы. Предпочтительные примеры группы включают метилсульфонил, этилсульфонил, н-пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, изобутилсульфонил, третичный бутилсульфонил, н-пентилсульфонил, изопентилсульфонил, неопентилсульфонил, н-гексилсульфонил и 1-метилпропилсульфонил."Метиленовой группой, которая может быть замещена 1 или 2 заместителями, выбранными из группы заместителей А 1", может быть, например, группа любой из формул В дополнение к указанным выше группой может быть любая метиленовая группа, которая может быть замещена 1 или 2 заместителями, выбранными из группы заместителей А 1."Виниленовой группой, которая может быть замещена 1 или 2 заместителями, выбранными из группы заместителей А 1", может быть, например, группа любой из формул В дополнение к указанным выше группой может быть любая виниленовая группа, которая может быть замещена 1 или 2 заместителями, выбранными из группы заместителей А 1."Иминогруппой, которая может быть замещена заместителями, выбранными из группы заместителей А 1", может быть, например, группа любой из формул Предпочтительные примеры "С 1-6 алкильной группы, где С 1-6 алкильная группа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу, С 1-6 алкоксигруппу и С 3-8 циклоалкоксигруппу", в группе заместителей А 1 включают метил, трифторметил, гидроксиметил, цианометил, этил, 2-гидроксиэтил, н-пропил, изопропил, 3-гидрокси-н-пропил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил,1-метилпропил, 1,2-диметилпропил, 1-этилпропил, 1-метил-2-этилпропил, 1-этил-2-метилпропил, 1,1,2 триметилпропил, 1-метилбутил, 2,2-диметилбутил, 2-этилбутил, 2-метилпентил и 3-метилпентил. Примеры "С 1-6 алкоксигруппы, где С 1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу и С 3-8 циклоалкоксигруппу", включают метокси, трифторметокси, гидроксиметокси, цианометокси, этокси, 2-гидроксиэтокси, н-пропокси, изопропокси, 3-гидрокси-н-пропокси, третбутокси, н-пентокси, изопентокси, неопентокси, н-гексокси, 1-метилпропокси, 1,2-диметилпропокси, 1 этилпропокси, 1-метил-2-этилпропокси, 1-этил-2-метилпропокси, 1,1,2-триметилпропокси, 1-метилбутокси, 2,2-диметилбутокси, 2-этилбутокси, 2-метилпентокси и 3-метилпентокси."Аминогруппа, которая может быть замещена одной или двумя С 1-6 алкильными группами, где С 16 алкильные группы могут быть замещены от 1 до 3 атомами галогена", относится к аминогруппе, в которой один или два атома водорода замещены одной или двумя С 1-6 алкильными группами, которые могут быть замещены 1-3 атомами галогена. Предпочтительные примеры группы включают метиламино,трифторметиламино, диметиламино, этиламино, диэтиламино, н-пропиламино, изопропиламино, 3-гидрокси-н-пропиламино, трет-бутиламино, н-пентиламино, изопентиламино, неопентиламино, н-гексиламино, 1-метилпропиламино, 1,2-диметилпропиламино, 1-этилпропиламино, 1-метил-2-этилпропиламино, 1-этил-2-метилпропиламино, 1,1,2-триметилпропиламино, 1-метилбутиламино, 2,2-диметилбутиламино, 2-этилбутиламино, 2-метилпентиламино, дифторметиламино, фторметиламино, 2,2,2 трифторэтиламино, 2,2-дифторэтиламино и 3-метилпентиламино."Карбамоильная группа, которая может быть замещена одной или двумя С 1-6 алкильными группами, где С 1-6 алкильные группы могут быть замещены от 1 до 3 атомами галогена", относится к карбамоильной группе, в которой один или два атома водорода замещены одной или двумя алкильными группами, содержащими 1-6 атомов углерода. Предпочтительные примеры группы включают метилкарбамоил,диметилкарбамоил, этилкарбамоил, диэтилкарбамоил, н-пропилкарбамоил, трифторметилкарбамоил и ди-н-пропилкарбамоил. Предпочтительные примеры "С 1-6 алкоксикарбонильной группы, где С 1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу и С 3-8 циклоалкоксигруппу", включают метоксикарбонил, трифторметоксикарбонил, гидроксиметоксикарбонил, цианометоксикарбонил, этоксикарбонил, 2-гидроксиэтоксикарбонил, н-пропоксикарбонил, изо-пропоксикарбонил, 3-гидрокси-нпропоксикарбонил, трет-бутоксикарбонил, н-пентоксикарбонил, изо-пентоксикарбонил, неопентоксикарбонил, н-гексоксикарбонил, 1-метилпропоксикарбонил, 1,2-диметилпропоксикарбонил, 1-этилпропоксикарбонил, 1-метил-2-этилпропоксикарбонил, 1-этил-2-метилпропоксикарбонил, 1,1,2-триметилпропоксикарбонил, 1-метилбутоксикарбонил, 2,2-диметилбутоксикарбонил, 2-этилбутоксикарбонил, 2 метилпентоксикарбонил и 3-метилпентоксикарбонил."С 1-6 алкилсульфонильная группа" относится к сульфонильной группе с линейной или разветвленной алкильной группой, содержащей 1-6 атомов углерода. Предпочтительные примеры группы включают линейный или разветвленный алкилсульфонил, такой как метансульфонил, этилметилсульфонил, нпропилсульфонил, изопропилсульфонил, н-бутилсульфонил, изобутилсульфонил, трет-бутилсульфонил,н-пентилсульфонил, изопентилсульфонил, неопентилсульфонил, н-гексилсульфонил, 1-метилпропилсульфонил и так далее. В данном описании нет определенных ограничений для "фармацевтически приемлемой соли", если она является фармацевтически приемлемой солью, полученной с соединением общей формулы (I) или(II), которое является профилактическим или терапевтическим агентом для заболевания, вызванного А. Предпочтительные конкретные примеры соли включают галогенводороды (такие как гидрофториды,гидрохлориды, гидробромиды и гидройодиды), соли неорганических кислот (такие как сульфаты, нитраты, перхлораты, фосфаты, карбонаты и бикарбонаты), органические карбоксилаты (такие как ацетаты,оксалаты, малеаты, тартраты, фумараты и цитраты), органические сульфонаты (такие как метансульфонаты, трифторметансульфонаты, этансульфонаты, бензолсульфонаты, толуолсульфонаты и камфорсуль- 12014427 фонаты), соли аминокислот (такие как аспартаты и глутаматы), соли четвертичного амина, соли щелочных металлов (такие как соли натрия и соли калия) и соли щелочно-земельных металлов (такие как соли магния и соли кальция). Далее описано соединение формулы (I) или (II) в соответствии с данным изобретением. В соединении формулы (I) или (II) или его фармацевтически приемлемой солиAr1 предпочтительно является фенильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей А 1, или пиридинильной группой, которая может быть замещена от 1 до 3 заместителями, выбранными из группы заместителей А 1,Ar1 более предпочтительно является фенильной группой, замещенной от 1 до 3 атомами галогена, иAr1 наиболее предпочтительно является фенильной группой, замещенной от 1 до 3 атомами фтора или хлора. В соединении формулы (I) или (II) или его фармацевтически приемлемой соли R1 и R2 предпочтительно являются атомом водорода; атомом галогена; гидроксильной группой; цианогруппой; С 3-8 циклоалкильной группой; С 3-8 циклоалкоксигруппой; С 1-6 алкильной группой, где С 1-6 алкильная группа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу, С 1-6 алкоксигруппу и С 3-8 циклоалкоксигруппу; С 1-6 алкоксигруппой, где С 1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу, цианогруппу, С 3-8 циклоалкильную группу и С 3-8 циклоалкоксигруппу; аминогруппой, где аминогруппа может быть замещена одной или двумя С 1-6 алкильными группами, которые соответствующе замещены от 1 до 3 атомами галогена; карбамоильную группу, где карбамоильная группа может быть замещена одной или двумя С 1-6 алкильными группами, которые соответствующе замещены от 1 до 3 атомами галогена; карбоксильную группу; или С 1-6 алкоксикарбонильную группу, где С 1-6 алкоксигруппа может быть замещена от 1 до 3 заместителями, выбранными из группы, включающей атом галогена, гидроксильную группу,цианогруппу, С 3-8 циклоалкильную группу и С 3-8 циклоалкоксигруппу. В соединении формулы (I) или (II) или его фармацевтически приемлемой соли более предпочтительно R1 и R2 одинаковые или разные и каждый является атомом водорода, С 1-6 алкильной группой,атомом галогена или гидроксильной группой. В соединении формулы (I) или (II) или его фармацевтически приемлемой соли Z1 предпочтительно является метиленовой группой, которая может быть замещена 1 или 2 заместителями, выбранными из группы заместителей А 1, и Z1 более предпочтительно является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С 1-6 алкильную группу, гидроксильную группу и атом галогена. В соединении формулы (I) или (II) или его фармацевтически приемлемой соли предпочтительно Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, гидроксильную группу и атом галогена; и р, q и r, каждый, равны 1. В соединении формулы (I) или его фармацевтически приемлемой соли предпочтительно Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С 1-6 алкильную группу, гидроксильную группу и атом галогена; р и q, каждый, равны 1 и r равен 0. В соединении формулы (I) или (II) или его фармацевтически приемлемой соли предпочтительно Z1 является атомом кислорода и р, q и r, каждый, равны 1. В соединении формулы (I) или его фармацевтически приемлемой соли предпочтительно Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями, выбранными из группы, включающей С 1-6 алкильную группу, атом галогена и гидроксильную группу; р равен 1 иq и r, каждый, равны 0. В соединении формулы (I) или (II) или его фармацевтически приемлемой соли предпочтительно Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, атом галогена и гидроксильную группу; p и r, каждый, равны 1 и q равен 0. В соединении формулы (I) или (II) или его фармацевтически приемлемой соли предпочтительно Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, атом галогена и гидроксильную группу; р равен 1; q равен 2 и r равен 0. В соединении формулы (I) или (II) или его фармацевтически приемлемой соли предпочтительно Z1 является метиленовой группой, где метиленовая группа может быть замещена 1 или 2 заместителями,выбранными из группы, включающей С 1-6 алкильную группу, атом галогена и гидроксильную группу; p и r, каждый, равны 1 и q равен 2. В соединении формулы (I) или (II) или его фармацевтически приемлемой соли предпочтительно Z1 является виниленовой группой, где виниленовая группа может быть замещена одной или двумя С 1-6 алкильными группами или атомами галогена; р равен 0 и q и r, каждый, равны 1.- 13014427 В соединении формулы (I) или (II) или его фармацевтически приемлемой соли предпочтительно Z1 является виниленовой группой, где виниленовая группа может быть замещена одной или двумя С 1-6 алкильными группами или атомами галогена; р и q, каждый, равны 1 и r равен 0. В частности, соединение, выбранное из представленной ниже группы, или его фармацевтически приемлемая соль является особенно предпочтительным, например, и применяется в качестве терапевтического или профилактического агента для заболевания, такого как болезнь Альцгеймера, старческое слабоумие, синдром Дауна или амилоидоз. 1) (E)-(3S)-(3,4,5-трифторфенил)-6-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил) бензилиден]-(9R)гексагидроиндолизин-5-он,2) (E)-(3R)-(3,4,5-трифторфенил)-6-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил) бензилиден]-(9R)гексагидроиндолизин-5-он,3) (Е)-(3S)-(3,4,5-трифторфенил)-6-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)бензилиден]-(9S)-гексагидроиндолизин-5-он,4) (E)-(3R)-(3,4,5-трифторфенил)-6-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)бензилиден]-(9S)-гексагидроиндолизин-5-он,5) (Е)-(3R)-(3,4-дифторфенил)-6-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)бензилиден]-(9R)-гексагидроиндолизин-5-он,6)(4S,9aR)-7-1-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)фенил]-(Е)-метилиден-2-метил-4(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,110) (4R,9aS)-7-1-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)фенил]-(Е)-метилиден-2-метил-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,111) (4S,9aR)-7-1-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)фенил]-(Е)-метилиден-2-пропил-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,112) (4R,9aS)-7-1-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)фенил]-(Е)-метилиден-2-пропил-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,113) (4R,9aS)-2-ацетил-7-1-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)фенил]-(Е)-метилиден-4-(3,4,5 трифторфенил)октагидропиридо[1,2-а]пиразин-6-он,114) (4R,9aS)-2-метансульфонил-7-1-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)фенил]-(Е)-метилиден 4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-6-он и 115) диметиламид (4R,9aS)-7-1-[3-метокси-4-(4-метил-1 Н-имидазол-1-ил)фенил]-(Е)-метилиден-6-оксо-4-(3,4,5-трифторфенил)октагидропиридо[1,2-а]пиразин-2-карбоновой кислоты. Предпочтительные варианты соединения общей формулы (I) описаны выше. Фармацевтически активный ингредиент в соответствии с данным изобретением не ограничен соединениями, конкретно описанными в данном описании, и любой вариант может быть произвольно выбран для определения соединения общей формулы (I).- 17014427 Способы получения соединения общей формулы (I) в соответствии с данным изобретением описаны ниже. Соединение представлено общей формулой (I) является одинарной связью или двойной связью и Ar1, Z1, R1, R2, p, q и r такие, как опрегде делены выше, синтезируют способами, описанными в общем способе получения 1 - общем способе получения 4, например. Очевидно, что для получения соединения в соответствии с данным изобретением способ включает стадию реакции защиты и стадию снятия защиты, соответственно, с применением защитной группы, известной специалисту в данной области техники, которую подходящим образом выбирают на каждой стадии (см. Т. Greene et al., "Protective Groups in Organic Synthesis", John WileySons,Inc., New York, 1981). Общий способ получения 1 Общий способ получения 1, обычно применяемый для получения соединения общей формулы (I) в соответствии с данным изобретением, описан ниже. В формуле является одинарной связью или двойной связью и Ar1, Z1, R1, R2, р, q и r такие,как определены выше. Представленный выше общий способ получения 1 является примером способа получения соединения общей формулы (I), включающим превращения соединения альдегида (1) и соединения лактама (2) в аддукт альдоля (3) путем реакции алдоля на стадии 1-1 с последующим дегидрированием аддукта. Получение соединения общей формулы (I) Соединение общей формулы (I) может быть получено из аддукта алдоля (3) согласно стадии 1-2. Более конкретно, реакция дегидрирования на стадии 1-2 варьируется в соответствии с исходным материалом и не имеет конкретных ограничений, пока условия похожи на те, которые применяются в данной реакции. Известный способ, описанный во множестве документов, может применяться для проведения реакции (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 19, Yuki Gosei (Organic Synthesis) [I], edited by The Chemical Society of Japan, Maruzen Co., Ltd., June 1992, p. 194-226, например). Предпочтительные примеры способа включают i) способ обработки аддукта алдоля (3) предпочтительно от 0,1 до 100,0 экв. кислоты, например (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 19,Yuki Gosei (Organic Synthesis) [I], edited by The Chemical Society of Japan, Maruzen Co., Ltd., June 1992, p. 194-196, например); и ii) способ превращения спиртовой группы аддукта алдоля (3) в уходящую группу,такую как ацетил, карбоксилат, сульфонат или атом галогена, с последующей обработкой аддукта предпочтительно от 1,0 до 10,0 экв. основания, например (см. Jikken Kagaku Koza (Courses in ExperimentalChemistry), vol. 19, Yuki Gosei (Organic Synthesis) [I], edited by The Chemical Society of Japan, Maruzen Co.,Ltd., June 1992, p. 198-205, например). В способе i) применяемые кислота, растворитель и температурные условия варьируются в зависимости от исходного материала и не имеют конкретных ограничений. Предпочтительные примеры применяемой кислоты включают хлористо-водородную кислоту, серную кислоту, фосфорную кислоту, сероводород калия, щавелевую кислоту, п-толуолсульфоновую кислоту, комплекс трифторид бора - простой эфир, тионилхлорид и окись алюминия. Способ может проводиться без применения растворителя или с применением растворителя или смеси растворителей, которые не препятствуют реакции и позволяют исходному материалу растворяться в них до определенной степени. Предпочтительные примеры применяемых растворителей включают неполярные растворители, такие как толуол и бензол; полярные растворители, такие как ацетон, диметилсульфоксид и гексаметилфосфорамид; галогенированные рас- 18014427 творители, такие как хлороформ и метиленхлорид; и воду. Кроме того, сочетание кислоты с органическим основанием, таким как пиридин, может предпочтительно улучшить скорость реакции и выход реакции в некоторых случаях, например. Температура реакции должна быть такой, которая позволит закончить реакцию, не вызывая образования нежелательных побочных продуктов, и предпочтительно составляет от комнатной температуры до 200 С, например. В предпочтительных условиях реакции реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Предпочтительные примеры уходящей группы в способе ii) включают ацетил, метансульфонат,п-толуолсульфонат, атом хлора, атом брома и атом йода. Способ превращения в такую уходящую группу варьируется в зависимости от исходного материала и не имеет конкретных ограничений. Может применяться способ, известный специалисту в данной области техники, такой как способ превращения. Предпочтительно от 1,0 до 10,0 экв. ацетилирующего агента, такого как ацетилхлорид или уксусный ангидрид; сульфонирующего агента, такого как метансульфонилхлорид или п-толуолсульфонилхлорид; или галогенирующего агента, такого как тионилхлорид, например, может применяться в галогенированном растворителе, таком как метиленхлорид или хлороформ; неполярном растворителе, таком как толуол или бензол; эфирном растворителе, таком как тетрагидрофуран или диметиловый эфир этиленгликоля; или смешанном растворителе, например. Целевой продукт может быть эффективно получен с применением основания, такого как предпочтительно пиридин или триэтиламин, в количестве предпочтительно от 1,0 до 10,0 экв., например, или в качестве растворителя реакции на этой стадии. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от -78 до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. В реакции удаления уходящей группы на второй стадии предпочтительно от 1,0 до 10,0 экв. органического основания, такого как диазабициклоундецен, пиридин, 4-диметиламинопиридин или триэтиламин; четвертичной аммониевой соли, такой как гидроксид тетрабутиламмония; соли щелочного металла, такой как метоксид натрия или третбутоксид калия; гидроксида щелочного металла, такого как гидроксид натрия; карбоната щелочного металла, такого как карбонат лития или карбонат калия; или органического металлического реагента, такого как диизопропиламид лития, предпочтительно применяют в качестве основания предпочтительно в галогенированном растворителе, таком как метиленхлорид или хлороформ; неполярном растворителе,таком как толуол или бензол; полярном растворителе, таком как ацетонитрил, диметилформамид или диметилсульфоксид; эфирном растворителе, таком как тетрагидрофуран или диметиловый эфир этиленгликоля; или смеси этих растворителей, например. Органическое основание, такое как пиридин, также может применяться в качестве растворителя. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от -78 до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Получение аддукта альдоля (3) Аддукт альдоля (3) может быть получен из соединения альдегида (1) и от 1,0 до 5,0 экв. соединения лактама (2) по отношению к соединению альдегида (1) согласно стадии 1-1, например. Более конкретно,реакция альдоля на стадии 1-1 варьируется в зависимости от исходных материалов и не имеет конкретных ограничений, насколько условия схожи с теми, которые применяются в этой реакции. Для проведения реакции может применяться способ, известный специалисту в данной области техники (см. JikkenChemical Society of Japan, Maruzen Co., Ltd., July 1992, p. 94-100, например). Предпочтительные примеры способа включают i) способ превращения соединения лактама (2) в энолат щелочного металла с применением предпочтительно от 1,0 до 5,0 экв. основания, например предпочтительно диизопропиламида лития, бутиллития, амида натрия, гидрида натрия, метоксида натрия или трет-бутоксида калия, например, с последующим взаимодействием энолата с соединением альдегида (1) (см. Jikken Kagaku Koza(Courses in Experimental Chemistry), vol. 20, Yuki Gosei (Organic Synthesis) [II], edited by The Chemical Society of Japan, Maruzen Co., Ltd., July 1992, p. 97-98, например), и ii) способ превращения соединения лактама (2) в энолат щелочного металла с применением предпочтительно от 1,0 до 5,0 экв. основания, например предпочтительно диизопропиламида лития, бутиллития, амида натрия, гидрида натрия, метоксида натрия или трет-бутоксида калия, например, взаимодействие энолата с реагентом на основе галогенида кремния (предпочтительно триметилхлорсилана или трет-бутилдиметилхлорсилана, например) с по- 19014427 лучением силиленольного эфира, с последующим взаимодействием эфира с соединением альдегида (1) в присутствии предпочтительно от 0,05 до 5,0 экв. кислоты Льюиса, например предпочтительно тетрахлорида титана или трифторида бора (см. Jikken Kagaku Koza (Courses in Experimental Chemistry),vol. 20, Yuki Gosei (Organic Synthesis) [II], edited by The Chemical Society of Japan, Maruzen Co., Ltd., July 1992, p. 96-97, например). Применяемые растворитель и температура реакции варьируются в зависимости от исходного материала и не имеют конкретных ограничений. В качестве растворителя, который не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени,предпочтительно применяют эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан, диэтиловый эфир; галогенированный растворитель, такой как метиленхлорид, 1,2-дихлорэтан или хлороформ; неполярный растворитель, такой как толуол или бензол; или смешанный растворитель из них, например. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от -78 С до комнатной температуры, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 0,5 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Получение соединения альдегида (1) В формуле L1 является атомом фтора, атомом хлора, атомом брома, атомом йода, сульфонатом, таким как трифлат, триалкилолово, бороновая кислота, боронат или подобные; и L2 является алкиловым эфиром, таким как метиловый эфир, альдегид, циано или подобные. Получение соединения альдегида (1) Соединение альдегида (1) может быть получено из соединения (1 а) в качестве исходного материала согласно стадии 2-5. Более конкретно, стадия 2-5 варьируется в зависимости от исходных материалов и не имеет конкретных ограничений, насколько ее условия схожи с условиями этой реакции. Для проведения этой реакции применяется способ, известный специалисту в данной области техники. Например, i) если L2 является алкиловым эфиром, может применяться реакция восстановления, описанная во многих известных документах (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 26, Yuki Gosei(Organic Synthesis) [VIII], edited by The Chemical Society of Japan, Maruzen Co., Ltd., April 1992, p. 159266, например). Предпочтительно желаемое соединение альдегида (1) может быть получено способом восстановления с применением от 1,0 до 10,0 экв. гидрида металла, такого как гидрид диизобутилалюминия, например. Более предпочтительно желаемое соединение альдегида (1) может быть эффективно получено способом восстановления с применением от 1,0 до 10,0 экв. комплекса гидрида алюминия, такого как алюмогидрид лития или бис-(2-метоксиэтокси)алюмогидрид натрия, по отношению к соединению (1 а) в присутствии от 1,0 до 10,0 экв. амина по отношению к восстанавливающему агенту (см. Т.Abe et al., "Tetrahedron", 2001, vol. 57, p. 2701-271). Например, ii) если L2 является циано, может применяться реакция восстановления, описанная во множестве документов (см. Jikken Kagaku Koza (Courses inJapan, Maruzen Co., Ltd., April 1992, p. 159-266, например). Предпочтительно желаемое соединение альдегида (1) может быть получено способом восстановления с применением от 1,0 до 10,0 экв. гидрида металла, такого как бис-(2-метоксиэтокси)алюмогидрида натрия или гидрида диизобутилалюминия (см.Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 26, Yuki Gosei (Organic Synthesis) [VIII], edited by The Chemical Society of Japan, Maruzen Co., Ltd., April 1992, p. 231). Альтернативно, например, iii) желаемое соединение альдегида (1) может быть эффективно получено восстановлением соединения (1 а) до соединения спирта с применением методики, известной специалисту в данной области техники (см.Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 26, Yuki Gosei (Organic Synthesis) [VIII], edited by The Chemical Society of Japan, Maruzen Co., Ltd., April 1992, p. 159-266, например), с последующим окислением соединения спирта до соединения альдегида (1) (см. Jikken Kagaku Koza (Courses in Experi- 20014427mental Chemistry), vol. 23, Yuki Gosei (Organic Synthesis) [V], edited by The Chemical Society of Japan, Maruzen Co., Ltd., October 1991, p. 1-550, например). Основание, применяемое в реакции восстановления, варьируется в зависимости от исходного материала и не имеет конкретных ограничений. В качестве основания может применяться вторичный амин. Предпочтительно желаемое соединение альдегида (1) может быть эффективно получено с применением от 1,0 до 10,0 экв. линейного или циклического вторичного алкиламина, такого как диэтиламин или пирролидин, по отношению к восстанавливающему агенту, например. Применяемый растворитель варьируется в зависимости от исходного материала и не имеет конкретных ограничений. В качестве растворителя, который не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени, предпочтительно применяют эфирный растворитель, такой как тетрагидрофуран,1,4-диоксан или диэтиловый эфир; неполярный растворитель, такой как толуол или бензол; или смешанный растворитель из них, например. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от -78 С до комнатной температуры, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Окисляющий агент, растворитель и температура реакции, применяемые в реакции окисления, варьируются в зависимости от исходного материала и не имеют конкретных ограничений. Предпочтительные примеры окисляющего агента включают окисляющие агенты на основе хромовой кислоты, такие как оксид хрома и дихромовая кислота; активный диоксид марганца; диметилсульфоксид; окисляющие агенты на основе йодной кислоты, такие как йодинат Десса-Мартина; и смесь N-оксида органического амина,такого как N-оксид 4-метилморфолина, с перрутенатом тетрапропиламмония (см. Jikken Kagaku KozaSociety of Japan, Maruzen Co., Ltd., February, 1991, p. 2-23, например). Предпочтительно применяют от 1,0 до 50,0 экв. окисляющего агента по отношению к соединению, например. В качестве растворителя, который не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени, предпочтительно применяют эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир; галогенированный растворитель, такой как метиленхлорид, 1,2-дихлорэтан или хлороформ; неполярный растворитель, такой как толуол или бензол; или смешанный растворитель из них, например. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от -78 до 100 С,например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч,например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Получение соединения (1 а) Соединение (1 а) может быть получено из i) соединения (4 а) в качестве исходного материала согласно стадии 2-1, например. Альтернативно, соединение (1 а) может быть получено из ii) соединения(4d) в качестве исходного материала согласно стадии 2-4. В способе i) стадия 2-1 варьируется в зависимости от исходных материалов и не имеет конкретных ограничений, насколько ее условия схожи с условиями этой реакции. Для проведения этой реакции применяется способ, известный специалисту в данной области техники. Например, соединение (4 а) и 4-метилимидазол предпочтительно подвергают реакции сочетания в нейтральных или основных условиях (см. D.D. Davey et al. J. Med. Chem., 1991, vol. 39, p. 2671-2677). Более конкретно, предпочтительно применяют от 1,0 до 5,0 экв. соединения (4 а) по отношению к 4-метилимидазолу, например. Предпочтительно реакция может эффективно проходить в некоторых случаях с применением от 1,0 до 5,0 экв. основания. Предпочтительные примеры основания включают гидрид натрия, гидроксид натрия, гидроксид калия, карбонат калия, карбонат натрия, карбонат цезия, карбонат бария и органические основания, такие как пиридин. Растворитель, применяемый в этой реакции, варьируется в зависимости от исходного материала и не имеет конкретных ограничений, насколько он не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени. Предпочтительные примеры растворителя включают тетрагидрофуран, диметилсульфоксид, N,N-диметилформамид, N-метилпирролидин и ацетонитрил. В качестве растворителя также может применяться органическое основание. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от 50 до 200 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. В способе ii) стадия 2-4 варьируется в зависимости от исходных материалов и не имеет конкретных- 21014427 ограничений, насколько ее условия схожи с условиями этой реакции. Для проведения этой реакции применяется способ, известный специалисту в данной области техники (см. ChemicalPharmaceutical Bulletin, 1986, vol. 34, p. 3111, например). Предпочтительно желаемое соединение (1a) может быть получено нагреванием соединения (4d) и от 1,0 до 100,0 экв. аммиака или аммониевой соли по отношению к соединению (4d), например. Растворитель и температура реакции могут варьироваться в зависимости от исходного материала и не имеют конкретных ограничений. В качестве растворителя, который не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени, предпочтительно применяют эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир; галогенированный растворитель, такой как метиленхлорид, 1,2-дихлорэтан или хлороформ; спиртовой растворитель, такой как этанол или метанол; полярный растворитель, такой как диметилформамид или N-метилпирролидон; неполярный растворитель, такой как толуол; органическую кислоту, такую как уксусная кислота; или смешанный растворитель из них, например. Более предпочтительно соединение(1 а) может быть эффективно получено с применением от 5,0 до 20,0 экв. ацетата аммония в уксусной кислоте, например. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от комнатной температуры до 200 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Получение соединения (4 а) Соединение (4 а) является коммерчески доступным или может быть получено способом, известным специалисту в данной области техники. Если оно не является коммерчески доступным, предпочтительное соединение (4 а), где L1 является атомом фтора, атомом хлора или атомом брома, может быть получено окислением соответствующего соединения метила или соединения спирта в реакции окисления, известной специалисту в данной области техники; восстановлением соответствующего соединения сложного эфира известной реакцией восстановления или метилированием соответствующего соединении фенола. Получение соединения (4d) Соединение (4d) может быть получено из соединения (4 с) в качестве исходного материала согласно стадии 2-3, например. Конкретно, стадия 2-3 варьируется в зависимости от исходных материалов и не имеет конкретных ограничений, насколько ее условия схожи с условиями этой реакции. Для проведения этой реакции применяется способ, известный специалисту в данной области техники (см. HelveticaChimica Acta, 1998, vol. 81, p. 1038). Предпочтительно соединение (4d) может быть получено перемешиванием соединения (4 с) и от 1,0 до 10,0 экв. 2-галогенированного ацетона (предпочтительно 2-хлорацетона, 2-бромацетона или 2-йодацетона, например) по отношению к соединению (4 с) в присутствии от 1,0 до 10,0 экв. основания по отношению к соединению (4 с), например. Предпочтительные примеры применяемого основания включают гидриды щелочного металла (предпочтительно гидрид натрия и гидрид лития, например), соли щелочного металла (предпочтительно карбонат калия, карбонат натрия и карбонат цезия, например) и алкоксиды металла (предпочтительно метоксид натрия и трет-бутилкалий,например). Растворитель и температура реакции могут варьироваться в зависимости от исходного материала и не имеют конкретных ограничений. В качестве растворителя, который не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени, предпочтительно применяют эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир; галогенированный растворитель, такой как метиленхлорид, 1,2-дихлорэтан или хлороформ; полярный растворитель,такой как диметилформамид или N-метилпирролидон; неполярный растворитель, такой как толуол или бензол; или смешанный растворитель из них, например. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от комнатной температуры до 200 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Получение соединения (4 с) Соединение (4 с) может быть получено из соединения (4b) в качестве исходного материала согласно стадии 2-2, например. Более конкретно, желаемое соединение формиламида (4 с) может быть предпочтительно получено способом нагревания при температуре кипения с обратным холодильником соединения(4b) в от 10,0 до 100,0 экв. муравьиной кислоты по отношению к соединению (4b) или с применением муравьиной кислоты и дегидратирующего агента (ангидрида кислоты или дициклогексилкарбодиимида,например) для соединения (4b), например. Предпочтительно соединение (4 с) может быть эффективно получено с применением от 1 до 20 экв. муравьиной кислоты по отношению к соединению (4b) и от 1 до 3 экв. агента дегидратирующей конденсации по отношению к соединению (4b), например. Растворитель- 22014427 и температура реакции могут варьироваться в зависимости от исходного материала и не имеют конкретных ограничений. В качестве растворителя, который не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени, предпочтительно применяют эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир; галогенированный растворитель,такой как метиленхлорид, 1,2-дихлорэтан или хлороформ; полярный растворитель, такой как диметилформамид или N-метилпирролидон; неполярный растворитель, такой как толуол или бензол; или смешанный растворитель из них, например. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от комнатной температуры до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Получение соединения (4b) Соединение (4b) является коммерчески доступным или может быть получено способом, известным специалисту в данной области техники. Если оно не является коммерчески доступным, соединение (4b) может быть получено метилированием соответствующего соединения нитрофенола способом, известным специалисту в данной области техники, с последующим восстановлением соединения нитроанизола. Получение соединения лактама (2) В формуле является одинарной связью или двойной связью; Ar1, Z1, R1, R2, p, q и r такие, как определены выше; L3 является алкиловым эфиром, таким как метиловый эфир или этиловый эфир, или алкилкетоном, арилкетоном или аралкилкетоном, таким как ацетил, бензоил или арилметилкетон; L4 является алкокси, такой как метокси или этокси; L5 является карбаматной защитной группой, такой как метилкарбамат, бензилкарбамат или трет-бутилкарбамат, или амидной защитной группой, такой как ацетил; L6 является атомом галогена, таким как атом брома или атом йода; L7 является нитрилом, алкиловым эфиром, таким как метиловый эфир, или алкилкетоном, таким как ацетил; L14 является атомом водорода, алкилом, таким как метил или этил, фенилом, который может быть замещен от 1 до 3 заместителями, выбранными из представленной выше группы заместителей А 1, сложным эфиром, таким как метиловый эфир или этиловый эфир, фосфатом, таким как диметилфосфат или диэтилфосфат, алкилсульфонилом, таким как метилсульфонил, арилсульфонилом, таким как фенилсульфонил, или подобным; и L15 является алкилкетоном, таким как ацетил, арилкетоном, таким как бензоил, формилом, алкиловым эфиром, таким как метиловый эфир или этиловый эфир, или ариловым эфиром, таким как фениловый эфир. Указанная выше формула реакции является примером способа получения соединения лактама (2). Более конкретно, формула показывает (i) способ получения соединения лактама (2), включающий превращение соединения имида (5 а) в качестве исходного материала, который является коммерчески доступным или может быть получен с применением способа, известного специалисту в данной области техники (см. Tetrahedron: Asymmetry, 1998, vol. 9, p. 4361, например), в соединение алкоксилактама (5b) согласно стадии 3-1 с последующей непрерывной реакцией удлинения углерода и реакцией циклизации на стадии 3-2; (ii) способ получения соединения лактама (2), включающий превращение соединения 4-пиридона (5 с) в качестве исходного материала, который является коммерчески доступным или может быть получен с применением способа, известного специалисту в данной области техники (см. Tetrahedron Letters, 1986, vol. 21, p. 4549, например), в ацилированное соединение (5d) согласно стадии 3-3 с последующей реакцией циклизации на стадии 3-4; (iii) способ получения соединения лактама (2), включающий превращение соединения оксазолидина (5 е) в качестве исходного материала, который является коммерчески доступным или может быть получен с применением способа, известного специалисту в данной- 23014427 области техники (см. European Journal of Organic Chemistry, 2004, vol. 23, p. 4823, например), в соединение амидного спирта (5f) согласно стадии 3-5 с последующей реакцией циклизации на стадии 3-6;(iv) способ получения соединения лактама (2), включающий превращение замещенного винилом циклического соединения амина (5g) в качестве исходного материала, который является коммерчески доступным или может быть получен с применением способа, известного специалисту в данной области техники(см. Tetrahedron Letters, 1998, vol. 39, p. 5421, and Tetrahedron Letters, 2004, vol. 45, p. 4895, например), в ацилированное соединение (5h) согласно стадии 3-7 с последующей реакцией циклизации на стадии 3-8;(v) способ получения соединения лактама (2), включающий превращение соединения циклоалкилкетона(5i) в качестве исходного материала, который является коммерчески доступным или может быть получен с применением способа, известного специалисту в данной области техники (см. The Journal of OrganicChemistry, 2001, vol. 66, p. 886, например), в соединение азида (5j) согласно стадии 3-9 с последующей реакцией циклизации на стадии 3-10; или (vi) способ получения соединения лактама (2), включающий превращение замещенного винилом соединения циклического амина (5g) в качестве исходного материала в соединение (5k) согласно стадии 3-11 с последующей реакцией циклизации на стадии 3-12. Превращение соединения имида (5 а) в соединение алкоксилактама (5b) Частичное восстановление имида на стадии 3-1 варьируется в зависимости от исходных материалов и может быть проведено способом, известным специалисту в данной области техники, насколько его условия схожи с условиями этой реакции. Предпочтительно желаемое соединение алкоксилактама (5b) может быть получено взаимодействием соединения имида (5 а) с от 1,0 до 5,0 экв. боргидрида натрия по отношению к соединению имида (5 а) в спиртовом растворителе, таком как метанол (см. Jikken KagakuChemical Society of Japan, Maruzen Co., Ltd., April 1992, p. 207-237, например), или взаимодействием соединения имида (5 а) с от 1,0 до 5,0 экв. бора по отношению к соединению имида (5 а) в эфирном растворителе, таком как тетрагидрофуран (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 26,Yuki Gosei (Organic Synthesis) [VIII], edited by The Chemical Society of Japan, Maruzen Co., Ltd., April 1992, p. 237-248, например); с последующей реакцией в спиртовом растворителе, таком как метанол, в присутствии от 0,1 до 10,0 экв. неорганической кислоты, такой как серная кислота, по отношению к соединению имида (5 а), например. Альтернативно, желаемое соединение алкоксилактама (5b) может быть предпочтительно получено в одну стадию перемешиванием соединения имида (5 а) и от 1,0 до 5,0 экв. боргидрида натрия по отношению к соединению имида (5 а) в спиртовом растворителе, таком как метанол, и в присутствии 0,1 до 5,0 экв. неорганической кислоты, такой как серная кислота, по отношению к соединению имида (5 а), например, см. Tetrahedron: Asymmetry, 1998, vol. 9, p. 4361. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от -78 до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Превращение соединения алкоксилактама (5b) в соединение лактама (2) На стадии 3-2 желаемое соединение лактама (2) может быть получено взаимодействием L3 соединения алкоксилактама (5b) с реагентом Виттига (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 25, Yuki Gosei (Organic Synthesis) [VII], edited by The Chemical Society of Japan, Maruzen Co.,Ltd., September, 1991, p. 254-262, например), реагентом Гриньяра (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 25, Yuki Gosei (Organic Synthesis) [VII], edited by The Chemical Society of Japan,Maruzen Co., Ltd., September, 1991, p. 59-72, например) или алкиллитиевым реагентом (см. Jikken KagakuChemical Society of Japan, Maruzen Co., Ltd., September, 1991, p. 9-51, например) с получением из него производного олефина и последующим взаимодействием производного с кислотой, такой как хлористоводородная кислота. Предпочтительно желаемое соединение лактама (2) может быть получено с высоким выходом перемешиванием соединения алкоксилактама (5b) и от 1,0 до 10,0 экв. реагента Гриньяра,такого как хлорид триметилсилилметилмагния, по отношению к соединению алкоксилактама (5b) в эфирном растворителе, таком как тетрагидрофуран, в присутствии от 1,0 до 10,0 экв. хлорида церия по отношению к соединению алкоксилактама (5b); с последующим взаимодействием раствора с неорганической кислотой, такой как хлористо-водородная кислота (см. Tetrahedron: Asymmetry, 1998, vol. 9,p. 4361, например). Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от -78 до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация.- 24014427 Превращение соединения 4-пиридона (5 с) в ацилированное соединение (5d) Стадия 3-3 включает реакцию снятия защиты с аминовой группы и последующую реакцию амидирования. В качестве реакции снятия защиты с соединения (5 с) может применяться реакция снятия защиты, описанная во множестве известных документов (см. T.W. Green, "Protective Groups in Organic Synthesis", John WileySons, Inc., 1981, например). В этой реакции соединение амина может быть получено из соответствующего соединения карбамата (предпочтительно соединения трет-бутилкарбамата, соединения бензилкарбамата или соединения 9-флуоренилметилкарбамата, например) или из соответствующего соединения амида (предпочтительно соединения формамида, соединения ацетамида, соединения трифторацетамида, например). Такая реакция снятия защиты варьируется в зависимости от исходных материалов и не имеет конкретных ограничений, насколько ее условия схожи с условиями этой реакции. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии и/или кристаллизация. Реакция амидирования варьируется в зависимости от исходных материалов и не имеет конкретных ограничений, насколько ее условия схожи с условиями этой реакции. Для этой реакции может применяться известный способ, описанный во множестве документов (см. Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry),vol. 14, Yuki Kagobutsu No Gosei To Hannou (Synthesis and Reaction of Organic Compounds) [II], edited byThe Chemical Society of Japan, Maruzen Co., Ltd., February, 1978, p. 1136-1162, например). Предпочтительные примеры способа включают i) способ взаимодействия соединения амина с от 1,0 до 5,0 экв. соединения галогенида кислоты по отношению к соединению амина (см. Shin Jikken Kagaku Koza (New CoursesCompounds) [II], edited by The Chemical Society of Japan, Maruzen Co., Ltd., February 1978, p. 1142-1145,например) и ii) способ взаимодействия соединения амина с от 1,0 до 5,0 экв. соединения карбоновой кислоты по отношению к соединению амина с применением от 1,0 до 5,0 экв. конденсирующего агента по отношению к соединению амина (см. "Yukikagaku Jikken No Tebiki (Introduction to Organic Chemistry Experiments) [4]", Kagaku-Dojin Publishing Company, Inc., September, 1990, p. 27-52, например). В способе i) применяемое основание варьируется в зависимости от исходного материала и не имеет конкретных ограничений. Основанием предпочтительно является от 1,0 до 100,0 экв. пиридина, триэтиламина, N,N-диизопропилэтиламина, лутидина, хинолина или изохинолина по отношению к соединению амина, например. Применяемый растворитель не имеет конкретных ограничений, насколько он не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени. Предпочтительные примеры растворителя включают тетрагидрофуран и 1,4-диоксан. В качестве растворителя может применяться основание. Альтернативно, возможно применять двухслойную систему разделения, состоящую из основания,находящегося в щелочном растворе, предпочтительно растворе гидроксида натрия или гидроксида калия,например, и галогенированного растворителя, такого как метиленхлорид или 1,2-дихлорэтан. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от температуры льда до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии и/или кристаллизация. В способе ii) применяемый конденсирующий агент варьируется в зависимости от исходного материала и не имеет конкретных ограничений. Например, могут применяться от 1,0 до 2,0 экв. 1,3-дициклогексилкарбодиимида, 1-этил-3-(3'-диметиламинопропил)карбодиимида, гексафторфосфата бензотриазол 1-илокситрис(диметиламино)фосфония, диэтилцианофосфоната или бис-(2-оксо-3-оксазолидинил)фосфинового хлорида по отношению к применяемой карбоновой кислоте. Предпочтительно может быть добавлено от 1,0 до 2,0 экв. N-гидроксисукцинимида или N-гидроксибензотриазола по отношению к применяемой карбоновой кислоте для эффективного прохождения реакции, например. Эту реакцию предпочтительно проводят в присутствии растворителя с точки зрения оперативности и эффективности перемешивания. Применяемый растворитель варьируется в зависимости от исходного материала и конденсирующего агента и не имеет конкретных ограничений, насколько он не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени. Предпочтительные примеры применяемых растворителей включают галогенированные растворители, такие как метиленхлорид и 1,2-дихлорэтан, и полярные растворители, такие как тетрагидрофуран и N,N-диметилформамид. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от температуры льда до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии и/или кристаллизация.- 25014427 Превращение ацилированного соединения (5d) в соединение лактама (2) Стадия 3-4 представляет собой реакцию циклизации через образование радикала. Более конкретно,например, желаемое соединение лактама (2) может быть предпочтительно получено с высоким выходом взаимодействием соединения (5d) с предпочтительно от 1,0 до 2,0 экв. реагента на основе алкилолова,такого как трибутилолово, по отношению к соединению (5d), например, в неполярном растворителе, таком как толуол, в присутствии предпочтительно от 0,1 до 1,0 экв. радикального инициатора, такого как 2,2-азобис-(изобутиронитрил), по отношению к соединению (5d), например. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от 50 до 150 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии и/или кристаллизация. После циклизации Z1 может быть превращен различными способами с применением кетона в качестве каркаса способом, известным специалисту в данной области техники, таким как реакция восстановления (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 26, Yuki Gosei (Organic Synthesis) [VIII], edited by The Chemical Society of Japan, Maruzen Co.,Ltd., April, 1992, p. 159-266, например), реакция присоединения (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 25, Yuki Gosei (Organic Synthesis) [VII], edited by The Chemical Society of Japan,Maruzen Co., Ltd., September, 1991, p. 9-72, например) или реакция присоединительной дегидратации (см.by The Chemical Society of Japan, Maruzen Co., Ltd., June, 1992, p. 57-85, например). Превращение соединения оксазолидина (5 е) в соединение амидного спирта (5f) Стадия 3-5 представляет собой реакцию окислительного расщепления оксазолидинового кольца,которая дает соединение амидного спирта (5f) из соединения (5 е). Конкретно, желаемое соединение амидного спирта (5f) может быть предпочтительно получено с высоким выходом взаимодействием соединения (5 е) с от 2,0 до 10,0 экв. перманганата калия по отношению к соединению (5 е) в водном растворителе, таком как смесь воды и ацетона (см. European Journal of Organic Chemistry, 2004, vol. 23, p. 4823, например), или соединение (5f) может быть предпочтительно получено взаимодействием соединения (5 е) с от 1,0 до 10,0 экв. брома по отношению к соединению (5 е) в галогенированном растворителе,таком как метиленхлорид (см. Synlett, 1994, vol. 2, p. 143, например). Применяемый растворитель варьируется в зависимости от исходного материала и окисляющего агента и не имеет конкретных ограничений, насколько он не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от температуры льда до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии и/или кристаллизация. Превращение соединения амидного спирта (5f) в соединение лактама (2) Стадия 3-6 включает превращение L7 соединения амидного спирта (5f) в спирт или амин и последующую реакцию циклизации. Конкретно, превращение L7 соединения амидного спирта (5f) в спирт варьируется в зависимости от исходного материала и может быть проведена способом, известным специалисту в данной области техники, насколько его условия схожи с условиями данной реакции (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 20, Yuki Gosei (Organic Synthesis) [II], edited byThe Chemical Society of Japan, Maruzen Co., Ltd., July, 1992, p. 1-30, например). Превращение L7 соединения амидного спирта (5f) в амин варьируется в зависимости от исходного материала и может быть проведена способом, известным специалисту в данной области техники, насколько его условия схожи с условиями данной реакции (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 20, Yuki Gosei(Organic Synthesis) [II], edited by The Chemical Society of Japan, Maruzen Co., Ltd., July, 1992, p. 279-318,например). Реакция циклизации спиртового соединения или аминового соединения варьируется в зависимости от исходного материала и может быть проведена способом, известным специалисту в данной области техники, насколько его условия схожи с условиями данной реакции (см. Journal of FluorineChemistry, 1997, vol. 2, p. 119, or Scientia Pharmaceutica, 1996, vol. 64, р. 3, например). Предпочтительно соединение лактама (2) может быть получено с высоким выходом нагреванием спиртового соединения в растворителе или без растворителя в присутствии от 0,1 до 10,0 экв. органической кислоты, такой как п-толуолсульфоновая кислота или камфорсульфоновая кислота, или неорганической кислоты, такой как серная кислота или хлористо-водородная кислота, по отношению к спиртовому соединению, например. Реакция циклизации аминового соединения варьируется в зависимости от исходного материала и может быть проведена способом, известным специалисту в данной области техники, насколько его условия схожи с условиями данной реакции (см. Petrochemia, 1990, vol. 30, p. 56; WO 2003/076386; or TetrahedronLetters, 1982, vol. 23, p. 229, например). Предпочтительно соединение лактама (2) может быть получено с- 26014427 высоким выходом перемешиванием аминового соединения в растворителе, таком как тетрагидрофуран,толуол, метиленхлорид или диметилформамид, в присутствии от 0,1 до 1,0 экв. органического металла,такого как тетракистрифенилфосфин палладия или тристрифенилфосфин рутения, по отношению к аминовому соединению, например. Очевидно, что применяемый на данной стадии растворитель варьируется в зависимости от исходного материала и применяемого реагента и не имеет конкретных ограничений,насколько он не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от температуры льда до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии и/или кристаллизация. Превращение замещенного винилом циклического соединения амина (5g) в ацилированное соединение (5h) Ацилированное соединение (5h) может быть получено из замещенного винилом циклического соединения амина (5g) в качестве исходного материала на стадии 3-7. Конкретно, стадию 3-7 проводят по методике проведения стадии 3-3. Превращение ацилированного соединения (5h) в соединение лактама (2) Стадия 3-8 включает реакцию обмена с замыканием кольца и последующую реакцию модификации двойной связи. Реакция обмена с замыканием кольца варьируется в зависимости от исходного материала и может быть проведена способом, известным специалисту в данной области техники, насколько его условия схожи с условиями данной реакции (см. Comprehensive Organometallic Chemistry, 1982, vol. 8,p. 499, or Angewandte Chemie International Edition, 2000, vol. 39, p. 3012, например). Предпочтительно реакция модификации двойной связи может проводиться, например, i) каталитическим гидрированием(см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 26, Yuki Gosei (Organic Synthesis) [VIII],edited by The Chemical Society of Japan, Maruzen Co., Ltd., April, 1992, p. 251-266, например); ii) гидроборированием (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 25, Yuki Gosei (Organic Synthesis) [VII], edited by The Chemical Society of Japan, Maruzen Co., Ltd., September, 1991, p. 83-134, например) или iii) окислением двойной связи углерод-углерод (см. Jikken Kagaku Koza (Courses in ExperimentalCo., Ltd., October, 1991, p. 237-267, например). Реакция обмена с замыканием кольца предпочтительно представляет собой способ перемешивания ацилированного соединения (5h) в растворителе в присутствии от 0,01 до 0,2 экв. металлического катализатора по отношению к ацилированному соединению (5h), например. Предпочтительные примеры растворителя включают галогенированные растворители, такие как метиленхлорид и хлороформ; эфирные растворители, такие как тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан; неполярные растворители,такие как бензол, толуол и ксилол; и смешанные растворители из них. Применяемый металлический катализатор варьируется в зависимости от применяемого исходного материала и растворителя. Предпочтительные примеры применяемого металлического катализатора включают рутениевые катализаторы, такие как дихлорид бис-(трициклогексилфосфин)бензилиден рутения(IV), бензилиден[1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлор(трициклогексилфосфин)рутений(IV) и [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлор(о-изопропоксифенилметилиден)рутений(IV); и молибденовые катализаторы, такие как 2,6-диизопропилфенилимидонеофилиден бифен молибден(VI) и бис-(гексафтор-трет-бутоксид) 2,6-диизопропилфенилимидонеофилиден молибдена(VI). Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от комнатной температуры до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Превращение соединения циклоалкилкетона (5i) в соединения азида (5j) Стадия 3-9 включает i) реакцию галогенирования в положенииароматического кольца (-CH2-Ar1) и ii) последующую реакцию введения азида. Реакция галогенирования i) варьируется в зависимости от исходного материала и может быть проведена способом, известным специалисту в данной области техники, насколько его условия схожи с условиями данной реакции (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 19, Yuki Gosei(Organic Synthesis) [I], edited by The Chemical Society of Japan, Maruzen Co., Ltd., June, 1992, p. 422-458,например). Предпочтительные примеры способа включают способ перемешивания соединения циклоалкилкетона (5i) и от 1,0 до 2,0 экв. галогенирующего агента по отношению к соединению циклоалкилкетона (5i) в растворителе. Предпочтительные примеры галогенирующего агента включают N-бромсукцинимид и бром. Кроме того, реакция может быть значительно ускорена добавлением предпочтительно от- 27014427 0,01 до 0,5 экв. радикального инициатора, такого как перекись бензоила или 2,2-азо-бис-изобутиронитрил, по отношению к соединению циклоалкилкетона (5i), например, или добавлением предпочтительно от 0,01 до 0,5 экв. кислого катализатора, такого как бромисто-водородная кислота, по отношению к соединению циклоалкилкетона (5i), например. Применяемый растворитель варьируется в зависимости от исходного материала и не имеет конкретных ограничений, насколько он не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени. Предпочтительные примеры растворителя включают четыреххлористый углерод и бензол. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от комнатной температуры до 150C, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Реакция азидирования ii) варьируется в зависимости от исходного материала и может быть проведена способом, известным специалисту в данной области техники, насколько его условия схожи с условиями данной реакции (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 20, Yuki Gosei(Organic Synthesis) [II], edited by The Chemical Society of Japan, Maruzen Co., Ltd., July, 1992, p. 415-420,например). Предпочтительно галогенированное соединение и от 1,0 до 5,0 экв. азидирующего агента по отношению к галогенированному соединению перемешивают в растворителе, например. Предпочтительные примеры применяемого азидирующего агента включают азид натрия и азид триметилсилила. Предпочтительно реакция может быть значительно ускорена добавлением от 0,1 до 5,0 экв. соли четвертичного амина, такой как фторид тетрабутиламмония, по отношению к применяемому азидирующему агенту,например. Применяемый растворитель варьируется в зависимости от исходного материала и не имеет конкретных ограничений, насколько он не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени. Предпочтительные примеры применяемого растворителя включают эфирные растворители, такие как тетрагидрофуран и диоксан; галогенированные растворители, такие как хлороформ и метиленхлорид; неполярные растворители, такие как бензол и толуол; и полярные растворители, такие как ацетон, ацетонитрил, диметилформамид и N-метилпирролидин. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от комнатной температуры до 150 С,например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч,например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Превращение соединения азида (5j) в соединение лактама (2) Стадия 3-10 представляет собой способ получения соединения лактама (2), включающий перемешивание соединения азида (5j) в растворителе в присутствии от 1,0 до 10,0 экв. кислоты по отношению к соединению азида (5j) с получением реакции перегруппировки. Конкретно, эта стадия варьируется в зависимости от исходного материала и может быть проведена способом, известным специалисту в данной области техники, насколько его условия схожи с условиями данной реакции (см. The Journal of OrganicChemistry, 2001, vol. 66, p. 886, например). Предпочтительные примеры применяемой кислоты включают трифторметансульфоновую кислоту, трифторуксусную кислоту, серную кислоту и хлористо-водородную кислоту. Хотя кислота может применяться в качестве растворителя, эту реакцию предпочтительно проводят в присутствии отдельного растворителя с точки зрения оперативности и эффективности перемешивания. Применяемый растворитель варьируется в зависимости от исходного материала и не имеет конкретных ограничений, насколько он не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени. Предпочтительные примеры применяемого растворителя включают галогенированные растворители, такие как хлороформ и метиленхлорид; и неполярные растворители, такие как бензол и толуол. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от -78 до 50 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Превращение замещенного винилом циклического соединения амина (5g) в соединение (5k) Соединение (5k) может быть получено из замещенного винилом циклического соединения амина(5g) в качестве исходного материала на стадии 3-11. Стадия 3-11 включает реакцию восстановления двойной связи и последующую реакцию удлинения углерода. Для проведения реакции восстановления двойной связи может применяться способ, описанный во многих известных документах. Предпочтительные примеры способа включают i) реакцию каталитического гидрирования (см. Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 26, Yuki Gosei (Or- 28014427Japan, Maruzen Co., Ltd., April, 1992, p. 165-1856, например). Примеры способа i) включают способ перемешивания соединения (5g) с источником водорода в растворителе в присутствии от 0,01 до 0.5 экв. металлического катализатора по отношению к соединению (5g). Применяемый металлический катализатор варьируется в зависимости от исходного материала и не имеет конкретных ограничений. Предпочтительные примеры катализатора включают палладий на угле, родий на угле, рутений на угле, гидроксид палладия, оксид платины, никель Ренея и катализатор Вилкинсона. Источник водорода варьируется в зависимости от исходного материала и применяемого металлического катализатора и не имеет конкретных ограничений. Предпочтительные примеры источника водорода включают газообразный водород, муравьиную кислоту, формиат аммония и циклогексадиен. Применяемый растворитель варьируется в зависимости от исходного материала и применяемого металлического катализатора и не имеет конкретных ограничений. Предпочтительные примеры растворителя включают метанол, этанол, этилацетат, толуол, ТГФ, 1,4-диоксан, хлороформ, метиленхлорид,воду и их смеси. Органическая кислота, неорганическая кислота или органическое основание могут быть подходящим образом добавлены для эффективного прохождения реакции. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от комнатной температуры до 150 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Примеры способа ii) включают способ перемешивания соединения (5g) в растворителе в присутствии от 1,0 до 10,0 экв. металла или соли металла по отношению к соединению (5g). Металл или соль металла варьируются в зависимости от исходного материала и не имеют конкретных ограничений. Предпочтительные примеры металла или соли металла включают щелочные металлы, такие как литий и натрий; щелочно-земельные металлы, такие как магний и кальций; и их соли. Применяемый растворитель варьируется в зависимости от исходного материала и применяемого металла и не имеет конкретных ограничений. Предпочтительные примеры растворителя включают аммиак, метанол, этанол, трет-бутанол,тетрагидрофуран, 1,4-диоксан, диэтиловый эфир, воду и их смеси. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от -78 до 100 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью известной методики хроматографии. Нежелательный побочный продукт может быть удален методами, известными специалистам в данной области техники, такими как обычная методика хроматографии, экстрагирование и/или кристаллизация. Способ, описанный во многих известных документах, может применяться для реакции удлинения углерода после восстановления двойной связи. Предпочтительные примеры способа включают i) реакцию Виттига, ii) реакцию Хорнера-Эммонса и iii) реакцию Петерсона (см. Jikken Kagaku Koza (Courses inExperimental Chemistry), vol. 19, Yuki Gosei (Organic Synthesis) [I], edited by The Chemical Society of Japan,Maruzen Co., Ltd., June, 1992, p. 57-85, например). Предпочтительные примеры реакции Виттига включают способ перемешивания в растворителе соединения альдегида, полученного из соединения (5g), и от 1,0 до 3,0 экв. известного реагента Виттига по отношению к соединению альдегида в присутствии от 1,0 до 5,0 экв. основания по отношению к соединению альдегида. Применяемый растворитель варьируется в зависимости от исходного материала и применяемого основания и не имеет конкретных ограничений, насколько он не препятствует реакции и позволяет исходному материалу растворяться в нем до определенной степени. Предпочтительные примеры применяемого растворителя включают полярные растворители, такие как нитрометан, ацетонитрил, 1-метил-2-пирролидон, N,N-диметилформамид и диметилсульфоксид; эфирные растворители, такие как тетрагидрофуран, 1,4-диоксан и 1,2-диметоксиэтан; неполярные растворители, такие как бензол, толуол и ксилол; спиртовые растворители, такие как этанол и метанол; галогенированные растворители,такие как хлороформ и метиленхлорид; воду и смешанные растворители из них. Применяемое основание варьируется в зависимости от исходного материала и растворителя. Предпочтительные примеры основания включают гидроксиды щелочных металлов, такие как гидроксид натрия и гидроксид лития; карбонаты щелочных металлов, такие как карбонат натрия; соли щелочных металлов со спиртами, такие как метоксид натрия и трет-бутоксид калия; органические основания, такие как триэтиламин, пиридин и диазабициклононен; органические металлы, такие как бутиллитий и диизобутиламид лития; и гидриды щелочных металлов, такие как гидрид натрия. Температура реакции должна быть такой, чтобы можно было закончить реакцию, не вызывая образование нежелательного побочного продукта, и предпочтительно составляет от -78 до 150 С, например. В предпочтительных условиях реакция предпочтительно завершается в течение от 1 до 24 ч, например, и прохождение реакции может отслеживаться с помощью извест- 29
МПК / Метки
МПК: C07D 471/04, A61K 31/4375, A61K 31/55, C07D 487/04, A61K 31/4178, A61P 25/28, A61K 31/437
Метки: соединение, циннамида, бициклического
Код ссылки
<a href="https://eas.patents.su/30-14427-soedinenie-biciklicheskogo-cinnamida.html" rel="bookmark" title="База патентов Евразийского Союза">Соединение бициклического циннамида</a>
Предыдущий патент: Пиримидинил бензотиофеновые соединения
Следующий патент: Производные бензоизоиндола для лечения боли
Случайный патент: Устройство ускоренной синхронизации приемника шумоподобных сигналов с минимальной частотной манипуляцией


































