Пиридиновые производные и их применение для лечения психотических расстройств
Номер патента: 13909
Опубликовано: 30.08.2010
Авторы: Андреотти Даниэле, Альваро Джузеппе, Ди Фабио Романо, Джованнини Риккардо, Фальки Алессандро, Белведере Сандро
Формула / Реферат
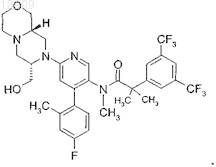
1. Соединение, которое представляет собой 2-[3,5-бис(трифторметил)фенил]-N-{4-(4-фтор-2-метилфенил)-6-[(7S,9aS)-7-(гидроксиметил)гексагидропиразино[2,1-с][1,4]оксазин-8(1Н)-ил]-3-пиридинил}-N,2-диметилпропанамид

или его фармацевтически приемлемая соль.
2. Соединение, которое представляет собой 2-[3,5-бис(трифторметил)фенил]-N-{4-(4-фтор-2-метилфенил)-6-[(7S,9aS)-7-(гидроксиметил)гексагидропиразино[2,1-с][1,4]оксазин-8(1Н)-ил]-3-пиридинил}-N,2-диметилпропанамид
3. Применение соединения или его фармацевтически приемлемой соли по п.1 или 2 в терапии.
4. Применение соединения или его фармацевтически приемлемой соли по п.1 или 2 при лечении психотических расстройств.
5. Применение соединения или его фармацевтически приемлемой соли по п.4, где психотическое расстройство представляет собой шизофрению.
6. Применение соединения или его фармацевтически приемлемой соли по п.3 при лечении депрессивных расстройств.
7. Применение соединения или его фармацевтически приемлемой соли по п.3 при лечении биполярных расстройств.
8. Применение по п.3 при лечении связанных с употреблением алкоголя расстройств.
9. Применение соединения или его фармацевтически приемлемой соли по п.8, где связанное с употреблением алкоголя расстройство представляет собой алкогольную зависимость.
10. Применение соединения или его фармацевтически приемлемой соли по п.1 или 2 для получения лекарственного средства для лечения психотических расстройств.
11. Применение соединения или его фармацевтически приемлемой соли по п.10, где психотическое расстройство представляет собой шизофрению.
12. Применение соединения или его фармацевтически приемлемой соли по п.1 или 2 для получения лекарственного средства для лечения депрессивных расстройств.
13. Применение соединения или его фармацевтически приемлемой соли по п.1 или 2 для получения лекарственного средства для лечения биполярных расстройств.
14. Применение соединения или его фармацевтически приемлемой соли по п.1 или 2 для получения лекарственного средства для лечения связанных с употреблением алкоголя расстройств.
15. Применение соединения или его фармацевтически приемлемой соли по п.14, где связанное с употреблением алкоголя расстройство представляет собой алкогольную зависимость.
16. Фармацевтическая композиция, которая содержит соединение по п.1 или 2 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
17. Фармацевтическая композиция, применяемая при лечении психотических расстройств, которая содержит соединение по п.1 или 2 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
18. Фармацевтическая композиция по п.17, где психотическое расстройство представляет собой шизофрению.
19. Фармацевтическая композиция по п.16, применяемая при лечении депрессивных расстройств.
20. Фармацевтическая композиция по п.16, применяемая при лечении биполярных расстройств.
21. Фармацевтическая композиция по п.16, применяемая при лечении связанных с употреблением алкоголя расстройств.
22. Фармацевтическая композиция по п.21, где связанное с употреблением алкоголя расстройство представляет собой алкогольную зависимость.
Текст
ПИРИДИНОВЫЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ПСИХОТИЧЕСКИХ РАССТРОЙСТВ СМИТКЛАЙН БИЧАМ КОРПОРЕЙШН (US) В соответствии с настоящим изобретением обеспечиваются новые соединения формулы (I) или их фармацевтически приемлемые соли, где X представляет собой атом азота; Y представляет собой -С(Н 2)-,(-С(Н 2)-)2, -S(O2)- или -С(=O)-; Z представляет собой -С(Н 2)-, -S(O2)-, -N(RZ)- или атом кислорода или серы; А представляет собой водород или -СН 2 ОН; Rz представляет собой водород, C1-6 алкил, C1-6 алкокси, -COR7 или -SO2R7; R1 представляет собой галоген, C1-6-алкил, C1-6-алкокси, =O, галоген-C1-6-алкил или галогенC1-6 алкокси, гидроксил или -CH2OH; m представляет собой целое число, имеющее значение от 0 до 3; R2 представляет собой галоген, =O, C1-6-алкил (необязательно замещенный одной или несколькими гидроксильными группами), COOR7, -CONR7R8, C1-6-алкокси, галогенC1-6-алкил, галогенC1-6-алкокси или C1-6 алкилC1-6 алкил; n представляет собой целое число, имеющее значение от 0 до 3; р и q независимо представляют собой целое число, имеющее значение от 0 до 2; R3 представляет собой группу -арил, -гетероарил,-гетероциклил, -арил-арил, -арил-гетероарил, -арил- гетероциклил, -гетероарил-арил, -гетероарилгетероарил, -гетероарил-гетероциклил, -гетероциклил-арил, гетероциклил-гетероарил или -гетероциклилгетероциклил, все из которых необязательно могут быть замещены одной или несколькими группами (например, 1, 2 или 3 группами) галоген, C1-6-алкил, С 3-8-циклоалкил, C1-6-алкокси, гидроксил, галогенC1-6 алкил, галогенC1-6-алкокси, циано, -S-C1-6-алкил, -SO-C1-6-алкил, -SO2-C1-6-алкил, -COR7, -CONR7R8, -NR7R8,NR7COC1-6-алкил, NR7SO2-C1-6-алкил, C1-6-алкил-NR7R8, -OCONR7R8, -NR7CO2R8 или -SO2NR7R8; R4 и R5 независимо представляют собой C1-6-алкил, или R4 и R5 вместе с атомом углерода, с которым они связаны,вместе могут образовывать C3-8-циклоалкильную группу; R6 представляет собой галоген, C1-6-алкил, C3-8 циклоалкил, C1-6-алкокси, галогенC1-6-алкил или галогенC1-6-алкокси; s представляет собой целое число,имеющее значение от 0 до 4; R7 и R8 независимо представляют собой водород, C1-6-алкил или C3-8 циклоалкил; или их сольваты. 013909 Настоящее изобретение относится к новым азотсодержащим бициклическим производным, обладающим фармакологической активностью, способам их получения, к композициям, содержащим такие соединения, и к их применению для лечения психотических расстройств, в частности шизофрении.WO 2005/002577 (F. Hoffmann-La Roche A.G.) описывает ряд пиридиновых производных, которые,как указывается, являются двойными антагонистами NK1/NK3, для лечения шизофрении. Настоящее изобретение обеспечивает, в первом аспекте, соединение формулы (I) или его фармацевтически приемлемую сольX представляет собой атом азота или серы;Z представляет собой -С(Н 2)-, -S(O2)-, -N(RZ)- или атом кислорода или серы;R1 представляет собой галоген, C1-6 алкил, C1-6 алкокси, =O, галогенС 1-6 алкил или галогенС 1-6 алкокси;m представляет собой целое число, имеющее значение от 0 до 3;R2 представляет собой галоген, =O, C1-6 алкил (необязательно замещенный одной или несколькими гидроксильными группами), -COOR7, -CONR7R8, C1-6 алкокси, галогенС 1-6 алкил или галогенС 1-6 алкокси;n представляет собой целое число, имеющее значение от 0 до 3; р и q независимо представляют собой целое число, имеющее значение от 0 до 2;R3 представляет собой группу -арил, -гетероарил, -гетероциклил, -арил-арил, -арил-гетероарил,-арил-гетероциклил, -гетероарил-арил, -гетероарил-гетероарил, гетероарил-гетероциклил, -гетероциклиларил, -гетероциклил-гетероарил или -гетероциклил-гетероциклил, все из которых, необязательно, могут быть замещены одной или несколькими (например, 1, 2 или 3) группами галогена, C1-6 алкил, С 3-8 циклоалкил, C1-6 алкокси, гидроксил, галогенС 1-6 алкил, галогенС 1-6 алкокси, циано, -S-C1-6 алкил, -SO-C1-6 алкил,-SO2-C1-6 алкил, -COR7, -CONR7R8, -NR7R8, NR7COC1-6 алкил, NR7SO2-C1-6 алкил, C1-6 алкил-NR7R8,-OCONR7R8, -NR7CO2R8 или-SO2NR7R8;R4 и R5 независимо представляют собой C1-6 алкил, или R4 и R5 вместе с атомом углерода, с которым они связаны, вместе могут образовывать C3-8 циклоалкильную группу;R6 представляет собой галоген, C1-6 алкил, С 3-8 циклоалкил, C1-6 алкокси, галогенС 1-6 алкил или галогенС 1-6 алкокси;s представляет собой целое число, имеющее значение от 0 до 4;R7 и R8 независимо представляют собой водород, C1-6 алкил или C3-8 циклоалкил; или их сольваты. В следующем аспекте настоящее изобретение обеспечивает соединение формулы (I) или его фармацевтически приемлемую сольX представляет собой атом азота;Z представляет собой -С(Н 2)-, -S(O2)-, -N(RZ)-, или атом кислорода или серы;R1 представляет собой галоген, C1-6 алкил, C1-6 алкокси, =O, галогенС 1-6 алкил или галогенС 1-6 алкокси;m представляет собой целое число, имеющее значение от 0 до 3;R2 представляет собой галоген, =O, C1-6 алкил (необязательно замещенный одной или несколькими гидроксильными группами), -COOR7, -CONR7R8, C1-6 алкокси, галогенС 1-6 алкил или галогенС 1-6 алкокси;n представляет собой целое число, имеющее значение от 0 до 3;-1 013909 р и q независимо представляют собой целое число, имеющее значение от 0 до 2;R3 представляет собой группу -арил, -гетероарил, -гетероциклил, -арил-арил, -арил-гетероарил, арил-гетероциклил, -гетероарил-арил, -гетероарил-гетероарил, гетероарил-гетероциклил, -гетероциклиларил, -гетероциклил-гетероарил или -гетероциклил-гетероциклил, все из которых, необязательно, могут быть замещены одной или несколькими (например, 1, 2 или 3) группами галогена, C1-6 алкил, С 3-8 циклоалкил, C1-6 алкокси, гидроксил, галогенС 1-6 алкил, галогенС 1-6 алкокси, циано, -S-C1-6 алкил, -SO-C1-6 алкил, SO2-C1-6 алкил, -COR7, -CONR7R8, -NR7R8, NR7COC1-6 алкил, NR7SO2-C1-6 алкил, C1-6 алкил-NR7R8, OCONR7R8, -NR7CO2R8 или -SO2NR7R8;R4 и R5 независимо представляют собой C1-6 алкил, или R4 и R5 вместе с атомом углерода, с которым они связаны, могут вместе образовывать C3-8 циклоалкильную группу;R6 представляет собой галоген, C1-6 алкил, С 3-8 циклоалкил, C1-6 алкокси, галогенС 1-6 алкил или галогенС 1-6 алкокси;s представляет собой целое число, имеющее значение от 0 до 4;R7 и R8 независимо представляют собой водород, C1-6 алкил или С 3-8 циклоалкил; или их сольваты. В другом аспекте настоящее изобретение обеспечивает соединение формулы (I) или его фармацевтически приемлемую сольX представляет собой атом азота;Z представляет собой -С(Н 2)-, -S(O2)-, -N(RZ)- или атом кислорода или серы; А представляет собой водород или -СН 2 ОН;m представляет собой целое число, имеющее значение от 0 до 3;R2 представляет собой галоген, =O, C1-6 алкил (необязательно замещенный одной или несколькими гидроксильными группами), -COOR7, -CONR7R8, C1-6 алкокси, галогенС 1-6 алкил, галогенС 1-6 алкокси илиn представляет собой целое число, имеющее значение от 0 до 3; р и q независимо представляют собой целое число, имеющее значение от 0 до 2;R3 представляет собой группу арил, -гетероарил, гетероциклил, -арил-арил, -арил-гетероарил, -арилгетероциклил, -гетероарил-арил, -гетероарил-гетероарил, -гетероарил-гетероциклил, -гетероциклил-арил,-гетероциклил-гетероарил или -гетероциклил-гетероциклил, все из которых, необязательно, могут быть замещены одной или несколькими (например, 1, 2 или 3) группами галогена, C1-6 алкил (необязательно замещенный одной или несколькими гидроксильными группами), C3-8 циклоалкил, C1-6 алкокси, гидроксил, галогенС 1-6 алкил, галогенС 1-6 алкокси, циано, -S-C1-6 алкил, -SO-C1-6 алкил, -SO2-C1-6 алкил, -COR7, CONR7R8, -NR7R8, -NR7COC1-6 алкил, -NR7SO2-C1-6 алкил, C1-6 алкил-NR7R8, -OCONR7R8, -NR7CO2R8 или SO2NR7R8;R4 и R5 независимо представляют собой C1-6 алкил, или R4 и R5 вместе с атомом углерода, с которым они связаны, могут вместе образовывать C3-8 циклоалкильную группу;R6 представляет собой галоген, C1-6 алкил, C3-8 циклоалкил, C1-6 алкокси, галогенС 1-6 алкил или галогенС 1-6 алкокси;s представляет собой целое число, имеющее значение от 0 до 4;R7 и R8 независимо представляют собой водород, C1-6 алкил или C3-8 циклоалкил; или их сольваты. Термин C1-6 алкил, как он использован в настоящем описании, как группа или часть группы, относится к линейной или разветвленной насыщенной углеводородной группе, содержащей от 1 до 6 атомов углерода. Примеры таких групп включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, вторбутил, трет-бутил, н-пентил, изопентил, неопентил или гексил и т.п. Термин C1-6 алкокси, как он использован в настоящем описании, относится к группе -O-C1-6 алкил,где C1-6 алкил имеет указанное выше значение. Примеры таких групп включают метокси, этокси, пропокси, бутокси, пентокси или гексокси и т.п.-2 013909 Термин C3-8 циклоалкил, как он использован в настоящем описании, относится к насыщенному моноциклическому углеводородному кольцу, состоящему из 3-8 атомов углерода. Примеры таких групп включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или циклооктил и т.п. Термин галоген, как он использован в настоящем описании, относится к атому фтора, хлора, брома или иода. Термин галогенС 1-6 алкил, как он использован в настоящем описании, относится к C1-6 алкильной группе, имеющей определенное выше значение, где по меньшей мере один атом водорода замещен галогеном. Примеры таких групп включают фторэтил, трифторметил или трифторэтил и т.п. Термин галогенС 1-6 алкокси, как он использован в настоящем описании, относится к C1-6 алкоксигруппе,имеющей определенное выше значение, где по меньшей мере один атом водорода замещен галогеном. Примеры таких групп включают дифторметокси или трифторметокси и т.п. Термин арил, как он использован в настоящем описании, относится к C6-12 моноциклическому или бициклическому углеводородному кольцу, где по меньшей мере одно кольцо является ароматическим. Примеры таких групп включают фенил, нафтил или тетрагидронафталинил и т.п. Термин гетероарил, как он использован в настоящем описании, относится к 5-6-членному моноциклическому ароматическому или конденсированному 8-10-членному бициклическому ароматическому кольцу, содержащему от 1 до 4 гетероатомов, выбранных из кислорода, азота и серы. Примеры таких моноциклических ароматических колец включают тиенил, фурил, фуразанил, пирролил, триазолил, тетразолил, имидазолил, оксазолил, тиазолил, оксодиазолил, изотиазолил, изоксазолил, тиадиазолил, пиранил, пиразолил, пиримидил, пиридазинил, пиразинил, пиридил, триазинил, тетразинил и т.п. Примеры таких конденсированных ароматических колец включают хинолинил, изохинолинил, хиназолинил, хиноксалинил, птеридинил, циннолинил, фталазинил, нафтиридинил, индолил, изоиндолил, азаиндолил,индолизинил, индазолил, пуринил, пирролопиридинил, фуропиридинил, бензофуранил, изобензофуранил, бензотиенил, бензоимидазолил, бензоксазолил, бензоизоксазолил, бензотиазолил, бензоизотиазолил,бензоксодиазолил, бензотиадиазолил и т.п. Термин гетероциклил относится к 4-7-членному моноциклическому кольцу или конденсированному 8-12-членному бициклическому кольцу, которое может быть насыщенным или частично ненасыщенным, содержащим от 1 до 4 гетероатомов, выбранных из кислорода, азота или серы. Примеры таких моноциклических колец включают пирролидинил, азетидинил, пиразолидинил, оксазолидинил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, тиазолидинил, гидантоинил, валеролактамил, оксиранил, оксетанил, диоксоланил, диоксанил, оксатиоланил, оксатианил, дитианил, дигидрофуранил, тетрагидрофуранил, дигидропиранил, тетрагидропиранил, тетрагидропиридинил, тетрагидропиримидинил,тетрагидротиофенил, тетрагидротиопиранил, диазепанил, азепанил и т.п. Примеры таких бициклических колец включают индолинил, изоиндолинил, бензопиранил, хинуклидинил, 2,3,4,5-тетрагидро-1 Н-3 бензазепин, тетрагидроизохинолинил и т.п. В одном варианте воплощения р и q оба имеют значение 1, X представляет собой атом азота, Y представляет собой -С(Н 2)- и Z представляет собой -С(H2)-, например, бициклическая группа, присоединенная к пиридинильному кольцу в формуле (I), представляет собой гексагидропирролопиразинил (например, гексагидропирроло[1,2-а]пиразин-2(1 Н)-ил). В альтернативном варианте воплощения р и q оба имеют значение 1, X представляет собой атом азота, Y представляет собой (-С(H2)-)2 и Z представляет собой атом кислорода, например, бициклическая группа, присоединенная к пиридинильному кольцу в формуле (I), представляет собой гексагидропиразино-оксазинил (например, гексагидропиразино[2,1-c][1,4]оксазин-8(1 Н)-ил). В следующем альтернативном варианте воплощения р и q оба имеют значение 1, X представляет собой атом азота, Y представляет собой -S(O2)- и Z представляет собой -С(Н 2)-, например, бициклическая группа, присоединенная к пиридинильному кольцу в формуле (I), представляет собой диоксидогексагидроизотиазолопиразинил (например, 1,1-диоксидогексагидро-5 Н-изотиазоло[2,3-а]пиразин-5-ил). Еще в одном альтернативном варианте воплощения р и q оба имеют значение 1, X представляет собой атом азота, Y представляет собой -С(=O)- и Z представляет собой -С(Н 2)-, например, бициклическая группа, присоединенная к пиридинильному кольцу в формуле (I), представляет собой оксогексагидропирролопиразинил (например, 6-оксогексагидропирроло[1,2-а]пиразин-2(1 Н)-ил). В следующем альтернативном варианте воплощения р имеет значение 1, q имеет значение 2, X представляет собой атом азота, Y представляет собой -С(Н 2)- и Z представляет собой -С(Н 2)-, например,бициклическая группа, присоединенная к пиридинильному кольцу в формуле (I), представляет собой октагидропирролодиазепинил (например, октагидро-3H-пирроло[1,2-d][1,4]диазепин-3-ил). В следующем альтернативном варианте воплощения р имеет значение 2, q имеет значение 1, X представляет собой атом азота, Y представляет собой -С(Н 2)- и Z представляет собой -С(Н 2)-, например,бициклическая группа, присоединенная к пиридинильному кольцу в формуле (I), представляет собой оксагексагидропирролодиазепинил (например, оксогексагидро-1 Н-пирроло[1,2-а][1,4]диазепин-2(3H)ил). В следующем альтернативном варианте воплощения р и q оба имеют значение 1, X представляет-3 013909 собой атом азота, Y представляет собой (-С(Н 2)-)2 и Z представляет собой -S(O2)-, например, бициклическая группа, присоединенная к пиридинильному кольцу в формуле (I), представляет собой диоксидогексагидропиразинотиазинил (например, 2,2-диоксидогексагидропиразино[2,1-c][1,4]тиазин-8(1 Н)-ил). В следующем варианте воплощения р и q оба имеют значение 1, X представляет собой азот, Y представляет собой (-С(Н 2)-)2 и Z представляет собой -N(RZ)-, например, бициклическая группа, присоединенная к пиридинильному кольцу в формуле (I), представляет собой октагидропиразинопиразинил(например, октагидро-2 Н-пиразино[1,2-а]пиразин-2-ил). В следующем варианте воплощения, когда р имеет значение 0 и q имеет значение 1, X представляет собой азот, Y представляет собой -С(Н 2)- и Z представляет собой -С(Н 2)-, например, бициклическая группа, присоединенная к пиридинильному кольцу в формуле (I), представляет собой оксотетрагидропирролоимидазолил (например, оксотетрагидро-1 Н-пирроло[1,2-c]имидазол-2(3H)-ил). В одном варианте воплощения m имеет значение 0. В другом варианте воплощения m имеет значение 1. В одном варианте воплощения, когда m имеет значение 1, R1 представляет собой =O, гидроксил,-CH2OH. В одном варианте воплощения n имеет значение 0 или 1. В следующем вариант воплощения, когда n имеет значение 1, R2 представляет собой =O или C1-6 алкил (необязательно замещенный одной или несколькими гидроксильными группами; например, -СН 2OH или СН 3). В другом варианте воплощения, когда n имеет значение 1, R2 представляет собой C1-6 алкилОС 1-6 алкил (например, -СН 2 ОСН 3) или галогенС 1-6 алкил (например, -CH2F). Еще в одном варианте воплощения, когда n имеет значение 1, R2 представляет собой C1-6 алкил, замещенный гидроксильной группой (например, -СН 2-OH). В одном варианте воплощения А представляет собой водород. В другом варианте воплощения А представляет собой -CH2OH. В одном варианте воплощения р и q либо оба имеют значение 1, либо один из р или q имеет значение 1, а другой из р или q имеет значение 2. В следующем варианте воплощения р и q оба имеют значение 1. В следующем варианте воплощения, когда q имеет значение 1, р имеет значение 0. В одном варианте воплощения R7 представляет собой C1-6 алкил (например, метил). В одном варианте воплощения, когда Z представляет собой -N(RZ)-, RZ представляет собой водород,C1-6 алкил, -COR7 или -SO2R7. В другом варианте воплощения RZ представляет собой -COR7. В другом варианте воплощения RZ представляет собой C1-6 алкил или -SO2R7. В следующем варианте воплощения, когда RZ представляет собой -COR7, R7 представляет собой C1-6 алкил (например, метил). В следующем варианте воплощения, когда RZ представляет собой -SO2R7, R7 представляет собой C16 алкил (например, метил). В одном варианте воплощения R3 представляет собой -арил (например, фенил), монозамещенный группой галогена (например, 2-хлор) или C1-6 алкила (например, 2-метил), или -арил (например, фенил),дизамещенный группой галогена (например, 4-фтор) и C1-6 алкила (например, 2-метил). В следующем варианте воплощения R3 представляет собой -арил (например, фенил), дизамещенный группой галогена (например, 4-фтор) и C1-6 алкила (например, 2-метил) (например, 4-фтор-2 метилфенил). В следующем варианте воплощения R3 представляет собой -арил (например, фенил), монозамещенный C1-6 алкилом, замещенным одной или несколькими гидроксильными группами (например, СН 2 ОН),или -арил (например, фенил), дизамещенный галогеном (например, 2-хлор-4-фторфенил) или группой галогена (например, 5-фтор) и C1-6 алкила (например, 2-метил) (например, 5-фтор-2-метилфенил). В следующем варианте воплощения R3 представляет собой -гетероарил (например, пиридинил) монозамещенный C1-6 алкилом (например, 6-метилпиридин-3-ил), или -гетероарил (например, пиридинил),дизамещенный группой галогена (например, 4-фтор) и C1-6 алкила (например, 2-метил) (например, 4 фтор-2-метилпиридин-3-ил). В одном варианте воплощения R4 и R5 оба представляют собой C1-6 алкил (например, метил), или R4 5 и R вместе с атомом углерода, с которым они связаны, образуют C3-8 циклоалкильную (например, циклопропильную) группу. В следующем варианте воплощения, R4 и R5 оба представляют собой C1-6 алкил(например, метил). Еще в одном варианте воплощения R4 и R5 вместе с атомом углерода, с которым они связаны, образуют C3-8 циклоалкильную (например, циклопропильную) группу. В одном варианте воплощения s имеет значение 2, и обе группы R6 представляют собой галогенС 1-6 алкил (такие как трифторметильные группы, например, 3,5-бис(трифторметил. В одном варианте воплощения, когда р и q оба имеют значение 1, X представляет собой атом азота,Y представляет собой (-С(H2)-)2 и Z представляет собой атом кислорода, n имеет значение 1, R2 пред-4 013909 ставляет собой C1-6 алкил, замещенный гидроксильной группой, R3 представляет собой -арил, дизамещенный группой галогена и C1-6 алкила, R4 и R5 оба представляют собой C1-6 алкил и s имеет значение 2,где обе группы R6 представляют собой галогенС 1-6 алкил. В одном варианте воплощения, когда р и q оба имеют значение 1, X представляет собой атом азота,Y представляет собой (-С(Н 2 Н)-)2 и Z представляет собой -S(O2)-, n имеет значение 1, R2 представляет собой C1-6 алкил, замещенный гидроксильной группой, R3 представляет собой -арил, дизамещенный группой галогена и C1-6 алкила, R4 и R5 оба представляют собой C1-6 алкил и s имеет значение 2, где обе группы R6 представляют собой галогенС 1-6 алкил. В одном варианте воплощения, когда р и q оба имеют значение 1, X представляет собой азот, Y представляет собой (-С(Н 2)-)2 и Z представляет собой -N(RZ)-, n имеет значение 1, R2 представляет собойC1-6 алкил, замещенный гидроксильной группой, R3 представляет собой -арил, дизамещенный группой галоген и C1-6 алкил, R4 и R5 оба представляют собой C1-6 алкил и s имеет значение 2, где обе группы R6 представляют собой галогенС 1-6 алкил. Еще в одном варианте воплощения р и q оба имеют значение 1, n и m оба имеют значение 0, А представляет собой водород, X представляет собой азот, Y представляет собой (-C(H2)-)2, Z представляет собой -N(RZ)-, R3 представляет собой -арил, замещенный группой галогена и C1-6 алкила, R4 и R5 оба представляют собой C1-6 алкил, s имеет значение 2, где обе группы R6 представляют собой галогенС 1-6 алкил и RZ представляет собой -COR7, где R7 представляет собой C1-6 алкил. Соединения по настоящему изобретению включают примеры Е 1-Е 33, представленные ниже, или их фармацевтически приемлемые соли. Соединения по настоящему изобретению, кроме того, включают примеры Е 34-Е 40, представленные ниже, или их фармацевтически приемлемые соли. Соединения по настоящему изобретению, кроме того, включают примеры Е 41-Е 104, представленные ниже, или их фармацевтически приемлемые соли. В одном варианте воплощения настоящее изобретение обеспечивает соединение, выбранное из группы, включающей 2-[3,5-бис(трифторметил)фенил]-N-4-(4-фтор-2-метилфенил)-6-[(7S,9aS)-7-(гидроксиметил)гексагидропиразино[2,1-с][1,4]оксазин-8(1 Н)-ил]-3-пиридинил-N,2-диметилпропанамид,2-[3,5-бис(трифторметил)фенил]-N-4-(4-фтор-2-метилфенил)-6-[(7S,9aR)-7-(гидроксиметил)гексагидропиразино[2,1-с][1,4]оксазин-8(1 Н)-ил]-3-пиридинил-N,2-диметилпропанамид,2-[3,5-бис(трифторметил)фенил]-N-4-(4-фтор-2-метилфенил)-6-[(7S)-7-(гидроксиметил)-2,2 диоксидогексагидропиразино[2,1-с][1,4]тиазин-8(1 Н)-ил]-3-пиридинил-N,2-диметилпропанамид,N-[6-[(3S)-8-ацетил-3-(гидроксиметил)октагидро-2 Н-пиразино[1,2-а]пиразин-2-ил]-4-(4-фтор-2 метилфенил)-3-пиридинил]-2-[3,5-бис(трифторметил)фенил]-N,2-диметилпропанамид или его фармацевтически приемлемую соль. В следующем варианте воплощения настоящее изобретение обеспечивает 2-[3,5 бис(трифторметил)фенил]-N-4-(4-фтор-2-метилфенил)-6-[(7S,9aR)-7-(гидроксиметил)гексагидропиразино[2,1-е][1,4]оксазин-8(1 Н)-ил]-3-пиридинил-N,2-диметилпропанамид или его фармацевтически приемлемую соль. В следующем варианте воплощения настоящее изобретение обеспечивает N-[6-[(9aS или 9aR)-8 ацетилоктагидро-2 Н-пиразино[1,2-а]пиразин-2-ил]-4-(4-фтор-2-метилфенил)-3-пиридинил]-2-[3,5 бис(трифторметил)фенил]-N,2-диметилпропанамид (Энантиомер 2) или его фармацевтически приемлемую соль, где "Энантиомер 2" означает отдельный энантиомер с неизвестной абсолютной стереохимией,полученный в соответствии с примером 72, описанным ниже. Соединения формулы (I) могут образовывать кислотно-аддитивные соли с кислотами, такими как традиционные фармацевтически приемлемые кислоты, например малеиновая, хлористоводородная, бромистоводородная, фосфорная, уксусная, фумаровая, салициловая, серная, лимонная, молочная, миндальная, винная и метансульфоновая. Соли, сольваты и гидраты соединений формулы (I) поэтому составляют аспект настоящего изобретения. Как это использовано в настоящем описании, термин "соль" относится к любой соли соединения по настоящему изобретению, полученной из неорганической или органической кислоты или основания,четвертичным аммониевым солям и внутренне образованным солям. Физиологически приемлемые соли являются особенно подходящими для медицинского применения благодаря их лучшей водорастворимости по сравнению с исходными соединениями. Такие соли определенно должны содержать физиологически приемлемый анион или катион. Подходяще физиологически приемлемые соли соединений по настоящему изобретению включают кислотно-аддитивные соли, образованные с неорганическими кислотами, такими как хлористо-водородная, бромисто-водородная, иодисто-водородная, фосфорная, метафосфорная, азотная и серная кислоты, и с органическими кислотами, такими как винная, уксусная, трифторуксусная, лимонная, яблочная, молочная, фумаровая, бензойная, муравьиная, пропионовая, гликолевая, глюконовая, малеиновая, янтарная, камфорсерная, 2-оксиэтансульфоновая, слизевая, гентизиновая,изоникотиновая, сахарная, глюкуроновая, фуранкарбоновая, глутаминовая, аскорбиновая, антраниловая,салициловая, фенилуксусная, миндальная, эмбоновая (памовая), метансульфоновая, этансульфоновая,-5 013909 пантотеновая, стеариновая, сульфиниловая, альгиновая, галактуроновая и арилсульфоновая, например,бензолсульфоновая и п-толуолсульфоновая, кислоты; основно-аддитивные соли, образованные с щелочными металлами и щелочно-земельными металлами и органическими основаниями, такими как N,Nдибензилэтилендиамин, хлорпрокаин, холин, диэтаноламин, этилендиамин, меглумин (Nметилглюкамин), лизин и прокаин; и внутренне образованные соли. Соли, содержащие физиологически неприемлемый анион или катион, входят в объем настоящего изобретения как полезные промежуточные соединения для получения физиологически приемлемых солей и/или для использования в нетерапевтических, например in vitro, ситуациях. Настоящее изобретение также включает изотопно-меченные соединения, которые являются идентичными соединениям, указанным в формуле (I) и следующих, но у них один или несколько атомов замещены атомом, имеющим атомную массу или массовое число, отличные от атомной массы или массового числа, обычно существующих в природе. Примеры изотопов, которые могут быть включены в соединения по настоящему изобретению и их фармацевтически приемлемые соли, включают изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора, иода и хлора, такие как 2 Н, 3H, 11 С, 13 С, 14 С,15N, 17O, 18O, 31 Р, 32 Р, 35S, 18F, 36Cl, 123I и 125I. Соединения по настоящему изобретению и фармацевтически приемлемые соли таких соединений,которые содержат указанные выше изотопы и/или другие изотопы других атомов, входят в объем настоящего изобретения. Изотопно-меченные соединения по настоящему изобретению, например, соединения, в которые включены радиоактивные изотопы, такие как 3H, 14 С, являются полезными для применения в анализах распределения лекарственных средств и/или субстрата в тканях. Тритированные, т.е. 3H, и углерод-14, т.е. 14 С, изотопы являются особенно предпочтительными из-за простоты их получения и возможности их детекции. НС и 18F изотопы являются особенно полезными в PET (позитронэмиссионная томография), и 125I изотопы являются особенно полезными в SPECT (однофотонная эмиссионная компьютерная томография), все они полезны для снимков головного мозга. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2 Н, может дать некоторые терапевтические преимущества, благодаря их лучшей метаболической стабильности, например, большему периоду полураспада in vivo или потребности в более низких дозах, и, следовательно, в некоторых обстоятельствах могут быть предпочтительными. Изотопно меченные соединения формулы I и следующих по настоящему изобретению, как правило, могут быть получены путем осуществления процедур, раскрытых на схемах и/или в примерах ниже, путем замещения немеченного изотопом реагента легко доступным изотопно меченным реагентом. Некоторые соединения формулы (I) могут существовать в стереоизомерных формах. Должно быть понятно, что настоящее изобретение охватывает все геометрические и оптические изомеры таких соединений и их смеси, включая рацематы. Указывает стереоцентрустановившейся, но неизвестной стереохимии, т.е. либо R, либо S стереохимии. Диастереоизомер 1 или диастереоизомер 2 означает соединение по настоящему изобретению или его промежуточное соединение как отдельный диастереоизомер, абсолютная конфигурация которого по одному стереоцентру не определена. Энантиомер 1 или энантиомер 2 означает соединение по настоящему изобретению или его промежуточное соединение как отдельный энантиомер, абсолютная конфигурация которого не определена. Таутомеры также составляют аспект настоящего изобретения. Настоящее изобретение также обеспечивает способ получения соединения формулы (I) или его фармацевтически приемлемой соли, при этом способ включает:(а) взаимодействие соединения формулы (II) где R3, R4, R5, R6 и s определены выше и L1 представляет собой подходящую удаляемую группу, такую как атом галогена (например, хлора), с соединением формулы (III) или его необязательно защищенным производным, где R1, R2, m, n, p, q, X, Y, Z и А определены выше; необязательно, с последующим(с) взаимопреобразованием в другие соединения формулы (I). Когда р и q оба имеют значение 1, X представляет собой атом азота, Y представляет собой -С(=O)-6 013909 и Z представляет собой -С(Н 2)-, способ (а) можно осуществлять в присутствии подходящего основания,такого как карбонат калия, и подходящего растворителя, такого как ДМСО, при подходящей температуре, такой как 150-180 С. Когда р и q оба имеют значение 1, X представляет собой атом азота, Y представляет собой -С(Н 2)- иZ представляет собой -С(H2)-, способ (а) можно осуществлять в присутствии подходящего основания,такого как карбонат калия, и подходящего растворителя, такого как DMSO, при подходящей температуре, такой как 180 С, при микроволновом облучении. Когда р и q оба имеют значение 1, X представляет собой атом азота, Y представляет собой -С(Н 2)- иZ представляет собой -С(Н 2)-, n имеет значение 1, R2 представляет собой C1-6 алкил, замещенный гидроксильной группой (например, -СН 2-OH), способ (а) можно осуществлять в присутствии подходящего основания, такого как трет-бутоксид калия или карбонат цезия, подходящего растворителя, такого какDMSO, подходящего катализатора, такого как бис(дибензилиденацетон)палладий (0,05 экв.), подходящего лиганда, такого как дициклогексилфосфино-2'-(N,N-диметиламино)бифенил (0,125 экв.), при подходящей температуре, такой как 120 С, при микроволновом облучении; или в качестве альтернативы, способ а) можно осуществлять в присутствии подходящего основания, такого как карбонат калия, и подходящего растворителя, такого как ДМСО, при подходящей температуре, такой как температура в пределах от 110 до 160 С. Альтернативно, когда р и q оба имеют значение 1, X представляет собой атом азота, Y представляет собой -С(Н 2)- и Z представляет собой -С(Н 2)-, n имеет значение 1, R2 представляет собой C1-6 алкил, замещенный гидроксильной группой (например, -СН 2-OH), способ (а) можно осуществлять с использованием производного, где гидроксильная группа R2 является защищенной в виде O-TBDMS производного,в подходящем растворителе, таком как толуол, в присутствии подходящего катализатора, такого как бистри-трет-бутилфосфинпалладий, подходящего основания, такого как водный раствор гидроксида натрия,и подходящего катализатора фазового переноса, такого как водный раствор цетилтриметиламмонийхлорида, при температуре, такой как 80-95 С. После осуществления этого способа можно осуществить удаление TBDMS защитной группы с использованием тетрабутиламмонийфторида в подходящем растворителе, таком как ТГФ, или хлористо-водородной кислоты в подходящем растворителе, таком как метанол. Альтернативно, когда р и q оба имеют значение 1, X представляет собой азот, У представляет собой-(С(Н 2)-)2, Z представляет собой атом кислорода, -S(O2)- или -N(RZ), n имеет значение 1 и R2 представляет собой C1-6 алкил, замещенный гидроксильной группой (например, -CH2-ОН), способ (а) можно осуществлять с использованием производного, где гидроксильная группа R2 является защищенной в виде ОTBDMS производного, в подходящем растворителе, таком как толуол, в присутствии подходящего катализатора, такого как бис-три-трет-бутилфосфинпалладий, подходящего основания, такого как водный раствор гидроксида натрия, и подходящего катализатора фазового переноса, такого как водный раствор гексадецилтриметиламмонийхлорида, при температуре, такой как 80-95 С. После осуществления этого способа можно осуществить удаление TBDMS защитной группы с использованием тетрабутиламмонийфторида в подходящем растворителе, таком как ТГФ, или хлористо-водородной кислоты в подходящем растворителе, таком как метанол. Альтернативно, когда р и q оба имеют значение 1, X представляет собой азот, Y представляет собой-(С(Н 2)-)2, Z представляет собой атом кислорода или -N(RZ), n имеет значение 1 и R2 представляет собойC1-6 алкил или галогенС 1-6 алкил, способ (а) можно осуществлять в подходящем растворителе, таком как толуол, в присутствии подходящего катализатора, такого как бис-три-трет-бутилфосфинпалладий, подходящего основания, такого как водный раствор гидроксида натрия, и подходящего катализатора фазового переноса, такого как водный гексадецилтриметиламмонийхлорид, при температуре, такой как 8095 С. Альтернативно, когда р и q оба имеют значение 1, X представляет собой азот, Y представляет собой-СН 2-OH, способ (а) можно осуществлять в присутствии подходящего основания, такого как карбонат калия, и подходящего растворителя, такого как DMSO, при подходящей температуре, такой как 150 С. Когда р и q оба имеют значение 1, X представляет собой атом азота, Y представляет собой (-С(Н 22 и Z представляет собой атом кислорода, или когда р и q оба имеют значение 1, X представляет собой атом азота, Y представляет собой -S(O2)- и Z представляет собой -С(Н 2)-, или когда р имеет значение 1, q имеет значение 2, X представляет собой атом азота, Y представляет собой -С(Н 2)- и Z представляет собой-С(Н 2)-, или когда р имеет значение 2, q имеет значение 1, X представляет собой атом азота, Y представляет собой -С(Н 2)-, Z представляет собой -С(Н 2)-, n имеет значение 1 и R2 представляет собой =O, способ(а) типично осуществляют в присутствии подходящего основания, такого как карбонат калия, подходящего промотора реакции, такого как иодид меди, в подходящем растворителе, таком как DMSO, при подходящей температуре, такой как 150 С, при микроволновом облучении. Когда р имеет значение 1, q имеет значение 1, X представляет собой атом азота, Y представляет собой -С(Н 2)-, Z представляет собой -С(Н 2)-, n имеет значение 1 и R2 представляет собой =O, способ (а) типично осуществляют в присутствии N,N'-диметилэтилендиамина, подходящего основания, такого как карбонат цезия, подходящего промотора реакции, такого как иодид меди, в подходящем растворителе,-7 013909 таком как диоксан, при подходящей температуре, такой как 80-120 С. Когда р и q оба имеют значение 1, m и n оба имеют значение 0, X представляет собой атом азота, Y представляет собой (-С(Н 2)-)2 и Z представляет собой NH, способ (а) можно осуществлять в присутствии подходящего основания, такого как карбонат калия, и подходящего растворителя, такого как ДМСО, при подходящей температуре, такой как 130 С. В способе (b) примеры защитных групп и способов их удаления можно найти в Т. W. Greene Protective Groups in Organic Synthesis (J. Wiley и Sons, 1991). Подходящие аминозащитные группы включают сульфонил (например, тозил), ацил (например, ацетил, 2',2',2'-трихлорэтоксикарбонил, бензилоксикарбонил или трет-бутоксикарбонил) и арилалкил (например, бензил), которые можно удалить при помощи гидролиза (например, с использованием кислоты, такой как хлористо-водородная кислота в диоксане, или трифторуксусная кислота в дихлорметане), или путем восстановления (например, гидрогенолиз бензильной группы или восстановительное удаление 2',2',2'-трихлорэтоксикарбонильной группы с использованием цинка в уксусной кислоте), как это является подходящим. Другие подходящие аминозащитные группы включают трифторацетил (-COCF3), который можно удалить при помощи катализируемого основанием гидролиза или связанной на твердофазной смоле бензильной группы, такой как связанная на смоле Merrifield 2,6-диметоксибензильная группа (линкер Ellman), которую можно удалить при помощи катализируемого кислотой гидролиза, например с использованием трифторуксусной кислоты. Способ (с) можно осуществлять с использованием традиционных процедур взаимопреобразования,таких как эпимеризация, окисление, восстановление, алкилирование, нуклеофильное или электрофильное ароматическое замещение, гидролиз сложноэфирной группы, образование амидной связи или реакции сочетания, опосредованные переходным металлом. Примеры опосредованных переходным металлом реакций сочетания, используемых в качестве процедур взаимопреобразования, включают следующие: катализируемую палладием реакцию сочетания между органическими электрофилами, такими как арилгалогениды, и металлоорганическими реагентами, например бороновыми кислотами (реакции перекрестного сочетания Сузуки); катализируемые палладием реакции аминирования и амидирования между органическими электрофилами, такими как арилгалогениды, и нуклеофилами, такими как амины и амиды; катализируемые медью реакции амидирования между органическими электрофилами (такими как арилгалогениды) и нуклеофилами, такими как амиды; и опосредованные медью реакции сочетания между фенолами и бороновыми кислотами. Например, соединения формулы (I), где р и q оба имеют значение 1, m и n оба имеют значение 0, X представляет собой атом азота, Y представляет собой (-С(Н 2)-)2, Z представляет собой N(RZ) и RZ представляет собой COR7, можно получить из соединений формулы (I), где р и q оба имеют значение 1, m и n оба имеют значение 0, X представляет собой атом азота, Y представляет собой (-С(Н 2)-)2 и Z представляет собой NH, через ацилирование с использованием соответствующего хлорангидрида кислоты, в присутствии подходящего основания, такого как триэтиламин, в подходящем растворителе, таком как дихлорметан. Аналогичным образом, соединения формулы (I), где р и q оба имеют значение 1, m и n оба имеют значение 0, X представляет собой атом азота, Y представляет собой (-С(Н 2)-)2, Z представляет собой N(RZ) и RZ представляет собой SO2R7, можно получить из соединений формулы (I), где р и q оба имеют значение 1, m и n оба имеют значение О, X представляет собой атом азота, Y представляет собой(-С(H2)-)2 и Z представляет собой NH, через сульфонилирование с использованием соответствующего сульфонилхлорида, в присутствии подходящего основания, такого как триэтиламин, в подходящем растворителе, таком как дихлорметан. Соединения формулы (I), где р и q оба имеют значение 1, m и n оба имеют значение 0, X представляет собой атом азота, Y представляет собой (-C(H2)-)2, Z представляет собой N(RZ) и Rz представляет собой C1-6 алкил, можно получить из соединений формулы (I), где р и q оба имеют значение 1, m и n оба имеют значение 0, X представляет собой атом азота, Y представляет собой (С(Н 2)-)2 и Z представляет собой NH, через восстановительное алкилирование с использованием соответствующего альдегида, в подходящем растворителе, таком как ацетонитрил, с последующей обработкой триацетоксиборгидридом натрия. Соединения формулы (I), где р и q оба имеют значение 1, m имеет значение 0, n имеет значение 1, R2 представляет собой C1-6 алкилОС 1-6 алкил, X представляет собой атом азота, Y представляет собой (-С(Н 2)-)2, Z представляет собой -S(O)2-, можно получить из соединений формулы (I), где р и q оба имеют значение 1, m имеет значение 0, n имеет значение 1, R2 представляет собойC1-6 алкил, замещенный одной гидроксильной группой, X представляет собой атом азота, Y представляет собой (-С(Н 2)-)2 и Z представляет собой -S(O)2, через алкилирование с использованием подходящего алкилгалогенида, в присутствии основания, такого как гидрид натрия, в подходящем растворителе, таком как ТГФ. Соединения формулы (II) можно получить в соответствии с методикой, раскрытой в WO 2005/002577. Соединения формулы (III), где р и q оба имеют значение 1, m и n оба имеют значение 0, X представляет собой атом азота, Y представляет собой -S(O2)- и Z представляет собой -С(H2)-, можно получить в соответствии со следующей схемой: где Р 1 представляет собой подходящую защитную группу, такую как Boc. В типичном случае стадия (i) включает взаимодействие соединения формулы (IV) с метансульфонилхлоридом в присутствии подходящего растворителя, такого как дихлорметан, и подходящего основания, такого как триэтиламин. В типичном случае стадия (ii) включает взаимодействие соединения формулы (V) с вторбутиллитием в присутствии подходящего растворителя, такого как тетрагидрофуран. В типичном случае стадия (iii) включает реакцию удаления защиты, например, когда Р 1 представляет собой Boc, указанная реакция удаления защиты в типичном случае может включать взаимодействие соединения формулы (VI) со смесью дихлорметана и трифторуксусной кислоты. Соединения формулы (III), где р и q оба имеют значение 1, m имеет значение 0, n имеет значение 1,R2 представляет собой =O, X представляет собой атом азота, Y представляет собой -С(Н 2)- и Z представляет собой -С(Н 2)-, можно получить в соответствии со следующей схемой: где Р 2 представляет собой подходяще защитную группу, такую как трет-бутокси. В типичном случае стадия (i) включает взаимодействие в присутствии триацетоксиборгидрида натрия и подходящей кислоты, такой как хлористо-водородная кислота. В типичном случае стадия (ii) включает реакцию удаления защиты, например, когда Р 2 представляет собой трет-бутокси, указанная реакция удаления защиты, в типичном случае, может включать взаимодействие соединения формулы (VIII) со смесью дихлорметана и трифторуксусной кислоты, с последующей очисткой на SCX (сильный катионообменный) картридже с диоксидом кремния и нагреванием основных метанольных фракций, при подходящей температуре, такой как 40 С. Соединения формулы (III), где р и q оба имеют значение 1, m имеет значение 0, n имеет значение 1,R2 представляет собой =O, X представляет собой атом азота, Y представляет собой -С(H2)- и Z представляет собой -С(H2)- , также можно получить в соответствии со следующей схемой: где Р 2 представляет собой подходящую защитную группу, такую как трет-бутокси. В типичном случае стадия (i) включает взаимодействие с хлорацетилхлоридом в присутствии подходящего основания, такого как N,N-диизопропилэтиламин, в дихлорметане. В типичном случае стадия (ii) включает реакцию удаления защиты, например, когда Р 2 представляет собой трет-бутокси, указанная реакция удаления защиты типично может включать взаимодействие соединения формулы (X) со смесью дихлорметана и трифторуксусной кислоты, с последующей очисткой на SCX (сильный катионообменный) картридже с диоксидом кремния и нагреванием полученного промежуточного соединения с основанием, таким как карбонат натрия, в ацетонитриле, при подходящей температуре, такой как 60 С. Соединения формулы (III), где р имеет значение 1, q имеет значение 2, m имеет значение 0, n имеет значение 1, R2 представляет собой =O, X представляет собой атом азота, Y представляет собой -С(Н 2)- иZ представляет собой -С(Н 2)-, или где р имеет значение 1, q имеет значение 2, m и n оба имеют значение 0, X представляет собой атом азота, Y представляет собой -С(Н 2)- и Z представляет собой -С(Н 2)-, можно получить в соответствии со следующей схемой: где Р 3 представляет собой подходящую защитную группу, такую как Boc. В типичном случае стадия (i) включает взаимодействие с 1,1-диметилэтил(2-оксоэтил)карбаматом в присутствии триацетоксиборгидрида натрия, в подходящем растворителе, таком как 1,2-дихлорэтан. В типичном случае стадия (ii) включает реакцию удаления защиты, например, когда Р 3 представляет собой Boc, указанная реакция удаления защиты типично может включать взаимодействие соединения формулы (XII) с трифторуксусной кислотой в дихлорметане и затем очистку продукта на SCX (сильный катионообменный) картридже с диоксидом кремния. В типичном случае стадия (iii) включает нагревание промежуточного соединения, у которого ранее была удалена защита, в подходящем растворителе, таком как ацетонитрил, при подходящей температуре,такой как 60 С. В типичном случае стадия (iv) включает использование раствора комплекса борантетрагидрофуран, при подходящей температуре, такой как 0 С, с последующей обработкой водным раствором кислоты, такой как хлористо-водородная кислота, и очисткой на SCX (сильный катионообменный) картридже с диоксидом кремния. Соединения формулы (III), где р и q оба имеют значение 1, m имеет значение 0, n имеет значение 1,R2 представляет собой =O, X представляет собой атом азота, Y представляет собой (-С(Н 2)-)2 и Z представляет собой атом кислорода, можно получить в соответствии со следующей схемой: где Р 4 и Р 5 представляют собой подходящую защитную группу, такую как Boc. В типичном случае стадия (i) включает взаимодействие соединения формулы (XV) с раствором триметилсилилдиазометана при комнатной температуре. В типичном случае стадия (ii) включает реакцию удаления защиты, например, когда Р 4 представляет собой Boc, указанная реакция удаления защиты типично может включать взаимодействие соединений формул (XVI)а и (XVI)b с трифторуксусной кислотой в дихлорметане. В типичном случае стадия (iii) включает взаимодействие соединений формул (XVII)а и (XVII)b с Nboc-2-аминоацетальдегидом в присутствии триацетоксиборгидрида натрия, в подходящем растворителе,таком как 1,2-дихлорэтан. В типичном случае стадия (iv) включает реакцию удаления защиты, например, когда Р 5 представляет собой Boc, указанная реакция удаления защиты типично может включать взаимодействие соединений формул (XVIII)3 и (XVIII)b с трифторуксусной кислотой в дихлорметане, с последующей очисткой наSCX (сильный катионообменный) картридже с диоксидом кремния. В типичном случае, стадия (v) включает нагревание при подходящей температуре, такой как 40 С,соединений формул (XIX)а и (XIX)b в подходящем растворителе, таком как метанол.- 10013909 Соединения формулы (III), где р и q оба имеют значение 1, m и n оба представляют собой О, X представляет собой атом азота, Y представляет собой (-С(Н 2)-)2 и Z представляет собой -S(O2)-, можно получить в соответствии со следующей схемой: где Р 6 и Р 7 представляют собой подходящую защитную группу, такую как Boc. В типичном случае стадия (i) включает взаимодействие соединения формулы (XX) с МСРВА (3 хлорпербензойная кислота) в дихлорметане. В типичном случае стадия (ii) включает реакцию удаления защиты, например, когда Р 6 представляет собой Boc, указанная реакция удаления защиты типично может включать взаимодействие соединения формулы (XXI) с трифторуксусной кислотой в дихлорметане. В типичном случае стадия (iii) включает взаимодействие соединения формулы (XXII) с N-boc-2 аминоацетальдегидом в присутствии триацетоксиборгидрида натрия, в подходящем растворителе, таком как 1,2-дихлорэтан. В типичном случае стадия (iv) включает реакцию удаления защиты, например, когда Р 7 представляет собой Boc, указанная реакция удаления защиты типично может включать взаимодействие соединения формулы (XXIII) с трифторуксусной кислотой в дихлорметане с последующей очисткой на SCX (сильный катионообменный) картридже с диоксидом кремния. В типичном случае стадия (v) включает взаимодействие соединения формулы (XXIV) с раствором комплекса боран-тетрагидрофуран, при подходящей температуре, такой как 50 С, с последующей обработкой водным раствором кислоты, такой как хлористо-водородная кислота, и очисткой на SCX (сильный катионообменный) картридже с диоксидом кремния. Соединения формулы (III), где р и q оба имеют значение 1, n имеет значение 0, X представляет собой атом азота, Y представляет собой -С(H2)-, Z представляет собой -C(H2)-, m имеет значение 2 и обе группы R1 представляют собой фтор, можно получить в соответствии со следующей схемой: где Р 8 представляет собой подходящую защитную группу, такую как трет-бутоксикарбонил. В типичном случае стадия (i) включает взаимодействие с подходящим основанием, таким как бис(диметилэтилсилил)амид лития, в подходящем растворителе, таком как ТГФ, при подходящей температуре, такой как -78 С, а затем с подходящим агентом фторирования, таким как Nфторбензолсульфонимид. В типичном случае стадия (ii) включает реакцию удаления защиты, например, когда Р 8 представляет собой трет-бутоксикарбонил, указанная реакция удаления защиты типично может включать взаимодействие соединения формулы (XXVI) со смесью дихлорметана и трифторуксусной кислоты, с последующей очисткой на SCX (сильный катионообменный) картридже с диоксидом кремния. В типичном случае, стадия (iii) включает взаимодействие соединения формулы (XXVII) с раствором комплекса боран-тетрагидрофуран, при подходящей температуре, такой как 50 С, с последующей обработкой водным раствором кислоты, такой как хлористо-водородная кислота, и очисткой на SCX(сильный катионообменный) картридже с диоксидом кремния. Соединения формулы (III), где р и q оба имеют значение 1, m имеет значение О, X представляет собой атом азота, Y и Z оба представляют собой -С(Н 2)-, n имеет значение 1 и R2 представляет собой галогенС 1-6 алкил (например, фторэтил) можно получить в соответствии со следующей схемой: где Р 9 представляет собой подходящую защитную группу, такую как бензил. В типичном случае стадия (i) включает взаимодействие с агентом фторирования, таким как DAST(трифторид(диэтиламино)серы) в подходящем растворителе, таком как дихлорметан, при подходящей температуре, такой как комнатная температура. В типичном случае стадия (ii) включает реакцию удаления защиты, например, когда Р 9 представляет собой бензил, указанная реакция удаления защиты типично может включать взаимодействие соединения формулы (XXIX) с водородом в присутствии подходящего катализатора, такого как палладий на углероде, с последующей очисткой на SCX (сильный катионообменный) картридже с диоксидом кремния. Соединения формулы (I), где р имеет значение 0, q имеет значение 1, m имеет значение 0, n имеет значение 1, R2 представляет собой =O, X представляет собой атом азота и Y и Z оба представляют собой-С(Н 2)-, можно получить в соответствии со следующей схемой: где L1, R3, R4, R5, R6 и s определены выше и Р 10 представляет собой подходящую удаляемую группу,такую как Boc. В типичном случае стадия (i) включает взаимодействие с 1,1-диметилэтил 2-(аминометил)-1 пирролидинкарбоксилатом в подходящем растворителе, таком как DMSO, в присутствии подходящего основания, такого как карбонат калия, при подходящей температуре, такой как 180 С, в условиях микроволнового облучения. В типичном случае стадия (ii) включает реакцию удаления защиты, например, когда Р 10 представляет собой Boc указанная реакция удаления защиты типично может включать взаимодействие соединения формулы (-) со смесью дихлорметана и трифторуксусной кислоты, с последующей очисткой на SCX(сильный катионообменный) картридже с диоксидом кремния. В типичном случае стадия (iii) включает взаимодействие соединения формулы (XXXI) с трифосгеном в присутствии подходящего основания, такого как триэтиламин, при подходящей температуре, такой как комнатная температура. Соединения формулы (I), где р и q оба имеют значение 1, m имеет значение 0, n имеет значение 1,R2 представляет собой -CONH2, CO2H или CO2Et, X представляет собой атом азота и Y и Z оба представляют собой -С(Н 2)-, можно получить в соответствии со следующей схемой: где L1, R3 R4, R5, R6 и s определены выше, и R представляет собой NH2, ОН или OEt. В типичном случае стадия (i) включает взаимодействие с октагидропирроло[1,2-а]пиразин-3 карбоновой кислотой, амидом или сложным эфиром в присутствии подходящего основания, такого как триэтиламин, при подходящей температуре, такой как 150 С.- 12013909 Соединения формулы (III), где р и q оба имеют значение 1, X представляет собой азот, Y представляет собой -(С(Н 2)-)2, Z представляет собой атом кислорода, m имеет значение 0, n имеет значение 1 и R2 представляет собой C1-6 алкил, замещенный гидроксильной группой, защищенный в виде TBDMS производного, можно получить в соответствии со следующей схемой: В типичном случае стадия (i) включает взаимодействие карбоновой кислоты (XV) с амином формулы (XXXV) в подходящем растворителе, таком как дихлорметан, в присутствии подходящего агента сочетания, такого как тетрафторборат O-бензотриазол-1-ил-N,N,N',N'-тетраметилурония(TBTU) и подходящего основания, такого как диизопропилэтиламин, при подходящей температуре, такой как комнатная температура. В типичном случае стадия (ii) включает удаление защиты у соединения (XXXIV) с использованием подходящего реагента, такого как трифторуксусная кислота, с последующей очисткой на SCX (сильный катионообменный) картридже с диоксидом кремния и последующей циклизацией, при подходящей температуре, такой как 50 С. В типичном случае стадия (iii) включает восстановление соединения (XXXVI) с использованием подходящего восстановителя, такого как ВН 3-ТГФ, при подходящей температуре, такой как температура кипения с обратным холодильником. В типичном случае стадия (iv) включает взаимодействие соединения(III)k с третбутилдиметилсилилхлоридом (TBDMSCI) в подходящем растворителе, таком как дихлорметан, в присутствии подходящего основания, такого как триэтиламин, при подходящей температуре, такой как комнатная температура. Соединения формулы (III), где р и q оба имеют значение 1, X представляет собой азот, Y представляет собой -(С(Н 2)-)2, Z представляет собой атом кислорода, m имеет значение 0, n имеет значение 1 и R2 представляет собой C1-6 алкил, можно получить способом, аналогичным описанному выше, исходя из соответствующего амина вместо соединения формулы (XXXV) выше. Соединения формулы (III), где р и q оба имеют значение 1, X представляет собой азот, Y представляет собой - (С(H2)-)2, Z представляет собой -N(RZ)-, m имеет значение 0, n имеет значение 1 и R2 представляет собой C1-6 алкил, замещенный гидроксильной группой, защищенный в виде TBDMS производного, можно получить способом, аналогичным описанному выше, когда Z представляет собой атом кислорода, исходя из соответствующей карбоновой кислоты, где Z представляет собой N-P11 и Р 11 представляет собой подходящую защитную группу, такую как Boc. Соединения формулы (III), где RZ представляет собой C1-6 алкил, C1-6 алкокси, -COR7 или -SO2R7,можно получить из соединений формулы (III), где RZ представляет собой водород, в любой подходящий момент последовательности синтеза, например, после стадии (iv), через депротонирование с использованием подходящего основания, такого как триэтиламин, с последующим взаимодействием полученного аниона с RZ-L2, где L2 представляет собой подходящую удаляемую группу, такую как галоген, в стандартных условиях, описанных во многих стандартных пособиях по органической химии, таких какMarch, fifth edition (Wiley, 2001), включенных в настоящую заявку посредством ссылки. Соединения формулы (III), где р и q оба имеют значение 1, X представляет собой азот, Y представляет собой -(С(Н 2)-)2, Z представляет собой -N(RZ)-, m имеет значение 0, n имеет значение 1 и R2 представляет собой C1-6 алкил, можно получить способом, аналогичным описанному выше, когда Z представляет собой атом кислорода, исходя из соответствующей карбоновой кислоты, где Z представляет собойN-P11 и Р 11 представляет собой подходящую защитную группу, такую как Boc, и соответствующего амина вместо соединения формулы (XXXV) выше. Соединения формулы (III), где RZ представляет собой C1-6 алкил, C1-6 алкокси, -COR7 или -SO2R7, можно получить из соединения формулы (III), когда RZ представляет собой водород, в любой подходящий момент последовательности синтеза через депротонирование,с использованием подходящего основания, такого как триэтиламин, с последующим взаимодействием полученного аниона с RZ-L2, где L2 представляет собой подходящую удаляемую группу, такую как галоген, в стандартных условиях, описанных во многих стандартных пособиях по органической химии, таких как March's Advanced органической Chemistry: Reactions, Mechanisms and Structure by Michael B. Smithand Jerry March, fifth edition (Wiley, 2001), включенных в настоящую заявку посредством ссылки. Соединения формулы (III), где р и q оба имеют значение 1, X представляет собой азот, Y представляет собой -(С(Н 2)-)2, Z представляет собой -S(O2)-, n имеет значение 1 и R2 представляет собой C1-6 алкил, замещенный гидроксильной группой, защищенный в виде TBDMS производного, можно получить в соответствии со следующей схемой: В типичном случае стадия (i) включает взаимодействие карбоновой кислоты (XXXVII) с амином формулы (XXXV) в подходящем растворителе, таком как дихлорметан, в присутствии подходящего агента сочетания, такого как тетрафторборат O-бензотриазол-1-ил-N,N, N',N'-тетраметилурония(TBTU),и подходящего основания, такого как диизопропилэтиламин, при подходящей температуре, такой как комнатная температура. В типичном случае стадия (ii) включает удаление защиты у соединения (XXXVIII) с использованием подходящего реагента, такого как трифторуксусная кислота, с последующей очисткой на SCX (сильный катионообменный) картридже с диоксидом кремния и последующей циклизацией в подходящих условиях, таких как микроволновое облучение. В типичном случае стадия (iii) включает окисление соединения (XXXIX) с использованием подходящего окислителя, такого как 3-хлорпероксибензойная кислота (m-СРВА), в подходящем растворителе,таком как дихлорметан, при подходящей температуре, такой как комнатная температура. В типичном случае стадия (iv) включает восстановление соединения (ХХХХ) с использованием подходящего восстановителя, такого как BH3-ТГФ, при подходящей температуре, такой как температура кипения с обратным холодильником. В типичном случае стадия (v) включает взаимодействие соединения(III)m с третбутилдиметилсилилхлоридом (TBDMSCl) в подходящем растворителе, таком как дихлорметан, в присутствии подходящего основания, такого как триэтиламин, при подходящей температуре, такой как комнатная температура. Соединения формулы (III), где р и q оба имеют значение 1, m имеет значение 0, n имеет значение 1,R2 представляет собой =O, X представляет собой атом азота, Y представляет собой (-С(Н 2)-)2 и Z представляет собой NH, можно получить в соответствии со следующей схемой:- 14013909 где Р 12 представляет собой подходящую защитную группу, такую как Boc. В типичном случае стадия (i) включает взаимодействие соединения формулы (XXXXI) с N-boc-2 аминоацетальдегидом в присутствии триацетоксиборгидрида натрия, в подходящем растворителе, таком как 1,2-дихлорэтан. В типичном случае стадия (ii) включает реакцию удаления защиты, например, когда Р 12 представляет собой Boc, указанная реакция удаления защиты типично может включать взаимодействие соединения формулы (XXXXII) с трифторуксусной кислотой в дихлорметане с последующей очисткой на SCX(сильный катионообменный) картридже с диоксидом кремния, с последующей циклизацией. Соединения формулы (III), где р и q оба имеют значение 1, m и n оба имеют значение О, X представляет собой атом азота, Y представляет собой (-С(Н 2)-)2 и Z представляет собой NH, можно получить из соединения формулы (III)n через восстановление с использованием подходящего восстановителя, такого как боран-ТГФ, при повышенной температуре, такой как 75 С, в подходящем растворителе, таком как ТГФ. Соединения формулы (III), где р и q оба имеют значение 1, m имеет значение 1, n имеет значение О,R1 представляет собой гидроксил, X представляет собой атом азота, Y представляет собой -С(H2) и Z представляет собой -С(Н 2), можно получить в соответствии со следующей схемой: В типичном случае стадия (i) включает взаимодействие соединения формулы (XXXXIII) с хлорацетилхлоридом в присутствии подходящего основания, такого как триэтиламин. В типичном случае стадия (ii) включает обработку соединения (XXXXIV) раствором аммиака в метаноле при комнатной температуре. В типичном случае стадия (iii) включает восстановление дикетопиперазина формулы (XXXXV) с использованием подходящего восстановителя, такого как LiAlH4, в подходящем растворителе, таком как ТГФ, при комнатной температуре. Соединения формулы (III), где р и q оба имеют значение 1, m и n оба имеют значение 0, X представляет собой атом азота, Y представляет собой -С(H2), Z представляет собой -С(H2) и А представляет собой CH2OH, можно получить в соответствии со следующей схемой: В типичном случае соединения формулы (XXXXVI) можно получить путем взаимодействия диэтиламиномалоната с 1,3-дибромпропаном в присутствии этоксида натрия, в подходящем растворителе, таком как этанол, при подходящей повышенной температуре, такой как температура кипения с обратным холодильником (стадия (i.- 15013909 В типичном случае стадию (ii) можно осуществлять через взаимодействие соединения (XXXXVI) с бромацетилбромидом в присутствии подходящего основания, такого как карбонат калия, при 0 С. В типичном случае стадия (iii) включает обработку соединения (XXXXVII) бензиламином в подходящем растворителе, таком как ацетонитрил, при комнатной температуре. В типичном случае стадия (iv) включает восстановление соединения (XXXXVIII) с использованием подходящего восстановителя, такого как LiAlH4, в подходящем растворителе, таком как ТГФ, при повышенной температуре, такой как температура кипения с обратным холодильником. В типичном случае стадия (v) включает удаление защиты в стандартных условиях, таких как обработка формиатом аммония и палладием на углероде, в подходящем растворителе, таком как метанол, при повышенной температуре, такой как температура кипения с обратным холодильником. Соединения формулы (III), где р и q оба имеют значение 1, m имеет значение 0, n имеет значение 1,R2 представляет собой СН 2 ОН, X представляет собой атом азота, Y представляет собой -С(H2), Z представляет собой -С(Н 2), можно получить в соответствии со следующей схемой: где Р 13 представляет собой подходящую защитную группу, такую как бензилоксикарбонил. В типичном случае стадию (i) можно осуществлять путем взаимодействия соединения формулы(ХХХХХ) с диэтилброммалонатом в присутствии основания, такого как карбонат калия, в подходящем растворителе, таком как ацетонитрил, при комнатной температуре. В типичном случае стадию (ii) можно осуществлять через удаление защиты у соединения(XXXXXI) в стандартных условиях, таких как взаимодействие в атмосфере водорода, в присутствии палладия на углероде, с последующей циклизацией при повышенной температуре, такой как 50 С. В типичном случае стадию (iii) можно осуществить через восстановление сложноэфирной группы соединения (XXXXXII) с использованием подходящего восстановителя, такого как LiBH4, в растворителе, таком как ТГФ, с последующим восстановлением амидкарбонильной группы с использованием подходящего реагента, такого как BH3-ТГФ, при повышенной температуре, такой как температура кипения с обратным холодильником. Соединения формулы (III), где р и q оба имеют значение 1, X представляет собой азот, Y представляет собой -(С(Н 2)-)2, Z представляет собой атом кислорода, m имеет значение 0, n имеет значение 1 и R2 представляет собой галогенС 1-6 алкил, можно получить из соединения формулы (III)k через защиту вторичного NH, например, с использованием бензильной группы, с последующим преобразованием гидроксиалкильной группы в галогенС 1-6 алкильную группу путем обработки агентом галогенирования, таким как DAST [трифторид(диэтиламино)серы], с последующим удалением защиты в стандартных условиях. Соединения формулы (III), где р имеет значение 1, q имеет значение 1, m имеет значение 0, n имеет значение 1, R2 представляет собой =O, X представляет собой атом азота, Y представляет собой -С(H2)- иZ представляет собой -С(H2)-, можно получить в соответствии со следующей схемой: где Р 14 представляет собой подходящую защитную группу, такую как Boc.- 16013909 В типичном случае стадию (i) можно осуществлять через взаимодействие соединения (XXXXXIII) с 1,1-диметилэтил (2-оксоэтил)карбаматом в присутствии триацетоксиборгидрида натрия, в подходящем растворителе, таком как 1,2-дихлорэтан. Стадия (ii) типично включает реакцию удаления защиты, например, когда Р представляет собойBoc, указанная реакция удаления защиты, в типичном случае, может включать взаимодействие соединения формулы (XXXXXIV) с трифторуксусной кислотой в дихлорметане, и затем очистку продукта наSCX (сильный катионообменный) картридже с диоксидом кремния. Промежуточное соединение, у которого была удалена защита, затем можно подвергнуть циклизации путем нагревания при подходящей температуре, такой как 40 С. Соединения формул (IV), (VII), (IX), (XI), (XV), (XX), (XXV), (XXVIII), (XXX), (XXXIII), (XXXV),(XXXVII), (XXXXI), (XXXXIII), (XXXXX) и (XXXXXIII) либо являются известными соединениями, либо их можно получить в соответствии с известными процедурами. Соединения формулы (I) и их фармацевтически приемлемые соли обладают аффинностью в отношении, и являются антагонистами, NK1 и NK3 рецептора и, таким образом, могут быть полезными для лечения психотических расстройств. В контексте настоящего изобретения термины, описывающие медицинские показания, используемые в настоящей заявке, классифицированы в Doagnistic and Statistical Manual of Mental Disorders, 4thDiseases, 10th Edition (ICD-10). Различные подтипы расстройств, указанные в настоящей заявке, рассматриваются как часть настоящего изобретения. Номера в скобках после перечисляемых ниже заболеваний относятся к классификационному коду в DSM-IV. В контексте настоящего изобретения термин "психотические расстройства" включает шизофрению,включая подтипы, такие как параноидного типа (295.30), дезорганизованного типа (295.10), кататонического типа (295.20), недифференцированного типа (295.90) и остаточного типа (295.60); расстройства по типу шизофрении (295.40); шизоаффективные расстройства (295.70), включая подтипы, такие как биполярного типа и депрессивного типа; бредовые расстройства (297.1), включая подтипы, такие как расстройства типа эротомании, мании величия, ревностного типа, типа преследования, соматического типа,смешанного типа и неустановленного типа; кратковременные психотические расстройства (298.8); совместные (разделяемые) психотические расстройства (297.3); психотические расстройства, являющиеся результатом общего медицинского состояния, включая подтипы с бредом и с галлюцинациями; индуцированные определенными веществами психотические расстройства, включая подтипы с бредом (293.81) и с галлюцинациями (293.82); и психотические расстройства, которые не определены более конкретно(298.9). Соединения формулы (I) и их фармацевтически приемлемые соли и их сольваты могут быть полезными для лечения следующих расстройств: депрессивных расстройств и расстройств настроения, включая сильный приступ депрессии, маниакальный эпизод, смешанный эпизод и гипоманиакальный эпизод; депрессивные расстройства, включая сильное депрессивное расстройство, дистимическое расстройство (300.4), депрессивное расстройство,которое не определено более конкретно (311); биполярные расстройства, включая биполярное расстройство I, биполярное расстройство II (повторяющиеся сильные приступы депрессии с гипоманиакальными эпизодами) (296.89), циклотимическое расстройство (301.13) и биполярное расстройство, которое не определено более конкретно (296.80); другие расстройства настроения, включая расстройство настроения,являющееся результатом общего медицинского состояния (293.83), которое включает подтипы с депрессивными признаками, с сильным приступом депрессивного типа, с маниакальными признаками и со смешанными признаками), индуцированные определенными веществами расстройства настроения(включая подтипы с депрессивными признаками, с маниакальными признаками и со смешанными признаками) и расстройства настроения, которые не определены более конкретно (296.90);. состояния тревоги, включая приступ паники; панические расстройства, включая панические расстройства без агорафобии (300.01) и панические расстройства с агорафобией (300.21); агорафобию; агорафобии без панических расстройств (300.22), специфические фобии (300.29, ранее - простые фобии),включая подтипы, такие как животного типа, типа природного окружения, типа кровь-инъекция-ранение,ситуационного типа и другого типа), социальные фобии (социальное тревожное расстройство, 300.23),обсессивно-компульсивные расстройства (300.3), расстройство, связанное с посттравматическим стрессом (309.81), острое стрессовое расстройство (308.3), генерализованное состояние тревоги (300.02), состояние тревоги, являющееся результатом общего медицинского состояния (293.84), индуцированное определенными веществами состояние тревоги, тревоги в результате разобщения (309.21), состояние тревоги в результате неприспособленности (309.24) и состояния тревоги, которые не определены более конкретно (300.00); расстройства, связанные с определенными веществами, включая расстройства, связанные с употреблением определенных веществ, такие как зависимость от веществ, тяга к определенному веществу и злоупотребление определенными веществами; индуцированные определенными веществами расстройства, такие как интоксикация определенными веществами, синдром отмены определенных веществ, ин- 17013909 дуцированный определенными веществами делириозный синдром, индуцированная определенными веществами персистентная деменция, индуцированное определенными веществами персистентное расстройство потери памяти, индуцированная определенными веществами психотическое расстройство,индуцированное определенными веществами расстройство настроения, индуцированная определенными веществами тревога, индуцированная определенными веществами сексуальная дисфункция, индуцированные определенными веществами расстройства сна и галюциногенное персистентное расстройство восприятия (Flashbacks); связанные с употреблением алкоголя расстройства, такие как алкогольная зависимость (303.90), злоупотребление алкоголем (305.00), алкогольная интоксикация (303.00), синдром отмены алкоголя (291.81), делириозный синдром в результате алкогольной интоксикации, делириозный синдром в результате отмены алкоголя, индуцированная алкоголем персистентная деменция, индуцированная алкоголем персистентное расстройство потери памяти, индуцированное алкоголем психотическое расстройство, индуцированное алкоголем расстройство настроения, индуцированная алкоголем тревога,индуцированная алкоголем сексуальная дисфункция, индуцированное алкоголем расстройство сна и связанные с алкоголем расстройства, которые не определены более конкретно (291.9); расстройства, связанные с амфетамином (или амфетамин-подобными веществами), такие как зависимость от амфетамина(304.40), злоупотребление амфетамином (305.70), амфетаминовая интоксикация (292.89), синдром отмены амфетамина (292.0), делириозный синдром в результате амфетаминовой интоксикации, амфетамининдуцированные психотические расстройства, амфетамин-индуцированные расстройства настроения,амфетамин-индуцированное беспокойство, амфетамин-индуцированная сексуальная дисфункция, амфетамин-индуцированные расстройства сна и связанные с амфетамином расстройства, которые не определены более конкретно (292.9); связанные с кофеином расстройства, такие как кофеиновая интоксикация(305.90), кофеин-индуцированное беспокойство, кофеин-индуцированные расстройства сна и связанные с кофеином расстройства, которые не определены более конкретно (292.9); связанные с гашишем расстройства, такие как зависимость от гашиша (304.30), злоупотребление гашишем (305.20), гашишная интоксикация (292.89), делириозный синдром в результате гашишной интоксикации, гашишиндуцированное психотическое расстройство, гашиш-индуцированное беспокойство и связанные с гашишем расстройства, которые не определены более конкретно (292.9); связанные с кокаином расстройства, такие как кокаиновая зависимость (304.20), злоупотребление кокаином (305.60), кокаиновая интоксикация (292.89), синдром отмены кокаина (292.0), делириозный синдром в результате кокаиновой интоксикации, кокаин-индуцированное психотическое расстройство, кокаин-индуцированное расстройство настроения, кокаин-индуцированное беспокойство, кокаин-индуцированная сексуальная дисфункция,кокаин-индуцированное расстройство сна и связанные с кокаином расстройства, которые не определены более конкретно (292.9); связанные с галюциногенами расстройства, такие как зависимость от галлюциногенов (304.50), злоупотребление галюциногенами (305.30), галюциногенная интоксикация (292.89),галюциногенные персистентные расстройства восприятия (Flashbacks) (292.89), делириозный синдром в результате галюциногенной интоксикации, галюциноген-индуцированное психотическое расстройство,галюциноген-индуцированное расстройство настроения, галюциноген-индуцированное беспокойство и связанные с галюциногенами расстройства, которые не определены более конкретно (292.9); связанные с ингалянтами расстройства, такие как зависимость от ингалянтов (304.60), злоупотребление ингалянтами(305.90), интоксикация ингалянтами (292.89), делириозный синдром в результате интоксикации ингалянтами, ингалянт-индуцированная персистентная деменция, ингалянт-индуцированное психотическое расстройство, ингалянт-индуцированное расстройство настроения, ингалянт-индуцированное беспокойство и связанные с ингалянтами расстройства, которые не определены более конкретно (292.9); связанные с никотином расстройства, такие как никотиновая зависимость (305.1), синдром отмены никотина (292.0) и связанные с никотином расстройства, которые не определены более конкретно (292.9); связанные с опиоидами расстройства, такие как опиоидная зависимость (304.00), злоупотребление опиоидами(305.50), опиоидная интоксикация (292.8 9), синдром отмены опиоидов (292.0), делириозный синдром в результате опиоидной интоксикации, опиоид-индуцированное психотическое расстройство, опиоидиндуцированное расстройство настроения, опиоид-индуцированная сексуальная дисфункция, опиоидиндуцированное расстройство сна и связанные с опиоидами расстройства, которые не определены более конкретно (292.9); связанные с фенциклидином (или фенциклидин-подобными средствами расстройства,такие как зависимость от фенциклидина (304.60), злоупотребление фенциклидином (305.90), фенциклидиновая интоксикация (292.89), делириозный синдром в результате фенциклидиновой интоксикации,фенциклидин-индуцированное психотическое расстройство, фенциклидин-индуцированное расстройство настроения, фенциклидин-индуцированное беспокойство и связанные с фенциклидином расстройства,которые не определены более конкретно (292.9); расстройства, связанные с седативными, снотворными или анксиолитическими средствами, такие как зависимость от седативных, снотворных или анксиолитических средств (304.10), злоупотребление седативными, снотворными или анксиолитическими средствами (305.40), интоксикация, вызванная седативными, снотворными или анксиолитическими средствами(292.8 9), синдром отмены седативных, снотворных или анксиолитических средств (292.0), делириозный синдром, связанный с седативными, снотворными или анксиолитическими средствами, делириозный синдром в результате отмены седативных, снотворных или анксиолитических средств, персистентная- 18013909 деменция, вызванная седативными, снотворными или анксиолитическими средствами, персистентное расстройство потери памяти, вызванное седативными, снотворными или анксиолитическими средствами,индуцированное седативными, снотворными или анксиолитическими средствами психотическое расстройство, индуцированное седативными, снотворными или анксиолитическими средствами расстройство настроения, индуцированное седативными, снотворными или анксиолитическими средствами беспокойство, индуцированная седативными, снотворными или анксиолитическими средствами сексуальная дисфункция, индуцированное седативными, снотворными или анксиолитическими средствами расстройство сна и связанные с седативными, снотворными или анксиолитическими средствами расстройства,которые не определены более конкретно (292.9); расстройства, связанные с зависимостью от нескольких средств, так как зависимость от нескольких средств (304.80); и другие (или неизвестные) расстройства,связанные с зависимостью от веществ, таких как анаболические стероиды, нитратные ингалянты и оксид азота; расстройства сна, включая первичные расстройства сна, такие как диссомнии, такие как первичная инсомния (307.42), первичная гиперсомния (307.44), нарколепсия (347), связанные с дыханием расстройства сна (780.59), связанные с циркадным ритмом расстройства сна (307.45) и диссомнии, которые не определены более конкретно (307.47); первичные расстройства сна, такие как парасомнии, такие как кошмарные сновидения (307.47), страхи во сне (307.46), хождение во сне (307.46), и парасомнии, которые не определены более конкретно (307.47); расстройства сна, связанные с другим психическим расстройством, такие как инсомния, связанная с другим психическим расстройством (307.42), и гиперсомния, связанная с другим психическим расстройством (307.44); расстройства сна, являющееся результатом общего медицинского состояния, в частности, беспокойный сон, связанный с такими заболеваниями, как неврологические расстройства, невропатическая боль, синдром усталых ног, сердечные и легочные заболевания; и индуцированное определенными веществами расстройство сна, включая подтипы, такие как типа инсомнии, типа гиперсомнии, типа парасомнии и смешанного типа; синдром апноэ во сне и синдром jet-lag: Расстройства питания, такие как нервная анорексия (307.1) включая подтипы, такие как ограничительного типа и обильная еда/слабительное средство; нервная булимия (307.51), включая подтипы с приемом слабительного средства и без слабительного средства; ожирение; компульсивное расстройство питания; неконтролируемый прием пищи; и расстройства питания, которые не определены более конкретно (307.50). Расстройства типа аутизма, включая аутистическое расстройство (299.00), расстройство Asperger(299.80), расстройство Rett (299.80), детское дезинтеграционное расстройство (299.10) и первазивное расстройство, которое не определено более конкретно (299.80, включая атипичный аутизм). Расстройство дефицита внимания/гиперактивности, включая подтипы, такие как объединенное расстройство дефицита внимания/гиперактивности (314.01), расстройство дефицита внимания/гиперактивности, преимущественно характеризующееся невниманием (314.00), расстройство дефицита внимания/гиперактивности импульсного типа (314.01) и расстройство дефицита внимания/гиперактивности, которое не определено более конкретно (314.9); гиперкинетическое расстройство; расстройства, связанные с нарушением поведения, такие как поведенческие расстройства, включая подтипы, возникающие в детском возрасте (321.81), в период полового созревания (312.82) и возникновение которых не установлено (312.89), оппозиционно-вызывающее поведение (313.81) и расстройства, связанные с нарушением поведения, которые не определены более конкретно; и расстройства, связанные с тиком, такие как расстройство Туретта (307.23). Расстройства изменения личности, включая подтипы, такие как расстройство изменения личности параноидного типа (301.0), расстройство изменения личности шизоидного типа (301.20), шизотипическое изменение личности (301,22), антисоциальное личностное расстройство (301.7), пограничное личностное расстройство (301,83), наигранное изменение личности (301.50), изменение личности по типу нарцисцизма (301,81), личностное расстройство, связанное с избеганием (301.82), зависимое личностное расстройство (301.6), обсессивно-компульсивное личностное расстройство (301.4) и личностное расстройство, которое не определено более конкретно (301.9). Улучшение познавательной способности, включая лечение нарушения познавательной способности при других заболеваниях, таких как шизофрения, биполярное расстройство, депрессия, другие психиатрические расстройства и психотические состояния, связанные с нарушением познавательной способности, например, болезнь Альцгеймера и сексуальные дисфункции, включая расстройства сексуального влечения, такие как гипоактивное сексуальное влечение (302.71) и сексуальное отвращение (302.79); нарушения сексуального возбуждения, такого как женское сексуальное возбуждение (302.72) и мужское сексуальное возбуждение (302.72); нарушения оргазма, такие как нарушение оргазма у женщин (302.73),нарушение оргазма у мужщин (302.74) и преждевременная эякуляция (302.75); сексуальные болевые расстройства, такие как диспареуния (302.76) и вагинизм (306.51); сексуальная дисфункция, которая не определена более конкретно (302.70); парафилии, такие как эксгибиционизм (302.4), фетишизм (302.81),фроттеуризм (302.89), педофилия (302.2), сексуальный мазохизм (302.83), сексуальный садизм (302.84),трансвеститный фетишизм (302.3), войеуризм (302.82) и парафилии, которые не определены более кон- 19013909 кретно (302.9); нарушения идентичности рода, такие как нарушения идентичности рода у детей (302.6) и нарушения идентичности рода у подростков или взрослых (302.85); и сексуальные расстройства, которые не определены более конкретно (302.9). Все из различных типов и подтипов расстройств, указанных в настоящей заявке, рассматриваются как часть настоящего изобретения. Таким образом, настоящее изобретение также обеспечивает соединение формулы (I) или его фармацевтически приемлемую соль для применения в качестве терапевтического вещества для лечения или профилактики указанных выше психотических расстройств, в частности шизофрении. Настоящее изобретение, кроме того, обеспечивает способ лечения шизофрении, который включает введение хозяину, нуждающемуся в этом, эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли. В другом аспекте настоящее изобретение обеспечивает применение соединения формулы (I) или его фармацевтически приемлемой соли для получения лекарственного средства для лечения шизофрении. Настоящее изобретение, кроме того, обеспечивает способ лечения или профилактики указанных выше расстройств у млекопитающих, включая человека, который включает введение пациенту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли. В другом аспекте настоящее изобретение обеспечивает применение соединения формулы (I) или его фармацевтически приемлемой соли для получения лекарственного средства, применяемого для лечения указанных выше расстройств. При использовании в терапии соединения формулы (I) обычно формулируют в стандартные фармацевтические композиции. Такие композиции можно получить с использованием стандартных процедур. Таким образом, настоящее изобретение также обеспечивает фармацевтическую композицию для применения для лечения указанных выше расстройств, которая содержит соединение формулы (I) или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель. Настоящее изобретение, кроме того, обеспечивает фармацевтическую композицию, которая содержит соединение формулы (I) или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для лечения или профилактики психотических расстройств: i) антипсихотическими средствами;ii) лекарственными средствами от экстрапирамидальных побочных эффектов, например антихолинергическими средствами (такими как бензтропин, бипериден, проциклидин и тригексифенидил), антигистаминными средствами (такими как дифенгидрамин) и допаминергическими средствами (такими как амантадин); iii) антидепрессантами; iv) анксиолитическими средствами; и v) средствами для улучшения познавательной способности, например ингибиторами холинэстеразы (такими как такрин, донепезил, ривастигмин и галантамин). Соединения по настоящему изобретению можно использовать в комбинации с антидепрессантами для лечения или профилактики депрессии и расстройств настроения. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для лечения или профилактики биполярного заболевания: i) стабилизаторами настроения; ii) антипсихотическими средствами и iii) антидепрессантами. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для лечения или профилактики беспокойств: i) анксиолитическими средствами; и ii) антидепрессантами. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для облегчения синдрома отмены никотина и уменьшения тяги к никотину: i) заменяющими никотин терапевтическими средствами, например сублингвальным препаратом никотин бетациклодекстрина и никотиновыми пластырями и ii) бупропионом. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для облегчения синдрома отмены алкоголя и уменьшения тяги к алкоголю: i) антагонистами рецептора NMDA, например акампросатом; ii) агонистами рецептора GABA, например, тетрабаматом; и iii) антагонистами опиоидного рецептора, например налтрексоном. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для облегчения синдрома отмены опиатов, синдром отмены и уменьшения тяги к опиату: i) агонистом опиоидного мю рецептора/антагонист опиоидного каппа рецептора, например, бупренофином; ii) антагонистами опиоидного рецептора, например, налтрексоном; и iii) сосудорасширяющими антигипертензивными средствами, например лофексидином. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для лечения или профилактики расстройств сна: i) бензодиазепинами, например темазепамом,лорметазепамом, эстазоламом и триазоламом; ii) небензодиазепиновыми снотворными, например золпидемом, зопиклоном, залеплоном и индипломом; iii) барбитуратами, например апробарбиталом, бутабарбиталом, пентобарбиталом, секобарбита и фенобарбиталом; iv) антидепрессантами; v) другими седатив- 20013909 ными-снотворными средствами, например хлоралгидратом и хлорметиазолом. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для лечения анорексии: i) средствами для стимуляции аппетита, например ципрогептидином; ii) антидепрессантами; iii) антипсихотическими средствами; iv) цинком; и v) пременстральными средствами, например пиридоксином и прогестеронами. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для лечения или профилактики булимии: i) антидепрессантами; ii) антагонистами опиоидного рецептора; iii) противорвотными средствами, например ондансетроном; iv) антагонистами рецептора тестостерона, например флутамидом; v) стабилизаторами настроения; vi) цинком и vii) пременстральными средствами. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для лечения или профилактики аутизма: i) антипсихотическими средствами; ii) антидепрессантами; iii) анксиолитическими средствами; и iv) стимуляторами, например метилфенидатом, амфетаминовыми препаратами и пемолином. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для лечения или профилактики ADHD: i) стимуляторами, например метилфенидатом, амфетаминовыми препаратами и пемолином; и ii) нестимуляторами, например ингибиторами повторного поглощения норэпинефрина (такими как атомоксетин), агонистами альфа 2 адренорецептора (такими как клонидин), антидепрессантами, модафинилом и ингибиторами холинэстеразы (такими как галантамин и донезипил). Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для лечения расстройств изменения личности: i) антипсихотическими средствами; ii) антидепрессантами; iii) стабилизаторами настроения; и iv) анксиолитическими средствами. Соединения по настоящему изобретению можно использовать в комбинации со следующими средствами для лечения или профилактики мужской сексуальной дисфункции: i) ингибиторами фосфодиэстеразы V, например варденафилом и силденафилом; ii) допаминовыми агонистами/ингибиторами транспорта допамина, например апоморфином и бупроприоном; iii) антагонистами альфа адренорецептора, например фентоламином; iv) агонистами простагландина, например алпростадилом; v) агонистами тестостерона, такими как тестостерон; vi) ингибиторами транспорта серотонина, например ингибиторами повторного поглощения серотонина; v) ингибиторами транспорта норадреналина, например ребоксетином, и vii) агонистами 5-НТ 1 А, например флибансерином. Соединения по настоящему изобретению можно использовать в комбинации с теми же средствами,которые указаны для мужской сексуальной дисфункции, для лечения или профилактики женской сексуальной дисфункции и, кроме того, агонистом эстрогена, такими как эстрадиол. Антипсихотические лекарственные средства включают типичные антипсихотические средства (например, хлорпромазин, тиоридазин, мезоридазин, флуфеназин, перфеназин, прохлорперазин, трифлуоперазин, тиотиксин, галоперидол, молиндол и локсапин); и нетипичные антипсихотические средства (например, клозапин, оланзапин, рисперидон, кветиапин, арипиразол, зипразидон и амисулприд). Антидепрессанты включают ингибиторы повторного поглощения серотонина (такие как циталопрам, эсциталопрам, флуоксетин, пароксетин и сертралин); двойные ингибиторы повторного поглощения серотонина/норадреналина (такие как венлафаксин, дулоксетин и милнаципран); ингибиторы повторного поглощения норадреналина (такие как ребоксетин); трициклические антидепрессанты (такие как амитриптилин, кломипрамин, имипрамин, мапротилин, нортриптилин и тримипрамин); ингибиторы моноаминоксидазы (такие как изокарбоксазид, моклобемид, фенелзин и транилципромин); и другие (такие как бупропион, миансерин, миртазапин, нефазодон и тразодон). Стабилизаторы настроения включают литий, натрий валпроат/валпроевая кислота/дивалпроекс,карбамазепин, ламотригин, габапентин, топирамат и тиагабин. Анксиолитические средства включают бензодиазепины, такие как алпразолам и лоразепам. Настоящее изобретение, таким образом, обеспечивает в следующем аспекте комбинацию, включающую соединение формулы (I) или его фармацевтически приемлемого производного вместе с дополнительным терапевтическим средством или средствами. Указанные выше комбинации можно удобным образом представить для использования в форме фармацевтического препарата, и, таким образом, фармацевтические препараты, включающие указанную выше комбинацию вместе с фармацевтически приемлемым носителем или эксципиентом, составляют следующий аспект настоящего изобретения. Отдельные компоненты таких комбинаций можно вводить либо последовательно, либо одновременно, в отдельных или объединенных фармацевтических препаратах. Когда соединение формулы (I) или его фармацевтически приемлемое производное применяют в комбинации со вторым терапевтическим средством, активным против того же заболевания, доза каждого соединения может отличаться от дозы этого соединения при его отдельном применении. Соответствующие дозы может легко определить специалист в данной области. Фармацевтическая композиция по настоящему изобретению, которую можно получить путем сме- 21013909 шивания, подходяще при температуре окружающей среды и атмосферном давлении, обычно может быть адаптирована для орального, парентерального или ректального введения и, как таковая, может быть в форме таблеток, капсул, пероральных жидких препаратов, порошков, гранул, лепешек, реструктурируемых порошков, растворов для инъекций или инфузий или суспензий или суппозиториев. Орально вводимые композиции, как правило, являются предпочтительными. Таблетки и капсулы для орального введения могут представлять собой единичную дозированную форму и могут содержать традиционные эксципиенты, такие как связующие, наполнители, лубриканты для таблетирования, дезинтегранты и приемлемые смачивающие вещества. На таблетки можно нанести покрытие в соответствии со способами, хорошо известными в обычной фармацевтической практике. Оральные жидкие препараты, могут быть, например, в форме водной или масляной суспензии, растворов, эмульсий, сиропов или эликсиров, или могут быть в форме сухого продукта для восстановления водой или другим подходящим носителем перед применением. Такие жидкие препараты могут содержать традиционные добавки, такие как суспендирующие вещества, эмульгаторы, неводные носители (которые могут включать пищевые масла), консерванты и, если это желательно, традиционные отдушки или красители. Для парентерального введения жидкие единичные дозированные формы получают с использованием соединения по настоящему изобретению или его фармацевтически приемлемой соли и стерильного носителя. Соединение, в зависимости от используемого носителя и концентрации, может быть либо суспендировано, либо растворено в носителе. При получении растворов соединение можно растворить для инъекции и стерилизовать при помощи фильтрации, затем ввести в подходящий флакон или ампулу и герметично закрыть. Удобно, когда адъюванты, такие как местный анестетик, консерванты и буферные вещества растворены в носителе. Для повышения стабильности композицию можно заморозить после заключения ее во флакон и воду удалить в вакууме. Парентеральные суспензии получают, по существу,тем же способом, за исключением того, что соединение суспендируют в носителе, а не растворяют, и стерилизацию нельзя осуществить путем фильтрования. Соединение можно стерилизовать путем воздействия этиленоксида перед суспендированием в стерильном носителе. Удобно, когда в композицию включают поверхностно-активное или смачивающее вещество, способствующее однородному распределению соединения. Композиции, подходящие для чрескожного введения, включают мази, гели и пластыри. Композиция может содержать от 0,1 до 99 мас.%, предпочтительно от 10 до 60 мас.% активного вещества в зависимости от способа введения. Доза соединения, применяемая для лечения указанных выше расстройств, обычно варьирует в зависимости от тяжести расстройства, массы тела субъекта, страдающего этим расстройством, и других подобных факторов. Однако в качестве общего указания подходящая единичная доза составляет от 0,05 до 1000 мг, более подходяще от 1,0 до 200 мг, и такие единичные дозы можно вводить более чем один раз в день, например два или три раза в день. Такую терапию можно проводить в течение нескольких недель или месяцев. Экспериментальная часть Представленные ниже описания и примеры иллюстрируют получение соединения по настоящему изобретению. Спектры ядерного магнитного резонанса (ЯМР) записывали на Varian Instruments при 300, 400 или 500 МГц, на Bruker Instrument при 300 МГц, химические сдвиги указаны в м.д.с использованием линии остаточного растворителя как внутреннего стандарта. Спектрограммы расщепления указаны как с синглет; д - дублет; т - триплет; кв - квартет; м - мультиплет; шир. - уширенный. Спектры ЯМР записывали при температуре в пределах от 25 до 90 С; при обнаружении более чем одного конформера химические сдвиги указываются для того, который присутствует в большем количестве. Масс-спектры (MS) определяли на тройном квадрупольном масс-спектрометре 4 II (Micromass UK) или на масс-спектрометреAgilent 1100 Series [LC/MS-ES (+): анализ осуществляли на Supelcosil ABZ + Plus (334,6 мм, 3 мкм)[вода +0,1% HCO2H] и 95% [CH3CN] в течение 5 мин, в завершение в этих же условиях в течение 2 мин; Т=40 С; скорость потока = 1 мл/мин; ЖХ/MC-ES(-): анализ осуществляли на Supelcosil ABZ + Plus+0,05% NH3 до 5% [вода +0,05% NH3] и 95% [CH3CN] в течение 5 мин, в завершение в этих же условиях в течение 2 мин; Т=40 С; скорость потока = 1 мл/мин]. В масс-спектрах указан только один пик в молекулярном ионном кластере. Оптические вращения определяли при 20 С с использованием устройстваJasco DIP360 (1 = 10 см, объем ячейки = 1 мл, =589 нм), если не указано иное. Флэш-хроматографию на силикагеле осуществляли на силикагеле 230-400 меш, поставляемом Merck AG Darmstadt, Germany, или на предварительно заполненных картриджах Varian Mega Be-Si, или на предварительно заполненных диоксидом кремния картриджах Biotage. ВЭЖХ (восходящая) относится к ВЭЖХ-анализу, осуществляемому на Luna C18 (подвижная фаза:Waters ZQ (один квадр.), MS-диапазон 100-1000. Данные, относящиеся к подвижной фазе UPLC: Градиент до пробоорганайзера А = H2O + 0,1% муравьиной кислоты Градиент после пробоорганайзера (отрегулирован для получения таких же показателей времени удерживания, как достигаемые до пробоорганайзера) кривая 6 = линейный градиент кривая 11 = изменение в конце ТСХ относится к тонкослойной хроматографии на 0,25-мм силикагелевых пластинах (60F-254Merck) при наблюдении с использованием УФ-света. Для фазового разделения, осуществляемого с использованием микрофильтровальных устройств: картридж фазового разделения с полипропиленовой фриттой от Whatman или Alltech. Средства для SCX: SCX-картриджи (загрузка 0,75 ммоль/г) от Varian. Растворы сушили над безводным сульфатом натрия. В тексте использованы следующие сокращения: AcOEt = этилацетат, СН = циклогексан, DCM = метиленхлорид, DIPEA = N,N-диизопропилэтиламин, DMF = N,N'-диметилформамид, Et2O = диэтиловый эфир, EtOH = этанол, МеОН = метанол, TEA = триэтиламин, ТГФ = тетрагидрофуран, TFA = трифторуксусная кислота, CH3CN= ацетонитрил, std = насыщенный. Указывает стереоцентр установившейся, но неизвестной стереохимии, т.е. либо R, либо S стереохимии. Диастереоизомер 1 или диастереоизомер 2 означает соединение по настоящему изобретению или его промежуточное соединение в виде отдельного диастереоизомера, абсолютная конфигурация которого по одному стереоцентру не определена. Энантиомер 1 или энантиомер 2 означает соединение по настоящему изобретению или его промежуточное соединение в виде отдельного энантиомера, абсолютная конфигурация которого не определена. 1-[3,5-Бис(трифторметил)фенил]циклопропанкарбоновую кислоту (400 мг, 1,34 ммоль) растворяли в дихлорметане (6 мл), добавляли оксалилхлорид (0,24 мл, 2,68 ммоль) с последующим добавлением диметилформамида (5 мкл, кат.). Раствор перемешивали в течение 3 ч. Раствор концентрировали в вакууме. Неочищенный продукт растворяли в толуоле, добавляли 6-хлор-4-(4-фтор-2-метилфенил)-3 пиридинамин (380 мг, 1,61 ммоль) с последующим добавлением диизопропилэтиламина (0,7 мл, 4 ммоль) и диметиламинопиридина (164 мг, 1,34 ммоль) и раствор нагревали при 100 С в течение ночи. Раствор добавляли к этилацетату, промывали насыщенным водным раствором NH4Cl и насыщенным солевым раствором и концентрировали в вакууме. Продукт выделяли хроматографией (диоксид кремния,циклогексан/EtOAc 90/10-80/20) в виде белого твердого вещества: 635 мг, 1,23 ммоль, выход 92%. МС(51,6 мкл, 1,2 ммоль) с последующим добавлением карбоната цезия (393 мг, 1,2 ммоль) и суспензию перемешивали в течение ночи). Суспензию распределяли между этилацетатом и насыщенным воднымNH4Cl и органическую фазу промывали насыщенным солевым раствором и концентрировали в вакууме. Продукт выделяли хроматографией (диоксид кремния, циклогексан/EtOAc 90/10-80/20) в виде белого твердого вещества: 300 мг, 0,56 ммоль, выход 93%. МС (ES/+): m/z=531 [M+H]+. ЯМР (ДМСО-d6):м.д. 8,34 (с, 1 Н), 7,88 (с, 1 Н), 7,70 (с, 2 Н), 7,40 (с, 1 Н), 7,06 (дд, 1 Н), 6,90 (м, 2 Н),2,97 (с, 3H), 2,11 (с,3H), 1,21-1,37 (м, 4 Н). 1,1-Диметилэтил (2R)-2-формил-1-пирролидинкарбоксилат (1 г, 5,02 ммоль) растворяли в 20 мл безводного дихлорэтана. Добавляли гидрохлорид метилглицината (0,95 г, 7,57 ммоль) с последующим добавлением через 30 мин триацетоксиборгидрида натрия (2,2 г, 10,38 ммоль). Реакционную смесь перемешивали в течение 8 ч при комнатной температуре. Реакционную смесь разбавляли метанолом с получением прозрачного раствора, который пропускали через SCX картридж. Продукт элюировали 1 М метанольным раствором аммиака. Продукт выделяли хроматографией (диоксид кремния, дихлорметан/метанол 95/5) в виде бесцветного масла: 800 мг, 2,94 ммоль. МС (ES/+): m/z=273 [M+H]+. ЯМР (CDCl3):м.д. 4,01 (ушир.с, 1 Н), 3,75 (с, 3H), 3,53-3,30 (м, 4 Н), 2,94-2,53 (м, 3H), 1,92-1,76 (м,3H), 1,48 (с, 9 Н).(2,5 мл) в течение 2 ч. Реакционную смесь загружали как таковую на SCX колонку и неосновные соединения вымывали метанолом. Нингидрин-положительные фракции, которые элюировали 1 М метанольным раствором аммиака, концентрировали в вакууме при 40 С в течение 30 мин, выделяя указанное в заголовке соединение в виде бледно-желтого масла: 410 мг, 2,92 ммоль, выход 99%. МС (ES/+): m/z=141 [M+H]+. ЯМР (ДМСО-d6):м.д. 3,69 (кв, 1 Н), 3,62-3,45 (м, 3H), 3,45-3,35 (м, 2 Н), 2,52 (т, 1 Н), 2,13-1,96 (м,2 Н), 1,85-1,72 (м, 1 Н), 1,50-1,37 (м, 1 Н). Описание 5. (9aS)-Гексагидро-1 Н-пирроло[1,2-d][1,4]диазепин-2(3H)-он (D5) Гидрохлорид метил (2S)-2-пирролидинилацетата (1,08 г, 6,04 ммоль) растворяли в 20 мл безводного дихлорэтана. Добавляли 1,1-диметилэтил (2-оксоэтил)карбамат (1,2 г, 7,25 ммоль) с последующим добавлением через 30 мин триацетоксиборгидрида натрия (2,68 г, 12,08 ммоль). Реакционную смесь перемешивали в течение 3 ч при комнатной температуре. Реакционную смесь разбавляли метанолом с получением прозрачного раствора, который пропускали через SCX картридж. Продукт элюировали 1 М метанольным раствором аммиака. Растворитель удаляли при пониженном давлении, оставляя продукт в виде бледно-желтого масла. Неочищенный продукт растворяли в метиленхлориде (20 мл) и обрабатывали трифторуксусной кислотой (5 мл) в течение 1 ч. Реакционную смесь загружали как таковую на SCX колонку и неосновные соединения вымывали метанолом. Нингидрин-положительные фракции, которые элюировали 1 М метанольным раствором аммиака, концентрировали. Остаток снова растворяли в ацетонитриле (20 мл) и перемешивали при 60 С в течение 2 ч. Растворитель удаляли при пониженном давлении и продукт очищали хроматографией (диоксид кремния, CH2Cl2/МеОН 95/5, Rf=0,4) и выделяли в виде белого твердого вещества: 315 мг, 2,04 ммоль, выход 34%. МС (ES/+): 155 [М+Н]+. ЯМР (ДМСО-d6):м.д. 7,50 (ушир.с, 1 Н), 3,35-3,21 (м, 1 Н), 3,05-2,95 (м, 2 Н), 2,56-2,43 (м, 2 Н),2,26-2,11 (м, 2 Н), 2,08-1,96 (м, 2 Н), 1,94-1,83 (м, 1 Н), 1,72-1,52 (м, 2 Н), 1,41-1,29 (м, 1 Н). Раствор комплекса боран-тетрагидрофуран (1 М, 17,8 мл) добавляли к раствору (9aS)-гексагидро 1 Н-пирроло[1,2-d][1,4]диазепин-2(3H)-она (D5; 160 мг, 1,04 ммоль) в тетрагидрофуране (5 мл) при 0 С и смесь перемешивали при комнатной температуре в течение 30 мин. Медленно добавляли 6 н водный раствор HCl (20 мл) при 0 С и раствор нагревали при 60 С в течение 4 ч. Растворитель удаляли при пониженном давлении и продукт выделяли при помощи элюирования 1 М метанольным раствором аммиака из К перемешиваемой суспензии N-Boc морфолин-2-карбоновой кислоты (991 мг, 4,29 ммоль) в 10 мл диэтилового эфира добавляли раствор триметилсилилдиазометана (4 мл, 2 М в гексане, 8 ммоль). После добавления метанола исходное вещество переходило в раствор и наблюдалось интенсивное выделение азота. Через 1 ч 30 мин ТСХ-анализ показал полное исчезновение исходного вещества. Растворитель удаляли при пониженном давлении, оставляя неочищенный продукт в виде масла (1,3 г), который содержал как ожидаемый метиловый эфир, так и триметилсилилметиловый эфир (МС (ES/+): m/z=268[M+Na]+, 146 [М-Вос]+, 340 [M+TMS+Na]+, 218 [M+TMS-Boc]+. Неочищенный продукт растворяли в метиленхлориде (10 мл) и обрабатывали трифторуксусной кислотой (2,5 мл) в течение 1 ч 30 мин. Свободные аминовые соединения получали, собирая нингидрин-положительные фракции, которые элюировали 1 М метанольным раствором аммиака из SCX колонки. После удаления растворителя неочищенный продукт (бледно-желтое масло, 670 мг, МС (ES/+): m/z=146 [M+H]+, 218 [M+TMS+H]+) подвергали взаимодействию с N-boc-2-аминоацетальдегидом (756 мг, 4,75 ммоль) в безводном 1,2-дихлорэтане (13 мл) в присутствии триацетоксиборгидрида натрия (1,8 г, 8,44 ммоль) в течение 16 ч в атмосфере азота. Реакци- 25013909 онную смесь разбавляли метанолом и загружали на SCX колонку. Фракции, которые элюировали 1 М метанольным раствором аммиака, концентрировали. Остаточное неочищенное масло (880 мг, МС (ES/+):m/z=289 [M+H]+, 361 [M+TMS+H]+) растворяли в безводном метиленхлориде (12 мл) и обрабатывали 4 мл TFA в течение 30 мин при 0 С и при комнатной температуре в течение 3 ч. Реакционную смесь загружали как таковую на SCX колонку и неосновные соединения вымывали метанолом. Нингидринположительные фракции, которые элюировали 1 М метанольным раствором аммиака, концентрировали. Остаток снова растворяли в метаноле (20 мл) и перемешивали при 40 С в течение 30 мин. Растворитель удаляли при пониженном давлении и продукт очищали хроматографией (диоксид кремния,CH2Cl2/МеОН 95/5, Rf=0,25) и выделяли в виде белого твердого вещества: получали 395 мг (2,53 ммоль). МС (ES/+): 157 [М+Н]+, 179 [M+Na]+. ЯМР (CDCl3):м.д. 5,77 (ушир.с, 1 Н), 4,32 (дд, 1 Н), 3,87 (ушир.д, 1 Н), 3,70 (т, 1 Н), 3,63 (тд, 1 Н),3,53 (т, 1 Н), 3,30-3,22 (м, 2 Н), 2,98-2,86 (м, 1 Н), 2,80 (д, 1 Н), 2,63 (тд, 1 Н), 2,49 (тд, 1 Н). Описание 8. 1,1-Диметилэтил 4-(метилсульфонил)-3-[(метилсульфонил)окси]метил-1 пиперазинкарбоксилат (D8) К раствору 4,65 г 1,1-диметилэтил 3-(гидроксиметил)-1-пиперазинкарбоксилата в 30 мл безводного дихлорметана в атмосфере N2 при 0 С добавляли 4,75 мл TEA с последующим медленным добавлением 3,7 мл метансульфонилхлорида. После 12 ч интенсивного перемешивания при комнатной температуре реакционную смесь забирали в дихлорметан/H2O, фазы разделяли и водную фазу обратно экстрагировали дихлорметаном. Собранные органические слои сушили над Na2SO4 и концентрировали в вакууме с получением неочищенного вещества, которое очищали хроматографией на диоксиде кремния, элюируя дихлорметаном/МеОН от 100/0 до 90/10 с получением 4 г чистого указанного в заголовке вещества в виде бесцветной пены. К раствору 4 г 1,1-диметилэтил 4-(метилсульфонил)-3-[(метилсульфонил)окси]метил-1 пиперазинкарбоксилата (D8) в 50 мл безводного ТГФ, в атмосфере N2 при -78 С, добавляли по каплям 11,8 мл 1 М втор-Bu-Li в ТГФ. Через 30 мин смеси давали медленно достичь комнатной температуры. Через 2,5 ч реакционную смесь гасили при помощи 20 мл воды, забирали в 100 мл этилацетата и фазы разделяли. Водную фазу обратно экстрагировали этилацетатом (250 мл). Собранные органические слои сушили над Na2SO4 и концентрировали в вакууме с получением неочищенного вещества, которое очищали хроматографией на диоксиде кремния, элюируя циклогексаном/EtOAc от 7/3/ до 6/4 с получением,после выпаривания растворителя, 2,438 г чистого указанного в заголовке вещества в виде белого твердого вещества. Rf (Су/ЕА 1/1)=0,45 МС (ES/+): 177 (М-Вос), 221 (M-iBu), 299 (M+Na+). 1 К раствору 1,5 г 1,1-диоксида 1,1-диметилэтил гексагидро-5 Н-изотиазоло[2,3-а]пиразин-5 карбоксилата (D9) в 20 мл безводного дихлорметана в атмосфере N2 при 0 С добавляли по каплям 5 млTFA и оставляли для взаимодействия при 0 С в течение 1 ч. Затем реакционную смесь упаривали в вакууме и неочищенное твердое вещество очищали при помощи 50 г SCX картриджа, с загрузкойDCM/MeOH, промывая DCM/MeOH, затем только МеОН; продукт выделяли, элюируя смесью 1 М NH3 в МеОН. После выпаривания растворителя получали 0,95 г чистого указанного в заголовке соединения в виде белого твердого вещества.DIPEA (1,34 мл, 7,5 ммоль) добавляли к раствору 1,1-диметилэтил (2S)-2-(аминометил)-1 пирролидинкарбоксилата (1 г, 5 ммоль) в 50 мл DCM; затем медленно добавляли хлорацетилхлорид(0,418 мл, 5,25 ммоль) и реакционную смесь перемешивали в течение 1 ч, а затем подергали обработке. Добавляли DCM и органическую фазу промывали насыщенным раствором хлорида аммония. Неочищенный продукт очищали флэш-хроматографией, элюируя смесью циклогексан/этилацетат 8/2, с получением 1,24 г указанного в заголовке вещества. МС (ES/+): 299-301 [M+Na]+. ЯМР (CDCl3):м.д. 8,43-8,28 (ушир.с, 1 Н), 4,03 (с, 2 Н), 3,76-3,65 (м, 1 Н), 3,31-3,14 (м, 3H), 3,153,04 (м, 1 Н), 1,89-1,60 (м, 4 Н), 1,40 (с, Н). Описание 12. (8aS)-Гексагидропирроло[1,2-а]пиразин-3(4 Н)-он (D12) 1,1-Диметилэтил (2S)-2-[(хлорацетил)амино]метил-1-пирролидинкарбоксилат (D11; 1,24, 4,5 ммоль) растворяли в 20 мл DCM и обрабатывали TFA (5 мл) при комнатной температуре. Через 1 ч наблюдали полное преобразование в желаемое вещество и реакционную смесь загружали на SCX картридж. Продукт, полученный после элюирования 2 М NH3 в МеОН затем растворяли в ацетонитриле (30 мл) и обрабатывали карбонатом натрия (1,43 г, 10,34 ммоль). Реакционную смесь нагревали при 60 С в течение 6 ч; неочищенный извлеченный продукт очищали флэш-хроматографией, элюируя смесью дихлорметан/МеОН 95/5, с получением 310 мг. МС (ES/+): 141 [М+Н]+ ЯМР (CDCl3):м.д. 7,80-7,59 (ушир.с, 1 Н), 3,38 (д, 1 Н), 3,28-3,17 (м, 1 Н), 2,99 (дт, 1 Н), 2,89 (т, 1 Н),2,69 (д, 1 Н), 2,30-2,17 (м, 1 Н), 2,06-1,96 (м, 1 Н), 1,92-1,80 (м, 1 Н), 1,81-1,71 (м, 2 Н), 1,41-1,29 (м, 1 Н). Описание 13. 1,1-Диметилэтил (2R)-2-[(хлорацетил)амино]метил-1-пирролидинкарбоксилатDIPEA (1,34 мл, 7,5 ммоль) добавляли к раствору 1,1-диметилэтил (2R)-2-(аминометил)-1 пирролидинкарбоксилата (1 г, 5 ммоль) в 50 мл DCM; затем медленно добавляли хлорацетилхлорид(0,418 мл, 5,25 ммоль) и реакционную смесь перемешивали в течение 1 ч, а затем подергали обработке. Добавляли DCM и органическую фазу промывали насыщенным раствором хлорида аммония. Неочищенный продукт очищали флэш-хроматографией, элюируя смесью циклогексан/этилацетат 8/2, с получением 1,28 г указанного в заголовке вещества. МС (ES/+): 299-301 [M+Na]+ ЯМР (CDCl3):м.д. 8,43-8,28 (ушир.с, 1 Н), 4,03 (с, 2 Н), 3,76-3,65 (м, 1 Н), 3,31-3,14 (м, 3H), 3,153,04 (м, 1 Н), 1,89-1,60 (м, 4 Н), 1,40 (с, Н). Описание 14. (8aR)-Гексагидропирроло[1,2-а]пиразин-3(4 Н)-он (D14) 1,1-Диметилэтил (2R)-2-[(хлорацетил)амино]метил-1-пирролидинкарбоксилат (D13; 1,24 г, 4,5 ммоль) растворяли в 20 мл DCM и обрабатывали TFA (5 мл) при комнатной температуре. Через 1 ч наблюдали полное преобразование в желаемое вещество и реакционную смесь загружали на SCX картридж. Продукт, полученный после элюирования 2 М NH3 в МеОН, затем растворяли в ацетонитриле (30 мл) и обрабатывали карбонатом натрия (1,43 г, 10,34 ммоль). Реакционную смесь нагревали при 60 С в течение 6 ч; неочищенный извлеченный продукт очищали флэш-хроматографией, элюируя смесью дихлорметан/МеОН 95/5, с получением 250 мг желаемого соединения. МС (ES/+): 141 [М+Н]+ ЯМР (CDCl3):м.д. 7,80-7,59 (ушир.с, 1 Н), 3,38 (д, 1 Н), 3,28-3,17 (м, 1 Н), 2,99 (дт, 1 Н), 2,89 (т, 1 Н),- 27013909 2,69 (д, 1 Н), 2,30-2,17 (м, 1 Н), 2,06-1,96 (м, 1 Н), 1,92-1,80 (м, 1 Н), 1,81-1,71 (м, 2 Н), 1,41-1,29 (м, 1 Н). Описание 15. 4-(1,1-Диметилэтил) 3-метил 3,4-тиоморфолиндикарбоксилат 1,1-диоксид (D15) Получение осуществляли в две партии. В первой к перемешиваемому раствору 4-(1,1-диметилэтил) 3-метил 3,4-тиоморфолиндикарбоксилата (WO 2001/040185) (936 мг, 3,59 ммоль) в 3 мл дихлорметана добавляли 55% 3-хлорпербензойную кислоту (2,353 г, 7,50 ммоль) при 0 С при перемешивании в атмосфере азота. Реакционной смеси давали достичь комнатной температуры в течение 1 ч. Добавляли дополнительную аликвоту 55% 3-хлорпербензойной кислоты (500 мг, 1,59 ммоль) и реакционную смесь перемешивали в течение 15 мин. Реакционный раствор промывали насыщенным водным раствором бикарбоната натрия и тиосульфатом натрия. Органическую фазу сушили над Na2SO4 и растворитель удаляли, оставляя неочищенный продукт, 1,01 г. Во второй партии использовали ту же процедуру для преобразования 714 мг (3,59 ммоль) 4-(1,1-диметилэтил) 3-метил 3,4-тиоморфолиндикарбоксилата с использованием 2,134 г 55% 3-хлорпербензойной кислоты (6,80 ммоль) в 5 мл дихлорметана с получением 1,23 г неочищенного продукта. Объединенные неочищенные реакционные продукты очищали хроматографией К раствору 1,1-диоксид 4-(1,1-диметилэтил) 3-метил 3,4-тиоморфолиндикарбоксилата (D15; 1,73 г,5,9 ммоль) в 17 мл безводного метиленхлорида добавляли по каплям при перемешивании трифторуксусную кислоту (4,2 мл) при 0 С в атмосфере азота. Раствор перемешивали в течение 3 ч, давая ему при этом достичь комнатной температуры. Растворитель удаляли при пониженном давлении и остаток загружали на SCX картридж, промывали метанолом и элюировали при помощи 0,5 М метанольного раствора аммиака. Основные фракции собирали и растворитель удаляли, оставляя 1,08 г целевого продукта. МС (ES/+): 194 [M+Na]+. ЯМР (ДМСО-d6):м.д. 4,14-3,92 (ушир.с, 1 Н), 3,84-3,70 (дд, 1 Н), 3,65-3,59 (с, 3H), 3,34-13,15 (м,2 Н), 3,11-2,99 (м, 1 Н), 3,11-2,78 (м, 2 Н), 3,05-2,80 (м, 1 Н). Описание 17. Метил 4-[2-([(1,1-диметилэтил)окси]карбониламино)этил]-3-тиоморфолинкарбоксилат 1,1-диоксид (D17) К перемешиваемому раствору 1,1-диоксида метил 3-тиоморфолинкарбоксилата (D16; 1,08 г, 5,6 ммоль) в 14 мл безводного 1,2-дихлорэтана добавляли N-boc-2-аминоацетальдегид (1,1 г, 6,7 ммоль) и уксусную кислоту (0,316 мл, 5,6 ммоль). Через 30 мин добавляли триацетоксиборгидрид натрия (1,78 г,8,4 ммоль) и раствор перемешивали при комнатной температуре. Добавляли дополнительные аликвотыN-boc-2-аминоацетальдегида и триацетоксиборгидрида натрия (1,0 г, 4,7 ммоль) и реакцию продолжали в течение ночи. Растворитель удаляли при пониженном давлении и остаток очищали на SCX колонке с последующей хроматографией (диоксид кремния, циклогексан:этилацетат 70:30 до 1:1) и снова SCX, с получением 295 мг целевого соединения. МС (ES/+): 337 [М+1]+. ЯМР (ДМСО-d6):м.д. 6,77-6,55 (м, 1 Н), 4,17-4,08 (м, 1 Н), 3,69-3,57 (с, 3H), 3,48-3,31 (м, 3H), 3,172,89 (м, 5 Н), 2,80-2,71 (м, 1 Н), 2,70-2,61 (м, 1 Н), 1,44-1,29 (с, 9 Н). Описание 18. Гексагидропиразино[2,1-с][1,4]тиазин-9(6 Н)-он 2,2-диоксид (D18) К раствору 1,1-диоксида метил 4-[2-([(1,1-диметилэтил)окси]карбониламино)этил]-3-тиомор- 28013909 фолинкарбоксилата (D17; 295 мг, 0,88 ммоль) в 3 мл безводного дихлорметана добавляли 1 мл трифторуксусной кислоты и полученный раствор перемешивали при комнатной температуре в атмосфере азота в течение 1 ч 30 мин. Растворитель удаляли при пониженном давлении и остаток загружали на SCX колонку, промывали метанолом и элюировали раствором аммиака в метаноле. Продукт затем очищали хроматографией (картридж с диоксидом кремния, циклогексанэтилацетат, затем дихлорметандихлорметан: метанол 70:30) с получением 165 мг целевого соединения. МС (ES/+): 205 [М+1]+. ЯМР (ДМСО-d6):м.д. 8,14-8,08 (ушир.с, 1 Н), 3,36-3,27 (м, 2 Н), 3,26-3,19 (м, 2 Н), 3,19-3,15 (м, 1 Н), 3,133,04 (м, 3H), 2,99-2,92 (дд, 1 Н), 2,68-2,61 (м, 1 Н), 2,59-2,52 (дт, 1 Н). Описание 19. Октагидропиразино[2,1-с][1,4]тиазин 2,2-диоксид (D19) К суспензии 2,2-диоксида гексагидропиразино[2,1-с][1,4]тиазин-9(6 Н)-она (D18; 165 мг, 0,81 ммоль) в 1 мл безводного ТГФ добавляли последовательно аликвоты 1 М раствора комплекса боран-ТГФ в ТГФ (всего 20,4 мл, 20,4 ммоль) и реакционную смесь перемешивали при комнатной температуре и 50 С, вплоть до исчезновения исходного вещества. К раствору добавляли хлористоводородную кислоту(5 М, 2 мл) и перемешивание продолжали при 50 С в течение 12 ч. Растворитель удаляли при пониженном давлении и остаток загружали на SCX картридж, промывали метанолом и элюировали при помощи 0,5 М метанольного раствора аммиака. Основные фракции собирали и растворитель удаляли, оставляя 172 мг целевого продукта, частично загрязненного исходным веществом. МС (ES/+): 191 [М+1]+. ЯМР (CD3OD):(м.д.): 3,50-2,70 (м, 13 Н), 2,42-2,33 (дт, 1 Н). Описание 20. (7R,9aR)-7-(Гидроксиметил)гексагидропиразино[2,1-с][1,4]оксазин-6,9-дион иN-Boc морфолин 2-карбоновую кислоту (Astatech, 1,34 г, 5,80 ммоль) суспендировали в 15 мл безводного дихлорметана и обрабатывали тетрафторборатомO-бензотриазол-1-ил-N,N,N',N'тетраметилурония (TBTU) (2,4 г, 7,47 ммоль) и диизопропилэтиламином (2 мл, 11,47 ммоль). Реакционную смесь перемешивали в течение 40 мин. Получали раствор гидрохлорида D-серинметилового эфира(1,8 г, 11,57 ммоль) и диизопропилэтиламина (2 мл, 11,47 ммоль) в дихлорметане (15 мл) и добавляли к реакционной смеси. Реакционную смесь оставляли для перемешивания при комнатной температуре в течение ночи. UPLC-MS анализ показал преобразование в продукт. Реакционную смесь разбавляли дихлорметаном (40 мл) и экстрагировали насыщенным раствором NaHCO3 (240 мл), сушили (Na2SO4) и растворитель удаляли. Неочищенный продукт использовали на следующей стадии без дополнительной очистки. Продукт растворяли в 20 мл дихлорметана и обрабатывали 10 мл TFA. Реакционную смесь перемешивали при комнатной температуре и анализировали при помощи UPLC-MS через 4 ч, при этом анализ показал исчезновение пика исходного вещества, который был заменен новым, характерным для соединений с удаленными защитными группами (m/z=233, M+1). Реакционную смесь загружали как таковую на SCX картридж, промывали при помощи МеОН (4 объема колонки) и элюировали при помощи 0,5 М метанольного раствора аммиака. Основные, нингидрин-положительные фракции, собирали и растворитель удаляли. Остаток растворяли в 10 мл МеОН и перемешивали при 50 С в атмосфере N2 в течение ночи (16 ч). Реакционную смесь охлаждали и происходило образование осадка, который собирали фильтрованием с получением 370 мг указанного в заголовке соединения. Прямой МС: m/z=223 (M+Na). 1 Н-ЯМР: согласуется со структурой. Примерно 60:40 соотношение диастереоизомеров: 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 8,17-8,26 (с, 0,4 Н), 8,09-8,17 (с, 0,6 Н), 5,17-5,25 (м, 0,4 Н), 5,095,17 (м, 0,6 Н), 3,95-4,29 (м, 3H), 3,60-3,91 (м, 3H), 3,33-3,55 (м, 2 Н), 2,61-2,90 (м, 0,6 Н), 1,03-1,15 (т, 0,4 Н). Описание 21.(7R,9aR)-7-(Гидроксиметил)гексагидропиразино[2,1-с][1,4]оксазин-6,9-дион и (7R,9aS)-7-(гидроксиметил)гексагидропиразино[2,1-с][1,4]оксазин-6,9-дион (D20) (365 мг, 1,82 ммоль) обрабатывали при помощи 20 мл 1 М ВН 3-ТГФ раствора при комнатной температуре. Суспензию кипятили с обратным хо- 29
МПК / Метки
МПК: A61K 31/4439, A61K 31/4985, C07D 498/04, C07D 513/04, C07D 487/04, A61K 31/542, A61K 31/5383, A61P 25/00, A61K 31/551
Метки: лечения, применение, психотических, пиридиновые, расстройств, производные
Код ссылки
<a href="https://eas.patents.su/30-13909-piridinovye-proizvodnye-i-ih-primenenie-dlya-lecheniya-psihoticheskih-rasstrojjstv.html" rel="bookmark" title="База патентов Евразийского Союза">Пиридиновые производные и их применение для лечения психотических расстройств</a>












