Имидазохинолины в качестве ингибиторов липидкиназы
Номер патента: 13434
Опубликовано: 30.04.2010
Авторы: Фюре Паскаль, Штауффер Фредерик, Гарсиа -Эчеверриа Карлос
Формула / Реферат
1. Соединение формулы (I)
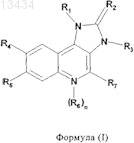
в которой R1 представляет собой нафтил или фенил, где указанный фенил замещен одним или двумя заместителями, независимо выбранными из группы, включающей
галоген;
C1-C7-алкил, незамещенный или замещенный галогеном, циано, имидазолилом или триазолилом;
циклоалкил;
амино, замещенный одним или двумя заместителями, независимо выбранными из группы, включающей C1-C7-алкил, C1-C7-алкилсульфонил, C1-C7-алкокси и С1-C7-алкокси-C1-C7-алкиламино;
пиперазинил, незамещенный или замещенный одним или двумя заместителями, независимо выбранными из группы, включающей C1-C7-алкил и C1-C7-алкилсульфонил;
2-оксопирролидинил;
C1-C7-алкокси-C1-C7-алкил;
имидазолил;
пиразолил;
и триазолил;
R2 представляет собой О или S;
R3 представляет собой C1-C7-алкил;
R4 представляет собой пиридил, незамещенный или замещенный галогеном, циано, C1-C7-алкилом, C1-C7-алкокси, или пиперазинил, незамещенный или замещенный C1-C7-алкилом;
пиримидинил, незамещенный или замещенный C1-C7-алкокси;
хинолинил, незамещенный или замещенный галогеном; или
хиноксалинил;
R5 представляет собой водород или галоген;
n представляет собой 0 или 1;
R6 представляет собой оксидо;
при условии, что если n=1, то атом азота, несущий радикал R6, имеет положительный заряд;
R7 представляет собой водород или амино;
или его таутомер или фармацевтически приемлемая соль, или его гидрат или сольват.
2. Соединение формулы (I), которое выбрано из группы, включающей
2-метил-2-[4-(3-метил-2-оксо-8-пиридин-4-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил] пропионитрил;
2-метил-2-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил] пропионитрил;
2-{4-[8-(6-метоксипиридин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил}-2-метилпропионитрил;
2-{4-[8-(5-метоксипиридин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил}-2-метилпропионитрил;
2-метил-2-{4-[3-метил-2-оксо-8-(6-пиперазин-1-илпиридин-3-ил)-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил}пропионитрил;
2-метил-2-(4-{3-метил-8-[2-(4-метилпиперазин-1-ил)пиридин-4-ил]-2-оксо-2,3-игидроимидазо[4,5-с]хинолин-1-ил}фенил)пропионитрил;
2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил] пропионитрил;
2-{4-[8-(2-фторхинолин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил}-2-метилпропионитрил;
2-метил-2-[4-(3-метил-2-оксо-8-хинолин-6-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-метил-2-[4-(3-метил-2-оксо-8-хинолин-5-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил] пропионитрил;
2-метил-2-[4-(3-метил-2-оксо-8-хиноксалин-6-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-этил-2-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]бутиронитрил;
2-этил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]бутиронитрил;
1-[3-фтор-4-(2-оксопирролидин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-фтор-4-(2-оксопирролидин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(2-оксопирролидин-1-ил)фенил]-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(2-оксопирролидин-1-ил)фенил]-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-{4-[бис-(2-метоксиэтил)амино]-3-фторфенил}-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-{4-[бис-(2-метоксиэтил)амино]-3-фторфенил}-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-{4-[бис-(2-метоксиэтил)амино]фенил}-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-{4-[бис-(2-метоксиэтил)амино]фенил}-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-нафталин-2-ил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-нафталин-2-ил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(2-хлорфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(2-хлорфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-о-толил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-о-толил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(2-этилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(2-этилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-(2-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-(2-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-фтор-2-метилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-фтор-2-метилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(2-хлор-4-фторфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(2-хлор-4-фторфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлорфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлорфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-(3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-(3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-метоксиметилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-метоксиметилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[2-хлор-4-(2-метоксиэтил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[2-хлор-4-(2-метоксиэтил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(2-метоксиэтил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(2-метоксиэтил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
2-метил-2-[4-(3-метил-2-оксо-5-окси-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-метил-2-[4-(3-метил-2-оксо-5-окси-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-[4-(7-фтор-3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]-2-метилпропионитрил;
2-[4-(7-фтор-3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]-2-метилпропионитрил;
N-метил-N-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]метансульфонамид;
трет-бутиловый эфир метил[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]карбаминовой кислоты;
метил[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]амид этансульфоновой кислоты;
метил[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]амид этансульфоновой кислоты;
N-этил-N-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]метансульфонамид;
N-этил-N-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]метансульфонамид;
2-[4-(3-этил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]-2-метилпропионитрил;
1-[3-фтор-4-(4-метансульфонилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-фтор-4-(4-метансульфонилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-фтор-4-пиперазин-1-илфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-фтор-4-пиперазин-1-илфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(4-метилпиперазин-1-ил)фенил]-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(4-метилпиперазин-1-ил)фенил]-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[2-хлор-4-(4-метилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[2-хлор-4-(4-метилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-метилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-метилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-2-метилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-2-метилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиразол-1-илфенил)-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиразол-1-илфенил)-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-(4-[1,2,4]-триазол-1-илфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-(4-[1,2,4]-триазол-1-илфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(4-метилпиперазин-1-ил)-3-трифторметилфенил]-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(4-метилпиперазин-1-ил)-3-трифторметилфенил]-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-[4-(4-метилпиперазин-1-ил)-3-трифторметилфенил]-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(5-метоксипиридин-3-ил)-3-метил-1-[4-(4-метилпиперазин-1-ил)-3-трифторметилфенил]-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[2-хлор-4-(4-метилпиперазин-1-ил)фенил]-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[2-хлор-4-(4-метилпиперазин-1-ил)фенил]-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-3-метил-8-хиноксалин-6-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(5-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-8-хиноксалин-6-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(цис-3,5-диметилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(цис-3,5-диметилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-этилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-этилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-изопропилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-изопропилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-изопропилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-изопропилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(4-этилпиперазин-1-ил)-3-трифторметилфенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(4-этилпиперазин-1-ил)-3-трифторметилфенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(4-этилпиперазин-1-ил)-3-трифторметилфенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(4-этилпиперазин-1-ил)-3-трифторметилфенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-(6-пиперазин-1-илпиридин-3-ил)-1-(3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-(3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(5-метоксипиридин-3-ил)-3-метил-1-(3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-имидазол-1-илфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо{4,5-с]хинолин-2-он;
1-(3-хлор-4-имидазол-1-илфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
2-метил-2-[4-(3-метил-8-хинолин-3-ил-2-тиоксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-метил-2-{4-[3-метил-8-(2-метилпиридин-4-ил)-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил}пропионитрил;
5-{1-[4-(цианодиметилметил)фенил]-3-метил-2-оксо-2,3-дигидро-1Н-имидазо[4,5-с]хинолин-8-ил}-пиридин-2-карбонитрил;
2-[4-(4-амино-3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]-2-метилпропионитрил;
2-метил-2-[4-(3-метил-8-хинолин-3-ил-2-тиоксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил] пропионитрил;
1-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]циклопропанкарбонитрил;
1-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]циклопропанкарбонитрил;
1-{4-[8-(6-метоксипиридин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил}циклопропанкарбонитрил;
1-[3-хлор-4-(4-метилпиперазин-1-ил)фенил]-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-метилпиперазин-1-ил)фенил]-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-метилпиперазин-1-ил)фенил]-3-метил-8-хиноксалин-6-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-8-(2-метоксипиримидин-5-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-3-метил-8-пиримидин-5-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-8-(2-метоксипиримидин-5-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-3-метил-8-пиримидин-5-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-3-метил-8-(2-метилпиридин-4-ил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(цис-3,5-диметилпиперазин-1-ил)фенил]-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(цис-3,5-диметилпиперазин-1-ил)фенил]-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(цис-3,5-диметилпиперазин-1-ил)-3-трифторметилфенил]-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(цис-3,5-диметилпиперазин-1-ил)-3-трифторметилфенил]-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(2-метоксипиримидин-5-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-8-пиримидин-5-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
5-[3-метил-2-оксо-1-(4-пиперазин-1-ил-3-трифторметилфенил)-2,3-дигидро-1Н-имидазо[4,5-с]хинолин-8-ил]пиридин-2-карбонитрил;
3-метил-8-(2-метилпиридин-4-ил)-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
8-(5-метоксипиридин-3-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
5-[3-метил-2-оксо-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-2,3-дигидро-1Н-имидазо[4,5-с]хинолин-8-ил]-пиридин-2-карбонитрил;
8-(6-фторпиридин-3-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(2,6-диметоксипиридин-3-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиримидин-5-ил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(2-метоксипиримидин-5-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(2,4-диметоксипиримидин-5-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(5-метоксипиридин-3-ил)-3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-[1,2,4]триазол-1-илфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-[1,2,4]триазол-1-илфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-3-трифторметилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-3-трифторметилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-3-трифторметилфенил)-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-3-трифторметилфенил)-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-(4-[1,2,4]триазол-1-илметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-(4-[1,2,4]триазол-1-илметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-илметилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он и
1-(4-имидазол-1-илметилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
или его таутомер или фармацевтически приемлемая соль, или его гидрат или сольват.
3. Соединение формулы (I), которое представляет собой 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил, или его таутомер, или фармацевтически приемлемая соль, или его гидрат или сольват.
4. Соединение формулы (I), которое представляет собой 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он, или его таутомер, или фармацевтически приемлемая соль, или его гидрат или сольват.
5. Применение соединения по любому из пп.1-4, или его N-оксида, или таутомера, или фармацевтически приемлемой соли такого соединения для лечения человека или животного.
6. Применение соединения по любому из пп.1-4, или его N-оксида, или таутомера, или фармацевтически приемлемой соли, или его гидрата или сольвата для приготовления лекарственного средства для лечения пролиферативного заболевания, воспалительного заболевания или обструктивного респираторного заболевания.
7. Фармацевтический препарат, содержащий соединение формулы (I) по любому из пп.1-4, или его N-оксид, или таутомер, или фармацевтически приемлемую соль, или его гидрат или сольват и по меньшей мере один фармацевтически приемлемый носитель.
8. Способ получения соединения формулы (I) по п.1 или его фармацевтически приемлемой соли, характеризующийся тем, что производное имидазохинолина формулы (II)
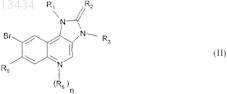
где R1, R2, R3, R5, R6и n имеют значения, указанные для соединения формулы (I),
подвергают реакции с бороновой кислотой формулы (III)
![]()
где R4имеет значения, указанные для соединения формулы (I),
в присутствии основания и соединения палладия (II), в присутствии инертного растворителя; где вышеописанные исходные соединения II и III также могут присутствовать с функциональными группами в защищенной форме, если это является необходимым, и/или в форме солей при условии, что присутствует солеобразующая группа и возможна реакция с соединением в форме соли; из защищенного производного соединения формулы (I) удаляют любые защитные группы; и
если это является желательным, полученное соединение формулы (I) превращают в другое соединение формулы (I), свободное соединение формулы (I) превращают в соль, полученную соль соединения формулы (I) превращают в свободное соединение или другую соль и/или смесь изомеров соединений формулы (I) разделяют на отдельные изомеры.
9. Способ лечения пролиферативного заболевания, которое реагирует на ингибирование липид-киназ и/или родственных PI3-киназе протеин-киназ, предпочтительно активности PI3-киназы и/или ДНК-протеин-киназы, который включает введение теплокровному животному, нуждающемуся в таком лечении, соединения формулы (I) по любому из пп.1-4, или его N-оксида, или таутомера, или фармацевтически приемлемой соли, или его гидрата или сольвата в количестве, эффективном по отношению к указанному заболеванию.
10. Применение соединения по любому из пп.1-4 в комбинации с одним или несколькими другими антипролиферативными соединениями для лечения опухолей.
Текст
013434 Изобретение относится к новым органическим соединениям, способам их получения, их использованию в способе лечения человека или животного, к их применению - отдельно или в комбинации с одним или несколькими другими фармацевтически активными соединениями - для лечения воспалительного или обструктивного заболевания дыхательных путей, такого как астма, заболеваний, обычно встречающихся при трансплантации, или пролиферативного заболевания, такого как опухолевое заболевание,которое может быть солидным или жидким; к способу лечения указанного заболевания у животных, в особенности у людей, и к применению такого соединения - отдельно или в комбинации с одним или несколькими другими фармацевтически активными соединениями - для приготовления фармацевтического препарата для лечения указанных заболеваний. Настоящее изобретение относится к соединениям формулы (I) в которой R1 представляет собой нафтил или фенил, где указанный фенил замещен одним или двумя заместителями, независимо выбранными из группы, включающей галоген; низший алкил, незамещенный или замещенный галогеном, циано, имидазолилом или триазолилом; циклоалкил; амино, замещенный одним или двумя заместителями, независимо выбранными из группы, включающей низший алкил, низший алкилсульфонил, низший алкокси и низший алкокси-низший алкиламино; пиперазинил, незамещенный или замещенный одним или двумя заместителями, независимо выбранными из группы, включающей низший алкил и низший алкилсульфонил; 2-оксопирролидинил; низший алкокси-низший алкил; имидазолил; пиразолил; и триазолил;R3 представляет собой низший алкил;R4 представляет собой пиридил, незамещенный или замещенный галогеном, циано, низшим алкилом, низшим алкокси, или пиперазинил, незамещенный или замещенный низшим алкилом; пиримидинил, незамещенный или замещенный низшим алкокси; хинолинил, незамещенный или замещенный галогеном; хиноксалинил, или фенил, замещенный алкокси;R5 представляет собой водород или галоген;R7 представляет собой водород или амино; или их таутомеру или фармацевтически приемлемой соли, или их гидрату или сольвату. Общие термины, используемые ранее в настоящем изобретении и в дальнейшем, предпочтительно имеют в контексте настоящего описания следующие значения, если специально не указано иначе. Префикс "низший" обозначает радикал, содержащий вплоть до и включающий максимально 7, в особенности вплоть до и включающий максимально 4 атома углерода, данные радикалы могут быть линейными или разветвленными с одним или многими разветвлениями. Если для соединений, солей и т.д. используется форма множественного числа, то она также охватывает отдельное соединение или др. В предпочтительном варианте осуществления алкил имеет вплоть максимально до 12 атомов углерода и в особенности представляет собой низший алкил. Низший алкил, предпочтительно алкил, содержащий от и включительно 1 вплоть до и включительно 7, предпочтительно от и включительно 1 до и включительно 4, является линейным или разветвленным; предпочтительно низший алкил представляет собой бутил, такой как н-бутил, втор-бутил, изобутил, трет-бутил, пропил, такой как н-пропил или изопропил, этил или предпочтительно метил. Циклоалкил предпочтительно представляет собой циклоалкил, содержащий от и включительно 3 вплоть до и включительно 6 атомов углерода в кольце; циклоалкил предпочтительно представляет собой циклопропил, циклобутил , циклопентил или циклогексил. Алкил, который замещен галогеном, предпочтительно представляет собой перфтор алкил, такой как трифторметил. Галоген главным образом представляет собой фтор, хлор, бром или йод, в особенности фтор, хлор или бром. Принимая во внимание большое сходство между новыми соединениями в свободной форме и в форме их солей, включая те соли, которые могут использоваться в качестве промежуточных соединений,например, для очистки или идентификации новых соединений, любая ссылка на свободные соединения в-1 013434 настоящем изобретении ранее и в дальнейшем подразумевается как также относящаяся к соответствующим солям, что является подходящим и целесообразным. Соли образуются, например, в виде солей присоединения кислоты, предпочтительно с органическими или неорганическими кислотами, из соединений формулы (I) с щелочным атомом азота, в особенности фармацевтически приемлемые соли. Подходящими неорганическими кислотами являются, например, галогеновые кислоты, такие как соляная кислота, серная кислота или фосфорная кислота. Подходящими органическими кислотами являются, например, карбоновые, фосфоновые, сульфоновые или сульфаминовые кислоты, например уксусная, пропионовая, каприловая, каприновая, додекановая, гликолевая, молочная, фумаровая, янтарная, малоновая, адипиновая, пимелиновая, субериновая, азелаиновая,яблочная, винная, лимонная кислоты; аминокислоты, такие как глутаминовая кислота или аспарагиновая,малеиновая, гидроксималеиновая, метилмалеиновая, циклогексанкарбоновая, адамантанкарбоновая, бензойная, салициловая, 4-аминосалициловая, фталевая, фенилуксусная, миндальная, коричная, метан- или этансульфоновая,2-гидроксиэтансульфоновая,этан-1,2-дисульфоновая,бензолсульфоновая,4-толуолсульфоновая, 2-нафталинсульфоновая, 1,5-нафталиндисульфоновая, 2- или 3-метилбензолсульфоновая, метилсерная, этилсерная, додецилсерная, N-циклогексилсульфаминовая, N-метил-, N-этилили N-пропилсульфаминовая кислоты; или другие органические протонные кислоты, такие как аскорбиновая кислота. Для выделения и очистки также представляется возможным использовать фармацевтически неприемлемые соли, например пикраты или перхлораты. Для терапевтического применения используются только фармацевтически приемлемые соли или свободные соединения (где подходяще, в форме фармацевтических препаратов), и, следовательно, они являются предпочтительными.R1 предпочтительно представляет собой фенил, где указанный фенил замещен одним или двумя заместителями, независимо выбранными из группы, включающей галоген; низший алкил, замещенный галогеном, циано, имидазолилом или триазолилом; амино, замещенный одним или двумя заместителями,независимо выбранными из группы, включающей низший алкил и низший алкилсульфонил; пиперазинил, где указанный пиперазинил незамещен или замещен одним или двумя низшими алкильными заместителями; имидазолил; пиразолил и триазолил.R2 предпочтительно представляет собой О.R3 предпочтительно представляет собой Me.R4 предпочтительно представляет собой пиримидинил или пиридил, незамещенный или замещенный галогеном, циано, низшим алкилом, низшим алкокси, или пиперазинил, незамещенный или замещенный низшим алкилом; хинолинил, незамещенный или замещенный галогеном; хиноксалинил или фенил, замещенный алкокси.R5 предпочтительно представляет собой водород.n предпочтительно представляет собой 0.R7 предпочтительно представляет собой водород. Предпочтительное соединение представляет собой соединение, выбранное из группы, включающей следующие соединения: 2-метил-2-[4-(3-метил-2-оксо-8-пиридин-4-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил; 2-метил-2-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил; 2-4-[8-(6-метоксипиридин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил 2-метилпропионитрил; 2-4-[8-(5-метоксипиридин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил 2-метилпропионитрил; 2-метил-2-4-[3-метил-2-оксо-8-(6-пиперазин-1-илпиридин-3-ил)-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенилпропионитрил; 2-метил-2-(4-3-метил-8-[2-(4-метилпиперазин-1-ил)пиридин-4-ил]-2-оксо-2,3-дигидроимидазо[4,5 с]хинолин-1-илфенил)пропионитрил; 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил; 2-4-[8-(2-фтор-хинолин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил-2 метилпропионитрил; 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-6-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил; 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-5-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил; 2-метил-2-[4-(3-метил-2-оксо-8-хиноксалин-6-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил; 2-этил-2-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]бутиронитрил;-5 013434 3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-8-пиримидин-5-ил-1,3-дигидроимидазо[4,5 с]хинолин-2-он; 5-[3-метил-2-оксо-1-(4-пиперазин-1-ил-3-трифторметилфенил)-2,3-дигидро-1H-имидазо[4,5-с]хинолин-8-ил]-пиридин-2-карбонитрил; 3-метил-8-(2-метилпиридин-4-ил)-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 8-(3,4-диметоксифенил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 3-метил-8-пиридин-3-ил-1-(4-[1,2,4]-триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5 с]хинолин-2-он; 3-метил-8-хинолин-3-ил-1-(4-[1,2,4]-триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5 с]хинолин-2-он; 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-[1,2,4]-триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 8-(5-метоксипиридин-3-ил)-3-метил-1-(4-[1,2,4]-триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 5-[3-метил-2-оксо-1-(4-[1,2,4]-триазол-1-ил-3-трифторметилфенил)-2,3-дигидро-1 Н-имидазо[4,5 с]хинолин-8-ил]пиридин-2-карбонитрил; 8-(6-фторпиридин-3-ил)-3-метил-1-(4-[1,2,4]-триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 8-(2,6-диметоксипиридин-3-ил)-3-метил-1-(4-[1,2,4]-триазол-1-ил-3-трифторметилфенил)-1,3 дигидроимидазо[4,5-с]хинолин-2-он; 3-метил-8-пиримидин-5-ил-1-(4-[1,2,4]-триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 8-(2-метоксипиримидин-5-ил)-3-метил-1-(4-[1,2,4]-триазол-1-ил-3-трифторметилфенил)-1,3 дигидроимидазо[4,5-с]хинолин-2-он; 8-(2,4-диметоксипиримидин-5-ил)-3-метил-1-(4-[1,2,4]-триазол-1-ил-3-трифторметилфенил)-1,3 дигидроимидазо[4,5-с]хинолин-2-он; 3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-8-пиридин-3-ил-1,3-дигидроимидазо[4,5 с]хинолин-2-он; 3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-8-хинолин-3-ил-1,3-дигидроимидазо[4,5 с]хинолин-2-он; 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 8-(5-метоксипиридин-3-ил)-3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 1-(3-хлор-4-[1,2,4]-триазол-1-илфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин 2-он; 1-(3-хлор-4-[1,2,4]-триазол-1-илфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин 2-он; 1-(4-имидазол-1-ил-3-трифторметилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 1-(4-имидазол-1-ил-3-трифторметилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 1-(4-имидазол-1-ил-3-трифторметилфенил)-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 1-(4-имидазол-1-ил-3-трифторметилфенил)-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 3-метил-8-пиридин-3-ил-1-(4-[1,2,4]-триазол-1-илметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 3-метил-8-хинолин-3-ил-1-(4-[1,2,4]-триазол-1-илметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 1-(4-имидазол-1-илметилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он; 1-(4-имидазол-1-илметилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он; или его таутомер или фармацевтически приемлемую соль, или его гидрат или сольват.-6 013434 Предпочтительными также являются соединения формулы (Ia) в которой R1 представляет собой нафтил или фенил, где указанный фенил замещен одним или двумя заместителями, независимо выбранными из группы, включающей галоген; низший алкил, незамещенный или замещенный галоген или циано; амино, замещенный одним или двумя заместителями, независимо выбранными из группы, включающей низший алкил, низший алкилсульфонил, низший алкокси и низший алкокси-низший алкиламино; пиперазинил, где указанный пиперазинил незамещен или замещен одним или двумя заместителями, независимо выбранными из группы, включающей низший алкил и низший алкилсульфонил; 2-оксопирролидинил; низший алкокси-низший алкил; имидазолил; пиразолил и триазолил;R3 представляет собой низший алкил;R4 представляет собой пиридил, незамещенный или замещенный низшим алкокси, или пиперазинил, незамещенный или замещенный низшим алкилом, или хинолинил, незамещенный или замещенный галогеном, или хиноксалинил;R5 представляет собой водород или галоген;R6 представляет собой оксидо; при условии, что если n=1, то атом азота, несущий радикал R6, имеет положительный заряд; или их таутомер или фармацевтически приемлемая соль, или их гидрат или сольват. Неожиданно, было обнаружено, что соединения формулы (I) обладают благоприятными фармакологическими свойствами и ингибируют активность липид-киназы, такой как PI3-киназа, и/или представителей семейства PI3-родственных протеин-киназ (так называемые PIKK и включающее ДНК-PK, ATM,ATR, hSMG-1 и mTOR), такие как ДНК-протеин-киназа, и могут применяться для лечения заболевания и расстройств, которые зависят от активности указанных киназ. Благодаря их ингибирующему действию на ферменты фосфатидилинозитол 3-киназы соединения формулы (I) в свободной форме или в форме фармацевтически приемлемой соли пригодны для лечения состояний, которые опосредуются активацией ферментов PI3-киназ, таких как пролиферативные, воспалительные или аллергические состояния, или расстройства, обычно встречающихся при трансплантации. Лечение в соответствии с изобретением может быть симптоматическим или профилактическим. Предпочтительным является соединение формулы (I) для применения для лечения пролиферативного заболевания, выбранного из доброкачественной или злокачественной опухоли, рака головного мозга, почки, печени, надпочечника, мочевого пузыря, молочной железы, желудка, опухолей желудка, яичников, ободочной кишки, прямой кишки, предстательной железы, поджелудочной железы, легкого, влагалища или щитовидной железы, саркомы, глиобластом, множественной миеломы или рака желудочнокишечного тракта, в особенности рака ободочной кишки или колоректальной аденомы или опухоли головы и шеи, эпидермальной гиперпролиферации, псориаза, гиперплазии предстательной железы, новообразования, новообразования эпителиального характера, лимфом, карциномы молочной железы или лейкоза. Другими заболеваниями являются синдром Каудена, болезнь Лермитте-Дудоса и синдром Баннаян-3 онана или заболевания, при которых аберрантно активирован путь PI3K/PKB. Соединения в соответствии с изобретением пригодны для лечения воспалительных или обструктивных заболеваний дыхательных путей, приводящего, например, к уменьшению повреждения ткани,воспаления дыхательных путей, бронхиальной гиперреактивности, коррекции или прогрессирования заболевания. Воспалительные или обструктивные заболевания дыхательных путей, при которых показано применение соединений в соответствии с настоящим изобретением, включают астму любого типа или происхождения, включая как наследственную (неаллергическую) астму, так и приобретенную (аллергическую) астму, слабую астму, умеренную астму, тяжелую астму, бронхиальную астму, астму, вызванную нагрузкой, профессиональную астму и астму, вызванную бактериальной инфекцией. Лечение астмы также подразумевается как охватывающее лечение субъектов, например, младше 4 или 5 лет, у которых проявляются симптомы стерторозного дыхания, и диагностируемые или предрасположенные к постановке диагноза "дети со стерторозным дыханием", установленной категории пациентов основной медицинской проблемы и в настоящее время часто идентифицируемых как астматики в начальной стадии или в ранней стадии. (Для удобства это предпочтительное астматическое состояние обозначается "синдром стерторозного дыхания у детей").-7 013434 Доказательствами профилактической эффективности при лечении астмы будут являться уменьшение частоты или тяжести симптоматических приступов, например острых астматических или бронхосуживающих приступов, улучшение функционирования легких или улучшение гиперреактивности дыхательных путей. Дополнительным подтверждением может являться уменьшение потребности в другом,симптоматическом лечении, т.е. лечении, предназначенном для ограничения или прекращения симптоматического приступа при его возникновении, например противовоспалительного лечения (например, с применением кортикостероидов), или введения бронхорасширяющих средств. Профилактические преимущества при астме предпочтительно могут проявляться у пациентов, подверженных "утреннему погружению". "Утреннее погружение" является установленным астматическим синдромом, проявляющимся у многих больных астмой, который характеризуется астматическим приступом, например, приблизительно в интервале от 4 до 6 ч утра, т.е. в промежуток времени, значительно отдаленный от любого вводимого ранее симптоматического лечения астмы. Соединения в соответствии с формулой (I) могут применяться при других воспалительных или обструктивных заболеваниях дыхательных путей и состояниях, при которых применимы соединения согласно настоящему изобретению, и включают острое повреждение легких (ОПЛ), острый респираторный дистресс-сидром у взрослых (ОРДС), хроническое обструктивное заболевание легких, дыхательных путей или легких (ХОЗЛ, ХОЗД или ХОЗЛ), включая хронический бронхит или связанное с ним диспноэ,эмфизему, а также обострение гиперреактивности дыхательных путей вследствие применения других лекарственных средств, в частности других ингалируемых лекарственных средств. Изобретение также применимо для лечения бронхита любого типа или происхождения, например острого, арахидного, катарального, крупозного, хронического или туберкулезного бронхита. Другими воспалительными или обструктивными заболеваниями дыхательных путей, при которых применимо настоящее изобретение, являются пневмокониоз (воспалительное, как правило, профессиональное заболевание легких, часто сопровождающееся непроходимостью дыхательных путей, которое может быть общим или хроническим,вызываемое повторным вдыханием пыли) любого типа или происхождения, включая, например, алюминоз, антракоз, асбестоз, халикоз, птилоз, сидероз, силикоз, табакоз и биссиноз. Благодаря их противовоспалительному действию, в особенности в связи с ингибированием активации эозинофилов, соединения в соответствии с изобретением также пригодны для лечения нарушений,связанных с эозинофилами, например эозинофилии, в особенности нарушений, связанных с эозинофилами в дыхательных путях (например, включая патологическую инфильтрацию эозинофилами легочной ткани), включая гиперэозинофилию, так как они оказывают влияние в дыхательных путях и/или в легких, а также, например, нарушений, связанных с эозинофилами, в дыхательных путях вследствие или сопровождающие синдром Леффлера, эозинофильной пневмонии, паразитической (в частности, многоклеточных паразитов) инвазии (включая тропическую эозинофилию), бронхолегочного аспергиллза,узелкового полиартериита (включая гранулематозный аллергический ангиит), эозинофильной гранулемы и нарушений, связанных с эозинофилами, оказывающих влияние в дыхательных путях, развивающихся вследствие реакции на лекарственных средства. Соединения в соответствии с изобретением также пригодны для лечения воспалительных или аллергических состояний кожи, например псориаза, контактного дерматита, атопического дерматита, очаговой алопеции, экссудативной многоформной эритемы, полиморфного дерматита, склеродермы, витилиго, гиперчувствительного ангиита, крапивницы, буллзного пемфигоида, красной волчанки, пузырчатки, приобретенного буллзного эпидермолиза и других воспалительных или аллергических состояний кожи. Соединения в соответствии с изобретением также могут применяться для лечения других заболеваний или состояний, таких как заболевания или состояния, имеющие воспалительный компонент, например лечения заболеваний и состояний глаз, таких как конъюнктивит, осушающий кератоконъюнктивит и весенний конъюнктивит, заболеваний, влияющих на нос, включая аллергический ринит, и воспалительных заболеваний, в которые вовлечены аутоиммунные реакции или имеющие аутоиммунный компонент или этиологию, включая аутоиммунные гематологические заболевания (например, гемолитическую анемию, апластическую анемию, истинную эритроцитарную анемию и идиопатическую тромбоцитопению),системную красную волчанку, полихондрию, склеродому, гранулематоза Вегенера, дерматомиозита,хронического активного гепатита, астенического бульбарного паралича, синдрома Стифена-Джонсона,идиопатической глютеновой болезни, аутоиммунного воспалительного заболевания кишечника (например, язвенного колита и болезни Крона), эндокринной офтальмопатии, базедовой болезни, саркоидоза,альвеолита, хронического гиперчувствительного пневмонита, рассеянного склероза, билиарного первичного цирроза печени, увеита (переднего и заднего), осушающего кератоконъюнктивита и весеннего конъюнктивита, интерстициального фиброза легких, псориатического артрита и гломерулонефрита (с нефротическим синдромом и без него, например, включая идиопатический нефротический синдром или нефропатию с незначительными изменениями). Кроме того, соединение обеспечивает применения соединения согласно изобретению в соответствии с определениями, приведенными в настоящем описании, или его фармацевтически приемлемой соли,или гидрата или сольвата для приготовления лекарственного средства для лечения пролиферативного-8 013434 заболевания, воспалительного заболевания или обструктивного респираторного заболевания, или заболевания, обычно встречающегося при трансплантации. Эффективность соединений формулы (I) и их солей в качестве ингибиторов PI3-киназы может быть продемонстрирована следующим образом. Киназную реакцию осуществляли в конечном объеме 50 мкл на лунку половины площади COSTAR,планшета на 96 лунок. Конечные концентрации АТФ и фосфатидилинозитола в исследовании составляли 5 мкМ и 6 мкг/мл соответственно. Реакцию запускали путем добавления PI3-киназы р 110. Компоненты исследования добавляли на лунку следующим образом: 10 мкл тестируемого соединения в 5% ДМСО на лунку в колонках 2-1; общую активность определяли путем добавления 10 мкл 5% (об./об.) ДМСО в первых 4-х лунках колонки 1 и последних 4-х лунках колонки 12; фон определяли путем добавления 10 мкМ контрольного соединения в последние 4 лунки колонки 1 и первые 4 лунки колонки 12; 2 мл "исследуемой смеси" готовили на планшет: 1,912 мл HEPES буфера для исследования,8,33 мкл 3 мМ маточного раствора АТФ, получая конечную концентрацию 5 мкМ на лунку,1 мкл [33 Р]АТФ на данные активности, получая 0,05 мкКи на лунку,30 мкл 1 мг/мл PI маточного раствора, получая конечную концентрацию 6 мкг/мл на лунку,5 мкл 1 М маточного раствора MgCl2, получая конечную концентрацию 1 мМ на лунку; добавляли 20 мкл исследуемой смеси на лунку; готовили 2 мл "ферментной смеси" на лунку (x мкл PI3-киназы p110 в 2 мл киназного буфера)."Ферментную смесь" выдерживали на льду при добавлении к исследуемым планшетам; для начала реакции добавляли 20 мкл "ферментной смеси" на лунку; затем планшет инкубировали при комнатной температуре в течение 90 мин; реакцию останавливали путем добавления 50 мкл суспензии шариков WGA-SPA на лунку; анализируемый планшет запечатывали с помощью TopSeal-S и инкубировали при комнатной температуре по меньшей мере в течение 60 мин; затем исследуемый планшет центрифугировали при 1500 об/мин в течение 2 мин с помощью центрифуги рабочей поверхности стола Jouan; затем подсчитывали количество импульсов в исследуемом планшете с помощью Packard TopCount,каждую лунку анализировали в течение 20 с.Объем фермента зависит от ферментативной активности анализируемой партии. Некоторые соединения проявляют определенный уровень активности по отношению к различным паралогам PI3K альфа, гамма и дельта. Описание биохимического исследования ДНК-PK. Исследования осуществляли с помощью набора V7870 от Promega, который количественно определяет ДНК-зависимую активность протеин-киназы, как в препаратах очищенного фермента, так и в экстрактах ядер клеток. ДНК-PK представляет собой ядерную серин/треонин протеин-киназу, которой для проявления активности необходима двухцепочечная ДНК (дцДНК). Связывание дцДНК с ферментом приводит к образованию активного фермента, а также сближает субстрат с ферментом, что делает возможным осуществление реакции фосфорилирования. Реакционный буфер ДНК-PK Х 5 (250 мМ HEPES, 500 мМ KCl, 50 мМ MgCl2, 1 мМ EGTA, 0,5 мМ ЭДТА, 5 мМ DTT, рН до 7,5 с помощью KOH) разводили 1/5 в деионизированной воде и добавляли БСА(маточный раствор = 10 мг/мл) до конечной концентрации 0,1 мг/мл. Активационный буфер состоял из 100 мкг/мл ДНК тимуса теленка в контрольном буфере (10 мМ Трис-HCl (рН 7,4), 1 мМ ЭДТА (рН 8,0. На пробирку реакционная смесь состояла из 2,5 мкл активационного или контрольного буфера,5 мкл Х 5 реакционного буфера,2,5 мкл биотинилированного пептидного субстрата,производного р 53 (маточный раствор = 4 мМ),0,2 мкл БСА (маточный раствор 10 мг/мл) и 5 мкл [-32 Р] АТФ (5 мкл 0,5 мМ холодного АТФ+0,05 мкл Redivue [-32 Р] АТФ = AmershamAA0068-250 мкКи, 3000 Ки/ммоль, 10 мкКи/мкл). Фермент ДНК-PK (Promega V5811, концентрация = 100 Ед./мкл) разводили 1/10 в X1 реакционном буфере и выдерживали на льду непосредственно до применения; 10,8 мкл разведенного фермента инкубировали с 1,2 мкл 100 мкМ соединения (разведенного 1/100 в воде с 10 мМ маточного раствора в неразведенном ДМСО) в течение 10 мин при комнатной температуре. В течение этого времени 15,2 мкл реакционной смеси добавляли в пробирки с завинчивающимися пробками, позади Perspex стекла. Затем в пробирки, содержащие реакционную смесь, переносили 9,8 мкл фермента и после инкубации в течение 5 мин при 30 С реакцию останавливали путем добавления 12,5 мкл терминирующего буфера (7,5 М гид-9 013434 рохлорида гуанидина). После смешивания лунки 10 мкл аликвоты каждой пробирки наносили в виде капли на SAM2R биотиновую захватывающую мембрану, которую оставляли высушиваться в течение нескольких минут. Затем мембрану тщательно промывали для удаления избытка свободного [-32 Р] АТФ и небиотинилированных белков: один раз в течение 30 с в 200 мл 2 М NaCl, 3 раза в течение 2 мин каждый раз в 200 мл 2 М NaCl, 4 раза в течение 2 мин каждый раз в 2 М NaCl в 1% Н 3 РО 4 и 2 раза в течение 30 с каждый раз в 100 мл деионизированной воды. Затем мембрану оставляли высушиваться на воздухе при комнатной температуре в течение 30-60 мин. Квадрат каждой мембраны отделяли с помощью пинцетов и ножниц и помещали в сцинтилляционный сосуд, после этого добавляли 8 мл сцинтилляционной жидкости (Flo-Scint 6013547 от Perkin-Elmer). После этого определяли количество Р, инкорпорированного в ДНК-PK биотинилированный петидный субтрат, с помощью жидкостного сцинтилляционного подсчета. Эффективность соединений в соответствии с изобретением в блокировании активации PI3K/PKB пути может быть продемонстрирована в клеточном исследовании, описанном ниже. Протокол определения фосфо-PKB и фосфо-GSK3. В день 1, U87MG клетки ( АТСС НТВ-14) трипсинизировали, подсчитывали в камере Neubauer и разводили в свежеприготовленной полной RPMI 1640 среде до конечной концентрации 6105 клеток/мл. Затем на 10 см чашки для культивирования тканей наносили 10 мл суспензии клеток и инкубировали в течение 18 ч. В день 2, среду в планшетах отбрасывали и заменяли полной RPMI 1640 средой, содержащей либо ДМСО, либо ингибиторы [соединения формулы (I)]. После контакта в течение 30 мин среду быстро удаляли путем отсасывания и клетки два раза промывали предварительно охлажденным ФСБР. Затем клетки помещали на лед и сразу лизировали. После этого образцы белков повторно растворяли с помощьюSDS-PAGE и переносили на мембраны Immbilon-P для определения уровней эндогенных GSK3, PKB,ФосфоТ 308-PKB и Фосфо 89-GSK3 с помощью вестерн-блоттинга. Затем мембраны высушивали и покрывали полиэтиленовой пленкой и измеряли хемилюминесценцию в MultiImage Light Cabinet (AlphaInnotech Corp) с помощью программного обеспечения FluorChem (Alpha Innotech Corp). Данные анализировали с помощью программного обеспечения AlphaEasy, графически представляя в виде % от контроля (клетки, обработанные ДМСО в экспериментальных условиях, идентичных используемым для ингибиторов киназы) с помощью SigmaPlot (SSPI Inc., версия 7) в виде кривой регрессии(Four Parameter Logistic Cubic) и таким образом определяли значения IC50. Ниже также приведены эксперименты, демонстрирующие противоопухолевую активность соединений формулы (I) в условиях in vivo. Самок атимических мышей Harlan nu/nu с подкожно трансплантированными опухолями глиобластом человека U87MG можно использовать для определения противоопухолевой активности ингибиторов PI3-киназы. В день 0, животным под пероральным фореновым наркозом подкожно в левый бок вводили фрагмент опухоли приблизительно 25 мг и небольшие резаные раны закрывали с помощью наложения зажимов. При достижении размера опухолей 100 мм 3 мышей случайным образом разделяли на группы по 6-8 животных и начинали лечение. Лечение осуществляли в течение 2-3-недельного периода с пероральным,внутривенным или внутрибрюшинным введением один раз в сутки (или менее часто) соединения формулы (I) в подходящем носителе в определенных дозах. Опухоли измеряли 2 раза в неделю с помощью штангенциркуля и рассчитывали объем опухолей. В качестве альтернативы клеточной линии U87MG аналогично также можно использовать другие клеточные линии, например клеточная линия аденокарциномы молочной железы MDA-MB 468 (АТССНТВ 132; см. также InVitro 14, 911-15 [1978]); клеточная линия рака молочной железы MDA-MB (АТССНТВ-26; см. также In Vitro 12, 331[1976]); клеточная линия рака молочной железы MDA-MB 453 (АТССНТВ-131); клеточная линия рака ободочной кишки Colo 205 (АТССCCL 222; см. также Cancer Res. 38,1345-55 [1978]); клеточная линия рака предстательной железы DU145 DU 145 ( АТСС НТВ 81; см. также CancerRes. 37, 4049-58 [1978]); клеточная линия рака предстательной железы РС-3 РС-3 (особенно предпочтительно; АТССCRL 1435; см. также Cancer Res. 40, 524-34 [1980]) и клеточная линия рака предстательной железы РС-3 М; аденокарцинома легкого человека А 549 (АТССCCL 185; см. также Int. J. Cancer 17, 62-70[1976]); клеточная линия NCI-H596 (АТССНТВ 178; см. также Science 246, 491-4 [1989]); клеточная линия рака поджелудочной железы SUIT-2 (см. Tomioka et al., Cancer Res. 61, 7518-24- 10013434 Соединения в соответствии с изобретением проявляют ингибирующую активность по отношению к Т-клеткам. Более предпочтительно соединения в соответствии с изобретением предотвращают активацию и/или пролиферацию Т-клеток, например, в водном растворе, например, как показано согласно следующему способу тестирования. Двусторонний MLR осуществляли согласно стандартным методикам(J. Immunol. Methods, 1973, 2, 279 и Мео Т. et al., Immunological Methods, New York, Academic Press, 1979,227-39). Вкратце, клетки селезенки, полученные у мышей СВА и BALB/c (1,6105 клеток из каждого штамма на лунку в микротитровальные планшеты для культивирования тканей с плоским дном, 3,2105 в целом), инкубировали в RPMI среде, содержащей 10% ФТС, 100 ед./мл пенициллина, 100 мкг/мл стрептомицина (Gibco BRL, Базель, Швейцария), 50 мкМ 2-меркаптоэтанола (Fluka, Buchs, Швейцария) и серийные разведения соединений. Для тестируемого соединения проводили семь трехкратных этапов разведения в двух повторах. После инкубирования в течение четырех дней добавляли 1 мкКи 3H-тимидина. Клетки собирали после дополнительного инкубирования в течение 5 ч и определяли инкорпорированный 3H-тимидин с помощью стандартных методик. Фоновые значения (низкий контроль) MLR представляли собой пролиферацию одних BALB/c клеток. Низкие контроли вычитали из всех значений. Высокие контроли без любого образца учитывали в качестве 100% пролиферации. Рассчитывали процент ингибирования образцами и определяли концентрацию, необходимую для 50% ингибирования (значения IC50). В этом исследовании соединения в соответствии с изобретением имели значения IC50 в интервале от 1 нМ до 10 мкМ, предпочтительно от 10 до 100 нМ. Соединения формулы (I) также благоприятно могут применяться в комбинации с другими антипролиферативными соединениями. Такими антипролиферативными соединениями являются, но не ограничиваясь только ими, ингибиторы ароматазы; антиэстрогены; ингибиторы топоизомеразы I; ингибиторы топоизомеразы II; соединения, активные по отношению к микротрубочкам; алкилирующие соединения; ингибиторы деацетилазы гистонов; соединения, которые индуцируют процессы дифференциации клеток; ингибиторы циклооксигеназы; ингибиторы ММР; ингибиторы mTOR; противоопухолевые антиметаболиты; соединения платины; соединения, нацеленные/снижающие активность протеин- или липид-киназы и другие антиангиогенные соединения; соединения, которые нацеленные, снижают или ингибируют активность протеин- или липид-фосфатазы; агонисты гонадорелина; антиандрогены; ингибиторы метионинаминопептидазы; бифосфонаты; модификаторы биологической ответной реакции; антипролиферативные антитела; ингибиторы гепараназы; ингибиторы онкогенных изоформ Ras; ингибиторы теломеразы; ингибиторы протеасомы; соединения, используемые для лечения злокачественных новообразований кроветворной системы; соединения, которые нацеленные, снижают или ингибируют активность Flt-3; ингибиторы Hsp90, такие как 17-AAG (17-аллиламиногельданамицин, NSC330507), 17-DMAG(17-диметиламиноэтиламино-17-деметоксигельданамицин, NSC707545), IPI-504, CNF1010, CNF2024,CNF10110 от Conforma Therapeutics; темозоломид (TEMODAL); ингибиторы белка веретена кинезина,такие как SB715992 или SB743921 от GlaxoSmithKline или пентамидин/хлорпромазин от CombinatoRx; ингибиторы MEK, такие как ARRY142886 от Array PioPharma, AZD6244 от AstraZeneca, PD181461 отPfizer и лековорин. Термин "ингибитор ароматазы", как он используется в настоящем изобретении, относится к соединению, которое ингибирует образование эстрогена, т.е. превращение субстратов андростендиона и тестостерона в эстрон и эстрадиол соответственно. Термин включает, но не ограничиваясь только ими, стероиды, в особенности атаместан, эксеместан и форместан, и, в частности, нестероиды, в особенности аминоглутетимид, роглетимид, пиридоглутетимид, трилостан, тестолактон, кетоконазол, ворозол, фадрозол, анастрозол и летрозол. Эксеместан может вводиться, например, в форме, как он продается на рынке,например, под товарным знаком AROMASIN. Форместан может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком LENTARON. Фадрозол может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком AFEMA. Анастрозол может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком ARIMIDEX. Летрозол может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком FEMARA или FEMAR. Аминоглутетимид может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком ORIMETEN. Комбинация в соответствии с изобретением, содержащая химиотерапевтическое средство, которое представляет собой ингибитор ароматазы, является чрезвычайно полезной для лечения опухолей, положительных по рецептору гормона, например опухоли молочной железы. Термин "антиэстроген", как он используется в настоящем изобретении, относится к соединению,которое проявляет антагонистическое действие по отношению к действию эстрогенов на уровне рецептора эстрогена. Термин включает, но не ограничиваясь только ими, тамоксифен, фульвестрант, ралоксифен и гидрохлорид ралоксифена. Тамоксифен может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком NOLVADEX. Гидрохлорид ралоксифена может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком EVISTA. Фульвестрант может быть приготовлен в виде лекарственного средства, как описано в US 4659516, или он может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком FASLODEX.- 11013434 Комбинация в соответствии с изобретением, содержащая химиотерапевтическое средство, которое представляет собой антиэстроген, является чрезвычайно полезной для лечения опухолей, положительных по рецептору эстрогена, например опухолей молочной железы. Термин "антиандроген", как он используется в настоящем изобретении, относится к любому веществу, которое способно ингибировать биологические действия андрогенных гормонов и включает, но не ограничиваясь только ими, бикалутамид (CASODEX), который может быть приготовлен в виде лекарственного средства, например, как описано в US 4636505. Термин "агонист гонадорелина", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, абареликс, гозерелин и ацетат гозерелина. Гозерелин описан в US 4100274 и может вводиться, например, в форме, как он продается на рынке, например, под товарным знакомZOLADEX. Абареликс может быть приготовлен в виде лекарственного средства, например, как описано в US 5,843,901. Термин "ингибитор топоизомеразы I", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, топотекан, гиматекан, иринотекан, камптотециан и его аналоги,9-нитрокамптотецин и макромолекулярный конъюгат камптотецина PNU-166148 (соединение А 1 вWO 99/17804). Иринотекан может вводиться, например, в форме, как он продается на рынке, например,под товарным знаком CAMPTOSAR. Топотекан может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком HYCAMTIN. Термин "ингибитор топоизомеразы II", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, антрациклины, такие как доксорубицин (включая, липосомальный препарат, например, CAELYX), даунорубицин, эпирубицин, идарубицин и неморубицин, антахиноны митоксантрон и лозоксантрон, и подофиллотоксины этопозид и тенипозид. Этопозид может вводиться, например, в форме, как он продается на рынке, например,под товарным знаком ETOPOPHOS. Тенипозид может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком VM 26-BRISTOL. Доксорубицин может вводиться, например,в форме, как он продается на рынке, например, под товарным знаком ADRIBLASTIN илиADRIAMYCIN. Эпирубицин может вводиться, например, в форме, как он продается на рынке, например,под товарным знаком FARMORUBICIN. Идарубицин может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком ZAVEDOS. Митоксантрон может вводиться, например,в форме, как он продается на рынке, например, под товарным знаком NOVANTRON. Термин "соединение, активное по отношению к микротрубочкам" относится к соединениям, которые стабилизируют микротрубочки, дестабилизируют микротрубочки и ингибиторы полимеризации микротубулина, включая, но не ограничиваясь только ими, таксаны, например, паклитаксел и доцетаксел, алкалоиды барвинка, например винбластин, в особенности винбластинсульфат, винкристин, в особенности винкристинсульфат, и винорелбюин, дискодермолиды, кохицин и эпотилоны и их производные, например эпотилон В или D или их производные. Паклитаксел может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком TAXOL. Доцетаксел может вводиться,например, в форме, как он продается на рынке, например, под товарным знаком TAXOTERE. Винбластинсульфат может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком VINBLASTIN RP. Винкристинсульфат может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком FARMISTIN. Дискодермолид может быть получен, например,как описано в US 5010099. Также сюда включаются производные эпотилона, которые описаны вWO 98/10121, US 6194181, WO 98/25929, WO 98/08849, WO 99/43653, WO 98/22461 и WO 00/31247. Особенно предпочтительными являются эпотилон А и/или В. Термин "алкилирующее средство", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, циклофосфамид, ифосфамид, мельфалан или нитрозомочевина (BCNU илиGliadel). Циклофосфамид может вводиться, например, в форме, как он продается на рынке, например,под товарным знаком CYCLOSTIN. Ифосфамид может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком HOLOXAN. Термин "ингибиторы деацетилазы гистонов" или "ингибиторы HDAC" относится к соединениям,которые ингибируют деацетилазу гистонов и которые обладают антипролиферативным действием. Он включает соединения, описанные в WO 02/22577, в особенностиN-гидрокси-3-[4-(2-гидроксиэтил)-[2-(1H-индол-3-ил)этил]амино]метил]фенил]-2 Е-2-пропенамид,N-гидрокси-3-[4-2-(2-метил-1H-индол-3-ил)этил]амино]метил]фенил]-2E-2-пропенамид и их фармацевтически приемлемые соли. Он дополнительно предпочтительно включает субероиланилидгидроксамовую кислоту (SAHA). Термин "противоопухолевые антиметаболиты" включает, но не ограничиваясь только ими,5-фторурацил или 5-ФУ, капецитабин, гемцитабин, соединения, метилирующие ДНК, такие как 5-азацитидин и децитабин, метотрексат и эдатрексат, и антагонисты фолиевой кислоты, такие как пеметрексед. Капецитабин может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком XELODA. Гемцитабин может вводиться, например, в форме, как он продается на рынке, например, под товарным знаком GEMZAR.- 12013434 Термин "соединение платины", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, карбоплатин, цисплатин, цисплатиний и оксалиплатин. Карбоплатин может вводиться, например, в форме, как он продается на рынке, например, под товарным знакомCARBOPLAT. Оксалиплатин может вводиться, например, в форме, как он продается на рынке, например,под товарным знаком ELOXATIN. Термин "соединения, нацеленные/снижающие активность протеин- или липид-киназы; или активность протеин- или липид-фосфатазы; или дополнительные антиангиогенные соединения", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, ингибиторы протеинтирозин-киназы и/или серин- и/или треонин-киназы или ингибиторы липид-киназы, например:a) соединения, нацеленные, снижающие или ингибирующие активность рецепторов факторов роста производных тромбоцитов (PDGFR), такие как соединения, которые нацеливают, снижают или ингибируют активность PDGFR, в особенности соединения, которые ингибируют рецептор PDGF, например,производное N-фенил-2-пиримидин-амина, например, иматиниб, SU101, SU6668 и GFB-111;b) соединения, нацеленные, снижающие или ингибирующие активность рецепторов фактора роста фибробластов (FGFR);c) соединения, нацеленные, снижающие или ингибирующие активность рецептора инсулинподобного фактора роста I (IGF-IR), такие как соединения, которые нацеливают, снижают или ингибируют активность IGF-IR, в особенности соединения, которые ингибируют активность киназы рецептора IGF-I,такие как соединения, описанные в WO 02/092599, или антитела, которые нацеленные на внеклеточный домен рецептора IGF-I или его факторов роста;d) соединения, нацеленные, снижающие или ингибирующие активность семейства рецепторных тирозин-киназ Trk, или ингибиторы эфрина В 4;e) соединения, нацеленные, снижающие или ингибирующие активность семейства рецепторных тирозин-киназ Axl;f) соединения, нацеленные, снижающие или ингибирующие активность рецепторной тирозинкиназы Ret;g) соединения, нацеленные, снижающие или ингибирующие активность рецепторной тирозинкиназы Kit/SCFR, например иматиниб;h) соединения, нацеленные, снижающие или ингибирующие активность рецепторных тирозинкиназ C-kit - (части семейства PDGFR), такие как соединения, которые нацеливают, снижают или ингибируют активность семейства рецепторных тирозин-киназ c-Kit, в особенности соединения, которые ингибируют c-Kit рецептор, например иматиниб;i) соединения, нацеленные, снижающие или ингибирующие активность представителей семействаc-Abl, их продуктов слитых генов (например, BCR-Abl киназы) и мутантов, такие как соединения, которые нацелены снижают или ингибируют активность представителей семейства c-Abl и их продуктов слитых генов, например производное N-фенил-2-пиримидин-амина, например иматиниб или нилотинибj) соединения, нацеленные, снижающие или ингибирующие активность представителей семейства протеин-киназы С (PKC) и Raf семейства серин/треонин-киназ, представителей семейства MEK, SRC,JAK, FAK, PDK1, PKB/Akt, и представителей семейства Ras/MAPK, и/или представителей семейства циклинзависимых киназ (CDK) и предпочтительно представляют собой производные стауроспорина,описанные в US 5093330, например мидостаурин; примерами других соединений являются, например,UCN-01, сафиндол, BAY 43-9006, Бриостатин 1, Перифозин; Илимофозин; RO 318220 и RO 320432;k) соединения, нацеленные, снижающие или ингибирующие активность ингибиторов протеинтирозин киназ, такие как соединения, которые нацеливают, снижают или ингибируют активность ингибиторов протеин-тирозин-киназ, включая иматиниб мезилат (GLEEVEC) или тирфостин. Тирфостин предпочтительно представляет собой соединение с небольшой молекулярной массой (Mr1500) или его фармацевтически приемлемую соль, в особенности соединение, выбранное из соединений класса бензилиденмалонитрила или S-арилбензолмалонитрила или соединений бисубстрата хинолина, более предпочтительно, любое соединение, выбранное из группы, включающей Тирфостин A23/RG-50810; AG 99; Тирфостин AG 213; Тирфостин AG 1748; Тирфостин AG 490; Тирфостин В 44; Тирфостин В 44 (+) энантиомер; Тирфостин AG 555; AG 494; Тирфостин AG 556, AG957 и адафостин (адамантиловый эфир 4-[(2,5-дигидроксифенил)метил]аминобензойной кислоты; NSC 680410, адафостин);l) соединения, нацеленные, снижающие или ингибирующие активность семейства фактора роста эпидермиса рецепторных тирозин-киназ (EGFR, ErbB2, ErbB3, ErbB4 в виде гомо- или гетеродимеров) и их мутантов, такие как соединения, которые нацеливают, снижают или ингибируют активность семейства рецепторов фактора роста эпидермиса, предпочтительно представляют собой соединения, белки или антитела, которые ингибируют представителей семейства тирозин-киназы рецептора EGF, напримерEGF рецептора, ErbB2, ErbB3 и ErbB4, или связываются с EGF или EGF родственными лигандами и представляют собой, в частности, те соединения, белки или моноклональные антитела, которые в общем- 13013434 или в частности раскрыты в WO 97/02266, например соединение из примера 39, или в ЕР 0564409,WO 99/03854, ЕР 0520722, ЕР 0566226, ЕР 0787722, ЕР 0837063, US 5747498, WO 98/10767,WO 97/30034, WO 97/49688, WO 97/38983 и в особенности WO 96/30347 (например, соединение, известное как СР 358774), WO 96/33980 (например, соединение ZD 1839) и WO 95/03283 (например, соединение ZM105180); например трастузумаб (Herceptin), цетуксимаб (Erbitux), Iressa, Tarceva, OSI-774,CI-1033, EKB-569, GW-2016, Е 1,1, E2,4, E2,5, E6,2, E6,4, Е 2,11, E6,3 или Е 7,6,3, и производные 7 Н-пирроло-[2,3-d]пиримидина, которые описаны в WO 03/013541; иm) соединения, нацеленные, снижающие или ингибирующие активность рецептора c-Met, такие как соединения, которые нацеливают, снижают или ингибируют активность c-Met, в особенности соединения, которые ингибируют активность киназы c-Met рецептора, или антитела, которые нацелены на внеклеточный: домен c-Met или связываются с HGF. Дальнейшие антиангиогенные соединения включают соединения, имеющие другой механизм действия, например не связанный с ингибированием протеин- или липид-киназы, например талидомид(THALOMID) и TNP-470. Соединения, которые нацеливают, снижают или ингибируют активность протеин- или липидфосфатазы, представляют собой, например, ингибиторы фосфатазы 1, фосфатазы 2 А или CDC25, например окадаевая кислота или ее производное. Соединения, которые индуцирую процессы дифференциации клеток, представляют собой, например, ретиноевую кислоту, - - или -токоферол или или-токотриенол. Термин ингибитор циклооксигеназы, как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, например, Сох-2 ингибиторы, 5-алкилзамещенная 2-ариламинофенилуксусная кислота и производные, такие как целекоксиб (CELEBREX), рофекоксиб (VIOXX), этикоксиб, вальдекоксиб, или 5-алкил-2-ариламинофенилуксусная кислота, например 5-метил-2-(2'-хлор-6'фторанилино)фенил уксусная кислота, люмиракоксиб. Термин "бифосфонаты", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, этридоновую, клодроновую, тилудроновую, памидроновую, алендроновую, ибандроновую, ризедроновую и золедроновую кислоты. "Этридоновая кислота" может вводиться, например, в форме, как она продается на рынке, например, под товарным знаком DIDRONEL. "Клодроновая кислота" может вводиться, например, в форме, как она продается на рынке, например, под товарным знакомBONEFOS. "Тилудроновая кислота" может вводиться, например, в форме, как она продается на рынке,например, под товарным знаком SKELID. "Памидроновая кислота" может вводиться, например, в форме,как она продается на рынке, например, под товарным знаком AREDIA. "Алендроновая кислота" может вводиться, например, в форме, как она продается на рынке, например, под товарным знаком FOSAMAX."Ибандроновая кислота" может вводиться, например, в форме, как она продается на рынке, например,под товарным знаком BONDRANAT. "Ризедроновая кислота" может вводиться, например, в форме, как она продается на рынке, например, под товарным знаком ACTONEL. "Золедроновая кислота" может вводиться, например, в форме, как она продается на рынке, например, под товарным знаком ZOMETA. Термин "ингибиторы mTOR" относится к соединениям, которые ингибируют цель рапамицин у млекопитающих (mTOR) и которые обладают антипролиферативной активностью, такие как сиролимус(Rapamune), эверолимус (Certican), CCI-779 и АВТ 578. Термин "ингибитор гепараназы", как он используется в настоящем изобретении, относится к соединениям, которые нацеливают, снижают или ингибируют дегидратацию сульфата гепарина. Термин включает, но не ограничиваясь только ими, PI-88. Термин "модификатор биологической ответной реакции", как он используется в настоящем изобретении, относится к лимфокину или интерферонам, например интерферону . Термин "ингибитор онкогенных изоформ Ras", например H-Ras, K-Ras, или N-Ras, как он используется в настоящем изобретении, относится к соединениям, которые нацеливают, снижают или ингибируют онкогенную активность Ras, например "ингибитор фарнезилтрансферазы", например L-744832,DK8G557 или R115777 (Zarnestra). Термин "ингибитор теломеразы", как он используется в настоящем изобретении, относится к соединениям, которые нацеливают, снижают или ингибируют активность теломеразы. Соединения, которые нацеливают, снижают или ингибируют активность теломеразы, предпочтительно представляют собой соединения, которые ингибируют рецептор теломеразы, например теломестатин. Термин "ингибитор метионинаминопептидазы", как он используется в настоящем изобретении, относится к соединениям, которые нацеливают, снижают или ингибируют активность метионинаминопептидазы. Соединения, которые нацеливают, снижают или ингибируют активность метионинаминопептидазы, представляют собой, например, бенгамид или его производное. Термин "ингибитор протеасомы", как он используется в настоящем изобретении, относится к соединениям, которые нацеливают, снижают или ингибируют активность протеасомы. Соединения, которые нацеливают, снижают или ингибируют активность протеасомы, включают, например, Бортезомид- 14013434 Термин "ингибитор матриксной металлопротеиназы" (или "ММР" ингибитор), как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, коллагеновые пептитомиметические и непептитомиметические ингибиторы, производные тетрациклина, например гидроксаматный пептитомиметический ингибитор батимастат и его перорально доступный аналог маримастат (ВВ-2516),приномастат (AG3340), метастат (NSC 683551) BMS-279251, BAY 12-9566, ТАА 211, MMI270B илиAAJ996. Термин "соединения, используемые для лечения злокачественных новообразований кроветворной системы", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, ингибиторы FMS-подобной тирозин-киназы, например соединения, нацеленные, снижающие или ингибирующие активность рецепторов FMS-подобной тирозин-киназы (Flt-3R); интерферон,1-b-D-арабинофурансилцитозин (ara-с) и бисульфан; и ингибиторы ALK, например соединения, которые нацеливают, снижают или ингибируют киназу анапластической лимфомы. Соединения, которые нацеливают, снижают или ингибируют активность рецепторов FMS-подобной тирозин-киназы (Flt-3R), предпочтительно представляют собой соединения, протеины или антитела, которые ингибируют представителей семейства Flt-3R рецепторной киназы, например PKC412, мидостаурин, производное стауроспорина, SU11248 и MLN518. Термин "ингибиторы HSP90", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, соединения, нацеленные, снижающие или ингибирующие присущую АТФ-азную активность HSP90; разлагающие, нацеленные, снижающие или ингибирующие клиентские белков HSP90 посредством убиквитин-протеасомного пути передачи сигналов. Соединения, нацеленные, снижающие или ингибирующие присущую АТФ-азную активность HSP90, предпочтительно представляют собой соединения, белки или антитела, которые ингибируют присущую АТФ-азную активность HSP90, например 17-аллиламино,17-деметоксигельданамицин (17AAG), производное гельданамицина; другие родственные гельданамицину соединения; радицикол и ингибиторы HDAC. Термин "антипролиферативные антитела", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, трастузумаб (Herceptin), Трастузумаб-DM1, эрбитукс, бевацизумаб(Avastin), ритуксимаб (Rituxan), PRO64553 (анти-CD40) и 2 С 4 Антитело. Под антителами подразумеваются, например, интактные моноклональные антитела, поликлональные антитела, полиспецифические антитела, образованные по меньшей мере с двух интактных антител, и фрагменты антитела при условии,что они проявляют желательную биологическую активность. Для лечения острого мелоидного лейкоза (ОМЛ) соединения формулы (I) могут применяться в комбинации со стандартным лечением лейкоза, в особенности в комбинации с лечениями, используемыми для лечения ОМЛ. В частности, соединения формулы (I) могут вводиться в комбинации, например, с ингибиторами фарнезилтрансферазы и/или другими лекарственными средствами, пригодными для лечения ОМЛ, такими как Дуанорубицин, Адриамицин, Ara-С, VP-16, Тенипозид, Митоксантрон, Идарубицин, Карбоплатин и PKC412. Термин "противолейкозные соединения" включает, например, ara-c, аналог пиримидина, который представляет собой 2'-альфа-гидроксирибозное (арабинозидное) производное дезоксицитидина. Также сюда включаются пуриновые аналоги гипоксантина, 6-меркаптопурина (6-МР) и фосфата флударабина. Соединения, которые нацеливают, снижают или ингибируют активность деацетилазы гистонов(HDAC), ингибиторы, такие как бутират натрия и субероиланилилгидроксамовая кислота (SAHA), ингибируют активность ферментов, известных как деацетилазы гистонов. Специфическими ингибиторамиHDAC являются MS275, SAHA, FK228 (в настоящий момент FR901228), Трихостатин А и соединения,описанные в US 6552065, в частности N-гидрокси-3-[4-2-(2-метил-1H-индол-3-ил)этил]амино]метил]фенил]-2 Е-2-пропенамид или его фармацевтически приемлемая соль и N-гидрокси-3-[4-[(2 гидроксиэтил)2-(1H-индол-3-ил)этил]амино]метил]фенил]-2E-2-пропенамид или его фармацевтически приемлемая соль, в особенности лактатная соль. Антагонисты рецептора соматостатина, как они используются в настоящем изобретении, относятся к соединениям, которые нацелены, лечат или ингибируют рецептор соматостатина, такие как октреотид и SOM230. Подходы, повреждающие опухолевые клетки, относятся к таким подходам, как ионизирующая радиация. Термин "ионизирующая радиация", используемый ранее в настоящем изобретении и в дальнейшем,обозначает ионизирующию радиацию, которая встречается или в виде электромагнитного излучения (такого как рентгеновское излучение и гамма-излучение) или корпускулярного (такого как альфа- и бетачастицы). Ионизирующая радиация обеспечивается с помощью, но не ограничиваясь только ею, лучевой терапией, и известна в данной области. См. Hellman, Principles of Radiation Therapy, Cancer, в Principlesand Practice of Oncology, Devita et al., ред., 4th ed., vol. 1, p. 248-275 (1993). Термин "EDG-связующие", как он используется в настоящем изобретении, относится к классу иммунодепрессантов, которые модулируют рециркуляцию лимфоцитов, такому как FTY720. Термин "ингибиторы рибонуклеозидредуктазы" относится к аналогам пиримидиновых или пуриновых нуклеозидов, включая, но не ограничиваясь только ими, флударабин и/или арабинозид цитозина(ara-c), 6-тиогуанин, 5-фторурацил, кладрибин, 6-меркаптопурин (в особенности в комбинации с ara-c для лечения ОЛЛ) и/или пентостатин. Ингибиторы рибонуклеозидредуктазы предпочтительно представляют собой гидроксимочевину или производные 2-гидрокси-1H-изоиндол-1,3-диона, такие как PL-1,PL-2, PL-3, PL-4, PL-5, PL-6, PL-7 или PL-8, описанные в Nandy et al., Acta Oncologica, vol. 33,8,с. 953-961 (1994). Термин " ингибиторы декарбоксилазы S-аденохилметионина", как он используется в настоящем изобретении, включает, но не ограничиваясь только ими, соединения, описанные в US 5461076. Также сюда предпочтительно включают те соединения, белки или моноклональные антитела VEGF,которые описаны в WO 98/35958, например 1-(4-хлоранилино)-4-(4-пиридилметил)фталазин или его фармацевтически приемлемая соль, например сукцинат, или в WO 00/09495, WO 00/27820, WO 00/59509,WO 98/11223, WO 00/27819 и ЕР 0769947; те, которые описаны Prewett et al., Cancer Res, vol. 59,с. 5209-5218 (1999); Yuan et al., Proc Natl Acad Sci USA, vol. 93, p. 14765-14770 (1996); Zhu et al., CancerZD4190; ZD6474; SU5416; SU6668; бевацизумаб; или антитела к VEGF, или антитела к рецептору VEGF,например rhuMAb и RHUFab, VEGF аптамер, например Macugon; FLT-4 ингибиторы, FLT-3 ингибиторы,VEGFR-2 IgG1 антитело, Ангиозим (RPI 4610) и Бевацизумаб (Avastin). Фототерапия, как она используется в настоящем изобретении, относится к лечению, при котором используются известные химические средства, известные в качестве фотосенсибилизирующих соединений для лечения или предотвращения злокачественных новообразований. Примером фитотерапии является лечение с помощью соединений, таких как, например, VISUDYNE и порфимер натрия. Ангиостатические стероиды, как они используются в настоящем изобретении, относятся к соединениям, которые блокируют или ингибируют ангиогенез, такие как, например, анекортав, триамцинолон. гидрокортизон,11 эпигидрокортизол, кортексолон, 17-гидроксипрогестерон, кортикостерон, дезоксикортикостерон,тестостерон, эстрон и дексаметазон. Имплантаты, содержащие кортикостероиды, относятся к соединениям, таким как, например, флуоцинолон, дексаметазон. Другие химиотерапевтические соединения включают, но не ограничиваясь только ими, растительные алкалоиды, гормональные соединения и антагонисты; модификаторы биологической ответной реакции, предпочтительно лимфокины или интерфероны; антисмысловые олигонуклеотиды или производные олигонуклеотидов; мшРНК (shRNA) или миРНК (siRNA) или разнообразные соединения или соединения с другим или неизвестным механизмом действия. Соединения в соответствии с изобретением также пригодны в качестве совместно вводимых при лечении соединений для применения с другими лекарственными средствами, такими как противовоспалительные, бронхорасширяющие или антигистаминные лекарственные средства, предпочтительно для лечения обструктивных или воспалительных заболеваний дыхательных путей, таких как заболевания, описанные в настоящем изобретении выше, например, в качестве потенцирующих средств терапевтической активности таких лекарственных средств или в качестве средств уменьшения необходимой дозы или потенциальных побочных действий таких лекарственных средств. Соединение по изобретению может быть смешано с другим лекарственным веществом в виде фиксированной фармацевтической композиции или может вводиться отдельно, до, одновременно с или после другого лекарственного вещества. Таким образом, изобретение охватывает комбинацию соединения согласно изобретению, как описано в настоящем описании выше, с противовоспалительным, бронхорасширяющим, антигистаминным или противокашлевым лекарственным веществом, где указанное соединение согласно изобретению и указанное лекарственное вещество находятся в одной и той же или другой фармацевтической композиции. Подходящими противовоспалительными лекарственными средствами являются стероиды, в особенности глюкокортикостероиды, такие как будесонид, бекламетазон дипропионат, флутиказон пропионат, циклезонад или мометазон фуроат, или стероиды, описанные в WO 02/88167, WO 02/12266,WO 02/100879, WO 02/00679 (в особенности те, которые описаны в примерах 3, 11, 14, 17, 19, 26, 34, 37,39, 51, 60, 67, 72, 73, 90, 99 и 101), WO 03/035668, WO 03/048181, WO 03/062259, WO 03/064445,WO 03/072592, агонисты нестероидного гликокортикоидного рецептора, такие как соединения, описанные в WO 00/00531, WO 02/10143, WO 03/082280, WO 03/082787, WO 03/104195, WO 04/005229; LTB4 антагонисты, такие как LY293111, CGS025019C, СР-195543, SC-53228, BIIL 284, ONO 4057, SB 209247 и те, которые описаны в US 5451700; LTD4 антагонисты, такие как монтелукаст и зафирлукаст; PDE4 ингибиторы, такие как циломиласт (Ariflo G1axoSmithKline), Рофлумиласт (Byk Gulden),V-11294 АWO 04/005258, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/018431,WO 04/018449, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/019944,WO 04/019945, WO 04/045607 и WO 04/037805; A2a агонисты, такие как те, которые описаны в ЕР 409595 А 2, ЕР 1052264, ЕР 1241176, WO 94/17090, WO 96/02543, WO 96/02553, WO 98/28319,WO 99/24449, WO 99/24450, WO 99/24451, WO 99/38877, WO 99/41267, WO 99/67263, WO 99/67264,WO 99/67265, WO 99/67266, WO 00/23457, WO 00/77018, WO 00/78774, WO 01/23399, WO 01/27130,WO 01/27131, WO 01/60835, WO 01/94368, WO 02/00676, WO 02/22630, WO 02/96462, WO 03/086408,WO 04/039762, WO 04/039766, WO 04/045618 и WO 04/046083; А 2b антагонисты, такие как те, которые описаны в WO 02/42298; и агонисты бета-2 адренорецептора, такие как альбутерол (сальбутамол), метапротеренол, тербуталин, сальметерол фенотерол, прокатерол, и в особенности, формотером и их фармацевтически приемлемые соли, и соединения (в свободной форме или в виде соли или сольвата) формулы(I), приведенной в заявке WO 0075114, этот документ включен в настоящее изобретение в качестве ссылки, предпочтительно соединения, описанные в примерах этой заявки, в особенности соединение формулы и их фармацевтически приемлемые соли, а также соединения (в свободной форме или в виде соли или сольвата) формулы (I), приведенной в заявке WO 04/16601, а также соединения, раскрытые в заявкеWO 04/033412. Подходящими бронхорасширяющими лекарственными средствами являются антихолинергические или антимускариновые соединения, в особенности ипратропий бромид, окситропий бромид, соли тиотропия и CHF 4226 (Chiesi) и гликопирролат, а также соединения, описанные в WO 01/04118,WO 02/51841, WO 02/53564, WO 03/00840, WO 03/87094, WO 04/05285, WO 02/00652, WO 03/53966,ЕР 424021, US 5171744, US 3714357, WO 03/33495 и WO 04/018422. Подходящими антигистаминными лекарственными средствами являются цетиризин гидрохлорид,ацетаминофен, клемастин фумарат, прометазин, лоратидин, деслоратидин, дифенгидрамин и фексофенадин гидрохлорид, активастин, астемизол, азеластин, эбастин, эпинастин, мизоластин и тефенадин, а также соединения, описанные в WO 03/099807, WO 04/026841 и JP 2004107299. Другими пригодными комбинациями соединений в соответствии с изобретением с противовоспалительными средствами являются комбинации с антагонистами хемокиновых рецепторов, напримерSC-351125, SCH-55700 и SCH-D, Takeda антагонисты, такие как хлорид N-4-6,7-дигидро-2-(4 метилфенил)-5 Н-бензоциклогептен-8-ил]карбонил]амино]фенил]метил]-тетрагидро-N,N-диметил-2 Нпиран-4-аминия (TAK-770), и CCR-5 антагонисты, описанные в US 6166037 (предпочтительно в пп. 18 и 19 формулы изобретения), WO 00/66558 (предпочтительно в п.8 формулы изобретения), WO 00/66559(предпочтительно в п.9 формулы изобретения), WO 04/018425 и WO 04/026873. Структуру активных соединений, идентифицируемых с помощью кодов nos., непатентованных названий или товарных знаков, можно определить с помощью действующего издания стандартного компендиума "The Merck Index" или из баз данных, например, Patents International (например, IMS WorldPublications). Вышеописанные соединения, которые могут применяться в комбинации с соединением формулы (I), могут быть приготовлены и вводиться, как описано в данной области техники, такой как документы, процитированные выше. Соединение формулы (I) также благоприятно могут применяться в комбинации с известными терапевтическими методами, например, для введения гормонов или в особенности облучения. Соединение формулы (I) предпочтительно может использоваться в качестве радиосенсибилизирующего средства, в особенности для лечения опухолей, которые проявляют плохую чувствительность к лучевой терапии. Под "комбинацией", в настоящем изобретении подразумевают или смешанную комбинацию в одной единичной дозированной форме, или набор частей комбинированного введения, при котором соединение формулы (I) и комбинируемый компонент могут вводиться независимо в одно и то же время или отдельно в течении промежутков времени, которые, в особенности, позволяют проявить компонентам комбинации коллективное, например, синергетическое действие. Изобретение также обеспечивает фармацевтический препарат, содержащий соединение формулы(I), как определено в настоящем изобретении, или его N-оксид, или таутомер или фармацевтически приемлемую соль такого соединения, или его гидрат или сольват и по меньшей мере один фармацевтически приемлемый носитель.- 17013434 Соединение формулы (I) может вводиться отдельно или в комбинации с одним или несколькими терапевтическими соединениями, возможная комбинированная терапия может осуществляться в виде фиксированных комбинаций или введение соединения согласно изобретению и одного или более других терапевтических соединений планируют или осуществляют независимо друг от друга, или объединяют введение фиксированных комбинаций и одного или нескольких других терапевтических соединений. Соединение формулы (I) можно совмещать или дополнительно вводить предпочтительно для лечения опухоли в комбинации с химиотерапией, лучевой терапией, иммунотерапией, фототерапией, хирургическим вмешательством или их комбинацией. Также представляется возможным осуществлять долговременное лечение в качестве адъювантной терапии в контексте других терапевтических стратегий, как описано выше. Другими возможными лечениями являются поддержание состояния пациента после регрессии опухоли или даже профилактическая химиотерапия, например, у пациентов из группы риска. Дозировка активного компонента зависит от различных факторов, включая тип, вид, возраст, вес,пол и медицинское состояние пациента; тяжесть состояния, подвергаемого лечению; путь введения; функционирования почек и печени у пациента и предпочтительное применяемое соединение. Лечащий врач, клинический врач или ветеринар в данной области легко может определить и прописать эффективное количество лекарственного средства, требуемое для предотвращения, противостояния или остановки прогрессирования состояния. Для оптимальной точности в достижении концентрации лекарственного средства в пределах, которые позволяют обеспечить эффективность, необходима схема лечения, исходя из кинетики доступности лекарственного средства в целевых участках. Это предполагает изучение распределения, равновесия и элиминации лекарственного средства. Доза соединения формулы (I) или его фармацевтически приемлемой соли, которую вводят теплокровным животным, например человеку весом около 70 кг, предпочтительно составляет от приблизительно 3 мг до приблизительно 5 г, более предпочтительно от приблизительно 10 мг до приблизительно 1,5 г, наиболее предпочтительно от приблизительно 100 до приблизительно 1000 мг на человека в сутки,предпочтительно разделенная на 1-3 единичные дозы, которые могут быть, например, равными. Обычно детям назначают половину дозы для взрослого. Соединения в соответствии с изобретением могут вводиться любым обычным путем, в частности парентерально, например в форме инъекционных растворов или суспензий, энтерально, например, перорально, например в форме таблеток или капсул, местно, например в форме лосьонов, гелей, мазей или кремов, или в форме для интранального введения или в виде суппозитория. Местное введение можно осуществлять, например, на кожу. Другую форму для местного введения можно вводить в глаза. Фармацевтические композиции, содержащие соединение согласно изобретению в сочетании по меньшей мере с одним фармацевтически приемлемым носителем или разбавителем, можно приготавливать общепринятым способом путем смешивания с фармацевтически приемлемым носителем или разбавителем. Изобретение также относится к фармацевтическим композициям, содержащим эффективное количество, в частности количество, эффективное для лечения одного из вышеописанных расстройств, соединения формулы (I), или его N-оксида, или таутомера совместно с фармацевтически приемлемыми носителями, которые пригодны для местного, энтерального, например перорального или рекатального,или парентерального введения и могут быть неорганическими или органическими, твердыми или жидкими. Для перорального введения в особенности пригодны таблетки или желатиновые капсулы, которые содержат активный компонент совместно с разбавителями, например лактозой, декстрозой, маннитом,и/или глицерином, и/или скользящими веществами, и/или полиэтиленгликолем. Таблетки также могут содержать связующие, например магнийалюминийсиликат, крахмалы, такие как кукурузный, пшеничный или рисовый крахмал, желатин, метилцеллюлоза, натрийкарбоксиметилцеллюлоза и/или поливинилпирролидон, и, если это является желательным, дезинтеграторы, например крахмалы, агар, альгиновую кислоту или ее соль, такую как альгинат натрия, и/или шипучие смеси, или абсорбенты, красители,ароматизаторы и подсластители. Также представляется возможным использовать фармакологически активные соединения согласно настоящему изобретению в форме парентерально вводимых композиций или в форме инфузионных растворов. Фармацевтические композиции можно стерилизовать и/или они могут содержать наполнители, например консерванты, стабилизаторы, смачивающие соединения и/или эмульсификаторы, солюбилизаторы, соли для регуляции осмотического давления и/или буферы. Фармацевтические композиции согласно настоящему изобретению, которые могут, если это является желательным, содержать другие фармакологически активные вещества, готовят с помощью метода, известного per se, например с помощью обычного способа смешивания, гранулирования, концекционирования,растворения или лиофилизации, и они содержат приблизительно от 1 до 99%, в частности от приблизительно 1 до приблизительно 20% активного(ых) компонента(ов). Дополнительно, настоящее изобретение обеспечивает соединение формулы (I), или его N-оксид,или таутомер или фармацевтически приемлемую соль такого соединения для применения в способе лечения человека или животного. Настоящее изобретение также относится к применению соединения формулы (I) или его таутомера или фармацевтически приемлемой соли такого соединения для приготовления лекарственного средства для лечения пролиферативного заболевания, воспалительного заболевания, или обструктивного заболе- 18013434 вания дыхательных путей, или расстройств, обычно встречающихся при трансплантации. Кроме того, изобретение относится к способу лечения пролиферативного заболевания, которое отвечает на ингибирование липид-киназ и/или родственных PI3-киназе протеин-киназ, в особенности PI3 киназы, и/или активности ДНК-протеин-киназы, который включает введение соединения формулы (I),или его N-оксида, или таутомера или его фармацевтически приемлемой соли, или гидрата или сольвата,где радикалы и символы имеют значения, определенные выше, в количестве, эффективном по отношению к указанному заболеванию, теплокровному животному, в особенности людям, нуждающемуся в таком лечении. Кроме того, изобретение относится к фармацевтической композиции для лечения солидных или жидких опухолей у теплокровных животных, включая людей, содержащей противоопухолеэффективную дозу соединения формулы (I), как описано выше, или фармацевтически приемлемую соль такого соединения совместно с фармацевтическим носителем. Изобретение также обеспечивает способ получения соединения формулы (I) по п.1 или его фармацевтически приемлемой соли. Соединение по изобретению может быть приготовлено с помощью способов, которые, несмотря на то, что до настоящего времени не применялись для новых соединений согласно настоящему изобретению, известны per se, в особенности с помощью способа, который характеризуется тем, что для синтеза соединения формулы (I), в котором символы R1, R2, R3, R4, R5, R6 и n имеют значения, указанные для соединения формулы (I), соединение формулы (II) где R1, R2, R3, R5, R6 и n имеют значения, указанные для соединения формулы (I),подвергают реакции с бороновой кислотой формулы (III) или формулы (IIIa) где R4 имеет значения, указанные для соединения формулы (I),в присутствии основания и катализатора в подходящем растворителе; где вышеописанные исходные соединения (II) и (III) также могут содержать функциональные группы в защищенной форме, если это является необходимым, и/или в форме солей, обеспечивая присутствие солеобразующей группы в реакции и возможной реакции в солевой форме; любые защитные группы в защищенном производном соединения формулы (I) удаляют и, если это является желательным, полученное соединение формулы (I) превращают в другое соединение формулы(I) или его N-оксид, свободное соединение формулы (I) превращают в соль, полученную соль соединения формулы (I) превращают в свободное соединение или другую соль и/или смесь изомерных соединений формулы (I) разделяют на отдельные изомеры. Подробное описание способа В более подробном описании способа R1, R2, R3, R4, R5, R6 и n имеют значения, указанные для соединений формулы (I), если специально не указано иначе. Взаимодействие соединения формул (II) и (III) предпочтительно осуществляют в условиях реакции Сузуки предпочтительно в смеси полярного апротонного растворителя, такого как ДМФА, и воды в присутствии катализатора, в особенности катализатора на основе благородного металла, такого как палладий(II), предпочтительно дихлорид бис-(трифенилфосфин)палладия (II); в присутствии основания, такого как карбонат калия. Защитные группы. Если одна или несколько других функциональных групп, например карбокси, гидрокси, амино или меркапто, присутствуют или нуждаются в защите в соединениях формул (II) или (III), так как они не должны участвовать в реакции, то они представляют собой такие группы, которые обычно используются в синтезе пептидных соединений, а также цефалоспоринов и пенициллинов, а также производных нуклеиновых кислот и сахаров. Защитные группы могут уже содержаться в предшественниках и должны защищать функциональные группы от нежелательных вторичных реакций, таких как ацилирование, этерификация, эстерификация, окисление, сольволиз и аналогичные реакции. Характеристикой защитных групп является возмож- 19013434 ность их легкого удаления, т.е. без нежелательных вторичных реакций, обычно путем ацетолиза, протонолиза, сольволиза, восстановления, фотолиза или также путем ферментативной активности, например, в условиях, аналогичных физиологическим условиям, и то, что они не содержатся в конечных продуктах. Специалист в данной области техники знает или легко может определить, какие защитные группы пригодны для реакций, указанных в настоящем изобретении ранее и в дальнейшем. Защита таких функциональных групп с помощью таких защитных групп, сами защитные группы и реакции для их удаления описаны, например, в стандартных пособиях, таких как J.F. W. McOmie,"Protective Groups in Organic Chemistry", Plenum Press, London и New York 1973; Т W. Greene, "ProtectiveBeach, и Basel 1982 и Jochen Lehmann, "Chemie der Kohlenhydrate: Monosaccharide und Derivate" (Химия углеводородов: моносахариды и производные), Georg Thieme Verlag, Stuttgart 1974. Дополнительные стадии способа. На дополнительных стадиях способа, которые осуществляют, если это является желательным,функциональные группы исходных соединений, которые не должны принимать участие в реакции, могут находиться в незащищенной форме или могут быть защищены, например, с помощью одной или нескольких защитных групп, упомянутых выше в настоящем изобретении в разделе "Защитные группы". После этого защитные группы полностью или частично удаляют в соответствии с одним из способов,раскрытых в настоящем изобретении. Соли соединения формулы (I) с солеобразующей группой могут быть получены способом, известным per se. Таким образом, соли присоединения кислоты соединений формулы (I) могут быть получены путем обработки кислотой или подходящим анионообменным реагентом. Соль с двумя молекулами кислоты (например, дигалогенид соединения формулы (I также может быть превращена в соль с одной молекулой кислоты на соединение (например, моногалогенид); это можно осуществить путем нагревания до расплавления или, например, путем нагревания в виде твердого вещества в высоком вакууме при повышенной температуре, например от 130 до 170 С, одна молекула кислоты вытесняется на молекулу соединения формулы (I). Соли обычно могут быть превращены в свободные соединения, например, путем обработки с подходящими щелочными соединениями, например с карбонатами щелочных металлов, гидрокарбонатами щелочных металлов или гидроксидами щелочных металлов, обычно карбонатом калия или гидроксидом натрия. Стереозомерные смеси, например смеси диастереомеров, могут быть разделены на их соответствующие изомеры способом, известным per se, с помощью подходящих методов разделения. Диастереомерные смеси могут быть разделены на их отдельные диастереоизомеры, например, путем фракционированной кристаллизации, хроматографии, распределения растворителя и аналогичных методик. Это разделение можно осуществлять либо на уровне исходного соединения, либо в самом соединении формулы(I). Энантиомеры могут быть разделены посредством образования диастереомерных солей, например путем образования соли с энантиомерно чистой хиральной кислотой или с помощью хроматографии,например ВЭЖХ, используя хроматографические субстраты с хиральными лигандами. Соединение формулы (I), в котором R2 представляет собой О, может быть превращено в соответствующее соединение, в котором R2 представляет собой S, например, с помощью подходящего соединения серы, например, используя реакцию с реагентом Лавессона (2,4-бис-(4-метоксифенил)2,4-дитиоксо 1,2,3,4-дитиафосфетан) в подходящем растворителе, таком как диоксан. Следует также обратить внимание на то, что реакции, аналогичные превращениям, описанным в этом разделе, также могут быть осуществлены на уровне подходящих промежуточных соединений. Общие условия способов. Все стадии способа, описанные в настоящем изобретении, могут быть осуществлены в известных условиях реакции, предпочтительно тех, которые специально упомянуты, при отсутствии или обычно в присутствии растворителей или разбавителей, предпочтительно таких, которые являются инертными по отношению к используемым реагентам и способны их растворять, при отсутствии или в присутствии катализаторов, конденсирующих средств или нейтрализующих средств, например ионообменников,обычно катионообменников, например, в Н+ форме, в зависимости от типа реакции и/или реагирующих веществ при пониженной, нормальной или повышенной температуре, например в интервале от -100 до приблизительно 190 С, предпочтительно от приблизительно -80 до приблизительно 150 С, например от-80 до -60 С, при комнатной температуре от -20 до 40 С или при точке кипения используемого растворителя, при атмосферном давлении или в закрытом сосуде, который подходяще находится под давлением,и/или в инертной атмосфере, например в атмосфере аргона или азота.- 20013434 Соли могут присутствовать во всех исходных соединениях и временных соединениях, если они содержат солеобразующие группы. Соли также могут присутствовать при осуществлении реакции таких соединений при условии, что осуществление реакции при этом не нарушается. На всех стадиях реакций изомерные смеси, которые встречаются, могут быть разделены на их отдельные изомеры, например диастереомеры или энантиомеры, или на любые смеси изомеров, например рацематы или диастереомерные смеси, обычно, как описано в разделе "Дополнительные стадии способа". Растворители, которые являются подходящими для указанной реакции, могут быть выбраны из группы, включающей, например, воду, сложные эфиры, обычно низший алкил-низшие алканоаты, например этилацетат, простые эфиры, обычно алифатические простые эфиры, например диэтиловый эфир,или циклические эфиры, например тетрагидрофуран, жидкие ароматические углеводороды, обычно бензол или толуол, спирты, обычно метанол, этанол или 1- или 2-пропанол, 1-бутанол, нитрилы, обычно ацетонитрил, галогенированные углеводороды, обычно дихлорметан, кислотные амиды, обычно диметилформамид, основания, обычно гетероциклические азотистые основания, например пиридин, карбоновые кислоты, обычно низшие алканкарбоновые кислоты, например уксусная кислота, ангидриды карбоновых кислот, обычно ангидриды низших алкановых кислот, например уксусный ангидрид, циклические,линейные или разветвленные углеводороды, обычно циклогексан, гексан или изопентан или смеси этих растворителей, например водные растворы, если специально не указано иначе при описании способа. Такие смеси растворителей также могут применяться при обработке, например при хроматографии или распределении. Соединения формулы (I), включая их соли, также получают в виде гидратов или их кристаллы могут включать, например, растворитель, используемый для кристаллизации (находящийся в виде сольватов). В предпочтительном варианте осуществления изобретения соединение формулы (I) получают в соответствии или аналогично способам и стадиям способов, описанных в примерах. Исходные вещества. Новые исходные вещества и/или промежуточные соединения, а также способы их получения являются объектом настоящего изобретения. В предпочтительном варианте осуществления изобретения такие исходные вещества используются, и условия реакций выбирают таким образом, чтобы обеспечить получения предпочтительных соединений. Исходные вещества формулы (II) и (III) являются известными, коммерчески доступными или могут быть синтезированы аналогично или в соответствии со способами, известными в данной области. Например, соединение формулы (II), в котором n представляет собой 0, может быть получено путем алкилирования аминосоединения формулы (IV) в котором R1, R2 и R5 имеют значения, указанные для формулы (I),с соединением формулы (V) где R3 имеет значения, указанные для формулы (I), иX представляет собой галоген или другую подходящую уходящую группу,в присутствии основания, например гидроксида натрия, в подходящем растворителе, например смеси дихлорметана и воды, предпочтительно в присутствии межфазного катализатора, например бромида тетрабутиламмония, при температуре в интервале от 0 до 50 С, предпочтительно при комнатной температуре. Соединение формулы (II), в котором n представляет собой 0, может быть превращено в соответствующее соединение, в котором n представляет собой 1, например, с помощью подходящего окислителя,например, используя реакцию с метахлорпербензойной кислотой в подходящем растворителе, таком как дихлорметан, при комнатной температуре. Соединение формулы IV), в котором R2 представляет собой О, может быть получено путем циклизации диаминосоединения формулы (VI) в котором R1 и R5 имеют значения, указанные для формулы (I),с трихлорметилхлорформиатом в присутствии основания, таком как триэтиламин, в подходящем раство- 21013434 рителе, таком как дихлорметан. Соединение формулы (VI) может быть получено путем восстановления нитросоединения формулы где R1 и R5 имеют значения, указанные для формулы (I). Восстановление предпочтительно осуществляют в присутствии подходящего восстановителя, такого как водород, в присутствии подходящего катализатора, такого как никель Ренея, под давлением, например, в интервале от 1,1 до 2 бар, в подходящем растворителе, например спирте или простом эфире,таком как метанол или тетрагидрофуран или их смеси. Температура реакции предпочтительно находится в интервале от 0 до 80 С, в особенности от 15 до 30 С. Соединение формулы (VII) может быть получено путем взаимодействия соединения (VIII) где R5 имеет значения, указанные для соединения формулы (I), иY представляет собой галоген или другую подходящую уходящую группу,подвергают реакции с соединением формулы (IX) где R1 имеет значения, указанные для соединения формулы (I), при температуре в интервале 0 С и 50 С, предпочтительно при комнатной температуре в подходящем растворителе, т.е. уксусной кислоте. Все оставшиеся исходные вещества, такие как исходные вещества формулы (III), (IV) и (V) известны, могут быть получены согласно известным способам или получены коммерчески; в частности, они могут быть получены с помощью способов, как описано в примерах. Сокращения Следующие примеры предназначены для иллюстрации изобретения, но никоим образом не ограничивают объем изобретения. Температуру измеряли в градусах Цельсия (С). Если специально не указано иначе, то реакции осуществляли при комнатной температуре (кт). Соотношение растворителей (например, в элюентах или смесях растворителей) приведено в объемном соотношении (об./об.). ЖХВД линейный градиент между А = H2O/ТФК 1000:1 и В = ацетонитрил/ТФК 1000:1. 37 мг (0,3 ммоль) 4-пиридинбороновой кислоты (Aldrich, Buchs, Швейцария), 8 мг дихлорид бис(трифенилфосфин)палладия (II) (Fluka, Buchs, Швейцария) и 0,5 мл 1 М раствора Na2CO3 добавляли к раствору 84 мг (0,2 ммоль) 2-[4-(8-бром-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]2-метилпропионитрила (пример 1i) в 2 мл ДМФА. Смесь перемешивали в течение 1 ч при 100 С. После этого смесь закаливали насыщенным водным NaHCO3 и экстрагировали EtOAc (2). Органический слой промывали соляным раствором, высушивали над Na2SO4, фильтровали и упаривали в вакууме. Остаток наносили на силикагель и очищали с помощью флэш-хроматографии (CH2Cl2-МеОН от 97:3 до 18:1),получая указанное в заглавии соединение в виде не совсем белого твердого вещества. ЕС-МС: 420 (М+Н)+; аналитическая ЖХВД: t уд=2,40 мин (Град 1). Пример 1a. 5-Бром-2-(2-нитровиниламино)бензойная кислота(255 ммоль) нитрометана (Fluka, Buchs, Швейцария) в течение 10 мин к смеси, охлажденной на ледяной бане, 35 г льда и 15,3 г (382 ммоль) NaOH. После перемешивания в течение 1 ч при 0 С и 1 ч при кт раствор добавляли при 0 С к 28 г льда и 42 мл HCl (37%) (раствор В). Растворы А и В объединяли и реакционную смесь перемешивали в течение 18 ч при кт. Желтый осадок отфильтровали, промывали H2O и высушивали в вакууме при 40 С, получая указанное в заглавии соединение. ЕС-МС: 287, 289 (М+Н)+, Br образец; 1 29 г (101 ммоль) 5-бром-2-(2-нитровиниламино)бензойной кислоты (пример 1a) и 11,9 г (121 ммоль) ацетата калия в 129 мл (152 ммоль) уксусного ангидрида перемешивали в течение 1,5 ч при 120 С. Осадок отфильтровали и промывали уксусной кислотой, пока фильтрат не обесцвечивался, затем его промывали Н 2 О и высушивали в вакууме, получая указанное в заглавии соединение. ЕС-МС: 269, 271 (М+Н)+, Br образец; аналитическая ЖХВД: t уд=2,70 мин (Град 1). Пример 1 с. 6-Бром-4-хлор-3-нитрохинолин 20 г (74,3 ммоль) 6-бром-3-нитрохинолин-4-ола (пример 1b) в 150 мл (1,63 моль) POCl3 перемешивали в течение 45 мин при 120 С. Смесь охлаждали до кт и медленно вливали в смесь воды со льдом.- 23013434 Осадок отфильтровали, промывали смесью воды со льдом и растворяли в CH2Cl2. Органическую фазу промывали холодным соляным раствором и водную фазу отбрасывали. После высушивания над MgSO4 органический растворитель упаривали насухо, получая указанное в заглавии соединение. 1 Н ЯМР (CDCl3):9,20/s (1 Н), 8,54/d (1H), 8,04/d (1H), 7,96/dd (1H); аналитическая ЖХВД: t уд=4,32 мин (Град 1). Пример 1d. 2-Метил-2-(4-нитрофенил)пропионитрил К 15 г (92,5 ммоль) (4-нитрофенил)ацетонитрила (Fluka, Buchs, Швейцария), 1,64 мг (5,09 ммоль) бромида тетрабутиламмония (Fluka, Buchs, Швейцария) и 43,3 г (305 ммоль) йодметана в 125 мл CH2Cl2 добавляли 10 г (250 ммоль) NaOH в 125 мл воды. Реакционную смесь перемешивали в течение 20 ч при кт. После этого органический слой отделяли, высушивали над MgSO4 и упаривали насухо. Остаток растворяли в простом диэтиловом эфире и обрабатывали черным углем в течение 30 мин, фильтровали через целит и упаривали в вакууме, получая указанное в заглавии соединение в виде светло-желтого твердого вещества. Аналитическая ЖХВД: t уд=3,60 мин (Град 1). Пример 1 е. (2-(4-Аминофенил)-2-метилпропионитрил 16 г (84,1 ммоль) 2-метил-2-(4-нитрофенил)пропионитрила (пример 1d) и 4,16 г никеля Ренея выдерживали в 160 мл ТГФ-МеОН (1:1) под давлением H2 1,1 бар в течение 12 ч при кт. После завершения реакции катализатор отфильтровали и фильтрат упаривали насухо. Остаток очищали с помощью флэшхроматографии на силикагеле (гексан-EtOAc от 3:1 до 1:2), получая указанное в заглавии соединение в виде масла. ЕС-МС: 161 (М+Н)+; аналитическая ЖХВД: t уд=2,13 мин (Град 1). Пример 1f. 2-[4-(6-Бром-3-нитрохинолин-4-иламино)фенил]-2-метилпропионитрил 18 г (62,6 ммоль) 6-бром-4-хлор-3-нитрохинолина (пример 1 с) и 11 г (68,9 ммоль) 2-(4-аминофенил)-2-метилпропионитрила (пример 1 е) растворяли в 350 мл уксусной кислоты и перемешивали в течение 2 ч. После этого добавляли воду и желтый осадок отфильтровали и промывали H2O. Твердое вещество растворяли в EtOAc-ТГФ (1:1), промывали насыщенным водным NaHCO3 и высушивали над MgSO4. Органическую фазу упаривали насухо, получая указанное в заглавии соединение в виде желтого твердого вещества. ЕС-МС: 411, 413 (М+Н)+, Br образец; аналитическая ЖХВД: t уд=3,69 мин (Град 1). Пример 1g. 2-[4-(3-Амино-6-бром-хинолин-4-иламино)фенил]-2-метилпропионитрил 24 г (58,4 ммоль) 2-[4-(6-бром-3-нитрохинолин-4-иламино)фенил]-2-метилпропионитрила (пример 1 е) выдерживали в 300 мл МеОН-ТГФ (1:1) под давлением H2 1,1 бар в присутствии 8,35 г никеля Ренея в течение 1 ч. После завершения реакции катализатор отфильтровали и фильтрат упаривали насухо, получая указанное в заглавии соединение в виде желтой пены. ЕС-МС: 381, 383 (М+ Н)+, Br образец; аналитическая ЖХВД: t уд=3,21 мин (Град 1).(пример 1g) и 1,59 г (15,7 ммоль) триэтиламина в 120 мл CH2Cl2 добавляли в течение 40 мин к раствору 2,85 г (14,4 ммоль) трихлорметилхлорформиата (Fluka, Buchs, Швейцария) в 80 мл CH2Cl2 при 0 С на ледяной бане. Реакционную смесь перемешивали в течение 20 мин при этой температуре, после этого закаливали насыщенным водным NaHCO3, перемешивали в течение 5 мин и экстрагировали CH2Cl2. Органический слой высушивали над Na2SO4, фильтровали и упаривали в вакууме, получая неочищенное указанное в заглавии соединение в виде коричневатого твердого вещества. ЕС-МС: 407, 409 (М+Н)+, Br образец; аналитическая ЖХВД: t уд=3,05 мин (Град 1). Пример 1i. 2-[4-(8-Бром-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]-2-метилпропионитрил(0,847 ммоль) бромид тетрабутиламмония (Fluka, Buchs, Швейцария) в 170 мл CH2Cl2 добавляли раствор 508 мг (12,7 ммоль) NaOH (Fluka, Buchs, Швейцария) в 85 мл H2O. Реакционную смесь перемешивали в течение 2 дней и добавляли 900 мг (6,35 ммоль) йодметана и 254 мг (6,35 ммоль) NaOH в 5 мл H2O. Реакционную смесь перемешивали в течение 1 дня при кт. После этого реакционную смесь закаливали с помощью H2O и экстрагировали CH2Cl2 (2). Органический слой промывали соляным раствором, высушивали над Na2SO4, фильтровали и упаривали в вакууме, получая указанное в заглавии соединение в виде бежевого твердого вещества. ЕС-МС: 421, 423 (М+Н)+, Br образец; аналитическая ЖХВД: t уд=3,15 мин (Град 1). Следующие соединения (табл. 1) готовили с помощью способа, аналогичного описанному в примере 1, путем взаимодействия 2-[4-(8-бром-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]2-метилпропионитрила (пример 1i) с подходящей бороновой кислотой. Пример 2. 3-Пиридинбороновая кислота (Aldrich, Buchs, Швейцария). Пример 3. 4-Метокси-3-пиридилбороновая кислота (Frontier Scientific, Logan, США). Пример 4. Пинеколовый эфир 3-метоксипиридин-5-бороновой кислоты (Frontier Scientific, Logan,США). Пример 5. трет-Бутиловый эфир 4-[5-(4,4,5,5-тетраметил[1,3,2]диоксаборолан-2-ил)пиридин-2 ил]пиперазин-1-карбоновой кислоты (СВ ResearchDevelopment, New Castle, США). Пример 6. 1-Метил-4-[4-(4,4,5,5-тетраметил[1,3,2]диоксаборолан-2-ил)пиридин-2-ил]пиперазин Пример 12 а. 2-(4-Аминофенил)-2-этилбутиронитрил. Указанное в заглавии соединение готовили с помощью способа, аналогичного описанному в примере 1 е, используя йодэтан (Fluka, Buchs, Швейцария) в примере 1d. ЕС-МС: 189 (М+Н)+, Br образец; аналитическая ЖХВД: t уд=2,50 мин (Град 1). Следующие соединения (табл. 3) готовили с помощью способа, аналогичного описанному в примере 1, путем взаимодействия 6-бром-4-хлор-3-нитрохинолина (пример 1 с) с 1-(4-амино-2 фторфенил)пирролидин-2-оном (пример 14 а) и с подходящей бороновой кислотой. Пример 14 а. 1-(4-Амино-2-фторфенил)пирролидин-2-он. 650 мг (2,9 ммоль) 1-(2-фтор-4-нитрофенил)пирролидин-2-она (пример 14b) и 65 мг Pd/C 10% выдерживали в 15 мл МеОН/ТГФ (1:1) под давлением H2 1,1 бар в течение 2 ч при кт. После завершения реакции катализатор отфильтровали и фильтрат упаривали в вакууме, получая указанное в заглавии соединение в виде не совсем белого твердого вещества. ЕС-МС: 195 (М+Н)+; аналитическая ЖХВД: t уд=1,91 мин (Град 1). Пример 14b. 1-(2-Фтор-4-нитрофенил)пирролидин-2-он. К 468 мг (5,5 ммоль) 2-пирролидона (Fluka, Buchs, Швейцария) в 10 мл ДМФА при 0 С добавляли 240 мг (5,5 ммоль) 55% NaH в масле. Реакционную смесь перемешивали в течение 30 мин при 0 С и в течение 30 мин при кт. После этого добавляли 795 мг (5 ммоль) 3,4-дифторнитробензола (Aldrich, Buchs,Швейцария) и реакционную смесь перемешивали в течение 1 ч при кт. Реакционную смесь закаливали с помощью 1 М водной HCl и экстрагировали EtOAc (2). Органические слои промывали водным насыщенным NaHCO3 и соляным раствором (3), высушивали над MgSO4, фильтровали и упаривали. Остаток очищали с помощью флэш-хроматографии на силикагеле (гексан-EtOAc от 5:1 до 1:3), получая указанное в заглавии соединение в виде твердого вещества. ЕС-МС: 225 (М+Н)+; аналитическая ЖХВД: t уд=2,99 мин (Град 1). Следующие соединения (табл. 4) готовили с помощью способа, аналогичного описанному в примере 1, путем взаимодействия 6-бром-4-хлор-3-нитрохинолина (пример 1 с) с 1-(4-аминофенил)пирролидин 2-оном (пример 16 а) и с подходящей бороновой кислотой. Таблица 4 Пример 16 а. 1-(4-Аминофенил)пирролидин-2-он. Указанное в заглавии соединение получали с помощью способа, аналогичного описанному в примере 14 а, используя в качестве исходного соединения 1-(4-нитрофенил)пирролидин-2-он (Acros, Basel,Швейцария). ЕС-МС: 177 (М+Н)+; аналитическая ЖХВД: t уд=2,71 мин (Град 1). Следующие соединения (табл. 5) готовили с помощью способа, аналогичного описанному в примере 1, путем взаимодействия 6-бром-4-хлор-3-нитрохинолина (пример 1 с) с 2-фтор-N1,N1-бис-(2 метоксиэтил)бензол-1,4-диамином (пример 18 а) и с подходящей бороновой кислотой. Таблица 5- 27013434 Пример 18 а. 2-Фтор-N1,N1-бис-(2-метоксиэтил)бензол-1,4-диамин. Указанное в заглавии соединение получали с помощью способа, аналогичного описанному в примере 14 а, используя в качестве исходного соединения (2-фтор-4-нитрофенил)-бис-(2-метоксиэтил)амин(пример 18b). ЕС-МС: 243 (М+Н)+; аналитическая ЖХВД: t уд=1,98 мин (Град 1). Пример 18b. (2-Фтор-4-нитрофенил)-бис-(2-метоксиэтил)амин. 1,13 г (7,1 ммоль) 3,4-дифторнитробензола (Aldrich, Buchs, Швейцария), 1,04 г (7,81 ммоль) бис-(2 метоксиэтил)амина (Fluka, Buchs, Швейцария) и 1,96 г (14,2 ммоль) K2CO3 в 7 мл ДМСО перемешивали в течение 1,5 ч при кт и затем нагревали до 80 С в течение 4 ч. Реакционную смесь гасили с помощью H2O и экстрагировали EtOAc (2). Органические слои промывали соляным раствором (3), высушивали над Пример 20 а. N,N-бис-(2-Метоксиэтил)бензол-1,4-диамин. Указанное в заглавии соединение получали с помощью способа, аналогичного описанному в примере 18b, используя в качестве исходного соединения 4-фторнитробензол (Aldrich, Buchs, Швейцария). ЕС-МС: 225 (М+Н)+; аналитическая ЖХВД: t уд=1,94 мин (Град 1). Следующие соединения (табл. 7) готовили с помощью способа, аналогичного описанному в примере 1, путем взаимодействия 6-бром-4-хлор-3-нитрохинолина (пример 1 с) с 2-нафтиламином (Aldrich,Buchs, Швейцария) и с подходящей бороновой кислотой. Таблица 7 Пример 40 а. 4-Метоксиметиланилин. Указанное в заглавии соединение известно из литературы (описано в Journal of Chemical Society. Пример 42 а. 2-Хлор-4-(2-метоксиэтил)фениламин. 2 г (13,2 ммоль) 4-(2-метоксиэтил)фениламина (пример 42b) и 1,85 г (13,9 ммоль) Nхлорсукцинимида (Aldrich, Buchs, Швейцария) в 26 мл изопропанола перемешивали при кт в течение 30 мин. Реакционную смесь упаривали насухо и остаток ресуспендировали в EtOAc. Органические слои промывали насыщенным водным NaHCO3 (2), высушивали над MgSO4, фильтровали и упаривали. Остаток очищали с помощью флэш-хроматографии на силикагеле (гексан-EtOAc от 5:1 до 2:1), получая указанное в заглавии соединение в виде масла. ЕС-МС: 186 (М+Н)+; аналитическая ЖХВД: t уд=2,42 мин (Град 1).
МПК / Метки
МПК: A61K 31/4188, A61P 35/00, C07D 471/04, A61P 29/00
Метки: ингибиторов, имидазохинолины, липидкиназы, качестве
Код ссылки
<a href="https://eas.patents.su/30-13434-imidazohinoliny-v-kachestve-ingibitorov-lipidkinazy.html" rel="bookmark" title="База патентов Евразийского Союза">Имидазохинолины в качестве ингибиторов липидкиназы</a>
Предыдущий патент: Аэрозольные и впрыскиваемые рецептуры лекарственных препаратов бензодиазепина, состоящего из наночастиц
Следующий патент: Антагонисты мускариновых ацетилхолиновых рецепторов
Случайный патент: Способ и устройство для выделения ароматической карбоновой кислоты из ее суспензии в растворителе












