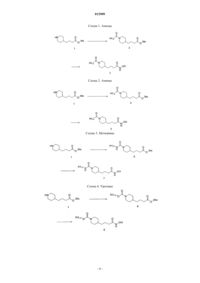
Гидроксаматы как ингибиторы гистондеацетилазы и содержащие их фармацевтические композиции
Номер патента: 12909
Опубликовано: 26.02.2010
Авторы: Росси Кристина, Порчеллони Марина, Фаттори Даниэла, Д'андреа Пьеро, Марастони Елена
Формула / Реферат
1. Соединение общей формулы II:
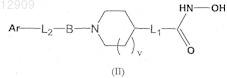
где v=1;
В означает химическую связь или выбран из группы -CO-, -NR5-CO-, -O-СO-, -SO2-, -NR5-SO2-, либо означает одну из следующих структур:
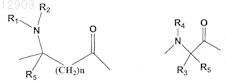
в которой n = 0, 1, 2, a R5 означает H или C1-3-алкил;
R1 означает H или выбран из группы: C1-3-алкил, C1-3-ацил либо ацил от одной из следующих кислот: бензойной, фенилуксусной, бензотиофенкарбоновой, индолкарбоновой;
R2 означает H или C1-3-алкил;
либо R1 и R2 вместе с атомом азота представляют собой 5- или 6-членный гетероцикл, выбранный из пирролидина, пиперидина, пиперазина, морфолина, тиоморфолина;
R3 означает H или выбран из группы: C1-6-алкил, С1-6-алкилен-W, где W выбрано из -OR5, -SR5, -CONR7R8,
-NR7R8, -OCOR6, -NR5COR6, гуанидина, a R7 и R8 независимо означают H или C1-3-алкил, либо R7 и R8 вместе с атомом азота представляют собой 5- или 6-членный гетероцикл, выбранный из пирролидина, пиперидина, пиперазина, морфолина, тиоморфолина, и R6 выбран из группы: водород, C1-3-алкил, Аr1, где Ar1 означает ароматическую группу, выбранную из фенила, нафтила, пиридина, хинолина, индола, бензофурана, бензотиофена, и необязательно может быть замещен (вплоть до трех) группами, выбранными независимо из C1-3-алкила, OR9, SR9, NR9R10, N(R9)COR10, NO2, CN, F, Cl, Br, -CF3, COOR9, CONR9R10, CN2NR9R10, N(R9)SO2R10, CH2OR9, SOH, CH2SO3H, где R9 означает группу, выбранную из H, C1-3-алкила, -(CH2)q-NR10R11, пирролидина, a R10 и R11 независимо означают группу, выбранную из H и C1-3-алкила, q может принимать значения 2 или 3;
R4 означает H или C1-3-алкил;
либо R4 и R3 вместе с атомом азота представляют собой гетероцикл, выбранный из пирролидина и пиперидина;
L1 выбран из группы алкилиден типа -(CH2)m-, необязательно замещенный по каждому атому С одной или двумя метальными группами, причем m может принимать значения 1, 2, 3;
L2 означает химическую связь или группу, выбранную из -(СН2)Р-, -(СН2)р-CH=CH-, -(CH2)P-T-(CH2)Z-, -(CH2)P-CO-, -(CH2)P-CH=CH-CO-, -CO-T-(CH2)Z, -(CH2)P-T-CO-, причем каждая группа необязательно замещена по атомам С одной или двумя метальными группами, при этом р и z независимо могут принимать значения 0, 1, 2, 3 или 4, a T выбран из -O-, -S-, -NR5-;
Ar означает группу, происходящую из следующих ароматических систем: фенил, пиридил, фурил, пиримидил, пиразил, пиперазил, триазолил, тетразолил, бифенил, имидазолил, нафтил, хинолин, изохинолин, дифенилметил, бензофурил, дигидробензофурил, бензотиенил, индолил, бензотиазолил, бензоксазолил, бензизоксазолил, оксазолилфенил, тиодиазолилфенил, пиридилфенил, пиразолилфенил, тиазолилфенил, фурилфенил, тиенилфенил, бензилоксифенил, тетразолил фенил, фенилоксазолил, фенилпиразолил, фенилтиазолил, фенилтиадиазолил, фенилизотиазолил, фенилоксадиазолил, фенилизоксазолил, фенилимидазолил, фенилтриазолил, фенилфурил, фенилтиофенил, фенилпирролил, фенилпирролидил, инданил, флуоренил, бензопиранил, дигидробензопиранил, бензодиоксолил, феноксифенил, бензоксазинил, дигидробензоксазинил, причем каждая группа необязательно может быть замещена вплоть до тремя группами, выбранными независимо из C1-3-алкила, OR9, SR9, NR9R10, N(R9)COR10, NO2, CN, F, Cl, Br, -CF3, -SCF3, COOR9, CONR9R10, -(CH2)q-NR9R10, N(R9)SO2R10, CH2OR9, SOH, CH2SO3H, где R9 означает группу, выбранную из H, C1-4-алкила, -(CH2)q-NR10R11, пирролидина, a R10 и R11 независимо выбраны из H и C1-3-алкила, q может принимать значения 1, 2 или 3;
либо Ar-L2-B совместно могут быть выбраны из группы, состоящей из
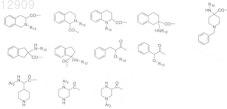
где группа R12 представляет собой H, C1-3-алкил или C1-3-ацил;
Ar2 означает ароматическую группу, выбранную из бензила или ацила, происходящего из бензойной, фенилуксусной или бензотиофенкарбоновой кислоты;
причем ароматическая часть может быть замещена (вплоть до трех) группами, выбранными независимо из C1-3-алкила, OR9, SR9, NR9R10, N(R9)COR10, NO2, CN, F, Cl, Br, -CF3, -SCF3, COOR9, CONR9R10, -(CH2)q-NR9R10, N(R9)SO2R10, CH2OR9, SOH, CH2SO3H, где R9 означает группу, выбранную из H, C1-4-алкила, -(CH2)q-NR10R11, пирролидина, a R10 и R11 независимо выбраны из H и C1-3-алкила, q может принимать значения 1, 2 или 3;
соответствующие пролекарственные формы общей формулы III и IV:

где L означает
![]()
при этом Ar, L2, B, v и L1 определены выше, Rx может означать Ac, COEt, CO-nPr, CO-iPr, CO-tBu, бензоил, pNO2-бeнзoил, CH3, Et, nPr, iPr, tBu, бензил, тетрагидропиранил, a Ry и Rz независимо означают H или C1-3-алкил;
за исключением тех продуктов, у которых В выбран из -NR5-CO- или -NR5-SO2- и в то же время L2 выбран из
-(СН2)р-СО- или -(СН2)р-СН=СН-СО-;
его возможные оптические изомеры, как-то энантиомеры и/или диастереоизомеры, их смеси, как рацемические, так и в разных пропорциях, и его соли неорганических и органических кислот.
2. Соединения по п.1 общей формулы II, где v=1;
В означает химическую связь или выбран из группы -CO-, -NR5-CO-, -O-СO-, либо означает одну из следующих структур:
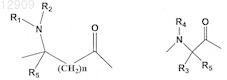
в которой n = 0, 1, a R5 означает H или C1-3-алкил;
R1 означает H или выбран из группы: C1-3-алкил, C1-3-ацил;
R2 означает H или C1-3-алкил;
R3 означает H или С1-6-алкилен-W, где W выбрано из -OR5, -NR7R8, a R7 и R8 независимо означают H или C1-3-алкил;
R4 означает H или C1-3-алкил;
L1 выбран из группы: алкилиден типа -(СН2)m-, необязательно замещенный по каждому атому С одной или двумя метальными группами, причем m может принимать значения 2, 3;
L2 означает химическую связь или группу, выбранную из -(СН2)Р-, -(СН2)Р-CH=CH-, -(CH2)p-T-(CH2)Z-, -(CH2)P-CO-, -CO-T-(CH2)z-, -(CH2)P-T-CO-, причем каждая группа необязательно замещена по атомам С одной или двумя метальными группами, при этом p и z независимо могут принимать значения 0,1, 2, 3, a T выбран из -O-, -S-, -NR5-;
Ar означает группу, происходящую из следующих ароматических систем: фенил, пиридил, фурил, триазолил, бифенил, нафтил, хинолин, изохинолин, бензофурил, бензотиенил, индолил, бензотиазолил, бензизоксазолил, оксазолилфенил, тиодиазолилфенил, пиридилфенил, пиразолилфенил, тиазолилфенил, фурилфенил, тиенилфенил, бензилоксифенил, тетразолилфенил, фенилоксазолил, фенилпиразолил, фенилтиазолил, фенилтиадиазолил, фенилизотиазолил, инданил, флуоренил, бензодиоксолил, феноксифенил, причем каждая группа необязательно может быть замещена (вплоть до трех) группами, выбранными независимо из C1-3-алкила, OR9, NR9R10, N(R9)COR10, CN, F, Cl, Br, -CF3, -SCF3, -(CH2)q-NR9R10, где R9 означает группу, выбранную из H, C1-4-алкила, a R10и R11 независимо выбраны из H и C1-3-алкила, q может принимать значения 2 или 3;
либо Ar-L2-B совместно могут быть выбраны из группы, состоящей из
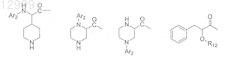
в которой группа R12 представляет собой H или C1-3-алкил;
Аr2 означает ароматическую группу, выбранную из бензила или ацила, происходящего из бензойной, фенилуксусной или бензотиофенкарбоновой кислоты;
причем ароматическая часть может быть замещена (вплоть до трех) группами,
выбранными независимо из C1-3-алкила, OR9, NR9R10, N(R9)COR10, CN, F, Cl, Br, -CF3, - SCF3, -(CH2)q-NR9R10, где R9 означает группу, выбранную из H, C1-4-алкила, a R10и R11 независимо выбраны из H и C1-3-алкила, q может принимать значения 2 или 3;
за исключением тех продуктов, у которых В выбран из -NR5-CO- и в то же время L2 выбран из -(СН2)р-СО-.
3. Соединения общей формулы II по п.2, а именно:
4-[1-(2-хлорбензолсульфонил)пиперидин-4-ил]-N-гидроксибутирамид,
N-гидрокси-4-[1-(4-метилнафталин-2-сульфонил)пиперидин-4-ил]бутирамид,
N-гидрокси-4-[1-(нафталин-2-карбонил)пиперидин-4-ил]бутирамид,
N-гидрокси-4-[1-(нафталин-1-карбонил)пиперидин-4-ил]бутирамид,
N-гидpoкcи-4-[1-(2-нафталин-1-илацетил)пиперидин-4-ил]бутирамид,
N-гидрокси-4-[1-(1-нафталин-1-илацетил)пиперидин-4-ил]бутирамид,
бензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
фениламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
N-гидрокси-4-[1-(нафталин-2-сульфонил)пиперидин-4-ил]-бутирамид,
N-гидрокси-4-[1-(нафталин-1-сульфонил)пиперидин-4-ил]-бутирамид,
N-{3-[4-(3-гидроксикарбамоилпропил)пиперидин-1-карбонил]фенил}бензамид,
4-[1-(бензофуран-2-карбонил)пиперидин-4-ил]-N-гидроксибутирамид,
N-гидрокси-4-[1-(6-метоксинафталин-2-карбонил)пиперидин-4-ил]бутирамид,
(3-фторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
N-гидрокси-4-[1-(2-метилнафталин-1-карбонил)пиперидин-4-ил]бутирамид,
(4-бромфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-хлорфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(3-хлорфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(3-фторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-метоксифенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(3-метоксифенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
n-толиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
о-толиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(бензо[b]тиофен-2-карбонил)пиперидин-4-ил]-N-гидроксибутирамид,
(3-фторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(бензилоксикарбонил)пиперидин-4-ил]-N-гидроксибутирамид,
N-гидрокси-4-[1-(3-фенилакрилоил)пиперидин-4-ил]бутирамид,
N-гидрокси-4-[1-(1-метил-1H-индол-3-карбонил)пиперидин-4-ил]бутирамид,
N-гидрокси-4-[1-(4-фенилбутирил)пиперидин-4-ил]-бутирамид,
N-гидрокси-4-[1-(2-1Н-индол-3-илацетил)пиперидин-4-ил]бутирамид,
N-гидрокси-4-{1-[2-(5-метил-2-фенилоксазол-4-ил)ацетил]пиперидин-4-ил}бутирамид,
N-гидрокси-4-{1-[2-(2-фенилтиазол-4-ил)ацетил]пиперидин-4-ил}бутирамид,
4-[1-(2-бензо[d]изоксазол-3-илацетил)пиперидин-4-ил]-N-гидроксибутирамид,
4-хлорбензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
1-нафтиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
2-нафтиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(2-метоксифенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(2-хлорфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
3-хлорбензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(2-(S)-амино-3-фенилпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
4-[1-(2-(R)-амино-3-фенилпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
2-метоксибензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
3-метоксибензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-метоксибензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
2-фторбензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
3-фторбензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
2-хлорбензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-диметиламинофенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-аминофенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
2-метилбензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
3-метилбензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-метилбензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(пиридин-4-илметил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(нафталин-1-илметил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(нафталин-2-илметил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(бифенил-4-илметил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-феноксибензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-фенэтиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
гидроксиамид 6-{[бензил-(2-гидроксиэтил)амино]метил}-7-фторбензо[b]тиофен-2-карбоновой кислоты,
4-{1-[2-амино-3-(4-хлорфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-{1-[2-амино-3-(3-хлорфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-{1-[2-(R)-амино-3-(3,4-дихлорфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-{1-[2-(R)-амино-3-(4-метоксифенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-[1-(2-(R)-амино-2-метил-3-фенил)пропионил)пиперидин-4-ил]-N-гидроксибутирамид,
4-{1-[2-(R)-амино-3-(1Н-индол-3-ил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-{1-[2-(S)-амино-3-(1Н-индол-3-ил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-[1-(2-(R)-амино-3-бензилоксипропионил)пиперидин-4-ил]-N-гидроксибутирамид,
4-{1-[2-(R)-амино-3-(4-трет-бутоксифенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-[1-(2-(R)-амино-3-бензилсульфанилпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
пиридин-3-иламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(пиридин-3-илметил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(3-аминофенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(2-аминофенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-диметиламинобензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-фторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
м-толиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
бензилметиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
N-гидрокси-4-{1-[2-(2-1Н-индол-3-илацетиламино)ацетил]пиперидин-4-ил}бутирамид,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-2-оксоэтил}амид бензо[b]тиофен-2-карбоновой кислоты,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-2-оксоэтил}амид нафталин-1-карболовой кислоты,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-2-оксоэтил}амид 2-метилнафталин-1-карбоновой кислоты,
4-[1-(2-(S)-амино-4-фенилбутирил)пиперидин-4-ил]-N-гидроксибутирамид,
(3-хлор-2-фторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(2,4-дифторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(3-хлор-4-метилфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(3,4-дифторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(3,4-диметилфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(3-хлор-4-фторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(2,5-дифторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-хлор-2-фторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(2,4-диметоксифенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
N-гидрокси-4-[1-(2-(R)-метиламино-3-фенилпропионил)пиперидин-4-ил]-бутирамид,
4-[1-(2-(R)-амино-3-нафталин-1-илпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
4-[1-(2-(R)-амино-3-бензо[b]тиофен-3-илпропионил)пиперидин-4-ил] -N-гидроксибутирамид,
4-[1-(2-(R)-амино-3-м-толилпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
4-{1-[2-(S)-амино-3-(4-бензоилфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-{1-[2-(R)-аминo-3-(2-фтopфeнил)пpoпиoнил]пипepидин-4-ил}-N-гидpoкcибутирамид,
4-{1-[2-(R)-амино-3-(3-фторфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-{1-[2-(R)-амино-3-(4-фторфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
N-гидрокси-4-[1-(2-(R)-гидрокси-3-фенилпропионил)пиперидин-4-ил]бутирамид,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-1-(S)-гидроксиметил-2-оксоэтил}амид бензо[b]тиофен-2-карбоновой кислоты,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-1-(R)-гидроксиметил-2-оксоэтил}амид бензо[b]тиофен-2-карбоновой кислоты,
4-[1-(2-(S)-диметиламино-4-фенилбутирил)пиперидин-4-ил]-N-гидроксибутирамид,
2,4-дихлорбензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(2-(S)-амино-4-фенилбутирил)пиперидин-4-ил]-N-гидроксибутирамид,
(фуран-2-илметил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
{4-амино-1-(R)-[4-(3-гидроксикарбамоилпропил)пиперидин-1-карбонил]бутил}амид бензо[b]тиофен-2-карбоновой кислоты,
4-[1-(3-(R)-амино-4-нафталин-2-илбутирил)пиперидин-4-ил]-N-гидроксибутирамид,
4-[1-(3-(S)-амино-3-нафталин-2-илпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
{3-гидрокси-1-(R)-[4-(3-гидроксикарбамоилпропил)пиперидин-1-карбонил]пропил}амид бензо[b]тиофен-2-карбоновой кислоты,
4-[1-(3-(R)-амино-3-нафталин-2-илпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
4-[1-(3-(S)-амино-3-фенилпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
{3-гидрокси-1-(S)-[4-(3-гидроксикарбамоилпропил)пиперидин-1-карбонил]пропил}амид бензо[b] тиофен-2-карбоновой кислоты,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-1-(S)-гидроксиметил-2-оксоэтил}амид бензо[b]тиофен-5-карбоновой кислоты,
{1-(R)-аминометил-2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-2-оксоэтил}амид бензо[b]тиофен-2-карбоновой кислоты,
4-{1-[2-(S)-(2-бензо[b]тиофен-3-илацетиламино)-3-гидроксипропионил]пиперидин-4-ил}-N-гидроксибутирамид,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-1-(S)-гидроксиметил-2-оксоэтил}амид бензо[b]тиофен-3-карбоновой кислоты,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-1-(S)-гидроксиметил-2-оксоэтил}амид бензофуран-2-карбоновой кислоты,
N-гидрокси-4-{1-[3-гидрокси-2-(S)-(2-нафталин-1-илацетиламино)пропионил]пиперидин-4-ил}бутирамид,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-1-(S)-гидроксиметил-2-оксоэтил}амид 1Н-индол-2-карбоновой кислоты,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-1-(S)-гидроксиметил-2-оксоэтил}амид хинолин-2-карбоновой кислоты,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-1-(S)-гидроксиметил-2-оксоэтил}амид изохинолин-1-карбоновой кислоты,
{2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-1-(S)-гидроксиметил-2-оксоэтил}амид изохинолин-3-карбоновой кислоты,
{1-аминометил-2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-2-оксоэтил}амид бензо[b]тиофен-2-карбоновой кислоты,
4-хлор-2-фторбензиламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(2-амино-4-метилфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(2-фтор-6-метоксифенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(2-фтор-5-метилфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(2-хлор-6-фторфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(3-(R)-амино-3-фенилпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
4-[1-(3-(S)-амино-5-фенилпентаноил)пиперидин-4-ил]-N-гидроксибутирамид,
(4-бутилфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
N-гидрокси-4-(1-фенил сульфамоилпиперидин-4-ил)бутирамид,
4-[1-(3-(R)-амино-5-фенилпентаноил)пиперидин-4-ил]-N-гидроксибутирамид,
бифенил-4-иламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(бензо[1,3]диоксол-5-илметил)амид 4-(3-]гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-феноксифенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-пропоксифенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-изопропоксифенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(1-(R)-фенилэтил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(1-(S)-фенилэтил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(3-(R)-амино-3-нафталин-2-илпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
хинолин-2-иламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(3-(R)-амино-4-нафталин-2-илбутирил)пиперидин-4-ил]-N-гидроксибутирамид,
[4-(2-диэтиламиноэтил)фенил]амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(3-(S)-амино-4-бензо[b]тиофен-3-илбутирил)пиперидин-4-ил]-N-гидроксибутирамид,
4-[1-(3-(R)-амино-4-бензо[b]тиофен-3-илбутирил)пиперидин-4-ил]-N-гидроксибутирамид,
{1-диметиламинометил-2-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-2-оксоэтил}амид бензо[b]тиофен-2-карбоновой кислоты,
4-[1-(3-(S)-амино-3-нафталин-2-илпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
бифенил-3-иламид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-пиридин-2-илфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-оксазол-5-илфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-пиридин-3-илфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(3-(S)-амино-4-нафталин-1-илбутирил)пиперидин-4-ил]-N-гидроксибутирамид,
4-[1-(3-(R)-амино-4-нафталин-1-илбутирил)пиперидин-4-ил]-N-гидроксибутирамид,
4-(4-(гидроксиамино)-4-оксобутил)-N-((2-фенилтиазол-4-ил)метил)пиперидин-1-карбоксамид,
N-(бензо[b]тиофен-3-илметил)-4-(4-(гидроксиамино)-4-оксобутил)пиперидин-1-карбоксамид,
4-[1-(3-(S)-амино-3-нафталин-1-илпропионил)пиперидин-4-ил] -N-гидроксибутирамид,
4-[1-(3-(R)-амино-3-нафталин-1-илпропионил)пиперидин-4-ил]-N-гидроксибутирамид,
4-(4-(гидроксиамино)-4-оксобутил)-N-(1-метоксинафталин-2-ил)пиперидин-1-карбоксамид,
4-(4-(гидроксиамино)-4-оксобутил)-N-(3-метоксинафталин-2-ил)пиперидин-1-карбоксамид,
4-(4-(гидроксиамино)-4-оксобутил)-N-((5-метил-2-фенилоксазол-4-ил)метил)пиперидин-1-карбоксамид,
N-(2-(1Н-индол-3-ил)этил)-4-(4-(гидроксиамино)-4-оксобутил)пиперидин-1-карбоксамид,
4-[1-(3-бензиламинопропионил)пиперидин-4-ил]-N-гидроксибутирамид,
(3'-фторбифенил-4-ил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4'-фторбифенил-4-ил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-{1-[3-(S)-амино-3-(2-хлорфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-{1-[3-(S)-амино-3-(3-хлорфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
(3'-метоксибифенил-4-ил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
N-(3-(1Н-индол-3-ил)пропил)-4-(4-(гидроксиамино)-4-оксобутил)пиперидин-1-карбоксамид,
4-{1-[3-(S)-амино-3-(3-хлорфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
N-гидрокси-4-[1-(4-метоксибензилтиокарбамоил)пиперидин-4-ил]бутирамид,
4-(1-бензилтиокарбамоилпиперидин-4-ил)-N-гидроксибутирамид,
4-{1-[3-(S)-амино-3-(4-фторфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-{1-[3-(S)-амино-3-(3-фторфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
4-{1-[3-(S)-амино-3-(2-фторфенил)пропионил]пиперидин-4-ил}-N-гидроксибутирамид,
N-(бензо[d]изоксазол-3-илметил)-4-(4-(гидроксиамино)-4-оксобутил)пиперидин-1-карбоксамид,
(4-[1,2,3]тиадиазол-4-илфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
[4-(3,5-диметилпиразол-1-ил)фенил]амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
[3-(2-метилтиазол-4-ил)фенил]амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
N-(6-аминонафталин-2-ил)-4-(4-(гидроксиамино)-4-оксобутил)пиперидин-1-карбоксамид,
4-(4-(гидроксиамино)-4-оксобутил)-N-(1Н-индол-5-ил)пиперидин-1-карбоксамид,
(5-метил-1-фенил-1Н-пиразол-4-ил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-пиррол-1-илфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(3-пиррол-1-илфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(3-(1)нафтиламинопропионил)пиперидин-4-ил}-N-гидроксибутирамид,
4-(4-(гидроксиамино)-4-оксобутил)-N-(1H-индол-3-ил)пиперидин-1-карбоксамид,
N-(5-хлорбензо[b]тиофен-3-илметил)-4-(4-(гидроксиамино)-4-оксобутил)пиперидин-1-карбоксамид,
N-(бензо[b]тиофен-5-ил)-4-(4-(гидроксиамино)-4-оксобутил)пиперидин-1-карбоксамид,
N-(4-(тиофен-3-ил)бензил)-4-(4-(гидроксиамино)-4-оксобутил)пиперидин-1-карбоксамид,
4-(4-(гидроксиамино)-4-оксобутил)-N-(3-фенилбензил)пиперидин-1-карбоксамид,
3-(4-(гидроксиамино)-4-оксобутил)-N-фенилпиперидин-1-карбоксамид,
2-(S)-амино-N-бензил-4-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-4-оксобутирамид,
2-(R)-амино-N-бензил-4- [4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-4-оксобутирамид,
N-(бензо[b]тиофен)-4-(4-(гидроксиамино)-4-оксобутил)пиперидин-1-карбоксамид,
4-(4-(гидроксиамино)-4-оксобутил)-N-((3-метилбензо[b]тиофен-2-ил)метил)пиперидин-1-карбоксамид,
N-((2,5-диметилтиазол-4-ил)метил)-4-(4-(гидроксиамино)-4-оксобутил)пиперидин-1-карбоксамид,
(5,6,7,8-тетрагидронафталин-1-ил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-бензилфенил)амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
(4-бензилоксифенил)амид 4-(3-гидроксикарбамоилпропил)-пиперидин-1-карбоновой кислоты,
{3-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-3-оксопропил}амид бензо[b]тиофен-2-карбоновой кислоты,
{4-[4-(3-гидроксикарбамоилпропил)пипериди[н-1-ил]-4-оксобутил}амид бензо[b]тиофен-2-карбоновой кислоты,
{2-(S)-амино-3-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-3-оксопропил}амид бензо[b]тиофен-2-карбоновой кислоты,
2-(S)-амино-4-[4-(3-гидроксикарбамоилпропил)пиперидин-1-ил]-N-нафталин-1-илметил-4-оксобутирамид,
[4-(2-метил-2Н-тетразол-5-ил)фенил]амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
[4-(2-изобутил-2Н-тетразол-5-ил)фенил]амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
[4-(3-метилпиразол-1-ил)фенил]амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
[2-(3-диметиламинопропил)-1Н-бензимидазол-5-ил]амид 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты,
4-[1-(1Н-бензимидазол-2-ил)-пиперидин-4-ил]-N-гидроксибутирамид.
4. Применение соединений по пп.1-3 для получения фармацевтических композиций, применимых в качестве ингибиторов гистондеацетилаз.
5. Применение по п.4 для получения фармацевтических композиций, применимых для лечения воспалительных заболеваний, диабета, осложнений диабета, гомозиготной талассемии, фиброза, цирроза, острой промиелоцитарной лейкемии (APL), отторжения трансплантатов, аутоиммунных заболеваний, протозойных инфекций и опухолевых патологий.
6. Применение по п.4 для получения фармацевтических композиций, применимых для лечения опухолевых патологий.
7. Применение соединений по пп.1-3 в комбинации с одним или несколькими активными началами, выбранными из химиотерапевтических средств, для получения фармацевтических композиций, применимых для лечения опухолевых патологий.
8. Применение соединений по пп.1-3 в комбинации с радиотерапевтическим лечением для получения фармацевтических композиций, применимых для лечения опухолевых патологий.
9. Применение по п.7 в комбинации с одним или несколькими соединениями, выбранными из групп: обычных цитотоксических средств, деметилирующих средств, ингибиторов циклинзависимых киназ, веществ, способствующих дифференцировке, модуляторов передачи сигналов, антагонистов HSP-90, ингибиторов протеасом.
10. Применение по п.9 в комбинации с одним или несколькими соединениями, выбранными из обычных цитотоксических средств: флударабина, гемцитабина, децитабина, паклитакселя, карбоплатина и ингибиторов топоизомеразы I/II, в том числе этопозида, иринотекана, топотекана, T-128, и таких антрациклинов, как доксорубицин, сабарубицин, даунорубицин; из деметилирующих средств: 5-аза-2'-дезоксицитидина (5-аза-dC), 5-азацитидина; из ингибиторов циклинзависимых киназ: флавопиридола, оломоуцина, росковитина, пурваланола В, GW9499, GW5181, CGP60474, CGP74514, AG12286, AG12275, стауроспорина, UCN-01; из веществ, способствующих дифференцировке: ретиноевой кислоты и ее производных (полностью транс-ретиноевой кислоты (ATRA), 13-цис-ретиноевой кислоты (CRA)), PMA (форболмиристатацетата); из модуляторов передачи сигналов: TRAIL, иматинибмезилата, LY-294002, бортезомиба; из антагонистов HSP-90: гелданамицина и его аналогов (17-AAG); из ингибиторов протеасом: лактацистина, MG132, бортезомиба (VelcadeÔ).
11. Фармацевтические композиции, содержащие в качестве активного начала соединение общей формулы I по пп.1-3, для лечения воспалительных заболеваний, диабета, осложнений диабета, гомозиготной талассемии, фиброза, цирроза, острой промиелоцитарной лейкемии (APL), отторжения трансплантатов, аутоиммунных заболеваний, протозойных инфекций и опухолевых патологий.
Текст
012909 Область техники, к которой относится изобретение Настоящее изобретение касается соединений-ингибиторов гистондеацетилазы, отличающихся наличием гидроксамовой группы, способов их получения и применения их для получения фармацевтических форм, предназначенных для лечения тех патологий, в которых важную роль играет механизм генной регуляции. В частности, настоящее изобретение касается соединений общей формулы I где v = 0, 1, 2; В означает химическую связь или выбран из группы -О-, -NR5, -CO-, -NR5-CO-, -O-СO-, -SO2-, -NR5SO2-, либо означает одну из следующих структур:R1 означает H или выбран из группы: C1-3-алкил, C1-3-ацил либо ацил от одной из следующих кислот: бензойной, фенилуксусной, бензотиофенкарбоновой, индолкарбоновой.R2 означает H или C1-3-алкил; либо R1 и R2 вместе с атомом азота представляют собой 5- или 6-членный гетероцикл, выбранный из пирролидина, пиперидина, пиперазина, морфолина, тиоморфолина;R3 означает H или выбран из группы: С 1-6-алкил, С 1-6-алкилен-W, где W выбрано из -OR5, -SR5,-CONR7R8, -NR7R8, -OCOR6, -NR5COR6, гуанидина, a R7 и R8 независимо означают H или C1-3-алкил, либоR7 и R8 вместе с атомом азота представляют собой 5- или 6-членный гетероцикл, выбранный из пирролидина, пиперидина, пиперазина, морфолина, тиоморфолина, и R6 выбран из группы: водород, C1-3-алкил,Ar1, где Ar1 означает ароматическую группу, выбранную из фенила, нафтила, пиридина, хинолина, индола, бензофурана, бензотиофена, и необязательно может быть замещен (вплоть до трех) группами, выбранными независимо из C1-3-алкила, OR9, SR9, NR9R10, N(R9)COR10, NO2, CN, F, Cl, Br, -CF3, COOR9,CONR9R10, CH2NR9R10, N(R9)SO2R10, CH2OR9, SOH, CH2SO3H, где R9 означает группу, выбранную из H,С 1-3-алкила, -(CH2)q-NR10R11, пирролидина, a R10 и R11 независимо означают группу, выбранную из H иC1-3-алкила, q может принимать значения 2 или 3;R4 означают группу, выбранную из H и C1-3 алкила; либо R4 и R3 вместе с атомом азота представляют собой гетероцикл, выбранный из пирролидина и пиперидина;L1 означает группу, присоединенную к любому из атомов углерода в гетероциклическом кольце и выбранную из группы: алкилиден типа -(СН 2)m-, необязательно замещенный по каждому атому С одной или двумя метальными группами, причем m может принимать значения 1, 2, 3, 4, 5, либо алкен, выбранный из -(CH2)e-CH=CH-(CH2)f, -(CH2)g-CH=CH-(CH2)h-CH=CH-(CH2)i-, необязательно замещенный по каждому атому С одной или двумя метальными группами, причем е, f, g, h и 1 независимо могут принимать значения 0, 1, 2, 3 или 4;L2 означает химическую связь или группу, выбранную из: -(СН 2)p-, -(СН 2)p-CH=CH-, -(CH2)p-T(CH2)z-, -(CH2)p-CO-, -(CH2)p-CH=CH-CO-, -CO-T-(CH2)z-, -(CH2)p-T-CO-, причем каждая группа необязательно замещена по атомам С одной или двумя метальными группами, при этом р и z независимо могут принимать значения 0, 1, 2, 3 или 4, a T выбран из -O-, -S-, -NR5-;Ar означает группу, происходящую из следующих ароматических систем: фенил, пиридил, фурил,пиримидил, пиразил, пиперазил, триазолил, тетразолил, бифенил, имидазолил, нафтил, хинолин, изохинолин, дифенилметил, бензофурил, дигидробензофурил, бензотиенил, индолил, бензотиазолил, бензоксазолил, бензизоксазолил, оксазолилфенил, тиодиазолилфенил, пиридилфенил, пиразолилфенил, тиазолилфенил, фурилфенил, тиенилфенил, бензилоксифенил, тетразолилфенил, фенилоксазолил, фенилпиразолил, фенилтиазолил, фенилтиадиазолил, фенилизотиазолил, фенилоксадиазолил, фенилизоксазолил, фенилимидазолил, фенилтриазолил, фенилфурил, фенилтиофенил, фенилпирролил, фенилпирролидил, инданил, флуоренил, бензопиранил, дигидробензопиранил, бензодиоксолил, феноксифенил, бензоксазинил, дигидробензоксазинил, причем каждая группа необязательно может быть замещена вплоть до тремя группами, выбранными независимо из С 1-3-алкила, OR9, SR9, NR9R10, N(R9)COR10, NO2, CN, F, Cl,Br, -CF3, -SCF3, COOR9, CONR9R10, -(CH2)q-NR9R10, N(R9)SO2R10, CH2OR9, SOH, CH2SO3H, где R9 означает группу, выбранную из H, C1-4-алкила, -(CH2)q-NR10R11, пирролидина, a R10 и R11 независимо выбраны из H и С 1-3-алкила, q может принимать значения 1, 2 или 3; либо Ar-L2-B совместно могут быть выбраныAr2 означает ароматическую группу, выбранную из бензила или ацила, происходящего из бензойной, фенилуксусной или бензотиофенкарбоновой кислоты; причем ароматическая часть может быть замещена (вплоть до трех) группами, выбранными независимо из C1-3-алкила, OR9, SR9, NR9R10, N(R9)COR10, NO2, CN, F, Cl, Br, -CF3, -SCF3, COOR9, CONR9R10,-(CH2)q-NR9R10, N(R9)SO2R10, CH2OR9, SOH, CH2SO3H, где R9 означает группу, выбранную из H, C1-4 алкила, -(CH2)q-NR10R11, пирролидина, a R10 и R11 независимо выбраны из H и C1-3-алкила, q может принимать значения 1, 2 или 3. Исключенными из настоящего изобретения следует считать продукты, у которых В выбран из -NR5CO- или -NR5-SO2- и в то же время L2 выбран из -(СН 2)р-СО- или -(СН 2)p-CH=CH-CO-. В настоящее изобретение также входят соответствующие пролекарственные формы общей формулы III и IV:H или C1-3-алкил. В настоящее изобретение также входят все возможные оптические изомеры, как-то энантиомеры и/или диастереоизомеры, возникающие вследствие возможного присутствия хиральных центров в соединениях общей формулы I, а также их возможные смеси, как рацемические, так и в разных пропорциях, и их соли неорганических и органических кислот. Уровень техники Гистондеацетилаза, как известно, играет важную роль в механизме, регулирующем экспрессию генов. Ингибиторы гистондеацетилазы (HDAC) вызывают гиперацетилирование гистонов с последующим изменением самой экспрессии генов. Следовательно, такие ингибиторы полезны как средства для терапии или профилактики патологических состояний, вызванных нарушением экспрессии генов, как-то воспалительных заболеваний, диабета, осложнений диабета, гомозиготной талассемии, фиброза, цирроза,острой промиелоцитарной лейкемии (APL), отторжения трансплантатов, аутоиммунных заболеваний,протозойных инфекций, опухолей и др. Фермент гистондеацетилаза уже хорошо изучен и, при исследовании различных классов ингибиторов методами рентгенографии и SAR, были установлены структурные характеристики, которыми должен обладать потенциальный ингибитор; в частности, это: а) домен, способный связывать металл (а именноZn), b) линкер, способный занимать канал фермента, и с) домен поверхностного узнавания, который взаимодействует со структурами, находящимися на кромке активного центра фермента (J. Med. Chem. 2003, 46(24), 5097-5116). За последние несколько лет появилось много примеров ингибиторов HDAC с вышеприведенными структурными характеристиками.Chem (2002) 45(4), 753-757; BioorganicMedicinal Chem. Letters (2004), 14, 449-453. В других публикациях отмечены гидроксамовые кислоты, у которых линкер не является линейным; в BioorganicMedicinal Chem. Letters (2001), 11, 2847-2890 линкер представлен фенилэтилом или стирилом, в BioorganicMedicinal Chem. Letters (2002), 12, 1347-1349 линкер представлен фенилом или циклогексилом, а в соединениях, описанных в WO 2004/013130, присутствует линкер, состоящий из тиофена. Другие авторы показали возможность замещения гидроксамовой кислоты другими группами, способными связывать металл из активного центра фермента, к примеру, амидами (J Med Chem (2003) 46,820-830; или в EP 847992) либо электрофильными кетонами. В WO 2004/069133 описаны соединения, у которых, в соответствии с вышеприведенной схемой, металлосвязывающая группа представлена фенилендиаминамидом, а линкер представлен гетероциклом, выбранным из индола, бензотиофена или бензофурана. В WO 2005/040101 (чтобы избежать возможного формального совпадения между заявленными соединениями и общей формулой, приведенной в этом документе, в п.1 настоящей формулы была вставлена соответствующая оговорка) также заявлены гидроксаматы, содержащие группы карбамоилпиперидина или что-то подобное в общем смысле. Несмотря на вс то, что уже известно по этой тематике, вс еще существует большая потребность в выявлении новых ингибиторов HDAC, что даст возможность получить новые лекарства для лечения многих патологий, которые потенциально излечимы по этому механизму действия. Осуществление изобретения Целью настоящего изобретения является получение новых ингибиторов HDAC общей формулы I,полезных в качестве лекарств, и фармацевтических композиций, содержащих их в качестве активных ингредиентов, для лечения или профилактики таких патологий, как воспалительные заболевания, диабет,осложнения диабета, гомозиготная талассемия, фиброз, цирроз, острая промиелоцитарная лейкемия(APL), отторжение трансплантатов, аутоиммунные заболевания, протозойные инфекции, опухоли и др. Настоящим изобретением предусмотрены соединения общей формулы I, как описано выше. Группу предпочтительных соединений настоящего изобретения составляют соединения общей формулы II: где v=1; В означает химическую связь или выбран из группы -CO-, -NR5-CO-, -O-СO-, -SO2-, -NR5-SO2-, либо означает одну из следующих структур:R1 означает H или выбран из группы: C1-3-алкил, C1-3-ацил либо ацил от одной из следующих кислот: бензойной, фенилуксусной, бензотиофенкарбоновой, индолкарбоновой.R2 означает H или C1-3-алкил; либо R1 и R2 вместе с атомом азота представляют собой 5- или 6-членный гетероцикл, выбранный из пирролидина, пиперидина, пиперазина, морфолина, тиоморфолина;R3 означает H или выбран из группы: -C1-6-алкил, -C1-6-алктлен-W, где W выбрано из -OR5, -SR5,-CONR7R8, -NR7R8, -OCOR6, -NR5COR6, гуанидина, a R7 и R8 независимо означают H или C1-3-алкил, либоR7 и R8 вместе с атомом азота представляют собой 5- или 6-членный гетероцикл, выбранный из пирролидина, пиперидина, пиперазина, морфолина, тиоморфолина, и R6 выбран из группы: водород, C1-3-алкил,Ar1, где Ar1 означает ароматическую группу, выбранную из фенила, нафтила, пиридина, хинолина, индола, бензофурана, бензотиофена, и необязательно может быть замещен (вплоть до трех) группами, выбранными независимо из C1-3-алкила, OR9, SR9, NR9R10, N(R9)COR10, NO2, CN, F, Cl, Br, -CF3, COOR9,CONR9R10, CN2NR9R10, N(R9)SO2R10, CH2OR9, SOH, CH2SO3H, где R9 означает группу, выбранную из H,C1-3-алкила, -(CH2)q-NR10R1, пирролидина, a R10 и R11 независимо означают группу, выбранную из H и C13-алкила, q может принимать значения 2 или 3;R4 означают H или C1-3-алкил; либо R4 и R3 вместе с атомом азота представляют собой гетероцикл, выбранный из пирролидина и пиперидина;L1 выбран из группы: алкилиден типа -(СН 2)m-, необязательно замещенный по каждому атому С од-3 012909 ной или двумя метальными группами, причем m может принимать значения 1, 2, 3;L2 означает химическую связь или группу, выбранную из: -(СН 2)p-, -(СН 2)p-CH=CH-, -(CH2)P-T(CH2)Z-, -(CH2)p-CO-, -(CH2)p-CH=CH-CO-, -CO-T-(CH2)Z-, -(CH2)P-T-CO-, причем каждая группа необязательно замещена по атомам С одной или двумя метильными группами, при этом р и z независимо могут принимать значения 0, 1, 2, 3 или 4, a T выбран из -O-, -S-, -NR5-;Ar означает группу, происходящую из следующих ароматических систем: фенил, пиридил, фурил,пиримидил, пиразил, пиперазил, триазолил, тетразолил, бифенил, имидазолил, нафтил, хинолин, изохинолин, дифенилметил, бензофурил, дигидробензофурил, бензотиенил, индолил, бензотиазолил, бензоксазолил, бензизоксазолил, оксазолилфенил, тиодиазолилфенил, пиридилфенил, пиразолилфенил, тиазолилфенил, фурилфенил, тиенилфенил, бензилоксифенил, тетразолилфенил, фенилоксазолил, фенилпиразолил, фенилтиазолил, фенилтиадиазолил, фенилизотиазолил, фенилоксадиазолил, фенилизоксазолил, фенилимидазолил, фенилтриазолил, фенилфурил, фенилтиофенил, фенилпирролил, фенилпирролидил, инданил, флуоренил, бензопиранил, дигидробензопиранил, бензодиоксолил, феноксифенил, бензоксазинил, дигидробензоксазинил, причем каждая группа необязательно может быть замещена вплоть до тремя группами, выбранными независимо из C1-3-алкила, OR9, SR9, NR9R10, N(R9)COR10, NO2, CN, F, Cl,Br, -CF3, -SCF3, COOR9, CONR9R10, -(CH2)q-NR9R10, N(R9)SO2R10, CH2OR9, SOH, CH2SO3H, где R9 означает группу, выбранную из H, С 1-4-алкила, -(CH2)q-NR10R1, пирролидина, a R10 и R11 независимо выбраны изH и C1-3-алкила, q может принимать значения 1, 2 или 3; либо Ar-L2-B совместно могут быть выбраны из группы, состоящей изAr2 означает ароматическую группу, выбранную из бензила или ацила, происходящего из бензойной, фенилуксусной или бензотиофенкарбоновой кислоты; причем ароматическая часть может быть замещена (вплоть до трех) группами, выбранными независимо из С 1-3-алкила, OR9, SR9, NR9R10, N(R9)COR10, NO2, CN, F, Cl, Br, -CF3, -SCF3, COOR9, CONR9R10,-(CH2)q-NR9R10, N(R9)SO2R10, CH2OR9, SOH, CH2SO3H, где R9 означает группу, выбранную из H, С 1-4 алкила, -(CH2)q-NR10R11, пирролидина, a R10 и R11 независимо выбраны из H и C1-3-алкила, q может принимать значения 1, 2 или 3. Исключенными из настоящего изобретения следует считать продукты, у которых В выбран из -NR5CO- или -NR5-SO2- и в то же время L2 выбран из -(СН 2)р-СО- или -(СН 2)Р-CH=CH-CO-. В настоящее изобретение также входят соответствующие пролекарственные формы общей формулы III и IV:H или C1-3-алкил. В настоящее изобретение также входят все возможные оптические изомеры, как-то энантиомеры и/или диастереоизомеры, возникающие вследствие возможного присутствия хиральных центров в соединениях общей формулы I, а также их возможные смеси, как рацемические, так и в разных пропорциях, и их соли от неорганических и органических кислот. Группу особенно предпочтительных соединений настоящего изобретения составляют соединения общей формулы II, где V=1;-4 012909 В означает химическую связь или выбран из группы -CO-, -NR5-CO-, -O-CO-, либо означает одну из следующих структур:R1 означает H или выбран из группы C1-3-алкил, C1-3-ацил;L1 выбран из группы: алкилиден типа -(CH2)m-, необязательно замещенный по каждому атому С одной или двумя метальными группами, причем m может принимать значения 2, 3;L2 означает химическую связь или группу, выбранную из -(СН 2)Р-, -(СН 2)Р-CH=CH-, -(CH2)P-T(CH2)z-, -(CH2)P-CO-, -CO-T-(CH2)z-, -(CH2)P-T-CO-, причем каждая группа необязательно замещена по атомам С одной или двумя метальными группами, при этом р и z независимо могут принимать значения 0,1, 2, 3, a T выбран из -O-, -S-, -NR5-;Ar означает группу, происходящую из следующих ароматических систем: фенил, пиридил, фурил,триазолил, бифенил, нафтил, хинолин, изохинолин, бензофурил, бензотиенил, индолил, бензотиазолил,бензизоксазолил, оксазолилфенил, тиодиазолилфенил, пиридилфенил, пиразолилфенил, тиазолилфенил,фурилфенил, тиенилфенил, бензилоксифенил, тетразолилфенил, фенилоксазолил, фенилпиразолил, фенилтиазолил, фенилтиадиазолил, фенилизотиазолил, инданил, флуоренил, бензодиоксолил, феноксифенил, причем каждая группа необязательно может быть замещена вплоть до тремя группами, выбранными независимо из C1-3-алкила, OR9, NR9R10, N(R9)COR10, CN, F, Cl, Br, -CF3, -SCF3, -(CH2)q-NR9R10, где R9 означает труппу, выбранную из H, C1-4-алкила, a R10 и R11 независимо выбраны из H и С 1-3-алкила, q может принимать значения 2 или 3; либо Ar-L2-B совместно могут быть выбраны из группы, состоящей изAr2 означает ароматическую группу, выбранную из бензила или ацила, происходящего из бензойной, фенилуксусной или бензотиофенкарбоновой кислоты; причем ароматическая часть может быть замещена (вплоть до трех) группами, выбранными независимо из C1-3-алкила, OR9, NR9R10, N(R9)COR10, CN, F, Cl, Br, -CF3, -SCF3, -(CH2)q-NR9R10, где R9 означает группу, выбранную из H, C1-4-алкила, a R10 и R11 независимо выбраны из H и C1-3-алкила, q может принимать значения 2 или 3. Исключенными из настоящего изобретения следует считать продукты, у которых В выбран из -NR5CO- и в то же время L2 выбран из -(СH2)р-СО-. В настоящем изобретении предпочтительными являются следующие значения: для C1-3-алкила группа, выбранная из метила, этила, пропила, изопропила; для С 1-4-алкила - группа, выбранная из метила,этила, пропила, изопропила, бутила, изобутила, трет-бутила; для C1-6-алкила - группа, выбранная из метила, этила, пропила, изопропила, бутила, изобутила, трет-бутила, пентила, гексила; для C1-6-алкилидена- группа, выбранная из метилена, этилена, пропилена, метилэтилена, тетраметилена, метилпропилена,пентаметилена, гексаметилена; для C1-3-ацила - группа, выбранная из формила, ацетила, пропионила. Кроме того, предпочтительными можно считать соли неорганических или органических кислот,выбранных их соляной, бромисто-водородной, фосфорной, серной, азотной, уксусной, трифторуксусной,метансульфоновой, толуолсульфоновой, щавелевой, янтарной, малоновой, адипиновой, бензойной кислот. Ингибиторы HDAC настоящего изобретения могут быть синтезированы согласно реакциям, которые известны в этой области, но могут сильно варьировать, исходя из серии стадий синтеза, необходимых для получения индивидуальных соединений, представленных общей формулой I. Некоторые описательные схемы приведены ниже в качестве неограничивающих примеров. Из таких схем специалисты могут вывести или экстраполировать синтез всех соединений, представленных общей формулой I. В некоторых случаях образование амидных связей также позволяет следовать по разработанным в химии пептидов путям твердофазного синтеза на основе применения смол. Примеры Далее приводятся некоторые репрезентативные примеры настоящего изобретения и способы синтеза. Общие методики Синтез амидов типа 2. Метиловый эфир 4-(1-фенилацетилпиперидин-4-ил)масляной кислоты. Вносили DIPEA (0,11 мл, 0,66 ммоль) и фенилацетилхлорид (0,043 мл, 0,33 ммоль) в суспензию гидрохлорида метилового эфира 4-пиперидиномасляной кислоты (100 мг, 0,33 ммоль) в безводнойCH2Cl2 (10 мл), содержащуюся при 0C в атмосфере N2. Полученную смесь оставляли с перемешиванием на 2 ч при комнатной температуре. По окончании реакции (по данным HPLC) смесь разбавляли CH2Cl2 и добавляли 15 мл 5% NaHCO3. Проводили разделение двух фаз, а затем органическую фазу дополнительно промывали 5% NaHCO3 (3 раза) и насыщенным раствором NaCl. Органическую фазу сушили над Na2SO4 и упаривали растворитель при пониженном давлении, получая требуемый амид с количественным выходом. Синтез гидроксаминовых кислот 3, 5, 7, 9, 11, исходя из соответствующих эфиров (способ А) или карбоновых кислот (способ Б). Способ А. Раствор KOH (210 мг, 3,74 ммоль) в MeOH (2 мл) вносили в раствор гидрохлорида гидроксиламина (190 мг, 2,72 ммоль) в MeOH (2 мл), содержащийся при 0C. Затем раствор перемешивали в течение 15 мин при 0C. Добавляли раствор метилового эфира (0,34 ммоль) в MeOH/THF (4 мл) и образовавшуюся смесь держали 12 ч при комнатной температуре с перемешиванием. По окончании реакции(по данным HPLC) значение рН доводили примерно до 8 добавлением 6N раствора HCl. На этой стадии можно предпринять экстрагирование в органическую фазу, если продукт плохо растворяется в воде, или, в противном случае, очистку методом обратнофазовой хроматографии. Способ Б. N-Гидрокси-4-(1-фенилацетилпиперидин-4-ил)бутирамид. Вносили DIPEA (0,085 мл, 0,48 ммоль) и BSA (0,234 мл, 0,96 ммоль) в раствор гидрохлорида 4 пиперидинмасляной кислоты (100 мл, 0,48 ммоль) в безводном CH2Cl2 (10 мл). Смесь оставляли для протекания реакции на 2 ч при комнатной температуре, а затем добавляли фенилацетилхлорид (0,063 мл,0,48 ммоль). Образовавшуюся смесь перемешивали при комнатной температуре в течение 12 ч. По окончании реакции (по данным HPLC) добавляли 15 мл 5% NaHCO3 и оставляли на 30 мин при сильном перемешивании. Проводили разделение двух фаз и водную фазу подкисляли до рН 2. Водную фазу экстрагировали EtOAc, органические экстракты промывали насыщенным растворомNaCl, сушили над Na2SO4 и упаривали растворитель при пониженном давлении, получая требуемую карбоновую кислоту (130 мг, 95%) с подходящей степенью чистоты. Вносили COCl2 (0,045 мл, 0,54 ммоль) и каталитическое количество DMF в раствор кислоты (130 мг, 0,45 ммоль) в 5 мл безводного CH2Cl2. Через два часа CH2Cl2 выпаривали при пониженном давлении,а неочищенный продукт дважды растворяли в CH2Cl2 и опять упаривали. К образовавшемуся при этом ацилхлориду, растворенному в 5 мл безводного CH2Cl2, медленно добавляли 5 мл водного раствораNH2OH HCl (32 мг, 0,45 ммоль) и NaHCO3 (75 мг, 0,9 ммоль). Смесь оставляли для протекания реакции на 1 ч при сильном перемешивании при комнатной температуре. По окончании реакции (по данным HPLC) проводили разделение двух фаз и органическую фазу промывали насыщенным раствором NaCl, сушили над Na2SO4 и концентрировали при пониженном давлении. Полученный при этом неочищенный продукт очищали методом обратнофазовой хроматографии,получая 82 мг требуемого продукта (60%). Синтез аминов 4. Метиловый эфир 4-(1-фенэтилпиперидин-4-ил)масляной кислоты. Последовательно вносили фенилуксусный альдегид (0,046 мл, 0,40 ммоль) и триацетоксиборогидрид натрия (190 мг, 0,90 ммоль) в раствор гидрохлорида метилового эфира 4-пиперидин-4-илмасляной кислоты (80 мг, 0,36 ммоль) в THF (3 мл). Образовавшуюся смесь перемешивали четыре часа при комнатной температуре. Затем добавляли 10% NaHCO3 (10 мл) и EtOAc (10 мл) и проводили разделение-7 012909 двух фаз. Органическую фазу промывали водой и насыщенным раствором NaCl и сушили над Na2SO4. После фильтрования и удаления растворителей при пониженном давлении получали требуемый продукт с количественным выходом, который можно использовать в таком виде при последующей реакции. Синтез мочевины 6. Метиловый эфир 4-(1-бензилкарбамоилпиперидин-4-ил)масляной кислоты. Раствор гидрохлорида метилового эфира 4-пиперидин-4-илмасляной кислоты (98 мг, 0,443 ммоль),DIPEA (0,091 мл, 0,532 ммоль) и бензилизоцианата (0,051 мл, 0,499 ммоль) в дихлорметане (4 мл) перемешивали 3 ч при комнатной температуре. По окончании реакции (по данным HPLC) добавляли порцию аминометилполистиреновой смолы,чтобы удалить излишек изоцианата, и полученную смесь перемешивали еще 2 ч. Раствор фильтровали и концентрировали при пониженном давлении, получая требуемый продукт (140 мг, 99%), который можно использовать в таком виде при последующей реакции. Синтез сульфонамидов 10. Метиловый эфир 4-(1-бензолсульфонилпиперидин-4-ил)масляной кислоты. Вносили порцию бензолсульфонилхлорида (45 мг, 0,26 ммоль) и порцию DIPEA (70 мг, 0,54 ммоль) в раствор гидрохлорида метилового эфира 4-пиперидин-4-илмасляной кислоты (60 мг, 0,27 ммоль) в безводной CH2Cl2 (2 мл). По окончании реакции (по данным HPLC) смесь разбавляли CH2Cl2 и промывали 5% NaHSO4. 5%NaHCO3 и насыщенным раствором NaCl; органическую фазу сушили над Na2SO4 и упаривали. Полученный при этом неочищенный продукт очищали методом хроматографии (силикагель, петролейный эфир/AcOEt = 8:2). Получали 75 мг (90%) требуемого продукта с подходящей степенью чистоты. Пример синтеза гидроксаминовых кислот типа 3, 7, 9,11 на твердой фазе. 4-[1-(2-(R)-Амино-3-фенилпропионил)пиперидин-4-ил]-N-гидроксибутирамид 200 мг коммерческой смолы N-Fmoc-гидроксиламин-2-хлортритилполистирена (конц. 0,5 ммоль/г) оставляли для набухания на 1 ч в 2 мл дихлорметана (DCM). Смолу отфильтровывали и суспендировали в 2 мл 20% раствора пиперидина в дихлорметане. Через 30 мин смолу отфильтровывали и ресуспендировали в 2 мл раствора,содержащего 20% пиперидина в DMF. Через 30 мин смолу отфильтровывали и промывали DCM (42 мл). После этого смолу снова оставляли для набухания в DCM на 20 мин. Раствор HOAt (68 мг, 0,50 ммоль) в 1,5 мл безводного DMF вносили в раствор 4-[N-(флуорен-9 илметоксикарбонил)пиперидин-4-ил]-бутановой кислоты (200 мг, 0,50 ммоль) в 1,5 мл DCM. Медленно добавляли 0,08 мл диизопропилкарбодиимида (63 мг, 0,50 ммоль) и смесь держали 1 ч с перемешиванием при комнатной температуре. Раствор выливали на полистиреновую смолу и перемешивали суспензию 18 ч при комнатной температуре. Смолу отфильтровывали и суспендировали в 2 мл 20% раствора пиперидина в дихлорметане. Через 30 мин смолу отфильтровывали и промывали последовательно DMF (22 мл) и DCM (22 мл). После этого смолу снова оставляли для набухания в DCM на 20 мин. Качественная проба с нингидрином на завершение реакции ацилирования (Kaiser et al., Anal. Biochem. 1970, 34, 595) была отрицательной. Раствор HOAt (68 мг, 0,05 ммоль) в 1,5 мл безводного DMF вносили в раствор Fmoc-D-Phe-OH (194 мг, 0,50 ммоль) в 1,5 мл DCM. Медленно добавляли диизопропилкарбодиимид (0,08 мл, 63 мг, 0,50 ммоль) и смесь держали 1 ч при комнатной температуре с перемешиванием. Раствор выливали на полистиреновую смолу и перемешивали суспензию 18 ч при комнатной температуре. Смолу отфильтровывали и суспендировали в 2 мл 20% раствора пиперидина в дихлорметане. Через 30 мин смолу отфильтровывали и промывали последовательно DMF (22 мл) и DCM (22 мл). К полученной при этом смоле,оставленной для набухания в 2 мл DCM на 20 мин, добавляли 100 мкл трифторуксусной кислоты и 100 мкл триэтилсилана. Все это держали 15 мин с перемешиванием при комнатной температуре. Смолу отфильтровывали и дважды поочередно промывали DCM и MeOH. Фильтраты объединяли и упаривали досуха. После растирания полученного неочищенного продукта с этиловым эфиром получали требуемый продукт (35 мг, выход 80%) с чистотой 95%. Мол. формула: C18H27N3O3, мол. вес: 333,43. 4-[1-(2-(R)-Ацетиламино-3-фенилпропионил)пиперидин-4-ил]-N-гидроксибутирамид. Добавляли 0,048 мл (51 мг, 0,50 ммоль) Ac2O и 0,085 мл DIPEA (65 мг, 0,50 ммоль) к полученной на стадии F смоле, оставленной для набухания в 2 мл DCM на 20 мин. Смолу перемешивали 18 ч при комнатной температуре, а затем отфильтровывали и промывали последовательно DMF (22 мл) и DCM (22 мл). К полученной при этом смоле, оставленной для набухания в 2 мл DCM на 20 мин, добавляли 100 мкл трифторуксусной кислоты и 100 мкл триэтилсилана. Все это держали 15 мин с перемешиванием при комнатной температуре. Смолу отфильтровывали и дважды поочередно промывали DCM и MeOH. Фильтраты объединяли и упаривали досуха. После растирания полученного неочищенного продукта с этиловым эфиром получали требуемый продукт (28 мг, выход 75%) с чистотой 95%. Мол. формула:C20H29N3O4, мол. вес: 375,47. 2-[(Бензо[b]тиофен-2-карбонил)-(R)-амино]-3-[4-(3-гидроксикарбамоилпропил)-пиперидин-1-ил]-3 оксопропиловый эфир бензо[b]тиофен-2-карбоновой кислоты. Смесь из HOAt (20 мг, 0,16 ммоль), Fmoc-D-Ser-OH (49 мг, 0,15 ммоль) и диизо-8 012909 пропилкарбодиимида (0,024 мл, 18 мг, 0,15 ммоль) в 3 мл DMF/DCM, предварительно выдержанную при комнатной температуре в течение часа, добавляли к полученной на стадии С смоле, оставленной для набухания в 2 мл DCM на 20 мин. Суспензию перемешивали 18 ч при комнатной температуре, а затем отфильтровывали и промывали последовательно DMF (22 мл) и DCM (22 мл). Смолу отфильтровывали и суспендировали в 2 мл 20% раствора пиперидина в дихлорметане. Через 30 мин смолу отфильтровывали и промывали последовательно DMF (22 мл) и DCM (22 мл). К полученной на стадии E смоле, оставленной для набухания в 2 мл DCM на 20 мин, добавляли смесь из HOAt (68 мг, 0,5 ммоль), бензо[b]тиофен-2-карбоновой кислоты (90 мг, 0,5 ммоль) и 0,08 мл диизопропилкарбодиимида (63 мг, 0,5 ммоль) в 3 мл DMF/DCM, предварительно выдержанную при комнатной температуре в течение часа. Суспензию перемешивали 18 часов при комнатной температуре. Смолу отфильтровывали и промывали последовательно DMF (22 мл) и DCM (22 мл). К полученной при этом смоле, оставленной для набухания в 2 мл DCM на 20 мин, добавляли 100 мкл трифторуксусной кислоты и 100 мкл триэтилсилана. Все это держали 15 мин с перемешиванием при комнатной температуре. Смолу отфильтровывали и дважды поочередно промывали DCM и MeOH. Фильтраты объединяли и упаривали досуха. После растирания полученного неочищенного продукта с этиловым эфиром получали требуемый продукт (41 мг, выход 75%) с чистотой 95%. Мол. формула:C30H31N3O6S2, мол. вес: 593,73. В настоящее изобретение также входят соответствующие пролекарственные формы общей формулы III и IV, для получения которых вообще предпочтительно получение подходящих синтонов, у которых функциональная группа гидроксамовой кислоты блокирована гидролизуемой группой пролекарственной формы. Такие синтоны затем используются для синтеза требуемых соединений такими способами, которые полностью аналогичны способам, используемым для соединений, не подходящих под определение пролекарственных форм. Далее следуют неограничивающие примеры синтеза синтонов для пролекарственных форм. Синтез пролекарственной формы А. Бензиламид 4-(3-ацетоксикарбамоилпропил)пиперидин-1 карбоновой кислоты. Вносили пиридин (0,019 мл, 0,23 ммоль, 1,5 экв.) и уксусный альдегид (0,022 мл, 0,23 ммоль, 1,5 экв.) в раствор бензиламида 4-(3-гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты (50 мг,0,16 ммоль, 1,0 экв.) в безводном DCM и полученную смесь оставляли для протекания реакции при комнатной температуре на 12 ч. По окончании реакции, после разбавления DCM и промывки 1 N HCl (5 мл), проводили разделение фаз. Органическую фазу промывали насыщенным раствором NaCl, сушили над Na2SO4 и концентрировали при пониженном давлении. Полученный при этом неочищенный продукт очищали методом флэшхроматографии (30% петролейного эфира в AcOEt, затем AcOEt), получая 45 мг требуемого моноацетилированного продукта в виде белого вещества (80%). 1 Н-ЯМР (DMSO-d6, 400 МГц):(ppm) 0,90-1,03 (2 Н, m), 1,16-1,29 (2 Н, m), 1,32-1,48 (1H, m), 1,481,67 (4 Н, m), 2,11 (2 Н, t, J = 6,8 Гц, CH2CO), 2,15 (3 Н, s, OCH3), 2,65 (2 Н, m, N(CHH)2), 3,98 (2 Н, m,N(CHH)2), 4,24 (2 Н, d, J = 5,2 Гц, PhCH2), 6,97 (1H, m, NCONH), 7,16-7,36 (5H, m, ArH), 11,53 (1H, s,NHO). Мол. формула: C19H27N3O4, мол. вес: 361,43. Синтез пролекарственной формы В. Бензиламид [3-(5,5-диметил-[1,4,2]диоксазол-3-ил)пропил]пиперидин-1-карбоновой кислоты. Вносили камфорсульфоновую кислоту (37 мг, 0,16 ммоль, 1,0 экв.) в раствор бензиламида 4-(3 гидроксикарбамоилпропил)пиперидин-1-карбоновой кислоты (50 мг, 0,16 ммоль, 1,0 экв.) и 2,2-диэтоксипропана (0,076 мл, 0,47 ммоль, 3,0 экв.) в безводном DCM (3 мл) и полученную смесь оставляли с перемешиванием при комнатной температуре на 4 ч. По окончании реакции добавляли насыщенный водный раствор Na2CO3 (5 мл) и проводили разделение фаз. Водную фазу промывали Et2O (45 мл). Наконец, объединенную органическую фазу сушили над Na2SO4 и концентрировали при пониженном давлении. Неочищенный продукт очищали методом флэш-хроматографии (30% петролейного эфира вAcOEt), получая 45 мг требуемого продукта (80%). 1 Н-ЯМР (DMSO-d6, 400 МГц):(ppm) 0,87-0,96 (2 Н, m), 1,17-1,30 (2 Н, m), 1,30-1,45 (1H, m), 1,461,68 (4 Н, m), 1,49 (6 Н, s, 2 СН 3), 2,28 (2 Н, t, J = 7,2 Гц, CH2CO), 2,63 (2 Н, m, N(CHH)2), 3,96 (2 Н, m,N(CHH)2), 4,22 (2 Н, d, J = 5,2 Гц, PhCH2), 7,01 (1H, m, NCONH), 7,16-7,33 (5 Н, m, ArH). Мол. формула:C20H29N3O3, мол. вес: 359,46. Синтез пролекарственной формы С. Бензиламид 4-[3-(тетрагидропиран-2-илоксикарбамоил)пропил]пиперидин-1-карбоновой кислоты. Вносили EDAC (69 мг, 0,36 ммоль, 1,0 экв.) и HOBt (49 мг, 0,36 ммоль, 1,0 экв.) в раствор бензиламида 4-(1-бензилкарбамоилпиперидин-4-ил)масляной кислоты (100 мг, 0,328 ммоль, 1,0 экв.) в безводном DMF (5 мл) и полученную смесь оставляли с перемешиванием при комнатной температуре на 1 ч. Затем добавляли O-(тетрагидро-2 Н-пиран-2-ил)гидроксиламин (13 мг, 0,33 ммоль, 1,0 экв.) и DIPEA(0,042 мл, 0,49 ммоль, 1,5 экв.) и полученную смесь оставляли с перемешиванием при комнатной температуре на 12 ч.-9 012909 По окончании реакции (по данным HPLC) добавляли раствор 5% раствор NaHCO3 (5 мл) и проводили разделение фаз. Органическую фазу промывали насыщенным раствором NaCl, сушили над Na2SO4 и концентрировали при пониженном давлении. Полученный при этом неочищенный продукт очищали методом флэш-хроматографии (AcOEt), получая 92 мг требуемого продукта (70%). 1(1H, m), 1,44-1,74 (10 Н, m), 1,96 (2 Н, t, J = 7,2 Гц, CH2CO), 2,62 (2 Н, m, N(CHH)2), 3,49 (1H, m, OCHH),3,84-4,05 (3 Н, m, N(CHH)2 и OCHH), 4,21 (2 Н, d, J = 5,6 Гц, PhCF2), 4,79 (1H, s, OCHO), 7,00 (1H, m,NCONH), 7,16-7,33 (5 Н, m, ArH), 10,91 (1H, s, NHO). Мол. формула: C22H33N3O4, мол. вес: 403,51. Далее приводятся неограничивающие примеры, представляющие осуществление настоящего изобретения в соответствии с вышеописанными схемами синтеза и их вариантами. Пример 1. 4-[1-(2-Хлорбензолсульфонил)пиперидин-4-ил]-N-гидроксибутирамид. 1H-ЯMP (DMSO-d6, 400 МГц):(ppm) 1,15-1,28 (4 Н, m), 1,49-1,58 (3 Н, m), 1,81 (2H, d, J = 12,3 Гц),3,26 (2 Н, t, J = 12,3 Гц, N(CH2)2), 4,01 (2 Н, d, J = 12,1 Гц, N(CH2)2), 7,22-7,38 (4 Н, m, ArH), 8,69 (1H, bs,ОН), 10,34 (1H, bs, NHOH), 12,90 (1H, brs, H бензимидазола). Мол. формула: C16H22N4O2, мол. вес: 302,37. Показания для терапии Ингибиторы гистондеацетилазы представляют собой класс потенциальных средств для терапии или профилактики патологических состояний, вызванных нарушением экспрессии генов, как-то воспалительных заболеваний, диабета, осложнений диабета, гомозиготной талассемии, фиброза, цирроза, острой промиелоцитарной лейкемии (APL), отторжения трансплантатов, аутоиммунных заболеваний, протозойных инфекций, опухолей и др. В частности, они возникают как новый класс лекарств с противоопухолевым действием. Описана связь между некоторыми опухолевыми патологиями, такими как рак молочной железы, толстой кишки и легких, и степенью ацетилирования хроматина в ядре. Препараты, способные модулировать перестройку хроматина, способны ингибировать пролиферацию опухолей и могли бы стать новыми инструменами для лечения раковых патологий в не столь отдаленном будущем. Многие экспериментальные данные ведут к предположению о том, что главной областью применения этого класса препаратов могла бы стать комбинированная терапия. Значительная переносимость, как следует из первых клинических испытаний, вызывает уверенность в том, что этот класс молекул подходит для комбинированной терапии вместе с традиционными лекарствами типа цитотоксических препаратов или вместе с радиотерапевтическим лечением или с противораковыми средствами нового поколения. В частности, настоящим изобретением также предусмотрено комбинирование обладающих активностью ингибиторов гистондеацетилазы соединений общей формулы I с одним или несколькими химиотерапевтическими соединениями из числа обычных цитотоксических средств, деметилирующих средств, ингибиторов циклинзависимых киназ,веществ, способствующих дифференцировке, модуляторов передачи сигналов, антагонистов HSP-90,ингибиторов протеасом. Предпочтительными соединениями являются соединения, выбранные из следующих групп: из обычных цитотоксических средств: флударабин, гемцитабин, децитабин, паклитаксель, карбоплатин и ингибиторы топоизомеразы I/II, в том числе этопозид, иринотекан, топотекан, Т-128, и такие антрациклины, как доксорубицин, сабарубицин, даунорубицин; из деметилирующих средств (вызывающих деметилирование ДНК): 5-аза-2'-дезоксицитидин (5-aзa- 29012909dC), 5-азацитидин; из ингибиторов циклинзависимых киназ: флавопиридол, оломоуцин, росковитин, пурваланол В,GW9499, GW5181, CGP60474, CGP74514, AG12286, AG12275, стауроспорин, UCN-01; из веществ, способствующих дифференцировке: ретиноевая кислота и е производные (полностью транс-ретиноевая кислота (ATRA), 13-цис-ретиноевая кислота (CRA, PMA (форболмиристатацетат); из модуляторов передачи сигналов: TRAIL, иматинибмезилат, LY-294002, бортезомиб; из антагонистов HSP-90: гелданамицин и его аналоги (17-AAG); из ингибиторов протеасом: лактацистин, MG132, бортезомиб (Velcade). Биологическая активность Активность соединений в качестве ингибиторов гистондеацетилаз (HDAC) измеряли методом ацетилирования in vitro. Затем соединения оценивали в качестве ингибиторов пролиферации раковых культур клеток человека. Сводка полученных данных представлена в таблице. Деацетилазная активность в экстрактах ядер клеток HeLa (раковых клеток шейки матки человека) Определение (набор Fluor de Lys, BioMol) состояло из двух стадий: на первой стадии субстрат,содержащий ацетилированный остаток лизина, реагировал с ядерным экстрактом (HeLa), содержащим энзиматическую активность, в присутствии и в отсутствие ингибиторов. На второй стадии добавляли флуорогенный реагент, который окрашивает деацетилированные остатки. При ингибировании деацетилазной активности происходит снижение флуоресценции. Результат выражали в процентах ингибирования относительно контроля, не содержащего ингибитора в концентрации 0,1 мкМ. Оценка цитотоксической активности на культуре клеток карциномы толстой кишки человека HCT-116 Клетки карциномы толстой кишки человека HCT-116 высевали на 96-луночные планшеты в культуральной среде RPMI1640 с добавлением 10% FBS и 2 мМ глутамина. Через 24 часа после посева добавляли соединения в различных концентрациях. Все соединения разводили DMSO таким образом, чтобы конечная концентрация в культурах не превышала 0,5%. Через 72 часа после добавления соединений измеряли жизнеспособность клеток при помощи красителя Alamar Blue. Результаты выражали в процентах жизнеспособных клеток среди обработанных относительно контроля, получавшего только носитель. Таблица. Биологическая активность новых соединений по ингибированию ацетилирования гистонов и по антипролиферативному действию на линию клеток карциномы толстой кишки человека HCT-116
МПК / Метки
МПК: A61K 31/4535, C07D 409/14, C07D 417/06, A61K 31/445, C07D 211/34, C07D 401/06, C07D 405/06, C07D 211/96, C07D 409/06, C07D 413/06, A61K 31/4525
Метки: фармацевтические, ингибиторы, содержащие, композиции, гидроксаматы, гистондеацетилазы
Код ссылки
<a href="https://eas.patents.su/30-12909-gidroksamaty-kak-ingibitory-gistondeacetilazy-i-soderzhashhie-ih-farmacevticheskie-kompozicii.html" rel="bookmark" title="База патентов Евразийского Союза">Гидроксаматы как ингибиторы гистондеацетилазы и содержащие их фармацевтические композиции</a>
Предыдущий патент: Применение фенилацетильных производных для производства лекарственных средств для лечения болезни фон хиппеля-линдау (vhl)
Следующий патент: Способ получения анилинов
Случайный патент: Сульфонамидные производные бензиламина для лечения заболеваний цнс