Пиримидины и триазины, ингибирующие вич репликацию
Номер патента: 11256
Опубликовано: 27.02.2009
Авторы: Гийемон Жером Эмиль Жорж, Беттенс Эва, Жанссен Поль Адриан Ян, Паскье Элизабет Тереза Жанна, Леви Паулус Йоаннес, Хэрес Ян, Винкерс Хендрик Мартен, Де Жонж Марк Рене, Койманс Люсьен Мария Хенрикус, Хертогс Курт, Дайер Фредерик Франс Дезире
Формула / Реферат
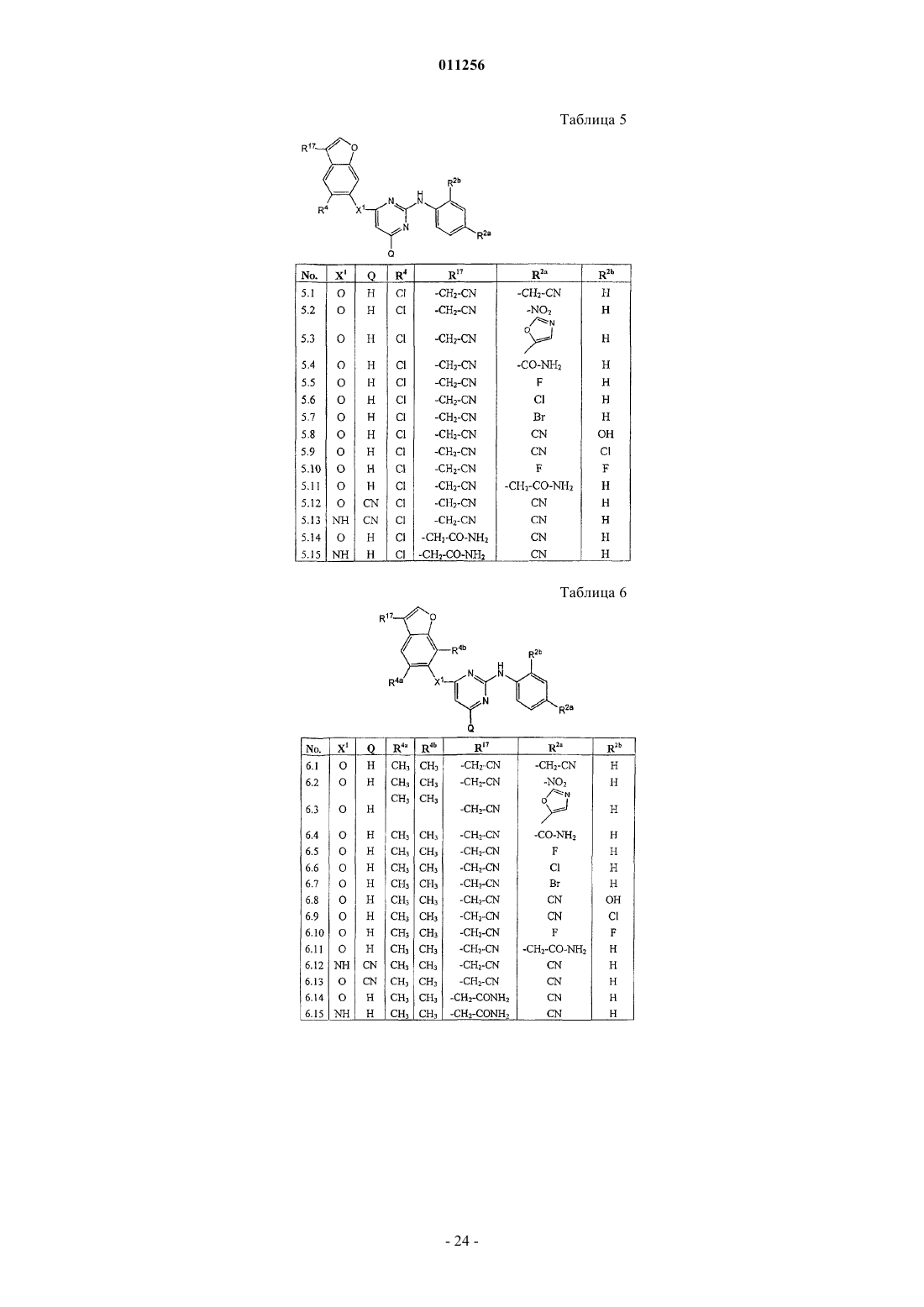
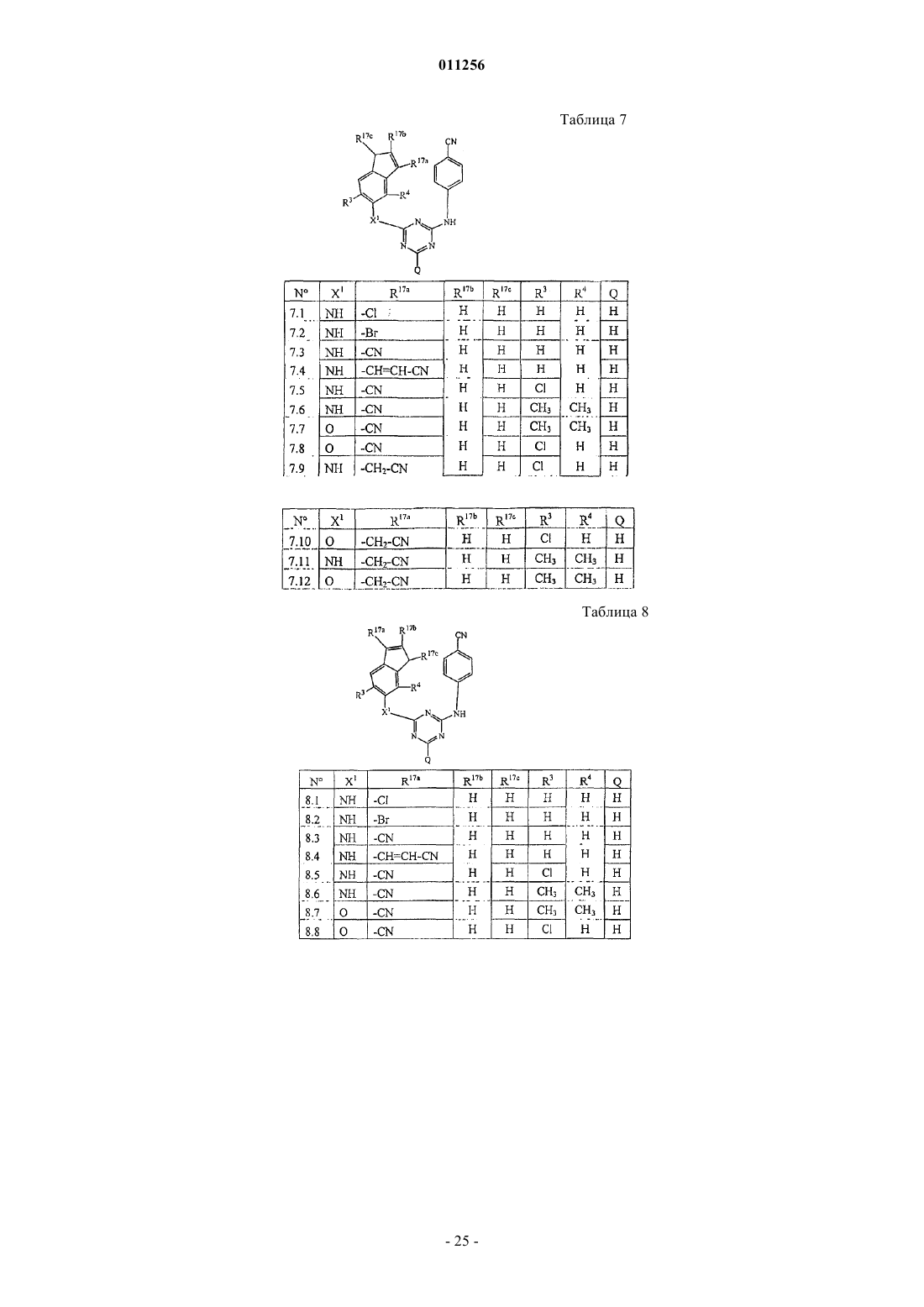
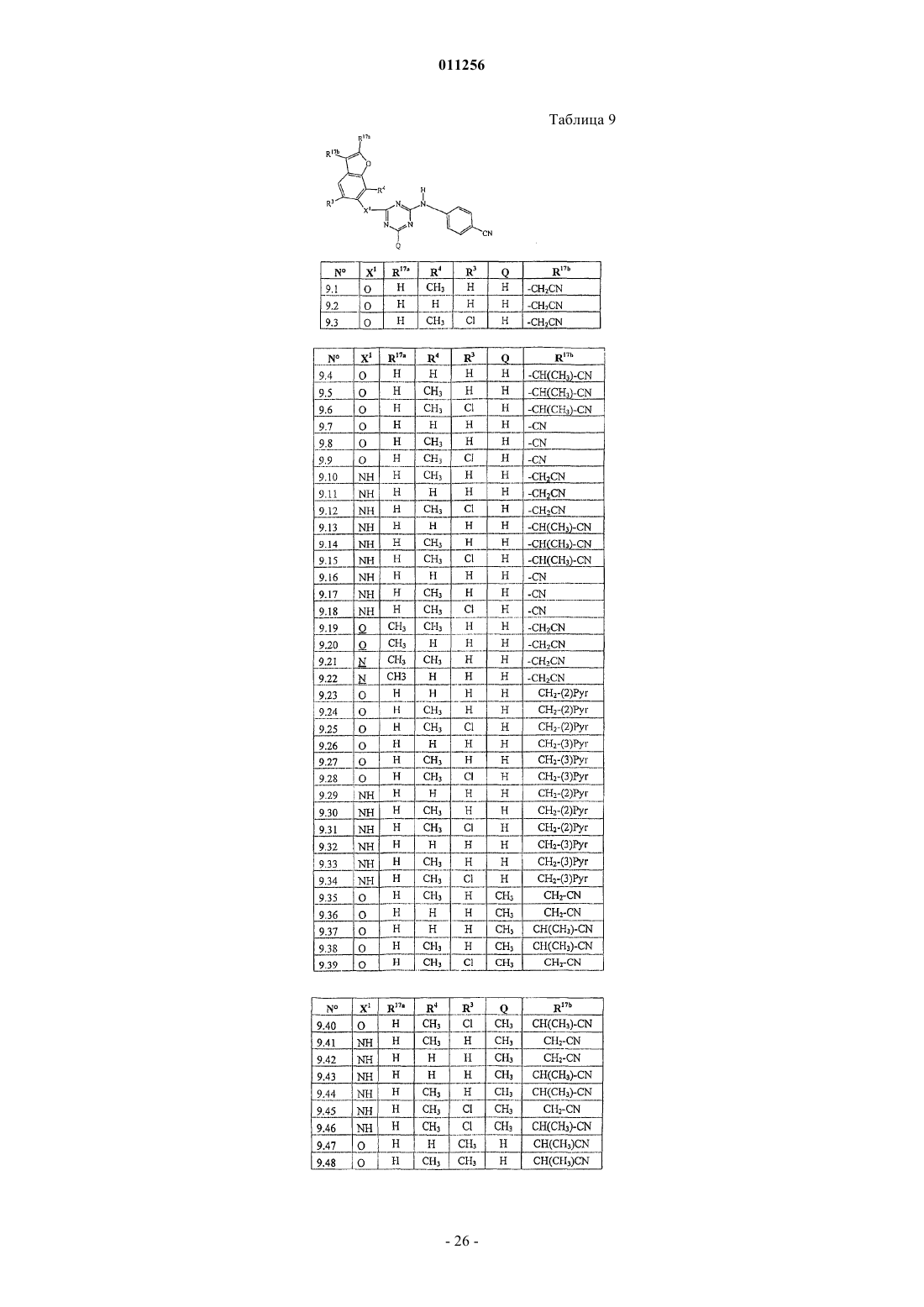
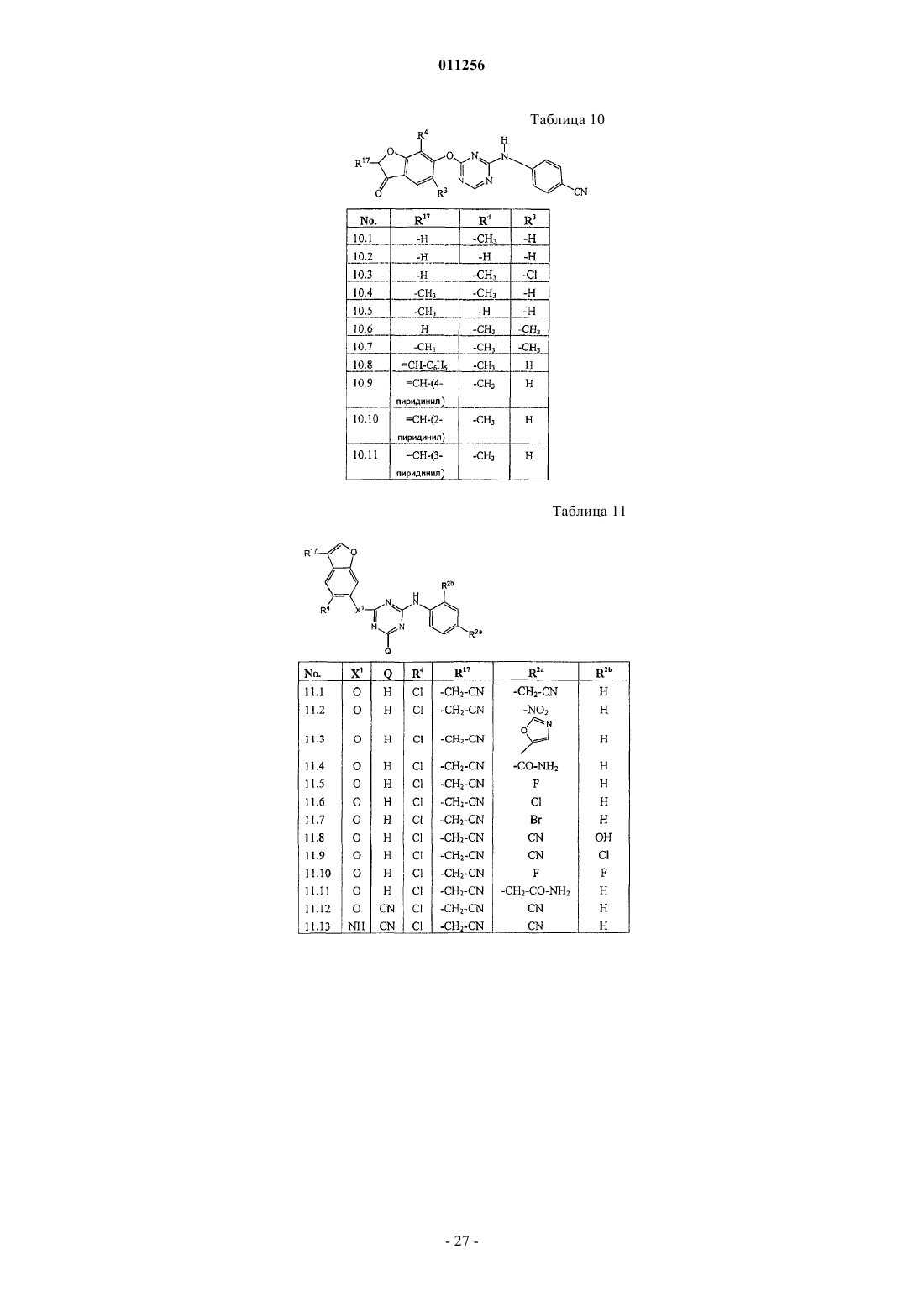
1. Соединение формулы (I)

его фармацевтически приемлемая аддитивная соль или стереохимически изомерная форма,
где -а1=а2-а3=а4- представляет собой двухвалентный радикал формулы
![]()
-b1-b2-b3- представляет собой двухвалентный радикал формулы

n равно 1;
m равно 0, 1;
q равно 1 или 2;
R1 представляет собой водород;
R2 представляет собой циано и
X1 представляет собой -NH-, -О-;
R3 представляет собой водород, галоген, C1-6алкил;
R4 представляет собой галоген, C1-6алкил;
R13 и R14, каждый независимо, представляет собой водород, C1-6алкил;
R17 представляет собой циано, галоген, -С(=O)-NR13R14, C1-6алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из циано, -С(=O)-NR13R14 или галогена; С2-6алкенил, необязательно замещенный циано, -С(=O)-NR13R14; и, когда это возможно, R17 может быть присоединенным к фрагменту -b1-b2-b3- двойной связью, в результате чего R17 тогда представляет собой =O;
Q представляет собой водород;
Z представляет собой C-Y,
где Y представляет собой водород, галоген.
2. Соединение по п.1, где n равно 1; m равно 0 или 1; q равно 1.
3. Соединение по п.1, где R13 и R14 представляют собой водород.
4. Соединение по п.1, где Y представляет собой водород.
5. Соединение по п.1, где R17 представляет собой циано, C1-6алкил, необязательно замещенный циано, С2-6алкенил, необязательно замещенный циано; или R17 представляет собой =O.
6. Соединение по п.1, где -b1-b2-b3- представляет собой двухвалентный радикал формулы

n равно 1;
m равно 0;
q равно 1;
R2 представляет собой циано;
Y представляет собой водород;
R17 представляет собой =O.
7. Соединение по п.1, где-b1-b2-b3- представляет собой двухвалентный радикал формулы

n равно 1;
m равно 0;
q равно 1;
R2 представляет собой циано;
Y представляет собой водород;
R17 представляет собой C1-6алкил, замещенный циано.
8. Соединение по п.7, где -b1-b2-b3- представляет собой двухвалентный радикал формулы

n равно 1;
m равно 0;
q равно 1;
R2 представляет собой циано;
R3 представляет собой галоген;
Y представляет собой водород;
R17 представляет собой C1-6алкил, замещенный циано.
9. Фармацевтическая композиция, включающая (а) эффективное количество соединения формулы (I) по п.1 и (b) фармацевтически приемлемый носитель.
10. Фармацевтическая композиция, включающая (а) соединение формулы (I) по п.1 и (b) другое противоретровирусное соединение в качестве комбинированного препарата.
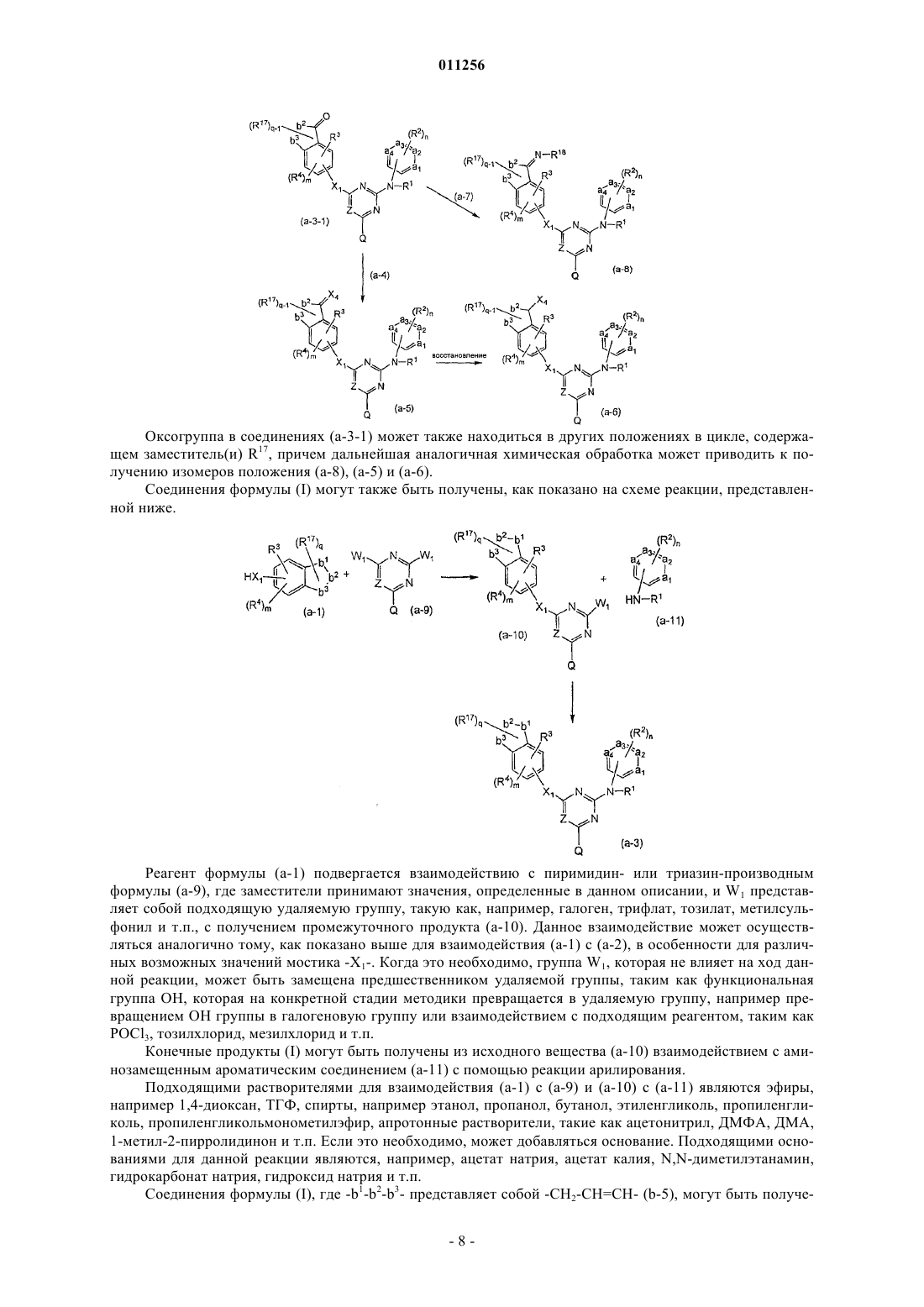
11. Способ получения соединения формулы (I) по п.1, отличающийся тем, что проводят взаимодействие промежуточного соединения формулы (а-1) с пиридиновым производным (а-2)
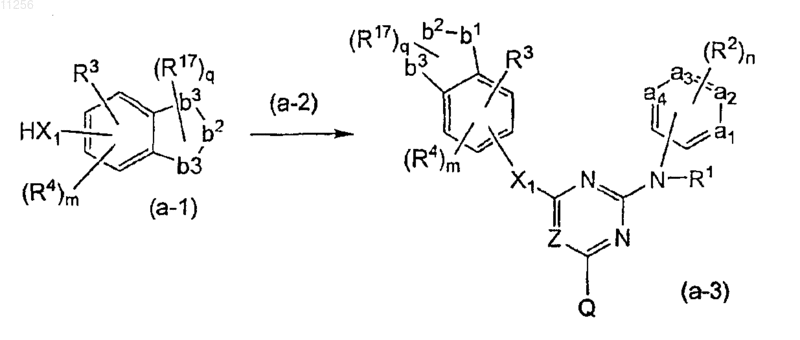
и где реагент (а-2) соответствует общей формуле
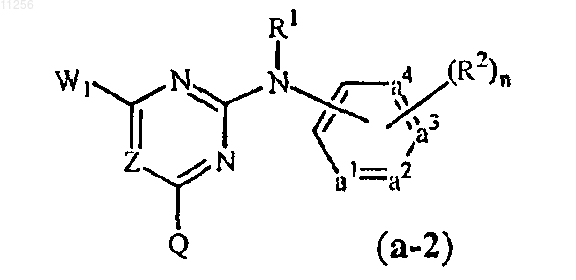
и W1 представляет собой подходящую удаляемую группу и X1 представляет собой -NR5-, -О-, где заместитель R5 представляет собой водород.
Текст
011256 Данное изобретение относится к производным пиримидина и триазина, обладающими способностью ингибировать репликацию вируса иммунодефицита человека (ВИЧ). Изобретение относится также к способам получения и фармацевтическим композициям, включающим данные соединения. Изобретение относится также к применению упомянутых производных для производства лекарственного средства для профилактики или лечения ВИЧ инфекции. В частности, целью данного изобретения является представление новой группы производных пиридина, обладающих активностью в отношении ВИЧ репликации. В публикациях WO 99/50250, WO 00/27825 и WO 01/85700 описываются некоторые замещенные аминопиридины, в публикациях WO 99/50256 и EP 834507 описываются аминотриазины, обладающие свойствами ингибирования ВИЧ репликации. Соединения данного изобретения отличаются от соединений предшествующего уровня по структуре, фармакологической активности и/или фармакологической эффективности. Было установлено, что соединения данного изобретения оказывают полезное действие не только с точки зрения их способности ингибировать репликацию вируса иммунодефицита человека (ВИЧ), но и ввиду их повышенной способности ингибировать репликацию мутантных штаммов, в частности штаммов, которые стали резистентными к коммерчески доступным лекарственным средствам (т.е. так называемых штаммов ВИЧ, стойких к лекарственному средству или множеству лекарственных средств). Таким образом, в соответствии с одним аспектом данное изобретение относится к соединению формулы (I) его фармацевтически приемлемой аддитивной соли или его стереохимически изомерной форме, где-а 1;=а 2-а 3=а 4- представляет собой двухвалентный радикал формулы-b1-b2-b3- представляет собой двухвалентный радикал формулыR17 представляет собой циано, галоген, -С(=O)-NR13R14, C1-6 алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из циано, -С(=O)-NR13R14 или галогена; С 2-6 алкенил, необязательно замещенный циано, -С(=O)-NR13R14; и, когда это возможно, R17 может быть присоединенным к фрагменту -b1-b2-b3- двойной связью, в результате чего R17 тогда представляет собойZ представляет собой C-Y,где Y представляет собой водород или галоген. Термин С 1-4 алкил, используемый в данном описании выше или далее при обозначении группы или части группы, относится к насыщенным углеводородным радикалам с прямой или разветвленной цепью, содержащим от 1 до 4 атомов углерода, таким как метил, этил, пропил, 1-метилэтил, бутил; термин C1-6 алкил при обозначении группы или части группы относится к насыщенным углеводородным радикалам с прямой или разветвленной цепью, содержащим от 1 до 6 атомов углерода, таким как группы, определяемые термином С 1-4 алкил, а также пентил, гексил, 2-метилбутил и т.п.; термин С 2-6 алкил при обозначении группы или части группы относится к насыщенным углеводородным радикалам,содержащим от 2 до 6 атомов углерода, таким как этил, пропил, 1-метилэтил, бутил, пентил, гексил, 2 метилбутил и т.п.; термин С 1-4 алкандиил относится к двухвалентным насыщенным углеводородным радикалам с прямой или разветвленной цепью, содержащим от 1 до 4 атомов углерода, таким как метилен, 1,2-этандиил или 1,2-этилиден, 1,3-пропандиил или 1,3-пропилиден, 1,4-бутандиил или 1,4-1 011256 бутилиден и т.п.; термин С 3-7 циклоалкил относится к циклопропилу, циклобутилу, циклопентилу, циклогексилу и циклогептилу; термин С 2-6 алкенил относится к углеводородным радикалам с прямой или разветвленной цепью, включающим от 2 до 6 атомов углерода и содержащим двойную связь, таким как этенил, пропенил, бутенил, пентенил, гексенил и т.п.; термин С 2-6 алкинил относится к углеводородным радикалам с прямой или разветвленной цепью, включающим от 2 до 6 атомов углерода и содержащим тройную свуязь, таким как этинил, пропинил, бутинил, пентинил, гексинил и т.п. В ряде примеров радикалы C1-6 алкинил, С 2-6 алкенил или С 2-6 алкинил могут быть замещенными одним или несколькими заместителями. В том случае, когда возможно присутствие 1, 2, 3, 4, 5, 6 и более заместителей, их количество ограничивается количеством атомов углерода и степенью ненасыщенности углеводородного радикала. Радикалы C1-6 алкинил, С 2-6 алкенил или С 2-6 алкинил предпочтительно являются замещенными и содержат до 3 заместителей. Моноциклический, бициклический или трициклический насыщенный карбоцикл представляет собой циклическую систему, содержащую 1, 2 или 3 цикла, причем указанная циклическая система состоит только из атомов углерода и содержит только одинарные связи; моноциклический, бициклический или трициклический частично насыщенный карбоцикл представляет собой циклическую систему, образованную 1, 2 или 3 циклами, причем указанная циклическая система состоит только из атомов углерода и включает по меньшей мере одну двойную связь при условии, что циклическая система не является ароматической циклической системой; моноциклический, бициклический или трициклический ароматический карбоцикл представляет собой ароматическую циклическую систему, образованную 1, 2 или 3 циклами, причем указанная циклическая система состоит только из атомов углерода; термин ароматический хорошо известен квалифицированным специалистам данной области техники и относится к циклически сопряженным системам 4n+2 электронов, то есть 6, 10, 14 и т.д. -электронов (правило Хюккеля); моноциклический, бициклический или трициклический насыщенный гетероцикл представляет собой циклическую систему, образованную 1, 2 или 3 циклами и включающую по меньшей мере один гетероатом, выбранный из атомов О, N или S, причем указанная циклическая система содержит только одинарные связи; моноциклический, бициклический или трициклический частично насыщенный гетероцикл представляет собой циклическую систему, образованную 1, 2 или 3 циклами и включающую по меньшей мере один гетероатом, выбранный из атомов О, N или S, и содержащую по меньшей мере одну двойную связь при условии, что циклическая система не является ароматической циклической системой; моноциклический, бициклический или трициклический ароматический гетероцикл представляет собой ароматическую циклическую систему, образованную 1, 2 или 3 циклами и включающую по меньшей мере один гетероатом, выбранный из атомов О, N или S. Конкретными примерами моноциклических, бициклических или трициклических насыщенных карбоциклов являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, бицикло[4,2,0]октанил, циклононанил, циклодеканил, декагидронафталенил, тетрадекагидроантраценил и т.п. Предпочтительными являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил; более предпочтительны циклопентил, циклогексил, циклогептил. Конкретными примерами моноциклических, бициклических или трициклических частично насыщенных карбоциклов являются циклопропенил, циклобутенил, циклопентенил, циклогексенил, циклогептенил, циклооктенил, бицикло[4,2,0]октенил, циклононенил, циклодеценил, октагидронафталенил,1,2,3,4-тетрагидронафталенил, 1,2,3,4,4 а,9,9 а,10-октагидроантраценил и т.п. Предпочтительными являются циклопентенил, циклогексенил, циклогептенил. Конкретными примерами моноциклических, бициклических или трициклических ароматических карбоциклов являются фенил, нафталенил, антраценил. Предпочтителен фенил. Конкретными примерами моноциклических, бициклических или трициклических насыщенных гетероциклов являются тетрагидрофуранил, пирролидинил, диоксоланил, имидазолидинил, тиазолидинил,тетрагидротиенил, дигидрооксазолил, изотиазолидинил, изоксазолидинил, оксадиазолидинил, триазолидинил, тиадиазолидинил, пиразолидинил, пиперидинил, гексагидропиримидинил, гексагидропиразинил,диоксанил, морфолинил, дитианил, тиоморфолинил, пиперазинил, тритианил, декагидрохинолинил, октагидроиндолил и т.п. Предпочтительны тетрагидрофуранил, пирролидинил, диоксоланил, имидазолидинил, тиазолидинил, дигидрооксазолил, триазолидинил, пиперидинил, диоксанил, морфолинил, тиоморфолинил, пиперазинил. Особенно предпочтительны тетрагидрофуранил, пирролидинил, диоксоланил, пиперидинил, диоксанил, морфолинил, тиоморфолинил, пиперазинил. Конкретными примерами моноциклических, бициклических или трициклических частично насыщенных гетероциклов являются пирролинил, имидазолинил, пиразолинил, 2,3-дигидробензофуранил,1,3-бензодиоксолил, 2,3-дигидро-1,4-бензодиоксинил, индолинил и т.п. Предпочтительны пирролинил,имидазолинил, 2,3-дигидробензофуранил, 1,3-бензодиоксолил, индолил. Конкретными примерами моноциклических, бициклических или трициклических ароматических гетероциклов являются азетил, оксетилиденил, пирролил, фурил, тиенил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, триазолил, тиадиазолил, оксадиазолил, тетразолил, пиридил,пиримидинил, пиразинил, пиридазинил, триазинил, пиранил, бензофурил, изобензофурил, бензотиенил,изобензотиенил, индолизинил, индолил, изоиндолил, бензоксазолил, бензимидазолил, индазолил, бензи-2 011256 зоксазолил, бензизотиазолил, бензопиразолил, бензоксадиазолил, бензотиадиазолил, бензотриазолил,пуринил, хинолинил, изохинолинил, циннолинил, хинолизинил, фталазинил, хиноксалинил, хиназолинил, нафтиридинил, птеридинил, бензопиранил, пирролопиридил, тиенопиридил, фуропиридил, изотиазолопиридил, тиазолопиридил, изоксазолопиридил, оксазолопиридил, пиразолопиридил, имидазопиридил, пирролопиразинил, тиенопиразинил, фуропиразинил, изотиазолопиразинил, тиазолопиразинил, изоксазолопиразинил, оксазолопиразинил, пиразолопиразинил, имидазопиразинил, пирролопиримидинил,тиенопиримидинил, фуропиримидинил, изотиазолопиримидинил, тиазолопиримидинил, изоксазолопиримидинил, оксазолопиримидинил, пиразолопиримидинил, имидазопиримидинил, пирролопиридазинил,тиенопиридазинил, фуропиридазинил, изотиазолопиридазинил, тиазолопиридазинил, изоксазолопиридазинил, оксазолопиридазинил, пиразолопиридазинил, имидазопиридазинил, оксадиазолопиридил, тиадиазолопиридил, триазолопиридил, оксадиазолопиразинил, тиадиазолопиразинил, триазолопиразинил, оксадиазолопиримидинил, тиадиазолопиримидинил, триазолопиримидинил, оксадиазолопиридазинил, тиадиазолопиридазинил, триазолопиридазинил, имидазооксазолил, имидазотиазолил, имидазоимидазолил,изоксазолотриазинил, изотиазолотриазинил, пиразолотриазинил, оксазолотриазинил, тиазолотриазинил,имидазотриазинил, оксадиазолотриазинил, тиадиазолотриазинил, триазолотриазинил, карбазолил, акридинил, феназинил, фенотиазинил, феноксазинил и т.п. Предпочтительными ароматическими гетероциклами являются моноциклические или бициклические ароматические гетероциклы. Представляющими интерес моноциклическими, бициклическими или трициклическими ароматическими гетероциклами являются пирролил, фурил, тиенил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, триазолил, тиадиазолил, оксадиазолил, тетразолил, пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, пиранил, бензофурил, изобензофурил,бензотиенил, изобензотиенил, индолил, изоиндолил, бензоксазолил, бензимидазолил, индазолил, бензизоксазолил, бензизотиазолил, бензопиразолил, бензоксадиазолил, бензотиадиазолил, бензотриазолил,пуринил, хинолинил, изохинолинил, фталазинил, хиноксалинил, хиназолинил, бензопиранил, пирролопиридил, тиенопиридил, фуропиридил, изотиазолопиридил, тиазолопиридил, изоксазолопиридил, оксазолопиридил, пиразолопиридил, имидазопиридил, пирролопиразинил, тиенопиразинил, фуропиразинил,изотиазолопиразинил, тиазолопиразинил, изоксазолопиразинил, оксазолопиразинил, пиразолопиразинил,имидазопиразинил, пирролопиримидил, тиенопиримидинил, фуропиримидинил, изотиазолопиримидинил, тиазолопиримидинил, изоксазолопиримидинил, оксазолопиримидинил, пиразолопиримидинил, имидазопиримидинил, оксадиазолопиридил, тиадиазолопиридил, триазолопиридил, оксадиазолопиразинил,тиадиазолопиразинил, триазолопиразинил, оксодиазолопиримидинил, тиодиазолопиримидинил, триазолопиридинил, карбазолил, акридинил, фенотиазинил, феноксазинил и т.п. Ароматическими гетероциклами, представляющими особый интерес, являются пирролил, фурил,тиенил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, триазолил, тиадиазолил,оксадидазолил, тетразолил, пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, пиранил, бензофурил, изобензофурил, бензотиенил, изобензотиенил, индолил, изоиндолил, бензоксазолил, бензимидазолил, индазолил, бензизоксазолил, бензизотиазолил, бензопиразолил, бензоксадиазолил, бензотиадиазолил, бензотриазолил, пуринил, хинолинил, изохинолинил, фталазинил, хиноксалинил, хиназолинил и т.п. Упомянутая выше группа (=O) образует карбонильный фрагмент, когда присоединена к атому углерода, сульфоксидный фрагмент, когда присоединена к атому серы, и сульфонильный фрагмент, когда две указанные группы присоединены к атому серы. Термин галоген относится к фтору, хлору, брому и йоду. Термин полигалогенметил, используемый в данном описании при обозначении группы или части группы, относится к моно- или полигалогензамещенному метилу, в частности метилу с одним или несколькими атомами фтора, например дифторметилу или трифторметилу; термин полигалогенС 1-4 алкил или полигалогенС 1-6 алкил, используемый в данном описании для обозначении группы или части группы, означает моно- или полигалогензамещенный С 1-4 алкил или C1-6 алкил, например группы, перечисленные в определении термина галогенметил, 1,1-дифторэтил и т.п. В том случае когда к алкильной группе в определении полигалогенметила, полигалогенС 1-4 алкила или полигалогенС 1-6 алкила присоединены несколько атомов галогена, они могут быть одинаковыми или разными. Подразумевается, что термин гетероцикл в определении R7 или R7a включает все возможные изомерные формы гетероциклов, например пирролил включает 1 Н-пирролил и 2 Н-пирролил. Карбоцикл или гетероцикл в определении R7 или R7a может быть присоединен к остатку молекулы формулы (I) через любой атом углерода цикла или гетероатом, как это подходит, кроме случаев, оговоренных особо. Таким образом, например, когда гетероциклом является имидазолил, он может представлять собой 1-имидазолил, 2-имидазолил, 4-имидазолил и т.п., или когда карбоциклом является нафталенил, он может представлять собой 1-нафталенил, 2-нафталенил и т.п. Когда любая переменная (например, R7, гетероатом, X2) встречается более одного раза в любом компоненте, каждое определенное значение является независимым. Линии, идущие от заместителей в циклические системы, показывают, что связь может присоединяться к любому из подходящих атомов цикла.-3 011256 Для терапевтического применения соли соединений формулы (I) представляют собой соли, в которых противоион является фармацевтически приемлемым. Однако соли кислот и оснований, которые не являются фармацевтически приемлемыми, также могут находить применение, например, при получении или очистке фармацевтически приемлемого соединения. Все соли, независимо от того являются они фармацевтически приемлемыми или нет, включены в область данного изобретения. Подразумевается, что термин фармацевтически приемлемые кислотно-аддитивные соли, упомянутый выше, включает терапевтически активные нетоксичные кислотно-аддитивные солевые формы,которые могут образовывать соединения формулы (I). Последние могут быть традиционно получены обработкой основной формы подходящими кислотами, такими как неорганические кислоты, например галогенисто-водородными кислотами, в частности хлористо-водородной, бромисто-водородной и т.п.; серной кислотой; азотной кислотой; фосфорной кислотой и т.п.; или органическими кислотами, например уксусной, пропановой, оксиуксусной, 2-оксипропановой, 2-кетопропановой, щавелевой, малоновой,янтарной, малеиновой, фумаровой, яблочной, винной, 2-гидрокси-1,2,3-пропантрикарбоновой, метансульфоновой, этансульфоновой, бензолсульфоновой, 4-метилбензолсульфоновой, циклогексансульфаминовой, 2-оксибензойной, 4-амино-2-оксибензойной и т.п. кислотами. И наоборот, солевая форма может быть превращена в форму свободного основания обработкой щелочью. Соединения формулы (I), содержащие кислотные протоны, могут быть превращены в терапевтически активные нетоксичные формы солей металлов или аддитивные аминные солевые формы обработкой подходящими органическими и неорганическими основаниями. Подходящие основные солевые формы включают, например, аммониевые соли, соли щелочных и щелочно-земельных металлов, например соли лития, натрия, калия, магния, кальция и т.п., соли с органическими основаниями, например с первичными, вторичными и третичными алифатическими и ароматическими аминами, такими как метиламин, этиламин, пропиламин, изопропиламин, четыре изомера бутиламина, диметиламин, диэтиламин, диэтаноламин, дипропиламин, диизопропиламин, ди-н-бутиламин, пирролидин, пиперидин, морфолин, триметиламин, триэтиламин, трипропиламин, хинуклидин, пиридин, хинолин и изохинолин, бензатин, N-метилD-глюкамин, 2-амино-2-(гидроксиметил)-1,3-пропандиол, гидрабаминные соли и соли с аминокислотами, такими как, например, аргинин, лизин и т.п. И наоборот, солевая форма может быть превращена обработкой кислотой в форму свободной кислоты. Термин аддитивная соль также включает гидраты и аддитивные формы с растворителем (сольваты), которые могут образовывать соединения формулы (I). Примерами таких форм являются, например, гидраты, алкоголяты и т.п. Термин четвертичный амин относится к четвертичным аммониевым солям, которые соединения формулы (I) могут образовывать при взаимодействии между основным азотом соединения формулы (I) и подходящим агентом, образующим четвертичное основание, таким как, например, необязательно замещенный алкилгалогенид, арилгалогенид или арилалкилгалогенид, например метилйодид или бензилйодид. Могут использоваться и другие реагенты с легко удаляемой группой, такие как алкилтрифторметансульфонаты, алкилметансульфонаты и алкил-п-толуолсульфонаты. Четвертичный амин содержит положительно заряженный атом азота. Фармацевтически приемлемые противоионы включают хлор, бром,йод, трифторацетат и ацетат. Выбранный противоион может вводиться с использованием ионнообменных смол. Подразумевается, что N-оксидные формы представленных соединений включают соединения формулы (I), где один или несколько третичных атомов азота окислены до так называемого N-оксида. Будет понятно, что некоторые соединения формулы (I) и их N-оксиды, аддитивные соли, четвертичные амины и стереохимические изомерные формы могут содержать один или несколько хиральных центров и существуют в виде стереохимически изомерных форм. Термин стереохимически изомерные формы, используемый выше, включает все возможные стереоизомерные формы, которыми могут обладать соединения формулы (I) и их N-оксиды, аддитивные соли, четвертичные амины или физиологически функциональные производные. За исключением особо оговоренных или указанных случаев, химическое описание соединений включает смесь всех возможных стереоизомерных форм, причем указанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры, а также каждую из отдельных изомерных форм формулы (I) и их N-оксидов,солей, сольватов или четвертичных аминов, по существу, свободную, т.е. содержащую менее 10%, предпочтительно менее 5%, особенно предпочтительно менее 2% и наиболее предпочтительно 1% других изомеров. Таким образом, когда соединение формулы (I) описано, например, как (E), это означает, что соединение по существу свободно от (Z) изомера. В частности, стереоизомерные центры могут иметь R- или S-конфигурацию; заместители на двухвалентных циклических (частично)насыщенных радикалах могут иметь цис- или трансконфигурацию. Соединения, включающие двойные связи, могут иметь E (entgegen) или Z (zusammen)-стереохимию при указанной двойной связи. Термины цис-, транс-, R, S, Е и Z известны квалифицированным специалистам данной области техники. Разумеется, что стереоизомерные формы соединений формулы(I) включены в области данного изобретения. Для некоторых соединений формулы (I), солей, сольватов, а также промежуточных продуктов, используемых при их получении, абсолютная стереохимическая конфигурация экспериментально не опре-4 011256 делена. В этих случаях стереоизомерная форма, которая была выделена первой, определяется как А, и вторая определяется как В без дополнительного указания действительной стереохимической конфигурации. Однако указанные стереоизомерные формы А и В могут однозначно характеризоваться, например, их оптическим вращением, когда А и В имеют энантиомерное отличие. Квалифицированный специалист может определить абсолютную конфигурацию таких соединений, используя известные методы, такие как, например, рентгенография. Когда А и В представляют собой стереоизомерные смеси, они могут быть разделены, и соответствующие первые выделенные фракции обозначаются как А 1 и В 1, а вторые как А 2 и В 2 без дополнительного указания действительной стереохимической конфигурации. Некоторые соединения формулы (I) могут также существовать в таутомерной форме. Подразумевается, что такие формы, хотя конкретно и не указаны в представленной выше формуле, но включены в область данного изобретения. Подразумевается, что термин соединения формулы (I), используемый в данном описании, включает соли и стереохимически изомерные формы. Особый интерес представляют соединения формулы (I),которые являются стереохимически чистыми. Всякий раз, когда в описании говорится, что заместители могут быть выбраны, каждый независимо,из перечня нескольких определений, подразумеваются все возможные сочетания, которые химически возможны и которые приводят к химически стабильным молекулам. Отдельную подгруппу соединений формулы (I) составляют соединения, в которых -b1-b2-b3- представляет собой двухвалентный радикал формулы В данной подгруппе соединения, в которых -b1-b2-b3- является радикалом (b-1), представляют особый интерес. Другую отдельную подгруппу соединений формулы (I) составляют соединения, в которых -b1-b2-b3 представляет двухвалентных радикал формулы Подгруппами соединений формулы (I), которые представляют интерес, являются соединения, в которых n равно 1, m равно 0, 1, q равно 1. Подгруппу соединений, представляющих особый интерес, составляют соединения формулы (I), в которых R13 и R14 представляют собой водород. Подгруппами соединений формулы (I), представляющих дополнительный интерес, являются соединения, в которых Y представляет собой водород. Особую подгруппу соединений формулы (I) составляют соединения, в которых R17 представляет собой циано, C1-6 алкил, замещенный циано, С 2-6 алкенил, замещенный циано, или R17 представляет собой=O. Особый интерес представляют любые подгруппы соединений формулы (I), в которых -b1-b2-b3 представляет собой двухвалентный радикал формулыR17 представляет собой =O. Особую подгруппу соединений формулы (I) составляют соединения, в которых -b1-b2-b3- принимает значение (b-2), n равно 1; m равно 0; q равно 1; R2 представляет собой циано; Y представляет собой водород; R17 представляет собой С 1-6 алкил, замещенный циано. Для соединений формулы (I), в которых -b1-b2-b3- принимает значение (b-5), подгруппы, где применяется одно или более приведенных далее ограничивающих условий, представляют особый интерес: n равно 1; m равно 0; q равно 1; R2 представляет собой циано; R3 представляет собой галоген, Y представляет собой водород; R17 представляет собой C1-6 алкил, замещенный циано. Дополнительные подгруппы соединений согласно данному изобретению составляют соединения формулы (I) или любые соединения из подгрупп соединений формулы (I), определенных в данном описании, в которых один или несколько из C1-6 алкилов ограничен(ы) С 1-4 алкилом, один или несколько С 1-4 алкилов ограничен(ы) С 1-2 алкилом; один или несколько С 2-6 алкенилов ограничен(ы) С 2-4 алкенилом; один или несколько С 2-6 алкинилов органичен(ы) С 2-4 алкинилом. Дополнительные подгруппы соединений согласно данному изобретению составляют соединения формулы (I) или любые соединения из подгрупп соединений формулы (I), определенных в данном опи-5 011256 сании, где один или несколько радикалов, которые представляют собой (или один или несколько радикалов, которые содержат) гетероциклы или карбоциклы, являются гетероциклами или карбоциклами, которые определены в данном описании. Синтез Соединения формулы (I) могут быть получены различными путями, некоторые из которых описаны далее более подробно. Обычно соединения формулы (I) могут быть получены взаимодействием промежуточного соединения формулы (а-1) с пиримидин- или триазинпроизводным (а-2). Группы HX1 и W1 выбраны таким образом, что образуется соединительный фрагмент X1. В частности, W1 представляет собой подходящую удаляемую группу и X1 представляет собой гетероатом. Примерами подходящих удаляемых групп в (а-2) являются галоген, в частности хлор и бром, а также тозилат, мезилат, трифлат и т.п. группы. Превращение (а-1) при взаимодействии с (а-2) в (а-3) на представленной выше схеме особенно применимо, когда W1 представляет собой удаляемую группу и X1 представляет собой гетероатом, например группу -NR5-, -NH-NH-, -N=N-, -О-, -S-, -Х 2-С 1-4 алкандиил. Данное превращение особенно подходит в том случае, когда X1 представляет собой -О-. Когда X1 представляет собой S, последний может быть удобно превращен в соответствующий сульфоксид или сульфон с использованием хорошо известных методик окисления. Описанная выше реакция обычно проводится в присутствии подходящего растворителя. Подходящими растворителями являются, например, ацетонитрил, спирты, такие как, например, этанол, 2 пропанол, этиленгликоль, пропиленгликоль, полярные апротонные растворители, такие как N,Nдиметилформамид; N,N-диметилацетамид, диметилсульфоксид, 1-метил-2-пирролидинон, [bmim]PF5; простые эфиры, такие как 1,4-диоксан, пропиленгликольмонометилэфир. Когда X1 представляет собой -С(=O)-, исходное вещество (а-1), где группа -X1H представляет собой группу реактива Гриньяра (-Mg-галоген) или литий, подвергается взаимодействию с исходным веществом (а-2), где W1 представляет собой функциональную группу сложного эфира (-СООалкил). Последний сложный эфир может также подвергаться восстановлению до спирта с использованием, например,LiAlH4 и затем подвергаться окислению умеренным окислителем, таким как MnO2, до соответствующего альдегида, который далее подвергается взаимодействию с исходным веществом (а-1), где -X1H представляет собой группу реактива Гриньяра (-Mg-галоген) или литий. Соединения, в которых -X1 представляет собой -С(=O)-, могут подвергаться превращению в -СНОН-аналоги с помощью подходящей реакции восстановления, например, с использованием LiAlH4. Когда X1 представляет собой С 1-4 алкандиил, мостик может вводиться в соответствии с реакцией Гриньяра, например, взаимодействием исходного вещества (а-1), где -X1H группа представляет собой С 1-4 алкандиил-Mg-галоген, с реагентом (а-2), где W1 представляет собой группу галогена, или наоборот. Когда X1 представляет собой метилен, метиленовая группа может подвергаться окислению до группы-С(=O)- (X1 представляет собой -С(=O)-), например, при использовании диоксида селена. Группа -С(=O)-, в свою очередь, может подвергаться восстановлению подходящим гидридом, таким как LiAlH4, с получением группы -CHOH-. Когда X1 представляет собой -NR13-C(=O)- или -С(=O)-NR13-, мостик X1 может быть получен с использованием подходящей реакции образования амидной связи, исходя из промежуточного соединения(а-1), где -X1H представляет собой -NHR13, и промежуточного соединения (а-2), где W1 представляет собой карбоксильную группу или ее активную производную группу, или наоборот, исходя из промежуточного соединения (а-1), где -X1H представляет собой карбоксильную группу или ее активную производную группу, и промежуточного соединения (а-2), где W1 представляет собой группу -NHR13. Образование амидной связи может осуществляться в соответствии с хорошо известными методиками, например активацией карбоксильной группы до группы хлоранангидрида или бромангидрида или использованием-6 011256 подходящего связующего агента. Когда X1 представляет собой -Х 2-С 1-4 алкандиил, промежуточное соединение (а-1), где -X1H представляет собой -X2H, подвергается взаимодействию с промежуточным соединением (а-2), где W1 представляет собой -С 1-4 алкандиил-W2 и W2 представляет собой подходящую удаляемую группу. Когда -X1 представляет собой -С 1-4 алкандиил-Х 2-, промежуточное соединение (а-1), где -X1H представляет собой-С 1-4 алкандиил-W2, и W2 представляет собой подходящую удаляемую группу, подвергается взаимодействию с промежуточным соединением (а-2), где W1 представляет собой -X2H. Мостиковые связи X2, не содержащие гетероатома (т.е. X2 представляет собой -С(=O)-, -CHOH-),могут быть получены в соответствии с методиками, аналогичными используемым для образования мостика X1. Когда X1 представляет собой -NR5-, взаимодействие (а-1) с реагентом (а-2) обычно проводится в нейтральной среде или, предпочтительно в кислой среде, обычно при повышенных температурах и при перемешивании. Кислотные условия могут быть получены добавлением соответствующих количеств подходящей кислоты или использованием кислотных растворителей, например соляной кислоты, растворенной в алканоле, таком как 1- или 2-пропанол. Описанная выше реакция может проводиться в присутствии подходящего растворителя. Подходящими растворителями являются, например, ацетонитрил, спирт, такой как, например, этанол, 2 пропанол, 2-пропанол-HCl; N,N-диметилформамид; N,N-диметилацетамид, 1-метил-2-пирролидинон; 1,4-диоксан, пропиленгликольмонометилэфир. Предпочтительно растворителем является 2-пропанол, 6 н.HCl в 2-пропаноле или ацетонитриле, особенно предпочтителен ацетонитрил. Необязательно, может присутствовать гидрид натрия. Когда X1 представляет собой -O-, реакцию обычно проводят следующим образом. Промежуточное соединение (а-1) сначала подвергается взаимодействию с перемешиванием при комнатной температуре с гидридами в органическом растворителе. После этого к смеси добавляется растворитель, такой как Nметилпирролидинон, диметилацетамид или диметилформамид, с последующим добавлением реагента (а 2). Обычно реакционная смесь перемешивается в течение ночи при повышенных температурах с получением соединения (а-3). Соединения формулы (а-3), содержащие заместитель R17, который представляет собой оксогруппу(=O) (представленные структурой (а-3-1, могут использоваться в качестве исходного вещества для получения соединений формулы (I), содержащих заместитель R17, который представляет собой =N-R18, где=N-R18 представляет собой =NH, =N-R15, =N-R7, =N-O-R15, =N-O-R7, как определено выше. В данном способе синтеза промежуточный продукт (а-3-1) подвергается взаимодействию с реагентом (а-7) (реагент(а-7) имеет общую формулу NH3, NH2-R15, NH2-R7, NH2-O-R15, NH2-O-R7, в частности Ar-C1-6 алкил-ONH2) при повышенных температурах в спиртовом растворителе в присутствии основания для получения соединения формулы (а-8). Аналогично, соединения формулы (а-3-1) могут использоваться в качестве исходного вещества для получения соединений формулы (I), содержащих заместитель R17, который представляет собой заместитель =Х, где =Х представляет собой =СН 2, =СН-С(=O)-NR13R14, =CH-R7 или =CH-R15, как определено выше. Промежуточный продукт (а-3-1) далее подвергается взаимодействию с реагегнтом (а-4) в соответствии с реакцией Виттига или реакцией Виттига-Хорнера. Реагент (а-4) представляет собой реагент Виттига, такой как трифенилфосфонийилид, или реагент Виттига-Хорнера, в частности фосфонат, такой как,например, реагент формулы ди(С 1-6 алкилокси)-P(=O)-X4, где X4 представляет собой заместитель R17, который может присоединяться к циклу посредством двойной связи (двойная оксосвязь). Реакцию ВиттигаХорнера обычно проводят в присутствии основания, предпочтительно сильного основания, в апротонном органическом растворителе при комнатной температуре. Реакция должна проводиться в течение времени, достаточного для полноты ее протекания, обычно в течение ночи, для получения соединения (а-5). Последнее может далее подвергаться взаимодействию в спиртовом растворителе в восстанавливающих условиях для получения соединения формулы (а-6). Обе реакции показаны на представленной ниже схеме. Оксогруппа в соединениях (а-3-1) может также находиться в других положениях в цикле, содержащем заместитель(и) R17, причем дальнейшая аналогичная химическая обработка может приводить к получению изомеров положения (а-8), (а-5) и (а-6). Соединения формулы (I) могут также быть получены, как показано на схеме реакции, представленной ниже. Реагент формулы (а-1) подвергается взаимодействию с пиримидин- или триазин-производным формулы (а-9), где заместители принимают значения, определенные в данном описании, и W1 представляет собой подходящую удаляемую группу, такую как, например, галоген, трифлат, тозилат, метилсульфонил и т.п., с получением промежуточного продукта (а-10). Данное взаимодействие может осуществляться аналогично тому, как показано выше для взаимодействия (а-1) с (а-2), в особенности для различных возможных значений мостика -X1-. Когда это необходимо, группа W1, которая не влияет на ход данной реакции, может быть замещена предшественником удаляемой группы, таким как функциональная группа ОН, которая на конкретной стадии методики превращается в удаляемую группу, например превращением ОН группы в галогеновую группу или взаимодействием с подходящим реагентом, таким какPOCl3, тозилхлорид, мезилхлорид и т.п. Конечные продукты (I) могут быть получены из исходного вещества (а-10) взаимодействием с аминозамещенным ароматическим соединением (а-11) с помощью реакции арилирования. Подходящими растворителями для взаимодействия (а-1) с (а-9) и (а-10) с (а-11) являются эфиры,например 1,4-диоксан, ТГФ, спирты, например этанол, пропанол, бутанол, этиленгликоль, пропиленгликоль, пропиленгликольмонометилэфир, апротонные растворители, такие как ацетонитрил, ДМФА, ДМА,1-метил-2-пирролидинон и т.п. Если это необходимо, может добавляться основание. Подходящими основаниями для данной реакции являются, например, ацетат натрия, ацетат калия, N,N-диметилэтанамин,гидрокарбонат натрия, гидроксид натрия и т.п. Соединения формулы (I), где -b1-b2-b3- представляет собой -CH2-CH=CH- (b-5), могут быть получе-8 011256 ны также исходя из инданового производного формулы (а-12), как показано на приведенной ниже схеме. Индановое производное (а-12) подвергается превращению в (а-13) с использованием реакции Виттига или Виттига-Хорнера, как показано выше. Превращение (а-12) в (а-13) осуществляется аналогично тому,как описано выше для реакции (а-3-1) с получением (а-5). W1 и HX1 выбраны таким образом, что образуется мостиковый фрагмент X1. После этого продукт (а-13) подвергается реакции сочетания с реагентом(а-2). Предпочтительно, W1 представляет собой подходящую удаляемую группу и X1 представляет собой гетероатом. Данная реакция проводится с использованием методик, аналогичных описанным выше для взаимодействия (а-1) с (а-2). X4 принимает значения, которые описаны выше для получения (а-5) и (а-6). В этой реакции сочетания получают два конечных продукта: с одной стороны соединение (а-14), с другой - изомер (а-14), где X4 соединен двойной оксо-связью. Соединение формулы (I), где -b1-b2-b3- представляет собой -CH2-CH=CH- (b-5), также может быть получено исходя из инданпроизводного формулы (а-16), как показано на представленной далее схеме. В этом альтернативном способе получения промежуточный продукт (а-15) подвергается взаимодействию с подходящим галогенирующим агентом, например оксихлоридом фосфора, для получения соединения формулы (а-16), где X5 представляет собой галоген. Обычно указанную реакцию проводят в течение ночи при повышенных температурах. Промежуточный продукт (а-15) также может подвергаться взаимодействию с бромпроизводным, таким как PBr5. Соединения формулы (I), где Z представляет собой N (триазины), также могут быть получены реакциями конденсации с образованием триазинов, как описано, например, в ЕР-А-834507. Триазиновые производные формулы (I), где радикал Q представляет собой NR9R10, могут быть получены взаимодействием триазинового производного формулы (I), где Q представляет собой галоген, в частности когда Q представляет собой хлор или бром, с амином H-NR9R10 в соответствии с известными методиками. В данном и следующих способах получения продукты реакции могут быть выделены из реакционной среды и, если это необходимо, подвергаться дополнительной очистке методами, хорошо известными в данной области, такими как, например, экстракция, кристаллизация, дистилляция, растирание и хроматография. Соединения формулы (I) могут быть также превращены соединения формулы (I) одного в другое в соответствии с известными реакциями трансформации групп. Соединения формулы (I) могут быть превращены в соответствующие N-оксидные формы в соответствии с известными методиками превращения трехвалентного азота в N-оксидную форму. Указанная реакция N-окисления обычно может проводиться взаимодействием исходного соединения формулы (I) с подходящим органическим или неорганическим пероксидом. Подходящие неорганические пероксиды включают, например, пероксид водорода, пероксиды щелочных или щелочно-земельных металлов, на-9 011256 пример пероксид натрия, пероксид калия; подходящие органические пероксиды могут включать надкислоты, такие как, например, надбензойная кислота или галогензамещенная надбензойная кислота, например 3-хлорнадбензойная кислота, надалкановые кислоты, например надуксусная кислота, алкилгидропероксиды, например трет-бутилгидропероксид. Подходящими растворителями являются, например,вода, низшие спирты, например этанол и т.п., углеводороды, например толуол, кетоны, например 2 бутанон, галогенированные углеводороды, например дихлорметан, и смеси таких растворителей. Например, соединение формулы (I), где R3 включает циано, может подвергаться превращению в соединение формулы (I), где R3 включает аминокарбонил, взаимодействием с HCOOH в присутствии подходящей кислоты, такой как соляная кислота. Соединение формулы (I), где R3 включает циано, также может подвергаться превращению в соединение формулы (I), где R3 включает тетразолил, взаимодействием с азидом натрия в присутствии хлорида аммония и N,N-диметилацетамида. Соединения формулы (I), где R3 включает аминокарбонил, могут подвергаться превращению в соединение формулы (I), где R3 включает циано, в присутствии подходящего агента дегидратации. Дегидратация может проводиться в соответствии с методиками, хорошо известными квалифицированным специалистам, таким как методики, описанные в публикации "Comprehensive Organic Transformations. Aguide to functional group preparations" Richard C. Laroc, John WileySons, Inc., 1999, p. 1983-1985, которая введена в данное описание в виде ссылки. В указанной публикации перечислены различные подходящие реагенты, такие как, например, SOCl2, HOSO2NH2, ClSO2NCO, MeO2CNSO2NEt3, PhSO2Cl, TsCl,P2O5, (Ph3PO3SCF3)O3SCF3, сложный полифосфатный эфир, (EtO)2POP(OEt)2, (EtO)3PI2, 2-хлор-1,3,2 диоксафосфолан, 2,2,2-трихлор-2,2-дигидро-1,3,2-диоксафосфолан, POCl3, PPh3, P(NCl2)3, P(NEt2)3,COCl2, NaClAlCl3, ClCOCOCl, ClCO2Me, Cl3CCOCl, (CF3CO)2O, Cl3CN=CCl2, 2,4,6-трихлор-1,3,5 триазин, NaClAlCl3, HN(SiMe2)3, N(SiMe2)4, LiAlH4 и т.п. Все реагенты, перечисленные в указанной публикации, введены в данное описание в виде ссылки. Соединения формулы (I), где R3 включает С 2-6 алкенил, может подвергаться превращению в соединение формулы (I), где R3 включает C1-6 алкил, восстановлением в присутствии подходящего восстановителя, такого как, например, H2, в присутствии подходящего катализатора, такого как, например, палладий на угле, и в присутствии подходящего растворителя, такого как, например, спирт, например, метанол. Соединения формулы (I), где R3 представляет собой CH(OH)-R16, может подвергаться превращению в соединение формулы (I), где R3 представляет собой C(=O)-R16, взаимодействием с реагентом Джонса в присутствии подходящего растворителя, такого как, например, 2-пропанон. Соединение формулы (I), где R3 представляет собой С(=O)-CH2-R16a, где R16a представляет собой циано или аминокарбонил, может подвергаться превращению в соединение формулы (I), где R3 представляет собой C(Cl)=CH-R16a, взаимодействием с POCl3. Соединения формулы (I), где R3 представляет собой моноциклический, бициклический или трициклический насыщенный, частично насыщенный или ароматический карбоцикл или моноциклический,бициклический или трициклический насыщенный, частично насыщенный или ароматический гетероцикл, замещенный формилом, могут подвергаться превращению в соединения формулы (I), где R3 представляет собой моноциклический, бициклический или трициклический насыщенный, частично насыщенный или ароматический карбоцикл или моноциклический, бициклический или трициклический насыщенный, частично насыщенный или ароматический гетероцикл, замещенный группой CH(=N-O-R8),взаимодействием с NH2OR8 в присутствии подходящего основания, такого как, например, гидроксид натрия, в подходящем растворителе, таком как, например, спирт, например этанол и т.п. Соединения формулы (I), где R3 представляет собой моноциклический, бициклический или трициклический насыщенный, частично насыщенный или ароматический карбоцикл или моноциклический, бициклический или трициклический насыщенный, частично насыщенный или ароматический гетероцикл, замещенный группой CH(=N-O-R8), могут подвергаться превращению в соединение формулы (I), где R3 представляет собой моноциклический, бициклический или трициклический насыщенный, частично насыщенный или ароматический карбоцикл или моноциклический, бициклический или трициклический насыщенный, частично насыщенный или ароматический гетероцикл, замещенный группой CN, взаимодействием с карбодиимидом в присутствии подходящего растворителя, такого как, например, тетрагидрофуран. Соединения формулы (I), где R4 представляет собой нитро, может подвергаться превращению в соединение формулы (I), где R4 представляет собой амино, в присутствии подходящего восстановителя,такого как, например, H2, в присутствии подходящего катализатора, такого как, например, никель Ренея,и в присутствии подходящего растворителя, такого как, спирт, например метанол. Соединения формулы (I), где R1 представляет собой водород, могут подвергаться превращению в соединение формулы (I), где R1 представляет собой С 1-6 алкил, взаимодействием с подходящим алкилирующим агентом, таким как, например, йод-С 1-6 алкил, в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, тетрагидрофуран. Некоторые соединения формулы (I) и некоторые промежуточные соединения в данном изобретении могут содержать асимметрический атом углерода. Стереохимически чистые изомерные формы указанных соединений и указанных промежуточных продуктов могут быть получены с помощью известных- 10011256 методик. Например, диастереоизомеры могут быть разделены физическими методами, такими как селективная кристаллизация или хроматографические методы, например хроматография с обращенной фазой,жидкостная хроматография и т.п. Энантиомеры могут быть получены из рацемических смесей сначала превращением указанных рацемических смесей с подходящими разделяющими растворителями, такими как, например, хиральные кислоты, в смеси диастереомерных солей или соединений; затем физическим разделением указанных смесей диастереомерных солей или соединений с помощью, например, селективной кристаллизации или хроматографическими методами, например жидкостной хроматографией и т.п.; и наконец, превращением указанных разделенных диастереомерных солей или соединений в соответствующие энантиомеры. Чистые стереоизомерные формы могут также быть получены из чистых стереоизомерных форм соответствующих промежуточных продуктов и исходных веществ, при условии, что реакции взаимодействия протекают стереоспецифически. Альтернативный способ разделения энантиомерных форм соединений формулы (I) промежуточных продуктов включает жидкостную хроматографию, в частности жидкостную хроматографию с использованием неподвижной хиральной фазы. Некоторые из промежуточных продуктов и исходных веществ являются известными соединениями и могут быть коммерчески доступными, могут быть получены в соответствии с известными методиками или некоторые соединения формулы (I) или желаемые промежуточные продукты могут быть получены в соответствии с методиками, описанными в публикациях WO 99/50250 и WO 00/27825. Промежуточные соединения формулы (а-2) могут быть получены взаимодействием промежуточного продукта формулы (b-1) с агентом введения удаляемой группы формулы (b-2), где W1 представляет собой удаляемую группу и R представляет собой остаток агента введения удаляемой группы, такой как,например, POCl3. Подходящими удаляемыми группами в представленной выше реакции являются, например, галоген, трифлат, тозилат, мезилат и т.п., предпочтительно W1 представляет собой галоген, более предпочтительно йод или бром. Подходящими основаниями в представленной выше реакции являются, например, ацетат натрия,ацетат калия, N,N-диэтилэтанамин, гидрокарбонат натрия, гидроксид натрия и т.п. Подходящими растворителями в представленной выше реакции являются, например, ацетонитрил,N,N-диметилацетамид, ионогенная жидкость, например [bmim]PF6, N,N-диметилформамид, вода, тетрагидрофуран, диметилсульфоксид, 1-метил-2-пирролидинон и т.п. Соединения формулы (I), содержащие двойную углерод-углеродную связь, могут подвергаться восстановлению в соответствующие соединения с одинарной связью с использованием методов каталитического гидрирования. В данных способах используется катализатор благородного металла. Таким наиболее известным катализатором является Pd. Палладиевый (Pd) катализатор может представлять собой гомогенный Pd катализатор, такой как, например, Pd(OAc)2, PdCl2, Pd(PPh3)4, Pd(PPh3)2Cl2,бис(дибензилидинацетон)палладий, металлоцикл тиометилфенилглютарамид палладия и т.п., или гетерогенный Pd катализатор, такой как, например, палладий на угле, палладий на оксидах металлов, палладий на цеолитах. Предпочтительно, Pd катализатор представляет собой гетерогенный палладиевый катализатор, более предпочтительно палладий на угле (Pd/C). Pd/C является регенерируемым катализатором, стабильным и относительно недорогим. Он может легко выделяться (фильтрование) из реакционной смеси, снижая таким образом риск попадания следовых количеств Pd в конечный продукт. Применение Pd/C также устраняет необходимость применения лигандов, таких как, например, фосфиновые лиганды, которые являются дорогостоящими, токсичными и загрязняют синтезированные продукты. Соединения формулы (I), полученные описанными выше способами, могут синтезироваться в виде смеси стереоизомерных форм, в частности в форме рацемических смесей энантиомеров, которые могут быть разделены известными методами разделения. Рацемические соединения формулы (I) могут подвергаться превращению в соответствующие диастереомерные солевые формы взаимодействием с подходящей хиральной кислотой. Указанные диастереомерные солевые формы затем разделяют, например, селективной или фракционированной кристаллизацией и энантиомеры высвобождают из них с помощью щелочи. Альтернативный способ разделения энантиомерных форм соединений формулы (I) включает жидкостную хроматографию с использованием хиральной неподвижной фазы. Указанные чистые стереохимически изомерные формы могут быть также получены из соответствующих чистых стереоизомерных форм соответствующих исходных веществ при условии, что реакция протекает стереохимически. Предпочтительно, если необходим специфический стереоизомер, указанное соединение будет син- 11011256 тезировано стереоспецифическими методами получения. В таких методах будут преимущественно применяться энантиомерно чистые исходные вещества. Квалифицированному специалисту будет понятно, что в способах, описанных выше, функциональные группы промежуточных соединений могут при необходимости блокироваться защитными группами. Функциональные группы, для которых желательна защита, включают гидроксильную группу, аминогруппу и группу карбоновой кислоты. Подходящие защитные группы для гидроксильной группы включают триалкилсилильные группы (например, трет-бутилдиметилсилил, трет-бутилдифенилсилил или триметилсилил), бензил и тетрагидропиранил. Подходящие защитные группы для аминогруппы включают трет-бутилоксикарбонил или бензилоксикарбонил. Подходящие защитные группы для группы карбоновой кислоты включают группы сложных C1-6 алкиловых или бензиловых эфиров. Защита и удаление защиты функциональных групп может осуществляться до и после реакционной стадии. Применение защитных групп подробно описано в публикациях "Protective Groups in Organic Chemistry", edited by J.W.F. McOmine, Plenum Press (1973); и " Protective Groups in Organic Sunthesis" 2nd edition,T.W. GreeneP.G.M. Wutz, Wiley Interscience (1991). Соединения формулы (I) проявляют противоретровирусные свойства (свойства ингибирования ревертазы), в частности в отношении вируса иммунодефицита человека (ВИЧ), который является этиологическим агентом синдрома приобретенного иммунодефицита (СПИД) у людей. ВИЧ вирус предпочтительно инфицирует T-4 клетки человека и разрушает их или изменяет их нормальную функцию, в частности, координацию иммунной системы. В результате у инфицированного пациента всегда снижается количество T-4 клеток, которые, кроме того, функционируют патологическим образом. Таким образом,защитная иммунная система не способна подавлять инфекции и новообразования, и ВИЧинфицированный субъект обычно умирает от условно-патогенных инфекций, таких как пневмония, или от злокачественных опухолей. Другие состояния, связанные с ВИЧ инфекцией, включают тромбопению,саркому Капоши и инфекцию центральной нервной системы, характеризующуюся прогрессирующей демиелинизацией, приводящей к слабоумию, и такими симптомами как прогрессирующая дизартрия,атаксия и дезориентировка. ВИЧ инфекция, кроме того, также ассоциировалась с периферической невропатией, прогрессирующей генерализированной лимфаденопатией и связанным со СПИДом комплексом. Соединения данного изобретения также проявляют активность в отношении штаммов ВИЧ, стойких к (множеству) лекарственных средств, в частности, в отношении стойких к (множеству) лекарственных средств штаммов ВИЧ-1, точнее, соединения данного изобретения проявляют активность в отношении штаммов ВИЧ, в особенности штаммов ВИЧ-1, которые обладают приобретенной стойкостью к одному или нескольким известным ненуклеозидным ингибиторам ревертазы, отличным от соединений данного изобретения, и в частности, коммерческим ненуклиозидным ингибиторам ревертазы. Соединения данного изобретения также обладают незначительным или не обладают сродством к связыванию с 1 кислотными гликопротеидами человека; -1 кислотные гликопротеиды не воздействуют или незначительно воздействуют на анти-ВИЧ активность соединений данного изобретения. Благодаря противоретровирусным свойствам, особенно анти-ВИЧ свойствам и, в частности, антиВИЧ-1 активности, соединения формулы (I), их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины и стереоизомерные формы применимы для лечения ВИЧ инфицированных пациентов и профилактики таких инфекций. В общем случае соединения данного изобретения могут применяться для лечения теплокровных животных, инфицированных вирусами, жизнедеятельность которых опосредуется или зависит от ферментной ревертазы. Состояния, которые могут предотвращаться или лечиться соединениями данного изобретения, особенно состояния, связанные с ВИЧ и другими патогенными ретровирусами, включают СПИД, связанный со СПИДом комплекс (ARC), прогрессирующую генерализированную лимфаденопатию (PGL), а также хронические заболевания центральной нервной системы, вызываемые ретровирусами, такие как, например, ВИЧ-опосредуемое слабоумие и рассеянный склероз. Таким образом, соединения данного изобретения или любая их подгруппа могут использоваться в качестве лекарственных средств при перечисленных выше состояниях. Указанное применение в качестве лекарственного средства или способ лечения включает введение ВИЧ-инфицированным субъектам количества, эффективного для борьбы с состояниями, связанными с ВИЧ и другими патогенными ретровирусами, особенно ВИЧ-1. В частности, соединения формулы (I) могут использоваться для производства лекарственного средства для лечения или профилактики ВИЧ инфекций. С учетом применимости соединений формулы (I) предоставляется способ лечения теплокровных животных, включая людей, страдающих от вирусных инфекций, в частности ВИЧ инфекций, или способ профилактики вирусных инфекций, в частности ВИЧ инфекций, у теплокровных животных, включая людей. Указанный способ включает введение, предпочтительно пероральное введение, эффективного количества соединения формулы (I), их N-оксидной формы, фармацевтически приемлемой аддитивной соли, четвертичного амина или возможной стереоизомерной формы теплокровным животным, включая людей.- 12011256 В соответствии с другим аспектом данное изобретение предоставляет также фармацевтические композиции, включающие терапевтически эффективное количество соединения формулы (I) и фармацевтически приемлемый носитель или наполнитель. В соответствии с еще одним аспектом предоставлен способ получения фармацевтической композиции, описанной выше, включающий смешение соединения формулы (I) с подходящим фармацевтически приемлемым носителем или наполнителем. Соединения данного изобретения или их любая подгруппа может вводиться в различные фармацевтические формы, предназначенные для введения. В качестве подходящих композиций можно указать все композиции, обычно применяемые для системного введения лекарственных средств. Для получения фармацевтических композиций данного изобретения эффективное количество отдельного соединения,необязательно в форме аддитивной соли, в качестве активного ингредиента объединяется в однородную смесь с фармацевтически приемлемым носителем, который может принимать самые разные формы в зависимости от формы препарата, желательной для введения. Фармацевтические композиции желательно представляют собой композиции стандартной дозы, подходящие, в частности, для введения перорально,ректально, подкожно или парентеральной инъекцией. Например, при получении композиции в лекарственной форме для перорального введения может использоваться любая полезная фармацевтическая среда, такая как, например, вода, гликоли, масла, спирты и т.п. - в случае жидких препаратов для перорального введения, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители,такие как крахмалы, сахара, каолин, разбавители, смазывающие вещества, связующие вещества, дезинтегрирующие средства и т.п. - для приготовления порошков, пилюль, капсул и таблеток. Ввиду легкости введения таблетки и капсулы представляют наиболее преимущественные стандартные лекарственные формы, в которых, разумеется, применяются твердые фармацевтические носители. В композициях для парентерального введения носитель будет обычно включать стерильную воду, по меньшей мере значительную часть, хотя могут включаться и другие ингредиенты, например, для способствования растворению. Могут приготавливаться растворы для инъекций, в которых, например, носитель включает раствор соли, раствор глюкозы или смесь раствора соли и глюкозы. Могут приготавливаться суспензии для инъекций, в которых могут применяться подходящие жидкие носители, суспендирующие агенты и т.п. Могут приготавливаться также препараты в твердой форме, которые предназначены для превращения непосредственно перед применением в жидкие формы. В композициях, подходящих для чрескожного введения, носитель необязательно включает добавку для повышения проникновения и/или подходящий смачивающий агент, необязательно объединенный с подходящими добавками любой природы в минимальных количествах, которые не оказывают значительного неблагоприятного воздействия на кожу. Указанные добавки могут способствовать введению через кожу и/или могут быть полезными для получения желательных композиций. Такие композиции могут вводиться различными способами, например в виде чрескожных заплат, нанесением на некоторую область или в виде мазей. Соединения данного изобретения могут также вводиться ингаляцией или инсуффляцией посредством методов и препаратов, используемых в данной области для введения таким способом. Таким образом, обычно соединения данного изобретения могут вводиться в легкие в форме раствора, суспензии или сухого порошка. Любая система, разработанная для доставки растворов, суспензий или сухих порошков посредством пероральной или интраназальной ингаляции или инсуффляции подходит для введения данных соединений. Для способствования растворимости соединений формулы (I) в композиции могут включаться подходящие ингредиенты, например циклодекстрины. Подходящими циклодекстринами являются -, -, циклодекстрины или простые эфиры и их смешанные простые эфиры, где одна или несколько гидроксильных групп ангидроглюкозных звеньев циклодекстрина являются замещенными С 1-6 алкилом, в частности метилом, этилом или изопропилом, например случайно метилированный -CD; гидроксиС 1-6 алкилом, в частности гидроксиэтилом, гидроксипропилом или гидроксибутилом; карбоксиС 1-6 алкилом, в частности карбоксиметилом или карбоксиэтилом; С 1-6 алкилкарбонилом, в частности ацетилом. Особенно интересными в качестве комплексообразователей и/или солюбилизирующих добавок являются -CD,неупорядоченно метилированный -CD, 2,6-диметилCD, 2-гидроксиэтилCD, 2-гидроксиэтилCD,2-гидроксипропилCD и (2-карбоксиметокси)пропилCD, в особенности 2-гидроксипропилCD (2HPCD). Термин смешанный простой эфир относится к циклодекстриновым производным, в которых по меньшей мере две гидроксильных группы циклодекстрина этерифицированы различными группами, такими как, например, гидроксипропил и гидроксиэтил. Среднее молекулярное замещение (M.З.) используется в качестве меры среднего числа молей алкоксифрагментов на моль ангидроглюкозы. Средняя степень замещения (С.З.) определяет среднее количество замещенных гидроксилов на ангидроглюкозный остаток. Значение М.З. и С.З. может определяться различными аналитическими методами, такими как ядерный магнитный резонанс (ЯМР), массспектрометрия (MC) и инфракрасная спекстроскопия (ИК). В зависимости от используемого метода для одного заданного производного могут быть получены немного отличающиеся значения. Предпочтительно, при измерении масс-спектрометрией значение М.З. находится в интервале от 0,125 до 10 и значение- 13011256 С.З. находится в интервале от 0,125 до 3. Другие подходящие композиции для перорального или ректального введения включают частицы,состоящие из твердой дисперсии, содержащей соединение формулы (I) и один или несколько соответствующих фармацевтически приемлемых водорастворимых полимеров. Термин твердая дисперсия, используемый выше, определяет систему в твердом состоянии (в отличие от жидкого или газообразного состояния), содержащую по меньшей мере два компонента, само соединение формулы (I) и водорастворимый полимер, где один компонент диспергирован более или менее равномерно в другом компоненте или компонентах (в случае, когда в препарат включены дополнительные фармацевтически приемлемые агенты, такие как пластификаторы, консерванты и т.д.). Когда указанная дисперсия компонентов является таковой, что система химически и физически однородна или гомогенна или состоит из одной фазы, как определяется в термодинамике, такая твердая дисперсия будет называться твердый раствор. Твердые растворы представляют собой предпочтительные физические системы, поскольку компоненты в них обычно легко биологически доступны для организмов, в которые они вводятся. Данное преимущество, вероятно, можно объяснить легкостью, с которой указанные твердые растворы могут образовывать жидкие растворы при контакте с жидкой средой, такой как желудочный сок и кишечный сок. Легкость растворения может быть отнесена, по меньшей мере, отчасти к тому факту, что энергия, необходимая для растворения компонентов из твердого состояния, меньше энергии,которая необходима для растворения компонентов из кристаллической или микрокристаллической твердой фазы. Термин твердая дисперсия включает также дисперсии, которые в целом являются менее однородные, чем твердые растворы. Такие дисперсии не являются в целом химически и физически однородными или включают более одной фазы. Например, термин твердая дисперсия относится также к системе, содержащей домены или небольшие области, где аморфное, микрокристаллическое или кристаллическое соединение формулы (I) или аморфный, микрокристаллический или кристаллический водорастворимый полимер или оба эти компонента диспергированы более или менее равномерно в другой фазе,содержащей водорастворимый полимер, или соединение формулы (I) или твердый раствор, содержащий соединение формулы (I) и водорастворимый полимер. Указанные домены представляет собой области в твердой дисперсии, четко отмеченные некоторыми физическими признаками: небольшие по размеру и равномерно или неупорядоченно распределены во всей твердой дисперсии. Существуют различные способы получения твердых дисперсий, включая экструзию из расплава,распылительную сушку и растворение-испарение. Способ растворение-испарение включает следующие стадии:a) растворение соединения формулы (I) и водорастворимого полимера в подходящем растворителе,необязательно при повышенных температурах;b) нагрев раствора, полученного как описано в пункте а), необязательно в вакууме, до тех пор пока раствор не испарится. Раствор также может быть вылит на большую поверхность для получения тонкой пленки и испарения из нее растворителя. В способе распылительной сушки два компонента также растворяют в соответствующем растворителе и полученый раствор затем распыляют через сопло распылительной сушилки с последующим испарением растворителя из образующихся капель при повышенных температурах. Предпочтительный способ получения твердых дисперсий представляет собой способ экструзии расплава, включающий следующие стадии: а) смешение соединения формулы (I) и соответствующего водорастворимого полимера,b) необязательно смешение добавок с полученной таким образом смесью,c) нагрев и перемешивание полученной таким образом смеси до получения гомогенного расплава,d) экструзию полученного таким образом расплава через одно или несколько литьевых отверстий,e) охлаждение расплава до твердого состояния. Термины расплав и плавление должны интерпретироваться в широком смысле. Данные термины означают не только переход из твердого состояния в жидкое состояние, но могут относиться и к переходу в стеклообразное состояние или эластичное состояние, при котором один компонент смеси можно распределить более или менее гомогенно в другом. В особых случаях один компонент будет плавиться, а другой(ие) компонент(ы) будет(ут) растворяться в расплаве с получением таким образом раствора,который при охлаждении может образовывать твердый раствор, обладающий преимущественными свойствами растворения. После получения твердых дисперсий, как описано выше, полученные изделия могут необязательно измельчаться и просеиваться. Твердое дисперсионное изделие может растираться или измельчаться до получения частиц размером менее 600 мкм, предпочтительно менее 400 мкм и наиболее предпочтительно менее 125 мкм. Из частиц, полученных, как описано выше, могут затем традициионными способами изготавливаться лекарственные формы стандартной дозы, такие как таблетки и капсулы. Очевидно, что квалифицированный в данной области специалист способен оптимизировать параметры способов получения твердых дисперсий, описанные выше, такие как выбор наиболее подходящего- 14011256 растворителя, рабочих температуры, вид используемого аппарата, скорость распылительной сушки и общая скорость в экструдере расплава. Водорастворимые полимеры в частицах представляют собой полимеры, которые обладают кажущейся вязкостью при растворении при 20 С в водном растворе с концентрацией 2% (мас./об.) в интервале от 1 до 5000 мПас, более предпочтительно в интервале от 1 до 700 мПас, наиболее предпочтительно от 1 до 100 мПас. Например, подходящие водорастворимые полимеры включают алкилцеллюлозы, гидроксиалкилцеллюлозы, гидроксиалкилалкилцеллюлозы, карбоксиалкилцеллюлозы, соли щелочных металлов карбоксиалкилцеллюлозы, карбоксиалкилалкилцеллюлозы, сложные эфиры карбоксиалкилцеллюлозы, крахмалы, пектины, производные хитина, ди-, олиго- и полисахариды, такие как трегалоза, альгиновая кислота и ее соли щелочных металлов и соли аммония, каррагинаны, галактоманнаны, трагакант, агар-агар, аравийская камедь, гуаровая камедь, ксантановая камедь, полиакриловые кислоты и их соли, полиметакриловые кислоты и их соли, сополимеры метакрилатов, поливиниловый спирт, поливинилпирролидон, сополимеры поливинилпирролидона с винилацетатом, сочетания поливинилового спирта и поливинилпирролидона, полиалкиленоксиды и сополимеры этиленоксида и пропиленоксида. Предпочтительными полимерами являются гидроксипропилметилцеллюлозы. Кроме того, в качестве водоростворимого полимера при получении описанных выше частиц, как описано в публикации WO 97/18839, могут использоваться один или несколько циклодекстринов. Указанные циклодекстрины включают фармацевтически приемлемые незамещенные и замещенные циклодекстрины, известные в данной области, в частности, -, - или -циклодекстрины или их фармацевтически приемлемые производные. Замещенные циклодекстрины, которые могут использоваться для получения описанных выше частиц, включают простые полиэфиры, описанные в патенте США 3459731. Кроме того, замещенными циклодекстринами являются простые эфиры, в которых водород одной или нескольких гидроксильных групп замещен C1-6 алкилом, гидроксиС 1-6 алкилом, карбоксиС 1-6 алкилом или С 1-6 алкилоксикарбонил-С 1-6 алкилом или их смешанными простыми эфирами. В частности, такими замещенными циклодекстринами являются простые эфиры, в которых водород одной или нескольких гидроксильных групп циклодекстрина замещен C1-3 алкилом, гидроксиС 2-4 алкилом или карбоксиС 1-2 алкилом, или, точнее, метилом, этилом, гидроксиэтилом, гидроксипропилом, гидроксибутилом, карбоксиметилом или карбоксиэтилом. Особенно полезными являются простые -циклодекстриновые эфиры, например диметилциклодекстрин, которые описаны в публикации M. Nogradi, Drugs of Future, Vol. 9, No. 8, p. 577-578 (1984), и простые полиэфиры, например гидроксипропилциклодекстрин и гидроксиэтилциклодекстрин. Такой простой алкиловый эфир может представлять собой метиловый эфир со степенью замещения в интервале примерно от 0,125 до 3. Например, в интервале примерно от 0,3 до 2. Такой гидроксипропилциклодекстрин может, например, быть получен взаимодействием -циклодекстрина с пропиленоксидом и может характеризоваться значением MS в интервале примерно от 0,125 до 10, например примерно от 0,2 до 3. Другим типом замещенных циклодекстринов является сульфобутилциклодекстрины. Соотношение соединения формулы (I) и водорастворимого полимера может изменяться в широких пределах. Например, могут применяться соотношения в интервале от 1/100 до 100/1. Предпочтительные соотношения соединения формулы (I) к циклодекстрину находятся в интервале примерно от 1/10 до 10/1. Более предпочтительные отношения находятся в интервале примерно от 1/5 до 5/1. Кроме того, можно удобно вводить соединения формулы (I) в препарат в форме наночастиц, которые содержат поверхностный модификатор, абсорбированный на их поверхности в количестве, достаточном для сохранения эффективного среднего размера частиц менее 1000 нм. Полезными поверхностными модификаторами считаются такие модификаторы, которые физически адгезируют к поверхности соединения формулы (I), но химически не присоединяются к указанному соединению. Подходящие поверхностные модификаторы могут быть выбраны из известных органических и неорганических фармацевтических наполнителей. Такие наполнители включают различные полимеры, низкомолекулярные олигомеры, натуральные продукты и поверхностно-активные вещества. Предпочтительные модификаторы поверхности включают неионогенные и анионогенные поверхностно-активные вещества. Еще один интересный способ введения соединений формулы (I) включает фармацевтическую композицию, в которой соединения формулы (I) вводятся в гидрофильные полимеры, и нанесение данной смеси в качестве покрывающей пленки на большое количество шариков с получением таким образом композиции, которая может стандартно производиться и которая подходит для получения фармацевтических лекарственных форм стандартной дозы для перорального введения. Указанные шарики включают центральное, скругленное или сферическое ядро, пленочное покрытие из гидрофильного полимера и соединение формулы (I), а также, необязательно, слой уплотняющего покрытия. Вещества, подходящие для применения в качестве ядер в шариках, многообразны при условии, что указанные вещества являются фармацевтически приемлемыми и имеют соответствующие размеры и- 15011256 плотность. Примерами таких веществ являются полимеры, неорганические вещества, органические вещества и сахариды и их производные. Особенно полезно изготавливать описанные выше фармацевтические композиции в форме лекарственного препарата стандартной дозы для простоты введения и единообразия дозировки. Термин лекарственная форма стандартной дозы в данном описании относится к физически дискретным единицам,подходящим для применения в качестве единичных доз, причем каждая единица содержит предопределенное количество активного ингредиента, рассчитанного для получения желаемого терапевтического эффекта, в сочетании с необходимым фармацевтическим носителем. Примерами таких лекарственных форм стандартной дозы являются таблетки (включая таблетки с насечкой или покрытые оболочкой),капсулы, пилюли, порошки, расфасованные в пакеты, пластины, свечи, растворы или суспензии для инъекций и т.п. и их сочетания. Квалифицированный специалист в области лечения ВИЧ-инфекции смог бы определить эффективное суточное количество из результатов испытаний, представленных в данном описании. Обычно считается, что эффективное количество должно составлять от 0,01 до 50 мг/кг массы тела, более предпочтительно от 0,1 до 10 мг/кг массы тела. Возможно введение нужной дозы в виде двух, трех, четырех или более небольших доз через соответствующие промежутки времени в течение дня. Указанные небольшие дозы могут быть приготовлены в виде лекарственных форм стандартной дозы, например, содержащих от 1 до 1000 мг, в частности от 5 до 200 мг, активного ингредиента на стандартную лекарственную форму. Точная дозировка и частота введения зависит от конкретного используемого соединения формулы(I), конкретного состояния, подлежащего лечению, тяжести состояния, подлежащего лечению, возраста,массы и общего физического состояния конкретного пациента, а также других лекарственных средств,которые может принимать пациент, как хорошо известно квалифицированному специалисту. Кроме того,очевидно, что указанное эффективное суточное количество может снижаться или повышаться в зависимости от того, как пациент поддается лечению, и/или оценки лечащего врача соединений данного изобретения. Интервалы значений эффективного суточного количества, указанные выше, являются лишь рекомендациями и ни в коей мере не предназначены для ограничения области или применения данного изобретения. Представленные соединения формулы (I) могут использоваться сами по себе или в сочетании с другими терапевтическими средствами, такими как противовирусные средства, антибиотики, иммуномодуляторы или вакцины для лечения вирусных инфекций. Они могут также использоваться сами по себе или в сочетании с другими профилактическими средствами для профилактики вирусных инфекций. Соединения данного изобретения могут применяться в вакцинах и других профилактических средствах для профилактики вирусных инфекций в течение продолжительного периода времени. Соединения могут применяться в таких вакцинах сами по себе или в сочетании с другими соединениями данного изобретения или с другими противовирусными средствами методом, согласующимся с обычным применением ингибиторов ревертазы в вакцинах. Таким образом, представленные соединения могут объединяться с фармацевтически приемлемыми адъювантами, традиционно применяемыми в вакцинах, и вводиться в профилактически эффективные количества для защиты субъекта в течение длительного периода времени от ВИЧ инфекций. Сочетание противоретровирусного соединения и соединения данного изобретения может использоваться в качестве лекарственного средства. Таким образом, данное изобретение относится также к изделию, содержащему (а) соединение данного изобретения и (b) другое противоретровирусное соединение в качестве комбинированного препарата для одновременного, раздельного или последовательного применения для профилактики или лечения ретровирусных инфекций, в частности, для лечения инфекций ретровирусов с множественной лекарственной резистентностью. Таким образом, для борьбы, профилактики или лечения ВИЧ инфекций или инфекций и заболеваний, связанных с ВИЧ инфекциями, таких как синдром приобретенного иммунодефицита (СПИД) или связанный со СПИДом комплекс (ARC), соединения данного изобретения могут вводиться совместно в сочетании, например, с ингибиторами связывания,такими как, например, сульфат декстрана, сурамин, полианионы, растворимый CD4, PRO-542, BMS-806; ингибиторами слияния, такими как, например, Т 20, Т 1249, RPR 103611, YK-FH312, IC 9564, 5-helix, Dpeptide ADS-J1; ингибиторами связывания сорецептора, такими как, например, AMD 3100, AMD-3465,AMD7049, AMD3451 (Bicyclams), TAK779, Т-22, ALX40-4C; SHC-C (SCH351125), SHC-D, PRO-140,RPR103611; RT ингибиторами, такими как, например, фоскарнет (foscarnet) и пролекарства; нуклеозидными RTI, такими как, например, AZT, 3TC, DDC, DDI, D4T, Abacavir, FTC, DAPD (Amdoxovir), dOTCCGP64222. При введении соединений данного изобретения вместе с другими противовирусными лекарственными средствами, которые направлены на различные стадии жизненного цикла вируса, терапевтическое действие этих соединений может усиливаться. Комбинационная терапия, описанная выше, дает синергический эффект в ингибировании ВИЧ репликации, поскольку каждый компонент комбинациии воздействует на отдельный сайт ВИЧ репликации. Применение таких комбинаций может снижать дозировку данного стандартного противоретровирусного средства, который требовался для желательного терапевтического или профилактического эффекта, по сравнению в тем эффектом, который имеет место, когда данное лекарственное средство вводится в качестве единственного терапевтического лекарственного средства. Такие сочетания могут снижать или устранять побочные действия традиционных противоретровирусных терапевтических средств, применяемых отдельно, без снижения противовирусной активности лекарственных средств. Такие сочетания снижают потенциальную резистентность к терапевтическим средствам, применяемым отдельно, поскольку снижают до минимума любую ассоциированную с ними токсичность. Такие сочетания могут также повышать эффективность традиционного терапевтического средства без повышения связанной с ним токсичности. Соединения данного изобретения также могут вводиться в сочетании с иммуномодуляторами, например левамисолом, бропиримином, анти-альфа-интерфероновым антителом человека, альфаинтерфероном, интерлейкином 2, метионинэнкефалином, диэтилдитиокарбаматом, фактором некроза опухоли, налтрексоном и т.п.; с антибиотиками, например пентамидинизетиоратом и т.п.; холинергическими лекарственными средствами, например такрином, ривастигмином, донепезилом, галантамином и т.п., блокаторами каналов NMDA, например мемантином, для предотвращения или подавления инфекции и заболеваний или симптомов заболеваний, связанных с ВИЧ инфекциями, таких как СПИД и ARC,например слабоумия. Соединение формулы (I) может также объединяться с другим соединением формулы (I). Хотя данное изобретения направлено на применение представленных соединений для профилактики или лечения ВИЧ инфекций, представленные соединения могут также применяться в качестве ингибиторов других вирусов, которые зависят от аналогичных ревертаз, для обязательных событий в их жизненном цикле. ПРИМЕРЫ Представленные далее примеры предназначены для иллюстрации данного изобретения. Встречающиеся далее в описании аббревиатуры имеют следующие значения: ДМФА означает N,Nдиметилформамид, DIPE означает диизопропиловый эфир, ТГФ означает тетрагидрофуран, ДМСО означает диметилсульфоксид, EtOAc означает этилацетат, "pyr" означает пиридин. Схема 1 Пример 1. Получение промежуточного продукта 1b.N-Хлорсукцинимид (0,025 моль) небольшими порциями добавляют к смеси 5-гидрокси-1-инданона 1a (0,022 моль) в ацетонитриле (60 мл). Смесь кипятят с обратным холодильником при перемешивании в течение ночи. Добавляют H2O и полученную смесь экстрагируют CH2Cl2. Органический слой отделяют,сушат над MgSO4, фильтруют и упаривают. Остаток (6 г) очищают колоночной хроматографией на силикагеле (элюент: циклогексан/EtOAc 60/40; 15-40 мкм). Собирают две фракции и упаривают их, получая 2,2 г F1 и 1,3 г исходного вещества. F1 кристаллизуют из диизопропилового эфира. Осадок отфильтровывают и сушат, получая 0,9 г промежуточного продукта 1b (22%) (температура плавления: 212 С).- 17011256 Пример 2. Гидрид натрия (60% в масле) (0,0054 моль) добавляют к смеси 1b (0,0049 моль) в 1,4-диоксане (10 мл). Смесь перемешивают в течение 10 мин. Добавляют 1-метилпирролидинон (10 мл). Смесь перемешивают в течение 10 мин. Добавляют промежуточный продукт 1-1 (0,0049 моль). Смесь перемешивают в течение ночи при 140C. Смесь экстрагируют CH2Cl2. Органический слой промывают 10% растворомK2CO3, сушат (MgSO4), фильтруют и растворитель выпаривают. Получают 1,6 г остатка. Остаток кристаллизуют из CH3CN. Осадок отфильтровывают и сушат. Получают 0,46 г соединения 1 (29%). Температура плавления: 260 С. (MH+):(388). Схема 2 Пример 3. Смесь 5-аминоиндан-1-она (0,0003 моль) и промежуточного продукта 1-1 (0,0003 моль) в 3 н. растворе HCl (2 мл) кипятят с обратным холодильником при перемешивании в течение 2 ч. Осадок отфильтровывают, промывают H2O и диизопропиловым эфиром и сушат. В результате получают 0,06 г(52%) продукта. Полученную фракцию перекристаллизовывают из смеси CH3CN/диизопропиловый эфир. Осадок отфильтровывают и сушат, получая 0,035 г промежуточного продукта 2b (30%). (Температура плавления: 260 С). Пример 4. Получение соединения 2.1. Смесь промежуточного продукта 2b (0,0012 моль) в POCl3 (1 мл) кипятят с обратным холодильником при перемешивании в течение ночи. Растворитель упаривают досуха. Остаток переносят в 10% раствор K2CO3. Смесь экстрагируют CH2Cl2. Органический слой отделяют, сушат (MgSO4), фильтруют и упаривают. Остаток (0,73 г) очищают колоночной хроматографией на кромасиле (элюент: CH2Cl2/CH3OH 99/1; 5 мкм) . Собирают две фракции, растворитель выпаривают, получая 0,08 г F1 (17%) и 0,14 г F2(33%). F1 кристаллизуют из смеси CH3CN/диизопропиловый эфир. Осадок отфильтровывают и сушат. Получают 0,038 г соединения 2.1. (Температура плавления: 270 С; (MH+):370). Примеры 5-8. Синтез других индензамещенных. 2,6-Диаминопиримидинов- 18011256 Пример 5. Получение промежуточного продукта 3b. Дымящую азотную кислоту (0,362 моль) добавляют при -40C к 5-хлор-1-индану (промежуточное соединение 3 а, 26,7 ммоль). Смесь перемешивают в течение 2 ч при -40C. Смесь выливают в лед и экстрагируют дихлорметаном. Органический слой отделяют, промывают насыщенным раствором соли, сушат над MgSO4, фильтруют и упаривают. Остаток очищают колоночной хроматографией на силикагеле(элюент: циклогексан/EtOAc 65/35 15-40 мкм). Чистые фракции собирают и растворитель упаривают,получая 4,15 г промежуточного продукта 3b (73%) (температура плавления: 129 С). Пример 6. Получение промежуточного продукта 3 с. В аппарате гидрирования Парра 0,5 г никеля Ренея добавляют к раствору промежуточного продукта 3b (8,60 ммоль) в смеси ТГФ и MeOH (6/1). Емкость продувают азотом и вводят в него атмосферу водорода (3 бара). Смесь перемешивают в течение 1 ч при комнатной температуре, фильтруют через целит и упаривают досуха, получая 1,50 г промежуточного продукта 3 с (96%) (температура плавления: 214 С). Пример 7. Получение промежуточного продукта 3d (E/Z 89/11). трет-Бутоксид калия (56,4 ммоль) порциями добавляют при 0C к раствору цианометилфосфоната(56,4 ммоль) в ТГФ. Смесь перемешивают в течение 15 мин при 15 С. Затем к смеси по каплям при 0C добавляют раствор промежуточного продукта 3 е (14,1 ммоль) в ТГФ. Реакционную смесь перемешивают при комнатной температуре в течение ночи, выливают в воду, подкисляют 3 М соляной кислотой и экстрагируют дихлорметаном. Органический слой отделяют, промывают 10% раствором карбоната калия,насыщенным раствором соли, сушат над сульфатом магния, фильтруют и упаривают. Остаток очищают колоночной хроматографией на силикагеле (элюент: дихлорметан; 35-70 мкм). Чистые фракции собирают и растворитель упаривают, получая 1,88 г промежуточного продукта 3d (65%) (температура плавления: 196 С). Пример 8. Получение соединения 1.9 и 3 е (Z 100%). Промежуточные соединения 3d и I-1 тщательно измельчают и сплавляют, нагревая тепловой пушкой. Остаток переносят в смесь дихлорметана и метанола (90/10) и 10% раствор карбоната калия. Органический слой отделяют, промывают насыщенным раствором соли, сушат над сульфатом магния, фильтруют и упаривают. Остаток очищают колоночной хроматографией на силикагеле (элюент: дихлорметан/AcOEt 85/15; 15-40 мкм). Фракции собирают и упаривают, получая 0,126 г изомера 3 е(13%) и 0,104 г соединения 1.9 (11%). Каждую фракцию перекристаллизовывают из ацетонитрила, получая изомер 3 е (температура плавления: 248-249 С) и соединение 1.9 (температура плавления: 250 С). Примеры 9-11. Синтез 2-амино-4-бензофуранзамещенных пиримидинов. Пример 9. Получение соединения 3.61. Гидрид натрия (60% в масле) (0,0134 моль) добавляют к смеси 1a (0,0122 моль) в 1,4-диоксане (20 мл) . Смесь перемешивают в течение 10 мин. Добавляют 1-метилпирролидинон (20 мл) и полученную смесь перемешивают в течение 10 мин. К смеси добавляют реагент I-1 (0,0122 моль) и смесь перемешивают при 140C в течение ночи. К смеси добавляют H2O, после чего смесь экстрагируют смесью CH2Cl2/CH3OH. Органический слой промывают 10% раствором K2CO3, сушат над MgSO4, фильтруют и упаривают. Остаток очищают колоночной хроматографией на силикагеле (элюент: CH2Cl2/CH3OH 99/1; 15-40 мкм). Две фракции собирают и упаривают. Получают, соответственно, 0,271 г F1 (6%) и 0,74 F2 (второй продукт). 0,1 г F1 перекристаллизовывают из смеси диизопропиловый эфир/CH3CN. Осадок фильтруют и сушат. Общей выход методики синтеза составляет 0,034 г соединения 3.61 (температура плавления: 253 С, (MH+): 359).- 19011256 Пример 10. Получение соединения 3.62. Гидрид натрия (60% в масле) (0,027 моль) добавляют к раствору 1b (0,027 моль) в 1,4-диоксане (40 мл). Смесь перемешивают при комнатной температуре в течение 15 мин. К смеси добавляют 1 метилпирролидинон (30 мл) и полученную смесь перемешивают в течение 10 мин, после чего добавляют реагент I-1 (0,027 моль). Смесь перемешивают при 140C в течение ночи, выливают в H2O и экстрагируют CH2Cl2. Органический слой отделяют, сушат над MgSO4, затем фильтруют и растворитель выпаривают. Остаток (9 г) очищают колоночной хроматографией на силикагеле (элюент: циклогексан/EtOAc 70/30; 20-45 мкм). Фракции собирают и растворитель выпаривают. Получают 0,6 г (9%) продукта. Данную фракцию, содержащую соединение 3.62, перекристаллизовывают из CH3OH. Осадок отфильтровывают и сушат, получая 0,044 г соединения 3.62 (температура плавления: 260 С; (MH+): 345). Соединения формулы 3.63 и 3.65 получают в соответствии с методиками примеров 9 и 10. Пример 11. Получение соединения 3.1. Гидрид натрия (60% в масле) (0,0008 моль) добавляют при 5 С к смеси диэтилцианометилфосфоната (0,0008 моль) в ТГФ (13 мл) в потоке N2. Смесь перемешивают. Добавляют соединение 3.61 (0,0005 моль). Смесь перемешивают при комнатной температуре в течение ночи, выливают в H2O и экстрагируют CH2Cl2. Органический слой отделяют, сушат (MgSO4), фильтруют и упаривают. Остаток (0,23 г) очищают колоночной хроматографией на силикагеле (элюент: CH2Cl2 100; 15-40 мкм). Фракции, содержащие соединение 3.1, собирают и упаривают (выход: 0,1 г). Полученный продукт перекристаллизовывают из смеси диизопропиловый эфир/CH3CN. Осадок отфильтровывают и сушат, получая 0,058 г соединения 3.1 (26%) (температура плавления: 226 С; (MH+): 382). Пример 12. Получение соединения 3.2. трет-Бутоксид калия (0,0013 моль) добавляют при 5 С к раствору диэтилцианометилфосфоната(0,0013 моль) в ТГФ (5 мл) в потоке N2. Смесь перемешивают при комнатной температуре в течение 1 ч. Добавляют смесь соединения 3.62 (0,0008 моль) и ТГФ (5 мл). Смесь перемешивают при комнатной температуре в течение 1 ч. К полученной смеси добавляют H2O и смесь экстрагируют CH2Cl2. Органический слой отделяют, сушат (MgSO4), фильтруют и упаривают (получая 0,3 г (93%. Фракцию, содержащую соединение 3.2, перекристаллизовывают из смеси CH3OH/CH2Cl2. Осадок отфильтровывают и сушат,получая 0,045 г соединения 3.2 (14%) (температура плавления: 227 С; (MH+): 368). Соединения формул 3.3-3.6 и 3.19-3.20 получают в соответствии со схемой примеров 11 или 12. Синтез соединений 4.8-4.11. Пример 13. Получение промежуточного продукта 4b-1. Соединение 4 а (12,2 ммоль) смешивают с 4-пиридинкарбоксальдигидом (13,4 ммоль) в этаноле. Добавляют гидроксид калия (97,6 ммоль) и реакционную смесь перемешивают в течение 2 ч при 50C. Осадок отфильтровывают. Маточную жидкость упаривают досуха. Осадок и остаток упаривания переносят в воду и подкисляют 3 М соляной кислотой. Осадок отфильтровывают и сушат, получая 2,59 г (84%) промежуточного продукта 4b-1 (температура плавления: 260 С). Пример 14. Получение соединений 4.8-4.11. Соединения 4.8, 4.9, 4.10 и 4.11 синтезируют в соответствии с методикой, описанной в примере 2,но используя промежуточный продукт 4b в качестве исходного вещества. Соединения, представленные в приведенных далее таблицах, могут быть получены в соответствии с методиками описанных выше примеров или их очевидных эквивалентов. Таблица 1 Примеры препаратов Капсулы Активный ингредиент, в данном случае соединение формулы (I), может быть растворен в органическом растворителе, таком как этанол, метанол или метиленхлорид, предпочтительно в смеси этанола и метиленхлорида. Полимеры, такие как сополимер поливинилпирролидона и винилацетата (PVP-VA) или гидроксипропилметилцеллюлоза (HPMC), обычно с вязкостью 5 мПас, могут быть растворены в органических растворителях, таких как этанол, метанол, метиленхлорид. Подходящим растворителем для полимера может быть этанол. Растворы полимера и соединения могут быть смешаны и затем высушены распылительной сушкой. Отношение соединение/полимер может быть выбрано в интервале от 1/1 до 1/6. Промежуточные интервалы могут иметь значения от 1/1,5 до 1/3. Подходящим отношением может быть 1/6. Высушенным распылительной сушкой порошком, твердой дисперсией, можно после этого заполнить капсулы для введения. Значение загрузки лекарственного средства в одну капсулу может находиться в интервале от 50 до 100 мг в зависимости от размера используемой капсулы. Таблетки, покрытые пленкой Получение ядра таблетки. Смесь 100 г активного ингредиента, в данном случае соединения формулы (I), 570 г лактозы и 200 г крахмала можно тщательно смешать и затем увлажнить раствором 5 г додецилсульфата натрия и 10 г поливинилпирролидона в примерно 200 мл воды. Влажную порошкообразную смесь можно просеять,высушить и снова просеять. Затем может добавляться 100 г микрокристаллической целлюлолозы и 15 г гидрированного растительного масла. Массу можно тщательно перемешать и прессовать в таблетки с получением 10000 таблеток, каждая из которых содержит 100 мг активного ингредиента. Покрытие Раствор 10 г метилцеллюлозы в 75 мл денатурированного этанола можно добавлять в раствор 5 г этилцеллюлозы в 150 мл дихлорметана. После этого можно добавить 75 мл дихлорметана и 2,5 мл 1,2,3 пропантриола. 10 г полиэтиленгликоля можно расплавить и растворить в 7 5 мл дихлорметана. Полученный раствор можно добавить к первому раствору, а затем можно добавить 2,5 г октадеканоата магния, 5 г поливинилпирролидона и 30 мл концентрированной суспензии красителя и всю смесь подвергнуть гомогенизации. Ядра таблеток можно покрывать полученной смесью в аппарате для нанесения покрытия. Определение противовирусной активности Соединения данного изобретения испытывались на противовирусную активность в клеточном испытании. Испытания показали, что соединения проявляют значительную анти-ВИЧ активность в отношении лабораторного ВИЧ штамма дикого типа (штамм ВИЧ-1 LAI). Испытание на клеточном уровне проводилось в соответствии со следующей методикой. Экспериментальный метод клеточного испытания МТ 4 клетки, ВИЧ-инфицированные или ложно-инфицированные, инкубируют в течение пяти дней в присутствии ингибитора различной концентрации. В конце инкубационного периода все ВИЧинфицированные клетки были убиты реплицирующим вирусом в контрольных культурах в отсутствие любого ингибитора. Жизнеспособность клеток определяют измерением концентрации MTT, желтого водорастворимого тетразолиевого красителя, который превращается в темно-красный водорастворимый- 28011256 формазан в митохондриях исключительно живых клеток. В процессе солюбилизации изопропанолом полученных кристаллов формазана спектральное поглощение раствора наблюдается при 540 нм. Значения коррелируют непосредственно с количеством живых клеток, оставшихся в культуре по истечении пяти дней инкубирования. Ингибиторную активность соединения отслеживают на инфицированных вирусом клетках и выражают в виде ЕС 50 и ЕС 90. Данные величины представляют количество соединения,необходимого для защиты 50 и 90% клеток, соответственно, от цитопатогенного действия вируса. Токсичность соединения определяют на ложно-инфицированных клетках и выражают в виде CC50, которая представляет концентрацию соединения, необходимую для ингибиторвания роста клеток на 50%. Показатель селективности (SI) (отношение СС 50/ЕС 50) является показателем селективности анти-ВИЧактивности ингибитора. Когда результаты выражаются в виде, например значений рЕС 50 или рСС 50, результат выражается в виде отрицательного логарифма полученного значения EC50 или CC50 соответственно. Антивирусный спектр. Ввиду увеличения числа лекарственно резистентных ВИЧ-штаммов, соединения данного изобретения испытывают на их активность в отношении клинически выделенных ВИЧ штаммов, включающих некоторые мутации. Такие мутации ассоциированы с резистентностью к ингибиторам ревертазы и приводят к тому, что вирусы проявляют различные степени перекрестной стойкости к коммерчески доступным в настоящее время лекарственным средствам, таким как AZT и делавирдин. Таблица 13 Противовирусную активность соединения данного изобретения оценивают в присутствии ВИЧ дикого типа и ВИЧ мутантов, имеющих мутации в ревертазном гене. Активность соединений оценивают с использованием клеточного испытания и остаточную активность выражают в виде значений рЕС 50. В колонке А представлены значения рЕС 50 в отношении штамма А (штамм А содержит мутацию 100I в ВИЧ ревертазе), в колонке В представлены значения рЕС 50 в отношении штамма В (штамм В содержит мутацию 100I и 103N в ВИЧ ревертазе), в колонке представлены значения рЕС 50 в отношении штамма С (штамм С содержит мутацию 103N в ВИЧ ревертазе), в колонке D представлены значения рЕС 50 в отношении штамма D (штамм D содержит мутацию 181 С в ВИЧ ревертазе), в колонке E представлены значения рЕС 50 в отношении штамма E (штамм E содержит мутацию 188L в ВИЧ ревертазе), в колонке F представлены значения рЕС 50 в отношении штамма F (штамм F содержит мутацию 227 С в ВИЧ ревертазе) и в колонке G представлены значения рЕС 50 в отношении штамма G (штамм G содержит мутацию 106 А и 227L в ВИЧ ревертазе). В колонке IIIB представлены значения pEC50 в отношении штамма ВИЧ-LAI дикого типа. ND означает, что данная величина не определялась. его фармацевтически приемлемая аддитивная соль или стереохимически изомерная форма,где -а 1=а 2-а 3=а 4- представляет собой двухвалентный радикал формулы-b1-b2-b3- представляет собой двухвалентный радикал формулыR2 представляет собой циано иR17 представляет собой циано, галоген, -С(=O)-NR13R14, C1-6 алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из циано, -С(=O)-NR13R14 или галогена; С 2-6 алкенил, необязательно замещенный циано, -С(=O)-NR13R14; и, когда это возможно, R17 может быть присоединенным к фрагменту -b1-b2-b3- двойной связью, в результате чего R17 тогда представляет собойZ представляет собой C-Y,где Y представляет собой водород, галоген. 2. Соединение по п.1, где n равно 1; m равно 0 или 1; q равно 1. 3. Соединение по п.1, где R13 и R14 представляют собой водород. 4. Соединение по п.1, где Y представляет собой водород. 5. Соединение по п.1, где R17 представляет собой циано, C1-6 алкил, необязательно замещенный циано, С 2-6 алкенил, необязательно замещенный циано; или R17 представляет собой =O. 6. Соединение по п.1, где -b1-b2-b3- представляет собой двухвалентный радикал формулыR17 представляет собой =O. 7. Соединение по п.1, где-b1-b2-b3- представляет собой двухвалентный радикал формулыR17 представляет собой C1-6 алкил, замещенный циано. 8. Соединение по п.7, где -b1-b2-b3- представляет собой двухвалентный радикал формулыR17 представляет собой C1-6 алкил, замещенный циано. 9. Фармацевтическая композиция, включающая (а) эффективное количество соединения формулы(I) по п.1 и (b) фармацевтически приемлемый носитель. 10. Фармацевтическая композиция, включающая (а) соединение формулы (I) по п.1 и (b) другое противоретровирусное соединение в качестве комбинированного препарата. 11. Способ получения соединения формулы (I) по п.1, отличающийся тем, что проводят взаимодействие промежуточного соединения формулы (а-1) с пиридиновым производным (а-2)
МПК / Метки
МПК: A61P 31/18, C07D 239/48, C07D 239/47, A61K 31/505, C07D 407/12
Метки: репликацию, вич, триазины, пиримидины, ингибирующие
Код ссылки
<a href="https://eas.patents.su/30-11256-pirimidiny-i-triaziny-ingibiruyushhie-vich-replikaciyu.html" rel="bookmark" title="База патентов Евразийского Союза">Пиримидины и триазины, ингибирующие вич репликацию</a>
Предыдущий патент: Производные 2-аминобензойной кислоты
Следующий патент: Улучшенные ферменты
Случайный патент: Способ продуцирования вирусных частиц ad26