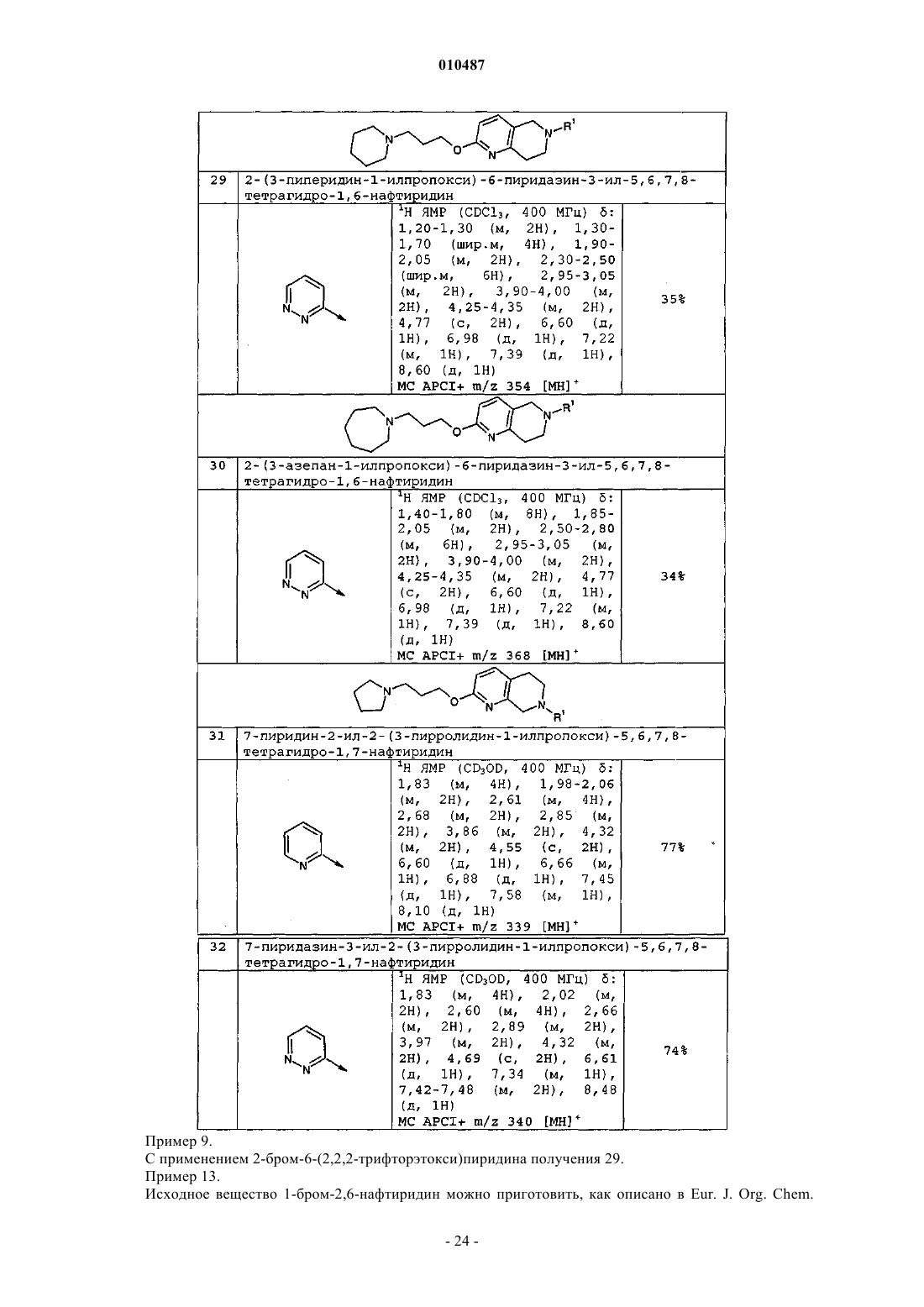
Производные тетрагидронафтиридина, пригодные в качестве лигандов рецептора н3 гистамина
Номер патента: 10487
Опубликовано: 30.10.2008
Авторы: Матиас Джон Пол, Лунн Грэхам, Стренг Росс Синклэр
Формула / Реферат
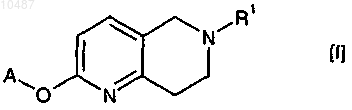
1. Соединение формулы (I)
или формулы (I')
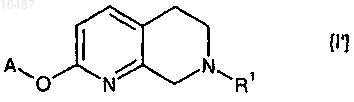
или его фармацевтически приемлемая соль или сольват, где
R1 представляет собой het1, необязательно замещенный одним или двумя заместителями, независимо выбранными из
галогена,
(С1-С4)алкила, необязательно замещенного галогеном,
(С1-С4)алкокси, необязательно замещенного галогеном,
-CN,
морфолино,
-NR2R3,
-(CH2)nC(O)NR2R3,
-(CH2)nC(O)O-R4,
-SO2-NR2R3,
-R6,
-O-R6,
где независимо для каждого заместителя n равен 0;
R2, R3, независимо друг от друга, выбраны из водорода и (C1-С4)алкила;
R4 представляет собой водород;
R6 представляет собой фенил, необязательно замещенный (C1-С4)алкокси;
А представляет собой:
(i) группу формулы
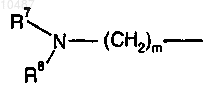
где m является целым числом от 2 до 6;
R7 и R8 вместе с атомом N, к которому они присоединены, образуют 5-, 6- или 7-членный насыщенный гетероцикл, необязательно замещенный одной или двумя группами, независимо выбранными из (С1-С4)алкила, или
(ii) группу формулы
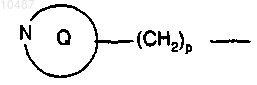
где р равно 0,
Q представляет 6-членный насыщенный гетероцикл, необязательно замещенный (C1-С6)алкилом,
где het1 выбран из моноциклических или бициклических гетероароматических групп, содержащих 5-10 атомов в кольце, которые включают 1, 2, 3 или 4 гетероатома (гетероатом), выбранных из азота и кислорода.
2. Соединение формулы (I) или (I'), как определено в п.1, где het1 выбран из моноциклических гетероароматических групп, содержащих 5 или 6 атомов в кольце, которые включают 1-2 атома азота или 1 атом азота и 1 атом кислорода, и бициклических гетероароматических групп, содержащих 9 или 10 атомов в кольце, которые включают 1-4 атома азота или 1 атом азота и 1 атом кислорода.
3. Соединение формулы (I) или (I'), как определено в п.2, где het1 выбран из моноциклических гетероароматических групп, содержащих 5 или 6 атомов в кольце, которые включают 1-2 атома азота.
4. Соединение формулы (I) или (I'), как определено в любом из предшествующих пунктов, где R1 замещен одним или двумя заместителями, выбранными из
галогена,
(С1-С4)алкила, необязательно замещенного галогеном,
(С1-С4)алкокси, необязательно замещенного галогеном,
CN,
морфолино,
-NR2R3,
-C(O)NR2R3,
-SO2-NR2R3,
-R6,
-O-R6,
где R2, R3 и R6 имеют значения, определенные в любом из предшествующих пунктов.
5. Соединение формулы (I) или (I'), как определено в п.4, где R1 не замещен или замещен (C1-C4)алкилом, (С1-С4)алкокси, C(O)NR2R3 или -SO2-NR2R3, где R2 и R3, независимо друг от друга, выбраны из водорода и (С1-С4)алкила.
6. Соединение формулы (I) или (I'), как определено в любом из предшествующих пунктов, где А представляет собой группу формулы
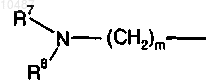
где m равняется 2 или 3, предпочтительно 3, и R7 и R8 вместе с атомом N, к которому они присоединены, образуют 5- или 6-членный насыщенный гетероцикл, который не замещен или замещен одним или двумя (C1-C4)алкилами, предпочтительно метилами.
7. Соединение формулы (I) или (I'), как определено в п.6, где R7 и R8 вместе с атомом N, к которому они присоединены, образуют 5-членный насыщенный гетероцикл, который не замещен или замещен одним или двумя метилами.
8. Соединение формулы (I) или (I'), как определено в любом из пп.1-5, где А представляет собой группу формулы

где р равно 0, и Q представляет собой насыщенный 6-членный гетероцикл, необязательно замещенный на атоме азота (C1-С4)алкилом.
9. Соединение по п.1, которое представляет собой 6-[2-[(1-изопропилпиперидин-4-ил)окси]-7,8-дигидро-1,6-нафтиридин-6(5Н)-ил]-N-метилникотинамид формулы
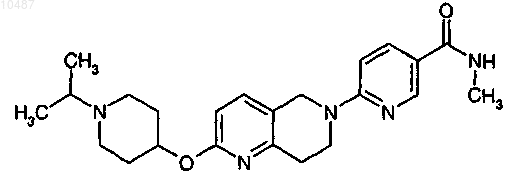
10. Соединение формулы (VII) или (XIV)
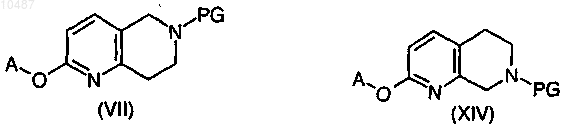
где А имеет значения, определенные в п.1, и PGпредставляет собой защитную группу, предпочтительно бензил или аллил.
11. Соединение формулы (VIII) или (XV)

где А имеет значения, определенные в п.1.
12. Применение соединения формулы (I) или (I'), как определено в любом из пп.1-9, или его фармацевтически приемлемой соли или сольвата для производства лекарственного средства для лечения заболевания, против которого показан лиганд H3.
13. Применение соединения формулы (I) или (I') по п.12 для производства лекарственного средства для лечения расстройств сна, мигрени, психотических расстройств, эпилепсии, болезней, связанных с дефицитом познавательных способностей, таких как болезнь Альцгеймера или умеренное ухудшение познавательных способностей, шизофрении, синдрома дефицита внимания с гиперактивностью (СДВГ), ожирения, астмы и аллергического ринита.
14. Способ получения соединения формулы (I) или (I') по любому из пп.1-9, включающий стадию взаимодействия галогенида формулы R1-X, где R1 имеет значения, определенные в любом из пп.1-9, и X представляет собой галоген, в присутствии основания с соединением формулы (VIII)
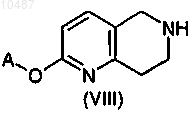
или формулы (XV)
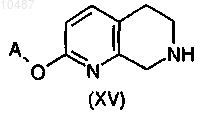
где А имеет значения, определенные в любом из пп.1-9.
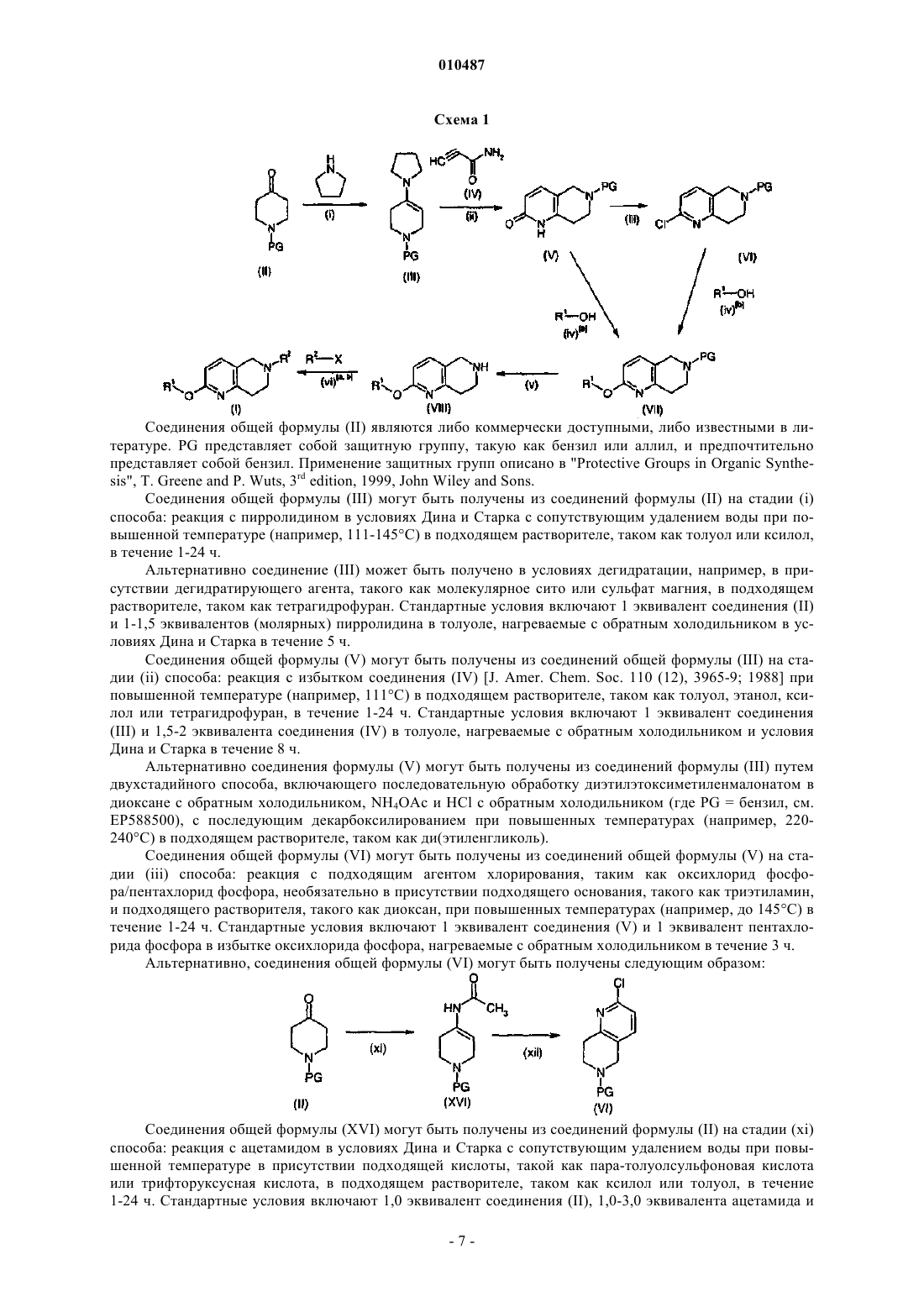
Текст
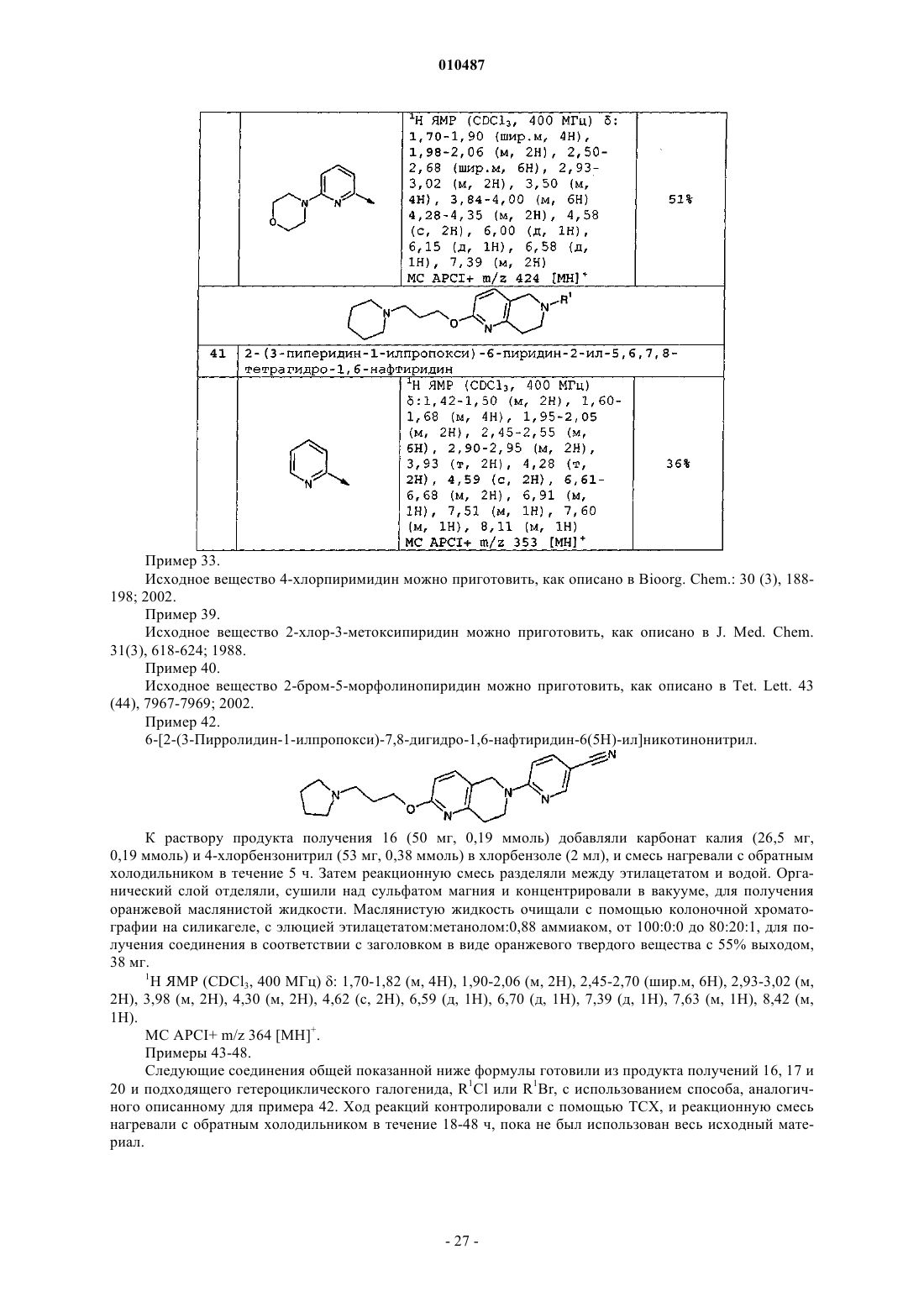
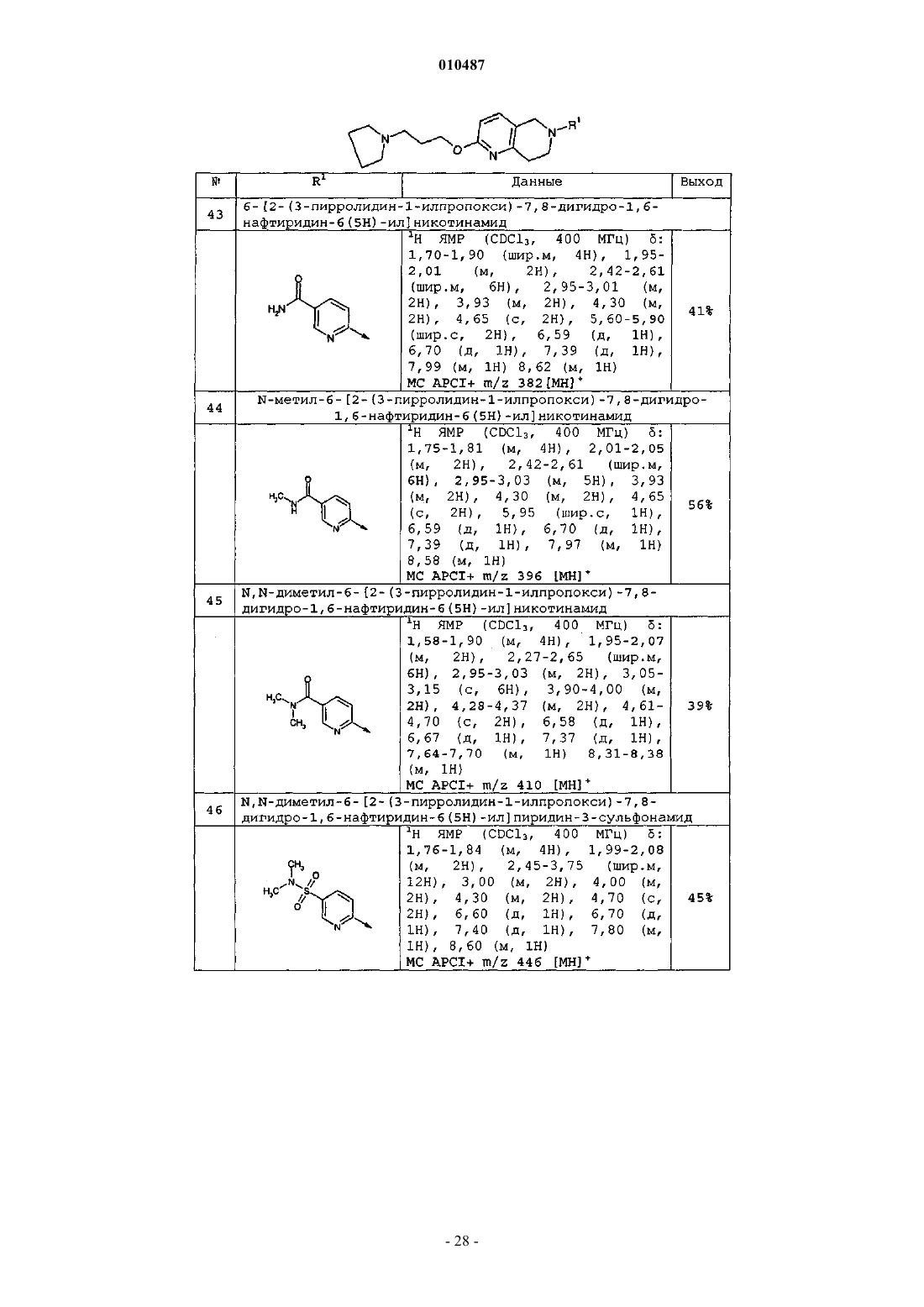
010487 Данное изобретение относится к производным тетрагидронафтиридина и к способам их получения,к промежуточным соединениям, используемым в их способе получения и к применениям таких производных. Производные тетрагидронафтиридина в соответствии с настоящим изобретением представляют собой лиганды рецептора H3 гистамина и имеют множество терапевтических назначений, в частности при лечении аллергического ринита. Рецепторы H3 гистамина найдены, среди прочего, на пресинаптических окончаниях периферических нервов, где они модулируют автономную нейропередачу и модулируют различные ответы органамишени под контролем автономной нервной системы. Они также являются гетерорецепторами, модулирующими высвобождение других многочисленных нейромедиаторов, таких как допамин, глутамат, норадреналин, серотонин, ГАМК, ацетилхолин, некоторые пептиды и комедиаторы. Недавно было разработано множество лигандов рецептора H3 гистамина. Краткий обзор текущих достижений в исследовании лиганда H3 и патентирование дано в Expert Opin. Ther. Patents (2003) 13(6). Примеры лигандов рецептора H3 гистамина могут быть найдены в WO 02/76925, WO 00/06254,WO 02/12190, WO 02/12214 и WO 02/06223. Считается, что лиганды рецептора H3 подходят для лечения различных заболеваний, включая как расстройства центральной нервной системы, так и воспалительные расстройства. Примерами заболеваний, для которых считается, что лечение лигандами H3 является полезным, являются воспалительное заболевание кишечника, болезнь Крона, язвенный колит, расстройства сна, мигрень, дискинезия, тревога,вызванная стрессом, психотические расстройства, эпилепсия, болезни, связанные с дефицитом познавательных способностей, такие как болезнь Альцгеймера или умеренное ухудшение познавательных способностей, депрессия, умеренное ухудшение познавательных способностей, депрессия, расстройства настроения, шизофрения, расстройства, связанные с тревогой, синдром дефицита внимания с гиперактивностью (СДВГ), психотические расстройства, ожирение, головокружение, эпилепсия, морская болезнь,вертиго, женская и мужская половая дисфункция, респираторные заболевания, такие как респираторный дистресс-синдром взрослых, острый респираторный дистресс-синдром, бронхит, хронический бронхит,хроническая обструктивная болезнь легких, муковисцедоз, астма, эмфизема, ринит, хронический синусит, аллергия, вызванные аллергией реакции дыхательных путей, аллергический ринит, вирусный ринит,неаллергический ринит, круглогодичный и сезонный ринит, заложенность носа, аллергическая заложенность носа. Несмотря на то, что лиганды H3 известны, существует потребность в обеспечении новых лигандовH3, которые являются хорошими кандидатами на применение в лекарственном средстве. В частности,предпочтительные соединения должны сильно связываться с рецептором H3 гистамина, проявляя небольшое сродство к другим рецепторам. Они должны хорошо всасываться в желудочно-кишечном тракте, быть метаболически устойчивыми и обладать предпочтительными фармакокинетическими свойствами. Они должны быть нетоксичными и не демонстрировать множество побочных эффектов. Следовательно, настоящее изобретение обеспечивает соединение формулы (I) или его фармацевтически приемлемую соль или сольват, гдеR1 представляет собой het1, необязательно замещенный одним или двумя заместителями, независимо выбранными из галогена,(С 1-С 4)алкила, необязательно замещенного галогеном,(С 1-С 4)алкокси, необязательно замещенного галогеном,-CN,морфолино,-NR2R3,-(CH2)nC(O)NR2R3,-(CH2)nC(O)O-R4,-SO2-NR2R3,-R6,-O-R6,где независимо для каждого заместителяn является 0,R2, R3, независимо друг от друга, выбраны из водорода и (С 1-С 4)алкила,-1 010487 где m является целым числом от 2 до 6,R7 и R8 вместе с атомом N, к которому они присоединены, образуют 5-, 6- или 7-членный насыщенный гетероцикл, необязательно замещен одной или двумя группами, независимо выбранными из где р является 0,Q представляет 6-членный насыщенный гетероцикл, необязательно замещенный (C1-С 6)алкилом,где het1 выбран из моноциклической или бициклической гетероароматической группы, содержащей 5-10 атомов в кольце, которые включают 1, 2, 3 или 4 гетероатома (гетероатом), выбранных из азота и кислорода. Преимущество соединений в соответствии с изобретением состоит в том, что они сочетают увеличенную H3 активность с возможностью сниженных сердечно-сосудистых побочных эффектов. Анализы для определения H3 активности и сердечно-сосудистых побочных эффектов даны в экспериментальной части ниже (функциональный анализ, основанный на клетке H3, и связывание дофетилида с продуктомhERG, соответственно). В настоящем описании используются следующие определения, если не определено иначе."(C1-Cx)алкил" обозначает насыщенную прямую или разветвленную углеводородную группу, содержащую от 1 до x атомов углерода и включает, например, (когда x=4) метил, этил, пропил, изопропил,н-бутил, изобутил, втор-бутил и трет-бутил и далее (когда x=6) пентил, изопентил, н-пентил и гексил. Это также относится к случаям, когда они имеют заместители или встречаются в виде заместителей других радикалов, например, в (C1-C4)алкокси радикалах, гидрокси(C1-C6)алкильных радикалах, (C1C4)алкокси(С 1-С 4)алкильных радикалах, (C1-C4)алкиламино радикалах, ди[(C1-C4)алкил]амино радикалах,(C1-C4)алкил-СООН радикалах, (C1-C4)алкил-О-(C1-C4)алкил-СООН радикалах и т.д. Примерами подходящих (C1-C4)алкокси радикалов являются метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси и трет-бутокси. Гидрокси(C1-C4)алкильные радикалы представляют собой алкильные радикалы, замещенные гидрокси. Они могут содержать 1 или несколько гидрокси-заместителей, если не формулируется иначе. Примерами подходящих гидрокси(C1-С 6)алкильных радикалов являются гидроксиметил, 1-гидроксиэтил или 2-гидроксиэтил. В случае, когда (C1-Cx)алкильные радикалы замещены галогеном, такой радикал может содержать 1 или несколько атомов галогена, если не формулируется иначе. Указанный галоген предпочтительно представляет собой фтор, хлор, бром или йод, в частности фтор или хлор. Например, во фторзамещенном алкильном радикале группа метил может присутствовать как дифторметильная или трифторметильная группа.(С 3-С 7)циклоалкил" обозначает насыщенную моноциклическую карбоциклическую группу, содержащую от 3 до 7 атомов углерода и включает, например, циклопропил, циклобутил, циклопентил, циклогексил и циклогептил."Насыщенный гетероцикл" обозначает насыщенную моноциклическую группу, имеющую 4-7 атомов в кольце, которая содержит 1 атом азота и 1 другой гетероатом, выбранный из азота (N), кислорода(О) и серы (S). Примерами подходящих насыщенных гетероциклов являются азетидинил, пирролидинил,пиперидинил, морфолинил, пиперазинил и азепанил."het1" определен в настоящем изобретении как моноциклическая или бициклическая гетероароматическая группа, имеющая 5-10 атомов в кольце, которая содержит 1, 2, 3 или 4 гетероатома (гетероатом). Гетероатомы выбраны из азота (N), кислорода (О) и серы (S). В частности, гетероароматическая группа содержит либо (а) 1-4 атома азота, (b) один атом кислорода или один атом серы, либо (с) 1 атом кислорода или 1 атом серы и 1 или 2 атома азота. Предпочтительно гетероароматическая группа содержит либо от 1 до 4 атомов (атом) азота в кольце, либо 1 или 2 атома азота и 1 атом кислорода. Гетероароматическая группа предпочтительно С-связанная, что означает, что группа связана с соседним атомом через атом углерода в кольце. Гетероароматическая группа может быть незамещенной, монозамещенной или замещенной двумя заместителями, как обозначено в определении R1 выше для общей формулы (I) и(I') в соответствии с настоящим изобретением. Замещение предпочтительно имеет место на кольцевом-2 010487 атоме углерода. Примеры гетероароматических групп включают, без ограничений, тиофенил, фуранил,пирролил, пиразолил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиранил, пиридинил, пиразинил, пиримидинил, пиридазинил, триазинил, тиадиазинил, изобензофуранил, бензофуранил, хроменил, индолизинил, изоиндолил, индолил, индазолил, пуринил, хинолинил, изохинолил, фталазинил, нафтиридинил, хиназолинил, хиноксалинил, бензоксазолил, бензотиазолил, бензимидазолил, бензофуранил и бензотиенил. В соответствии с предпочтительным аспектом изобретения het1 выбран из моноциклических гетероароматических групп, имеющих 5 или 6 атомов в кольце, которые содержат 1-2 атома азота или 1 атом азота и 1 атом кислорода, и бициклических ароматических гетероароматических групп, имеющих 9 или 10 атомов в кольце, которые содержат 1-4 атома азота или 1 атом азота и 1 атом кислорода. Более предпочтительно, het1 выбран из моноциклических гетероароматических групп, имеющих 5 или 6 атомов,которые содержат от 1 до 2 атомов азота. het1 предпочтительно является С-связанным. В соединениях формулы (I) или (I') R4 и R5 предпочтительно представляет собой водород или метил, и R6 предпочтительно представляет собой фенил, замещенный метокси. Один или два заместителя на R1 предпочтительно выбраны из галогена,(C1-C4)алкила, необязательно замещенного галогеном,(C1-C4)алкокси, необязательно замещенного галогеном,CN,морфолино,-NR2R3,-C(O)NR2R3,-SO2-NR2R3,-R6,-O-R6,где R2, R3 и R6 определены выше. Более предпочтительно, R1 не замещен или замещен (С 1-С 4)алкилом, (C1-C4)алкокси, C(O)NR2R3 или -SO2-NR2R3, где R2 и R3, независимо друг от друга, выбраны из водорода и (C1-C4)алкила, предпочтительно метила. В соответствии с предпочтительным аспектом А представляет собой группу формулы где m равняется 2 или 3, предпочтительно 3, и R7 и R8 вместе с атомом N, к которому они присоединены,образуют 5- или 6-членный насыщенный гетероцикл, который не замещен или замещен одним или двумя(C1-C4)алкилами, предпочтительно, метилами. Более предпочтительно, R7 и R8 вместе с атомом N, к которому они присоединены, образуют 5-членный насыщенный гетероцикл, который не замещен или замещен одним или двумя метилами. В соответствии с другим предпочтительным аспектом А представляет собой группу формулыQ представляет собой насыщенный 6-членный гетероцикл, необязательно замещенный на атоме азота (C1-С 4)алкилом, предпочтительно изопропилом. Отдельные предпочтительные соединения в соответствии с настоящим изобретением представляют собой следующие соединения, перечисленные ниже: 7-пиридазин-3-ил-2-(3-пирролидин-1-илпропокси)-5,6,7,8-тетрагидро-1,7-нафтиридин,6-пиразин-2-ил-2-(3-пирролидин-1-илпропокси)-5,6,7,8-тетрагидро-1,6-нафтиридин,6-(6-метилпиридин-3-ил)-2-(3-пирролидин-1-илпропокси)-5,6,7,8-тетрагидро-1,6-нафтиридин,6-пиридазин-3-ил-2-(3-пирролидин-1-илпропокси)-5,6,7,8-тетрагидро-1,6-нафтиридин,N-метил-6-[2-(3-пирролидин-1-илпропокси)-7,8-дигидро-1,6-нафтиридин-6(5 Н)-ил]никотинамид,6-[2-(3-пиперидин-1-илпропокси)-7,8-дигидро-1,6-нафтиридин-6(5 Н)-ил]никотинамид,2-(3-пиперидин-1-илпропокси)-6-пиридазин-3-ил-5,6,7,8-тетрагидро-1,6-нафтиридин,N,N-диметил-6-[2-(3-пирролидин-1-илпропокси)-7,8-дигидро-1,6-нафтиридин-6(5 Н)ил]никотинамид,2-3-[(2R)-2-метилпирролидин-1-ил]пропокси-6-пиридазин-3-ил-5,6,7,8-тетрагидро-1,6 нафтиридин,6-(6-метилпиридин-3-ил)-2-3-[(2R)-2-метилпирролидин-1-ил]пропокси-5,6,7,8-тетрагидро-1,6 нафтиридин,2-3-[(2R)-2-метилпирролидин-1-ил]пропокси-6-пиразин-2-ил-5,6,7,8-тетрагидро-1,6-нафтиридин,-3 010487N-метил-5-[2-(3-пирролидин-1-илпропокси)-7,8-дигидро-1,6-нафтиридин-6(5 Н)-ил]пиридин-2 карбоксамид,2-3-[(2S)-2-метилпирролидин-1-ил]пропокси-6-пиридазин-3-ил-5,6,7,8-тетрагидро-1,6 нафтиридин,2-3-[(2S)-2-метилпирролидин-1-ил]пропокси-6-пиразин-2-ил-5,6,7,8-тетрагидро-1,6-нафтиридин,6-(6-метилпиридин-3-ил)-2-3-[(2S)-2-метилпирролидин-1-ил]пропокси-5,6,7,8-тетрагидро-1,6 нафтиридин,N-метил-6-[2-3-[(2R)-2-метилпирролидин-1-ил]пропокси-7,8-дигидро-1,6-нафтиридин-6(5 Н)ил]никотинамид,2-[(1-изопропилпиперидин-4-ил)окси]-6-пиразин-2-ил-5,6,7,8-тетрагидро-1,6-нафтиридин,N,N-диметил-5-[2-(3-пирролидин-1-илпропокси)-7,8-дигидро-1,6-нафтиридин-6(5 Н)-ил]пиридин-2 карбоксамид,N-метил-5-[2-3-[(2R)-2-метилпирролидин-1-ил]пропокси-7,8-дигидро-1,6-нафтиридин-6(5 Н)ил]пиридин-2-карбоксамид,N-метил-6-[2-3-[(2S)-2-метилпирролидин-1-ил]пропокси-7,8-дигидро-1,6-нафтиридин-6(5 Н)ил]никотинамид,2-[(1-изопропилпиперидин-4-ил)окси]-6-(6-метилпиридин-3-ил)-5,6,7,8-тетрагидро-1,6-нафтиридин,6-[2-[(1-изопропилпиперидин-4-ил)окси]-7,8-дигидро-1,6-нафтиридин-6(5 Н)-ил]-Nметилникотинамид,5-[2-[(1-изопропилпиперидин-4-ил)окси]-7,8-дигидро-1,6-нафтиридин-6(5 Н)-ил]-N-метилпиридин 2-карбоксамид и 5-[2-(3-пирролидин-1-илпропокси)-7,8-дигидро-1,6-нафтиридин-6(5 Н)-ил]пиридин-2-карбоксамид и их фармацевтически приемлемые соли и сольваты. Фармацевтически приемлемые соли соединений формулы (I) или формулы (I') включают их кислотно-аддитивные и основные соли. Подходящие кислотно-аддитивные соли образованы из кислот, которые образуют нетоксичные соли. Примеры включают ацетатную, аспартатную, бензоатную, безилатную, бикарбонатную/карбонатную,бисульфатную/сульфатную, боратную, камзилатную, цитратную, эдисилатную, эзилатную, формиатную,фумаратную, глюцептатную, глюконатную, глюкуронатную, гексафторфосфатную, гибензатную, гидрохлоридную/хлоридную, гидробромидную/бромидную, гидроиодидную/иодидную, изетионатную, лактатную, малатную, малеатную, малонатную, мезилатную, метилсульфатную, нафтилатную, 2 напсилатную, никотинатную, нитратную, оротатную, оксалатную, пальмитатную, памоатную, фосфатную/гидрофосфатную/дигидрофосфатную, сахаратную, стеаратную, сукцинатную, тартратную, тозилатную и трифторацетатную соли. Подходящие основные соли образованы из оснований, которые образуют нетоксичные соли. Примеры включают соли алюминия, аргинина, бензатина, кальция, холина, диэтиламина, диоламина, глицина, лизина, магния, меглумина, оламина, калия, натрия, трометамина и цинка. Также могут быть образованы гемисоли кислот и оснований, например, гемисульфатные и гемикальциевые соли. Для обзора подходящих солей см. Handbook of Pharmaceutical Salts: Properties, Selection, and Use byStahl and Wermuth (Wiley-VCH, Weinheim, Germany, 2002). Фармацевтически приемлемые соли соединений формулы (I) или формулы (I') могут быть получены одним или более из трех способов:(i) взаимодействием соединения формулы (I) или формулы (I') с требуемой кислотой или основанием;(ii) удалением кислотно- или основно-лабильной защитной группы с подходящего исходного соединения формулы (I) или формулы (I') или размыканием кольца подходящего циклического исходного соединения, например, лактона или лактама, с применением требуемой кислоты или основания; или(iii) преобразованием одной соли соединения формулы (I) или формулы (I') в другую реакцией с подходящей кислотой или основанием или посредством подходящей ионообменной колонки. Все три реакции обычно выполняют в растворе. Полученную соль можно осадить и собрать путем фильтрации или можно восстановить путем выпаривания растворителя. Степень ионизации в полученной соли может изменяться от полностью ионизированного до почти неионизированного состояния. Соединения в соответствии с изобретением могут существовать как в сольватированной, так и в несольватированной формах. Термин "сольват" здесь используют для описания молекулярного комплекса,содержащего соединение в соответствии с изобретением и стехиометрическое количество одной или нескольких молекул фармацевтически приемлемого растворителя, например этанола. Термин "гидрат" используют, когда указанный растворитель представляет собой воду. В рамки изобретения включены такие комплексы, как клатраты, комплексы включения препаратноситель, где, в отличие от указанных выше сольватов, препарат и носитель присутствуют в стехиометрических или нестехиометрических количествах. Также включены комплексы препарата, содержащие два или более органических и/или неорганических компонента, которые могут быть в стехиометриче-4 010487 ских или нестехиометрических количествах. Получающиеся комплексы могут быть ионизированы, частично ионизированы или не ионизированы. Для обзора таких комплексов см. J. Pharm Sci., 64 (8), 1269-1288, by Haleblian (August 1975). Ниже все обращения к соединениям формулы (I) или формулы (I') включают обращения к их солям,сольватам и комплексам и к сольватам и комплексам их солей. Соединения в соответствии с изобретением включают соединения формулы (I) или формулы (I'),как определено выше, включая все их полиморфы и кристаллические формы, их пролекарства и изомеры(включая оптические, геометрические и таутомерные изомеры), как определено ниже, и меченые изотопами соединения формулы (I) или формулы (I'). Как обозначено, так называемые "пролекарства" соединений формулы (I) или формулы (I') также находятся в рамках изобретения. Таким образом, определенные производные соединений формулы (I) или формулы (I'), которые сами по себе могут не обладать или обладать небольшой фармакологической активностью при введении в тело или на тело, могут быть преобразованы в соединения формулы (I) или формулы (I'), обладающие требуемой активностью, например, путем гидролитического расщепления. Такие производные называются "пролекарствами". Дополнительная информация относительно применения пролекарств может быть найдена в Prodrugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T. Higuchi and W. Stella) и Bioreversible Carriers in Drug Design, Pergamon Press, 1987 (ed. E. B. Roche,American Pharmaceutical Association). Пролекарства в соответствии с изобретением могут, например, быть продуцированы путем замещения подходящих функциональных групп, присутствующих в соединениях формулы (I) или формулы (I'),определенными группами, известными специалистам в данной области как "прогруппы", как описано,например, в Design of Prodrugs by H. Bundgaard (Elsevier, 1985). Некоторые примеры пролекарств в соответствии с изобретением включают:(i) где соединение формулы (I) или формулы (I') содержит функциональную группу карбоновой кислоты (-COOH), ее сложный эфир, например, соединение, где водород функциональной группы карбоновой кислоты соединения формулы (I) или формулы (I') замещен (C1-C8)алкилом;(ii) где соединение формулы (I) или формулы (I') содержит спиртовую функциональную группу(-OH), ее простой эфир, например, соединение, где водород спиртовой функциональной группы соединения формулы (I) или формулы (I') замещен (С 1-С 6)алканоилоксиметилом; и(iii) где соединение формулы (I) или формулы (I') содержит функциональную группу первичного или вторичного амина (-NH2 или-NHR, где RH), ее амид, например, соединение, где, в зависимости от случая, один или оба водорода функциональной группы амина соединения формулы (I) или формулы (I') замещены (C1-С 10)алканоилом. Дополнительные примеры замещающих групп в соответствии с предшествующими примерами и примерами других типов пролекарства могут быть найдены в указанных выше ссылках. Кроме того, определенные соединения формулы (I) или формулы (I') могут сами по себе действовать как пролекарства других соединений формулы (I) или формулы (I'). Также в рамки изобретения включены метаболиты соединений формулы (I) или формулы (I'), т.е. соединения, образованные in vivo при введении лекарственного средства. Некоторые примеры метаболитов в соответствии с изобретением включают:(i) где соединение формулы (I) или формулы (I') содержит метильную группу, ее гидроксиметильное производное (-CH3-CH2OH);(ii) где соединение формулы (I) или формулы (I') содержит алкоксигруппу, ее гидрокси производное(iii) где соединение формулы (I) или формулы (I') содержит группу третичного амина, ее производное вторичного амина (-NRaRb-NHRa или -NHRb);(iv) где соединение формулы (I) или формулы (I') содержит группу вторичного амина, ее производное первичного амина (-NHRa-NH2);(v) где соединение формулы (I) или формулы (I') содержит фенильную группу, ее фенольное производное (-Ph-PhOH) и(vi) где соединение формулы (I) или формулы (I') содержит амидную группу, ее производное карбоновой кислоты (-CONRcRdCOOH). Соединения формулы (I) или формулы (I'), содержащие один или несколько асимметричных атомов углерода, могут существовать как два или более стереоизомера. Где структурные изомеры равноценны за счет низкого энергетического барьера, может встречаться таутомерная изомерия ("таутомерия"). Она может принимать форму протонной таутомерии в соединениях формулы (I) или формулы (I'), содержащих, например, имино, кето или оксимную группу или так называемой валентной таутомерии в соединениях, которые содержат ароматическую группу. Из этого следует, что отдельное соединение может демонстрировать более одного типа изомерии. В рамки настоящего изобретения включены все стереоизомеры, геометрические изомеры и таутомерные формы соединений формулы (I) или формулы (I'), включая соединения, демонстрирующие более-5 010487 одного типа изомерии и смеси одного или более из них. Также включены кислотно-аддитивные или основные соли, в которых противоион является оптически активным, например d-лактат или l-лизин, или рацемическим, например dl-тартрат или dl-аргинин. Обычные методики для получения/выделения отдельных знантиомеров включают хиральный синтез из подходящего оптически чистого предшественника или разделение рацемата (или рацемата соли или производного) с применением, например, хиральной жидкостной хроматографии высокого давления(ЖХВД). Альтернативно, рацемат (или рацемический предшественник) может быть подвергнут реакции с подходящим оптически активным соединением, например, спиртом, или, в случае, где соединение формулы (I) или формулы (I') содержит кислотную или основную группу, основанием или кислотой, такой как 1-фенилэтиламин или винная кислота. Получающаяся диастереоизомерная смесь может быть разделена с помощью хроматографии и/или дробной кристаллизации, и один или оба из диастереоизомеров могут быть преобразованы в соответствующий чистый энантиомер (энантиомеры) средствами, известными специалисту. Хиральные соединения в соответствии с изобретением (и их хиральные предшественники) могут быть получены в обогащенной энантиомерами форме с применением хроматографии, обычно ЖХВД, на асимметричной смоле с подвижной фазой, состоящей из углеводорода, обычно гептана или гексана, содержащей от 0 до 50% по объему изопропанола, обычно от 2 до 20%, и от 0 до 5% по объему алкиламина, обычно 0,1% диэтиламина. Концентрация элюата обеспечивает обогащенную смесь. Стереоизомерные конгломераты могут быть разделены обычными методиками, известными специалистам в данной области, см., например, Stereochemistry of Organic Compounds by E.L. Eliel and S.H.Wilen (Wiley, New York, 1994). Настоящее изобретение включает все фармацевтически приемлемые меченые изотопами соединения формулы (I) или формулы (I'), где один или несколько атомов замещены атомами, имеющими тот же номер атома, но массу атома или массовое число, отличное от массы атома или массового числа, которое преобладает в природе. Примеры изотопов, подходящих для включения в соединения в соответствии с изобретением,включают изотопы водорода, такие как 2H и 3H, углерода, такие как 11C, 13C и 14C, хлора, такие как 36Cl,фтора, такие как 18F, йода, такие как 123I и 125I, азота, такие как 13N и 15N, кислорода, такие как 15O, 17O и 18O, фосфора, такие как 32P и серы, такие как 35S. Определенные меченые изотопами соединения формулы (I) или формулы (I'), например, те, которые включают радиоактивный изотоп, являются полезными в лекарственном препарате и/или исследованиях распространения в субстратной ткани. В частности, радиоактивные изотопы тритий, т.е. 3H, и углерод-14, т.е. 14C, являются полезными для этой цели ввиду легкости их включения и доступных средств обнаружения. Замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2H, может обеспечить определенные терапевтические преимущества, следующие из большей метаболической стабильности, например,увеличение времени полужизни in vivo или требование уменьшенной дозировки, и, следовательно, может быть предпочтительным при некоторых обстоятельствах. Замещение испускающими позитроны изотопами, такими как 11C, 18F, 15O и 13N, может быть полезно в исследованиях Позитронной Эмиссионной Топографии (ПЭТ) для того, чтобы исследовать заполнение субстратного рецептора. По существу, меченые изотопами соединения формулы (I) или формулы (I') могут быть получены путем обычных методик, известных специалистам в данной области или процессов, аналогичных описанным в сопутствующих разделах примеров и получений с применением подходящего меченого изотопом реагента вместо немеченого реактива, используемого до этого. Фармацевтически приемлемые сольваты в соответствии с изобретением включают сольваты, в которых растворитель кристаллизации может быть изотопически замещенным, например, D2O, d6-ацетон,d6-диметилсульфоксид. Соединения по формуле (I) и (I') в соответствии с настоящим изобретением могут быть получены с помощью процедур, описанных в общих способах, представленных ниже, или помощью конкретных способов, описанных в разделе примеров и разделе получений, или путем обычных их модификаций. Настоящее изобретение также охватывает любой один или несколько этих способов для получения соединения формулы (I) или формулы (I'), в дополнение к любым используемым в них новым промежуточным соединениям. Соединения общей формулы (I), где А и R1 определены выше, могут быть получены в соответствии со схемой 1 реакции. Соединения общей формулы (II) являются либо коммерчески доступными, либо известными в литературе. PG представляет собой защитную группу, такую как бензил или аллил, и предпочтительно представляет собой бензил. Применение защитных групп описано в "Protective Groups in Organic Synthesis", Т. Greene and P. Wuts, 3rd edition, 1999, John Wiley and Sons. Соединения общей формулы (III) могут быть получены из соединений формулы (II) на стадии (i) способа: реакция с пирролидином в условиях Дина и Старка с сопутствующим удалением воды при повышенной температуре (например, 111-145 С) в подходящем растворителе, таком как толуол или ксилол,в течение 1-24 ч. Альтернативно соединение (III) может быть получено в условиях дегидратации, например, в присутствии дегидратирующего агента, такого как молекулярное сито или сульфат магния, в подходящем растворителе, таком как тетрагидрофуран. Стандартные условия включают 1 эквивалент соединения (II) и 1-1,5 эквивалентов (молярных) пирролидина в толуоле, нагреваемые с обратным холодильником в условиях Дина и Старка в течение 5 ч. Соединения общей формулы (V) могут быть получены из соединений общей формулы (III) на стадии (ii) способа: реакция с избытком соединения (IV) [J. Amer. Chem. Soc. 110 (12), 3965-9; 1988] при повышенной температуре (например, 111 С) в подходящем растворителе, таком как толуол, этанол, ксилол или тетрагидрофуран, в течение 1-24 ч. Стандартные условия включают 1 эквивалент соединения(III) и 1,5-2 эквивалента соединения (IV) в толуоле, нагреваемые с обратным холодильником и условия Дина и Старка в течение 8 ч. Альтернативно соединения формулы (V) могут быть получены из соединений формулы (III) путем двухстадийного способа, включающего последовательную обработку диэтилэтоксиметиленмалонатом в диоксане с обратным холодильником, NH4OAc и HCl с обратным холодильником (где PG = бензил, см. ЕР 588500), с последующим декарбоксилированием при повышенных температурах (например, 220240 С) в подходящем растворителе, таком как ди(этиленгликоль). Соединения общей формулы (VI) могут быть получены из соединений общей формулы (V) на стадии (iii) способа: реакция с подходящим агентом хлорирования, таким как оксихлорид фосфора/пентахлорид фосфора, необязательно в присутствии подходящего основания, такого как триэтиламин,и подходящего растворителя, такого как диоксан, при повышенных температурах (например, до 145 С) в течение 1-24 ч. Стандартные условия включают 1 эквивалент соединения (V) и 1 эквивалент пентахлорида фосфора в избытке оксихлорида фосфора, нагреваемые с обратным холодильником в течение 3 ч. Альтернативно, соединения общей формулы (VI) могут быть получены следующим образом: Соединения общей формулы (XVI) могут быть получены из соединений формулы (II) на стадии (xi) способа: реакция с ацетамидом в условиях Дина и Старка с сопутствующим удалением воды при повышенной температуре в присутствии подходящей кислоты, такой как пара-толуолсульфоновая кислота или трифторуксусная кислота, в подходящем растворителе, таком как ксилол или толуол, в течение 1-24 ч. Стандартные условия включают 1,0 эквивалент соединения (II), 1,0-3,0 эквивалента ацетамида и-7 010487 1,0-1,2 эквивалента пара-толуолсульфоновой кислоты в толуоле, нагретом при 50 С в течение 18 ч. Соединения общей формулы (VI) могут быть получены из соединений формулы (XVI) на стадии(xii) способа: реакция типа Вильсмейера-Хаака в присутствии подходящего реактива Вильсмейера, такого как N,N-диметилформамид или хлорид (хлорметилен)диметилиминия, и хлорангидрида фосфорной кислоты, необязательно в присутствии подходящего растворителя, такого как дихлорметан, при повышенной температуре в течение 6-72 ч. Стандартные условия включают 1,0 эквивалент соединения (XVI),1,0-1,2 эквивалента N,N-диметилформамида и избыток оксихлорида фосфора, нагреваемые при 75 С в течение 6 ч. Соединения общей формулы (VII) могут быть получены из соединения (V) на стадии (iv)[а] способа: реакция Митсунобу с подходящим спиртом A-OH в присутствии подходящего фосфина, такого как трин бутилфосфин или трифенилфосфин и подходящего азосоединения, такого как диэтилазокарбоксилат или 1'1'-азобис(N,N-диметилформамид), в подходящем растворителе, таком как толуолтетрагидрофуран или N,N-диметилформамид, при повышенной температуре в течение 1-48 ч. Стандартные условия включают 1 эквивалент соединения (V), 1,0-1,2 эквивалента A-OH, 1,0-1,2 эквивалента три-нбутилфосфина и 1,01,2 эквивалента 1'1'-азобис (N,N-диметилформамида) в толуоле, нагреваемые при 85 С в течение 18 ч. Предпочтительно, соединения общей формулы (VII) могут быть получены из соединений общей формулы (VI) на стадии (iv)[b] способа: реакция со спиртом A-OH в присутствии подходящего основания,такого как гидрид натрия или тбутоксид калия в подходящем растворителе, таком как тетрагидрофуран или N,N-диметилформамид при повышенной температуре (например, 67 С) в течение 12-24 ч. Стандартные условия включают 1,0 эквивалент соединения (VI), 1-2 эквивалента тбутоксида калия и 1,0-1,5 эквивалента спирта A-OH, в тетрагидрофуране, нагреваемые с обратным холодильником в течение 18 ч. Соединения формулы (VIII) могут быть получены из соединений общей формулы (VII) на стадии(v) способа: снятие защитной группы с соединения (VII) с применением стандартных методологий, как описано в "Protecting Groups in Organic Synthesis" by T.W. Greene and P. Wutz (см. выше). Когда PG представляет собой бензил, стандартные условия включают 1,0 эквивалент соединения (VII), 5,0 эквивалентов формиата аммония и 10% (мас./мас.) Pd/C (катализатора), нагреваемые с обратным холодильником в этаноле, в течение 1 ч. Соединения формулы (I) могут быть получены из соединений формулы (VIII) на стадии (vi)[a] способа: реакция с галогенидом R1X (где R1 определен выше и X представляет собой галоген и, предпочтительно, хлор или бром) в присутствии подходящего основания, такого как тбутоксид натрия или триэтиламин и подходящей каталитической системы, такой как Pd2(dba)3 с BINAP, в подходящем растворителе,таком как тбутанол, нагреваемые при повышенной температуре (например, 110 С) в микроволновом реакционном нагревателе. Стандартные условия включают 1 эквивалент соединения (VIII), 1-3 эквивалентаR1-X, 1,2-3,6 эквивалента тбутоксида натрия, 5-15 моль.% Pd2(dba)3 и 10-30 моль.% BINAP в тбутаноле при 110 С в течение 0,5-3,0 ч. Альтернативно, соединения формулы (I) могут быть получены из соединений формулы (VIII) на стадии (vi)[b] способа: реакция с галогенидом R1X, (где R1 определен выше и X представляет собой галоген и предпочтительно представляет собой хлор или бром), необязательно в присутствии подходящего основания, такого как карбонат калия, тбутоксид натрия или карбонат натрия, в подходящем растворителе, таком как хлорбензол, диметилсульфоксид или тбутанол и NMP, в 25-150 С в течение 1-48 ч. Стандартные условия включают 1 эквивалент соединения (VIII), 1-1,5 эквивалента R2X и 1-1,5 эквивалента карбоната калия в хлорбензоле и NMP, нагреваемые с обратным холодильником в течение 24-48 ч. Соединения общей формулы (I'), где А и R1 определены выше, могут быть получены в соответствии со схемой 2 реакции. Соединение (IX) может быть получено по аналогии со способом L. Estel и др. (J. Org. Chem. 53 (12),2740-4; 1988). Соединение (X) может быть получено из соединения (IX) на стадии (vii) способа: гидролиз с подходящей кислотой, такой как серная кислота или соляная кислота, в подходящем растворителе, таком как вода или метанол, при повышенной температуре (например, 100 С) в течение 1-6 ч. Стандартные условия включают 1 эквивалент соединения (IX) в избытке разбавленной серной кислоты, нагреваемые с обратным холодильником в течение 1 ч. Соединение (XI) может быть получено из соединения (X) на стадии (viii) способа: способ, аналогичный таковому от Т. Sakamoto и др. (Chem. and Pharm. Bull. 33(11) 4764-8; 1985). Стандартные условия включают 1,0 эквивалент соединения (X), 1,2 эквивалента этилакрилата, 10 моль.% ацетата палладия,20 моль.% три-(О-толил)фосфина, и 1-1,5 эквивалента триэтиламина в N,N-диметилформамиде при 80 С в течение 3 ч. Соединение (XII) может быть получено из соединения (XI) на стадии (ix) способа, как описано вChem. and Pharm. Bull. 33(11), 4764-8; 1985. Стандартные условия включают 1 эквивалент соединения(XI) и 4 эквивалента этилата натрия в этаноле, нагреваемые с обратным холодильником в течение 1 ч. Соединения общей формулы (XIII) могут быть получены из соединения (XII) на стадии (х) способа: присоединение защитной группы к атому N с помощью подходящего агента защиты, такого как аллилбромид или бензилбромид, с использованием стандартной методологии, как описано в "Protecting Groupsin Organic Synthesis" by T.W. Greene and P. Wutz, с последующим восстановлением с помощью восстановителя, такого как боргидрид натрия, гидрид диизобутиламмония или алюмогидрид лития. Стандартные условия включают 1 эквивалент соединения (XII) и 1-1,5 эквивалента бензилбромида в этаноле, нагреваемые с обратным холодильником в течение 1-5 ч, с последующим добавлением 4,0-6,0 эквивалентов боргидрида натрия при 0-4 С в течение 0-60 мин. Соединения общей формулы (XIV) могут быть получены из соединений общей формулы (XIII) на стадии (iv) способа, как описано в схеме 1. Соединения общей формулы (XV) могут быть получены из соединений общей формулы (XIV) на стадии (v) способа, как описано в схеме 1. Соединения общей формулы (I) могут быть получены из соединений общей формулы (XV) на стадии (vi)[a] способа, как описано в схеме 1. Все приведенные выше реакции и получения новых исходных материалов с применением в описанных выше способах представляют собой обычные и подходящие реактивы и условия реакции для их выполнения или получения, а также процедуры для выделения требуемых продуктов известны специалистам в данной области с обращением к прецедентам из литературных источников и прилагающимся примерам и получениям. Соединения в соответствии с изобретением, предназначенные для фармацевтического применения,-9 010487 могут быть введены в виде кристаллических или аморфных продуктов. Они могут быть получены, например, в виде твердых цилиндров, порошков или пленок такими способами, как осаждение, кристаллизация, сублимационная сушка, сушка путем распыления или сушка путем выпаривания. Для этой цели может быть использована микроволновая или радиочастотная сушка. Они могут быть введены отдельно или в комбинации с одним или несколькими другими соединениями в соответствии с изобретением или в комбинации с одним или несколькими другими препаратами(или в виде любого их сочетания). По существу, их вводят в виде препарата вместе с одним или несколько фармацевтически приемлемыми наполнителями. Термин "наполнитель" используется в настоящем изобретении для описания любого ингредиента кроме соединения (соединений) в соответствии с изобретением. Выбор наполнителя в большой степени зависит от таких факторов, как конкретный способ введения, действие инертного наполнителя на растворимость и стабильность и природа лекарственной формы. Фармацевтические композиции, подходящие для доставки соединений в соответствии с настоящим изобретением, и способы их получения будут очевидны специалистам в данной области. Такие композиции и способы для их получения могут быть найдены, например, в Remington's Pharmaceutical Sciences,19th Edition (Mack Publishing Company, 1995). Соединения в соответствии с изобретением могут быть введены перорально. Пероральное введение может подразумевать проглатывание, так, чтобы соединение поступило в желудочно-кишечный тракт,или может быть использовано щечное или подъязычное введение, за счет которого соединение поступает в кровоток непосредственно изо рта. Препараты, подходящие для перорального введения, включают твердые препараты, такие как таблетки, капсулы, содержащие твердые частицы, жидкости, или порошки, пастилки (включая заполненные жидкостью), жевательные препараты, мульти- и наночастицы, гели, твердый раствор, липосому, пленки,суппозитории, спреи и жидкие препараты. Жидкие препараты включают суспензии, растворы, сиропы и эликсиры. Такие препараты могут быть использованы в качестве наполнителей в мягких или твердых капсулах и обычно содержат носитель, например воду, этанол, полиэтиленгликоль, пропиленгликоль, метилцеллюлозу, или подходящее масло и один или несколько эмульгаторов и/или суспендирующих агентов. Жидкие препараты также могут быть получены путем разбавления твердого вещества, например, из пакета. Соединения в соответствии с изобретением также могут быть использованы в быстрорастворимой,быстрорасщепляемой лекарственной форме, такой как описанные в Expert Opinion in Therapeutic Patents,11 (6), 981-986, by Liang and Chen (2001). Для лекарственных форм таблеток, в зависимости от дозы, лекарственное средство может составлять от 1 до 80 мас.% лекарственной формы, чаще от 5 до 60 мас.% лекарственной формы. В целом, в дополнение к лекарственному средству, таблетки содержат дезинтегрант. Примеры дезинтегрантов включают крахмалгликолят натрия, карбоксиметилцеллюлозу натрия, карбоксиметилцеллюлозу кальция,кроскармеллозу натрия, кросповидон, поливинилпирролидон, метилцеллюлозу, микрокристаллическую целлюлозу, гидроксипропилцеллюлозу, замещенную низшим алкилом, крахмал, пептизированный крахмал и альгинат натрия. В целом, дезинтегрант составляет от 1 до 25 мас.%, предпочтительно от 5 до 20 мас.% лекарственной формы. В целом, связывающие вещества используют для придания когезионных качеств препарату таблетки. Подходящие связывающие вещества включают микрокристаллическую целлюлозу, желатин, сахар,полиэтиленгликоль, природную и синтетическую камедь, поливинилпирролидон, пептизированный крахмал, гидроксипропилцеллюлозу и гидроксипропилметилцеллюлозу. Таблетки могут также содержать разбавители, такие как лактоза (моногидрат, высушенный путем распыления моногидрат, безводную и т.п.), маннит, ксилит, декстроза, сахароза, сорбит, микрокристаллическая целлюлоза, крахмал и двуосновный дигидрат фосфата кальция. Таблетки могут также необязательно содержать поверхностно-активные вещества, такие как лаурилсульфат натрия и полисорбат 80, и вещества, способствующие скольжению, такие как диоксид кремния и тальк. Если присутствуют, поверхностно-активные вещества могут включать от 0,2 до 5 мас.% таблетки, и смазывающие вещества могут составлять от 0,2 до 1 мас.% таблетки. В целом, таблетки также содержат смазывающие вещества, такие как стеарат кальция, стеарат цинка, стеарилфумарат натрия и смеси стеарата магния с лаурилсульфатом натрия. В целом, смазывающие вещества составляют от 0,25 до 10 мас.%, предпочтительно от 0,5 до 3 мас.% таблетки. Другие возможные ингредиенты включают антиоксиданты, красители, ароматизаторы, консерванты и вещества, исправляющие вкус. Иллюстративные таблетки содержат до приблизительно 80% лекарственного препарата, от приблизительно 10 мас.% до приблизительно 90 мас.% связывающих веществ, от приблизительно 0 мас.% до приблизительно 85 мас.% разбавителей, приблизительно от 2 мас.% до приблизительно 10 мас.% дезинтегранта и от приблизительно 0,25 мас.% до приблизительно 10 мас.% смазывающих веществ. Смеси для таблеток могут быть спрессованы непосредственно или валиком для образования таблеток. Альтернативно, смеси для таблеток или части смесей могут быть гранулированными во влажном,- 10010487 сухом или расплавленном состоянии, могут затвердевать после плавления или могут быть спрессованы перед изготовлением таблеток. Конечный препарат может содержать один или несколько слоев и может быть покрытым или непокрытым; кроме того, он может быть инкапсулированным. Получение таблеток обсуждается в Pharmaceutical Dosage Forms: Tablets, Vol. 1, by H. Lieberman иL. Lachman (Marcel Dekker, New York, 1980). Годные к потреблению пероральные пленки для применения людьми или в ветеринарных целях обычно представляют собой пластичные водорастворимые или набухающие в воде лекарственные формы в виде тонкой пленки, которые могут быстро расщепляться или быть мукоадгезивными и обычно содержат соединение формулы (I) или формулы (I'), пленкообразующий полимер, связывающее вещество, растворитель, увлажнитель, пластификатор, стабилизатор или эмульгатор, модификатор вязкости и растворитель. Некоторые компоненты препарата могут выполнить более одной функции. Соединение формулы (I) или формулы (I') может быть водорастворимым или нерастворимым. Водорастворимое соединение обычно включает от 1 до 80 мас.%, чаще от 20 до 50 мас.% растворенных веществ. Менее растворимые соединения могут содержать большую долю композиции, обычно до 88 мас.% растворенных веществ. Альтернативно, соединение формулы (I) или формулы (I') может быть в форме гранул - мультичастиц. Пленкообразующий полимер может быть выбран из естественных полисахаридов, белков или синтетических гидроколлоидов и обычно содержится в диапазоне от 0,01 до 99 мас.%, чаще в диапазоне от 30 до 80 мас.%. Другие возможные ингредиенты включают антиоксиданты, красители, ароматизаторы и усилители вкуса, консерванты, стимуляторы слюноотделения, охлаждающие средства, дополнительные растворители (включая масла), смягчающие средства, наполнители, вещества, препятствующие образованию пены, поверхностно-активные вещества и вещества, исправляющие вкус. Пленки в соответствии с изобретением обычно готовят путем сушки выпариванием тонких водных пленок на поверхности легко отслаивающегося основания или бумаги. Это может быть проделано в сушильном шкафу или туннельной печи, обычно в сушилке, комбинированной с установкой для нанесения покрытий, или с помощью сублимационной сушки или путем помещения в вакуум. Твердые препараты для перорального введения могут быть получены для обеспечения непосредственного и/или модифицированного высвобождения. Препараты для модифицированного высвобождения включают запаздывающее, задержанное, импульсное, управляемое, нацеленное и запрограммированное высвобождение. Подходящие препараты для модифицированного высвобождения для целей изобретения описаны в патенте США 6106864. Детали других подходящих технологий высвобождения, такие как высокоэнергетические дисперсии и осмотические и покрытые частицы, следует искать в Pharmaceutical Technology On-line, 25(2), 1-14, by Verma et al. (2001). Применение жевательной резинки, для обеспечения управляемого высвобождения описано в WO 00/35298. Соединения в соответствии с изобретением также могут быть введены непосредственно в кровоток,в мышцу или во внутренний орган. Подходящие средства для парентерального введения включают внутривенное, внутриартериальное, интраперитонеальное, интратекальное, внутрижелудочковое, интрауретральное, надчревное, внутричерепное, внутримышечное и подкожное. Подходящие устройства для парентерального введения включают инъекторы с иглой (включая микроиглу), инъекторы без иглы и методики вливания. Парентеральные препараты обычно представляют собой водные растворы, которые могут содержать инертные наполнители, такие как соли, углеводы и буферные вещества (предпочтительно до pH от 3 до 9), но, для некоторых приложений, они могут быть более подходящим образом получены в виде стерильного неводного раствора или в высушенной форме, которую используют в сочетании с подходящим носителем, таким как стерильная апирогенная вода. Получение парентеральных препаратов в стерильных условиях, например, путем лиофилизации,может быть легко обеспечено с применением стандартных фармацевтических методик, известных специалистам в данной области. Растворимость соединений формулы (I) или формулы (I'), используемых в получении парентеральных растворов, может быть увеличена при помощи подходящих методик получения, таких как внесение усиливающих растворимость веществ. Препараты для парентерального введения могут быть получены для обеспечения непосредственного и/или модифицированного высвобождения. Препараты для модифицированного высвобождения включают запаздывающее, задержанное, импульсное, управляемое, нацеленное и запрограммированное высвобождение. Таким образом, соединения в соответствии с изобретением могут быть получены в виде твердого вещества, полутвердого вещества, или тиксотропной жидкости для введения в качестве внутреннего депо, обеспечивающего модифицированное высвобождение активного соединения. Примеры таких препаратов включают покрытые лекарственным препаратом стенты и микросферы сополимера dlмолочной и гликолевой кислот (PGLA). Соединения изобретения можно также наносить местно на кожу или слизистую оболочку, т.е. дер- 11010487 мально или трасдермально. Типичные препараты для этой цели включают гели, гидрогели, лосьоны, растворы, кремы, мази, присыпки, повязки, пены, пленки, кожные пластыри, пластинки, имплантанты, губки, волокна, бандажи и микроэмульсии. Также можно использовать липосомы. Типичные носители включают спирт, воду, минеральное масло, вазелиновое масло, белый вазелин, глицерин, полиэтиленгликоль и пропиленгликоль. Могут быть включены усилители проникновения - см., например, J. Pharm.Sci., 88 (10), 955-958, by Finnin and Morgan (October 1999). Другие средства местного нанесения включают доставку путем инъекции с помощью электропорации, ионтофореза, фонофореза, сонофореза и микроиглы или без иглы (например, Powderject, Bioject и т.д.). Препараты для местного введения могут быть получены для обеспечения непосредственного и/или модифицированного высвобождения. Препараты для модифицированного высвобождения включают запаздывающее, задержанное, импульсное, управляемое, нацеленное и запрограммированное высвобождение. Соединения в соответствии с изобретением можно также вводить через нос или с помощью ингаляции, обычно в форме сухого порошка (либо отдельно, в виде смеси, например, сухой смеси с лактозой,либо в виде смешанных составляющих частиц, например, смешанный с фосфолипидами, такими как фосфатидилхолин) из ингалятора с сухим порошком или в виде аэрозольного спрея из резервуара под давлением, насоса, спрея, распылителя (предпочтительно, распылителя с применением электрогидродинамики для получения мелкодисперсного аэрозоля), или небулайзера, с применением или без применения подходящего сжатого газа, такого как 1,1,1,2-тетрафтороэтан или 1,1,1,2,3,3,3-гептафторпропан. Для введения через нос порошок может содержать биоадгезивный агент, например, хитозан или циклодекстрин. Резервуар под давлением, насос, спрей, распылитель или небулайзер содержат раствор или суспензию соединения (соединений) в соответствии с изобретением, содержащий, например, этанол, водный этанол или подходящий альтернативный агент для диспергирования, растворения или продления высвобождения активного компонента, сжатый газ (газы) в качестве растворителя и необязательное поверхностно-активное вещество, такое как сорбитан триолеат, олеиновая кислота или олигомолочная кислота. До применения в препарате сухого порошка или суспензии продукт лекарственного препарата микронизируют до размера, подходящего для доставки путем ингаляции (обычно меньше 5 мкм). Это может быть достигнуто с помощью любого подходящего способа измельчения, такого как перемалывание в спиральной струе, перемалывание в струе кипящего слоя, надкритическая обработка жидкости для образования наночастиц, гомогенизация под высоким давлением или сушка путем распыления. Капсулы (например, изготовленные из желатина или гидроксипропилметилцеллюлозы), ячейки и картриджи для применения в ингаляторе или инсуффляторе могут быть получены для содержания порошковой смеси соединения в соответствии с изобретением, подходящей порошковой основы, такой как лактоза или крахмал и модификатора эффективности, такого как 1-лейцин, маннит или стеарат магния. Лактоза может быть безводной или в форме моногидрата, последняя является предпочтительной. Другие подходящие инертные наполнители включают декстран, глюкозу, мальтозу, сорбит, ксилит, фруктозу,сахарозу и трегалозу. Подходящий препарат раствора для применения в распылителе с применением электрогидродинамики для получения мелкодисперного аэрозоля может содержать от 1 мкг до 20 мг соединения в соответствии с изобретением в каждом впрыске, и объем впрыска может изменяться от 1 до 100 мкл. Типичный препарат может содержать соединение формулы (I) или формулы (I'), пропиленгликоль, стерилизованную воду, этанол и хлорид натрия. Альтернативные растворители, которые могут быть использованы вместо пропиленгликоля, включают глицерин и полиэтиленгликоль. К данным препаратам, предназначенным для ингаляционного/внутриносового введения, в соответствии с изобретением могут быть добавлены подходящие ароматизаторы, такие как ментол и левоментол, или посластители, такие как сахарин или сахарин натрия. Препараты для ингаляционного/внутриносового введения могут быть получены для обеспечения непосредственного и/или модифицированного высвобождения с применением, например, PGLA. Препараты для модифицированного высвобождения включают запаздывающее, задержанное, импульсное,управляемое, нацеленное и запрограммированное высвобождение. В случае сухих порошковых ингаляторов и аэрозолей, стандартная доза определяется с помощью клапана, который обеспечивает измеренное количество. Стандартные дозы в соответствии с изобретением обычно распределены так, чтобы обеспечить введение измеренной дозы или "впрыск", содержащий от 1 до 4000 мкг соединения формулы (I) или (I'). Полная суточная доза обычно находится в диапазоне от 1 мкг до 20 мг, которая может быть введена в виде однократной дозы или, чаще, в виде разделенных доз в течение дня. Соединения в соответствии с изобретением можно вводить ректально или вагинально, например, в форме свечи, пессария или клизмы. Масло какао представляет собой традиционную основу для свечи, но как подходящие можно использовать различные варианты. Препараты для ректального/вагинального введения могут быть получены для обеспечения непо- 12010487 средственного и/или модифицированного высвобождения. Препараты для модифицированного высвобождения включают запаздывающее, задержанное, импульсное, управляемое, нацеленное и запрограммированное высвобождение. Соединения в соответствии с изобретением можно также непосредственно наносить на глаз или вводить в ухо, обычно в форме капель микронизированной суспензии или раствора в изотоническом,стерильном солевом растворе с установленным pH. Другие препараты, подходящие для глазного и ушного введения, включают мази, биоразлагаемые (например, абсорбируемые губки геля, коллаген) и небиоразлагаемые (например, силикон) имплантанты, пластинки, линзы и дисперсные или везикулярные системы, такие как ниосомы или липосомы. Наряду с консервантом, таким как хлорид бензалкония, может быть включен полимер, такой как сетчатая полиакриловая кислота, поливиниловый спирт, гиалуроновая кислота, целлюлозный полимер, например, гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза или метилцеллюлоза, или гетерополисахаридный полимер, например, гелановая камедь. Такие препараты также можно доставлять с помощью ионтофореза. Препараты для глазного/ушного введения могут быть получены для обеспечения непосредственного и/или модифицированного высвобождения. Препараты для модифицированного высвобождения включают запаздывающее, задержанное, импульсное, управляемое, нацеленное и запрограммированное высвобождение. Соединения в соответствии с изобретением могут быть комбинированы с растворимыми макромолекулярными объектами, такими как циклодекстрин и его подходящие производные или полимеры, содержащие полиэтиленгликоль, для улучшения растворимости, скорости растворения, исправления вкуса,биопригодности и/или стабильности для применения в любом из указанных выше способов введения. Например, обнаружено, что комплексы циклодекстрина и лекарственного препарата, по существу,пригодны для большинства лекарственных форм и путей введения. Можно использовать как комплексы включения, так и не комплексы включения. В качестве альтернативы прямому комплексообразованию с лекарственным препаратом, циклодекстрин можно использовать в качестве вспомогательной добавки,т.е. в качестве носителя, разбавителя или солюбилизатора. Обычно для данных целей используют альфа-,бета- и гамма-циклодекстрины, примеры которых могут быть найдены в международных заявках на патент номера WO 91/11172, WO 94/02518 и WO 98/55148. Поскольку может потребоваться применение сочетания активных соединений, например, с целью лечения конкретного заболевания или состояния, в рамках настоящего изобретения две или больше фармацевтических композиции, по меньшей мере одна из которых содержит соединение в соответствии с изобретением, могут быть удобным образом комбинированы в форме набора, подходящего для совместного введения композиций. Таким образом, набор в соответствии с изобретением включает две или больше отдельные фармацевтические композиции, по меньшей мере одна из которых содержит соединение формулы (I) или формулы (I') в соответствии с изобретением, и средства для раздельного хранения указанных композиции,такие как разделенная емкость, разделенный пакет из фольги. Примером такого набора является известная блистерная упаковка, используемая для расфасовки таблеток, капсул и т.п. Набор в соответствии с изобретением, в частности, подходит для введения различных лекарственных форм, например, пероральной и парентеральной, для введения раздельных композиций в различные интервалы дозировки, или для титрования раздельных композиций по отношению друг к другу. Для того чтобы способствовать совместимости, набор обычно содержит указания для введения и может быть снабжен так называемой памяткой. Для введения людям, полная суточная доза соединений в соответствии с изобретения обычно находится в диапазоне между 0,001 и 2000 мг, обязательно в зависимости от способа введения. Например, для перорального введения может потребоваться полная суточная доза от 1 до 2000 мг, в то время как для внутривенной дозы может потребоваться только от 0,01 до 100 мг. Полную суточную дозу можно вводить в виде единичной или разделенных доз и, по усмотрению врача, выходить за пределы обычного диапазона, приведенного в данном изобретении. Данные дозировки исходят из данных для среднестатистического человека, имеющего вес приблизительно от 60 до 70 кг. Врач легко сможет определить дозы для индивидуумов, вес которых находится вне этого диапазона, например, для младенцев и пожилых людей. Во избежание неопределенности, в данном изобретении указания на "лечение" включают указания на терапевтическое, облегчающее и профилактическое лечение. В соответствии с другим вариантом выполнения настоящего изобретения соединения по формуле(I) или (I'), или их фармацевтически приемлемые соли, производные формы или композиции, также можно использовать в виде комбинации с одним или несколькими дополнительными терапевтическими агентами, которые совместно вводят пациенту для получения какого-либо частного требуемого терапевтического результата. Второй и далее дополнительные терапевтические агенты могут также представлять собой соединение формулы (I) или (I'), или его фармацевтически приемлемую соль, производные формы или композиции, или один или несколько лигандов рецептора H3 гистамина, известные в уровне техники. Чаще, второй и далее терапевтические агенты выбирают из другого класса терапевтических агентов.- 13010487 Предполагается, что в используемом в настоящем изобретении смысле термины "совместное введение", "совместно введенный" и "в сочетании с" в отношении соединений формулы (I) или (I') и одного или нескольких других терапевтических агентов обозначают и имеют указанный смысл и включают следующее: одновременное введение такого сочетания соединения (соединений) формулы (I) или (I') и терапевтического агента (агентов) пациенту, которому требуется лечение, когда такие компоненты получены вместе в единой лекарственной форме, которая высвобождает указанные компоненты, главным образом,одновременно указанному пациенту; главным образом, одновременное введение такого сочетания соединения (соединений) формулы (I) или (I') и терапевтического агента (агентов) пациенту, которому требуется лечение, когда такие компоненты получены отдельно друг от друга в раздельных лекарственных формах, которые указанный пациент принимает, главным образом, одновременно, после чего указанные компоненты высвобождаются,главным образом, одновременно указанному пациенту; последовательное введение такого комбинированного соединения (соединений) формулы (I) или (I') и терапевтического агента (агентов) пациенту, которому требуется лечение, когда такие компоненты получены отдельно друг от друга в раздельных лекарственных формах, которые указанный пациент принимает последовательно со значительным временным интервалом между каждым введением, после чего указанные компоненты высвобождаются, главным образом, в разное время указанному пациенту; и последовательное введение такого сочетания соединения (соединений) формулы (I) или (I') и терапевтического агента (агентов) пациенту, которому требуется лечение, когда такие компоненты получены вместе в единой лекарственной форме, которая высвобождает указанные компоненты контролируемым образом, после чего указанный пациент вводит их одновременно, последовательно и/или с наложением,применяемый в одно и то же и/или в разное время, где каждую часть можно вводить либо одним и тем же, либо различными путями. Подходящие примеры других терапевтических агентов, которые можно использовать в сочетании с соединением (соединениями) формулы (I) или (I'), или их фармацевтически приемлемыми солями, производными формами или композициями, включают, но ни в коем случае не ограничены ими: антагонисты рецептора H1 гистамина, например, лоратидин, деслоратидин, фексофенадин и цетиризин,антагонисты рецептора Н 4 гистамина,антагонисты рецептора Н 2 гистамина,антагонисты лейкотриена, включая антагонисты LTB4, LTC4, LTD4 и LTE4, в частности, Монтелукаст,ингибиторы фосфодиэстеразы, такие как ингибиторы PDE4 или ингибиторы PDE5,ингибиторы обратного захвата нейромедиаторов, например, флуоксетин, сетралин, пароксетин,зипрасидон,ингибиторы 5-липооксигеназы (5-LO) или антагонисты активирующего белка 5-липооксигеназы(FLAP),вазоконстрикторные симпатомиметические агенты-агонисты 1- и 2-адреномиметика для противоотечного применения,антагонисты мускаринового М 3 рецептора или антихолинергические агенты,агонисты 2-адреномиметика,теофиллин,хромогликат натрия,ингибиторы СОХ-1 (NSAID) и селективные ингибиторы СОХ-2,пероральные глюкокортикостероиды или в виде ингаляций,моноклональные антитела, активные против эндогенных возбудителей воспалительных процессов,агенты противоопухолевого фактора некроза (анти-TNF-),ингибиторы адгезивных молекул, включая антагонисты VLA-4,антагонисты рецептора кинина-B1 - и -В 2,иммуносупрессивные агенты,ингибиторы металлопротеаз (ММР) матрикса,антагонисты рецептора NK1, NK2 и NK3 тахикинина,ингибиторы эластазы,агонисты рецептора А 2 а аденозина,ингибиторы урокиназы,соединения, действующие на рецепторы допамина, например, агонисты D2,модуляторы пути NF, например, ингибиторы IKK,агенты, которые можно классифицировать как муколитики или средство от кашля,антибиотики,модуляторы пути сигнала цитокина, такие как р 38 МАР-киназа, syk-киназа или ингибитор JAK- 14010487 киназы,ингибиторы HDAC и ингибиторы PI3-киназы. В соответствии с настоящим изобретением предпочтительным является сочетание соединений формулы (I) или (I') с антагонистами рецептора H1 гистамина (например, лоратидином, деслоратидином,фексофенадином и цетиризином), антагонистами рецептора Н 4 гистамина, антагонистами рецептора Н 2 гистамина, антагонистами лейкотриена, включая антагонисты LTB4, LTC4, LTD4 и LTE4 (в частности,монтелукаст), ингибиторами фосфодиэстеразы PDE4 и ингибиторами обратного захвата нейромедиаторов (например, флуоксетином, сетралином, пароксетином, зипрасидоном). Соединения формулы (I) или (I') могут взаимодействовать с рецептором H3 и, таким образом, иметь широкий спектр терапевтических приложений, как описано ниже, в силу важной роли, которую рецепторH3 играет в физиологии всех млекопитающих. В соответствии с данным изобретением предполагается,что лиганды H3 включают антагонисты, агонисты и обратные агонисты рецептора H3. Для предпочтительных показаний, которые лечат в соответствии с изобретением, считается, что антагонисты H3 являются самыми подходящими. В связи с этим, дальнейший аспект настоящего изобретения относится к соединениям формулы (I) или (I') или их фармацевтически приемлемым солям, производным формам или композициям для применения в лечении заболеваний, нарушений и состояний, в которых участвует рецептор H3. Более конкретно, настоящее изобретение также касается соединений формулы (I) или (I') или их фармацевтически приемлемых солей, производных форм для применения в лечении заболеваний, нарушений, и состояний,выбранных из группы, состоящей из заболеваний центральной нервной системы: расстройства сна, мигрень, психотические расстройства, эпилепсия, болезни, связанные с дефицитом познавательных способностей, такие как болезнь Альцгеймера или умеренное ухудшение познавательных способностей, депрессия, расстройства настроения, шизофрения, синдром дефицита внимания с гиперактивностью (СДВГ), ожирение,респираторных заболеваний, таких как астма, и аллергического ринита. Соединения формулы (I) или (I') в соответствии с изобретением, в частности, подходят для лечения аллергии, вызванных аллергией реакций дыхательных путей, аллергического ринита, вирусного ринита,неаллергического ринита, круглогодичного и сезонного ринита, заложенности носа, аллергической заложенности носа. Еще один дополнительный аспект настоящего изобретения также относится к применению соединений формулы (I) или (I'), или их фармацевтически приемлемых солей, производных форм или композиций для производства лекарственного препарата, представляющего собой лиганд H3. В частности, настоящее изобретение касается применения соединений формулы (I) или (I') или их фармацевтически приемлемых солей, производных форм или композиций для производства лекарственного препарата для лечения заболеваний и/или состояний, обусловленных H3, в частности заболеваний и/или состояний,приведенных выше. Как следствие, настоящее изобретение обеспечивает представляющий особенный интерес способ для лечения млекопитающего, включая человека, эффективным количеством соединения формулы (I) или (I') или его фармацевтически приемлемой соли, производной формы или композиции. Точнее, настоящее изобретение обеспечивает представляющий особенный интерес способ для лечения заболеваний и/или состояний, обусловленных H3 у млекопитающего, включая человека, в частности заболеваний и/или состояний, приведенных выше, включающий введение указанному млекопитающему эффективного количества соединения формулы (I) или (I'), его фармацевтически приемлемых солей и/или производных форм. Следующие примеры поясняют получение соединений формулы (I) и (I') в соответствии с настоящим изобретением. Примеры Спектры ядерного магнитного резонанса (ЯМР) 1 Н во всех случаях соответствовали предложенным структурам. Характеристические значения химического сдвигаданы в частях на миллион с напряженностью поля ниже значений для тетраметилсилана с применением обычных сокращений для обозначения главных пиков: например, s - синглет; d - дублет; t - триплет; q - квартет; m - мультиплет; br - широкий. Массспектры (m/z) регистрировали с применением либо электрораспылительной ионизации (ESI), либо химической ионизации при атмосферном давлении (APCI). Использовали следующие сокращения: Pd2(dba)3 обозначает трис(дибензилиденацетон)дипалладий,BINAP означает 2,2'-бис(дифенилфосфино)-1,1'-бинафтил, TMEDA означает N,N,N'N'-тетраметилэтилендиамин, NMP означает 1-метил-2-пирролидинон. "Аммиак" означает концентрированный раствор аммиака в воде, имеющий удельный вес 0,88. Где использовали тонкослойную хроматографию (ТСХ),подразумевается ТСХ на силикагеле с применением пластин с силикагелем 60 F254, Rf означает длину отрезка, пройденного соединением, разделенную на длину отрезка, пройденного фронтом растворителя на пластине для ТСХ. Микроволновое оборудование представляет собой Personal Chemistry Emrys Lib- 15010487 Продукт получения 16 (80 мг, 0,31 ммоль) и 2-бромпиримидин (49 мг, 0,31 ммоль) смешивали в трет-бутаноле (8 мл) и перемешивали при 25 С в течение 12 ч. Затем температуру увеличили до 45 С, и реакционную смесь перемешивали в течение 7 ч с добавлением по истечении 3 ч дополнительного количества 2-бромпиримидина (5 мг). Затем растворитель выпаривали при пониженном давлении, и остаток очищали с помощью колоночной хроматографии на силикагеле с элюцией этилацетатом:пентаном:0,88 аммиаком, от 20:80:1 до 60:40:1, с последующим добавлением дихлорметана:метанола:0,88 аммиака, от 100:0:1 до 90:10:1, для получения белого твердого вещества. Перекристаллизация твердого вещества из циклогексана давала соединение в соответствии с заголовком в виде белого твердого вещества с 24% выходом, 25 мг. 1 Н ЯМР (CDCl3, 400 МГц) : 1,70-1,90 (м, 4 Н), 2,00-2,10 (м, 2 Н), 2,47-2,75 (м, 6 Н), 2,93-3,00 (м, 2 Н),4,18 (м, 2 Н), 4,35 (м, 2 Н), 4,80 (с, 2H), 6,50-6,60 (м, 2H), 7,38 (м, 1 Н), 8,39 (д, 2 Н). МС APCI+ m/z 340 [МН]+. Пример 2. 6-Пиридин-2-ил-2-(3-пирролидин-1-илпропокси)-5,6,7,8-тетрагидро-1,6-нафтиридин. Смесь продукта получения 16 (68 мг, 0,26 ммоль), 2-бромпиридина (62 мг, 0,39 ммоль), третбутоксида натрия, (30 мг, 0,31 ммоль), Pd2(dba)3 (4 мг, 4 мкмоль) и BINAP (9 мг, 14 мкмоль) суспендировали в трет-бутаноле (2 мл), и смесь нагревали при 110 С в микроволновом излучении в течение 30 мин. Затем реакционную смесь растворяли в метаноле, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле, с элюцией дихлорметаном:метанолом:0,88 аммиаком, от 100:0:0 до 80:20:1, для получения соединения в соответствии с заголовком с 64% выходом, 57 мг. 1(36 мг, 0,37 ммоль), Pd2(dba)3 (7 мг, 8 мкмоль) и BINAP (22 мг, 35 мкмоль) суспендировали в третбутаноле (2 мл), и смесь нагревали при 110 С в микроволновом излучении в течение 3 ч. В смесь добавляли дополнительное количество 2-хлорпиразина (36 мг, 0,31 ммоль), трет-бутоксида натрия (36 мг,0,37 ммоль), Pd2(dba)3 (7 мг, 8 мкмоль) и BINAP (22 мг, 30 мкмоль) в часовые интервалы. Затем реакционную смесь переводили в азеотропное состояние с помощью метанола и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле с элюцией этилацетатом:метанолом:0,88 аммиаком, от 100:0:0 до 90:10:1. После этого следовала дополнительная очистка с помощью колоночной хроматографии на аминосиликагеле Biotage с элюцией пентаном:этилацетатом,от 100:0 до 0:100, для получения соединения в соответствии с заголовком в виде бесцветной маслянистой жидкости с 76% выходом, 80 мг. 1(м, 1 Н). МС APCI+ m/z 340 [МН]+. Микроанализ позволил обнаружить (%); C (67,21), Н (7,46), N (20,60); для C19H25N5O необходимо(%); С (67,31), H (7,42), N (20,63) Примеры 4-32. Следующие соединения общей показанной ниже формулы были получены из продукта получений- 16010487 16, 17, 18, 19, 20, 21 и 28 и подходящего гетероциклического галогенида: R1Cl или R1Br. Использовали способ, аналогичный описанному для примера 3, где реакционную смесь нагревали в микроволновом излучении при 110 С в течение 1-3 ч. Ход реакций контролировали с помощью ТСХ, и реакционную смесь обрабатывали дополнительным количеством гетероциклического галогенида, трет-бутоксида натрия, Pd2(dba)3 и BINAP через равные интервалы времени, пока не был использован весь исходный материал.Chem. 53 (4), 786-790; 1988. Пример 20. С применением 6-бром-N,N-диметилпиридин-2-сульфонамида получения 33. Пример 21. Исходное вещество 3-хлорпиридазин можно приготовить, как описано в J. Med. Chem. 30 (2), 23949; 1987 Примеры 33-41. Следующие соединения по общей формуле, показанной ниже, готовили из продукта получений 16 или 17 и подходящего гетероциклического галогенида: R1Cl или R1Br. Использовали способ, аналогичный описанному для примера 3, где реакционную смесь нагревали при микроволновом излучении при 110 С в течение 30-60 мин. К раствору продукта получения 16 (50 мг, 0,19 ммоль) добавляли карбонат калия (26,5 мг,0,19 ммоль) и 4-хлорбензонитрил (53 мг, 0,38 ммоль) в хлорбензоле (2 мл), и смесь нагревали с обратным холодильником в течение 5 ч. Затем реакционную смесь разделяли между этилацетатом и водой. Органический слой отделяли, сушили над сульфатом магния и концентрировали в вакууме, для получения оранжевой маслянистой жидкости. Маслянистую жидкость очищали с помощью колоночной хроматографии на силикагеле, с элюцией этилацетатом:метанолом:0,88 аммиаком, от 100:0:0 до 80:20:1, для получения соединения в соответствии с заголовком в виде оранжевого твердого вещества с 55% выходом,38 мг. 1 Н ЯМР (CDCl3, 400 МГц) : 1,70-1,82 (м, 4 Н), 1,90-2,06 (м, 2 Н), 2,45-2,70 (шир.м, 6 Н), 2,93-3,02 (м,2 Н), 3,98 (м, 2 Н), 4,30 (м, 2 Н), 4,62 (с, 2 Н), 6,59 (д, 1 Н), 6,70 (д, 1 Н), 7,39 (д, 1 Н), 7,63 (м, 1 Н), 8,42 (м,1 Н). МС APCI+ m/z 364 [МН]+. Примеры 43-48. Следующие соединения общей показанной ниже формулы готовили из продукта получений 16, 17 и 20 и подходящего гетероциклического галогенида, R1Cl или R1Br, с использованием способа, аналогичного описанному для примера 42. Ход реакций контролировали с помощью ТСХ, и реакционную смесь нагревали с обратным холодильником в течение 18-48 ч, пока не был использован весь исходный материал. Примеры 44, 45 и 47 и 48. Также добавили несколько капель NMP для того, чтобы способствовать растворимости. Пример 45. С применением 6-бром-N,N-диметилникотинамида получения 36. Пример 46. Исходное вещество 2-хлор-5-N,N-диметилсульфонамидопиридин можно приготовить, как описано в Helv. Chim. Acta. 22, 912-920, 1939. Пример 49. 6-(1,3-Бензоксазол-2-ил)-2-(3-пирролидин-1-илпропокси)-5,6,7,8-тетрагидро-1,6-нафтиридин. В толуол (1 мл) добавили продукт получения 16 (50 мг, 0,19 ммоль), 2-хлорбензоксазол (29 мг,0,19 ммоль), трет-бутоксид натрия (20 мг, 0,21 ммоль), трифторацетат палладия (каталитическое количество) и три-тбутилфосфин (каталитическое количество), и смесь нагревали при 80 С в течение 16 ч в изолированной пробирке Reactivial. Затем реакционную смесь растворяли в этилацетате и очищали с помощью колоночной хроматографии на силикагеле с элюцией этилацетатом:метанолом:0,88 аммиаком,90:10:1, для получения соединения в соответствии с заголовком в виде желтого твердого вещества с 55% выходом, 40 мг. 1 Н ЯМР (CDCl3, 400 МГц) : 1,59-1,90 (шир.м, 4 Н), 1,99-2,05 (м, 2 Н), 2,45-2,65 (шир.м, 6 Н), 3,02 (м,2 Н), 4,00 (м, 2 Н), 4,30 (м, 2 Н), 4,75 (с, 2 Н), 6,60 (д, 1 Н), 7,01 (м, 1 Н), 7,19 (м, 1 Н), 7,30 (д, 1 Н), 7,35-7,42- 29010487 В ксилол (1 мл) добавляли продукт получения 16 (50 мг, 0,19 ммоль), 2-хлор-1-метил-1 Нбензимидазол [(32 мг, 0,19 ммоль), J. Heterocyclic. Chem., 34(6) 1781-1788; 1997] фосфат калия, (45 мг,0,21 ммоль), трифторацетат палладия (каталитическое количество) и три-тбутилфосфин (каталитическое количество), и смесь нагревали при 120 С в течение 3 ч в изолированной пробирке Reactivial. Добавляли дополнительное количество три-тбутилфосфина (1,8 мг), и смесь нагревали в течение еще 18 ч. Затем реакционную смесь растворяли в метаноле и очищали с помощью колоночной хроматографии на силикагеле с элюцией этилацетатом:метанолом:0,88 аммиаком, от 100:0:0 до 80:20:2. Необработанный продукт дополнительно очищали с помощью колоночной хроматографии на аминосиликагеле Biotage с элюцией пентаном:этилацетатом от 100:0 до 0:100 для получения соединения в соответствии с заголовком в виде бесцветной маслянистой жидкости с 9% выходом, 7 мг. 1 Н ЯМР (CDCl3, 400 МГц) : 1,79-1,90 (м, 4 Н), 1,99-2,05 (м, 2 Н), 2,50-2,65 (шир.м, 6 Н), 3,10 (м, 2 Н),3,60 (м, 2 Н), 3,64 (с, 3 Н), 4,30 (м, 2 Н), 4,48 (с, 2 Н), 6,60 (д, 1 Н), 7,19 (м, 3 Н), 7,38 (д, 1 Н), 7,60 (м, 1 Н). МС APCI+ m/z 392 [МН]+. Пример 51. 6-(1,3-Оксазол-2-ил)-2-(3-пирролидин-1-илпропокси)-5,6,7,8-тетрагидро-1,6-нафтиридин. Соединение в соответствии с заголовком приготовили из продукта получения 16 и 2-бромоксазола Продукт получения 16 (8 мг, 31 мкмоль), триэтиламин (4,5 мкл, 34 мкмоль), фторид цезия (9 мг,0,059 ммоль) и 2-хлор-5-(4-метоксифенил)пиримидин [(6,8 мг, 31 мкмоль), Bioorg. and Med. Chem. Lett. 13(4), 761-765; 2003] смешивали в диметилсульфоксиде (300 мкл) и нагревали при 100 С в течение 24 ч. Затем реакционную смесь охлаждали и очищали с помощью ЖХВД с применением системы PhenomenexLuna C18 с элюцией от 95:5 до 5:95 ацетонитрилом:водой/ацетонитрилом/ацетатом аммония (95:5:0,005) для получения соединения в соответствии с заголовком. МС ES+ m/z 446 [МН]+. Примеры 53-58. Следующие соединения общей показанной ниже формулы были получены из продукта получения 16 и подходящего гетероциклического галогенида, R2Cl или R2Br, с использованием способа, аналогичного описанному для примера 52.
МПК / Метки
МПК: A61P 25/00, C07D 519/00, A61K 31/4985, A61K 31/52, A61K 31/4745, C07D 471/04
Метки: пригодные, производные, лигандов, качестве, гистамина, рецептора, тетрагидронафтиридина
Код ссылки
<a href="https://eas.patents.su/30-10487-proizvodnye-tetragidronaftiridina-prigodnye-v-kachestve-ligandov-receptora-n3-gistamina.html" rel="bookmark" title="База патентов Евразийского Союза">Производные тетрагидронафтиридина, пригодные в качестве лигандов рецептора н3 гистамина</a>
Предыдущий патент: Замещенные оксиндолсульфонамидные ингибиторы вич-протеазы широкого спектра действия
Следующий патент: 6-замещённые 2-хинолиноны и 2-хиноксалиноны как ингибиторы поли(адф-рибоза)полимеразы
Случайный патент: Поддерживаемые силикоалюминофосфатные (sapo) мембраны высокой избирательной способности