Замещенные оксиндолсульфонамидные ингибиторы вич-протеазы широкого спектра действия
Формула / Реферат
1. Соединение, имеющее формулу
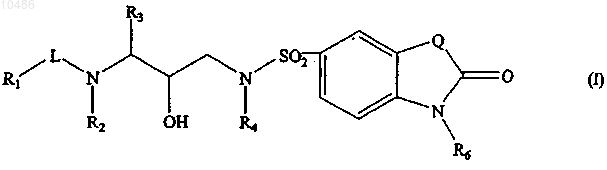
его N-оксид, соль, стереоизомерная форма, рацемическая смесь или сложный эфир, где
R1 представляет собой Het;
L означает -O-С(=O)-;
R2 и R6 представляют собой водород;
R3 представляет собой С1-4алкиларил;
R4 представляет собой C1-6алкил;
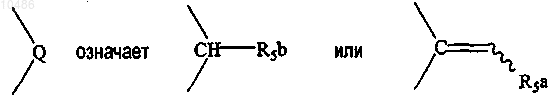
R5a выбирают из C1-6алкила, арила или Het,
где арил необязательно замещен по одному или нескольким атомам углерода заместителем, независимо выбранным из группы, включающей ди(С1-4алкил)амино, гидрокси, карбоксил, C1-4алкилокси, С1-4 алкилкарбонил, Het;
Het представляет собой моноциклический или бициклический гетероцикл, содержащий 5-9-членов в цикле, включающий один гетероатом, независимо выбранный из азота, кислорода или серы; указанный гетероцикл необязательно замещен C1-6алкилом, C1-4алкилкарбонилокси;
R5b представляет собой водород.
2. Соединение по п.1, где R1 представляет собой 5-8-членный гетероцикл, имеющий кислород в качестве гетероатома.
3. Соединение по п.1 или 2, где L означает -O-C(=O)-.
4. Соединение по любому из пп.1-3, где R5a выбирают из C1-6алкила, арила или Het,
где арил необязательно замещен по одному или нескольким атомам углерода заместителем, независимо выбранным из группы, включающей ди(С1-4алкил)амино, гидрокси, карбоксил, C1-4алкилокси, С1-4 алкилкарбонил, Het;
Het представляет собой моноциклический или бициклический гетероцикл, содержащий 5-9-членов в цикле, включающий один гетероатом, выбранный из азота, кислорода или серы; указанный гетероцикл необязательно замещен С1-С6алкилом, C1-4алкилкарбонилокси;
R5b представляет собой водород.
5. Соединение по п.1, где соединением является
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{изобутил[2-оксо-3-(1Н-пиррол-2-илметилен)-2,3-дигидро-1Н-индол-5-сульфонил]амино}пропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{изобутил[3-(5-метилфуран-2-илметилен)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]амино}пропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{изобутил[3-(5-метилтиофен-2-илметилен)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]амино}пропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{изобутил[3-(1-метил-1Н-пиррол-2-илметилен)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]амино}пропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-3-{3-[2-этилбутилиден)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]изобутиламино}-2-гидроксипропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир {1-бензил-2-гидрокси-3-[изобутил(3-изобутилиден-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил)амино]пропил}карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир {1-бензил-3-[(3-фуран-2-илметилен-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил)изобутиламино]-2-гидроксипропил}карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{изобутил[3-(4-метоксибензилиден)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]амино}пропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{изобутил[3-(2-метоксибензилиден)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]амино}пропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{[3-(4-гидрокси-3-метоксибензилиден)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]изобутиламино}пропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{изобутил[2-оксо-3-(4-пиридин-2-илбензилиден)-2,3-дигидро-1Н-индол-5-сульфонил]амино}пропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{[3-(4-гидрокси-3,5-диметилбензилиден)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]изобутиламино}пропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-3-{[3-(4-диметиламинобензилиден)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]изобутиламино}-2-гидроксипропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{[3-(1Н-индол-2-илметилен)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]изобутиламино}пропил)карбаминовой кислоты;
5-(5-{[3-(гексагидрофуро[2,3-b]фуран-3-илоксикарбониламино)-2-гидрокси-4-фенилбутил]изобутилсульфамоил}-2-оксо-1,2-дигидроиндол-3-илиденметил)фуран-2-илметиловый эфир уксусной кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир {1-бензил-3-[(3-бензилиден-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил)изобутиламино]-2-гидроксипропил}карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-3-{[3-(4-диэтиламино-3-гидроксибензилиден)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]изобутиламино}-2-гидроксипропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-{[3-(2-гидроксибензилиден)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]изобутиламино}пропил)карбаминовой кислоты;
гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-3-{изобутил[3-(5-метилфуран-2-илметилен)-2-оксо-2,3-дигидро-1Н-индол-5-сульфонил]амино}-2-фосфонооксипропил)карбаминовой кислоты;
4-(5-{[3-(гексагидрофуро[2,3-b]фуран-3-илоксикарбониламино)-2-гидрокси-4-фенилбутил]изобутилсульфамоил}-2-оксо-1,2-дигидроиндол-3-илиденметил)бензойная кислота,
его N-оксид и соль или его стереоизомерная форма.
6. Фармацевтическая композиция, включающая эффективное количество по крайней мере одного соединения по любому из пп.1-5 и фармацевтически приемлемый эксципиент.
7. Способ ингибирования протеазы устойчивого ко многим лекарствам ретровируса у млекопитающего, инфицированного указанным ретровирусом, который включает введение ингибирующего протеазу количества соединения по любому из пп.1-5 нуждающемуся в этом указанному млекопитающему.
8. Способ лечения или борьбы с инфекцией или заболеванием, связанным с инфекцией млекопитающего, устойчивой ко многим лекарствам ретровируса, который включает введение указанному млекопитающему эффективного количества по крайней мере одного соединения по любому из пп.1-5.
9. Способ ингибирования репликации устойчивого ко многим лекарствам ретровируса, который включает контактирование ретровируса с эффективным количеством по крайней мере одного соединения по любому из пп.1-5.
10. Применение соединения по любому из пп.1-5 в качестве лекарства.
11. Применение соединения по любому из пп.1-5 при изготовлении лекарственного средства для лечения или борьбы с инфекцией или заболеванием, связанным с инфекцией млекопитающего, устойчивой ко многим лекарствам ретровируса.
Текст
010486 По настоящей заявке испрашивается приоритет на основании Европейской заявки ЕР 02078384.1,поданной 14 августа 2002 г., содержание которой специально включено в данное описание посредством ссылки. Настоящее изобретение относится к замещенным оксиндолсульфонамидам, их применению в качестве ингибиторов ВИЧ-протеазы широкого спектра действия, способам их получения, а также к содержащим их фармацевтическим композициям и диагностическим наборам. Настоящее изобретение относится также к комбинациям замещенных оксиндолсульфонамидов с другими антиретровирусными реагентами. Оно также относится к их применению в анализах в качестве вещества, выбранного для сравнения, или в качестве реагентов. Вирус, который вызывает синдром приобретенного иммунодефицита (СПИД), известен под многими названиями, в том числе Т-вирус лимфоцитов III (HTLV-III), или лимфаденопатия-ассоциированный вирус (LAV), или вирус, ассоциируемый со СПИД (ARV), или вирус иммунодефицита человека (ВИЧ). В настоящее время идентифицированы два отдельных семейства, т.е. ВИЧ-1 и ВИЧ-2. Далее аббревиатура ВИЧ используется как общий термин для обозначения указанных вирусов. Одним из критических путей в жизненном цикле ретровируса является процессинг предшественников полипротеина аспартатной протеазой. Например, в случае ВИЧ белок gag-pol процессируется ВИЧпротеазой. Правильный процессинг предшественников полипротеинов аспартатной протеазой необходим для сборки инфекционных вирионов, и, таким образом, аспартатная протеаза является привлекательной мишенью для антивирусной терапии. В частности, для лечения ВИЧ привлекательной мишенью является ВИЧ-протеаза. Ингибиторы ВИЧ-протеазы (PI) обычно назначают больным СПИД в сочетании с другими антиВИЧ соединениями, такими как, например, нуклеозидные ингибиторы обратной транскриптазы (NRTI),ненуклеозидные ингибиторы обратной транскриптазы (NNRTI), нуклеотидные ингибиторы обратной транскриптазы (NtRTI) или другие ингибиторы протеазы. Несмотря на то, что указанные антиретровирусные агенты весьма полезны, они обладают общим ограничением, а именно, ферменты-мишени в ВИЧ способны мутировать таким образом, что известные лекарства становятся менее эффективными или даже неэффективными против этих мутантных ВИЧ. Или другими словами, ВИЧ создает всевозрастающую резистентность к имеющимся лекарствам. Резистентность ретровирусов и, в частности, ВИЧ, к действию ингибиторов является основной причиной неудачи в терапии. Например, половина пациентов, получающих комбинированную ВИЧ терапию, не полностью реагируют на лечение, главным образом вследствие резистентности вируса к одному или нескольким лекарствам. Более того, было показано, что резистентный вирус передается вновь инфицированным индивидуумам, что приводит к существенному ограничению выбора терапии для указанных пациентов, ранее не получавших лекарства. На Международной конференции по проблеме СПИД, которая проходила в Париже в июле 2003 г., исследователи сообщали, что наиболее широко проведенное в настоящее время исследование, посвященное устойчивости по отношению к лекарствам от СПИД, показывало, что приблизительно 10% всех вновь инфицированных людей в Европе заражены штаммами, резистентными к лекарствам. Меньшие по объему тесты с целью определения распространения резистентности были проведены в центре повышенного риска в Сан-Франциско. Эти тесты показали, что наибольший процент резистентности составляет 27%. Таким образом, в данной области существует потребность в новых соединениях для ретровирусной терапии, в частности для лечения СПИД. Особенно остро ощущается потребность в соединениях, которые активны не только против ВИЧ дикого типа, но также и против все чаще встречающихся резистентных ВИЧ. Известные антиретровирусные препараты, которые часто вводят по схемам приема лекарств с использованием комбинированной терапии, как указано выше, со временем развивают резистентность. Часто это может заставить врача повышать уровни активных лекарств в плазме с тем, чтобы указанные антиретровирусные препараты восстановили свою активность против видоизмененных ВИЧ. Следствием этого является крайне нежелательное повышение количества назначаемых таблеток. Повышение уровней лекарства в плазме может также приводить к повышению риска несоблюдения предписанной терапии. Таким образом, важно не только иметь в распоряжении соединения, активные по отношению к широкому кругу ВИЧ-мутантов, но и важно, чтобы отсутствовало или же существовало небольшое различие в отношении, касающемся активности против видоизмененного вируса и активности против ВИЧ дикого типа (это отношение также называют показателем резистентности, или FR) для широкого диапазона видоизмененных ВИЧ-штаммов. В этом случае для пациентов в течение более длительного периода времени могут быть сохранены прежние схемы приема лекарств с использованием комбинированной терапии,т.к. повышается вероятность того, что видоизмененный ВИЧ будет чувствителен к активным ингредиентам. Важно также осуществлять поиск высокоэффективных соединений против вируса дикого типа и против широкого круга мутантов, поскольку количество назначаемых таблеток может быть снижено,если удается сохранить минимальные терапевтические уровни. Одним из дополнительных путей снижения указанного количества назначаемых таблеток является поиск анти-ВИЧ соединений, обладающих хорошей биодоступностью, т.е. обладающих благоприятным фармакокинетическим и метаболическим-1 010486 профилем, с тем, чтобы дневная доза могла быть минимизирована и, следовательно, уменьшено количество таблеток, которое необходимо принимать. Другим благоприятным свойством анти-ВИЧ соединения является то, что связывание ингибитора белком плазмы оказывает минимальное или не оказывает никакого влияния на его эффективность. Таким образом, в медицине существует острая потребность в ингибиторах протеазы, которые способны бороться с широким спектром мутантов ВИЧ и характеризуются небольшими изменениями в показателе резистентности. Дополнительными преимуществами обладают те ингибиторы протеазы, которые обладают хорошей биодоступностью и на эффективность которых оказывает небольшое влияние или вовсе не оказывает влияние связывание их белком плазмы. В настоящее время на рынке имеется или разработано несколько ингибиторов протеазы. Одна из конкретных структур основного ядра соединения (приводится ниже) раскрывается в ряде ссылок, таких как WO 95/06030, WO 96/22287, WO 96/28418, WO 96/28463, WO 96/28464, WO 96/28465 и WO 97/18205. Раскрываемые там соединения описываются как ингибиторы протеазы ретровируса. В WO 99/67254 раскрываются 4-замещенные фенилсульфонамиды, способные ингибировать протеазы ретровируса, устойчивые к действию многих лекарств. Было показано, что замещенные оксиндолсульфонамиды по настоящему изобретению имеют благоприятный фармакологический профиль. Они не только активны по отношению к ВИЧ дикого типа, но и показывают широкий спектр активности против различных видоизмененных ВИЧ, обладающих устойчивостью по отношению к известным ингибиторам протеазы. Настоящее изобретение относится к замещенным оксииндольным ингибиторам протеазы, имеющим формулуR1 может также обозначать радикал формулы где R9, R10a и R10b, каждый независимо, означает водород, С 1-4 алкилоксикарбонил, карбоксил, аминокарбонил, моно- или ди(С 1-4 алкил)аминокарбонил, С 3-7 циклоалкил, С 2-6 алкенил, С 2-6 алкинил или С 1-4 алкил,необязательно замещенный арилом, Het1, Het2, С 3-7 циклоалкилом, С 1-4 алкилоксикарбонилом, карбоксилом, аминокарбонилом, моно- или ди(С 1-4 алкил)аминокарбонилом, аминосульфонилом, C1-4 алкилS(O)t,гидрокси, циано, галогеном или необязательно моно- или дизамещенной аминогруппой, где каждый из заместителей независимо выбирают из С 1-4 алкила, арила, арилС 1-4 алкила, С 3-7 циклоалкила, С 3-7 цикло-2 010486 алкилС 1-4 алкила, Het1, Het2, Het1 С 1-4 алкила и Het2C1-4 алкила; при этом R9, R10a и атом углерода, к которому они присоединены, могут также образовывать С 3-7 циклоалкилльный радикал; если L означает -O-C1-6 алкандиил-С(=O)- или -NR8-С 1-6 алкандиил-С(=O)-, то R9 может также обозначать оксогруппу;R11a означает водород, С 2-6 алкенил, С 2-6 алкинил, С 3-7 циклоалкил, арил, необязательно моно- или дизамещенный аминокарбонил, необязательно моно- или дизамещенный аминоС 1-4 алкилкарбонилокси, С 1-4 алкилоксикарбонил, арилоксикарбонил, Het1 оксикарбонил, Het2 оксикарбонил, арилоксикарбонилС 1-4 алкил, арилС 1-4 алкилоксикарбонил, С 1-4 алкилкарбонил, С 3-7 циклоалкилкарбонил, С 3-7 циклоалкилС 1-4 алкилоксикарбонил, С 3-7 циклоалкилкарбонилокси, карбоксиС 1-4 алкилкарбонилокси, С 1-4 алкилкарбонилокси,арилС 1-4 алкилкарбонилокси,арилкарбонилокси,арилоксикарбонилокси,Het1 карбонил,1 1 2 2Het карбонилокси, Het С 1-4 алкилоксикарбонил, Het карбонилокси, Het C1-4 алкилкарбонилокси, Het2C1-4 алкилоксикарбонилокси или С 1-4 алкил, необязательно замещенный арилом, арилокси, Het2 или гидрокси; при этом заместители в аминогруппах, каждый независимо, выбирают из С 1-4 алкила, арила, арилС 1-4 алкила, С 3-7 циклоалкила, С 3-7 циклоалкилС 1-4 алкила, Het1, Het2, Het1C1-4 алкила и Het2 С 1-4 алкила;R11b означает водород, С 3-7 циклоалкил, С 2-6 алкенил, С 2-6 алкинил, арил, Het1, Het2 или С 1-4 алкил, необязательно замещенный галогеном, гидрокси, С 1-4 алкилS(=O)t, арилом, С 3-7 циклоалкилом, Het1, Het2,необязательно моно- или дизамещенной аминогруппой, где каждый заместитель независимо выбирают из С 1-4 алкила, арила, арилС 1-4 алкила, С 3-7 циклоалкила, С 3-7 циклоалкилС 1-4 алкила, Het1, Het2, Het1 С 1-4 алкила и Het2C1-4 алкила; где R11b может быть присоединен к остальной части молекулы через сульфонильную группу;R2 означает водород или C1-6 алкил;L означает -С(=O)-, -O-С(=O)-, -NR8-C(=O)-, -O-С 1-6 алкандиил-С(=O)-, -NR8-C1-6 алкандиил-С(=O)-,-S(=O)2-, -O-S(=O)2-, -NR8-S(=O)2, где либо группа С(=O), либо группа -S(=O)2 присоединена к фрагментуNR2; и где независимо каждый С 1-6 алкандиильный фрагмент необязательно может быть замещен гидрокси, арилом, Het1 или Het2;R3 означает C1-6 алкил, арил, С 3-7 циклоалкил, С 3-7 циклоалкилС 1-4 алкил или арилС 1-4 алкил;R4 означает водород, С 1-4 алкилоксикарбонил, карбоксил, аминокарбонил, моно- или ди(С 1-4 алкил) аминокарбонил, С 3-7 циклоалкил, С 2-6 алкенил, С 2-6 алкинил или C1-6 алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбирают из арила, Het1, Het2, С 3-7 циклоалкила, С 1-4 алкилоксикарбонила, карбоксила, аминокарбонила, моно или ди(С 1-4 алкил)аминокарбонила, аминосульфонила, моно или ди(С 1-4 алкил)аминосульфонила, C1-4 алкилS(=O)t, гидрокси, циано,галогена или необязательно моно- или дизамещенной аминогруппы, где каждый заместитель независимо выбирают из С 1-4 алкила, арила, арилС 1-4 алкила, С 3-7 циклоалкила, С 3-7 циклоалкилС 1-4 алкила, Het1, Het2,Het1 С 1-4 алкила и Het2 С 1-4 алкила;R5a и R5b, каждый независимо, выбирают из водорода, C1-6 алкила, С 2-6 алкенила, С 2-6 алкинила, С 3-7 циклоалкила, арила, Het1, Het2; где каждый из заместителей, выбранных из С 1-6 алкила, С 2-6 алкенила, С 2-6 алкинила или С 3-7 циклоалкила, необязательно замещен по одному или нескольким атомам углерода заместителем, независимо выбранным из группы, включающей амино, моно- или ди(С 1-4 алкил)амино, гидрокси, карбоксил, оксо, меркапто, галоген, циано, нитро, С 1-4 алкилокси, С 1-4 алкилкарбонил, С 1-4 алкилкарбонилокси, С 1-4 алкилоксикарбонил, арил, С 3-7 циклоалкил, Het1, Het2, С 1-4 алкилкарбонилокси, С 1-4 алкилоксикарбонил;R6 означает водород или C1-6 алкил, один или несколько атомов углерода которого необязательно замещены одним или несколькими заместителями, независимо выбранными из группы, включающей амино, моно- или ди(С 1-4 алкил)амино, гидрокси, меркапто, оксо, циано, нитро, галоген, карбоксилС 1-4 алкилокси, С 1-4 алкилкарбонил, С 1-4 алкилкарбонилокси, С 1-4 алкилоксикарбонил, С 3-7 циклоалкил, арил,Het1, Het2; где каждый С 1-4 алкил необязательно может быть замещен амино, моно- или ди(С 1-4 алкил) амино, гидрокси, меркапто, оксо, циано, нитро, галогеном, карбокси. Особый интерес представляют свободное основание, соль или N-оксид соединений формулы (I) и их стереоизомерные формы. Мутанты фермента ВИЧ-протеазы определяют как фермент ВИЧ-протеазу, которая имеет по крайней мере одно видоизменение в последовательности аминокислот, по сравнению с последовательностью аминокислот в ВИЧ-протеазе дикого типа. Чтобы в данном описании обозначить мутации, ссылка на дикий тип дается как НХВ 2 (дикий тип ВИЧ IIIB LAI), последовательность которого можно найти в хранилище GenBank Национального института здоровья США. Стандарт "чувствительности" или альтернативно "устойчивости" фермента ВИЧ-протеазы к действию лекарства устанавливают с помощью коммерчески доступных ингибиторов ВИЧ-протеазы. Как указывалось выше, существующие коммерческие ингибиторы ВИЧ-протеазы могут с течением времени терять эффективность против популяции ВИЧ пациента. Причина состоит в том, что благодаря действию-3 010486 имеющегося конкретного ингибитора ВИЧ-протеазы существующая популяция ВИЧ, в основном обычно фермент ВИЧ-протеаза дикого типа, видоизменяется в другие мутанты, которые значительно менее чувствительны к действию того же самого ингибитора ВИЧ-протеазы. Если наблюдается подобный феномен, то говорят о резистентных мутантах. Если указанные мутанты устойчивы не только к одному конкретному ингибитору ВИЧ-протеазы, но и к множеству других коммерчески доступных ингибиторов ВИЧ-протеазы, то говорят о ВИЧ-протеазе, устойчивой по отношению ко многим лекарствам. Одним из способов выражения устойчивости мутанта к конкретному ингибитору ВИЧ-протеазы является отношение между величиной ЕС 50 указанного ингибитора ВИЧ-протеазы по отношению к мутантной ВИЧпротеазе и величиной ЕС 50 указанного ингибитора ВИЧ-протеазы по отношению к ВИЧ-протеазе дикого типа. Указанное отношение называют также кратностью резистентности (FR). Многие из мутантов, имеющиеся в клинике, имеют величину кратности резистентности, равную 100 или более, по отношению к коммерчески доступным ингибиторам ВИЧ-протеазы, таким как саквинавир, индинавир, ритонавир и нелфинавир. Имеющиеся в клиниках мутанты фермента ВИЧ-протеазы могут быть охарактеризованы мутацией по месту кодона 10, 71 и/или 84. Примеры подобных имеющихся в клиниках мутантов ВИЧ-протеазы приведены в табл. 2. Соединения по настоящему изобретению показывают величину кратности резистентности в диапазоне от 0,01 до 100 по отношению по крайней мере к одному, и в некоторых случаях и к широкому кругу имеющихся в клиниках мутантов ВИЧ-протеаз. Особую группу соединений формулы (I) составляют такие соединения формулы (I), которые имеют величину кратности резистентности по отношению по крайней мере к одной мутантной протеазе в диапазоне от 0,1 до 100, предпочтительно в диапазоне от 0,1 до 50 и более предпочтительно в диапазоне от 0,1 до 30. Особый интерес представляют соединения формулы (I), которые имеют величину кратности резистентности по отношению по крайней мере к одной мутантной протеазе в диапазоне от 0,1 до 20, и еще больший интерес представляют такие соединения формулы (I), которые имеют величину кратности резистентности по отношению по крайней мере к одной мутантной протеазе в диапазоне от 0,1 до 10. Таким образом, настоящее изобретение относится к соединению формулы (I) для изготовления лекарственного средства, которое можно применять для ингибирования репликации ВИЧ, имеющего мутантную ВИЧ-протеазу, в частности мутантную ВИЧ-протеазу, обладающую устойчивостью по отношению ко многим лекарствам. Оно также относится к применению соединения формулы (I) для изготовления лекарственного средства, которое можно применять для лечения или борьбы с болезнью, связанной с вирусной инфекцией ВИЧ, при этом протеаза ВИЧ является мутантной, в частности является мутантной ВИЧ-протеазой, обладающей устойчивостью по отношению ко многим лекарствам. Другими словами, настоящее изобретение относится к способу ингибирования мутантной ВИЧпротеазы, в частности мутантной ВИЧ-протеазы, обладающей устойчивостью по отношению ко многим лекарствам, у млекопитающего, инфицированного указанной мутантной ВИЧ-протеазой, при этом указанный способ включает контактирование указанной мутантной ВИЧ-протеазы у указанного млекопитающего с эффективным количеством соединения формулы (I). Настоящее изобретение относится также к способу ингибирования репликации ВИЧ, который имеет мутантную ВИЧ-протеазу, в частности мутантную ВИЧ-протеазу, обладающую устойчивостью по отношению ко многим лекарствам, у млекопитающего, при этом указанный способ включает контактирование указанного ВИЧ, обладающего мутантной ВИЧ-протеазой, у указанного млекопитающего с эффективным количеством соединения формулы(I). Далее настоящее изобретение относится к способу лечения или борьбы с болезнью млекопитающего,связанной с вирусной инфекцией ВИЧ, где протеаза ВИЧ является мутантной, в частности мутантной ВИЧ-протеазой, обладающей устойчивостью по отношению ко многим лекарствам, при этом указанный способ включает контактирование указанного ВИЧ, инфицирующего указанное млекопитающее, у которого протеаза ВИЧ является мутантной, с эффективным количеством соединения формулы (I). Особый интерес представляют такие соединения по настоящему изобретению, которые могут быть использованы при изготовлении лекарственного средства для лечения индивидуумов, инфицированных мутантной ВИЧ-протеазой, содержащей мутацию по крайней мере одной аминокислоты в положении 10,71 или 84, или, по крайней мере, комбинацию мутаций в двух указанных положениях или, по крайней мере, комбинацию мутаций во всех трех положениях. Обладающий основными свойствами атом азота в соединениях по настоящему изобретению может быть превращен в четвертичный атом азота с помощью любого агента, известного специалистам в данной области, в том числе, например, с помощью низших алкилгалогенидов, диалкилсульфатов, галогенидов с длинной цепью и аралкилгалогенидов. Встречающийся в данном описании термин "замещенный", который используют для определения соединений формулы (I), означает, что один или несколько атомов водорода, указанных в выражении"замещенный", заменен(ы) набором из указанной группы, при условии, что нормальная валентность указанного атома не превышена и что замещение приводит к получению химически стабильного соединения, т.е. соединения, которое достаточно устойчиво, чтобы его можно было выделить из реакционной смеси с необходимой степенью чистоты и приготовить из него терапевтический агент. Используемый в данном описании термин "галоген" как группа или часть группы является общим-4 010486 термином для обозначения фтора, хлора, брома или иода. Термин "С 1-4 алкил" как группа или часть группы означает насыщенные углеводородные радикалы с прямой или разветвленной цепью, имеющие от 1 до 4 атомов углерода, такие как, например, метил, этил,пропил, бутил и 2-метилпропил и т.п. Термин "C1-6 алкил" как группа или часть группы означает насыщенные углеводородные радикалы с прямой или разветвленной цепью, имеющие от 1 до 6 атомов углерода, такие как группы, определенные для С 1-4 алкила, и пентил, гексил, 2-метилбутил, 3-метилпентил и т.п. Термин "С 1-6 алкандиил" как группа или часть группы означает двухвалентные насыщенные углеводородные радикалы с прямой или разветвленной цепью, имеющие от 1 до 6 атомов углерода, такие как,например, метилен, этан-1,2-диил, пропан-1,3-диил, пропан-1,2-диил, бутан-1,4-диил, пентан-1,5-диил,гексан-1,6-диил, 2-метилбутан-1,4-диил, 3-метилпентан-1,5-диил и т.п. Термин "С 2-6 алкенил" как группа или часть группы означает углеводородные радикалы с прямой или разветвленной цепью, имеющие от 2 до 6 атомов углерода и содержащие по крайней мере одну двойную связь, такие как, например, этенил, пропенил, бутенил, пентенил, гексенил и т.п. Термин "С 2-6 алкинил" как группа или часть группы означает углеводородные радикалы с прямой или разветвленной цепью, имеющие от 2 до 6 атомов углерода и содержащие по крайней мере одну тройную связь, такие как, например, этинил, пропинил, бутинил, пентинил, гексинил и т.п. Термин "С 3-7 циклоалкил" как группа или часть группы является общим термином для обозначения циклопропила, циклобутила, циклопентила, циклогексила или циклогептила. Термин "арил" как группа или часть группы по определению включает фенил и нафтил, оба необязательно могут быть замещены одним или несколькими заместителями, независимо выбранными из C1-6 алкила, необязательно моно- или дизамещенного аминоС 1-6 алкила, C1-6 алкилокси, галогена, гидрокси,необязательно моно- или дизамещенного амино, нитро, циано, галогенС 1-6 алкила, гидроксиС 1-6 алкила,карбоксила, С 1-6 алкоксикарбонила, С 1-6 алкилкарбонилоксиС 1-6 алкила, С 1-6 алкилоксикарбонилоксиС 1-6 алкила, С 3-7 циклоалкила, Het1, Het2, необязательно моно- или дизамещенного аминокарбонила, метилтио,метилсульфонила и фенила, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из C1-6 алкила, необязательно моно- или дизамещенного аминоС 1-6 алкила,С 1-6 алкилокси, галогена, гидрокси, необязательно моно- или дизамещенного амино, нитро, циано, галогенС 1-6 алкила, карбоксила, С 1-6 алкоксикарбонила, С 3-7 циклоалкила, Het1, необязательно моно- или дизамещенного аминокарбонила, метилтио и метилсульфонила; при этом необязательные заместители в аминогруппе независимо выбирают из С 1-6 алкила, С 1-6 алкокси-А-, Het1-A-, Het1 С 1-6 алкила, Het1 С 1-6 алкил-А-,Het1 окси-A-, Het1 оксиC1-4 алкил-А-, фенил-А-, фенилокси-А-, фенилоксиС 1-4 алкил-А-, фенилС 1-6 алкил-А-,С 1-6 алкилоксикарбониламино-А-, амино-А-, аминоС 1-6 алкила и аминоС 1-6 алкил-А-, где каждая из аминогрупп необязательно может быть монозамещена или там, где это возможно, дизамещена С 1-4 алкилом, и А означает С 1-6 алкандиил, -С(=O)-, -C(=S)-, -S(=O)2-, С 1-6 алкандиил-С(=O)-, C1-6 алкандиил-C(=S)- или С 1-6 алкандиил-S(=O)2-; где местом присоединения А к атому азота является C1-6 алкандиильная группа в тех фрагментах, которые содержат указанную группу. Термин "галогенС 1-6 алкил" как группа или часть группы определяется как С 1-6 алкил, замещенный одним или несколькими атомами галогена, предпочтительно атомами хлора или фтора, более предпочтительно атомами фтора. Предпочтительные галогенС 1-6 алкильные группы включают, например, трифторметильную или дифторметильную группу. Термин "гидроксиС 1-6 алкил" как группа или часть группы определяется как C1-6 алкил, замещенный одним или несколькими гидроксигруппами. Термин "Het1" как группа или часть группы определяется как насыщенный или частично ненасыщенный моноциклический, бициклический или трициклический гетероцикл, имеющий 3-14 членов в кольце, предпочтительно 5-10 членов в кольце и более предпочтительно 5-8 членов в кольце, содержащий в качестве членов в кольце один или несколько гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы, и необязательно замещенный по одному или нескольким атомам углерода С 1-6 алкилом, необязательно моно- и дизамещенным аминоС 1-6 алкилом, C1-6 алкилокси, галогеном,гидрокси, оксо, необязательно моно- и дизамещенным амино, нитро, циано, галогенС 1-6 алкилом, гидроксиС 1-6 алкилом, карбоксилом, C1-6 алкоксикарбонилом, С 1-6 алкилкарбонилоксиС 1-6 алкилом, С 1-6 алкилоксикарбонилС 1-6 алкилом, С 3-7 циклоалкилом, необязательно моно- и дизамещенным аминокарбонилом,метилтио, метилсульфонилом, арилом и насыщенным или частично ненасыщенным моноциклическим,бициклическим или трициклическим гетероциклом, имеющим 3-14 членов в кольце и содержащим в качестве членов в кольце один или несколько гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы, и где необязательные заместители в любой аминогруппе независимо выбирают из C1-6 алкила, С 1-6 алкилокси-А-, Het2-A-, Het2 С 1-6 алкила, Het2 С 1-6 алкил-А-, Het2 окси-A-, Het2 оксиС 1-4 алкил-А-, арил-А-, арилокси-А-, арилоксиС 1-4 алкил-А-, арилС 1-6 алкил-А-, C1-6 алкилоксикарбониламино-А-,амино-А-, аминоС 1-6 алкила и аминоС 1-6 алкил-А-, где каждая из аминогрупп необязательно может быть монозамещена или там, где это возможно, дизамещена С 1-4 алкилом, и значение А указано выше. Термин "Het2" как группа или часть группы определяется как ароматический моноциклический, бициклический или трициклический гетероцикл, имеющий 3-14 членов в кольце, предпочтительно 5-10-5 010486 членов в кольце и более предпочтительно 5-6 членов в кольце, содержащий в качестве членов в кольце один или несколько гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы,и необязательно замещенный по одному или нескольким атомам углерода С 1-6 алкилом, необязательно моно- и дизамещенным аминоС 1-6 алкилом, C1-6 алкилокси, галогеном, гидрокси, необязательно моно- и дизамещенным амино, нитро, циано, галогенС 1-6 алкилом, гидроксиС 1-6 алкилом, карбоксилом, C1-6 алкоксикарбонилом, С 1-6 алкилкарбонилоксиС 1-6 алкилом, С 1-6 алкилоксикарбонилС 1-6 алкилом, С 3-7 циклоалкилом, необязательно моно- и дизамещенным аминокарбонилом, метилтио-, метилсульфонилом, арилом,группой Het1 и ароматическим моноциклическим, бициклическим или трициклическим гетероциклом,имеющим 3-14 членов в кольце; где необязательные заместители в любой аминогруппе независимо выбирают из C1-6 алкила, C1-6 алкилокси-А-, Het1-A-, Het-C1-6 алкила, Het1 С 1-6 алкил-А-, Het1 окси-A-,Het1 оксиС 1-4 алкил-А-, арил-А-, арилокси-А-, арилоксиС 1-4 алкил-А-, арилС 1-6 алкил-А-, C1-6 алкилоксикарбониламино-А-, амино-А-, аминоС 1-6 алкила и аминоС 1-6 алкил-А-, где каждая из аминогрупп необязательно может быть монозамещена или там, где это возможно, дизамещена С 1-4 алкилом, и значение А указано выше. Как использовано в данном описании, элемент (=O) вместе с атомом углерода, к которому он присоединен, образует карбонильный фрагмент. Элемент (=O) вместе с атомом серы, к которому он присоединен, образует сульфоксид. Элемент (=O)2 вместе с атомом серы, к которому он присоединен, образует сульфонил. Как использовано в данном описании, элемент (=S) вместе с атомом углерода, к которому он присоединен, образует тиокарбонильный фрагмент. Как использовано в данном описании, термин "один или несколько" означает возможность того, что все доступные атомы углерода, замещены там, где это возможно, предпочтительно одним, двумя или тремя заместителями. В том случае, когда переменная группа (например, галоген или С 1-4 алкил) появляется один или несколько раз в любой составной части, каждое определение является независимым. Термин "пролекарство", как использовано в данном описании, означает фармакологически приемлемые производные, такие как сложные эфиры, амиды и фосфаты, так, что полученный in vivo продукт биотрансформации производного является активным лекарственным средством, как это показано для соединений формулы (I). В данное описание включена ссылка на Goodman and Gilman (The Pharmacological Basis of Therapeutics, 8th ed, McGraw-Hill, Int. Ed. 1992, "Biotransformation of Drugs", p. 13-15), которые в общем виде описывают пролекарства. Пролекарства из соединения по настоящему изобретению получают путем модификации имеющихся в соединении функциональных групп таким образом, чтобы модификации могли расщепляться, как при проведении обычных манипуляций, так и в условиях in vivo,в исходное родственное соединение. Пролекарства включают соединения по настоящему изобретению, в которых гидроксигруппа, например гидроксигруппа при асимметрическом атоме углерода, или аминогруппа присоединена к любой такой группе, которая после того, как пролекарство вводят пациенту, расщепляется с образованием, соответственно, свободной гидроксигруппы или свободной аминогруппы. Типичные примеры пролекарств описаны, например, в WO 99/33795, WO 99/33815, WO 99/33793 иWO 99/33792, которые включены в настоящее описание посредством ссылки. Пролекарства отличаются превосходной растворимостью в воде, повышенной биодоступностью и легко метаболизируются in vivo в активные ингибиторы. Для использования в терапии соли соединений формулы (I) являются такими солями, в которых противоион является фармацевтически или физиологически приемлемым. Тем не менее, соли, имеющие фармацевтически неприемлемый противоион, также находят применение, например, при получении или очистке фармацевтически приемлемого соединения формулы (I). Все соли как фармацевтически приемлемые, так и неприемлемые, входят в объем настоящего изобретения. Фармацевтически приемлемые или физиологические переносимые аддитивные солевые формы, которые соединения по настоящему изобретению способны образовывать, удобно получать с использованием соответствующих кислот, например, таких неорганических кислот, как галогено-водородные кислоты, в частности хлористо-водородная или бромисто-водородная кислота; серная, гемисерная, азотная,фосфорная и подобные кислоты; или, например, таких органических кислот, как уксусная, аспарагиновая, додецилсерная, гептановая, гексановая, никотиновая, пропановая, гидроксиуксусная, молочная, пировиноградная, щавелевая, малоновая, янтарная, малеиновая, фумаровая, яблочная, винная, лимонная,метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, памовая и подобные кислоты. И наоборот, указанные кислотно-аддитивные солевые формы обработкой соответствующим основанием могут быть превращены в форму свободного основания. Соединения формулы (I), содержащие кислый протон, могут быть превращены в их нетоксичные аддитивные соли металлов и аминов обработкой соответствующими органическими и неорганическими основаниями. Подходящие основные солевые формы включают, например, аммониевые соли, соли щелочных или щелочно-земельных металлов, в частности соли лития, натрия, калия, магния, кальция и подобные соли, соли с органическими основаниями, в частности соли с бензатином, N-метил-D-6 010486 глютамином, гидрабамином, и соли с аминокислотами, такими как, например, аргинин, лизин и т.п. И наоборот, указанные основно-аддитивные солевые формы могут быть превращены в формы свободной кислоты обработкой соответствующей кислотой. Термин "соли" включает также гидраты и аддитивные формы с растворителями, которые способны образовывать соединения по настоящему изобретению. Примерами подобных форм являются, в частности, гидраты, алкоголяты и т.п. Следует понимать, что N-оксидные формы по настоящему изобретению включают соединения формулы (I), в которых один или несколько атомов азота окислены с образованием так называемых Nоксидов. Соединения по настоящему изобретению могут также существовать в своих таутомерных формах. Следует понимать, что подобные формы, хотя они не указаны в явном виде в приведенной выше формуле, входят в объем настоящего изобретения. Термин стереохимически изомерные формы соединений по настоящему изобретению, как указано выше в настоящем описании, означает все возможные соединения, полученные из тех же самых атомов,связанных той же самой последовательностью связей, но отличающиеся трехмерными структурами, не совместимыми друг с другом, которые могут образовывать соединения по настоящему изобретению. Если не упоминается или не указывается иное, химическое обозначение соединения включает смеси всех возможных стереохимически изомерных форм, которые может иметь указанное соединение по настоящему изобретению. Указанные смеси могут содержать все диастереомеры и/или энантиомеры основной молекулярной структуры указанного соединения. Следует понимать, что все стереохимически изомерные формы соединений по настоящему изобретению, как в чистом виде, так и в смеси друг с другом,входят в объем настоящего изобретения. Чистые стереоизомерные формы соединений и промежуточных соединений, которые приведены в настоящем описании, определяют как изомеры, в значительной степени свободные от других энантиомерных или диастереомерных форм той же самой основной молекулярной структуры указанных соединений и промежуточных соединений. В частности, термин "стереохимически чистый" относится к соединениям или промежуточным соединениям, имеющим изомерный избыток, составляющий по крайней мере 80% (т.е. минимум 90% одного изомера и максимум 10% других возможных изомеров) вплоть до стереохимического избытка 100% (т.е. 100% одного изомера при отсутствии других изомеров), в частности, к соединениям или промежуточным соединениям, имеющим изомерный избыток, составляющий от 90 вплоть до 100%, еще более предпочтительно к соединениям, имеющим изомерный избыток, составляющий от 94 вплоть до 100%, и наиболее предпочтительно к соединениям, имеющим изомерный избыток, составляющий от 97 вплоть до 100%. Термины "энантиомерно чистый" и "диастереомерно чистый" следует понимать аналогично, но в этом случае учитывают, соответственно, энантимерный и диастереомерный избыток рассматриваемой смеси. Чистые стереоизомерные формы соединений и промежуточных соединений по настоящему изобретению могут быть получены с помощью хорошо известных в данной области методов. Например, энантиомеры могут быть отделены друг от друга избирательной кристаллизацией их диастереомерных солей с оптически активными кислотами и основаниями. Примерами указанных солей являются винная кислота, дибензоилвинная кислота, дитолуоилвинная кислота и камфосульфоновая кислота. Кроме того, энантиомеры могут быть разделены методами хроматографии с применением хиральных неподвижных фаз. Указанные чистые стереохимически изомерные формы могут быть также получены из соответствующих чистых стереохимически изомерных форм соответствующих исходных соединений, при условии, что реакция протекает стереоспецифично. Если необходимы конкретные стереоизомеры, то указанные соединения предпочтительно синтезируют с помощью стереохимических способов получения. В указанных способах успешно применяют энантиомерно чистые исходные соединения. Диастереомерные рацематы формулы (I) могут быть получены отдельно с помощью обычных способов. Подходящими физическими способами, которые могут успешно использоваться, являются, например, селективная кристаллизация и хроматография, в частности колоночная хроматография. Для специалиста в данной области должно быть понятно, что соединения формулы (I) содержат по крайней мере два асимметрических центра и, таким образом, могут существовать в различных стереоизомерных формах. Эти два асимметрических центра обозначены звездочкойна приведенной ниже фигуре. Абсолютная конфигурация каждого асимметрического центра, который может присутствовать в соединении формулы (I), может быть показана стереохимическими идентификаторами R и S, при этом обо-7 010486 значения R и S соответствуют правилам, изложенным в Pure Appl. Chem. 1976, 45, 11-30. Атом углерода,несущий гидроксигруппу и отмеченный звездочкой , предпочтительно имеет R-конфигурацию. Атом углерода, несущий группу R3 и обозначенный звездочкой , предпочтительно имеет S-конфигурацию. Следует понимать, что настоящее изобретение включает все изотопы атомов, встречающихся в соединениях по настоящему изобретению. Изотопы включают такие атомы, которые имеют тот же атомный номер, но различные величины массы. В качестве общего примера и без ограничения, изотопы водорода включают тритий и дейтерий. Изотопы углерода включают С-13 и С-14. Независимо от того, в каком месте настоящего описания он используется, термин "соединение формулы (I)" или "соединение по настоящему изобретению", или аналогичный термин включает соединения общей формулы (I), их N-оксиды, соли, стереомерные формы, рацемические смеси, пролекарства,сложные эфиры и метаболиты, а также их аналоги с четвертичным атомом азота. Особую группу соединения составляют такие соединения формулы (I), для которых возможно одно или несколько следующих ограничений:R1 означает водород, Het1, Het2, арил, Het1 С 1-6 алкил, Het2 С 1-6 алкил, арилС 1-6 алкил; в частности, R1 означает водород, насыщенный или частично ненасыщенный моноциклический или бициклический гетероцикл, имеющий 5-8 членов в кольце, содержащий в качестве членов в кольце один или несколько гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы, и необязательно замещенный; фенил, необязательно замещенный одним или несколькими заместителями; ароматический моноциклический гетероцикл, имеющий 5-6 членов в кольце, содержащий в качестве членов в кольце один или несколько гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы,и необязательно замещенный по одному или нескольким атомам углерода; или C1-6 алкил, замещенный ароматическим моноциклическим гетероциклом, имеющим 5-6 членов в кольце, содержащим в качестве членов в кольце один или несколько гетероатомов, каждый из которых независимо выбирают из азота,кислорода и серы, и необязательно замещенным по одному или нескольким атомам углерода;R4 означает необязательно замещенный C1-6 алкил, в частности C1-6 алкил, необязательно замещенный арилом, Het1, Het2, С 3-7 циклоалкилом или моно- или дизамещенным амино, где каждый заместитель независимо выбирают из С 1-4 алкила, арила, Het1 и Het2;Q означает C=C-R5a, где R5a означает арил, Het1, Het2; где каждый из указанных заместителей необязательно замещен по одному или нескольким атомам заместителем, независимо выбранным из группы, включающей амино, моно- или ди(С 1-4 алкил)амино, гидрокси, C1-6 алкилокси, карбоксил, оксо, C1-6 алкил, гидроксиС 1-6 алкил, С 1-4 алкилкарбонилокси, С 1-4 алкилоксикарбонил, С 1-4 алкилкарбонилоксиС 1-4 алкил, С 1-4 алкилоксикарбонилС 1-4 алкил, Het1;R5a может также означать C1-6 алкил, необязательно дополнительно замещенный аминогруппой, моно- или ди(С 1-4 алкил)амино, гидрокси, С 1-6 алкилокси, карбонилом, оксо, меркапто, С 14 алкилкарбонилокси, С 1-4 алкилоксикарбонилом;R6 означает водород. Специальную группу соединений составляют такие соединения формулы (I), в которойQ означает C=C-R5a, где R5a означает Het1, арил, Het2; где каждый из указанных заместителей необязательно замещен по одному или нескольким атомам заместителем, независимо выбранным из группы, включающей амино, моно- или ди(С 1-4 алкил) амино, гидрокси, C1-6 алкилокси, аминоС 1-6 алкил, моноили ди(С 1-4 алкил)аминоС 1-4 алкил, карбоксил, оксо, C1-6 алкил, гидроксиС 1-6 алкил, меркапто, С 1-4 алкилкарбонилокси, С 1-4 алкилоксикарбонил, С 1-4 алкилкарбонилоксиС 1-4 алкил, С 1-4 алкилоксикарбонилС 1-4 алкил,С 3-7 циклоалкил, арил, Het1, Het2. Другую специальную группу соединений составляют такие соединения формулы (I), в которойQ означает C=C-R5a, где R5a означает арил, необязательно замещенный по одному или нескольким атомам заместителем, независимо выбранным из группы, включающей амино, моно- или ди(С 1-4 алкил) амино, гидрокси, C1-6 алкилокси, аминоС 1-6 алкил, моно- или ди(С 1-4 алкил)аминоС 1-4 алкил, карбоксил, оксо, C1-6 алкил, гидроксиС 1-6 алкил, меркапто, С 1-4 алкилкарбонилокси, С 1-4 алкилоксикарбонил, С 1-4 алкилкарбонилоксиС 1-4 алкил, С 1-4 алкилоксикарбонилС 1-4 алкил, С 3-7 циклоалкил, арил, Het1, Het2.-8 010486 Еще одну специальную группу соединений составляют такие соединения формулы (I), в которойQ означает C=C-R5a, где R5a означает водород. Другую, представляющую интерес группу соединений составляют такие соединения формулы (I), в которой R2 означает водород;Q означает C=C-R5a, где R5a означает Het2, необязательно замещенный по одному или нескольким атомам заместителем, независимо выбранным из группы, включающей амино, моно- или ди(С 1-4 алкил) амино, гидрокси, С 1-6 алкилокси, аминоС 1-6 алкил, моно- или ди(С 1-4 алкил)аминоС 1-4 алкил, карбоксил, оксо, C1-6 алкил, гидроксиС 1-6 алкил, меркапто, С 1-4 алкилкарбонилокси, С 1-4 алкилоксикарбонил, С 1-4 алкилкарбонилоксиС 1-4 алкил, С 1-4 алкилоксикарбонилС 1-4 алкил. Другую особую группу соединений составляют соединения формулы (I), в которойQ означает C=C-R5a, где R5a означает алкильную группу, необязательно замещенную по одному или нескольким атомам заместителем, независимо выбранным из группы, включающей амино, моно- или ди(С 1-4 алкил)амино, гидрокси, С 1-6 алкилокси, карбоксил, оксо, С 1-4 алкилкарбонилокси, С 1-4 алкилоксикарбонил, С 3-7 циклоалкил, арил, Het1, Het2. Другую, представляющую интерес группу соединений составляют такие соединения формулы (I), в которой L означает -O-C1-6 алкандиил-(С=O)-. Еще одну, представляющую интерес группу соединений составляют такие соединения формулы (I),в которой Q означает C=C-R5a, где R5a означает C1-6 алкил, арил или Het2, каждый из которых необязательно замещен по одному или нескольким атомам заместителем, независимо выбранным из группы,включающей амино, моно- или ди(С 1-4 алкил)амино, гидрокси, С 1-4 алкилокси, карбоксил, оксо, сульфгидрил, С 1-4 алкилкарбонилокси, С 1-4 алкилоксикарбонил, С 3-7 циклоалкил, арил, Het1 и Het2. Другую группу соединений составляют такие соединения формулы (I) или любая их подгруппа, гдеQ означает C=C-R5a, где R5a является водородом. Специальную группу соединений составляют такие соединения формулы (I), в которой R1-L означает группу Het1-O-C(=O), Het2-C1-6 алкандиил-О-С(=O), арил-O-С 1-6 алкандиил-С (=O) или арил-С(=O). Особый интерес представляют такие соединения формулы (I), в которой R1 означает водород, C1-6 алкил, С 2-6 алкенил, арилС 1-6 алкил, С 3-7 циклоалкил, С 3-7 циклоалкилС 1-6 алкил, арил, Het1, Het1C1-6 алкил,Het2, Het2 С 1-6 алкил; в частности R1 означает водород, C1-6 алкил, С 2-6 алкенил, арилС 1-6 алкил, С 3-7 циклоалкил, С 3-7 циклоалкилС 1-6 алкил, арил, Het2, Het2C1-6 алкил. Представляющую интерес группу соединений составляют такие соединения формулы (I), в которойR1 означает водород, C1-6 алкил, С 2-6 алкенил, арилС 1-6 алкил, С 3-7 циклоалкил, С 3-7 циклоалкилС 1-6 алкил,арил, Het1, Het1 С 1-6 алкил, Het2, Het2C1-6 алкил; где Het1 представляет собой 5 или 6-членное кольцо, включающее в качестве членов кольца один или несколько гетероатомов, выбранных из азота, кислорода или серы, и необязательно замещенное по одному или нескольким членам кольца. Предпочтительную группу соединений составляют такие соединения, в которых сульфонамидная группа присоединена к оксиндольной группе в положении 6. Подходящую группу соединений составляют такие соединения формулы (I), в которой R1 означает арил или арилС 1-6 алкил; в частности арильный фрагмент в определении R1 дополнительно замещен по одному или нескольким из членов кольца, при этом каждый заместитель независимо выбирают из С 1-4 алкила, гидрокси, галогена, необязательно моно- или ди(С 1-4 алкил)амино, необязательно моно- или ди(С 1-4 алкил)аминоС 1-4 алкила, нитро и циано; заместитель предпочтительно выбирают из метила, этила,хлора, иода, брома, гидроксигруппы и циано, и, в частности, арильный фрагмент является 6-12-членным кольцом, более предпочтительно арильный фрагмент в определении R1 представляет собой 6-членное кольцо. Подходящей группой соединений являются такие соединения формулы (I), в которой R1 означаетHet2 или Het2 С 1-6 алкил, где Het2 в определении R1 содержит один или несколько гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы; в частности фрагмент Het2 в определении R1 дополнительно замещен по одному или нескольким из членов кольца, при этом каждый заместитель независимо выбирают из С 1-4 алкила, гидрокси, галогена, необязательно моно- или дизамещенного амино,нитро и циано; заместитель предпочтительно выбирают из метила, этила, хлора, иода, брома, гидрокси,амино и циано.-9 010486 Другую группу соединений составляют такие соединения формулы (I), в которой R1 означает Het2 или Het2 С 1-6 алкил, L означает -C(=O)-, -O-С(=O)-, -O-C1-6 алкандиил-С(=O)-; в частности фрагмент Het2 в определении R1 представляет собой ароматический гетероцикл, имеющий 5-6 членов в кольце и содержащий в кольце один или несколько гетероатомов, каждый из которых независимо выбирают из азота,кислорода и серы, в частности фрагмент Het2 представляет собой ароматический гетероцикл, имеющий 5-6 членов в кольце и содержащий в кольце два или более гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы. Подходящую группу соединений составляют такие соединения формулы (I), в которой R1 означаетHet1 или Het1 С 1-6 алкил, где Het1 в определении R1 содержит один или несколько гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы; в частности фрагмент Het1 в определении R1 дополнительно замещен по одному или нескольким из членов кольца, при этом каждый заместитель независимо выбирают из С 1-4 алкила, гидрокси, галогена, необязательно моно- или дизамещенного амино и циано; заместитель предпочтительно выбирают из метила, этила, хлора, иода, брома, гидрокси и циано. Подходящую группу соединений составляют такие соединения формулы (I), в которой R1 означаетHet1 С 1-6 алкил, Het1, где указанный Het1 в определении R1 представляет собой моноциклическую группу,имеющую 5-6 членов в кольце, где Het1 содержит один или несколько гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы; в частности фрагмент Het1 в определении R1 дополнительно замещен по одному или нескольким атомам углерода, при этом каждый заместитель независимо выбирают из С 1-4 алкила, гидрокси, галогена, необязательно моно- или дизамещенного амино и циано; заместитель предпочтительно выбирают из метила, этила, хлора, иода, брома, гидрокси и циано. Подходящую группу соединений составляют такие соединения формулы (I), в которой R1 означаетHet1, где указанный Het1 является бициклической группой и имеет 7-10 членов, при этом Het1 содержит один или несколько гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы; в частности, фрагмент Het1 в определении R1 дополнительно замещен по одному или нескольким атомам углерода, при этом каждый заместитель независимо выбирают из С 1-4 алкила, гидрокси, галогена, необязательно моно- или дизамещенного амино и циано; заместитель предпочтительно выбирают из метила,этила, хлора, иода, брома, гидрокси, амино и циано, и, в частности, фрагмент Het1 содержит 2 или более гетероатомов, выбранных из азота, кислорода и серы; в соответствии с одним аспектом R1 означает бициклический Het1, содержащий в одном из колец гетероатом кислорода, L выбран из -O-(С=O)-, и Q означает C=C-R5a, где R5a и R6 являются водородом. Подходящую группу соединений составляют такие соединения формулы (I), в которой R1 означаетHet1, где указанный Het1 является насыщенной бициклической группой и имеет 5-10 членов в кольце,при этом Het1 содержит один или несколько гетероатомов, каждый из которых независимо выбирают из азота, кислорода и серы; в частности фрагмент Het1 в определении R1 дополнительно замещен по одному или нескольким атомам углерода, при этом каждый заместитель независимо выбирают из С 1-4 алкила,гидрокси, галогена, необязательно моно- или дизамещенного амино и циано; заместитель предпочтительно выбирают из метила, этила, хлора, иода, брома, гидрокси, амино и циано; в частности фрагментHet1 имеет 5-8 членов в кольце; в частности фрагмент Het имеет 6-8 членов в кольце, при этом Het1 содержит 2 или более гетероатомов, выбранных из азота, кислорода и серы. Подходящей группой соединений являются такие соединения формулы (I), в которой R1-L означает группу бистетрагидрофуран-O-С(=O)-. Представляющую интерес группу соединений составляют такие соединения формулы (I), в которойR1 является группой G или G-C1-6 алкил, где группу G выбирают из тиазолильной, имидазолильной, оксазолильной, оксадиазолильной, диоксазолильной, пиразолильной, пиразинильной, имидазолинонильной,хинолинильной, изохинолинильной, индолильной, пиридазинильной, пиридинильной, пирролильной,пиранильной, пиримидинильной, фуранильной, триазолильной, тетразолильной, бензофуранильной, бензоксазолильной, изоксазолильной, изотиазолильной, тиадиазолильной, тиофенильной, тетрагидрофурофуранильной, тетрагидропиранофуранильной, бензотиофенильной, карбазоильной, имидазолонильной,оксазолонильной, индолизинильной, триазинильной, хиноксалинильной, пиперидинильной, пиперазинильной, морфолинильной, тиаморфолинильной, пиразинильной, тиенильной, тетрагидрохинолинильной, тетрагидроизохинолинильной, -карболинильной, диоксанильной, дитианильной, оксоланильной,диоксоланильной, тетрагидротиофенильной, тетрагидропиранильной, тетрагидропиранильной группы; где группа G необязательно конденсирована с бензольным кольцом; где группа G необязательно дополнительно замещена по одному или нескольким членам кольца; группу G предпочтительно выбирают из тиазолильной, имидазолильной, оксазолильной, оксадиазолильной, пиразолильной, пиридинильной группы, необязательно замещенной по одному или нескольким членам кольца. Представляющими интерес соединениями являются такие соединения формулы (I), где R1 означает гексагидрофуро[2,3-b]фуранил или оксазолил. Другими, представляющими интерес соединениями являются такие соединения формулы (I) или такие соединения, принадлежащие к любой их подгруппе, где R1 означает гексагидрофуро[2,3b]фуранил, тетрагидрофуранил, оксазолил, тиазолил, и L означает прямую связь. Представляющими интерес соединениями являются также такие соединения формулы (I) или такие- 10010486 соединения, принадлежащие к любой их подгруппе, где R1 означает гексагидрофуро[2,3-b]фуранил, тетрагидрофуранил, оксазолил, тиазолил, пиридинил или фенил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-6 алкила, гидрокси, амино, галогена, аминоС 1-4 акила и моно- или ди(С 1-4 алкил)аминогруппы; и L является -О-. Еще одними, представляющими интерес соединениями являются такие соединения формулы (I) или такие соединения, принадлежащие к любой их подгруппе, где R1 означает гексагидрофуро[2,3b]фуранил, тетрагидрофуранил, оксазолил или фенил, замещенный одним или несколькими заместителями, независимо выбранными из C1-6 алкила, гидрокси, амино, галогена, аминоС 1-4 алкила и моно- или ди(С 1-4 алкил)аминогруппы; и L означает С 1-6 алкандиил-O-, где -О- присоединен к атому азота амида. Также представляющими интерес соединениями являются такие соединения формулы (I) или такие соединения, принадлежащие к любой их подгруппе, где R1 означает гексагидрофуро[2,3-b]фуранил, тетрагидрофуранил, оксазолил, тиазолил, пиридинил или фенил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из гидрокси, амино, галогена, аминоС 1-4 алкила и моно- или ди(С 1-4 алкил)аминогруппы; и L означает -C1-6 алкандиил, где -О- присоединен к группе R1. Особый интерес представляют такие соединения формулы (I) или такие соединения, принадлежащие к любой их подгруппе, где -L-R1 означает -О-(гексагидрофуро[2,3-b]фуранил), -О-тетрагидрофуранил, -О-метил (необязательно замещенный фенил), -О-метилпиридинил, -О-метилтиазолил, -Ометилоксазолил, -метил-O- (необязательно замещенный фенил) или необязательно замещенный фенил. Предпочтительными заместителями в фенильной группе являются метил, амино, гидрокси, галоген и аминометил. Специальный интерес представляют такие соединения формулы (I) или такие соединения, принадлежащие к любой их подгруппе, где R1 означает гексагидрофуро[2,3-b]фуранил, тетрагидрофуранил, оксазолил, тиазолил, пиридинил или фенил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из С 1-6 алкила, гидрокси, амино, хлора, брома, аминоС 1-4 акила и моноили ди(С 1-4 акил)амино. Другую специальную подгруппу соединений формулы (I) или соединений, принадлежащих к любой их подгруппе, представляют такие соединения, где -L-R1 означает -О-(гексагидрофуро[2,3-b]фуранил),-О-тетрагидрофуранил, -О-метилтиазолил, -O-метилоксазолил, -метил-O-(2,6-диметифенил), -метил-O(4-аминометил-2,6-диметилфенил), -метил-O-(4-амино-2,6-диметилфенил), 3-гидрокси-2-метилфенил или 3-амино-2-метилфенил; и Q означает C=C-R5a, где R5a означает метил или водород, и R6 является водородом. Подходящую группу соединений представляют соединения формулы (I) в виде соли, где соль выбирают из трифторацетата, фумарата, хлорацетата и метансульфоната. Представляющую интерес группу соединений представляют соединения формулы (I), у которых кратность резистентности, определяемая в соответствии с методами, приведенными в настоящем описании, составляет в интервале от 0,01 до 100 по отношению к образцам ВИЧ, имеющим по крайней мере одну мутацию в ВИЧ-протеазе, по сравнению с последовательностью дикого типа (в частности, М 38432,K03455, gi 327742) в положении, выбранном из 10, 71 и 84; в частности в ВИЧ-протеазе имеются по крайней мере две мутации в положениях, выбранных из 10, 71 и 84; в частности соединения имеют кратность резистентности в диапазоне от 0,1 до 100, в частности в диапазоне от 0,1 до 50, преимущественно в диапазоне от 0,1 до 30. Особую группу соединений представляют соединения формулы (I), у которых кратность резистентности по отношению по крайней мере к одной мутантной ВИЧ-протеазе составляет диапазон от 0,1 до 20, и еще больший интерес представляют такие соединения формулы (I), у которых кратность резистентности по отношению по крайней мере к одной мутантной ВИЧ-протеазе составляет диапазон от 0,1 до 10. Представляющие интерес соединения дополнительно имеют величину IC50 по крайней мере 100 нМ по отношению к вирусу дикого типа при проведении in vitro скрининга в соответствии с приведенными в настоящем описании методами. Предпочтительными соединениями являются такие энантиомерные формы соединений формулы (I) или соединений, принадлежащих к любой их подгруппе, которые имеют (1S,2R)-1-бензил-2 гидроксипропильную конфигурацию. Представляющую интерес группу соединений формулы (I) составляют соединения, в которых R5a означает водород. Наиболее предпочтительными соединениями являются гексагидрофуро[2,3-b]фуран-3-иловый эфир(1-бензил-2-гидрокси-3-изобутил[3-(2-метоксибензилиден)-2-оксо-2,3-дигидро-1 Н-индол-5-сульфонил]аминопропил)карбаминовой кислоты; гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-2-гидрокси-3-[3-(4-гидрокси-3-метоксибензилиден)-2-оксо-2,3-дигидро-1 Н-индол-5-сульфонил]изобутиламинопропил)карбаминовой кислоты; гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-3-изобутил[3-(5-метилфуран-2-илметилен)2-оксо-2,3-дигидро-1 Н-индол-5-сульфонил]амино-2-фосфонооксипропил)карбаминовой кислоты; 4-(5-[3-(гексагидрофуро[2,3-b]фуран-3-илоксикарбониламино)-2-гидрокси-4-фенилбутил]изобутилсульфамоил-2-оксо-1,2-дигидроиндол-3-илиденметил)бензойная кислота,их N-оксиды и соли и их стереоизомерные формы. Соединения формулы (I) в общем случае могут быть получены способами, аналогично описанным вWO 95/06030, WO 96/22287, WO 96/28418, WO 96/28463, WO 96/28464, WO 96/28465 и W0 97/18205. Конкретные методики осуществления реакций для получения соединений по настоящему изобретению приведены ниже. В приведенных ниже методиках получения продукты реакций могут быть выделены из реакционной среды и, если необходимо, подвергнуты дальнейшей очистке методами, хорошо известными в данной области, такими как экстракция, кристаллизация, растирание и хроматография. Схема А-1 Промежуточные соединения формулы (а-2) могут быть получены взаимодействием 1,3 дигидроиндол-2-она (а-1) с хлорсульфоновой кислотой при повышенной температуре, предпочтительно в интервале 50-60 С, при перемешивании. Для получения замещенных по атому азота 1,3-дигидроиндол-2-онов формулы (а-3), 1,3 дигидроиндол-2-оны можно подвергнуть взаимодействию с активированным алкильным производнымR6X, таким как алкилгалогенид, в подходящем полярном апротонном растворителе и в присутствии основания. Промежуточные соединения формулы а-4 могут быть получены из промежуточных соединений формулы а-3 в соответствии со схемой А-1. Схема В Получение b-1. Это промежуточное соединение можно получить по методике, приведенной в WO 97/18205. Получение b-2. Промежуточное соединение b-1 перемешивают в органическом растворителе в присутствии катализатора, такого как Pd/C или Pd(OH)2/C в атмосфере водорода. В указанных условиях удаляют защитную группу P1. Получение b-3. К промежуточному соединению b-2 в органическом растворителе добавляют R1-(L)(уходящая группа) и основание. Альтернативно, реагент R1-(L)-(уходящая группа) можно добавлять в присутствии комплекса 1-(3-диметиламинопропил)-3-этилкарбодиимид-хлористо-водородная кислота(EDC) и 1-гидроксибензотриазола (НОВТ) в органическом растворителе. Реакционную смесь перемешивают в течение 6-24 ч при температуре в интервале от 15 до 40 С и затем растворитель выпаривают. Получение b-4. Спиртовой раствор промежуточного соединения b-3 подкисляют с целью удаления защитной группы Р 2. Смесь перемешивают в течение 6-24 ч при температуре в интервале от 15 до 40 С и затем добавляют органический растворитель. рН смеси доводят до нейтрального значения и промывают насыщенным раствором соли. Органический слой сушат и концентрируют, получая промежуточное соединение b-4. Получение b-5. Промежуточное соединение а-4 добавляют к промежуточному соединению b-4 в органическом растворителе в присутствии амина. Смесь перемешивают при температуре в интервале от 15 до 40 С в течение 4-24 ч и промывают щелочным раствором. Органический слой сушат и растворитель выпаривают. Получение b-6. Взаимодействие промежуточного соединения b-5 с альдегидами (R5a-C(=O)-Н) приводит к получению b-6. Реакцию преимущественно проводят в спиртах в присутствии органического основания при повышенной температуре в интервале от 50 С до температуры дефлегмации. Промежуточное соединение с-2 можно получить добавлением амина формулы H2N-R4 к промежуточному соединению с-1 в подходящем растворителе, таком как изопропанол. По схеме С энантиомерно чистые соединения формулы с-2 получают лишь в том случае, когда с-1 является энантимерно чистым. Если с-1 представляет собой смесь стереоизомеров, то с-2 также состоит из смеси стереоизомеров. Подробное описание синтеза 1. Схема А-1. Смесь 46 мл хлорсульфоновой кислоты и 10 г 1,3-дигидроиндол-2-она (а-1) нагревают до 50 С в течение 12 ч. После охлаждения смеси до комнатной температуры ее выливают в воду со льдом и экстрагируют дихлорметаном. Органический слой отделяют, сушат над MgSO4 и растворитель выпаривают,получая 16,33 г (94%) промежуточного соединения а-2 (2-оксо-2,3-дигидро-1 Н-индол-5 сульфонилхлорида). 2. Схема А-2. Для получения замещенных по атому азота 1,3-дигидроиндол-2-онов формулы (а-3), 1,3 дигидроиндол-2-он подвергают взаимодействию с активированным алкильным производным R6X, таким как алкилгалогенид, в подходящем полярном апротонном растворителе, таком как тетрагидрофуран(ТГФ), диметилформамид (ДМФА), дихлорметан (DCM), в присутствии основания, такого как NaH, карбонат калия или карбонат натрия. Смесь перемешивают при комнатной температуре и добавляют активированные алкилы, такие как алкилгалогенид или ацилгалогенид (R6-X, где X является галогеном, преимущественно выбранным из Cl, I, Br; R6 выбран из С 1-6 алкила, -С(=O)-С 1-6 алкила, -СН 2-С(=O)О-С 1-6 алкила). Реакционную смесь перемешивают в течение ночи при комнатной температуре. Затем добавляют воду и смесь экстрагируют подходящим растворителем и сушат над сульфатом магния. Промежуточное соединение а-3 выделяют кристаллизацией или очисткой на силикагеле. Промежуточное соединение а-4 получают в соответствии с методикой, приведенной на схеме А-1. 3. Схема В. 3.1. Получение b-1. Это промежуточное соединение может быть получено в соответствии с методикой, приведенной вWO 97/18205. 3.2. Получение b-2. Смесь промежуточного соединения b-1 в присутствии Pd/C в спиртах и или Pd(OH)2/C в циклогексене или 1,3-циклогексадиене перемешивают в течение ночи в атмосфере водорода с целью удаления защитной группы P1. Для проведения синтеза соединений по настоящему изобретению R2 на этой стадии синтеза может также представлять собой защитную группу P1. Предпочтительной защитной группой является бензил, более предпочтительно P1 и R2 оба являются бензилом, образуя тем самым дибензильный фрагмент. Подходящими спиртами для проведения указанной реакции являются, например, МеОН,EtOH, изопропанол. Смесь отфильтровывают и растворитель упаривают, получая промежуточное соединение b-2. 3.3. Получение b-3. К промежуточному соединению b-2 в органическом растворителе добавляют R1-(L)-(уходящая группа) и основание. Эта реакция представляет собой предпочтительный путь получения карбаматов. Альтернативно, реагент R1-(L)-(уходящая группа) можно добавлять в присутствии комплекса 1-(3 диметиламинопропил)-3-этилкарбодиимид-хлористо-водородная кислота (EDC) и 1-гидроксибензотриазола (НОВТ) или спирта, такого как трет-бутанол, в подходящем растворителе, таком как дихлорметан. Применяя альтернативную стратегию, можно получить амиды. Реакционную смесь перемешивают в течение ночи при комнатной температуре и растворитель выпаривают. Промежуточное соединение очищают на силикагеле. 3.4. Получение b-4. Смесь промежуточного соединения В-3 в спирте, таком как метанол, этанол или изопропанол, подкисляют (например, добавлением HCl) с целью удаления защитной группы Р 2. Подходящими защитными группами являются, в частности, boc, Fmoc, Cbz. Предпочтительной защитной группой является boc. Смесь перемешивают в течение ночи при комнатной температуре. Затем добавляют органический рас- 14010486 творитель. Подходящими растворителями являются, например, этилацетат, ацетонитрил, ацетон, циклогексан, хлороформ, толуол. рН смеси доводят до нейтрального значения и затем смесь промывают насыщенным раствором соли. Нейтрализацию предпочтительно проводят карбонатом натрия. Органический слой сушат над MgSO4 и концентрируют, получая промежуточное соединение b-4. 3.5. Получение b-5. а-4 добавляют к смеси промежуточного соединения b-4 в органическом растворителе в присутствии амина. Этилацетат, ацетонитрил, ацетон, циклогексан, хлороформ и толуол являются примерами подходящих органических растворителей. Амины предпочтительно выбирают, например, из триэтиламина,диизопропиламина. Смесь перемешивают при комнатной температуре в течение 6-18 ч и промывают раствором бикарбоната натрия и затем насыщенным раствором соли. Органический слой сушат надMgSO4 и растворитель выпаривают. Соединение очищают на силикагеле. 3.6. Получение b-6. Взаимодействие промежуточного соединения b-5 с альдегидами (R5a-C(=O)-Н) приводит к получению b-6. Реакцию преимущественно проводят в спиртах в присутствии органического основания, например пиперидина, при температуре в интервале от 65-100 С. 4. Получение соединения 7. 4.1. Получение d-2. Смесь 76,9 г промежуточного соединения d-1 в МеОН и 5 г 10%-ного Pd/C перемешивают в течение ночи в атмосфере водорода. Смесь фильтруют, используя фильтр, такой как целит, и растворитель выпаривают, получая 48 г (96%) промежуточного соединения d-2 (трет-бутил-N-[3-амино-2-гидрокси-4 фенилбутил]-N-изобутилкарбамат). 4.2. Получение d-3. К смеси 7 г промежуточного соединения d-2 в 300 мл дихлорметана (DCM) добавляют 5,63 г 1(3R,3aS,6aR)-гексагидрофуро[2,3-b]фуран-3-ил]оксикарбонилокси]-2,5-пирролидинона (полученный в соответствии с методикой, приведенной в WO 99/67417) и 2,1 г триэтиламина. Реакционную смесь перемешивают в течение ночи при комнатной температуре и растворитель выпаривают. Соединение очищают на силикагеле, получая 9 г (88%) промежуточного соединения с-3 (гексагидро[2,3-b]фуран-3-ил-N-1 бензил-3-[(трет-бутоксикарбонил)(изобутил)амино]-2-гидроксипропилкарбамат). 4.3. Получение d-4. К смеси 9 г промежуточного соединения d-3 в 200 мл этанола по каплям добавляют раствор хлористо-водородной кислоты (например, 6N HCl) в изопропаноле. Смесь перемешивают в течение ночи при комнатной температуре. Добавляют 300 мл этилацетата и смесь трижды промывают раствором бикарбоната натрия и насыщенным раствором соли. Органический слой сушат над MgSO4 и концентрируют, получая 5,5 г (77%) промежуточного соединения d-3 (гексагидро[2,3-b]фуран-3-ил-N-[1-бензил-2-гидрокси 3-(изобутиламино)пропил]карбамат).- 15010486 4.4. Получение d-5. К смеси 3,34 г соединения d-4 в 100 мл DCM и 1,72 г триэтиламина добавляют 2,4 г 2-оксо-2,3 дигидро-1 Н-индол-5-сульфонилхлорида. Смесь перемешивают при комнатной температуре в течение 12 ч и промывают раствором бикарбоната натрия и насыщенным раствором соли. Органический слой сушат над MgSO4 и растворитель удаляют. Соединение очищают на силикагеле и получают 4 г (80%) промежуточного соединения с-5 (гексагидро[2,3-b]фуран-3-ил-N-(1-бензил-2-гидрокси-3-изобутил[(2-оксо-2,3 дигидро-1 Н-индол-5-ил)сульфонил]аминопропил)карбамат) (соединение 21). 4.5. Получение d-6 (соединение 7). К смеси 1 г промежуточного соединения d-5 в 40 мл этанола и 217 мг пиперидина добавляют 206 мг фурфурола. Смесь перемешивают при 85 С в течение 6 ч. Добавляют воду и смесь экстрагируют этилацетатом. Органический слой сушат над MgSO4 и растворитель удаляют. Соединение очищают на силикагеле и получают 1,1 г (95%) соединения 7 (d-6) (гексагидро[2,3-b]фуран-3-ил-N-1-бензил-3-[(3-[(Е)2-фурилметилиден]-2-оксо-2,3-дигидро-1 Н-индол-5-илсульфонил)(изобутил)амино]-2-гидроксипропил карбамат) в смеси 70/30 E/Z по данным ЯМР. Соединения формулы (I) могут быть также превращены в соответствующие N-оксидные формы с помощью известных в данной области методов превращения трехвалентного азота в его N-оксидные формы. Указанную реакцию N-окисления в общем случае можно осуществлять взаимодействием исходного соединения формулы (I) с подходящим органическим или неорганическим пероксидом. Подходящие неорганические пероксиды включают, например, пероксид водорода, пероксиды щелочных или щелочно-земельных металлов, в частности пероксид натрия, пероксид калия; подходящие органические пероксиды включают надкислоты, такие как, например, бензолкарбопероксокислота или галогензамещенная бензолкарбопероксокислота, например 3-хлорбензолкарбопероксокислота, пероксоалкановые кислоты, в частности надуксусная кислота, алкилгидропероксиды, в частности трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие алканолы, в частности этанол и т.п.,углеводороды, в частности толуол, кетоны, в частности 2-бутанон, галогензамещенные углеводороды, в частности дихлорметан, и смеси указанных растворителей. Соединения по настоящему изобретению могут, таким образом, применяться для животных, предпочтительно млекопитающих, и, в частности, для человека в качестве фармацевтических средств как таковые, в смеси друг с другом или в форме фармацевтических препаратов. Кроме того, настоящее изобретение относится к фармацевтическим препаратам, которые в качестве активных компонентов содержат эффективную дозу по крайней мере одного соединения формулы (I) в дополнение к обычным фармацевтически безвредным эксципиентам и вспомогательным агентам. Фармацевтические препараты обычно содержат 0,1-90 мас.% соединения формулы (I). Фармацевтические препараты могут быть приготовлены с помощью известных специалистам в данной области способов,как таковыми. Для этого по крайней мере одно соединение формулы (I) вместе с одним или несколькими твердыми или жидкими фармацевтическими эксципиентами и/или вспомогательными агентами и, если необходимо, в комбинации с другими фармацевтически активными соединениями переводят в подходящую для введения форму или дозированную форму, которую затем можно использовать в качестве фармацевтического средства в терапии человека или ветеринарии. Фармацевтические средства, которые содержат соединение по настоящему изобретению, могут вводиться перорально, парентерально, в частности внутривенно, ректально, путем ингаляции или местно,при этом предпочтительный путь введения будет зависеть от индивидуального случая, в частности от конкретного хода протекания расстройства, лечение которого проводят. Пероральное введение является предпочтительным. Специалист в данной области благодаря своему опыту знаком с вспомогательными средствами, которые подходят для требуемого фармацевтического состава. Помимо растворителей полезными являются также гелеобразующие агенты, основы для суппозиториев, вспомогательные средства для таблеток и другие носители для активных соединений, антиоксиданты, диспергаторы, эмульгаторы, пеногасители,отдушки, консерванты, солюбилизаторы, агенты для создания эффекта депо, буферные соединения или красители. Благодаря своим благоприятным фармацевтическим свойствам, в частности благодаря их активности по отношению к стойким ко многим лекарствам ферментам ВИЧ-протеазам, соединения по настоя- 16010486 щему изобретению полезны при лечении ВИЧ-инфицированных индивидуумов и для профилактики указанных индивидуумов. В общем случае, соединения по настоящему изобретению могут быть полезны при лечении теплокровных животных, инфицированных вирусами, существование которых опосредуется или зависит от фермента протеазы. Состояния, которые можно предупреждать или лечить соединениями по настоящему изобретению, особенно состояния, связанные с ВИЧ и другими патогенными ретровирусами, включают СПИД, СПИД-связанный комплекс (ARC), прогрессирующую генерализованную лимфаденопатию (PGL), а также заболевания центральной нервной системы (ЦНС), вызываемые ретровирусами, такие как, например, опосредованное ВИЧ слабоумие и рассеянный склероз. Таким образом, соединения по настоящему изобретению или любая их подгруппа могут применяться в качестве лекарственных средств против вышеуказанных состояний. Указанное применение в качестве лекарственного средства или способ лечения включают системное введение ВИЧинфицированным субъектам количества соединения, эффективного для борьбы со связанными с ВИЧ состояниями и другими патогенными ретровирусами, особенно ВИЧ-1. Следовательно, соединения по настоящему изобретению могут применяться для приготовления лекарственного средства, полезного для лечения состояний, связанных с ВИЧ и другими патогенными ретровирусами, в частности, лекарственных средств, полезных для лечения пациентов, инфицированных ВИЧ, устойчивым ко многим лекарствам ВИЧ. В соответствии с предпочтительным осуществлением настоящее изобретение относится к применению соединения формулы (I) или любой его подгруппы при изготовлении лекарственного средства для лечения или борьбы с инфекцией или заболеванием, связанным с инфекцией устойчивого ко многим лекарствам ретровируса у млекопитающих, в частности ВИЧ-1 инфекции. Изобретение относится также к способу лечения ретровирусной инфекции или заболевания, связанного с инфекцией устойчивого ко многим лекарствам ретровируса, который заключается во введении нуждающемуся в этом млекопитающему эффективного количества соединения формулы (I) или любой его подгруппы. В соответствии с другим предпочтительным осуществлением настоящее изобретение относится к применению соединения формулы (I) или любой его подгруппы для изготовления лекарственного средства для ингибирования протеазы устойчивого ко многим лекарствам ретровируса у млекопитающего,инфицированного указанным ретровирусом, в частности ретровирусом ВИЧ-1. В соответствии с еще одним предпочтительным осуществлением настоящее изобретение относится к применению соединения формулы (I) или любой его подгруппы для изготовления лекарственного средства для ингибирования репликации устойчивого ко многим лекарствам ретровируса, в частности репликации ВИЧ-1. Соединения по настоящему изобретению могут также найти применение в ингибировании ex vivo образцов, содержащих ВИЧ, или которые, как ожидается, подвергаются действию ВИЧ. Таким образом,соединения по настоящему изобретению могут применяться для подавления ВИЧ, присутствующего в образце выделенной из организма жидкости, которая содержит ВИЧ или, как ожидается, может содержать ВИЧ или может быть подвергнута действию ВИЧ. Также в качестве лекарственного средства может быть использована комбинация антиретровирусного соединения и соединения по настоящему изобретению. Таким образом, настоящее изобретение относится также к продукту, содержащему (а) соединение по настоящему изобретению и (b) другое артиретровирусное соединение в качестве комбинированного препарата для одновременного, раздельного или последовательного применения при лечении ретровирусных инфекций, в частности лечении инфекций, вызываемых устойчивыми ко многим лекарствам ретровирусами. Так, при борьбе или лечении ВИЧ-инфекций, или инфекций, или заболеваний, связанных с ВИЧ-инфекциями, такими как синдром приобретенного иммунодефицита (СПИД) или СПИД-связанный комплекс (ARC), соединения по настоящему изобретению могут совместно вводиться в комбинации, например, с ингибиторами связывания, такими как, например, сульфат декстрана, сурамин, полианионы, растворимый CD4, PRO-542, BMS806; с ингибиторами слияния, такими как, например, Т 20, Т 1249, 5-хеликс, D-пептид, ADS-J1; с ингибиторами связывания корецептора, такими как, например, AMD 3100, AMD-3465, AMD7049, AMD3451GW908, ритонавир, нелфинавир, саквинавир, индинавир, лопинавир, палинавир, BMS 186316, атазанавир, DPC 681, DPC 684, типранавир, AG1776, мозенавир, GS3333, KNI-413, KNI-272, L754394, L756425,LG-71350, PD161374, PD173606, PD177298, PD178390, PD178392, PNU 140135, ТМС-114, маслиновая кислота, U-140690; с ингибиторами гликозилирования, такими как, например, кастаноспермин, деокси- 17010486 ноджиримицин. Комбинация может обеспечить синергический эффект, при этом вирусная инфективность и связанные с ней симптомы могут быть предупреждены, значительно снижены или полностью устранены. Соединения по настоящему изобретению могут также вводиться в комбинации с иммуномодуляторами (в частности, с бропиримином, антителом против -интерферона человека, IL-2, метионинэнкефалином, -интерфероном и налтрексоном), антибиотиками (в частности, пентамидина изотиоратом), цитокинами (в частности, Th2), модуляторами цитокинов, хемокинами или их рецепторами (в частности, CCR5) или гормонами (в частности, гормоном роста) с целью уменьшения интенсивности симптомов заболевания, борьбы или устранения ВИЧ-инфекции и ее симптомов. Указанная комбинированная терапия в виде различных составов может назначаться одновременно, последовательно или независимо друг от друга. Альтернативно, такая комбинация может быть введена в виде единого состава, где активные ингредиенты высвобождаются из состава одновременно или раздельно. Соединения по настоящему изобретению могут также вводиться в комбинации с модуляторами метаболизации, которые применяют после введения лекарственного средства индивидууму. Указанные модуляторы включают соединения, которые препятствуют метаболизации у цитохромов, таких как цитохром Р 450. Известно, что существует несколько изоферментов цитохрома Р 450, одним из которых является цитохром Р 450 ЗА 4. Примером модулятора метаболизации при посредничестве цитохрома Р 450 является ритонавир. Такая комбинированная терапия в виде различных составов может назначаться одновременно, последовательно или независимо друг от друга. Альтернативно, такая комбинация может быть введена в виде единого состава, где активные ингредиенты высвобождаются из состава одновременно или раздельно. Указанный модулятор может вводиться в той же или другой пропорции, что и соединение по настоящему изобретению. Массовое отношение модулятора к соединению по настоящему изобретению (модулятор:соединение по настоящему изобретению) предпочтительно составляет 1:1 или менее,более предпочтительно отношение составляет 1:3 или менее, преимущественно отношение составляет 1:10 или менее, более преимущественно отношение составляет 1:30 или менее. Для получения формы для перорального введения соединения по настоящему изобретению смешивают с подходящими добавками, такими как эксципиенты, стабилизаторы или инертные разбавители, и с помощью обычных методов им придают подходящие формы, такие как таблетки, таблетки с покрытием,твердые капсулы, водные, спиртовые или масляные растворы. Примерами подходящих инертных носителей являются гуммиарабик, магнезия, карбонат магния, фосфат калия, лактоза, глюкоза или крахмал, в частности кукурузный крахмал. В этом случае препарат можно получить в виде сухих или влажных гранул. Подходящими масляными эксципиентами или растворителями являются растительные или животные масла, такие как подсолнечное масло или рыбий жир. Подходящими растворителями для водных и спиртовых растворов являются вода, этанол, растворы сахара и их смеси. Для других форм введения в качестве дополнительных вспомогательных веществ применимы также полиэтиленгликоли и полипропиленгликоли. Для подкожного или внутривенного введения активные соединения, если необходимо, вместе с веществами, которые обычно используют для этой цели, такими как солюбилизаторы, эмульгаторы или другие вспомогательные соединения, вводят в растворы, суспензии или эмульсии. Соединения формулы(I) могут быть лиофилизованы, и полученные лиофилизаты используют, например, для получения инъекций или препаратов для инфузии. Подходящими растворителями являются, например, вода, физиологический раствор или спирты, в частности этанол, пропанол, глицерин, а также растворы сахара, такие как растворы глюкозы или маннита, или же смеси указанных различных растворителей. Подходящими фармацевтическими составами для введения в форме аэрозолей или спреев являются, например, растворы, суспензии или эмульсии соединений формулы (I) или их физиологически переносимых солей в фармацевтически приемлемом растворителе, таком как этанол или вода, или смеси указанных растворителей. Если необходимо, составы могут дополнительно содержать другие фармацевтические вспомогательные соединения, такие как поверхностно-активные вещества, эмульгаторы или стабилизаторы, а также пропеллент. Указанные препараты обычно содержат активное соединение с концентрацией в диапазоне приблизительно от 0,1 до 50%, в частности приблизительно от 0,3 до 3 мас.%. Для увеличения растворимости и/или стабильности соединений формулы (I) в фармацевтических композициях преимущественно применяют -, - или -циклодекстрины и их производные. Растворимость и/или стабильность соединений формулы (I) в фармацевтических композициях могут быть также улучшены сорастворителями, такими как спирты. При получении водных растворов аддитивные соли соединений по настоящему изобретению, очевидно, более подходят благодаря их большей растворимости в воде. Подходящими циклодекстринами являются -, - или -циклодекстрины (CD) или их простые эфиры и их смеси, при этом одна или несколько гидроксигрупп в андроглюкозных фрагментах циклодекстрина замещены С 1-6 алкилом, в частности метилом, этилом или изопропилом, например случайным образом метилированный -CD; гидроксиС 1-6 алкил, в частности гидроксиэтил, гидроксипропил или гидроксибутил; карбоксиС 1-6 алкил, в частности карбоксиметил или карбоксиэтил; C1-6 алкилкарбонил, в част- 18010486 ности ацетил; С 1-6 алкилоксикарбонилС 1-6 алкил или карбоксиС 1-6 алкилоксиС 1-6 алкил, в частности карбоксиметоксипропил или карбоксиэтоксипропил; С 1-6 алкилкарбонилоксиС 1-6 алкил, в частности 2 ацетилоксипропил. В качестве комплексообразователей и/или солюбилизаторов особо следует отметить-CD, случайным образом метилированный -CD, 2,6-диметилCD, 2-гидроксиэтилCD, 2 гидроксиэтилCD, 2-гидроксипропил-Y-CD и (2-карбоксиметокси)пропилCD, и особенно 2 гидроксипропилCD (2-HPCD). Термин "смешанный простой эфир" означает производные циклодекстринов, в которых по крайней мере две гидроксигруппы циклодекстрина этерифицированы различными группами, такими как, например, гидроксипропильная или гидроксиэтильная группа. Представляющий интерес способ получения составов из соединений по настоящему изобретению в комбинации с циклодекстрином или его производными описан в ЕР-А-721331. Хотя приведенные там составы описаны для ингредиентов с противогрибковой активностью, они в равной степени интересны для получения составов с соединениями по настоящему изобретению. Приведенные составы особенно пригодны для перорального введения и включают ингредиент, обладающий антигрибковой активностью,достаточное количество циклодекстрина или его производного в качестве солюбилизатора, водную кислую среду в качестве объемного жидкого носителя и спиртовой сорастворитель, что значительно упрощает приготовление композиции. Указанные составы можно сделать более приятными на вкус путем добавления фармацевтически приемлемых подсластителей и/или отдушек. Другие удобные способы увеличения растворимости соединений по настоящему изобретению в фармацевтических композициях описаны в WO 94/05263, WO 98/42318, ЕР-А-499299 и WO 97/44014,которые все включены в настоящее описание посредством ссылки. Более конкретно соединения по настоящему изобретению могут быть составлены в виде фармацевтической композиции, содержащей терапевтически эффективное количество частиц, содержащих твердую дисперсию, включающую (а) соединение формулы (I) и (b) один или несколько фармацевтически приемлемых водорастворимых полимеров. Термин "твердая дисперсия" означает систему в твердом состоянии (в противоположность жидкому или газообразному состоянию), включающую по крайней мере два компонента, при этом один компонент более или менее равномерно диспергирован в другом компоненте или других компонентах. В том случае, когда указанная дисперсия компонентов такова, что указанная система полностью химически и физически однородна, или гомогенна, или состоит из одной фазы в соответствии с принятым в термодинамике определением, то такую твердую дисперсию называют "твердым раствором". Твердые растворы являются предпочтительными физическими системами, поскольку содержащиеся в них компоненты обычно легко биодоступны для организма, в который их вводят. Термин "твердая дисперсия" охватывает также дисперсии, которые характеризуются меньшей гомогенностью в объеме, чем твердые растворы. Такие дисперсии не полностью химически или физически однородны или содержат более одной фазы. Водорастворимым полимером в частицах преимущественно является полимер, кажущаяся вязкость 2%-ного водного раствора которого при 20 С составляет 1-100 мПас. Предпочтительными водорастворимыми полимерами являются гидроксипропилметилцеллюлоза,или НРМС. В общем случае растворимыми в воде являются НРМС, степень метоксилирования в которых составляет приблизительно от 0,8 до 2,5, и молярное гидроксипропильное замещение составляет приблизительно от 0,05 до приблизительно 3,0. Степень метоксилирования означает среднее количество простых метильных эфирных групп на ангидроглюкозную единицу в молекуле целлюлозы. Молярное гидроксипропильное замещение означает среднее количество молей оксида пропилена, которые вступили во взаимодействие с каждой ангидроглюкозной единицей молекулы целлюлозы. Частицы, указанные выше, можно изготовить, получив сначала твердую дисперсию компонентов, и затем указанную дисперсию необязательно перетирают или перемалывают. Для получения твердых дисперсий существует множество способов, включая экструзию из расплава, сушку распылением и испарение раствора, при этом предпочтительной является экструзия из расплава. Соединения по настоящему изобретению предпочтительно составляют в форме наночастиц, на поверхности которых адсорбирован модификатор поверхности в количестве, достаточном для того, чтобы поддерживать эффективный размер частиц менее 1000 нм. Как полагают, полезными модификаторами поверхности являются такие модификаторы, которые физически прикрепляются к поверхности антиретровирусного агента, но не связываются химически с антиретровирусным агентом. Подходящие модификаторы поверхности могут быть преимущественно выбраны из известных органических и неорганическихфармацевтических эксципиентов. Указанные эксципиенты включают различные полимеры, олигомеры с низкой молекулярной массой, натуральные продукты и поверхностноактивные вещества. Предпочтительные модификаторы поверхности включают неионогенные и анионогенные поверхностно-активные вещества. Еще один, представляющий интерес способ получения составов из соединений по настоящему изобретению предусматривает фармацевтическую композицию, в которой соединения по настоящему изо- 19010486 бретению введены в гидрофильные полимеры, и нанесение полученной смеси в виде пленки на множество небольших шариков, получая, таким образом, композицию с хорошей биодоступностью, которая легко может быть изготовлена и из которой удобно готовить фармацевтические дозировки для перорального введения. Указанные шарики содержат (а) центральное ядро округленной или сферической формы, (b) покрывающую его пленку из гидрофильного полимера и антиретровирусного агента и (с) защитный полимерный слой. Вещества, пригодные в качестве центрального ядра в шариках многообразны, при условии, что указанные вещества являются фармацевтически приемлемыми и имеют подходящие размеры и твердость. Примерами подобных веществ являются полимеры, неорганические соединения, органические соединения и сахариды и их производные. Путь введения может зависеть от состояния субъекта, совместно применяемых лекарств и т.п. Другим аспектом настоящего изобретения является набор или контейнер, содержащий соединение формулы (I) в количестве, эффективном для применения в качестве стандарта или реагента при проведении теста или анализа, с целью определения способности потенциального фармацевтического средства ингибировать ВИЧ-протеазу, рост ВИЧ или и то, и другое. Этот аспект изобретения может найти применение в исследовательских фармацевтических программах. Соединения по настоящему изобретению могут использоваться в фенотипических анализах на устойчивость, таких как известные рекомбинантные анализы, при клиническом лечении болезней, развивающих устойчивость, таких как ВИЧ. Наиболее приемлемой системой мониторинга резистентности является рекомбинантный анализ, известный как Antivirogram. Antivirogram представляет собой высокоавтоматизированный и высокопроизводительный рекомбинантный анализ второго поколения, который позволяет измерить чувствительность, особенно чувствительность вирусов по отношению к соединениям по настоящему изобретению (Hertogs K. et al., Antimicrob Agents Chemother, 1998; 42(2): 269-276,включенной в данное описание посредством ссылки). Интересно, что соединения по настоящему изобретению могут включать химически активные фрагменты, способные образовывать ковалентные связи в локализованных местах таким образом, что указанное соединение обладает повышенной способностью удерживаться в тканях и увеличенным периодом полужизни. Термин "химически активные группы", как использовано в данном описании, означает группы, способные образовывать ковалентную связь. Реакционноспособные группы обычно устойчивы в водной среде и обычно представляют собой карбоксильные, фосфорильные или преимущественно ацильные группы или в виде сложного эфира, или смешанного ангидрида, или имидата, или малеимидата за счет их способности образовывать ковалентную связь с такими функциональными группами, как амино, гидрокси или тиольная группа по месту-мишени, например, в компонентах крови, таких как альбумин. Соединения по настоящему изобретению могут связываться с малеимидом или его производными с образованием конъюгатов. Доза вводимых соединений по настоящему изобретению или их физиологически переносимых солей зависит от индивидуального случая и для достижения оптимального эффекта, как правило, должна быть адаптирована к условиям индивидуального случая. Так, в каждом случае терапии или профилактики она, конечно, зависит не только от частоты введения и эффективности и продолжительности действия применяемых соединений, но и от типа и тяжести инфекции и симптомов, от пола, возраста, массы, совместно применяемых лекарств и индивидуальной восприимчивости человека или животного к лечению,а также от того, является ли терапия неотложной или профилактической. Как правило, дневная доза соединения формулы (I) в случае введения пациенту массой приблизительно 75 кг составляет от 1 мг до 1 г, предпочтительно от 3 мг до 0,5 г. Доза может вводиться в форме индивидуальной дозы или же она может быть разделена на несколько, например две, три, четыре индивидуальные дозы. Экспериментальная часть Получение соединений формулы (I) и их промежуточных соединений.- 20010486 Таблица 1 Соединения по настоящему изобретению получены в соответствии с указанными выше способами. Если стереохимия не указана, то соединение присутствует в виде рацемической смеси. Волнистая связь указывает на то, что заместитель Ra может быть в цис- или транс-положении или в виде рацемической смеси указанных изомеров. Антивирусные анализы Соединения по настоящему изобретению анализируют на антивирусную активность в клеточном анализе. Анализ показывает, что указанные соединения обладают высокой активностью против ВИЧ дикого типа лабораторного штамма ВИЧ (штамм ВИЧ LAI). Клеточный анализ проводят согласно следующей методике. Экспериментальный метод клеточного анализа ВИЧ-инфицированные МТ 4 клетки или МТ 4 клетки с имитацией инфекции инкубируют в течение 5 дней в присутствии различных концентраций ингибитора. По окончании инкубационного периода ВИЧинфицированные клетки были убиты реплицирующим вирусом в контрольных культурах в отсутствие какого-либо ингибитора. Жизнеспособность клеток определяют путем измерения концентрации МТТ,растворимого в воде тетразолиевого красителя желтого цвета, который в митохондриях лишь живых клеток превращается в нерастворимый в воде формазан розового цвета. После солюбилизации изопропанолом полученных кристаллов формазана поглощение раствора определяют на длине волны 540 нм. Величина поглощения напрямую коррелирует с количеством оставшихся в культуре живых клеток после 5 дней инкубирования. Ингибирующую активность соединения контролируют в инфицированных вирусом клетках и выражают величинами ЕС 50 и ЕС 90. Указанные значения обозначают количество соединения,необходимое для защиты, соответственно, 50% и 90% клеток от цитопатогенного воздействия вируса. Токсичность соединения измеряют в клетках с имитацией инфекции и выражают величиной СС 50, которая означает концентрацию соединения, необходимую для 50%-ного ингибирования роста клеток. Индекс селективности (SI) (отношение СС 50/ЕС 50) указывает на избирательность действия ингибитора против ВИЧ. В том случае, когда результаты указаны в виде, например, величин рЕС 50 или рСС 50, то это означает, что результат выражают в виде отрицательного логарифма результата, выраженного, соответственно, величинами ЕС 50 или CC50. Антивирусный спектр Вследствие возрастания числа устойчивых к лекарствам штаммов ВИЧ соединения по настоящему изобретению исследуют на их эффективность по отношению к выделенным в клинических условиях штаммам ВИЧ, которые содержат несколько мутаций (табл. 2 и 3). Указанные мутации связаны со стойкостью к ингибиторам протеазы и приводят к вирусам, которые показывают различную степень фенотипической перекрестной резистентности по отношению к коммерчески доступным лекарствам, таким как,например, саквинавир, ритонавир, нелфинавир, индинавир и ампренавир. Таблица 2 Список мутаций, имеющихся в использованных генах протеазы штаммов ВИЧ (A-F) Результаты. В качестве оценки широты спектра активности соединений по настоящему изобретению определяют кратность резистентности (FR), выражаемую отношением FR=EC50(мутантный штамм)/ЕС 50(штамм- 22010486 ВИЧ LAI). В табл. 3 приведены результаты антивирусных исследований в терминах кратности резистентности. Как видно из таблицы, соединения по настоящему изобретению эффективны для ингибирования широкого спектра мутантных штаммов: Столбец А: значение FR по отношению к мутанту А, столбец В: значение FR по отношению к мутанту В, столбец С: значение FR по отношению к мутанту С, столбец D: значение FR по отношению к мутанту D, столбец Е: значение FR по отношению к мутанту Е, столбец F: значение FR по отношению к мутанту F. Токсичность (Тох) выражают в виде величины рСС 50, которую определяют с использованием клеток с имитацией инфекции. Столбец WT показывает величину рЕС 50 по отношению к штамму ВИЧ-LAI дикого типа. Таблица 3 Результаты исследования токсичности и резистентности по отношению к мутантным штаммам A-F (выражены в виде FR)In vitro фармакокинетические исследования Проникающую способность различных соединений оценивают с использованием методики теста Сасо-2, описанного Augustijns et al. (Augustijns et al. (1998), Int. J. of Pharm., 166, 45-54), где клетки Сасо 2 с количеством пассажей в диапазоне от 32 до 45 выращивают на 24-луночных планшетах для культивирования в течение 21-25 дней. Целостность монослоя клеток определяют, измеряя трансэпителиальное электрическое сопротивление (TEER). Тестирование проводят при рН 7,4 и при концентрации 100 мкМ донорного соединения. Равновесная растворимость в искусственных желудочных соках в термодинамических условиях является хорошей мерой профиля растворимости соединения в желудке и в различных частях кишечника. Кислотность искусственного желудочного сока (SGF) (без пепсина) устанавливают на уровне рН 1,5. Кислотность искусственного кишечного сока (SIF) (без желчных солей) устанавливают на уровне рН 5,рН 6,5, рН 7 и рН 7,5. В экспериментальной методике применяют 96-луночные микропланшеты с плоским дном, при этом в каждую лунку добавляют 1 мг соединения (исходный раствор в метаноле) и упаривают досуха. Соединения вновь солюбилизуют в SCF или SIF и инкубируют в течение ночи на смесителе-качалке при температуре 37 С. После фильтрования концентрацию соединения определяют с помощью УФ-спектрофотометрии. Пероральная доступность у крыс и собак Соединения готовят в виде раствора или суспензии с концентрацией 20 м/мл в ДМСО, PEG400 или 40%-ном циклодекстрине (CD40%) в воде. Для большинства экспериментов с мышами формируют три группы по величине дозы: 1) однократная внутрибрюшинная доза 20 мг/кг состава в ДМСО; 2) однократная оральная доза 20 мг/кг состава в PEG400 и 3) однократная оральная доза 20 мг/кг состава в циклодекстрине. Через регулярные интервалы времени после введения дозы берут пробы крови и определяют концентрацию лекарственного средства в сыворотке с помощью биоаналитического метода ЖХ-МС. Повышение системной биодоступности Для описываемого типа соединений (ингибиторы протеазы) известно, что ингибирование процессов метаболической деградации может заметно повысить системную доступность за счет уменьшения обмена при первичной метаболизации в печени и уменьшения коэффициента очищения в плазме. Этот принцип "повышения" может быть применен к фармакологическому действию лекарства в клинических условиях. Этот принцип может быть также исследован как на крысах, так и на собаках путем одновременного ведения соединения, которое ингибирует ферменты обмена веществ Cyt-р 450. Известными блокираторами являются, например, ритонавир и кетоконазол. Анализы на связывание белком Известно, что белки сыворотки человека, такие как альбумин (HSA) или -1 кислый гликопротеин(AAG), связывают многие лекарства, что приводит к возможному уменьшению эффективности этих соединений. Для того чтобы определить, будет ли это связывание оказывать неблагоприятное воздействие на соединения по настоящему изобретению, активность соединений против ВИЧ измеряют в присутствии сыворотки человека и таким образом оценивают эффект связывания ингибиторов протеазы с указанными белками. Клетки МТ 4 инфицируют ВИЧ LAI со значением разнообразия инфекций (MOI) 0,001-0,01 CCID50(50%-ная инфекционная доза клеточной культуры на клетку, CCID50). После инкубирования в течение 1 ч клетки промывают и помещают на 96-луночный планшет, содержащий серии разбавлений соединения в присутствии 10% FCS (сыворотка плода коровы), 10% FCS+1 мг/мл AAG (1-кислый гликопротеин),10% FCS+45 мг/мл HSA (альбумин сыворотки человека) или 50% сыворотки человека (HS). Через 5 или 6 дней инкубирования рассчитывают величину ЕС 50 (50%-ная эффективная концентрация в анализах на клетках) путем определения жизнеспособности клеток или путем количественной оценки уровня ВИЧрепликации. Жизнеспособность клеток измеряют с помощью вышеуказанного анализа. На 96-луночный планшет, содержащий последовательные разбавления соединения в присутствии 10% FCS или 10%FCS+1 мг/мл AAG, добавляют ВИЧ (дикий тип или устойчивый штамм) и клетки МТ 4 до конечной концентрации, соответственно, 200-250 CCID50/лунка и 30000 клеток/лунка. Через 5 дней инкубирования(37 С, 5% СО 2) жизнеспособные клетки определяют колориметрическим способом с использованием тетразолия МТТ (3-[4,5-диметилтиазол-2-ил]-2,5-дифенилтетразолийбромид) (Pauwels et al., J. Virol.Methods 1988, 20, 309321). Составы Активный ингредиент, в данном случае любое соединение формулы (I), растворяют в органическом растворителе, таком как этанол, метанол или метиленхлорид, предпочтительно смесь этанола и метиленхлорида. Полимеры, такие как сополимер поливинилпирролидона с винилацетатом (PVP-VA) или гидроксипропилметилцеллюлоза (НРМС), обычно с вязкостью 5 мПас, растворяют в органических растворителях, таких как этанол, метанол или метиленхлорид. Полимер преимущественно растворяют в этаноле. Растворы полимера и соединения смешивают и затем сушат методом распыления. Отношение соединение/полимер выбирают в диапазоне от 1/1 до 1/6. Промежуточные значения составляют 1/1,5 и 1/3. Подходящее отношение составляет 1/6. Твердую дисперсию высушенного методом распыления порошка затем помещают в капсулы для введения. Количество лекарственного средства в одной капсуле составляет диапазон от 50 до 100 мг, в зависимости от размера используемых капсул. Таблетки с покрытием Приготовление ядра таблетки. Смесь 100 г активного ингредиента, в данном случае любого соединения формулы (I), 570 г лактозы и 200 г крахмала тщательно смешивают и увлажняют раствором 5 г додецилсульфата натрия и 10 г поливинилпирролидона приблизительно в 200 мл воды. Влажную порошкообразную смесь просеивают, сушат и вновь просеивают. Затем добавляют 100 г микрокристаллической целлюлозы и 15 г гидрированного растительного масла. Все полученное количество хорошо смешивают и прессуют в таблетки, получая 10000 таблеток, каждая из которых содержит 10 мг активного ингредиента. Покрытие. К раствору 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляют раствор 5 г этилцеллюлозы в 150 мл дихлорметана. Затем добавляют 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. Расплавляют 10 г полиэтиленгликоля и растворяют в 75 мл дихлорметана. Последний раствор добавляют к ранее полученному раствору и затем добавляют 2,5 г октадеканоата магния, 5 г поливинилпирролидона и 30 мл концентрированной суспензии красителя и всю полученную смесь гомогенизуют. Ядра таблеток покрывают полученной смесью в аппарате для нанесения покрытий. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение, имеющее формулу его N-оксид, соль, стереоизомерная форма, рацемическая смесь или сложный эфир, гдеR5a выбирают из C1-6 алкила, арила или Het,где арил необязательно замещен по одному или нескольким атомам углерода заместителем, независимо выбранным из группы, включающей ди(С 1-4 алкил)амино, гидрокси, карбоксил, C1-4 алкилокси, С 1-4 алкилкарбонил, Het;Het представляет собой моноциклический или бициклический гетероцикл, содержащий 5-9-членов в цикле, включающий один гетероатом, независимо выбранный из азота, кислорода или серы; указанный гетероцикл необязательно замещен C1-6 алкилом, C1-4 алкилкарбонилокси;R5b представляет собой водород. 2. Соединение по п.1, где R1 представляет собой 5-8-членный гетероцикл, имеющий кислород в качестве гетероатома. 3. Соединение по п.1 или 2, где L означает -O-C(=O)-. 4. Соединение по любому из пп.1-3, где R5a выбирают из C1-6 алкила, арила или Het,где арил необязательно замещен по одному или нескольким атомам углерода заместителем, независимо выбранным из группы, включающей ди(С 1-4 алкил)амино, гидрокси, карбоксил, C1-4 алкилокси, С 1-4 алкилкарбонил, Het;Het представляет собой моноциклический или бициклический гетероцикл, содержащий 5-9-членов в цикле, включающий один гетероатом, выбранный из азота, кислорода или серы; указанный гетероцикл необязательно замещен С 1-С 6 алкилом, C1-4 алкилкарбонилокси;R5b представляет собой водород. 5. Соединение по п.1, где соединением является гексагидрофуро[2,3-b]фуран-3-иловый эфир- 25010486 гексагидрофуро[2,3-b]фуран-3-иловый эфир (1-бензил-3-изобутил[3-(5-метилфуран-2-илметилен)2-оксо-2,3-дигидро-1 Н-индол-5-сульфонил]амино-2-фосфонооксипропил)карбаминовой кислоты; 4-(5-[3-(гексагидрофуро[2,3-b]фуран-3-илоксикарбониламино)-2-гидрокси-4-фенилбутил]изобутилсульфамоил-2-оксо-1,2-дигидроиндол-3-илиденметил)бензойная кислота,его N-оксид и соль или его стереоизомерная форма. 6. Фармацевтическая композиция, включающая эффективное количество по крайней мере одного соединения по любому из пп.1-5 и фармацевтически приемлемый эксципиент. 7. Способ ингибирования протеазы устойчивого ко многим лекарствам ретровируса у млекопитающего, инфицированного указанным ретровирусом, который включает введение ингибирующего протеазу количества соединения по любому из пп.1-5 нуждающемуся в этом указанному млекопитающему. 8. Способ лечения или борьбы с инфекцией или заболеванием, связанным с инфекцией млекопитающего, устойчивой ко многим лекарствам ретровируса, который включает введение указанному млекопитающему эффективного количества по крайней мере одного соединения по любому из пп.1-5. 9. Способ ингибирования репликации устойчивого ко многим лекарствам ретровируса, который включает контактирование ретровируса с эффективным количеством по крайней мере одного соединения по любому из пп.1-5. 10. Применение соединения по любому из пп.1-5 в качестве лекарства. 11. Применение соединения по любому из пп.1-5 при изготовлении лекарственного средства для лечения или борьбы с инфекцией или заболеванием, связанным с инфекцией млекопитающего, устойчивой ко многим лекарствам ретровируса.
МПК / Метки
МПК: A61K 31/40, C07D 209/34, A61P 31/18, C07D 493/04
Метки: замещенные, оксиндолсульфонамидные, спектра, действия, ингибиторы, широкого, вич-протеазы
Код ссылки
<a href="https://eas.patents.su/27-10486-zameshhennye-oksindolsulfonamidnye-ingibitory-vich-proteazy-shirokogo-spektra-dejjstviya.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные оксиндолсульфонамидные ингибиторы вич-протеазы широкого спектра действия</a>
Предыдущий патент: Производное n,n’ -дифенилмочевины, фармацевтическая композиция (варианты) и способ лечения и предупреждения заболеваний и состояний с его использованием (варианты)
Следующий патент: Производные тетрагидронафтиридина, пригодные в качестве лигандов рецептора н3 гистамина
Случайный патент: Катализатор и способ получения алкилированных ароматических углеводородов












