Производные 1-арилсульфонилбензазола в качестве лигандов 5-гидрокситриптамина-6
Формула / Реферат
1. Соединение формулы I
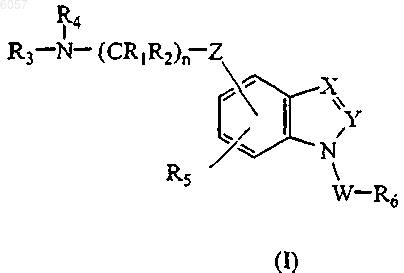
где W означает SO2;
X означает CR7;
Y означает CR8 или N;
Z означает O;
каждый из R1 и R2 означает H;
n означает целое число 2, 3 или 4;
каждый из R3 и R4 независимо означает H, CNR10NR11R12 или группу: C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C3-C6циклоалкил, циклогетероалкил, арил или гетероарил, каждую необязательно замещенную, либо R3 и R4 вместе с атомом, к которому они присоединены, могут образовывать необязательно замещенное 3-6-членное кольцо, необязательно содержащее дополнительный гетероатом, выбираемый из O, N или S;
R5 означает H;
R6 означает необязательно замещенную арильную или гетероарильную группу;
каждый из R7 и R8 означает H;
каждый из R10, R11 и R12 независимо означает H или C1-C4алкил;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где n равно 2.
3. Соединение по п.1 или 2, где R6 означает замещенную арильную или гетероарильную группу.
4. Соединение по п.1 или 2, где R6 означает незамещенную арильную или гетероарильную группу.
5. Соединение по одному из пп.1-4, где R3 и R4, взятые вместе с атомом, к которому они присоединены, образуют 5- или 6-членное кольцо, необязательно содержащее один атом кислорода.
6. Соединение по п.1, выбираемое из группы, включающей
2-{[1-(фенилсульфонил)-1H-индол-4-ил]окси}этиламин;
4-(2-морфолин-4-илэтокси)-1-(фенилсульфонил)-1H-индол;
1-(фенилсульфонил)-4-(2-пиперидин-1-илэтокси)-1H-индол;
N-(2-{[1-(фенилсульфонил)-1H-индол-4-ил]окси}этил)тетрагидро-2H-пиран-4-амин;
N,N-бис(3-метоксибензил)-2-{[1-(фенилсульфонил)-1H-индол-4-ил]окси}этанамин;
N-(3-метоксибензил)-2-{[1-(фенилсульфонил)-1H-индол-4-ил]окси}этанамин;
N,N-диметил-2-{[1-(фенилсульфонил)-1H-индол-4-ил]окси}этанамин;
1-(фенилсульфонил)-4-[2-(1-пиперидинил)этокси]-1H-индазол;
2-{[1-(фенилсульфонил)-1H-индазол-4-ил]окси}этиламин;
N-(2-{[1-(фенилсульфонил)-1H-индазол-4-ил]окси}этил)тетрагидро-2H-пиран-4-амин;
N-(2-{[1-(фенилсульфонил)-1H-индазол-4-ил]окси}этил)тетрагидро-2H-тиопиран-4-амин;
1-[(4-нитрофенил)сульфонил]-4-[2-(1-пиперидинил)этокси]-1H-индазол;
1-[(4-фторфенил)сульфонил]-4-[2-(1-пиперидинил)этокси]-1H-индазол;
4-({4-[2-(1-пиперидинил)этокси]-1H-индазол-1-ил}сульфонил)анилин;
и его фармацевтически приемлемая соль.
7. Способ лечения расстройства центральной нервной системы, связанного с или опосредованного рецептором 5-HT6, у нуждающегося в таком лечении пациента, который включает введение указанному пациенту терапевтически эффективного количества соединения формулы I по одному из пп.1-6.
8. Способ по п.7, где указанное расстройство означает моторное нарушение, патологическое состояние тревоги или нарушение познавательной способности.
9. Способ по п.7, где указанное расстройство означает шизофрению или депрессию.
10. Способ по п.8, где указанное нарушение познавательной способности означает недостаток внимания.
11. Способ по п.8, где указанное нарушение познавательной способности означает болезнь Альцгеймера или болезнь Паркинсона.
12. Фармацевтическая композиция, которая содержит фармацевтически приемлемый носитель и соединение формулы I по одному из пп.1-6.
13. Способ получения соединения по п.1, включающий взаимодействие соединения формулы (Va)
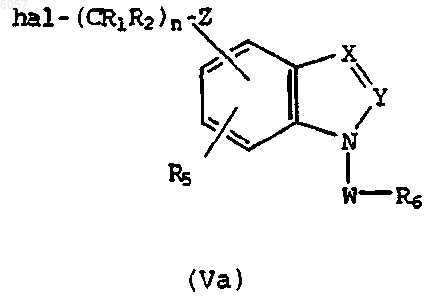
где hal означает галоген, например хлор или бром, и n, W, X, Y, Z, R1, R2, R5 и R6 принимают значения по п.1, с амином формулы
HNR3R4,
где R3 и R4 принимают значения по п.1, причем указанные реагенты защищены, если необходимо, по реакционноспособным участкам и/или по реакционноспособным группам заместителей,
и удаление защитных групп, что приводит к соответствующему соединению формулы (I);
и превращение, в случае необходимости, соединения формулы (I), имеющего реакционноспособную группу заместителя, в другое соединение формулы I или превращение основного соединения формулы (I) в кислотно-аддитивную соль или наоборот.
14. Способ получения соединения по п.1, включающий восстановление соединения формулы (VIa)
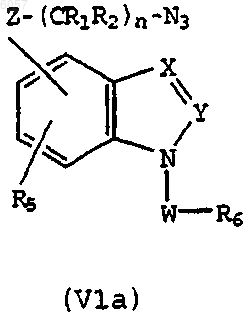
где n, Z, W, X, Y, R1, R2, R5 и R6 принимают значения по п.1, что приводит к соединению формулы (I), где R3 и R4 оба означают H;
и превращение, в случае необходимости, соединения формулы (I), имеющего реакционноспособную группу заместителя, в другое соединение формулы I или превращение основного соединения формулы (I) в кислотно-аддитивную соль, или наоборот.
15. Способ получения соединения по п.1, включающий гидроалкилирование соединения формулы (I) по п.1, где R3 и R4 означают водород, алкилирующим агентом формулы
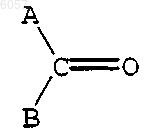
где A и B независимо означают H или необязательно замещенный алкил с 1-5 атомами углерода, алкенил с 2-5 атомами углерода, алкинил с 2-5 атомами углерода, арил, гетероарил или циклогетероалкил,
или A и B вместе означают необязательно замещенное 3-6-членное кольцо циклоалкила или циклогетероалкила, что приводит к соединению формулы (I), где R3 и R4 оба означают метил, или R3 означает водород и R4 означает необязательно замещенный алкил с 1-6 атомами углерода, алкенил с 2-6 атомами углерода, алкинил с 2-6 атомами углерода, арил-CH2-, гетероарил-CH2-, циклоалкил или циклогетероалкил;
и превращение, в случае необходимости, соединения формулы (I), имеющего реакционноспособную группу заместителя, в другое соединение формулы I или превращение основного соединения формулы (I) в кислотно-аддитивную соль или наоборот.
16. Способ получения соединения формулы Ia
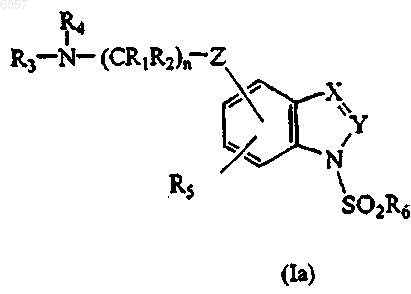
где X означает CR7;
Y означает CR8 или N;
Z означает O;
каждый из R1 и R2 независимо означает H;
n означает целое число 2, 3 или 4;
каждый из R3 и R4 независимо означает H, CNR10NR11R12 или группу: C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C3-C6циклоалкил, циклогетероалкил, арил или гетероарил, каждую необязательно замещенную, либо R3 и R4 вместе с атомом, к которому они присоединены, могут образовывать необязательно замещенное 3-6-членное кольцо, необязательно содержащее дополнительный гетероатом, выбираемый из O, N или S;
R5 означает H;
R6 означает необязательно замещенную группу арил или гетероарил;
каждый из R7 и R8 означает H;
каждый из R10, R11 и R12 независимо означает H или C1-C4алкил;
включающий взаимодействие соединения V'

где Hal означает Cl, Br или I и X, Y, Z, n, R1, R2, R5 и R6 принимают вышеуказанные значения, с амином, HNR3R4, где R3 и R4 принимают вышеуказанные значения, в присутствии растворителя, что дает требуемое соединение формулы Ia.
Текст
006057 Настоящее изобретение касается производных 1-арилсульфонилбензазола, полезных в качестве лигандов 5-гидрокситриптамина-6, способов их получения, содержащих их фармацевтических композиций и способов лечения с применением указанных соединений. Предпосылки изобркетения Считается, что в различные расстройства центральной нервной системы, такие как состояние тревоги, депрессии, моторные нарушения и прочее, вовлечено нарушение нейромедиатора 5-гидрокситриптамина (5-НТ) или серотонина. Серотонин локализован в центральной и периферической нервных системах и известно, что он влияет на многие типы патологических состояний, включающих, среди прочих, психические расстройства, моторную активность, пищевое поведение, сексуальную активность и нейроэндокринную регуляцию. Влияния серотонина регулируются различными подтипами 5-НТрецепторов. Известные 5-НТ-рецепторы включают подтипы семейства 5-НТ 1 (например, 5-НТ 1 А), семейства 5-НТ 2 (например, 5-НТ 2 А), 5-НТ 3, 5-НТ 4, 5-НТ 5, 5-НТ 6 и 5-НТ 7. Недавно идентифицированный подтип рецептора 5-гидрокситриптамина-6 (5-НТ 6) человека был клонирован, и поступило сообщение о пространном распределении его мРНК. Наибольшие уровни мРНК рецептора 5-НТ 6 обнаружены в обонятельном бугорке, неостриатуме, nucleus accumbens, зубчатой извилине и СА 1-, СА 2- и СА 3-областях гиппокапма. Более низкие уровни мРНК рецептора 5-НТ 6 обнаружены в зернистом слое мозжечка, некоторых диэнцефальных ядрах, миндалевидном теле и коре головного мозга. Нозерн-блоттинги позволили обнаружить, что мРНК рецептора 5-НТ 6, по-видимому, исключительно присутствует в головном мозге с незначительной вероятностью его присутствия в периферических тканях. Высокое сродство ряда антипсихотических средств к рецептору 5-НТ 6, в дополнение к локализации его мРНК в неостриатуме, обонятельном бугорке и nucleus accumbens, наводит на мысль о том, что некоторые клинические воздействия таких соединений могут быть опосредованы данным рецептором. Поэтому предполагается, что лиганды рецептора 5-НТ 6 могут найти потенциальное применение при лечении некоторых расстройств ЦНС, таких как состояние тревоги, депрессия, эпилепсия, обсессивно-компульсивное расстройство, нарушения, связанные с недостатком внимания, мигрень, в целях усиления познавательной способности (например, для лечения болезни Альцгеймера), при лечении нарушений сна, пищевых нарушений (например, анорексии или булимии), нейродегенеративных расстройств (например, травма головы или удар), приступов панического расстройства, абстиненции, связанной со злоупотреблением лекарственными средствами (например, кокаином, этанолом, никотином или бензодиазепинами), шизофрении или тому подобного; или при лечении некоторых желудочнокишечных нарушений, таких как синдром раздраженного кишечника. Поэтому цель настоящего изобретения состоит в предложении соединений, полезных в качестве терапевтических средств при лечении ряда расстройств центральной нервной системы, связанных с или опосредованных рецептором 5-НТ 6. Другая цель настоящего изобретения состоит в предоставлении терапевтических способов и фармацевтических композиций, полезных для лечения ряда расстройств центральной нервной системы, связанных с или опосредованных рецептором 5-НТ 6. Особенность настоящего изобретения состоит в том, что предложенные соединения могут также быть использованы для дальнейшего изучения и выяснения роли рецептора 5-НТ 6. Эти и другие цели и особенности настоящего изобретения станут более очевидны из приведенного ниже подробного описания. Краткое описание изобретения Настоящее изобретение касается соединения формулыn означает целое число 2, 3 или 4; каждый из R3 и R4 независимо означает Н, CNR10NR11R12 или группу: C1-С 6 алкил, С 2-С 6 алкенил, С 2 С 6 алкинил, С 3-С 6 циклоалкил, циклогетероалкил, арил или гетероарил, каждую необязательно замещенную, либо R3 и R4 вместе с атомом, к которому они присоединены, могут образовывать необязательно-1 006057 замещенное 3-6-членное кольцо, необязательно содержащее дополнительный гетероатом, выбираемый из О, N или S;R6 означает необязательно замещенную арильную или гетероарильную группу; каждый из R7 и R8 означает Н; каждый из R10, R11 и R12 независимо означает Н или С 1-С 4 алкил; или его фармацевтически приемлемой соли. Настоящее изобретение также касается способов и композиций, полезных для терапевтического лечения расстройств центральной нервной системы, связанных с или опосредованных рецептором 5-НТ 6, а также способов получения соединений формулы (I). Подробное описание изобретения Рецептор 5-гидрокситриптамина-6 (5-НТ 6) является одним из открытых совсем недавно рецепторов, который был идентифицирован молекулярным клонированием. Способность указанного рецептора связывать широкий ряд терапевтических соединений, используемых в психиатрии, в совокупности с его интригующим распределением в головном мозге, вызвала значительный интерес к новым соединениям,которые способны взаимодействовать с указанным рецептором или оказывать на него влияние. В настоящее время не известно полностью селективных агонистов. Предприняты значительные усилия с целью понять возможную роль рецептора 5-НТ 6 в психиатрии, дисфункции познавательной способности,моторной функции и регуляции памяти, настроения и тому подобного. С этой целью проведен широкий поиск соединений, обладающих сродством к связыванию рецептора 5-НТ 6, рассматриваемых в качестве средства для изучения рецептора 5-НТ 6 и в качестве потенциальных терапевтических агентов при лечении расстройств центральной нервной системы. Неожиданно было найдено, что производные 1-арилсульфонилбензазола формулы I обладают сродством к 5-НТ 6. Указанные производные бензазола могут успешно применяться в качестве эффективных терапевтических средств для лечения расстройств центральной нервной системы (ЦНС), связанных с или опосредованных рецептором 5-НТ 6. Таким образом, настоящее изобретение предлагает производные 1 арилсульфонилбензазола формулы In означает целое число 2, 3 или 4; каждый из R3 и R4 независимо означает Н, CNR10NR11R12 или группу: C1-С 6 алкил, С 2-С 6 алкенил, С 2 С 6 алкинил, С 3-С 6 циклоалкил, циклогетероалкил, арил или гетероарил, каждую необязательно замещенную, либо R3 и R4, вместе с атомом, к которому они присоединены, могут образовывать необязательно замещенное 3-6-членное кольцо, необязательно содержащее дополнительный гетероатом, выбираемый из О, N или S;R6 означает необязательно замещенную арильную или гетероарильную группу; каждый из R7 и R8 означает Н; каждый из R10, R11 и R12 независимо означает Н или С 1-С 4 алкил; или их фармацевтически приемлемую соль. Как использовано в описании и формуле изобретения, термин галоген означает Br, Cl, I или F и термин арил означает ароматический углеводород с 6-10 атомами углерода, такой как фенил и нафтил. Термин циклогетероалкил означает 5-7-членную кольцевую систему, содержащую 1 или 2 гетероатома,которые могут быть одинаковыми или различными, выбираемых из N, О или S, и необязательно содержащую одну двойную связь. Характерными примерами циклогетероалкильных кольцевых систем, охватываемых вышеуказанным термином, являются следующие кольца, где Q означает NR, О или S; и R означает Н или необязательный заместитель, как определено ниже. Например, термин циклогетероалкил включает радикалы, полученные из колец, таких как пиперидин, морфолин, пиперазин и пирролидин. Подобным образом, как использовано в описании и формуле изобретения, термин гетероарил означает 5-10-членную ароматическую кольцевую систему, содержащую 1 или 2 гетероатома, которые могут быть одинаковыми или различными, выбираемых из N, О или S, например моно- или бициклическую. Такие гетероарильные кольцевые системы включают пирролил, азолил, оксазолил, тиазолил, имидазолил, фурил, тиенил, хинолинил, изохинолинил, индолинил, бензотиенил, бензофуранил, бензизоксазолил и тому подобное; термин галогеналкил означает группу CnH2n+1, имеющую от 1 до 2n+1 атомов галогенов, которые могут быть одинаковыми или различными; и термин галогеналкокси означает группуOCnH2n+1, имеющую от 1 до 2n+1 атомов галогенов, которые могут быть одинаковыми или различными. В описании и формуле изобретения, когда термины C1-С 6 алкил, С 2-С 6 алкенил, С 2-С 6 алкинил, С 3 С 7 циклоалкил, циклогетероалкил, арил или гетероарил определяются как необязательно замещенные,группами заместителей, которые необязательно присутствуют, могут быть одна или более из числа групп, обычно используемых при получении фармацевтических соединений или в целях модификации таких соединений для воздействия на их структуру/активность, устойчивость, абсорбцию, стабильность или другие полезные характеристики. Конкретные примеры таких заместителей включают атомы галогенов, группы: нитро, циано, тиоцианато, цианато, гидроксил, алкил, галогеналкил, алкокси, галогеналкокси, амино, алкиламино, диалкиламино, формил, алкоксикарбонил, карбоксил, алканоил, алкилтио, алкилсульфинил, алкилсульфонил,карбамоил, алкиламидо, фенил, фенокси, бензил, бензилокси, циклогетероалкил, гетероарил или циклоалкил, предпочтительно атомы галогенов или низшие алкильные группы из 1-6 атомов углерода. Обычно могут присутствовать 0-3 заместителя. Когда любой из вышеуказанных заместителей означает или содержит группу алкильного заместителя, указанный алкильный заместитель может быть прямым или разветвленным и может содержать до 12, предпочтительно до 6, более предпочтительно до 4 атомов углерода, как метил, этил, пропил, изопропил, и н- и трет-бутил. Фармацевтически приемлемые соли могут означать любую кислотно-аддитивную соль, образованную соединением формулы I и фармацевтически приемлемой кислотой, такой как фосфорная, серная,хлористо-водородная, бромисто-водородная, лимонная, малеиновая, малоновая, миндальная, янтарная,фумаровая, уксусная, молочная, азотная, сульфоновая, п-толуолсульфоновая, метансульфоновая кислота или тому подобное. Примерами R6 являются вышеуказанные фенильная, нафтильная и гетероарильная группы, каждая из которых необязательно замещена вышеуказанными заместителями. Примерами Y являются N и СН. Примерами X является СН. Примером n служит целое число 2. Примерами R3 и R4 независимо являются Н, метил, который может быть замещен вышеуказанными заместителями, например необязательно замещенным фенилом, таким как C1-С 6 алкоксифенил; циклогетероалкил, имеющий гетероатом, выбираемый из О или S и, например, имеющий шесть членов в кольце,например, пиранил или тиопиранил, чье кольцо может быть необязательно замещено; либо R2 и R4 могут вместе с азотом означать шестичленное кольцо, такое как морфолинил или пиперидинил, чье кольцо может быть необязательно замещенным. Примерами необязательных заместителей арила (например, фенила) или арилзамещенных алкильных групп (например, бензила) являются атомы галогенов, группы нитро, циано, тиоцианато, цианато,гидроксил, алкил, галогеналкил, алкокси, галогеналкокси, амино, алкиламино, диалкиламино, формил,алкоксикарбонил, карбоксил, алканоил, алкилтио, алкилсульфинил, алкилсульфонил, карбамоил, алкиламидо, фенил, фенокси, бензил и бензилокси, и циклогетероалкил, гетероарилциклоалкил, как указано выше. Предпочтительными соединениями по изобретению являются те соединения формулы I, в которыхn равно 2. Кроме того, предпочтительными соединениями по изобретению являются те соединения формулы I, в которых R6 означает замещенную арильную или гетероарильную группу. Предпочтительными соединениями по изобретению также являются те соединения формулы I, в которых R6 означает незамещенную арильную или гетероарильную группу. Более предпочтительными соединениями по изобретению являются те соединения формулы I, в которых W означает SO2; R1 и R2 означают Н и n равно 2. Другой группой более предпочтительных соединений по изобретению являются те соединения формулы I, в которых W означает SO2; Z означает О; X-3 006057 означает CR7, и R3 и R4, взятые вместе с атомом, к которому они присоединены, образуют 5- или 6 членное кольцо, необязательно содержащее один атом кислорода. К числу предпочтительных соединений по изобретению относятся 2-[1-(фенилсульфонил)-1 Н-индол-4-ил]оксиэтиламин; 4-(2-морфолин-4-илэтокси)-1-(фенилсульфонил)-1 Н-индол; 1-(фенилсульфонил)-4-(2-пиперидин-1-илэтокси)-1 Н-индол;N-(2-[1-(фенилсульфонил)-1 Н-индазол-4-ил]оксиэтил)тетрагидро-2 Н-тиопиран-4-амин; 1-[(4-нитрофенил)сульфонил]-4-[2-(1-пиперидинил)этокси]-1 Н-индазол; 1-[(4-фторфенил)сульфонил]-4-[2-(1-пиперидинил)этокси]-1 Н-индазол; 4-(4-[2-(1-пиперидинил)этокси]-1 Н-индазол-1-илсульфонил)анилин; или их фармацевтически приемлемые соли. Настоящее изобретение также касается способов получения соединений формулы (I), к числу которых относятся следующие: а) взаимодействие соединения формулы (Va) где hal означает галоген, например хлор или бром, и n, m, W, X, Y, Z, R1, R2, R5 и R6 принимают вышеуказанные значения, с амином формулыHNR3R4,где R3 и R4 принимают вышеуказанные значения, причем указанные реагенты защищены соответствующим образом по реакционноспособным участкам и/или по реакционноспособным группам заместителей,и удаление защитных групп, что приводит к соответствующему соединению формулы (I); илиb) восстановление соединения формулы (VIa) где n, Z, W, X, Y, R1, R2, R5 и R6 принимают вышеуказанные значения, что приводит к соединению формулы (I), где R3 и R4 оба означают Н; или с) гидроалкилирование вышеуказанного соединения формулы (I), где R3 и R4 означают водород, алкилирующим агентом формулы где А и В независимо означают Н или необязательно замещенный алкил с 1-5 атомами углерода, алкенил с 2-5 атомами углерода, алкинил с 2-5 атомами углерода, арил, гетероарил или циклогетероалкил, или А и В вместе означают необязательно замещенное 3-6-членное циклоалкильное или циклогетероалкильное кольцо, что приводит к соединению формулы (I), где R3 и R4 оба означают метил, или R3 означает водород и R4 означает необязательно замещенный алкил с 1-6 атомами углерода, алкенил с 2-6 атомами угле-4 006057 рода, алкинил с 2-6 атомами углерода, арил-СН 2-, гетероарил-СН 2-, циклоалкил или циклогетероалкил; илиd) превращение соединения формулы (I), имеющего реакционноспособную группу заместителя, в другое соединение формулы I; илиe) превращение основного соединения формулы (I) в кислотно-аддитивную соль или наоборот. При необходимости в описанных здесь способах реагенты могут быть защищены по реакционноспособным участкам и/или по реакционноспособным группам заместителей путем применения защитных групп. Соединения по изобретению могут быть получены с применением общепринятых синтетических способов и по необходимости стандартных методик разделения и выделения. Например, соединения формулы I, где W означает SO2, R1 и R2 означают Н, и Z означает О, могут быть получены взаимодействием промежуточного гидроксибензазола формулы II с галогеналканолом формулы III в присутствии трифенилфосфина и диэтилазодикарбоксилата с получением галогеналкоксипроизводного формулы IV; сульфонированием производного формулы IV с получением соединения 1-сульфонилбензазола формулыV и замещением галогеновой группы указанного соединения формулы V соответствующим амином, что дает требуемые соединения формулы Iа. Последовательность реакций иллюстрируется схемой процесса Альтернативно, соединения формулы Iа могут быть получены взаимодействием промежуточного соединения формулы V с NaN3, что приводит к соответствующему бензазолилоксиалкилазиду формулыVI; восстановление указанного азида формулы VI дает соединение формулы I, где Z означает О и R1, R2,R3 и R4 означают Н (Ib); и необязательное алкилирование указанного соединения формулы Ib дает соединения формулы Iа. Взаимодействия иллюстрируются схемой процесса II. Схема процесса II-5 006057 Подобным образом, соединения формулы I, где W означает SO2 и Z означает S, могут быть получены с использованием в качестве исходного материала соответствующего бензазолилтиола и с применением, по существу, тех же реакционных последовательностей, что приведены выше на схемах процесса I и II. Соединения формулы I, где W означает SO2 и Z означает NH (Iс), могут быть получены сульфонированием промежуточного нитробензазола формулы VII, приводящим к образованию соответствующего 1-сульфонилпроизводного формулы VIII; восстановлением соединения формулы VIII, приводящим к образованию соответствующего амина формулы IX; взаимодействием указанного амина с галогеналкилальдегидом формулы X, приводящим к образованию производного галогеналкиламина формулы XI; и замещением галогеновой группы производного формулы XI с применением соответствующего амина,что приводит к образованию требуемых соединений формулы Iс. Последовательность взаимодействий представлена схемой процесса III. Схема процесса III Соединения формулы I, где W означает СО и Z означает О, могут быть получены взаимодействием соединения формулы IV с соответствующим галогенидом изоцианата либо карбонила или карбамоила в присутствии основания. Соединения формулы I могут быть получены с использованием указанных и других общепринятых способов из уже готовых исходных материалов. Соединения по изобретению формулы I удобны для применения при лечении расстройств центральной нервной системы (ЦНС), связанных с или опосредованных рецептором 5-НТ 6, таких как моторное, связанное со сменой настроения, психическое, познавательное, нейродегенеративное или тому подобные нарушения. Таким образом, настоящее изобретение предлагает способ лечения расстройства центральной нервной системы (ЦНС), связанного с или опосредованного рецептором 5-НТ 6, у нуждающегося в таком лечении пациента, где данный способ включает введение указанному пациенту терапевтически эффективного количества вышеуказанного соединения формулы I. Соединения могут быть предназначены для введения пероральным и парентеральным способом либо любым другим общепринятым способом, известным как обеспечивающее эффективное введение терапевтического средства нуждающемуся в этом пациенту. Терапевтически эффективное количество, предусмотренное для лечения конкретного расстройства ЦНС, может варьироваться в зависимости от конкретного состояния (состояний), которое лечат, массы,возраста и характера реакции пациента, тяжести расстройства, оценки лечащего врача и тому подобного. Обычно эффективные количества для суточного перорального введения могут составлять приблизительно от 0,01 до 1000 мг/кг, предпочтительно от 0,5 до 500 мг/кг и эффективные количества для парентерального введения могут составлять приблизительно от 0,1 до 100 мг/кг, предпочтительно от 0,5 до 50 мг/кг.-6 006057 Реально на практике соединения изобретения доставляются в организм путем введения соединения или его предшественника в твердой или жидкой форме, либо в чистом виде, либо в комбинации с одним или более общепринятыми фармацевтическими носителями или эксципиентами. Следовательно, настоящее изобретение касается фармацевтической композиции, которая включает фармацевтически приемлемый носитель и эффективное количество вышеуказанного соединения формулы I. Твердые носители, подходящие для применения в композиции по изобретению, включают одно или более веществ, которые могут также действовать как корригенты, лубрикаты, солюбилизаторы, суспендирующие средства, наполнители, средства для скольжения, уплотняющие добавки, связывающие средства, дезинтегрирующие таблетку средства или инкапсулирующие материалы. В порошках носитель может быть тонко измельченным твердым веществом, которое находится в смеси с тонко измельченным соединением формулы I. В таблетках соединение формулы I может быть смешано в подходящих пропорциях с носителем, обладающим необходимыми уплотняющими свойствами, и спрессовано до требуемой формы и размера. Указанные порошки и таблетки могут содержать до 99 мас.% соединения формулы I. Твердые носители, подходящие для применения в композиции по изобретению, включают фосфат кальция, стеарат магния, тальк, сахара, лактозу, декстрин, крахмал, желатин, целлюлозу, метилцеллюлозу, натрийкарбоксиметилцеллюлозу, поливинилпирролидин, низкоплавкие воски и ионообменные смолы. В композиции по изобретению может быть использован любой фармацевтически приемлемый жидкий носитель, подходящий для получения растворов, суспензий, эмульсий, сиропов и эликсиров. Соединения формулы I могут быть растворены или суспендированы в фармацевтически приемлемом жидком носителе, таком как вода, органический растворитель или фармацевтически приемлемые масло или жир,или в их смесях. Указанная жидкая композиция может содержать другие подходящие фармацевтические добавки, такие как солюбилизаторы, эмульгаторы, буферы, консерванты, подсластители, корригенты,суспендирующие средства, загустители, красители, регуляторы вязкости, стабилизаторы, осморегуляторы и тому подобные. Примеры жидких носителей, подходящих для перорального или парентерального введения, включают воду (в частности, содержащую вышеуказанные добавки, например производные целлюлозы, предпочтительно раствор натрийкарбоксиметилцеллюлозы), спирты (включая одноатомные спирты и многоатомные спирты, например гликоли) или их производные, или масла (например, фракционированное кокосовое масло и арахисовое масло). Для целей парентерального введения носителем могут также быть жирные сложные эфиры, такие как этилолеат или изопропилмиристат. Композиции по изобретению, представляющие собой стерильные растворы или суспензии, пригодны для внутримышечного, внутрибрюшинного или подкожного введения. Стерильные растворы могут также быть введены внутривенно. Композиции по изобретению, предназначенные для перорального введения, могут быть в форме либо жидкой, либо твердой композиции. Для лучшего понимания и с целью более наглядной иллюстрации изобретения ниже приведены конкретные примеры. Следующие примеры являются исключительно иллюстративными и не могут рассматриваться как ограничивающие каким-либо образом объем изобретения и приложенных пунктов. Если не оговорено иное, все части означают массовые части. Термины ВЭЖХ и ЯМР означают высокоэффективную жидкостную хроматографию и ядерный магнитный резонанс соответственно. Термины EtOAc and Et2O означают этилацетат и диэтиловый эфир соответственно. Пример 1. Получение 4-(2-хлорэтокси)-1 Н-индола. Раствор 4-гидроксииндола (3,99 г, 30 ммоль), 2-хлорэтанола (6,03 мл, 90 ммоль) и трифенилфосфина (23,6 г, 90 ммоль) в тетрагидрофуране обрабатывают диэтилазодикарбоксилатом (14,1 мл, 90 ммоль) в атмосфере азота при комнатной температуре, перемешивают в течение 2 ч при комнатной температуре и концентрируют в вакууме, получая остаток. К остатку добавляют охлажденный диэтиловый эфир и твердый оксид трифенилфосфина осаждают и удаляют путем фильтрования. Фильтрат концентрируют и очищают флэш-хроматографией (силикагель, EtOAc/гексан: 1,5/8,5), получая масло. После растирания в порошок со смесью Et2O/гексан (1/10) получают указанное в заголовке соединение в виде белого твердого вещества, 4,8 г (82%), т.пл. 60 С, идентифицируемого путем анализа методами ЯМР и массспектроскопии. Перемешиваемый раствор 4-(2-хлорэтокси)-1 Н-индола (3,4 г, 17,4 ммоль) в тетрагидрофуране обрабатывают гидридом натрия (60% в минеральном масле, 1,04 г, 26,1 ммоль) в атмосфере азота при комнатной температуре, перемешивают 30 мин, обрабатывают бензолсульфонилхлоридом (3,4 мл, 26,1 ммоль), перемешивают при комнатной температуре в течение ночи и обрабатывают насыщеннымNаНСО 3 и EtOAc. Образовавшиеся фазы разделяют. Водную фазу экстрагируют EtOAc и объединенные органические фазы промывают последовательно Н 2 О и насыщенным NaCl, сушат над MgSO4 и концентрируют в вакууме, получая остаток. Остаток очищают флэш-хроматографией (силикагель,EtOAc/гексан: 2/8), получая указанное в заголовке соединение в виде не совсем белого твердого вещества, 4,94 г (86%), т.пл. 85-87 С, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 3. Получение 2-[1-(фенилсульфонил)-1 Н-индол-4-ил]оксиэтилазида. Суспензию 4-(2-хлорэтокси)-1-(фенилсульфонил)-1 Н-индола (3,35 г, 10 ммоль) и азида натрия (1,95 г, 30 ммоль) в безводном диметилформамиде перемешивают в атмосфере азота в течение 20 ч при 60 С,выливают в воду и экстрагируют диэтиловым эфиром. Экстракты объединяют, промывают последовательно 1 н. НСl, Н 2 О и насыщенным NaCl, сушат над MgSO4 и концентрируют в вакууме, получая указанный в заголовке продукт в виде не совсем белого твердого вещества, 3,3 г (96%), идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 4. Получение 2-([1-(фенилсульфонил)-1 Н-индол-4-ил]оксиэтиламина. Смесь 2-[1-(фенилсульфонил)-1 Н-индол-4-ил]оксиэтилазида (3,3 г, 9,6 ммоль) и трифенилфосфина (3,67 г, 14 ммоль) в тетрагидрофуране и воде перемешивают в атмосфере азота 24 ч при комнатной температуре и фильтруют. Фильтрат концентрируют в вакууме и полученный остаток очищают флэшхроматографией (силикагель, EtOAc/MeOH/NH4OH: 8,5/1,5/0,05), получая указанное в заголовке соединение в виде не совсем белого твердого вещества, 2,54 г (80%), т.пл. 71-73 С, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 5. Получение 2-[1-(фенилсульфонил)-1 Н-индол-4-ил]оксиэтиламингидрохлорида. Раствор 2-[1-(фенилсульфонил-1 Н-индол-4-ил]оксиэтиламина (0,20 г, 0,63 ммоль) в этилацетате обрабатывают НСl в диэтиловом эфире (1 М, 0,7 мл) и фильтруют. Плотный осадок на фильтре сушат в вакууме, получая указанный в заголовке продукт в виде розового твердого вещества, 0,21 г, т.пл. 198200 С, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 6. Получение N-(2-[1-(фенилсульфонил)-1 Н-индол-4-ил]оксиэтил)тетрагидро-2 Н-пиран 4-амингидрохлорида.-8 006057 обрабатывают уксусной кислотой (0,06 мл) при комнатной температуре, перемешивают в атмосфере азота 18 ч, реакцию гасят добавлением концентрированного водного NH4OH и смесь разбавляют метиленхлоридом и водой. Водный слой отделяют и экстрагируют метиленхлоридом. Органический слой и экстракты объединяют, промывают насыщенным NaCl, сушат над Na2SO4 и концентрируют в вакууме. Полученный остаток очищают флэш-хроматографией (силикагель, EtOAc/MeOH/NH4OH: 9/1/0,05), получая свободный амин указанного в заголовке продукта в виде прозрачного масла, 0,36 г (90%).HCl-соль получают в НСl и этилацетате, что приводит к образованию указанного в заголовке продукта в виде не совсем белого твердого вещества, т.пл. 229-230 С, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Примеры 7 а и 7b. Получение (а). N,N-бис(3-метоксибензил)-N-(2-[1-(фенилсульфонил)-1 Н-индол-4-ил]оксиэтиламина и (b) N-(3-метоксибензил)-N-(2-[1-(фенилсульфонил)-1 Н-индол-4-ил]оксиэтиламингидрохлорида. Смесь 2-[1-(фенилсульфонил)-1 Н-индол-4-ил]оксиэтиламина (0,316 г, 1,0 ммоль), м-анисового альдегида (0,12 мл, 1,0 ммоль) и триацетоксиборгидрида натрия (0,312 г, 1,4 ммоль) в 1,2-дихлорэтане обрабатывают уксусной кислотой (0,06 мл) при комнатной температуре, перемешивают в атмосфере азота при комнатной температуре 18 ч, реакцию гасят добавлением концентрированного водного NH4OH и смесь разбавляют метиленхлоридом и водой. Водный слой отделяют и экстрагируют метиленхлоридом. Органический слой и экстракты объединяют и промывают насыщенным NaCl, сушат над Na2SO4 и концентрируют в вакууме, получая остаток. Остаток очищают флэш-хроматографией (силикагель,EtOAc/MeOH/NH4OH: 9,5/0,5/0,05), получая свободный амин соединения 7 а, 0,20 г (36%) в виде прозрачного масла и свободный амин соединения 7b, 0,135 г (31%) в виде прозрачного масла.HCl-соль соединения 7 а получают в этилацетате и безводном НСl в диэтиловом эфире, что приводит к образованию указанного в заголовке продукта 7 а в виде белого твердого вещества, т.пл. 194-196 С,идентифицируемого путем анализа методами ЯМР и масс-спектроскопии.HCl-соль соединения 7b получают в этилацетате и безводном НСl в диэтиловом эфире, что приводит к образованию указанного в заголовке продукта 7b в виде белого твердого вещества, т.пл. 189-190 С,идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 8. Получение N,N-диметил-N-(2-[1-фенилсульфонил)-1 Н-индол-4-ил]оксиэтиламингидрохлорида.(0,16 мл, 2,0 ммоль) и триацетоксиборгидрида натрия (0,44 6 г, 2,0 ммоль) в 1,2-дихлорэтане перемешивают в атмосфере азота при комнатной температуре в течение 48 ч, реакцию гасят добавлением концентрированного водного NH4OH и смесь разбавляют метиленхлоридом. Водный слой отделяют и экстрагируют метиленхлоридом. Органический слой и экстракты объединяют, промывают насыщенным NaCl,сушат над Na2SO4 и концентрируют в вакууме. Полученный остаток очищают флэш-хроматографией(силикагель, EtOAc/MeOH/NH4OH: 9,5/0,5/0,03), получая свободный амин в виде белого твердого вещества, 0,215 г (36%).HCl-соль получают в этилацетате и безводном НСl в диэтиловом эфире, что приводит к образованию указанного в заголовке продукта в виде белого твердого вещества, т.пл. 140-142 С, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 9. Получение 4-(2-морфолин-4-илэтокси)-1-(фенилсульфонил)-1 Н-индолгидрохлорида. Смесь 4-(2-хлорэтокси)-1-фенилсульфонил-1 Н-индола (0,50 г, 1,5 ммоль) и морфолина (1,30 мл, 15 ммоль) в диметилформамиде (ДМФ) перемешивают в атмосфере азота при 80 С в течение 18 ч, охлаждают до комнатной температуры, гасят водой и экстрагируют диэтиловым эфиром. Объединенные эфирные экстракты промывают насыщенным хлоридом натрия, сушат над MgSO4 и концентрируют в вакууме. Полученный остаток очищают флэш-хроматографией (силикагель, EtOAc/MeOH/NH4OH: 9,7/0,5/0,05), получая свободный амин в виде белого твердого вещества, 0,48 г (83%).HCl-соль получают в этилацетате и НСl, что приводит к образованию указанного в заголовке продукта в виде белого твердого вещества, т.пл. 140-142 С, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 10. Получение 1-(фенилсульфонил)-4-(2-пиперидин-1-илэтокси)-1 Н-индолгидрохлорида. Смесь 4-(2-хлорэтокси)-1-фенилсульфонил-1 Н-индола (0,323 г, 1,0 ммоль) и пиперидина (0,99 мл,10 ммоль) в диметилформамиде (ДМФ) перемешивают в атмосфере азота при 80 С в течение 18 ч, охлаждают до комнатной температуры, гасят водой и экстрагируют диэтиловым эфиром. Эфирные экстракты объединяют, промывают насыщенным хлоридом натрия, сушат над MgSO4 и концентрируют в вакууме. Полученный остаток очищают флэш-хроматографией (силикагель, EtOAc/MeOH/NH4OH: 9,7/0,5/0,05),получая свободный амин в виде светло-желтого масла, 0,34 г (88%).HCl-соль получают в этилацетате и НСl, что приводит к образованию указанного в заголовке продукта в виде светло-желтого твердого вещества, т.пл. 131-133 С, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 11. Получение 4-(2-хлорэтокси)-1 Н-индазола. Перемешиваемый раствор 1-ацетил-4-(2-хлорэтокси)индазола (1,50 г, 6,3 ммоль) в метаноле обрабатывают соляной кислотой (6,3 мл, 1,0 М НСl в Et2O, 6,3 ммоль) при комнатной температуре, нагревают при 65 С в атмосфере азота в течение 18 ч, охлаждают до комнатной температуры и концентрируют в вакууме. Полученный остаток нейтрализуют 1 н NaOH (6,0 мл) и разбавляют Н 2 О и этилацетатом. Фазы разделяют и водную фазу экстрагируют этилацетатом. Объединенные органические фазы промывают водой и насыщенным NaCl, сушат над Na2SO4 и концентрируют в вакууме, получая указанный в заголовке продукт (1,2 г) в виде желтого твердого вещества, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 12. Получение 4-(2-хлорэтокси)-1-(фенилсульфонил)-1 Н-индазола. Перемешиваемый раствор 4-(2-хлорэтокси)-1 Н-индазола (1,1 г, 5,59 ммоль) в тетрагидрофуране обрабатывают NaH (0,335 г, 60% в минеральном масле, 8,39 ммоль) в атмосфере азота при комнатной температуре, перемешивают 30 мин, обрабатывают бензолсульфонилхлоридом (0,86 мл, 6,71 ммоль), перемешивают при комнатной температуре в течение 18 ч, гасят водой и разбавляют этилацетатом. Фазы разделяют и органическую фазу промывают водой и насыщенным раствором соли, сушат над MgSO4 и концентрируют в вакууме. Полученный остаток очищают флэш-хроматографией (силикагель,- 10006057EtOAc/гексан: 3/7), получая требуемый продукт в виде белого твердого вещества, 1,75 г (93%), т.пл. 102104 С, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 13. Получение 1-(фенилсульфонил)-4-[(1-пиперидинил)этокси]-1 Н-индазолгидрохлорида. Смесь 4-(2-хлорэтокси)-1-(фенилсульфонил)-1 Н-индазола (0,337 г, 1,0 ммоль) и пиперидина (0,20 мл, 2,0 ммоль) в N,N-диметилформамиде (ДМФ) перемешивают в атмосфере азота при 80 С в течение 18 ч, охлаждают, гасят водой со льдом и разбавляют этилацетатом. Фазы разделяют. Водную фазу экстрагируют этилацетатом. Органические фазы объединяют, промывают водой и насыщенным растворомNaCl, сушат над MgSO4 и концентрируют в вакууме, получая желтый маслянистый остаток. Остаток растворяют в этилацетате, обрабатывают 1 М НСl (1 мл, 1 М НСl в Et2O) и фильтруют. Плотный осадок на фильтре сушат в вакууме, получая указанный в заголовке продукт в виде не совсем белого твердого вещества, 354 мг, т.пл. 87-89 С, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Пример 14. Получение 2-[(1-фенилсульфонил)-1 Н-индазол-4-ил]оксиэтиламингидрохлорида.(0,382 г, 5,87 ммоль) в N,N-диметилформамиде перемешивают в атмосфере азота при 60 С в течение 24 ч, охлаждают, гасят 1 н. НСl и экстрагируют этилацетатом. Объединенные экстракты промывают водой и насыщенным NaCl, сушат над Na2SO4 и концентрируют в вакууме, получая желтый твердый остаток. Остаток растворяют в тетрагидрофуране, обрабатывают трифенилфосфином (0,771 г, 2,94 ммоль) и водой, перемешивают при комнатной температуре в течение 18 ч и концентрируют в вакууме. Полученный остаток очищают флэш-хроматографией (силикагель, EtOAc/2M NH3 в МеОН: 90/10), получая свободный амин (0,41 г) в виде смолы. Смолу растворяют в этилацетате и обрабатывают безводным НСl в диэтиловом эфире. Реакционную смесь фильтруют и плотный осадок на фильтре сушат на воздухе, что приводит к указанному в заголовке продукту в виде белого твердого вещества, т.пл. 201-203 С, идентифицируемого путем анализа методами ЯМР и масс-спектроскопии. Примеры 15 и 16. Получение 1-(арилсульфонил)-4-[2-(1-пиперидинил)этокси]-1 Н-индазолгидрохлорида. Применяя в основном те же методики, что описаны в примерах 11, 12 и 13, но используя соответствующий арилсульфонилхлорид, соединения, приведенные в табл. I, получают и идентифицируют путем анализа методами ЯМР и масс-спектроскопии. Таблица I Суспензию 2-[1-(фенилсульфонил)-1 Н-индазол-4-ил]оксиэтиламина (0,10 г, 0,31 ммоль), тетрагидро-4 Н-пиран-4-она (0,03 мл, 0,31 ммоль) и триацетоксиборгидрида натрия (0,097 г, 0,43 ммоль) в 1,2 дихлорэтане обрабатывают уксусной кислотой (0,03 мл) при комнатной температуре, оставляют перемешиваться в атмосфере азота при комнатной температуре в течение 18 ч, гасят 1 н. NaOH (2 мл) и разбавляют водой и смесью 4:1 метиленхлорид:изопропанол. Фазы разделяют и водную фазу дополнительно экстрагируют смесью 4:1 метиленхлорид:изопропанол. Органические фазы объединяют, промывают водой и насыщенным раствором соли, сушат надNa2SO4 и концентрируют в вакууме. Полученный остаток растворяют в смеси 4:1 этилацетат: изопропанол, обрабатывают безводным НСl в диэтиловом эфире и фильтруют, получая указанный в заголовке продукт в виде белого твердого вещества, т.пл. 173-175 С, идентифицируемый путем анализа методами ЯМР и масс-спектроскопии. Пример 18. Получение N-(2-[(1-фенилсульфонил)-1 Н-индазол-4-ил]оксиэтил)тетрагидро-2 Нтиопиран-4-амингидрохлорида. Применяя в основном те же методики, что описаны в примере 17, и заменяющий один из реагентов тетрагидротиопиран-4-он, получают указанный в заголовке продукт в виде белого твердого вещества,т.пл. 182-184 С, идентифицируемый путем анализа методами ЯМР и масс-спектроскопии. Пример 19. Получение 4-(4-[2-(1-пиперидинил)этокси]-1 Н-индазол-1-илсульфонил)анилина.(0,39 г, 0,91 ммоль) в метаноле обрабатывают никелем Ренея с последующей обработкой гидразином (0,2 мл, 6,3 ммоль), перемешивают при 0 С в течение 2 ч и декантируют. Катализатор промывают смесью 3:7 метанол:метиленхлорид. Промывные воды и декантированный ранее отстоявшийся верхний слой объединяют и концентрируют в вакууме. Полученный остаток очищают флэш-хроматографией (силикагель,EtOAc/2M NH3 в метаноле 8:2), получая указанный в заголовке продукт в виде белого твердого вещества,0,15 г, т.пл. 149-150 С (разл.), идентифицируемый путем анализа методами ЯМР и масс-спектроскопии. Пример 20. Сравнительная оценка испытуемых соединений на сродство к связыванию 5-НТ 6. Сродство испытуемых соединений к рецептору 5-НТ 6 серотонина оценивают следующим способом. Клетки, культивируемые в питательной среде Hela, экспрессирующие клонированные рецепторы 5 НТ 6 человека, собирают и центрифугируют при низкой скорости (1000 х g) в течение 10,0 мин для удаления культуральной среды. Собранные клетки суспендируют в половинном объеме свежего физиологического раствора, содержащего фосфатный буфер, и повторно центрифугируют при той же скорости. Указанную операцию повторяют. Собранные клетки затем гомогенизируют в десяти объемах 50 мМTris.HCl (pH 7,4) и 0,5 мМ EDTA. Гомогенат центрифугируют при 40000 х g в течение 30,0 мин и собирают осадок. Полученный в пробирке после центрифугирования осадок ресуспендируют в 10 объемахTris.HCl-буфера и повторно центрифугируют при той же скорости. Конечный осадок в пробирке после центрифугирования суспендируют в небольшом объеме Tris.HCl-буфера, и содержание тканевого белка определяют в аликвотах объемом 10-25 мкл. Альбумин сыворотки теленка используют в качестве стандартного белка в анализе на белок по методу, описанному в Lowry et al., J. Biol. Chem., 193:265 (1951). Объем суспендированных мембран клеток доводят до величины, требуемой для получения концентрации тканевого белка в суспензии 1,0 мг/мл. Полученную суспензию мембран (10-кратно сконцентрированные) делят на аликвотные пробы объемом 1,0 мл и хранят при -70 С до использования в последующих экспериментах на связывание. Эксперименты на связывание выполняют в 96-луночных титрационных микропланшетах в общем объеме 200 мкл. К каждой лунке добавляют следующую смесь: 80,0 мкл инкубационного буфера, полу- 12006057 ченного в 50 мМ Tris.HCl-буфере (рН 7,4), содержащем 10,0 мМ MgCl2 и 0,5 мМ EDTA, и 20 мкл [3H]LSD (S.A., 86,0 Кю/ммоль, поставщик Amersham Life Science), 3,0 нМ. Константа диссоциации, KD, для[3H]LSD на рецепторе 5-НТ 6 серотонина человека равна 2,9 нМ, как определено по связыванию при насыщении с возрастающими концентрациями [3H]LSD. Взаимодействие инициируют заключительным добавлением 100,0 мкл суспензии ткани. Неспецифическое связывание измеряют в присутствии 10,0 мкМ метиотепина. Испытуемые соединения добавляют в объеме 20,0 мкл. Взаимодействию дают осуществляться в темноте в течение 120 мин при комнатной температуре, по прошествии указанного времени комплекс связанный лиганд-рецептор отфильтровывают на 96 луночном унифильтре Packard Filtermate 196 Harvester. Задержанный на фильтровальном диске связанный комплекс оставляют сушиться на воздухе и радиоактивность измеряют на Packard TopCount,снабженном шестью фотоумножителями, после добавления 40,0 мкл сцинтиллятора Microscint-20 к каждой плоской лунке. Унифильтровальный планшет теплоизолируют и подсчитывают радиоактивность в PackardTopCount при эффективности трития 31,0%. Специфическое связывание с рецептором 5-НТ 6 определяют по общей связанной радиоактивности за вычетом количества, связанного в присутствии 10,0 мкМ немеченого метиотепина. Связывание в присутствии различных концентраций выражают через процент от специфического связывания в отсутствие испытуемого соединения. Результаты представляют в виде графика зависимости log % связывания от log концентрации испытуемого соединения. Анализ полученных точек методом нелинейной регрессии, выполненный на компьютере с помощью программы Prism, дает значения как IC50, так и Ki для испытуемых соединений с доверительными пределами 95%. На основе полученных точек строят графическую кривую, рассчитанную методом линейной регрессии, из которой определяют значение IC50, и значение Ki определяют из следующего уравнения:Ki = IC50/(1 + L/KD),где L означает концентрацию используемого радиоактивного лиганда и KD означает константу диссоциации лиганда для данного рецептора, обе величины выражены в нМ. Используя данный анализ, получают следующие значения Ki, которые сравнивают с соответствующими значениями, полученными для характерных соединений, известных своей способностью к связыванию рецептора 5-НТ 6. Данные приведены в табл. II ниже. Таблица II% ингибирования при концентрации 1 мкМ- 13006057 Как видно из приведенных выше результатов, соединения по настоящему изобретению обладают высокой степенью сродства к рецептору 5-НТ 6 серотонина. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы In означает целое число 2, 3 или 4; каждый из R3 и R4 независимо означает Н, CNR10NR11R12 или группу: C1-С 6 алкил, С 2-С 6 алкенил, С 2 С 6 алкинил, С 3-С 6 циклоалкил, циклогетероалкил, арил или гетероарил, каждую необязательно замещенную, либо R3 и R4 вместе с атомом, к которому они присоединены, могут образовывать необязательно замещенное 3-6-членное кольцо, необязательно содержащее дополнительный гетероатом, выбираемый из О, N или S;R6 означает необязательно замещенную арильную или гетероарильную группу; каждый из R7 и R8 означает Н; каждый из R10, R11 и R12 независимо означает Н или С 1-С 4 алкил; или его фармацевтически приемлемая соль. 2. Соединение по п.1, где n равно 2. 3. Соединение по п.1 или 2, где R6 означает замещенную арильную или гетероарильную группу. 4. Соединение по п.1 или 2, где R6 означает незамещенную арильную или гетероарильную группу. 5. Соединение по одному из пп.1-4, где R3 и R4, взятые вместе с атомом, к которому они присоединены, образуют 5- или 6-членное кольцо, необязательно содержащее один атом кислорода. 6. Соединение по п.1, выбираемое из группы, включающей 2-[1-(фенилсульфонил)-1 Н-индол-4-ил]оксиэтиламин; 4-(2-морфолин-4-илэтокси)-1-(фенилсульфонил)-1 Н-индол; 1-(фенилсульфонил)-4-(2-пиперидин-1-илэтокси)-1 Н-индол;N-(2-[1-(фенилсульфонил)-1 Н-индазол-4-ил]оксиэтил)тетрагидро-2 Н-тиопиран-4-амин; 1-[(4-нитрофенил)сульфонил]-4-[2-(1-пиперидинил)этокси]-1 Н-индазол; 1-[(4-фторфенил)сульфонил]-4-[2-(1-пиперидинил)этокси]-1 Н-индазол; 4-(4-[2-(1-пиперидинил)этокси]-1 Н-индазол-1-илсульфонил)анилин; и его фармацевтически приемлемая соль. 7. Способ лечения расстройства центральной нервной системы, связанного с или опосредованного рецептором 5-НТ 6, у нуждающегося в таком лечении пациента, который включает введение указанному пациенту терапевтически эффективного количества соединения формулы I по одному из пп.1-6. 8. Способ по п.7, где указанное расстройство означает моторное нарушение, патологическое состояние тревоги или нарушение познавательной способности. 9. Способ по п.7, где указанное расстройство означает шизофрению или депрессию. 10. Способ по п.8, где указанное нарушение познавательной способности означает недостаток внимания. 11. Способ по п.8, где указанное нарушение познавательной способности означает болезнь Альцгеймера или болезнь Паркинсона.- 14006057 12. Фармацевтическая композиция, которая содержит фармацевтически приемлемый носитель и соединение формулы I по одному из пп.1-6. 13. Способ получения соединения по п.1, включающий взаимодействие соединения формулы (Va) где hal означает галоген, например хлор или бром, и n, W, X, Y, Z, R1, R2, R5 и R6 принимают значения по п.1, с амином формулыHNR3R4,где R3 и R4 принимают значения по п.1, причем указанные реагенты защищены, если необходимо, по реакционноспособным участкам и/или по реакционноспособным группам заместителей,и удаление защитных групп, что приводит к соответствующему соединению формулы (I); и превращение, в случае необходимости, соединения формулы (I), имеющего реакционноспособную группу заместителя, в другое соединение формулы I или превращение основного соединения формулы (I) в кислотно-аддитивную соль или наоборот. 14. Способ получения соединения по п.1, включающий восстановление соединения формулы (VIa) где n, Z, W, X, Y, R1, R2, R5 и R6 принимают значения по п.1, что приводит к соединению формулы (I),где R3 и R4 оба означают Н; и превращение, в случае необходимости, соединения формулы (I), имеющего реакционноспособную группу заместителя, в другое соединение формулы I или превращение основного соединения формулы (I) в кислотно-аддитивную соль, или наоборот. 15. Способ получения соединения по п.1, включающий гидроалкилирование соединения формулы где А и В независимо означают Н или необязательно замещенный алкил с 1-5 атомами углерода, алкенил с 2-5 атомами углерода, алкинил с 2-5 атомами углерода, арил, гетероарил или циклогетероалкил,или А и В вместе означают необязательно замещенное 3-6-членное кольцо циклоалкила или циклогетероалкила, что приводит к соединению формулы (I), где R3 и R4 оба означают метил, или R3 означает водород и R4 означает необязательно замещенный алкил с 1-6 атомами углерода, алкенил с 2-6 атомами углерода, алкинил с 2-6 атомами углерода, арил-СН 2-, гетероарил-СН 2-, циклоалкил или циклогетероалкил; и превращение, в случае необходимости, соединения формулы (I), имеющего реакционноспособную группу заместителя, в другое соединение формулы I или превращение основного соединения формулы (I) в кислотно-аддитивную соль или наоборот. 16. Способ получения соединения формулы Iаn означает целое число 2, 3 или 4; каждый из R3 и R4 независимо означает Н, CNR10NR11R12 или группу: C1-С 6 алкил, С 2-С 6 алкенил, С 2 С 6 алкинил, С 3-С 6 циклоалкил, циклогетероалкил, арил или гетероарил, каждую необязательно замещенную, либо R3 и R4 вместе с атомом, к которому они присоединены, могут образовывать необязательно замещенное 3-6-членное кольцо, необязательно содержащее дополнительный гетероатом, выбираемый из О, N или S;R6 означает необязательно замещенную группу арил или гетероарил; каждый из R7 и R8 означает Н; каждый из R10, R11 и R12 независимо означает Н или С 1-С 4 алкил; включающий взаимодействие соединения V' где Hal означает Cl, Br или I и X, Y, Z, n, R1, R2, R5 и R6 принимают вышеуказанные значения, с амином,HNR3R4, где R3 и R4 принимают вышеуказанные значения, в присутствии растворителя, что дает требуемое соединение формулы Iа.
МПК / Метки
МПК: C07D 209/08, A61P 25/28, A61K 31/4045
Метки: лигандов, 5-гидрокситриптамина-6, производные, 1-арилсульфонилбензазола, качестве
Код ссылки
<a href="https://eas.patents.su/17-6057-proizvodnye-1-arilsulfonilbenzazola-v-kachestve-ligandov-5-gidroksitriptamina-6.html" rel="bookmark" title="База патентов Евразийского Союза">Производные 1-арилсульфонилбензазола в качестве лигандов 5-гидрокситриптамина-6</a>
Предыдущий патент: Инертный анод для электролиза алюминия
Следующий патент: Способ улучшения качества осаждения материала на катод
Случайный патент: Оконное стекло для транспортного средства и способ его получения












