Соли и полиморфные формы эффективного антидиабетического соединения
Формула / Реферат
1. Бензолсульфонатная соль соединения формулы (I)
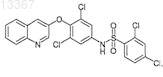
2. Полиморфная форма I соединения по п.1.
3. Полиморфная форма по п.2, которая имеет максимум температуры плавления, определенный дифференциальной сканирующей калориметрией, приблизительно от 186,3 до 189,5°С.
4. Полиморфная форма по п.2, которая обладает теплотой плавления, определенной дифференциальной сканирующей калориметрией, приблизительно от 81,5 до 89,9 Дж/г.
5. Полиморфная форма по п.2, которая имеет точку плавления приблизительно между 180 и 200°С.
6. Полиморфная форма по п.2, которая имеет точку плавления приблизительно 186°С.
7. Полиморфная форма по п.2, которая обнаруживает основные пики дифракции рентгеновских лучей на порошке приблизительно на 7,0, 19,5, 22,0, 24,0, 24,5 и 28° 2q при использовании Cu Ka излучения.
8. Полиморфная форма по п.2, которая обнаруживает основные пики абсорбции в инфракрасной области спектра приблизительно при длине волны 1567, 1461, 913, 895 и 881 см-1.
9. Полиморфная форма по п.2, которую получают путем кристаллизации безилатной соли указанного соединения формулы (I) из этанола.
10. Полиморфная форма II соединения по п. 1.
11. Полиморфная форма по п.10, которая имеет максимум температуры плавления, определенный дифференциальной сканирующей калориметрией, приблизительно 233,7°С.
12. Полиморфная форма по п.10, которая обладает теплотой плавления, определенной дифференциальной сканирующей калориметрией, приблизительно 98,9 Дж/г.
13. Полиморфная форма по п.10, которая имеет точку плавления выше чем приблизительно 230°С.
14. Полиморфная форма по п.10, которая имеет точку плавления приблизительно 233°С.
15. Полиморфная форма по п.10, которая обнаруживает основные пики дифракции рентгеновских лучей на порошке приблизительно на 15, 19, 20,5, 23,5, 24,5, 25, 26,5, 29,5 и 30,5° 2q при использовании Cu Ka излучения.
16. Полиморфная форма по п.10, которая обнаруживает основные пики абсорбции в инфракрасной области спектра приблизительно при длине волны 1573, 1469, 1459, 912 и 859 см-1.
17. Полиморфная форма по п.10, которую получают путем кристаллизации безилатной соли указанного соединения формулы (I) из этанола.
18. Фармацевтическая композиция, содержащая соль по п.1 и фармацевтически приемлемый разбавитель, наполнитель или носитель.
19. Фармацевтическая композиция, содержащая полиморфную форму по п.2 или 10 и фармацевтически приемлемый разбавитель, наполнитель или носитель.
20. Фармацевтическая композиция по п.19, где полиморфная форма находится в чистом виде.
21. Способ лечения состояния или нарушения, опосредованного рецептором PPAR-g, у субъекта, где указанный способ включает в себя введение субъекту терапевтически эффективного количества соединения по пп.1, 2 или 10.
22. Способ в соответствии с п.21, где указанное PPAR-g-опосредованное состояние или нарушение является нарушением метаболизма или воспалительным состоянием.
23. Способ в соответствии с п.22, где указанное нарушение метаболизма выбирают из группы, состоящей из диабета, ожирения, гиперхолестеринемии, гиперлипидемии, дислипидемии, гипертриглицеридемии, гипергликемии, инсулинорезистентности и гиперинсулинемии.
24. Способ в соответствии с п.23, где указанным расстройством метаболизма является диабет II типа.
25. Способ в соответствии с п.22, где указанное воспалительное состояние выбирают из группы, состоящей из ревматоидного артрита и атеросклероза.
26. Способ в соответствии с п.21, где указанным субъектом является человек.
Текст
013367 1. Ссылка на родственные заявки Данная заявка подтверждает преимущество предварительной заявки США No. 60/508470, зарегистрированной 3 октября 2003, которая включена в текст в виде ссылки во всей полноте. 2. Область изобретения Настоящее изобретение относится к солям эффективного модулятора активируемого пероксисомным пролифератором -рецептора ("PPAR-") и к его полиморфным формам, композициям, содержащим соли и полиморфные формы, способам получения солей или полиморфных форм и способам их использования для диагностики или лечения, например, диабета II типа (и его осложнений), гиперхолестеринемии (и родственных заболеваний, связанных с аномально высокими или низкими уровнями липопротеинов или триглицеридов в плазме) и воспалительных заболеваний. 3. Предыдущий уровень техники в данной области Активируемые пероксисомным пролифератором рецепторы (PPAR) являются белкамитрансдукторами, принадлежащими к суперсемейству стероидных/тиреоидных/ретиноидных рецепторов. Первоначально, рецепторы PPAR были идентифицированы как одиночные рецепторы, без известных лигандов, тем не менее получили название по их способности опосредовать плейотропные эффекты пероксисомных пролифераторов жирных кислот. Указанные рецепторы функционируют как регулируемые лигандом факторы транскрипции, которые контролируют экспрессию генов-мишеней путем связывания с их чувствительной ДНК-последовательностью как гетеродимеры с ретиноидным X рецептором("RXR"). Гены-мишени кодируют ферменты, вовлеченные в метаболизм липидов и дифференцировку адипоцитов. Таким образом, обнаружение факторов транскрипции, вовлеченных в контролирование метаболизма липидов, способствует пониманию регуляции энергетического гомеостаза у позвоночных, и также определению целей для развития терапевтических средств, предназначенных для лечения заболеваний, таких как ожирение, диабет и дислипидемия. Активируемый пероксисомным пролифератором -рецептор ("PPAR-") является одним из членов суперсемейства ядерных рецепторов лиганд-активируемых факторов транскрипции и, как было показано, экспрессируется в жировой ткани. Экспрессия рецептора индуцируется на ранних стадиях дифференцировки некоторых преадипоцитных клеточных линий. Проведенное дополнительное исследование показывает, что PPAR- играет главнейшую роль в липогенезе, участвуя в каскаде передачи сигнала. Рецептор PPAR- также регулирует ob/лептин ген, вовлекаемый в регулирование энергетического гомеостаза и дифференцировку адипоцитов, которая, как было показано, является критической стадией, на которую направлены средства для лечения ожирения и диабетических состояний. С учетом клинического значения PPAR-, соединения, которые модулируют функцию PPAR-, могут быть использованы для развития новых терапевтических средств. Эффективные модуляторы PPARбыли описаны, например, в международной патентной публикации WO 01/00579 (соответствующей заявке США No. 09/606433), патентной публикации США No. US 2002/0037928 А 1 и патентах СШАUS 6200995 В 1 и US 6583157 В 2. Один из указанных модуляторов, идентифицированный в тексте как соединение 101, находится в стадии клинических разработок для диагностики или терапевтического лечения диабета II типа. Разработка модулятора может способствовать пероральной терапии для лечения указанного выше заболевания. Каждое фармацевтическое соединение имеет оптимальную терапевтическую концентрацию в крови и летальную концентрацию. Биодоступность соединения определяет эффективность дозировки в лекарственной композиции, необходимой для достижения идеального уровня в крови. Если лекарственное средство может кристаллизоваться в виде двух или более полиморфных форм, различающихся по биодоступности, оптимальная доза будет зависеть от присутствующей в композиции полиморфной формы. Такие лекарственные средства проявляют минимальную разницу между терапевтическими и летальными концентрациями. Хлорамфеникол-3-пальмитат (САРР), например, является антибиотиком широкого спектра действия, который, как известно, кристаллизуется в виде по крайней мере трех полиморфных форм и одной аморфной формы. Наиболее устойчивая форма, А, продается. Разница в биоактивности между этой полиморфной формой и другой формой, В, составляет восемь раз, таким образом, возникает риск смертельных передозировок соединения при непреднамеренном введении как формы В, вследствие изменений в течение получения и/или хранения. Поэтому, органы государственного регулирования, такие как Департамент США по контролю за качеством пищевых продуктов, медикаментов и косметических средств, начали устанавливать жесткие контроли за содержанием полиморфных форм активного компонента в твердых дозированных формах. Вообще, что касается лекарственных средств, которые существуют в виде полиморфных форм, во всяком случае, отличных от чистых средств, следует выпускать для продажи термодинамически предпочтительную полиморфную форму, а орган государственного регулирования может требовать контролирования от партии к партии. Таким образом, как для медицинских, так и для коммерческих целей, важно производить и продавать чистое лекарственное средство в его наиболее термодинамически устойчивой полиморфной форме, по существу, свободной от других кинетически благоприятных полиморфных форм.-1 013367 Новые формы таких модуляторов могут способствовать развитию композиций для лечения заболеваний, таких как диабет II типа. Например, соединения в виде солей и полиморфных форм солей, как известно в фармацевтической области, оказывают влияние, например, на растворимость, скорость распада, биодоступность, химическую и физическую устойчивость, текучесть, ломкость и способность соединения к сжимаемости, а также безопасность и эффективность лекарственных продуктов, приготовленных на основе соединения (смотри, например, Knapman, К. Modern Drug Discoveries, 2000: 53). Таким образом, идентификация соли или свободного основания модуляторов с оптимальными физическими и химическими свойствами будет содействовать развитию таких модуляторов PPAR- в качестве фармацевтических средств. Наиболее благоприятными физическими и химическими свойствами являются легкость и воспроизводимость приготовления, кристалличность, негигроскопичность, растворимость в воде, устойчивость к излучению в видимой и ультрафиолетовой области спектра, низкая скорость деградации в условиях повышения температуры и влажности, низкая скорость изомеризации между изомерными формами и безопасность при продолжительном введении человеку. Свободное основание и определенные фармацевтически приемлемые соли соединения 101 описаны в заявке США No. 09/606433, соответствующей международной патентной публикации WO01/00579 и патенту США No. 6583157 В 2. Фармацевтически приемлемые соли кислоты, перечисленные в указанных патентах, включают в себя, наряду с другими, соли, произведенные из неорганических кислот, подобных хлористо-водородной кислоте, бромисто-водородной кислоте, азотной кислоте, угольной кислоте, также включены кислые соли угольной кислоты, соли, произведенные из фосфорной кислоты, вторичные кислые соли фосфорной кислоты, первичные кислые соли фосфорной кислоты, соли, произведенные из серной кислоты, кислые соли серной кислоты, соли, произведенные из йодисто-водородной кислоты или фосфористой кислоты, и соли, произведенные из относительно нетоксичных органических кислот, подобных уксусной кислоте, пропионовой кислоте, изомасляной кислоте, щавелевой кислоте, малеиновой кислоте, малоновой кислоте, бензойной кислоте, янтарной кислоте, пробковой кислоте, фумаровой кислоте, миндальной кислоте, фталевой кислоте, бензолсульфокислоте, п-толуолсульфокислоте, лимонной кислоте, винной кислоте и метансульфокислоте. Не следует принимать как указание, что любые из описанных солей указанной выше структуры являются лучше других. Заявители обнаружили, что не все соли в равной степени являются пригодными, исходя из перечисленных выше свойств. Таким образом, настоящее изобретение обращает внимание на необходимость в создании эффективных модуляторов рецептора PPAR- в твердом состоянии с улучшенными свойствами для промышленного производства и биодоступности. 4. Сущность изобретения. Настоящее изобретение относится к новым солям и новым полиморфным формам модулятора рецептора PPAR-, которые используют в лечении или профилактике состояний и нарушений, включающих, но не ограниченных состояниями и нарушениями, связанными с энергетическим гомеостазом, метаболизмом липидов, дифференцировкой адипоцитов, воспалительными и диабетическими состояниями,такими как, например, гипергликемия и гиперинсулинемия. В некоторых аспектах, полиморфные формы являются полиморфными формами солей согласно изобретению. Изобретение также охватывает как водные, так и безводные полиморфные формы модулятора рецептора PPAR-. He стремясь ограничиться каким-либо отдельным теоретическим подходом, заявители полагают, что такие свойства, как устойчивость при хранении, сжимаемость, объемная плотность или способность к растворению солей и полиморфных форм соединения, представляются благоприятными для промышленного производства, приготовления композиции и биодоступности модулятора PPAR-. Изобретение также относится к фармацевтическим композициям, содержащим соли и/или полиморфные формы модулятора PPAR-, и к способам использования указанных композиций для лечения, например, состояний и нарушений, связанных с энергетическим гомеостазом, метаболизмом липидов, дифференцировкой адипоцитов, воспалительными и диабетическими состояниями, включающими, но не ограничивающимися гипергликемией и гиперинсулинемией. Соли и полиморфные формы образуются из соединения 101, которое описано в заявке США No. 09/606433, соответствующей международной патентной публикацииWO 01/00579, и в патенте СШАNo. US 6583157 В 2, содержание которых включено в текст в виде ссылки во всей полноте. Соединение 101 имеет следующую структуру (I): В некоторых предпочтительных аспектах настоящее изобретение предоставляет соли соединения-2 013367 101, произведенные из бензолсульфокислоты. Заявители обнаружили, что соли соединения 101, произведенные из бензолсульфокислоты, обладают превосходными свойствами, описанными подробно ниже. В других аспектах настоящее изобретение предоставляет полиморфные формы солей соединения 101, произведенных из бензолсульфокислоты, идентифицированных как форма I и форма II, причем каждая описана подробно ниже. Настоящее изобретение также предоставляет фармацевтические композиции, содержащие соль или полиморфную форму соединения согласно изобретению и фармацевтически приемлемый разбавитель,наполнитель или носитель. Настоящее изобретение также предоставляет способы лечения или профилактики диабета II типа,гиперхолестеринемии, воспалительных заболеваний или родственного нарушения, включающие в себя введение субъекту, нуждающемуся в таком лечении или такой профилактике, терапевтически эффективного количества соли или полиморфной формы соединения согласно изобретению. Настоящее изобретение также предоставляет способы лечения или профилактики состояния или нарушения, опосредованного рецептором PPAR-, включающие в себя введение субъекту, нуждающемуся в таком лечении или такой профилактике, терапевтически эффективного количества соли или полиморфной формы соединения согласно изобретению. В других вариантах осуществления изобретения настоящее изобретение предоставляет способы получения, выделения и/или проверки качеств солей и полиморфных форм соединения согласно изобретению. Новые соли и полиморфные формы соединения согласно изобретению являются особенно пригодными в качестве активных фармацевтических ингредиентов для приготовления композиций с целью использования для животных или человека. Таким образом, настоящее изобретение охватывает использование указанных твердых форм в качестве конечного продукта лекарственного средства. Соли, полиморфные формы и конечные продукты лекарственного средства согласно изобретению используют, например, для лечения или профилактики состояний и нарушений, связанных с энергетическим гомеостазом, метаболизмом липидов, дифференцировкой адипоцитов и воспалением. 5. Краткое описание рисунков На фиг. 1 представлена структура соединения 101; На фиг. 2 представлена типичная схема синтеза соединения 101; На фиг. 3 представлена другая типичная схема синтеза соединения 101; На фиг. 4 представлена термограмма дифференциальной сканирующей калориметрии образца, содержащего форму I; На фиг. 5 представлена картина дифракции рентгеновских лучей на порошке образца, содержащего форму I; На фиг. 6 представлена изотерма сорбции влаги образцом, содержащим форму I; На фиг. 7 представлен спектр образца, содержащего форму I, в инфракрасной области излучения; На фиг. 8 представлена термограмма дифференциальной сканирующей калориметрии образца, содержащего форму II; На фиг. 9 представлена картина дифракции рентгеновских лучей на порошке образца, содержащего форму II; На фиг. 10 представлен спектр образца, содержащего форму II, в инфракрасной области излучения. 6. Подробное описание изобретения 6.1. Определения. Термины "лечить", "обработка" или "лечение", употребляемые в тексте, относятся к способу ослабления или устранения заболевания и/или сопутствующих ему симптомов. Термины "предотвращать","предотвращение" или "профилактика", употребляемые в тексте, относятся к способу защиты субъекта от заболевания. Употребляемый в тексте термин "диабет" относится к сахарному диабету I типа (ювенильный диабет) или сахарному диабету II типа (инсулиннезависимый сахарный диабет или NIDDM), предпочтительно сахарному диабету II типа. Употребляемый в тексте термин "опосредованное PPAR- состояние или нарушение" или "опосредованное PPAR- состояние или заболевание" или тому подобное относится к состоянию, нарушению или заболеванию, характеризующемуся аномальной активностью PPAR-, например, меньшей или большей по сравнению с нормой. Несоответствующая активность рецептора PPAR- может возникать в результате экспрессии рецептора PPAR- в таких клетках, которые в норме не экспрессируют PPAR-, также может возникать в результате повышения экспрессии рецептора PPAR- (приводящей, например, к определенному энергетическому гомеостазу, метаболизму липидов, дифференцировке адипоцитов и воспалительным нарушениям и заболеваниям) или уменьшения экспрессии рецептора PPAR- (приводящей, например, к определенному энергетическому гомеостазу, метаболизму липидов, дифференцировке адипоцитов и воспалительным нарушениям и заболеваниям). Опосредованное рецептором PPAR- состояние или нарушение может быть полностью или частично опосредовано несоответствующей активно-3 013367 стью рецептора PPAR-. Однако состояние или нарушение, опосредованное рецептором PPAR-, является состоянием или нарушением, в котором модулирование рецептора PPAR- приводит к некоторому воздействию на основное состояние или заболевание (например, модулятор рецептора PPAR- приводит к некоторому улучшению здоровья у больных, по крайней мере, у некоторых больных). Типичные состояния и заболевания, опосредованные рецептором PPAR-, включают в себя нарушения метаболизма,например, диабет, диабет II типа, ожирение, гипергликемию, инсулинорезистентность, гиперинсулинемию, гиперхолестеринемию, гипертензию, гиперлипопротеинемию, гиперлипидемию, гипертриглицеридемию и дислипидемию, и воспалительные состояния, например, ревматоидный артрит и атеросклероз,но не ограничиваются указанными состояниями и заболеваниями. Термин "модулировать" в его различных видах относится к способности соединения увеличивать или уменьшать функцию или активность, связанную с отдельным рецептором, активируемым пероксисомным пролифератором, предпочтительно рецептором PPAR-у. Модулирование, как оно описано в тексте, включает в себя ингибирование или активацию рецептора PPAR-, либо прямо, либо косвенно. Ингибиторы представляют собой соединения, которые, например, при связывании частично или полностью блокируют стимуляцию, уменьшают, предотвращают, замедляют активацию, инактивируют, уменьшают или ликвидируют чувствительность или регулируют сигнальную трансдукцию по типу обратной связи,например, как антагонисты. Активаторы представляют собой соединения, которые, например, при связывании индуцируют, повышают, делают возможным, активируют, облегчают, усиливают активацию,повышают чувствительность или осуществляют позитивную регуляцию сигнальной трансдукции, например, как агонисты. Также, модулирование активности рецептора PPAR- предназначено охватить антагонистический эффект, агонистический эффект, частичный антагонистический и/или агонистический эффект относительно активности, связанной с рецептором PPAR-. Термин "композиция", который употребляют в тексте, предназначен охватить продукт, содержащий заданные ингредиенты (и в заданных количествах, если указано), а также любой продукт, который образуется, прямо или косвенно, из комбинации заданных ингредиентов в заданных количествах. Под "фармацевтически приемлемым" подразумевают разбавитель, наполнитель или носитель, который должен быть совместимым с другими ингредиентами композиции и не должен оказывать отрицательное воздействие на реципиент. Термин "терапевтически эффективное количество" относится к количеству соли или полиморфной формы соединения, которое будет вызывать биологический или медицинский ответ ткани, системы, животного или человека в целом, изучаемый исследователем, ветеринаром, лечащим врачом или другим клиницистом, или которое является достаточным для предотвращения развития одного или более симптомов заболевания, подвергаемого лечению, или для ослабления до некоторой степени одного или более симптомов заболевания. Термин "субъект" определяют в тексте, чтобы включить животных, таких как млекопитающие,включая, но не ограничиваясь приматами (например, человек), крупным рогатым скотом, овцами, козами, лошадьми, собаками, кошками, кроликами, крысами, мышами и тому подобными. В предпочтительных вариантах осуществления изобретения субъектом является человек. Термин "алкил", сам по себе или как часть другого заместителя, означает, если не указано особо,углеводородный радикал с прямой или разветвленной цепью или циклический углеводородный радикал,или их комбинацию, который может быть полностью насыщенным, моно- или полиненасыщенным радикалом и может включать в себя ди- и мультивалентные радикалы, имеющие намеченное число атомов углерода (т.е., C1-С 10 означает от одного до десяти углеродов). Примеры насыщенных углеводородных радикалов включают в себя группы, такие как метил, этил, н-пропил, изопропил, н-бутил, трет-бутил,изобутил, сек-бутил, циклогексил, (циклогексил)метил, циклопропилметил, гомологи и изомеры, например, н-пентила, н-гексила, н-гептила, н-октила и тому подобных. Ненасыщенная алкильная группа является группой, имеющей одну двойную связь или более двойных связей или тройных связей. Примеры ненасыщенных алкильных групп включают в себя винил, 2-пропенил, кротил, 2-изопентенил, 2(бутадиенил), 2,4-пентадиенил, 3-(1,4-пентадиенил), этинил, 1- и 3-пропинил, 3-бутинил и более высокие гомологи и изомеры. Термин "алкил", если не указано особо, также предназначен включить производные алкила, определенные более подробно ниже как "гетероалкил", "циклоалкил" и "алкилен". Термин "алкилен", сам по себе или как часть другого заместителя, означает двухвалентный радикал, произведенный из алкана, примером чего является -СН 2 СН 2 СН 2 СН 2-. Обычно алкильная группа имеет от 1 до 24 атомов углерода, причем группы, имеющие 10 или меньше атомов углерода, будут предпочтительными в настоящем изобретении. "Низший алкил" или "низший алкилен" является алкильной или алкиленовой группой с более короткой цепью, обычно имеющей восемь или меньше атомов углерода. Термин "гетероалкил", сам по себе или в сочетании с другим термином, означает, если не указано особо, углеводородный радикал с устойчивой прямой или разветвленной цепью или циклический углеводородный радикал или их комбинацию, состоящий из установленного числа атомов углерода и из одного - трех гетероатомов, выбранных из группы, состоящей из О, N, Si и S, и где атомы азота и серы,возможно, являются окисленными, и гетероатом азота, возможно, является четвертичным.-4 013367 Гетероатом(ы) О, N и S может находиться у любого положения внутренней части гетероалкильной группы. Гетероатом Si может находиться у любого положения гетероалкильной группы, включая положение, у которого алкильная группа присоединена к остатку молекулы. Примеры включают в себя группы -СН 2-СН 2-О-СН 3, -CH2-CH2-NH-CH3, -CH2-CH2-N(CH3)-CH3, -CH2-S-CH2-CH3, -CH2-CH2-S(O)-CH3, CH2-CH2-S(O)2-CH3, -CH=CH-O-CH3, -Si(CH3)3, -CH2-CH=N-OCH3 и -CH=CH-N (CH3)-CH3. До двух гетероатомов может следовать один за другим, как, например, у групп -CH2-NH-OCH3 и -CH2-OSi(CH3)3.Также в термин "гетероалкил" включены такие радикалы, которые подробно описаны ниже как"гетероалкилен" и "гетероциклоалкил". В некоторых вариантах осуществления изобретения, арильная группа является "замещенной". В таких вариантах, заместители для арильных групп являются различными и выбранными из галогена, -OR', OC(O)R', -NR'R", -SR', -R', -CN, -NO2, -CO2R', -CONR'R", -C(O)R', -OC(O)NR'R", -NR"C(O)R',-NR"C(O)2R', -NR'-C(O)NR"R"', -NH-C(NH2)=NH, -NR'С (NH2) =NH, -NH-C (NH2) =NR', -S(O)R', -S(O)2R',-S(O)2NR'R", -N3, -CH(Ph)2, перфтор (C1-C4) алкокси и перфтор (C1-C4) алкила, в количестве, варьирующем от нуля до общего числа свободных валентностей на ароматической кольцевой системе; и где R', R" и R'" независимо выбирают из группы, состоящей из водорода, (C1-C8) алкила и гетероалкила, незамещенного арила, (незамещенный арил)-(C1-C4)алкила и (незамещенный арил) окси-(C1-C4)алкила. Термин "фармацевтически приемлемые соли" предназначен включить соли активных соединений,которые получают с использованием относительно нетоксичных кислот. Аддитивные соли кислоты могут быть получены путем взаимодействия нейтральной формы таких соединений с достаточным количеством желаемой кислоты, либо неразбавленной, либо в подходящем инертном растворителе. Примеры фармацевтически приемлемых аддитивных солей кислоты включают такие, которые произведены из неорганических кислот, подобных хлористоводородной кислоте, бромистоводородной кислоте, азотной кислоте, угольной кислоте, также включены кислые соли угольной кислоты, соли, произведенные из фосфорной кислоты, вторичные кислые соли фосфорной кислоты, первичные кислые соли фосфорной кислоты, соли, произведенные из серной кислоты, кислые соли серной кислоты, соли, произведенные из йодистоводородной кислоты или фосфористой кислоты и тому подобное, а также соли, произведенные из относительно нетоксичных органических кислот, подобных уксусной кислоте, пропионовой кислоте,изомасляной кислоте, щавелевой кислоте, малеиновой кислоте, малоновой кислоте, бензойной кислоте,янтарной кислоте, пробковой кислоте, фумаровой кислоте, миндальной кислоте, фталевой кислоте, бензолсульфокислоте, толуолсульфокислоте, включая п-толуолсульфокислоту, м-толуолсульфокислоту и отолуолсульфокислоту, лимонной кислоте, винной кислоте, метансульфокислоте и тому подобное. Также включены соли аминокислот, такие как аргинат и тому подобное, и соли органических кислот, подобных глюкуроновой кислоте или галактуроновой кислоте и тому подобной (смотри, например, Berge et al., J.Pharm. Sci. 66:1-19 (1977. Нейтральные формы соединений могут быть регенерированы путем взаимодействия соли с основанием или кислотой и выделения исходного соединения обычным способом. Исходная форма соединения отличается от различных солей соединения некоторыми физическими свойствами, такими, как растворимость в полярных растворителях, но во всем остальном соли эквивалентны исходной форме соединения, что касается целей настоящего изобретения. Отдельные соли, описанные ниже, включают в себя "безилатные соли" или "бензолсульфонатные соли" соединения 101 согласно изобретению. Безилатная или бензолсульфонатная соль является аддитивной солью кислоты, образованной из бензолсульфокислоты. Термины "полиморфы" и "полиморфные формы" и родственные термины, которые употребляют в тексте, относятся к кристаллическим формам одной и той же молекулы, и различные полиморфные формы могут иметь различные физические свойства, такие как, например, температуры плавления, теплоты плавления, растворимости, скорости распада и/или колебательные спектры, как результат расположения или конформации молекул в кристаллической решетке. Различия в физических свойствах, проявляемые полиморфными формами, оказывают влияние на фармацевтические параметры, такие как устойчивость при хранении, сжимаемость и плотность (важные свойства в композиции и в промышленном производстве продукта), и скорость распада (важный фактор в биодоступности). Различия в устойчивости могут возникать в результате изменений в химической реактивности (например, различное окисление приводит к тому, что дозированная форма изменяет цвет быстрее, когда состоит из одной полиморфной формы,чем когда состоит из другой полиморфной формы) или в результате механических изменений (например,таблетки крошатся при хранении, поскольку кинетически благоприятная полиморфная форма превращается в термодинамически более устойчивую полиморфную форму) или в результате обоих факторов (например, таблетки из одной полиморфной формы являются более чувствительными к разрушению при высокой влажности). В исключительном случае вследствие различий растворимости/распада некоторые полиморфные переходы могут приводить к отсутствию активности или, в другом исключительном случае, к токсичности. Кроме того, физические свойства кристалла могут оказаться важными при обработке,например, одна полиморфная форма, наиболее вероятно, образует сольваты, или она, возможно, трудно фильтруется или отмывается от примесей (т.е., форма частицы и распределение по размеру могут отличаться между полиморфными модификациями).-5 013367 Полиморфные формы молекулы могут быть получены рядом способов, известных в данной области. Такие способы включают в себя, но не ограничиваются кристаллизацией из расплава, охлаждением расплава, перекристаллизацией из растворителя, десольватацией, быстрым выпариванием, быстрым охлаждением, медленным охлаждением, диффузией паров и возгонкой. Методы, с помощью которых определяют свойства полиморфных форм, включают в себя, без ограничений, дифференциальную сканирующую калориметрию (DSC), порошковую дифрактометрию рентгеновских лучей (XRPD), дифрактометрию рентгеновских лучей единичного кристалла, колебательную спектроскопию, например, IR и рамановскую спектроскопию, ЯМР в твердом состоянии, оптическую микроскопию в горячем состоянии, сканирующую электронную микроскопию (SEM), электронную кристаллографию и количественный анализ, анализ размера частиц (PSA), анализ площади поверхности,изучения растворимости и изучения распада. Термин "сольват", употребляемый в тексте, относится к кристаллической форме вещества, которое содержит растворитель. Термин "гидрат" относится к сольвату, где растворителем является вода. Термин "десольватированный сольват", употребляемый в тексте, относится к кристаллической форме вещества, которая может быть образована путем удаления растворителя из сольвата. Термин "аморфная форма" относится к некристаллической форме вещества. Кроме солей и полиморфных форм, изобретение предоставляет соединения, которые находятся в пролекарственной форме. Пролекарства соединений, описанных в тексте, являются структурно модифицированными формами соединения, которые с легкостью претерпевают химические изменения при физиологических условиях с образованием соединения. Кроме того, пролекарства могут быть превращены в конечное соединение химическими и биохимическими способами в ex vivo окружающей среде. Например, пролекарства могут быть медленно превращены в соединение, когда их помещают в емкость трансдермального пластыря с подходящим ферментом или химическим реагентом. Пролекарства часто используют, поскольку в некоторых ситуациях их легче вводить, чем соединение или родительское лекарственное средство. Они могут быть, например, биодоступными при пероральном введении, в то время как родительское лекарственное средство не может. Пролекарство также может иметь улучшенную растворимость в фармацевтических композициях по сравнению с родительским лекарственным средством. Широкий ряд производных пролекарств известен в данной области, такие как производные, которые основываются на гидролитическом расщеплении или окислительной активации пролекарства. Например,без ограничения, пролекарство должно быть соединением, которое вводят в виде сложного эфира ("пролекарство"), который затем метаболически гидролизуется до карбоновой кислоты, активной субстанции. Дополнительные примеры включают в себя пептидильные производные соединения. Соединение согласно настоящему изобретению также может включать в себя неприродные части атомных изотопов у одного или более атомов. Например, соединение может быть меченным радиоактивными изотопами, такими как, например, тритий (3 Н), йод-125 (125I), cepa-35 (35S) или углерод-14 (14 С). Меченные радиоактивными изотопами соединения используют в качестве терапевтических средств, например, противораковых терапевтических средств, реагентов для исследований, например, реагентов для анализа связывания, и диагностических средств, например, in vivo радиофармацевтических препаратов. Все варианты изотопов соединения согласно настоящему изобретению, является ли оно радиоактивными или нет, предназначены быть включенными в сферу настоящего изобретения. 6.2. Варианты осуществления изобретения. Настоящее изобретение относится к солям и полиморфным формам соединения 101, композициям,содержащим соли и полиморфные формы отдельно или в комбинации с другими активными ингредиентами, к способам их использования в модулировании активности рецептора, в частности, активности рецептора PPAR-. Не стремясь быть связанными с какой-либо отдельной теорией механизма действия,заявители полагают, что такие качества, как устойчивость при хранении, способность к сжатию, плотность или распад солей и полиморфных форм являются благоприятными для промышленного производства, для композиции и для биодоступности модулятора PPAR-. Предпочтительными солями и полиморфными формами согласно изобретению являются такие, которые отличаются физическими свойствами, например, устойчивостью, растворимостью и скоростью распада, соответствующими для клинических и терапевтических дозированных форм. Предпочтительные полиморфные формы согласно изобретению являются такими, которые отличаются физическими свойствами, например, морфологией кристаллов, сжимаемостью и твердостью, подходящими для производства твердой дозированной формы. Такие свойства могут быть определены методами, такими как дифракция рентгеновских лучей, микроскопия, ИК-спектроскопия и термический анализ, как описано в тексте и известно в данной области. Соли и полиморфные формы согласно изобретению используют в лечении или предотвращении состояний и нарушений, связанных с диабетическими состояниями, энергетическим гомеостазом, метаболизмом липидов, дифференцировкой адипоцитов и воспалением (смотри, Ricote et al., Nature 391:79-82(1998) и Jiang et al., Nature 391:82-86 (1998. Например, соли и полиморфные формы согласно изобретению используют в лечении нарушений метаболизма, таких как диабет II типа. Кроме того, соединения-6 013367 согласно изобретению используют для профилактики и лечения осложнений нарушений метаболизма,таких как диабет II типа, например, нейропатии, ретинопатии, гломерулосклероза и сердечно-сосудистых нарушений. 6.2.1. Соли соединения 101. В одном аспекте настоящее изобретение предоставляет отдельные фармацевтически приемлемые соли соединения 101, эффективного модулятора рецептора PPAR-, имеющие особую применимость в лечении или профилактике состояний и нарушений, связанных с энергетическим гомеостазом, метаболизмом липидов, дифференцировкой адипоцитов, воспалением и диабетом и диабетическими состояниями. Данный аспект осуществляется с помощью солей соединения 101, произведенных из кислот HCl,HBr, а также таких солей соединения 101, как тозилаты и безилаты. В предпочтительных вариантах осуществления изобретения, настоящее изобретение предоставляет безилатные соли соединения 101. Как показано выше, соединение 101 имеет общую формулу (I) В таких солях, как бензолсульфонаты соединения 101, бензолсульфокислота представлена формулой (II) В формуле (II) фенильное кольцо, возможно, замещено посредством радикала R, который может быть любым арильным заместителем, описанным выше, и n равно любому целому числу от 1 до 5. В некоторых вариантах осуществления изобретения R является гетероалкилом, алкилом или водородом, и n равно любому целому числу от 1 до 5. В других вариантах осуществления изобретения R может быть алкилом или водородом и n равно любому целому числу от 1 до 5. В некоторых вариантах осуществления изобретения R является низшим алкилом или водородом и n равно любому целому числу от 1 до 5. В отдельных воплощениях изобретения каждый R является водородом. Предпочтительная безилатная соль соединения 101 представлена формулой (III) Каждая соль согласно изобретению может быть получена из препарата соединения 101 (см. фиг. 1). Соединение 101 может быть синтезировано или получено любым способом, очевидным специалистам в данной области. В предпочтительных вариантах осуществления изобретения, соединение 101 получают способами, подробно описанными в примерах ниже, в патенте США No. 6583157 и в международной патентной публикации WO 01/00579, содержание которых включено в текст в виде ссылки во всей полноте. В качестве альтернативы соединение 101 может быть получено путем выделения соли соединения 101, как описано ниже, и превращения такой соли соединения 101 в нейтральную форму обработкой соответствующим основанием. Например, соединение 101 может быть получено путем выделения хлористоводородной соли соединения 101 фильтрацией, затем превращения ее в нейтральную форму путем обработки одноосновным карбонатом натрия в этилацетате, или другим подходящим основанием. В таких вариантах осуществления изобретения хлористо-водородная соль соединения 101 может быть получена любым способом, известным в данной области. Например, хлористо-водородная соль соединения 101 может быть получена путем взаимодействия 3,5-дихлор-4-(хинолин-3-илокси)фениламина с 2,4 дихлорбензолсульфонилхлоридом и хлористо-водородной кислотой с получением гидрохлорида 2,4 дихлор-N-[3,5-дихлор-4-хинолин-3-илокси)фенил]бензолсульфонамида, как описано в примере 7. Типичные схемы синтеза соединения 101 из 3-гидроксихинолина представлены на фиг. 2 и 3 и описаны подробно в примерах ниже. Соединение 101, полученное любым способом, может быть подвергнуто взаимодействию с соответствующей кислотой, либо неразбавленной, либо в подходящем инертном растворителе, с получением солевых форм согласно изобретению. Например, соединение 101 может быть подвергнуто взаимодействию с соответствующей бензолсульфокислотой с получением безилатных солей согласно изобретению. Как показано подробно в примерах ниже, безилатная соль соединения 101 и его полиморфные формы обладают превосходными устойчивостью и гигроскопичными свойствами по сравнению с другими-7 013367 солями соединения 101. 6.2.2. Полиморфные формы. Настоящее изобретение также предоставляет полиморфные формы соединения 101, эффективного модулятора рецептора PPAR-, имеющие особую применимость в лечении или профилактике состояний и нарушений, связанных с энергетическим гомеостазом, метаболизмом липидов, дифференцировкой адипоцитов и воспалением. В некоторых вариантах осуществления изобретения, полиморфные формы согласно изобретению являются полиморфными формами безилатной соли соединения 101, как описано ниже. Соединение 101 и его препарат описан выше и в примерах ниже. Каждая полиморфная форма согласно изобретению может быть получена из препарата соединения 101 (смотри фиг. 1). Твердое соединение 101 может быть растворено и затем кристаллизовано из смеси растворителей, описанных ниже, с получением полиморфных форм согласно изобретению. В отдельных воплощениях изобретения безилатная соль соединения 101 может быть растворена и затем подвергнута кристаллизации из смеси растворителей, описанных ниже, с получением полиморфных форм согласно изобретению. В одном варианте осуществления изобретения настоящее изобретение предоставляет форму I безилатной соли соединения 101 (бензолсульфонатная соль 2,4-дихлор-N-[3,5-дихлор-4-(хинолин-3 илокси)фенил]бензолсульфонамида). В одном воплощении изобретения полиморфная форма I безилатной соли соединения 101 имеет точку плавления приблизительно 180 С или выше. В отдельном воплощении изобретения полиморфная форма I имеет точку плавления приблизительно между 180 и 200 С. Когда типичная полиморфная форма I была проверена с помощью дифференциальной сканирующей калориметрии способами, описанными в примерах ниже, оказалось, что эндотермический эффект имеет место приблизительно между 186,3 и 189,5 С, и энтальпия плавления составляет приблизительно между 81,5 и 89,9 Дж/г. В других вариантах осуществления изобретения полиморфная форма I безилатной соли соединения 101 имеет картину дифракции рентгеновских лучей на порошке, подобную картине дифракции рентгеновских лучей, изображенной на фиг. 5, используя Cu K излучение. Например, основные пики дифракции рентгеновских лучей отдельной полиморфной формы I согласно изобретению наблюдают на 7,0, 19,5, 22,0, 24,0, 24,5 и 28 2, используя Cu K излучение. В некоторых вариантах осуществления изобретения основные пики дифракции рентгеновских лучей полиморфной формы I согласно изобретению наблюдают при одном, двух, трех, четырех, пяти или шести пиках картины дифракции рентгеновских лучей на 7,0, 19,5, 22,0, 24,0, 24,5 и 28 2, используя Cu K излучение. В других воплощениях изобретения полиморфная форма I согласно изобретению имеет точку плавления приблизительно между 186 и 200 С и основные пики дифракции рентгеновских лучей наблюдают на одном, двух,трех, четырех, пяти или шести пиках картины дифракции рентгеновских лучей на порошке на 7,0, 19,5,22,0, 24,0, 24,5 и 28 2, используя Cu K излучение. В других вариантах осуществления изобретения основные пики абсорбции в инфракрасной области спектра полиморфной формы I согласно изобретению наблюдают на одном, двух, трех, четырех или пяти пиках абсорбции в инфракрасной области спектра при 1567, 1461, 913, 895 и 881 см-1. Форма I безилатной соли соединения 101 может быть получена любым способом получения формыI, очевидным специалистам в данной области с учетом данного описания. В некоторых воплощениях изобретения форма I может быть подвергнута кристаллизации из этанольных растворов соединения 101 и гидрата бензолсульфокислоты. Предпочтительно, этанольный раствор гидрата бензолсульфокислоты(Aldrich) может быть добавлен к твердому соединению 101 при нагревании, чтобы получить раствор; охлаждение раствора дает форму I. Форма I может быть кристаллизована из растворов этилацетата и этанола, как описано в примерах ниже. В другом варианте осуществления изобретения настоящее изобретение предоставляет форму II безилатной соли соединения 101 (бензолсульфонатная соль 2,4-дихлор-N-[3,5-дихлор-4-(хинолин-3 илокси)фенил]бензолсульфонамида). В одном воплощении изобретения полиморфная форма II безилатной соли соединения 101 имеет точку плавления приблизительно 230 С или выше. В отдельном воплощении изобретения полиморфная форма II имеет точку плавления приблизительно между 230 и 240 С. Характерная форма II безилатной соли соединения 101 проявляет удивительную устойчивость и имеет температуру плавления приблизительно 233 С. Когда характерная полиморфная форма II была проверена с помощью дифференциальной сканирующей калориметрии способами, описанными в примерах ниже, оказалось, что эндотермический эффект имеет место приблизительно при 233,7 С, и энтальпия плавления составляет приблизительно 98,9 Дж/г. В других вариантах осуществления изобретения, полиморфная форма II безилатной соли соединения 101 имеет картину дифракции рентгеновских лучей на порошке, подобную картине дифракции рентгеновских лучей, изображенной на фиг. 9, используя Cu К излучение. Например, основные пики на картине дифракции рентгеновских лучей на порошке отдельной полиморфной формы II согласно изобретению наблюдают на 15, 19, 20,5, 23,5, 24,5, 25, 2 6,5, 29,5 и 30,5 2, используя Cu К излучение. В некоторых вариантах осуществления изобретения, основные пики дифракции рентгеновских лучей полиморфной формы II согласно изобретению наблюдают при одном,двух, трех, четырех, пяти, шести, семи или восьми пиках картины дифракции рентгеновских лучей на-8 013367 порошке на 15, 19, 20,5, 23,5, 24,5, 25, 26,5, 29,5 и 30,5 2, используя Cu K излучение. В некоторых воплощениях изобретения, полиморфная форма II согласно изобретению имеет точку плавления приблизительно между 230 и 240 С, и основные пики дифракции рентгеновских лучей наблюдают на одном,двух, трех, четырех, пяти, шести, семи или восьми пиках картины дифракции рентгеновских лучей на 15,19, 20,5, 23,5, 24,5, 25, 26,5, 29,5 и 30,5 2, используя Cu K излучение. В других вариантах осуществления изобретения, основные пики абсорбции в инфракрасной области спектра полиморфной формы II согласно изобретению наблюдают на одном, двух, трех, четырех или пяти пиках абсорбции в инфракрасной области спектра при 1573, 1469, 1459, 912 и 859 см-1. Форма II безилатной соли соединения 101 может быть получена любым способом получения формы II, очевидным специалистам в данной области с учетом данного описания. В некоторых воплощениях изобретения форма II может быть подвергнута кристаллизации из растворов этилацетата и этанола, как описано в примерах ниже. Предпочтительно, форма II безилатной соли соединения 101 может быть получена путем добавления этанольного раствора бензолсульфокислоты к твердому соединению 101 при нагревании. Реакционная суспензия может быть подвергнута перемешиванию при нагревании, затем охлаждению при дальнейшем перемешивании, что, в результате, приводит к форме II безилатной соли соединения 101. В некоторых вариантах осуществления изобретения настоящее изобретение также рассматривает получение формы I или II безилатной соли соединения 101 путем кристаллизации любой из форм I или II безилатной соли соединения 101 и превращения кристаллизованной формы до другой формы (например,кристаллизация формы I и превращение формы I в форму II) в растворе или в твердом состоянии. Как показано подробно в примерах ниже, безилатная соль соединения 101 проявляет превосходные свойства относительно других аддитивных солей кислоты соединения 101. Полиморфная форма I и форма II безилатной соли соединения 101, и его полиморфные формы, проявляют устойчивость и гигроскопичность, благоприятную для использования в композиции для введения животным и человеку. Форма II безилатной соли соединения 101 является предпочтительной в сравнении с формой I безилатной соли соединения 101 из-за ее более высокой устойчивости. 6.2.3. Композиции. В другом аспекте настоящее изобретение предоставляет фармацевтические композиции для модулирования активности рецептора PPAR- у человека и животных. Композиции содержат соль или полиморфную форму согласно настоящему изобретению и фармацевтически приемлемый разбавитель, наполнитель или носитель. В некоторых воплощениях изобретения фармацевтическая композиция согласно изобретению содержит чистую соль или полиморфную форму соединения 101. Например, фармацевтическая композиция согласно изобретению может содержать чистую форму I или чистую форму II. Как описано в тексте, соль или полиморфная форма, которая является "чистой", т.е., в значительной степени свободной от других полиморфных форм, содержит менее чем приблизительно 10% одной или более других полиморфных форм, предпочтительно менее чем приблизительно 5% одной или более других полиморных форм, более предпочтительно менее чем приблизительно 3% одной или более других полиморфных форм, наиболее предпочтительно менее чем приблизительно 1% одной или более других полиморфных форм. Фармацевтические композиции для введения солей или полиморфных форм согласно изобретению легко могут быть представлены в стандартной лекарственной форме и могут быть приготовлены любым из способов, хорошо известных в области фармации. Все способы включают в себя стадию объединения активного ингредиента с носителем, который составляет один или более добавочных ингредиентов. Вообще, фармацевтические композиции получают путем объединения активного ингредиента с жидким носителем или тонко измельченным твердым носителем или с обоими типами носителей с образованием однородной смеси и затем, если необходимо, формирования продукта в виде желаемой композиции. В фармацевтической композиции соль или полиморфная форма включены в количестве, достаточном для достижения желаемого эффекта относительно процесса, состояния или заболевания, которые подвергают модулированию, профилактике или лечению. Фармацевтические композиции, содержащие активный ингредиент, могут находиться в виде, подходящем для перорального использования, например, в виде таблеток, пастилок, лепешек, водных или масляных суспензий, дисперсных порошков или гранул, эмульсий, твердых или мягких капсул или сиропов, растворов или эликсиров. Предназначенные для перорального использования композиции могут быть приготовлены любым способом, известным в области производства фармацевтических композиций,и такие композиции могут содержать одно или более реагентов, выбранных из группы, состоящей из подсластителей, ароматизаторов, красителей и консервантов для того, чтобы получить фармацевтически наилучшие и приятные на вкус препараты. Таблетки содержат активный ингредиент в смеси с нетоксичными фармацевтически приемлемыми наполнителями, которые подходят для производства таблеток. Указанными наполнителями могут быть, например, разбавители, такие как карбонат кальция, карбонат натрия, лактоза, фосфат кальция и фосфат натрия; гранулирующие и дезинтегрирующие реагенты, например, кукурузный крахмал или альгиновая кислота; связывающие реагенты, например, крахмал, жела-9 013367 тин или гуммиарабик, и смазывающие реагенты, например, стеарат магния, стеариновая кислота или тальк. Таблетки могут быть непокрытыми, или они могут быть покрыты оболочками известными способами для задержки дезинтеграции и всасываемости в желудочно-кишечном тракте и, тем самым, могут обеспечить замедленное действие в течение длительного периода. Например, материал замедленного действия, такой как глицерилмоностеарат или глицерилдистеарат, может быть использован. Таблетки также могут быть покрыты способами, описанными в патентах США No. 4256108, 4166452 и 4265874,для получения осмотических терапевтических таблеток с контролируемым высвобождением. Композиции для перорального использования также могут быть представлены в виде твердых желатиновых капсул, где активный ингредиент смешан с инертным твердым разбавителем, например карбонатом кальция, фосфатом кальция, каолином или микрокристаллической целлюлозой, или в виде мягких желатиновых капсул, где активный ингредиент смешан с водой или масляной средой, например арахисовым маслом, жидким парафином или оливковым маслом. Водные суспензии содержат активные материалы в смеси с наполнителями, подходящими для производства водных суспензий. Такими наполнителями являются суспендирующие реагенты, например,карбоксиметилцеллюлоза натрия, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия,поливинилпирролидон, трагакантовая камедь и аравийская камедь; диспергирующими или смачивающими реагентами может быть природный фосфатид, например, лецитин, или продукты конденсации алкиленоксида с жирными кислотами, например, полиоксиэтиленстеарат, или продукты конденсации окиси этилена с алифатическими спиртами с длинной цепью, например гептадекаэтиленоксицетанол, или продукты конденсации окиси этилена с частичными сложными эфирами, произведенными из жирных кислот и гексита, такие как полиоксиэтиленсорбитмоноолеат, или продукты конденсации окиси этилена с частичными сложными эфирами, произведенными из жирных кислот и ангидридов гексита, например,полиэтиленсорбитанмоноолеат. Водные суспензии также могут содержать один или более консервантов,например, этил или н-пропил, п-гидроксибензоат, один или более красителей, один или более ароматизаторов и один или более подсластителей, таких как сахароза или сахарин. Масляные суспензии могут быть приготовлены путем суспендирования активного ингредиента в растительном масле, например, арахисовом масле, оливковом масле, кунжутном масле или кокосовом масле, или в минеральном масле, таком как жидкий парафин. Масляные суспензии могут содержать загуститель, например пчелиный воск, твердый парафин или цетиловый спирт. Подсластители, такие как описаны выше, и ароматизаторы могут быть добавлены для получения приятного на вкус перорального препарата. Указанные композиции могут быть защищены путем добавления антиоксиданта, такого как аскорбиновая кислота. Дисперсные порошки и гранулы, подходящие для приготовления водной суспензии путем добавления воды, включают активный ингредиент в смеси с диспергирующим или смачивающим реагентом,суспендирующим реагентом и одним или более консервантами. Подходящими диспергирующими или смачивающими реагентами являются такие, которые уже упоминались выше. Дополнительные наполнители, например, подсластители, ароматизаторы и красители, также могут быть представлены. Фармацевтические композиции согласно изобретению также могут находиться в виде эмульсий масло-в-воде. Масляной фазой может быть растительное масло, например, оливковое масло или арахисовое масло, или минеральное масло, например, жидкий парафин, или смеси масел. Подходящими эмульгаторами могут быть природные камеди, например, аравийская камедь или трагакантная камедь; природные фосфатиды, например, соя культурная, лецитин и сложные эфиры или частичные сложные эфиры, произведенные из жирных кислот; ангидриды гексита, например, сорбитанмоноолеат; и продукты конденсации частичных сложных эфиров с окисью этилена, например, полиоксиэтиленсорбитанмоноолеат. Эмульсии также могут содержать подсластители и ароматизаторы. Сиропы и эликсиры могут быть приготовлены с подсластителями, например глицерином, пропиленгликолем, сорбитом или сахарозой. Такие композиции также могут содержать успокоительное средство, консервант и ароматизаторы и красители. Фармацевтические композиции могут быть представлены в виде инъецируемой водной или масляной суспензии. Такая суспензия может быть приготовлена способом, известным в данной области, с использованием подходящих диспергирующих или смачивающих реагентов и суспендирующих средств,которые были упомянуты выше. Стерильный инъецируемый препарат также может быть стерильным инъецируемым раствором или суспензией в нетоксичном приемлемом для парентерального использования разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. В числе приемлемых носителей и растворителей, которые могут быть использованы, находится вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерилизованные, жирные масла обычно используют в качестве растворителя или суспендирующей среды. С этой целью любое жирное масло может быть использовано, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, находят свое применение в приготовлении инъецируемых форм. Соли и полиморфные формы согласно настоящему изобретению могут быть введены в виде суппозиториев для ректального применения лекарственного средства. Такие композиции могут быть приготовлены путем смешивания лекарственного средства с подходящим, не вызывающим раздражение на- 10013367 полнителем, который находится в твердом состоянии при обычных температурах, но становится жидким при ректальной температуре и, следовательно, плавится в прямой кишке с высвобождением лекарственного средства. Такие материалы включают в себя, но не ограничиваются маслом какао и полиэтиленгликолями. Для местного использования используют кремы, мази, гели, растворы или суспензии, и т.д., содержащие соли и полиморфные формы согласно настоящему изобретению. Как описано в тексте, для местного применения также предполагают включить жидкости или растворы для полоскания рта. Фармацевтическая композиция и способ согласно настоящему изобретению также может включать в себя другие терапевтически активные соединения, упомянутые в тексте, которые обычно применяют в лечении или профилактике вышеуказанных патологических состояний. 6.2.4 Способы использования. В другом аспекте, настоящее изобретение предоставляет способы лечения состояний или нарушений, опосредованных рецептором PPAR-, путем введения субъекту, испытывающему такое нарушение или состояние, терапевтически эффективного количества соли или полиморфной формы или композиции согласно изобретению. Субъектом может быть животное, такое как, например, млекопитающее, включая,но не ограничиваясь приматом (например, человеком), крупным рогатым скотом, овцой, козой, лошадью,собакой, кошкой, кроликом, крысой, мышью и тому подобным. В зависимости от биологической среды (например, тип клетки, патологическое состояние хозяина и т.д.), указанные соединения могут активировать или тормозить действие рецептора PPAR-. В случае активации рецептора PPAR-, указанные соединения найдут применение как терапевтические средства,способные модулировать состояния, опосредованные рецептором PPAR-. Как указано выше, примеры таких состояний включают в себя диабет II типа. Таким образом, агонисты рецептора PPAR- могут быть использованы для лечения состояний, включающих диабет II типа. Кроме того, соединения используют для профилактики и лечения осложнений диабета (например, нейропатия, ретинопатия, гломерулосклероз и сердечно-сосудистые заболевания) и профилактики или лечения гиперлипидемии. Кроме того, соединения используют для модулирования воспалительных состояний, которые, как было обнаружено в последнее время, регулируются рецептором PPAR- (смотри, Ricote et al., Nature 391:79-82 (1998) Jiang etal., Nature 391:82-86 (1998. Примеры воспалительных состояний включают в себя ревматоидный артрит и атеросклероз. Соединения, которые действуют посредством антагонизма рецептора PPAR-, используют для лечения ожирения, гипертензии, гиперлипидемии, гиперхолестерилемии, гиперлипопротеинемии и нарушений метаболизма. При терапевтическом использовании с целью лечения ожирения, диабета, воспалительных состояний или других состояний или нарушений, опосредованных рецептором PPAR-, соединения, применяемые в фармацевтическом способе согласно изобретению, вводят в первоначальной дозировке приблизительно от 0,001 до 100 мг/кг в сутки. Диапазон суточной дозы приблизительно от 0,1 до 10 мг/кг является предпочтительным. Дозировки, однако, могут изменяться в зависимости от потребностей больного, тяжести состояния, которое подвергается лечению, и соединения, которое используется для лечения. Определение подходящей дозировки для отдельной ситуации находится в компетенции врача-практика. Обычно лечение начинают с меньших дозировок, которые являются меньше чем оптимальная доза соединения. После этого, дозировку увеличивают посредством малых добавок до тех пор, пока в этих условиях не достигнут оптимального эффекта. Для удобства общую суточную дозировку можно разделить и вводить порциями в течение дня, если желательно. В зависимости от заболевания, которое подвергается лечению, и состояния субъекта, полиморфные формы согласно настоящему изобретению могут быть введены пероральным, парентеральным путем(например, внутримышечное, внутрибрюшинное, внутривенное введение, ICV, интрацистернальная инъекция или инфузия, подкожная инъекция или имплантат), ингаляцией аэрозолем, назальным, вагинальным, ректальным, подъязычным или местным путем введения и могут быть приготовлены отдельно или вместе, в виде подходящих, стандартных композиций, содержащих обычные нетоксичные, фармацевтически приемлемые разбавители, наполнители или носители, соответствующие каждому способу введения. В лечении или профилактике состояний, которые требуют модулирования рецептора PPAR-, соответствующий дозированный уровень будет, в основном, составлять приблизительно от 0,001 до 100 мг на кг веса тела больного в день, который можно вводить в виде одной дозы или множества доз. Предпочтительно, дозированный уровень будет составлять приблизительно от 0,01 до 25 мг/кг в день; более предпочтительно, приблизительно от 0,05 до 10 мг/кг в день. Подходящий дозированный уровень может составлять приблизительно от 0,01 до 25 мг/кг в день, приблизительно от 0,05 до 10 мг/кг в день или приблизительно от 0,1 до 5 мг/кг в день. В пределах данного диапазона дозировка может составлять от 0,005 до 0,05, от 0,05 до 0,5 или от 0,5 до 5,0 мг/кг в день. Для перорального введения композиции, предпочтительно, находятся в виде таблеток, содержащих от 1,0 до 1000 мг активного ингредиента, особенно 1,0,5,0, 10,0, 15,0, 20,0, 25,0, 50,0, 75,0, 100,0, 150,0, 200,0, 250,0, 300,0, 400,0, 500,0, 600,0, 750,0, 800,0, 900,0 и 1000,0 мг активного ингредиента для симптоматического индивидуального подбора дозировки боль- 11013367 ному, который подвергается лечению. Полиморфные формы могут быть введены по схеме от 1 до 4 раз в день, предпочтительно один или два раза в день. Следует признать, однако, что специфический дозовый уровень и частота дозировки для любого отдельного больного может изменяться и зависеть от ряда факторов, включающих активность конкретной используемой полиморфной формы, метаболическую устойчивость и продолжительность действия данной полиморфной формы, возраст больного, его вес тела, общее состояния здоровья, пол, питание, а также способ и временной режим введения, скорость выведения, комбинацию лекарственных средств,тяжесть отдельного состояния и хозяина, подвергающегося терапии. Соли и полиморфные формы согласно настоящему изобретению могут быть комбинированы с другими соединениями, применяемыми в родственных ситуациях, для лечения или профилактики метаболических нарушений и воспалительных состояний, их осложнений и связанных с ними патологий (например, сердечно-сосудистое заболевание и гипертензия). Во многих случаях, введение соединений или композиций, являющихся предметом изобретения, в сочетании с указанными альтернативными средствами повышает эффективность таких средств. Соответственно, в некоторых случаях настоящие соединения при комбинировании или при введении в комбинации, например с антидиабетическими средствами, могут быть использованы в дозировках,которые являются меньше предполагаемых количеств, когда соединения вводят отдельно, или меньше количеств, рассчитываемых для комбинированной терапии. Например, подходящие средства для комбинированной терапии включают в себя такие средства,которые в настоящее время являются коммерчески доступными, и такие средства, которые находятся в развитии или которые следует развивать. Типичные средства, используемые в лечении нарушений метаболизма, включают в себя, без ограничений: (а) антидиабетические средства, такие как инсулин, сульфонилмочевины (например, меглинатид, толбутамид, хлорпропамид, ацетогексамид, толазамид, глибурид,глипизид и глимепирид), бигуаниды, например, метформин (Глюкофаг (Glucophage, ингибиторы глюкозидазы (акарбоза), тиазолидиноновые соединения, например, розиглитазон (Avandia, троглитазон(Резулин (Rezulin) и пиоглитазон (Actos; (b) агонисты 3 адренергических рецепторов, лептин или его производные и антагонисты нейропептида Y; (с) секвестранты желчных кислот (например, холестирамин и холестипол), ингибиторы HMG-CoA-редуктазы, например, статины (например, ловастатин,аторвастатин, флувастатин, правастатин и симвастатин), никотиновую кислоту (ниацин), производные кислоты (например, гемфиброзил и клофибрат) и нитроглицерин. Типичные средства, используемые в лечении воспалительных состояний, включают в себя, без ограничений: (а) нестероидные противовоспалительные средства (NSAID), такие как производные пропионовой кислоты (например, алминопрофен,беноксапрофен, буклоксовая кислота, карпрофен, фенбуфен, фенопрофен, флупрофен, флурбипрофен,ибупрофен, индопрофен, кетопрофен, миропрофен, напроксен, оксапрозин, пирпрофен, пранопрофен,супрофен, тиапрофеновая кислота и тиоксапрофен), производные уксусной кислоты (например, индометацин, ацеметацин, алклофенак, клиданак, диклофенак, фенклофенак, фенклозовая кислота, фентиазак,фурофенак, ибуфенак, изоксепак, окспинак, сулиндак, тиопинак, толметин, зидометацин и зомепирак),производные фенамовой кислоты (например, флуфенамовая кислота, меклофенамовая кислота, мефенамовая кислота, нифлумовая кислота и толфенамовая кислота), производные бифенилкарбоновой кислоты(например, дифлунизал и флуфенизал), оксикамы (например, изоксикам, пироксикам, судоксикам и теноксикан), салицилаты (например, ацетилсалициловая кислота и сульфасалазин) и пиразолоны (например, апазон, безпиперилон, фепрозон, мофебутазон, оксифенбутазон и фенилбутазон); (b) ингибиторы циклооксигеназы-2 (СОХ-2), такие как целекоксиб (Celebrex) и рофекоксиб (Vioxx) и (с) ингибиторы фосфодиэстеразы типа IV (PDE-IV). Весовое отношение полиморфной формы согласно настоящему изобретению ко второму активному ингредиенту может варьировать и зависеть от эффективной дозы каждого ингредиента. Обычно используют эффективную дозу каждого ингредиента. Таким образом, в случае, когда полиморфную форму согласно настоящему изобретению комбинируют с NSAID, весовое отношение полиморфной формы согласно настоящему изобретению к NSAID будет варьировать приблизительно от 1000:1 до 1:1000, предпочтительно приблизительно от 200:1 до 1:200. Комбинации соли или полиморфной формы согласно настоящему изобретению и других активных ингредиентов будут также находиться в пределах вышеупомянутой области, но в каждом случае должна использоваться эффективная доза каждого активного ингредиента. В некоторых вариантах осуществления изобретения, соли и полиморфные формы согласно настоящему изобретению могут быть использованы для лечения или предотвращения ряда других признаков. Такие признаки включают в себя, без ограничений, метаболические нарушения, такие как, например,диабет (включая диабет I типа и диабет II типа), гипертензия, стенокардия, дислипидемия (включая гипертриглицеридемию, гиперлипопротеинемию и гиперхолестерилемию), подагра, нефропатия и другие почечные заболевания, вторичные по отношению к диабету, диабетическая нейропатия, другие заболевания, связанные с инсулинорезистентностью, синдром поликистоза яичников, инсулинорезистентность,вызванная глюкокортикоидами, ожирение, заболевания кости, специфические для женщин состояния(включая чрезмерные маточные кровотечения в климактерический период) и угри; неврологические рас- 12013367 стройства, такие как болезнь Альцгеймера, нейровоспаление, ишемический инсульт, закрытая травма головы и рассеянный склероз; пролиферативные нарушения, такие как атеросклероз, рестеноз, рак толстой кишки, рак простаты, рак молочной железы, липосаркома, опухоли эпителиального происхождения,опухоль мочеполовой системы эпителиального происхождения и другие опухоли; и воспаление или иммунные нарушения, такие как ревматоидный артрит, воспалительное кишечное заболевание, колит, болезнь Крона, дистрофия желтого пятна, другие воспалительные расстройства и другие иммунные нарушения. Основные причины, объясняющие применимость солей и полиморфных форм согласно настоящему изобретению для лечения или профилактики таких признаков, обсуждаются ниже. Полагают, что модуляторы рецептора PPAR- пригодны для лечения ожирения, поскольку агонисты рецептора PPAR- стимулируют дифференцировку адипоцитов и накопление жиров. Модуляторы рецептора PPAR- также блокируют нормальное опосредованное гормонами превращение преадипоцитов в адипоциты (смотри Wright et al., J. Biol. Chem. 275 (3) :1873-1877 (2000. Агонисты PPAR- могут ингибировать экспрессию ob-гена (продукция лептина) в зрелых адипоцитах. Отсюда следует, что модуляторы рецептора PPAR- будут повышать продукцию лептина и способствовать снижению аппетита и потребности в пище (смотри, Sinha et al., Metab. Clin. Exp., 48(6):786-791 (1999. Кроме того, признаки гиперлептинемии, индуцированные посредством модулятора PPAR- у крыс, приводят к отрицательной негативной регуляции экспрессии рецептора PPAR- и активации ферментов, окисляющих жирные кислоты. Данные эффекты сопровождаются полным изменением дифференцировки адипоцитов. Кроме того, агонисты рецептора PPAR- повышают регуляцию экспрессии UCP2 в адипоцитах и скелетных мышцах, приводя к увеличению расхода энергии. (Viguerie-Bascands et al., Biochem. Biophys.PPAR- является важным для регулирования экспрессии UPC2 и UPC3 в жировой ткани. (Kelly et al., Endocrinology 139 (12) :4920-4927 (1998. Полученные результаты свидетельствуют о том, что краткосрочное лечение высокой дозой модулятора PPAR- будет способствовать продолжительным эффектам при лечении ожирения; стандартные способы лечения ожирения приводят к снижению содержания жиров в зрелых адипоцитах, но сохраняют липогенные ферменты, способные к быстрому повторному синтезу жиров. Такой быстрый повторный синтез жиров, вероятно, является следствием неудачного лечения.(Zhou et al., Proc. Natl. Acad. Sci USA 96 (5) :2391-2395 (1999. Исследователи полагают, что модуляторы PPAR- пригодны для лечения гипертензии, поскольку агонисты рецептора PPAR- подавляют секрецию эндотелина-1 клетками сосудистого эндотелия и способствуют снижению кровяного давления. (Satoh et al., Biochem. Biophys. Res. Commun. 254 (3) :757-763(1999) и Itoh et al., Clin. Exp. Pharmacol. Physiol. 26(7):558-560 (1999. Агонисты PPAR- также снижают кровяное давление в различных моделях гипертензии. (Komers et al., Physiol. Res. (Prague) 47(4):215-225(1998. Исследователи полагают, что модуляторы PPAR- пригодны для лечения нарушений липидного обмена, поскольку рецептор PPAR- участвует в системном гомеостазе глюкозы и липидов. (Kliewer etal., Curr. Opin. Genet. Dev. 8(5):576-581 (1998. Агонисты PPAR- также ослабляют гипертриглицеридемию. (Berger et al., J. Biol. Chem. 274 (10) :6718-6725 (1999. Кроме того, агонисты PPAR- являются антигиперлипидемическими средствами. (Henke et al., J. Med. Chem. 41 (25) :5020-5036 (1998. И, наконец,активатор рецептора PPAR-, как было показано, повышает уровень липопротеинов высокой плотностиRes. 39(10:17-30 (1998. Исследователи полагают, что модуляторы рецептора PPAR- пригодны для лечения атеросклероза,поскольку активированные моноциты/макрофаги экспрессируют PPAR-, и активация рецептора PPARуменьшает регуляцию продукции IL-1 и TNF, индуцируемой макрофагами. Полученные данные указывают на возможное участие рецептора PPAR- в регуляции атеросклероза. (McCarty et al., J. Med. Foodl(3):217-226 (1999. Кроме того, рецептор PPAR- опосредует влияние неэтерифицированных жирных кислот (NEFA) на клетки гладких мышц, которые изменяют внеклеточный матрикс в интиме малых и больших артерий. Данные изменения могут привести к повышенному отложению LDL и могут быть связаны с этиологией атеросклероза. Модуляторы рецептора PPAR- могут влиять на данный процесс. (Olsson et al., Diabetes 48 (3) :616-622 (1999. Кроме того, агонисты PPAR- ингибируют пролиферацию, гипертрофию и миграцию клеток гладких мышц сосудов, индуцируемых факторами роста. Эти процессы являются ключевыми в развитии ремоделирования сосудов и атеросклероза. Рецептор PPAR-y участвует в отрицательной регуляции функции моноцита/макрофага в образовании атеросклеротических бляшек и регулирует экспрессию матриксной металлопротеиназы-9, фермента, вовлеченного в разрушение бляшки. В этом случае, агонист PPAR- может оказаться полезным. (Marx et al., Am. J. Pathol. 153(1):17-23(1998) и Shu et al., Biochem. Biophys. Res. Commun. 267 (1) :345-349 (2000. Рецептор PPAR- экспрессируется в макрофагальных пенистых клетках склеротических поражений человека. (Ricote et al., Proc. Natl.Acad. Sci. USA 95 (13) :7614-7619 (1998. Рецептор PPAR- также экспрессируется в атеросклеротических бляшках и в эндотелиальных клетках. В эндотелиальных клетках агонисты PPAR- в значительной- 13013367 степени ослабляют индуцированную фактором TNFa экспрессию VCAM-1 и ICAM-1 (молекулы адгезии сосудистых клеток) in vitro. Агонисты PPAR-y в значительной степени снижают поступление моноцита/макрофага к атеросклеротическим бляшкам у апо-Е-дифицитных мышей. Данные комбинированные эффекты могут оказывать благоприятное действие при модулировании воспалительного ответа в случае атеросклероза. (Pasceri et al., Circulation 101 (3) :235-238 (2000. И, наконец, генетические признаки человека свидетельствуют о том, что рецептор PPAR- играет существенную роль при атеросклерозе, независимо от влияния на ожирение и метаболизм липидов, возможно, через прямое локальное воздействие на сосудистую стенку. (Wang et al., Cardiovasc. Res. 44(3):588-594 (1999. За последний год значительно увеличилось количество исследований, посвященных участию рецептора PPAR- в биологии макрофага, регуляции клеточного цикла и атеросклерозе, особенно в качестве регулятора функции моноцита/макрофага. (Ricote et al., J. Leukocyte Biol. 66 (5):733-739(1999. Исследователи полагают, что модуляторы рецептора PPAR- пригодны для лечения болезней костей, поскольку TZD ингибируют in vitro образование костного узла и минерализацию. (Johnson et al., Endocrinology 140 (7) :3245-3254 (1999. Полиморфизм рецептора PPAR- оказывает влияние на минеральную плотность костной ткани в климактерический период у женщин. (Ogawa et al., Biochem. Biophys.Res. Coraraun. 260 (1):122-126 (1999. TZD являются потенциальными ингибиторами резорбции кости invitro. Таким образом, TZD могут подавлять резорбцию кости у диабетических больных и предотвращать потерю костной массы. (Okazaki et al., Endocrinology 140 (11) :5060-5065 (1999. Краткосрочное лечение диабетических больных посредством TZD снижает метаболизм костной ткани. Данный эффект отмечается до значительного улучшения метаболизма глюкозы, свидетельствуя о том, что действие оказывается прямо на костную ткань. Двойное воздействие на метаболизм глюкозы и костной ткани может привести к сохранению костной массы у диабетических больных. (Okazaki. et al., Endocr. J. (Tokyo) 46(6):795-801(1999. Исследователи полагают, что модуляторы рецептора PPAR- пригодны для лечения специфических для женщин состояний, поскольку агонисты PPAR- могут быть использованы для подавления избыточного маточного кровотечения у женщин в климактерический период. (Urban et al., WO 98/39006). Исследователи полагают, что модуляторы PPAR- пригодны для лечения угрей, поскольку рецепторPPAR- участвует в дифференцировке себоцитов. Агонисты PPAR- могут быть использованы в лечении угрей, других кожных поражений, связанных с дифференцировкой эпидермальных клеток, или других пролиферативных заболеваний кожи. (Rosenfield et al., Dermatology (Basel) 196(1):43-46 (1998); Rivier etal., FR 2773075 A1, и Pershadsingh et al., патент США No. 5981586). Исследователи полагают, что модуляторы PPAR- пригодны для лечения расстройств, связанных с клеточной пролиферацией, поскольку в комбинации с агонистом рецептора ретиноида-Х, агонист PPAR снижает неконтролируемую клеточную пролиферацию, включающую рак, рестеноз и атеросклероз. Агонисты PPAR-, либо отдельно, либо в комбинации с известными средствами, могут снижать пролиферативный ответ, появляющийся после ангиопластики, сосудистого трансплантата и эндарэктомии. Исследователи полагают, что модуляторы PPAR- пригодны для лечения болезни Альцгеймера, поскольку агонисты PPAR- ингибируют стимулированную b-амилоидом секрецию провоспалительных продуктов микроглией и моноцитами, которые ответственны за нейротоксичность и активацию астроцитов. Агонисты также тормозят дифференцировку моноцитов в активированные макрофаги и ингибируют стимулированную b-амилоидом экспрессию IL-6, TNF и циклооксигеназы-2. (Combs et al., Neuroscience 20 (2) : 558-567 (2000. В коре головного мозга височной области больных с диагнозом болезни Альцгеймера уровни циклооксигеназы-1, циклооксигеназы-2 и рецептора PPAR- повышались. Некоторые средства, которые активируют рецептор PPAR-, ингибируют экспрессию фермента СОХ-2 в глиальных клетках. (Kitamura et al., Biochem. Biophys. Res. Commun. 254 (3) :582-586 (1999. Кроме того, агонистыPPAR- защищают клетки-зерна мозжечка от индуцируемой цитокинами апоптической гибели путем ингибирования iNOS. (Heneka et al., J. Neuroimmunol. 100(1-2):156-168 (1999. И, наконец, активированные моноциты/макрофаги экспрессируют рецептор PPAR-, и активация PPAR- снижает регуляцию индуцированной макрофагами продукции IL-1 и TNF. Этот процесс потенциально вовлекается в болезнь Альцгеймера. (McCarty et al., J. Med. Food 1(3):217-226 (1999. Исследователи полагают, что модуляторы PPAR- пригодны для лечения нейровоспаления, поскольку агонисты PPAR- ингибируют LPS и IFN-g индуцированную экспрессию iNOS глиальными клетками. (Kitamura et al., Neurosci. Lett. 262 (2) :129-132 (1999. Также, лиганды PPAR- могут оказаться важными для других нарушений, связанных с нейровоспалением, таким как ишемический инсульт, закрытая травма головы и рассеянный склероз. Исследователи полагают, что модуляторы PPAR- пригодны для лечения некоторых опухолей, поскольку противоангиогенный эффект агонистов рецептора PPAR- опосредуется апоптическим стимулирующим воздействием на эндотелиальные клетки. (Bishop-Bailey et al., J. Biol. Chem. 274 (24) :1704217048 (1999. Кроме того, агонисты рецептора PPAR- индуцируют терминальную дифференцировку и- 14013367 замедление роста раковых клеток толстой кишки человека. (Kitamura et al., Jpn. J. Cancer Res. 90(1):75-80(1999) и Sarraf et al., Nat. Med. (NY) 4(9):1046-1052 (1998. Агонисты рецептора PPAR- также усиливают антипролиферативное действие ретиноевой кислоты на раковые клетки толстой кишки человека. (Brockman et al., Gastroenterology 115 (5):1049-1055 (1998. Кроме того, специфический агонист рецептора PPAR- проявляет сильный противоопухолевый эффект против рака простаты человека in vitro и in vivo. (Kubota et al. , Cancer Res. 58 (15) :3344-3352 (1998. Агонисты PPAR- также могут ингибировать пролиферацию культивированных опухолевых клеток молочной железы женщины и вызывать апоптоз. Подобные эффекты также наблюдаются in vivo у мышей. (Elstner et al., Proc. Natl. Acad. Sci. USA 95(15):8806-8811 (1998. Агонисты PPAR- могут вызывать терминальную дифференцировку злокачественных эпителиальных клеток молочной железы. (Mueller etal., Mol. Cell l(3):465-470 (1998) и Yee et al., Int. J. Oncol. 15 (5) :967-973 (1999. Агонисты PPAR- используют в лечении липосарком. (Evans et al. , WO 98/29120). Рецептор PPAR- является высоко экспрессированным во всех переходно-клеточных опухолях эпителиального происхождения, включающих эпителиальные опухоли мочеполовой системы человека. Агонисты рецептора PPAR- индуцируют дифференцировку и ингибируют пролиферацию. (Guan et al., Neoplasia (NY) 1(4):330-339 (1999. И, наконец, в дифференцировку многих типов клеток (гепатоциты, фибробласты, адипоциты, кератиноциты, миоциты и моноциты/макрофаги) вовлекается рецептор PPAR-. Следовательно, модуляторы PPAR- могут играть роль в лечении злокачественных опухолей, которые происходят из данных и других типов клеток. (Varmecq et al., Lancet 354 ( 9173) :141-148 (1999. Исследователи полагают, что модуляторы рецептора PPAR- пригодны для лечения воспаления или иммунных нарушений, поскольку рецептор PPAR- в значительной степени позитивно регулируется в активированных макрофагах. Рецептор PPAR- участвует в отрицательной негативной регуляции функции моноцитов/макрофагов, включая образование воспалительных цитокинов и экспрессию iNOS, желатиназы В и "уборщика"-рецептора А. Следовательно, агонисты PPAR- могут представлять ценность.(Marx et al., Am. J. Pathol. 153(1):17-23 (1998. Возрастающие результаты благоприятного терапевтического действия NSAID (некоторые из них активируют рецептор PPAR-) в лечении ревматоидного артрита могут быть опосредованы через активацию рецептора PPAR-. (Jiang et al., Nature 391 (6662):82-86(1998. Агонисты рецептора PPAR- ингибируют продукцию iNOS активированными макрофагами. Следовательно, агонисты рецептора PPAR- могут быть пригодными. (Colville-Nash et al., J. Immunol. 161(2):978-984 (1998. Кроме того, агонисты рецептора PPAR- ослабляют антиген-индуцированную продукцию цитокинов тучными клетками, произведенными костным мозгом. (Sugiyama et al., FEBS Lett. 467 (2-3):259-262(2000. Недавно иммуномодулирующая роль рецептора PPAR- была описана в клетках, важных для врожденной иммунной системы, включая моноциты и макрофаги. Агонисты рецептора PPAR- опосредуют ингибирование в значительной степени пролиферативных ответов клонов Т-клеток-хелперов и свежевыделенных спленоцитов. Таким образом, продукция IL-2 Т-клеточными клонами ингибируется агонистами рецептора PPAR-, которые, таким образом, могут иметь применимость в качестве иммуносупрессоров. (Clark et al., J. Immunol. 164 (3) :1364-1371 (2000. Рецептор PPAR- также участвует в регуляции функции моноцитов/макрофагов. (Ricote et al., J. Leukocyte Biol. 66 (5):733-739 (1999. Экспрессия рецептора PPAR- в лейкоцитах может играть роль в ответе хозяина на признаки острого воспаления и может оказаться важной мишенью для противовоспалительного контроля. (Leininger et al., Biochem. Biophys. Res. Commun. 263 (3) :749-753 (1999. Кроме того, активаторы рецептора PPAR- могут способствовать ограничению хронического воспаления, опосредованного молекулой адгезии сосудистых клеток VCAM-1 и моноцитами. (Jackson et al.,Arterioscler. Thromb. Vase. Biol. 19(9):2094-2104 (1999. Агонисты рецептора PPAR- также в значительной степени снижают воспаление толстой кишки в модели воспалительного кишечного заболевания мыши (IBD). Агонисты рецептора PPAR- могут быть использованы в лечении колита и болезни Крона. (Suet al., J. Clin. Invest. 104(4):383-389 (1999. И, наконец, модуляторы рецептора PPAR-, как полагают, пригодны для лечения глазных расстройств, таких как образование желтого пятна, поскольку антиангиогенный эффект агонистов PPAR-у опосредуется апоптическими стимулирующими воздействиями на эндотелиальные клетки. Исходя из этих данных полагают, что такие агонисты могут быть использованы в лечении дегенерации желтого пятна. (Bishop-Bailey et al., J. Biol. Chem. 274 (24): 17042-17048 (1999. В отдельных предпочтительных вариантах осуществления изобретения настоящие способы направлены на лечение или профилактику диабета II типа с использованием соли или полиморфной формы согласно изобретению, в отдельности или в комбинации со вторым терапевтическим средством, выбранным из противодиабетических средств, таких как инсулин, сульфонилмочевины (например, меглинатид,толбутамид, хлорпропамид, ацетогексамид, толазамид, глибурид, глипизид и глимепирид), бигуаниды,например, метформин (Glucophage), ингибиторы -глюкозидазы (акарбоза) , тиазолидиноновые соединения, например, розиглитазон (Avandia), троглитазон (Rezulin) и пиоглитазон (Actos). В случае,- 15013367 когда средства используют в комбинации, практикующий врач может вводить комбинацию терапевтических агентов или введение может быть последовательным. 7. Примеры Реагенты и растворители, используемые в описанных ниже примерах, могут быть получены из коммерческих источников, таких как Aldrich Chemical Co. (Milwaukee, Wis., USA). Н 1-ЯМР-спектры были записаны на ЯМР-спектрометре 400 МГц Varian Gemini. Значительные пики сведены в таблицы в следующем порядке: количество протонов, мультиплетность (s, синглет; d, дублет; t, триплет; q, квартет; m,мультиплет; br s, уширенный синглет) и коэффициент(ы) связывания в герцах (Гц). Масс-спектрометрию с ионизацией электроспреем проводили на масс-спектрометре с электроспреем Hewlett-Packard 1100MSD, используя HP 1100 ВЭЖХ для доставки образца. Данные масс-спектрометрии выражены в виде отношения массы к заряду. Соединение растворяли в метаноле при концентрации 0,1 мг/мл, и 1 мкл вливали с растворителем для доставки в массспектрометр, который сканировал от 100 до 1500 Да. Соединение могло быть анализировано в положительном режиме ESI с использованием смеси ацетонитрил/вода 1:1 с 1% уксусной кислотой в качестве растворителя для доставки. Соединение также могло быть анализировано в отрицательном режиме ESI с использованием 2 мМ NH4OAc в смеси ацетонитрил/вода в качестве растворителя для доставки. Рентгеноструктурный анализ проводили с использованием порошкового дифрактометра для рентгеноструктурного анализа Shimadzu XDR-6000, используя излучение Cu К. Тонкая фокусировка рентгеновской трубки прибора позволила установить напряжение и силу тока 40 кВ и 40 мА, соответственно. Щели отклонения и рассеяния были установлены на 1, и щель приемного устройства установлена на 0,15 мм. Интенсивность дифрагированного луча определяли с помощью NaI сцинтилляционного детектора. Использовали тета-два тета непрерывное сканирование при 3/мин (0,4 с/0,020 на ступень) от 2,5 до 40 2. Кремниевый стандарт анализировали для проверки правильной регулировки прибора. Данные собирали и анализировали, используя XRD-6000 v.4.1. В некоторых экспериментах дифференциальную сканирующую калориметрию выполняли с использованием ТА инструментария дифференциального сканирующего калориметра 2 920, калиброванного индиевым стандартом. Образцы помещали в алюминиевые сосуды для образцов и покрывали. Образцы уравновешивали при 25 С и нагревали при продувании азотом с контролируемой скоростью 10 С/мин вплоть до конечной температуры 350 С. В других экспериментах дифференциальную сканирующую калориметрию осуществляли с использованием инструментария дифференциального сканирующего калориметра Q100. Образцы помещали в алюминиевые сосуды для образцов и покрывали. Образцы уравновешивали при 25 С и нагревали при продувании азотом с контролируемой скоростью 10 С/мин вплоть до конечной температуры 250 С. Данные сорбции/десорбции влаги собирали с помощью анализатора сорбции паров VTI SGA-100. Данные сорбции и десорбции собирали в области от 5 до 95% относительной влажности ("RH") при 10% интервалах RH при продувании азотом. Образцы не сушили до анализа. Критерии равновесия, использованные для анализа, если весовой критерий не удовлетворял, были менее, чем 0,0100% изменения веса за 5 мин, с максимумом времени установления равновесия 3 ч. Данные не уточняли для исходного содержания влаги в образцах. NaCl и PVP использовали в качестве калибровочных стандартов. Сканирующую электронную микроскопию (SEM) выполняли, используя сканирующий электронный микроскоп FEI Quanta 200. Детектор больших полей использовали при низком давлении. Полюсный наконечник прибора снабжали детектором вторичных электронов. Напряжение электронного луча варьировало между 4,7-5,0 кВ, и давление в камере изменялось от 69,3 до 118,7 Па. Разрешение изображения составляло 1024948. Образцы приготовляли для анализа путем помещения малого количества на углеродную ленту, приспособленную на алюминиевую подставку. Прибор калибровали относительно увеличения, используя стандарты NIST. Данные собирали, используя xTm, конструкцию номер 1564, и анализировали, используя XT Docu (v.3.2). Увеличение, переданное на изображениях SEM, рассчитывали на основе исходных данных. Инфракрасные спектры (IR) соединения в твердом состоянии получали с помощью инфракрасного спектрометра Perkin-Elmer 1600. Соединение подвергали диспергированию приблизительно при 1% вKBr таблетке. 7.1. Пример 1. Синтез соединения 101. Данный пример предоставляет типичный синтез соединения 101. Альтернативные способы синтеза соединения 101, включающие способы синтеза аддитивных солей кислоты соединения 101, описаны ниже; другие альтернативные способы синтеза будут очевидны специалистам в данной области.(1990 (3 г) и 1,2,3-трихлор-5-нитробензол (4,7 г) растворяли в ДМФ (80 мл) и нагревали с карбонатом цезия (7,4 г) в течение 2 ч при 60 С. Реакционную смесь выливали в воду со льдом (500 мл). Полученный осадок не совсем белого цвета собирали фильтрацией и промывали гексаном с получением соединения II в виде твердого вещества (6,9 г), подходящего для использования в следующей реакции. 1 Н ЯМР в CDCl38,863 (д, J=2,2 Гц, 1 Н), 8,360 (с, 2 Н), 8,106 (д, J=8,6 Гц, 1 Н), 7,646 (м, 2 Н), 7,529(д, J=8,6 Гц, 1 Н), 7,160 (д, J=2,2 Гц, 1 Н). 3,5-Дихлор-4-(3,4-дигидрохинолин-3-илокси)фениламин (III). К раствору соединения II (6,9 г) в смеси этанол/ТГФ/вода (отношение 40:20:10) добавляли хлорид аммония (3,3 г) и порошкообразное железо (3,4 г). Полученную смесь нагревали с обратным холодильником в течение 5 ч. Затем горячую смесь фильтровали через целит и концентрировали. Остаток растворяли в этилацетате и промывали насыщенным раствором NaHCO3 с последующим промыванием водой и насыщенным солевым раствором. Раствор сушили над сульфатом магния и концентрировали с получением соединения III в виде твердого вещества не совсем белого цвета (5,6 г). 1 Н ЯМР в (ДМСО)8,846 (д, J=2,9 Гц, 1 Н), 8,010 (м, 1 Н) , 7,915 (м, 1 Н), 7,645 (м, 1 Н) , 7,560 (м,1 Н), 7,401 (д, J=2,9 Гц, 1 Н), 6,778 (с, 2 Н) , 5,762 (с, 2 Н). 2,4-Дихлор-N-[3,5-дихлор-4-(хинолин-3-илокси)фенил]бензолсульфонамид (101). Обработка анилина III посредством. 2,4-дихлорбензолсульфонилхлорида обычными способами привела к соединению 101. 1 Н ЯМР (d6 -ацетон)9,9 (1H, ушир. с), 8,794 (1 Н, д, J=2,9 Гц), 8,23 (1 Н, д, J=8,4 Гц), 8,035 (1 Н,ушир. д, J=8,4 Гц), 7,793 (1 Н, д, J=l,5 Гц), 7,78 (1 Н, м), 7,62-7,70 (2 Н, м), 7,57 (1 Н, тд, J=6,8, 1,2 Гц), 7,476(2 Н, с), 7,364 (1 Н, д, J=2,6 Гц). МС (М-Н) 511,0. 7.2 Пример 2. Связывание рецептора PPAR- с лигандом. С помощью способов, подобных описанным исследователем Lehmann et al., J. Biol. Chem. 270:12953-12956 (1995), соединение 101, полученное согласно примеру 1, имело IC50 менее чем 1 мкМ,как было показано посредством анализа связывания лиганда с рецептором PPAR- с использованием в качестве меченного радиоактивным изотопом лиганда [3 Н]-BRL 49653. 7.3 Пример 3. Кристаллизация HCl-соли соединения 101. Соединение 101 перекристаллизовывали как HCl-соль. Соединение 101, полученное согласно примеру 1, за исключением того, что восстановление посредством SnCl2 использовали для восстановления соединения II до соединения III, суспендировали в 3,5 л подогретого этанола. Приблизительно 240 мл 21%-ного NaOEt в этаноле добавляли с образованием полного раствора. Раствор 145 мл концентрированной HCl (3 экв.) в 450 мл этанола добавляли к теплому раствору и оставляли медленно охлаждать до комнатной температуры. Твердый осадок собирали вакуум-фильтрацией. Продукт суспендировали в воде (2 л) и вновь собирали фильтрацией. После воздушной сушки продукт сушили в вакууме при 70 С до постоянного веса 311 г. Получение безводной HCl-соли соединения 101 было подтверждено посредством ЯМР и CHN.HCl-соли соединения 101 образовывали маленькие ромбовидные кристаллы или игольчатые кристаллы. Посредством микроскопии SEM были выявлены пластинки или призматические частицы. Калориметрия DSC выявила различные эндотермические события, например, 125,2, 161,5, 222,6, 190,3, 224,9,235,6, 242,4 и 182 С; кривые, характеризующие эндотермические реакции, были широкими, и энтальпии- 17013367 плавления не могли быть рассчитаны. Анализ XRPD выявил присутствие кристаллических или частично кристаллических частиц. 7.4 Пример 4. Кристаллизация HBr-соли соединения 101. Соединение 101 перекристаллизовывали как HBr-соль. Раствор 0,98 г 48% HBr (3 экв.) в этаноле(3 мл) добавляли к раствору свободного основания соединения 101 (1 г) в этаноле (20 мл). Для этого примера соединение 101 получали согласно примеру 1, за исключением того, что восстановление посредством SnCl2 использовали для восстановления соединения II до соединения III. Полученный прозрачный раствор помещали в ультразвуковую ванну до тех пор, пока не образовывался осадок белого цвета. После оставления при комнатной температуре в течение 10 мин, суспензию нагревали для достижения прозрачности раствора. Данный раствор оставляли медленно охлаждаться в колбе с рубашкой в течение ночи. Твердые частицы (0,829 г) собирали вакуум-фильтрацией и сушили до постоянного веса в вакууме. Получение HBr-соли соединения 101 было подтверждено посредством ЯМР и CHN.HBr-соли соединения 101 образовывали кристаллы, SEM-микроскопия которых обнаружила наличие пластинчатых кристаллов. Калориметрия DSC выявила эндотермические эффекты при 255,4 и 261,7 С у одного образца, и энтальпия плавления была 158,5 Дж/г. Один или оба эндотермических эффекта могли возникнуть вследствие плавления образца. Анализ XRPD показал наличие кристаллических или частично кристаллических частиц. 7.5 Пример 5. Кристаллизация тозилатной соли соединения 101. Соединение 101 перекристаллизовывали в виде тозилатной соли. Раствор моногидрата птолуолсульфокислоты (4,5 г, 2 экв.) в смеси этанол (55 мл)/вода (11 мл) добавляли к раствору соединения 101 в виде свободного основания (6 г) в этаноле (120 мл). Для данного примера соединение 101 получали согласно примеру 1, за исключением того, что восстановление посредством SnCl2 использовали для восстановления соединения II до соединения III. Смесь нагревали с образованием прозрачного раствора. После охлаждения до комнатной температуры некоторое количество растворителя удаляли в токе азота до тех пор, пока не образовывался осадок белого цвета. Повторное нагревание суспензии привело к образованию прозрачного раствора, который оставляли перемешиваться при медленном охлаждении в течение 60 час. Твердые частицы собирали вакуум-фильтрацией и сушили до постоянного веса в вакууме с получением 6,4 г твердого вещества, имеющего точку плавления 215-220 С. Вещество ресуспендировали в этаноле (30 мл) и нагревали для растворения. После медленного охлаждения твердое вещество собирали и сушили в вакууме с получением 6,19 г твердого вещества, имеющего точку плавления 218-220 С. Наличие тозилатной соли соединения 101 было подтверждено посредством ЯМР. Тозилатная соль соединения 101 образовывала кристаллы, и SEM-микроскопия выявила частицы неправильной формы. DSC-калориметрия обнаружила эндотермический эффект при 220,6 С, и энтальпия плавления составила 86,76 Дж/г. Анализ XRPD показал наличие кристаллических или частично кристаллических частиц. Пример 6. Кристаллизация формы I безилатной соли соединения 101. Данный пример представляет собой пример кристаллизации в малом масштабе формы I безилатной соли соединения 101 из свободного основания соединения 101. Соединение 101 перекристаллизовывали как форму I с бензолсульфокислотой (PhSO3H-xH2O; Aldrich). Бензолсульфокислоту в количестве 3,9 г растворяли в 5 мл этанола, и полученный этанольный раствор добавляли к 5,02 г свободного основания соединения 101 в твердом состоянии. Для данного примера, соединение 101 получали согласно примеру 1, за исключением того, что восстановление посредством SnCl2 использовали для восстановления соединения II до соединения III. Смесь промывали 5 мл этанола, и затем дополнительно добавляли этанол до общего объема 25 мл. Смесь нагревали для образования полного раствора и затем медленно охлаждали при перемешивании. Твердую форму I, 5,57 г собирали фильтрацией и промывали этанолом.- 18013367 Синтез солей соединения 101 согласно примерам 7 и 8. 7.7 Пример 7. Синтез безилатной соли соединения 101 в крупном масштабе. Данный пример предоставляет типичный синтез безилатной соли соединения 101 из предшественников соединения 101. Альтернативные способы синтеза безилатной соли соединения 101 из таких предшественников будут очевидны специалистам в данной области. 3-Гидроксихинолин (3). 3-Аминохинолин (2) превращали в 3-гидроксихинолин (3) через диазониевую соль с выходом 96%. 3-(2,6-Дихлор-4-нитрофенокси)хинолин (4). 3-Гидроксихинолин (3) и 1,2,3-трихлор-5-нитробензол растворяли в ДМФ и нагревали с карбонатом кальция с получением, после растирания в изопропаноле, 3-(2,6-дихлор-4-нитрофенокси)хинолина (4) с 93% выходом. 3,5-Дихлор-4-(хинолин-3-илокси)фениламин (5). Функциональность нитрогруппы 3-(2,6-дихлор-4-нитрофенокси)хинолина (4) каталитически восстанавливали в атмосфере водорода с 5 мас./мас.% (катализатор/соединение 4) суспензии катализатора 1% платины/2% ванадия на угле в этилацетате при 0 С. Материал нагревали до 20 С, фильтровали через целит. Целит промывали посредством ТГФ, и фильтраты объединяли и упаривали с получением 3,5 дихлор-4-(хинолин-3-илокси)фениламина (5) с 98% выходом. Гидрохлорид 2,4-дихлор-N-[3,5-дихлор-4-хинолин-3-илокси)фенил]бензолсульфонамида (1). 3,5-Дихлор-4-(хинолин-3-илокси)фениламин (5) подвергали взаимодействию с 2,4-дихлорбензолсульфонилхлоридом с последующей обработкой хлористо-водородной кислотой с получением гидрохлорида 2,4-дихлор-N-[3,5-дихлор-4-хинолин-3-илокси)фенил]бензолсульфонамида (1; хлористоводородная соль соединения 101) с 99% выходом. 7.8 Пример 8. Получение и перекристаллизация хлористо-водородной соли соединения 101. В данном примере описан способ, который можно использовать для синтеза и перекристаллизации хлористо-водородной соли соединения 101 из предшественника соединения 101. 3,5-Дихлор-4-(хинолин 3-илокси)фениламин, полученный согласно примеру 7, в метиленхлориде обрабатывали 2,4-дихлорбензолсульфонилхлоридом и 2 эквивалентами пиридина. Раствор концентрировали путем дистилляции метиленхлорида. По окончании реакции остаток растворителя удаляли в вакууме с получением вещества в виде густой пены. Пену повторно растворяли в метиленхлориде. Добавление 4 эквивалентов 3N HCl приводило к образованию вязкого осадка, который собирали фильтрацией. Твердые частицы промывали метиленхлоридом и затем водой. После сушки в вакууме получали аморфное твердое вещество. Анализ сжиганием углерода, водорода, азота (CHN) показал, что аморфное твердое вещество являлось HClсолью соединения 101 + 0,5 H2O. Дальнейшая очистка хлористо-водородной соли соединения 101 была достигнута путем превращения до свободного основания экстракцией в этилацетате раствором NaHCO3. Сушка над MgSO4 и концентрирование привели к свободному основанию в виде твердого вещества белого цвета. В данном примере свободное основание соединения 101 превращали обратно в хлористо-водородную соль. Однако процедуры, описанные в данном примере, могут быть использованы для получения любой аддитивной соли кислоты соединения 101, как описано в данном тексте. Свободное основание соединения 101 (300 г) суспендировали в 3,5 л теплого этанола. NaOEt в этаноле (21%, 240 мл) добавляли с образованием полного раствора. Раствор 145 мл конц. HCl (3 эквивалента) в 450 мл этанола добавляли к теплому раствору, и смесь оставляли медленно охлаждаться до комнатной температуры. Твердый осадок собирали вакуум-фильтрацией. Продукт суспендировали в воде (2 л) и вновь собирали фильтрацией. После воздушной сушки, продукт сушили в вакууме при 70 С до постоянного веса 311 г. Анализом ЯМР и CHN было подтверждено, что данный продукт является безводной HCl-солью соединения 101. Пример 9. Получение безилатной соли соединения 101. Безилатную соль соединения 101 синтезировали из гидрохлорида 2,4-дихлор-N-[3,5-дихлор-4 хинолин-3-илокси)фенил]бензолсульфонамида, полученного согласно примеру 7. Хлористо-водородную соль 2,4-дихлор-N-[3,5-дихлор-4-хинолин-3-илокси)фенил]бензолсульфонамида превращали в безилатную соль, через свободное основание, используя двухфазный раствор бикарбонат натрия/этилацетат. Отделение органического слоя с последующей заменой растворителя на этанол привело к осаждению безилатной соли (6) соединения 101 с 84% выходом. Начиная от 4-аминохинолина (2), общий выход безилатной соли (6) соединения 101 составил 73%. Получение, описанное в примерах 7 и 8, было выполнено два раза; одна загрузка дала смесь форм I и II безилатной соли соединения 101. Другая загрузка дала только полиморфную форму II безилатной соли соединения 101. Пример 10. Перекристаллизация формы II безилатной соли соединения 101 Соединение 101 перекристаллизовывали как форму II с бензолсульфокислотой (PhSO3H-хН 2 О; Aldrich). Смесь форм I и II безилатной соли (6) соединения 101 (6,938 кг), полученную согласно примерам 7 и 8, перемешивали в этилацетате (115 л) при слабом нагревании (приблизительно 28 С). Насыщенный раствор бикарбоната натрия (13 л) добавляли порциями (эндотермическая реакция с газовыделением). Двухфазную смесь перемешивали приблизительно в течение 1 ч. Фазы разделяли, и органический слой промывали насыщенным раствором хлорида натрия (13 л). Органический слой отделяли и концентрировали дистилляцией (91 л дистиллята было удалено). Этилацетат (91 л) добавляли, раствор обесцвечивали обработкой активированным углем, затем фильтровали через целит. Осадок на фильтре промывали этилацетатом (215 л), и фильтраты объединяли с этилацетатным фильтратом, полученным на стадии обесцвечивания активированным углем. Раствор концентрировали путем дистилляции приблизительно 135 л. Этанол (16 л) добавляли, и раствор нагревали до 77 С. Добавляли бензолсульфокислоту (4,126 кг),растворенную в этаноле (5 л). Добавочные 2 л этанола использовали для промывки сосуда, содержащего раствор бензолсульфокислоты. После охлаждения приблизительно до 69 С, добавляли 36 г безилатной соли (6) соединения 101. Суспензию перемешивали при температуре приблизительно от 67 до 69 С в течение 38 мин, затем охлаждали до 20 С и перемешивали в течение приблизительно 4 ч. 6,377 кг (92%) твердого вещества было получено после фильтрования и сушки в вакууме. Пример 11. Анализ формы I. В данном примере приведены данные дифференциальной сканирующей калориметрии (DSC) и анализа гигроскопичности формы I, приготовленной согласно примеру 6. Анализ XRPD образца 1 (см. фиг. 5) выявил основные пики приблизительно на 7,0, 19,5, 24,0, 24,5 и 28,5 2. Форма I обладала удивительно низкой гигроскопичностью с увеличением веса только на 0,6% в области от 25 до 95% относительной влажности и с потерей веса только на 0,6% от 95 до 25% относительной влажности (смотри фиг. 6). Пример 12. Анализ формы I. Данный пример иллюстрирует результаты анализа дифракции рентгеновских лучей на порошке(XRPD) и дифференциальной сканирующей калориметрии (DSC) формы I, полученной согласно примеру 8. Полиморфная форма I примера 8 проявила подобные свойства полиморфной формы I примера 6. Анализ XRPD образца 5 выявил основные пики приблизительно на 7,0, 19,5, 22,0, 24,0, 24,5 и 28 2. Сканирующая электронная микроскопия обнаружила, что форма I образует различного размера частицы в виде пластин с бороздками и, возможно, уложенными слоями. Инфракрасный спектр (смотри фиг. 7) показал, что форма I имеет пики приблизительно при 1567, 1461, 913, 895 и 881 см-1. Пример 13. Анализ формы II. Данный пример иллюстрирует результаты анализа дифференциальной сканирующей калориметрии(DSC) и гигроскопичности формы II, полученной согласно примеру 8. Анализ XRPD образца 6 (см. фиг. 9) выявил основные пики приблизительно на 15, 19, 20,5, 23,5,24,5, 25, 26,5, 29,5 и 30,5 2. Инфракрасный спектр (фиг. 10) показал, что форма II имеет пики приблизительно при 1573, 1469, 1459, 912 и 859 см-1. Все публикации и патентные заявки, цитированные в данном описании, включены посредством ссылки, как если каждая индивидуальная публикация или патентная заявка была специально и индивидуально предназначена для включения посредством ссылки. Хотя для ясности представления вышеприведенное изобретение описано в некоторых подробностях посредством иллюстрации и примера, обычным специалистам в данной области станет очевидно, исходя из описания данного изобретения, что некоторые изменения и модификации могут быть произведены без отступления от сущности или объема приложенной формулы изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Бензолсульфонатная соль соединения формулы (I) 2. Полиморфная форма I соединения по п.1. 3. Полиморфная форма по п.2, которая имеет максимум температуры плавления, определенный дифференциальной сканирующей калориметрией, приблизительно от 186,3 до 189,5 С. 4. Полиморфная форма по п.2, которая обладает теплотой плавления, определенной дифференциальной сканирующей калориметрией, приблизительно от 81,5 до 89,9 Дж/г. 5. Полиморфная форма по п.2, которая имеет точку плавления приблизительно между 180 и 200 С. 6. Полиморфная форма по п.2, которая имеет точку плавления приблизительно 186 С. 7. Полиморфная форма по п.2, которая обнаруживает основные пики дифракции рентгеновских лучей на порошке приблизительно на 7,0, 19,5, 22,0, 24,0, 24,5 и 28 2 при использовании Cu K излучения. 8. Полиморфная форма по п.2, которая обнаруживает основные пики абсорбции в инфракрасной области спектра приблизительно при длине волны 1567, 1461, 913, 895 и 881 см-1. 9. Полиморфная форма по п.2, которую получают путем кристаллизации безилатной соли указанного соединения формулы (I) из этанола. 10. Полиморфная форма II соединения по п. 1. 11. Полиморфная форма по п.10, которая имеет максимум температуры плавления, определенный дифференциальной сканирующей калориметрией, приблизительно 233,7 С. 12. Полиморфная форма по п.10, которая обладает теплотой плавления, определенной дифференциальной сканирующей калориметрией, приблизительно 98,9 Дж/г. 13. Полиморфная форма по п.10, которая имеет точку плавления выше чем приблизительно 230 С. 14. Полиморфная форма по п.10, которая имеет точку плавления приблизительно 233 С. 15. Полиморфная форма по п.10, которая обнаруживает основные пики дифракции рентгеновских лучей на порошке приблизительно на 15, 19, 20,5, 23,5, 24,5, 25, 26,5, 29,5 и 30,5 2 при использованииCu K излучения. 16. Полиморфная форма по п.10, которая обнаруживает основные пики абсорбции в инфракрасной области спектра приблизительно при длине волны 1573, 1469, 1459, 912 и 859 см-1. 17. Полиморфная форма по п.10, которую получают путем кристаллизации безилатной соли указанного соединения формулы (I) из этанола. 18. Фармацевтическая композиция, содержащая соль по п.1 и фармацевтически приемлемый разбавитель, наполнитель или носитель. 19. Фармацевтическая композиция, содержащая полиморфную форму по п.2 или 10 и фармацевтически приемлемый разбавитель, наполнитель или носитель. 20. Фармацевтическая композиция по п.19, где полиморфная форма находится в чистом виде. 21. Способ лечения состояния или нарушения, опосредованного рецептором PPAR-, у субъекта,где указанный способ включает в себя введение субъекту терапевтически эффективного количества соединения по пп.1, 2 или 10. 22. Способ в соответствии с п.21, где указанное PPARопосредованное состояние или нарушение является нарушением метаболизма или воспалительным состоянием.- 21013367 23. Способ в соответствии с п.22, где указанное нарушение метаболизма выбирают из группы, состоящей из диабета, ожирения, гиперхолестеринемии, гиперлипидемии, дислипидемии, гипертриглицеридемии, гипергликемии, инсулинорезистентности и гиперинсулинемии. 24. Способ в соответствии с п.23, где указанным расстройством метаболизма является диабет II типа. 25. Способ в соответствии с п.22, где указанное воспалительное состояние выбирают из группы, состоящей из ревматоидного артрита и атеросклероза. 26. Способ в соответствии с п.21, где указанным субъектом является человек.
МПК / Метки
МПК: A61K 31/47, C07D 215/16, A61P 3/10
Метки: формы, эффективного, антидиабетического, соли, соединения, полиморфные
Код ссылки
<a href="https://eas.patents.su/25-13367-soli-i-polimorfnye-formy-effektivnogo-antidiabeticheskogo-soedineniya.html" rel="bookmark" title="База патентов Евразийского Союза">Соли и полиморфные формы эффективного антидиабетического соединения</a>
Предыдущий патент: Способ и система управления для снижения тепловой нагрузки на животных
Следующий патент: Производные 2,4(4,6)-пиримидинов
Случайный патент: Способ усовершенствования восстановления золота из двойных тугоплавких золотосодержащих руд












