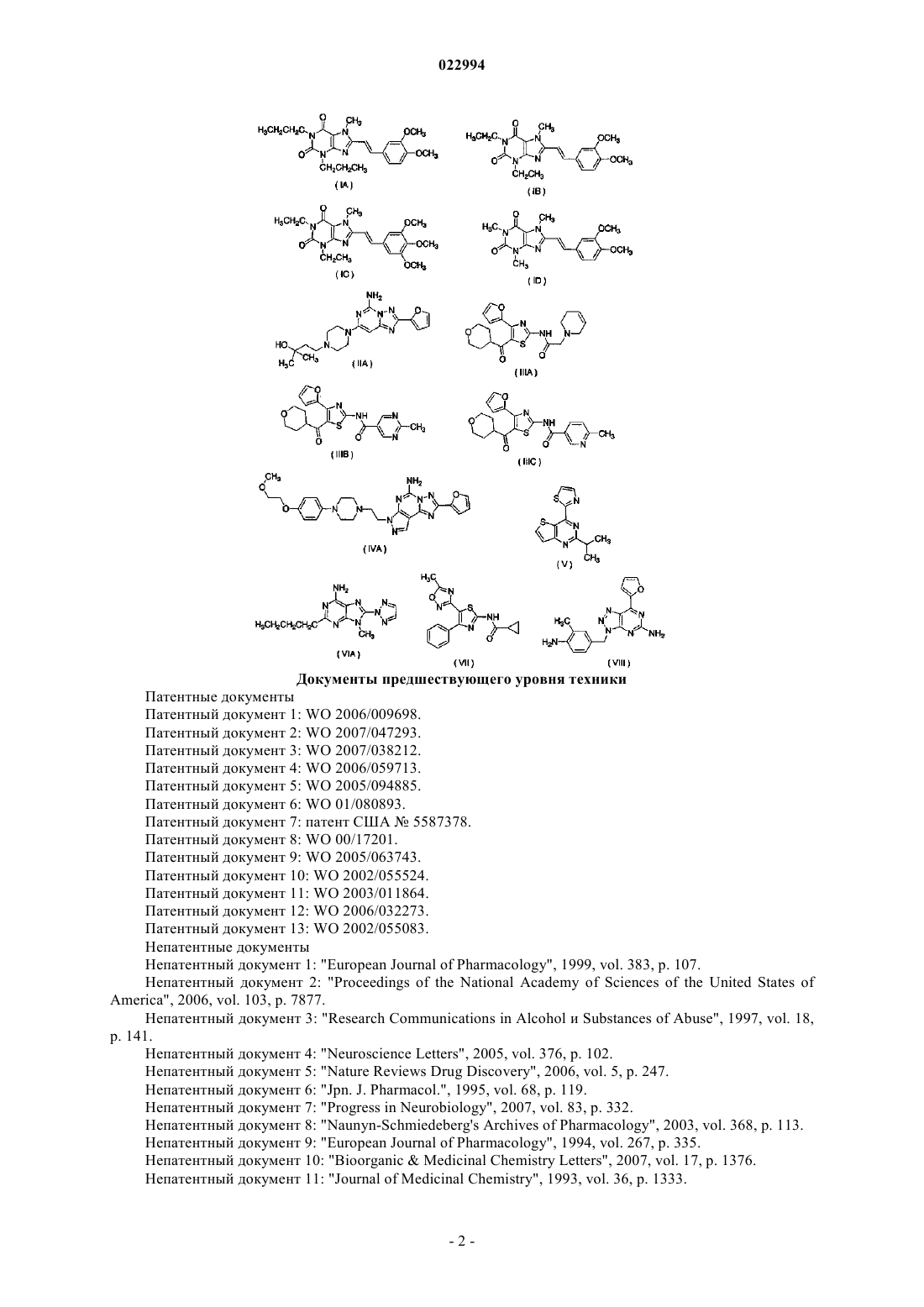
Способ подавления толерантности к опиоидному анальгетику
Номер патента: 22994
Опубликовано: 29.04.2016
Авторы: Синода Кацуми, Кодзима Йозо, Сиракура Сиро, Кунори Сундзи, Сасаки Кацутоси, Оути Дзун
Формула / Реферат
1. Способ подавления толерантности к опиоидному анальгетику, который включает введение эффективного количества соединения, представленного формулой (IIIB) или (IIIC):
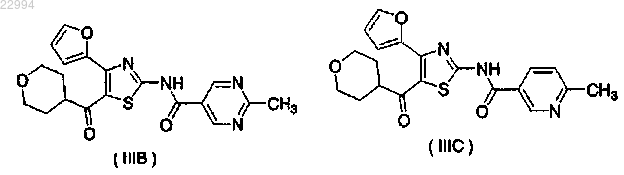
или его фармацевтически приемлемой соли, где опиоидный анальгетик представляет собой морфин.
2. Способ по п.1, где соединение представляет собой соединение, представленное следующей формулой (IIIC):
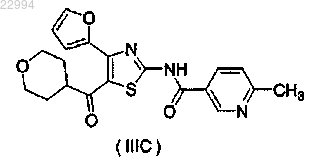
3. Применение соединения, представленного следующей формулой (IIIB) или (IIIC):

или его фармацевтически приемлемой соли для получения средства для подавления толерантности к опиоидному анальгетику, где опиоидный анальгетик представляет собой морфин.
4. Применение по п.3, где соединение представляет собой соединение, представленное следующей формулой (IIIC):
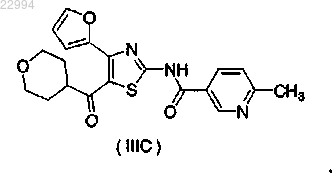
Текст
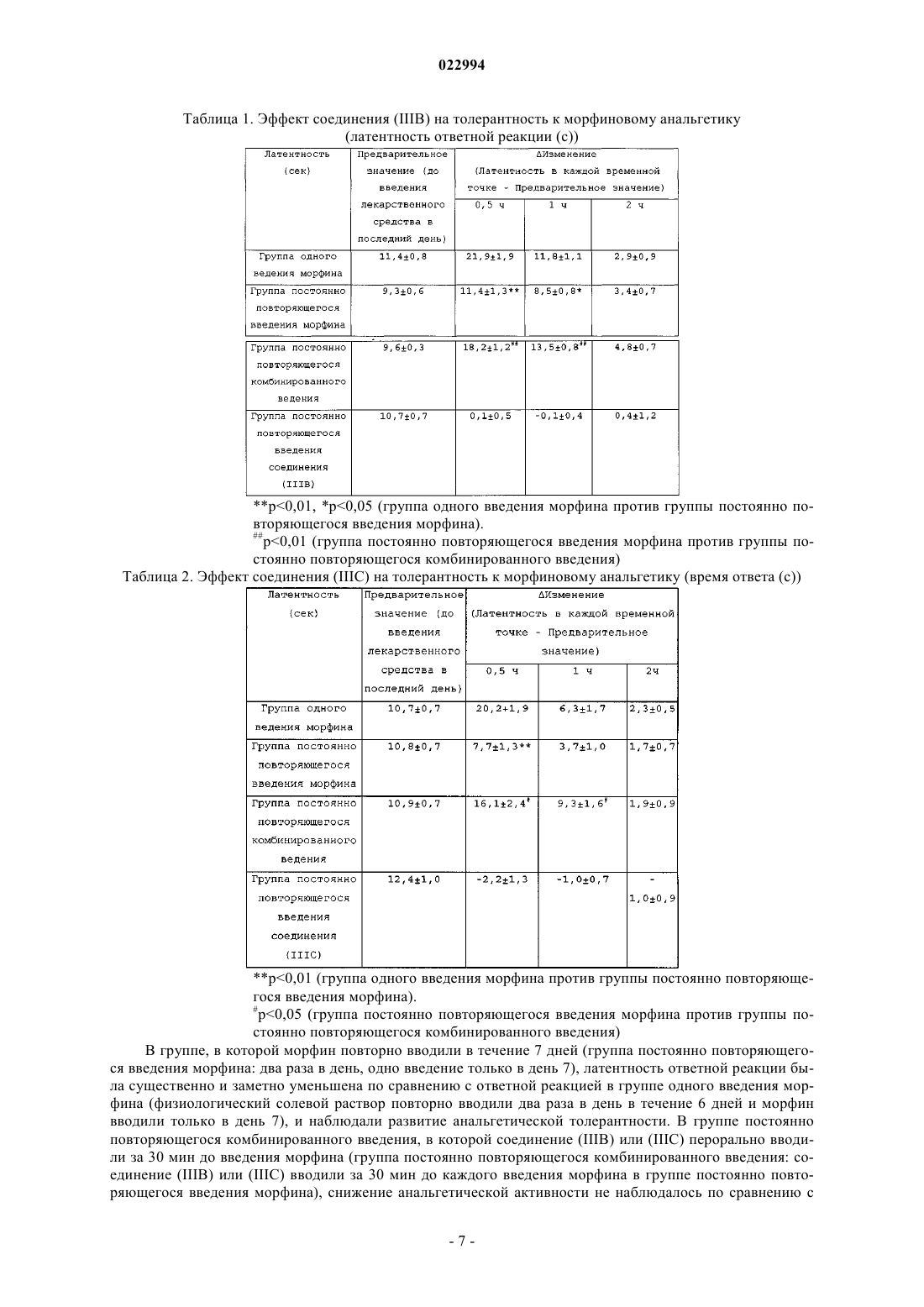
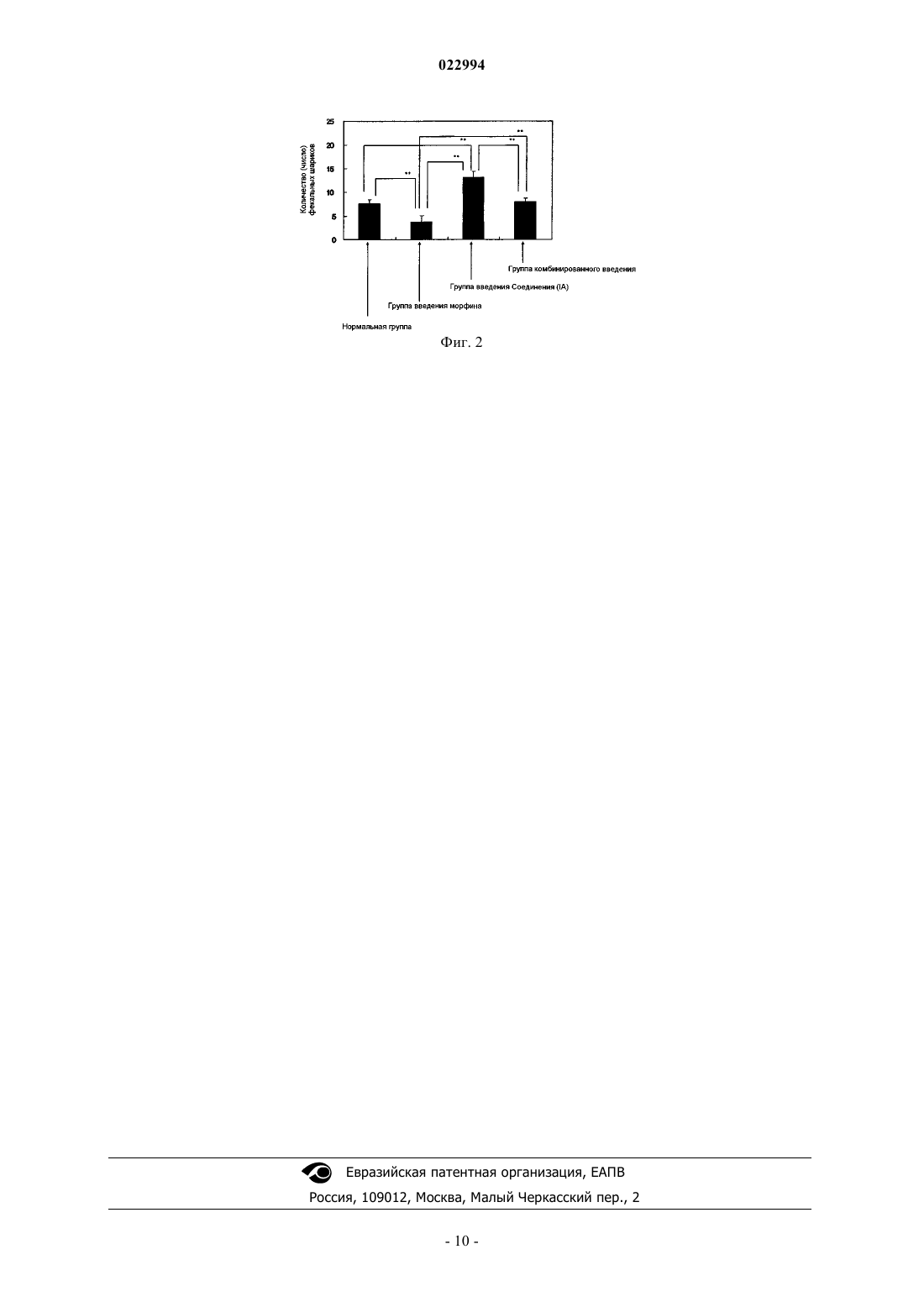
СПОСОБ ПОДАВЛЕНИЯ ТОЛЕРАНТНОСТИ К ОПИОИДНОМУ АНАЛЬГЕТИКУ Настоящее изобретение относится к способу подавления толерантности к опиоидному анальгетику,такому как морфин, введением эффективного количества соединения формулы (IIIB) или (IIIC) или его фармацевтически приемлемой соли, а также применению соединения (IIIB) или (IIIC),обладающего антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемой соли для получения средства для подавления толерантности к опиоидному анальгетику.(71)(73) Заявитель и патентовладелец: КИОВА ХАККО КИРИН КО., ЛТД. Область техники, к которой относится изобретение Настоящее изобретение относится к способу подавления нежелательных эффектов, таких как толерантность к анальгетикам, анальгетика опиоидного типа (опиоидного анальгетика), в частности морфина,применению соединений, обладающих антагонистической активностью в отношении аденозинового A2A рецептора, или их фармацевтически приемлемой соли для получения средства для подавления толерантности к опиоидному анальгетику, представляющему собой морфин. Предпосылки создания изобретения Опиоидный анальгетик широко используется при сильной острой боли и хронической боли. Известно, что опиоидный анальгетик проявляет сильный анальгетический эффект и также обнаруживает нежелательные эффекты, такие как толерантность к анальгетику, повышенная болевая чувствительность,запор, зависимость и сонливость (The Medical Clinics of North America, 2007, vol. 91, p. 199). Обычно в качестве основного способа лечения и/или предупреждения толерантности к анальгетикам или повышенной болевой чувствительности, вызванной опиоидным анальгетиком, увеличивают дозу опиоидного анальгетика, ротацию опиоидного анальгетика, изменяют способ введения лекарства или подобное. Однако увеличение дозы опиоидного анальгетика вызывает проблему усиления побочных эффектов самого опиоидного анальгетика, таких как запор, тошнота, сонливость, дыхательная недостаточность, спутанность сознания и подавление иммунитета, и, в целом, критическая эффективность снижается. Кроме того, что касается ротации опиоидного анальгетика или изменения способа введения, известно немало случаев, когда возможность принятия лекарственного средства ограничена из-за участка локализации боли или анамнеза пациента (например, нефропатия, гепатопатия и т.д.). В качестве метода для снижения нежелательного эффекта опиоидного анальгетика, такого как зависимость, например, существуют перечисленные далее сообщения: (1) Окситрекс ("The Journal of Pain",2005, vol. 6, p. 392) или Эмбеда ("Annual Meeting of The American Society of Anesthesiologists", 2007, Abstract A1370), оба из которых являются смешанным препаратом опиоидного анальгетика с ультранизкой дозой опиоидного антагониста, снижают физическую зависимость от опиоидов по сравнению с введением только опиоидного анальгетика; (2) метилналтрексон нормализует запор, вызванный введением опиоидного анальгетика ("The Annals of Pharmacotherapy", 2007, vol. 41, p. 984); (3) аминогуанидин подавляет толерантность и физическую зависимость от морфинового анальгетика ("European Journal of Pharmacology", 2006, vol. 540, pp. 60-66); (4) финастерид подавляет толерантность и физическую зависимость от морфинового анальгетика ("Hormones and Behavior", 2007, vol. 51, p. 605); (5) антагонист рецептора Nметил-D-аспарагиновой кислоты (NMDA) подавляет толерантность и зависимость от опиоидного анальгетика ("Naunyn-Schmiedeberg's Archives of Pharmacology", 2000, vol. 361, p. 425; "The Clinical Journal ofPain", 2000, vol. 16, pp. S73-9); (6) ингибитор GM1 ганглиозида подавляет толерантность и физическую зависимость от морфинового анальгетика и т.п. (US 2004-0087607); (7) 3,7-диметил-1-пропаргилксантин(DMPX), который является антагонистом аденозинового рецептора, подавляет психологическую зависимость от морфина (см. непатентный документ 1); (8) DMPX подавляет психологическую зависимость от героина (см. непатентный документ 2 и патентный документ 1); (9) 8-(3-хлорстирил)кофеин (CSC) подавляет психологическую зависимость от морфина (см. непатентный документ 3); (10) ZM241385, который является антагонистом аденозинового рецептора, влияет на возбуждающий постсинаптический ток,индуцированный DAMGO, который представляет собой один из опиоидных пептидов (см. непатентный документ 4); и (11) SCH59261 и CSC, оба из которых представляют собой антагонист аденозинового рецептора, подавляющий физическую зависимость от морфина (см. непатентный документ 8). С другой стороны, известно, что аденозин широко распространен в организме и проявляет различные физиологические эффекты на центральную нервную систему, сердечную мышцу, почки, гладкую мускулатуру и т.п. через свои рецепторы (см. непатентный документ 5). Например, известно, что антагонист аденозина A1 обладает активностью стимулирования дефекации (см. непатентный документ 6). Также известно, что аденозиновые A2A рецепторы вовлечены, в частности, в центральную нервную систему и известно, что антагонист аденозинового A2A рецептора используют в качестве терапевтического средства, например, при болезни Паркинсона и т.п. (см. непатентный документ 7). Помимо этого также известна композиция, включающая антагонист аденозинового A2A рецептора и опиоидный анальгетик для лечения синдрома усталых ног (RLS) и тому подобного (см. патентные документы 2 и 3). Кроме того, известен способ частичного снятия хронической зависимости от таких средств, как этанол или опиоидный анальгетик, с использованием антагониста аденозинового A2A рецептора (см. патентные документы 1 и 4), способ лечения заболеваний с хронической мышечноскелетной болью (см. патентный документ 5) и т.п. Кроме того, также известно, что антагонист аденозинового рецептора A2B является полезным в качестве терапевтического средства для лечения запора (см. патентный документ 6). В качестве соединения, обладающего антагонистической активностью в отношении аденозиновогоA2A рецептора, известны например, соединения, представленные следующими формулами (IA), (IB), (IC),(ID), (IIA), (IIIA), (IIIB), (IIIC), (IVA), (V), (VIA), (VII), (VIII) и подобные (см. патентные документы 7-13 и непатентные документы 9-11). Документы предшествующего уровня техники Патентные документы Патентный документ 1: WO 2006/009698. Патентный документ 2: WO 2007/047293. Патентный документ 3: WO 2007/038212. Патентный документ 4: WO 2006/059713. Патентный документ 5: WO 2005/094885. Патентный документ 6: WO 01/080893. Патентный документ 7: патент США 5587378. Патентный документ 8: WO 00/17201. Патентный документ 9: WO 2005/063743. Патентный документ 10: WO 2002/055524. Патентный документ 11: WO 2003/011864. Патентный документ 12: WO 2006/032273. Патентный документ 13: WO 2002/055083. Непатентные документы Непатентный документ 1: "European Journal of Pharmacology", 1999, vol. 383, p. 107. Непатентный документ 2: "Proceedings of the National Academy of Sciences of the United States of Краткое описание изобретения Задачи, решаемые настоящим изобретением Настоящее изобретение обеспечивает способ подавления нежелательного эффекта опиоидного анальгетика, такого как толерантность к опиоидному анальгетику, представляющему собой морфин, а также применение соединения (IIIB) или (IIIC), обладающего антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемой соли для получения средства для подавления нежелательного эффекта, такого как толерантность к анальгетику, опиоидного анальгетика, такого как морфин. Средства для решения задач Настоящее изобретение относится к следующим объектам (1)-(4).(1) Способ подавления толерантности к опиоидному анальгетику, который включает введение эффективного количества соединения, представленного формулой (IIIB) или (IIIC) или его фармацевтически приемлемой соли, где опиоидный анальгетик представляет собой морфин.(2) Способ по пункту (1), где соединение представляет собой соединение, представленное следующей формулой (IIIC):(3) Применение соединения, представленного следующей формулой (IIIB) или (IIIC): или его фармацевтически приемлемой соли для получения средства для подавления толерантности к опиоидному анальгетику, где опиоидный анальгетик представляет собой морфин.(4) Применение по пункту (3), где соединение представляет собой соединение, представленное следующей формулой (IIIC) Эффекты настоящего изобретения В соответствии с настоящим изобретением может быть обеспечен способ и получено средство для подавления толерантности к опиоидному анальгетику, такому как морфин, которое содержит соединение, представленное формулой (IIIB) или (IIIC) обладающее антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемую соль в качестве активного ингредиента. Описание вариантов воплощения настоящего изобретения Соединение, обладающее антагонистической активностью в отношении аденозинового A2A рецептора для применения в настоящем изобретении, представляет собой соединение формулы (IIIB) или или его фармацевтически приемлемую соль. Фармацевтически приемлемые соли указанных соединений включают фармацевтически приемлемые кислотноаддитивные соли, соли металлов, аммониевые соли, органические аддитивные соли аминов, аддитивные соли аминокислот и т.п. Кислотноаддитивные соли соединения, обладающего антагонистической активностью в отношении аденозинового A2A рецептора, для применения в настоящем изобретении включают, например, соли неорганических кислот, такие как гидрохлорид, сульфат, гидробромид, нитрат и фосфат; и соли органических кислот, такие как ацетат, мезилат, сукцинат, малеат, фумарат, цитрат и тартрат. Фармацевтически приемлемые соли металлов включают, например, соли щелочных металлов, такие как соли натрия и соли калия; соли щелочно-земельных металлов, такие как соли магния и соли кальция; соли алюминия, соли цинка и т.п. Фармацевтически приемлемые соли аммония включают, например, соли аммония, тетраметиламмоний и т.п. Фармацевтически приемлемые аддитивные соли органических аминов включают, например, аддитивные соли морфолина, пиперидина и т.п. Фармацевтически приемлемые аддитивные соли аминокислот включают, например, аддитивные соли глицина, фенилаланина, лизина, аспарагиновой кислоты, глутаминовой кислоты и т.п. Соединения, обладающие антагонистической активностью в отношении аденозинового A2A рецептора, или их фармацевтически приемлемые соли для применения в настоящем изобретении могут быть получены в соответствии с обычными известными способами, например способом, описанным в WO 2005/063743 или подобным. В случае, когда необходимо получить соль соединения, обладающего антагонистической активностью в отношении аденозинового A2A рецептора, для применения в настоящем изобретении, когда соответствующие соединения получают в форме соли, соединения могут быть очищены как таковые, и, когда соответствующие соединения получают в свободной форме, соли могут быть получены путем растворения или суспендирования каждого соединения в соответствующем растворителе и добавления к нему кислоты или основания, с последующим выделением и очисткой. Опиоидный анальгетик для применения в настоящем изобретении представляет собой морфин. Морфин может быть получен как коммерчески доступный продукт или путем его получения в соответствии с обычными известными способами. Что касается соединения, обладающего антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемой соли, которые могут использоваться в средстве для подавления толерантности к опиоидному анальгетику, где опиоидный анальгетик представляет собой морфин, и способа подавления толерантности к опиоидному анальгетику по настоящему изобретению, описанное выше соединение формулы (IIIB) или (IIIC), обладающее антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемую соль можно вводить отдельно как таковое, однако, как правило, они предпочтительно представляются в виде различных фармацевтических препаратов. Кроме того, такой фармацевтический препарат применяют для животных или людей. Фармацевтические препараты, относящиеся к средству для подавления толерантности к опиоидному анальгетику и способу подавления толерантности к опиоидному анальгетику по настоящему изобретению, могут содержать соединение (IIIB) или (IIIC), обладающее антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемую соль в качестве активного ингредиента. Кроме того, эти фармацевтические препараты получают путем смешивания активного ингредиента с одним или несколькими фармацевтически приемлемыми носителями (например, разбавителем, растворителем, эксципиентом и т.д.) и затем подвергают смесь обработке любыми из способов, хорошо известных в области фармацевтической технологии. Что касается способа введения, предпочтительно использовать наиболее эффективные пути введения, и примеры этих способов включают пероральное введение и парентеральное введение, такое как внутривенное введение и чрескожное введение. Примеры дозированной формы включают таблетки, инъекции, свечи, пластыри и т.п. Подходящую дозированную форму для перорального введения, например таблетку и т.п., можно получить с использованием эксципиента, такого как лактоза, дезинтегранта, такого как крахмал, лубриканта, такого как стеарат магния, связующего, такого как гидроксипропилцеллюлоза, или подобного вещества. Подходящую дозированную форму для парентерального введения, например для инъекций и тому подобного, можно получить с использованием разбавителя, растворителя и т.д., такого как солевой раствор, раствор глюкозы или смешанный раствор насыщенного солевого раствора и раствора глюкозы. Кроме того, суппозитории, пластыри и т.п. могут быть получены обычными известными способами. Дозы и частота введения соединения, обладающего антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемой соли могут варьироваться в зависимости от дозированной формы; типа; эффективности; дозы и/или дозируемой формы опиоидного анальгетика; возраста и массы тела пациента и тому подобного. Однако при пероральном введении, как правило, взрослому пациенту вводят один раз или несколько раз в день дозу от 0,01 до 1000 мг, предпочтительно от 0,05 до 100 мг. При парентеральном введении, таком как внутривенное введение, взрослому пациенту вводят один раз или несколько раз в день, в целом, дозу от 0,001 до 1000 мг, предпочтительно от 0,01 до 100 мг. Однако эти дозы и частота введения могут варьироваться в зависимости от различных условий, описанных выше.(а) Соединение (IIIB) или (IIIC), обладающее антагонистической активностью в отношении аденозинового А 2 А рецептора, или его фармацевтически приемлемая соль и (b) опиоидный анальгетик, такой как морфин, для использования в средстве для подавления толерантности к опиоидному анальгетику по настоящему изобретению могут быть использованы или введены в виде отдельного препарата (комбинированного препарата) или в виде комбинации нескольких препаратов, при условии, что, например, композицию получают вместе с фармацевтически приемлемым носителем таким образом, чтобы эти соответствующие активные ингредиенты были в нее включены. В частности, предпочтительной является комбинация двух или более препаратов. Когда такие активные ингредиенты используют или вводят в виде комбинации нескольких препаратов, эти активные ингредиенты можно использовать или вводить одновременно или раздельно через определенный промежуток времени. Следует заметить, что эти препараты предпочтительно использовать в виде, например, таблетки, раствора для инъекций, суппозитория, пластыря или подобного. Соотношение доз (мас./мас.) (а) соединения, обладающего антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемой соли и (b) опиоидного анальгетика можно соответствующим образом регулировать в соответствии с используемой комбинацией (а) соединения, обладающего антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемой соли и (b) опиоидного анальгетика, однако, в частности, соотношение находится в пределах от 1/100000 а) соединение, обладающее антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемая соль/(b) опиоидный анальгетик) до 1000/1, предпочтительно от 1/50000 до 500/1, более предпочтительно от 1/6000 до 100/1, еще более предпочтительно в пределах от 1/4000 до 15/1, еще более предпочтительно от 1/1000 до 10/1 и наиболее предпочтительно от 1/100 до 10/1. Когда эти активные ингредиенты вводят в виде комбинации нескольких препаратов, например, (а) первый компонент, содержащий соединение, обладающее антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемую соль, и (b) второй компонент, содержащий опиоидный анальгетик, отдельно формулируют в препараты и получают в виде набора, и соответствующие компоненты могут быть введены одновременно или раздельно через определенный интервал одному и тому же субъекту одним и тем же способом введения или разными способами введения с использованием этого набора. Как описано выше, средство для подавления толерантности к опиоидному анальгетику можно использовать, вводить или получать в виде отдельного препарата или комбинации нескольких препаратов,при условии, что они получены путем формулирования (а) соединения, обладающего антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемой соли и(b) опиоидного анальгетика в препарат таким образом, что соответствующие активные вещества являются включенными в этот препарат. Средство для лечения и/или предупреждения боли и подобные средства являются предпочтительными в виде единичной дозированной формы, подходящей для перорального введения, такой как таблетка, или для парентерального введения, такой как инъекция, суппозиторий или пластырь. Такие препараты получают путем смешивания соответствующих активных ингредиентов с одним или несколькими фармацевтически приемлемыми носителями (например, разбавитель, растворитель,эксципиент и т.д.), отличными от этих активных ингредиентов, и затем подвергают смесь обработке любым из способов, хорошо известных в такой области техники, как фармацевтика. Подходящие для перорального введения, например таблетки и т.п., могут быть получены с использованием эксципиента, такого как лактоза, дезинтегранта, такого как крахмал, лубриканта, такого как стеарат магния, связующего, такого как гидроксипропилцеллюлоза, и т.п. Подходящие для парентерального введения, например препарат для инъекций и подобные, могут быть получены с использованием разбавителя, растворителя и т.д., такого как солевой раствор, раствор глюкозы или смесь насыщенного солевого раствора и раствора глюкозы. Кроме того, суппозитории, пластыри и т.п. могут быть получены хорошо известными способами. В случае, когда (а) соединение, обладающее антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемая соль и (b) опиоидный анальгетик используют или вводят в виде комбинации нескольких препаратов для указанных выше целей, дозы и частота введения соответствующих активных ингредиентов могут варьировать в зависимости от дозированной формы, возраста, массы тела пациента и т.п. Однако, как правило, (а) соединение, обладающее антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемая соль и (b) опиоидный анальгетик предпочтительно вводят при следующих суточных дозах соответственно. В случае перорального введения в форме, например, таблеток, (а) соединение, обладающее антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемую соль и (b) опиоидный анальгетик вводят при дозах от 0,1 до 1000 мг и от 0,1 до 10000 мг, пред-5 022994 почтительно от 0,1 до 500 мг и от 0,1 до 5000 мг, более предпочтительно от 0,5 до 500 мг и от 1 до 3000 мг, еще более предпочтительно от 0,5 до 300 мг и от 1 до 2000 мг соответственно взрослому пациенту,как правило, один раз или несколько раз в день, одновременно или раздельно через определенный интервал времени. В случае парентерального введения в форме, например, инъекции и т.п., (а) соединение, обладающее антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемую соль и (b) опиоидный анальгетик вводят при дозах от 0,1 до 1000 мг и от 0,1 до 10000 мг, предпочтительно от 0,1 до 500 мг и от 0,1 до 5000 мг, более предпочтительно от 0,5 до 500 мг и от 1 до 3000 мг, еще более предпочтительно от 0,5 до 300 мг и от 1 до 2000 мг соответственно, взрослому пациенту, как правило, один раз или несколько раз в день, одновременно или раздельно через определенный интервал времени. Также, в случае, когда (а) соединение, обладающее антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемую соль и (b) опиоидный анальгетик используют или вводят в виде одного препарата для указанных выше целей, дозы и частота введения могут варьировать в зависимости от активности соответствующих активных ингредиентов; дозированной формы; возраста, массы тела и симптома пациента; и т.п. Однако предпочтительно, когда соответствующие активные ингредиенты формулируют в один препарат при таких же дозах, как в указанном выше случае, где соответствующие активные ингредиенты используют и вводят в виде комбинации нескольких препаратов, и полученный единый препарат используют или вводят. Однако эти дозы и частота введения варьируют в зависимости от указанных выше различных условий. Далее супрессорный эффект соединения (IIIB) или (IIIC), обладающего антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемой соли на нежелательный эффект опиоидного анальгетика, а также эффект введения (а) соединения (IIIB) или (IIIC),обладающего антагонистической активностью в отношении аденозинового А 2 А рецептора, или его фармацевтически приемлемой соли и (b) опиоидного анальгетика, в комбинации, конкретно описан в примере испытания. Пример испытания. Супрессорное действие соединения (III) на толерантность к морфиновому анальгетику Экспериментальные материалы и методы 1. Используемые животные Использовали самцов ddY мышей (возраст 3-4 недели, Japan SLC, Inc.) с массой тела от 19 до 25 г и животных поддерживали в следующих условиях: комнатная температура от 19 до 25C, влажность от 30 до 70% и 12-часовой цикл свет/темнота (период света от 7 ч утра до 7 ч вечера, период темноты от 7 ч вечера до 7 ч утра) вплоть до момента, когда их подвергали эксперименту. Пищу и воду обеспечивали adlibitum. 2. Используемые средства и способы получения Далее, испытание осуществляли в соответствии с инструкциями исследователей, занимающихся наркотическими веществами, и в соответствии с правилами обращения с наркотическими веществами каждый раз, когда использовали морфин. Морфин растворяли в физиологическом растворе при концентрации 0,6 мг/мл и подкожно вводили при дозе 6 мг/кг. Соединение (IIIB) суспендировали в 0,5% МС при концентрации 0,3 мг/мл и перорально вводили при дозе 3 мг/кг. Соединение (IIIC) суспендировали в 0,5% МС при концентрации 0,1 мг/мл и перорально вводили при дозе 1 мг/кг. 3. Определение анальгетической активности Ноцицептивную боль определяли методом горячей пластины. Каждую мышь помещали на устройство с горячей пластиной (35100, Ugo Basile, Comerio, VA, Italy), установленное на 53C, и время (латентность) до индукции реакции избегания (зализывание, покусывание, подергивание лапы или прыгание) определяли как болевой порог. В этом эксперименте использовали животных, у которых латентность ответной реакции составляла от 6 до 16 с перед тем, как использовали первое введение лекарственного средства. Кроме того, чтобы свести к минимуму повреждение на участке стимуляции, устанавливали отсечку времени 45 с. Анальгетическую активность оценивали путем определения латентности ответной реакции до введения лекарственного средства и через 30, 60 и 120 мин после введения лекарственного средства в последний день постоянно повторяющегося введения лекарственного средства (в день 7). 4. Статистическая обработка Результаты эксперимента выражали как среднее значение + стандартная ошибка. Статистический анализ осуществляли с использованием программы для статистического анализа SAS (SAS Institute Inc.,Cary, NC, USA). Сравнение между двумя группами осуществляли с использованием оценочного критерия Wilcoxn. p - Значение меньше чем 0,05% считалось значимым различием. 5. Результаты эксперимента Результаты представлены в табл. 1 и 2. р 0,01, р 0,05 (группа одного введения морфина против группы постоянно повторяющегося введения морфина). р 0,01 (группа постоянно повторяющегося введения морфина против группы постоянно повторяющегося комбинированного введения) Таблица 2. Эффект соединения (IIIC) на толерантность к морфиновому анальгетику (время ответа (с р 0,01 (группа одного введения морфина против группы постоянно повторяющегося введения морфина). р 0,05 (группа постоянно повторяющегося введения морфина против группы постоянно повторяющегося комбинированного введения) В группе, в которой морфин повторно вводили в течение 7 дней (группа постоянно повторяющегося введения морфина: два раза в день, одно введение только в день 7), латентность ответной реакции была существенно и заметно уменьшена по сравнению с ответной реакцией в группе одного введения морфина (физиологический солевой раствор повторно вводили два раза в день в течение 6 дней и морфин вводили только в день 7), и наблюдали развитие анальгетической толерантности. В группе постоянно повторяющегося комбинированного введения, в которой соединение (IIIB) или (IIIC) перорально вводили за 30 мин до введения морфина (группа постоянно повторяющегося комбинированного введения: соединение (IIIB) или (IIIC) вводили за 30 мин до каждого введения морфина в группе постоянно повторяющегося введения морфина), снижение анальгетической активности не наблюдалось по сравнению с группой единственного введения морфина, и развитие анальгетической толерантности предотвращалось. Следует отметить, что в группе, в которой повторно вводили только соединение (IIIB) или (IIIC) (группа постоянно повторяющегося введения соединения (IIIB), группа постоянно повторяющегося введения(IIIC, эффект на латентность ответной реакции не наблюдали. Исходя из результатов описанного выше испытания, было подтверждено, что соединения (IIIB) и(IIIC) обладают эффектом супрессии и толерантности к морфиновому анальгетику. Исходя из этого, считают, что развитие толерантности к анальгетикам после постоянного в течение длительного периода времени введения опиоидного анальгетика можно предотвратить путем использования соединения (III),такого как соединение (IIIB) или (IIIC), и опиоидного анальгетика в комбинации. Далее, аспекты настоящего изобретения более конкретно описаны при помощи примеров, однако объем настоящего изобретения не ограничивается этими примерами. Пример 1 Таблетки, имеющие следующий состав, получали в соответствии с традиционным способом. Соединение (IIIB) (40 г), лактозу (286,8 г) и картофельный крахмал (60 г) смешивали и затем добавляли к смеси 10% водного раствора гидроксипропилцеллюлозы (120 г). Полученную смесь перемешивали, гранулировали, сушили и просеивали через сито в соответствии с традиционным способом, получая, таким образом, гранулы для таблетирования. Добавляли стеарат магния (1,2 г) и все смешивали и полученную смесь подвергали таблетированию с использованием машины для таблетирования (RT-15, изготовительKikusui Seisakusho Ltd.) со штампом, имеющим диаметр 8 мм, таким образом получали таблетки (содержащие 20 мг активного ингредиента в расчете на таблетку). Таблица 3 Пример 2 Таблетки, имеющие следующий состав, получали таким же способом, как в примере 1. Таблица 4 Пример 3 Таблетки, имеющие следующий состав, получали таким же способом, как в примере 1. Таблица 5 Пример 4 Препарат для инъекций, имеющий следующий состав, получали в соответствии с традиционным способом. Морфин добавляли к дистиллированной воде для инъекций и все смешивали. Затем добавляли хлористо-водородную кислоту и водный раствор гидроксида натрия для доведения pH смеси до 7 и добавляли к смеси дистиллированную воду для инъекций для доведения общего объема смеси до 1000 мл. Полученную жидкую смесь использовали для асептического заполнения стеклянных флаконов в количестве 2 мл на флакон, получая, таким образом, препарат для инъекций (содержащий 2 мг активного ингредиента в расчете на флакон). Промышленная применимость В соответствии с настоящим изобретением могут быть предоставлены способ подавления нежелательного эффекта опиоидного анальгетика, такого как толерантность к опиоидному анальгетику, представляющему собой морфин, а также применение соединения, обладающего антагонистической активностью в отношении аденозинового A2A рецептора, или его фармацевтически приемлемой соли для получения средства для подавления нежелательного эффекта, такого как толерантность к анальгетику, опиоидного анальгетика, такого как морфин. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ подавления толерантности к опиоидному анальгетику, который включает введение эффективного количества соединения, представленного формулой (IIIB) или (IIIC): или его фармацевтически приемлемой соли, где опиоидный анальгетик представляет собой морфин. 2. Способ по п.1, где соединение представляет собой соединение, представленное следующей формулой (IIIC): 3. Применение соединения, представленного следующей формулой (IIIB) или (IIIC): или его фармацевтически приемлемой соли для получения средства для подавления толерантности к опиоидному анальгетику, где опиоидный анальгетик представляет собой морфин. 4. Применение по п.3, где соединение представляет собой соединение, представленное следующей формулой (IIIC):
МПК / Метки
МПК: C07D 495/04, A61K 31/52, C07D 473/34, A61K 31/506, A61K 45/00, C07D 473/06, A61K 31/522, A61K 31/343, A61K 31/4439, C07D 487/04, A61P 43/00, A61P 25/04, A61K 31/519, C07D 417/14, A61K 31/427, C07D 487/14
Метки: опиоидному, способ, толерантности, анальгетику, подавления
Код ссылки
<a href="https://eas.patents.su/11-22994-sposob-podavleniya-tolerantnosti-k-opioidnomu-analgetiku.html" rel="bookmark" title="База патентов Евразийского Союза">Способ подавления толерантности к опиоидному анальгетику</a>
Предыдущий патент: Молекулы нуклеиновой кислоты, кодирующие альфа- и бета-цепи фолликулостимулирующего гормона человека (fsh)
Следующий патент: Непрерывный способ превращения природного газа в жидкие углеводороды
Случайный патент: Продукт, подобный лярду, и сособ его получения