Фенил – или пиридиламидные соединения в качестве антагонистов простагландина е2
Номер патента: 9201
Опубликовано: 28.12.2007
Авторы: Окумура Йосиюки, Нукуи Сейдзи, Накао Казунари, Ямагиси Тацуя
Формула / Реферат
1. Соединение формулы I

где А представляет собой фенильную группу или пиридильную группу;
В представляет собой фенильную группу, нафтильную группу, пиридильную группу, хинолильную группу или изохинолильную группу;
Е представляет собой 1,4-фениленовую группу; R1 и R2 независимо представляют собой атом водорода, атом галогена, галогеналкильную группу, имеющую от 1 до 4 атомов углерода, цианогруппу или аминокарбонильную группу; R3 и R4 независимо представляют собой атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода; или группы R3 и R4, взятые вместе, могут образовывать алкиленовую цепь, имеющую от 2 до 6 атомов углерода; R5 представляет собой
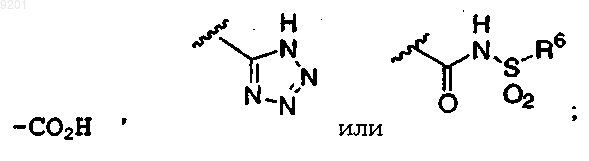
R6 представляет собой алкильную группу, имеющую от 1 до 6 атомов углерода, циклоалкильную группу, имеющую от 3 до 7 атомов в кольце, фенильную или пиридильную группу;
X представляет собой метиленовую группу или атом кислорода;
указанные фенильная, нафтильная, пиридильная, хинолильная и изохинолильная группы в определениях значений В не замещены или замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей a;
указанная 1,4-фениленовая группа в определениях значений Е не замещена или замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей b;
указанные фенильная, пиридильная, тиазолильная и имидазолильная группы в определениях значений R6 и a не замещены или замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей b;
указанные заместители a выбраны из группы, состоящей из атомов галогена, алкильных групп, имеющих от 1 до 4 атомов углерода, алкоксигрупп, имеющих от 1 до 4 атомов углерода, галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода, цианогрупп, алкинильных групп, имеющих от 2 до 6 атомов углерода, циклоалкильных групп, имеющих от 3 до 7 атомов в кольце, тизолильной группы, имидазолильной группы, пиридильной группы, фенильной группы, бензилоксигруппы, бензоильной группы, двух соседних a-групп, которые, взятые вместе, могут образовывать алкиленовую цепь, имеющую 3 или 4 атома углерода, алкилтиогрупп, имеющих от 1 до 4 атомов углерода, диалкиламиноалкильных групп, имеющих от 1 до 6 атомов углерода в каждой алкильной части;
указанные заместители b выбраны из группы, состоящей из атомов галогена, алкильных групп, имеющих от 1 до 4 атомов углерода, и алкоксигрупп, имеющих от 1 до 4 атомов углерода; при условии, что R1 и R2 одновременно не являются атомом водорода;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, в котором Е представляет собой незамещенную 1,4-фениленовую группу.
3. Соединение по п.1, в котором Е представляет собой 1,4-фениленовую группу, замещенную по меньшей мере одним заместителем, выбранным из группы, состоящей из атомов галогена и алкильных групп, имеющих от 1 до 4 атомов углерода.
4. Соединение по любому из пп.1-3, в котором
В представляет собой фенильную или пиридильную группу;
указанная группа не замещена или замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей a; указанные заместители a выбраны из группы, состоящей из атомов галогена, алкильных групп, имеющих от 1 до 4 атомов углерода, алкоксигрупп, имеющих от 1 до 4 атомов углерода, галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода, цианогрупп, алкинильных групп, имеющих от 2 до 6 атомов углерода, циклоалкильных групп, имеющих от 3 до 7 атомов в кольце, тиазолильной группы, имидазолильной группы, пиридильной группы, фенильной группы, бензилоксигруппы, бензоильной группы, двух соседних a-групп, которые, взятые вместе, могут образовывать алкиленовую цепь, содержащую 3 атома углерода, алкилтиогрупп, имеющих от 1 до 4 атомов углерода и диалкиламиноалкильных групп, имеющих от 1 до 6 атомов углерода в алкильной части; где указанные тизолильная, имидазолильная и пиридильная группы, рассмотренные в определении заместителей a, не замещены или замещены алкильными группами, имеющими от 1 до 4 атомов углерода.
5. Соединение по любому из пп.1-3, в котором
B представляет собой фенильную группу, которая может быть замещена заместителем, выбранным из группы, состоящей из заместителей a;
указанные заместители a выбраны из группы, состоящей из атомов галогена, алкильных групп, имеющих от 1 до 4 атомов углерода, алкоксигрупп, имеющих от 1 до 4 атомов углерода, галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода, цианогрупп, алкинильных групп, имеющих от 2 до 6 атомов углерода, циклоалкильных групп, имеющих от 3 до 7 атомов в кольце, алкилтиогрупп, имеющих от 1 до 4 атомов углерода, диалкиламиноалкильных групп, имеющих от 1 до 6 атомов углерода в алкильной части, тиазолильных, имидазолильных, пиридильных, бензилокси-, фенильных или бензоильных групп;
указанные тиазолильные, имидазолильные и пиридильные группы, рассмотренные в определении заместителей a, не замещены или замещены алкильными группами, имеющими от 1 до 4 атомов углерода.
6. Соединение по любому из пп.1-3, в котором
В представляет собой фенильную группу, которая может быть замещена заместителем, выбранным из группы, состоящей из заместителей a;
указанные заместители a выбраны из группы, состоящей из атомов фтора, атомов хлора, метильных групп, этильных групп, метоксигрупп, трифторметоксигрупп, цианогрупп, этинильных групп, циклопентильных групп, метилтиогрупп, диметиламиноэтильных групп, фенильных групп, имидазолильных групп, необязательно замещенных метильными группами, тиазолильных групп, необязательно замещенных метильными группами, пиридильных групп или бензилоксигрупп.
7. Соединение по любому из пп.1-3, в котором R1 представлет собой атом галогена, a R2 представляют собой атом водорода.
8. Соединение по любому из пп.1-3, в котором R3 и R4 независимо представляют собой атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода.
9. Соединение по любому из пп.1-3, в котором R3 представлет собой алкильную группу, имеющую от 1 до 4 атомов углерода, a R4 представлет собой атом водорода.
10. Соединение по любому из пп.1-3, в котором R3 представлет собой метильную группу, a R4 представляет собой атом водорода.
11. Соединение по любому из пп.1-3, в котором R5 представлет собой
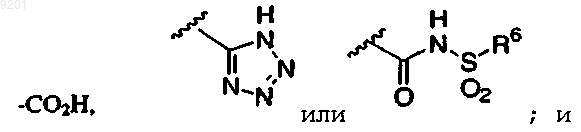
R6 представлет собой фенильную группу, необязательно замещенную атомами галогена, или пиридильную группу.
12. Соединение по любому из пп.1-3, в котором R5 представлет собой
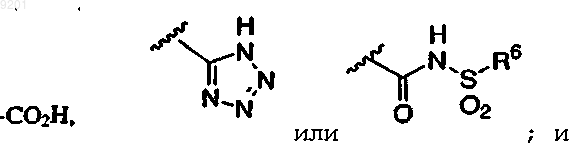
R6 представлет собой фенильную группу, необязательно замещенную атомами галогена.
13. Соединение по любому из пп.1-3, в котором R5 представлет собой

14. Соединение по п.1, выбранное из
4-((1S)-1-{[5-хлор-2-(4-фторфенокси)бензоил]амино}этил)бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(4-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-цианофенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-хлорфенокси)пиридин-3-ил ]карбонил}амино)этил]бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3-фторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3-метоксифенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3-хлорфенокси)бензоил]амино}этил)бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2,4-дифторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(4-хлор-3-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2-хлор-4-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2,6-дифторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3,4-дифторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-{(1S)-1-[({5-хлор-2-[3-(1,3-тиазол-2-ил)фенокси]пиридин-3-ил}карбонил)амино]этил}бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2,3-дифторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2,5-дифторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты
4-[(1S)-1-({[5-хлор-2-(4-хлорфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(4-хлор-2-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2-хлор-5-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-метилфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(4-фтор-3-метилфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3,5-дифторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(2,3-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(2,4-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3,4-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-хлор-5-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-хлор-2-метилфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3,5-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(2,5-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-хлор-2-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-пиридин-2-илфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(4-пиридин-2-илфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(4-пиридин-4-илфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-хлор-5-метилфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3-метилфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3-хлор-5-фторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(2,6-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[(5-хлор-2-феноксипиридин-3-ил)карбонил]амино}этил)бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2,3-диметилфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2,3-дихлорфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3,4-дихлорфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3,5-дихлорфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
и 4-[(1S)-1-({[5-хлор-2-(3-фтор-4-метилфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты; или их фармацевтически приемлемой соли.
15. Соединение по п.1, выбранное из
4-((1S)-1-{[5-хлор-2-(4-фторфенокси)бензоил]амино}этил)бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(4-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-цианофенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-хлорфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3-фторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3-хлорфенокси)бензоил]амино}этил)бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2-хлор-4-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2,6-дифторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2- (3,4-дифторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2,3-дифторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2,5-дифторфенокси)пиридин-3-ил ]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2-хлор-5-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-метилфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3,5-дифторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(2,3-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3,4-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-хлор-5-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3,5-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(2,5-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3-хлор-5-метилфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3-метилфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(3-хлор-5-фторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[5-хлор-2-(2,6-дифторфенокси)бензоил]амино}этил)бензойной кислоты;
4-((1S)-1-{[(5-хлор-2-феноксипиридин-3-ил)карбонил]амино}этил)бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(2,3-дихлорфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3,4-дихлорфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
4-[(1S)-1-({[5-хлор-2-(3,5-дихлорфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты; и
4-[(1S)-1-({[5-хлор-2-(3-фтор-4-метилфенокси)пиридин-3-ил]карбонил}амино)этил]бензойной кислоты;
или их фармацевтически приемлемой соли.
16. Фармацевтическая композиция для лечения опосредуемого простогландином патологического состояния у индивидуума-млекопитающего, которая включает терапевтически эффективное количество соединения по любому из пп.1-15 или его фармацевтически приемлемой соли и подходящий фармацевтически приемлемый носитель, где указанным заболеванием является боль, воспаление, остеоартрит или ревматоидный артрит.
17. Комбинация соединения формулы I по любому из пп.1-15 и дополнительного фармакологически активного агента.
18. Соединение формулы II
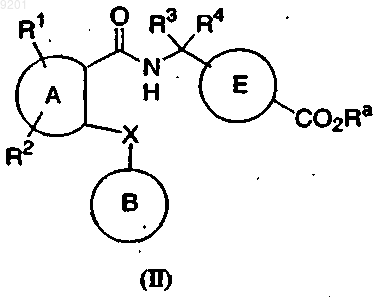
где А представляет собой фенильную группу или пиридилькую группу;
В представляет собой фенильную группу, нафтильную группу, пиридильную группу, хинолильную группу или изохинолильную группу;
Е представляет собой 1,4-фениленовую группу;
R1 и R2 независимо представляют собой атом водорода, атом галогена, галогеналкильную группу, имеющую от 1 до 4 атомов углерода, цианогруппу или аминокарбонильную группу;
R3 и R4 независимо представляют собой атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода; или группы R3 и R4, взятые вместе, могут образовывать алкиленовую цепь, имеющую от 2 до 6 атомов углерода;
Ra представляет собой алкильную группу, имеющую от 1 до 6 атомов углерода;
X представляет сосющ метиленовую группу или атом кислорода;
указанные фенильная, нафтильная, пиридильная, хинолильная и изохинолильная группы, рассмотренные в определениях В, не замещены или замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей a;
указанная 1,4-фениленовая группа, рассмотренная в определении Е, не замещена или замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей b;
указанные фенильная, пиридильная, тиазолильная и имидазолильная группы, рассмотренные в определениях R6 и a, не замещены или замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей b;
указанные заместители a выбраны из группы, состоящей из атомов галогена, алкильных групп, имеющих от 1 до 4 атомов углерода, алкоксигрупп, имеющих от 1 до 4 атомов углерода, галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода, цианогрупп, алкинильных групп, имеющих от 2 до 6 атомов углерода, циклоалкильных групп, имеющих от 3 до 7 атомов в кольце, тиазолильной группы, имидазолильной группы, пиридильной группы, фенильной группы, бензилоксигруппы, бензоильной группы, двух соседних a-групп, которые, взятые вместе, могут образовывать алкиленовую цепь, имеющую 3 или 4 атома углерода, алкилтиогрупп, имеющих от 1 до 4 атомов углерода, диалкиламиноалкильных групп, имеющих от 1 до 6 атомов углерода в каждой алкильной части;
указанные заместители b выбраны из группы, состоящей из атомов галогена, алкильных групп, имеющих от 1 до 4 атомов углерода, и алкоксигрупп, имеющих от 1 до 4 атомов углерода;
при условии, что R1 и R2 одновременно не являются атомом водорода;
или его фармацевтически приемлемая соль.
19. Соединение формулы III
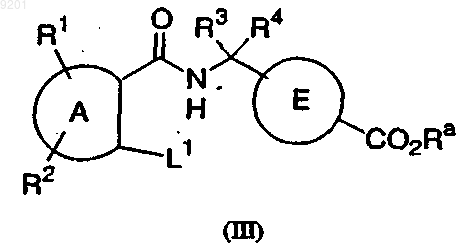
где А представляет собой фенильную группу или пиридильную группу;
Е представляет собой 1,4-фениленовую группу;
R1 и R2 независимо представляют собой атом водорода, атом галогена, галогеналкильную группу, имеющую от 1 до 4 атомов углерода, цианогруппу или аминокарбонильную группу;
R3 и R4 независимо представляют собой атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода; или группы R3 и R4, взятые вместе, могут образовывать алкиленовую цепь, имеющую от 2 до 6 атомов углерода;
Ra представляет собой алкильные группы, имеющие от 1 до 6 атомов углерода;
L1 представляет собой атом галогена, алкансульфонилоксигруппу, имеющую от 1 до 4 атомов углерода, арилсульфонилоксигруппу, необязательно замещенную алкильной группы, имеющей от 1 до 4 атомов углерода, галогеналкансульфонилоксигруппу, имеющую от 1 до 4 атомов углерода, или группу бороновой кислоты (В(ОН)2);
указанная 1,4-фениленовая группа, рассмотренная в определении Е, не замещена или замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей b;
указанные заместители b выбраны из группы, состоящей из атомов галогена, алкильных групп, имеющих от 1 до 4 атомов углерода, и
алкоксигрупп, имеющих от 1 до 4 атомов углерода;
при условии, что R1 и R2 одновременно не являются атомом водорода; а также при условии, что соединение формулы III не представляет собой трет-бутил-4-[(5-бром-2-иодбензоиламино)метил]бензоат.
20. Соединение формулы I
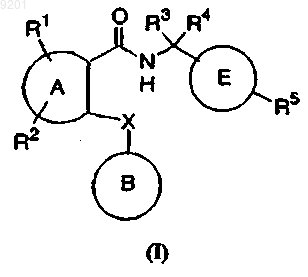
где А представлет собой фенильную группу или пиридильную группу;
В представлет собой фенильную группу, нафтильную группу, пиридильную группу, хинолильную группу или изохинолильную группу;
Е представляет собой фениленовую группу;
R1 и R2 независимо представляют собой атом водорода, атом галогена, галогеналкильную группу, имеющую от 1 до 4 атомов углерода, цианогруппу или аминокарбонильную группу; R3 и R4 независимо представляют собой атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода; или группы R3 и R4, взятые вместе, могут образовывать алкиленовую цепь, имеющую от 3 до 6 атомов углерода; R5 представляет собой
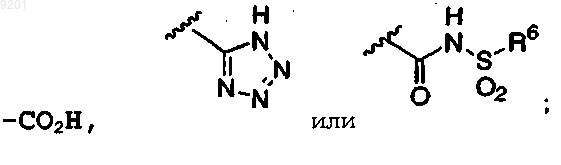
R6 представляет собой алкильную группу, имеющую от 1 до 6 атомов углерода, циклоалкильную группу, имеющую фенильную группу или пиридильную группу, содержащую от 3 до 7 атомов в кольце;
X представляет собой метиленовую группу или атом кислорода; указанные фенильная, нафтильная, пиридильная, хинолильная или изохинолильная группы в определениях значений В не замещены или замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей a;
указанная фениленовая группа в определениях значений Е не замещена или замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей b; указанные фенильная, пиридильная, тиазолильная и имидазолильная группы в определениях значений R6 и a не замещены или замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей b;
указанные заместители a выбраны из группы, состоящей из атомов галогена, алкильных групп, имеющих от 1 до 4 атомов углерода, алкоксигрупп, имеющих от 1 до 4 атомов углерода, галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода, цианогрупп, алкинильных групп, имеющих от 2 до 6 атомов углерода, циклоалкильных групп, имеющих от 3 до 7 атомов в кольце, тиазолильной группы, имидазолильной группы, пиридильной группы, фенильной группы, бензилоксигруппы, бензоильной группы двух соседних a-групп, которые, взятые вместе, могут образовывать алкиленовую цепь, имеющую 3 или 4 атома углерода, алкилтиогрупп, имеющих от 1 до 4 атомов углерода, диалкиламиноалкильных групп, имеющих от 1 до 6 атомов углерода в каждой алкильной части;
указанные заместители b выбраны из группы, состоящей из атомов галогена, алкильных групп, имеющих от 1 до 4 атомов углерода, и алкоксигрупп, имеющих от 1 до 4 атомов углерода;
или его фармацевтически приемлемая соль.
21. Соединение по п.20, в котором Е представлет собой незамещенную 1,4-фениленовую группу.
22. Соединение по п.20, в котором Е представляет собой 1,4-фениленовую группу, замещенную по меньшей мере одним заместителем, выбранным из группы, состоящей из атомов галогена и алкильных групп, имеющих от 1 до 4 атомов углерода.
Текст
009201 Настоящее изобретение относится к новым арил- или гетероариламидным соединениям и к их применению в терапии. Данные соединения могут быть использованы в качестве антагонистов рецептора простагландина Е 2, а поэтому они могут быть использованы для лечения боли и воспаления и других заболеваний, ассоциированных с воспалением, таких как артрит, и для лечения расстройств или патологических состояний, выбранных из боли, воспалительных заболеваний и т.п., у млекопитающих, а в частности у людей. Настоящее изобретение также относится к фармацевтической композиции, содержащей описанные выше соединения. Предшествующий уровень техники Простагландины представляют собой медиаторы боли, повышения температуры и других симптомов, связанных с воспалением. Простагландин Е 2 (PGE2) представляет собой эйкозаноид, обнаруживаемый преимущественно при воспалительных состояниях. Кроме того, он также участвует в различных физиологических и/или патологических процессах, таких как гипералгезия, сокращение матки, перистальтика пищеварительного тракта, бодрствование, супрессия секреции желудочной кислоты, кровяное давление, функция тромбоцитов, метаболизм костей, ангиогенез и т.п. Были клонированы четыре подтипа рецептора PGE2 (EP1, EP2, ЕР 3 и ЕР 4), обладающие различными фармакологическими свойствами. Подтип ЕР 4, Gs-сопряженный рецептор, стимулирует продуцирование сАМР, и распространен в тканях широкого спектра, что позволяет предположить о его главной роли в биологических процессах, опосредованных PGE2. Некоторые соединения согласно изобретению, по существу, описаны в WO 98/45268 и ЕР-А 1229034 как ингибиторы PDE4, в WO 03/16254 как антагонисты рецептора ЕР 4, в WO 00/64876 как вещества, связывающиеся с рецептором лиганда PPAR, и в DE2500157 (US4221815) и DE2706977(US4181658) как противодиабетические вещества. В WO 00/20371 описано семейство антагонистов рецептора PGE, которые отличаются от соединений согласно изобретению тем, что в их фенильном кольце имеется ортозамещение. В WO 01/57036 описан ряд ингибиторов PDE4 никотинамида. Целью настоящего изобретения является получение модуляторов рецептора ЕР 4 (например, агонистов и антагонистов), которые обладали бы улучшенной способностью модулировать рецептор ЕР 4, (например, агонистической или антагонистической активностью). В частности, настоящее изобретение относится к получению антагонистов рецептора ЕР 4, которые могут быть использованы в терапии, а особенно для лечения боли и воспалений. Описание сущности изобретения В настоящее время было обнаружено, что арил- или гетероариламидные соединения являются селективными антагонистами рецептора ЕР 4, которые, при их системном введении, обладают аналгетической активностью. Соединения согласно изобретению могут обнаруживать незначительную токсичность, хорошее всасывание, нужную локализацию, хорошую растворимость, низкую аффинность связывания с белком, низкий уровень взаимодействия с другими лекарственными средствами и хорошую метаболическую стабильность. Настоящее изобретение относится к соединению следующей формулы (I): где А представляет собой фенильную группу или пиридильную группу; В представляет собой арильную группу или гетероарильную группу; Е представляет собой 1,4-фениленовую группу;R1 и R2 независимо представляют атом водорода, атом галогена, алкильную группу, имеющую от 1 до 4 атомов углерода, алкоксигруппу, имеющую от 1 до 4 атомов углерода, галогеналкильную группу,имеющую от 1 до 4 атомов углерода, галогеналкоксигруппу, имеющую от 1 до 4 атомов углерода, цианогруппу или аминокарбонильную группу;R3 и R4 независимо представляют атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода; или группы R3 и R4, взятые вместе, могут образовывать алкиленовую цепь, имеющую от 2 до 6 атомов углерода;R6 представляет собой алкильную группу, имеющую от 1 до 6 атомов углерода, циклоалкильную группу, имеющую, содержащий от 3 до 7 атомов в кольце, арильную группу или гетероарильную группу;X представляет собой метиленовую группу, атом кислорода или атом серы; где указанные арильные группы имеют от 6 до 10 атомов углерода; указанные гетероарильные группы представляют собой 5-10-членные ароматические гетероциклические группы, содержащие от 1 до 3 гетероатомов, выбранных из группы, состоящей из атомов серы,кислорода и азота; указанные арильные и гетероарильные группы, в соответствии с определениями значений В, не замещены или замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей ; указанная 1,4-фениленовая группа, в соответствии с определениями значений Е, не замещена или замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей ; указанные арильные и гетероарильные группы, в соответствии с определениями значений R6 и , не замещены или замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей ; указанные заместителивыбраны из группы, состоящей из атомов галогена, алкильных групп,имеющих от 1 до 4 атомов углерода, алкоксигрупп, имеющих от 1 до 4 атомов углерода, галогеналкильных групп, имеющих от 1 до 4 атомов углерода, галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода, цианогрупп, алкинильных групп, имеющих от 2 до 6 атомов углерода, алканоильных групп, имеющих от 1 до 5 атомов углерода, циклоалкильных групп, имеющих от 3 до 7 атомов в кольце, гетероарильных групп, арильных групп, аралкоксигрупп, имеющих от 7 до 10 атомов углерода, арилкарбонильных групп, или двух соседних -групп, которые, взятые вместе, могут образовывать алкиленовую или алкениленовую цепь, имеющую 3 или 4 атома углерода, аминокарбонильных групп, алкенильных групп,имеющих от 2 до 5 атомов углерода, алкилтиогрупп, имеющих от 1 до 4 атомов углерода, аминосульфинильных групп, аминосульфонильных групп, гидроксигрупп, гидроксиалкильных групп, имеющих от 1 до 4 атомов углерода, нитрогрупп, аминогрупп, карбоксигрупп, алкоксикарбонильных групп, имеющих от 2 до 5 атомов углерода, алкоксиалкильных групп, имеющих от 1 до 4 атомов углерода, алкилсульфонильных групп, имеющих от 1 до 4 атомов углерода, алканоиламиногрупп, имеющих от 1 до 4 атомов углерода, алканоил(алкил)аминогрупп, имеющих от 1 до 6 атомов углерода, алканоиламиноалкильных групп, имеющих от 1 до 6 атомов углерода как в алканоильной части, так и в алкильной части, алканоил(алкил)аминоалкильных групп, имеющих от 1-6 атомов углерода как в алканоильной части, так и в каждой алкильной части, алкилсульфониламиногрупп, имеющих от 1 до 4 атомов углерода, моно- или диалкиламинокарбонильных групп, имеющих от 1 до 6 атомов углерода, моно- или диалкиламиносульфинильных групп, имеющих от 1 до 6 атомов углерода, моно- или диалкиламиносульфонильных групп,имеющих от 1 до 6 атомов углерода, аминоалкильных групп, имеющих от 1 до 4 атомов углерода, моноили диалкиламиногрупп, имеющих от 1 до 6 атомов углерода, моно- или диалкиламиноалкильных групп,имеющих от 1 до 6 атомов углерода в каждой алкильной части, аралкильных групп, имеющих от 7 до 10 атомов углерода, гетероарилалкильных групп, имеющих от 1 до 4 атомов углерода в алкильной части,гетероарилалкоксигрупп, имеющих от 1 до 4 атомов углерода в алкокси части и алкилсульфониламиногрупп, имеющих от 1 до 4 атомов углерода; указанные заместителивыбраны из группы, состоящей из атомов галогена, алкильных групп,имеющих от 1 до 4 атомов углерода, алкоксигрупп, имеющих от 1 до 4 атомов углерода, галогеналкильных групп, имеющих от 1 до 4 атомов углерода, галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода и цианогрупп;W представляет собой фармацевтически приемлемую сложноэфирную группу пролекарства,при условии, что R1 и R2 одновременно не являются атомом водорода; или к его фармацевтически приемлемой соли. Арил- или гетероариламидные соединения согласно изобретению оказывают антагонистическое действие по отношению к простагландину, а поэтому они могут быть использованы в терапии, а в частности, для лечения расстройства или состояния, выбранного из группы, состоящей из боли, нервнопатической боли, висцеральной боли, воспалительной боли, ноцицептивной боли, хронической боли, острой боли, жара или воспаления, связанного с ревматической атакой, гриппом или другими вирусными инфекциями, насморка, боли в пояснице и в области шеи, боли в костях, послеродовой боли, дисменореи,головной боли, мигрени, зубной боли, вывихов и растяжений, миозита, невралгии, фибромиалгии, синовита, артрита, включая ревматоидный артрит, дегенеративных заболеваний суставов (остеоартрита), подагры и анкилозирующего спондилита, бурсита, ожогов, включая поражения, вызванные радиацией и едкими химикатами, солнечных ожогов, боли после хирургических операций и лечения зубов, переломов кости, иммунных и аутоиммунных заболеваний; неопластической трансформации клеток или роста метастатических опухолей; диабетической ретинопатии, ангиогенеза опухоли; индуцированного простаноидами сокращения гладких мышц, связанного с дисменореей, преждевременными родами, аллергическим ринитом, атопическим дерматитом, астмой или расстройствами, опосредуемыми эозинофилами,гипериммуноглобулинемией, заболеванием Каслмана, миеломой; болезни Альцгеймера, нарушений сна,эндокринного расстройства; глаукомы; потери костной массы; остеопороза; активизации формирования-2 009201 костной ткани; болезни Педжета: цитопротекции при пептических язвах, гастрита, регионального энтерита, язвенного колита, дивертикулита или других поражений желудочно-кишечного тракта; желудочнокишечных (ЖК) кровотечений; состояний пациентов, проходящих химиотерапию; нарушений свертывания крови, выбранных из гипопротромбинемии, гемофилии и других нарушений кровообращения; заболеваний почек; тромбоза; окклюзионного сосудистого заболевания; состояния перед хирургической операцией; состояний, вызванных лечением антикоагулянтами; рефлекторной боли; боли в результате ампутации, кожных болезней (например, экземы, псориаза); глазных болезней, таких как глаукома, ретинит,ретинопатия, увеит и острое повреждение глазной ткани (например, конъюнктивит); болезней легких(например, бронхита, эмфиземы, аллергического ринита, респираторного дистресс-синдрома, болезней любителей голубей, легочных болезней фермеров, ХОБД); желудочно-кишечных расстройств (например,афтозной язвы, аллергического гастрита, болезни Крона, оспоподобного гастрита, язвенного колита, заболеваний брюшной полости, регионарного илеита, синдрома раздражнной толстой кишки, воспалительного заболевания кишечника, желудочно-кишечного рефлюкса); трансплантации органов; других состояний с воспалительной составляющей, таких как сосудистое заболевание, мигрень, нодозный полиартериит, тиреоидит, апластическая анемия, болезнь Ходжкина, склеродома, тяжелая миастения, рассеянный склероз, саркоидоз, нефротический синдром, синдром Бечета, полимиозит, гингивит, ишемия миокарда, пирексия, системная красная волчанка, тендонит, бурсит и синдром Сьегрена; патологической функции тромбоцитов (например, окклюзивных сосудистых заболеваний); диуреза; импотенции или нарушения эрекции; заболевания костей, характеризующегося патологическим метаболизмом или резорбцией костей, такого, как остеопороз; гиперкальцемии, гиперпаратиреоза, костных заболеваний Педжета,остеолиза, гиперкальцемии злокачественной опухоли с метастазами или без метастазов в кость, ревматоидного артрита, периодонтита, остеоартрита, боли в костях, нарушения остеогенеза, кахексии при раке,калькулеза, камнеобразования (в частности, мочекаменной болезни), солидной раковой опухоли, подагры и анкилозирующего спондилита, тендинита и бурсита; резорбции кости, гемодинамических побочных эффектов ингибиторов НСПВС и СОХ-2, сердечно-сосудистых заболеваний, гипертензии или ишемии миокарда; функциональной или органической венозной недостаточности; нарушений, связанных с варикозной терапией; геморроя; и шоковых состояний, связанных с сильным падением артериального давления (например, септического шока); нейродегенеративных заболеваний и нейродегенерации таких, как деменция, а в частности дегенеративная деменция (включая сенильную деменцию, болезнь Альцгеймера,болезнь Пика, хорею Гентингтона, болезнь Паркинсона и болезнь Крейтцфельда-Якоба, АБС, заболевание моторных нейронов); сосудистой деменции (включая деменцию, вызванную множественными инфарктами); а также деменции, связанной с поражениями внутричерепного пространства; травм; инфекций и ассоциированных с ними состояний (включая ВИЧ-инфекцию); метаболизма; состояний, вызываемых токсинами; аноксии и авитаминоза; и легкого нарушения познавательной способности, связанного со старением, а в частности, возрастного нарушения памяти; нейропротекции, нейродегенерации после инсульта, остановки сердца, шунтирования легких, травматического повреждения головного мозга, повреждения спинного мозга; шума в ушах, осложнений диабета типа 1 (например, диабетической микроангиопатии, диабетической нефропатии, дегенерации желтого пятна, глаукомы), нефротического синдрома, апластической анемии, увеита, болезни Кавасаки и саркоидозов; дисфункции почек (например,нефрита, а в частности, мезангиального пролиферативного гломерулонефрита, нефротического синдрома), дисфункции печени (гепатита, цирроза), дисфункции желудочно-кишечного тракта (диареи), алкогольного цирроза, амилоидоза, атеросклероза, болезней сердца, склероза, реакций на трансплантацию органов, остеопороза, индуцированного глюкокортикоидами, потери зубов, переломов кости, множественной миеломы, различных отеков, артериальной гипертензии, предменструального синдрома, мочевого конкремента, олигурии, гиперфосфатурии, уртикарной сыпи, дерматита контактного типа, лугового дерматита, поллакиурии, неспособности к обучению, гингивита, периодонтита, повреждения легких, повреждения печени и констипации и т.п. у млекопитающих, а в частности у человека. Соединение формулы (I) может быть также использовано для предотвращения или ослабления зависимости от вещества, вызывающего зависимость, либо для предотвращения или ослабления толерантности или обратимой толерантности к такому веществу. Примерами веществ, вызывающих зависимость,являются опиоиды (например, морфин), депрессанты ЦНС (например, этанол), психостимуляторы (например, кокаин) и никотин. Соединение формулы (I) также обладает диуретической активностью широкого спектра, такой как пониженная калийуретическая активность по отношению к натрийуретическому эффекту, повышенная экскреция фосфора. Соединения согласно изобретению могут быть использованы для общего лечения боли, а в частности воспалительной или невропатической боли. Физиологическая боль является важным защитным механизмом, направленным на предупреждение организма от воздействия потенциально опасных факторов внешней среды. Данная система действует посредством конкретной группы первичных сенсорных нейронов и активируется исключительно вредными раздражителями посредством периферических механизмов передачи сигналов (общий обзор см. Millan 1999 Prog. Neurobio. 57:1-164). Эти сенсорные волокна известны как болевые рецепторы и характеризуются аксонами малого диаметра с малыми скоростями-3 009201 проводимости. Болевые рецепторы преобразуют интенсивность, продолжительность и качество вредного раздражителя в зависимости от их топографически организованной проекции на спинной мозг и локализации данного раздражителя. Болевые рецепторы обнаружены в ноцицептивных нервных волокнах, принадлежащих к двум главным типам, волокнам А-дельта (миелинизированным) и С-волокнам (немиелинизированным). Активность, генерируемая на входе болевого рецептора, передается после сложных процессов преобразования в спинном роге, либо непосредственно или опосредованно путем передачи сигнала из ядра ствола головного мозга в вентробаэальный таламус, а затем в кору головного мозга, где генерируются болевые ощущения. Интенсивная острая боль и хроническая боль могут генерироваться теми же самыми путями, управляемыми патофизиологическими процессами и, по существу, блокировать защитный механизм, а вместо этого индуцировать возникновение изнуряющих симптомов, связанных с широким спектром патологических состояний. Боль является характерной особенностью множества травматических и патологических состояний. При возникновении значительного повреждения ткани тела, вызванного заболеванием или травмой, активирующие свойства болевых рецепторов изменяются. Повышение чувствительности происходит на периферии, в области повреждения и в центре повреждения, где находятся окончания болевых рецепторов. Это приводит к гиперчувствительности в области повреждения и в близлежащей нормальной ткани. При острой боли эти механизмы могут быть полезны - стимулируют процессы репарации, при этом после заживления повреждения гиперчувствительность возвращается к норме. Однако при многих состояниях хронической боли гиперчувствительность присутствует гораздо дольше, чем процесс заживления, и обычно возникает вследствие повреждения нервной системы. Данное повреждение часто приводит к плохой адаптации афферентных волокон (WoolfSalter 2000 Science 288:1765-1768). Клиническая боль присутствует в случае, если симптомы пациента включают дискомфорт и патологическую чувствительность. Все пациенты абсолютно отличаются друг от друга, и у них могут быть различные болевые симптомы. Существует множество типичных подтипов боли: 1) спонтанная боль, которая может быть тупой, острой или колющей; 2) повышенные болевые реакции на вредные раздражители (гипералгезия); 3) боль, вызываемая безвредными раздражителями (аллодиния) (Meyer et al., 1994 Textbook ofPain 13-44). Хотя пациенты с болью в спине, артритной болью, травмой ЦНС или нервнопатической болью могут иметь сходные симптомы, однако, механизмы, лежащие в их основе, различны, а поэтому,необходимы различные стратегии лечения пациентов. Следовательно, в соответствии с различной патофизиологией, боль может быть подразделена на ряд различных типов, включая ноцицептивную, воспалительную, невропатическую боль и т.д. Следует отметить, что некоторые типы боли имеют различную этиологию, и, таким образом, они могут быть классифицированы по более, чем одной области их локализации; так, например, боль в спине и боль при раке включает как ноцицептивные, так и невропатические компоненты. Ноцицептивная боль индуцируется повреждением ткани или интенсивными раздражителями, потенциально вызывающими повреждение. Афферентные пути боли активируются передачей сигнала от раздражителей болевых рецепторов в области повреждения и делают спинной мозг чувствительным на уровне их окончания этих рецепторов. Затем боль передается по спинномозговым путям к мозгу, где происходит ее восприятие (Meyer et al., 1994 Textbook of Pain 13-44). Активация болевых рецепторов стимулирует два типа афферентных нервных волокон. Миелинизированные А-дельта-волокна обладают высокой скоростью проводимости и ответственны за острые и колющие болевые ощущения, в то время как немиелинизированные С-волокна обладают меньшей скоростью проводимости и передают тупую или ноющую боль. Острая ноцицептивная боль, от умеренной до тяжелой, наиболее часто возникает, но не только, при вывихе/растяжении связок, после операции (боль после хирургической операции любого типа), после травмы, при ожогах, инфаркте миокарда, остром панкреатите и при почечной колике. Также ассоциированные с раком синдромы острой боли обычно обусловлены терапевтическими взаимодействиями, такими как токсичность при химиотерапии, иммунотерапии, гормональной терапии и лучевой терапии. Острая ноцицептивная боль, от умеренной до тяжелой, наиболее часто возникает, но не только при раке, и может представлять собой боль, связанную с опухолью (например, боль в костях, головная боль и лицевая боль, боль во внутренних органах) или боль, связанную с терапией рака (например, постхимиотерапевтические синдромы, синдромы хронической послеоперационной боли, синдромы, возникающие после лучевой терапии), боли в спине, которые могут быть вызваны грыжей, разрывом межпозвоночных дисков или аномалиями фасеточных суставов поясницы, крестцово-подвздошных суставов,параспинальных мышц или задней продольной связки. Невропатическую боль определяют как боль, инициированную или вызванную первичным поражением или дисфункцией нервной системы (определение, данное IASP). Повреждение нерва может быть вызвано травмой и заболеванием, а поэтому, термин "невропатическая боль" охватывает множество нарушений разнообразной этиологии. Они включают, но не ограничивается ими, диабетическую невропатию, постгерпетическую невралгию, боль в спине, невропатию при раке, невропатию при ВИЧ, фантомную боль конечности, синдром канала запястья, хронический алкоголизм, гипотиреоз, невралгию тройничного нерва, уремию или авитоминозы. Невропатическая боль является патологической, поскольку она не играет защитной роли. Она часто появляется гораздо позже исчезновения вызывающей ее причи-4 009201 ны и обычно длится в течение многих лет, значительно снижая качество жизни пациентов (Woolf andMannion 1999 Lancet 353: 1959-1964). Симптомы невропатической боли трудно поддаются лечению, потому, что они часто бывают разнообразными даже у пациентов с одним тем же заболеванием (WoolfDecosterd 1999 Pain Supp. 6: S141-S147; Woolf and Mannion 1999 Lancet 353: 1959-1964). Эти боли включают спонтанную боль, которая может быть непрерывной или пароксизмальной и атипичной болью, такой, как гипералгезия (повышенная чувствительность к вредному раздражителю и аллодиния (чувствительность обычно к безвредному раздражителю). Воспалительный процесс представляет собой сложный ряд биохимических и клеточных процессов,активируемых в ответ на повреждение ткани или наличие чужеродных веществ, которые приводят к опуханию и боли (Levine et al., 1994 Taiwo: Textbook of Pain 45-56). Артритная боль составляет большую часть случаев воспалительной боли у населения. Ревматоидное заболевание является одним из самых распространенных хронических воспалительных состояний в развитых странах, а ревматоидный артрит является обычной причиной нетрудоспособности. Точная этиология РА не известна, однако, в настоящее время существует предположение, что важную роль в его патогенезе могут играть генетические и микробиологические факторы (GrennanJayson 1994 Textbook of Pain 397-407). По оценкам специалистов,почти 16 миллионов американцев страдают симптоматическим остеоартритом (ОА) или дегенеративным заболеванием суставов, и большинство из них имеют возраст более, чем 60 лет, при этом, ожидается, что с увеличением возраста населения, число заболевших может достигнуть 40 миллионов, что создаст огромную проблему для здравоохранения. (HougeMersfelder 2002 Ann Pharmacother. 36: 679-686;McCarthy et al., 1994 Textbook of Pain 387-395). Большинство пациентов с ОА обращаются к врачу с жалобами на боли. Артрит оказывает значительное влияние на психосоциальную и физическую функцию и,как известно, является главной причиной нетрудоспособности в будущем. Другие типы воспалительной боли включают, но не ограничивается ими, воспалительные заболевания кишечника (ВЗК). Другими типами боли являются, но не ограничиваются ими: мышечно-скелетные расстройства, включая, без ограничений, миалгию, фибромиалгию, спондилит,серонегативные (неревматоидные) артропатии, несуставный ревматизм, дистрофинопатию, гликогенолиз, полимиозит, пиомиозит; центральная боль или "таламическая боль", определяемая как боль, вызванная поражением или расстройством нервной системы, включая, без ограничений, центральную боль после инсульта, рассеянный склероз, повреждение спинного мозга, болезнь Паркинсона и эпилепсию; сердечная и сосудистая боль, включая, без ограничений, боль при стенокардии, при инфаркте миокарда, стенозе митрального клапана, перикардите, феномене Рейно, склередеме, ишемии скелетной мышцы; висцеральная боль и боль при желудочно-кишечных расстройствах. Внутренние органы охватывают органы брюшной полости. Данные органы включают половые органы, селезенку и часть пищеварительной системы. Боль, возникающая во внутренних органах, может быть подразделена на висцеральную боль пищеварительного тракта и висцеральную боль, не связанную с пищеварительным трактом. Наиболее распространенными желудочно-кишечными (ЖК) расстройствами являются функциональные расстройства кишечника (ФРК) и воспалительные заболевания кишечника (ВЗК). Такие желудочнокишечные расстройства включают патологические состояния широкого ряда, которые в настоящее время лишь частично поддаются лечению, включая - для ФРК, гастроэзофагальный рефлюкс, диспепсию, синдром раздраженного кишечника (СРК) и функциональный синдром боли в брюшной полости (FAPS), и для ВЗК, болезнь Крона, илеит и язвенный колит, каждый из которых обычно вызывает висцеральную боль. Другими типами висцеральной боли являются боли, связанные с дисменореей, боли в области таза,боли при цистите и панкреатите; головная боль, включая, без ограничений, мигрень, мигрень с аурой, мигрень без ауры, гистаминовую головную боль, головную боль напряжения; боль в полости рта и лицевая боль, включая, без ограничений, зубную боль, боль в области мышечно-лицевого височно-нижнечелюстного сустава. Настоящее изобретение относится к способу лечения опосредованного простагландином патологического состояния у млекопитающего, предусматривающему введение указанному индивидууму терапевтически эффективного количества соединенияформулы (I) или его соли. Кроме того, настоящее изобретение также относится к композиции, которая содержит терапевтически эффективное количество арил- или гетероариламидного соединения формулы (I) или его фармацевтически приемлемой соли в комбинации с фармацевтически приемлемым носителем. Указанная композиция, предпочтительно, предназначена для лечения заболевания, определенного выше, а в частности боли, воспаления, остеоартрита или ревматоидного артрита. Кроме того, настоящее изобретение также относится к соединению формулы (I) или к его фармацевтически приемлемой соли в качестве лекарственного средства. Кроме того, настоящее изобретение относится к способу лечения определенных выше патологических состояний, включая боль, воспаление, остеоартрит или ревматоидный артрит, где указанный способ предусматривает введение указанному индивидууму терапевтически эффективного количества соедине-5 009201 ния формулы (I) или его соли. Кроме того, настоящее изобретение относится к способу лечения определенных выше патологических состояний, а в частности боли, воспаления, остеоартрита или ревматоидного артрита, у млекопитающего, предпочтительно человека, где указанный способ включает введение указанному индивидууму терапевтически эффективного количества соединения формулы (I) или его соли. Кроме того, настоящее изобретение относится к способу применения терапевтически эффективного количества соединения формулы (I) или его соли в целях получения лекарственного средства для лечения определенных выше патологических состояний, а в частности боли, воспаления, остеоартрита или ревматоидного артрита. Кроме того, настоящее изобретение относится к комбинации, содержащей соединение формулы (I) или его соль и один или несколько других фармакологически активных ингредиентов, например, СОХ-2 селективное, СОХ-1-селективное или неселективное НСПВС (нестероидное противовоспалительное лекарственное средство), опиоид, противосудорожное средство, антидепрессант, местный анестетик, противоревматоидное лекарственное средство, влияющее на течение заболевания, или стероид. Кроме того, настоящее изобретение относится к соединению следующей формулы (II), являющемуся пролекарством или промежуточным реакционным продуктом: где А представляет собой фенильную группу или пиридильную группу; В представляет собой арильную группу или гетероарильную группу; Е представляет собой 1,4-фениленовую группу;R1 и R2 независимо представляют собой атом водорода, атом галогена, алкильную группу, имеющую от 1 до 4 атомов углерода, алкоксигруппу, имеющую от 1 до 4 атомов углерода, галогеналкильную группу, имеющую от 1 до 4 атомов углерода, галогеналкоксигруппу, имеющую от 1 до 4 атомов углерода, цианогруппу или аминокарбонильную группу;R3 и R4 независимо представляют собой атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода; или группы R3 и R4, взятые вместе, могут образовывать алкиленовую цепь, имеющую от 2 до 6 атомов углерода;Ra представляет собой алкильную группу, имеющую от 1 до 6 атомов углерода, или аралкильную группу, имеющую от 7 до 12 атомов углерода,X представляет собой метиленовую группу, атом кислорода или атом серы; указанные арильные группы содержат от 6 до 10 атомов углерода; указанные гетероарильные группы представляют собой 5-10-членные ароматические гетероциклические группы, имеющие от 1 до 3 гетероатомов, выбранных из группы, состоящей из атомов серы, кислорода и азота; указанные арильные и гетероарильные группы, рассмотренные в определениях В, не замещены или замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей ; указанная 1,4-фениленовая группа, рассмотренная в определении Е, не замещена или замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей ; указанные арильные и гетероарильные группы, рассмотренные в определениях R6 и , не замещены или замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей; указанные заместителивыбраны из группы, состоящей из атомов галогена, алкильных групп,имеющих от 1 до 4 атомов углерода, алкоксигрупп, имеющих от 1 до 4 атомов углерода, галогеналкильных групп, имеющих от 1 до 4 атомов углерода, галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода, цианогрупп, алкинильных групп, имеющих от 2 до 6 атомов углерода, алканоильных групп, имеющих от 1 до 5 атомов углерода, циклоалкильных групп, имеющих от 3 до 7 атомов в кольце, гетероарильных групп, арильных групп, аралкоксигрупп, имеющих от 7 до 10 атомов углерода, арилкарбонильных групп, двух соседних -групп, которые, взятые вместе, могут образовывать алкиленовую или алкениленовую цепь, имеющую 3 или 4 атома углерода, аминокарбонильных групп, алкенильных групп,имеющих от 2 до 5 атомов углерода, алкилтиогрупп, имеющих от 1 до 4 атомов углерода, аминосульфинильных групп, аминосульфонильных групп, гидроксигрупп, гидроксиалкильных групп, имеющих от 1 до 4 атомов углерода, нитрогрупп, аминогрупп, карбоксигрупп, алкоксикарбонильных групп, имеющих от 2 до 5 атомов углерода, алкоксиалкильных групп, имеющих от 1 до 4 атомов углерода, алкилсульфонильных групп, имеющих от 1 до 4 атомов углерода, алканоиламиногрупп, имеющих от 1 до 4 атомов углерода, алканоил(алкил)аминогрупп, имеющих от 1 до 6 атомов углерода, алканоиламиноалкильных-6 009201 групп, имеющих от 1 до 6 атомов углерода как в алканоильной части, так и в алкильной части, алканоил(алкил)аминоалкильных групп, имеющих от 1-6 атомов углерода как в алканоильной части, так и в каждой алкильной части, алкилсульфониламиногрупп, имеющих от 1 до 4 атомов углерода, моно- или диалкиламинокарбонильных групп, имеющих от 1 до 6 атомов углерода, моно- или диалкиламиносульфинильных групп, имеющих от 1 до 6 атомов углерода, моно- или диалкиламиносульфонильных групп,имеющих от 1 до 6 атомов углерода, аминоалкильных групп, имеющих от 1 до 4 атомов углерода, моноили диалкиламиногрупп, имеющих от 1 до 6 атомов углерода, моно- или диалкиламиноалкильных групп,имеющих от 1 до 6 атомов углерода в каждой алкильной части, аралкильных групп, имеющих от 7 до 10 атомов углерода, гетероарилалкильных групп, имеющих от 1 до 4 атомов углерода в алкильной части,гетероарилалкоксигрупп, содержащий от 1 до 4 атомов углерода в алкокси части и алкилсульфониламиногрупп, имеющих от 1 до 4 атомов углерода; указанные заместителивыбраны из группы, состоящей из атомов галогена, алкильных групп,имеющих от 1 до 4 атомов углерода, алкоксигрупп, имеющих от 1 до 4 атомов углерода, галогеналкильных групп, имеющих от 1 до 4 атомов углерода, галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода и цианогрупп,при условии, что R1 и R2 одновременно не являются атомом водорода; или к его фармацевтически приемлемой соли. Кроме того, настоящее изобретение относится к промежуточному соединению следующей формулы (III): где А представляет собой фенильную группу или пиридильную группу; Е представляет собой 1,4-фениленовую группу;R1 и R2 независимо представляют собой атом водорода, атом галогена, алкильную группу, имеющую от 1 до 4 атомов углерода, алкоксигруппу, имеющую от 1 до 4 атомов углерода, галогеналкильную группу, имеющую от 1 до 4 атомов углерода, галогеналкоксигруппу, имеющую от 1 до 4 атомов углерода, цианогруппу или аминокарбонильную группу;R3 и R4 независимо представляют собой атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода; или группы R3 и R4, взятые вместе, могут образовывать алкиленовую цепь, имеющую от 2 до 6 атомов углерода;Ra представляет собой алкильные группы, имеющие от 1 до 6 атомов углерода, или аралкильную группу, имеющую от 7 до 12 атомов углерода,L1 представляет собой атом галогена, алкансульфонилоксигруппу, имеющую от 1 до 4 атомов углерода, арилсульфонилоксигруппу, необязательно замещенную алкильной группой, имеющей от 1 до 4 атомов углерода, галогеналкансульфонилоксигруппу, имеющую от 1 до 4 атомов углерода, или группу бороновой кислоты (В(ОН)2); указанная 1,4-фениленовая группа, рассмотренная в определении Е, не замещена или замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей ; указанные заместителивыбраны из группы, состоящей из атомов галогена, алкильных групп,имеющих от 1 до 4 атомов углерода, алкоксигрупп, имеющих от 1 до 4 атомов углерода, галогеналкильных групп, имеющих от 1 до 4 атомов углерода,галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода и цианогрупп,при условии, что R1 и R2 одновременно не являются атомом водорода; или к его фармацевтически приемлемой соли. Подробное описание изобретения Используемый здесь термин "галоген" означает фтор, хлор, бром и иод, а предпочтительно фтор или хлор. Используемый здесь термин "алкил" означает насыщенный радикал с прямой или разветвленной цепью, включая, без ограничений, метил, этил, н-пропил, изопропил, н-бутил, изобутил, вторичный бутил, третичный бутил. Используемый здесь термин "алкилен" означает насыщенный углеводород (с прямой или разветвленной цепью), в котором атом водорода удален у каждого из концевых атомов углерода, такой как метилен, этилен, метилэтилен, пропилен, бутилен, пентилен, гексилен и т.п. Используемый здесь термин "алкенилен" означает углеводородный радикал, содержащий по меньшей мере одну двойную связь (с прямой или разветвленной цепью), где атом водорода удален у каждого из концевых атомов углерода, такой как этенилен, пропенилен, и т.п. Используемый здесь термин "алкенил" означает углеводородный радикал, содержащий по меньшей-7 009201 мере одну двойную связь, включая, без ограничений, этенил, пропенил, 1-бутенил, 2-бутенил и т.п. Используемый здесь термин "алкинил" означает углеводородный радикал, содержащий по меньшей мере одну тройную связь, включая, без ограничений, этинил, пропинил, 1-бутинил, 2-бутинил и т.п. Используемый здесь термин "алкокси" означает алкил-О-, включая, без ограничений, метокси,этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси. Используемый здесь термин "циклоалкил" означает насыщенное кольцо карбоциклического радикала, имеющего 3-8 атомов углерода, включая, без ограничений, циклопропил, циклобутил, циклогексил,циклогептил, циклооктил, циклононил, циклодецил и т.п. Используемый здесь термин "алканоил" означает группу, содержащую карбонил, такую, как R'-C(O)-,где R' представляет собой собой Н, C1-6 алкил, фенил или С 3-6 циклоалкил, включая, без ограничений, формил, ацетил, этил-С(О)-, н-пропил-С(О)-, изопропил-С(О)-, н-бутил-С(О)-, изобутил-С(О)-, вторичный бутил-С(О)-, третичный бутил-С(О)-, циклопропил-С(О)-, циклобутил-С(О)-, циклопентил-С(О)-, циклогексил-С(О)- и т.п. Используемый здесь термин "арил" означает моноциклическое или бициклическое ароматическое карбоциклическое кольцо из 6-10 атомов углерода; или бициклическое частично насыщенное карбоциклическое кольцо из 6-10 атомов углерода, включая, без ограничений, фенил, нафтил, инданил, инденил,тетралинил, а предпочтительно фенил, инданил и нафтил. Используемый здесь термин "галогеналкил" означает алкильный радикал, замещенный атомами галогена, как определено выше, включая, без ограничений, фторметильную, дифторметильную, трифторметильную, 2-фторэтильную, 2,2-дифторэтильную, 2,2,2-трифторэтильную, 2,2,2-трихлорэтильную, 3 фторпропильную, 4-фторбутильную, хлорметильную, трихлорметильную, иодметильную и бромметильную группы и т.п. Используемый здесь термин "галогеналкокси" означает галогеналкил-О-, включая, без ограничений,фторметокси-, дифторметокси-, трифторметокси-, 2-фторэтокси-, 2,2-дифторэтокси-, 2,2,2-трифторэтокси-,2,2,2-трихлорэтокси-, 3-фторпропокси-, 4-фторбутокси-, хлорметокси-, трихлорметокси-, иодметокси- и бромметоксигруппы и т.п. Термин "гетероарил" означает 5-10-членное ароматическое или частично насыщенное гетеро моноили бициклическое кольцо, состоящее из 1-3 гетероатомов, независимо выбранных из группы, состоящей из атомов серы, атомов кислорода и атомов азота, включая, без ограничений, пиразолил, фурил, тиенил,оксазолил, тетразолил, тиазолил, имидазолил, тиадиазолил, пиридил, пиримидинил, пирролил, тиофенил,пиразинил, пиридазинил, изооксазолил, изотиазолил, триазолил, фуразанил, индолинил, бензотиенил,бензофуранил, бензоимидазолинил, хинолил, пиперидил, 4-пиперидонил, пирролидинил, 2-пирролидонил, тетрагидрофуранил, тетрагидрохинолил, тетрагидроизохинолил, декагидрохинолил или октагидроизохинолил, пиперазинил и т.п. Используемый здесь термин "аралкил" означает алкильный радикал, замещенный арильной группой, определенной выше, например бензил. Используемый здесь термин "аралкокси" означает аралкил-О-, где термин аралкил определен выше,включая, без ограничений, бензилокси. Если соединения формулы (I) содержат гидрокси, то они могут образовать сложные эфиры. Примеры таких сложных эфиров включают сложные эфиры с гидроксигруппой и сложные эфиры с карбоксигруппой. Остаток сложного эфира может быть обычной защитной группой или защитной группой, которая может быть отщеплена in vivo биологическим методом, таким как гидролиз. Термин "обычная защитная группа" означает защитную группу, которая может быть отщеплена химическим методом, таким как гидрогенолиз, гидролиз, электролиз или фотолиз."W" означает сложноэфирную группу пролекарства, которая может быть отщеплена in vivo биологическим методом, таким как гидролиз, и образует свободную кислоту или соль этой кислоты и соединения формулы (I). Является ли соединение таким производным или нет, можно определить после его введения посредством внутривенной инъекции экспериментальному животному, такому как крыса или мышь, а затем путем исследования физиологической жидкости животного можно определить, присутствует ли в ней данное соединение или его фармацевтически приемлемая соль. Предпочтительные примеры сложного эфира карбоксильной группы или гидроксигруппы включают: низшие алифатические ацильные группы, например алканоильные группы, такие как формильная,ацетильная, пропионильная, бутирильная, изобутирильная, пентаноильная, пивалоильная, валерильная,изовалерильная, октаноильная, нонаноильная, деканоильная, 3-метилнонаноильная, 8-метилнонаноильная, 3-этилоктаноильная, 3,7-диметилоктаноильная, ундеканоильная, додеканоильная, тридеканоильная, тетрадеканоильная, пентадеканоильная, гексадеканоильная, 1-метилпентадеканоильная, 14-метилпентадеканоильная, 13,13-диметилтетрадеканоильная, гептадеканоильная, 15-метилгексадеканоильная,октадеканоильная, 1-метилгептадеканоильная, нонадеканоильная, эйкозаноильная и генейкозаноильная группы; галогенированные алкилкарбонильные группы, такие как хлорацетильная, дихлорацетильная,трихлорацетильная, и трифторацетильная группы; алкоксиалкилкарбонильные группы, такие как метоксиацетильная группа; и ненасыщенные алкилкарбонильные группы, такие как акрилоильная, пропиолоильная, метакрилоильная, кротоноильная, изокротоноильная и (Е)-2-метил-2-бутеноильная группы; а-8 009201 более предпочтительно, низшие алифатические ацильные группы, имеющие от 1 до 6 атомов углерода; ароматические ацильные группы, например, арилкарбонильные группы, такие как бензоильная, нафтоильная и -нафтоильная группы; галогенированные арилкарбонильные группы, такие как 2 бромбензоильная и 4-хлорбензоиольная группы; низшие алкилированные арилкарбонильные группы,такие как 2,4,6-триметилбензоильная и 4-толуоильная группы; низшие алкоксилированные арилкарбонильные группы, такие, как 4-анизоильная группа; нитрированные арилкарбонильные группы, такие как 4-нитробензоильная и 2-нитробензоильная группы; низшие алкоксикарбонилированные арилкарбонильные группы, такие как 2-(метоксикарбонил)бензоильная группа; арилированные арилкарбонильные группы, такие как 4-фенилбензоильная группа; алкоксикарбонильные группы, например низшие алкоксикарбонильные группы, такие как метоксикарбонильная, этоксикарбонильная, пропоксикарбонильная,бутоксикарбонильная, втор-бутоксикарбонильная, трет-бутоксикарбонильная и изобутоксикарбонильная группы; и галоген- или три(низший алкил)силилзамещенные низшие алкоксикарбонильные группы, такие как 2,2,2-трихлорэтоксикарбонильная и 2-триметилсилилэтоксикарбонильная группы; тетрагидропиранильная или тетрагидротиопиранильная группы, такие как, тетрагидропиран-2-ильная, 3-бромтетрагидропиран-2-ильная, 4-метокситетрагидропиран-4-ильная, тетрагидротиопиран-2-ильная и 4 метокситетрагидротиопиран-4-ильная группы; тетрагидрофуранильная или тетрагидротиофуранильная группы, такие как тетрагидрофуран-2-ильная и тетрагидротиофуран-2-ильная группы; силильные группы, например, три(низший алкил)силильные группы, такие как триметилсилильная, триэтилсилильная,изопропилдиметилсилильная, трет-бутилдиметилсилильная, метилдиизопропилсилильная, метилди-третбутилсилильная и триизопропилсилильная группы; и три(низший алкил)силильные группы, замещенные 1 или 2 арильными группами, такие как дифенилметилсилильная, дифенилбутилсилильная, дифенилизопропилсилильная и фенилдиизопропилсилильная группы; алкоксиметильные группы, например низшие алкоксиметильные группы, такие как метоксиметильная, 1,1-диметил-1-метоксиметильная, этоксиметильная, пропоксиметильная, изопропоксиметильная, бутоксиметильная и трет-бутоксиметильная группы; замешенные низшим алкокси низшие алкоксиметильные группы, такие как 2-метоксиэтоксиметильная группа; и галоген(низший алкокси)метильные группы, такие как 2,2,2-трихлорэтоксиметильная и бис(2-хлорэтокси)метильная группы; замещенные этильные группы, например, низшие алкоксилированные этильные группы, такие как 1-этоксиэтильная и 1-(изопропокси)этильная группы; и галогенированные этильные группы, такие как 2,2,2-трихлорэтильная группа; аралкильные группы, например, низшие алкильные группы, замещенные 1-3 арильными группами, такие как бензильная, нафтилметильная, -нафтилметильная, дифенилметильная, трифенилметильная, -нафтилдифенилметильная и 9-антрилметильная группы; и низшие алкильные группы, замещенные 1-3 замещенными арильными группами, где одна или несколько арильных групп замещены одним или несколькими низшими алкильными, низшими алкокси-, нитро-, галогеновыми или циано-3 аместителями, такие как 4 метилбензильная, 2,4,6-триметилбензильная, 3,4,5-триметилбензильная, 4-метоксибензильная, 4-метоксифенилдифенилметильная, 2-нитробензильная, 4-нитробензильная, 4-хлорбензильная, 4-бромбензильная и 4-цианобензильная группы; алкенилоксикарбонильные группы, такие как винилоксикарбонильная и арилоксикарбонильная группы; и аралкилоксикарбонильные группы, в которых арильное кольцо может быть замещено 1 или 2 низшими алкокси- или нитрогруппами, такие как бензилоксикарбонильная, 4-метоксибензилоксикарбонильная, 3,4-диметоксибензилоксикарбонильная, 2-нитробензилоксикарбонильная и 4-нитробензилоксикарбонильная группы. Используемый здесь термин терапия означает радикальную, профилактическую или паллиативную терапию, то есть терапию, приводящую к ремиссии, ослаблению и к подавлению прогрессирования или предупреждению возникновения рассматриваемого расстройства или состояния или одного или более симптомов такого расстройства или состояния. Используемый здесь термин "лечение" означает курс терапии, где термин "терапия" определен непосредственно выше. Предпочтительным соединением формулы (I) согласно изобретению является соединение, в котором Е представляет собой незамещенную 1,4-фениленовую группу. Другим предпочтительным соединением формулы (I) согласно изобретению является соединение, в котором Е представляет собой 1,4-фениленовую группу, замещенную по меньшей мере одним заместителем, выбранным из группы, состоящей из атомов галогена (например, фтора, хлора) или алкильных групп, имеющих от 1 до 4 атомов углерода (например, метила). Предпочтительным соединением формулы (I) согласно изобретению является соединение, в котором В представляет собой арильную или гетероарильную группу, такую как фенил, нафтил, пиридил,хинолил или изохинолил. В предпочтительно не замещен или замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из заместителей , где указанные заместителивыбраны из группы, состоящей из атомов галогена (например, фтора, хлора), алкильных групп, имеющих от 1 до 4 атомов углерода (например, метила, этила), алкоксигрупп, имеющих от 1 до 4 атомов углерода (например, метокси) , галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода (например, трифторметокси),цианогрупп, алкинильных групп, имеющих от 2 до 6 атомов углерода (например, этинила), алканоильных групп, имеющих от 1 до 5 атомов углерода (например, ацетила), циклоалкильных групп, имеющих-9 009201 от 3 до 7 атомов на кольце (например, циклопентила), гетероарильных групп (например, 2-, 3- или 4 пиридила, 1-метилимидазол-2-ила, тиазол-2-ила, 2-метилтиазол-4-ила), арильных групп (например, фенила), аралкоксигрупп, имеющих от 7 до 10 атомов углерода (например, бензилокси), арилкарбонильных групп (например, бензоила), двух соседних -групп, которые, взятые вместе, необязательно образуют алкиленовую цепь, имеющую 3 атома углерода, алкилтиогрупп, имеющих от 1 до 4 атомов углерода (например, метилтио) и диалкиламиноалкильных групп, имеющих от 1 до 6 атомов углерода в алкильной части; где указанные гетероарильные группы, описанные в определениях , не замещены или замещены алкильными группами, имеющими от 1 до 4 атомов углерода (например, метилом). Более предпочтительно, В представляет собой фенильную группу, необязательно замещенную заместителем, выбранным из группы, состоящей из заместителей , где указанные заместителивыбраны из группы, состоящей из атомов галогена (например, фтора, хлора), алкильных групп, имеющих от 1 до 4 атомов углерода (например, метила, этила), алкоксигрупп, имеющих от 1 до 4 атомов углерода (например, метокси), галогеналкоксигрупп, имеющих от 1 до 4 атомов углерода (например, трифторметокси), цианогрупп, алкинильных групп, имеющих от 2 до 6 атомов углерода (например, этинила), алканоильных групп, имеющих от 1 до 4 атомов углерода (например, ацетила), циклоалкильных групп, имеющих от 3 до 7 атомов на кольце (например, циклопентила), алкилтиогрупп, имеющих от 1 до 4 атомов углерода (например, метилтио), диалкиламиноалкильных групп, имеющих от 1 до 6 атомов углерода в алкильной части, тиазолильных групп, изотиазолильных групп, оксазолильных групп, изоксазолильных групп, имидазолильных групп, пиридильных групп, бензилоксигрупп, фенильных групп или бензоильных групп; где указанные тиазолильные группы, изотиазолильные группы, оксазолильные группы, изоксазолильные группы, имидазолильные группы и пиридильные группы, описанные в определениях заместителей , не замещены или замещены алкильными группами, имеющими от 1 до 4 атомов углерода. Более предпочтительно В представляет собой фенильную группу, необязательно замещенную заместителем, выбранным из группы, состоящей из заместителей ; где указанные заместителивыбирают из группы, состоящей из атомов фтора, атомов хлора, метильных групп, этильных групп, метоксигрупп, трифторметоксигрупп, цианогрупп, этинильных групп, ацетильных групп, циклопентильных групп, метилтиогрупп, диметиламиноэтильных групп, фенильных групп, имидазолильных групп, необязательно замещенных метильными группами, тиазолильных групп, необязательно замещенных метильными группами, пиридильных групп или бензилоксигрупп. Более предпочтительно В представляет собой фенильную группу, замещенную 1 или 2 заместителями, такими как фтор или хлор. Более предпочтительно В представляет собой фенильную группу, замещенную 1 заместителем, таким как фтор или хлор. Наиболее предпочтительно В представляет собой 3-фторфенил. Предпочтительным соединением формулы (I) согласно изобретению является соединение, в котором X представляет собой метиленовую группу или атом кислорода. Предпочтительно X представляет собой атом кислорода. Предпочтительным соединением формулы (I) согласно изобретению является соединение, в котором R1 и R2 независимо представляют собой атом водорода, атом фтора, атом хлора, трифторметил, циано или аминокарбонил. Предпочтительным соединением формулы (I) согласно изобретению является соединение, в котором R1 представляет собой атом галогена (например, фтор, хлор), a R2 представляет собой атом водорода. Предпочтительным соединением формулы (I) согласно изобретению является соединение, в котором R3 и R4 независимо представляют собой атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода (например, метил, этил). Более предпочтительно R3 представляет собой алкильную группу, имеющую от 1 до 4 атомов углерода (например, метил, этил), a R4 представляет собой атом водорода. Наиболее предпочтительно, R3 представляет собой метильную группу, a R4 представляет собой атом водорода. Предпочтительным соединением формулы (I) согласно изобретению является соединение, в котором R5 представляет собойa R6 представляет собой арильную группу, необязательно замещенную атомами галогена или представляет собой гетероарильную группу. Более предпочтительно R5 представляет собойa R6 представляет арильную группу, необязательно замещенную атомами галогена. Предпочтительно, R6 представляет собой метил, циклогексил, 2-, 3- или 4-хлорфенил, 3-фторфенил, 3-метилфенил, 3 метоксифенил или 5-метил-2-пиридил. Еще более предпочтительно, R5 представляет собойa R6 представляет собой фенильную группу, необязательно замещенную атомами галогена. Наиболее предпочтительно, R5 представляет собой В определении В, арил предпочтительно представляет собой фенил или нафтил, а гетероарил представляет собой 5-10-членную ароматическую гетероциклическую группу, содержащую либо от 1 до 3 гетероатомов азота, либо 1 или 2 гетероатомов азота и/или 1 гетероатом кислорода или 1 гетероатом серы. Особенно предпочтительными соединениями согласно изобретению являются соединения, в которых каждое значение для каждой группы в формуле (I) выбирают из предпочтительных групп. Еще более предпочтительными соединениями согласно изобретению являются соединения, в которых каждое значение для каждой группы в формуле (I) выбирают из более предпочтительных групп. Предпочтительное отдельное соединение согласно изобретению выбирают из 4-1S)-l-[5-хлор-2-(4-фторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-цианофенокси)пиридин-3-ил] карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-фторфенокси)пиридин-3-ил] карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-хлорфенокси)пиридин-3-ил] карбониламино)этил]бензойной кислоты; 4-1S)-1-[5-хлор-2-(3-фторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-1-[5-хлор-2-(3-метоксифенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(3-хлорфенокси)бензоил]аминоэтил)бензойной кислоты; 4-[(1S)-l-([5-хлор-2-(2,4-дифторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-l-([5-хлор-2-(4-хлор-3-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-l-([5-хлор-2-(2-хлор-4-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2,6-дифторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3,4-дифторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-(1S)-l-[(5-хлор-2-[3-(1,3-тиазол-2-ил)фенокси]пиридин-3-илкарбонил)амино]этилбензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2,3-дифторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2,5-дифторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(4-хлорфенокси)пиридин-3-ил] карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(4-хлор-2-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2-хлор-5-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-метилфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(4-фтор-3-метилфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3,5-дифторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-1S)-l-[5-хлор-2-(2,3-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(2,4-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(3,4-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-хлор-5-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-l-([5-хлор-2-(3-хлор-2-метилфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-1S)-l-[5-хлор-2-(3,5-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(2,5-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-хлор-2-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-l-([5-хлор-2-(3-пиридин-2-илфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(4-пиридин-2-илфенокси)пиридин-3-ил]карбониламино)этил]бензойной ки- 11009201 слоты; 4-[(1S)-1-([5-хлор-2-(4-пиридин-4-илфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-хлор-5-метилфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-1S)-l-[5-хлор-2-(3-метилфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(3-хлор-5-фторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(2,6-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[(5-хлор-2-феноксипиридин-3-ил)карбонил]аминоэтил)бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2,3-диметилфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2,3-дихлорфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-l-([5-хлор-2-(3,4-дихлорфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3,5-дихлорфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; и 4-[(1S)-l-([5-хлор-2-(3-фтор-4-метилфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; или их фармацевтически приемлемой соли. Другое предпочтительное отдельное соединение согласно изобретению выбирают из 4-1S)-l-[5-хлор-2-(4-фторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-цианофенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-хлорфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-1S)-l-[5-хлор-2-(3-фторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(3-хлорфенокси)бензоил]аминоэтил)бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2-хлор-4-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2,6-дифторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-l-([5-хлор-2-(3,4-дифторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2,3-дифторфенокси)пиридин-3-ил] карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2,5-дифторфенокси)пиридин-3-ил] карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(2-хлор-5-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-l-([5-хлор-2-(3-метилфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3,5-дифторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-1S)-l-[5-хлор-2-(2,3-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(3,4-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-хлор-5-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-1S)-l-[5-хлор-2-(3,5-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(2,5-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3-хлор-5-метилфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-1S)-l-[5-хлор-2-(3-метилфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(3-хлор-5-фторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[5-хлор-2-(2,6-дифторфенокси)бензоил]аминоэтил)бензойной кислоты; 4-1S)-l-[(5-хлор-2-феноксипиридин-3-ил)карбонил]аминоэтил)бензойной кислоты; 4-[(1S)-l-([5-хлор-2-(2,3-дихлорфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-1-([5-хлор-2-(3,4-дихлорфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; 4-[(1S)-l-([5-хлор-2-(3,5-дихлорфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; и 4-[(1S)-1-([5-хлор-2-(3-фтор-4-метилфенокси)пиридин-3-ил]карбониламино)этил]бензойной кислоты; или их фармацевтически приемлемой соли. Общий синтез Соединения согласно изобретению могут быть получены различными хорошо известными способами синтеза соединений данного типа, например, как показано на следующих схемах реакций. Если это не оговорено особо, то R1-R6 и А, В, Е и X в нижеследующих схемах реакций и обсуждениях имеют значения, определенные выше. Используемый ниже термин защитная группа, означает защитную гидрокси- или аминогруппу, выбранную из типичных защитных гидрокси- или аминогрупп, описанных в Protective Groups in Organic Synthesis, edited by T. W. Greene et al., (John WileySons, 1991);- 12009201 Получение соединений формулы (I) проиллюстрировано в нижеследующих схемах реакций. Схема 1: в данной схеме проиллюстрировано получение соединений формулы (Ia), где R5 представляет собой -СО 2 Н. Схема 1 В вышеуказанной формуле L1 представляет собой атом галогена, такой как хлор, бром или йод; алкансульфонилоксигруппу, такую как метансульфонильная группа; арилсульфонилоксигруппу,такую как п-толуолсульфонилоксигруппа; галогеналкансульфонилоксигруппу, такую как трифторметансульфонилоксигруппа; или группу бороновой кислоты;Ra представляет собой алкильные группы, имеющие от 1 до 6 атомов углерода или аралкильную группу, имеющую от 7 до 12 атомов углерода; а все другие символы являются такими, как они были определены выше. Стадия 1 А. На данной стадии, соединение формулы 1-3 может быть получено с помощью реакции сочетания соединения сложного эфира формулы 1-1 с циклическим соединением формулы 1-2 в инертном растворителе. Реакция сочетания может быть проведена в отсутствии или в присутствии основания в инертном реакционном растворителе или без растворителя. Предпочтительное основание, например, выбирают из гидроксида, алкоксида, карбоната или гидрида щелочного или щлочно-земельного металла, такого как гидроксид натрия, гидроксид калия, метоксид натрия, этоксид натрия, трет-бутоксид калия, карбонат натрия, карбонат цезия или карбонат калия, 2-трет-бутилимино-2-диэтиламино-1,3-диметилпергидро 1,3,2-диазофосфорина (ВЕМР), трет-бутилимино-три(пирролидино)фосфорана (ВТРР), фторида цезия(CsF), фторида калия, гидрида натрия или гидрида калия или амина, такого как триэтиламин, трибутиламин, диизопропилэтиламин, 2,6-лутидин, пиридин или диметиламинопиридин. Предпочтительными инертными реакционными растворителями являются, например, ацетон, бензол, толуол, ксилол, одихлорбензол, нитробензол, нитрометан, пиридин, дихлорметан, дихлорэтан, тетрагидрофуран, диметилформамид (ДМФ), диметилацетамид (ДМА), диоксан, диметилсульфоксид (ДМСО), ацетонитрил,сульфолан, N-метилпирролидинон (NMP), метилэтилкетон (2-бутанон), тетрагидрофуран (ТГФ), диме- 13009201 токсиэтан (ДМЭ) или их смеси. По существу, температуры реакции составляют в пределах от 0 до 200 С,а предпочтительно в пределах от комнатной температуры до 150 С. По существу, время реакции составляет от 1 мин до одного дня, а предпочтительно от 1 до 10 ч. Если это необходимо, то реакция может быть проведена в присутствии металлического катализатора, такого как медь (например, медная бронза или иодид меди) и никель. Если L1 представляет собой группу бороновой кислоты, то реакция может быть проведена в присутствии подходящего катализатора с образованием соединения формулы 1-3 в соответствии с любой процедурой синтеза, подходящей для получения структурно родственных соединений, известных из литературных источников (например, Lam, P. Y. S. ; Clark, С. С; Saubern, S; Adams, J; Winters, M. P.; Chan,D. M. Т.; Combs, A., Tetpahedron Lett., 1998, 39, 2941-2944., Kiyomori, A.; Marcoux, J.; Buchwald, S. L.,Tetpahedron Lett., 1999, 40, 2657-2660., Lam, P. Y. S. ; Deudon, S.; Averill, K. M. ; Li, R. ; He, M. Y.;DeShong, P.; Clark, С G., J. Am. Chem. Soc, 2000,122, 7600-7601., Collman, J. P.; Zhong, M. , Org. Lett.,2000, 2, 1233-1236.). Предпочтительный катализатор реакции выбирают, например, из теракис(трифенилфосфин)палладия, хлорида бис(трифенилфосфин)палладия(II), меди(0), ацетата меди(I),бромида меди(I) , хлорида меди(I) , иодида меди(I) , оксида меди(I), трифторметансульфоната меди(II),ацетата меди(II), бромида меди(II), хлорида меди(II), иодида меди(II), оксида меди(II) или трифторметансульфоната меди (II). Стадия 1B. В этой стадии, кислотное соединение формулы 1-7 может быть получено путем гидролиза соединения сложного эфира формулы 1-3 в растворителе. Гидролиз может быть проведен в соответствии со стандартными процедурами. В типичной процедуре, гидролиз осуществляют в основных условиях, например, в присутствии гидроксида натрия, гидроксида калия или гидроксида лития. Подходящими растворителями являются, например, спирты, такие как метанол, этанол, пропанол, бутанол, 2-метоксиэтанол и этиленгликоль; простые эфиры, такие как тетрагидрофуран (ТГФ), 1,2-диметоксиэтан (ОМЭ) и 1,4-диоксан; амиды, такие как N,N-диметилформамид (ДМФ) и гексаметилфосфотриамид; и сульфоксиды, такие как диметилсульфоксид (ДМСО). Данная реакция может быть проведена при температуре в пределах от -20 до 100 С, обычно от 20 до 65 С в течение периода времени от 30 мин до 24 ч, а обычно от 60 мин до 10 ч. Гидролиз может быть также осуществлен в кислотных условиях, например, в присутствии галогенводородов, таких как гидрохлорид и гидробромид; сульфоновых кислот, таких как п-толуолсульфоновая кислота и бензолсульфоновая кислота; п-толуолсульфонат пиридия; и карбоновых кислот, таких как уксусная кислота и трифторуксусная кислота. Подходящими растворителями являются, например, спирты,такие как метанол, этанол, пропанол, бутанол, 2-метоксиэтанол и этиленгликоль; эфиры, такие как тетрагидрофуран (ТГФ), 1,2-диметоксиэтан (ДМЭ) и 1,4-диоксан; амиды, такие как N,N-диметилформамид(ДМФ) и гексаметилфосфотриамид; и сульфоксиды, такие как диметилсульфоксид (ДМСО). Данная реакция может быть проведена при температуре в пределах от -20 до 100 С, обычно от 20 С до 65 С в течение периода времени от 30 мин до 24 ч, а обычно от 60 мин до 10 ч. Стадия 1 С. В этой стадии кислотное соединение формулы 1-7 может быть также получено с помощью реакции сочетания кислотного соединения формулы 1-4 с циклическим соединением формулы 1-5. Данная реакция, по существу, представляет собой ту же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий как в стадии 1 А в схеме 1. Стадия 1D. В этой стадии кислотное соединение формулы 1-7 может быть также получено с помощью реакции сочетания кислотного соединения формулы 1-6 с циклическим соединением формулы 1-2. Данная реакция, по существу, представляет собой ту же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий как в стадии 1 А в схеме 1. Стадия 1E. В этой стадии амидное соединение формулы 1-12 может быть получено с помощью реакции сочетания аминового соединения формулы 1-10 с кислотным соединением формулы 1-7 в присутствии или в отсутствии реагента сочетания в инертном растворителе. Если это необходимо, то данная реакция может быть проведена в присутствии или в отсутствии добавки такой, как 1-гидроксибензотриазол или 1-гидроксиазабензотриазол. Реакцию обычно и предпочтительно проводят в присутствии растворителя. При этом, может быть использован растворитель любой природы без каких-либо ограничений, при условии, что он не оказывает неблагоприятного воздействия на реакцию или на используемые реактивы, и что он способен, по меньшей мере, до некоторой степени, растворять реактивы. Примерами подходящих растворителей являются ацетон, нитрометан, ДМФ, сульфолан, ДМСО, NMP, 2-бутанон, ацетонитрил; галогенированные углеводороды, такие как дихлорметан, дихлорэтан, хлороформ; и простые эфиры, такие как тетрагидрофуран и диоксан. Реакция может быть проведена в широких пределах температур, и точная температура реакции не- 14009201 играет решающей роли для осуществления изобретения. Предпочтительная температура реакции зависит от таких факторов, как природа растворителя и используемый исходный материал или реактив. Однако по существу, авторы считают, что подходящей температурой для проведения реакции является температура от -20 до 100 С, а более предпочтительно приблизительно от 0 до 60 С. Время, требуемое для проведения реакции, может также варьироваться в широких пределах, в зависимости от множества факторов, а в частности от температуры реакции и природы используемых реактивов и растворителей. Однако при проведении реакции в предпочтительных условиях, описанных выше, обычно достаточным является период времени от 5 мин до 1 недели, а более предпочтительно от 30 мин до 24 ч. Подходящими реагентами для реакции сочетания, обычно используемыми в пептидном синтезе, являются, например, диимиды (например, дициклогексилкарбодиимид (DCC), растворимый в воде карбодиимид (WSC, 2-этокси-N-этоксикарбонил-1,2-дигидрохинолин, тетрафторборат 2-бром-1-этилпиридиния (ВЕР), хлорид 2-хлор-1,3-диметилимидазолиния, гексафторфосфат бензотриазол-1-илокситрис(диметиламино)фосфония (ВОР), диэтилазодикарбоксилаттрифенилфосфин, диэтилцианофосфат,диэтилфосфорилазид, иодид 2-хлор-1-метилпиридиния, N,N'-карбонилдиимидазол, бензотриазол-1 илдиэтилфосфат, этилхлорформиат или изобутилхлорформиат. Если это необходимо, то реакция может быть проведена в присутствии основания, такого как, N,N-диизопропилэтиламин, N-метилморфолин и триэтиламин. Амидное соединение формулы 1-12 может быть получено через ацилгалогенид, который может быть получен путем проведения реакции с галогенирующими реагентами такими, как оксалилхлорид, оксихлорид фосфора и тионилхлорид. Полученный ацилгалогенид может быть превращен в соответствующее амидное соединение; путем обработки аминового соединения формулы 1-10 в условиях,описанных в этой стадии. Стадия 1F. В этой стадии амидное соединение формулы 1-11 может быть получено с помощью реакции сочетания кислотного соединения формулы 1-6 с аминовым соединением формулы 1-10. Данная реакция по существу представляет собой такую же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 1E в схеме 1. Стадия 1G. В этой стадии амидное соединение формулы 1-12 может быть получено с помощью реакции сочетания соединения формулы 1-11 с циклическим соединением формулы 1-2. Данная реакция по существу представляет собой такую же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 1 А в схеме 1. Стадия 1 Н. В этой стадии амидное соединение формулы 1-9 может быть получено с помощью реакции сочетания кислотного соединения формулы 1-7 с аминовым соединением формулы 1-8. Данная реакция, по существу, представляет собой такую же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 1E в схеме 1. Стадия 1I. В этой стадии амидное соединение формулы 1-12 может быть также получено путем взаимодействия амидного соединения формулы 1-9 с моноксидом углерода и спиртом (например, метанолом или этанолом) в присутствии катализатора и/или основания в инертном растворителе. Примерами подходящих катализаторов являются палладиевые реактивы, такие как ацетат палладия и дибензилацетон-палладий. Примерами подходящих оснований являются N,N-диизоопропилэтиламин,N-метилморфолин и триэтиламин. Если это необходимо, данная реакция может быть проведена в отсутствии или в присутствии добавки, такой как 1,1'-бис(дифенилфосфино)ферроцен, трифенилфосфин или 1,3-бис-(дифенилфосфино)пропан (DPPP). Реакцию обычно и предпочтительно проводят в присутствии растворителя. При этом, может быть использован растворитель любой природы без каких-либо ограничений, при условии, что он не оказывает неблагоприятного воздействия на реакцию или на используемые реактивы, и что он способен, по меньшей мере, до некоторой степени, растворять реактивы. Примерами подходящих растворителей являются ацетон, нитрометан, ДМФ, сульфолан, ДМСО, NMP, 2-бутанон, ацетонитрил; галогенированные углеводороды, такие как дихлорметан, дихлорэтан, хлороформ; и простые эфиры, такие как тетрагидрофуран и диоксан. Реакция может быть проведена в широких пределах температур, и точная температура реакции не играет решающей роли для осуществления изобретения. Предпочтительная температура реакции зависит от таких факторов, как природа растворителя и используемый исходный материал или реактив. Однако,по существу, авторы считают, что подходящей температурой для проведения реакции является температура от -20 до 150 С, а более предпочтительно приблизительно от 50 до 80 С. Время, требуемое для проведения реакции, может также варьироваться в широких пределах в зависимости от множества факторов,а в частности от температуры реакции и природы используемых реактивов и растворителей. Однако при проведении реакции в предпочтительных условиях, описанных выше, обычно достаточным является период времени от 30 мин до 24 ч, а более предпочтительно от 1 до 10 ч.- 15009201 Стадия 1J. В этой стадии, кислотное соединение формулы Ia может быть получено путем гидролиза соединения сложного эфира формулы 1-12. Данная реакция, по существу, представляет собой ту же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 1 В в схеме 1. Схема 2. В этой схеме проиллюстрировано получение соединений формулы (Ib), где R5 представляет собой-СО 2 Н; и X представляет собой группу формулы, в которой Rb и Rc независимо представляют собой атом водорода или алкильную группу, имеющую от 1 до 3 атомов углерода. Схема 2 В приведенной выше формуле L2 представляет собой атом галогена, такой как хлор, бром или йод; а все другие символы являются такими, как они определены выше. Стадия 2 А. В данной стадии соединение циклического 2-алкилового сложного эфира формулы 2-1 может быть превращено в соединение формулы 2-2, имеющее уходящую группу L2, в условиях, известных специалистам в данной области. Галогенированное соединение 2-2, по существу, может быть получено путем реакции галогенирования с галогенирующим реактивом в инертном реакционном растворителе. Примерами подходящих растворителей являются водные или безводные органические растворители, такие как тетрагидрофуран,диоксан, диметилформамид, ацетонитрил; спирты, такие как метанол или этанол; галогенированные углеводороды, такие как дихлорметан, дихлорэтан или хлороформ; и уксусная кислота. Подходящими галогенирующими реактивами являются, например, бром, хлор, йод, N-хлорсукцимид, N-бромсукцимид,1,3-дибром-5,5-диметилгидантоин, трибромид бис(диметилацетамид)водорода, трибромид тетрабути- 16009201 ламмония, бромид бромдиметилсульфония, гидропероксид бромистого водорода, нитродибромацетонитрил или бромид меди(II). Реакция может быть проведена при температуре от 0 до 200 С, а более предпочтительно от 20 до 120 С. Время, достаточное для проведения реакции, обычно составляет от 5 мин до 48 ч, а более предпочтительно от 30 мин до 24 ч. Стадия 2 В. В данной стадии, соединение формулы 2-5 может быть получено с помощью реакции сочетания галогенированного соединения формулы 2-2 с соединением бороновой кислоты формулы 2-3 в инертном растворителе. Примерами подходящих растворителей являются ароматические углеводороды, такие как бензол,толуол, ксилол, нитробензол и пиридин; галогенированные углеводороды, такие как метиленхлорид,хлороформ, тетрахлорметан и дихлорэтан; эфиры, такие как диэтиловый эфир, диизопропиловый эфир,ДМЭ, тетрагидрофуран и диоксан; этилацетат, ацетонитрил, N,N-диметилформамид, диметилсульфоксид и вода. Реакция может быть проведена при температуре от -100 до 250 С, а более предпочтительно от 0 С до температуры кипячения с обратным холодильником. В целом, время, достаточное для проведения реакции, составляет от 1 мин до 10 дней, предпочтительно от 20 мин до 5 дней, более предпочтительно от 1 мин до одного дня, а наиболее предпочтительно от 1 до 10 ч. Данная реакция может быть проведена в присутствии подходящего катализатора. Как и в предыдущих случаях, природа используемого катализатора не имеет конкретных ограничений, и в этой реакции могут быть использованы любые катализаторы, обычно используемые в реакциях этого типа. Примерами таких катализаторов являются тетракис(трифенилфосфин)палладий, хлорид бис(трифенилфосфин) палладия(II), медь(0), ацетат меди(I), бромид меди(I), хлорид меди(I), иодид меди(I), оксид меди(I), трифторметансульфонат меди(II), ацетат меди(II), бромид меди(II), хлорид меди(II), иодид меди(II), оксид меди(II), трифторметансульфонат меди(II), ацетат палладия(II), хлорид палладия(II), бисацетонитрилдихлорпалладий(0), бис(дибензилиденацетон)палладий(0), трис(дибензилиденацетон)дипалладий(0) или дихлорид [1,1'-бис(дифенилфосфино)ферроцен]палладия(II). Данная реакция может быть проведена в присутствии подходящей добавки. Примерами таких добавок являются трифенилфосфин, три-трет-бутилфосфин, 1,1'-бис(дифенилфосфино)ферроцен, три-2 фурилфосфин, три-о-толилфосфин, 2-(дихлоргексилфосфино)дифенил или трифениларсин. Данная реакция может быть проведена в присутствии или в отсутствии основания. Как и в предыдущих случаях, природа используемых оснований не имеет конкретных ограничений, и в этой реакции могут быть использованы любые основания, обычно используемые в реакциях этого типа. Примерами таких оснований являются гидроксид лития, гидроксид натрия, гидроксид калия, гидроксид бария, карбонат натрия, карбонат калия, бикарбонат натрия, карбонат цезия, карбонат таллия(I), этоксид натрия,трет-бутоксид калия, ацетат калия, фторид цезия, фторид тетрабутиламмония, хлорид тетрабутиламмония, иодид тетрабутиламмония, пиридин, 1,8-диазабицикло[5.4.0]ундекан, пиколин, 4-(N,N-диметиламино)пиридин, триэтиламин, трибутиламин, дииизопропилэтиламин, N-метилморфолин и N-метилпиперидин. Данная реакция может быть проведена в присутствии или в отсутствии дегидратирующего реактива. Как и в предыдущих случаях, природа используемого дегидратирующего реактива не имеет конкретных ограничей, и в этой реакции могут быть использованы любые дегидратирующие реактивы,обычно используемые в реакциях этого типа. Примерами таких дегидратирующих реактивов являются молекулярные сита. Стадия 2 С. В данной стадии, соединение формулы 2-7 может быть получено посредством реакции сочетания цинкового соединения формулы 2-4 с соединением формулы 1-5 в инертном растворителе. Примерами подходящих растворителей являются ароматические углеводороды, такие как бензол,толуол, ксилол, нитробензол, и пиридин; галогенированные углеводороды, такие как метиленхлорид,хлороформ, тетрахлорметан и дихлорэтан; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран и диоксан; этилацетат, ацетонитрил, N,N-диметилформамид, диметилсульфоксид. Данная реакция может быть проведена в присутствии подходящего катализатора. примерами подходящих катализаторов являются дихлорбис[трифенилфосфин]никель, тетракис(трифенилфосфин) палладий, хлорид бис(трифенилфосфин)палладия(II), медь(0), ацетат меди(I), бромид меди(I), хлорид меди(I), иодид меди(I), оксид меди(I), трифторметансульфонат меди(II), ацетат меди(II), бромид меди(II),хлорид меди(II), иодид меди(II), оксид меди(II), трифторметансульфонат меди(II), ацетат палладия(II),хлорид палладия(II), бисацетонитрилдихлорпалладий(0), бис(дибензилиденацетон)палладий(0), трис(дибензилиденацетон)дипалладий(0) или дихлорид [1,1'-бис(дифенилфосфино)ферроцен]палладия(II). Данная реакция может быть проведена при температуре от -50 до 150 С, предпочтительно примерно от -10 до 30 С в течение 5 мин - 48 ч, а более предпочтительно от 30 мин до 24 ч. Стадия 2D. В данной стадии, соединение формулы 2-7 может быть получено путем проведения реакции сочетания цинкового соединения формулы 2-6 с соединением формулы 1-1 в инертном растворителе.- 17009201 Данная реакция, по существу, представляет собой такую же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 2 С в схеме 2. Стадия 2 Е. В данной стадии кислотное соединение формулы 2-8 может быть получено путем гидролиза соединения сложного эфира формулы 2-7. Данная реакция, по существу, представляет собой такую же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 1 В в схеме 1. Стадия 2F. В данной стадии амидное соединение формулы 2-9 может быть получено путем проведения реакции сочетания кислотного соединения формулы 2-8 с аминовым соединением формулы 1-10. Данная реакция, по существу, представляет собой такую же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 1E в схеме 1. Стадия 2F В данной стадии кислотное соединение формулы Ib может быть получено путем гидролиза соединения сложного эфира формулы 2-9. Данная реакция, по существу, представляет собой такую же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 1 В в схеме 1. Схема 3. На этой схеме проиллюстрировано получение соединений формулы (Ic), где R5 представляет собойa R6 представляет собой алкильную группу, имеющую от 1 до 6 атомов углерода, циклоалкильную группу, имеющую от 3 до 7 атомов в кольце, арильную группу или гетероарильную группу. Схема 3 В вышеуказанной формуле все символы являются такими, как они были определены выше. Стадия 3 А. В данной стадии целевое соединение формулы Ic может быть получено путем проведения реакции сочетания соединения формулы Ia или Ib, полученного как описано в стадии 1J в схеме 1 и в стадии 2F в схеме 2, соответственно, с соединением формулы R6SO2NH2 в инертном растворителе. Данная реакция, по существу, представляет собой такую же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 1E в схеме 1. Схема 4. На этой схеме проиллюстрировано получение соединений формулы (Id), где R5 представ ляет собой В вышеуказанной формуле все символы являются такими, как они были определены выше. Стадия 4 А. В данной стадии тетразоловое соединение формулы Id может быть получено путем проведения реакции сочетания кислотного соединения формулы 1-7 с аминовым соединением формулы 4-1. Данная реакция, по существу, представляет собой такую же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 1E в схеме 1. Стадия 4 В. В данной стадии амидное соединение формулы 4-3 может быть получено путем проведения реакции сочетания кислотного соединения формулы 1-7 с аминовым соединением формулы 4-2. Данная реакция, по существу, представляет собой такую же реакцию, и она может быть проведена таким же способом и с применением тех же реактивов и реакционных условий, описанных в стадии 1E в схеме 1. Стадия 4 С. В данной стадии тетразоловое соединение формулы Id может быть получено путем превращения нитрильной группы соединения формулы 4-3 в тетразольную группу в инертном растворителе. Примерами подходящих растворителей являются ароматические углеводороды, такие как бензол или толуол; ДМФ, ДМСО, 2-метоксиэтанол, вода и ТГФ. Примерами подходящих тетразолобразующих реактивов являются азид натрия, азид лития, азид триалкилолова (алкил обычно представляет собой метил или бутил) и триметилсилилазид. Данная реакция может быть проведена в присутствии или в отсутствии катализатора. Примерами подходящих катализаторов являются оксид диалкилолова (алкил обычно представляет собой метил или бутил), алкиламиногидрохлорид, алкиламиногидробромид или хлорид лития. Если это необходимо, то такая реакция может быть проведена в присутствии или в отсутствии кислоты или основания. Примерами подходящих оснований являются триметиламин, триэтиламин иN,N-диизопропилэтиламин. Примерами подходящих кислот являются хлорид аммония, хлористый водород, хлорид алюминия или бромид цинка. Данная реакция может быть проведена при температуре от 50 до 200 С, предпочтительно примерно от 80 до 150 С в течение 5 мин - 48 ч, а предпочтительно 30 мин 30 ч. Если необходимо, то данная реакция может быть проведена в герметично закрывающейся пробирке. Исходные материалы в вышеописанных процедурах общего синтеза могут быть коммерчески доступными, либо они могут быть получены стандартными способами, известными специалистам в данной области. В вышеприведенных схемах 1-4, примерами подходящих растворителей являются смесь любых двух или более растворителей, описанных в каждой стадии. Соединения формулы (I) и промежуточные соединения, полученные вышеописанными способами,могут быть выделены и очищены в соответствии со стандартными процедурами, такими как перекристаллизация или хроматографическая очистка. Кроме того, предполагается, что соединения формулы (I) будут оказывать более эффективное терапевтическое действие при их совместном введении с СОХ-2-селективными НСПВС. Кроме того, настоящее изобретение также относится к комбинированному лечению воспаления,ревматоидного артрита, боли, насморка, остеоартрита, невропатической боли, опухоли головного мозга,диуреза или т.п., которое предусматривает введение терапевтически эффективного количества соединения формулы (I) или его соли и СОХ-2-селективного НСПВС. Соединения согласно изобретению могут быть преимущественно использованы в комбинации с од- 19009201 ним или несколькими другими терапевтическими ингредиентами, например, с СОХ-2-селективным,СОХ-1-селективным или неселективным НСПВС, опиоидом, противосудорожным средством, антидепрессантом, местным анестетиком, противоревматоидным лекарственным средством, влияющим на течение заболевания, или стероидом. Комбинация с СОХ-2-селективным НСПВС является особенно подходящей для профилактики и лечения боли и артрита. Примерами СОХ-2-селективных НСПВС являются нимесулид, целекоксиб, рофекоксиб и валдекоксиб. Было обнаружено, что соединения формулы (I) обладают антагонистической активностью по отношению к рецептору простагландина Е 2, а предпочтительно антагонистической активностью по отношению к рецептору ЕР 4. Эти соединения предпочтительно использовать в качестве аналгетика, противовоспалительного средства, диуретика и т.п. для введения индивидуумам-млекопитающим, а в частности человеку, который нуждается во введении указанных средств. Аффинность, антигонистическая активность и аналгетическая активность могут быть продемонстрированы в нижеследующих тестах, соответственно. Способ оценки биологических активностей: анализы in vitro Анализ на связывание клеточной мембраны с человеческим рецептором ЕР Стабильная экспрессия человеческих рецепторов ЕР 1, 2, 3 и 4 в эмбриональной клеточной линии почек человека (HEK293) Клоны кДНК человеческих рецепторов ЕР 1, 2, 3 и 4 получали с помощью полимеразной цепной реакции (ПЦР) из библиотек кДНК почки или сердца крысы (Clontech). Клетки почек человеческого эмбриона (HEK 293) стабильно трансфецировали экспрессионными векторами для человеческих рецепторов ЕР 1, 2, 3 и 4 методом, описанным в статье: The journal of biological chemistry vol.271 No.39, pp. 2364223645. Получение мембранной фракции Трансфектант ЕР 1, 2, 3 и 4 выращивали в модифицированной по способу Дульбекко среде Игла,содержащей 10% фетальную бычью сыворотку, 50 ед/мл пенициллина, 50 мкг/мл стептомицина и 500 мкл/мл G418 (селективной среды) при 37 С в атмосфере повышенной влажности с 5% CO2 на воздухе. Для приготовления мембранного препарата клетки собирали с использованием забуференного фосфатом физиологического раствора (PBS) и центрифугировали при 400 х g в течение 5 мин. Осадок суспендировали в охлажденном (4 С) PBS, содержащем 1/100 объема смеси ингибиторов протеаз (SIGMA) (1 мМ (4(2-аминоэтил)бензолсульфонилфторида (AEBSF, 0,8 мкМ апротинина, 22 мкМ лейпептина, 40 мкМ бестатина, 15 мкМ пепстатина А и 14 мкМ Е-64). Клетки разрушали на ультразвуковом дезинтеграторе клеток путем 60-секундной обработки ультразвуком. Затем смеси клеток центрифугировали при 1000 х g в течение 10 мин. Супернатант центрифугировали при 160000 х g в течение 30 мин при 4 С. Осадок ресуспендировали в аналитическом буфере (10 мМ 2-морфолиноэтансульфоновой кислоты (MES)-KOH, 1 мМ этилендиаминтетрауксусной кислоты (EDTA), 10 мМ MgCl2, рН 6,0) и концентрацию белка определяли методом Брэдфорда (анализ Bio-Rad). Данный мембранный препарат хранили при -80 С в холодильнике до его применения в анализе на связывание. Анализ на связывание: анализ на связывание с мембраной Анализы на связывание [3H]-PGE2 с мембраной проводили в реакционной смеси, содержащей 10 мМ MES/KOH (рН 6,0), 10 мМ MgCl2, 1 мМ EDTA, 1 нМ [3 Н]-PGE2 (Amersham TRK431, 164 Ки/ммоль),210 мкг белка из мембранной фракции (человеческие ЕР 1, 2, 3, и 4/трансфектант НЕК 293), и тестируемое соединение (полный объем составляет 0,1 мл в полипропиленовом 96-луночном планшете). Инкубирование проводили в течение 60 мин при комнатной температуре с последующим разделением связанного и свободного радиоактивно меченого лиганда с помощью быстрой фильтрации через стекловолоконные фильтры (фильтр Printed Filtermat В, 1205-404, стекловолоконный, двойной толщины, размер 102 х 258 мм, Wallac inc., предварительно смоченный в 0,2% полиэтиленимине). Фильтры промывали аналитическим буфером, и уровень остаточного [3 Н]-PGE2, связанного с фильтром, определяли на жидкостном сцинтилляционном счетчике (1205 Betaplate). Специфическое связывание определяли как разность между общим связыванием и неспецифическим связыванием, которое оценивали в присутствии 10 мкМPGE2. Анализ на сАМР в трансфектанте человеческого ЕР 4 Клетки НЕК 2 93, экспрессирующие рецепторы человеческого ЕР 4 (клетки hEP4) , поддерживали вDMEM, содержащей 10% FBS и 500 мкг/мл генетицина. Для сбора клеток hEP4, культуральную среду отсасывали, и клетки в 75 см 2-флаконе промывали 10 мл забуференным фосфатом физиологическим раствором (PBS). Затем в клетки добавляли еще 10 мл PBS и смесь инкубировали в течение 20 мин при комнатной температуре. Клетки человеческого ЕР 4 собирали пипеткой и центрифугировали при 300 х g в течение 4 мин. Клетки ресуспендировали в среде DMEM без нейтрального красного при плотности 7 х 105 клеток/мл, содержащей 0,2 мМ IBMX (ингибитор PDE), 1 нМ PGE2 и тестируемые соединения в ПЦРпробирках, и инкубировали при 37 С в течение 10 мин. Реакцию прекращали путем нагревания при 100 С в течение 10 мин в термоячейке. Концентрацию сАМР в реакционных смесях определяли с помощью набора SPA сАМР Kit (Amersham) или сАМР Screen (Applied BiosysteMC) в соответствии с инст- 20009201 рукцией производителя. Ссылка: Eur. J.Pharmacol. 340 (1997) 227-241. Таблица. Результат анализа на связывание человеческого рецептора ЕР (в кислотном и гипотоническом буфере, буфере ММЕ) и функционального анализа Анализы in vivo Индуцированная харрагенаном механическая гипералгезия у крыс 4-недельных самцов крыс SD не кормили в течение ночи. Гипералгезию индуцировали путем инъекции в подошву лапы А-каррагенина (0,1 мл 1% мас./об. суспензии в физиологическом растворе, Zushikagaku). Тестируемые соединения (1 мл 0,1 % метилцеллюлозы/100 г массы тела) вводили перорально через 5,5 ч после инъекции каррагенина. Через 4, 5, 6,5 и 7,5 ч после инъекции каррагенина определяли механический порог болевой чувствительности с помощью прибора для измерения аналгезии (UgoBasile) и вычисляли изменение порога болевой чувствительности. Ссылка: Randall L.0Selitto I.J., Arch. Int. Pharmacodyn. 111, 409-419, 1957 Индуцированная простагландином Е 2 (PGE2) термогипералгезия у крыс 4-недельных самцов крыс SD не кормили в течение ночи. Гипералгезию индуцировали путем инъекции в подошву правой задней лапы крыс 100 нг PGE2 в 0,05% этанола/физиологического раствора (100 мкл). Перед инъекцией PGE2, животным перорально или внутривенно вводили либо носитель (перорально: 0.1% метилцеллюлозы, внутривенно: 10% ДМСО/физиологического раствора), либо тестируемое соединение, соответственно. Крыс помещали в пластиковые клетки, снабженные прибором для проведения теста на подошвах лап (Ugo Basile), и на подушечку правой задней лапы крыс направляли подвижный источник теплового излучения. Задержку отдергивания лапы при тепловом нагревании (сек.) измеряли через 15 мин после инъекции PGE2. Ссылка: Hargreaves К. et al., Pain 32, 77-88, 1988. Лекарственное средство Фармацевтически приемлемые соли соединений формулы (I) включают их кислотно-аддитивные и основно-аддитивные соли. Подходящие кислотно-аддитивные соли получают из кислот, образующих нетоксичные соли. Примерами таких солей являются ацетат, аспартат, бензоат, безилат, бикарбонат/карбонат, бисульфат/сульфат, борат, камзилат, цитрат, эдисилат, эсилат, формиат, фумарат, глуцептат, глюконат, глюкуронат, гексафторфосфат, гибензат, гидрохлорид/хлорид, гидробромид/бромид, гидроиодид/иодид, изетионат, лактат, малат, малеат, малонат, мезилат, метилсульфат, нафтилат, 2-напсилат, никотинат, нитрат,оротат, оксалат, пальмитат, памоат, фосфат/гидрофосфат/дигидрофосфат, сахарат, стеарат, сукцинат,тартрат, тозилат и трифторацетат. Подходящие основные соли получают из оснований, образующих нетоксичные соли. Примерами таких солей являются соли алюминия, аргинина, бензатина, кальция, холина, диэтиламина, диоламина,глицина, лизина, магния, меглумина, оламина, калия, натрия, трометамина и цинка. Обзор подходящих солей можно найти в руководстве "Hadbook of Pharmaceutical Salts" от Stahl иWermuth (Wiley-VCH, Weinheim, Germany, 2002). Фармацевтически приемлемая соль соединения формулы (I) может быть получена путем простого смешивания растворов соединения формулы (I) и нужной кислоты или основания. Соль может осаждаться из раствора и она может быть собрана путем фильтрации или выделена путем выпаривания растворителя. Степень ионизации соли может варьироваться от полностью ионизованной до почти неионизованной. Соединения согласно изобретению могут находиться как в несольватированной, так и в сольвати- 21009201 рованной форме. Используемый здесь термин сольват означает молекулярный комплекс, содержащий соединение согласно изобретению и одну или несколько фармацевтически приемлемых молекул растворителя, например этанола. Термин гидрат используется в случае, если указанным растворителем является вода. В объем настоящего изобретения входят комплексы, такие как клатраты, комплексы включения типа лекарственное средство-хозяин, в которых, в отличие от вышеупомянутых сольватов, лекарственное средство и хозяин присутствуют в стехиометрических или нестехиометрических количествах. В объем настоящего изобретения также входят комплексы лекарственных средств, содержащие два или более органических и/или неорганических компонентов, которые могут присутствовать в стехиометрических или нестехиометрических количествах. Полученные комплексы могут быть ионизованными, частично ионизованными или неионизованными. Обзор таких комплексов можно найти в J Pharm Sci, 64 (8), 1269-1288 Haleblian (August 1975). Все приведенные ниже указания на соединения формулы (I) включают их соли, сольваты и комплексы, и сольваты и комплексы их солей. Соединения согласно изобретению включают соединения формулы (I), определенные выше, их полиморфы, пролекарства и изомеры (включая оптические, геометрические и таутомерные изомеры), определенные ниже, и меченые изотопами соединения формулы (I). Как указывалось выше, настоящее изобретение включает все полиморфы соединений формулы (I),определенные выше. В объем настоящего изобретения также входят так называемые пролекарства соединений формулы (I). Так, например, некоторые производные соединений формулы (I), которые сами могут обладать небольшой фармакологической активностью или вообще не обладать такой активностью, при их введении в организм или нанесении на его отдельные участки, могут превращаться в соединения формулы (I),обладающие нужной активностью, например, путем гидролитического расщепления. Такие производные называют пролекарствами. Дополнительную информацию по применению пролекарств можно найти вPro-drugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T Higuchi и W Stella) и Bioreversible Carriers in Drug Design, Pergamon Press, 1987 (ed. E В Roche, American Pharmaceutical Association). Пролекарства согласно изобретению, например, могут быть получены путем замены соответствующих функциональных групп, присутствующих в соединениях формулы (I), определенными группами, известными специалистам как про-группы, описанные, например, в Design of Prodrugs H Bundgaard (Elsevier, 1985). Некоторыми примерами пролекарств согласно изобретению являются пролекарства:(i) где соединение формулы (I) содержит функциональную группу карбоновой кислоты (-СООН) или ее сложный эфир, образующийся, например, при замещении водорода (C1-C8)алкилом;(ii) где соединение формулы (I) содержит спиртовую функциональную группу (-ОН) или ее простой эфир, образующийся, например, при замещении водорода (C1-С 6)алканоилоксиметилом; и(iii) где соединение формулы (I) содержит функциональную группу первичного или вторичного амина (-NR2 или -NHR, где RН) или ее амид, образующийся, например, при замещении одного или двух атомов водорода (C1-С 10)алканоилом. Дополнительные примеры групп-заместителей в соответствии с предшествующими примерами и примерами других типов пролекарств можно найти в приведенных выше ссылках. И наконец, некоторые соединения формулы (I) могут сами по себе действовать как пролекарства других соединений формулы (I). Соединения формулы (I), содержащие один или несколько асимметрических атомов углерода, могут находиться в виде двух или более стереоизомеров. Если соединение формулы (I) содержит алкенильную или алкениленовую группу, то могут образовываться геометрические, цис/транс (или Z/E)-изомеры. Если указанное соединение содержит, например, кетогруппу, оксимовую группу или ароматическую группу, такую как тетразолильная группа, то может иметь место таутомерная изомерия (таутомерия). Из этого следует, что одно соединение может иметь изомеры нескольких типов. В объем настоящего изобретения входят все стереоизомеры, геометрические изомеры и таутомерные формы соединений формулы (I), включая соединения, имеющие изомеры нескольких типов, и смеси одного или нескольких из указанных изомеров. Настоящее изобретение также включает кислотноаддитивные соли или основно-аддитивные соли, в которых противоион является оптически активным,например, D-лактат или L-лизин, или рацемическим, например, DL-тартрат или DL-аргинин. Цис/транс изомеры могут быть разделены стандартными методами, хорошо известными специалистам, например, путем проведения хроматографии и фракционированной кристаллизации. Стандартные методы получения/выделения отдельных энантиомеров включают хиральный синтез из подходящего оптически чистого предшественника или разделение рацемата (рацемата соли или производного) с применением, например, хиральной жидкостной хроматографии высокого давления(ЖХВД). Альтернативно, рацемат (или рацемический предшественник) может быть подвергнут реакции с подходящим оптически активным соединением, например спиртом, или, в случае, когда соединение- 22009201 формулы (I) содержит кислотную или основную группу, с кислотой или основанием, такими как винная кислота или 1-фенилэтиламин. Полученная диастереомерная смесь может быть разделена с помощью хроматографии и/или фракционированной кристаллизации, и один или оба диастереоизомера могут быть превращены в соответствующий(е) чистый(е) энантиомер(ы) методами, хорошо известными специалисту. Хиральные соединения согласно изобретению (и их хиральные предшественники) могут быть получены в энантиомерно обогащенной форме с помощью хроматографии, обычно ЖХВД, на асимметричной смоле с подвижной фазой, состоящей из углеводорода, обычно гептана или гексана, и содержащей от 0 до 50% изопропанола, обычно от 2 до 20%, и от 0 до 5% алкиламина, обычно 0,1% диэтиламина. Концентрирование элюата дает обогащенную смесь. Стереоизомерные конгломераты могут быть разделены стандартными методами, известными специалистам, см., например, "Stereochemistry of Organic Compounds" E. L. Eliel (Wiley, New York, 1994) . Настоящее изобретение включает все фармацевтически приемлемые меченые изотопами соединения формулы (I), где один или несколько атомов замещены атомами, имеющими тот же самый атомный номер, но, при этом, имеющими атомные массы или массовые числа, отличающиеся от атомной массы или массового числа соединений, обычно встречающихся в природе. Примерами изотопов, подходящих для включения в соединения согласно изобретению, являются изотопы водорода, такие как 2 Н и 3 Н; углерода, такие как 11 С, 13 С и 14 С; хлора, такие как 36Cl; фтора, такие как 18F; йода, такие как 123I и 125I; азота, такие как 13N и 15N; кислорода, такие как 15O, 17O и 18O; фосфора, такие как 32 Р; и серы, такие как 35S. Некоторые меченые изотопами соединения формулы (I), например соединения, включающие радиоактивный изотоп, могут быть использованы в исследованиях распределения лекарственного средства и/или субстрата в тканях. Радиоактивные изотопы, например тритий, то есть 3 Н, и углерод-14, то есть 14 С, являются особенно подходящими для этой цели из-за легкости их включения и обнаружения. Замещение более тяжелыми изотопами, такими как дейтерий, то есть 2 Н, может давать некоторые терапевтические преимущества, такие как более высокая метаболическая стабильность, например, увеличенный период полужизни in vivo, или возможность снижения доз, а, поэтому, в некоторых случаях,такое замещение может оказаться предпочтительным. Замещение изотопами, испускающими позитроны, такими как 11C, 18F, 15O и 13N, может применяться в исследованиях методами позитронно-эмиссионной топографии (PET) для оценки связывания рецептора с субстратом. Меченные изотопами соединения формулы (I), по существу, могут быть получены стандартными методами, известными специалистам, или способами, аналогичными описанным в прилагаемых примерах и препаративных примерах, с использованием подходящих меченных изотопами реагентов вместо используемого ранее немеченного реагента. Фармацевтически приемлемыми сольватами согласно изобретению являются сольваты, в которых,растворитель кристаллизации может быть заменен изотопами, например, D2O, d6-ацетоном, d6-ДМСО. Готовые лекарственные формы Соединения согласно изобретению, предназначенные для фармацевтического применения, могут быть введены в виде кристаллических или аморфных продуктов. Они могут быть получены, например, в виде твердых тампонов, порошков или пленок такими методами, как осаждение, кристаллизация, лиофилизация, сушка распылением или сушка выпариванием. Для этих целей может быть использована сушка в микроволновой печи или в высокочастотной сушилке. Указанные соединения могут быть введены отдельно или в сочетании с одним или несколькими другими соединением согласно изобретению или в сочетании с одним или несколькими другими лекарственными средствами (или в виде любой их комбинации). В основном, они могут быть введены в виде композиции в сочетании с одним или несколькими фармацевтически приемлемыми наполнителями. Используемый здесь термин наполнитель означает любой ингредиент, кроме соединения(й) согласно изобретению. Выбор наполнителей в значительной степени зависит от таких факторов, как конкретный способ введения, влияние наполнителя на растворимость и стабильность, и природа лекарственной формы. Фармацевтические композиции, подходящие для доставки соединений согласно изобретению, и методы их приготовления очевидны для специалистов в данной области. Такие композиции и методы их приготовления можно найти, например, в руководстве Remington's Pharmaceutical Sciences, 19th Edition(Mack Publishing Company, 1995). Пероральное введение Соединения согласно изобретению могут быть введены перорально. Пероральное введение может включать проглатывание, благодаря которому соединение поступает в желудочно-кишечный тракт, либо трансбуккальное или подъязычное введение, благодаря которому соединение поступает в кровоток непосредственно из ротовой полости. Композициями, подходящими для перорального введения, являются твердые композиции, такие как таблетки, капсулы, содержащие частицы, жидкости или порошки, пастилки (включая пастилки, запол- 23009201 ненные жидкостью), жевательные резинки, мульти-и наночастицы, гели, твердые растворы, липосомы,пленки (включая мукоадгезивы), овули, спреи и жидкие композиции. Жидкими композициями являются суспензии, растворы, сиропы и эликсиры. Такие композиции могут быть использованы в качестве наполнителей в мягких или твердых капсулах, и они обычно содержат носитель, например воду, этанол, полиэтиленгликоль, пропиленгликоль, метилцеллюлозу или подходящее масло, и одно или несколько эмульгирующих веществ и/или суспендирующих веществ. Жидкие композиции могут быть также получены путем разведения твердого препарата, например, из саше. Соединения согласно изобретению могут быть также использованы в быстрорастворимых и быстро распадающихся лекарственных формах, таких как формы, описанные в Expert Opinion in Therapeutic Patents, 11 (6), 981-986 Liang и Chen (2001). Для лекарственных форм типа таблеток, в зависимости от дозы, лекарственное средство может составлять от 1 до 80 мас.% от всей лекарственной формы, а обычно от 5 до 60 мас.% от всей лекарственной формы. Помимо лекарственного средства, таблетки обычно содержат дезинтегратор. Примерами дезинтеграторов являются натрийсодержащий гликолят крахмала, натрийсодержащая карбоксиметилцеллюлоза, кальцийсодержащая карбоксилметилцеллюлоза, натрийсодержащая кроскармелоза, кросповидон, поливинилпирролидон, метилцеллюлоза, микрокристаллическая целлюлоза, гидроксипропилцеллюлоза, замещенная низшим алкилом, крахмал, предварительно желатинизированный крахмал и альгинат натрия. Дезинтегратор обычно составляет от 1 до 25 мас.%, а предпочтительно от 5 мас.% до 20 мас.% от всей лекарственной формы. Связующие вещества обычно используют для придания препарату-таблетке когезионных свойств. Подходящими связующими веществами являются микрокристаллическая целлюлоза, желатин, сахара,полиэтиленгликоль, природные и синтетические смолы, поливинилпирролидон, предварительно желатинизированный крахмал, гидроксипропилцеллюлоза и гидроксипропилметилцеллюлоза. Таблетки также могут содержать разбавители, такие как лактоза (моногидрат, моногидрат, высушенный путем распыления, безводный и т.п.), маннит, ксилит, декстроза, сахароза, сорбит, микрокристаллическая целлюлоза, крахмал и двуосновный дигидрат фосфата кальция. Таблетки могут также, но необязательно, содержать поверхностно-активные вещества, такие как лаурилсульфат натрия и полисорбат 80 и вещества, улучшающие скольжение, такие как диоксид кремния и тальк. Поверхностно-активные вещества, если они присутствуют, могут составлять от 0,2 до 5 мас.% таблетки, а вещества, улучшающие скольжение, могут составлять от 0,2 до 1 мас.% таблетки. Таблетки могут также содержать замасливатели, такие как стеарат магния, стеарат кальция, стеарат цинка, натрий-содержащий стеарилфумарат, и смеси стеарата магния с лаурилсульфатом натрия. Замасливатели, в основном, составляют от 0,25 до 10 мас.%, а предпочтительно от 0,5 мас.% до 3 мас.% таблетки. Другими возможными ингредиентами являются антиоксиданты, красители, ароматизаторы, консерванты и вещества для маскировки вкуса. Типичные таблетки содержат приблизительно до 80% лекарственного средства, приблизительно от 10 до 90 мас.% связующего вещества, приблизительно от 0 до 85 мас.% разбавителя, приблизительно от 2 до 10 мас.% дезинтегрирующего агента и приблизительно от 0,25 мас.% до 10 мас.% замасливателя. Смеси для приготовления таблеток могут быть спрессованы непосредственно или с помощью валика для формования таблеток. Альтернативно, смеси для приготовления таблеток или части этих смесей могут быть подвергнуты мокрой грануляции, сухой грануляции или грануляции в расплаве, а затем отверждению в расплаве или экструзии с последующим таблетированием. Конечный препарат может содержать один или несколько слоев и может иметь, а может и не иметь покрытие, причем он может быть также заключен в капсулу. Препарат в виде таблеток обсуждается в "Pharmaceutical Dosage Forms: Tablets, Vol. 1", H. Lieberman и L. Lachman, Marcel Dekker, N.Y., N.Y., 1980 (ISBN 0-8247-6918-X). Твердые препараты для перорального введения могут быть изготовлены в форме для немедленного и/или модифицированного высвобождения. Препаратами модифицированного высвобождения являются препараты замедленного, пролонгированого, импульсного, регулируемого, нацеленного и запрограммированного высвобождения. Подходящие препараты модифицированного высвобождения, которые могут быть использованы в целях настоящего изобретения, описаны в патенте США 6106864. Подробное описание других подходящих методов получения препаратов с регулируемым высвобождением, таких как высокоэнергетические дисперсии, осмотические частицы и частицы с покрытиями, можно найти в руководстве Verma и др. ,Pharmaceutical Technology On-line, 25(2), 1-14 (2001). Применение жевательной резинки для обеспечения регулируемого высвобождения описано в WO 00/255298. Парентеральное введение Соединения согласно изобретению могут быть также введены непосредственно в кровоток, в мышцу или во внутренний орган. Подходящими способами парентерального введения являются внутривенное, внутриартериальное, внутрибрюшинное, интратекальное, интравентрикулярное, интрауретральное,интрастернальное, внутричерепное, внутримышечное и подкожное введение. Подходящими устройства- 24009201 ми для парентерального введения являются шприцы с иглой (включая микроиглу), безыгольные инъекторы и устройства для вливания. Парентеральные препараты обычно представляют собой водные растворы, которые могут содержать наполнители, такие как соли, углеводы и забуферивающие вещества (с рН предпочтительно от 3 до 9), но в некоторых случаях, они могут быть приготовлены в виде стерильных безводных растворов или сухих форм, которые затем разводят подходящим носителем, таким как стерильная, апирогенная вода. Приготовление парентеральных препаратов в стерильных условиях, например, путем лиофилизации, может быть легко осуществлено с применением стандартных фармацевтических технологий, хорошо известных специалистам. Растворимость соединений формулы (I), используемых в приготовлении парентеральных растворов,может быть увеличена с применением подходящих методов приготовления лекарственных препаратов,таких как включение веществ, повышающих растворимость. Композиции для парентерального введения могут быть изготовлены в форме для немедленного и/или модифицированного высвобождения. Препаратами модифицированного высвобождения являются препараты замедленного, пролонгированого, импульсного, регулируемого, целевого и запрограммированного высвобождения. Таким образом, соединения согласно изобретению могут быть приготовлены в виде твердого препарата, полутвердого препарата или тиксотропной жидкости для введения в виде депоимплантата, обеспечивающего модифицированное высвобождение активного соединения. Примерами таких композиций являются стенты и PGLA-микросферы, покрытые лекарственным средством. Местное введение Соединения согласно изобретению могут быть также нанесены местно на кожу или слизистую оболочку, то есть, наружно или трансдермально. Типичными композициями, подходящими для этой цели,являются гели, гидрогели, лосьоны, растворы, кремы, мази, присыпки, повязки, пены, пленки, кожные пластыри, облатки, имплантанты, губки, волокна, бандажи и микроэмульсии. Могут быть также использованы липосомы. Типичными носителями являются спирт, вода, минеральное масло, жидкое вазелиновое масло, белый вазелин, глицерин, полиэтиленгликоль и пропиленгликоль. Могут быть также включены усилители пенетрации, см., например, J Pharm Sci, 88 (10), 955-958 by Finnin and Morgan (October 1999). Другими методами местного введения является доставка путем электропорации, ионтофореза, фонофореза, сонофореза и микроигольная или безыгольная (например, Powderject, Bioject, и т.д.) инъекции. Композиции для местного введения могут быть приготовлены в форме для немедленного и/или модифицированного высвобождения. Препаратами модифицированного высвобождения являются препараты замедленного, пролонгированого, импульсного, регулируемого, целевого и запрограммированного высвобождения. Введение путем ингаляции/интраназальное введениие Соединения согласно изобретению могут быть также введены интраназально или путем ингаляции,обычно в форме сухого порошка (отдельно, в виде смеси, например, в виде сухой смеси с лактозой или в виде смеси частиц с различными компонентами, например с фосфолипидами, такими как фосфатидилхолин) из инсуффлятора, или в виде аэрозольного спрея из емкости под давлением, из насоса, аэрозольного ингалятора (предпочтительно электрогидродинамического ингалятора с образованием мелкодисперсного аэрозоля), или распылителя с использованием подходящего пропеллента, такого как 1,1,1,2 тетрафторэтан или 1,1,1,2,3,3,3-гептафторпропан, или без него. Порошок для интраназального введения может содержать биоадгезивное вещество, например, хитозан или циклодекстрин. Емкость под давлением, насос, аэрозольный ингалятор или распылитель включает раствор или суспензию соединения(й) согласно изобретению, содержащие, например, этанол, водный этанол или подходящий альтернативный агент для диспергирования, солюбилизации или пролонгированного высвобождения активного компонента; пропеллент(ы) в качестве растворителя, и необязательно, поверхностноактивное вещество, такое как сорбитантриолеат, олеиновая кислота или олигомолочная кислота. Перед использованием в препарате в виде сухого порошка или суспензии готовую лекарственную композицию измельчают до получения частиц с размером, подходящим для доставки путем ингаляции(обычно менее 5 мкм). Это может быть достигнуто с применением любого подходящего способа измельчения, такого как размол на спиральной струйной мельнице, размол в мельнице с псевдоожиженным слоем, обработка надкритической жидкостью с образованием наночастиц, гомогенизация под высоким давлением, или сушка распылением. Для применения в ингаляторе или в инсуффляторе могут быть получены капсулы (например, изготовленные из желатина или НРМС), блистерные упаковки и картриджи, содержащие порошковую смесь соединения согласно изобретению, подходящую порошковую основу, такую как лактоза или крахмал, и технологическую модифицирующую добавку, такую как L-лейцин, маннит или стеарат магния. Лактоза может быть безводной, либо она может иметь форму моногидрата, причем последняя является предпочтительной. Другими подходящими наполнителями являются декстран, глюкоза, мальтоза, сорбит, ксилит, фруктоза, сахароза и трегалоза.- 25009201 Подходящая композиция в виде раствора, предназначенная для использования в электрогидродинамическом распылителе с получением мелкодисперсного аэрозоля, может содержать от 1 до 20 мкг соединения согласно изобретению на один впрыск, и объем впрыска может варьироваться от 1 до 100 мкл. Типичная композиция может содержать соединение формулы (I), пропиленгликоль, стерильную воду,этанол и хлорид натрия. Альтернативными растворителями, которые могут быть использованы вместо пропиленгликоля, являются глицерин и полиэтиленгликоль. В данные композиции согласно изобретению, предназначенные для введения путем ингаляции/интраназального введения, могут быть добавлены подходящие ароматизаторы, такие как ментол и левометанол, или подсластители, такие как сахарин или замещенный натрием сахарин. Композиции для введения путем ингаляции/интраназального введения могут быть изготовлены в форме для немедленного и/или модифицированного высвобождения с применением, например, поли(DL-молочной-гликолевой кислоты (PGLA. Препаратами модифицированного высвобождения являются препараты замедленного, пролонгированого, импульсного, регулируемого, целевого и запрограммированного высвобождения. В случае применения ингаляторов и аэрозолей для сухих порошков, унифицированная доза определяется посредством дозирующего клапана, обеспечивающего подачу нужного количества лекарственного средства. Унифицированная доза согласно изобретению, в основном, может быть доставлена в виде отмеренной клапаном дозы, необходимой для введения, или отдельного впрыска, содержащего от 1 мкг до 10 мг соединения формулы (I). Полная суточная доза обычно составляет в пределах от 1 мкг до 10 мг, и эта доза может быть введена в виде разовой дозы или, чаще, в виде дробных доз, вводимых в течение дня. Ректальное/интравагинальное введение Соединения изобретения могут быть введены ректально или вагинально, например, в форме суппозиториев, пессариев или клизмы. Традиционной основой для суппозиториев является масло какао, но могут быть использованы различные альтернативные варианты. Композиции для ректального/вагинального введения могут быть изготовлены в форме для немедленного и/или модифицированного высвобождения. Препаратами модифицированного высвобождения являются препараты замедленного, пролонгированого, импульсного, регулируемого, целевого и запрограммированного высвобождения. Внутриглазное/внутриушное введение Соединения согласно изобретению могут быть также введены непосредственно в глаз или в ухо,обычно в форме капель мелкодисперсной суспензии или раствора в изотоническом, стерильном физиологическом растворе со скорректированным рН. Другими композициями, подходящими для внутриглазного и внутриушного введения, являются мази, биоразлагаемые (например, гемостатические губки, коллаген) и биологически неразлагаемые (например, силиконовые) имплантанты, прокладки, линзы и дисперсные или везикулярные системы, такие как ниосомы или липосомы. Вместе с консервантом, таким как хлорид бензалкония, может быть включен полимер такой, как полиакриловая кислота с поперечными связями, поливиниловый спирт, гиалуроновая кислота, целлюлозный полимер, например, гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза или метилцеллюлоза, либо гетерополисахаридный полимер, например, гелановая камедь. Такие композиции могут быть также доставлены с помощью ионтофореза. Композиции для внутриглазного/внутриушного введения могут быть изготовлены в форме для немедленного и/или модифицированного высвобождения. Препаратами модифицированного высвобождения являются препараты замедленного, пролонгированого, импульсного, регулируемого, целевого и запрограммированного высвобождения. Другие технологии Для применения в любом из описанных выше способов введения, соединения согласно изобретению могут быть объединены с растворимыми макромолекулярными компонентами, такими как циклодекстрин и его подходящие производные или полимеры, содержащие полиэтиленгликоль, в целях улучшения растворимости, скорости растворения, маскировки вкуса, биологической доступности и/или стабильности. Было обнаружено, например, что комплексы лекарственное средство - циклодекстрин, по существу, могут быть использованы в большинстве лекарственных форм и способах введения. При этом могут быть использованы как комплексы включения, так и комплексы, не являющиеся комплексами включения. Альтернативно, циклодекстрин, помимо его применения для прямого образования комплексов с лекарственным средством, может быть использован в качестве вспомогательной добавки, то есть в качестве носителя, разбавителя, или солюбилизатора. Обычно для этих целей используют альфа-, бета- и гамма-циклодекстрины, примеры которых можно найти в Международных патентных заявках . WO 91/11172, WO 94/02518 и WO 98/55148. Набор компонентов Поскольку может оказаться желательным введение комбинации активных соединений, например,для лечения конкретного заболевания или состояния, то в объем настоящего изобретения входят две или более фармацевтических композиций, по меньшей мере одна из которых содержит соединение согласно- 26009201 изобретению, которые могут быть соответствующим образом объединены в наборе, подходящем для совместного введения указанных композиций. Таким образом, набор согласно изобретению включает две или более отдельных фармацевтических композиций, по меньшей мере одна из которых содержит соединение формулы I согласно изобретению,и средство для отдельного хранения указанных композиций, такое как контейнер, отдельный флакон или отдельный пакет из фольги. Примером такого набора является обычная блистерная упаковка, используемая для упаковки таблеток, капсул и т.п. Набор согласно изобретению является особенно подходящим для введения различных унифицированных лекарственных форм, например, пероральной и парентеральной формы, для введения отдельных композиций в различные интервалы времени или для титрования отдельных композиций относительно друг друга. Для удобства такой набор обычно содержит инструкции по введению лекарственного средства, и в него может быть вложена так называемая памятка. Дозировка Для введения пациентам полная суточная доза соединений согласно изобретению обычно составляет в пределах от 0,1 до 3000 мг, предпочтительно от 1 до 500 мг, в зависимости от способа введения. Так,например, для перорального введения может потребоваться полная суточная доза от 0,1 до 3000 мг, а предпочтительно от 1 до 500 мг, а для внутривенного введения может потребоваться лишь доза, составляющая от 0,1 до 1000 мг, а предпочтительно от 0,1 до 300 мг. Полная суточная доза может быть введена в виде разовой дозы или дробных доз. Эти дозы вычисляют в расчете на среднего индивидуума, имеющего массу приблизительно от 65 до 70 кг. Для пациентов, масса которых выходит за пределы этого интревала, таких как дети и пожилые люди, соответствующие дозы могут быть легко определены лечащим врачом. Во избежание неопределенности, в настоящем изобретении понятие "лечение" включает радикальное, паллиативное или профилактическое лечение. Примеры Настоящее изобретение проиллюстрировано в следующих неограничивающих примерах, в которых, если это не оговорено особо, все операции проводили при комнатной температуре или температуре окружающей среды, то есть, в интервале 18-25 С; выпаривание растворителя проводили на роторном испарителе при пониженном давлении и при температуре бани до 60 С; мониторинг реакции проводили с помощью тонкослойной хроматографии (ТСХ), а время реакции приводится лишь для иллюстрации; приведенные температуры плавления (т.пл.) не были скорректированы (полиморфизм может приводить к различным температурам плавления); структуру и степень очистки всех выделенных соединений подтверждали по меньшей мере одним из следующих способов, таких как ТСХ (ТСХ-пластины, предварительно покрытые силикагелем Merck 60 F254) , масс-спектрометрия, спектрометрия ядерного магнитного резонанса (ЯМР), инфракрасная (ИК) абсорбционная спектроскопия или микроанализ. Выходы приводятся лишь в целях иллюстрации. Колоночную флеш-хроматографию осуществляли на силикагеле Merck 60 (230-400 меш, ASTM). Данные масс-спектроскопии низкого разрешения (EI) получали на массспектрометре Integrity (Waters). Данные масс-спектроскопии низкого разрешения (ESI) получали на массспектрометре ZMD (Micromass). Данные ЯМР определяли при 270 МГц (на спектрометре JEOL JNM-LA 27 0) или при 300 МГц (на спектрометре JEOL JNM-LA300), с использованием дейтерированного хлороформа (99,8% D) или диметилсульфоксида (99,9% D) в качестве растворителя, если это не оговорено особо, где в качестве внутреннего стандарта использовали тетраметилсилан (ТМС) в миллионных долях(ppm); при этом, были использованы следующие условные сокращения: s = синглет, d (д) = дуплет, t (т) = триплет, q (кв.)= квартет, quint (квин.) = квинтет, m (м) = мультиплет, br. (шир.) = широкий, и т.д. ИКспектры измеряли на инфракрасном спектрометре Shimadzu (IR-470). Химические символы имеют свои обычные значения; bp (т.кип.) (точка кипения), mp (т.пл.) (точка плавления), л (литр (литры, мл (миллилитр (миллилитры, г (грамм (граммы, мг (миллиграмм (миллиграммы, моль (моли), ммоль (миллимоли), экв. (эквивалент (эквиваленты, колич., (количественный выход). ПРИМЕР 1. 4-[([5-ФТОР-2-(4-ФТОРФЕНОКСИ)ПИРИДИН-3-ИЛ]КАРБОНИЛАМИНО)МЕТИЛ] БЕНЗОЙНАЯ КИСЛОТА Стадия 1. Метил 5-фтор-2-(4-фторфенокси)никотинат. Смесь 2-хлор-5-фторникотиновой кислоты (2,61 г, 14,9 ммоль), 4-фторфенола (2,02 г, 18 ммоль),карбоната калия (4,56 г, 33 ммоль), медной бронзы (211 мг, 3,3 ммоль) и иодида меди (230 мг, 1,2 ммоль) в N,N-диметилформамиде (40 мл) кипятили с обратным холодильником в масляной бане в течение 6 ч. Реакционную смесь фильтровали через слой целита. Фильтрат распределяли между этилацетатом (200 мл) и 2 н. соляной кислотой (200 мл). Органическую фазу отделяли, а водную фазу экстрагировали этил- 27009201 ацетатом (200 мл). Объединенные органические экстракты промывали насыщенным раствором соли (50 мл) и сушили (сульфатом натрия). После удаления растворителя, остаточное масло растворяли в метаноле (50 мл). К раствору добавляли конц. соляную кислоту (1 мл), и смесь кипятили с обратным холодильником в течение 4 ч. Летучие компоненты удаляли при пониженном давлении и остаток очищали с помощью колоночной флеш хроматографии на силикагеле (150 г), элюируя гексаном/этилацетатом (3/1), с получением 2,63 г (67%) указанного в заголовке соединения: 1 Н-ЯМР (CDCl3)8,11 (1 Н, д, J = 3,1 Гц),8,02 (1 Н, дд, J = 7,7, 3,1 Гц), 7,11-7,07 (4 Н, м) , 3,96 (3 Н, с); МС (ESI) m/z 266 (М + Н)+. Стадия 2. 5-Фтор-2-(4-фторфенокси)никотиновая кислота. К перемешиваемому раствору метил 5-фтор-2-(4-фторфенокси)никотината (стадия 1, 2,63 г, 9,9 ммоль) в метаноле (50 мл) добавляли 2 н. водный раствор гидроксида натрия (10 мл). Реакционную смесь перемешивали при 40 С в течение 3 ч. После охлаждения, рН доводили до 4,0 добавлением 2 н. соляной кислоты. Смесь разбавляли водой (100 мл) и экстрагировали дихлорметаном (100 мл х 3). Объединенный органический слой промывали насыщенным раствором соли (100 мл), сушили (сульфатом натрия) и концентрировали с получением 2,2 6 г (91%) указанного в заголовке соединения в виде не совсем белого твердого вещества: 1H-ЯМР (CDCl3)8,25 (1 Н, дд, J = 7,5, 3,1 Гц), 8,16 (1 Н, д, J = 3,1 Гц), 7,16-7,13 (4 Н,м); МС (ESI) m/z 252 (М + Н)+. Стадия 3. Метил 4-[([5-фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)метил]бензоат. К перемешиваемому раствору 5-фтор-2-(4-фторфенокси)никотиновой кислоты (стадия 2, 300 мг, 1,2 ммоль) и гидрохлорида метил 4-(аминометил)бензоата (28 4 мг, 1,4 юдоль) в дихлорметане (10 мл) последовательно добавляли гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (EDCI) (670 мг,3,5 ммоль), гидрат 1-гидроксибензотриазола (НОВТ) (368 мг, 2,4 ммоль) и триэтиламин (3 мл) . После перемешивания в течение ночи реакцию гасили добавлением насыщенного водного раствора бикарбоната натрия (50 мл). Водный слой экстрагировали дихлорметаном (50 мл х 2), и объединенные органические слои промывали насыщенным раствором соли (50 мл), сушили (сульфатом натрия) и выпаривали. Остаток очищали колоночной флеш-хроматографией на силикагеле (50 г), элюируя гексаном/этилацетатом (3/1) с получением 407 мг (85%) указанного в заголовке соединение в виде белого твердого вещества: 1H-ЯМР (CDCl3)8,39 (1 Н, дд, J = 8,3, 3,1 Гц), 8,28 (1 Н, шир.с), 8,05 (1 Н, д, J = 3,1 Гц), 8,01 (2 Н, д,J = 8,1 Гц), 7,42 (2 Н, д, J = 8,1 Гц), 7,17-7,05 (4 Н, м), 4,76 (2 Н, д, J = 5,9 Гц), 3,91 (3 Н, с); МС (ESI) m/z 399(М + Н)+, 397 (М -Н)-. Стадия 4. 4-[([5-Фтор-2-(4-фторфенокси)пиридин-3-ил]карбонил амино)метил]бензойная кислота. К перемешиваемому раствору метил 4-[([5-фтор-2-(4-фторфенокси)пиридин-3-ил]карбонил амино)метил]бензоата (стадия 3, 407 мг, 1,02 ммоль) в метаноле (10 мл) добавляли 2 н. водный раствор гидроксида натрия (2 мл). Реакционную смесь перемешивали при комнатной температуре в течение 3 ч, а затем выпаривали. Остаток распределяли между этилацетатом (100 мл) и 2 н. соляной кислотой (100 мл). Органическую фазу отделяли, а водную фазу экстрагировали этилацетатом (100 мл). Объединенные органические экстракты промывали насыщенным раствором соли (50 мл), сушили (сульфатом натрия) и концентрировали. Остаточные твердые вещества перекристаллизовали из этилацетата с получением 248 мг (64%) указанного в заголовке соединения в виде белого твердого вещества: 1 Н-ЯМР (CDCl3)8,40 Стадия 1. N-[1-(4-Бромфенил)этил]-5-фтор-2-(4-фторфенокси)никотинамид. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 3 примера 1, из 5-фтор-2-(4-фторфенокси)никотиновой кислоты (стадия 2 примера 1) и [1-(4-бромфенил) этил] амина: 1H-ЯМР (CDCl3)8,31 (1 Н, ддд, J = 8,2, 3,1, 0,9 Гц), 8,14 (1 Н, д, J = 7,2 Гц), 8,03 (1 Н, дд, J = 3,1, 1,1 Гц), 7,45 (2 Н, дд, J = 7,0, 0,9 Гц), 7,25-7,09 (6 Н, м) , 5,28 (1 Н, дкв, J = 7,2, 7,0 Гц), 1,57 (3 Н, д, J = 7,0 Гц); МС (ESI) m/z 433 (М + Н)+, 431 (М - Н)-. Стадия 2. Метил 4-[1-([5-фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)этил]бензоат. Смесь N-[1-(4-бромфенил)этил]-5-фтор-2-(4-фторфенокси)никотинамида (стадия 1, 398 мг, 0,92 ммоль), 1,3-бис(дифенилфосфино)пропана (38 мг, 0,09 ммоль), ацетата палладия(II) (21 мг, 0,09 ммоль),триэтиламина (0,38 мл, 2,76 ммоль), N,N-диметилформамида (6 мл) и метанола (4 мл) перемешивали при 80 С в течение 16 ч в атмосфере моноксида углерода. После охлаждения до комнатной температуры смесь разбавляли простым эфиром (100 мл) и промывали водой (60 мл х 3). Органический слой сушили над сульфатом магния и выпаривали. Остаток очищали колоночной флеш-хроматографией на силикагеле, элюируя гексаном/этилацетатом (2:1) с получением 296 мг (78%) указанного в заголовке соединения- 28009201 в виде белого твердого вещества: 1H-ЯМР (CDCl3)8,32 (1 Н, дд, J = 8,1, 3,1 Гц), 8,21 (1 Н, д, J = 7,3 Гц),8,04-7,99 (3 Н, м), 7,43 (2 Н, д, J = 8,2 Гц), 7,27-7,13 (4 Н, м), 5,38 (1 Н, дкв, J = 7,3, 6,9 Гц), 3,90 (3 Н, с), 1,60(3 Н, д, J = 6,9 Гц); МС (ESI) m/z 413 (М + Н)+, 411 (М - Н)-. Стадия 3. 4-[1-([5-Фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойная кислота. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 4 примера 1, из метил 4-[1-([5-фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)этил]бензоата (стадия 2): 1H-ЯМР (ДМСО-d6)9,01 (1 Н, д, J = 7,9 Гц), 8,23 (1 Н, дд, J = 3,1, 1,3 Гц), 8,02 (1 Н, ддд, J = 7,9,3,1, 1,3 Гц), 7,86 (2 Н, д, J = 8,3 Гц), 7,52 (2 Н, д, J = 7,5 Гц), 7,30-7,24 (4 Н, м) , 5,18 (1 Н, дкв, J = 7,9, 7,0 Гц), 1,46 (3 Н, д, J = 7,0 Гц); МС (ESI) m/z 399 (М + Н)+, 397 (М - Н)-. ПРИМЕР 3. 4-[1-([5-ФТОР-2-(4-ФТОРФЕНОКСИ)ПИРИДИН-3-ИЛ]КАРБОНИЛАМИНО)ПРОПИЛ]БЕНЗОЙНАЯ КИСЛОТА Сстадия 1. Метил 4-[1-([5-фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)пропил]бензоат. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 3 примера 1, из 5-фтор-2-(4-фторфенокси)никотиновой кислоты (стадия 3 примера 1) и метил 4-(1 аминопропил) бензоата: 1H-ЯМР (CDCl3)8,33-8,26 (2 Н, м) , 8,05-7,99 (3 Н, м), 7,39 (2 Н, д, J = 8,4 Гц),7,20-7,15 (4 Н, м), 5,15 (1 Н, кв, J = 7,3 Гц), 3,90 (3 Н, с), 1,92 (2 Н, дкз, J = 7,3, 7,3 Гц), 0,95 (3 Н, т, J = 7,3 Гц); МС (ESI) m/z 427 (М + Н)+, 425 (М - Н)-. Стадия 2. 4-[1-([5-Фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)пропил]бензойная кислота. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 4 примера 1, из метил 4-[1-([5-фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)пропил]бензоата Стадия 1. Метил 4-[1-([5-Фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)-1-метилэтил] бензоат. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 3 примера 1, из 5-фтор-2-(4-фторфенокси)никотиновой кислоты (стадия 3 примера 1) и метил 4-(1-амино 1-метилэтил)бензоата: 1 Н-ЯМР (CDCl3)8,33 (1 Н, шир.с), 8,24 (1 Н, дд, J = 8,2, 3,1 Гц), 8,04-7,99 (3 Н, м),7,51 (2 Н, дд, J = 6,7, 1,9 Гц), 7,18-7,16 (4 Н, м) , 3,90 (3 Н, с), 1,80 (6 Н, с); МС (ESI) m/z 427 (М + Н)+, 425(М - Н)-. Стадия 2. 4-[1-([5-Фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)-1-метилэтил]бензойная кислота. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 4 примера 1, из метил 4-[1-([5-фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)-1-метилэтил] бензоата (стадия 1): 1 Н-ЯМР (ДМСО-d6)8,82 (1 Н, с), 8,23 (1 Н, д, J = 3,1 Гц), 8,00 (1 Н, дд, J = 7,9, 3,1 Гц),7,83 (2 Н, д, J = 8,4 Гц), 7,57 (2 Н, д, J = 8,4 Гц), 7,29-7,27 (4 Н, м) , 1,65 (6 Н, с); МС (ESI) m/z 413 (М + Н)+,411 (М - Н)-. ПРИМЕР 5. 4-[(1S)-1-([5-ФТОР-2-(4-ФТОРФЕНОКСИ)ПИРИДИН-3-ИЛ]КАРБОНИЛАМИНО) ЭТИЛ]БЕНЗОЙНАЯ КИСЛОТА- 29009201 Стадия 1. трет-Бутил [(1S)-1-(4-бромфенил)этил]карбамат. Смесь [(1S)-1-(4-бромфенил)этил]амина (10,00 г, 50,0 ммоль) и ди-трет-бутилбикарбоната (11,45 г,52,5 ммоль), триэтиламина (7,66 мл, 55,0 ммоль) в дихлорметане (200 мл) перемешивали при комнатной температуре в течение 1 ч. Смесь разбавляли дихлорметаном (500 мл) и промывали 1 н. соляной кислотой(300 мл), насыщенным водным бикарбонатом натрия (300 мл) и насыщенным раствором соли (300 мл). Органический слой сушили над сульфатом магния и концентрировали при пониженном давлении. Остаток промывали холодным гексаном с получением 14,73 г (98%) указанного в заголовке соединения в виде твердых веществ белого цвета: 1H-ЯМР (CDCl3)7,47-7,42 (2 Н, м) , 7,18 (2 Н, д, J = 8,4 Гц), 5,30 (2 Н,шир.с), 1,41 (12 Н, шир.с). Стадия 2. Метил 4-(1S)-1-[(трет-бутоксикарбонил)амино]этилбензоат. Смесь трет-бутил [(1S)-1-(4-бромфенил)этил]карбамата (стадия 1, 14,73 г, 49,1 ммоль), 1,3 бис(дифенилфосфино)пропана (2,03 г, 4,91 ммоль), ацетата палладия(II) (1,10 г, 4,91 ммоль), триэтиламина (20,5 мл, 147 ммоль), N,N-диметилформамида (120 мл) и метанол (180 мл) перемешивали при 80 С в течение 16 ч в атмосфере моноксида углерода. После охлаждения до комнатной температуры, смесь разбавляли простым эфиром (800 мл) и промывали водой (500 мл х 3). Органический слой сушили над сульфатом магния и выпаривали. Остаток очищали колоночной флеш-хроматографией на силикагеле,элюируя гексаном/этилацетатом (5:1) с получением 12,83 г (94%) указанного в заголовке соединения в виде белого твердого вещества: 1H-ЯМР (CDCl3)8,02-7,99 (2 Н, м), 7,37 (2 Н, д, J = 8,4 Гц), 4,83 (2 Н,шир.с), 3,91 (3 Н, с), 1,46-1,42 (12 Н, м). Стадия 3. Гидрохлорид метил 4-[(1S)-1-аминоэтил]бензоата. Метил 4-(1S)-1-[(трет-бутоксикарбониламино]этилбензоат (12,83 г, 45,9 ммоль) обрабатывали трифторуксусной кислотой (100 мл) и дихлорметаном (100 мл) при комнатной температуре в течение 16 ч. После удаления растворителя остаток разбавляли 10% раствором хлороводорода в метаноле (100 мл) . Смесь концентрировали при пониженном давлении, и остаток промывали этилацетатом с получением 9,40 г (95%) указанного в заголовке соединения в виде белого твердого вещества: 1 Н-ЯМР (ДМСО-d6)8,67 (2 Н, шир.с), 8,01 (2 Н, д, J = 8,4 Гц), 7,68 (2 Н, д, J = 8,4 Гц), 4,49 (1 Н, кв, J = 6,9 Гц), 3,87 (3 Н, с), 1,53(3 Н, д, J = 6,9 Гц). Стадия 4. Метил 4-[(1S)-1-([5-фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)этил]бензоат. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 3 примера 1, из 5-фтор-2-(4-фторфенокси)никотиновой кислоты (стадия 3 примера 1) и гидрохлорида метил 4- [ (1S)-1-аминоэтил]бензоата (стадия 3): 1 Н-ЯМР (CDCl3) -данные указанного в заголовке соединения были идентичны данным, полученным для рацемата (стадия 2 примера 2); МС (ESI) m/z 413 (М + Н)+, 411 (М - Н)-. Стадия 5. 4-[(1S)-1-([5-Фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойная кислота. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 4 примера 1, из метил 4-[(1S)-l-([5-фтор-2-(4-фторфенокси)пиридин-3-ил]карбониламино)этил]бензоата(стадия 4): 1 Н-ЯМР (ДМСО-d6)-данные указанного в заголовке соединения были идентичны данным,полученным для рацемата (стадия 3 примера 2); МС (ESI) m/z 399 (М + Н)+, 397 (М-Н)-. ПРИМЕР 6. 4-[(1S)-1-([5-ФТОР-2-(3-ФТОРФЕНОКСИ)ПИРИДИН-3-ИЛ]КАРБОНИЛАМИНО) ЭТИЛ]БЕНЗОЙНАЯ КИСЛОТА Стадия 1. 5-Фтор-2-(3-фторфенокси)никотиновая кислота. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 1 и 2 примера 1, из 2-гидрокси-5-фторникотиновой кислоты и 3-фторфенола; 1 Н-ЯМР (ДМСО-d6)8,37 (1 Н,м), 8,23-8,15 (1 Н, м), 7,49-7,35 (1 Н, м), 7,10-6,90 (3 Н, м). Стадия 2. Метил 4-[(1S)-1-([5-фтор-2-(3-фторфенокси)пиридин-3-ил]карбониламино)этил] бензоат. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 3 примера 1, из 5-фтор-2-(3-фторфенокси)никотиновой кислоты (стадия 1) и гидрохлорида метил 4-[(1S)-1 аминоэтил]бензоата (стадия 3 примера 5): 1 Н-ЯМР (CDCl3)8,33 (1 Н, дд, J = 8,2, 3,1 Гц), 8,12-7,98 (4 Н,м), 7,47-7,38 (3 Н, м), 7,05-6,89 (3 Н, м), 5,36 (1 Н, м), 3,90 (3 Н, с), 1,60 (3 Н, Д, J = 6,9 Гц). Стадия 3. 4-[(1S)-1-([5-Фтор-2-(3-фторфенокси)пиридин-3-ил]карбониламино)этил]бензойная кислота. Указанное в заголовке соединение получали в соответствии с процедурой, описанной в стадии 4 примера 1, из метил 4-[(1S)-l-([5-фтор-2-(3-фторфенокси)пиридин-3-ил]карбониламино)этил]бензоата
МПК / Метки
МПК: C07C 235/60, C07D 213/64, C07D 213/82, C07C 233/87, C07D 401/12, C07D 257/04, C07D 213/65, C07D 417/12, A61K 31/166, A61K 31/44, A61K 31/444
Метки: пиридиламидные, соединения, фенил, простагландина, качестве, антагонистов
Код ссылки
<a href="https://eas.patents.su/30-9201-fenil-ili-piridilamidnye-soedineniya-v-kachestve-antagonistov-prostaglandina-e2.html" rel="bookmark" title="База патентов Евразийского Союза">Фенил – или пиридиламидные соединения в качестве антагонистов простагландина е2</a>
Предыдущий патент: Восстановительное аммиачное выщелачивание никель- и кобальтсодержащих материалов
Следующий патент: Устройство для приготовления гомеопатических продуктов
Случайный патент: Новые производные бензоилмочевины