Соединения пиперазинилпиразинов в качестве антагонистов серотонин 5-ht2 рецептора
Формула / Реферат
1. Соединение общей формулы (I)
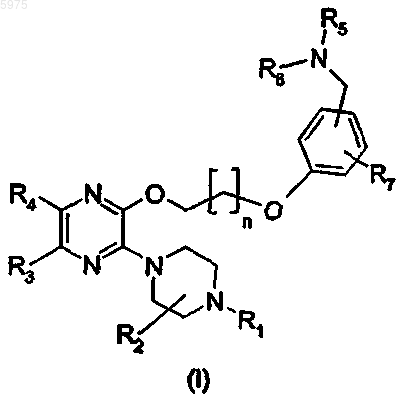
в которой R1 является водородом, C1-C4-алкилом, C3-C4-алкенилом, C1-C4-ацилом, C1-C4-алкоксикарбонилом, 2-гидроксиэтилом, 2-цианоэтилом, тетрагидропиран-2-илом или группой, защищающей азот;
R2 является водородом, C1-C4-алкилом, гидроксиметилом, C1-C4-алкоксиметилом или фторметилом;
R3 и R4, каждый независимо, являются водородом, метилом, C1-C4-алкилом, арилом, гетероарилом, где арильные и гетероарильные остатки, в свою очередь, могут быть замещены в одном или более положениях независимо друг от друга галогеном, C1-C4-алкилом, C1-C4-алкокси, C1-C4-алкилтио, C1-C4-алкилсульфонилом, метансульфонамидо, ацетилом, нитро, циано, гидрокси, трифторметилом, трифторметокси, трифторметилтио, амино, метиламино, диметиламино или ацетамидо; или
R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют 5- или 6-членное ароматическое или гетероароматическое кольцо, которое необязательно независимо замещено в одном или более положениях галогеном, метилом, метокси, метилтио, метилсульфонилом, нитро, циано, гидрокси, трифторметилом, трифторметилтио, амино, метиламино, диметиламино или ацетамидо;
R5 и R6 независимо друг от друга являются водородом, C1-C4-алкокси-C2-C4-алкилом, гидрокси-C2-C4-алкилом, C1-C6-алкилом, C2-C6-ацилом, арилом, гетероарилом, арил-C1-C2-алкилом, гетероарил-C1-C2-алкилом, арил-C1-C2-ацилом, гетероарил-C1-C2-ацилом, и где любой арил или гетероарил, один или в составе другой группы, может быть независимо замещен в одном или более положениях C1-C4-алкилом, C1-C4-алкокси, C1-C4-алкилтио, C2-C4-ацилом, C1-C4-алкилсульфонилом, циано, нитро, гидрокси, C2-C3-алкенилом, C2-C3-алкинилом, фторметилом, трифторметилом, трифторметокси, галогеном, диметиламино или метиламино; или
R5 и R6 вместе с атомом азота, к которому они присоединены, образуют насыщенное гетероциклическое кольцо, имеющее 4-7 членов в кольце, где данное кольцо может содержать дополнительный гетероатом, который может быть замещен метилом, оксо или гидрокси;
R7 является водородом или заместителем, выбранным из галогена, метила, метокси и этокси; и
n = 1-3;
и их фармацевтически приемлемые соли, гидраты, геометрические изомеры, таутомеры, оптические изомеры, N-оксиды и пролекарства.
2. Соединение по п.1, в котором R1 является водородом или метилом.
3. Соединение по п.2, в котором R1 является водородом.
4. Соединение по любому из пп.1-3, в котором R2 является водородом или метилом.
5. Соединение по любому из пп.1-4, в котором R3 и R4 независимо являются водородом, галогеном или метилом или в котором R3 и R4 образуют кольцо вместе с атомами углерода, к которым они присоединены, и кольцо является бензолом с образованием хиноксалина или тиофеном для получения тиено[3,4-b]пиразина, и где, если кольца замещены, они являются моно- или дизамещенными.
6. Соединение по п.5, в котором R3 и R4 оба являются водородом.
7. Соединение по любому из пп.1-6, в котором R7 является водородом.
8. Соединение по п.7, в котором R7 является водородом и группа -CH2N(R5)(R6) присоединена в мета-положении.
9. Соединение по любому из пп.1-8, в котором R5 и R6 вместе с атомом азота, к которому они присоединены, образуют кольцо, выбранное из азетидина, пирролидина, пиперазина, гомопиперазина, морфолина, тиоморфолина и пиперидина.
10. Соединение по любому из пп.1-9, в котором n = 1.
11. Соединение по п.1, выбранное из
2-(1-пиперазинил)-3-{2-[3-(4-морфолинилметил)фенокси]этокси}пиразина;
2-(1-пиперазинил)-3-{2-[3-(1-пирролидинилметил)фенокси]этокси}пиразина;
2-(1-пиперазинил)-3-{2-[3-(4-метил-1-пиперазинилметил)фенокси]этокси}пиразина;
2-(1-пиперазинил)-3-{2-[(3-{(2-метоксиэтил)амино}метил)фенокси]этокси}пиразина и
2-(1-пиперазинил)-3-{2-[3-{(изопропиламино)метил}фенокси]этокси}пиразина
и их фармакологически приемлемых солей и сольватов.
12. Фармацевтическая композиция, содержащая соединение по любому из пп.1-11 в качестве активного ингредиента вместе с фармакологически и фармацевтически приемлемым носителем.
13. Способ профилактики или лечения связанных с серотонином заболеваний у человека или животного, где способ включает введение пациенту при необходимости эффективного количества соединения по любому из пп.1-11.
14. Способ по п.13, в котором указанным заболеванием является заболевание, связанное с 5-HT2c рецептором.
15. Способ по п.13 или 14, в котором указанное заболевание выбирают из расстройства питания, расстройства памяти, шизофрении, расстройства настроения, тревоги, боли, злоупотребления препаратами, половых расстройств, эпилепсии и расстройств мочеиспускания.
16. Способ по п.15, в котором расстройством питания является ожирение.
17. Применение соединения по любому из пп.1-11 в производстве лекарственного средства для профилактики или лечения связанных с серотонином заболеваний.
18. Применение по п.17, в котором указанным заболеванием является заболевание, связанное с 5-HT2c рецептором.
19. Применение по п.17 или 18, в котором указанное заболевание выбирают из расстройства питания, расстройства памяти, шизофрении, расстройства настроения, тревоги, боли, злоупотребления препаратами, половых расстройств, эпилепсии и расстройств мочеиспускания.
20. Применение по п.19, в котором расстройством питания является ожирение.
21. Способ модулирования функций 5-HT2c рецептора у человека или животного, включающий введение пациенту при необходимости эффективного количества соединения по любому из пп.1-11.
22. Способ получения соединения по п.1, включающий взаимодействие соединения формулы (II)
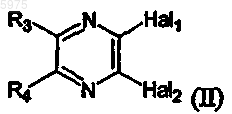
где R3 и R4 независимо друг от друга являются водородом, метилом, C1-C4-алкилом, арилом, гетероарилом, где арильные и гетероарильные остатки могут быть замещены в одном или более положениях независимо друг от друга галогеном, C1-C4-алкилом, C1-C4-алкокси, C1-C4-алкилтио, C1-C4-алкилсульфонилом, метансульфонамидо, ацетилом, нитро, циано, гидрокси, трифторметилом, трифторметокси, трифторметилтио, амино, метиламино, диметиламино или ацетамидо; или R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют 5- или 6-членное ароматическое или гетероароматическое кольцо, которое необязательно независимо замещено в одном или более положениях галогеном, метилом, метокси, метилтио, метилсульфонилом, нитро, циано, гидрокси, трифторметилом, трифторметилтио, амино, метиламино, диметиламино или ацетамидо; и каждый из Hal1 и Hal2 независимо является галогеном; с соединением формулы (III)
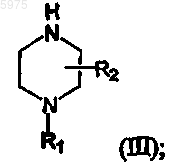
где R1 является водородом или C1-C4алкилом, C3-C4-алкенилом, C1-C4-ацилом, C1-C4-алкоксикарбонилом, 2-гидроксиэтилом, 2-цианоэтилюь, тетрагидропиран-2-илом или аминозащитной группой; и
R2 является водородом, C1-C4-алкилом, гидроксиметилом, C1-C4-алкоксиметилом или фторметилом;
с получением первого промежуточного соединения формулы (IV)
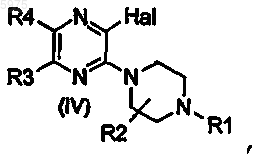
в котором Rl, R2, R3, R4 и Hal имеют значения, указанные выше, взаимодействие первого промежуточного соединения с соединением формулы (V)
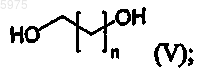
в котором n равно 1-3;
с получением второго промежуточного соединения (VI)
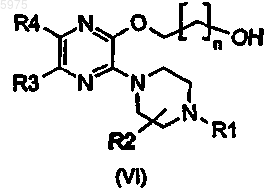
в котором Rl, R2, R3 и R4 имеют значения, указанные выше, взаимодействие второго промежуточного соединения с соединением формулы (VII)
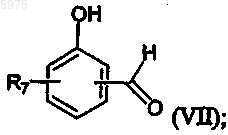
в котором R7 является водородом или заместителем, выбранным из галогена, метила, метокси и этокси;
с получением третьего промежуточного соединения (VIII)
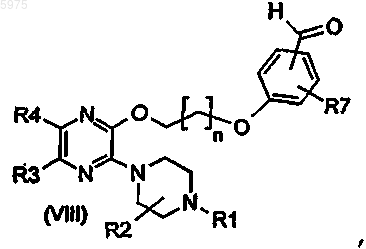
в котором Rl, R2, R3, R4 и R7 имеют значения, указанные выше, взаимодействие третьего промежуточного соединения с соединением формулы (IX)
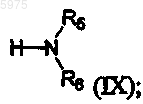
где R5 и R6 независимо друг от друга являются водородом, C1-C4-алкокси-C2-C4-алкилом, гидрокси-C2-C4-алкилом, C1-C6-алкилом, C2-C2-ацилом, арилом, гетероарилом, арил-C1-C2-алкилом, гетероарил-C1-C2-алкилом, арил-C1-C2-ацилом, гетероарил-C1-C2-ацилом и где любой арил или гетероарил, один или в составе другой группы, может быть независимо замещен в одном или более положениях C1-C4-алкилом, C1-C4-алкокси, C1-C4-алкилтио, C2-C4-ацилом, C1-C4-алкилсульфонилом, циано, нитро, гидрокси, C2-C3-алкенилом, C2-C3-алкинилом, фторметилом, трифторметилом, трифторметокси, галогеном, диметиламино или метиламино; или R5 и R6 вместе с атомом азота, к которому они присоединены, образуют насыщенное гетероциклическое кольцо, имеющее 4-7 членов в кольце, где данное кольцо может содержать дополнительный гетероатом, который может быть замещен метилом, оксо или гидрокси;
с получением соединения по п.1.
23. Способ по п.22, в котором R1 является водородом или метилом.
24. Способ по п.22, в котором R2 является водородом или метилом.
25. Способ по п.22, в котором R3 и R4 оба являются водородом.
26. Способ по п.22, в котором R5 и R6 вместе с атомом азота, к которому они присоединены, образуют кольцо, выбранное из азетидина, пирролидина, пиперазина, гомопиперазина, морфолина, тиоморфолина или пиперидина.
Текст
005975 Область техники Данное изобретение относится к новым соединениям, фармацевтическим композициям, содержащим соединения, способам их получения, а также к применению соединения для получения лекарственных средств, которые воздействуют особенно на центральную нервную систему. Уровень техники На многие заболевания центральной нервной системы влияют адренергические, допаминергические и серотонергические нейротрансмиттерные системы. Например, серотонин вовлечен во многие заболевания и состояния, которые зарождаются в центральной нервной системе. Несколько фармакологических и генетических экспериментов, включающих рецепторы серотонина, в значительной степени вовлекают подтип 5-НТ 2 с рецептора в регулирование поглощения пищи (Obes. Res. 1995, 3, Suppl. 4, 449+S-462S). Подтип 5-НТ 2 с рецептора транскрибируется и экспрессируется в структурах гипоталамуса, связанных с регулированием аппетита. Было показано, что агонист 5-НТ 2 с рецептора м-хлорфенилпиперазин (мХФП),который имеет некоторое предпочтение по отношению к 5-НТ 2c рецептору, снижает поглощение пищи у мышей, которые экспрессируют нормальный 5-НТ 2 с рецептор, в то время как это соединение теряет активность у мышей, экспрессирующих мутированную неактивную форму 5-НТ 2 с рецептора (Nature 1995,374, 542-546). В недавно описанных клинических экспериментах незначительное, но постоянное снижение массы тела получили через 2 недели лечения мХФП пациентов с ожирением (Psychopharmacology 1997, 133, 309-312). Недавно несколько производных пирроло[3,2,1-ij]хинолина были идентифицированы как агонисты 5-НТ 2c рецептора, селективные в отношении 5-НТ 2A рецептора (Isaac M., et al., Bioorg. Med.Chem. Lett. 2000, 10, 919-921). Было описано, что соединения обеспечивают новый подход к лечению ожирения и эпилепсии. Снижение веса также было описано в клинических исследованиях с применением других серотонергических агентов (см., например, IDrugs 1998, 1, 456-470). Например, ингибитор повторного поглощения 5-НТ флуоксетин и агент высвобождения/ингибитор повторного поглощения 5-НТ дексфенфлурамин дают снижение веса в контролируемых экспериментах. Однако оказывается, что доступные в настоящее время лекарственные средства, которые повышают серотонергическую трансмиссию, оказывают только умеренное и, в некоторых случаях, кратковременное действие на массу тела. Полагают, что подтип 5-НТ 2 с рецептора также вовлечен в расстройства ЦНС, такие как депрессия и тревога (Exp. Opin. Invest. Drugs 1998, 7, 1587-1599; IDrugs 1999, 2, 109-120). Также полагают, что подтип 5-НТ 2 с рецептора вовлечен в расстройства мочеиспускания, такие как недержание мочи (IDrugs 1999, 2, 109-120). Соединения, которые оказывают селективное действие на 5-НТ 2 с рецептор, могут иметь терапевтический потенциал в лечении расстройств, указанных выше. Конечно, селективность также снижает потенциальные побочные эффекты, медиированные другими рецепторами серотонина. Известный уровень техники В US-A-3253989 описано применение мХФП в качестве агента, снижающего аппетит. В ЕР-А 1-863136 описаны производные азетидина и пирролидина, которые являются селективными агонистами 5-НТ 2 с рецептора, обладающими антидепрессивным действием, и которые могут применяться для лечения или профилактики связанных с серотонином заболеваний, включая расстройства питания и тревогу. В ЕР-А-657426 описаны трициклические производные пиррола, обладающие действием на 5-НТ 2 с рецептор, которые, кроме того, могут применяться для лечения расстройств питания. В ЕР-А-655440 описаны 1-аминоэтилиндолы, обладающие действием на 5-НТ 2 с рецептор, которые могут применяться для лечения расстройств питания. В ЕР-А-572863 описаны пиразиноиндолы, обладающие действием на 5-НТ 2c рецептор, которые могут применяться для лечения расстройств питания. В J. Med. Chem. 1978, 21, 536-542 и US-A-4081542 описан ряд пиперазинилпиразинов, имеющих центральное серотонинмиметическое действие. В J. Med. Chem. 1981, 24, 93-101 описан ряд пиперазинилхиноксалинов, имеющих центральное серотонинмиметическое действие. В WO 00/12475 описаны производные индолина в качестве лигандов 5-НТ 2b рецептора и/или 5-НТ 2 с рецептора, особенно для лечения ожирения. В WO 00/12510 описаны пирролоиндолы, пиридоиндолы и азепиноиндолы в качестве агонистов 5 НТ 2 с рецептора, особенно для лечения ожирения. В WO 00/12482 описаны производные индазола в качестве селективных, обладающих прямым действием лигандов 5-НТ 2c рецептора, предпочтительно агонистов 5-НТ 2c рецептора, особенно для применения в качестве агентов против ожирения. В WO 00/12502 описаны пирролохинолины в качестве агонистов 5-НТ 2c рецептора, особенно для применения в качестве агентов против ожирения. В WO 00/35922 описаны 2,3,4,4 а-тетрагидро-1 Н-пиразино[1,2-а]хиноксалин-5(6 Н)оны в качестве агонистов 5-НТ 2 с рецептора, которые могут применяться для лечения ожирения. В WO 00/44737 описаны аминоалкилбензофураны в качестве агонистов 5-НТ 2c рецептора, которые-1 005975 могут применяться для лечения ожирения. Другие соединения, описанные как агонисты 5-НТ 2 с рецептора, включают, например, индазолилпропиламины, такие как описаны в WO 00/12481; индазолы, такие как описаны в WO 00/17170; пиперазинилпиразины, такие как описаны в WO 00/76984; конденсированные с гетероциклом -карболины, такие как описаны в WO 00/77001, WO 00/77002 и WO 00/77010; бензофурилпиперазины, такие как описаны в WO 01/09111 и WO 01/09123; бензофураны, такие как описаны в WO 01/09122; бензотиофены, такие как описаны в 01/09126; аминоалкилиндазолы, такие как описаны в WO 98/30548; индолы, такие как описаны в WO 01/12603; индолины, такие как описаны в WO 01/12602; пиразино(аза)индолы, такие как описаны в WO 00/44753 и трициклические пирролы или пиразолы, такие как описаны в WO 98/56768. В GB-B-1457005 описаны производные 1-пиперазинил-2-[2-(фенил)этенил]хиноксалина, которые обладают противовоспалительным действием. В Chem. Pharm. Bull. 1993, 41(10) 1832-1841 описаны антагонисты 5-НТ 3, включающие 2-(4-метил 1-пиперазинил)-4-феноксихиноксалин. В GB-B-1440722 описаны производные 2-(1'-пиперазинил)хиноксалина, обладающие фармацевтическим действием против депрессии. В WO 96/11920 описаны ЦНС-активные производные пиридинилмочевины. В WO 95/01976 описаны производные индолина в качестве антагонистов 5-НТ 2c и имеющие потенциальное применение в лечении расстройств ЦНС. В WO 97/14689 описаны производные арилпиперазин циклического амина, которые являются селективными антагонистами 5-HT1d рецептора. В WO 98/42692 описаны пиперазины, полученные из циклических аминов, которые являются селективными антагонистами человеческих 5-HT1a, 5-НТ 1d и 5-HT1b рецепторов. В GB-B-1465946 описаны замещенные соединения пиридазинила, пиримидинила и пиридила, которые являются активными в качестве агентов, блокирующих -рецептор. В ЕР-А-711757 описаны производные [3-(4-фенилпиперазин-1-ил)пропиламино]пиридина, пиримидина и бензола в качестве антагонистов -адреноцептора. В WO 99/03833 описаны производные арилпиперазина, которые являются антагонистами 5-НТ 2 рецептора и агонистами 5-HT1a рецептора и, следовательно, могут применяться в качестве лекарственных средств или профилактических средств при психоневрозе. В WO 96/02525 описаны полученные из арилпиперазина производные пиперазида, обладающие антагонистическим действием по отношению к 5-НТ рецептору. В WO 99/58490 описаны арилгидронафталиналканамины, которые могут влиять на частичную или полную блокаду серотонергических 5-НТ 2 с рецепторов в организме. Объект изобретения Объектом данного изобретения являются новые соединения. Другим объектом данного изобретения является фармацевтическая композиция, содержащая соединения для применения в терапии в качестве активного ингредиента. Наконец, объектом данного изобретения является способ лечения или профилактики связанных с серотонином заболеваний, особенно заболеваний, связанных с 5-НТ 2c рецептором. Краткое описание изобретения В соответствии с данным изобретением представлены новые соединения общей формулы (I)R3 и R4, каждый независимо, являются водородом, метилом, С 1-С 4-алкилом, арилом, гетероарилом,где арильные и гетероарильные остатки, в свою очередь, могут быть замещены в одном или более положениях независимо друг от друга галогеном, С 1-С 4-алкилом, С 1-С 4-алкокси, С 1-С 4-алкилтио, C1-C4 алкилсульфонилом, метансульфонамидо, ацетилом, нитро, циано, гидрокси, трифторметилом, трифторметокси, трифторметилтио, амино, метиламино, диметиламино или ацетамидо; илиR3 и R4 вместе с атомами углерода, к которым они присоединены, образуют 5- или 6-членное аро-2 005975 матическое или гетероароматическое кольцо, которое необязательно независимо замещено в одном или более положениях галогеном, метилом, метокси, метилтио, метилсульфонилом, нитро, циано, гидрокси,трифторметилом, трифторметилтио, амино, метиламино, диметиламино или ацетамидо;R5 и R6 независимо друг от друга являются водородом, C1-C4-алкокси-С 2-С 4-алкилом, гидрокси-С 2 С 4-алкилом, C1-С 6-алкилом, С 2-С 6-ацилом, арилом, гетероарилом, арил-С 1-С 2-алкилом, гетероарил-C1-С 2 алкилом, арил-С 1-С 2-ацилом, гетероарил-С 1-С 2-ацилом, и где любой арил или гетероарил, один или в составе другой группы, может быть независимо замещен в одном или более положениях C1-С 4-алкилом,С 1-С 4-алкокси, C1-C4-алкилтио, С 2-С 4-ацилом, C1-C4-алкилсульфонилом, циано, нитро, гидрокси, С 2-С 3 алкенилом, С 2-С 3-алкинилом, фторметилом, трифторметилом, трифторметокси, галогеном, диметиламино или метиламино; илиR5 и R6 вместе с атомом азота, к которому они присоединены, образуют насыщенное гетероциклическое кольцо, имеющее 4-7 членов в кольце, где данное кольцо может содержать дополнительный гетероатом, и которое может быть замещено метилом, оксо или гидрокси;R7 является водородом или заместителем, выбранным из галогена, метила, метокси и этокси; иn = 1-3; и их фармацевтически приемлемые соли, гидраты, геометрические изомеры, таутомеры, оптические изомеры, N-оксиды и пролекарства. Если соединения формулы (I) могут существовать в виде оптических изомеров, данное изобретение включает рацемические смеси, а также отдельные энантиомеры как таковые. Если соединения формулы (I) содержат группы, которые могут существовать в таутомерных формах, данное изобретение включают таутомерные формы соединений, а также их смеси. Если соединения формулы (I) могут существовать в виде геометрических изомеров, данное изобретение включает геометрические изомеры, а также их смеси. В другом аспекте данное изобретение представляет способ получения соединения в соответствии с данным изобретением. Способ включает превращение соединения формулы (II) в указанное выше соединение. В формуле (II) R3 и R4 независимо друг от друга являются водородом, метилом, С 1-С 4-алкилом,арилом, гетероарилом, где арильные и гетероарильные остатки могут быть замещены в одном или более положениях независимо друг от друга галогеном, C1-C4-алкилом, С 1-С 4-алкокси, С 1-С 4-алкилтио, С 1-С 4 алкилсульфонилом, метансульфонамидо, ацетилом, нитро, циано, гидрокси, трифторметилом, трифторметокси, трифторметилтио, амино, метиламино, диметиламино или ацетамидо; илиR3 и R4 вместе с атомами углерода, к которым они присоединены, образуют 5- или 6-членное ароматическое или гетероароматическое кольцо, которое необязательно независимо замещено в одном или более положениях галогеном, метилом, метокси, метилтио, метилсульфонилом, нитро, циано, гидрокси,трифторметилом, трифторметилтио, амино, метиламино, диметиламино или ацетамидо; и каждый из Hal1 и На 12 независимо является галогеном. В другом аспекте данное изобретение представляет соединения формулы (I) для применения в терапии. В еще одном аспекте данного изобретения представлена фармацевтическая композиция, содержащая соединения формулы (I) в качестве активного ингредиента, предпочтительно вместе с фармацевтически приемлемым носителем и, при желании, другими фармакологически активными агентами. В еще одном аспекте данное изобретение представляет способ лечения человека или животного,страдающего связанным с серотонином расстройством, особенно связанным с 5-НТ 2c рецептором, особенно расстройством питания, особенно ожирением; расстройством памяти, шизофренией, расстройствами настроения, тревогой, болью, злоупотреблением препаратами, половыми расстройствами, эпилепсией и расстройствами мочеиспускания. Другим аспектом данного изобретения является применение соединений формулы (I) для получения лекарственного средства для лечения связанного с серотонином заболевания, особенно связанного с 5-НТ 2c рецептором, особенно расстройства питания, особенно ожирения; расстройства памяти, шизофрении, расстройств настроения, тревоги, боли, злоупотребления лекарственными средствами, половых расстройств, эпилепсии и расстройств мочеиспускания. Наконец, аспектом данного изобретения является способ модулирования функции 5-НТ 2c рецептора. Подробное описание изобретения Согласно данному изобретению разработан класс новых соединений, которые связываются с 5-НТ 2c рецептором (агонисты и антагонисты) и которые поэтому могут применяться для лечения связанных с серотонином заболеваний. Сначала объясняются различные термины, применяемые отдельно или в сочетании в указанных-3 005975 выше определениях соединений, имеющих общую формулу (I). Под гетероатомом понимают азот, кислород, серу и в гетероароматических кольцах также селен. Термин арил включает фенил, 1-нафтил и 2-нафтил. Термин гетероарил включает пяти- и шестичленные гетероароматические кольца, такие как пиррол, имидазол, тиофен, фуран, селенофен, тиазол, изотиазол, тиадиазол, оксазол, изоксазол, оксадиазол,пиридин, пиразин, пиримидин, пиридазин, пиразол, триазол и тетразол.C1-С 6-алкилом, который может быть прямым или разветвленным, предпочтительно является С 1-С 4 алкил. Примеры алкильных групп включают метил, этил, пропил, изопропил, бутил, втор-бутил, третбутил, пентил, изопентил, гексил и изогексил. С 1-С 4-алкокси может быть прямым или разветвленным. Примеры алкоксигрупп включают метокси,этокси, пропокси, изопропокси, бутокси, втор-бутокси и трет-бутокси. С 2-С 4-алкенил может быть прямым или разветвленным. Примеры алкенильных групп включают винил, 2-пропенил и 1-метил-2-пропенил. С 1-С 4-алкокси-С 2-С 4-алкил может быть прямым или разветвленным. Примеры групп включают 2(метокси)этил, 3-метокси-1-пропил, 4-этокси-1-бутил и подобные. Примеры арил-С 1-С 2-ацила включают бензоил и фенилацетил. Примеры гетероарил-С 1-С 2-ацила включают никотиноил и 3-пиридинилацетил и подобные. С 2-С 4-ацил может быть насыщенным или ненасыщенным. Примеры ацильных групп включают ацетил, пропионил, бутирил, изобутирил и бутеноил (например, 3-бутеноил). Галоген включает фтор, хлор и бром. Там, где выше указано, что арильные и гетероарильные остатки могут быть замещены, это относится как к арилу и гетероарилу как таковому, так и к любым объединенным группам, содержащим арильные или гетероарильные остатки, таким как гетероарил-С 1-С 2-алкил и арил-С 1-С 2-ацил. Термин N-оксиды означает, что один или более атомов азота, если присутствует в соединении,имеет форму N-оксида (N10). Термин пролекарства означает фармакологически приемлемое производное, такое как сложный эфир или амид, где такое производное биотрансформируется в организме с образованием активного лекарства. Ссылка дана по Goodman and Gilman's, the Pharmacological basis of Therapeutics, 8th ed., McGrawHill, Int. Ed. 1992, "Biotransformation of Drugs", p. 13-15. Фармацевтически приемлемое означает, что соединение может применяться для получения фармацевтических композиций, которые в основном безопасны, не токсичны и не являются нежелательными ни биологически, ни каким-либо другим образом и могут применяться как в ветеринарии, так и в медицине. Фармацевтически приемлемая соль относится к соли, которая является фармацевтически приемлемой и которая обладает желаемым фармакологическим действием. Такие соли включают кислотноаддитивные соли, полученные с органическими и неорганическими кислотами, такими как хлороводород, бромоводород, йодоводород, серная кислота, фосфорная кислота, уксусная кислота, гликолевая кислота, малеиновая кислота, малоновая кислота, щавелевая кислота, толуолсульфокислота, метансульфокислота, фумаровая кислота, янтарная кислота, винная кислота, лимонная кислота, бензойная кислота,аскорбиновая кислота и подобные.R1 предпочтительно является водородом или метилом. Наиболее предпочтительно R1 является водородом.R1 также может служить в качестве группы, защищающей азот, и тогда R1 является третбутоксикарбонил (трет-БОК), бензилом или тритилом.R2 предпочтительно является водородом или метилом (особенно в положении 2 пиперазинового кольца).R3 и R4 предпочтительно (независимо) являются водородом, галогеном или метилом. Если R3 и R4 образуют кольцо вместе с атомами углерода, к которым они присоединены, такое кольцо предпочтительно является бензолом (для получения хиноксалина) или тиофеном (для получения тиено[3,4b]пиразина). Если они замещены, кольца предпочтительно являются моно- или дизамещенными, предпочтительно галогеном или метилом. Если R7 отличен от водорода, он может занимать любое доступное положение фенильного кольца. Группа -CH2N(R5)(R6) может быть присоединена в орто-, мета- или пара-положении по отношению к боковой цепи алкилендиокси, или фенильному кольцу, предпочтительно, в мета-положении.n в формуле (I) равно 1-3, где n представляет собой количество метиленовых групп, n предпочтительно равно 1, что означает, что два атома кислорода в формуле (I) разделены между собой -СН 2 СН 2 группой; Предпочтительными соединениями формулы (I) являются 2-(1-пиперазинил)-3-2-[3-(4-морфолинилметил)фенокси]этоксипиразин; 2-(1-пиперазинил)-3-2-[3-(1-пирролидинилметил)фенокси]этоксипиразин; 2-(1-пиперазинил)-3-2-[3-(4-метил-1-пиперазинилметил)фенокси]этоксипиразин; 2-(1-пиперазинил)-3-2-[3-(2-метоксиэтил)аминометил)фенокси]этоксипиразин;-4 005975 2-(1-пиперазинил)-3-2-[3-(изопропиламино)метилфенокси]этоксипиразин,и их фармацевтически приемлемые соли и сольваты. В другом аспекте данное изобретение относится к соединениям любой из представленных здесь формул и их применению, описанному выше, в которых R5 и R6 вместе с атомом азота, к которому они присоединены, образуют насыщенное гетероциклическое кольцо, имеющее 4-7 членов в кольце, и которое может содержать дополнительный гетероатом. Примеры колец включают азетидин, пирролидин,пиперазин, гомопиперазин, морфолин, тиоморфолин или пиперидин. Насыщенное гетероциклическое кольцо может быть замещено метилом, оксо или гидрокси. Как отмечено выше, соединения в соответствии с данным изобретением применяют для лечения(включая профилактику) связанных с серотонином расстройств, особенно связанных с 5-НТ 2c рецептором, у человека или животного (включая, например, домашних животных), таких как расстройства питания, особенно ожирение; расстройства памяти, такие как болезнь Альцгеймера; шизофрения; расстройства настроения, включая, но не ограничиваясь ими, общую депрессию и биполярную депрессию, включая как легкое, так и маниакальное биполярное расстройство, сезонное аффективное расстройство (САР); тревогу, включая ситуационную тревогу, общую тревогу, первичную тревогу (паническое состояние,фобии, навязчиво-компульсивные расстройства и посттравматический стресс), и вторичную тревогу (например, тревогу, связанную со злоупотреблением препаратами); боль; злоупотребление препаратами; половые расстройства; эпилепсия и расстройства мочеиспускания, такие как недержание мочи. Соединения в соответствии с данным изобретением в форме, меченной радиоактивными изотопами,могут применяться в качестве диагностических агентов. Соединения общей формулы (I) также могут быть получены способом в соответствии с данным изобретением, или аналогично, обычным способом. Данное изобретение относится к способам получения соединений любой представленной здесь формулы, включающим взаимодействие любого одного или более соединений или формул, представленных здесь, включая любые процессы, описанные здесь. Например, как показано на схеме 1, соединение формулы (I) может быть получено сначала обработкой соединения формулы (II), где Hal является галогеном и R3 и R4 такие, как определены выше, подходящим пиперазином формулы (III), где R1 и R2 имеют такие же значения, как и в формуле (I) , и где R1 может быть подходящей аминозащитной группой, такой как тритил, бензил или трет-бутоксикарбонил, с получением соединения формулы (IV). Реакцию проводят в растворителе, таком как ацетонитрил, диоксан, тетрагидрофуран (ТГФ), н-бутанол, N,N-диметилформамид (ДМФ) или смеси растворителей, такой как ДМФ/диоксан, необязательно в присутствии основания, такого как K2 СО 3, Na2CO3, Cs2CO3, NaOH,триэтиламин, пиридин или подобные, при температуре от 0 до 200 С в течение от 1 до 24 ч. Соединение формулы (IV) подвергают взаимодействию с диолом формулы (V), в котором n имеет такое же значение, как в формуле (I), с получением промежуточного соединения (VI). Реакцию проводят в растворителе, таком как диоксан, ТГФ, ДМФ или пиридин и подобные, в присутствии основания, такого как K-трет-ВuО, Na-трет-ВuО, NaH или подобные, при температуре от 0 до 150 С в течение от 1 до 24 ч. Промежуточное соединение (VI) подвергают взаимодействию с гидроксибензальдегидным соединением формулы (VII), в котором R7 имеет такое же значение, как в формуле (I), с получением промежуточного альдегида (VIII). Реакцию проводят в присутствии диэтилазодикарбоксилата (ДЭАД) или 1,1'азобис(N,N-диметилформамида) (см. Tetrahedron Lett. 1995, 36, 3789-3792), предпочтительно ДЭАД, и трифенилфосфина (РРh3) в растворителе, таком как ТГФ или дихлорметан (реакция Мицуноби; см. Org.React. 1992, 42, 335-656). Стандартное восстановительное алкилирование промежуточного соединения (VIII) (такое как описано в J. Org. Chem. 1996, 61, 3849-3862) подходящим амином формулы (IX), где R5 и R6 имеют такие же значения, как в формуле (I), дает соединение в соответствии с данным изобретением (I). Если R1 в формуле (I) является группой, защищающей азот, такой как определена ниже, последующее снятие N-защиты может быть проведено в стандартных условиях, таких как описаны в ProtectiveGroups in Organic Synthesis, John WileySons, 1991, с получением соединений формулы (I), в которыхR1 является водородом. Группы, защищающие азот, известны в данной области техники и включают описанные в Т.W. Green and P.G.M. Wuts, Protective Groups in Organic Synthesis, 2nd Ed., John Wiley and Полученное соединение формулы (I) может быть превращено в другое соединение формулы (I) методами, хорошо известными в данной области техники. Описанные выше процессы могут проводиться с получением соединения в соответствии с данным изобретением в виде свободного основания или кислотно-аддитивной соли. Фармацевтически приемлемые кислотно-аддитивные соли могут быть получены растворением свободного основания в подходящем органическом растворителе, таком как простой эфир или смесь простого эфира и метанола, и обработкой раствора кислотой, согласно обычным методам получения кислотно-аддитивных солей из основных соединений. Примеры кислот, образующих кислотно-аддитивные соли, включают малеиновую кислоту, фумаровую кислоту, янтарную кислоту, метансульфокислоту, уксусную кислоту, щавелевую кислоту, бензойную кислоту, хлористо-водородную кислоту, серную кислоту,фосфорную кислоту и подобные. Соединения формулы (I) могут иметь один или более хиральных атомов углерода, и поэтому они могут быть получены в виде оптических изомеров, например, в виде чистого энантиомера, или в виде смеси энантиомеров (рацемат) или в виде смеси, содержащей диастереомеры. Разделение смесей оптических изомеров для получения чистых энантиомеров хорошо известно в данной области техники и может,например, быть достигнуто фракционной кристаллизацией солей с оптически активными (хиральными) кислотами или хроматографическим разделением на хиральных колонках. В соответствии с данным изобретением соединения формулы (I) в виде свободных оснований или солей с физиологически приемлемыми кислотами могут быть добавлены в подходящие галеновые формы, такие как композиции для перорального применения, для инъекций, для введения в виде назального спрея или подобные, в соответствии с принятыми фармацевтическими методами. Такие фармацевтические композиции в соответствии с данным изобретением включают эффективное количество соединений формулы (I) в сочетании с совместимыми фармацевтически приемлемыми носителями или разбавителями, которые хорошо известны в данной области техники. Носители могут быть инертными материалами,органическими или неорганическими, подходящими для энтерального, чреcкожного, подкожного или парентерального введения, такими как вода, желатин, аравийская камедь, лактоза, микрокристаллическая целлюлоза, крахмал, гликолят натрия крахмала, гидрофосфат кальция, стеарат магния, тальк, коллоидная двуокись углерода и подобные. Такие композиции также могут содержать другие фармакологически активные агенты и обычные добавки, такие как стабилизаторы, увлажняющие агенты, эмульгаторы, вкусовые добавки, буферы и подобные. Композиции в соответствии с данным изобретением могут, например, быть получены в твердой или жидкой форме для перорального введения, такой как таблетки, пилюли, капсулы, порошки, сиропы,эликсиры, диспергируемые гранулы, крахмальные капсулы, суппозитории и подобные, в виде стерильных растворов, суспензий или эмульсий для парентерального введения, спреев, например, назальных спреев, чреcкожных препаратов, например пластырей, и подобных. Как отмечено выше, соединения в соответствии с данным изобретением могут применяться для лечения связанных с серотонином заболеваний у человека или животных, таких как расстройства питания,особенно ожирение, расстройства памяти, шизофрения, расстройства настроения, тревога, боль, злоупотребление препаратами, половые расстройства, эпилепсия и расстройства мочеиспускания. Доза и частота-6 005975 введения определенного соединения будут варьироваться в зависимости от множества факторов, включая эффективность определенного применяемого соединения, метаболической стабильности и продолжительности действия этого соединения, возраста пациента, массы тела, общего состояния здоровья, пола, диеты, способа и времени введения, скорости выделения, сочетания лекарственных средств, тяжести лечимого состояния и терапии, которой подвергается пациент. Ежедневная доза может, например, варьироваться от около 0,001 до около 100 мг на килограмм массы тела, вводиться однократно или множественными дозами, например от 0,01 до около 25 мг каждая. Обычно такая доза вводится перорально, но может быть выбрано парентеральное введение. Представленные ниже определенные примеры даны только как иллюстративные и не ограничивают данное изобретение каким-либо образом. Не вдаваясь в подробности, предполагается, что специалист в данной области техники, основываясь на представленном описании, сможет применять данное изобретение в широчайшем смысле. Все указанные здесь публикации включены в качестве ссылок в их полном объеме. Примеры Общие сведения ЯМР спектр записывают на спектрометре Bruker Advance DPX 400 МГц при температуре 25 С. Химические сдвиги даны в м.д. по отношению к тетраметилсилану. ЖХ/МС данные получают с помощью ВЭЖХ системы НР 1100 в сочетании с ЖХ масс-спектрометром, сопряженным с платформой Micromass с применением MassLynx. Детали ВЭЖХ: колонка Phenomenex C18 Luna, 3046 мм при температуре 401 С. Градиент элюента Т=0,95% (0,1% муравьиной кислоты в воде) и 5% (0,1% муравьиной кислоты в ацетонитриле), затем линейный градиент до Т=2,5 мин, 5% (0,1% муравьиной кислоты в воде) и 95%(0,1% муравьиной кислоты в ацетонитриле), затем еще 1 мин в этих условиях. Объемный расход элюента составляет 2 мл/мин. Определение проводят с применением УФ диодной матрицы в полосе при окне 210400 нм. Чередующийся +ve и -ve ионный APCI масс-спектр накапливают в течение 3,5 мин, сканируют между 100 и 650 мас. ед. МС высокого разрешения получают на спектрометре Micromass LCT. Проявляющие растворители для ТСХ на двуокиси кремния представляют собой диизопропиловый эфир или смеси этилацетат/петролейный эфир. Пример 1. 2-(1-Пиперазинил)-3-2-[3-(4-морфолинилметил)фенокси]этоксипиразин. Стадия 1. 2-Хлор-3-(4-трет-бутоксикарбонил-1-пиперазинил)пиразин. Указанное в заголовке соединение получают по методике, описанной в WO 00/76984. Смесь N-Bocпиперазина (11,47 г, 61,5 ммоль), K2 СО 3 (8,5 г, 61 ммоль) и 2,3-дихлорпиразина (9,20 г, 61,7 ммоль) в ацетонитриле (100 мл) перемешивают при температуре 100 С в течение 40 ч. Реакционную смесь концентрируют, растворяют в толуоле, промывают водой, сушат (MgSO4) и концентрируют. Остаток очищают хроматографией на колонке с силикагелем с применением толуола/EtOAc (7:3) в качестве элюента с получением 18,3 г (100%) указанного в заголовке соединения. МСВР m/z, вычислено для C13H19N4O2 (М)+ 298,1197, найдено 298,1206. Стадия 2. 2-[3-(4-трет-Бутоксикарбонил-1-пиперазинил)-2-пиразинилокси]этанол. Указанное в заголовке соединение получают по методике, описанной в WO 00/76984. KO-t-Bu (9,92 г, 103 ммоль) добавляют к смеси продукта, полученного на стадии 1 (18,14 г, 60,7 ммоль) и этиленгликоля (25 мл, 448 ммоль) в пиридине (125 мл) при температуре 85 С. Реакционную смесь перемешивают в течение 15 ч и затем выливают в ледяную воду и экстрагируют толуолом. Органическую фазу сушат(MgSO4) и концентрируют. Остаток очищают хроматографией на колонке с силикагелем с применением толуола/EtOAc (1:1) в качестве элюента с получением 16,9 г (85%) указанного в заголовке соединения. МСВР m/z, вычислено для C15H24N4O4(M)+ 324,1798, найдено 324,1784. Стадия 3. трет-Бутил 4-3-[2-(3-формилфенокси)этокси]-2-пиразинил-1-пиперазинкарбоксилат. Раствор соединения, полученного на стадии 2 выше (1,5 г, 4,7 ммоль) в безводном тетрагидрофуране (ТГФ; 10 мл), обрабатывают 3-гидроксибензальдегидом (0,74 г, 6,06 ммоль) и трифенилфосфином(1/59 г, 6,06 ммоль). Этот раствор перемешивают при комнатной температуре и затем обрабатывают диэтилазодикарбоксилатом (0,96 мл, 6,06 ммоль) в безводном ТГФ (5 мл). Через 1 ч ТСХ показывает некоторое количество оставшегося 2-[3-(4-трет-бутоксикарбонил-1-пиперазинил)-2-пиразинилокси]этанола. Реакционную смесь кипятят с обратным холодильником в атмосфере азота в течение 5 ч, затем охлаждают до комнатной температуры в течение ночи. ТСХ снова показывает непрореагировавшее исходное соединение. Смесь опять обрабатывают трифенилфосфином (0,80 г, 3,03 ммоль), диэтилазодикарбоксилатом (0,5 мл, 3,03 ммоль) и 3-гидроксибензальдегидом (0,40 г, 3,03 ммоль), затем перемешивают при комнатной температуре в течение еще 3 ч (завершение реакции подтверждают ТСХ). Летучие вещества удаляют в вакууме и остаток очищают флэш-хроматографией на колонке с силикагелем, элюируя петролейным эфиром/этилацетатом (2:1). Получают 0,33 г (16%) указанного в заголовке соединения в виде бесцветного масла. 1 Н ЯМР (CDC13)1,5 (с, 9 Н); 3,5 (ш.с, 8 Н), 4,45 (м, 2 Н); 4,75 (м, 2 Н); 7,2 (д, 1 Н); 7,45 (с, 1 Н); 7,5-7 005975 Стадия 4. трет-Бутил 4-(3-2-[3-(4-морфолинилметил)фенокси]этокси-2-пиразинил)-1-пиперазинкарбоксилат. Перемешиваемый раствор альдегида со стадии 3 выше (71,2 мг, 0,166 ммоль) в 1,2-дихлорэтане (5 мл) обрабатывают морфолином (19 мг, 0,22 ммоль), 3 молекулярными ситами и триацетоксиборгидридом натрия (52 мг, 0,25 ммоль). Смесь перемешивают при комнатной температуре в течение 5 ч (ТСХ мониторинг). Раствор фильтруют и фильтрат обрабатывают избытком насыщенного водного бикарбоната натрия. Эфирные экстракты отделяют и сушат над сульфатом магния. Смесь фильтруют и растворитель удаляют в вакууме с получением 54 мг (65%) указанного в заголовке соединения в виде желтого масла. Чистый по данным ЯМР. 1 Н ЯМР (CDC13)1,4 (с, 9 Н); 2,35 (м, 4 Н); 3,4 (м, 10 Н); 3,65 (м, 4 Н); 4,3 (м, 2 Н); 4,65 (м, 2 Н); 6,75(д, 1 Н); 6,9 (м, 2 Н); 7,2 (т, 1 Н); 7,5 (с, 1 Н); 7,7 (с, 1 Н). Стадия 5. 2-(1-Пиперазинил)-3-2-[3-(4-морфолинилметил)фенокси]этоксипиразин. Продукт со стадии 4 выше (54 мг, 0,11 ммоля) растворяют в безводном диэтиловом эфире (20 мл),перемешивают при комнатной температуре и обрабатывают хлороводородом в диэтилом эфире (6 М; 5 мл). Полученную белую суспензию перемешивают в течение 2 ч, затем быстро отфильтровывают. Гидрохлорид (гигроскопичный) растворяют в воде и нейтрализуют карбонатом натрия. Свободное основание экстрагируют дихлорметаном. Органические слои сушат над сульфатом магния, фильтруют и концентрируют в вакууме с получением 13 мг (29%) указанного в заголовке соединения в виде бледножелтого масла. LS/MC чистота 100%. 1 Н ЯМР (CDCl3)1,8 (ш, 1 Н); 2,45 (м, 4 Н); 2,95 (м, 4 Н); 3,45 (с, 2 Н); 3,55 (м, 4 Н); 3,7 (м, 4 Н); 4,35(т, 2 Н); 4,7 (т, 2 Н); 6,85 (д, 1 Н); 6,95 (м, 2 Н); 7,25 (т, 1 Н); 7,55 (с, 1 Н); 7,75 (с, 1 Н). Представленные ниже соединения получают аналогично из трет-бутил 4-3-[2-(3 формилфенокси)этокси]-2-пиразинил-1-пиперазинкарбоксилата (полученного в примере 1, стадия 3) и соответствующего амина. Пример 2. 2-(1-Пиперазинил)-3-2-[3-(1-пирролидинилметил)фенокси]этоксипиразин. Выход 31%, LS/MC чистота 100%. 1LS/MC чистота 97%. Получение фармацевтических композиций Пример. Получение таблеток. Ингредиенты мг/таблетку Активное соединение 10,0 Целлюлоза микрокристаллическая 57,0 Гидрофосфат кальция 15,0 Гликолят крахмала, натриевая соль 5,0 Диоксид кремния, коллоидный 0,25 Стеарат магния 0,75 Активный ингредиент 1 смешивают с ингредиентами 2, 3, 4 и 5 в течение около 10 мин. Затем добавляют стеарат магния и полученную смесь смешивают в течение около 5 мин и прессуют в таблетки с или без покрытия. Фармакологические тесты Способность соединения в соответствии с данным изобретением связываться или воздействовать на определенные подтипы 5-НТ рецептора может быть определена с помощью in vitro и in vivo исследова-8 005975 ний, известных в данной области техники. Биологическую активность соединений, полученных в примерах, тестируют с применением различных тестов. Определение сродства Сродство 5-НТ 2c рецептора к соединениям, полученным в примерах, определяют с помощью сравнительных экспериментов, в которых способность каждого соединения в серии разбавлений, замещать 3 Н-меченный 5-НТ, связанный с мембранами, полученный из трансфицированных клеток НЕК 293, стабильно экспрессирующих человеческий 5-НТ 2c рецепторный белок, проверяют с помощью технологииScintillation Proximity Assay. Неспецифическое связывание определяют с помощью 5 мкМ миансерина. Полученные результаты для отобранных соединений в соответствии с данным изобретением показаны в таблице ниже. Обычно значения сродства 5-НТ 2 с рецептора (Ki, нМ) составляют от 1 до 1500 нМ, предпочтительно от 1 до 100 нМ. Таблица. Сродство к 5-HT2 с рецептору. Исследование эффективности Агонистическое действие соединений, полученных в примерах, на 5-НТ 2 с рецептор определяют на основе способности каждого соединения мобилизовать внутриклеточный кальций в трансфицированных клетках НЕК 293, стабильно экспрессирующих человеческий 5-НТ 2 с рецепторный белок, с применением кальций-хелатирующего флуоресцентного красителя FLUO-3 (Sigma, St. Louis, МО, USA). Обычно максимальный ответ агонистов 5-НТ 2c составляет от 15 до 100% по отношению к максимальному ответу 5-НТ (серотонин) при концентрации 1 мкМ. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение общей формулы (I)R3 и R4, каждый независимо, являются водородом, метилом, C1-С 4-алкилом, арилом, гетероарилом,где арильные и гетероарильные остатки, в свою очередь, могут быть замещены в одном или более положениях независимо друг от друга галогеном, С 1-С 4-алкилом, С 1-С 4-алкокси, С 1-С 4-алкилтио, С 1-С 4 алкилсульфонилом, метансульфонамидо, ацетилом, нитро, циано, гидрокси, трифторметилом, трифторметокси, трифторметилтио, амино, метиламино, диметиламино или ацетамидо; илиR3 и R4 вместе с атомами углерода, к которым они присоединены, образуют 5- или 6-членное ароматическое или гетероароматическое кольцо, которое необязательно независимо замещено в одном или более положениях галогеном, метилом, метокси, метилтио, метилсульфонилом, нитро, циано, гидрокси,трифторметилом, трифторметилтио, амино, метиламино, диметиламино или ацетамидо;R5 и R6 независимо друг от друга являются водородом, С 1-С 4-алкокси-С 2-С 4-алкилом, гидрокси-С 2 С 4-алкилом, C1-C6-алкилом, С 2-С 6-ацилом, арилом, гетероарилом, арил-С 1-С 2-алкилом, гетероарил-С 1-С 2 алкилом, арил-С 1-С 2-ацилом, гетероарил-С 1-С 2-ацилом, и где любой арил или гетероарил, один или в составе другой группы, может быть независимо замещен в одном или более положениях С 1-С 4-алкилом,С 1-С 4-алкокси, С 1-С 4-алкилтио, С 2-С 4-ацилом, С 1-С 4-алкилсульфонилом, циано, нитро, гидрокси, С 2-С 3 алкенилом, С 2-С 3-алкинилом, фторметилом, трифторметилом, трифторметокси, галогеном, диметиламино или метиламино; илиR5 и R6 вместе с атомом азота, к которому они присоединены, образуют насыщенное гетероциклическое кольцо, имеющее 4-7 членов в кольце, где данное кольцо может содержать дополнительный гетероатом, который может быть замещен метилом, оксо или гидрокси;R7 является водородом или заместителем, выбранным из галогена, метила, метокси и этокси; иn = 1-3; и их фармацевтически приемлемые соли, гидраты, геометрические изомеры, таутомеры, оптические изомеры, N-оксиды и пролекарства. 2. Соединение по п.1, в котором R1 является водородом или метилом. 3. Соединение по п.2, в котором R1 является водородом. 4. Соединение по любому из пп.1-3, в котором R2 является водородом или метилом. 5. Соединение по любому из пп.1-4, в котором R3 и R4 независимо являются водородом, галогеном или метилом или в котором R3 и R4 образуют кольцо вместе с атомами углерода, к которым они присоединены, и кольцо является бензолом с образованием хиноксалина или тиофеном для получения тиено[3,4-b]пиразина, и где, если кольца замещены, они являются моно- или дизамещенными. 6. Соединение по п.5, в котором R3 и R4 оба являются водородом. 7. Соединение по любому из пп.1-6, в котором R7 является водородом. 8. Соединение по п.7, в котором R7 является водородом и группа -CH2N(R5)(R6) присоединена в мета-положении. 9. Соединение по любому из пп.1-8, в котором R5 и R6 вместе с атомом азота, к которому они присоединены, образуют кольцо, выбранное из азетидина, пирролидина, пиперазина, гомопиперазина, морфолина, тиоморфолина и пиперидина. 10. Соединение по любому из пп.1-9, в котором n = 1. 11. Соединение по п.1, выбранное из 2-(1-пиперазинил)-3-2-[3-(4-морфолинилметил)фенокси]этоксипиразина; 2-(1-пиперазинил)-3-2-[3-(1-пирролидинилметил)фенокси]этоксипиразина; 2-(1-пиперазинил)-3-2-[3-(4-метил-1-пиперазинилметил)фенокси]этоксипиразина; 2-(1-пиперазинил)-3-2-[(3-(2-метоксиэтил)аминометил)фенокси]этоксипиразина и 2-(1-пиперазинил)-3-2-[3-(изопропиламино)метилфенокси]этоксипиразина и их фармакологически приемлемых солей и сольватов. 12. Фармацевтическая композиция, содержащая соединение по любому из пп.1-11 в качестве активного ингредиента вместе с фармакологически и фармацевтически приемлемым носителем. 13. Способ профилактики или лечения связанных с серотонином заболеваний у человека или животного, где способ включает введение пациенту при необходимости эффективного количества соединения по любому из пп.1-11. 14. Способ по п.13, в котором указанным заболеванием является заболевание, связанное с 5-НТ 2c рецептором. 15. Способ по п.13 или 14, в котором указанное заболевание выбирают из расстройства питания,расстройства памяти, шизофрении, расстройства настроения, тревоги, боли, злоупотребления препаратами, половых расстройств, эпилепсии и расстройств мочеиспускания. 16. Способ по п.15, в котором расстройством питания является ожирение. 17. Применение соединения по любому из пп.1-11 в производстве лекарственного средства для профилактики или лечения связанных с серотонином заболеваний. 18. Применение по п.17, в котором указанным заболеванием является заболевание, связанное с 5 НТ 2c рецептором. 19. Применение по п.17 или 18, в котором указанное заболевание выбирают из расстройства питания, расстройства памяти, шизофрении, расстройства настроения, тревоги, боли, злоупотребления препаратами, половых расстройств, эпилепсии и расстройств мочеиспускания. 20. Применение по п.19, в котором расстройством питания является ожирение. 21. Способ модулирования функций 5-НТ 2c рецептора у человека или животного, включающий введение пациенту при необходимости эффективного количества соединения по любому из пп.1-11. 22. Способ получения соединения по п.1, включающий взаимодействие соединения формулы (II) где R3 и R4 независимо друг от друга являются водородом, метилом, C1-C4-алкилом, арилом, гетероарилом, где арильные и гетероарильные остатки могут быть замещены в одном или более положениях независимо друг от друга галогеном, С 1-С 4-алкилом, С 1-С 4-алкокси, C1-C4-алкилтио, C1-С 4-алкилсульфонилом, метансульфонамидо, ацетилом, нитро, циано, гидрокси, трифторметилом, трифторметокси, трифторметилтио, амино, метиламино, диметиламино или ацетамидо; или R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют 5- или 6-членное ароматическое или гетероароматическое кольцо, которое необязательно независимо замещено в одном или более положениях галогеном,метилом, метокси, метилтио, метилсульфонилом, нитро, циано, гидрокси, трифторметилом, трифторметилтио, амино, метиламино, диметиламино или ацетамидо; и каждый из Hal1 и На 12 независимо является галогеном; где R1 является водородом или С 1-С 4 алкилом, С 3-С 4-алкенилом, С 1-С 4-ацилом, С 1-С 4-алкоксикарбонилом,2-гидроксиэтилом, 2-цианоэтилом, тетрагидропиран-2-илом или аминозащитной группой; иR2 является водородом, С 1-С 4-алкилом, гидроксиметилом, C1-С 4-алкоксиметилом или фторметилом; с получением первого промежуточного соединения формулы (IV) в котором R1, R2, R3, R4 и Hal имеют значения, указанные выше, взаимодействие первого промежуточного соединения с соединением формулы (V) в котором n равно 1-3; с получением второго промежуточного соединения (VI) в котором R1, R2, R3 и R4 имеют значения, указанные выше,взаимодействие второго промежуточного соединения с соединением формулы (VII) в котором R7 является водородом или заместителем, выбранным из галогена, метила, метокси и этокси; с получением третьего промежуточного соединения (VIII) в котором R1, R2, R3, R4 и R7 имеют значения, указанные выше,взаимодействие третьего промежуточного соединения с соединением формулы (IX) где R5 и R6 независимо друг от друга являются водородом, С 1-С 4-алкокси-С 2-С 4-алкилом, гидрокси-С 2 С 4-алкилом, C1-С 6-алкилом, С 2-С 2-ацилом, арилом, гетероарилом, арил-С 1-С 2-алкилом, гетероарил-С 1-С 2 алкилом, арил-С 1-С 2-ацилом, гетероарил-С 1-С 2-ацилом и где любой арил или гетероарил, один или в составе другой группы, может быть независимо замещен в одном или более положениях С 1-С 4-алкилом,С 1-С 4-алкокси, С 1-С 4-алкилтио, С 2-С 4-ацилом, С 1-С 4-алкилсульфонилом, циано, нитро, гидрокси, С 2-С 3 алкенилом, С 2-С 3-алкинилом, фторметилом, трифторметилом, трифторметокси, галогеном, диметиламино или метиламино; или R5 и R6 вместе с атомом азота, к которому они присоединены, образуют насыщенное гетероциклическое кольцо, имеющее 4-7 членов в кольце, где данное кольцо может содержать дополнительный гетероатом, который может быть замещен метилом, оксо или гидрокси; с получением соединения по п.1. 23. Способ по п.22, в котором R1 является водородом или метилом. 24. Способ по п.22, в котором R2 является водородом или метилом.
МПК / Метки
МПК: C07D 241/18, A61K 31/497, A61P 25/00
Метки: пиперазинилпиразинов, качестве, соединения, 5-ht2, рецептора, серотонин, антагонистов
Код ссылки
<a href="https://eas.patents.su/13-5975-soedineniya-piperazinilpirazinov-v-kachestve-antagonistov-serotonin-5-ht2-receptora.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения пиперазинилпиразинов в качестве антагонистов серотонин 5-ht2 рецептора</a>
Предыдущий патент: N-замещенные неарильные гетероциклические антагонисты nmda/nr2b
Следующий патент: Хинолинил и бензотиазолил ppar-гамма модуляторы
Случайный патент: Морской источник для возбуждения сейсмических колебаний












