Нафтилсульфоновые кислоты и родственные соединения в качестве агонистов поглощения глюкозы
Номер патента: 6704
Опубликовано: 24.02.2006
Авторы: Сонюйянь Ши, Робинсон Луиз, Спивак Уэйн Р., Прасад В.В.С.В.Манчем, Скоу Стивен Р., Парк Джеонг Веонг, Козловски Майкл Р., Лум Роберт Т.
Формула / Реферат
1. Соединение формулы
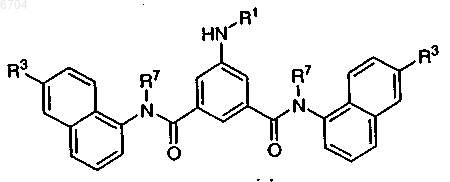
где R1 означает -C(O)R45 -SO2R4 или -C(O)NHR4;
R3, каждый независимо, означает OH, -SO2OH, -SO2NH2, -C(O)OH или тетразолил;
R4 выбирают из группы, включающей C1-C6алкил [необязательно замещенный одним или двумя карбонильными аминогруппами, фенилами (необязательно замещенными одним галогеном, C1-C6алкилом или C1-C6алкокси), фенилокси (необязательно замещенным одним галогеном, C1-C6алкилом или C1-C6алкокси), нафтил или нафтилокси], фенил или нафтил (каждый необязательно замещенный 1-3 галогенами, гидрокси, C1-C6алкилами, C1-C6акилокси, нитро, карбокси, серой или амино) или фуранил, пиридинил, хиноксалин или бензо[b]фуранил (каждый независимо замещенный одним галогеном, гидрокси, C1-C6алкилом, C1-C6алкокси, нитро, карбокси, серой или амино);
R7, каждый независимо друг от друга, означает водород или C1-C6алкил,
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где
R3 означает -SO2OH, -C(O)OH или тетразолил и
R7 означает водород.
3. Соединение по п.2, где каждый R3 означает -SO2OH.
4. Соединение по любому из пп.1-3, где R1 означает -C(O)R4.
5. Соединение по п.5, где R4 означает фенил (необязательно замещенный 1-3 галогенами, гидрокси, C1-C6алкилами, C1-C6алкокси, нитро, кабокси, серами или амино).
6. Соединение по п.5, выбранное из группы, состоящей из
5-({3-[(4-метилфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенил}карбониламино)нафталин-2-сульфоновой кислоты,
5-({3-[(4-метоксифенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенил}карбониламино)нафталин-2-сульфоновой кислоты,
5-({3-[(3-хлорфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенил}карбониламино)нафталин-2-сульфоновой кислоты,
5-({3-[(3-нитро-4-метилфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенил}карбониламино)нафталин-2-сульфоновой кислоты
и их фармацевтически приемлемых солей.
7. Соединение по любому из пп.1-3, где R1 означает -SO2R4.
8. Соединение по любому из пп.1-3, где R1 означает -C(O)NHR4.
9. Фармацевтическая композиция, включающая терапевтически эффективное количество соединения по любому из пп.1-8.
10. Фармацевтическая композиция по п.9 для лечения гипергликемии, диабета типа I и диабета типа II.
11. Способ лечения гипергликемии, диабета типа I и диабета типа II, включающий введение млекопитающему терапевтически эффективного количества соединения по любому из пп.1-8 или композиции по п.9.
12. Применение соединения по любому из пп.1-8 для получения лекарственного средства для лечения гипергликемии, диабета типа I и диабета типа II.
Текст
(а) Область изобретения Настоящее изобретение относится к способам, фармацевтическим композициям и соединениям для усиления инсулинозависимого поглощения глюкозы. Соединения по изобретению активируют киназу инсулинового рецептора, приводя к повышенной чувствительности к инсулину и усилению поглощения глюкозы. В частности, изобретение относится к применению соединений в способах для лечения пациентов с гипергликемией и особенно для лечения диабета типа II.(б) Описание уровня техники Среди многочисленных функций, осуществляемых пептидами и белковыми гормонами в ходе метаболизма, имеется способность взаимодействовать с рецепторами с высокой специфичностью. Рецептор инсулина присутствует фактически на всех клетках и в высоких концентрациях на клетках печени, скелетных мышц и жировой ткани. Стимуляция инсулинового рецептора является существенным элементом метаболизма и накопления углеводов. Больные диабетом или лишены достаточной эндогенной секреции инсулинового гормона (тип I),или имеют опосредованный инсулиновым рецептором сигнальный путь, который устойчив к эндогенному или экзогенному инсулину (тип II или инсулиннезависимый сахарный диабет (NIDDM. Диабет типаII является наиболее распространенной формой диабета, поражающей около 5% населения развитых стран. У больных диабетом типа II большинство восприимчивых к инсулину тканей, таких как печень,скелетная мышца и жировая ткань, обладают устойчивостью к инсулину (Haring, Mehnert, Diabetologia,36:176-182 (1993); Haring и др., Diabetologia, 37 Suppl., 2:c.149-54 (1994. Устойчивость к инсулину при диабете типа II является сложной и, очевидно, многофакторной, но, по-видимому, вызывается нарушенным сигналом от инсулинового рецептора к транспортной системе глюкозы и гликогенсинтазе. Недостаточность киназы инсулинового рецептора вовлечена в патогенез этого сигнального дефекта. Инсулиновая резистентность найдена также у многих пациентов, не страдающих диабетом, и может быть основным этиологическим фактором в развитии заболевания (Reaven, Diabetes, 37:1595-1607 (1988. Известна значительная информация, касающаяся самого рецептора инсулина. Рецептор состоит из четырех отдельных субъединиц, включающих две идентичные - и две идентичные -цепи. Субъединица имеет тирозинкиназную активность и АТФ-связывающие сайты. Инсулиновый рецептор активируется аутофосфорилированием ключевых остатков тирозина в своем цитоплазматическом тирозинкиназном домене. Это аутофосфорилирование необходимо для последующей активности инсулинового рецептора. Аутофосфорилироваие стабилизирует киназу активированного рецептора, приводя к аскаду фосфорилирования, включающему внутриклеточные сигнальные белки. В настоящее время подходы к лечению диабета типа II ограничены. Для лечения в настоящее время используют инсулин, но это невыгодно, поскольку инсулин должен быть инъецирован и поскольку его чрезвычайная эффективность требует тщательного титрования дозы. Несмотря на то, что описаны некоторые пептидные аналоги инсулина, ни один из них с молекулярной маcсой ниже 5000 Да не сохраняет его активность. Некоторые пептиды, которые взаимодействуют с сайтами на -субъединице инсулинового рецептора, проявили усиление активности инсулина на его рецепторе (Kole и др., J. Biol. Chem.,271:31619-31626(1996); Kasuya и др., Biochem. Biophys. Res. Commun., 200:777-83 (1994. Kohanski и др. сообщили о разнообразных поликатионных веществах, которые вызывают базальный эффект, но лишь незначительно усиливают действие инсулина (Kohanski, J. Biol. Chem., 264:20984-91 (1989); Xu и др.,Biochemistry, 30:11811-19 (1991. Очевидно, эти пептиды действуют на цитоплазматическом киназном домене инсулинового рецептора. Кроме того, было найдено, что некоторые непептидные компоненты усиливают агонистические свойства пептидных гормонов, но ни один из них, по-видимому, не действует на киназу инсулинового рецептора. Например, описана способность тиазолидиндионов, таких как пиоглитазон, усиливать дифференцировку адипоцитов (Kletzien и др., Mol. Pharmacol., 41:393 (1992. Эти тиазолидиндионы представляют класс потенциальных антидиабетических соединений, которые усиливают ответ тканеймишеней на инсулин (Kobayashi, Diabetes, 41:476 (1992. Тиазолидиндионы действуют на неизвестном сайте ниже самого рецептора инсулина и не оказывают прямого воздействия на киназу инсулинового рецептора. Применяемые в настоящее время другие антидиабетические агенты включают как средства,усиливающие секрецию инсулина (такие, как сульфонилмочевины), так и бигуаниды (такие, как метформин), которые ингибируют печеночный выброс глюкозы. До настоящего времени не удалось обнаружить непептидные вещества, которые могут имитировать активирующий эффект инсулина на инсулиновый рецептор. Разнообразные производные полианионных сульфокислот, включая сурамин, азокрасители и родственные соединения, известны специалистам и были созданы в качестве потенциальных терапевтических средств для ряда болезненных симптомов. Сурамин, описанный в 1917 году, представляет собой полисульфокислоту, которая широко исследована (Dressel, J. Chem. Ed., 38:585 (1961), Dressel, J. Chem. Ed.,39:320 (1962. Сурамин применяется в терапии как антигельминтное и антипротозойное средство. Позднее он был описан как ингибитор обратной транскриптазы некоторых птичьих и мышиных ретровирусов(De Clercq, Cancer Letter, 8:9 (1979); Mitsuya и др., Science, 226:172 (1984. Существует большое количество соединений, родственных сурамину. Большинство сураминовых аналогов, о которых сообщено,имеют многочисленные функциональные сульфокислотные группы в каждом ароматическом кольце. Недавние исследования указывают на то, что полианионные сураминовые аналоги обладают антиангиогенной, антипролиферативной активностью и противовирусной активностью (Gagliardi и др., CancerChem., 2:215 (1991. Многие другие биснафтилсульфокислоты описаны в патентной литературе как ингибиторы комплемента (патенты США 4132730, 4129591, 4120891, 41029176, 4051176). Кроме того,имеется множество патентов на азокрасители (патент Германии 19521589, патент США 3716368,патент Германии 2216592, патент Франции 1578556), которые раскрывают полисульфированные нафталиназопроизводные. Однако ни один из аналогов сурамина или азокрасителей не предложен для применения в лечении гипергликемии или диабета. Сущность изобретения Данное изобретение относится к фармацевтическим композициям, включающим нафталинсульфоновые кислоты и родственные соединения, которые усиливают поглощение глюкозы в клетках, к нафталинсульфоновым кислотам и родственным соединениям и к способам усиления поглощения глюкозы у млекопитающих с применением данных фармацевтических композиций и соединений. В одном аспекте данное изобретение относится к фармацевтическим композициям, включающим (i) фармацевтически приемлемый носитель и (ii) в качестве активного ингредиента соединение формулы IR1 и R2 означают независимо друг от друга водород, алкил, замещенный алкил, арил, замещенный арил, -C(O)R4, -C(O)OR4, -C(O)NR4R5, -S(O)2R4, -S(O)2OR4, гетероарил, замещенный гетероарил, гетероциклил, замещенный гетероциклил, арил(низш.)алкил, замещенный арил(низш.)алкил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил или (низш.)алкенил, илиR1 и R2 означают вместе с присоединенным азотом гетероарил С 3-С 9, гетероциклил С 3-С 5, или как R1, так и R2 означают кислород и вместе с присоединенным азотом образуют -NO2;R3 означает заместитель в кольце В и означает -SO2OR6, -C(O)OR6, -SO2NR62, -C(O)NR62 или тетразолил; каждый линкер -WY- между нафтилом и фенилом отделяет кольцо А нафтила и означает независимо друг от друга -C(O)NR7-, -NR7C(O)-, -С(О)О-, -ОС(О)-, -СН=СН-, -NR7CH 2-, -CH2NR7-,-NR7C(O)NR7-, -NR7C(O)O-, -OC(O)NR7-, -NR7SO2O-, -OSO2NR7-, -OC(O)O-, -SO2NR7-, -NR7SO2-,-OSO2- или -SO2O-;R4 и R5 означают каждый независимо друг от друга водород, алкил, замещенный алкил, арил, замещенный арил, арил(низш.)алкил, замещенный арил(низш.)алкил, замещенный гетероарил, гетероарил,гетероа-рил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил или (низш.)алкенил;R6 и R7 означают каждый независимо друг от друга водород или (низш.)алкил;R8 означает каждый независимо друг от друга водород, (низш.)алкил, замещенный (низш.)алкил,арил(низш.)алкил, замещенный арил(низш.)алкил, замещенный гетероарил, гетероарил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил,(низш.)алкенил, нитро, галоид, циано, -OR9, -SR9, -C(O)R9, -OC(O)R9, -C(O)OR9, -NR92, -C(O)NR92,-NR9C(O)R9, -OSO2R9, -SO2OR9, -SO2NR92 или -NR9SO2R9;R9 означает каждый независимо друг от друга водород, (низш.)алкил, замещенный (низш.)алкил,арил, замещенный арил, гетероарил, замещенный гетероарил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил, арил(низш.)алкил или замещенный арил(низш.)алкил;Z означает каждый немешающий заместитель; х и v означают каждый независимо друг от друга 0, 1, 2 или 3; иR10 означает арил, замещенный арил, гетероарил или замещенный гетероарил,необязательно в виде одного стереоизомера или смеси стереоизомеров, или его фармацевтически приемлемую соль. Во втором аспекте изобретение обеспечивает способ стимуляции киназной активности инсулинового рецептора, включающий контакт инсулинового рецептора или его киназной части с соединением по первому аспекту данного изобретения в количестве, достаточном для стимуляции киназной активности-2 006704 инсулинового рецептора. В третьем аспекте данное изобретение обеспечивает способ активации инсулинового рецептора или усиление активации инсулинового рецептора с помощью инсулина, включающий контакт инсулинового рецептора или его киназной части с соединением по первому аспекту данного изобретения в количестве,достаточном для активации инсулинового рецептора или усиления активации инсулинового рецептора под действием инсулина. Усиление способности инсулина активировать его рецептор у млекопитающих может быть достигнуто введением млекопитающему соединения по первому аспекту данного изобретения. В четвертом аспекте изобретение обеспечивает применение соединения по первому аспекту данного изобретения в способе стимуляции поглощения глюкозы клетками, которые обладают рецептором инсулина. Данный способ стимуляции поглощения глюкозы клетками, которые обладают рецептором инсулина, включает контакт клеток в присутствии инсулина с соединением по первому аспекту данного изобретения в количестве, достаточном для стимуляции поглощения глюкозы клетками. На поглощение глюкозы клетками у млекопитающего можно повлиять введением ему соединения по первому аспекту данного изобретения. Другие аспекты изобретения связаны с применением соединения по первому аспекту данного изобретения в лечении гипергликемии, диабета типа I или типа II у млекопитающего, такого как человек. Все эти способы лечения включают этап введения млекопитающему терапевтически эффективного количества соединения по первому аспекту данного изобретения. Необязательно способы лечения могут также включать введение млекопитающему инсулина. Другой аспект изобретения относится к соединениям формулы I, в которой каждый R4 и R5 означают независимо друг от друга водород, алкил, R11-замещенный алкил, арил, R11-замещенный арил,арил(низш.)алкил, R11-замещенный арил(низш.)алкил, R11-замещенный гетероарил, гетероарил, гетероарил(низш.)алкил, замещенный R11-замещенный гетероарил(низш.)алкил, гетероциклил, R11 замещенный гетероциклил или (низш.)алкенил; каждый R11 означает независимо друг от друга арил, замещенный арил, алкил, замещенный алкил, замещенный гетероарил, гетероарил, гетероциклил, замещенный гетероциклил, (низш.)алкенил, нитро, галоид, циано, -OR12, -SR12, -C(O)R12, -OC(O)R12,-C(O)OR12, -NR122, -C(O)NR132, -NR12C(O)R13, -OSO2R12, -SO2OR12, -SO2NR12 или -NR12SO2R12; и каждый R12 и R13 означают независимо друг от друга водород, (низш.)алкил, замещенный (низш.)алкил,арил, замещений арил, гетероарил, замещенный гетероарил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил, арил(низш.)алкил или замещенный арил(низш.)алкил; при условии, что если R10 означает нафтил, v означает 0 и каждый -WY- означает-C(O)NR7 -или -NR7C(O)-, то (i) Z не означает -SO2OH; и (ii) если R1 или R2 означают -C(O)NR4R5, то R13 не означает ни арил, ни замещенный арил. Еще в одном аспекте изобретение обеспечивает фармацевтические композиции, содержащие фармацевтически приемлемый носитель и данные соединения по изобретению в качестве активных ингредиентов. Краткое описание чертежей На фиг. 1 показано влияние соединения по изобретению, соединения 8, в комбинации с инсулином на уровни глюкозы в крови у мышей db/db, полученных скрещиванием особей, устойчивых к инсулину. На фиг. 2 показано влияние другого соединения по изобретению, соединения 10, в комбинации с инсулином на уровни глюкозы в крови у мышей db/db. На фиг. 3 показано влияние соединения 8 на клетки линии 3 Т 3 HIR. Подробное описание изобретения(а) Определения и общие параметры Термин алкил, как в алкиле или алкокси, означает одновалентный углеводородный остатокC1-С 20, который может быть линейным, разветвленным или циклическим. Термин (низш.)алкил, как в(низш.)алкиле, гало-ид(низш.)алкиле, арил(низш.)алкиле или гетероарил(низш:)алкиле, означает алкил C1-C10. Термин (низш.)алкил включает такие углеводородные остатки, как метил, этил, изопропил, пропил, бутил, изобутил, втор, -бутил, трет, -бутил, пентил, гексил, циклопентил, циклопропилметил, циклогексил или циклогексилметил. Предпочтительными являются (низш.)алкилы C1-С 6. Термин замещенный алкил или замещенный (низш.)алкил означает алкил или (низш.)алкил,соответственно, который обычно моно-, ди- или тризамещен таким остатком, как арил, R'-замещенный арил, гетероарил, нитро, циано, галоид, -OR, -SR, -COR, -OC(O)R, -C(O)OR, -NR2, -SO2OR, -OSO2R,-SO2NR2, -NRSO2R, -CONR2 или -NRCOR, где каждый R означает независимо друг от друга водород,(низш.)алкил, R'-замещенный (низш.)алкил, арил, R'-замещенный арил, гетероарил, гетероарил(низш.)алкил, R'-замещенный арил(низш.)алкил или арил(низш.)алкил, и каждый R' означает независимо друг от друга гидрокси, галоид, (низш.)алкокси, циано, тио, нитро, (низш.)алкил, галоид(низш.)алкил или амино. Замещенные алкилы или замещенные (низш.)алкилы, которые замещены одним-тремя заместителями, выбранными из группы, состоящей из циано, галоида, (низш.)алкокси, тио,нитро, амино или гидрокси, являются особенно предпочтительными. Термин галоид(низш.)алкил означает (низш.)алкил, замещенный одним-тремя атомами галоида и далее иллюстрируется в качестве примера такими радикалами, как -CF3, -CH2CF3 и -CH2CCl3.-3 006704 Термин арил, как в ариле, арилокси и арил(низш.)алкиле, означает радикал, происходящий от ароматического углеводорода, содержащего 6-20 кольцевых атомов углерода, имеющего одно кольцо(например, фенил) или два либо несколько конденсированных колец, предпочтительно 2-3 конденсированных кольца (например, нафтил), или два либо несколько ароматических колец, предпочтительно 2-3 ароматических кольца, которые связаны одинарной связью (например, бифенил). Предпочтителен арилC6-C16 и даже более предпочтителен арил С 6-С 14. Термин замещенный арил означает любой арильный радикал, который замещен, многократно или однократно, таким остатком, как алкил, R'-замещенный алкил, галоид, циано, нитро, -SR, -OR, -COR,-OCOR, -SO2OR, -OSO2R, -SO2NR2, -NRSO2R, -COOR, -NR2, -CONR2 или -NRCOR, где каждый R означает независимо друг от друга водород, (низш.)алкил, R'-замещенный (низш.)алкил, арил, R'-замещенный арил, гетероарил, гетероарил(низш.)алкил, арил(низш)алкил или R'-замещенный арил(низш.)алкил, и каждый R' означает независимо друг от друга гидрокси, галоид, (низш.)алкокси, циано, тио, нитро,(низш.)алкил, галоид(низш.)алкил или амино. Замещенный арил может быть замещен от одного до семи раз с любой комбинацией радикалов, перечисленных выше. Однако предпочтительными являются моно-,ди- или тризамещенные арилы. Особенно предпочтительными заместителями в замещенном ариле являются (низш.)алкил, галоид(низш.)алкил, галоид, циано, тио, нитро, амино, (низш.)алкокси или гидрокси. Радикалы -SO2OR, -SO2NR2, -COOR и -CONR2, в которых R означает водород или (низш.)алкил, также являются особенно предпочтительными заместителями замещенных арилов в соединениях по настоящему изобретению. Термин гетероарил, как в гетероариле и гетероарил(низш.)алкиле, означает радикал, происходящий от ароматического углеводорода, содержащего 5-14 кольцевых атомов, из которых 1-5 являются гетероатомами, выбранными независимо друг от друга из N, О или S, и включает моноциклические,конденсированные гетероциклические, конденсированные карбоциклические и гетероциклические ароматические кольца (например, тиенил, фурил, пирролил, пиримидинил, изоксазолил, оксазолил, индолил,изобензофуранил, пуринил, изохинолил, птеридинил, имидазолил, пиридил, пиразолил, пиразинил, хинолил и т.д.). Замещенный гетероарил может иметь один-три заместителя, таких как алкил, R'-замещенный алкил, галоид, циано, нитро, -SR, -OR, -COR, -OOCR, -SO2OR, -OSO2R, -SO2NR2, -NRSO2R, -COOR, -NR2,-CONR2 или -NRCOR, где каждый R означает независимо друг от друга водород, (низш.)алкил, R'замещенный (низш.)алкил, арил, R'-замещенный арил, гетероарил, гетероарил(низш.)алкил,арил(низш.)алкил или R'-замещенный арил(низш.)алкил, и каждый R' означает независимо друг от друга гидрокси, галоид, (низш.)алкилокси, циано, тио, нитро, (низш.)алкил, галоид(низш.)алкил или амино. Кроме того, любые два смежных заместителя в гетероариле необязательно могут образовать вместе(низш.)алкилендиоксигруппу. Особо предпочтительные заместители в замещенном гетероариле включают гидрокси, галоид, (низш.)алкилокси, циано, тио, нитро, (низш.)алкил, галоид(низш.)алкил или амино. Термин гетероциклил означает радикал, происходящий от алифатического циклического углеводорода, содержащего 5-14 кольцевых атомов, из которых 1-5 являются гетероатомами, выбранными независимо друг от друга из N, О или S. Предпочтительными являются моноциклические кольца (например, тетрагидрофуранил, тетрагидропиранил, пиперидинил и т.д.). Замещенный гетероциклил может иметь один-три заместителя, предпочтительно такие заместители, как алкил, R'-замещенный алкил, галоид, циано, нитро, -SR, -OR, -COR, -OOCR, -SO2OR, -OSO2R,-SO2NR2, -NRSO2R, -COOR, -NR2 или -NRCOR, где каждый R означает независимо друг от друга водород,(низш.)алкил,R'-замещенный алкил,арил,R'-замещенный арил,гетероарил,гетероарил(низш.)алкил, арил(низш.)алкил или R'-замещенный арил(низш.)алкил, и каждый R' означает независимо друг от друга гидрокси, галоид, (низш.)алкилокси, циано, тио, нитро, (низш.)алкил, галоид(низш.)алкил или амино. Предпочтительные заместители в замещенном гетероциклиле включают(низш.)алкил, галоид(низш.)алкил, галоид, циано, тио, амино, (низш.)алкилокси или гидрокси. Термин арил(низш.)алкил означает (низш.)алкильный радикал, который замещен арилом, как определено ранее. Термин замещенный арил(низш.)алкил означает арил(низш.)алкильный радикал, содержащий один-три заместителя в арильной части или алкильной части радикала, или в обеих частях. Термин гетероарил(низш.)алкил означает (низш.)алкильный радикал, который замещен гетероарилом, как определено ранее. Термин замещенный гетероарил(низш.)алкил означает гетероарил(низш.)алкильный радикал, содержащий один-три заместителя в гетероарильной части, или в алкильной части радикала, или в обеих частях. Термин (низш.)алкилокси означает радикал -OR, в котором R означает (низш.)алкил. Термин (низш.)алкенил означает любую разветвленную или неразветвленную ненасыщенную группу С 2-С 10, содержащую заданное число атомов углерода или до 10 атомов углерода, если нет ограничения по числу заданных атомов углерода; и содержащую 1 или несколько двойных связей в группе. В качестве примеров (низш.)алкенил иллюстрируется этенилом, пропенилом, бутенилом, пентенилом и гексенилом в их различных изомерных формах, в которых ненасыщенные связи или ненасыщенная связь могут располагаться в группе где угодно. Термин галоид означает бром, йод, фтор или хлор.-4 006704 Термин немешающий заместитель означает заместитель, который, присутствуя в данном соединении, фактически не снижает или иным способом не подавляет его конкретную желаемую биологическую активность, такую как способность соединения стимулировать киназную активность инсулинового рецептора, активировать инсулиновый рецептор или стимулировать поглощение глюкозы в клетках, обладающих рецептором инсулина. Наличие немешающего заместителя не должно оказывать отрицательного воздействия на биологическую активность соединения более чем примерно на 30%. Предпочтительно немешающий заместитель понижает биологическую активность соединения менее чем примерно на 10%. Наиболее предпочтительно немешающий заместитель не понижает биологическую активность соединения до какого-либо определяемого значения. Однако эффект присутствия немешающего заместителя в соединении не должен быть нейтральным. Например, немешающий заместитель может необязательно повышать конкретную биологическую активность соединения. Приемлемые немешающие заместители включают, но без ограничения, алкил, замещенный алкил, циано, галоид, нитро, -SR, -OR и - NR2,где каждый R независимо друг от друга означает водород, (низш.)алкил или замещенный (низш.)алкил. Фармацевтически приемлемая соль может быть любой солью, полученной из неорганической или органической кислоты либо неорганического или органического основания. Термин фармацевтически приемлемый анион относится к аниону таких кислотно-аддитивных солей. Термин фармацевтически приемлемый катион относится к катиону, образованному присоединением основания. Выбираемые соль и/или анион либо катион не должны быть биологически или каким-либо другим образом нежелательными. Термин стереоизомеры означает соединения, которые имеют одинаковую последовательность ковалентных связей и отличаются относительным расположением их атомов в пространстве. Внутренние соли или цвиттер-ионы могут быть образованы переносом протона от карбоксильной группы к свободной паре электронов атома азота в аминогруппе. Термин терапевтически эффективное количество означает, что количество, которое при введении млекопитающему для лечения заболевания достаточно, чтобы повлиять на такое лечение заболевания. Термины обработка или лечение заболевания у млекопитающего включают:(1) предупреждение развития заболевания у млекопитающего, которое может быть предрасположенным к нему, но еще не проявляет или не обнаруживает симптомы болезни,(2) подавление заболевания, т.е. остановка его развития, или(3) ослабление заболевания, т.е. индукция регрессии заболевания. По отношению к рецептору инсулина термин киназная часть его означает домен цитоплазматической тирозинкиназы инсулинового рецептора. Выражение до некоторой степени известным по сути, используемое при описании способов получения соединений по изобретению, относится к аналогичным способам или способам, известным в данной области для получения аналогичных соединений.(б) Соединения и их фармацевтические композиции Один аспект настоящего изобретения обеспечивает фармацевтические композиции, которые включают (i) фармацевтически приемлемый носитель и (ii) в качестве активного ингредиента соединение формулы I Формула I где R1 и R2 означают независимо друг от друга водород, алкил, замещенный алкил, арил, замещенный арил, -C(O)R4, -C(O)OR4, -C(O)NR4R5, -S(O)2R4, -S(O)2OR4, гетероарил, замещенный гетероарил, гетероциклил, замещенный гетероциклил, арил(низш.)алкил, замещенный арил(низш.)алкил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил или (низш.)алкенил, илиR1 и R2 означают вместе с присоединенным азотом гетероарил С 3-С 9, гетероциклил С 3-С 5, или как 1R , так и R2 означают кислород и вместе с присоединенным азотом образуют -NO2;R3 означает заместитель в кольце В и означает -SO2OR6, -C(O)OR6, -SO2NR62, -C(O)NR62 или тетразолил; линкер -WY- между нафтилом и фенилом отделяет кольцо А нафтила и означает каждый независимо друг от друга -C(O)NR7-, -NR7 С(О)-, -С(О)О-, -ОС(О)-, -СН=СН-, -NR7CH2-, -CH2NR7-, -NR7C(O)NR7-, -NR7C(O)O-,-OC(O)NR7-, -NR7SO2O-, -OSO2NR7-, -OC(O)O-, -SO2NR7-, -NR7SO2-, -OSO2- или -SO2O-;R4 и R5 означают каждый независимо друг от друга водород, алкил, замещенный алкил, арил, замещенный арил, арил(низш.)алкил, замещенный арил(низш.)алкил, замещенный гетероарил, гетероарил,гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклилR6 и R7 означают каждый независимо друг от друга водород или (низш.)алкил;R8 означает каждый независимо друг от друга водород, (низш.)алкил, замещенный (низш.)алкил,арил(низш.)алкил, замещенный арил(низш.)алкил, замещенный гетероарил, гетероарил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил,(низш.)алкенил, нитро, галоид, циано, -OR9, -SR9, -C(O)R9, -OC(O)R9, -C(O)OR9, -NR92, -C(O)NR92, -NR9C(O)R9,-OSO2R9, -SO2OR9, -SO2NR92 или -NR9SO2R9,R9 означает каждый независимо друг от друга водород, (низш.)алкил, замещенный (низш.)алкил,арил, замещенный арил, гетероарил, замещенный гетероарил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил, арил(низш.)алкил или замещенный арил(низш.)алкил,R10 означает арил, замещенный арил, гетероарил или замещенный гетероарил, Z означает каждый немешающий заместитель, и х и v означают каждый независимо друг от друга 0, 1, 2 или 3, необязательно в виде одного стереоизомера или смеси стереоизомеров, или его фармацевтически приемлемую соль. Левый линкер обозначается как -YW- просто для того, чтобы указать на его направленность. Данный фармацевтический состав применим для стимуляции поглощения глюкозы клетками млекопитающего или для лечения болезненного состояния млекопитающего, такого как гипергликемия,диабет типа I и диабет типа II. Другой аспект изобретения относится к соединению формулы I, в которой каждый R4 и R5 означают независимо друг от друга водород, алкил, R11-замещенный алкил, арил, R11-замещенный арил,арил(низш.)алкил, R11-замещенный арил(низш.)алкил, R11-замещенный гетероарил, гетероарил, гетероарил(низш.)алкил, замещенный RI1-гeтepoapил(низш.)aлкил, гетероциклил, R11-замещенный гетероциклил или (низш.)алкенил; каждый R11 означает независимо друг от друга арил, замещенный арил, алкил, замещенный алкил, арил(низш.)алкил, замещенный арил(низш.)алкил, замещенный гетероарил, гетероарил, гетероарил(низш.)алкил, замешенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил, (низш.)алкенил, нитро, галоид, циано, -OR12, -SR12, -C(O)R12, -OC(O)R12, -C(O)OR12,-NR122, -C(O)NR132, -NR12C(O)R13, -OSO2R12, -SO2OR12, -SO2NR12 или -NR12SO2R12; и каждый R12 и R13 означают независимо друг от друга водород, (низш.)алкил, замещенный (низш.)алкил, арил, замещений арил, гетероарил, замещенный гетероарил, гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил, арил(низш.)алкил или замещенный арил(низш.)алкил; при условии,что если R10 означает нафтил, v означает 0 и каждый -WY- означает -C(O)NR7- или -NR7C(O)-, то (i) Z не означает -SO2OH; и (ii) если R1 или R2 означают -C(O)NR4R5, то R13 не означает ни арил, ни замещенный арил. Предпочтительно соединениями формулы I являются соединения формулы II Формула II где каждый R1-R3, R8, R10, v, Z, -WY- и х имеют значения, приведенные ранее для соединений формулы I,необязательно в виде единственных стереоизомеров или смесей стереоизомеров, или их фармацевтически приемлемые соли. В соединениях формул I и II заместитель R10 означает предпочтительно арил или замещенный арил. Арилом или замещенным арилом являются предпочтительно нафтил или замещенный нафтил. В качестве альтернативы арилом или замещенным арилом может быть фенил или замещенный фенил. В альтернативном предпочтительном варианте воплощения изобретения R10 означает гетероарил или замещенный гетероарил. Например, R10 может означать хинолил. В соединениях формулы I или II, если v означает 1, 2 или 3, то предпочтительно каждый R8 означает независимо друг от друга водород, (низш.)алкил, замещенный (низш.)алкил, нитро, галоид, циано,-OR9, -SR9, -C(O)R9, -OC(O)R9, -C(O)OR9, -NR92, -C(O)NR92, -NR9C(O)R9, -OSO2R9, -SO2OR9 или-NR9SO2R9, где R9 означает водород или (низш.)алкил. В особо предпочтительном варианте воплощения изобретения R9 означает водород, (низш.)алкил, галоид(низш.)алкил, нитро, галоид, циано, амино,(низш.)алкилокси, тио или -C(O)OR9, где R9 означает (низш.)алкил или водород. В соединениях формулыI и II число v означает предпочтительно ноль. Другими предпочтительными соединениями формулы I являются соединения формулы III Формула III где каждый заместитель R1, R2, R3, -WY-, Z и х независимо друг от друга имеют значения, как в формулеI, необязательно в виде единственных стереоизомеров или смесей стереоизомеров, или их фармацевтически приемлемые соли. Особенно предпочтительными соединениями формулы III являются соединения формулы IV Формула IV где каждый заместитель R1, R2, R3, -WY-, Z и х независимо друг от друга имеют значения, как в формулеI, необязательно в виде единственных стереоизомеров или смесей стереоизомеров, или их фармацевтически приемлемые соли. Предпочтительно каждый немешающий заместитель Z в соединениях формул I, II, III и IV означает независимо друг от друга алкил, замещенный алкил, циано, галоид, нитро, -SR14, -OR14 или -NR142, где каждый R14 означает независимо друг от друга водород, (низш.)алкил или замещенный (низш.)алкил. Предпочтительно каждый Z означает (низш.)алкил, галоид(низш.)алкил, (низш.)алкилокси, циано, галоид, тио, амино, нитро или гидрокси. В предпочтительных соединениях формул I-IV каждый х означает 0 или 1. В наиболее предпочтительных соединениях каждый х означает 0. В предпочтительных соединениях формул I, II, III и IV заместитель R1 означает алкил, замещенный алкил, арил, замещенный арил, -C(O)R4 , -C(O)OR4, -C(O)NR4R5, -S(O)2R4, -S(O)2OR4, гетероарил,арил(низш.)алкил, замещенный арил(низш.)алкил или гетероарил(низш.)алкил, и R2 означает водород или (низш.)алкил. Наиболее предпочтительно R1 означает -C(O)R4, -C(O)NR4R5 или -SO2R4, и R2 означает водород или (низш.)алкил. В предпочтительном варианте воплощения изобретения R3 в соединениях формул I-IV означает-SO2OR6 или -SO2NR62. В предпочтительных соединениях по изобретению R3 означает -SO2OH. В альтернативном предпочтительном варианте воплощения изобретения R3 означает взамен -C(O)OR6,-C(O)NR62 или тетразолил. Например, R3 может означать -С(О)ОН. В предпочтительных соединениях формул I-IV каждый R4 и R5 означают независимо друг от друга водород, алкил, R11-замещенный алкил, арил, R11-замещенный арил, арил(низш.)алкил, R11-замещенный арил(низш.)алкил, R11-замещенный гетероарил, гетероарил, гетероарил(низш.)алкил, замещенный R11 гетероарил(низш.)алкил, гетероциклил, R11-замещенный гетероциклил или (низш.)алкенил, где каждыйR11 означает независимо друг от друга арил, замещенный арил, алкил, замещенный алкил, замещенный гетероарил, гетероарил, гетероциклил, замещенный гетероциклил, (низш.)алкенил, нитро, галоид, циано,-OR12, -SR12, -C(O)R12, -OC(O)R12, -C(O)OR12, -NR122, -C(O)NR122, -NR12C(O)R13, -OSO2R12, -SO2OR12,-SO2NR122 или -NR12SO2R12, и каждый R12 и R13 означают независимо друг от друга водород,(низш.)алкил, замещенный (низш.)алкил, арил, замещенный арил, гетероарил, замещенный гетероарил,гетероарил(низш.)алкил, замещенный гетероарил(низш.)алкил, гетероциклил, замещенный гетероциклил, арил(низш.)алкил или замещенный арил(низш.)алкил. В дополнительных предпочтительных соединениях формул I-IV заместитель R4 означает(низш.)алкил. Предпочтительно каждый R11 означает независимо друг от друга арил, R15-замещенный арил,(низш.)алкил, R15-замещенный (низш.)алкил, гетероарил, нитро, галоид, циано, амино, тио, -OR12,-C(O)R12, -OC(O)R12, -C(O)OR12, -C(O)NR132 или -NR12C(O)R13, каждый R12 и R13 означают независимо друг от друга водород, (низш.)алкил, R15-замещенный (низш.)алкил, арил, R15-замещенный арил, гетероарил, гетероарил(низш.)алкил, арил(низш.)алкил или R15-зaмeщeнный арил(низш.)алкил, и каждый R15 означает независимо друг от друга галоид, тио, амино, нитро, циано, гидрокси, (низш.)алкил, галоид(низш.)алкил или (низш.)алкилокси.-7 006704 В предпочтительных соединениях формул I, II, III и IV каждый линкер -WY- означает независимо друг от друга -C(O)NR7-, -NR7C(O)-, -SO2NR7-, -NR7SO2- или -NR7C(O)NR7-. В одном варианте воплощения изобретения каждый линкер -WY- означает -SO2NR7- или -NR7SO2-. В другом варианте воплощения изобретения каждый линкер -WY- означает -NR C(O)NR7 -. В одном особо предпочтительном варианте воплощения изобретения каждый линкер -WY- означает независимо друг от друга -C(O)NR7- или-NR7C(O)-. Соединения формул I-IV, где каждый линкер -WY- означает -C(O)NR7, являются наиболее предпочтительными. В соединениях формул I-IV каждый R7 означает предпочтительно водород. Предпочтительными являются соединения формул I-IV, в которых линкеры -WY- идентичны. Это особенно справедливо для соединений формул III и IV. Предпочтительно также, что в соединениях формул III и IV заместители R3 идентичны друг другу и нафтильные или замещенные нафтильные группы, с которыми соединены радикалы R3, также идентичны друг другу. Однако эта симметрия не является необходимой. Например, в соединении формулы IV один R3 может означать -С(О)ОН, а другой R3 может означать -SO2OH. Соединения формулы I, II, III или IV, содержащие более одного предпочтительного заместителя, особенно предпочтительны. Если соединение содержит больше предпочтительных заместителей, чем второе соединение, то первое соединение имеет преимущество над вторым. Например, соединения формулы IV, содержащие предпочтительные радикалы для заместителей (Z)x, R1, R2 и -WY-, предпочтительнее соединений формулы I, содержащих предпочтительные радикалы только для заместителей (Z)x и -WY-. Примеры предпочтительных соединений формулы I включают соединения формулы VR11 означает каждый независимо друг от друга арил, R15-замещенный арил, (низш.)алкил, R15 замещенный (низш.)алкил, гетероарил, нитро, галоид, циано, амино, тио, -OR12, -C(O)R12, -OC(O)R12,-C(O)OR12, -C(O)NR132 или -NR12C(O)R13;R12 и R13 означают каждый независимо друг от друга водород, (низш.)алкил, R15-замещенныйR15 означает независимо друг от друга галоид, тио, амино, нитро, циано, гидрокси, (низш.)алкил или (низш.)алкилокси;Z означает (низш.)алкил, галоид(низш.)алкил, (низш.)алкилокси, циано, галоид, тио, амино, нитро или гидрокси; и х означает 0, 1 или 2,необязательно в виде единственных стереоизомеров или смесей стереоизомеров, или их фармацевтически приемлемые соли. Особо предпочтительной группой являются соединения формулы V, где х означает ноль;R4 означает R11-замещенный фенил, где каждый R11 означает независимо друг от друга(низш.)алкил, R15-замещенный (низш.)алкил, (низш.)алкилокси, циано, галоид, тио, амино, амидо, нитро или гидрокси. Другие предпочтительные соединения формулы I включают соединения формулы VIR11 означает каждый независимо друг от друга арил, R15-замещенный арил, (низш.)алкил, R15 зaмeщeнный (низш.)алкил, гетероарил, нитро, галоид, циано, амино, тио, -OR12, -C(O)R12, -OC(O)R12,-C(O)NR132 -C(O)OR12, -C(O)NR132 или -NR12C(O)R13;R12 и R13 означают каждый независимо друг от друга водород, (низш.)алкил, R15-замещенныйR15 означает независимо друг от друга галоид, тио, амино, нитро, циано, гидрокси, (низш.)алкил или (низш.)алкокси;Z означает (низш.)алкил, галоид(низш.)алкил, (низш.)алкилокси, циано, галоид, тио, амино, нитро или гидрокси; и х означает 0, 1 или 2,необязательно в виде единственных стереоизомеров или смесей стереоизомеров, или их фармацевтически приемлемые соли. Альтернативные предпочтительные соединения формулы I включают соединения формулы VIIR11 означает каждый независимо друг от друга, арил, R15-замещенный арил, (низш.)алкил, R15 замещенный (низш.)алкил, гетероарил, нитро, галоид, циано, амино, тио, -OR12, -C(O)R12, -OC(O)R12,-C(O)OR12, -C(O)NR132 или -NR12C(O)R13;R12 означает каждый независимо друг от друга водород, (низш.)алкил;R13 означает каждый независимо друг от друга водород, (низш.)алкил, R15-замещенныйR15 означает независимо друг от друга галоид, тио, амино, нитро, циано, гидрокси, (низш.)алкил или (низш.)алкилокси;Z означает (низш.)алкил, галоид(низш.)алкил, (низш.)алкокси, циано, галоид, тио, амино, нитро или гидрокси; и х означает 0, 1 или 2,необязательно в виде единственных стереоизомеров или смесей стереоизомеров, или их фармацевтически приемлемые соли. Дополнительные предпочтительные соединения формулы I представлены формулой VIIIR8 означает каждый независимо друг от друга водород, (низш.)алкил, замещенный (низш.)алкил,нитро, галоид, циано, -OR9, -SR9, -C(O)R9 , -OC(O)R9, -C(O)OR9, -NR92, -C(O)NR92, -NR9C(O)R9, -OSO2R9,-SO2OR9, -SO2NR92 или -NR9SO2R9; иR9 означает каждый независимо друг от друга водород или (низш.)алкил;R11 означает каждый независимо друг от друга арил, R15-замещенный арил, (низш.)алкил, R15 замещенный (низш.)алкил, гетероарил, нитро, галоид, циано, амино, тио, -OR12, -C(O)R12, -OC(O)R12,-C(O)OR12, -C(O)NR132 или -NR12C(O)R13;R12 и R13 означают каждый независимо друг от друга водород, (низш.)алкил, R15-замещенныйR15 означает независимо друг от друга галоид, тио, амино, нитро, циано, гидрокси, (низш.)алкил или (низш.)алкилокси;Z означает (низш.)алкил, галоид(низш.)алкил, (низш.)алкилокси, циано, галоид, тио, амино, нитро или гидрокси; и х означает каждый независимо друг от друга 0, 1 или 2,необязательно в виде единственных стереоизомеров или смесей стереоизомеров, или их фармацевтически приемлемые соли. Соединения формул V-VIII особенно предпочтительны, когда каждый R3 означает -SO3H или тетразолил, и каждый R7 означает водород. Альтернативно каждый R3 означает -СООН, и каждый R7 означает водород. Соединения по настоящему изобретению, пригодные для применения в фармацевтических композициях и способах по изобретению, включают, но без ограничения, следующие соединения: 5-(3-[(3-метилфенил)карбониламино]-5-[N[-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-[(4-метилфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-[(4-метоксифенил)карониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-[(3-хлорфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-[(3-фторфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-[(4-фторфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-[(3-метоксифенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-[(4-нитрофенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-[(3-нитрофенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-[(3-нитро-4-метилфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 2-(N-3,5-бис[N-(6-сульфонафтил)карбамоил]фенилкарбамоил)бензойная кислота; 2-(N-3,5-бис[N-(6-сульфонафтил)карбамоил]фенилкарбамоил)-4,5-дихлорбензойная кислота; 5-(3-[(4-хлорфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 2-(N-3,5-бис[N-(6-сульфонафтил)карбамоил]фенилкарбамоил)-3,5-дихлорбензойная кислота; 2-(N- 3,5 -бис[N-(6-сульфонафтил)карбамоил] фенил карбамоил)-6-гидроксибензойная кислота; 5-(3-(фенилкарбониламино)-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2 сульфоновая кислота; 5-(3-(ацетиламино)-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-(2-нафтилкарбониламино)-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-(1-нафтилкарбониламино)-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(3-[(2-метилфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота;(2S)-2-(5-[(4-метилфенил)карбониламино]-3-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)-3-фенилпропановая кислота; 5-(3-[(4-метилфенил)карбониламино]-5-[N-(6-сульфамоилнафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновая кислота; 5-(5-[N-(6-карбоксинафтил)карбамоил]-3-[(4-метилфенил)карбониламино]фенилкарбониламино)нафталин-2-карбоновая кислота; 5-(3-амино-5-[N-метил-N-(6-сульфонафтил)карбамоил]фенил-N-метилкарбониламино)нафталин 2-сульфоновая кислота; и 5-(5-[(3-хлорфенил)карбониламино]-3-[N-метил-N-(6-сульфонафтил)карбамоил]фенил-Nметилкарбониламино)нафталин-2-сульфоновая кислота; необязательно в виде единственных стереоизомеров или смесей стереоизомеров, и их фармацевтически приемлемые соли. Синтезы и описания данных соединений приведены в примерах 1-11. Некоторые соединения по изобретению могут иметь один или несколько хиральных центров. В таких случаях все стереоизомеры также охватываются объемом данного изобретения. Соединения по изобретению включают выделенные в индивидуальном состоянии стереоизомеры, а также смеси таких стереоизомеров. Фармацевтически приемлемые соли, катионы и анионы соединений по изобретению также охвачены настоящим изобретением и применяются в способах и фармацевтических композициях, описанных в изобретении. Фармацевтически приемлемые соли включают соли, которые могут образоваться, если присутствуют кислотные протоны, способные реагировать с неорганическими или органическими основаниями. Обычно исходное соединение обрабатывают избытком щелочного реагента, такого как гидроксид, карбонат или алкоксид, содержащего соответствующий катион. Примерами катионов, присутствующих в фармацевтически приемлемых солях, являются такие катионы, как Na+, K+, Са 2+ и NH4+. Соли Na+ являются особенно пригодными. Следовательно, приемлемые неорганические основания включают гидроксид алюминия, гидроксид кальция, гидроксид калия, карбонат натрия и гидроксид натрия. Соли могут быть также получены с использованием органических оснований, таких как соли первичных, вторичных и третичных аминов, замещенных аминов, включая природные замещенные амины, и циклических аминов, включая изопрпиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, 2 диметиламиноэтанол, трометамин, лизин, аргинин, гистидин, кофеин, прокаин, гидрабамин, холин, бетаин, этилендиамин, глюкозамин, N-алкилглюкамины, теобромин, пурины, пиперазин, пиперидин, Nэтилпиперидин и тому подобное. Если соединения по изобретению содержат основную группу, то может быть получена кислотноаддитивная соль. Кислотно-аддитивные соли соединений получают стандартным способом в подходящем растворителе из исходного соединения и избытка кислоты, такой как хлористо-водородная кислота,бромисто-водородная кислота, серная кислота (образующая сульфатные и бисульфатные соли), азотная кислота, фосфорная кислота и тому подобное, и органических кислот, таких как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота,малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота,этансульфоновая кислота, салициловая кислота, n-толуолсульфокислота, гексановая кислота, гептановая кислота, циклопентанпропионовая кислота, молочная кислота, о-(4-гидроксибензоил)бензойная кислота,1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, nхлорбензолсульфоновая кислота, 2-нафталинсульфоновая кислота, камфорсульфоновая кислота, 4- 12006704 метилбицикло[2.2.2]окт-2-ен-1-карбоновая кислота, глюкогептоновая кислота, глюконовая кислота, 4,4'метиленбис(3-гидрокси-2-нафтойная) кислота, 3-фенилпропионовая кислота, триметилуксусная кислота,трет-бутилуксусная кислота, лаурилсерная кислота, глюкуроновая кислота, глютаминовая кислота, 3 гидрокси-2-нафтойная кислота, стеариновая кислота, муконовая кислота и тому подобное. Некоторые из соединений образуют внутренние соли или цвиттерионы. Фармацевтические композиции по изобретению преимущественно содержат предпочтительное соединение формулы I. Например, фармацевтическая композиция может содержать в качестве активного ингредиента соединение формулы II, III, IV, V, VI, VII или VIII. Однако предполагаются фармацевтические композиции, которые содержат любое из соединений по изобретению. Во всех случаях фармацевтические композиции по изобретению включают также фармацевтически приемлемый носитель. Фармацевтические композиции по данному изобретению могут быть разработаны в виде растворов или лиофилизированных порошков для парентерального введения. Перед употреблением содержание влаги в порошке может быть восстановлено прибавлением соответствующего разбавителя или другого фармацевтически приемлемого носителя. Жидкая лекарственная форма обычно представляет собой забуференный изотонический водный раствор. Примерами подходящих разбавителей являются обычный изотонический физиологический раствор, 5% декстроза в воде или забуференный раствор ацетата натрия или аммония. Такие лекарственные формы особенно подходят для парентерального введения, но могут также применяться для перорального введения. Может быть желательным добавление наполнителей. Таких, как поливинилпирролидон, желатин, гидроксицеллюлоза, гуммиарабик, полиэтиленгликоль, маннит, хлорид натрия или цитрат натрия. В качестве альтернативы эти соединения могут быть инкапсулированы, таблетированы или получены в виде эмульсии или сиропа для перорального введения. Могут быть добавлены фармацевтически приемлемые твердые или жидкие носители, чтобы усилить или стабилизировать композицию или облегчить приготовление композиции. Жидкие носители включают сироп,арахисовое масло, оливковое масло, глицерин, физиологический раствор, спирты и воду. Твердые носители включают крахмал, лактозу, дигидрат сульфата кальция, гипс, стеарат магния или стеариновую кислоту, тальк, пектин, гуммиарабик, агар или желатин. Носитель может также включать материал с замедленным высвобождением, такой как моностеарат глицерина или дистеарат глицерина, один или с воском. Количество твердого носителя изменяется, но предпочтительно будет между примерно 20 мг и примерно 1 г на дозированную единицу. Фармацевтические препараты получают, следуя общепринятым методикам фармации, включающим измельчение, смешивание, гранулирование и при необходимости прессование в случае таблеточных форм; или измельчение, смешивание и заполнение для лекарственных форм в виде твердых желатиновых капсул. Если используется жидкий носитель, препарат будет в форме сиропа,эликсира, эмульсии или водной либо неводной суспензии. Такая жидкая лекарственная форма может быть введена непосредственно перорально или заключенной в мягкую желатиновую капсулу. Некоторые специфические образцы применимых фармацевтических композиций описаны ниже в примерах 15-17. Как правило, фармацевтическая композиция по настоящему изобретению была бы упакована в емкость с наклейкой, указывающей на применение фармацевтической композиции в лечении гипергликемии, диабета типа I либо диабета типа II или сочетания проявлений этих заболеваний.(в) Способы применения соединений по данному изобретению Найдено, что соединения по изобретению связываются с киназным доменом и стимулируют аутофосфорилирование рецептора (пример 12, ниже). Кроме того, показано, что данные соединения усиливают способность инсулина воздействовать на транспорт глюкозы в культивированные клетки фибробластов (пример 13, ниже). Показано также, что соединения снижают уровни глюкозы в крови у мышей db/db (фиг. 1 и 2, пример 14). Способность соединений по изобретению стимулировать аутофосфорилирование инсулинового рецептора и стимулировать поглощение глюкозы клетками, что продемонстрировано ниже в специальных примерах 12-14, указывает на их полезность в лечении и ведении пациентов с диабетом. Безотносительно к какой-либо теории считается, что соединения по данному изобретению действуют непосредственно на киназную функцию инсулинового рецептора и необязательно конкурируют с инсулином за связывание в инсулинсвязывающем сайте, также не влияют на активацию рецептора по механизму, подобному тому,который присущ инсулину. Таким образом, они способны непосредственно активировать киназу для аутофосфорилирования, потенцировать эффект инсулина, активировать киназную функцию рецептора при фосфорилировании экзогенных субстратов и влиять на повышенное поглощение глюкозы адипоцитами и вообще клетками, имеющими рецепторы инсулина, и снижать содержание глюкозы в крови у пациентов с диабетом. Соответственно на основании активности соединений по изобретению они могут применяться для стимуляции киназной активности инсулинового рецептора, для усиления активации инсулинового рецептора инсулином, для усиления стимуляции инсулином поглощения глюкозы в клетках и стимуляции поглощения глюкозы у пациентов с диабетом. Таким образом, соединения по данному изобретению применимы в лечении диабета. В одном аспекте изобретение относится к способу стимуляции киназной активности инсулинового рецептора. Этот способ включает контакт инсулинового рецептора или его киназной части с соединением по изобретению в количестве, достаточном для того, чтобы стимулировать киназную активность ин- 13006704 сулинового рецептора. При стимуляции киназной активности инсулинового рецептора одновременно усиливается аутофосфорилирование, а также фосфорилирование экзогенных субстратов. Стимуляция киназной активности инсулинового рецептора может происходить или in vivo, или in vitro. Показано, что соединения по изобретению обладают стимулирующим действием на инсулиновый рецептор с последующим снижением циркулирующих уровней глюкозы в крови для потенциального терапевтического эффекта при заболевании диабетом. Подобным образом другие соединения, проявляющие такие же воздействия на инсулиновый рецептор и, следовательно, на циркуляцию глюкозы, являются потенциальными для применения в лечении диабета. Соединения, заявленные в пределах данного патента, могут использоваться в качестве модели для открытия других новых агентов, которые действуют на инсулиновый рецептор и тем самым снижают циркулирующие уровни глюкозы у пациентов с диабетом. Этапы в способе, по которому эти агенты могут использоваться для открытия новых агонистов/активаторов инсулиновых рецепторов и понижающих уровень глюкозы терапевтических агентов,можно успешно выполнить следующим образом. Соединения могут использоваться для того, чтобы подтвердить достоверность, оптимизировать и стандартизовать анализы, необходимые для открытия других соединений, которые: 1. Активируют/стимулируют цитоплазматический киназный домен инсулинового рецептора или киназу инсулинового рецептора. 2. Активируют/стимулируют инсулиновый рецептор. 3. Стимулируют поглощение глюкозы в клетках и тканях. 4. Снижают циркулирующие уровни глюкозы у млекопитающих. 5. Снижают циркулирующие уровни глюкозы у человека. 6. Подавляют липолиз в клетках и тканях. 7. Подавляют липолиз у млекопитающих. Эти соединения могут использоваться в качестве эталонного теста для открытия соединений, проявляющих в испытаниях улучшенную активность, которые: 1. Активируют/стимулируют цитоплазматический киназный домен инсулинового рецептора или киназу инсулинового рецептора. 2. Активируют/стимулируют инсулиновый рецептор. 3. Стимулируют поглощение глюкозы в клетках и тканях. 4. Снижают циркулирующие уровни глюкозы у млекопитающих. 5. Снижают циркулирующие уровни глюкозы у человека. 6. Подавляют липолиз в клетках и тканях. 7. Подавляют липолиз у млекопитающих. В комбинации с алгоритмами для сравнения структур или химических свойств и/или равноценных структур или химических свойств внутри библиотек исследуемых веществ эти соединения могут использоваться для открытия соединений, обладающих активностью в биологических испытаниях, соединений,которые: 1. Активируют/стимулируют цитоплазматический киназный домен инсулинового рецептора или киназу инсулинового рецептора. 2. Активируют/стимулируют инсулиновый рецептор. 3. Стимулируют поглощение глюкозы в клетках и тканях. 4. Снижают циркулирующие уровни глюкозы у млекопитающих. 5. Снижают циркулирующие уровни глюкозы у человека. 6. Подавляют липолиз в клетках и тканях. 7. Подавляют липолиз у млекопитающих. В комбинации с алгоритмами для сравнения структур и/или равноценных структур с целью моделирования молекулярных взаимодействий эти соединения могут использоваться для открытия соединений, обладающих активностью в биологических исследованиях, соединений, которые: 1. Активируют/стимулируют цитоплазматический киназный домен инсулинового рецептора или киназу инсулинового рецептора. 2. Активируют/стимулируют инсулиновый рецептор. 3. Стимулируют поглощение глюкозы в клетках и тканях. 4. Снижают циркулирующие уровни глюкозы у млекопитающих. 5. Снижают циркулирующие уровни глюкозы у человека. 6. Подавляют липолиз в клетках и тканях. Подавляют липолиз у млекопитающих. В другом аспекте по изобретению инсулиновый рецептор активируется путем контакта инсулинового рецептора или его киназной части с соединением по изобретению в количестве, достаточном для инсулиновой активации его рецептора, необязательно в присутствии инсулина. Инсулиновый рецептормишень необязательно может находиться на поверхности клетки млекопитающего. В таком случае контакт осуществляется введением млекопитающему соединения или его фармацевтической композиции. Еще в одном аспекте по изобретению соединения по изобретению применяют для стимуляции поглощения глюкозы клетками, обладающими рецептором инсулина. Данный способ включает контакт- 14006704 клеток с соединением по изобретению, необязательно в присутствии инсулина и в количестве, достаточном для стимуляции поглощения глюкозы клетками. Клетки-мишени необязательно могут быть у млекопитающего, и этап контакта рецептора с соединением может осуществляться введением млекопитающему соединения или его фармацевтической композиции. Способ лечения гипергликемии у млекопитающего, предпочтительно у человека, предусмотрен другим аспектом изобретения. Способ лечения гипергликемии у млекопитающего включает введение млекопитающему терапевтически эффективного количества соединения по изобретению или его фармацевтической композиции. Необязательно способ в дальнейшем включает лечение млекопитающего с помощью дополнительного вида терапии для гипергликемии. Например, один способ может также включать введение млекопитающему инсулина в дополнение к соединениям по изобретению. В качестве альтернативы соединения по изобретению могут вводиться млекопитающему в комбинации с неинсулиновым препаратом или в сочетании с другим альтернативным курсом лечения гипергликемии. Общее количество комбинации препаратов, введенных млекопитающему, должно быть терапевтически эффективным, хотя количества каждого из индивидуальных препаратов могут по отдельности быть субоптимальными для терапевтических целей. Очень опасным побочным эффектом введения инсулина является гипогликемия, индуцированная инсулином, с потенциальной комой и, возможно, смертью. Эта проблема может стать довольно острой у пациентов с диабетом, у которых проявляется непредсказуемая реакция на инсулин или сверхизменчивые уровни циркулирующей в крови глюкозы. Для таких пациентов совместное введение соединений по изобретению и субтерапевтических доз инсулина снизит до минимума возможность того, что пациенту с диабетом будет передозирован инсулин, и он пострадает от тяжелых последствий, таких как кома или смерть. Данные соединения, по-видимому, неспособны вызвать гипогликемию в присутствии инсулина. По-видимому, они повышают эффективность инсулина, но не проявляют эффекты мимикрии истинного инсулина, подобные гипогликемии. Таким образом, данные соединения являются эффективными детоксикантами инсулина. Еще один аспект изобретения относится к способу лечения диабета типа I у млекопитающих. Данный способ включает введение млекопитающему терапевтически эффективного количества соединения по изобретению или его фармацевтической композиции. В предпочтительном варианте осуществления изобретения млекопитающим является человек. Способ необязательно может включать далее лечение млекопитающего с помощью дополнительного вида терапии для диабета типа I. Например, инсулин может также вводиться млекопитающему. Количество инсулина, доставляемое млекопитающему, должно быть терапевтически эффективным количеством при совместном применении с соединением по изобретению. Однако количество инсулина, доставляемое млекопитающему, в сочетании с соединением по изобретению, предпочтительно меньше того количества, которое было бы терапевтически эффективным при введении млекопитающему одного инсулина. Понятно, что инсулин, который вводят при любых способах лечения по данному изобретению, может быть или выделенным из природного источника, или может быть или выделенным из природного источника, или рекомбинантным. Кроме того, аналог инсулина может заменять инсулин при любых способах лечения но настоящему изобретению. Еще в дополнительных аспектах по изобретению соединения по изобретению или их фармацевтические композиции применяют для лечения диабета типа II у млекопитающего. Данный способ включает введение млекопитающему терапевтически эффективного количества соединения по изобретению или его фармацевтической композиции. Снова предпочтительным субъектом является человек. Снова, как и другие способы лечения по изобретению, данный способ может в дальнейшем включать лечение млекопитающего с помощью дополнительного вида терапии для диабета типа II, такого как введение млекопитающему инсулина. Соединения по изобретению или их фармацевтические композиции применяют для усиления поглощения глюкозы у пациентов, которым необходимо такое лечение. Способ лечения включает парентеральное или пероральное введение эффективного количества выбранного соединения, предпочтительно диспергированного в фармацевтическом носителе. Эффективные дозы соединения по изобретению обычно выбирают в диапазоне от 0,01 до 1000 мг/кг, предпочтительно 0,01-100 мг/кг и более предпочтительно 1-30 мг/кг, но они будут легко определены специалистом в этой области в зависимости от пути введения, возраста и состояния пациента. Стандартные дозы можно вводить один-десять раз ежедневно в случае острого или хронического заболевания. Не ожидаются никакие неприемлемые токсикологические эффекты, если соединения по изобретению вводят в соответствии с настоящим изобретением. Соединения по изобретению или их фармацевтические композиции могут быть введены любым путем, применимым к пациенту, подвергающемуся лечению, и характеру его симптомов. Пути введения без ограничения охватывают введение с помощью инъекции, включая внутривенную, внутрибрюшинную, внутримышечную и подкожную инъекцию, путем трансмукозальной или трансдермальной доставки, посредством местного применения, назального аэрозоля, суппозитория и тому подобного, или могут включать пероральное введение. Лекарственные формы необязательно могут быть липосомальными лекарственными формами, эмульсиями, лекарственными формами, создаваемыми для введения препарата через мембраны слизистой оболочки, или трансдермальными лекарственными формами. При- 15006704 менимые лекарственные формы для каждого из этих способов введения можно найти, например, в(г) Способы получения соединений по изобретению Другой аспект изобретения относится к способу получения соединений формулы I. Соединения по изобретению получают обычными способами органической химии, до некоторой степени известными по сути. В отдельных случаях могут быть введены и затем удалены защитные группы. Применимые защитные группировки для амино, гидроксильной и карбоксильной групп описаны в монографии Green и др.,Protective Groups in Organic Synthesis, второе издание, изд-во John Wiley and Sons, New York, 1991. В некоторых случаях для осуществления реакции требуется активация функциональных групп. Например,активация карбоновых кислот может быть достигнута с использованием большого числа различных реагентов, как описано у Larock, Comprehensive Organic Transformations, изд-во VCH Publishers, New York,1989. Соединения по изобретению могут быть получены ацилированием или алкилированием аминогруппы, до некоторой степени известными по сути. Например, подробности ацилирования приведены на реакционной схеме I. При алкилировании алкильная группа присоединяется или замещает соединение. Алкилирование проходит в подходящем растворителе, таком как, например, ацетонитрил, ДМФ или ТГФ, при 0-160 С, обычно примерно при 25 С кипении, и требует 1-18 ч. Подобным образом соединения могут быть синтезированы с помощью реакций конденсации, до некоторой степени известных по сути. Например, подробности конденсации приведены на реакционной схеме IV. В реакции конденсации при соединении двух или нескольких молекул выделяется простое вещество, такое как вода или НСl. Реакция конденсации может происходить при присоединении какого-либо из многочисленных исходных веществ, используемых в органических синтезах, при температуре между 50 и 125 С. Реакция конденсаии может быть также внутримолекулярной. В реакции конденсации соединения формулы I компонуют из субструктур ,и , которые образуют молекулу. Субструктуры ,иприведены в основном пункте формулы изобретения на способ. В компоновку молекулы вовлекаются реагирующие группы, способные образовать линкер -WZ-. Например, образование молекулы может включать конденсацию активированной субструктурыс готовой субструктурой - или конденсацию готовой субструктуры - с активированной субструктурой , или конденсацию субструктурис субструктурой . В последнем случае предпочтительна идентичность субструктури , чтобы избежать образования смесей продуктов реакции. Для того, чтобы соединять такие компоненты формулы I , одна активированная субструктураможет реагировать с двумя субструктурами(см. реакционную схему V). Компоненты формулы I могут быть также получены восстановлением нитрогруппы, до некоторой степени известным по сути, как показано на реакционных схемах I или II. Сложный эфир соединения формулы I может быть гидролизован с образованием соли или свободной кислоты, как показано на реакционной схеме IV. При гидролизе сложный эфир может омыляться при взаимодействии с водой или с алканолом в присутствии основания. Гидролиз катализируется кислотой или основанием и может потребовать такой продолжительности времени, как 18 ч. Дальнейшие общеизвестные способы получения соединений формулы I включают введение или превращение заместителей. Например, бром в качестве заместителя может быть превращен в гидроксигруппу, и наоборот. Кроме того, могут быть получены фармацевтически приемлемые соли соединений по изобретению,а также соответствующие им свободные основания, и рацемическая смесь соединения по изобретению в любых соотношениях может быть разделена с образованием его стереоизомера. При образовании соли свободную кислоту превращают в соль путем прибавления основного реагента, такого как водный раствор гидроксида натрия или триэтаноламина, который заменяет все или часть водородных ионов кислоты одним или несколькими катионами основания. Соединения по изобретению могут быть синтезированы, как показано в следующих примерах, или путем модификации приведенных в примерах синтезов способами, известными специалистам в этой области.(д) Примеры Последующие примеры служат иллюстрацией данного изобретения. Примеры никоим образом не ограничивают объем данного изобретения, а представлены для того, чтобы показать, как получать и применять соединения по изобретению. Пример 1. Синтез 5-(3-[3-метилфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновой кислоты (соединение 7) Один из синтетических путей по настоящему изобретению представлен ниже на реакционной схеме I(5-нитробензол-1,3-дикарбонилхлорид, соединение 2) действием избытка тионилхлорида в пиридине. Далее дихлорангидрид кислоты реагировал с 2 эквивалентами 5-амино-2-нафталинсульфоновой кислоты, соединением 3, давая бисамид (5-(3-нитро-5-[N-(6-сульфонафтил)карбамоил]фе-нилкарбониламино)нафталин-2-сульфоновую кислоту, соединение 4). Нитрогруппу в соединении 4 восстанавливали с использованием дихлорида олова в водном кислотном растворе, получая 5-(3-амино-5-[N-(6 сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновую кислоту, соединение 5. Соединение 5 реагировало с 3-метилбензоилхлоридом, соединением 6, с образованием соединения 7. Получение 5-(3-нитро-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновой кислоты (соединение 4) Суспендировали 10,56 г (0,05 моля) 5-нитробензол-1,3-дикарбоновой кислоты в 18 мл (0,165 моля) тионилхлорида и затем прибавляли 10 мл пиридина. Смесь перемешивали при комнатной температуре до полного растворения и затем перемешивали в течение еще одного часа. Избыток тионилхлорида удаляли в вакууме. Суспендировали 22,33 г (0,10 моля) 5-амино-2-нафталинсульфоновой кислоты в 150 мл пиридина и прибавляли к описанному выше дихлорангидриду кислоты в 50 мл диоксана и хлороформа (50:50) при интенсивном перемешивании в течение 1-2 ч. Неочищенный продукт осаждали диоксаном. Маслянистый продукт собирали на воронке Бюхнера. Маслянистый продукт коричневого цвета растворяли в 500 мл воды, затем давали осаждаться в течение 30 мин. Твердое вещество собирали фильтрованием. Получали 16,2 г. Получение 5-(3-амино-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновой кислоты (соединение 5) Растворяли 7,00 г (31,0 ммоль) дигидрата дихлорида олова в 35 мл концентрированной НСl и охлаждали до 0-5 С в бане со льдом. Раствор одной порцией прибавляли к 7,5 г (9,6 ммоля) соединения 4. Смесь тщательно перемешивали при комнатной температуре в течение 2-3 ч, затем охлаждали в бане со льдом. Твердое белое вещество собирали фильтрованием и промывали концентрированной НСl (15 мл х 3), 6 н. НСl (15 мл х 3) и 1 н. НСl (20 мл х 4). Затем твердое вещество сушили в эксикаторе и получали 5,65 г. Получение 5-(3-[(3-метилфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновой кислоты (соединение 7) Суспендировали 100 мг (0,17 ммоля) соединения 5 в 5 мл пиридина и 2 мл сульфолана и прибавляли 0,030 мл (0,23 ммоля) 3-метилбензоилхлорида. Смесь перемешивали при комнатной температуре в течение примерно 16 ч. Реакционная смесь становилась прозрачным раствором, твердое вещество осаждали тетрагидрофураном (ТГФ) (100 мл). Твердое вещество собирали фильтрованием и промывали трижды ТГФ. Получали 80 мг не совсем белого порошка. Пример 2. Синтез 5-(3-[(3-метилфенил)карбониламино]-5-[N-(6-сульфонафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновой кислоты (соединение 7) К 100 мг (0,17 ммоля) соединения 5, суспендированного в 5 мл пиридина и 2 мл сульфолана, прибавляли 23 мкл (0, 172 ммоля) 3-метилбензоилхлорида. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Прибавляли дополнительные 12 мкл (0,085 ммоля) 3-метилбензоилхлорида и оставляли реакционную смесь перемешиваться в течение еще 2 ч. Избыток- 17006704 хлорангидрида гасили добавлением 0,5 мл метанола. Продукт реакции осаждали при добавлении ТГФ(0,337 ммоля) фталевого ангидрида. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Прибавляли дополнительные 25 мг (0,17 ммоля) фталевого ангидрида, реакционную смесь перемешивали в течение дополнительных 24 ч. Продукт реакции осаждали при добавлении ТГФ (100 мл) и собирали фильтрованием в вакууме, получая 74 мг требуемого соединения. Продукт идентифицировали с помощью 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ. Пример 4. Синтез дополнительных соединений формулы V Следующие соединения, приведенные в табл. 1, получали с использованием методик, подобных тем, которые описаны в примерах 1-3. Методики, описанные в примерах 1-3, могут быть легко модифицированы специалистами для получения обширного набора соединений формулы V. Например, использование различных альтернативных хлорангидридов кислот вместо соединения 6 в реакционной схеме примера 1 дало бы множество различных соединений формулы V. Названия по номенклатуре ИЮПАК соединений, приведенных выше в табл. 1, перечислены ниже в табл. 2. Названия по номенклатуре ИЮПАК получены с использованием программного обеспечения Пример 5. Синтез 5-[(3-[(4-хлорфенил)сульфонил]амино-5-[N-(6-сульфонафтил)карбамоил]фенил)карбониламино]нафталин-2-сульфоновой кислоты (соединение 50) К 100 мг (0,17 ммоля) соединения 5, суспендированного в 5 мл пиридина и 2 мл сульфолана, прибавляли 36 мг (0,172 ммоля) 4-хлорбензолсульфонилхлорида. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Прибавляли дополнительные 18 мг (0,085 ммоля) 4-хлорбензолсульфонилхлорида и оставляли реакционную смесь перемешиваться в течение еще 2 ч. Продукт реакции осаждали при добавлении ТГФ и собирали фильтрованием в вакууме. Продукт идентифицировали с использованием 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ. Пример 6. Синтез дополнительных соединений формулы VI Соединения, перечисленные в табл. 3, получали модификацией синтеза, описанного в примере 5, с использованием методик, хорошо известных специалистам. Названия по номенклатуре ИЮПАК соединений, приведенных выше в табл. 3, перечислены ниже в табл. 4. Названия по номенклатуре ИЮПАК получены с использованием программного обеспечения Пример 7. Получение 5-[(3-[(2-хлорфенил)амино]карбониламино-5-[N-(6-сульфонафтил)карбамоил]фенил)карбониламино]нафталин-2-сульфоновой кислоты (соединение 59) К 100 мг (0,17 ммоля) соединения 5, растворенного в 10 мл диметилфор-мамида и 1 мл пиридина,прибавляли 25 мкл (0,207 ммоля) 2-хлорфенилизоцианата. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Прибавляли дополнительные 12 мкл (0,103 ммоля) 2-хлорфенилизоцианата и реакционную смесь перемешивали в течение дополнительных 2 ч. Продукт реакции осаждали при добавлении ТГФ и собирали фильтрованием в вакууме, получая 57 мг требуемого соединения. Продукт идентифицировали с использованием 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ. Пример 8. Синтез дополнительных соединений формулы VII Соединения, приведенные в табл. 5, получали модификацией синтеза, описанного в примере 7, с использованием методик, хорошо известных специалистам.- 23006704 Названия по номенклатуре ИЮПАК соединений, приведенных выше в табл. 5, перечислены ниже в табл. 6. Названия по номенклатуре ИЮПАК получены с использованием программного обеспечения Пример 9. Синтез натриевой соли 5-(3-[(3-хлорфенил)карбониламино]-5-[N-(6-гидроксинафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновой кислоты (соединение 82) Соединение 82 синтезировали в соответствии с методиками, представленными на реакционных схемах II, III и IV, и как описано ниже. Реакционная схема II Получение 3-амино-5-(метоксикарбонил)бензойной кислоты (соединение 68) К 2,75 г монометилового эфира 5-нитроизофталевой кислоты (или 5-(метоксикарбонил)-3 нитробензойной кислоты), соединения 67, растворенного в 30 мл ТГФ, прибавляли 100 мг 10% палладия на угле. Реакционную смесь помещали в прибор Парра для гидрирования при давлении водорода 45 фунтов/дюйм 2 и встряхивали в течение 16 ч. Твердый палладиевый катализатор удаляли фильтрованием через слой целита в вакууме и к фильтрату прибавляли 5 мл 1 н. НСl в диэтиловом эфире. После перемешивания в течение 12 ч твердое вещество собирали фильтрованием в вакууме и промывали этилацетатом. Получали 1,82 г требуемого продукта. Продукт идентифицировали с использованием 1 Н-ЯМР и- 24006704 масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ. Получение 3-[(3-хлорфенил)карбониламино]-5-(метоксикарбонил)бензойной кислоты (соединение 70) К 0,576 г (2,49 ммоля) соединения 68 прибавляли 10 мл ТГФ, 10 мл воды и 2,6 мл 1 н. водного раствора гидроксида натрия. К данному реакционному раствору прибавляли по отдельности небольшими порциями раствор 341 мкл (2,74 ммоля) 3-хлорбензоилхлорида (соединение 69) в 5 мл ТГФ и 2,6 мл 1 н. водного раствора гидроксида натрия. В ходе прибавления рН реакционного раствора контролировали с помощью бумажного индикатора, в реакционной смеси поддерживали значение рН выше 8. По окончании прибавления по данным ТСХ оставалось некоторое количество соединения 68. Описанную выше методику повторяли, используя 150 мкл (1,21 ммоля) 3-хлорбензоилхлоида в 5 мл ТГФ и дополнительный 1 н. водный раствор гидроксида натрия для поддержания значения рН реакционного раствора выше 8. После того, как анализ методом ТСХ показал полное исчезновение соединения 68, реакционную смесь экстрагировали этилацетатом и 0.5 н. водным раствором бикарбоната натрия. Затем водный слой подкисляли 6 н. НСl и экстрагировали этилацетатом. Органический слой сушили (MgSO4), фильтровали,летучие вещества удаляли в вакууме. Полученный остаток обрабатывали смесью этилацетат/диэтиловый эфир 50/50 с образованием твердого белого вещества, которое собирали фильтрованием в вакууме. Получали 0,604 г требуемого продукта. Продукт идентифицировали с использованием 1 НЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ. Получение метилового эфира 3-(хлоркарбонил)-5-[(3-хлорфенил)карбониламино]бензойной кислоты(соединение 71) К 0,319 г (0,96 ммоля) соединения 70 прибавляли 8 мл тионилхлорида, полученную суспензию оставляли перемешиваться при температуре окружающей среды в течение 2 ч. Затем прибавляли 5 капель пиридина. Реакционная смесь мгновенно становилась гомогенным раствором. Через 30 мин летучие вещества удаляли в вакууме и дважды прибавляли и удаляли в вакууме хлороформ (10 мл). Получали твердый продукт, который использовали без характеристики. Реакционная схема III Получение 5-(ацетиламино)нафталин-2-сульфоновой кислоты (соединение 73) К 29,3 г (0,13 моля) 5-амино-2-нафталинсульфоновой кислоты (соединение 72) прибавляли 40 мл пиридина и 26 мл уксусного ангидрида. Полученную суспензию оставляли перемешиваться при температуре окружающей среды. Через 24 ч полученный раствор разбавляли 60 мл метанола. Затем прибавляли раствор 3,6 г (0,156 моля) натрия в 100 мл метанола. После того, как начал образовываться твердый осадок, прибавляли 200 мл диэтилового эфира и суспензию перемешивали. Твердое вещество собирали фильтрованием в вакууме и промывали диэтиловым эфиром. Получали 38,9 г (0,11 моля) требуемого продукта. Продукт идентифицировали с использованием 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ. Получение 5-(ацетиламино)нафталин-2-сульфонилхлорида (соединение 74) К 38,9 г (0,11 моля) соединения 73 прибавляли 52 мл хлорокиси фосфора, 105 мл сульфолана, 105 мл ацетонитрила и 4 мл диметилацетамида. Полученную суспензию оставляли перемешиваться при температуре окружающей среды в течение 24 ч. Прибавляли дополнительно по 10 мл сульфолана и ацетонитрила, температуру реакционной смеси повышали до 50 С. Через 2 ч реакционная смесь становилась непрозрачной. Температуру реакционной смеси снижали до 25 С, затем реакционной содержимое выливали на 2 л льда. После того, как весь лед расплавился, полученное твердое вещество собирали фильтрованием в вакууме и промывали холодной водой. Получали 33,5 г (0,11 моля) требуемого продукта. Продукт идентифицировали с использованием 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью оф-ВЭЖХ. Получение 4-метилфенилового эфира 5-(ацетиламино)нафталин-2-сульфоновой кислоты (соединение 75) К 15,7 мл (150 ммолей) n-крезола в 100 мл пиридина, охлажденных в бане со смесью лед/вода, при- 25006704 бавляли половину от 27,7 г (97,6 ммоля) соединения 74. Через 10 мин прибавляли остающуюся половину соединения 74. Еще через 10 мин убирали охлаждающую баню, реакционной смеси давали нагреться до температуры окружающей среды. Реакционную смесь выливали на лед и экстрагировали дихлорметаном. Органический слой промывали 0,1 н. водным раствором НСl, затем 1,25 н. водным раствором гидроксида натрия. Органический слой сушили (MgSO4), фильтровали, летучие вещества удаляли в вакууме. Остаток перекристаллизовывали из смеси этипацетат/трет.-бутилметиловый эфир, получая 11,9 г (33,5 ммоля) требуемого продукта. Из фильтрата удаляли летучие вещества и выделяли дополнительные 10,5 г(29,5 ммоля) требуемого продукта. Продукт идентифицировали с использованием 1 Н-ЯМР и массспектрометрии, чистоту оценивали с помощью офВЭЖХ. Получение 4-метилфенилового эфира 5-аминонафталин-2-сульфоновой кислоты (соединение 76) К 9,05 г (0,03 моля) соединения 75 прибавляли 40 мл диоксана и 120 мл 6 н. водного раствора НСl. Реакционную суспензию нагревали до 75 С в течение 7 ч. Полученный раствор охлаждали до комнатной температуры и нейтрализовали 10 н. водным раствором гидроксида натрия до рН 10. Реакционную смесь экстрагировали этилацетатом. Органический слой сушили (MgSO4), фильтровали и уменьшали в вакууме до небольшого объема. Затем прибавляли 50 мл 1 н. раствора НСl в диэтиловом эфире для образования твердого вещества, собранного фильтрованием в вакууме. Получали 8,57 г (0,02 моля) требуемого продукта. Продукт идентифицировали с использованием 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ. Реакционная схема IV Получение метилового эфира 5-[(3-хлорфенил)карбониламино]-3-(N-6-[(4-метилфенил)оксисульфонил]нафтил)карбамоил)бензойной кислоты (соединение 77) К 0,34 г (0,96 ммоля) соединения 71 прибавляли 0,33 г (0,96 ммоля) соединения 76, 15 мл дихлорметана и 162 мкл пиридина. Через 16 ч реакционную смесь дважды экстрагировали из этилацетата 0,5 н. водным раствором НСl. Затем органический слой экстрагировали 1 М водным раствором бикарбоната натрия. Органический слой сушили (MgSO4), фильтровали, летучие вещества удаляли в вакууме. Полученный остаток дважды соупаривали с дихлорметаном, и образующееся твердое вещество суспендировали в дихлорметане. Твердое вещество собирали фильтрованием в вакууме. Получали 0,28 г (0,44 ммоля) требуемого продукта. Продукт идентифицировали с использованием 1 Н-ЯМР и масс-спектрометрии,чистоту оценивали с помощью оф-ВЭЖХ. Получение 5-[(3-хлорфенил)карбониламино]-3-(N-6-[(4-метилфенил)оксисульфонил]нафтилкарбамоил)бензойной кислоты (соединение 78) К 0,28 г (0,44 ммоля) соединения 77 прибавляли 50 мл ТГФ для образования гомогенного раствора. Затем прибавляли 2,24 мл (2,24 ммоля) 1 н. водного раствора гидроксида лития. Образовалось твердое вещество, которое растворяли добавлением 15 мл воды. Через 10 ч снижали рН реакционной смеси до 1,летучий ТГФ удаляли с помощью роторного испарителя. Полученное твердое вещество собирали фильтрованием в вакууме. Получали 0,28 г (0,44 ммоля) требуемого продукта. Продукт идентифицировали с использованием 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ.- 26006704 Получение 4-метилфенилового эфира 5-(3-(хлоркарбонил)-5-[(3-хлорфенил)карбониламино]фенилкарбониламино)нафталин-2-сульфоновой кислоты (соединение 79) К 23,4 мг (38,1 мкмоля) соединения 78 прибавляли 0,5 мл тионилхлорида. Суспензию оставляли перемешиваться при температуре окружающей среды в течение 1 ч. Затем прибавляли 1 мл ацетонитрила. Еще через час реакционная смесь оставалась суспензией, поэтому прибавляли 1 мл ТГФ. Реакционная смесь становилась гомогенной в течение часа. После перемешивания в течение дополнительных 30 мин летучие вещества удаляли в вакууме, полученный остаток дважды соупаривали с хлороформом. Получали твердый продукт, который использовали без характеристики. Получение 4-метилфенилового эфира 5-(3-[(3-хлорфенил)карбониламино]-5-[N-(6-гидроксинафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновой кислоты (соединение 81) К 24,1 мг (38,1 мкмоля) соединения 79 прибавляли 10 мл дихлорметана, затем 16,7 мг (105 мкмолей) 5-амино-2-нафтола (80), растворенного в 5 мл смеси дихлорметан:ТГФ, 1:1. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Реакционную смесь экстрагировали этилацетатом и 1 н. водным раствором НСl. Органический слой сушили (MgSO4), фильтровали, летучие вещества удаляли в вакууме. Полученный остаток обрабатывали дихлорметаном и диэтиловым эфиром с образованием желтого раствора и твердого осадка. Твердое вещество собирали фильтрованием в вакууме, получая 15 мг (19,9 мкмоля) требуемого соединения. Продукт идентифицировали с использованием 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ. Получение натриевой соли 5-(3-[(3-хлорфенил)карбониламино]-5-[N-(6-гидроксинафтил)карбамоил]фенилкарбониламино)нафталин-2-сульфоновой кислоты (соединение 82) К 12,0 мг (15,0 мкмолей) соединения 81 прибавляли 400 мкл метанола. К данной перемешиваемой суспензии прибавляли 400 мкл 1,37 М раствора метилата натрия в метаноле. Суспензия быстро становилась гомогенной. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 40 ч. Реакционную смесь подкисляли до рН 1 с 6 н. НСl, летучие вещества удаляли с помощью роторного испарителя. Полученное твердое вещество суспендировали в 0,5 мл воды, твердое вещество собирали центрифугированием. Получали 10 мг (15 мкмолей) требуемого соединения. Продукт идентифицировали с использованием 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ. Пример 10. Синтез дополнительных соединений формулы VIII Модификацией синтезов, описанных в примере 9, с использованием методик, хорошо известных специалистам, получали соединения, представленные ниже в табл. 7. Названия по номенклатуре ИЮПАК соединений, приведенных выше в табл. 7, перечислены ниже в табл. 8. Названия по номенклатуре ИЮПАК получены с использованием программного обеспечения Пример 11. Синтез 5-(-5-[N-(6-карбоксинафтил)карбамоил]-3-[(4-метилфенил)карбониламино]фенилкарбониламино)нафталин-2-карбоновой кислоты (соединение 91) Соединение 91 синтезировали в соответствии с методиками, приведенными на реакционной схеме Реакционная схема V Получение метилового эфира 3-(метоксикарбонил)-5-[(4-метилфенил)карбониламино]бензойной кислоты (соединение 88) К 1,20 г (5,74 ммоля) метилового эфира 5-амино-3-(метоксикарбонил)бензойной кислоты, соединения 87, суспендированного в 50 мл хлороформа и 1,05 мл (6,00 ммолей) диизопропилэтиламина, прибавляли 836 мкл (6,32 ммоля) n-толуилхлорида в 10 мл хлороформа в течение 30 мин. Реакционную смесь оставляли перемешиваться при температуре окружающей среды в течение 2 ч. Затем прибавляли еще 100 мкл (0,60 ммоля) диизопропилэтиламина и 100 мкл (0,76 ммоля) n-толуилхлорида в 2 мл хлороформа. Через 30 мин летучие вещества удаляли с помощью роторного испарителя, полученный остаток растворяли в этилацетате и экстрагировали 0,1 н. водным NaOH с последующей экстракцией водой. Органический слой сушили (MgSO4), фильтровали и удаляли летучие вещества в вакууме. Получали 1,86 г (5,68 ммоля) требуемого соединения. Продукт идентифицировали с помощью 1 Н-ЯМР и масс-спектрометрии,чистоту оценивали с помощью офВЭЖХ. Получение 5-[(4-метилфенил)карбониламино]бензол-1,3-дикарбоновой кислоты (соединение 89) К 1,50 г (4,58 ммоля) соединения 88, суспендированного в 50 мл метанола, прибавляли 11 мл (11 ммолей) 1 М водного раствора LiOH. Суспензию оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Получали почти прозрачный раствор, который фильтровали для удаления небольшого количества нерастворимого материала. Метанол удаляли из фильтрата с помощью роторного испарителя, рН водного раствора снижали до 1 с 1 н. НСl. Образующийся твердый осадок собирали фильтрованием в вакууме и промывали водой. Получали 1,37 г (4,57 ммоля) требуемого соединения. Продукт идентифицировали с помощью 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ.- 28006704 Получение 5-[(4-метилфенил)карбониламино]бензол-1,3-дикарбонилхлорида (соединение 90) К 40,0 мг (13,4 ммоля) соединения 89 прибавляли 2 мл тионилхлорида. Полученную суспензию оставляли перемешиваться в течение 16 ч. Затем прибавляли 100 мкл пиридина. Реакционная смесь становилась прозрачным раствором через 30 мин. Реакционную смесь оставляли при перемешивании в течение дополнительных 4 ч. Летучие вещества удаляли в вакууме, дважды прибавляли и удаляли в вакууме хлороформ (10 мл). Получали твердый продукт, который использовали без характеристики. Получение 5-(5-[N-(6-карбоксинафтил)карбамоил]-3-[(4-метилфенил)карбониламино]фенилкарбониламино)нафталин-2-карбоновой кислоты (соединение 91) К 13,4 ммоля соединения 90, растворенного в 3 мл хлороформа, прибавляли 50,0 мг (26,7 ммоля) 5 амино-2-нафтойной кислоты (см. Price С.С., Michel R.H. J. Amer. Chem. Soc. 74, 3652 (1952, растворенной в 4 мл пиридина. Реакционный раствор оставляли перемешиваться при температуре окружающей среды в течение 16 ч. Прибавляли диэтиловый эфир для образования осадка, который собирали центрифугированием. Данное твердое вещество растворяли в метаноле и оставляли стоять в течение 2 дней. Мелкий осадок собирали центрифугированием, и целевое соединение очищали с помощью офВЭЖХ(буфер А: 5% ацетонитрил, 95% вода, 0,05% ТФУ; буфер Б: 95% ацетонитрил, 5% вода, 0,05% ТФУ). Получали 1,1 мг (1,73 мкмоля) требуемого соединения. Продукт идентифицировали с помощью 1 Н-ЯМР и масс-спектрометрии, чистоту оценивали с помощью офВЭЖХ. Пример 12. Синтез дополнительных биснафталинсульфоновых кислот Следующие дополнительные соединения, приведенные в табл. 9, получали с использованием методик, описанных в примерах 1-3. Названия по номенклатуре ИЮПАК соединений, приведенных выше в табл. 9, перечислены ниже в табл. 10. Названия по номенклатуре ИЮПАК получены с использованием программного обеспечения Пример 13. Исследование аутофосфорилирования 32 Р-цитоплазматического киназного домена (CKD) Полный -киназный домен человеческого рецептора инсулина (CKD) экспрессировали в бакуловирусе и очищали от него. CKD (4,0 мкг/мл) в растворе, состоящем из 50 мМ трис-НСl, 2 мМ МnСl2, 10 мМMgCl2 (конечный объем 50 мкл), объединяли с 50 мкмолями АТФ и 5 мкКи 32 Р-АТФ (3000 Ки/ммоль). Исследуемое соединение или наполнитель (ДМСО) прибавляли до конечной концентрации ДМСО, составляющей 1%. Смесь инкубировали в течение 10 мин при комнатной температуре. Реакцию прекращали добавлением 10 мкл 200 мМ EDTA (этилендиаминтетрауксусной кислоты). Отбирали 30 мкл объема,смешивали с 5 мкл 6 Х обработочного буфера Laemmeli с додецилсульфатом натрия (SDS) и нагревали до 94 С в течение 5 мин. Затем аликвоту 20 мкл прогоняли в SDS-PAGE (в электрофорезе на полиакриламидном геле с SDS). Радиоактивность, включенную в полосу CKD, определяли количественно проявлением геля на фосфор или счетом вырезанных полос в сцинтилляционной камере. Результаты данного исследования приведены в табл. 11. Эффективность соединения в усилении фосфорилирования выражали в процентах от уровня наполнителя.
МПК / Метки
МПК: C07D 213/82, C07C 311/13, C07C 237/42, C07D 213/81, C07D 307/85, A61K 31/18, C07C 309/51, C07C 311/29, C07C 309/59, C07C 311/21, A61K 31/16
Метки: агонистов, глюкозы, родственные, соединения, качестве, нафтилсульфоновые, поглощения, кислоты
Код ссылки
<a href="https://eas.patents.su/30-6704-naftilsulfonovye-kisloty-i-rodstvennye-soedineniya-v-kachestve-agonistov-pogloshheniya-glyukozy.html" rel="bookmark" title="База патентов Евразийского Союза">Нафтилсульфоновые кислоты и родственные соединения в качестве агонистов поглощения глюкозы</a>
Следующий патент: Антитела против vla-1
Случайный патент: Устройство для тренировки мышц