Оксаминовые кислоты и их производные в качестве лигандов тиреоидных рецепторов
Формула / Реферат
1. Соединение формулы
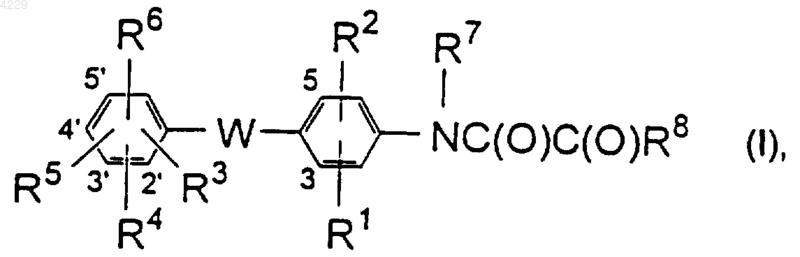
его пролекарство, его геометрический или оптический изомер либо фармацевтически приемлемая соль указанного соединения, указанного пролекарства или указанного изомера,
где R1, R2 и R3, каждый независимо, представляет собой водород, галоген, C1-6алкил, трифторометил, -CN, -OCF3 или -OC1-6алкил;
R4 представляет собой водород, C1-12алкил, возможно замещенный заместителями в количестве от одного до трех, независимо выбранными из группы Z, C2-12алкенил, галоген, -CN, арил, гетероарил, C3-10циклоалкил, гетероциклоалкил, -S(O)2NR9R10, -C(O)NR9R10, -(C1-6алкил)-NR9R10, -NR9C(O)R10, -NR9C(O)NR9R10, -NR9S(O)2R10, -(C1-6алкил)-OR11, -OR11 или -S(O)aR12, при условии, что если R5 не является фторо, то R4 представляет собой -S(O)2NR9R10, -C(O)NR9R10, -(C1-6алкил)-NR9R10, -NR9C(O)R10, -NR9C(O)NR9R10, -NR9S(O)2R10 -(C1-6алкил)-OR11, -OR11 или -S(O)aR12;
либо R3 и R4 могут быть взяты вместе с образованием карбоциклического кольца A формулы -(CH2)b- или гетероциклического кольца A, выбранного из группы, состоящей из -Q-(CH2)c- и -(CH2)j-Q-(CH2)k-, где Q представляет собой O, S или NR17, где указанное карбоциклическое кольцо A и указанное гетероциклическое кольцо A, каждое независимо, возможно замещено одним или более чем одним заместителем, независимо выбранным из C1-4алкила, галогенида или оксо;
R5 представляет собой фторо, гидрокси, C1-4алкокси или OC(O)R9;
либо R4 и R5 могут быть взяты вместе с образованием гетероциклического кольца B, выбранного из группы, состоящей из -CR9=CR10-NH-, -N=CR9-NH-, -CR9=CH-O- и -CR9=CH-S-;
R6 представляет собой водород, галоген, C1-4алкил или трифторометил;
R7 представляет собой водород или C1-6алкил;
R8 представляет собой -OR9 или -NR19R20;
R9 и R10 для каждого случая независимо представляют собой (А) водород, (Б) C1-12алкил, возможно замещенный одним или более чем одним заместителем, независимо выбранным из группы V, (В) C2-12алкенил, (Г) C3-10циклоалкил, возможно замещенный одним или более чем одним заместителем, независимо выбранным из C1-6алкила, C2-5алкинила, C3-10циклоалкила, -CN, -NR13R14, оксо, -OR18, -COOR18 или арила, возможно замещенного X и Y, (Д) арил, возможно замещенный X и Y, или (Е) het, возможно замещенный X и Y;
либо R9 и R10 для любого случая могут быть взяты вместе с образованием гетероциклического кольца C, возможно дополнительно содержащего вторую гетерогруппу, выбранную из группы, состоящей из -O-, -NR13- и -S-, и возможно дополнительно замещенного одним или более чем одним заместителем, независимо выбранным из C1-5алкила, оксо, -NR13R14, -OR18, -C(O)2R18, -CN, -C(O)R9, арила, возможно замещенного X и Y, het, возможно замещенного X и Y, C5-6спироциклоалкила и карбоциклического кольца B, выбранного из группы, состоящей из 5-, 6-, 7- и 8-членных частично и полностью насыщенных и ненасыщенных карбоциклических колец, включая любую бициклическую группу, в которой указанное карбоциклическое кольцо B конденсировано с карбоциклическим кольцом C, выбранным из группы, состоящей из 5-, 6-, 7- и 8-членных частично и полностью насыщенных и ненасыщенных карбоциклических колец;
R11 представляет собой C1-12алкил, возможно замещенный одним или более чем одним заместителем, независимо выбранным из группы V, C2-12алкенил, C3-10циклоалкил, трифторометил, дифторометил, монофторометил, арил, возможно замещенный X и Y, het, возможно замещенный X и Y, -C(O)NR9R10 или -C(O)R9;
R12 представляет собой C1-12алкил, возможно замещенный одним или более чем одним заместителем, независимо выбранным из группы V, C2-12алкенил, C3-10циклоалкил, арил, возможно замещенный X и Y, или het, возможно замещенный X и Y;
R13 и R14 для каждого случая независимо являются водородом, C1-6алкилом, C2-6алкенилом, -(C1-6алкил)-C1-6алкокси, арилом, возможно замещенным X и Y, het, возможно замещенным X и Y, -(C1-4алкил)арилом, возможно замещенным X и Y, -(C1-4алкил)гетероциклом, возможно замещенным X и Y, -(C1-4алкил)гидрокси, -(C1-4алкил)галогено, -(C1-4алкил)полигалогено, -(C1-4алкил)-CONR15R16 или C3-10циклоалкилом;
R15 и R16 для каждого случая независимо представляют собой водород, C1-6алкил, C3-10циклоалкил или арил, возможно замещенный X и Y;
R17 представляет собой водород, C1-6алкил, -COR9 или -SO2R9;
R18 является водородом, C1-6алкилом, C2-6алкенилом, -(C1-6алкил)-C1-6алкокси, арилом, возможно замещенным X и Y, het, возможно замещенным X и Y, -(C1-4алкил)арилом, возможно замещенным X и Y, -(C1-4алкил)гетероциклом, возможно замещенным X и Y, -(C1-4алкил)гидрокси, -(C1-4алкил)галогено, -(C1-4алкил)полигалогено, -(C1-4алкил)-CONR15R16, -(C1-4алкил)-(C1-4алкокси) или C3-10циклоалкилом;
R19 представляет собой водород или C1-6алкил;
R20 представляет собой водород или C1-6алкил;
W представляет собой O, S(O)d, CH2 или NR9;
группа Z представляет собой C2-6алкенил, C2-6алкинил, галоген, -CF3, -OCF3, гидрокси, оксо, -CN, арил, гетероарил, C3-10циклоалкил, гетероциклоалкил, -S(O)aR12, -S(O)2NR9R10, -C(O)R9R10 и -NR9R10;
группа V представляет собой галоген, -NR13R14, -OCF3, -OR9, оксо, трифторометил, -CN, C3-10циклоалкил, арил, возможно замещенный X и Y, и het, возможно замещенный X и Y;
het для каждого случая представляет собой гетероциклическое кольцо D, выбранное из группы, состоящей из 4-, 5-, 6-, 7- и 8-членных, частично и полностью насыщенных и ненасыщенных гетероциклических колец, содержащих от одного до четырех гетероатомов, независимо выбранных из группы, состоящей из N, O и S, включая любую бициклическую группу, в которой указанное гетероциклическое кольцо D конденсировано с бензольным кольцом или с гетероциклическим кольцом E, выбранным из группы, состоящей из 4-, 5-, 6-, 7- и 8-членных, частично и полностью насыщенных и ненасыщенных гетероциклических колец, содержащих от одного до четырех гетероатомов, независимо выбранных из группы, состоящей из N, O и S;
X и Y для каждого случая независимо представляют собой (А) водород, (Б) галоген, (В) трифторметил, (Г) -OCF3, (Д) -CN, (Е) C1-6алкил, возможно замещенный одним или более чем одним заместителем, независимо выбранным из группы, состоящей из галогена, -OCF3, -CF3 и фенила, (Ж) C1-6 алкокси, (З) арил, возможно замещенный одним или более чем одним заместителем, независимо выбранным из группы, состоящей из галогена, -OCF3, -CF3, C1-4алкила и C1-4алкокси, (И) -C(O)2R13, (К) -C(O)NR13R14, (Л) -C(O)R13, (M) -NR13C(O)NR13R14 и (Н) -NR13C(O)R14;
либо X и Y для любого случая в одном и том же варианте могут быть взяты вместе с образованием (а) карбоциклического кольца D формулы -(CH2)e- или (б) гетероциклического кольца F, выбранного из группы, состоящей из -O(CH2)fO-, -(CH2)gNH- и -CH=CHNH-;
a и d, каждый независимо, составляет 0, 1 или 2;
b составляет 3, 4, 5, 6 или 7;
c, f, g, j и k, каждый независимо, составляет 2, 3, 4, 5 или 6 и
e составляет 3, 4, 5, 6 или 7.
2. Соединение или фармацевтически приемлемая соль по п.1, где W представляет собой кислород.
3. Соединение или фармацевтически приемлемая соль по п.2, где R1 находится в положении 3, R2 находится в положении 5, R3 находится в положении 2', R4 находится в положении 3', R5 находится в положении 4' и R6 находится в положении 5'.
4. Соединение или фармацевтически приемлемая соль по п.3, где R1 и R2, каждый независимо, представляет собой водород, C1-6алкил, бромо или хлоро, R3 представляет собой водород, R4 представляет собой -C(O)NR9R10, -S(O)2NR9R10 или S(O)aR12, либо R3 и R4 взяты вместе с образованием указанного карбоциклического кольца A формулы -(CH2)b- или указанного гетероциклического кольца A, выбранного из группы, состоящей из -Q-(CH2)c- и -(CH2)j-Q-(CH2)k-, где Q представляет собой O, S или NR17, где указанное карбоциклическое кольцо A и указанное гетероциклическое кольцо A, каждое независимо, возможно замещено одним или более чем одним заместителем, независимо выбранным из C1-4алкила, галогенида или оксо, R5 представляет собой фторо или гидрокси, R8 представляет собой гидрокси, метокси, этокси, изопропокси, NH2 или NH(CH3), R6 и R7 каждый представляет собой водород.
5. Соединение или фармацевтически приемлемая соль по п.4, где R3 и R4 взяты вместе с образованием указанного карбоциклического кольца A формулы -(CH2)b-, возможно замещенного одним или более чем одним заместителем, независимо выбранным из C1-4алкила, галогенида или оксо.
6. Соединение или фармацевтически приемлемая соль по п.5, где R1 и R2, каждый независимо, представляет собой метил или хлоро, R3 и R4, взятые вместе, образуют -(CH2)3-, -CH2-C(CH3)2-CH2- или -(CH2)4-, R5 представляет собой гидрокси и R8 представляет собой гидрокси или этокси.
7. Соединение или фармацевтически приемлемая соль по п.4, где R4 представляет собой -C(O)NR9R10.
8. Соединение или фармацевтически приемлемая соль по п.7, где R1 и R2, каждый независимо, представляет собой метил или хлоро, R5 представляет собой гидрокси, R8 представляет собой гидрокси или этокси, R9 представляет собой метил, этил, изопропил, н-пропил, изобутил, н-бутил, н-пентил, н-гексил, 4-фторофенил, -CH2-2-тиенил, циклопропил, -CH2-циклопропил, циклобутил, циклопентил, циклогексил, -CH2-циклогексил, эндо-2-норборнил, экзо-2-норборнил, (S)-1-фенилэтил, (R)-1-фенилэтил, -CH2-2-хлорофенил, -CH2-4-хлорофенил, -CH2-4-фторофенил, -CH2-3-хлоро-4-фторофенил, -CH2-2-хлоро-4-фторофенил, -CH2-2-фторо-4-хлорофенил, -CH2-3,4-дифторофенил, -CH2-4-изопропилфенил, -CH2-2,3-дихлорофенил, -CH2-2,4-дихлорофенил, -CH2-3,4-дихлорофенил, -CH2-3-трифторометил-4-хлорофенил, 4-фенилфенил, 3-(2,4-диметил)пентил, (R)-1-(1-нафтил)этил, 1,1-диметилпропил, 1,2-диметилпропил, 2,2-диметилпропил, (R)-1-(2-нафтил)этил, (R)-2-(1-нафтил)этил, -CH2-(1-нафтил), (R)-1-циклогексилэтил, (S)-1-циклогексилэтил, -CH2-3,4-метилендиоксифенил, -CH2-4-трет-бутилфенил, -CH2-2,3-дихлорфенил, 1-инданил, (R)-1-инданил, (S)-1 -инданил, 5-инданил, 1-(1,2,3,4-тетрагидронафтил) или (R)-1-циклогексилэтил и R10 представляет собой водород, метил или этил, либо R9 и R10 взяты вместе с атомом азота, к которому они присоединены, с образованием N(CH2)7, N(CH2)6, N(CH2)5, N(CH2)4, морфолина,
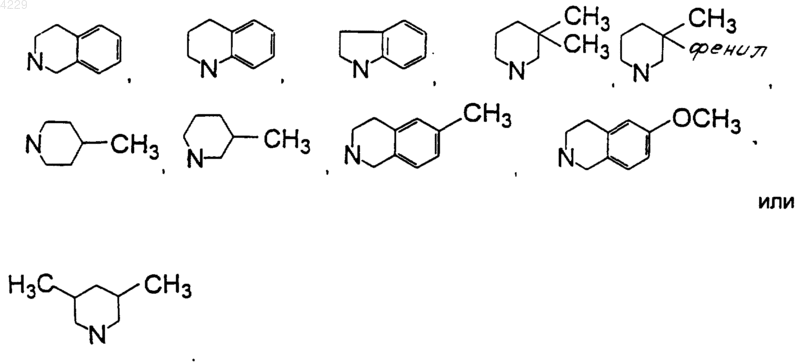
9. Соединение или фармацевтически приемлемая соль по п.4, где R4 представляет собой -S(O)2NR9R10.
10. Соединение или фармацевтически приемлемая соль по п.9, где R1 и R2, каждый независимо, представляет собой метил или хлоро, R8 представляет собой гидрокси, изопропокси или этокси, R9 представляет собой водород, изопропил, -CH2-2-тиенил, -CH2-циклопропил, циклопропил, -(CH2)2OH, экзо-2-норборнил, метил, этил, 4-фторофенил, циклобутил, циклопентил, циклогексил, н-пропил, н-бутил, н-пентил, н-гексил, н-октил или н-децил и R10 представляет собой водород или метил, либо R9 и R10 взяты вместе с атомом азота, к которому они присоединены, с образованием N(CH2)4, N(CH2)5, морфолина или

11. Соединение или фармацевтически приемлемая соль по п.4, где R4 представляет собой -S(O)aR12.
12. Соединение или фармацевтически приемлемая соль по п.11, где R1 и R2, каждый независимо, представляет собой метил или хлоро, R8 представляет собой гидрокси или этокси и R12 представляет собой 4-хлорофенил, фенил, 1-нафтил, 2-нафтил, CH2-циклопропил, изопропил, CH2-циклобутил, CH2-циклогексил, циклопентил, CH2-4-фторофенил, 4-толил, метил, этил, н-бутил, CH2-фенил или н-пропил.
13. Фармацевтически приемлемая соль по п.6, где указанная соль представляет собой соль натрия или соль калия.
14. Фармацевтически приемлемая соль по п.8, где указанная соль представляет собой соль натрия или соль калия.
15. Фармацевтически приемлемая соль по п.10, где указанная соль представляет собой соль натрия или калия.
16. Фармацевтически приемлемая соль по п.12, где указанная соль представляет собой соль натрия или калия.
17. Соединение, пролекарство, изомер или фармацевтически приемлемая соль по п.1, где указанное соединение выбрано из группы, состоящей из
N-[3-хлоро-4-(3-циклопропилсульфамоил-4-гидроксифенокси)-5-метилфенил]оксаминовой кислоты,
N-[4-(3-циклопропилсульфамоил-4-гидроксифенокси)-3,5-диметилфенил]оксаминовой кислоты,
N-{4-[3-(циклобутилметилкарбамоил)-4-гидроксифенокси]-3,5-диметилфенил}оксаминовой кислоты,
N-{3-хлоро-4-[3-(циклобутилметилкарбамоил)-4-гидроксифенокси]-5-метилфенил}оксаминовой кислоты,
N-[4-(7-гидроксииндан-4-илокси)-3,5-диметилфенил]оксаминовой кислоты,
N-{3,5-дихлоро-4-[3-(циклобутилметилкарбамоил)-4-гидроксифенокси]фенил}оксаминовой кислоты,
N-[3,5-дихлоро-4-(3-циклопентансульфонил-4-гидроксифенокси)фенил]оксаминовой кислоты,
N-[3,5-дихлоро-4-(3-циклопропилметансульфонил-4-гидроксифенокси)фенил]оксаминовой кислоты,
N-[3,5-дихлоро-4-(3-циклобутилметансульфонил-4-гидроксифенокси)фенил]оксаминовой кислоты,
N-[4-(3-циклопропилметансульфонил-4-гидроксифенокси)-3,5-диметилфенил]оксаминовой кислоты,
N-[3-хлоро-4-(3-циклобутилметансульфонил-4-гидроксифенокси)-5-метилфенил]оксаминовой кислоты,
N-[4-(3-циклобутилметансульфонил-4-гидроксифенокси)-3,5-диметилфенил]оксаминовой кислоты,
N-[4-(3-циклопентилметансульфонил-4-гидроксифенокси)-3,5-диметилфенил]оксаминовой кислоты,
N-[3-хлоро-4-(3-циклопентилметансульфонил-4-гидроксифенокси)-5-метилфенил]оксаминовой кислоты,
N-[3,5-дихлоро-4-(3-циклопентилметансульфонил-4-гидроксифенокси)фенил]оксаминовой кислоты,
N-[4-(3-циклогексилметансульфонил-4-гидроксифенокси)-3,5-диметилфенил]оксамиковой кислоты,
N-[3-хлоро-4-(3-циклогексилметансульфонил-4-гидроксифенокси)-5-метилфенил]оксаминовой кислоты,
N-[3,5-дихлоро-4-(3-циклогексилметансульфонил-4-гидроксифенокси)фенил]оксаминовой кислоты,
N-[3,5-дихлоро-4-[3-(4-фторобензолсульфонил)-4-гидроксифенокси)фенил]оксаминовой кислоты,
N-{4-[3-(4-фторобензолсульфонил)-4-гидроксифенокси]-3,5-диметилфенил}оксаминовой кислоты и
N-{3-хлоро-4-[3-(4-фторобензолсульфонил)-4-гидроксифенокси]-5-метилфенил}оксаминовой кислоты.
18. Фармацевтически приемлемая соль по п.17, где указанная соль представляет собой соль натрия или соль калия.
19. Соединение или фармацевтически приемлемая соль по п.1, где указанное соединение выбрано из группы, состоящей из
N-[3-хлоро-4-(3-циклопропилсульфамоил-4-гидроксифенокси)-5-метилфенил]оксаминовой кислоты этилового эфира,
N-[4-(3-циклопропилсульфамоил-4-гидроксифенокси)-3,5-диметилфенил]оксаминовой кислоты этилового эфира,
N-{4-[3-(циклобутилметилкарбамоил)-4-гидроксифенокси]-3,5-диметилфенил}оксаминовой кислоты этилового эфира,
N-{3-хлоро-4-[3-(циклобутилметилкарбамоил)-4-гидроксифенокси]-5-метилфенил}оксаминовой кислоты этилового эфира,
N-[4-(7-гидроксииндан-4-илокси)-3,5-диметилфенил]оксаминовой кислоты этилового эфира,
N-{3,5-дихлоро-4-[3-(циклобутилметилкарбамоил)-4-гидроксифенокси]фенил}оксаминовой кислоты этилового эфира,
N-[3,5-дихлоро-4-(3-циклопентансульфонил-4-гидроксифенокси)фенил]оксаминовой кислоты этилового эфира,
N-[3,5-дихлоро-4-(3-циклопропилметансульфонил-4-гидроксифенокси)фенил]оксаминовой кислоты этилового эфира,
N-[3,5-дихлоро-4-(3-циклобутилметансульфонил-4-гидроксифенокси)фенил]оксаминовой кислоты этилового эфира,
N-[4-(3-циклопропилметансульфонил-4-гидроксифенокси)-3,5-диметилфенил]оксаминовой кислоты этилового эфира,
N-[3-хлоро-4-(3-циклобутилметансульфонил-4-гидроксифенокси)-5-метилфенил]оксаминовой кислоты этилового эфира,
N-[4-(3-циклобутилметансульфонил-4-гидроксифенокси)-3,5-диметилфенил]оксаминовой кислоты этилового эфира,
N-[4-(3-циклопентилметансульфонил-4-гидроксифенокси)-3,5-диметилфенил]оксаминовой кислоты этилового эфира,
N-[3-хлоро-4-(3-циклопентилметансульфонил-4-гидроксифенокси)-5-метилфенил]оксаминовой кислоты этилового эфира,
N-[3,5-дихлоро-4-(3-циклопентилметансульфонил-4-гидроксифенокси)фенил]оксаминовой кислоты этилового эфира,
N-[4-(3-циклогексилметансульфонил-4-гидроксифенокси)-3,5-диметилфенил]оксаминовой кислоты этилового эфира,
N-[3-хлоро-4-(3-циклогексилметансульфонил-4-гидроксифенокси)-5-метилфенил]оксаминовой кислоты этилового эфира,
N-[3,5-дихлоро-4-(3-циклогексилметансульфонил-4-гидроксифенокси)фенил]оксаминовой кислоты этилового эфира,
N-[3,5-дихлоро-4-[3-(4-фторобензолсульфонил)-4-гидроксифенокси]фенил]оксаминовой кислоты этилового эфира,
N-{4-[3-(4-фторобензолсульфонил)-4-гидроксифенокси]-3,5-диметилфенил}оксаминовой кислоты этилового эфира и
N-{3-хлоро-4-[3-(4-фторобензолсульфонил)-4-гидроксифенокси]-5-метилфенил}оксаминовой кислоты этиловый эфир.
20. Способ лечения состояния, выбранного из группы, состоящей из ожирения, гиперлипидемии, глаукомы, сердечной аритмии, кожных расстройств, заболевания щитовидной железы, гипотиреоза, сахарного диабета, атеросклероза, гипертензии, ишемической болезни сердца, гиперхолестеринемии, депрессии и остеопороза, у млекопитающего, при котором указанному млекопитающему вводят эффективное лечебное количество соединения, пролекарства, изомера или фармацевтически приемлемой соли по п.1.
21. Способ по п.20, где указанное состояние представляет собой ожирение.
22. Способ по п.20, при котором дополнительно вводят агент, снижающий аппетит, или ингибитор липазы.
23. Фармацевтическая композиция, содержащая соединение, пролекарство, изомер или фармацевтически приемлемую соль по п.1 и фармацевтически приемлемый наполнитель, разбавитель или носитель.
24. Фармацевтическая композиция для лечения состояния, выбранного из группы, состоящей из ожирения, гиперлипидемии, глаукомы, сердечной аритмии, кожных расстройств, заболевания щитовидной железы, гипотиреоза, сахарного диабета, атеросклероза, гипертензии, ишемической болезни сердца, гиперхолестеринемии, депрессии и остеопороза, у млекопитающего, содержащая соединение, пролекарство, изомер или фармацевтически приемлемую соль по п.1 и фармацевтически приемлемый наполнитель, разбавитель или носитель.
25. Фармацевтическая композиция по п.24, где указанное состояние представляет собой ожирение.
26. Фармацевтическая композиция по п.24, дополнительно включающая в себя агент, снижающий аппетит, или ингибитор липазы.
27. Набор для лечения состояния, выбранного из группы, состоящей из ожирения, гиперлипидемии, глаукомы, сердечной аритмии, кожных расстройств, заболевания щитовидной железы, гипотиреоза, сахарного диабета, атеросклероза, гипертензии, ишемической болезни сердца, гиперхолестеринемии, депрессии и остеопороза, который содержит первое соединение, представляющее собой соединение, пролекарство, изомер или фармацевтически приемлемую соль по п.1, и фармацевтически приемлемый наполнитель, носитель или разбавитель, в первой стандартной лекарственной форме; второе соединение, представляющее собой агент, снижающий аппетит, или ингибитор липазы и фармацевтически приемлемый наполнитель, носитель или разбавитель, во второй стандартной лекарственной форме; и контейнер.
28. Набор по п.27, где указанное состояние представляет собой ожирение.
Текст
1 Область изобретения Настоящее изобретение относится к новым лигандам тиреоидных рецепторов и, более конкретно, - к новым оксаминовым кислотам и их производным, которые полезны в лечении ожирения, гиперлипидемии, глаукомы, сердечной аритмии, кожных расстройств, заболевания щитовидной железы, гипотиреоза и родственных расстройств и заболеваний, таких как сахарный диабет, атеросклероз, гипертензия, ишемическая болезнь сердца, гиперхолестеринемия, депрессия и остеопороз. Предложены также способы,фармацевтические композиции и наборы для лечения таких заболеваний и расстройств. Предпосылки изобретения Считается общепринятым, что тиреоидные гормоны, а именно биологически активные иодотиронины, существенны для нормального развития и для поддержания метаболического гомеостаза. Тиреоидные гормоны стимулируют метаболизм холестерина до желчных кислот и усиливают липолитические ответы жировых клеток на другие гормоны. Тиреоидные гормоны влияют также на сердечную функцию как прямо, так и косвенно,то есть посредством повышения скорости метаболизма. Например, тахикардию, повышенный ударный объем сердца, повышенный сердечный индекс, сердечную гипертрофию, пониженное периферическое сосудистое сопротивление и повышенное пульсовое артериальное давление наблюдают у пациентов с гипертиреозом. Расстройства щитовидной железы, как правило, лечат гормональным замещением путем введения либо встречающихся в природе тиреоидных гормонов, либо их тиреомиметических аналогов, которые имитируют эффекты тиреоидных гормонов. Ниже показаны два встречающихся в природе тиреоидных гормона, а именно тироксин или 3,5,3',5'-тетраиодо-L-тиронин (обычно называемый Т 4) и 3,5,3'-трииодо-L-тиронин Т 3 является более биологически активным из этих двух гормонов, и, как должно быть понятно из представленных выше структурных формул, отличается от Т 4 отсутствием 5'-иода. Т 3 можно получить непосредственно из щитовидной железы, либо в периферических тканях путем удаления 5'-иода ферментами деиодиназами. Тиреомиметические аналоги часто конструируют так, чтобы они были структурно подобны Т 3. Кроме того, известны встречающиеся в природе метаболиты Т 3. Как обсуждалось выше, тиреоидные гормоны влияют на сердечную деятельность, например, вызывая повышение частоты сердечных 2 сокращений и, соответственно, повышение потребления кислорода. Хотя повышение потребления кислорода может приводить в результате к некоторым желательным метаболическим эффектам, тем не менее оно приводит к чрезмерной нагрузке на сердце, которая в некоторых ситуациях может вызывать вредные побочные эффекты. Вследствие этого, как известно в данной области техники, например, как описано А.Н. Underwood et al. в статье, опубликованной в Nature, Vol. 324: pp. 425-429 (1986), были предприняты попытки синтезировать аналоги тиреоидных гормонов, функция которых состоит в том, чтобы снижать липиды и сывороточный холестерин, не производя вредных сердечных эффектов, упомянутых выше. В патентах США 4766121; 4826876; 4910305 и 5061798 описаны некоторые миметики тиреоидных гормонов, а именно 3,5 дибромо-3'-[6-оксо-3(1 Н)-пиридазинилметил]тиронины. В патенте США 5284971 описаны некоторые тиреомиметические агенты, снижающие холестерин, а именно соединения 4-(3-циклогексил-4-гидрокси или -метоксифенилсульфонил)-3,5-дибромофенилуксусной кислоты. В патентах США 5401772; 5654468 и 5569674 описаны некоторые агенты, снижающие липиды, а именно производные гетероуксусной кислоты, которые конкурируют с меченным радиоактивным изотопом Т 3 в анализах связывания, в которых используют препараты ядер печени крыс и плазматических мембран. Некоторые оксаминовые кислоты и их производные известны в данной области техники, например, в патенте США 4069343 описано применение некоторых оксаминовых кислот для предупреждения реакций гиперчувствительности немедленного типа; в патенте США 4554290 описано применение некоторых оксаминовых кислот для борьбы с паразитами и вредителями животных и растений; в патенте США 5401772 описано применение некоторых оксаминовых кислот в качестве агентов, снижающих липиды; в патенте США 5232947 описано применение некоторых оксаминовых кислот для улучшения поврежденных церебральных функций головного мозга; и в описании к европейскому патенту, опубликованному как ЕР 580550, описаны некоторые производные оксаминовой кислоты в качестве гипохолестеринемических агентов. Кроме того, в данной области техники известны некоторые оксаминовокислотные производные тиреоидных гормонов. Например, N.(1995), описывают замену -СН 2 группы во встречающемся в природе метаболите Т 3 -NH группой, что дает в результате -HNCOCO2H. Также R.E. Steele et al. в статье, опубликованной в International Congressional Service (Atheroscle 3rosis X) 1066: 321-324 (1995), и Z.F. Stephan et al. в статье, опубликованной в Atherosclerosis, 126: 53-63 (1996), описывают некоторые производные оксаминовой кислоты, полезные в качестве тиреомиметических агентов, снижающих липиды, и лишенные нежелательных сердечных активностей. Все документы, цитируемые здесь, включая упомянутые выше, включены здесь путем ссылки в их полном объеме. Краткое изложение сущности иззобретения В настоящем изобретении предложены соединения формулы I их пролекарства, их геометрические и оптические изомеры, а также фармацевтически приемлемые соли указанных соединений, указанных пролекарств и указанных изомеров, гдеR4 представляет собой водород, С 1-12 алкил,возможно замещенный заместителями в количестве от одного до трех, выбранными из группы-S(O)2NR9R10, -C(O)NR9R10, -(C1-6 алкил)-NR9R10,-NR9C(O)R10, -NR9C(O)NR9R10, -NR9S(O)2R10,-(С 1-6 алкил)-ОR11, -OR11 или -S(O)aR12; либо R3 и R4 могут быть взяты вместе с образованием карбоциклического кольца А формулы -(СН 2)b- или гетероциклического кольца А, выбранного из группы, состоящей из-Q-(CH2)c- и -(CH2)j-Q-(CH2)k-, где Q представляет собой О, S или NR17, где указанное карбоциклическое кольцо А и указанное гетероциклическое кольцо А каждое независимо возможно замещено одним или более чем одним заместителем, независимо выбранным из С 1-4 алкила,галогенида или оксо;R5 представляет собой фторо, гидрокси,С 1-4 алкокси или OC(O)R9; либо R4 и R5 могут быть взяты вместе с образованием гетероциклического кольца В, выбранного из группы,состоящей изR7 представляет собой водород или C1-6 алкил;R9 и R10 для каждого случая независимо представляют собой (А) водород, (Б) С 1-12 алкил,возможно замещенный одним или более чем одним заместителем, независимо выбранным из группы V, (В) С 2-12 алкенил, (Г) С 3-10 циклоалкил,возможно замещенный одним или более чем одним заместителем, независимо выбранным изC1-6 алкила, С 2-5 алкинила, С 3-10 циклоалкила,-CN,-NR13R14, оксо, -OR18, -COOR18 или арила,возможно замещенного Х и Y, (Д) арил, возможно замещенный Х и Y или (Е) het, возможно замещенный Х и Y; либо R9 и R10 для каждого случая могут быть взяты вместе с образованием гетероциклического кольца С, возможно дополнительно содержащего вторую гетерогруппу, выбранную из группы, состоящей из -О-, -NR13- и -S-, и возможно дополнительно замещенного одним или более чем одним заместителем, независимо выбранным из С 1-5 алкила, оксо, -NR13R14, -OR18,-C(O)2R18, -CN, -C(O)R9, арила, возможно замещенного X и Y, het, возможно замещенного Х иY, С 5-6 спироциклоалкила и карбоциклического кольца В, выбранного из группы, состоящей из 5-, 6-, 7- и 8-членных частично или полностью насыщенных и ненасыщенных карбоциклических колец, включая любую бициклическую группу, в которой указанное карбоциклическое кольцо В конденсировано с карбоциклическим кольцом С, выбранным из группы, состоящей из 5-, 6-, 7- и 8-членных частично или полностью насыщенных и ненасыщенных карбоциклических колец;R11 представляет собой C1-12 алкил, возможно замещенный одним или более чем одним заместителем, независимо выбранным из группы V, С 2-12 алкенил, С 3-10 циклоалкил, трифторометил, дифторометил, монофторометил, арил,возможно замещенный Х и Y, или het, возможно замещенный Х и Y, -С(O)NR9R10 илиR12 представляет собой С 1-12 алкил, возможно замещенный одним или более чем одним заместителем, независимо выбранным из группы V, C2-12 алкенил, С 3-10 циклоалкил, арил, возможно замещенный Х и Y, или het, возможно замещенный Х и Y;R13 и R14 для каждого случая независимо являются собой водородом, C1-6 алкилом, С 2-6 алкенилом, -(С 1-6 алкил)-С 1-6 алкокси, арилом,возможно замещенным Х и Y, het, возможно,замещенным Х и Y, -(С 1-4 алкил)арилом, возможно замещенным Х и Y, -(С 1-4 алкил)гетероциклом, возможно замещенным Х и Y, -(C1-4 алкил)гидрокси, -(С 1-4 алкил)галогено, -(С 1-4 алкил)полигалогено, -(С 1-4 алкил)-СОNR15R16 или С 3-10 циклоалкилом;R15 и R16 для каждого случая независимо представляют собой водород, С 1-6 алкил, С 3-10 циклоалкил или арил, возможно замещенный Х и Y;R19 представляет собой водород или С 1-6 алкил;R20 представляет собой водород или C1-6 алкил;het для каждого случая представляет собой гетероциклическое кольцо D, выбранное из группы, состоящей из 4-, 5-, 6-, 7- и 8-членных частично или полностью насыщенных и ненасыщенных гетероциклических колец, содержащих от одного до четырех гетероатомов, независимо выбранных из группы, состоящей из N,О и S, включая любую бициклическую группу, в которой указанное гетероциклическое кольцо D конденсировано с бензольным кольцом или с гетероциклическим кольцом Е, выбранным из группы, состоящей из 4-, 5-, 6-, 7- и 8-членных частично или полностью насыщенных и ненасыщенных гетероциклических колец, содержащих от одного до четырех гетероатомов, независимо выбранных из группы, состоящей из N,О и S; Х и Y для каждого случая независимо представляют собой (А) водород, (Б) галоген,(В) трифторометил, (Г) -ОСF3, (Д) -CN, (Е) C1-6 алкил, возможно замещенный одним или более чем одним заместителем, независимо выбранным из группы, состоящей из галогена, -ОСF3,-СF3 и фенила, (Ж) C1-6 алкокси, (З) арил, возможно замещенный одним или более чем одним заместителем, независимо выбранным из группы, состоящей из галогена, -OCF3, -СF3, С 1-4 алкила и С 1-4 алкокси, (И) -C(O)2R13, (К)Y для любого случая в одном и том же варианте могут быть взяты вместе с образованием (а) карбоциклического кольца D формулы -(СН 2)eили (б) гетероциклического кольца F, выбранного из группы, состоящей из -O(CH2)fO-,-(CH2)gNH- и -СН=СНNН-;b составляет 3, 4, 5, 6 или 7; с, f, g, j и k каждый независимо составляет 2, 3, 4, 5 или 6; и е составляет 3, 4, 5, 6 или 7. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений, обозначенная как группа А, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где W представляет собой О. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы А, обозначенная как группа Б,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R1 находится в положении 3, R2 находится в положении 5, R3 находится в положении 2', R4 находится в положении 3',R5 находится в положении 4', и R6 находится в положении 5'. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Б, обозначенная как группа В,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R3 представляет собой водород, либо R3 и R4 взяты вместе с образованием карбоциклического кольца А формулы-(СН 2)b- или гетероциклического кольца А, выбранного из группы, состоящей из -Q-(СН 2)c- и-(CH2)i-Q-(CH2)k-, где Q представляет собой О, S или NR17, где указанное карбоциклическое кольцо А и указанное гетероциклическое кольцо А каждое независимо возможно замещено одним или более чем одним заместителем, независимо выбранным из С 1-4 алкила, галогенида или оксо, R5 представляет собой гидрокси, R6 представляет собой водород и R7 представляет собой водород. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы В, обозначенная как группа Г,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R1 и R2 каждый независимо представляет собой метил, бромо или хлоро, и R8 представляет собой гидрокси, метокси,этокси, изопропокси, NH2 или NН(СН 3). Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Г, обозначенная как группа Д,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R4 представляет собой-S(O)2NR9R10, и R10 представляет собой водород или метил. Особенно предпочтительными соединениями группы Д являются соединения, где (а)R1 представляет собой хлоро, R2 представляет собой метил, R8 представляет собой этокси или 7 гидрокси, R9 представляет собой этил, и R10 представляет собой водород, (б) R1 представляет собой хлоро, R2 представляет собой метил, R8 представляет собой этокси или гидрокси, R9 представляет собой н-бутил, и R10 представляет собой водород, (в) R1 представляет собой хлоро,R2 представляет собой метил, R8 представляет собой этокси или гидрокси, R9 представляет собой -СН 2-циклопропил, и R10 представляет собой водород; и (г) R1 представляет собой хлоро, R2 представляет собой метил, R8 представляет собой изопропокси или гидрокси, R9 представляет собой циклопропил, и R10 представляет собой водород; и фармацевтически приемлемые соли указанных соединений. Другая предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Г, обозначенная как группа Е, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R4 представляет собой -S(O)2NR9R10, а R9 и R10 взяты вместе с атомом азота, к которому они присоединены, с образованием N(CH2)4, N(CH2)5, морфолина или Особенно предпочтительными соединениями группы Е являются те, где R9 и R10 взяты вместе с атомом азота, к которому они присоединены, с образованием N(СН 2)4. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Д, обозначенная как группа Ж, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R9 представляет собой водород, изопропил, -СН 2-2-тиенил, -СН 2 циклопропил, циклопропил, -(CH2)2OH, экзо-2 норборнил, метил, этил, 4-фторфенил, циклобутил, циклопентил, циклогексил, н-пропил, нбутил, м-пентил, н-гексил, н-октил или н-децил. Особенно предпочтительными соединениями группы Ж являются соединения, где (а)R1 представляет собой хлоро, R2 представляет собой метил, R8 представляет собой гидрокси или этокси, R9 представляет собой циклопропил, и R10 представляет собой водород, (б) R1 представляет собой метил, R2 представляет собой метил, R8 представляет собой гидрокси или этокси, R9 представляет собой циклопропил, иR10 представляет собой метил, (в) R1 представляет собой метил, R2 представляет собой метил,R8 представляет собой гидрокси или этокси, R9 представляет собой циклобутил, и R10 представляет собой метил, (г) R1 представляет собой метил, R2 представляет собой метил, R8 представляет собой гидрокси или этокси, R9 представляет собой циклопропил, и R10 представляет собой водород, и (д) R1 представляет собой метил, R2 представляет собой метил, R8 представляет собой гидрокси или этокси, R9 представляет собой циклобутил, и R10 представляет собой водород; 8 и фармацевтически приемлемые соли указанных соединений. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Г, обозначенная как группа К,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R4 представляет собой-C(O)NR9R10, и R10 представляет собой водород,метил или этил. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы К, обозначенная как группа Л,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R9 представляет собой метил, этил, изопропил, н-пропил, изобутил, нбутил, н-пентил, н-гексил, 4-фторфенил, -СН 2-2 тиенил, циклопропил, -СН 2-циклопропил, циклобутил, циклопентил, циклогексил, -СН 2-циклогексил, эндо-2-норборнил, экзо-2-норборнил,(S)-1-фенилэтил, (R)-1-фенилэтил, -СН 2-2-хлорофенил, -СН 2-4-хлорофенил, -СН 2-4-фторофенил, -СН 2-3-хлоро-4-фторофенил, -СН 2-2 хлоро-4-фторофенил, -СН 2-2-фторо-4-хлорофенил, -СН 2-3,4-дифторофенил, -СН 2-4-изопропилфенил, -СН 2-2,3-дихлорофенил, -СН 2-2,4 дихлорофенил, -СН 2-3,4-дихлорофенил, -СН 2-3 трифторометил-4-хлорофенил, 4-фенилфенил,3-(2,4-диметил)пентил,(R)-1-(1-нафтил)этил,1,1-диметилпропил, 1,2-диметилпропил, 2,2 диметилпропил, (R)-1-(2-нафтил)этил, (R)-2-(1 нафтил)этил, -СН 2-(1-нафтил), (R)-1-циклогексилэтил, (S)-1-циклогексилэтил, -СН 2-3,4 метилендиоксифенил, -СН 2-4-третбутилфенил,-СН 2-2,3-дихлорфенил, 1-инданил, (R)-1-инданил, (S)-1-инданил, 5-инданил, 1-(1,2,3,4 тетрагидронафтил) или (R)-1-циклогексилэтил. Особенно предпочтительными соединениями группы Л являются соединения, где (а)R1 представляет собой хлоро, R2 представляет собой хлоро, R8 представляет собой гидрокси или этокси, R9 представляет собой 3-(2,4 диметил)пентил, и R10 представляет собой водород, (б) R1 представляет собой метил, R2 представляет собой метил, R8 представляет собой гидрокси или этокси, R9 представляет собой циклопропил, и R10 представляет собой метил,(в) R1 представляет собой метил, R2 представляет собой метил, R8 представляет собой гидрокси или этокси, R9 представляет собой циклобутил,и R10 представляет собой метил, (г) R1 представляет собой метил, R2 представляет собой метил,R8 представляет собой гидрокси или этокси, R9 представляет собой 3-(2,4-диметил)пентил, и R10 представляет собой водород, (д) R1 представляет собой метил, R2 представляет собой метил, R8 представляет собой гидрокси или этокси, R9 представляет собой н-пентил, и R10 представляет собой метил, (ж) R1 представляет собой метил,R2 представляет собой метил, R8 представляет собой гидрокси или этокси, R9 представляет 9 собой изопропил и R10 представляет собой метил, (з) R1 представляет собой метил, R2 представляет собой метил, R8 представляет собой гидрокси, этокси или NH2, R9 представляет собой циклобутил, и R10 представляет собой метил, и (и) R1 представляет собой хлоро, R2 представляет собой хлоро, R8 представляет собой гидрокси или этокси, R9 представляет собой циклобутил, и R10 представляет собой метил; и фармацевтически приемлемые соли указанных соединений. Другая предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений, обозначенная как группа М,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R4 представляет собой-C(O)NR9R10, a R9 и R10 взяты вместе с атомом азота, к которому они присоединены, с образованием N(СН 2)7, N(СН 2)6, N(CH2)5, N(CH2)4,морфолина, Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Г, обозначенная как группа Н,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R4 представляет собой-CH2NR9R10, и R10 представляет собой водород,метил или -СОСН 3. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Н, обозначенная как группа О,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R9 представляет собой метил, н-пропил, изопропил, циклопропил, циклобутил, циклопентил, циклогексил, экзо-2 норборнил, -СН 2-4-фторофенил, -СН 2-4-хлорофенил, -СН 2-4-изопропилфенил, -СН 2-3,4-метилендиоксифенил, (R)-1-(1-нафтил)этил, (R)-1 фенилэтил, (S)-1-фенилэтил, (R)-1-циклогексилэтил, 1-(1,2,3,4-тетрагидронафтил), 1-инданил или -СН 2-(1-нафтил). Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Н, обозначенная как группа П,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R9 и R10 взяты вместе с атомом азота, к которому они присоединены, с образованием N(СН 2)6, морфолина, Предпочтительная группа соединений и фармацевтически приемлемых солей таких со 004229 10 единений группы Г, обозначенная как группа Р,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R4 представляет собой-NHCOR9. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Р, обозначенная как группа С,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R9 представляет собой циклопропил или циклобутил. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Г, обозначенная как группа Т,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R4 представляет собой-S(O)2R12, и R12 представляет собой 4-хлорофенил, фенил, 1-нафтил, 2-нафтил, -СН 2 циклопропил, изопропил, -СН 2-циклобутил,-СН 2-циклогексил, циклопентил, -СН 2-4-фторофенил, 4-толил, метил, этил, н-бутил, -СН 2 фенил или н-пропил. Особенно предпочтительными соединениями группы Т являются соединения, где (а) R1 представляет собой хлоро, R2 представляет собой хлоро, R8 представляет собой гидрокси или этокси, и R12 представляет собой этил, (б) R1 представляет собой хлоро, R2 представляет собой хлоро, R8 представляет собой гидрокси или этокси, и R12 представляет собой -CH2 циклобутил, (в) R1 представляет собой хлоро, R2 представляет собой хлоро, R8 представляет собой гидрокси или этокси, и R12 представляет собой -СН 2-циклогексил, (г) R1 представляет собой хлоро, R2 представляет собой хлоро, R8 представляет собой гидрокси или этокси, и R12 представляет собой циклопентил, (д) R1 представляет собой хлоро, R2 представляет собой хлоро, R8 представляет собой гидрокси или этокси, и R12 представляет собой -СН 2 циклопропил, (е) R1 представляет собой хлоро,R2 представляет собой хлоро, R8 представляет собой гидрокси или этокси, и R12 представляет собой -СН 2-циклобутил, и (ж) R1 представляет собой метил, R2 представляет собой метил, R8 представляет собой гидрокси или этокси, и R12 представляет собой -СН 2-циклопропил; и фармацевтически приемлемые соли указанных соединений. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Б, обозначенная как группа У,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R1 и R2 каждый независимо представляет собой метил, бромо или хлоро, R3 представляет собой водород, R4 и R5 взяты вместе с образованиемR6 представляет собой водород, R7 представляет собой водород, R8 представляет собой этокси, гидрокси или NH2, и R10 представляет собой водород или метил. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Г, обозначенная как группа Ф,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R3 представляет собой водород, и R4 представляет собой -OR11. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы У, обозначенная как группа X,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R11 представляет собой фенил, 4-хлорофенил или 4-фторофенил. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Г, обозначенная как группа Ц,содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R3 представляет собой водород, и R4 представляет собой -(C1-6 алкил)OR11. Особенно предпочтительными соединениями группы Ц являются соединения, где R4 представляет собой -СН 2-OR11. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Ц, обозначенная как группа Ш, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R11 представляет собой фенил или 4-фторофенил. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Г, обозначенная как группа Щ, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R3 и R4 взяты вместе с образованием карбоциклического кольца А формулы -(СН 2)b- или гетероциклического кольца А, выбранного из группы, состоящей из-Q-(CH2)c и -(CH2)j -Q-(CH2)k-, где Q представляет собой О, S или NR17, где указанное карбоциклическое кольцо А и указанное гетероциклическое кольцо А каждое независимо возможно замещено одним или более чем одним заместителем, независимо выбранным из C1-4 алкила,галгенида или оксо. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Щ, обозначенная как группа Э, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений,как показано выше, где R3 и R4 взяты вместе с образованием указанного карбоциклического кольца А. 12 Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Э, обозначенная как группа Ю, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R3 и R4 взяты вместе с образованием -(СН 2)3-, -СН 2-С(СН 3)2-СН 2 или -(СН 2)4-. Особенно предпочтительными соединениями группы Ю являются соединения, где (а)R1 представляет собой метил, R2 представляет собой метил, R8 представляет собой гидрокси или этокси, и R3 и R4 взяты вместе с образованием -(СН 2)3-, (б) R1 представляет собой хлоро,R2 представляет собой метил, R8 представляет собой гидрокси или этокси, и R3 и R4 взяты вместе с образованием -(СН 2)3-, и (в) R1 представляет собой метил, R2 представляет собой метил,R8 представляет собой гидрокси или этокси, иR3 и R4 взяты вместе с образованием -(СН 2)4-; и фармацевтически приемлемые соли указанных соединений. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений, обозначенная как группа АА, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R8 представляет собой -OR9. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы AА, обозначенная как группа АБ, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R9 представляет собой С 1-12 алкил. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы АБ, обозначенная как группа АВ, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R9 представляет собой метил, изопропил или этил. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы АВ, обозначенная как группа АГ, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R9 представляет собой этил. Предпочтительная группа фармацевтически приемлемых солей таких соединений формулы I и их пролекарств, геометрических и оптических изомеров содержит те фармацевтически приемлемые соли этих соединений, их пролекарств, геометрических и оптических изомеров, где эта соль представляет собой соль натрия или калия. Предпочтительная группа соединений формулы I, обозначенная как группа АД, включает в себя конкретные соединения: 14 метрические и оптические изомеры и фармацевтически приемлемые соли этих соединений,пролекарств и изомеров. Предпочтительная группа фармацевтически приемлемых солей соединений, пролекарств и геометрических и оптических изомеров группы АД, обозначенная как группа АЕ, содержит те фармацевтически приемлемые соли этих соединений, их пролекарств и геометрических и оптических изомеров, где эта соль представляет собой соль натрия или калия. Предпочтительная группа соединений и их геометрических и оптических изомеров соединений группы АД, обозначенная как группа АЖ, содержит этиловые эфиры этих соединений. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы Б, обозначенная как группаA3, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R5 представляет собой фторо. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы A3, обозначенная как группа АИ, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R4 представляет собой водород, фторо, хлоро, метил или циклобутилметилкарбамоил. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы АИ, обозначенная как группа АК, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R1 и R2, каждый независимо, представляет собой метил или хлоро. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы АК, обозначенная как группа АЛ, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R1 и R2 каждый представляет собой метил. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы АК, обозначенная как группаAM, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R1 и R2 каждый представляет собой хлоро. Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы АК, обозначенная как группа АН, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R7 представляет собой водород и R8 представляет собой водород или -OR9. 15 Предпочтительная группа соединений и фармацевтически приемлемых солей таких соединений группы АН, обозначенная как группа АО, содержит те соединения формулы I и фармацевтически приемлемые соли таких соединений, как показано выше, где R9 представляет собой метил или этил. Предпочтительная группа соединений формулы I, обозначенная как группа АП, включает в себя конкретные соединения:N-[4-(4-фторофенокси)-3,5-диметилфенил] оксаминовая кислота,N-[3,5-дихлоро-4-(4-фторофенокси)фенил] оксаминовая кислота,N-[3,5-дихлоро-4-(3,4-дифторофенокси) фенил]оксаминовая кислота,N-[4-(3-метил-4-фторофенокси)-3,5 дихлорофенил]оксаминовая кислота,N-[3,5-дихлор-4-(3-хлоро-4-фторофенокси) фенил]оксаминовая кислота,N-[4-(3,4-дифторофенокси)-3,5-диметилфенил]оксаминовая кислота,N-[4-(3-хлоро-4-фторофенокси)-3,5-диметилфенил]оксаминовая кислота,N-[4-(3-метил-4-фторофенокси)-3,5-диметилфенил]оксаминовая кислота,N-[3,5-дихлор-4-(4-фторофенокси)фенил] оксаминовая кислота,N-[3,5-дихлор-4-(3,4-дифторофенокси)фенил]оксаминовая кислота,N-4-[3-(циклобутилметилкарбамоил)-4 фторофенокси]-3,5-диметилфенилоксаминовая кислота,N-[4-(4-фторофенокси)-3,5-диметилфенил] оксаминовая кислота, а также их пролекарства и геометрические и оптические изомеры и фармацевтически приемлемые соли этих соединений, пролекарств и изомеров. Предпочтительная группа фармацевтически приемлемых солей соединений, пролекарств и геометрических и оптических изомеров группы АП, обозначенная как группа АР, содержит те фармацевтически приемлемые соли этих соединений, их пролекарств и геометрических и оптических изомеров, где эта соль представляет собой соль натрия или калия. Предпочтительная группа соединений и их геометрических и оптических изомеров соединений группы АП, обозначенная как группа АС,содержит этиловые эфиры этих соединений. В данном изобретении предложены способы лечения состояния, выбранного из ожирения,гиперлипидемии, глаукомы, сердечной аритмии,кожных расстройств, заболевания щитовидной железы, гипотиреоза, сахарного диабета, атеросклероза, гипертензии, ишемической болезни сердца, гиперхолестеринемии, депрессии и остеопороза, у млекопитающего (включая человека), при котором указанному млекопитающему вводят эффективное лечебное количество соединения формулы I, либо его пролекарства, 004229 16 либо его геометрического или оптического изомера, либо фармацевтически приемлемой соли такого соединения, такого пролекарства или такого изомера, как описано выше. В другом аспекте в данном изобретении предложены способы лечения состояния, выбранного из ожирения, гиперлипидемии, глаукомы, сердечной аритмии, кожных расстройств,заболевания щитовидной железы, гипотиреоза,сахарного диабета, атеросклероза, гипертензии,ишемической болезни сердца, гиперхолестеринемии, депрессии и остеопороза, у млекопитающего (включая человека), при котором указанному млекопитающему вводят эффективные лечебные количества соединения формулы I,либо его пролекарства, либо его геометрического или оптического изомера, либо фармацевтически приемлемой соли такого соединения, такого пролекарства или такого изомера, как описано выше, и агента, снижающего аппетит. В другом аспекте в данном изобретении предложены способы лечения состояния, выбранного из ожирения, гиперлипидемии, глаукомы, сердечной аритмии, кожных расстройств,заболевания щитовидной железы, гипотиреоза,сахарного диабета, атеросклероза, гипертензии,ишемической болезни сердца, гиперхолестеринемии, депрессии и остеопороза, у млекопитающего (включая человека), при котором указанному млекопитающему вводят эффективные лечебные количества соединения формулы I,либо его пролекарства, либо его геометрического или оптического изомера, либо фармацевтически приемлемой соли такого соединения, такого пролекарства или такого изомера, как описано выше, и ингибитора липазы. В предпочтительном аспекте в данном изобретении предложены способы лечения ожирения у млекопитающих (включая человека), при котором указанному млекопитающему вводят эффективное для лечения ожирения количество соединения формулы I, либо его пролекарства, либо его геометрического или оптического изомера, либо фармацевтически приемлемой соли такого соединения, такого пролекарства или такого изомера, как описано выше. В другом аспекте в данном изобретении предложены способы лечения ожирения у млекопитающих (включая человека), при котором указанному млекопитающему вводят эффективные для лечения ожирения количества соединения формулы I, либо его пролекарства, либо его геометрического или оптического изомера, либо фармацевтически приемлемой соли такого соединения, такого пролекарства или такого изомера, как описано выше, и агента, снижающего аппетит. В другом аспекте в данном изобретении предложены способы лечения ожирения у млекопитающих (включая человека), при котором указанному млекопитающему вводят эффективные для лечения ожирения количества соедине 17 ния формулы I, либо его пролекарства, либо его геометрического или оптического изомера, либо фармацевтически приемлемой соли такого соединения, такого пролекарства или такого изомера, как описано выше, и ингибитора липазы. В другом аспекте в данном изобретении предложены фармацевтические композиции,содержащие соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения, пролекарства или изомера, как описано выше, и фармацевтически приемлемый наполнитель, разбавитель или носитель. В другом аспекте в данном изобретении предложены фармацевтические композиции,содержащие соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения, пролекарства или изомера, как описано выше, агент, снижающий аппетит, и фармацевтически приемлемый наполнитель, разбавитель или носитель. В другом аспекте в данном изобретении предложены фармацевтические композиции,содержащие соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения, пролекарства или изомера, как описано выше, ингибитор липазы и фармацевтически приемлемый наполнитель, разбавитель или носитель. В другом аспекте в данном изобретении предложены фармацевтические композиции для лечения состояния, выбранного из ожирения,гиперлипидемии, глаукомы, сердечной аритмии,кожных расстройств, заболевания щитовидной железы, гипотиреоза, сахарного диабета, атеросклероза, гипертензии, ишемической болезни сердца, гиперхолестеринемии, депрессии и остеопороза, у млекопитающего (включая человека), содержащие соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения, пролекарства или изомера, как описано выше, и фармацевтически приемлемый наполнитель, разбавитель или носитель. В другом аспекте в данном изобретении предложены фармацевтические композиции для лечения состояния, выбранного из ожирения,гиперлипидемии, глаукомы, сердечной аритмии,кожных расстройств, заболевания щитовидной железы, гипотиреоза, сахарного диабета, атеросклероза, гипертензии, ишемической болезни сердца, гиперхолестеринемии, депрессии и остеопороза, у млекопитающего (включая человека), содержащие соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения, пролекарства или изомера, как описано выше, агент, сни 004229 18 жающий аппетит, и фармацевтически приемлемый наполнитель, разбавитель или носитель. В другом аспекте в данном изобретении предложены фармацевтические композиции для лечения состояния, выбранного из ожирения,гиперлипидемии, глаукомы, сердечной аритмии,кожных расстройств, заболевания щитовидной железы, гипотиреоза, сахарного диабета, атеросклероза, гипертензии, ишемической болезни сердца, гиперхолестеринемии, депрессии и остеопороза, у млекопитающего (включая человека), содержащие соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения, пролекарства или изомера, как описано выше, ингибитор липазы и фармацевтически приемлемый наполнитель, разбавитель или носитель. В другом аспекте в данном изобретении предложены фармацевтические композиции для лечения ожирения у млекопитающего (включая человека), содержащие соединение формулы I,либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения,пролекарства или изомера, как описано выше, и фармацевтически приемлемый наполнитель,разбавитель или носитель. Еще в одном аспекте в данном изобретении предложены фармацевтические композиции для лечения ожирения у млекопитающего(включая человека), содержащие соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения, пролекарства или изомера, как описано выше, агент, снижающий аппетит, и фармацевтически приемлемый наполнитель, разбавитель или носитель. Еще в одном аспекте в данном изобретении предложены фармацевтические композиции для лечения ожирения у млекопитающего(включая человека), содержащие соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения, пролекарства или изомера, как описано выше, ингибитор липазы и фармацевтически приемлемый наполнитель, разбавитель или носитель. В другом аспекте в данном изобретении предложены наборы для лечения состояния,выбранного из ожирения, гиперлипидемии,глаукомы, сердечной аритмии, кожных расстройств, заболевания щитовидной железы, гипотиреоза, сахарного диабета, атеросклероза,гипертензии, ишемической болезни сердца, гиперхолестеринемии, депрессии и остеопороза,которые содержат: первое соединение, представляющее собой соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически при 19 емлемую соль такого соединения, пролекарства или изомера, как описано выше, и фармацевтически приемлемый наполнитель, носитель или разбавитель, в первой стандартной лекарственной форме; второе соединение, представляющее собой агент, снижающий аппетит, или ингибитор липазы, и фармацевтически приемлемый наполнитель, носитель или разбавитель, во второй стандартной лекарственной форме; и контейнер. В другом предпочтительном аспекте в данном изобретении предложены наборы для лечения ожирения, которые содержат: первое соединение, представляющее собой соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения, пролекарства или изомера, как описано выше, и фармацевтически приемлемый наполнитель, носитель или разбавитель, в первой стандартной лекарственной форме; второе соединение, представляющее собой агент, снижающий аппетит, или ингибитор липазы, и фармацевтически приемлемый наполнитель,носитель или разбавитель, во второй стандартной лекарственной форме; и контейнер. Если не указано иначе, приведенные здесь алкил означает радикал с нормальной или разветвленной углеводородной цепью,включая, в зависимости от обстоятельств, например, метил, этил, н-пропил, изопропил, нбутил и тому подобное; алкенил означает нормальный или разветвленный ненасыщенный одновалентный алифатический радикал; алкокси означает алкильный радикал,который присоединен к остальной части молекулы через кислород, включая, в зависимости от обстоятельств, например, метокси; алкинил означает нормальный или разветвленный ациклический углеводородный радикал с одной тройной связью, включая, в зависимости от обстоятельств, например, ацетилен; карбоциклический (карбоцикл) означает ненасыщенное либо частично или полностью насыщенное кольцо, имеющее в своем ядре только атомы углерода, включая, в зависимости от обстоятельств, арил (органический радикал,полученный из ароматического углеводорода удалением одного атома, например фенил из бензола, включая также, например, нафтил); циклоалкан означает насыщенный моноциклический углеводород, включая, в зависимости от обстоятельств, например, циклогексан; циклоалкил означает моноциклический или полициклический радикал, полученный из циклоалкана, включая, в зависимости от обстоятельств, например, циклогексил; галогено или галоген означает радикал, полученный из элементов фтора, хлора,брома или иода; 20 гетероциклический (гетероцикл) означает радикал, полученный из ненасыщенного либо частично или полностью насыщенного моноциклического или полициклического кольца из атомов различных типов и включает в себя ароматические и неароматические гетероциклические группы, содержащие один или более чем один гетероатом, каждый из которых выбран из О, S и N; примеры гетероциклических групп включают в себя, например, бензимидазолил, бензофуранил, бензотиофенил, бензоксазолил, фурил,имидазолил, индолил, изохинолил, изотиазолил,изоксазолил, морфолинил, оксадиазолил, оксазолил, пиперазинил, пиперидил, пиранил, пиразинил, пиразолил, пиридил, пиримидил, пирролил, хинолил, тетрагидроизохинолил, тетрагидрохинолил, тетрагидротиенил, тетразолил, тиадиазолил, тиазолил, тиенил, тиоморфолинил,тиофенил и триазолил; при этом, когда гетероциклические группы конкретно перечислены или включены в качестве заместителей для соединений формулы I, следует понимать, что,если конкретно не указано иначе, подразумеваются все подходящие изомеры таких гетероциклических групп; гидрат представляет собой кристаллическое вещество, содержащее одну или более чем одну молекулу кристаллизационной воды, то есть, вещество, содержащее воду, присоединенную в молекулярной форме; фармацевтически приемлемый означает,что эксципиенты, представляющие собой носитель, разбавитель, наполнитель, и/или соль должны быть совместимы с другими ингредиентами препарата и не должны быть вредными для его реципиента; фармацевтически приемлемые соли соединений по данному изобретению могут быть образованы самим соединением, пролекарствами, например эфирами, изомерами и тому подобным, и включают в себя все фармацевтически приемлемые соли, которые наиболее часто используют в фармацевтической химии; например, соли могут быть образованы с неорганическими или органическими кислотами, такими как соляная кислота, бромистоводородная кислота, иодистоводородная кислота, карбоновые кислоты, сульфоновые кислоты, включая такие агенты, как нафталинсульфоновая, этансульфоновая, гидроксиэтансульфоновая, метансульфоновая (мезилат), бензолсульфоновая (безилат) и толуолсульфоновая кислоты, например,пара-толуолсульфоновая (тозилат), серная кислота, азотная кислота, фосфорная кислота,винная кислота, пиросерная кислота, метафосфорная кислота, янтарная кислота, муравьиная кислота, фталевая кислота, яблочная кислота,малеиновая кислота, молочная кислота, аскорбиновая кислота, гликолевая кислота, глюконовая кислота, миндальная кислота, глутаминовая кислота, аспарагиновая кислота, фумаровая ки 21 слота, пировиноградная кислота, фенилуксусная кислота, памовая кислота, никотиновая кислота и тому подобные; подходящие фармацевтически приемлемые соли также включают в себя соли щелочных металлов (например соли натрия,калия), соли щелочно-земельных металлов (например соли магния, кальция), соли аминов (например соли аммония, алкиламмония, диалкиламмония, триалкиламмония, тетраалкиламмония, диэтаноламиния, триэтаноламиния, триэтаноламиния и гуанидиния); предпочтительные соли включают в себя соли органических кислот, выбранных из муравьиной, уксусной,трифторуксусной, пропионовой, бензойной,лимонной, малеиновой, винной, метансульфоновой, бензолсульфоновой или толуолсульфоновой, соли неорганических кислот, выбранных из соляной, бромистоводородной, серной или фосфорной, аминокислот, выбранных из аспарагиновой и глутаминовой, а также соли натрия и калия; полиморф представляет собой вещество,которое встречается в двух или более чем двух формах; пролекарство представляет собой предшественник лекарства, который после введения высвобождает лекарство in vivo посредством некоторого химического или физического процесса (например, пролекарство под воздействием физиологического рН или под действием фермента превращается в желаемую лекарственную форму); примерные пролекарства при расщеплении высвобождают соответствующую свободную кислоту, и такие гидролизуемые образующие эфир остатки соединений формулы I включают в себя, но не ограничены ими, остатки, имеющие карбоксильную группировку, где свободный водород заменен (С 1-С 4)алкилом,(С 2-С 7)алканоилоксиметилом, 1-(алканоилокси) этилом, имеющим от 4 до 9 атомов углерода, 1 метил-1-(алканоилокси)этилом, имеющим от 5 до 10 атомов углерода, алкоксикарбонилоксиметилом, имеющим от 3 до 6 атомов углерода,1-(алкоксикарбонилокси)этилом, имеющим от 4 до 7 атомов углерода, 1-метил-1-(алкоксикарбонилокси)этилом, имеющим от 5 до 8 атомов углерода, N-(алкоксикарбонил)аминометилом,имеющим от 3 до 9 атомов углерода, 1-(N(алкоксикарбонил)амино)этилом, имеющим от 4 до 10 атомов углерода, 3-фталидилом, 4 кротонолактонилом,гамма-бутиролактон-4 илом, ди-N,N-(С 1-С 2)алкиламино(С 2-С 3)алкилом(таким как b-диметиламиноэтил), карбамоил(С 1-С 2)алкилом, N,N-ди(С 1-С 2)алкилкарбамоил(С 1-С 2)алкилом и пиперидино-, пирролидиноили морфолино(С 2-С 3)алкилом; радикал представляет собой группу атомов, которая ведет себя как единый атом в химической реакции, например органический радикал представляет собой группу атомов, которая придает характерные свойства соединению, 004229 22 содержащему эту группу, или которая остается неизменной в течение серии реакций; сольват представляет собой молекулярный или ионный комплекс молекул или ионов растворителя с молекулами или ионами растворенного вещества; сольват, где растворителем является вода, образует гидраты или гидратированные ионы; спироциклоалкил означает циклоалкил,имеющий спирсвязь (спиросвязь, образованная одним атомом, который является единственным общим членом этих колец); и лечение, лечить или терапия включает в себя среди прочего превентивную (например профилактическую), паллиативную и лечебную терапию. Подробное описание изобретения Если не указано иначе, на протяжении всего данного документа: С означает градусы стоградусной шкалы, % означает процент,вычислено означает вычисленные данные,см означает сантиметр, ДЭЭ означает диэтиловый эфир, ДМЭ означает диметиловый эфир,ДМФ означает диметилформамид, ДМСО означает диметилсульфоксид, ДТТ означает дитиотрейтол, EtOAc означает этилацетат, EtOH означает этанол, обнаружено означает обнаруженные данные, г означает грамм или граммы, ч означает час или часы, кг означает килограмм или килограммы, КОН означает гидроксид калия, л означает литр или литры,М означает молярная (концентрация), МеОН означает метанол, мг означает миллиграмм или миллиграммы, мин означает минуту или минуты, мл означает миллилитр или миллилитры, мм означает миллимоль или миллимоли, мМ означает миллимолярная (концентрация), МС означает масс-спектр, н означает нормальная (концентрация), NaOH означает гидроксид натрия, нМ означает наномолярная(концентрация), ЯМР означает спектр протонного ядерного магнитного резонанса, фунт на кв. дюйм означает фунты на квадратный дюйм, КТ означает комнатную температуру,ТЭА означает триэтиламин, ТФУ означает трифторуксусную кислоту, ТГФ означает тетрагидрофуран, мкг означает микрограмм или микрограммы, и мкл означает микролитр или микролитры. Как описано здесь, следует все время понимать, что соединение в пределах объема формулы I включает в себя все активные формы таких соединений, включая, например, их свободную форму, например форму свободной кислоты или основания, а также все пролекарства,полиморфы, гидраты, сольваты, стереоизомеры,например диастереомеры и энантиомеры, и тому подобное, а также все фармацевтически приемлемые соли, как описано выше. Следует также понимать, что подходящие активные метаболиты соединений в пределах объема формулыI в любой подходящей форме также включены здесь. Более конкретно некоторые соединения,подходящие для применения в настоящем изобретении, такие как, например, некоторые соединения формулы I, могут иметь асимметрические центры и, следовательно, существовать в различных энантиомерных формах. Все подходящие оптические изомеры и стереоизомеры таких соединений и их смеси следует считать находящимися в объеме изобретения. В отношении таких соединений настоящее изобретение включает в себя применение рацемата, отдельной энантиомерной формы, отдельной диастереомерной формы или их смесей, как целесообразно. Кроме того, такие соединения могут также существовать в виде таутомеров. Соответственно настоящее изобретение относится к применению всех таких подходящих таутомеров и их смесей. Кроме того, специалистам в данной области техники легко понять, что физиологически активные соединения, которые имеют доступные гидроксигруппы, часто вводят в форме фармацевтически приемлемых сложных эфиров. Соединения по данному изобретению можно вводить в виде сложных эфиров, образованных на гидрокси группах. Хотя механизм еще не исследован, и нежелательно связывать его теорией, считают, что такие эфиры расщепляются в организме метаболическим путем, и что действительное лекарство представляет собой гидрокси-соединение само по себе. Как давно известно в фармацевтической химии, возможно регулировать скорость или продолжительность действия соединения с помощью подходящего выбора эфирных групп. На основании данного описания специалистам в данной области техники понятно, как получить соединения по настоящему изобретению, используя любой подходящий известный способ. Кроме того, реакционные схемы настоящего описания иллюстрируют получение соединений по настоящему изобретению, и, если не указано иначе, R1, R2, R3, R4, R6, R7, R9,R10, Х и Y в этих реакционных схемах являются такими, как описаны выше, Q соединения 14 схемы А предпочтительно представляет собой натрий или калий, X1 схем Г, И и М предпочтительно представляет собой галогенид или сульфонат, Т схем Л и М является таким, как описан ниже. Кроме того, приведенные здесь примеры дополнительно иллюстрируют получение соединений по настоящему изобретению. Объект изобретения также включает в себя меченые изотопами соединения, которые являются идентичными соединениям, подпадающим под формулу I, кроме того факта, что один или более чем один атом заменен атомом, имеющим атомную массу или массовое число, отличные от атомной массы или массового числа, обычно обнаруживаемых в природе. Примеры изотопов, 004229 24 которые могут быть включены в соединения по изобретению, включают в себя изотопы водорода, углерода, азота, фосфора, фтора и хлора,такие как 2H, 3H, 13 С, 14 С, 15N, 18 О, 17 О, 31 Р, 32 Р,35S, 18F и 36Cl, соответственно. Соединения по настоящему изобретению, их пролекарства и фармацевтически приемлемые соли указанных соединений или указанных пролекарств, которые содержат вышеупомянутые изотопы и/или другие изотопы других атомов, находятся в пределах объема данного изобретения. Некоторые меченые изотопами соединения по настоящему изобретению, например те, в которые включены радиоактивные изотопы, такие как 3H и 14 С, являются полезными в анализах тканевого распределения лекарства и/или субстрата. Изотопы тритий, то есть 3 Н, и углерод-14, то есть 14 С, являются особенно предпочтительными благодаря легкости их получения и обнаружения. Кроме того, замена более тяжелыми изотопами, такими как дейтерий, то есть 2H, может давать некоторые терапевтические преимущества в результате большей метаболической стабильности, например увеличенного периода полураспада in vivo, или сниженных потребностей в дозировке, и, следовательно, может быть предпочтительной в некоторых обстоятельствах. Меченые изотопами соединения формулы I по данному изобретению и их пролекарства можно, как правило, получить путем осуществления методик, описанных в приведенных ниже схемах и/или примерах, путем замены легкодоступного меченного изотопом реагента не меченным изотопом реагентом. Исходные материалы для каждых схемы и примера синтеза, предложенных в данном описании, либо являются коммерчески доступными, либо их можно получить согласно способам,известным специалистам в данной области техники, таким как описанные, например, в вышеупомянутых патентах США 5401772; 5569674 и 5654468, и в описании к европейскому патенту, опубликованному как ЕР 580550. Соединения по настоящему изобретению можно получить из общего промежуточного соединения 1, как описано ниже причем само это соединение можно синтезировать согласно любому подходящему способу,известному в данной области техники. Более конкретно специалистам в данной области техники на основании настоящего описания будет понятно, как получить это общее промежуточное соединение 1, где W представляет собой кислород, S(O)d, CH2 или NR9, где d и R9 являются такими, как описано выше. Особенно предпочтительно, чтобы W представлял собой кислород. 25 Например, общее промежуточное соединение 1, где W представляет собой кислород сочетанием 4-нитрофенола (или соответствующего тиофенола) 2 с бис-арилиодония тетрафторборатом 3 примерно при КТ в подходящем органическом растворителе, таком как, например, дихлорметан, хлороформ, ДМФ или ДМСО, в присутствии подходящего медного катализатора, такого как, например, медная бронза, и подходящего основания, такого как,например, ТЭА, трет-бутоксид калия или гидрид натрия (J. Med. Chem., 38: 695-707 (1995; либо (б) сочетанием 4-галогенонитробензола 4 (М представляет собой галоген), такого как, например,4-иодонитробензол, 4-бромонитробензол или 4 хлоронитробензол, с фенолом (или тиофенолом) 5, таким как, например, 4-фторофенол, при подходящей повышенной температуре (более чем примерно 120 С, например примерно 130 С) в присутствии подходящего основания, такого как, например, карбонат калия, гидроксид калия или трет-бутоксид калия, в полярном инертном растворителе, таком как, например, ДМСО или сочетанием (при КТ в дихлорметане) фенилбороновой кислоты 6 с 4-нитрофенолом 2 в присутствии ацетата меди (II) и подходящего основания, такого как, например, ТЭА, пиридин или смесь ТЭА и пиридина (Tetrahedron Lett., 39: 2933-2936, 2937-2940 (1998. Воплощения настоящего изобретения, гдеR4 соединения формулы I находится в 3' положении и представляет собой сульфонамид,амид, например карбоксамид, метиламино, карбамоил или сульфамоил, арилокси, например фенилокси или бензилокси, фенилсульфон или алкилсульфон, можно получить, например, согласно схемам А и Б, В и Г, Д, Е, Ж и К, 3 и И,соответственно, предложенных в настоящем описании здесь ниже. Кроме того, соединение формулы I, где R4 находится в 3' положении, и R3 находится в 2' положении и, взятые вместе, представляют собой инданил или тетрагидронафталил, можно получить согласно схемам Л и М, также предложенных в настоящем описании здесь ниже. 26 Кроме того, соединение формулы I, где R4 находится в 3' положении, и R5 находится в 4' положении, и R4 и R5 взяты вместе с образованием индолила, можно получить согласно схеме Н, приведенной здесь ниже. Кроме того, соединение формулы I, где R5 находится в 4' положении и представляет собой фторо, можно получить согласно схеме О, приведенной здесь ниже. В схемах А и В, описанных здесь ниже,исходный материал (А) представляет собой общее промежуточное соединение 1, где R5 находится в 4' положении и представляет собой метокси или (МеО). В схемах Д, З и И, описанных здесь ниже, исходный материал (В) представляет собой общее промежуточное соединение 1, где R5 находится в 4' положении и представляет собой МеО, и R4 находится в 3' положении и представляет собой водород. На схеме О исходный материал (С) представляет собой соединение 5, где R5 находится в 4' положении и представляет собой фторо. Следует понимать, что следующие схемы предложены исключительно в целях иллюстрации и не ограничивают изобретение, которое определено формулой изобретения. Схема А По схеме А: промежуточное нитросоединение А можно превратить в 3'-сульфонамид 7 или 8 взаимодействием 3'-хлоросульфонилированного промежуточного соединения А и первичного или вторичного амина в подходящем растворителе, таком как, например, дихлорметан, ТГФ, МеОН, ЕtOН или ацетонитрил, в присутствии подходящего основания, такого как,например, ТЭА или диизопропилэтиламин. Хлоросульфонилирование А можно проводить путем перемешивания раствора А в неразбавленной хлоросульфоновой кислоте при температуре от примерно 0 С до примерно 25 С. Сульфонамид 7 можно превратить в сульфонамид 8 путем алкилирования. При предпочтительном способе алкилирования используют подходящий алкилирующий агент, такой как,например, алкилгалогенид, в присутствии подходящего основания, такого как, например, карбонат калия, гидрид натрия, трет-бутоксид калия, NaOH или КОН, в подходящем органическом растворителе, таком как, например, ацетон, ТГФ, ДМСО, 2-пропанол или водный раствор МеОН. Деметилирование соединения 8 до фенола 9 можно выполнять взаимодействием 8 с подходящим тригалогенидом бора, таким как, например, трибромид бора или трихлорид бора, в подходящем органическом растворителе, таком как, например, дихлорметан или хлороформ. Нитровосстановление соединения 9 до анилина 10 можно выполнять, используя способы, хорошо известные в данной области техни 004229 38 ки, такие как, например, гидрирование или восстановление цинковой пылью или хлоридом олова (II). Анилин 10 можно превратить в оксамат 11 взаимодействием соединения 10 с диэтилоксалатом при примерно 120 С в течение промежутка времени от примерно 5 до примерно 24 ч или с этилоксалилхлоридом примерно при КТ в подходящем безводном апротонном растворителе, таком как, например, ДЭЭ, дихлорметан,хлороформ или ТГФ. Оксамат 11 можно превратить в оксаминовую кислоту 12 и оксамид 13, используя общепринятые способы, хорошо известные в соответствующей области техники. Например,сложный эфир 11 можно гидролизовать до кислоты 12, используя подходящие водные щелочи, такие как, например, карбонаты или гидроксиды щелочных металлов, в водном растворе МеОН. Оксамид 13 можно синтезировать взаимодействием сложного эфира 11 с амином в подходящем растворителе, таком как, например,дихлорметан, хлороформ, ТГФ или МеОН. Кислоту 12 можно превратить в соли 14,такие как, например, соли металлов или аммония, обработкой соединения 12 эквивалентным количеством соответствующего основания, такого как, например, щелочные гидроксиды или гидроксид аммония, либо обменом с солями карбоновых кислот или щелочными силоксидами, либо с помощью способов ионного обмена,известных в данной области техники. По схеме Б: первичный анилин 10 можно превратить во вторичный анилин 15 согласно способам, хорошо известным в данной области техники для превращения первичного амина во вторичный амин, таких как, например, восстановительное алкилирование. При предпочтительном способе восстановительного алкилирования используют альдегид или кетон и восстанавливающий агент в подходящем растворителе, и лучше всего проводить его в присутствии молекулярных сит примерно 3. Предпочтительными восстанавливающими агентами являются цианобороидрид натрия, триацетоксиборогидрид натрия и боргидрид натрия. Предпочтительными органическими растворителями являются EtOH и МеОН. Полученный в результате анилин 15 можно превратить в оксамат 16, а затем в кислоту 17, например способами, аналогичными тем,которые описаны ранее к схеме А, обсуждавшейся выше. По схеме В: Промежуточное нитросоединение А можно превратить в альдегид 18 с помощью формилирования. Предпочтительный способ формилирования можно выполнять взаимодействием соединения А с гексаметилентетрамином примерно при 65 С в подходящем растворителе, таком как, например, ТФУ. Альдегид 18 можно окислять до карбоновой кислоты 19 способами, хорошо известными 39 в данной области техники, например окислением Джонса. Предпочтительные способы окисления включают в себя окисление Джонса и способы, в которых используют гипохлорит натрия. Взаимодействием альдегида 18 с реагентом Джонса (хромовая кислота/водная серная кислота) в ацетоне получают карбоновую кислоту 19. Соединение 19, представляющее собой нитросодержащую карбоновую кислоту, можно превратить в оксамат 20 в три стадии (деметилирование, нитровосстановление и образование оксамата) с помощью методик, аналогичных описанным к схеме А, приведенной здесь выше. Оксамат 20 можно превратить в 3'карбоксамидное производное 21 согласно способам, известным в данной области техники. Например, двумя обычно используемыми способами являются использование хлорангидрида или ангидрида (симметричного или смешанного) соединения 20 с амином в подходящем сухом апротонном растворителе, таком как, например, дихлорметан, ТГФ, ДМЭ или ДЭЭ, в присутствии основания, такого как ТЭА, диметиламинопиридин или пиридин. При другом способе используют взаимодействие 20 и необходимого амина в апротонном растворителе с любым из стандартных реагентов сочетания карбодиимида, таких как, например, дициклогексилкарбодиимид,2-этокси-1-этоксикарбонил-1,2-дигидрохинолон и бензотриазол-1 илокситрис(диметиламино)фосфонийгексафторфосфат. Сложный эфир 21 можно гидролизовать до оксаминовой кислоты 22 с помощью, например,методики, аналогичной описанной к схеме А,обсуждаемой выше. По схеме Г: амид 23 можно получить взаимодействием хлорангидрида или ангидрида(симметричного или смешанного) соединения 19 с первичным амином в подходящем растворителе, таком как, например, дихлорметан,ТГФ, ДМФ, ДЭЭ, в присутствии основания, такого как, например, ТЭА, ДМАП или пиридин. Амид 23 можно алкилировать до амида 24 взаимодействием карбоксамидного аниона соединения 23 с подходящим алкилирующим агентом, таким как, например, алкилгалогенид. Карбоксамидный анион соединения 23 можно образовать в ДМФ с подходящим основанием,таким как, например, гидрид натрия или гидрид калия. Алкилирование соединения 23 можно также проводить с помощью катализа фазового переноса без растворителя или с подходящим растворителем, таким как, например, ДМФ или ДМСО. В реакции фазового переноса используют тетрабутиламмония бромид (ТБАБ) в качестве агента фазового переноса и карбонат калия, КОН или NaOH в качестве основания. Амид 24 можно превратить в соответствующее соединение 21, например в три стадии с 40 помощью методик, аналогичных описанным к схеме А, обсуждаемой выше. По схеме Д: соединение В можно превратить в оксамат 25, например в три стадии, с помощью методик, аналогичных описанным в схеме А, приведенной здесь выше. Формилирование соединения 25 можно выполнять с помощью методики формилирования, аналогичной описанной к схеме В, приведенной здесь выше. Альдегид 26 можно превратить, например,в метиламино, производное 27, способами, известными в данной области техники. При предпочтительном способе используют восстановительное аминирование. Например, восстановительное аминирование можно выполнять взаимодействием альдегида 26 с амином и восстанавливающим агентом в подходящем растворителе, и лучше всего проводить его в присутствии молекулярных сит примерно 3. Предпочтительными восстанавливающими агентами являются цианоборогидрид натрия, триацетоксиборгидрид натрия и боргидрид натрия. Предпочтительные органические растворители включают в себя EtOH, MeOH и 1,2-дихлорэтан. По схеме Е: оксамат 25 можно превратить в нитросоединение 28 нитрованием. Нитросоединение 28 можно восстановить до соответствующего анилина 29, например каталитическим гидрированием или химическим восстановлением цинковой пылью или хлоридом олова (II). Ацилированием соединения 29 карбонилхлоридом в присутствии подходящего основания, такого как, например, ТЭА или N,N-диизопропилэтиламин, получают диацилированное соединение 30. Этот диацилированный оксамат 30 можно превратить в оксаминовую кислоту 32 гидролизом подходящим основанием, таким как,например, NaOH или КОН, в водном растворе МеОН. Сульфонилированием соединения 29 сульфонилхлоридом в присутствии подходящего основания, такого как, например, ТЭА илиN,N-диизопропилэтиламин, получают дисульфонилированное соединение 31. Гидролизом соединения 31 подходящим основанием, таким как, например, NaOH или КОН, в водном растворе МеОН примерно при 50 С получают оксаминовую кислоту 33. По схеме Ж: бензиловый эфир 37 можно превратить в фенол 38 дебензилированием. Обработкой соединения 37 тиоанизолом в ТФУ при температуре окружающей среды получают соединение 38. Превращение 38 в фениловый эфир 39 можно проводить путем сочетания соединения 38 с арилиодония тетрафтороборатом и медной бронзой в присутствии триэтиламина в дихлорметане или сочетания соединения 38 с арилбороновой кислотой и ацетатом меди (II) в присутствии подходящего основания, такого как, например, ТЭА, пиридин или смесь ТЭА и пиридина. Превращение соединения 39 в оксамат 40 можно выполнять, например, в три ста 41 дии (деметилирование, нитровосстановление и образование оксамата) согласно методикам,аналогичным описанным в схеме А, обсуждаемой выше. Оксаминовую кислоту 41 получают щелочным гидролизом сложного эфира 40. По схеме З: обработкой В арилсульфоновой кислотой в присутствии реагента Итона при повышенной температуре получают 3'-арилсульфон 42. Деметилированием 42 с последующим гидрированием, а затем взаимодействием с этилоксалилхлоридом получают оксамат 43. Оксамат 43 можно гидролизовать до оксаминовой кислоты 44, используя основание, такое как,например, NaOH или КОН. По схеме И: нитросоединение В можно превратить в 3'-сульфиновую кислоту 45 обработкой хлорсульфоновой кислотой с последующим восстановлением сульфитом натрия в присутствии основания, такого как, например, бикарбонат натрия или NaOH. Обработкой этой сульфиновой кислоты 45 алкилгалогенидом в присутствии основания, такого как, например,NaOH, КОН, трет-бутоксид калия, гидрид натрия или метоксид натрия, получают алкилсульфон 46. Это нитросоединение 46 можно превратить в оксамат 47 посредством деметилирования, гидрирования и образования оксамата. Гидролизом оксамата 47 в щелочных условиях получают оксаминовую кислоту 48. По схеме К: метиловый эфир 18 можно превратить в фенол 49, используя методики,аналогичные описанным к схеме А. Фенол 49 можно защитить как триметилсилилэтоксиметиловый эфир 50 обработкой сильным основанием, таким как, например, гидрид натрия или трет-бутоксид калия в апротонном растворителе, например ТГФ, с последующей обработкой триметилсилилэтоксиметилхлоридом (СЭМХЛ). Обработкой альдегида 50 восстанавливающим агентом, таким как, например, диизобутилалюминия гидрид (ДИБАЛГ) в апротонном растворителе, например дихлорметане или ТГФ, получают соединение 51. Взаимодействием спирта 51 с подходящим фенолом, используя азодикарбонильное соединение, например 1,1'(азодикарбонил)дипиперидин или диэтилазодикарбоксилат, и фосфин, такой как, например,трифенил- или трибутилфосфин, в апротонном растворителе, например ТГФ или толуоле, получают эфир 52. Удалением защитной группы СЭМ, присутствующей в соединении 52, в кислых условиях, таких как, например, серная или минеральная кислота в спиртовом растворителе, например МеОН или EtOH, или альтернативно, в опосредованных фтором условиях (тетрабутиламмония фторид/ТГФ, фтороводород/ацетонитрил) получают фенол 53. Восстановлением нитрогруппы, присутствующей в 53, с помощью кипячения с обратным холодильником в уксусной кислоте с порошкообразным металлом, например цинком или железом, получают амин 54. 42 Превращение в оксамат 55 и соответствующие оксаминовые кислоты и оксамиды выполняют,используя методики, аналогичные подробно описанным в схеме А. По схеме Л: соединения 56-62 можно получить согласно методикам, аналогичным подробно описанным выше, в соответствии со способами, хорошо известными в данной области техники. На основании настоящего описания и,в частности, схемы А, специалистам в данной области техники понятно, как превратить соединение 62 в оксаматные производные, подробно описанные в схеме Л. Т составляет, как описано выше, где R3 и R4 взяты вместе, карбоциклическое кольцо А формулы -(СН 2)b- или гетероциклическое кольцо А, выбранное из группы, состоящей из -Q-(CH2)c- и -(СН 2)j-Q(СН 2)k-, где b, Q, с, j и k являются такими, как описаны выше, и где указанное карбоциклическое кольцо А и указанное гетероциклическое кольцо А каждое независимо возможно замещено одним или более чем одним заместителем(например R21, R22), независимо выбранным из С 1-4 алкила, галогенида или оксо, как также описано выше. По схеме М: истощающей обработкой соединения 63 сильным основанием, таким как,например, гексаметилдисилизан лития, диизопропиламид лития или трет-бутоксид калия, и подходящим алкилгалогенидом в апротонном растворителе, например ТГФ, получают бисалкилированное промежуточное соединение 65. Этот процесс осуществляют стадийным способом, когда R21 и R22 являются различными, и в одной реакционной колбе, когда R21 и R22 являются одинаковыми. С одного из метиловых эфиров, присутствующих в соединении 65, можно избирательно снять защиту путем использования трихлорида бора или хлорида алюминия в апротонном растворителе, например дихлорметане или толуоле. Восстановление кетона, функционально присутствующего в соединении 66, можно выполнять обработкой гидросиланом, предпочтительно триэтилсиланом, в присутствии кислоты,например метансульфоновой кислоты или ТФУ,в присутствии или в отсутствие растворителя. Растворители могут быть либо протонными,либо апротонными, причем предпочтительным является дихлорметан. На основании настоящего описания специалистам в данной области понятно, как превратить полученные в результате восстановленные соединения в целевые оксаматные производные. Т является таким, как описан для схемы Л. По схеме Н: индол 69 можно получить сочетанием коммерчески доступного 5 гидроксииндола 67 с 4-иодонитробензолом 68 примерно при 125 С в присутствии карбоната калия в течение примерно 3 ч. Нитросоединение 69 превращают в целевое соединение 70 по 43 средством гидрирования и образования оксамата. По схеме О: диариловый эфир 72 получают сочетанием коммерчески доступного фторофенола с 4-галогенонитробензолом 4 при 130 С в NMP (N-метилпирролидон) в присутствии КОН. Оксаминовую кислоту 73 синтезируют из нитросоединения 72 посредством гидрирования,ацилирования и гидролиза. Следует отметить, что при получении соединений формулы I, как это очевидно специалистам в данной области техники, некоторые способы, применимые для получения таких соединений, например, те, примеры которых приведены в схемах К и М, обсуждаемых выше,могут требовать защиты конкретных функциональных групп, например, чтобы предотвратить взаимодействие таких функциональных групп при реакциях в других местах в пределах молекулы или для того, чтобы сохранить целостность таких функциональных групп. Специалист в данной области техники легко определяет необходимость такой защиты и типы такой защиты, и они будут варьировать в зависимости,например, от природы функциональных групп и от условий выбранного способа полученияGroups in Organic Synthesis, John WileySons,New York, 1991). Подходящие защитные группы для любой конкретной функциональной группы будут включать в себя те группы, которые, по существу, не являются химически реактивными в описанных условиях реакции, и которые можно удалить без существенного химического изменения других функциональных групп любого данного промежуточного соединения для соединения формулы I или самого соединения формулы I. Защитную группу можно удалить,если это желательно, при любом заданном способе получения, например на более поздней стадии. Некоторые из соединений формулы I по данному изобретению являются кислыми, и они образуют соль с фармацевтически приемлемым катионом. Некоторые из соединений формулы I по данному изобретению являются основными,и они образуют соль с фармацевтически приемлемым анионом. Все такие соли находятся в пределах объема данного изобретения, и их можно получить с помощью общепринятых способов, таких как объединение кислого и основного вещества, обычно в стехиометрическом соотношении, либо в водной, либо в неводной или частично водной среде, как целесообразно. Соли выделяют либо фильтрованием, либо осаждением осадителем с последующим фильтрованием, либо выпариванием растворителя, либо,в случае водных растворов, лиофилизацией, как целесообразно. Эти соединения можно получить в кристаллической форме путем растворения в подходящем растворителе (растворителях), таком как этанол, гексаны или смеси вода/ этанол. 44 Предпочтительные агенты, снижающие аппетит, в композициях, способах и наборах по данному изобретению включают в себя фенилпропаноламин, эфедрин, псевдоэфедрин, фентермин, антагонист нейропептида Y, агонист холецистокинина-А, ингибитор обратного захвата моноамина, симпатомиметический агент,серотонинэргический агент, агонист дофамина,агонист или миметик рецептора меланоцитстимулирующего гормона, антагонист каннабиноидного рецептора,аналог меланоцитстимулирующего гормона, антагонист меланинконцентрирующего гормона, белок OВ, аналог лептина, антагонист галанина и антагонист рецептора орексина. Предпочтительным ингибитором обратного захвата моноамина является сибутрамин. Предпочтительные серотонинэргические агенты включают в себя дексфенфлурамин и фенфлурамин. Предпочтительным агонистом дофамина является бромокриптин. Предпочтительным ингибитором липазы является тетрагидролипстатин. Предпочтительные агенты, снижающие аппетит, для композиций, способов и наборов по данному изобретению можно получить, используя способы, известные специалистам в данной области техники, например, фентермин можно получить, как описано в патенте США 2408345; сибутрамин можно получить, как описано в патенте США 4929629; фенфлурамин и дексфенфлурамин можно получить, как описано в патенте США 3198834; и бромокриптин можно получить, как описано в патентах США 3752814 и 3752888. Подходящие ингибиторы липазы можно получить, используя способы, известные специалистам в данной области техники, например,тетрагидролипстатин (2S,3S,5S)-5-[(S)-2-формамидо-4-метилвалерилокси]-2-гексил-3-гидроксигексадекановой 1,3 кислоты лактон можно получить, как описано, например, в патентах США 5274143; 5420305; 5540917 и 5643874. Введение соединения, пролекарства, изомера или фармацевтически приемлемой соли по настоящему изобретению и агента, снижающего аппетит, или ингибитора липазы, в зависимости от обстоятельств, согласно данному изобретению может быть либо последовательным во времени, либо одновременным, причем одновременный способ, как правило, является предпочтительным. При последовательном введении соединение, пролекарство, изомер или фармацевтически приемлемую соль по настоящему изобретению и агент, снижающий аппетит, или ингибитор липазы, в зависимости от обстоятельств, можно вводить в любом порядке. Кроме того, при последовательном введении соединение, пролекарство, изомер или фармацевтически приемлемую соль по настоящему изобретению и агент, снижающий аппетит, (или ингиби 45 тор липазы, в зависимости от обстоятельств) можно вводить в любом порядке. Как правило,предпочтительно, чтобы такое введение было пероральным. Даже более предпочтительно,чтобы это введение было пероральным и одновременным. Однако, например, если субъект,подлежащий лечению, неспособен глотать, либо пероральное всасывание по другой причине является нарушенным или нежелательным, подходящим будет парентеральное или чрескожное введение. Там, где введение является последовательным, введение соединения, пролекарства,изомера или фармацевтически приемлемой соли по настоящему изобретению и агента, снижающего аппетит, или ингибитора липазы, в зависимости от обстоятельств, можно осуществлять либо одним и тем же способом, либо различными способами. Доза соединения, пролекарства, изомера или фармацевтически приемлемой соли по данному изобретению, которую следует вводить человеку или животному, достаточно широко варьирует и является предметом суждения лечащего врача или ветеринара. Как следует понимать специалистам в данной области техники,может быть необходимо регулировать дозу соединения, пролекарства или изомера по данному изобретению, когда их вводят в форме соли,например когда солеобразующая группировка имеет значимую молекулярную массу. Обычный диапазон эффективных норм введения соединений, пролекарств, изомеров или фармацевтически приемлемых солей по данному изобретению составляет от примерно 0,001 мг/кг массы тела до примерно 100 мг/кг массы тела субъекта в сутки. Предпочтительный диапазон эффективных норм введения соединений, пролекарств, изомеров или фармацевтически приемлемых солей по данному изобретению составляет от примерно 0,01 мг/кг массы тела до примерно 50 мг/кг массы тела субъекта в сутки. Когда может оказаться целесообразным вводить суточную дозу соединения, пролекарства, изомера или фармацевтически приемлемой соли по данному изобретению порциями в различные часы суток, в любом конкретном случае количество вводимых соединения, пролекарства, изомера или фармацевтически приемлемой соли будет зависеть от таких факторов, как растворимость соединения, пролекарства, изомера или фармацевтически приемлемой соли по данному изобретению, применяемый препарат и путь введения (например перорально, чрескожно,парентерально или местно). Дозировки соединений, пролекарств, изомеров и фармацевтически приемлемых солей по данному изобретению можно вводить людям любым подходящим путем, причем предпочтительным является пероральное введение. Индивидуальные таблетки или капсулы должны, как правило, содержать от примерно 0,1 мг до примерно 100 мг соединения, пролекарства, изоме 004229 46 ра или фармацевтически приемлемой соли по данному изобретению в подходящих фармацевтически приемлемых наполнителе, разбавителе или носителе. Дозировки для внутривенного введения, как правило, находятся в диапазоне от примерно 0,1 мг до примерно 10 мг на одну дозу, как требуется. Для интраназального или ингаляционного введения дозировку обычно готовят как препарат в виде раствора от примерно 0,1% до примерно 1% (мас./об.). На практике врач будет определять действительную дозировку, которая будет наиболее подходящей для индивидуального пациента, и она будет варьировать соответственно, например, возрасту,массе и ответу конкретного пациента. Вышеуказанные дозировки являются примерными для среднего случая, но, конечно, могут быть индивидуальные случаи, где более высокие или более низкие диапазоны дозировки являются предпочтительными, и все такие дозировки соединений, пролекарств, изомеров и фармацевтически приемлемых солей по данному изобретению находятся в пределах объема настоящего изобретения. Любую подходящую дозировку агента,снижающего аппетит, можно применять в аспектах настоящего изобретения, включающих такие агенты. Дозировка агента, снижающего аппетит, как правило, находится в диапазоне от примерно 0,01 до примерно 50 мг/кг массы тела субъекта в сутки, предпочтительно от примерно 0,1 до примерно 10 мг/кг массы тела субъекта в сутки при введении однократно или в виде разделенной дозы. Например, если агент, снижающий аппетит, представляет собой фентермин, то дозировка фентермина составляет от примерно 0,01 до примерно 50 мг/кг массы тела субъекта в сутки, предпочтительно от примерно 0,1 до примерно 1 мг/кг массы тела субъекта в сутки. Кроме того, если агент, снижающий аппетит,представляет собой сибутрамин, то диапазон дозировки составляет от примерно 0,01 до примерно 50 мг/кг массы тела субъекта в сутки,предпочтительно от примерно 0,1 до примерно 1 мг/кг массы тела субъекта в сутки; если агент,снижающий аппетит, представляет собой дексфенфлурамин или фенфлурамин, то диапазон дозировки составляет от примерно 0,01 до примерно 50 мг/кг массы тела субъекта в сутки,предпочтительно от примерно 0,1 до примерно 1 мг/кг массы тела субъекта в сутки; и если агент, снижающий аппетит, представляет собой бромокриптин, то диапазон дозировки составляет от примерно 0,01 до примерно 10 мг/кг массы тела субъекта в сутки, предпочтительно от примерно 0,1 до примерно 10 мг/кг массы тела субъекта в сутки. На практике врач будет определять действительную дозировку агента, снижающего аппетит, которая будет наиболее подходящей для индивидуального пациента, и она будет варьировать соответственно, например,возрасту, массе и ответу конкретного пациента. 47 Вышеуказанные дозировки агента, снижающего аппетит, являются примерными, но, конечно,могут быть индивидуальные случаи, где более высокие или более низкие диапазоны дозировки таких агентов, снижающих аппетит, являются предпочтительными, и все такие дозировки находятся в пределах объема настоящего изобретения. Любую подходящую дозировку ингибитора липазы можно применять в аспектах настоящего изобретения, включающих такие ингибиторы. Дозировка ингибитора липазы, как правило, находится в диапазоне от примерно 0,01 до примерно 50 мг/кг массы тела субъекта в сутки,предпочтительно от примерно 0,05 до примерно 10 мг/кг массы тела субъекта в сутки при введении однократно или в виде разделенной дозы. Например, если ингибитор липазы представляет собой тетрагидролипстатин, дозировка тетрагидролипстатина предпочтительно составляет от примерно 0,05 до 2 мг/кг массы тела субъекта в сутки. На практике врач будет определять действительную дозировку ингибитора липазы,которая будет наиболее подходящей для индивидуального пациента, и она будет варьировать соответственно, например, возрасту, массе и ответу конкретного пациента. Вышеуказанные дозировки ингибиторов липазы являются примерными, но, конечно, могут быть индивидуальные случаи, где более высокие или более низкие диапазоны дозировок таких ингибиторов липазы являются предпочтительными, и все такие дозировки находятся в пределах объема настоящего изобретения. Любой подходящий путь введения можно применять по настоящему изобретению. Обычно предпочтительно вводить соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению перорально по соображениям удобства; однако их можно вводить, например, чрескожно или в виде суппозиториев для всасывания прямой кишкой, как является желательным в данном случае. Как описано выше, это введение можно осуществлять в однократных или многократных дозах,как целесообразно. Соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению можно вводить отдельно, и предпочтительно вводить их в виде фармацевтических композиций, содержащих фармацевтически приемлемые наполнитель, носитель или разбавитель. Фармацевтические композиции по изобретению будут содержать подходящее количество соединения, пролекарства, изомера или фармацевтически приемлемой соли по данному изобретению, то есть количество, достаточное для того, чтобы обеспечить желаемую дозировку. Соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению можно вводить в широком разно 004229 48 образии различных лекарственных форм, то есть их можно объединять с различными фармацевтически приемлемыми инертными носителями в любой подходящей форме. Такие носители включают в себя твердые разбавители или наполнители, стерильные водные среды и различные нетоксичные органические растворители. Фармацевтические композиции можно изготавливать в виде препаратов, содержащих суточную дозу или удобную часть суточной дозы в унифицированной дозе, которая может представлять собой отдельную таблетку или капсулу, либо удобный объем жидкости. В настоящем изобретении можно использовать все обычные типы фармацевтических композиций, включая таблетки, лепешки, твердые леденцы, жевательные таблетки, гранулы,порошки, распыляемые растворы, капсулы, пилюли, микрокапсулы, растворы, парентеральные растворы, пастилки, инъекции (например внутривенная, внутрибрюшинная, внутримышечная или подкожная), суппозитории, эликсиры, сиропы и суспензии. Для парентерального введения соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению можно применять в виде растворов в кунжутном или арахисовом масле, либо в виде водных растворов (например водный полипропиленгликоль), в зависимости от обстоятельств, и лучше всего применять их в форме стерильного водного раствора, который может содержать другие вещества, например соли или глюкозу в количестве, достаточном для того, чтобы сделать раствор изотоническим, причем рН этого раствора подходящим образом доводят и забуферивают,где это необходимо, а также поверхностноактивные вещества, такие как, например, гидроксипропилцеллюлоза. Такие масляные растворы являются подходящими для целей внутрисуставной, внутримышечной и подкожной инъекции. Такие водные растворы являются подходящими для целей внутривенной инъекции. Соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению можно также вводить местно, что можно осуществить с помощью, например, кремов, желе, бальзамов, лосьонов, гелей, паст,мазей и тому подобного, в соответствии со стандартной фармацевтической практикой. Соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению по настоящему изобретению можно также вводить чрескожно (например посредством применения пластыря). Можно использовать любой подходящий препарат для чрескожного применения, содержащий соединение по настоящему изобретению, и желательно, чтобы такие препараты, как правило, также содержали подходящий чрескожный носитель, например всасываемый фармакологически приемлемый растворитель, 49 чтобы способствовать и помогать прохождению соединений через кожу субъекта. Например,подходящие чрескожные устройства могут принимать форму бандажа, имеющего каркас и резервуар, содержащий соединение-объект. Такие чрескожные устройства бандажного типа могут дополнительно включать в себя подходящие носители, барьеры регуляции скорости и средства для закрепления этого чрескожного устройства на коже субъекта. Как будет подробно описано здесь ниже,фармацевтические композиции можно получить обычно применяемыми способами, используя общепринятые органические или неорганические добавки, такие как эксципиент (например сахароза, крахмал, маннит, сорбит, лактоза,глюкоза, целлюлоза, тальк, фосфат кальция или карбонат кальция), связывающий агент (например целлюлоза, метилцеллюлоза, гидроксиметилцеллюлоза, полипропилпирролидон, поливинилпирролидон, желатин, аравийская камедь,полиэтиленгликоль, сахароза или крахмал), разрыхлитель (например крахмал, карбоксиметилцеллюлоза, гидроксипропилкрахмал, низкозамещенная гидроксипропилцеллюлоза, бикарбонат натрия, фосфат кальция или цитрат кальция), смазывающий агент (например стеарат магния, светлая безводная кремниевая кислота,тальк или лаурилсульфат натрия), корригент(например лимонная кислота, ментол, глицин или апельсиновый порошок), консервант (например бензоат натрия, бисульфит натрия, метилпарабен или пропилпарабен), стабилизатор(например лимонная кислота, цитрат натрия или уксусная кислота), суспендирующий агент (например метилцеллюлоза, поливинилпирролидон или стеарат алюминия), диспергирующий агент(например гидроксипропилметилцеллюлоза),разбавитель (например вода), красящий агент,эмульгирующий агент и восковая основа (например масло какао, белый вазелин или полиэтиленгликоль). Препарат любого из соединений, пролекарств, изомеров или фармацевтически приемлемых солей по данному изобретению можно легко изготавливать в виде таблеток, капсул и тому подобного. Растворы предпочтительно готовить из водорастворимых солей, таких как соль гидрохлорид. Как правило, все фармацевтические композиции получают согласно способам, обычным в фармацевтической химии. Капсулы можно получить путем смешивания соединения, пролекарства, изомера или фармацевтически приемлемой соли по изобретению с подходящим разбавителем и наполнения капсул надлежащим количеством этой смеси. Обычные разбавители включают в себя инертные порошкообразные вещества, такие как крахмал многих различных видов, порошкообразная целлюлоза, особенно кристаллическая и микрокристаллическая целлюлоза, сахара, такие 50 как фруктоза, маннит и сахароза, зерновую муку и подобные пищевые порошки. Таблетки можно получить путем прямого прессования, влажной грануляции или сухой грануляции. Такие препараты обычно включают в себя разбавители, связывающие агенты, смазывающие агенты и разрыхлители, а также соединение, пролекарство, изомер или фармацевтически приемлемую соль по данному изобретению. Обычные разбавители включают в себя,например, различные виды крахмала, лактозу,маннит, каолин, фосфат или сульфат кальция,неорганические соли, такие как хлорид натрия,и сахарную пудру. Можно также использовать порошкообразные производные целлюлозы. Обычные связывающие агенты таблеток включают в себя такие вещества, как крахмал, желатин и сахара, такие как лактоза, фруктоза, глюкоза и тому подобные. Удобными также являются природные и синтетические смолы, включая акацию, альгинаты, метилцеллюлозу, поливинилпирролидон и тому подобные. В качестве связывающих агентов могут также служить полиэтиленгликоль и воски. Смазывающий агент, как правило, необходим в таблеточном препарате для предотвращения прилипания таблетки к матрице штамповочного пресса. Смазывающий агент выбирают из таких скользких твердых веществ, как тальк,стеарат магния или кальция, стеариновая кислота и гидрированные растительные масла. Разрыхлители таблеток включают в себя вещества, которые набухают при увлажнении с тем, чтобы разрушить таблетку и высвободить соединение, пролекарство, изомер или фармацевтически приемлемую соль по данному изобретению. Они включают в себя крахмалы, глины, целлюлозы, альгины и смолы. Более конкретно можно использовать, например, кукурузный и картофельный крахмалы, метилцеллюлозу, агар, бентонит, древесную целлюлозу,порошкообразную природную губку, катионообменные смолы, альгиновую кислоту, гуаровую камедь, пульпу цитрусовых и карбоксиметилцеллюлозу, а также лаурилсульфат натрия. Для того, чтобы модифицировать их свойства растворимости, таблетки часто покрывают сахаром в качестве корригента и уплотнителя,либо пленкообразующими защитными агентами. Соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению можно также включать в препараты в виде жевательных таблеток путем использования в таком препарате больших количеств веществ приятного вкуса, таких как маннит, как в настоящее время хорошо установлено в данной области техники. Если желательно вводить соединение, пролекарство, изомер или фармацевтически приемлемую соль по данному изобретению в виде суппозитория, можно использовать любую подходящую основу. Традиционной суппозиторной 51 основой является масло какао, которое можно модифицировать добавлением восков, чтобы повысить его температуру плавления. Широкое применение находят смешиваемые с водой суппозиторные основы, содержащие, в частности,полиэтиленгликоли различных молекулярных масс. Как обсуждалось выше, эффект соединения, пролекарства, изомера или фармацевтически приемлемой соли по данному изобретению может быть замедлен или пролонгирован с помощью соответствующего препарата. Например, можно получить медленно растворяющуюся гранулу соединения, пролекарства, изомера или фармацевтически приемлемой соли по данному изобретению и включить ее в таблетку или капсулу. Эту методику можно усовершенствовать, получая гранулы с несколькими различными скоростями растворения и наполняя капсулы смесью этих гранул. Таблетки или капсулы можно покрыть оболочкой, которая устойчива к растворению в течение предопределенного периода времени. Можно также получать парентеральные препараты длительного действия путем растворения или суспендирования соединения, пролекарства, изомера или фармацевтически приемлемой соли по данному изобретению, в зависимости от обстоятельств, в масляных или эмульгированных наполнителях,которые дают им возможность только медленного диспергирования в сыворотке. Соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению можно также вводить млекопитающему иному, чем человек. Способ введения и дозировка, которую следует вводить такому млекопитающему, будут зависеть, например, от вида животного и от заболевания или расстройства, которые нужно лечить. Соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению можно вводить животных любым подходящим способом, например перорально, парентерально или чрескожно, в любой подходящей форме, такой как, например, капсула, болюс, таблетка, пилюля, например, полученная смешиванием соединения, пролекарства, изомера или фармацевтически приемлемой соли по данному изобретению с подходящим разбавителем, таким как карбовоск или carnuba воск, со смазывающим агентом; жидкое питье или паста, например,полученная диспергированием соединения,пролекарства, изомера или фармацевтически приемлемой соли по данному изобретению в фармацевтически приемлемом масле, таком как арахисовое масло, кунжутное масло или кукурузное масло. Соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению можно также вводить животным в виде имплантата. Такие препараты также изготавливают общепринятым способом в соответствии со стандартной ветеринарной 52 практикой. В качестве альтернативы соединения, пролекарства, изомеры и фармацевтически приемлемые соли по данному изобретению можно вводить с подачей воды, например, в форме жидкого или водорастворимого концентрата. Кроме того, соединения, пролекарства,изомеры и фармацевтически приемлемые соли по данному изобретению, например, в составе фармацевтических композиций по изобретению,можно вводить в корм животного, например,можно получить концентрированную пищевую добавку или премикс для смешивания с обычным кормом животного, обычно вместе с подходящим носителем для этого. Этот носитель способствует однородному распределению соединения, пролекарства, изомера или фармацевтически приемлемой соли по данному изобретению, например, в готовом корме, с которым смешивают этот премикс. Подходящие носители включают в себя жидкости, например воду,масла, такие как соевое, кукурузное, хлопковое,или летучие органические растворители, а также твердые вещества, например, небольшую порцию корма или различные подходящие пищевые добавки, включая люцерновое, соевое,хлопковое масло, льняное масло, стержни кукурузных початков, кукурузу, мелассы, мочевину и кости, а также минеральные смеси, но не ограничены ими. Поскольку в настоящем изобретении есть аспект, который относится к лечению заболеваний/состояний, описанных здесь, комбинацией активных ингредиентов, которые можно вводить по-отдельности, изобретение также относится к комбинированию отдельных фармацевтических композиций в форме набора. Этот набор содержит две отдельные фармацевтические композиции: соединение формулы I, либо его пролекарство, либо его геометрический или оптический изомер, либо фармацевтически приемлемую соль такого соединения, пролекарства или изомера, и второе соединение, как описано выше. Этот набор содержит контейнер для помещения отдельных композиций, такой как разделенный флакон или разделенный пакет из фольги. Обычно этот набор содержит инструкции по введению отдельных компонентов. Форма набора имеет особенное преимущество, когда отдельные компоненты предпочтительно вводить в различных лекарственных формах(например пероральной и парентеральной), вводить в различных интервалах дозировки, либо когда по предписанию врача желательно титрование индивидуальных компонентов комбинации. Примером такого набора является так называемая блистерная упаковка. Блистерные упаковки хорошо известны в упаковочной промышленности, и их широко применяют для упаковки фармацевтических стандартных лекарственных форм (таблеток, капсул и тому подобного). Блистерные упаковки обычно состоят из 53 листа из относительно жесткого материала, покрытый фольгой из предпочтительно прозрачного пластичного материала. Во время процесса упаковки в этой пластичной фольге образуют углубления. Эти углубления имеют размер и форму таблеток или капсул, которые нужно упаковывать. Затем таблетки или капсулы помещают в эти углубления, и лист из относительно жесткого материала припаивают к пластичной фольге на лицевой стороне этой фольги, которая является противоположной направлению, в котором образуют углубления. В результате таблетки или капсулы запаяны в углубления между пластиковой фольгой и листом. Предпочтительно жесткость листа является такой, чтобы таблетки или капсулы можно было извлечь из блистерной упаковки, прилагая вручную давление на углубления, посредством чего в листе образуется отверстие на месте углубления. Затем через указанное отверстие можно извлечь таблетку или капсулу. Может быть желательным обеспечить набор вспомогательной памяткой, например, в форме номеров рядом с таблетками или капсулами, где эти номера соответствуют суткам схемы приема, в которые следует принимать эти таблетки или капсулы. Другой пример такой вспомогательной памятки представляет собой календарь, напечатанный на карточке, например следующим образом: Первая неделя, понедельник, вторник и т. д.Вторая неделя, понедельник, вторник,и т. д. Другие варианты вспомогательных памяток также очевидны. Суточная доза может составлять одну таблетку или капсулу, либо несколько таблеток или капсул, которые следует принимать в данные сутки. Также суточная доза соединения формулы I, либо его пролекарства, либо его геометрического или оптического изомера, либо фармацевтически приемлемой соли такого соединения, пролекарства или изомера может состоять из одной таблетки или капсулы, тогда как суточная доза второго соединения может состоять из нескольких таблеток или капсул, и наоборот. Это должно быть отражено во вспомогательной памятке. В другом конкретном воплощении изобретения предложено дозирующее устройство,предназначенное для дозировки суточных доз по одной в порядке их назначенного применения. Предпочтительно это дозирующее устройство снабжено запоминающим устройством,чтобы дополнительно способствовать соблюдению режима. Примером такого запоминающего устройства является механический счетчик, который указывает число суточных доз, которые были дозированы. Другим примером такого запоминающего устройства является микросхема памяти с питанием от батареек, соединенная с жидкокристаллическим считывающим устройством или со звуковым напоминающим сигналом, которая, например, считывает данные о 54 том, что последняя суточная доза принята, и/или напоминает, когда следует принимать следующую дозу. О пользе соединений формулы I, либо их изомеров, либо фармацевтически приемлемых солей таких соединений или их изомеров может свидетельствовать активность по меньшей мере в одном из двух анализов, описанных ниже. Анализ 1. Потребление кислорода. Как следует понимать специалистам в соответствующей области техники, во время повышенного расхода энергии животные, как правило, потребляют больше кислорода. Кроме того, метаболическое топливо, например глюкоза и жирные кислоты, окисляется до СО 2 и Н 2O с сопутствующим выделением тепла, обычно называемым в данной области техники термогенезом. Таким образом, измерение потребления кислорода у животных, включая людей и домашних животных, является непрямой мерой термогенеза. Чтобы измерять такие расходы энергии, специалисты в соответствующей области техники обычно используют непрямую калориметрию у животных, например, людей. Специалисты в данной области техники понимают, что повышенный расход энергии и сопутствующее сжигание метаболического топлива, приводящее в результате к продуцированию тепла, могут быть эффективными при лечении, например, ожирения. Как хорошо известно специалистам в данной области техники,тиреоидные гормоны влияют на функционирование сердца, например, вызывая повышение частоты сердечных сокращений и, соответственно, повышение потребления кислорода с сопутствующим продуцированием тепла. Способность соединений, их изомеров и фармацевтически приемлемых солей указанных соединений и изомеров по данному изобретению генерировать термогенный ответ можно продемонстрировать согласно следующему протоколу. Анализ 1. А. Эксперимент. Данный скрининг in vivo разработан для оценки эффективности и сердечных эффектов соединений, которые являются тканеспецифичными агонистами тиреоидных гормонов. Измеряемыми показателями эффективности являются потребление кислорода целым организмом и активность митохондриальной альфа-глицерофосфатдегидрогеназы печени (мГФДГ). Измеряемыми сердечными показателями являются масса сердца и активность сердечной мГФДГ. Протокол включает в себя: (а) дозирование крысам Zucker с ожирением в течение примерно 6 суток, (б) измерение потребления кислорода и(в) сбор ткани для препаратов митохондрий и последующий анализ ферментативной активности в этих препаратах. Б. Подготовка крыс. Перед началом исследования самцов крыс 55 тела от примерно 400 г до примерно 500 г содержат в течение от примерно 3 до примерно 7 суток в индивидуальных клетках в стандартных лабораторных условиях. Соединение формулы I, либо его изомер,либо фармацевтически приемлемую соль такого соединения или изомера, наполнитель или натриевую соль Т 3 вводят посредством перорального зондового питания в однократной суточной дозе, даваемой между примерно 3 ч после полудня и примерно 6 ч после полудня в течение примерно 6 суток. Соединение формулы I,либо его изомер, либо фармацевтически приемлемую соль такого соединения или изомера,либо натриевую соль Т 3 растворяют в подходящем небольшом объеме примерно 1 н. NaOH, а затем доводят до подходящего объема примерно 0,01 н. NaOH, содержащим 0,25% метилцеллюлозы (10:1, 0,01 н. NaOH/МЦ: 1 н. NaOH). Дозируемый объем составляет примерно 1 мл. В. Потребление кислорода. Примерно через 1 сутки после введения последней дозы соединения измеряют потребление кислорода, используя непрямой калориметр с незамкнутым контуром (Oxymax, Columbus Instruments, Columbus, ОН 43204). Газовые датчики Oxymax калибруют газообразным N2 и газовой смесью (примерно 0,5% СO2, примерно 20,5% O2, примерно 79% N2) перед каждым экспериментом. Крыс, подлежащих эксперименту, извлекают из клеток для содержания и записывают их массы тела. Этих крыс помещают в герметичные камеры (43 х 43 х 10 см) Oxymax, камеры помещают в мониторы активности, а затем устанавливают скорость потока воздуха через камеры от примерно 1,6 л/мин до примерно 1,7 л/мин. Затем программное обеспечение Охуmax вычисляет потребление кислорода (мл/кг/ч) крысами на основании скорости потока воздуха через камеры и разности в содержании кислорода на входе и на выходе. Мониторы активности имеют 15 инфракрасных световых лучей, расположенных на расстоянии примерно одного дюйма (примерно 2,5 см) на каждой оси, и амбулаторную активность регистрируют, когда прерываются два последовательных луча, и результаты регистрируют в виде отсчетов. Потребление кислорода и амбулаторную активность измеряют примерно каждые 10 мин в течение от примерно 5 ч до примерно 6,5 ч. Потребление кислорода в покое вычисляют у индивидуальных крыс путем усреднения значений, исключая первые 5 значений и значения,полученные в течение периодов времени, когда амбулаторная активность превышает примерно 100 отсчетов. Анализ 2. Связывание с рецепторами тиреоидных гормонов. Способность соединения формулы I, либо его изомера, либо фармацевтически приемлемой 56 соли такого соединения или изомера (тестируемые тиреомиметические соединения) связываться с рецепторами тиреоидных гормонов можно продемонстрировать в следующем протоколе. А. Получение ядерных экстрактов клеток насекомых. Осадки клеток High Five (BTI-TN-5B1-4,номер по каталогу В 855-02, Invitrogen,Carlsbad, California), полученные через примерно 48 ч после инфекции бакуловирусом (GibcoBRL, Gaithersburg, Maryland), экспрессирующим человеческий TR или человеческийTR, суспендировали в охлажденном во льду буфере для образца (10 мМ Трис, рН 8,0; 1 мМMgCl2; 1 мМ ДТТ; 0,05% Твин 20; 1 мМ 4-(2 аминоэтил)-бензолсульфонилфторид; 25 мкг/мл лейпептина). Примерно через 10 мин инкубации на льду эту суспензию гомогенизировали 20 ударами в гомогенизаторе Dounce (VWR Scientific Products, West Chester, Pennsylvania) и центрифугировали при 800xg в течение примерно 15 мин при 4 С. Остаток (ядра) суспендировали в гипертоническом буфере (0,4 М KCl; 10 мМ Трис, рН 8,0; 1 мМ MgCl2; 1 мМ ДТТ; 0,05% Твин 20) и инкубировали в течение примерно 30 мин на льду. Эту суспензию центрифугировали при 100000g в течение примерно 30 мин при 4 С. Супернатант (ядерный экстракт) хранили в 0,5 мл аликвотах при -80 С. Б. Анализ связывания. Анализы конкурентного связывания для измерения взаимодействия тестируемых тиреомиметических соединений с рецепторами тиреоидных гормонов 1 и 1 (TR и TR) осуществляют согласно следующему протоколу. Растворы тестируемых тиреомиметических соединений (конечная концентрация соединения 20 мМ) получают, используя 100%-ный ДМСО в качестве растворителя. Каждое соединение серийно разбавляют в буфере для анализа (5 мМ Трис HCl, рН 8,0; 50 мМ NaCl; 2 мМ ЭДТА; 10% (об./об.) глицерин; 1 мМ ДТТ, буфер для анализа),содержащем 0,4 нМ 125I-Т 3 (удельная активность примерно 220 Ки/ммоль) с получением растворов, которые варьируют по концентрации соединения от примерно 10 мкМ до примерно 0,1 нМ. Ядерный экстракт клеток насекомых HighFive, содержащий либо TR, либо TR, разбавляют до суммарной концентрации белка 0,0075 мг/мл, используя буфер для анализа в качестве разбавителя. Один объем (100 мкл) разведения каждого тиреомиметического соединения (содержащий 0,4 нМ 125I-Т 3) объединяют с равным объемом(100 мкл) разбавленного ядерного экстракта,содержащего TR или TR, и инкубируют при КТ в течение примерно 90 мин. Отбирают 150 мкл образец смеси для реакции связывания и помещают в 96-луночный фильтровальный 57 планшет (Millipore, Bedford, Massachusetts),который предварительно был промыт охлажденным во льду буфером для анализа. Планшет подвергают вакуумному фильтрованию, используя фильтрующий коллектор (Millipore). Каждую лунку промывают пять раз добавлением 200 мкл охлажденного во льду буфера для анализа и последующим вакуумным фильтрованием. Планшет извлекают из вакуумного фильтрационного коллектора, дно планшета быстро высушивают на бумажных полотенцах, затем в каждую лунку добавляют 25 мкл сцинтилляционной смеси Wallac (EGG Wallac,Gaithersburg, Maryland) Optiphase Supermix, и верх планшета покрывают пластиковой герметизирующей лентой (Microplate Press-on Adhesive seating Film, Packard Instrument Co., Inc.,Downers Grove, Illinois) и подсчитывают радиоактивность, используя сцинтилляционный счетчик 96-луночных планшетов Wallac Microbeta. Следующие примеры предложены исключительно в целях иллюстрации и не ограничивают изобретение, которое определено формулой изобретения. Пример 1. N-3,5-Дихлоро-4-[4-гидрокси 3-(пирролидин-1-сульфонил)фенокси]фенил оксаминовая кислота. Стадия А. 2',6'-Дихлоро-4-метокси-4'-нитродифениловый эфир получили сочетанием 2,6 дихлоро-4-нитрофенола с (4,4'-диметоксидифенил)иодония тетрафторборатом в присутствии медного порошка и ТЭА согласно методике,описанной в J. Med. Chem., 38: 695-707 (1995). Стадия Б. Раствор чистого 2',6'-дихлоро-4 метокси-4'-нитродифенилового эфира (500 мг,1,6 ммоль) при 0 С обрабатывали хлорсульфоновой кислотой (877 мл, 7,5 ммоль), и эта реакционная смесь немедленно становилась темнокоричневой. Эту смесь перемешивали в течение 5 мин при 0 С и давали ей нагреться до КТ. После перемешивания в течение 30 мин при КТ эту реакционную смесь медленно капали в 100 мл ледяной воды при перемешивании. Коричневый осадок экстрагировали этилацетатом (3 х 75 мл). Объединенные органические экстракты промывали бикарбонатом натрия (1 х 100 мл), водой(1 х 100 мл), высушивали и концентрировали с получением коричневого твердого вещества. Этот сырой продукт использовали в следующей стадии без дальнейшей очистки. ЯМР (400 МГц, CDCl3) d 8.32 (s, 2H), 7.40 58 пирролидин (85 мл, 1,0 ммоль). После перемешивания в течение 2 ч при КТ реакционную смесь гасили 1 н. HCl (5 мл) и экстрагировалиCH2Cl2 (3 х 10 мл). Объединенные экстракты промывали 1 н. HCl (3 х 5 мл), насыщенным водным NаНСО 3 (2 х 5 мл), высушивали и концентрировали. Остаток очищали препаративной ТСХ (гексан : EtOAc = 2:1) с получением белого твердого вещества. ЯМР (400 МГц, CDCl3) d 8.30 (s, 2H), 7.39(М+1). Стадия Г. К раствору 1-[5-(2,6-дихлоро-4 нитрофенокси)-2-метоксибензолсульфонил] пирролидина (178,5 мг, 0,4 ммоль) в 8 мл хлороформа при КТ добавляли по каплям трибромид бора (1 н. в CH2Cl2, 2,4 мл, 2,4 ммоль). После перемешивания в течение 16 ч при КГ реакционную смесь гасили 10 мл воды. Эту смесь перемешивали в течение 1 ч при КГ, экстрагировали CH2Cl2 (1 х 5 мл) и EtOAc (2 х 10 мл). Объединенные органические экстракты высушивали и концентрировали. Этот продукт использовали в следующей стадии без дальнейшей очистки. ЯМР (400 МГц, CD3OD) d 8.31 (s, 2H), 7.09(275,8 кПа) при КГ в течение 1 ч. Этот раствор фильтровали через Celite и концентрировали с получением коричневого твердого вещества. Этот продукт использовали в следующей стадии без дальнейшей очистки. ЯМР (400 МГц, CDCl3) d 8.34 (s, 2H), 6.967.22 (широкий s + m, 5H), 3.19 (m, 4H), 1.73 (m,4H). МС вычислено: 402; обнаружено: 401,1 (M1). Стадия Е. Смесь 4-(4-амино-2,6-дихлорофенокси)-2-(пирролидин-1-сульфонил)фенола(154 мг, 0,38 ммоль) и диэтилоксалата (1,49 г,10,2 ммоль) перемешивали при 120 С в течение 4 ч. Избыток диэтилоксалата отгоняли в вакууме. Остаток очищали препаративной ТСХ (0,5% МеОН в CH2Cl2) с получением беловатого твердого вещества. ЯМР (400 МГц, CDCl3) d 9.06 (s, 1H), 8.60(m, 4H), 1.74-1.78 (m, 4 Н), 1.39 (t, 3H). МС вычислено: 502; обнаружено: 501,1 (M-1). Стадия Ж. К раствору N-3,5-дихлоро-4[4-гидрокси-3-(пирролидин-1-сульфонил)фенокси]фенилоксаминовой кислоты диэтилового эфира (10 мг, 0,02 ммоль) в смеси Н 2O (0,5 59 мл) и МеОН (0,5 мл) добавляли 2 капли 3 н. КОН. Эту реакционную смесь перемешивали при КТ в течение 2 ч, подкисляли 1 н. HCl и экстрагировали EtOAc (4 х 5 мл). Объединенные органические экстракты высушивали и концентрировали с получением соединения, указанного в заголовке, в виде беловатого твердого вещества. ЯМР (400 МГц, CD3OD) d 7.96 (s, 2H),7.02-7.06 (m, 2H), 6.95-6.98 (d, 1H), 3.28-3.31 (m,4H), 1.78-1.81 (m, 4H). МС вычислено: 474,3; обнаружено: 473,1 (M-1). Используя соответствующие исходные материалы, примеры 1-1 - 1-57 получили способом, аналогичным описанному в примере 1. Пример 1-1. N-[4-(3-Циклопропилсульфамоил-4-гидроксифенокси)-3,5-диметилфенил] оксаминовой кислоты этиловый эфир. МС вычислено: 448,5; обнаружено: 447,3 (M-1). Пример 1-2. N-[4-(4-Гидрокси-3-метилсульфамоилфенокси)-3,5-диметилфенил]оксаминовой кислоты этиловый эфир. МС вычислено: 422,5; обнаружено: 421,3 (M-1). Пример 1-3. N-4-[3-(4-Фторофенилсульфамоил)-4-гидроксифенокси]-3,5-диметилфенилоксаминовой кислоты этиловый эфир. МС вычислено: 502,5; обнаружено: 501,1 (M-1). Пример 1-4. N-[4-(3-Диметилсульфамоил 4-гидроксифенокси)-3,5-диметилфенил]оксаминовой кислоты этиловый эфир. МС вычислено: 436,5; обнаружено: 435,3 (M-1). Пример 1-5. N-4-[3-(Циклопропилметилсульфамоил)-4-гидроксифенокси]-3,5-диметилфенилоксаминовой кислоты этиловый эфир. МС вычислено: 462,5; обнаружено: 461,2 (M-1). Пример 1-6. N-4-[3-(Циклобутилметилсульфамоил)-4-гидроксифенокси]-3,5-диметилфенилоксаминовой кислоты этиловый эфир. МС вычислено: 476,6; обнаружено: 475,3 (M-1). Пример 1-7. N-[4-(3-Циклобутилсульфамоил-4-гидроксифенокси)-3,5-диметилфенил] оксаминовой кислоты этиловый эфир. МС вычислено: 462,5; обнаружено: 461,2 (M-1). Пример 1-8. N-[4-(3-Циклопентилсульфамоил-4-гидроксифенокси)-3,5-диметилфенил] оксаминовой кислоты этиловый эфир. МС вычислено: 476,6; обнаружено: 475,3 (M-1). Пример 1-9. N-4-[4-Гидрокси-3-(пирролидин-1-сульфонил)фенокси]-3,5-диметилфенил оксаминовой кислоты этиловый эфир. МС вычислено: 462,5; обнаружено: 461,3 (M-1). Пример 1-10. N-4-[4-Гидрокси-3-(пиперидин-1-сульфонил)фенокси]-3,5-диметилфенил оксаминовой кислоты этиловый эфир. МС вычислено: 476,6; обнаружено: 475,2 (M-1). Пример 1-11. N-[4-(3-Циклогексилсульфамоил-4-гидроксифенокси)-3,5-диметилфенил] оксаминовой кислоты этиловый эфир. МС вычислено: 490,6; обнаружено: 489,3 (M-1). Пример 1-12. N-[4-(4-Гидрокси-3-пропилсульфамоилфенокси)-3,5-диметилфенил]оксаминовой кислоты этиловый эфир. МС вычислено: 450,5; обнаружено: 449,3 (M-1).(M-1). Пример 1-25. N-[3-Хлоро-4-(3-диметилсульфамоил-4-гидроксифенокси)-5-метилфенил]оксаминовой кислоты этиловый эфир. МС вычислено: 456,1; обнаружено: 457,3 (М+1). Пример 1-26. N-[3-Хлоро-4-(4-гидрокси-3 метилсульфамоилфенокси)-5-метилфенил]оксаминовой кислоты этиловый эфир. МС вычислено: 442,1; обнаружено: 441,2 (M-1). Пример 1-27. N-[3-Хлоро-4-(4-гидрокси-3 пропилсульфамоилфенокси)-5-метилфенил] оксаминовой кислоты этиловый эфир. МС вычислено: 470,1; обнаружено: 469,2 (M-1).
МПК / Метки
МПК: A61K 31/165, C07C 235/74, A61P 5/16
Метки: оксаминовые, производные, качестве, лигандов, тиреоидных, рецепторов, кислоты
Код ссылки
<a href="https://eas.patents.su/30-4229-oksaminovye-kisloty-i-ih-proizvodnye-v-kachestve-ligandov-tireoidnyh-receptorov.html" rel="bookmark" title="База патентов Евразийского Союза">Оксаминовые кислоты и их производные в качестве лигандов тиреоидных рецепторов</a>
Предыдущий патент: Модулятор иммунного ответа alpha2- макроглобулиновый комплекс
Следующий патент: Способ получения лигнинсодержащего фармацевтического препарата, обладающего антиоксидантным, антигипоксическим, радиопротекторным и противоопухолевым действием
Случайный патент: Модуляторы регулятора трансмембранной проводимости при муковисцидозе












