Производные бензил (иден)-лактамов, их получение и применение в качестве селективных (ант)агонистов рецепторов 5-нт1а и/или 5-нт1d
Формула / Реферат
1. Соединение формулы I, изображенной ниже,
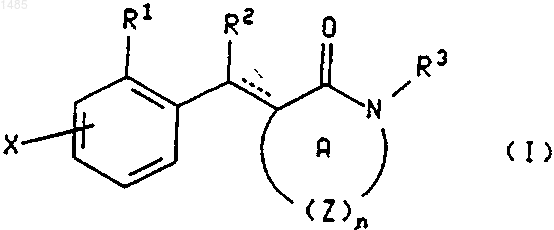
где R1 представляет собой 2-диметиламиноэтоксигруппу или группу формулы G1, G2, G3, G4 или G5, которые изображены ниже,
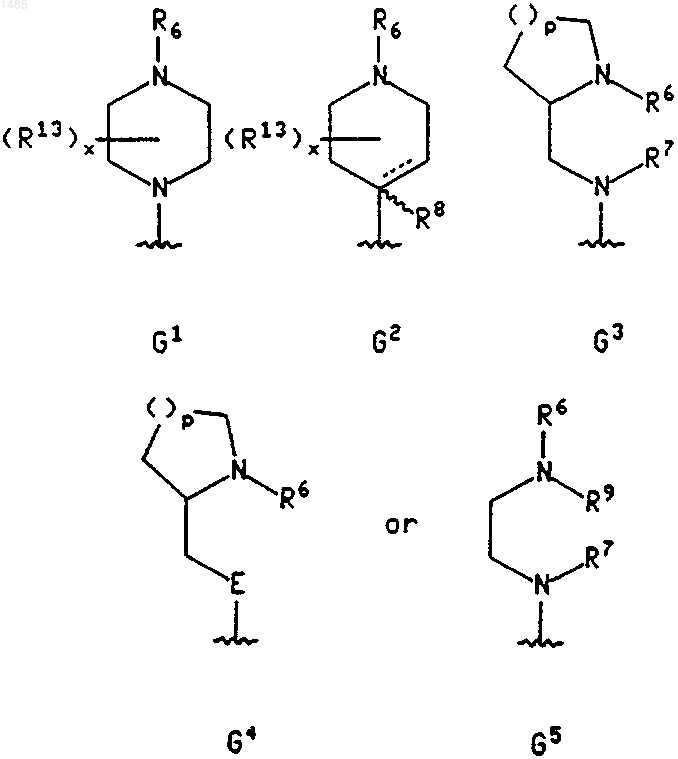
где Е представляет собой кислород, серу, SO или SO2;
R6 и R7 независимо выбраны из водорода, (С1-С6)алкила, [(С2-С4)алкил]арила, где арильная группировка представляет собой фенил или нафтил, и гетероарила-(СН2)q, где гетероарильная группировка выбрана из пиридила, пиримидила, бензоксазолила, бензотиазолила, бензизоксазолила и бензизотиазолила, a q равно 0, 1, 2, 3 или 4, и где указанные арильная и гетероарильная группировки могут быть возможно замещены одним или более чем одним заместителем, независимо выбранным из хлоро, фторо, бромо, иодо, (С1-С6)алкила, (С1-С6)алкокси, трифторометила, циано и SOg(С1-С6)алкила, где g равно 0, 1 или 2;
или R6 и R7 вместе образуют цепь, содержащую от 2 до 4 атомов углерода;
x равно числу от 0 до 8;
каждый R13 независимо представляет собой (С1-С4)алкил или (C1-С4)метиленовый мостик от одного из кольцевых углеродов пиперазинового или пиперидинового кольца G1 или G2 соответственно к тому же самому или другому кольцевому углероду или к кольцевому азоту пиперазинового или пиперидинового кольца G1 или G2 соответственно имеющему доступный центр связывания, или к кольцевому углероду радикала R6, имеющему доступный центр связывания;
R8 выбран из водорода и (С1-С3)алкила;
R9 выбран из водорода и (С1-С6)алкила;
или R6 и R9 вместе с атомом азота, к которому они присоединены, образуют кольцо, содержащее от 5 до 7 членов;
и р равно 1, 2 или 3;
R2 представляет собой водород, (С1-С4)алкил, фенил или нафтил, где названные фенил или нафтил могут быть возможно замещены одним или более чем одним заместителем, предпочтительно заместителями числом от нуля до трех, независимо выбранными из хлоро, фторо, бромо, иодо, (С1-С6)алкила, (С1-С6)алкокси, трифторметила, циано и SОg(С1-С6)алкила, где g равно 0, 1 или 2;
R3 представляет собой (CH2)mВ, где m равно 0, 1, 2 или 3, а В представляет собой водород, фенил, нафтил или 5- или 6-членную гетероарильную группу, содержащую от одного до четырех гетероатомов в кольце (например фурил, тиенил, пиридил, пиримидил, тиазолил, пиразолил, изотиазолил, оксазолил, изоксазолил, пирролил, триазолил, тетразолил, имидазолил и т.п.), и где каждая из вышеуказанных арильных и гетероарильных групп может быть возможно замещена одним или более чем одним заместителем, предпочтительно заместителями числом от нуля до трех, независимо выбранными из хлоро, фторо, бромо, иодо, (С1-С6)алкила, (С1-С6)алкокси, трифторметила, циано, гидрокси, СООН и SОg(С1-С6)алкила, где g равно 0, 1 или 2;
Z представляет собой CR4R5, где R4 и R5 независимо выбраны из водорода, (C1-С6)алкила и трифторметила, или Z может быть одной из арильных или гетероарильных групп, указанных выше в определении В, и где два соседних члена кольца Z являются также членами кольца А;
X представляет собой водород, хлоро, фторо, бромо, иодо, циано, (C1-С6)алкил, гидрокси, трифторметил, (С1-С6)алкокси, SОg(С1-С6)алкил, где g равно 0, 1 или 2, CO2R10 или CONR11R12;
каждый из R10, R11 и R12 независимо выбран из радикалов, указанных ранее в определении R2; или R11 и R12 вместе с азотом, к которому они присоединены, образуют кольцо, содержащее от 5 до 7 членов, которое может содержать от нуля до четырех гетероатомов, выбранных из азота, серы и кислорода;
n равно 1, 2, 3 или 4, а
прерывистая линия указывает на возможную двойную связь;
при условии, что n должно быть равно 1, когда Z представляет собой гетероарильную группу;
и при условии, что когда R1 представляет собой 2-диметиламиноэтоксигруппу, R2 представляет собой водород, m равно 0, В представляет собой 3,4-дихлорфенильную группу, X представляет собой водород, каждый из R4 и R5 представляет собой водород, n равно 2, а прерывистая линия указывает на двойную связь;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где R1 представляет собой пиперазинил.
3. Соединение по п.1, где Z представляет собой СН2.
4. Соединение по п.1, где n равно 2 или 3.
5. Соединение по п.1, где R3 представляет собой замещенный фенил.
6. Соединение по п.2, где Z представляет собой СН2.
7. Соединение по п.6, где R3 представляет собой замещенный фенил.
8. Соединение по п.7, где n равно числу два или три.
9. Соединение по п.1, где указанное соединение выбрано из
3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1,3-дигидро-индол-2-он;
6-хлор-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1,3-дигидро-индол-2-он;
5-хлор-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1,3-дигидро-индол-2-он;
1-метил-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1,3-дигидро-индол-2-он;
3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-фенил-1,3-дигидро-индол-2-он;
1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он;
1-(3,4-дихлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1,3-дигидро-индол-2-он;
1-(4-хлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он;
1-(4-хлорбензил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он;
1-(3,4-дифторфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он;
1-(2,4-дихлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он;
1-(3,4-дихлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он;
1-(4-хлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он;
1-(3,4-дихлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он;
1-(4-хлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он;
1-(3,4-дихлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он;
3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-фенил-пирролидин-2-он;
3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-(4-трифторметилфенил)-пирролидин-2-он;
1-(3,4-дифторфенил)-3-[2-(4-метилпиперазин-1-ил)-бензил]-пирролидин-2-он;
3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он;
3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он;
3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он;
1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензил]-пиперидин-2-он;
1-(4-метоксифенил )-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-3,4-дигидро-1Н-хинолин-2-он;
1-(3,4-дихлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензил]-пиперидин-2-он;
3-[2-(4-метилпиперазин-1-ил)-бензил]-1-фенил-пирролидин-2-он;
3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-(п-толил)-пирролидин-2-он;
3-[4-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-1-фенил-пирролидин-2-он;
1-(3,4-дихлорфенил)-3-[2-фтор-6-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он;
1-(3,4-дифторфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пиперин-2-юэ;
1-[2-(4-хлорфенил)этил]-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он;
1-(3,4-дихлорфенил)-3-[2-(2-диметиламиноэтокси)-бензилиден]-пирролидин-2-он; и
3-[2-(4-метилпиперазин-1-ил)-бензил]-1-(4-трифторметилфенил)-пирролидин-2-он;
и фармацевтически приемлемые соли таких соединений.
10. Фармацевтическая композиция для лечения или предупреждения расстройства или состояния, выбранного из гипертензии, депрессии, общего состояния тревоги, фобий, посттравматического стресс-синдрома, расстройства сенситивная личность, преждевременной эякуляции, расстройств аппетита, ожирения, токсикомании, "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти, болезней Паркинсона, эндокринных расстройств, вазоспазма, церебеллярной атаксии, расстройств желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами, у млекопитающего, содержащая такое количество соединения по п.1, которое является эффективным при лечении или предупреждении такого расстройства или состояния, и фармацевтически приемлемый носитель.
11. Фармацевтическая композиция для лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего, содержащая такое количество соединения по п.1, которое является эффективным при лечении или предупреждении такого расстройства или состояния, и фармацевтически приемлемый носитель.
12. Способ лечения или предупреждения расстройства или состояния, выбранного из гипертензии, депрессии, общего состояния тревоги, фобий, посттравматического стресс-синдрома, расстройства сенситивная личность, преждевременной эякуляции, расстройств аппетита, ожирения, токсикомании, "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти, болезней Паркинсона, эндокринных расстройств, вазоспазма, церебеллярной атаксии, расстройств желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами, у млекопитающего, при котором млекопитающему, нуждающемуся в таком лечении или предупреждении, вводят такое количество соединения по п.1, которое является эффективным при лечении или предупреждении такого расстройства или состояния.
13. Способ лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего, при котором млекопитающему, нуждающемуся в таком лечении или предупреждении, вводят такое количество соединения по п.1, которое является эффективным при лечении или предупреждении такого расстройства или состояния.
14. Фармацевтическая композиция для лечения или предупреждения расстройства или состояния, выбранного из гипертензии, депрессии, общего состояния тревоги, фобий, посттравматического стресс-синдрома, расстройства сенситивная личность, преждевременной эякуляции, расстройств аппетита, ожирения, токсикомании, "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти, болезней Паркинсона, эндокринных расстройств, вазоспазма, церебеллярной атаксии, расстройств желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами, у млекопитающего, содержащая эффективное антагонистирующее или агонистирующее рецепторы серотонина количество соединения по п.1 и фармацевтически приемлемый носитель.
15. Фармацевтическая композиция для лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего, содержащая эффективное антагонистирующее или агонистирующее рецепторы серотонина количество соединения по п.1 и фармацевтически приемлемый носитель.
16. Способ лечения или предупреждения расстройства или состояния, выбранного из гипертензии, депрессии, общего состояния тревоги, фобий, посттравматического стресс-синдрома, расстройства сенситивная личность, преждевременной эякуляции, расстройств аппетита, ожирения, токсикомании, "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти, болезней Паркинсона, эндокринных расстройств, вазоспазма, церебеллярной атаксии, расстройств желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами, у млекопитающего, при котором млекопитающему, которому требуется такое лечение или предупреждение, вводят эффективное антагонистирующее или агонистирующее рецепторы серотонина количество соединения по п.1.
17. Способ лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего, при котором млекопитающему, которому требуется такое лечение или предупреждение, вводят эффективное антагонистирующее или агонистирующее рецепторы серотонина количество соединения по п.1.
18. Фармацевтическая композиция для лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего, содержащая
а) фармацевтически приемлемый носитель;
б) соединение по п.1; и
в) ингибитор обратного захвата 5-НТ или его фармацевтически приемлемую соль;
где количество активных соединений таково, что данная комбинация эффективна при лечении или предупреждении такого расстройства или состояния.
19. Способ лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего, при котором млекопитающему, которому требуется такое лечение или предупреждение, вводят
а) соединение по п.1;
б) ингибитор обратного захвата 5-НТ или его фармацевтически приемлемую соль;
где количества активных соединений таковы, что данная комбинация эффективна при лечении или предупреждении такого расстройства или состояния.
20. Фармацевтическая композиция по п.18, где ингибитор обратного захвата 5-НТ представляет собой сертралин или его фармацевтически приемлемую соль.
21. Способ по п.19, при котором ингибитор обратного захвата 5-НТ представляет собой сертралин или его фармацевтически приемлемую соль.
22. Способ лечения или предупреждения расстройства или состояния, выбранного из гипертензии, депрессии, общего состояния тревоги, фобий, посттравматического стресс-синдрома, расстройства сенситивная личность, преждевременной эякуляции, расстройств аппетита, ожирения, токсикомании, "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти, болезней Паркинсона, эндокринных расстройств, вазоспазма, церебеллярной атаксии, расстройств желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами, у млекопитающего, при котором млекопитающему, которому требуется такое лечение или предупреждение, вводят
а) соединение по п.1; и
б) ингибитор обратного захвата 5-НТ или его фармацевтически приемлемую соль;
где количества активных соединений таковы, что данная комбинация эффективна при лечении или предупреждении такого расстройства или состояния.
Текст
1 Предпосылки изобретения Настоящее изобретение относится к производным лактамов, к способам и промежуточным соединениям для их получения, к содержащим их фармацевтическим композициям и к их медицинскому применению. Соединения по настоящему изобретению включают в себя селективные агонисты и антагонисты рецепторов серотонина 1 (5-HT1), конкретно одного или обоих рецепторов 5-HT1A и 5-HT1D. Они полезны при лечении или предупреждении мигрени,депрессии и других расстройств, для которых показан агонист или антагонист 5-HT1. Европейский патент 434561, опубликованный 26 июня 1991, относится к 7-алкил, алкокси- и гидроксизамещенным-1-(4-замещенным-1-пиперазинил)-нафталинам. Соединения относятся к 5-НТ 1-агонистам и антагонистам,полезным при лечении мигрени, депрессии, тревожности, шизофрении, стресса и боли. Европейский патент 343050, опубликованный 23 ноября 1989, относится к 7 незамещенным, галогенированным и метоксизамещенным-1-(4-замещенным-1-пиперазинил)нафталинам в качестве полезных 5-HT1A лигандных терапевтических средств.Glennon et al. ссылаются на 7-метокси-1-(1 пиперазинил)-нафталин как на полезный 5-НТ 1 лиганд в своей статье "5-НТ 1D Serotonine Receptors" [Clinical Drug Res. Dev., 22, 25-36, 1991]. Статья Glennon "Serotonin Receptors: Clinical Implications" [Neuroscience and BehavoralReviews, 4, 35-47, 1991] посвящена фармакологическим эффектам, связанным с серотониновыми рецепторами, включая подавление аппетита, терморегуляцию, сердечно-сосудистые/ гипотензивные эффекты, сон, психоз, состояние тревоги, депрессию, тошноту, рвоту, болезнь Альцгеймера, болезнь Паркинсона и болезнь Гентингтона. Лиганды с сильным сродством к 5-HT1 рецепторам хорошо известны как обладающие терапевтической ценностью для лечения состояний человека, вызванных дисбалансом серотонина. Международная патентная заявка WO 95/31988, опубликованная 30 ноября 1995, относится к применению антагониста 5-НТ 1D в комбинации с антагонистом 5-HT1A для лечения расстройств ЦНС (центральной нервной системы), таких как депрессия, общее состояние тревоги, паническое состояние, агорафобия, социальные фобии, обсессивно-компульсивное расстройство, посттравматический стресс, нарушения памяти, нервная анорексия и нервная булимия, болезнь Паркинсона, поздние дискинезии,эндокринные расстройства, такие как гиперпролактинемия, вазоспазм (в частности, мозговых сосудов) и гипертензия, расстройства желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, а также сексуальные нарушения.G. Maura et al. [J. Neurochem., 66 (1), pp. 203-209, 1996] установили, что введение агонистов, селективных в отношении рецепторов 5HT1A или в отношении рецепторов как 5-HT1A,так и 5-НТ 1D, может представлять собой значительное усовершенствование в лечении мозжечковых атаксий у человека, многогранного синдрома, для которого не создано доступной терапии. Сущность изобретения Настоящее изобретение относится к соединениям формулы I, изображенной ниже, гдеR1 представляет собой 2 диметиламиноэтоксигруппу или группу формулы G1, G2, G3, G4 или G5, где Е представляет собой кислород, серу, SO или SO2;R6 и R7 независимо выбраны из водорода,(С 1-С 6)алкила, [(С 2-С 4)алкил]арила, в котором арильная группировка представляет собой фенил или нафтил, и группы гетероарил-(СН 2)q, в которой гетероарильная группировка выбрана из пиридила, пиримидила, бензоксазолила, бензотиазолила, бензизоксазолила и бензизотиазолила, a q равно 0, 1, 2, 3 или 4, и где указанные арильная и гетероарильная группировки могут быть возможно замещенными одним или более чем одним заместителем, независимо выбранным из хлоро, фторо, бромо, иодо, (С 1-С 6) алкила, (С 1-С 6)алкокси, трифторметила, циано иSОg(С 1-С 6)алкила, где g равно 0, 1 или 2; или R6 и R7 вместе образуют цепь, содержащую от 2 до 4 атомов углерода; х равно числу от 0 до 8; каждый R13 независимо представляет собой (С 1-С 4)алкил или (С 1-С 4)метиленовый мостик от одного из кольцевых углеродов пиперазинового или пиперидинового кольца G1 или G2,соответственно, к тому же самому или другому кольцевому углероду, или к кольцевому азоту пиперазинового или пиперидинового кольца G1 или G2, соответственно, имеющему доступный 3 центр связывания, или к кольцевому углероду радикала R6, имеющему доступный центр связывания;R8 выбран из водорода и (С 1-С 3)алкила;R9 выбран из водорода и (С 1-С 6)алкила; или R6 и R9 вместе с атомом азота, к которому они присоединены, образуют кольцо,включающее в себя от 5 до 7 членов; и р равно 1, 2 или 3;R2 представляет собой водород, (С 1-С 4) алкил, фенил или нафтил, где указанный фенил или нафтил могут быть возможно замещены одним или более чем одним заместителем,предпочтительно заместителями числом от нуля до трех, независимо выбранными из хлоро, фторо, бромо, иодо, (С 1-С 6)алкила, (С 1-С 6)алкокси,трифторметила, циано и SОg(С 1-С 6)алкила, где g равно 0, 1 или 2;R3 представляет собой (СН 2)mВ, где m равно 0, 1, 2 или 3, а В представляет собой водород,фенил, нафтил или 5- либо 6-членную гетероарильную группу, содержащую от одного до четырех гетероатомов в кольце (например фурил,тиенил, пиридил, пиримидил, тиазолил, пиразолил, изотиазолил, оксазолил, изоксазолил, пирролил, триазолил, тетразолил, имидазолил и т.д.), и где каждая из вышеуказанных арильных и гетероарильных групп может быть возможно замещена одним или более чем одним заместителем, предпочтительно заместителями числом от нуля до трех, независимо выбранными из хлоро, фторо, бромо, иодо, (С 1-С 6)алкила, (С 1 С 6)алкокси, трифторметила, циано, гидрокси,СООН и SОg(С 1-С 6)алкила, где g равно 0, 1 или 2;Z представляет собой CR4R5, где R4 и R5 независимо выбраны из водорода, (С 1-С 6)алкила и трифторметила, или Z может быть одной из арильных или гетероарильных групп, указанных выше в определении В, и где два соседних члена кольца Z являются также членами кольца А;CONR11R12; каждый из R10, R11 и R12 независимо выбран из радикалов, указанных ранее в определении R2; или R11 и R12 вместе с азотом, к которому они присоединены, образуют кольцо, включающее в себя от 5 до 7 членов, которое может содержать от нуля до четырех гетероатомов,выбранных из азота, серы и кислорода, например, если NR11R12 представляет собой пирролидинил, пирролил, имидазолил, триазолил, тетразолил, пиперидил, пиперазинил, морфолинил,тиоморфолинил, гексаметилениминил, диазепинил, оксазепинил, тиазепинил, оксадиазепинил,тиадиазепинил или триазепинил;n равно 1, 2, 3 или 4, а прерывистая линия указывает на возможную двойную связь; 4 при условии, что n должно быть равно 1,когда Z представляет собой арильную или гетероарильную группу; и при условии, что когда R1 представляет собой 2-диметиламиноэтоксигруппу,R2 представляет собой водород, m равно 0,В представляет собой 3,4-дихлорфенильную группу, X представляет собой водород, каждый из R4 и R5 представляет собой водород, n равно 2, а прерывистая линия указывает на двойную связь; и их фармацевтически приемлемым солям. Более конкретными воплощениями групп Настоящее изобретение также относится к фармацевтически приемлемым солям присоединения кислоты соединений формулы I. Кислотами, которые используют для получения фармацевтически приемлемых солей присоединения кислоты вышеупомянутых основных соединений по данному изобретению, являются кислоты, которые образуют нетоксичные соли присоединения кислоты, то есть соли, содержащие фармацевтически приемлемые анионы, такие соли как гидрохлорид, гидробромид, гидроиодид, нитрат, сульфат, бисульфат, фосфат,кислый фосфат, ацетат, лактат, цитрат, кислый цитрат, тартрат, битартрат, сукцинат, малеат,фумарат, глюконат, сахарат, бензоат, метансульфонат, этансульфонат, бензолсульфонат, птолуолсульфонат и памоат [то есть 1,1'-метиленбис-(2-гидрокси-3-нафтоат)]. 5 Изобретение также относится к солям присоединения основания формулы I. Химические основания, которые можно применять в качестве реагентов для получения фармацевтически приемлемых солей присоединения основания соединений формулы I, которые являются кислыми по природе, являются основания, которые образуют нетоксичные основные соли с такими соединениями. Такие нетоксичные основные соли включают в себя, но не ограничиваются ими, соли, которые образованы фармацевтически приемлемыми катионами, такими как катионы щелочных металлов (например калия и натрия) и щелочно-земельных металлов (например кальция и магния), аммония, водорастворимые соли присоединения амина, такие какN-метилглюкамин-(меглюмин), и низшего алканоламмония, а также другие основные соли фармацевтически приемлемых органических аминов. Соединения по настоящему изобретению включают в себя все стереоизомеры и все оптические изомеры соединений формулы I (например, R и S энантиомеры), а также рацемические,диастереомерные и другие смеси таких изомеров. Если не указано иначе, алкильные и алкенильные группы, описанные здесь, а также алкильные группировки других групп, описанные здесь (например алкокси), могут быть нормальными или разветвленными, а также циклическими (например, циклопропил, циклобутил,циклопентил или циклогексил), либо они могут быть нормальными или разветвленными, но содержать циклические группировки. Если не указано иначе, галоген включает в себя фтор,хлор, бром и иод. Предпочтительные соединения формулы I включают в себя соединения, в которых R1 представляет собой пиперазинил. Предпочтительные соединения формулы I также включают в себя соединения, в которых Z представляет собой СН 2. Предпочтительные соединения формулы I также включают в себя соединения, в которых n равно 2 или 3. Предпочтительные соединения формулы I также включают в себя соединения, в которыхR3 представляет собой замещенный фенил. Примерами конкретных предпочтительных соединений формулы I являются следующие: 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1,3-дигидро-индол-2-он; 6-хлоро-3-[2-(4-метилпиперазин-1-ил)бензилиден]-1,3-дигидро-индол-2-он; 5-хлоро-3-[2-(4-метилпиперазин-1-ил)бензилиден]-1,3-дигидро-индол-2-он; 1-метил-3-[2-(4-метилпиперазин-1-ил)бензилидeн]-1,3-дигидро-индол-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-фенил-1,3-дигидро-индол-2-он; 6 1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(3,4-дихлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1,3-дигидро-индол-2 он; 1-(4-хлорбензил)-3-[2-(4-метилпиперазин 1-ил)-бензилиден]-пирролидин-2-он; 1-(4-хлорбензил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(3,4-дифторфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(2,4-дихлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(3,4-дихлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(4-хлорбензил)-3-[2-(4-метилпиперазин 1-ил)-бензилиден]-пиперидин-2-он; 1-(3,4-дихлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он; 1-(4-хлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он; 1-(3,4-дихлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-фенил-пирролидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-(4-трифторометилфенил)-пирролидин-2 он; 1-(3,4-дифторфенил)-3-[2-(4-метилпиперазин-1-ил)-бензил]-пирролидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 3-[5-фтор-2-(4-метилпиперазин-1-ил)бензилиден]-пирролидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он; 1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензил]-пиперидин-2-он; 1-(4-метоксифенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-3,4-дигидро-1 Нхинолин-2-он; 1-(3,4-дихлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензил]-пиперидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензил]-1 фенил-пирролидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-(п-толуил)-пирролидин-2-он; 3-[4-фтор-2-(4-метилпиперазин-1-ил)бензилиден]-1-фенил-пирролидин-2-он; 1-(3,4-дихлорфенил)-3-[2-фтор-6-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(3,4-дифторфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пиперин-2-он; 1-[2-(4-хлорфенил)этил]-3-[5-фтор-2-(4 метилпиперазин-1-ил)-бензилиден]-пиперидин 2-он; 1-(3,4-дихлорфенил)-3-[2-(2-диметиламиноэтокси)-бензилиден]-пирролидин-2-он; и 3-[2-(4-метилпиперазин-1-ил)-бензил]-1(4-трифторметилфенил)-пирролидин-2-он. Другие соединения формулы I включают в себя следующие: 7 1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-азетидин-2-он; 1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-азепин-2-он; 1-(3,4-дихлорфенил)-3-1-[2-(4-метилпиперазин-1-ил)фенил]этил-пирролидин-2-он; 1-(3,4-дихлорфенил)-3-1-[2-(4-метилпиперазин-1-ил)фенил]этил-пиперидин-2-он; 1-(3,4-дихлорфенил)-3-1-[2-(4-метилпиперазин-1-ил)фенил]этилиден-пирролидин-2-он; 1-(3,4-дихлорфенил)-3-1-[2-(4-метилпиперазин-1-ил)фенил]этилиден-пиперидин-2-он; 1-(3,4-дихлорфенил)-3-1-[2-(4-метилпиперазин-1-ил)фенил]-фенилметилен-пирролидин 2-он; 1-(3,4-дихлорфенил)-3-2-[(2-диметиламиноэтил)-метиламино]-бензилиден-пирролидин 2-он; 1-(3,4-дихлорфенил)-3-[2-(пирролидин-1 ил-этокси)-бензилиден]-пирролидин-2-он; 1-(3,4-дихлорфенил)-3-[2-(2-диметиламиноэтиламино)-бензилиден]-пирролидин-2-он; 2-(3,4-дихлорфенил)-3-[2-(2-диметиламиноэтиламино)-бензилиден]-пирролидин-2-он; 2-(3,4-дихлорфенил)-4-[2-(4-метилпиперазин-1-ил)-бензилиден]-октагидроизохинолин 3-один; 1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-октагидрохинолин-2 он; 1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-октагидроиндол-2-он; и 1-(3,4-дихлорфенил)-5,5-диметил-3-[2-(4 метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он. Настоящее изобретение также относится к фармацевтической композиции для лечения или предупреждения расстройства или состояния,выбранного из гипертензии, депрессии, общего состояния тревоги, фобий (например, агорафобии, социальной фобии и простых фобий), посттравматического стресс-синдрома, расстройства типа сенситивная личность, преждевременной эякуляции, расстройств аппетита (например, нервной анорексии и нервной булимии), ожирения, токсикомании (например, зависимости от алкоголя, кокаина, героина, фенобарбитала, никотина и бензодиазепинов), "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти (например деменции, амнестических расстройств и возрастного ухудшения памяти), болезней Паркинсона (например деменции при болезни Паркинсона, нейролептически индуцированного паркинсонизма и поздних дискинезий), эндокринных расстройств (например гиперпролактинемии), вазоспазма (в частности, сосудов мозга), церебеллярной атаксии, расстройств желудочно-кишечного тракта,в которые вовлечены изменения перистальтики 8 и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами у млекопитающего,преимущественно у человека, содержащей такое количество соединения формулы I или его фармацевтически приемлемой соли, которое эффективно при лечении или предупреждении такого расстройства или состояния, и фармацевтически приемлемый носитель. Настоящее изобретение относится также к фармацевтической композиции для лечения или предупреждения расстройства или состояния,которое можно лечить или предупреждать путем усиления серотонергической нейротрансмиссии у млекопитающего, преимущественно у человека, содержащей такое количество соединения формулы I или его фармацевтически приемлемой соли, которое эффективно при лечении или предупреждении такого расстройства или состояния, и фармацевтически приемлемый носитель. Примеры таких расстройств и состояний перечислены в предыдущем абзаце. Настоящее изобретение также относится к способу лечения или предупреждения расстройства или состояния, выбранного из гипертензии,депрессии, общего состояния тревоги, фобий(например, агорафобии, социальной фобии и простых фобий), посттравматического стресссиндрома, расстройства типа сенситивная личность, преждевременной эякуляции, расстройств аппетита (например, нервной анорексии и нервной булимии), ожирения, токсикомании (например, зависимости от алкоголя, кокаина, героина, фенобарбитала, никотина и бензодиазепинов), "гистаминовой" головной боли,мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти (например, деменции, амнестических расстройств и возрастного ухудшения памяти), болезней Паркинсона(например деменции при болезни Паркинсона,нейролептически индуцированного паркинсонизма и поздних дискинезий), эндокринных расстройств (например, гиперпролактинемии),вазоспазма (в частности, сосудов мозга), церебеллярной атаксии, расстройств желудочнокишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли,связанной с сосудистыми расстройствами, у млекопитающего, преимущественно у человека,включающему в себя введение млекопитающему, нуждающемуся в таком лечении или предупреждении, такого количества соединения формулы I или его фармацевтически приемлемой соли, которое эффективно при лечении или предупреждении такого расстройства или состояния. Настоящее изобретение также относится к фармацевтической композиции для лечения или предупреждения расстройства или состояния,выбранного из гипертензии, депрессии, общего 9 состояния тревоги, фобий (например, агорафобии, социальной фобии и простых фобий), посттравматического стресс-синдрома, расстройства типа сенситивная личность, преждевременной эякуляции, расстройств аппетита (например, нервной анорексии и нервной булимии), ожирения, токсикомании (например, зависимости от алкоголя, кокаина, героина, фенобарбитала, никотина и бензодиазепинов), "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера,обсессивнокомпульсивного расстройства, панического состояния, нарушений памяти (например, деменции, амнестических расстройств и возрастного ухудшения памяти), болезней Паркинсона (например, деменции при болезни Паркинсона,нейролептически индуцированного паркинсонизма и поздних дискинезий), эндокринных расстройств (например, гиперпролактинемии),вазоспазма (в частности, сосудов мозга), церебеллярной атаксии, расстройств желудочнокишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли,связанной с сосудистыми расстройствами, у млекопитающего, преимущественно у человека,содержащей эффективное антагонистическое или агонистическое по отношению к рецепторам серотонина количество соединения формулы I или его фармацевтически приемлемой соли, и фармацевтически приемлемый носитель. Настоящее изобретение также относится к фармацевтической композиции для лечения или предупреждения расстройства или состояния,которое можно лечить или предупреждать путем усиления серотонергической нейротрансмиссии у млекопитающих, преимущественно у человека, содержащей эффективное антагонистическое или агонистическое по отношению к рецепторам серотонина количество соединения формулы I или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель. Настоящее изобретение также относится к способу лечения или предупреждения расстройства или состояния, выбранного из гипертензии,депрессии, общего состояния тревоги, фобий(например, агорафобии, социальной фобии и простых фобий), посттравматического стресссиндрома, расстройства типа сенситивная личность, преждевременной эякуляции, расстройств аппетита (например, нервной анорексии и нервной булимии), ожирения, токсикомании (например, зависимости от алкоголя, кокаина, героина, фенобарбитала, никотина и бензодиазепинов), "гистаминовой" головной боли,мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти (например, деменции, амнестических расстройств и возрастного ухудшения памяти), болезней Паркинсона(например, деменции при болезни Паркинсона, 001485 10 нейролептически индуцированного паркинсонизма и поздних дискинезий), эндокринных расстройств (например, гиперпролактинемии),вазоспазма (в частности, сосудов мозга), церебеллярной атаксии, расстройств желудочнокишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли,связанной с сосудистыми расстройствами, у млекопитающего, преимущественно у человека,включающему в себя введение млекопитающему, которому требуется такое лечение или предупреждение, эффективного антагонистического или агонистического по отношению к рецепторам серотонина количества соединения формулы I или его фармацевтически приемлемой соли. Настоящее изобретение также относится к способу лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать путем усиления серотонергической нейротрансмиссии у млекопитающего,преимущественно у человека, включающему в себя введение млекопитающему, которому требуется такое лечение или предупреждение, эффективного антагонистического или агонистического по отношению к рецепторам серотонина количества соединения формулы I или его фармацевтически приемлемой соли. Настоящее изобретение также относится к фармацевтической композиции для лечения или предупреждения расстройства или состояния,которое можно лечить или предупреждать путем усиления серотонергической нейротрансмиссии у млекопитающего, преимущественно у человека, содержащей: а) фармацевтически приемлемый носитель; б) соединение формулы I или его фармацевтически приемлемую соль; и в) ингибитор обратного захвата 5-НТ,предпочтительно сертралин, или его фармацевтически приемлемую соль; где количества активных соединений (т.е. соединения формулы I и ингибитора обратного захвата 5-НТ) таковы, что их комбинация эффективна при лечении или предупреждении такого расстройства или состояния. Настоящее изобретение также относится к способу лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать путем усиления серотонергической нейротрансмиссии у млекопитающих, преимущественно у человека, включающему в себя введение млекопитающему, которому требуется такое лечение или предупреждение: а) соединения формулы I, которое определено выше, или его фармацевтически приемлемой соли; и б) ингибитора обратного захвата 5-НТ,предпочтительно сертралина, или его фармацевтически приемлемой соли; 11 где количества активных соединений (т.е. соединения формулы I и ингибитора обратного захвата 5-НТ) таковы, что их комбинация эффективна для лечения или предупреждения такого расстройства или состояния. Настоящее изобретение также относится к способу лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать путем усиления серотонергической нейротрансмиссии у млекопитающих, преимущественно у человека, включающему в себя введение указанному млекопитающему, которому требуется такое лечение или предупреждение: а) антагониста 5-HT1A или его фармацевтически приемлемой соли; и б) антагониста 5-НТ 1D или его фармацевтически приемлемой соли; где количества каждого из активных соединений (т. е. антагониста 5-HT1A и антагониста 5-НТ 1D) таковы, что их комбинация эффективна при лечении или предупреждении такого расстройства или состояния."Усиленная серотонергическая нейротрансмиссия" здесь относится к усилению или улучшению нейронного процесса, при котором серотонин высвобождается пресинаптической клеткой при возбуждении и пересекает синапс, чтобы стимулировать или ингибировать постсинаптическую клетку."Токсикомания" здесь означает аномальную потребность или страстное желание лекарства, либо зависимость от него. Такие лекарства обычно вводят возбужденному индивидууму любым из множества способов введения, включая пероральное, парентеральное, назальное,или путем ингаляции. Примерами токсикомании, подлежащей лечению способами по настоящему изобретению, являются зависимость от алкоголя, никотина, кокаина, героина, фенобарбитала и бензодиазепинов (например, Valium(товарный знак. "Лечение токсикомании" здесь означает снижение или облегчение такой зависимости. Сертралин, (1S-цис)-4-(3,4-дихлорфенил)1,2,3,4-тетрагидро-N-метил-1-нафталинамин,здесь имеет химическую формулу C17H17NCl2 и следующую структурную формулу: Его синтез описан в патенте США 4536518, принадлежащему Pfizer Inc.). Сертралина гидрохлорид является полезным антидепрессантом и аноректическим агентом, и также полезен при лечении депрессии, токсикомании,неврозов тревожных навязчивых состояний,фобий, панического состояния, невроза по 001485 12 сттравматического стресса и преждевременной эякуляции. Подробное описание изобретения Соединения формулы I можно получить согласно следующим реакционным схемам и комментариям к ним. Если не указано иначе, R1R12, G1-G5, X, А, В, Е, Z, n, m, р, q и g, и структурная формула I на реакционных схемах и в последующих комментариях является такой, как определено выше. Схема 1 Схема 1 иллюстрирует способ синтеза соединений формулы I, где прерывистая линия обозначает связь углерод-углерод, a R1 представляет собой группу формулы G1, G3, G4 илиG5. Согласно схеме 1, соединение формулы II, в которой Q представляет собой подходящую отщепляемую группу (например, хлоро, фторо,бромо, мезилат, тозилат и т.п.), подвергают 14 взаимодействию с соединением формулы R1H, в которой R1 представляет собой группу формулыG1, G3, G4 или G5, в присутствии основания, с образованием соответствующего соединения формулы III. Эту реакцию, как правило, проводят при температуре от примерно 0 С до примерно 140 С, предпочтительно при примерно температуре дефлегмации, в полярном растворителе, таком как диметилсульфоксид (ДМСО),N,N-диметилформамид (ДМФ), N,N-диметилацетамид (ДМА) или N-метил-2-пирролидон(NМП), предпочтительно в ДМФ. Подходящие основания включают в себя безводный карбонат натрия (Nа 2 СО 3), карбонат калия (К 2 СО 3), гидроксид натрия (NaOH) и гидроксид калия(КОН), а также третичные амины, такие как пирролидин, триэтиламин и пиридин. Безводный карбонат калия является предпочтительным. Соединения формулы III могут быть превращены в соединения формулы I, в которой R3 представляет собой радикал, иной чем водород(т.е. соединения формулы IB, как изображено на схеме 1), подвергая их альдольной конденсации или реакции Виттига. Например, в случае альдольной конденсации соединение формулы III может быть подвергнуто взаимодействию с соединением формулы в присутствии основания с образованием альдольного промежуточного соединения формулыV, которое может быть выделено или превращено непосредственно на этой же реакционной стадии в соединение формулы IВ посредством отщепления молекулы воды. Степень полноты конверсии соединений формулы III в альдольный продукт формулы IВ можно оценить, используя одну или более чем одну аналитическую методику, такую как тонкослойная хроматография (тcх) или масс-спектрометрия. В некоторых случаях может быть возможно или желательно выделить промежуточное соединение формулы V. В таком случае соединение формулы V может быть превращено в соединение формулы IВ удалением воды с использованием методик, которые известны специалистам, например, нагреванием до температуры дефлегмации раствора соединения формулы V в растворителе, таком как бензол, толуол или ксилол,в присутствии каталитического количества бензол- или п-толуол-сульфоновой кислоты, при условии удаления образующейся воды. Такие методики удаления воды могут включать в себя использование молекулярных сит или ловушки Дин-Старка для отделения воды, образующейся в виде азеотропа с растворителем. Альдольную реакцию обычно проводят в полярном растворителе, таком как ДМСО,ДМФ, тетрагидрофуран (ТГФ), метанол или этанол, при температуре от примерно -25 С до примерно 80 С. Предпочтительно эту реакцию проводят в ТГФ при 25 С. Подходящие основания для использования на стадии образования альдоля, включают в себя К 2 СО 3, Na2CO3, гидрид натрия (NaH), пирролидин и пиперидин. Предпочительным является гидрид натрия. Альдольные конденсации описаны в "ModernSynthetic Reactions", Herbert О. House, 2d. Edition, W.A. Benjamin, Menlo Park, California 1972,pp. 629-682. Соединения формулы I, где R3 представляет собой водород (соединения формулы IA, как изображено на схеме 1), могут быть получены путем альдольной конденсации аналогично описанному выше способу с образованием соединений формулы IВ, но при использовании в качестве исходного материала соединения формулы IV, где R3 представляет собой водород или -C(=O)R13, где R13 представляет собой (С 1 С 6) алкил или трифторометил. Соединения формулы IA можно превратить в соединения формулы IB, подвергая их взаимодействию с соединением формулы R3Y, где Y представляет собой отщепляемую группу и обозначен как Q,как определено выше. Эти взаимодействия можно проводить в растворителе, таком как ди(алкил)эфир, ТГФ, ДМФ, ДМА или ДМСО,предпочтительно в ДМФ, в присутствии основания, такого как карбонат калия, карбонат натрия, гидрид натрия, гидрид калия, гидроксид натрия или гидроксид калия. Реакционные температуры могут находиться в пределах от примерно 0 С до примерно 150 С, предпочтительно от примерно 25 С до примерно температуры дефлегмации растворителя. Альтернативно, соединение формулы IV может быть превращено в соединение формулы Так, соединение формулы IV может быть превращено в соответствующий бромид формулы XI в условиях стандартного броминирования с последующей обработкой трифенилфосфином в безводном ТГФ с образованием промежуточного соединения формулы XII. Соединение 16 формулы XII можно обработать сильным основанием (например, водным Na2CO3) с образованием соответствующего фосфониийилида, который можно подвергнуть взаимодействию с подходящим промежуточным соединением формулы III с получением соединений общей формулы I. Эта трансформация описана вMaercker, Organic Reactions, 1965, 14, 270. Соединения формулы I, где прерывистая линия изображает одинарную связь углеродуглерод, можно получить путем гидрогенирования соответствующих соединений, где прерывистая линия изображает двойную связь углерод-углерод, с использованием стандартных методик, хорошо известных специалистам. Например, восстановление двойной связи может быть осуществлено газообразным водородом с использованием катализаторов, таких как палладий-на-угле (Pd/C), палладий-на-сульфате бария (Pd/Ba2SO4), платина-на-угле (Pt/C) или трис(трифенилфосфин)родийхлорид (катализатор Уилкинсона), в подходящем растворителе,таком как метанол, этанол, ТГФ, диоксан или этилацетат, при давлении от примерно 1 до примерно 5 атмосфер и при температуре от примерно 10 С до примерно 60 С, как описано в Catalytic Hydrogenation in Organic Synthesis,Paul Rylander, Academic Press Inc., San Diego,1979, pp. 31-63. Предпочтительными являются следующие условия: Pd-на-угле, метанол, 25 С и давление газообразного водорода 350 кПа (50 фунт/кв.дюйм). Этот способ обеспечивает также введение изотопов водорода (т.е. дейтерия, трития) путем замещения 1 Н 2 на 2 Н 2 или 3 Н 2 в вышеописанной методике. Альтернативная методика с использованием таких реагентов, как формиат аммония иPd/C в метаноле при температуре дефлегмации в инертной атмосфере (например азота или аргона), также эффективна для восстановления двойной связи углерод-углерод соединений формулы I. Другой альтернативный способ включает в себя селективное восстановление двойной связи углерод-углерод с использованием самария и иода или иодида самария (Sml2) в метаноле или этаноле при примерно комнатной температуре, как описано в R. Yanada et al.,Synlett., 1995, pp. 443-4. Исходные материалы формул II и IV либо имеются в продаже, либо известны специалистам. Например, соединения формулы II, где R2 представляет собой водород, легко доступны из коммерческих источников, или их можно получить, используя методики, описанные в химической литературе. Их можно также получить из соответствующих карбоновых кислот или эфиров (т.е. формула II, в которой R2=ОН или О-алкил), которые имеются в продаже. Эти кислоты или эфиры можно восстановить до соответствующих спиртов формулы XIII, изображенной ниже, в которой Q определен так же, как и для 17 формулы II, с использованием одного или более чем одного из множества восстанавливающих агентов и условий в зависимости от природы заместителей Q и X. Такие восстанавливающие агенты включают в себя боргидрид натрия (NаВН 4), цианоборгидрид натрия (NaCNBH3), литийалюминийгидрид (LiAlH4) и боран в ТГФ (BH3THF) в растворителях, таких как метанол, этанол, ТГФ,диэтиловый эфир и диоксан. Окисление спирта формулы XIII в соответствующий альдегид формулы II может быть осуществлено с использованием селективного окислителя, такой как реагент Джонса (гидрохромат (Н 2 СrО 4, пиридиния хлорхромат (ПХХ) или диоксид марганца(МnО 2). Ссылки на такие превращения общедоступны (например, К.В. Wilberg, Oxidation inOrganic Chemistry, Part A, Academic Press Inc.,N.Y. 1965, pp. 69-72). Исходные материалы формулы IV могут быть получены несколькими способами, включая методики, описанные в литературе. Например, соединения формулы IV, где Z представляет собой ароматическое кольцо и n=1 (т.е. 1,3 дигидро-индол-2-он и его замещенные аналоги),имеются в продаже, либо их можно получить способами, описанными, например, в H.R. Howard and R. Sarges, патент США 4476307, 9 октября 1984. Один из способов получения исходных материалов формулы IV, где Z представляет собой CR4R5 и n равно числу один, два или три, включает в себя конденсацию циклического лактона формулы VIII с амином формулыH2NR3, которая показана ниже, в присутствии сильной минеральной кислоты, такой как соляная кислота (HCl). (См. M.J. Kornet, J. Pharm. Альтернативно, соединения формулы IV,где R3 представляет собой водород (соединения формулы IVA), можно алкилировать с образованием соответствующих соединений, где R3 представляет собой радикал, иной чем водород(соединения формулы IVB), используя стандартные методики, доступные специалистам,например, (а) продуцированием аниона желаемого соединения формулы IVA с использованием системы растворителей сильное основание/ полярный растворитель, такой как NaH/ТГФ,NaH/ДМФ или н-бутиллитий/ТГФ (n-buLi/THF),при температуре от примерно -30 С до пример 001485 18 но температуры дефлегмации растворителя, в течение от примерно 5 мин до примерно 24 ч, и(б) обработкой аниона алкилирующим агентом формулы R3Y, где Y представляет собой отщепляемую группу, такую как хлоро, бромо, иодо или мезилат. Этот процесс изображен ниже. Вышеописанного превращения соединений формулы IVA в соединения формулы IVB можно достичь также, используя условия катализа фазового переноса, как описано Takahata etal. в Heterocycles, 1979, 12(11), pp. 1449-1451. Соединения формулы R1H, используемые при получении промежуточных соединений формулы III, общедоступны, либо их можно получить, используя стандартные методики органического синтеза, известные специалистам и приспособленные из описанных в химической литературе. Например, соединения формулыR1H, где R1 представляет собой G1, можно получить, используя следующую последовательность реакций, которая начинается с имеющегося в продаже N-трет-бутоксикарбонилпиперазина (VI) Алкилирование соединений формулы VI соединением формулы R6Y, где Y такой, как определено выше, a R6 представляет собой (С 1 С 6)алкил, арил-(С 2-С 4)алкил, где арильная часть представляет собой фенил или нафтил, или гетероарил-(СН 2)q, где q равно числу ноль, один,два, три или четыре, а гетероарильная часть представляет собой пиридил, пиримидил, бензоксазолил, бензотиазолил, бензизоксазолил или бензизотиазолил, в присутствии нейтрализатора кислот (например бикарбоната натрия (NaHCO3), бикарбоната калия (КНСО 3), карбоната натрия (Na2CO3) или карбоната калия (К 2 СО 3 в полярном растворителе, таком как ацетон, при температуре от примерно 10 С до примерно температуры дефлегмации растворителя, даст промежуточное соединение формулы VII. Удаление трет-бутоксикарбонильной группы может быть осуществлено с использованием кислотных условий, например, НВr в уксусной кислоте или трифторуксусной кислотой, до тех пор, пока реакция не будет сочтена законченной. Соединения формулы III, где R1 представляет собой тетрагидропиридин или пиперидин,a R2 представляет собой водород, может быть получено из 2-бромбензальдегида, который имеется в продаже, как изображено на схеме 2. 19 Согласно схеме 2, соединение формулы II сначала превращают в защищенный альдегид или кетон формулы XIV, где Р представляет собой полностью защищенную альдегидную или кетонную группировку, используя методики, хорошо известные специалистам. Например, 1,3 диоксолановое производное альдегида или кетона можно получить методом, описанным J.E.Cole et al., в J. Chem. Soc., 1962, pp. 244, путем кипячения с обратным холодильником раствора альдегида формулы II и 1,3-пропандиола в безводном бензоле с каталитическим количеством п-толуолсульфоновой кислоты. Когда R2 в формуле II представляет собой радикал, иной чем водород, кетон может быть защищен с использованием подходящей защитной группы. Подходящие защитные группы могут быть выбраны из множества таких групп на основе наличия и природы заместителя X. Примеры подходящих защитных групп можно найти в T.W. Greene.WileySons, New York, 1981. Наиболее предпочтительными защитными группами являются группы, которые устойчивы к каталитическому гидрогенированию (например, 1,3-диоксолан) и которые будут, следовательно, давать возможность для последующего восстановления, если требуется, двойной связи углерод-углерод тетрагидропиридинов формулы XVI. Соединения формулы XIV могут быть затем обработаны винилстаннанами формулы XV,например,1-ВОС-4-триметилстаннил-1,2,5,6 тетрагидропиридином(ВОС=трет-бутилоксикарбонил), в присутствии катализатора с образованием соответствующего соединения формулы XVIA. Предпочтительным катализатором является палладий (например, (PH3P)4Pd или(Pd2(dba)3), где dba=дибензилиденацетон. Эта реакция может быть проведена как описано вYork, New York, 1982. Соединения формулы III, где R1 представляет собой пиперидин (G2), могут быть получены каталитическим гидрогенированием тетрагидропиридина формулы XIVA из предыдущего абзаца с использованием стандартных методик,известных специалистам, как правило с использованием палладия-на-угле в качестве катализатора, с образованием соответствующих соединений формулы XVIB. Реакцию обычно проводят в инертном растворителе, таком как этанол или этилацетат, либо без, либо с протонной кислотой, такой как уксусная кислота или HCl. Предпочтительной является уксусная кислота. Защитные группы на G2 (т.е. ВОС) могут быть удалены с использованием одной или более чем одной методики, описанной в Greene (см. выше), например, перемешиванием соединения формулы XVI в этилацетате и 3 М соляной кислоте при примерно комнатной температуре в 20 течение примерно 30 мин. Защитную группу для альдегида или кетона, Р, можно превратить в незащищенный кетон или альдегид формулы-C(=O)R2, используя одну или более чем одну методику, описанную в Greene, например, перемешивая раствор соединения формулы XVI в ТГФ и 5% соляной кислоте при комнатной температуре в течение 20 ч. Соединения формулы XIV из предыдущей реакционной схемы могут также быть обработаны алкиллитиевыми реагентами, например,бутиллитием, втор-бутиллитием или третбутиллитием, предпочтительно бутиллитием в инертном растворителе, как показано на схеме 3, с образованием промежуточного литиевого аниона формулы XVII. Подходящие растворители для этой реакции включают в себя, например, эфир или тетрагидрофуран, предпочтительно тетрагидрофуран. Реакционные температуры могут находиться в пределах от примерно-110 С до примерно 0 С. Промежуточные литиевые анионы формулы XVII можно затем подвергнуть дальнейшему взаимодействию с подходящим электрофилом, выбор которого зависит от наличия и природы заместителя. Подходящие электрофилы, используемые в получении соединений формулы III, где R1 представляет собой группу формулы G2, включают в себя, например, карбонильные производные или алкилирующие агенты (например, 1-ВОС-4 пиперидон). В случае, когда в качестве электрофила используют альдегид или кетон, гидрокси-группу можно удалить из промежуточного соединения формулы XVIII, как изображено ниже, с образованием соответствующего соединения формулы III. Эта стадия может быть осуществлена по одной из нескольких стандартных методик, известных специалистам. Например, производное тиокарбонила, такое как ксантат, может быть получено и удалено посредством свободнорадикальных процессов, которые оба известны специалистам. Альтернативно, гидроксильная группа может быть удалена восстановлением источником гидрида, таким как триэтилсилан, в кислотных условиях с использованием, например, трифтороуксусной кислоты или трифторида бора. Реакцию восстановления можно проводить в чистом виде или в растворителе, таком как метиленхлорид. Другой альтернативой может быть сначала превратить гидроксильную группу в подходящую отщепляемую группу, 21 такую как тозилат или хлорид, используя стандартные способы, известные специалистам, а затем удалить отщепляемую группу нуклеофильным гидридом, таким как например литийалюминийгидрид. Последнюю реакцию обычно проводят в инертном растворителе, таком как эфир или тетрагидрофуран. Можно также использовать восстановитель для восстановительного удаления бензильного заместителя. Подходящие восстановители включают в себя, например, никель Ренея в этаноле и натрий или литий в жидком аммиаке. Другой альтернативный способ удаления гидроксильной группы состоит в том, что сначала спирт формулы XVIII дегидратируют до олефина таким реагентом, как соль Бургесса (J. Org. Chem., 1973, 38, 26), а затем каталитически гидрогенируют двойную связь при стандартных условиях с использованием катализатора, такого как палладий на угле. Спирт можно также дегидратировать до олефина обработкой кислотой, такой как птолуолсульфокислота. Соединения формулы III, где R1 представляет собой G2, a R6 представляет собой водород,могут быть превращены в соответствующие соединения формулы III, где R1 представляет собой G2, a R6 представляет собой радикал, иной чем водород, подвергая их взаимодействию с соединением формулы R6Y, как описано выше для получения соединений формулы VII. Если не указано иначе, давление на каждой из вышеописанных реакций не является принципиальным. Обычно реакции следует проводить при давлении от примерно одной до примерно трех атмосфер, предпочтительно при давлении окружающей среды (около одной атмосферы). Соединения формулы I, которые имеют основную природу, способны к образованию широкого разнообразия различных солей с разнообразными неорганическими и органическими кислотами. Хотя такие соли должны быть фармацевтически приемлемыми для введения животным, на практике часто бывает желательно сначала выделить соединение формулы I из реакционной смеси в виде фармацевтически неприемлемой соли, а затем просто превратить последнюю обратно в свободное основное соединение обработкой щелочным реагентом, а затем превратить свободное основание в фармацевтически приемлемую соль присоединения кислоты. Соли присоединения кислоты основных соединений по данному изобретению легко получают обработкой основного соединения по существу эквивалентным количеством выбранной минеральной или органической кислоты в среде водного растворителя или в подходящем органическом растворителе, таком как метанол или этанол. При осторожном выпаривании растворителя получают желаемую твердую соль. Для получения фармацевтически приемлемых солей присоединения кислоты основных 22 соединений по данному изобретению используют такие кислоты, которые образуют нетоксичные соли присоединения кислоты, т.е. соли,содержащие фармацевтически приемлемые анионы, такие как гидрохлорид, гидробромид,гидроиодид, нитрат, сульфат или бисульфат,сукцинат, малеат, фумарат, глюконат, сахарат,бензоат, метансульфонат и памоат [т.е. 1,1'метилен-бис-(2-гидрокси-3-нафтоат)]. Те соединения формулы I, которые также кислотные по своей природе, например, когдаR3 включает в себя СООН или тетразольную группировку, способны к образованию основных солей с разнообразными фармацевтически приемлемыми катионами. Примеры таких солей включают в себя соли щелочных или щелочноземельных металлов, и в частности, соли натрия и калия. Все эти соли получают по стандартным методикам. В качестве реагентов для получения фармацевтически приемлемых основных солей по данному изобретению используют такие химические основания, которые образуют нетоксичные основные соли с описанными здесь кислотными соединениями формулы I. Эти нетоксичные основные соли включают в себя производные таких фармацевтически приемлемых катионов, как натрий, калий, кальций и магний и т.д. Эти соли можно легко получить обработкой соответствующих кислотных соединений водным раствором, содержащим желаемые фармацевтически приемлемые катионы, а затем выпариванием полученного раствора до сухости, предпочтительно при пониженном давлении. Их можно также получить альтернативным путем, смешивая растворы кислотных соединений в низших алканолах с алкоксидом желаемого щелочного металла, а затем выпаривая полученный раствор до сухости тем же путем. В любом случае, предпочтительно использовать стехиометрические количества реагентов, чтобы обеспечить завершенность реакции и максимальные выходы продукта. Соединения формулы I и их фармацевтически приемлемые соли (в дальнейшем называемые совокупно "активные соединения") полезны в качестве психотерапевтических средств и представляют собой сильнодействующие агонисты и/или антагонисты рецепторов серотонина 1 А (5-HT1A) и/или серотонина 1D (5-НТ 1D). Активные соединения полезны в лечении гипертензии, депрессии, общего состояния тревоги, фобий (например, агорафобии, социальной фобии и простых фобий), посттравматического стресс-синдрома, расстройства типа сенситивная личность, сексуальных расстройств (например, преждевременной эякуляции), расстройств аппетита (например, нервной анорексии и нервной булимии), ожирения, токсикомании (например, зависимости от алкоголя, кокаина, героина, фенобарбитала, никотина и бензодиазепинов), "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно 23 компульсивного расстройства, панического состояния, расстройств памяти (например, деменции, амнестических расстройств и возрастного ухудшения памяти), болезней Паркинсона (например, деменции при болезни Паркинсона,нейролептически индуцируемого паркинсонизма и поздних дискинезий), эндокринных расстройств (например, гиперпролактинемии), вазоспазма (в частности, сосудов головного мозга), церебеллярной атаксии, расстройств желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами. Эти соединения также полезны в качестве сосудорасширяющих средств. Сродство соединений по данному изобретению к различным рецепторам серотонина-1 можно определить с использованием стандартных анализов на связывание радиолигандов, как описано в литературе. Сродство по отношению к 5-НТ 1 А можно измерить с использованием методики, описанной Hoyer et al. (Brain Res.,1986, 376, 85). Сродство по отношению к 5-НТ 1D можно измерить с использованием методики,описанной Heuring и Peroutka (J. Neurosci, 1987,7, 894). Активность in vitro соединений по настоящему изобретению по сайту связывания 5-HT1D можно определить по следующей методике. Бычью хвостатую ткань гомогенизируют и суспендируют в 20 объемах буфера, содержащего 50 мМ ТRISгидрохлорида (трис[гидроксиметил]аминометана гидрохлорида) с рН 7,7. Затем гомогенат центрифугируют при 45000 G в течение 10 мин. Надосадочную жидкость удаляют, а полученный остаток заново суспендируют приблизительно в 20 объемах 50 мМ ТRISгидрохлоридного (HCl) буфера с рН 7,7. Эту суспензию затем пре-инкубируют в течение 15 мин при 37 С, после чего суспензию снова центрифугируют при 45000 G в течение 10 мин и надосадочную жидкость удаляют. Полученный остаток (приблизительно 1 г) заново суспендируют в 150 мл буфера 15 мМ ТRISгидрохлорида (HCl),содержащего 0,01 процент аскорбиновой кислоты, с конечным рН 7,7, и содержащего также 10 мкМ паргилина и 4 мМ хлорида кальция(СаСl2). Суспензию выдерживают на льду, по меньшей мере, в течение 30 мин до того, как использовать. Ингибитор, контроль или наполнитель затем инкубируют согласно следующей процедуре. К 50 мкл раствора 20 процентов диметилсульфоксида (ДМСО)/80 процентов дистиллированной воды добавляют 200 мкл меченого тритием 5-гидрокситриптамина (2 нМ) в буфере 50 мМ ТRISгидрохлорида, содержащего 0,01 процент аскорбиновой кислоты, с рН 7,7, и содержащего также 10 мкМ паргилина и 4 мкМ хлорида кальция, плюс 100 нМ 8-гидрокси 001485 24 ДПАТ (дипропиламинотетралина) и 100 нМ мезулергина. К этой смеси добавляют 750 мкл бычьей хвостатой ткани, и полученную суспензию гомогенизируют на вортексе (гомогенизатор Vortex) для гарантии гомогенного суспендирования. Суспензию затем инкубируют в качающейся водяной бане в течение 30 мин при 25 С. После завершения инкубации суспензию фильтруют с использованием фильтров из стекловолокна (например, Whatman GF/B-filters). Остаток промывают три раза 4 мл буфера 50 мМ ТRISгидрохлорида, рН 7,7. Затем остаток помещают в сцинтилляционный виал с 5 мл сцинтилляционной жидкости (aquasol 2) и дают возможность осесть в течение ночи. Процент ингибирования может быть вычислен для каждой дозы соединения. Величина IС 50 затем может быть вычислена из значений процента ингибирования. Активность соединений по настоящему изобретению в отношении сродства связывания 5-НТ 1 А можно определить по следующей методике. Ткань коры головного мозга крысы гомогенизируют и делят на образцы по 1 г и разводят в 10 объемах 0,32 М раствора сахарозы. Затем суспензию центрифугируют при 900 G в течение 10 мин, отделяют надосадочную жидкость и снова центрифугируют его при 70000 G в течение 15 мин. Надосадочную жидкость удаляют, а остаток заново суспендируют в 10 объемах 15 мМ ТRISгидрохлорида с рН 7,5. Суспензию инкубируют в течение 15 мин при 37 С. После завершения пре-инкубации суспензию центрифугируют при 70000 G в течение 15 мин и удаляют надосадочную жидкость. Полученный остаток ткани заново суспендируют в буфере 50 мМ ТRISгидрохлорида, рН 7,7, содержащем 4 мМ хлорида кальция и 0,01 процент аскорбиновой кислоты. Ткань хранят при -70 С до готовности для эксперимента. Затем ткань оттаивают непосредственно перед использованием, разводят в 10 мкМ паргилина и выдерживают на льду. Затем ткань инкубируют согласно следующей процедуре. Пятьдесят микролитров контроля, ингибитора или наполнителя (конечная концентрация ДМСО 1 процент) готовят в различных дозировках. К этому раствору добавляют 200 мкл меченого тритием ДПАТ при концентрации 1,5 нМ в буфере 50 мМ ТRISгидрохлорида, рН=7,7, содержащем 4 мМ хлорида кальция, 0,01 процент аскорбиновой кислоты и паргилин. К этому раствору затем добавляют 750 мкл ткани, и полученную суспензию гомогенизируют на вортексе для гарантии гомогенности. Затем суспензию инкубируют на качающейся водяной бане в течение 30 мин при 37 С. Затем раствор фильтруют, и осадок промывают дважды 4 мл 10 мМTRISгидрохлорида при рН 7,5, содержащего 154 мМ хлорида натрия. Процент ингибирова 25 ния вычисляют для каждой дозы соединения,контроля и наполнителя. Величины IC50 вычисляют из значений процента ингибирования. Соединения формулы I, описанные в следующих примерах настоящего изобретения,исследовали на сродство к 5-НТ 1 А и 5-НТ 1D с использованием вышеописанных методик. Все они соединения показали IC50 менее чем 0,60 мкМ относительно сродства к 5-НТ 1D и менее чем 1,0 мкМ относительно сродства к 5-НТ 1 А. Агонистическую и антагонистическую активность соединений по данному изобретению по 5-HT1A и 5-НТ 1D рецепторам можно определить, используя единственную концентрацию насыщения, по следующей методике. Самцов морских свинок линии Хартли обезглавливают,5-HT1A рецепторы вырезают из гиппокампа, a 5HT1D рецепторы получают нарезанием ткани на срезы 350 нм на микротоме Mcllwain и вырезанием черного вещества из соответствующих срезов. Индивидуальные ткани гомогенизируют в 5 мМ буфере HEPES (N-2-гидроксиэтилпиперазин-N-2-этансульфоновая кислота), содержащем 1 мМ EGTA (этиленгликольтетрауксусная кислота) (рН 7,5), с применением ручного стеклянного гомогенизатора Teflon и центрифугируют при 35 000 х g в течение 10 мин при 4 С. Остатки заново суспендируют в 100 мМ буфере HEPES, содержащем 1 мМ EGTA ( (рН 7,5), до конечной концентрации 20 мг (гиппокамп) или 5 мг (черное вещество) белка на пробирку. В реакционную смесь добавляют следующие реагенты так, чтобы каждая пробирка содержала 2,0 мМ MgCl2, 0,5 мМ АТР (аденозинтрифосфат, АТФ), 1,0 мМ сАМР (циклический аденозинмонофосфат, цАМФ), 0,5 мМ(30 Кюри/ммоль: NEG-003 - New England Nuclear). Инкубацию начинают добавлением ткани в силиконизированные микроцентрифужные пробирки (в трех экземплярах) при 30 С и проводят в течение 15 мин. Каждая пробирка получает 20 мкл ткани, 10 мкл лекарства или буфера(при 10-кратной конечной концентрации), 10 мкл 32 нМ агониста или буфера (при 10-кратной конечной концентрации), 20 мкл форсколина(конечная концентрация 3 мкМ) и 40 мкл ранее приготовленной реакционной смеси. Инкубацию останавливают добавлением 100 мкл раствора 2% SDS (додецилсульфат натрия), 1,3 мМ сАМР, 45 мМ АТР, содержащего 40000 расп./мин (число распадов в минуту) [3 Н]-сАМР(30 Кюри/ммоль: NET-275 - New England Nuclear), для регистрации выделения сАМР с колонок. Разделение [32 Р]-АТР и [32 Р]-сАМР осуществляют с использованием способа Salomonet al. (Analytical Biochemistry, 1974, 58, 541-548). Радиоактивность количественно определяют счетом жидкостной сцинтилляции. Максимальное ингибирование определяют по 10 мкМ (R) 001485 26 8-OH-ДПAT относительно рецепторов 5-HT1A и 320 нМ 5-НТ относительно рецепторов 5-НТ 1D. Процент ингибирования для тестируемых соединений вычисляют по отношению к ингибиторному эффекту 10 мкМ (R)-8-ОН-ДПАТ относительно рецепторов 5-НТ 1 А и 320 нМ 5-НТ относительно рецепторов 5-HT1D. Реверсирование индуцированного агонистом ингибирования стимулируемой форсколином активности аденилатциклазы вычисляют по отношению к эффекту 32 нМ агониста. Соединения по изобретению можно тестировать in vivo на активность в отношении антагонизма гипотермии, индуцируемой агинистом 5-HT1D у морских свинок согласно следующей методике. Объектами эксперимента служат самцы морских свинок линии Хартли из Charles River с массой тела 250-275 г при поступлении и 300600 г при тестировании. Морских свинок содержат в стандартных лабораторных условиях при световом режиме с 7 ч утра до 7 ч вечера,по меньшей мере, в течение 7 дней до эксперимента. Пища и вода доступны ad libitum до момента тестирования. Соединения по изобретению можно вводить в виде растворов в объеме 1 мл/кг. Используемый растворитель варьируют в зависимости от растворимости соединения. Тестируемые соединения обычно вводят либо за 60 мин перорально (p.o.), либо за 0 мин подкожно (s.c.) до 5HT1D агониста, который вводят в дозе 5,6 мг/кг,s.c. Перед первым измерением температуры каждую морскую свинку помещают в чистую пластмассовую обувную коробку, содержащую древесные стружки и пол из металлической сетки, и дают возможность акклиматизироваться к окружающей среде в течение 30 мин. Затем,после каждого измерения температуры, животных возвращают в ту же коробку. Перед каждым измерением температуры каждое животное крепко держат одной рукой в течение 30 секундного периода. Для измерений температуры применяют пальцевидный термометр с зондом для маленьких животных. Зонд выполнен из полугибкого нейлона с пластмассовым наконечником. Температурный зонд вставляют на 6 см в прямую кишку и держат в течение 30 с,пока не получат стабильный показатель. Затем температуры протоколируют. В экспериментах перорального скрининга базовую "предлекарственную" температуру замеряют в -90 мин, тестируемое вещество дают в-60 минут и дополнительно замеряют в -30 мин. 5-НТ 1D агонист затем вводят в 0 мин и замеряют температуру через 30, 60, 120 и 240 мин. В экспериментах подкожного скрининга базовую "предлекарственную" температуру замеряют в -30 мин. Тестируемое соединение и 5HT1D агонисты дают одновременно и замеряют температуру через 30, 60, 120 и 240 мин. 27 Данные оценивают двухфакторным анализом вариант с повторными измерениями в анализе по Newman-Keuls. Активные соединения по изобретению могут расцениваться как противомигреневые агенты тестированием степени, до которой они имитируют суматриптан в сокращении изолированной полоски подкожной вены собаки [Р. P.A.(1988)]. Этот эффект можно блокировать метиоцепином, известным антагонистом серотонина. Известно, что суматриптан полезен при лечении мигрени и дает избирательное повышение сосудистой резистентности сонной артерии у анестезированной собаки. Фармакологическая основа эффективности суматриптана обсуждалась в W.Fenwick et al., Br. J. Pharmacol., 96, 83 ,1989. Сродство к 5-НТ 1 рецептору серотонина можно определить in vitro анализами на связывание рецептора, как описано относительно 5HT1A рецептора, используя кору головного мозга крыс в качестве источника рецептора и [3 Н]8-ОН-ДПАТ в качестве радиолиганда [D. Hoyeret al. Eur. J. Pharm., 118, 13 (1985)] и используя ткань бычьего хвостатого ядра в качестве источника рецептора и [3 Н] серотонина в качестве радиолиганда, как описано относительно 5-HT1D рецептора [R.E. Heuring and S.J. Peroutka, J. Neuroscience, 7, 894 (1987)]. Из тестированных активных соединений все показали в любом из анализов IC50=1 мкМ или менее. Соединения формулы I можно выгодно применять в сочетании с одним или более чем одним терапевтическим агентом, например, с различными антидепрессантными агентами,такими как трициклические антидепрессанты(например, амитриптилин, дотиепин, доксепин,тримипрамин, бутрипилин, домипрамин, дезипрамин, имипрамин, иприндол, лофепрамин,нортриптилин или протриптилин), ингибиторы моноаминоксидазы (например, изокарбоксазид,фенелзин или транилциклопрамин) или ингибиторы обратного захвата 5-НТ (например, флувоксамин, сертралин, флуоксетин или пароксетин), и/или с антипаркинсонными агентами,такими как дофаминергические антипаркинсонные агенты (например, леводофа, предпочтительно в комбинации с периферическим ингибитором декарбоксилазы, например, бензеразидом или карбидофой, или с агонистом дофамина, например, бромкриптином, лизуридом или перголидом). Должно быть понятно, что настоящее изобретение охватывает применение соединения общей формулы (I) или его физиологически приемлемой соли или сольвата в сочетании с одним или более чем одним терапевтическим агентом. Соединения формулы I и их фармацевтически приемлемые соли в сочетании с ингибитором обратного захвата 5-НТ (например, флувоксамином, сертралином, флуоксетином или 28 пароксетином), предпочтительно сертралином,или его фармацевтически приемлемой солью или полиморфом (комбинация соединения формулы I с ингибитором обратного захвата 5-НТ названа здесь "активной комбинацией") полезны как психотерапевтические агенты и могут применяться для лечения или предупреждения таких расстройств, лечение или предупреждение которых обеспечивается повышенной серотонергической нейротрансмиссией (например,гипертензии, депрессии, общего состояния тревоги, фобий, посттравматического стресссиндрома, расстройства типа сенситивная личность, сексуальных расстройств, расстройств аппетита, ожирения, токсикомании, "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, расстройств памяти (например, деменции, амнестических расстройств и возрастного ухудшения памяти),болезней Паркинсона (например, деменции при болезни Паркинсона, нейролептически индуцированного Паркинсонизма и поздних дискинезий), эндокринных расстройств (например, гиперпролактинемии), вазоспазма (в частности,сосудов головного мозга), церебеллярной атаксии, расстройств желудочно-кишечного тракта,в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами. Ингибиторы обратного захвата серотонина(5-НТ), предпочтительно сертралин, оказывают положительное действие против депрессии, токсикомании, состояний тревоги, включая паническое состояние, общего состояния тревоги, агорафобии, простых фобий, социальной фобии,посттравматического стресса, обсессивно-компульсивного расстройства, расстройства типа сенситивная личность и преждевременной эякуляции у млекопитающих, включая людей, отчасти благодаря их способности блокировать синаптосомальный захват серотонина. В патенте США 4536518 описан синтез,фармацевтическая композиция и применение сертралина для лечения депрессии, и этот патент здесь полностью включен ссылкой. Активность активной комбинации в качестве антидепрессантов и родственные фармакологические свойства можно определить способами (1)-(4), упомянутыми ниже, которые описаны в Кое, В. et al., Journal of Pharmacology andExperimental Theurapeutics, 226 (3), 686-700,1983. Конкретно активность может быть определена путем исследования (1) их способности влиять на усилия мыши по спасению из плавательного резервуара (мышиный тест Порсолта на "поведение отчаяния"), (2) их способности усиливать 5-гидрокситриптофан-индуцированные поведенческие симптомы у мышей in vivo,(3) их способности в качестве антагонистов серотонин-истощающей активности п-хлороам 29 фетамина гидрохлорида в мозгу крысы in vivo и(4) их способности блокировать захват серотонина, норэпинефрина и дофамина синаптосомальными клетками мозга крыс in vitro. Способность активной комбинации противодействовать резерпиновой гипотермии у мышей invivo можно определить методами, описанными в патенте США 4029731. Композиции по настоящему изобретению могут быть приготовлены стандартным способом с использованием одного или более чем одного фармацевтически приемлемого носителя. Так, активные соединения по изобретению могут быть приготовлены для перорального,буккального, интраназального, парентерального(например, внутривенного, внутримышечного или подкожного) или ректального введения или приготовлены в форме, подходящей для введения путем ингаляции или инсуффляции. Для перорального введения фармацевтические композиции могут принимать форму, например, таблеток или капсул, которые готовят стандартными способами с использованием фармацевтически приемлемых эксципиентов,таких как связующие агенты (например, предварительно желатинизированный кукурузный крахмал, поливинилпирролидон или гидроксипропил-метилцеллюлоза); наполнители (например, лактоза, микрокристаллическая целлюлоза или фосфат кальция), смазки (например, стеарат магния, тальк или двуокись кремния); разрыхлители (например, картофельный крахмал или крахмальный гликолят натрия); или смачивающие агенты (например, лаурилсульфат натрия). Таблетки могут быть покрыты способами, хорошо известными специалистам. Жидкие препараты для перорального введения могут принимать форму например, растворов, сиропов или суспензий, либо они могут быть представлены в виде сухого продукта для разведения водой или другим подходящим растворителем перед употреблением. Такие жидкие препараты могут быть приготовлены стандартными способами с использованием фармацевтически приемлемых добавок, таких как суспендирующие агенты (например, сироп сорбита, метилцеллюлоза или гидрогенированные пищевые жиры); эмульгирующие агенты (например, лецитин или аравийская камедь), неводные растворители(например, миндальное масло, масляные эфиры или этиловый спирт); и консерванты (например,метил- или пропил-п-гидроксибензоаты или сорбиновая кислота). Для буккального введения композиция может принимать форму таблеток или облаток,приготовленных традиционным образом способом. Активные соединения по изобретению могут быть приготовлены в форме для парентерального введения путем инъекции, в том числе с использованием стандартных технических приемов катетеризации или инфузии. Препара 001485 30 ты для инъекции могут быть представлены в стандартной лекарственной форме, например в ампулах или в контейнерах для многократных доз с добавлением консерванта. Композиции могут принимать такие формы, как суспензии,растворы или эмульсии в масляных или водных растворителях, и могут содержать фармацевтические агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие. Альтернативно, активный ингредиент может находиться в форме порошка, предназначенного для разведения подходящим растворителем, например стерильной апирогенной водой, перед употреблением. Активные соединения по изобретению могут также быть приготовлены в виде ректальных композиций, таких как суппозитории или удерживающие клизмы, например содержащие традиционные основы для суппозиториев, такие как масло какао или другие глицериды. Для интраназального введения или введения путем ингаляции активные соединения обычно вводят в форме раствора или суспензии из контейнера для распыления накачкой, так чтобы пациент выдавливал или накачивал его,или в виде аэрозольного распылителя из контейнера под давлением, либо небулайзера с применением подходящего пропеллента, например дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, двуокиси углерода или другого подходящего газа. В случае аэрозоля под давлением единица дозирования может быть определена посредством снабжения клапаном, поставляющим отмеренное количество. Контейнер под давлением или небулайзер может содержать раствор или суспензию активного соединения. Капсулы и картриджи (изготовленные, например, из желатина) для использования в ингаляторе или инсуффляторе могут содержать порошковую смесь соединения по изобретению и подходящей порошковой основы, такой как лактоза или крахмал. Предлагаемая доза активных соединений по изобретению для перорального, парентерального или буккального введения среднему взрослому человеку для лечения состояний, указанных выше (например, мигрени), составляет от 0,1 до 200 мг активного ингредиента на стандартную дозу, которую можно вводить, например, от 1 до 4 раз в сутки. Аэрозольные препараты для лечения состояний, указанных выше (например, мигрени),у среднего взрослого человека предпочтительно сконструированы таким образом, что каждая отмеренная доза или прыск аэрозоля содержит от 20 мкг до 1000 мкг соединения по изобретению. Общая суточная доза аэрозоля должна быть в пределах от 100 мкг до 10 мг. Введение можно производить несколько раз в сутки,например, 2, 3, 4 или 8 раз, причем по 1, 2 или 3 дозы каждый раз. 31 В связи с применением активного соединения по данному изобретению с ингибитором обратного захвата 5-НТ, предпочтительно сертралином, для лечения лиц, обладающих любым из вышеуказанных состояний, следует отметить,что эти соединения можно вводить либо по отдельности, либо в комбинации с фармацевтически приемлемыми носителями любым ранее указанным способом, и что такое введение может быть проведено как в однократной дозировке, так и в многократных дозировках. Более конкретно, активную комбинацию можно вводить в широком ассортименте различных лекарственных форм, т.е. их можно комбинировать с разнообразными фармацевтически приемлемыми инертными носителями в форме таблеток,капсул, облаток, пастилок, твердых леденцов,порошков, аэрозолей, водной суспензии, растворов для инъекций, эликсиров, сиропов и тому подобного. Такие носители включают в себя твердые разбавители или наполнители, стерильную водную среду и различные нетоксичные органические растворители и т.п. Более того,такие пероральные фармацевтические препараты могут быть соответственно подслащены и/или корригированы посредством разнообразных агентов, традиционно используемых для таких целей. Как правило, соединения формулыI присутствуют в таких лекарственных формах в концентрации в пределах от примерно 0,5% до примерно 90% от общей массы композиции, то есть в количествах, достаточных для обеспечения желаемой стандартной дозировки, и ингибитор обратного захвата 5-НТ, предпочтительно сертралин, присутствует в таких лекарственных формах в концентрации в пределах от примерно 0,5% до примерно 90% от общей массы композиции, то есть в количествах, достаточных для обеспечения желаемой стандартной дозировки. Предлагаемая суточная доза активного соединения по данному изобретению в комбинированном препарате (препарате, содержащем активное соединение по данному изобретению и ингибитор обратного захвата 5-НТ) для перорального, парентерального, ректального или буккального введения среднему взрослому человеку для лечения состояний, указанных выше,составляет от примерно 0,1 мг до примерно 200 мг активного ингредиента формулы I на стандартную дозу, которую можно вводить, например, от 1 до 4 раз в день. Предлагаемая суточная доза ингибитора обратного захвата 5-НТ, предпочтительно сертралина, в комбинированном препарате для перорального, парентерального, ректального или буккального введения среднему взрослому человеку для лечения состояний, указанных выше,составляет от примерно 0,1 мг до примерно 2000 мг, предпочтительно от примерно 1 мг до примерно 200 мг ингибитора обратного захвата 5-НТ на стандартную дозу, которую можно вводить, например, от 1 до 4 раз в сутки. 32 Предпочтительное соотношение доз сертралина и активного соединения по данному изобретению в комбинированном препарате для перорального, парентерального или буккального введения среднему взрослому человеку для лечения состояний, указанных выше, составляет от примерно 0,00005 до примерно 20000, предпочтительно от примерно 0,25 до примерно 2000. Аэрозольные комбинированные препараты для лечения состояний, указанных выше, у среднего взрослого человека, предпочтительно сконструированы таким образом, что каждая отмеренная доза или "прыск" аэрозоля содержит от примерно 0,01 мкг до примерно 1000 мкг активного соединения по данному изобретению,предпочтительно от примерно 1 мкг до примерно 10 мкг такого соединения. Вводить можно несколько раз в сутки, например 2, 3, 4 или 8 раз по например 1, 2 или 3 дозы каждый раз. Аэрозольные препараты для лечения состояний, указанных выше, у среднего взрослого человека, предпочтительно сконструированы таким образом, что каждая отмеренная доза или"прыск" аэрозоля содержит от примерно 0,01 мкг до примерно 2000 мкг ингибитора обратного захвата 5-НТ, предпочтительно сертралина,предпочтительно от примерно 1 мкг до примерно 200 мкг сертралина. Вводить можно несколько раз в сутки, например, 2, 3, 4 или 8 раз по, например, 1, 2 или 3 дозы каждый раз. Как указано ранее, ингибитор обратного захвата 5-НТ, предпочтительно сертралин, в комбинации с соединениями формулы I, хорошо адаптирован к терапевтическому применению в качестве антидепрессантного агента. Как правило, эти антидепрессантные композиции, содержащие ингибитор обратного захвата 5-НТ,предпочтительно сертралин, и соединение формулы I, обычно вводят при дозировках в пределах от примерно 0,01 мг до примерно 100 мг на кг массы тела в день ингибитора обратного захвата 5-НТ, предпочтительно сертралина, предпочтительно от примерно 0,1 мг до примерно 10 мг на кг массы тела в день сертралина; и от примерно 0,0001 мг до примерно 100 мг на кг массы тела в день соединения формулы I, предпочтительно от примерно 0,01 мг до примерно 100 мг на кг массы тела в день соединения формулы I, хотя вариации неизбежно встречаются в зависимости от состояний пациента и конкретного выбранного способа введения. Следующие примеры иллюстрируют получение соединений по настоящему изобретению. Точки плавления не скорректированы. Данные ЯМР приведены в частях на миллиони отнесены к сигналу дейтериевого пучка от растворителя-стандарта (дейтериохлороформа, если не указано иначе). Удельные вращения измеряли при комнатной температуре с использованием натриевой D линии (589 нм). Коммерческие реагенты использовали без дальнейшей очистки. 33 ки. ТГФ означает тетрагидрофуран. ДМФ означает N,N-диметилформамид. Хроматография означает колоночную хроматографию, осуществляемую с использованием силикагеля 32-63 мкм и выполняемую под давлением азота(флэш-хроматография). Комнатная температура,или температура окружающей среды, означает 20-25 С. Все неводные реакции проводили в атмосфере азота для удобства и получения максимальных выходов. Концентрирование при пониженном давлении означает, что использовали роторный испаритель. Пример 1. 3-[2-(4-Метилпиперазин-1-ил)бензилиден]-1,3-дигидроиндол-2-он. В атмосфере азота в сухую круглодонную колбу, снабженную конденсатором и магнитной мешалкой, помещали 2-(4-метил-1-пиперазинил)-бензальдегид (0,152 г, 0,75 г, 0,75 ммоль),оксиндол (0,104 г, 0,78 ммоль) пирролидин (62 мкл) и этанол (7,0 мл). Смесь нагревали до дефлегмации в течение 16 ч, охлаждали и выпаривали при пониженном давлении. Остаток парционировали между этилацетатом и водой, и органический слой промывали насыщенным водным хлоридом натрия (NaCl), сушили над сульфатом магния (MgSO4), фильтровали и адсорбировали на 437 мг силикагеля. Элюацией этилацетатом (ЕtOАс) (125 мл), 1% метанолом(100 мл) и 4% СН 3 ОН + 1% триэтиламина (EtN3) в ЕtOАс (50 мл) получили 280 мг желтого твердого вещества. Перекристаллизацией из горячего СН 3 ОН получили указанный в заголовке продукт, Tпл=226-228 С. 1 Н ЯМР (CDCl3, 250 МГц)7,93 (1 Н, s) 7,84 (1 Н, br s), 7,79 (1 Н, dd), 7,66 (1 Н, d, J=7,94 Гц), 7,42 (1 Н, dt), 7,12-7,03 (2 Н, m), 3,06 (4 Н, t),2,66-2,53 (4 Н, m), 2,35 (3 Н, s). Элементный анализ: Вычислено для C20H21N3O0,5 Н 2 О: С 73,15,Н 6,75, N 12,79. Найдено: С 73,00, Н 6,51, N 13,01. Таким же образом получали следующие аналоги примеров 2-6. Пример 2. 6-Хлор-3-[2-(4-метилпиперазин 1-ил)-бензилиден]-1,3-дигидроиндол-2-он гидрохлорид дигидрат. Тпл=265-267 С.(60% масляная дисперсия) и 2165 мл безводного ТГФ. После охлаждения до 0 С добавляли раствор 48,8 г (0,212 моль) 1-(3,4-дихлорфенил)пирролидин-2-она и 42,7 г (0,209 моль) 2-(4 метил-1-пиперазинил)-бензальдегида в 1300 мл ТГФ с охлаждением на ледяной бане. После добавления смесь нагревали с обратным холодильником в течение 7 ч, затем концентрировали в вакууме до темно-коричневого остатка,который растирали с горячими смесями 10% ЕtOА:гексан. Оставшийся остаток фильтровали и сушили на воздухе с получением 95,6 г рыжевато-коричневого твердого вещества, которое перекристаллизовывали из 16 л МеОН с получением 24,2 г не совсем белого твердого вещества. Дополнительной перекристаллизацей из смеси СНСl3:МеОН получали продукт, указанный в заголовке, в виде не совсем белого твердого вещества, 14,4 г, Tпл= 224-225 С. 35 Найдено: С 62,06, Н 5,39, N 9,69. Дополнительные количества продукта,указанного в заголовке, были также выделены из маточных жидкостей, оставшихся после перекристаллизации. Свободное основание превращали в гидрохлоридную соль растворением основания в метаноле и добавлением 1 н. HCl в Et2O для осаждения соли, которую перекристаллизовывали из смеси метанол:Et2O с получением белого кристаллического твердого вещества,Тпл=177-179 С. Элементный анализ: Вычислено для С 22 Н 23N3 ОС 12 НCl1,5 Н 2 О: С 55,07, Н 5,67, N 8,76. Найдено: С 55,22, Н 5,61, N 8,73. По такой же методике получали также следующие соединения примеров 8-28. Пример 8. 1-(2,4-Дихлорфенил)-3-[2-(4 метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он. Тпл=228-229 С.(40 мг) в 30 мл безводного метанола кипятили с обратным холодильником в атмосфере азота в течение 18 ч. После охлаждения катализатор удаляли в вакууме, и остаток обрабатывали насыщенным водным бикарбонатом натрия и метиленхлоридом. Органический слой удаляли,объединяли с вторичным экстрактом из водного слоя дополнительным метиленхлоридом, промывали насыщенным водным хлористым натрием (NaCl) и высушивали. Растворитель снова удаляли в вакууме с получением неочищенного продукта в виде белого твердого вещества (111 мг). Это твердое вещество растворяли в горячем этилацетате и кристаллизовали путем добавления нескольких капель гексанов. Продукт, указанный в заголовке, 29 мг, имеет Тпл 130-131 С. Из фильтрата получали также дополнительный(1 Н, m). Элементный анализ: Вычислено для С 22 Н 25F2N3 О: С 68,55, Н 6,54, N 10,90. Найдено: С 68,55, Н 6,53, N 10,90. Пример 30. 3-[2-(4-Метилпиперазин-1-ил)бензил]-1-фенил-пирролидин-2-он. По методике, аналогичной методике из примера 29,3-[2-(4-метилпиперазин-1-ил)бензилиден]-1-фенил-пирролидин-2-он превращали в 3-[2-(4-метилпиперазин-1-ил)-бензил]-1 фенил-пирролидин-2-он. Тпл 104-105,5 С. Масс-спектр: 350 (М+1). 1 Н ЯМР (CDCl3, 250 МГц)7,68 (2 Н, dd,J=8,7, 1,1 Гц), 7,39 (2 Н, t), 7,26-7,03 (5 Н, m),3,76-3,69 (2 Н, m), 3,40 (1 Н, dd, J=13,5, 3,9 Гц),3,06 (1 Н, m), 2,96 (4 Н, dd, J=5,2, 3,5 Гц), 2,81(2 Н, t, J=6,7 Гц), 3,50-3,33 (2 Н, m), 3,22-2,94 (8 Н,m), 2,78 (3 Н, s), 2,70 (1 Н, dd, J=13,7, 10,2 Гц),2,03 (1 Н, m), 1,74 (1H, m). Элементный анализ: Вычислено для С 23 Н 26N3 ОF3 НСl1/2 Н 2 О: С 59,67, Н 6,10, N 9,08. Найдено: С 59,84, Н 6,06, N 8,96. Пример 32. 1-(3,4-Дихлорфенил)-3-[2-(4 метилпиперазин-1-ил)-бензил]-пиперидин-2-он гидрохлорид. Раствор 1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидина-2 она (260 мг, 0,60 ммоль) в 20 мл метанола соединяли со 100 мг 10% палладия-на-углероде и гидрогенировали на аппарате Parr Shaker при 345 кПа (50 фунт/кв.дюйм) в течение суммарно 4 ч. Затем катализатор удаляли фильтрацией через диатомитовую землю, и растворитель удаляли в вакууме с получением желтого смолистого остатка. Хроматографией (силикагель) 39 с элюцией смесью 5% метанол(СН 3 ОН)/95% метиленхлорид (СН 2 Сl) получали чистый продукт, 70 мг, в виде чистой смолы, которую растворяли в сухом этиловом эфире (Еt2 О) и обрабатывали этиловым эфиром, насыщенным HCl,с получением гидрохлоридной соли, 61 мг, Тпл 106-108 С. Масс-спектр: 432 (М+1), 434. Пример 33. 1-(3,4-Дихлорфенил)-3-[5 фтор-2-(4-метилпиперазин-1-ил)-бензил]пиперидин-2-он гидрохлорид. Используя методику, аналогичную методике примера 32, 1-(3,4-дихлорфенил)-3-[5 фтор-2-(4-метилпиперазин-1-ил)-бензилиден]пиперидин-2-он (270 мг, 0,6 ммоль) восстанавливали в течение 18 ч с получением, после превращения в гидрохлоридную соль, 1-(3,4 дихлорфенил)-3-[5-фтор-2-(4-метилпиперазин 1-ил)-бензил]-пиперидин-2-он гидрохлорида. Тпл 83-85 С, белого твердого вещества. Масс-спектр: 450 (М+1), 452. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы I, изображенной ниже, где R1 представляет собой 2-диметиламиноэтоксигруппу или группу формулы G1, G2, G3,G4 или G5, которые изображены ниже, где Е представляет собой кислород, серу, SO или SO2;R6 и R7 независимо выбраны из водорода,(С 1-С 6)алкила, [(С 2-С 4)алкил]арила, где арильная группировка представляет собой фенил или нафтил, и гетероарила-(СН 2)q, где гетероарильная группировка выбрана из пиридила, пиримидила, бензоксазолила, бензотиазолила, бензизоксазолила и бензизотиазолила, a q равно 0, 1,2, 3 или 4, и где указанные арильная и гетероарильная группировки могут быть возможно замещены одним или более чем одним заместителем, независимо выбранным из хлоро, фторо,бромо, иодо, (С 1-С 6)алкила, (С 1-С 6)алкокси, 001485x равно числу от 0 до 8; каждый R13 независимо представляет собой (С 1-С 4)алкил или (C1-С 4)метиленовый мостик от одного из кольцевых углеродов пиперазинового или пиперидинового кольца G1 или G2,соответственно, к тому же самому или другому кольцевому углероду или к кольцевому азоту пиперазинового или пиперидинового кольца G1 или G2, соответственно, имеющему доступный центр связывания, или к кольцевому углероду радикала R6, имеющему доступный центр связывания;R8 выбран из водорода и (С 1-С 3)алкила;R9 выбран из водорода и (С 1-С 6)алкила; или R6 и R9 вместе с атомом азота, к которому они присоединены, образуют кольцо, содержащее от 5 до 7 членов; и р равно 1, 2 или 3;R2 представляет собой водород, (С 1 С 4)алкил, фенил или нафтил, где названные фенил или нафтил могут быть возможно замещены одним или более чем одним заместителем,предпочтительно заместителями числом от нуля до трех, независимо выбранными из хлоро, фторо, бромо, иодо, (С 1-С 6)алкила, (С 1-С 6)алкокси,трифторметила, циано и SОg(С 1-С 6)алкила, где g равно 0, 1 или 2;R3 представляет собой (CH2)mВ, где m равно 0, 1, 2 или 3, а В представляет собой водород,фенил, нафтил или 5- или 6-членную гетероарильную группу, содержащую от одного до четырех гетероатомов в кольце (например фурил,тиенил, пиридил, пиримидил, тиазолил, пиразолил, изотиазолил, оксазолил, изоксазолил, пирролил, триазолил, тетразолил, имидазолил и т.п.), и где каждая из вышеуказанных арильных и гетероарильных групп может быть возможно замещена одним или более чем одним заместителем, предпочтительно заместителями числом от нуля до трех, независимо выбранными из хлоро, фторо, бромо, иодо, (С 1-С 6)алкила, (С 1 С 6)алкокси, трифторметила, циано, гидрокси,СООН и SОg(С 1-С 6)алкила, где g равно 0, 1 или 2;Z представляет собой CR4R5, где R4 и R5 независимо выбраны из водорода, (C1-С 6)алкила и трифторметила, или Z может быть одной из арильных или гетероарильных групп, указанных выше в определении В, и где два соседних члена кольца Z являются также членами кольца А;CONR11R12; каждый из R10, R11 и R12 независимо выбран из радикалов, указанных ранее в определении R2; или R11 и R12 вместе с азотом, к которо 41 му они присоединены, образуют кольцо, содержащее от 5 до 7 членов, которое может содержать от нуля до четырех гетероатомов, выбранных из азота, серы и кислорода;n равно 1, 2, 3 или 4, а прерывистая линия указывает на возможную двойную связь; при условии, что n должно быть равно 1,когда Z представляет собой гетероарильную группу; и при условии, что когда R1 представляет собой 2-диметиламиноэтоксигруппу, R2 представляет собой водород, m равно 0, В представляет собой 3,4-дихлорфенильную группу, X представляет собой водород, каждый из R4 и R5 представляет собой водород, n равно 2, а прерывистая линия указывает на двойную связь; или его фармацевтически приемлемая соль. 2. Соединение по п.1, где R1 представляет собой пиперазинил. 3. Соединение по п.1, где Z представляет собой СН 2. 4. Соединение по п.1, где n равно 2 или 3. 5. Соединение по п.1, где R3 представляет собой замещенный фенил. 6. Соединение по п.2, где Z представляет собой СН 2. 7. Соединение по п.6, где R3 представляет собой замещенный фенил. 8. Соединение по п.7, где n равно числу два или три. 9. Соединение по п.1, где указанное соединение выбрано из 3-[2-(4-метилпиперазин-1-ил)бензилиден]-1,3-дигидро-индол-2-он; 6-хлор-3-[2-(4-метилпиперазин-1-ил)бензилиден]-1,3-дигидро-индол-2-он; 5-хлор-3-[2-(4-метилпиперазин-1-ил)бензилиден]-1,3-дигидро-индол-2-он; 1-метил-3-[2-(4-метилпиперазин-1-ил)бензилиден]-1,3-дигидро-индол-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-фенил-1,3-дигидроиндол-2-он; 1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(3,4-дихлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1,3-дигидроиндол-2-он; 1-(4-хлорбензил)-3-[2-(4-метилпиперазин 1-ил)-бензилиден]-пирролидин-2-он; 1-(4-хлорбензил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(3,4-дифторфенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(2,4-дихлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(3,4-дихлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 1-(4-хлорбензил)-3-[2-(4-метилпиперазин 1-ил)-бензилиден]-пиперидин-2-он; 1-(3,4-дихлорбензил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он; 42 1-(4-хлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он; 1-(3,4-дихлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-фенил-пирролидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-(4-трифторметилфенил)-пирролидин-2 он; 1-(3,4-дифторфенил)-3-[2-(4 метилпиперазин-1-ил)-бензил]-пирролидин-2 он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пирролидин-2-он; 3-[5-фтор-2-(4-метилпиперазин-1-ил)бензилиден]-пирролидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-пиперидин-2-он; 1-(3,4-дихлорфенил)-3-[2-(4-метилпиперазин-1-ил)-бензил]-пиперидин-2-он; 1-(4-метоксифенил)-3-[2-(4-метилпиперазин-1-ил)-бензилиден]-3,4-дигидро-1 Нхинолин-2-он; 1-(3,4-дихлорфенил)-3-[5-фтор-2-(4-метилпиперазин-1-ил)-бензил]-пиперидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензил]-1 фенил-пирролидин-2-он; 3-[2-(4-метилпиперазин-1-ил)-бензилиден]-1-(п-толил)-пирролидин-2-он; 3-[4-фтор-2-(4-метилпиперазин-1-ил)бензилиден]-1-фенил-пирролидин-2-он; 1-(3,4-дихлорфенил)-3-[2-фтор-6-(4 метилпиперазин-1-ил)-бензилиден]пирролидин-2-он; 1-(3,4-дифторфенил)-3-[5-фтор-2-(4 метилпиперазин-1-ил)-бензилиден]-пиперин-2 он; 1-[2-(4-хлорфенил)этил]-3-[5-фтор-2-(4 метилпиперазин-1-ил)-бензилиден]-пиперидин 2-он; 1-(3,4-дихлорфенил)-3-[2-(2-диметиламиноэтокси)-бензилиден]-пирролидин-2-он; и 3-[2-(4-метилпиперазин-1-ил)-бензил]-1(4-трифторметилфенил)-пирролидин-2-он; и фармацевтически приемлемые соли таких соединений. 10. Фармацевтическая композиция для лечения или предупреждения расстройства или состояния, выбранного из гипертензии, депрессии, общего состояния тревоги, фобий, посттравматического стресс-синдрома, расстройства сенситивная личность, преждевременной эякуляции, расстройств аппетита, ожирения,токсикомании, "гистаминовой" головной боли,мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти, болезней Паркинсона, эндокринных расстройств, вазоспазма,церебеллярной атаксии, расстройств желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной 43 боли, связанной с сосудистыми расстройствами,у млекопитающего, содержащая такое количество соединения по п.1, которое является эффективным при лечении или предупреждении такого расстройства или состояния, и фармацевтически приемлемый носитель. 11. Фармацевтическая композиция для лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего,содержащая такое количество соединения по п.1, которое является эффективным при лечении или предупреждении такого расстройства или состояния, ифармацевтически приемлемый носитель. 12. Способ лечения или предупреждения расстройства или состояния, выбранного из гипертензии, депрессии, общего состояния тревоги,фобий,посттравматического стресссиндрома, расстройства сенситивная личность,преждевременной эякуляции, расстройств аппетита, ожирения, токсикомании, "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти, болезней Паркинсона, эндокринных расстройств, вазоспазма, церебеллярной атаксии,расстройств желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами, у млекопитающего, при котором млекопитающему, нуждающемуся в таком лечении или предупреждении, вводят такое количество соединения по п.1, которое является эффективным при лечении или предупреждении такого расстройства или состояния. 13. Способ лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего, при котором млекопитающему, нуждающемуся в таком лечении или предупреждении, вводят такое количество соединения по п.1, которое является эффективным при лечении или предупреждении такого расстройства или состояния. 14. Фармацевтическая композиция для лечения или предупреждения расстройства или состояния, выбранного из гипертензии, депрессии, общего состояния тревоги, фобий, посттравматического стресс-синдрома, расстройства сенситивная личность, преждевременной эякуляции, расстройств аппетита, ожирения,токсикомании, "гистаминовой" головной боли,мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти, болезней Паркинсона, эндокринных расстройств, вазоспазма,церебеллярной атаксии, расстройств желудочно-кишечного тракта, в которые вовлечены из 001485 44 менения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами,у млекопитающего, содержащая эффективное антагонистирующее или агонистирующее рецепторы серотонина количество соединения по п.1 и фармацевтически приемлемый носитель. 15. Фармацевтическая композиция для лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего,содержащая эффективное антагонистирующее или агонистирующее рецепторы серотонина количество соединения по п.1 и фармацевтически приемлемый носитель. 16. Способ лечения или предупреждения расстройства или состояния, выбранного из гипертензии, депрессии, общего состояния тревоги,фобий,посттравматического стресссиндрома, расстройства сенситивная личность,преждевременной эякуляции, расстройств аппетита, ожирения, токсикомании, "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти, болезней Паркинсона, эндокринных расстройств, вазоспазма, церебеллярной атаксии,расстройств желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами, у млекопитающего, при котором млекопитающему, которому требуется такое лечение или предупреждение, вводят эффективное антагонистирующее или агонистирующее рецепторы серотонина количество соединения по п.1. 17. Способ лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего, при котором млекопитающему, которому требуется такое лечение или предупреждение, вводят эффективное антагонистирующее или агонистирующее рецепторы серотонина количество соединения по п.1. 18. Фармацевтическая композиция для лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего,содержащая а) фармацевтически приемлемый носитель; б) соединение по п.1; и в) ингибитор обратного захвата 5-НТ или его фармацевтически приемлемую соль; где количество активных соединений таково, что данная комбинация эффективна при лечении или предупреждении такого расстройства или состояния. 19. Способ лечения или предупреждения расстройства или состояния, которое можно лечить или предупреждать посредством усиления серотонергической нейротрансмиссии, у млекопитающего, при котором млекопитающему, которому требуется такое лечение или предупреждение, вводят а) соединение по п.1; б) ингибитор обратного захвата 5-НТ или его фармацевтически приемлемую соль; где количества активных соединений таковы, что данная комбинация эффективна при лечении или предупреждении такого расстройства или состояния. 20. Фармацевтическая композиция по п.18,где ингибитор обратного захвата 5-НТ представляет собой сертралин или его фармацевтически приемлемую соль. 21. Способ по п.19, при котором ингибитор обратного захвата 5-НТ представляет собой сертралин или его фармацевтически приемлемую соль. 22. Способ лечения или предупреждения расстройства или состояния, выбранного из ги 46 пертензии, депрессии, общего состояния тревоги,фобий,посттравматического стресссиндрома, расстройства сенситивная личность,преждевременной эякуляции, расстройств аппетита, ожирения, токсикомании, "гистаминовой" головной боли, мигрени, боли, болезни Альцгеймера, обсессивно-компульсивного расстройства, панического состояния, нарушений памяти, болезней Паркинсона, эндокринных расстройств, вазоспазма, церебеллярной атаксии,расстройств желудочно-кишечного тракта, в которые вовлечены изменения перистальтики и секреции, и хронической пароксизмальной гемикрании и головной боли, связанной с сосудистыми расстройствами, у млекопитающего, при котором млекопитающему, которому требуется такое лечение или предупреждение, вводят а) соединение по п.1; и б) ингибитор обратного захвата 5-НТ или его фармацевтически приемлемую соль; где количества активных соединений таковы, что данная комбинация эффективна при лечении или предупреждении такого расстройства или состояния.
МПК / Метки
МПК: A61P 25/00, C07D 209/34, A61K 31/395
Метки: селективных, бензил, производные, 5-нт1а, антагонистов, рецепторов, 5-нт1d, применение, получение, иден)-лактамов, качестве
Код ссылки
<a href="https://eas.patents.su/25-1485-proizvodnye-benzil-iden-laktamov-ih-poluchenie-i-primenenie-v-kachestve-selektivnyh-antagonistov-receptorov-5-nt1a-i-ili-5-nt1d.html" rel="bookmark" title="База патентов Евразийского Союза">Производные бензил (иден)-лактамов, их получение и применение в качестве селективных (ант)агонистов рецепторов 5-нт1а и/или 5-нт1d</a>
Предыдущий патент: Композиции, содержащие ингибитор вич протеазы, а именно as vx 478, и водорастворимое соединение витамина e, а именно витамин e-tpgs.
Следующий патент: Бензоксазиноновые антагонисты рецептора допамина d4.
Случайный патент: Надцентровое запирающее устройство












