Новые иммуномодуляторные и противовоспалительные соединения
Номер патента: 24702
Опубликовано: 31.10.2016
Авторы: Висванадха Срикант, Ваккаланка Сваруп Кумар В.С., Бхавар Прашнант Кашинат, Мерикапуди Гаятри Сваруп, Мутуппаланиаппан Мейяппан
Формула / Реферат
1. Соединение формулы (I)
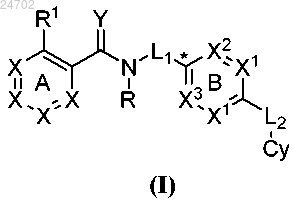
или его таутомер, стереоизомер или фармацевтически приемлемая соль,
где кольцо A независимо выбрано из моноциклического арила, содержащего 6 атомов углерода, и моноциклического 6-членного гетероарила, содержащего один или более атомов N, при этом X в каждом случае независимо представляет собой CR4 или N;
кольцо B независимо выбрано из моноциклического арила, содержащего 6 атомов углерода, и моноциклического 6-членного гетероарила, содержащего один или два гетероатома, представляющих собой N;
при этом X1 представляет собой CH или N;
X2 представляет собой CR2, где R2 выбран из водорода и галогена; и
X3 представляет собой CR3, где R3 представляет собой галоген;
R представляет собой водород;
R1 выбран из -COOH, -CRaRbOH и -SO3Ra;
L1 и L2 отсутствуют;
Cy выбран из замещенной или незамещенной 3-15-членной гетероциклической группы, содержащей один или более гетероатомов, выбранных из N, O и S; замещенного арила, содержащего 6 атомов углерода; и замещенного или незамещенного 5-14-членного гетероарила, содержащего один или более гетероатомов, выбранных из N, O и S;
R4 независимо выбран из водорода, (C1-C8)алкила и галогена;
Ra и Rb в каждом случае представляют собой водород;
Y в каждом случае представляет собой O;
при этом термин "замещенный" относится к замещению любым одним или любой комбинацией следующих заместителей, которые могут быть одинаковыми или разными и выбраны из гидрокси, галогена, незамещенного (C1-C8)алкила, незамещенного (C1-C8)алкокси, галоген(C1-C8)алкокси, (C3-C8)циклоалкилокси, (C1-C8)алкилтио, -S(O)(C1-C8)алкила и -O(C1-C8)алкилфенила.
2. Соединение по п.1, отличающееся тем, что кольцо A выбрано из
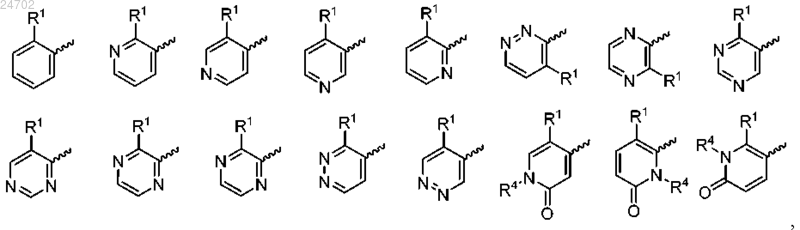
необязательно замещенных одним или более R4.
3. Соединение по п.1 или 2, отличающееся тем, что
R1 представляет собой -COOH;
X в каждом случае представляет собой CH, C-Cl, C-F или N;
X1 в каждом случае представляет собой CH;
X2 представляет собой C-Cl или C-F;
X3 представляет собой C-Cl или C-F.
4. Соединение по любому из пп.1-3, отличающееся тем, что кольцо B выбрано из
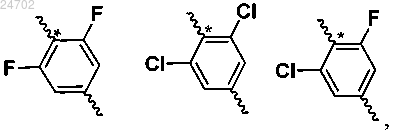
необязательно замещенных одним или более R4.
5. Соединение формулы (IA)
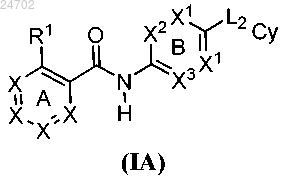
или его таутомер, стереоизомер или фармацевтически приемлемая соль,
где кольцо A, включающее X, выбрано из
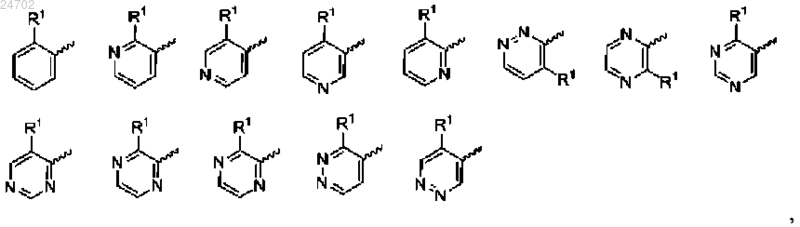
необязательно замещенных одним или более R4;
R1 представляет собой -COOH;
кольцо B выбрано из
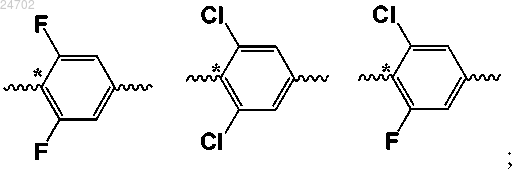
L2 отсутствует;
Cy выбран из замещенной или незамещенной 3-15-членной гетероциклической группы, содержащей один или более гетероатомов, выбранных из N, O и S; замещенного арила, содержащего 6 атомов углерода; и замещенного или незамещенного 5-14-членного гетероарила, содержащего один или более гетероатомов, выбранных из N, O и S;
R4 представляет собой галоген;
Y представляет собой O.
6. Соединение формулы (IA)
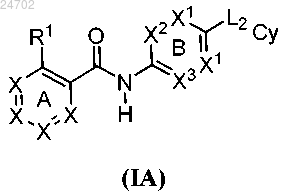
или его таутомер, стереоизомер или фармацевтически приемлемая соль,
где кольцо A, включающее R1, выбрано из
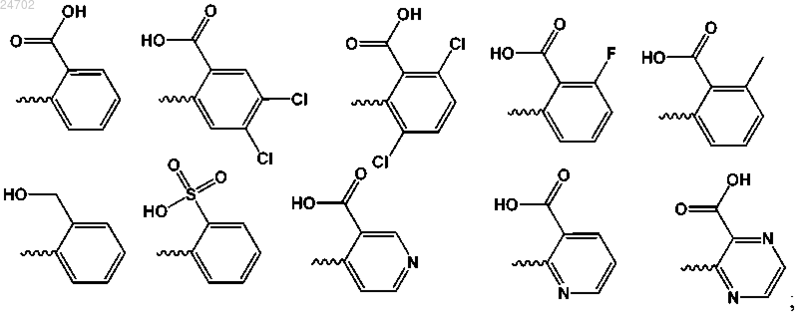
кольцо B выбрано из
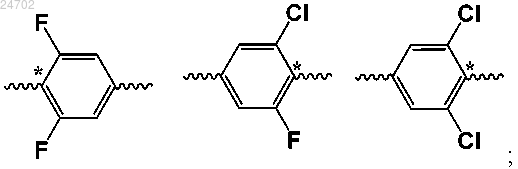
L2 отсутствует;
Cy представляет собой замещенный или незамещенный фенил, индол или индазол, при этом термин "замещенный" относится к замещению любым одним или любой комбинацией следующих заместителей, которые могут быть одинаковыми или разными и выбраны из гидрокси, галогена, незамещенного (C1-C8)алкила, незамещенного (C1-C8)алкокси, галоген(C1-C8)алкокси, (C3-C8)циклоалкилокси, (C1-C8)алкилтио, -S(O)(C1-С8)алкила и -О(C1-C8)алкилфенила.
7. Соединение по любому из пп.1-6, отличающееся тем, что Cy представляет собой
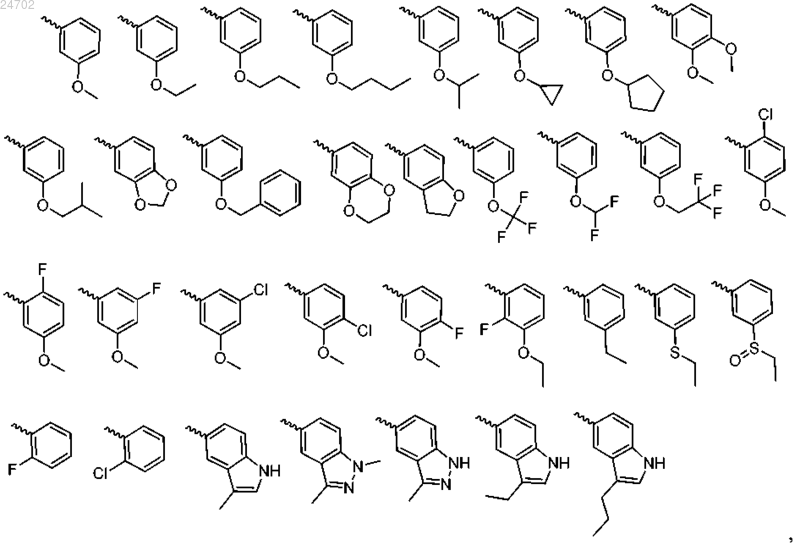
необязательно замещенный одним или более атомами галогена.
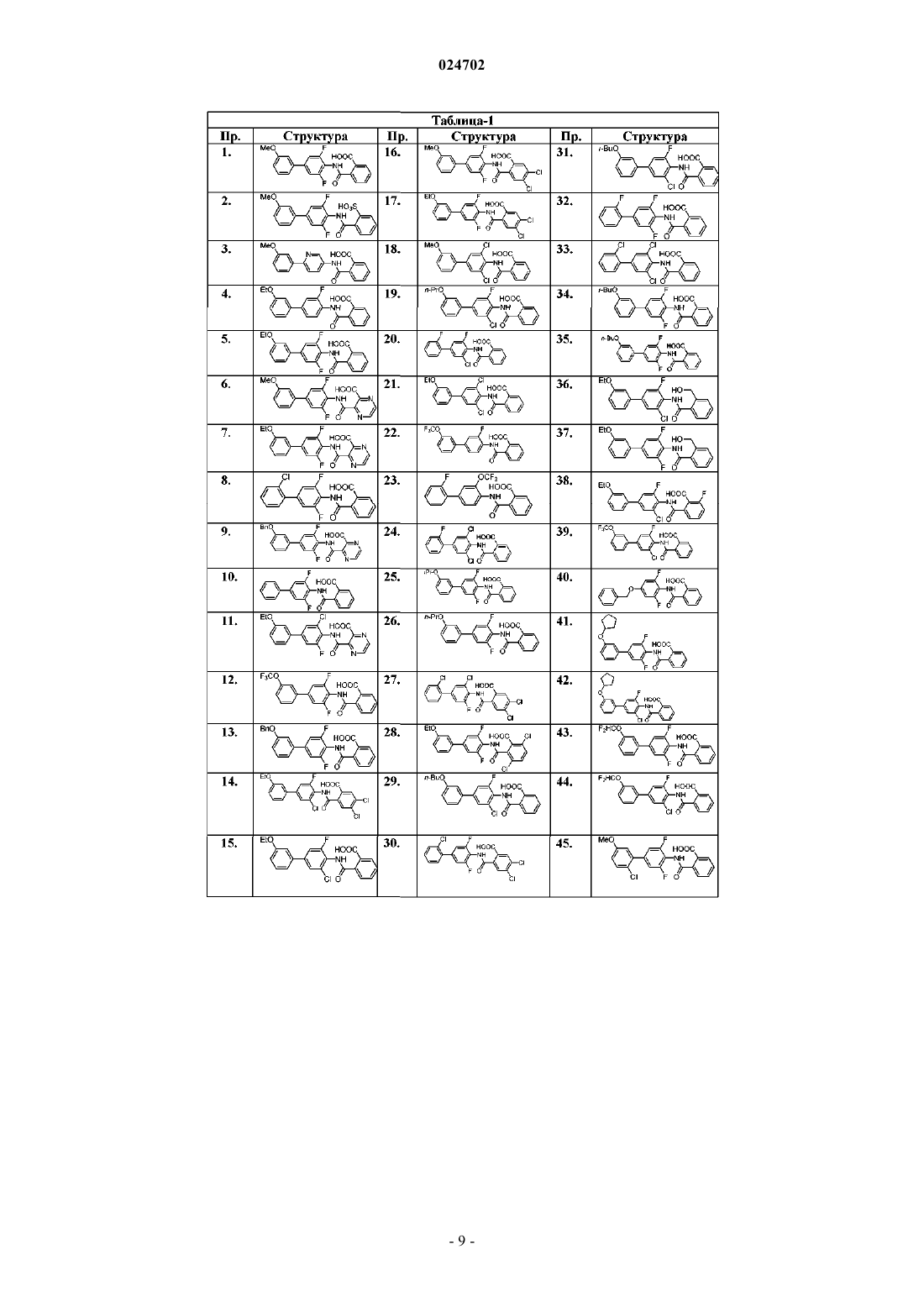
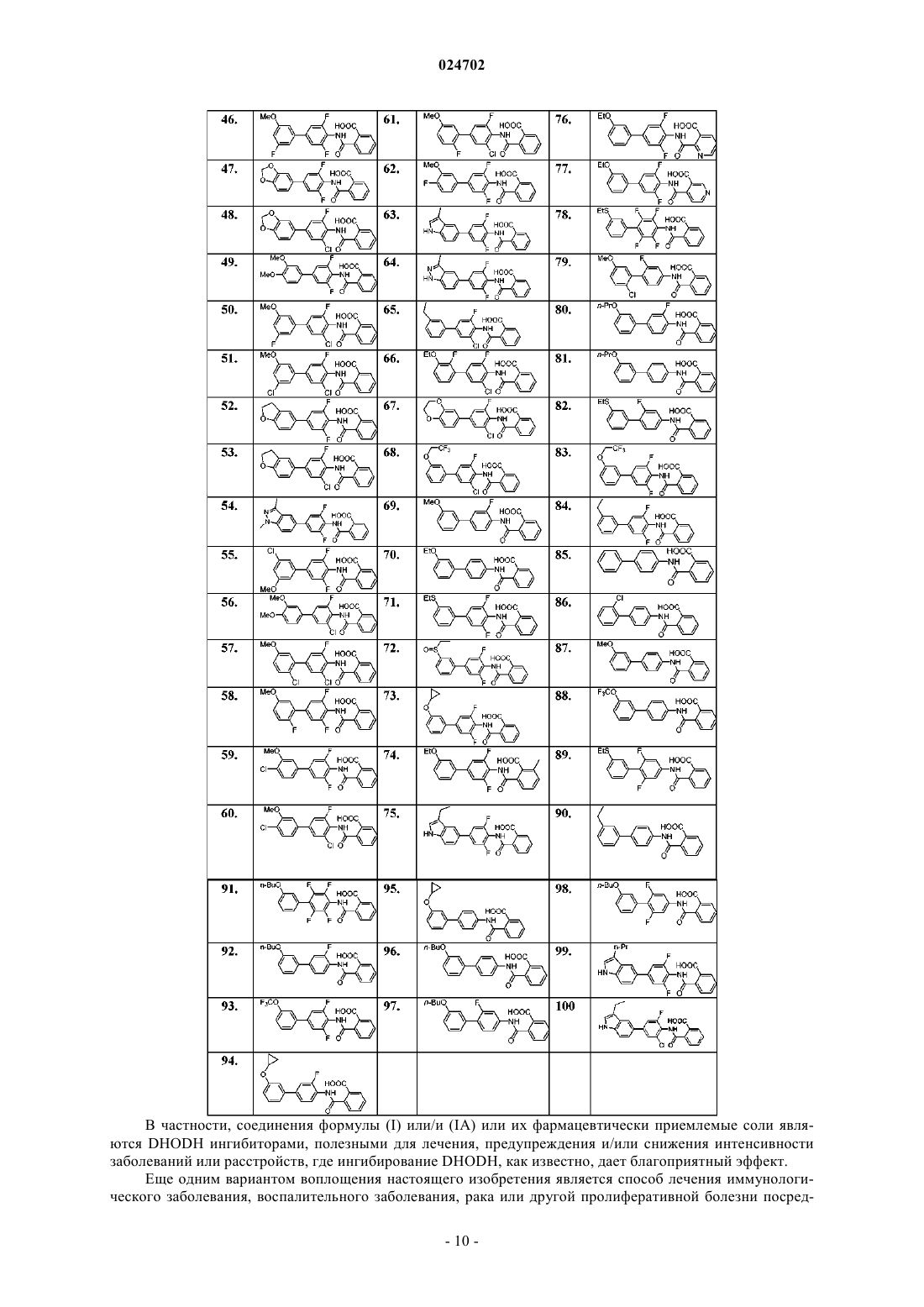
8. Соединение, выбранное из
2-(3,5-дифтор-3'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(3,5-дифтор-3'-метоксибифенил-4-илкарбамоил)бензолсульфоновой кислоты;
2-(6-(3-метоксифенил)пиридин-3-илкарбамоил)бензойной кислоты;
2-(3'-этокси-3-фторбифенил-4-илкарбамоил)бензойной кислоты;
2-(3'-этокси-3,5-дифторбифенил-4-илкарбамоил)бензойной кислоты;
2-(2'-хлор-3,5-дифторбифенил-4-илкарбамоил)бензойной кислоты;
2-[3,5-дифтор-3'-(трифторметокси)бифенил-4-илкарбамоил]бензойной кислоты;
2-[3'-(бензилокси)-3,5-дифторбифенил-4-илкарбамоил]бензойной кислоты;
4,5-дихлор-2-(3-хлор-3'-этокси-5-фторбифенил-4-илкарбамоил)бензойной кислоты;
2-(3-хлор-3'-этокси-5-фторбифенил-4-илкарбамоил)бензойной кислоты;
4,5-дихлор-2-(3,5-дифтор-3'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
4,5-дихлор-2-(3'-этокси-3,5-дифторбифенил-4-илкарбамоил)бензойной кислоты;
2-(3,5-дихлор-3'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(3-хлор-5-фтор-3'-пропоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(3-хлор-2',5-дифторбифенил-4-илкарбамоил)бензойной кислоты;
2-(3,5-дихлор-3'-этоксибифенил-4-илкарбамоил)бензойной кислоты;
2-[3-фтор-3'-(трифторметокси)бифенил-4-илкарбамоил]бензойной кислоты;
2-(3,5-дихлор-2'-фторбифенил-4-илкарбамоил)бензойной кислоты;
2-(3,5-дифтор-3'-изопропоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(3,5-дифтор-3'-пропоксибифенил-4-илкарбамоил)бензойной кислоты;
4,5-дихлор-2-(2',3-дихлор-5-фторбифенил-4-илкарбамоил)бензойной кислоты;
3,6-дихлор-2-(3'-этокси-3,5-дифторбифенил-4-илкарбамоил)бензойной кислоты;
N-(3'-бутокси-3-хлор-(5-фторбифенил-4-ил))фталаминовой кислоты;
2-(3-хлор-5-фтор-3'-изобутоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(2',3,5-трифторбифенил-4-илкарбамоил)бензойной кислоты;
2-(2',3,5-трихлорбифенил-4-илкарбамоил)бензойной кислоты;
2-(3,5-дифтор-3'-изобутоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(3'-бутокси-3,5-дифторбифенил-4-илкарбамоил)бензойной кислоты;
2-(3-хлор-3'-этокси-5-фторбифенил-4-илкарбамоил)-6-фторбензойной кислоты;
2-[3-хлор-5-фтор-3'-(трифторметокси)бифенил-4-илкарбамоил]бензойной кислоты;
2-[3'-(циклопентилокси)-3,5-дифторбифенил-4-илкарбамоил]бензойной кислоты;
2-(3-хлор-3'-(циклопентилокси)-5-фторбифенил-4-илкарбамоил)бензойной кислоты;
2-[3'-(дифторметокси)-3,5-дифторбифенил-4-илкарбамоил]бензойной кислоты;
2-[3-хлор-3'-(дифторметокси)-5-фторбифенил-4-илкарбамоил]бензойной кислоты;
2-(2'-хлор-3,5-дифтор-5'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(3,3',5-трифтор-5'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-[4-(бензо[d][1,3]диоксол-5-ил)-2,6-дифторфенилкарбамоил]бензойной кислоты;
2-[4-(бензо[d][1,3]диоксол-5-ил)-2-хлор-6-фторфенилкарбамоил]бензойной кислоты;
2-(3,5-дифтор-3',4'-диметоксибифенил-4-илкарбамоил)бензойной кислоты;
2-((3-хлор-3',5-дифтор-5'-метокси-[1,1'-бифенил]-4-ил)карбамоил)бензойной кислоты;
2-(3,3'-дихлор-5-фтор-5'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-[4-(2,3-дигидробензофуран-5-ил)-2,6-дифторфенилкарбамоил]бензойной кислоты;
2-[2-хлор-4-(2,3-дигидробензофуран-5-ил)-6-фторфенилкарбамоил]бензойной кислоты;
2-[4-(1,3-диметил-1H-индазол-5-ил)-2,6-дифторфенилкарбамоил]бензойной кислоты;
2-(3'-хлор-3,5-дифтор-5'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(3-хлор-5-фтор-3',4'-диметоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(2',3-дихлор-5-фтор-5'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(2',3,5-трифтор-5'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(4'-хлор-3,5-дифтор-3'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(3,4'-дихлор-5-фтор-3'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(3-хлор-2',5-дифтор-5'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-(3,4',5-трифтор-3'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-[2,6-дифтор-4-(3-метил-1H-индол-5-ил)фенилкарбамоил]бензойной кислоты;
2-[2,6-дифтор-4-(3-метил-1H-индазол-5-ил)фенилкарбамоил]бензойной кислоты;
2-(3-хлор-3'-этил-5-фторбифенил-4-илкарбамоил)бензойной кислоты;
2-(3-хлор-3'-этокси-2',5-дифторбифенил-4-илкарбамоил)бензойной кислоты;
2-[2-хлор-4-(2,3-дигидробензо[b][1,4]диоксин-6-ил)-6-фторфенилкарбамоил]бензойной кислоты;
2-[3-хлор-5-фтор-3'-(2,2,2-трифторэтокси)бифенил-4-илкарбамоил]бензойной кислоты;
2-(3-фтор-3'-метоксибифенил-4-илкарбамоил)бензойной кислоты;
2-[3'-(этилтио)-3,5-дифторбифенил-4-илкарбамоил]бензойной кислоты;
2-[3'-(этилсульфинил)-3,5-дифторбифенил-4-илкарбамоил]бензойной кислоты;
2-(3'-циклопропокси-3,5-дифторбифенил-4-илкарбамоил)бензойной кислоты;
2-[4-(3-этил-1H-индол-5-ил)-2,6-дифторфенилкарбамоил]бензойной кислоты;
2-(3-фтор-3'-пропоксибифенил-4-илкарбамоил)бензойной кислоты;
2-[3,5-дифтор-3'-(2,2,2-трифторэтокси)бифенил-4-илкарбамоил]бензойной кислоты;
2-(3'-этил-3,5-дифторбифенил-4-илкарбамоил)бензойной кислоты;
2-(3'-бутокси-3-фторбифенил-4-илкарбамоил)бензойной кислоты;
2-[3,5-дифтор-3'-(трифторметокси)бифенил-4-илкарбамоил]бензойной кислоты;
2-(3'-циклопропокси-3-фторбифенил-4-илкарбамоил)бензойной кислоты;
2-[2,6-дифтор-4-(3-пропил-1H-индол-5-ил)фенилкарбамоил]бензойной кислоты;
2-[2-хлор-4-(3-этил-1H-индол-5-ил)-6-фторфенилкарбамоил]бензойной кислоты;
4,5-дихлор-2-(2'-хлор-3,5-дифторбифенил-4-илкарбамоил)бензойной кислоты;
2-(3'-этокси-3,5-дифторбифенил-4-илкарбамоил)-6(5)-метилбензойной кислоты.
9. Соединение, выбранное из
3-(3,5-дифтор-3'-метоксибифенил-4-илкарбамоил)пиразин-2-карбоновой кислоты;
3-(3,5-дифтор-3'-этоксибифенил-4-илкарбамоил)пиразин-2-карбоновой кислоты;
3-[3'-(бензилокси)-3,5-дифторбифенил-4-илкарбамоил]пиразин-2-карбоновой кислоты;
3-(3-хлор-3'-этокси-5-фторбифенил-4-илкарбамоил)пиразин-2-карбоновой кислоты;
N-(3-хлор-3'-этокси-5-фторбифенил-4-ил)-2-(гидроксиметил)бензамида;
N-(3'-этокси-3,5-дифторбифенил-4-ил)-2-(гидроксиметил)бензамида;
2-(3'-этокси-3,5-дифторбифенил-4-илкарбамоил)никотиновой кислоты;
4-(3'-этокси-3,5-дифторбифенил-4-илкарбамоил)никотиновой кислоты.
10. Фармацевтическая композиция для лечения заболевания, нарушения или состояния, на которое оказывает положительное воздействие ингибирование любого или обоих из дигидрооротатдегидрогеназы (DHODH) и цитокина IL 17, содержащая соединение по любому из пп.1-9 и фармацевтически приемлемый носитель.
11. Фармацевтическая композиция по п.10, дополнительно содержащая один или более дополнительных терапевтических агентов, выбранных из противовоспалительных агентов, иммунодепрессивных и/или иммуномодулирующих агентов, стероидов, нестероидных противовоспалительных агентов, антигистаминных средств, анальгетиков и их подходящих смесей.
12. Способ лечения заболевания, нарушения или состояния, на которое оказывает положительное воздействие ингибирование любого или обоих из дигидрооротатдегидрогеназы (DHODH) и цитокина IL 17, включающий введение субъекту, который нуждается в этом, эффективного количества соединения по любому из пп.1-9.
13. Способ лечения аутоиммунных заболеваний, иммунных и воспалительных заболеваний, деструктивных заболеваний костей, разных видов рака и злокачественных неопластических заболеваний, нарушений, связанных с ангиогенезом, вирусных заболеваний или инфекционных заболеваний путем ингибирования DHODH или IL 17, или их комбинации, включающий введение субъекту, который нуждается в этом, эффективного количества соединения по любому из пп.1-9.
14. Способ лечения ревматоидного артрита, псориатического артрита, системной красной волчанки, рассеянного склероза, псориаза, анкилозирующего спондилоартрита, грануломатоза Вегенера, многосуставного ювенильного идиопатического артрита, воспалительного заболевания кишечника, болезни Крона, синдрома Рейтера, фибромиалгии, хронического панкреатита, заболевания "трансплантат против хозяина", хронического саркоидоза, отторжения трансплантата, контактного дерматита, атопического дерматита, аллергического ринита, аллергического конъюктивита, синдрома Бехчета; воспалительных состояний глаз, таких как конъюктивит, увеит; остеопороза, остеоартрита, гемангиом, окулярной неоваскуляризации, дегенерации желтого пятна, ВИЧ-инфекции, гепатитной и цитомегаловирусной инфекции, сепсиса, септического шока, эндотоксического шока, грамотрицательного сепсиса, синдрома токсического шока, шигеллеза и других протозойных инвазий, таких как малярия, хронического обструктивного заболевания легких, астмы, колита, язвенного колита, артрита; заболеваний костей, связанных с повышенной резорбцией костной ткани, или хронического обструктивного заболевания дыхательных путей, синдрома Фелти, саркоидоза, болезни Стилла, пемфигоида, артериита Такаясу, системного склероза, рецидивирующего полихондрита, рефракторной IgA нефропатии, синдрома SAPHO2 (SAS), цитомегаловирусной инфекции, включая ринит или кисту, при этом указанный способ включает введение субъекту, который нуждается в этом, эффективного количества соединения по любому из пп.1-9.
15. Способ лечения ревматоидного артрита, рассеянного склероза или воспалительного заболевания кишечника, включающий введение субъекту, который нуждается в этом, эффективного количества соединения по любому из пп.1-9.
Текст
Изобретение представляет ингибиторы дигидрооротатдегидрогеназы формулы (I), содержащие их фармацевтические композиции и способы лечения заболеваний или расстройств, при которых,как известно, ингибирование дигидрооротатдегидрогеназы дает благоприятный эффект. Данная заявка объявляет приоритет предварительной индийской патентной заявки с номером 1265/CHE/2009 от 6 мая 2010 г., которая включена сюда путем ссылки. Область изобретения Настоящее изобретение представляет ингибиторы дигидрооротатдегидрогеназы, содержащие их фармацевтические композиции и способы лечения заболеваний или расстройств, при которых, как известно, ингибирование дигидрооротатдегидрогеназы дает благоприятный эффект. Уровень техники В недавнем прошлом интенсивные исследования были посвящены открытию и изучению структуры и функций энзимов и биомолекул, связанных с различными заболеваниями. Одним таким важным классом энзимов, который является предметом обширных исследований, является дигидрооротатдегидрогеназа (DHODH).DHODH представляет собой энзим, который катализирует четвертую стадию в de novo биосинтезе пиримидина. Он превращает дигидрооротат (DHO) в оротат (ORO). DHODH человека является вездесущей флавиновой мононуклеотидной (FMN) составляющей флавопротеина. В бактериях (ген pyrD) он локализован на внутренней стороне цитозольной мембраны. В некоторых дрожжах, таких как Saccharomyces cerevisiae (ген URA1), он является цитозольным протеином, тогда как в других эукариотах он находится в митохондриях (см. работу Proc. Natl. Acad. Sci. U.S.A., 89 (19), 8966-8970). DHODH классифицируется как семейство протеинов класса I или класса II на основе ко-фактора. DHODH человека принадлежит к семейству класса 2, в котором используется флавин как редокс ко-фактор, в отличие от протеина бактериального семейства класса 1, в котором вместо этого используется фумарат или NAD+. В данной клетке протеин млекопитающего закреплен на внутреннем митохондриальном листке. Именно этот DHODH катализирует конверсию DHO в ORO, что представляет лимитирующую скорость стадию вde novo пиримидиновом биосинтезе (см. работу McLean et al., Biochemistry 2001, 40, 2194-2200). Кинетические исследования указывают на последовательный механизм типа пинг-понга для превращения DHO в ORO (см. работу Knecht et al., Chem. Biol. Interact. 2000, 124, 61-76). Первая полуреакция включает восстановление DHO до ORO. Происходит перенос электронов к FMN, который окисляется до дигидрофлавин мононуклеотида (FMNH2). После диссоциации ORO из энзима FMNH2 регенерируется молекулой убихинона, которая рекрутируется из внутренней митохондриальной мембраны. Кинетические и структурные исследования выявили два отдельных связывающих сайта для DHO/ORO и убихинона соответственно.DHODH человека состоит из двух доменов - большого C-концевого домена (Met78-Arg396) и меньшего N-концевого домена (Met30-Leu68), соединенных удлиненной петлей. Большой C-концевой домен может быть лучше всего описан как /-бочковая складка с центральной бочковой структурой из восьми параллельных -нитей, окруженных восемью -спиралями. Редокс сайт, образованный связывающим субстрат карманом, и сайт, который связывает ко-фактор FMN, размещены на этом большом Cконцевом домене. Малый N-концевой домен, с другой стороны, состоит из двух -спиралей (маркированных 1 и 2), соединенных вместе короткой петлей. Этот малый N-концевой домен содержит связывающий сайт для кофакторного убихинона. Спирали 1 и 2 перекрывают щель размером примерно 1020 2 в так называемом гидрофобном петче с помощью короткой 1-2 петли в узком конце данной щели. Щель образует вход в туннель, который оканчивается у FMN полости возле 1-2 петли. Этот туннель суживается в направлении проксимального редокс сайта и оканчивается несколькими заряженными или полярными боковыми цепями (Gln47, Tyr356, Thr360 и Arg136). Структурные особенности,как обсуждалось выше, совместно с кинетическими исследованиями предполагают, что убихинон, который может легко диффундировать в митохондриальную внутреннюю мембрану, использует этот туннель, чтобы приблизиться к FMN ко-фактору для осуществления редокс реакции (см. работу Baumgartneret al., J. Med. Chem. 2006, 49, 1239-1247). Исследование, раскрытое в журнале The Journal of Biological Chemistry 2005, 280(23), 21847-21853,формально демонстрирует возможность идентифицировать сильные ингибиторы P. falciparum DHODH,которые не ингибируют человеческий энзим. Сравнение человеческих DHODH кристаллических структур с малярийной DHODH аминокислотной последовательностью дополнительно предполагает наличие возможностей для специфического в отношении вида ингибиторного связывания. В организме DHODH катализирует синтез пиримидинов, которые необходимы для роста клеток. Ингибирование DHODH ингибирует рост (патологически) быстро пролиферирующих клеток, тогда как клетки, которые растут с нормальной скоростью, могут получать необходимые пиримидиновые основания из нормального метаболического цикла. Важнейшие типы клеток для иммунной реакции, лимфоциты, используют исключительно синтез пиримидинов для своего роста и реагируют особенно чувствительно на ингибированиеDHODH ингибирование приводит к сниженным клеточным уровням рибонуклеотидного уридин монофосфата (rUMP), задерживая, таким образом, пролиферирующие клетки в Gl фазе клеточного цикла. Ингибирование de novo пиримидинового нуклеотидного синтеза представляет значительный интерес в связи с наблюдениями того, что лимфоциты, как представляется, не могут претерпевать клональную экспансию, когда этот путь заблокирован. Вещества, которые ингибируют рост лимфоцитов, являются важными медикаментами для лечения аутоиммунных заболеваний. В процессе гомеостатической пролиферации путь утилизации, который не зависит от DHODH,представляется достаточным для снабжения клеток пиримидиновыми основаниями. Только клетки с высокой оборачиваемостью и, в частности, T- и B-лимфоциты нуждаются в de novo пути для пролиферации. В этих клетках DHODH ингибирование останавливает ход клеточного цикла, подавляя синтез ДНК и, следовательно, пролиферацию клеток (см. работу Breedveld et al., Ann Rheum Dis 2000). Поэтому ингибиторы DHODH проявляют благоприятные иммунодепрессантные и антипролиферативные эффекты в болезнях человека, характеризующихся аномальной и неконтролируемой пролиферацией клеток, вызывающей хроническое воспаление и деструкцию тканей. Человеческий энзим дигидрооротатдегидрогеназа(DHODH) является хорошо описанной мишенью для лекарств малого молекулярного веса Disease Modifying Antirheumatic Drugs (DMARDs). Список известных DHODH ингибиторов включает лефлуномид, терифлуномид, брекинар (NSC 368390) (Cancer Research 1992, 52, 3521-3527), дихлораллил лоузон (The Journal of Biological Chemistry 1986, 261(32), 14891-14895), маритимус (FK 778) (Drugs of the Future 2002, 27(8), 733-739) и редоксалDHODH проявляют благоприятные иммунодепрессантные и антипролиферативные активности, наиболее выраженные в отношении T-клеток (см. работу Fairbanks et al., J. Biol. Chem. 1995, 270, 29682-29689). Брекинар и лефлуномид являются двумя примерами ингибиторов DHODH низкого молекулярного веса,которые прошли клинические испытания. Последний используется в лечении ревматоидного артрита,рефракторного к метотрексату (см. работу Rozman J. Rheumatol Suppl. 1998, 53, 27-31; Pally et al., Toxicology 1998, 127, 207-222). Клиническое применение обеих молекул затруднено из-за различных побочных эффектов. Исходя из очень высокой эффективности в моделях на животных, брекинар первоначально был разработан для терапии отторжения трансплантатов органов, но затем был переключен на рак как вторичное показание. Данное соединение оказалось неудачным в клинических испытаниях вследствие его узкого терапевтического окна. Пероральное использование брекинара и некоторых его аналогов дало токсические эффекты, включая лейкоцитопению и тромбоцитопению, при его введении в комбинации с циклоспорином. Применение лефлуномида может быть ограничено его длительным периодом полувыведения, составляющим приблизительно 2 недели, что представляет серьезную помеху для пациентов, у которых развились побочные эффекты (см. работы Fox et al. J. Rheumatol Suppl. 1998, 53, 20-26; Alldred etal., Expert Opin. Pharmacother. 2001, 2, 125-137). Кроме аннулирования пролиферации лимфоцитов, ингибиторы DHODH (например, терифлуномид,маритимус (FK778) и брекинар) оказывают противовоспалительное действие путем ингибирования продуцирования цитокинов и нуклеарного фактора (NF)-kB-сигнализирования, миграции моноцитов и усиленного продуцирования трансформирующего фактора роста бета-1, а также индуцируют дифференцировку T-клеток-хелперов типа 1 (TM) в субпопуляцию типа 2 (Th2) (Manna et al., J. Immunol 2000; Dimitrova et al., J. Immunol 2002). Кроме того, дифференцировка остеокластов, опосредованная лигандом Receptor Activator for Nuclear Factor kB (RANKL), снижалась посредством DHODH ингибирования (Urushibara et al., Arthrititis Rheum 2004). В сокристаллизационных экспериментах с двумя ингибиторамиDHODH, которые достигли клинических испытаний, брекинар (Dexter et al., Cancer Res. 1985) и терифлуномид (A77-1726), как было найдено, оба связываются в общий сайт, который, как также считают, является связывающим сайтом ко-фактора убихинона (Liu et al., Struc. Fold. Des. 2000). Лефлуномид, который продается под торговой маркой Arava (EP 0780128, WO 97/34600), был первым DHODH ингибитором, который достиг рынка. Лефлуномид является промедикаментом терифлуномида, который представляет собой активный метаболит, ингибирующий DHODH человека с умеренной активностью (Fox et al.,J. Rheumatol. Suppl. 1998). Лефлуномид является DMARD от фирмы Авентис (Aventis), который был утвержден FDA для лечения ревматоидного артрита в 1998 году и EMEA - для лечения псориатического артрита в 2004 г. В настоящее время лефлуномид находится на стадии активной разработки для лечения системной красной волчанки, грануломатоза Вегенера (Wegener) (Metzler et al., Rheumatology 2004, 43(3), 315-320) и ВИЧинфекции. Более того, терифлуномид, его активный метаболит, является эффективным при рассеянном склерозе и в настоящее время находится в фазе III клинических испытаний (O'Connor et al., Neurology 2006). Другие данные появляются в других близко связанных заболеваниях, таких как анкилозирующий спондилоартрит (Haibel et al., Ann. Rheum. Dis. 2005), многосуставный ювенильный идиопатический артрит (Silverman et al., Arthritis Rheum. 2005) и саркоидоз (Baughman et al., Sarcoidosis Vase. Diffuse LungDis. 2004). Кроме того, лефлуномид и FK778 выявили антивирусную активность против цитомегаловируса. Лефлуномид в настоящее время показан как терапия второй линии для цитомегаловирусного заболевания после трансплантации органа (John et al., Transplantation 2004). Кроме того, лефлуномид снижает ВИЧ-репликацию приблизительно на 75% при концентрации, которая может быть достигнута при обычном дозировании (Schlapfer et al., AIDS 2003). DHODH ингибиторами, которые исследуются на разных стадиях клинических испытаний, являются 4SC-101 (фаза-II) от 4SC AG; LAS-186323 (фаза-I) от лабораторий Almirall SA и ABR-224050, ABR-222417 и ABR-214658 (предклинические) от фирмы Active Biotech AB. Точные структуры всех этих молекул еще не раскрыты. Различные DHODH ингибиторы раскрыты для лечения или предупреждения аутоиммунных заболеваний, иммунных и воспалительных заболеваний, деструктивных костных заболеваний, злокачественных неопластических заболеваний, ангиогенсвязанных болезней, вирусных болезней и инфекционных заболеваний; смотри, например, WO2009137081; WO2009133379; WO 2009021696; WO2009082691;WO9938846; WO9941239; EP767167 и US5976848. В отношении дополнительных обзоров и литературы, касающейся DHODH ингибиторов, смотри работы BioMed. Chem. Letters, 20(6), 2010, Pages 1981-1984; J. Med. Chem. 2009, 52, 2683-2693; J. Med.Chem. 2008, 51 (12), 3649-3653. Все эти патенты, патентные заявки и литературные обзоры включены сюда путем ссылки во всей своей полноте для всех целей. Несмотря на прогресс, достигнутый в области DHODH ингибирования в болезнях человека, проблемы остаются в рамках побочных эффектов и необходимых клинических преимуществ от низкомолекулярных ингибиторов. Соответственно все еще имеется неудовлетворенная и крайне необходимая потребность в низкомолекулярных DHODH ингибиторах для лечения и/или ослабления интенсивности болезней и расстройств, которые, как известно, ассоциируются с DHODH. Сущность изобретения Настоящее изобретение касается соединений формулы (I), содержащих их фармацевтических композиций и способов их применения. Соединение формулы (I) имеет структуру или его таутомер, стереоизомер или фармацевтически приемлемая соль, где кольцо A независимо выбрано из моноциклического арила, содержащего 6 атомов углерода, и моноциклического 6-членного гетероарила, содержащего один или более атомов N, при этом X в каждом случае независимо представляет собой CR4 или N; кольцо B независимо выбрано из моноциклического арила, содержащего 6 атомов углерода, и моноциклического 6-членного гетероарила, содержащего один или два гетероатома, представляющих собойX2 представляет собой CR2, где R2 выбран из водорода и галогена; иCy выбран из замещенной или незамещенной 3-15-членной гетероциклической группы, содержащей один или более гетероатомов, выбранных из N, O и S; замещенного арила, содержащего 6 атомов углерода; и замещенного или незамещенного 5-14-членного гетероарила, содержащего один или более гетероатомов, выбранных из N, O и S;R4 независимо выбран из водорода, галогена или (C1-C8)алкила;Ra и Rb в каждом случае представляют собой водород;Y в каждом случае представляет собой O. Некоторые из соединений настоящего изобретения имеют различные таутомерные формы. Например, кольцо A может включать -C(OH)=N-группу, которая взаимопревращается в -C(O)-NH- и обратно вновь в -C(OH)=N-. Еще один вариант воплощения представляет соединение, имеющее формулу (I), где кольцо A выбрано из необязательно замещенных одним или более R4. Еще одним вариантом воплощения является соединение, имеющее формулу (I), где R1 представляет собой -COOH. Еще одним вариантом воплощения является соединение, имеющее формулу (I), где X в каждом случае представляет собой CH, C-Cl или C-F. Еще одним вариантом воплощения является соединение, имеющее формулу (I), где X1 в каждом случае представляет собой CH или N. Еще одним вариантом воплощения является соединение, имеющее формулу (I), где X2 представляет собой CH, CCl или CF. Еще одним вариантом воплощения является соединение, имеющее формулу (I), где X3 является CCl или CF. Еще одним вариантом воплощения является соединение, имеющее формулу (I), где кольцо B выбрано из необязательно замещенных одним или более R4. Еще одним вариантом воплощения является соединение, имеющее формулу (I), где Cy выбран из при этом каждое необязательно замещено одним или более атомами галогена. В одном предпочтительном варианте воплощения кольцо A представляет собой фенил, кольцо B представляет собой фенил, Су представляет собой 3-этил-1H-индол-5-ил, R1 является -COOH, Y являетсяO, L1 отсутствует и L2 отсутствует. В одном более предпочтительном варианте воплощения Су является фенилом, замещенным одной или более С 1-С 4-алкокси, -S-(C1-C4-алкилом) и/или галогеном. В более предпочтительном варианте воплощения кольцо B является фенилом, замещенным одной или более фторогруппами. Еще одним вариантом воплощения является соединение формулы (IA) или его таутомер, стереоизомер или фармацевтически приемлемая соль, где кольцо A выбрано из: необязательно замещенных одним или более R4; и все другие переменные являются такими же самыми, как описано выше относительно формулы(I). Еще одним вариантом воплощения является соединение формулы (IA) или его таутомер, стереоизомер или фармацевтически приемлемая соль, где кольцо A выбрано изCy представляет собой замещенный фенил, замещенный индол или замещенный индазол, такой как а все другие переменные являются такими же самыми, как описано выше относительно формулы(I). Репрезентативные соединения настоящего изобретения включают те, что определены ниже, и их фармацевтически приемлемые соли (табл. 1). Настоящее изобретение не следует истолковывать как ограничивающееся ими. В частности, соединения формулы (I) или/и (IA) или их фармацевтически приемлемые соли являются DHODH ингибиторами, полезными для лечения, предупреждения и/или снижения интенсивности заболеваний или расстройств, где ингибирование DHODH, как известно, дает благоприятный эффект. Еще одним вариантом воплощения настоящего изобретения является способ лечения иммунологического заболевания, воспалительного заболевания, рака или другой пролиферативной болезни посред- 10024702 ством ингибирования DHODH путем введения пациенту, который нуждается в таком лечении, эффективного количества по меньшей мере одного соединения формулы (I) или/и (IA), как определено выше. Еще одним вариантом воплощения настоящего изобретения является способ лечения иммунологического заболевания, воспалительного заболевания, рака или другой пролиферативной болезни посредством ингибирования IL-17 либо непосредственно, либо посредством ингибирования DHODH путем введения пациенту, который нуждается в таком лечении, эффективного количества по меньшей мере одного соединения формулы (I) или/и (IA), как определено выше. Еще одним вариантом воплощения настоящего изобретения является способ лечения иммунологического заболевания, воспалительного заболевания, рака или другой пролиферативной болезни посредством ингибирования IL-17, также как и DHODH, путем введения пациенту, который нуждается в таком лечении, эффективного количества по меньшей мере одного соединения формулы (I) или/и (IA), как определено выше. Соединения формулы (I) или/и (IA) полезны в лечении различных заболеваний, включая, но не ограничиваясь этим, аутоиммунные заболевания, иммунные и воспалительные заболевания, деструктивные костные заболевания, рак и злокачественные неопластические заболевания, ангиогенно-связанные расстройства, вирусные болезни и инфекционные болезни. Такие заболевания включают, но не ограничиваются этим: аутоиммунные заболевания, которые могут быть предупреждены (профилактически) или излечены,включают, не ограничиваясь этим, ревматоидный артрит, псориатический артрит, системную красную волчанку, рассеянный склероз, псориаз, анкилозирующий спондилоартрит, грануломатоз Вегенера (Wegener), многосуставной ювенильный идиопатический артрит, воспалительное кишечное заболевание,такое как язвенный колит, и болезнь Крона, синдром Рейтера (Reiter), фибромиалгию и диабет типа 1; иммунные и воспалительные заболевания, которые могут быть предупреждены (профилактически) или излечимы, включают, не ограничиваясь этим, астму, COPD (хроническое обструктивное заболевание легких), респираторный дистресс-синдром, острый или хронический панкреатит, болезнь трансплантат против хозяина, хронический саркоидоз, отторжение трансплантата, контактный дерматит, атопический дерматит, аллергический ринит, аллергический конъюктивит, синдром Бехчета, воспалительные состояния глаза, такие как конъюктивит и увеит; деструктивные костные заболевания, которые могут быть предупреждены или излечены, включают,не ограничиваясь этим, остеопороз, остеоартрит и связанные с множественной миеломой костные заболевания; рак и злокачественные неопластические заболевания, которые могут быть предупреждены (профилактически) или излечены, включают, не ограничиваясь этим, рак предстательной железы, рак яичника и рак мозга, карциному, включая карциному мочевого пузыря, молочной железы, ободочной кишки, почки,печени, легких, включая мелкоклеточный рак легких, пищевода, желчного пузыря, яичника, поджелудочной железы, желудка, шеи, щитовидной железы, предстательной железы, и кожи, включая плоскоклеточный рак; гемопоэтические опухоли лимфоидного происхождения, включая лейкоз, острый лимфолейкоз, острый лимфобластный лейкоз, B-клеточную лимфому, T-клеточную лимфому, лимфому Ходжкина,неходжкинскую лимфому, ворсинчатоклеточную лимфому и лимфому Беркитта (Burkett); гемопоэтические опухоли миелоидного происхождения, включая острые и хронические миелогенные лейкозы, миелодиспластический синдром и промиелоцитарный лейкоз; опухоли мезенхимального происхождения,включая фибросаркому и рабдомиосаркому; опухоли центральной и периферической нервной системы,включая астроцитому, нейробластому, глиому и невриномы; и другие опухоли, включая меланому, семиному, тератокарциному, остеосаркому, ксенодерому пигментозум, кератоктантому, фолликулярный рак щитовидной железы и саркому Капоши (Kaposi); связанные с ангиогенезом заболевания, которые могут быть предупреждены или излечены, включают, не ограничиваясь этим, гемангиомы, глазную неоваскуляризацию, дегенерацию желтого пятна или диабетическую ретинопатию; вирусные болезни, которые могут быть предупреждены или излечены, включают, не ограничиваясь этим, ВИЧ-инфекцию, гепатитную и цитомегаловирусную инфекцию; инфекционные болезни, которые могут быть предупреждены или излечены, включают, не ограничиваясь этим, сепсис, септический шок, эндотоксиновый шок, грамотрицательный сепсис, синдром токсического шока, шигеллез и другие протозойные инвазии, такие как малярия. Соединения настоящего изобретения как модуляторы апоптоза полезны в лечении рака (включая,но не ограничиваясь типами, упомянутыми выше), вирусных инфекций (включая, но не ограничиваясь этим, герпетовирус, вирус оспы, Эпштейна-Барра (Epstein-Barr) вирус, Синдбис (Sindbis) вирусы и аденовирус), предупреждении развития СПИД у ВИЧ-инфицированных пациентов, аутоиммунных заболеваний (включая, но не ограничиваясь этим, системную красную волчанку, аутоиммунный гломерулонефрит, ревматоидный артрит, псориаз, воспалительное кишечное заболевание и аутоиммунный сахарный диабет), нейродегенеративных заболеваний (включая, но не ограничиваясь этим, болезнь Альцгеймера, деменцию, связанную со СПИДом, болезнь Паркинсона, боковой амиотрофический склероз, пигментный ретинит, спинальную мышечную атрофию и мозжечковую дегенерацию), миелодиспластиче- 11024702 ских синдромов, гипопластической анемии, ишемической травмы, связанной с инфарктом миокарда,удара и реперфузионной травмы, аритмии, атеросклероза, индуцированных токсином или связанных с алкоголем болезней печени, гематологических заболеваний (включая, но не ограничиваясь этим, хроническую анемию и гипопластическую анемию), дегенеративных болезней мышечноскелетной системы(включая, но не ограничиваясь этим, остеопороз и артрит), аспирин-чувствительного риносинусита, муковисцидоза, рассеянного склероза, болезней почек и раковой боли. Соединения настоящего изобретения могут модулировать уровень клеточного РНК и ДНК синтеза. Поэтому эти агенты полезны в лечении вирусных инфекций (включая, но не ограничиваясь этим, ВИЧ,вирус папиломы человека, герпесвирус, вирус оспы, Эпштейна-Барра вирус, Синдбис вирусы и аденовирус). Соединения настоящего изобретения полезны в химиопредупреждении рака. Химиопредупреждение определяется как ингибирование развития инвазивного рака путем либо блокирования инициирующего мутагенного события, либо путем блокирования развития клеток в состоянии злокачественного перерождения, которые уже пережили поражение, или ингибирования рецидива опухоли. Данные соединения также полезны в ингибировании ангиогенеза и метастаза опухолей. Соединения настоящего изобретения могут также комбинироваться с другими активными соединениями при лечении заболеваний, где ингибирование DHODH, как известно, дает благоприятный эффект. В других вариантах воплощения болезни, состояния или расстройства, лечение которых выигрывает от ингибирования DHODH, включают, не ограничиваясь этим, заболевания, связанные с иммунной системой (например, аутоиммунное заболевание), заболевание или расстройство, включающее воспаление (например, астму, хроническое обструктивное заболевание легких, ревматоидный артрит, воспалительное кишечное заболевание, гломерулонефрит, нейровоспалительные заболевания, рассеянный склероз, увеит и расстройства иммунной системы), рак или другое пролиферативное заболевание, болезни или расстройства печени и почек. В одном варианте воплощения описанные здесь соединения используются как иммунодепрессанты для предупреждения отторжений трансплантатов, отторжения при аллогенной или ксеногенной трансплантации (органа, костного мозга, стволовых клеток, других клеток и тканей), болезни трансплантат против хозяина. В других вариантах воплощения отторжения трансплантата вызваны трансплантацией ткани или органа. В дополнительных вариантах воплощения болезнь тансплантат против хозяина вызвана трансплантацией костного мозга или стволовых клеток. В частности, соединения формулы (I) или/и (IA) полезны в лечении множества воспалительных заболеваний, включая, но не ограничиваясь этим, воспаление, гломерулонефрит, увеит, болезни или расстройства печени, почечные болезни или расстройства, хроническое обструктивное заболевание легких,ревматоидный артрит, воспалительное кишечное заболевание, васкулит, дерматит, остеоартрит, воспалительное мышечное заболевание, аллергический ринит, вагинит, интерстициальный цистит, склеродерму,остеопороз, экзему, аллогенную или ксеногенную трансплантацию, отторжение трансплантата, болезнь трансплантат против хозяина, отторжение роговичного трансплантата, красную волчанку, системную красную волчанку, пролиферативный люпус-нефрит, диабет типа I, легочный фиброз, дерматомиозит,тироидит, тяжелую миастению, аутоиммунную гемолитическую анемию, муковисцидоз, хронический рецидивирующий гепатит, первичный билиарный цирроз, аллергический конъюктивит, гепатит и атопический дерматит, астму и синдром Шегрена. В одном варианте воплощения описанные здесь соединения полезны в лечении множества болезней, включая синдром Фелти (Felty), грануломатоз Вегенера (Wegener), болезнь Крона, саркоидоз, болезнь Стилла (Still), пемфигоид, артериит Такаясу (Takayasu), системную склеродермию, рецидивирующий полихондрит, рефракторную IgA нефропатию, синдром SAPHO2 (SAS), цитомегаловирусную инфекцию, включая ринит или кисту, псориаз и множественную миелому. Данное изобретение также представляет фармацевтические композиции, содержащие соединения,имеющие формулу (I) или/и (IA), совместно с фармацевтически приемлемым носителем. Подробное описание изобретения Если не указано иное, все технические и научные термины, использованные здесь, имеют такое же самое значение, как это принято в данной области техники, к которой принадлежит настоящая заявка. В случае наличия множества определений для данных терминов преобладают содержащиеся в этом разделе. Там, где сделана ссылка на URL или другой такой идентификатор или адрес, понятно, что такие идентификаторы обычно изменяются, и конкретная информация в интернете приходит и уходит, но эквивалентную информацию находят путем поиска в интернете. Кроме того, ссылка свидетельствует о наличии и распространенности среди исследователей такой информации. Следует понимать, что предшествующее общее описание и последующее подробное описание являются лишь иллюстративными и пояснительными и не ограничивают заявленный предмет изобретения. В этой заявке, если специально не оговорено, единственное число включает множественное. Следует заметить, что, как используется в данной спецификации и прилагаемой формуле изобретения, формы единственного числа включают множественное число, если в контексте четко не указано иное. В этой заявке использование "или" означает "и/или", если не указано иное. Кроме того, использование термина "включающий", также как и дру- 12024702 гих форм, таких как "включает" и "включенный", не является ограничивающим. Определения терминов стандартной химии и молекулярной биологии можно найти в следующих работах, включая, но не ограничиваясь этим, Carey and Sundberg "ADVANCED ORGANIC CHEMISTRY 4th edition" Vols. A (2000) and В (2001), Plenum Press, New York and "MOLECULAR BIOLOGY OF THECELL 5th edition" (2007), Garland Science, New York. Если не указано иное, в рамках раскрытых здесь вариантов воплощения предусмотрены обычные методы масс-спектроскопии, ЯМР, высокоэффективной жидкостной хроматографии, химии белков, биохимии, рекомбинантной ДНК и фармакологии. Если не представлены специфические определения, использованная терминология в связи с описанными здесь лабораторными процедурами и методами аналитической химии, а также лекарственной и фармацевтической химии в целом отвечает общепринятой. В некоторых вариантах воплощения используются стандартные методы для химического анализа, получения фармацевтических препаратов и их доставки, а также лечения пациентов. В других вариантах воплощения используются стандартные методы в отношении рекомбинантной ДНК, олигонуклеотидного синтеза, культивирования и преобразования тканей (например, электропорация, липофекция). В некоторых вариантах воплощения реакции и очистка проводятся, например, с использованием наборов согласно спецификации производителя или как здесь описано. Вышеупомянутые методики и процедуры реализуются в общем с использованием обычных методов и как это описано в различных литературных источниках общего и более специфического плана,которые цитируются и обсуждаются в настоящей спецификации. Как здесь используется, будут применяться следующие определения, если не оговорено иное. Кроме того, многие из определенных здесь групп могут быть, необязательно, замещены. Перечень заместителей в данном определении является иллюстративным, и его не следует рассматривать как ограничитель заместителей, которые определены где-либо в ином месте настоящей спецификации. Термин "алкил" касается углеводородного радикала с прямой или разветвленной цепью, состоящего лишь из углеродных и водородных атомов, который не содержит ненасыщения, имеет от одного до восьми углеродных атомов и который присоединен к остатку данной молекулы одинарной связью, например метил, этил, н-пропил, 1-метилэтил (изопропил), н-бутил, н-пентил и 1,1-диметилэтил (t-бутил). Термин замещенный или незамещенный (C1-2)алкил касается алкильной группы, как определено выше,имеющей до 2 углеродных атомов, а термин замещенный или незамещенный (C1-6)алкил касается алкильной группы, как определено выше, имеющей до 6 углеродных атомов. Термин "алкенил" касается алифатической углеводородной группы, содержащей двойную связь углерод-углерод, которая может быть прямой или разветвленной, или разветвленной цепи, имеющей от приблизительно 2 до приблизительно 10 углеродных атомов, например этенил, 1-пропенил, 2-пропенил(аллил), изо-пропенил, 2-метил-1-пропенил, 1-бутенил и 2-бутенил. Термин замещенный или незамещенный (C2)алкенил касается алкенильной группы, как определено выше, имеющей 2 углеродных атома. Термин "алкинил" касается гидрокарбильного радикала с прямой или разветвленной цепью, имеющего по меньшей мере одну тройную связь углерод-углерод и имеющего от 2 до 12 углеродных атомов(где предпочтение в данном случае отдается радикалам, имеющим от 2 до 10 углеродных атомов), например этинил, пропинил и бутинил. Термин замещенный или незамещенный (C2)алкинил касается алкинильной группы, как определено выше, имеющей 2 углеродных атома. Термин "алкокси" обозначает алкильную группу, как определено выше, присоединенную через кислородную связь к остатку молекулы. Репрезентативные примеры этих групп включают -OCH3 и -OC2H5. Термин "циклоалкил" отвечает неароматической моно или мультициклической кольцевой системе из приблизительно от 3 до 12 углеродных атомов, такой как циклопропил, циклобутил, циклопентил и циклогексил. Примеры мультициклических циклоалкильных групп включают пергидронафтильную,адамантильную и норборнильную группы, мостиковые циклические группы и спиробициклические группы, например спиро(4,4)нон-2-ил. Термин "циклоалкилалкил" касается циклического кольцо-содержащего радикала, содержащего от 3 до 8 углеродных атомов, непосредственно присоединенных к алкильной группе, которая затем присоединена к основной структуре на любом углеродном атоме из алкильной группы, что приводит к созданию стабильной структуры, такой как циклопропилметил, циклобутилэтил и циклопентилэтил. Термин "циклоалкенил" касается циклических кольцо-содержащих радикалов, содержащих от 3 до 8 углеродных атомов, по меньшей мере с одной двойной связью углерод-углерод, такой как циклопропенил, циклобутенил и циклопентенил. Термин "циклоалкенилалкил" касается циклоалкенильной группы,непосредственно присоединенной к алкильной группе, которая затем присоединена к основной структуре на любом углеродном атоме из алкильной группы, что приводит к созданию стабильной структуры. Термин "арил" касается ароматического радикала, имеющего от 6 до 20 углеродных атомов, таких как фенил, нафтил, тетрагидронафтил, инданил и бифенил. Термин "арилалкил" касается арильной группы, как определено выше, непосредственно связанной с алкильной группой, как определено выше, например -CH2C6H5 и -C2H5C6H5. Термин "гетероциклическое кольцо" касается неароматического 3-15-членного кольцевого радика- 13024702 ла, который состоит из углеродных атомов и по меньшей мере одного гетероатома, который выбирается из группы, состоящей из азота, фосфора, кислорода и серы. Для целей этого изобретения гетероциклический кольцевой радикал может представлять моно-, би-, три- или тетрациклическую кольцевую систему,которая может включать слитую, мостиковую или спирокольцевую системы, и атомы азота, фосфора,углерода, кислорода или серы в данном гетероциклическом кольцевом радикале могут быть, необязательно, окислены до различных состояний окисления. Кроме того, атом азота может быть, необязательно, кватернизован. Данный гетероциклический кольцевой радикал может быть присоединен к основной структуре на любом гетероатоме или углеродном атоме, что приводит к образованию стабильной структуры. Термин "гетероарил" касается замещенного, необязательно, 5-14-членного ароматического кольца,имеющего один или более гетероатомов, которые выбираются из N, O и S как кольцевых атомов. Данный гетероарил может представлять моно-, би- или трициклическую кольцевую систему. Примеры таких гетероарильных кольцевых радикалов включают, не ограничиваясь этим, оксазолил, тиазолил, имидазолил,пирролил, фуранил, пиридинил, пиримидинил, пиразинил, бензофуранил, индолил, бензотиазолил, бензоксазолил, карбазолил, хинолил и изохинолил. Данный гетероарильный кольцевой радикал может быть присоединен к основной структуре на любом гетероатоме или углеродном атоме, что приводит к образованию стабильной структуры. Примеры таких "гетероциклических кольцевых" или "гетероарильных" радикалов включают, не ограничиваясь этим, азетидинил, акридинил, бензодиоксолил, бензодиоксанил, бензофуранил, карбазолил,циннолинил, диоксоланил, индолизинил, нафтиридинил, пергидроазепинил, феназинил, фенотиазинил,феноксазинил, фталазинил, пиридил, птеридинил, пуринил, хиназолинил, хиноксалинил, хинолинил,изохинолинил, тетразолил, имидазолил, тетрагидроизоуинолили, пиперидинил, пиперазинил, 2 оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, 2-оксоазепинил, азепинил, пирролил, 4 пиперидонил, пирролидинил, пиразинил, пиримидинил, пиридазинил, оксазолил, оксазолинил, оксазолидинил, триазолили, инданил, изоксазолил, изоксазолидинил, морфолинил, тиазолил, тиазолинил, тиазолидинил, изотиазолил, хинуклидинил, изотиазолидинил, индолили, изоиндолил, индолинил, изоиндолинил, октагидроиндолил, октагидроизоиндолил, хинолил, изохинолил, декагидроизохинолил, бензимидазолил, тиадиазолил, бензопиранил, бензотиазолил, бензооксазолил, фурил, тетрагидрофурил, тетрагидропиранил, тиенил, бензотиенил, тиаморфолинил, тиаморфолинил сульфоксид, тиаморфолинил сульфон,диоксафосфоланил, оксадиазолил, хроманил и изохроманил. Термин "гетероарилалкил" касается гетероарильного кольцевого радикала, как определено выше,непосредственно связанного с алкильной группой. Данный гетероарилалкильный радикал может быть присоединен к основной структуре на любом углеродном атоме из алкильной группы, что приводит к созданию стабильной структуры. Термин "гетероциклил" касается гетероциклического кольцевого радикала, как определено выше. Данный гетероциклильный кольцевой радикал может быть присоединен к основной структуре на любом гетероатоме или углеродном атоме, что приводит к образованию стабильной структуры. Термин "гетероциклилалкил" касается гетероциклического кольцевого радикала, как определено выше, непосредственно связанного с алкильной группой. Данный гетероциклилалкильный радикал может быть присоединен к основной структуре на углеродном атоме в алкильной группе, что приводит к образованию стабильной структуры. Термин "циклическое кольцо" касается циклического кольца, содержащего 3-10 углеродных атомов, необязательно, один или более из кольцевых углеродных атомов могут быть заменены гетероатомом, таким как N, O или S атом. Термин "моноциклическое кольцо" касается отдельного циклического кольца, содержащего 3-10 углеродных атомов, необязательно, один или более кольцевых углеродных атомов могут быть заменены гетероатомом, таким как атом N, O или S. Префикс "моноциклическое кольцо", использующийся, например, для моноциклического арила, касается отдельного арильного кольца, где данный арил является таким, как определено выше. Схожим образом термин моноциклический гетероарил касается отдельного гетероарильного кольца, где данный гетероарил является таким, как определено выше. То же самое применимо и к каждому из терминов моноциклический циклоалкил и моноциклическое гетероциклическое кольцо. Термин "замещенный", если не указано иное, касается замещения любым одним заместителем или любой их комбинацией из следующих заместителей, которые могут быть одинаковыми или разными и выбираются из водорода, гидрокси, галогена, карбоксила, циано, нитро, оксо (=O), тио (=S), замещенного или незамещенного алкила, замещенного или незамещенного алкокси, замещенного или незамещенного алкенила, замещенного или незамещенного алкинила, замещенного или незамещенного циклоалкила,замещенного или незамещенного циклоалкенила, замещенного или незамещенного циклоалкилалкила,замещенного или незамещенного циклоалкенилалкила, замещенного или незамещенного гетероциклического кольца, замещенного или незамещенного гетероциклилалкила, замещенного или незамещенного арила, замещенного или незамещенного арилалкила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероарилалкила, замещенного или незамещенного гуанидина, -COORx,- 14024702-C(O)Rx, -C(S)Rx, -C(O)NRxRy, -C(O)ONRxRy, -NRyRz, -NRxCONRyRz, -N(Rx)SORy, -N(Rx)SO2Ry, -(=NN(Rx)Ry), -NRxC(O)ORy, -NRxRy, -NRxC(O)Ry-, -NRxC(S)Ry -NRxC(S)NRyRz, -SONRxRy-, -SO2NRxRy-, -ORx,-ORxC(O)NRyRz, -ORxC(O)ORy-, -OC(O)Rx, -OC(O)NRxRy, -RxNRyC(O)Rz, -RxORy, -RxC(O)ORy,-RxC(O)NRyRz, -RxC(O)Rx, -RxOC(O)Ry, -SRx, -SORx, -SO2Rx, -ONO2, где Rx, Ry и Rz в каждой из вышеуказанных групп может представлять собой водород, замещенный или незамещенный алкил, замещенный или незамещенный алкокси, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный циклоалкил, замещенный или незамещенный циклоалкенил,замещенный или незамещенный циклоалкилалкил, замещенный или незамещенный циклоалкенилалкил,замещенное или незамещенное гетероциклическое кольцо, замещенный или незамещенный гетероциклилалкил, замещенный или незамещенный арил, замещенный или незамещенный арилалкил, замещенный или незамещенный гетероарил, замещенный или незамещенный гетероарилалкил, или любые две изRx, Ry и Rz могут быть объединены с образованием замещенного или незамещенного насыщенного или ненасыщенного 3-10-членного кольца, которое может, необязательно, включать гетероатомы, которые могут быть одинаковыми или разными и выбираются из О, NRx или S. Замещение или комбинация заместителей, предусмотренные этим изобретением, являются предпочтительно такими, которые приводят к образованию стабильных или химически возможных соединений. Термин стабильный, как здесь используется, касается соединений или структуры, которые существенно не изменяются под действием условий, необходимых для их получения, обнаружения и предпочтительно их регенерации, очистки и инкорпорирования в фармацевтическую композицию. Термин "галоген" или "гало" касается радикалов фтора, хлора, брома и йода. Термин "защитная группа" или "PG" касается заместителя, который используется для блокирования или защиты конкретной функциональной группы. Другие функциональные группы на данном соединении могут оставаться реакционными. Например, "аминозащитная группа" представляет собой заместитель, присоединенный к аминогруппе, который блокирует или защищает аминофункциональную группу в данном соединении. Подходящие аминозащитные группы включают, не ограничиваясь этим, ацетил,трифторацетил,трет-бутоксикарбонил(CBz) и 9 флуоренилметиленоксикарбонил (Fmoc). Схожим образом "гидроксизащитная группа" касается заместителя гидрокси группы, который блокирует или защищает гидрокси функциональную группу. Подходящите гидроксизащитные группы включают, не ограничиваясь этим, ацетил и силил. "Карбоксизащитная группа" касается заместителя карбокси группы, который блокирует или защищает карбокси функциональную группу. Подходящие карбоксизащитные группы включают, не ограничиваясь этим,цианоэтил,2-(триметилсилил)этил,2-(триметилсилил)этоксиметил,-2-(п-CH2CH2SO2Ph,толуолсульфонил)этил, 2-(п-нитрофенилсульфенил)этил, 2-(дифенилфосфино)этил и нитроэтил. Общее описание защитных групп и их использование можно найти в работе Т.W. Greene, Protective Groups inOrganic Synthesis, John WileySons, New York, 1991. Термин "стереоизомер" касается соединений, которые имеют идентичный химический состав, но отличаются в отношении расположения атомов и групп в пространстве. Они включают энантиомеры,диастереомеры, геометрические изомеры, атропизомеры или конформационные изомеры. Все стереоизомеры соединений, описанных здесь, находятся в пределах действия этого изобретения. Рацемические смеси также охватываются данным изобретением. Таким образом, отдельные стереохимические изомеры, также как и энантиомерные, диастереоизомерные и геометрические (или конформационные) смеси настоящих соединений находятся в пределах действия данного изобретения. Термин "таутомеры" касается соединений, которые характеризуются относительно легким взаимопревращением изомерных форм при равновесии. Эти изомеры, как предполагается, покрываются этим изобретением. Термин "пролекарство" касается соединения, которое является инактивным предшественником соединения, превращающимся в свою активную форму в организме посредством нормальных метаболических процессов. Термин "сложный эфир" касается соединения, которое образуется путем реакции между кислотой и спиртом с элиминацией воды. Сложный эфир может быть представлен формулой RCOOR'. Дополнительно настоящее изобретение также включает соединения, которые отличаются только присутствием одного или более изотопно обогащенных атомов, например, при замене водорода дейтерием и тому подобного. Фармацевтически приемлемые соли, составляющие часть этого изобретения, включают соли, полученные из неорганических оснований, таких как Li, Na, K, Ca, Mg, Fe, Cu, Zn, и Mn; соли органических оснований, таких как N,N'-диацетилэтилендиамин, глюкамин, триэтиламин, холин, гидроксид, дициклогексиламин, метформин, бензиламин, триалкиламин, тиамин и тому подобное; хиральных оснований подобных алкилфениламину, глицинолу и фенил глицинолу, соли природных аминокислот, таких как глицин, аланин, валин, лейцин, изолейцин, норлейцин, тирозин, цистин, цистеин, метионин, пролин,гидрокси пролин, гистидин, омитин, лизин, аргинин и серин; соли четвертичного аммония соединений изобретения с алкил галогенидами и алкилсульфаты, такие как MeI и (Me)2SO4, неприродных аминокислот, таких как D-изомеры или замещенные аминокислоты; гуанидин, замещенный гуанидин, где данные заместители выбираются из нитро, амино, алкила, алкенила, алкинила, аммония, или замещенные аммониевые соли и соли алюминия. Соли могут включать кислые соли присоединения, где это требуется, которыми являются сульфаты, нитраты, фосфаты, перхлораты, бораты, гидрогалогениды, ацетаты, татртраты, малеаты, цитраты, фумараты, сукцинаты, пальмоаты, метансульфонаты, бензоаты, салицилаты, бензолсульфонаты, аскорбаты, глицерофосфаты и кетоглютараты. Фармацевтически приемлемые сольваты могут быть гидратами или включать другие кристаллизационные растворители, такие как спирты. Дополнительно настоящее изобретение также включает соединения, которые отличаются только присутствием одного или более изотопно обогащенных атомов, например, при замене водорода дейтерием и тому подобного. Термин "субъект" или "пациент" охватывает млекопитающих и немлекопитающих. Примеры млекопитающих включают, не ограничиваясь этим, любого представителя класса млекопитающих: людей,приматов, кроме человека, таких как шимпанзе, и других человекообразных обезьян и обезьян других видов; сельскохозяйственных животных, таких как крупный рогатый скот, лошади, овцы, козы и свиньи; домашние животные, такие как кролики, собаки и коты; и лабораторных животных, включая грызунов,таких как крысы, мыши и морские свинки. Примеры немлекопитающих включают, не ограничиваясь этим, птиц, рыбу и тому подобное. В одном варианте воплощения представленных здесь способов и композиций млекопитающим является человек. Термины "лечить," "лечение" или "терапия", как здесь используется, включают облегчение, ослабление или улучшение симптомов болезни, расстройства или состояния, предупреждение дополнительных симптомов, ослабление или предупреждение основных причин появления данных симптомов, ингибирование данного заболевания, расстройства или состояния,например остановку развития данной болезни, расстройства или состояния, ослабление болезни, расстройства или состояния, вызывающих регресс данной болезни, расстройства или состояния, облегчение состояния, вызванного данной болезнью, расстройством или состоянием, или остановку проявления симптомов данной болезни, расстройства или состояния или профилактически, и/или терапевтически. Как здесь используется, "улучшение" касается положительной динамики заболевания или состояния или,по меньшей мере, частичного ослабления симптомов, связанных с болезнью или состоянием, и, как здесь используется, улучшение симптомов конкретной болезни, расстройства или состояния путем введения конкретного соединения или фармацевтической композиции касается любого снижения тяжести, задержки наступления, замедления развития или сокращения продолжительности, постоянного или временного, длительного или кратковременного, которые относятся к или ассоциируются с введением данного соединения или композиции. Термины "ингибирует", "ингибирующий" или "ингибитор" DHODH, как здесь используется, касаются ингибирования энзима DHODH. Термин "фармацевтически приемлемый", как здесь используется, касается материала, такого как носитель или разбавитель, который не ухудшает биологическую активность или свойства данного соединения и является относительно нетоксичным, т.е. данный материал вводится индивидууму, не вызывая нежелательных биологических эффектов или не взаимодействуя вредным образом с любым из компонентов данной композиции, в которую он входит. Термин "фармацевтическая композиция" касается смеси соединения, способного ингибироватьDHODH, как здесь описано, с другими химическими компонентами, такими как носители, стабилизаторы, разбавители, диспергаторы, суспендирующие агенты, загустители и/или наполнители. Фармацевтическая композиция облегчает введение данного соединения в организм. Соединения и фармацевтические композиции настоящего изобретения могут использоваться с применением различных схем введения,включая, но не ограничиваясь этим, внутривенную, пероральную, аэрозольную, парентеральную, глазную, пульмонарную и местную схемы введения. Термины "эффективное количество" или "терапевтически эффективное количество", как здесь используется, касаются достаточного количества используемого агента или соединения, которое ослабит в некоторой степени один или более симптомов данной болезни или состояния, которые подвергаются лечению. Результатом является ослабление и/или смягчение признаков, симптомов или причин болезни,или любого другого желательного изменения биологической системы. Например, "эффективное количество" для терапевтических применений является таким количеством композиции, содержащей соединение, способное ингибировать DHODH, как здесь описано, которое требуется для получения клинически значимого ослабления симптомов болезни. В некоторых вариантах воплощения подходящее "эффективное" количество в любом индивидуальном случае определяют с использованием методов, таких как исследование по увеличению дозировки. Термин "носитель", как здесь используется, касается относительно нетоксичных химических соединений или агентов, которые облегчают введение соединения в клетки или ткани. Термин "разбавитель" касается химических соединений, которые используются для разбавления необходимого соединения перед его доставкой. В некоторых вариантах воплощения разбавители используются для стабилизации соединений, так как они предоставляют более устойчивую среду. В качестве разбавителей используются соли, растворенные в буферных растворах (которые также служат для контроля или поддержания величины pH), включая, но не ограничиваясь этим, фосфатный буферный соле- 16024702 вой раствор. Как здесь используется, термин "иммунный" включает клетки иммунной системы и клетки, которые осуществляют функцию в иммунной реакции, такие как, но не ограничиваясь этим, T-клетки, Bклетки, лимфоциты, макрофаги, дендритные клетки, нейтрофилы, эозинофилы, базофилы, тучные клетки, плазмациты, лейкоциты, антиген-представляющие клетки и природные клетки-киллеры. Как здесь используется, термин "цитокин" или "цитокины" касается малых растворимых протеинов,секретируемых клетками, которые в некоторых вариантах воплощения изменяют поведение или свойства секретирующей клетки или другой клетки. Цитокины связываются с цитокиновыми рецепторами и служат пусковым механизмом внутри клетки, например пролиферации клетки, ее смерти или дифференцировки. Иллюстративные цитокины включают, не ограничиваясь этим, интерлейкины (например, IL-2, IL3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12, IL-13, IL-15, IL-16, IL-17, IL-18, IL-1, IL-1 и IL-1RA), гранулоцитарный колониестимулирующий фактор (G-CSF), гранулоцитарный макрофагальный колониестимулирующий фактор (GM-CSF), онкостатин М, эритропоэтин, фактор, ингибирующий лейкоз(LIF), интерфероны, В 7.1 (также известный как CD80), В 7.2 (также известный как В 70, CD86), члены семейства TNF (TNF-, TNF-, LT-, CD40 лиганд, Fas лиганд, CD27 лиганд, CD30 лиганд, 4-1BBL,Trail) и MIF. Соединения настоящего изобретения также полезны в комбинации (при совместном или последовательном использовании) с известными иммуномодуляторами и/или противовоспалительными агентами,полезными в лечении аутоиммунных заболеваний, иммунных и воспалительных заболеваний, деструктивных костных болезней, злокачественных неопластических заболеваний, расстройств, связанных с ангиогенезом, вирусных болезней и инфекционных болезней, такими как: анти-TNF-альфа моноклональные антитела, такие как инфликсимаб (Infliximab), цертолизумаб пегол (Certolizumab pegol), голимумаб (Golimumab), адалимумаб (Adalimumab) и AME-527, от фирмы Applied Molecular Evolution; антиметаболитные соединения, такие как мизорибин, циклофосфамид и азатиопирин(Azathiopirine); кальцинейрин (PP-2B) ингибиторы/ингибиторы INS экспрессии, такие как циклоспорин A, такролимус (Tacrolimus) и ISA-247 от фирмы Isotechnika; ингибиторы циклооксигеназы, такие как ацеклофенак (Aceclofenac), диклофенак (Diclofenac), целекоксиб (Celecoxib). Рофекоксиб (Rofecoxib), Эторикоксиб (Etoricoxib), вальдекоксиб (Valdecoxib), лумиракоксиб (Lumiracoxib), цимикоксиб (Cimicoxib) и LAS-34475 от лабораторий Laboratories Almirall, S.A.;TNF-альфа антагонисты, такие как этанерцепт (Etanercept), ленерцепт (Lenercept), онерцепт (Onercept) и пегсунерцепт (Pegsunercept);NF-каппаВ (NFKB) ингибиторы активации, такие как сульфасалазин (Sulfasalazine) и игуратимод(Iguratimod); антагонисты IL-1 рецептора, такие как анакинра (Anakinra) и AMG-719 от фирмы Amgen; ингибиторы дигидрофолатредуктазы (DHFR), такие как метотрексат (Methrotexate), аминоптерин(Aminopterin) и CH-1504 от фирмы Челси; ингибиторы инозин 5'-монофосфатдегидрогеназы (IMPDH), такие как мизорибин (Mizoribine), рибавирин (Ribavirin), тиазофурин (Tiazofurin), амитивир (Amitivir), микофенолат мофетил (Mycophenolatemofetil), рибамидин (Ribamidine) и меримеподиб (Merimepodib); глюкокортикоиды, такие как преднизолон (Prednisolone), метилпреднизолон (Methylprednisolone),дексаметазон (Dexamethasone), кортизол (Cortisol), гидрокортизон (Hydrocortisone), триамцинолон ацетонид (Triamcinolone acetonide), флюоцинолон ацетонид (Fluocinolone acetonide), флюоцинонид (Fluocinonide), клокортолон пивалат (Clocortolone pivalate), гидрокортизон ацепонат (Hydrocortisone aceponate), метилпреднизолон сулептанат (Methylprednisolone suleptanate); бетаметазон бутират пропионат, дельтакортизон (Deltacortisone), дельтадегидрокортизон (Deltadehydrocortisone), преднизон (Prednisone), дексаметазон натрий фосфат (Dexamethasone sodium phosphate),триамцинолон (Triamcinolone), бетаметазон валерат (Betamethasone valerate), бетаметазон, гидрокортизон натрий сукцинат, преднизолон натрий фосфат, гидрокортизон пробутат и дифлупреднат (Difluprednate); анти-CD20 моноклональные антитела, такие как ритуксимаб (Rituximab), офатумумабS1 P1 агонисты, такие как финголимод (Fingolimod), CS-0777 от Sankyo и R-3477 от Actelion, ONO4641 и KRP-203 от фирмы Novartis; анти-CD49 моноклональные антитела, такие как натализумаб (Natalizumab); интегриновые ингибиторы, такие как циленгитид (Cilengitide), фиратеграст (Firategrast), валатеграст(Valategrast) гидрохлорид, SB-273005, SB-683698 (все от Glaxo), HMR-1031 от фирмы Sanofi-Aventis, R1295 от Roche, BMS-587101 от BMS и CDP-323 от UCB Celltech; анти-CD88 моноклональные антитела, такие как экулизумаб (Eculizumab) и пекселизумаб (Pexelizumab);(w) анти IL-6 моноклональные антитела, такие как элсилимомаб (Elsilimomab), CNTO-328 от Centocor и VX-30 от Vaccinex; анти-CD152 моноклональные антитела, такие как ипилимумаб и тицилимумаб; слитые протеины, содержащие экстрацеллюлярный домен цитотоксичного T-лимфоцитассоциированного антигена человека 4 (CTLA-4), связанные с участками человеческого иммуноглобулина G1, такие как абатацепт (Abatacept); агенты, полезные в лечении костных заболеваний, такие как бисфофонаты, такие как динатрий тилудронат (Tiludronate), динатрий клодронат (Clodronate), динатрий памидронат, динатрий этидронат (Etidronate), ксидифон (Xydiphone) (KlNa соль), натрий алендронат (Alendronate), неридронат (Neridronate),диметил-APD, натриевая соль ольпадроновой кислоты, минодроновая кислота, апомин, ибандронат(lbandronate) натрий гидрат и натрий ризедронат (Risedronate); ингибиторы VEGF Try киназы, такие как октанатрий пегаптаниб (Pegaptanib), ваталаниб сукцинат; сорафениб (Sorafenib), вандетаниб (Vandetanib), сунитиниб малат, цедираниб (Cediranib), пазопаниб гидрохлорид и AE-941 от фирмы AEterna Zentaris; другие соединения, эффективные в аутоиммунных заболеваниях, такие как соли золота, гидроксиклорохинин, пенициламин, K-832, SMP114 и AD452; ингибиторы пурин-нуклеозид фосфорилазы, такие как фородезин (Forodesine) гидрохлорид, R-3421 от Albert Einstein College of Medicine, CI-972 и CI-1000 от фирмы Pfizer; анти-RANKL моноклональные антитела, такие как денозумаб (Denosumab); анти-CD25 моноклональные антитела, такие как инолимомаб (Inolimomab), дакликсимаб (Dacliximab), базиликсимаб (Basiliximab) и LMB-2 от Национального института рака (США); ингибиторы гистондеацетилазы (HDAC), такие как натрий дивалпроекс (Divalproex), ацетилдиналин, депсипептид, бутират натрия, фенилбутират натрия, вориностат (Vorinostat), MS-27-275 от Mitsui,вальпроевая кислота, пироксамид (Pyroxamide), трибутирин, PX-105684 от TopoTarget, MG-0103 от MethylGene, G2M-777 от TopoTarget и CG-781 от Celera; и анти-колониестимулирующий фактор (GM-CSF), моноклональные антитела, такие как KB-002 от фирмы KaloBios. Соединения данного изобретения используются для лечения ревматоидного артрита, псориатического артрита, анкилозирующего спондилоартрита, рассеянного склероза, грануломатоза Вегенера (Wegener), системной красной волчанки, псориаза и саркоидоза, и может быть полезно использовать их в комбинации с другими активными соединениями, которые, как известно, полезны в лечении таких заболеваний как ревматоидный артрит, псориатический артрит, анкилозирующий спондилоартрит, рассеянный склероз, грануломатоз Вегенера (Wegener), системная красная волчанка, псориаз и саркоидоз. Комбинации данного изобретения могут быть использованы в лечении заболеваний и/или расстройств, где,как известно, ингибирование DHODH дает благоприятный эффект. Таким образом, настоящая заявка охватывает способы лечения таких заболеваний, также как и использование комбинаций изобретения в производстве медикаментов для лечения этих заболеваний. Соединения настоящего изобретения также полезны в комбинации (при совместном или последовательном использовании) с известными противораковыми терапиями, такими как лучевая терапия, или с цитостатическими или цитотоксическими, или противораковыми агентами, такими как, например, но не ограничиваясь этим, ДНК интерактивные агенты, такие как цисплатин или доксорубицин; ингибиторы топоизомеразы II, такие как этопозид; ингибиторы топоизомеразы I, такие как CPT-11 или топотекан; агенты, взаимодействующие с тубулином, такие как паклитаксел, доцетаксел или эпотилоны (например,иксабепилон), как природные, так и синтетические; гормональные агенты, такие как тамоксифен; ингибиторы тимидилатсинтазы, такие как 5-флуороурацил; и анти-метаболиты, такие как метотрексат, другие ингибиторы тирозинкиназы, такие как пресса (Iressa) и OSI-774; ингибиторы ангиогенеза; EGFингибиторы; VEGF-ингибиторы; CDK-ингибиторы; SRC-ингибиторы; c-Kit-ингибиторы; Her1/2 ингибиторы и моноклональные антитела, направленные против рецепторов фактора роста, такие как эрбитукс (EGF) и герцептин (Her2), а также другие модуляторы протеинкиназы. В некоторых вариантах воплощения заболевания, расстройства или состояния, которые лечатся или предупреждаются с использованием раскрытых здесь соединений, которые способны ингибироватьDHODH, их композиций и представленных здесь способов для идентификации соединений, способных ингибировать DHODH, включают болезни, состояния или расстройства, включающие воспаление и/или те, что связаны с иммунной системой. Эти заболевания включают, не ограничиваясь этим, астму, хроническое обструктивное заболевание легких, ревматоидный артрит, воспалительное кишечное заболевание,гломерулонефрит, нейровоспалительные заболевания, такие как рассеянный склероз, и расстройства иммунной системы. Так, в некоторых вариантах воплощения ингибирование DHODH дает способ лечения иммунных и иммунно-связанных болезней, включая, например, хронические иммунные болезни/расстройства, острые иммунные болезни/расстройства, аутоиммунные и иммунодефицитные болезни/расстройства, включая воспаление, отторжения трансплантатов органов и болезнь трансплантат против хозяина, и измененные(например, гиперактивные) иммунные реакции. Примеры иммунных заболеваний включают псориаз, ревматоидный артрит, васкулит, воспалительное кишечное заболевание, дерматит, остеоартрит, астму, воспалительное мышечное заболевание, аллергический ринит, вагинит, интерстициальный цистит, склеродерму, остеопороз, экзему, отторжение трансплантата при аллогенной или ксеногенной трансплантации (органа, костного мозга, стволовых клеток и других клеток и тканей), отторжение трансплантата, болезнь трансплантат против хозяина, красную волчанку, воспалительное заболевание, диабет типа I, фиброз легких, дерматомиозит, синдром Шагрена, тироидит (например, зоб Хашимото (Hashimoto) и аутоиммунный тироидит), тяжелую миастению,аутоиммунную гемолитическую анемию, рассеянный склероз, муковисцидоз, хронический рецидивирующий гепатит, первичный билиарный цирроз, аллергический конъюктивит и атопический дерматит. В других вариантах воплощения раскрытые здесь соединения, которые способны ингибироватьDHODH, их композиции и представленные здесь способы для идентификации соединений, способных модулировать DHODH ингибиторы, используются в связи с лечением злокачественных образований,включая, но не ограничиваясь этим, злокачественные образования лимфоретикулярного происхождения,рак мочевого пузыря, рак молочной железы, рак ободочной кишки, эндометриальный рак, рак головы и шеи, рак легких, меланому, рак яичника, рак предстательной железы и ректальный рак. Считается, чтоDHODH играет важную роль в пролиферации клеток у раковых клеток. Описанная здесь следующая общая методология представляет способ и процесс получения и использования соединения настоящего изобретения и является, скорее, иллюстративной, а не ограничивающей. Для достижения и реализации целей данного изобретения может также быть проведена дополнительная модификация представленной методологии и разработаны дополнительные новые способы. Соответственно следует понимать, что здесь могут быть другие варианты, которые также отвечают сути и объему данного изобретения, как определено данной спецификацией. Общий способ получения соединений данного изобретения Соединения настоящего изобретения могут быть получены посредством следующих процессов. Если не указано иное, переменные (например, A, B, Cy, R1, R, Y, L1, X, X1, X2, X3 и L2), использующиеся в нижеприведенных формулах, как следует понимать, представляют группы, описанные выше в связи с формулами (I), (IA). Схема 1. Эта схема представляет способ получения соединения формулы (I), где A представляет собой замещенный или незамещенный моноциклический арил и замещенный или незамещенный моноциклический гетероарил, и другие переменные, такие как B, Cy, R1, R, Y, L1, X, X1, X2, X3 и L2, являются такими же самыми как описано выше относительно формулы (I). Схема 1 Соединение формулы (1), где Lg является отщепляемой группой, такой как гидроксил или галоген,может быть сцеплено с соединением формулы (2) в подходящем растворителе с использованием амидного связующего реагента, такого как DCC, или, необязательно, в присутствии подходящего основания с получением промежуточного соединения (например, R1 является COOEt), которое затем может быть превращено либо на протяжении одной, либо множества стадий в необходимое соединение формулы (I),например, для R1, являющейся СООН, где A представляет собой замещенный или незамещенный моноциклический арил или замещенный или незамещенный моноциклический гетероарил, и других переменных, таких как L, B, Cy, R2, R3, R4, m и n являются такими же самыми, как описано выше относительно формулы (I). Схема 2.- 19024702 Эта схема представляет способ получения соединения формулы (I), где R1 является COOH, L2 отсутствует, а другие переменные, такие как A, B, Cy, R1, R, Y, L1, X, X1, X2 и X3, являются такими же самыми, как описано выше относительно формулы (I). Схема 2 Соединение формулы (3), где Hal представляет галоген, может быть сцеплено с соединением формулы (4) в присутствии Pd(PPh3)4 и карбоната металла, такого как K2CO3 (сочетание Сузуки) с получением соединения формулы (2a). Соединение формулы (2a) может реагировать с подходящим соединением формулы (1a) в присутствии подходящего растворителя с получением необходимого соединения формулы (I), где R1 является COOH, L2 отсутствует, а другие переменные, такие как A, B, Cy, R, Y, L1, X, X1, X2 и X3, являются такими же самыми, как описано относительно формулы (I). Схема 3. Эта схема представляет способ получения соединения формулы (I), где R1 является COOH, L2 является -О-, а другие переменные, такие как A, B, Cy, R1, R, Y, Li, X, X1, X2, X3 и n, явлются такими же самыми, как описано выше относительно формулы (I). Схема 3 Соединение формулы (1a) может реагировать с подходящим соединением формулы (2a), где Hal представляет галоген, в присутствии подходящего растворителя с получением необходимого соединения формулы (5). Соединение формулы (5) может быть сцеплено с соединением формулы (6) в присутствии подходящего основания, такого как K2CO3, с получением необходимого соединения формулы (I), где R1 является COOH, L2 является -O-, а другие переменные, такие как A, B, Cy, R, Y, L1, X, X1, X2 и X3, являются такими же самыми, как описано выше относительно формулы (I). Схожие методологии с некоторыми модификациями, известными специалистам в данной области техники, могут быть использованы для синтеза соединения формулы (I) или/и (IA), где данные переменные, как следует понимать, представляют описанные выше группы относительно формулы (I) или/и (IA) с использованием подходящих промежуточных соединений и реагентов. Экспериментальная часть. Если не указано иное, обработка подразумевает распределение реакционной смеси между водной и органической фазами, указанными в скобках, разделение и осушивание над Na2SO4 органического слоя,и выпаривание растворителя с получением остатка. Если не отмечено иное, очистка осуществляется методом колоночной хроматографии с использованием силикагеля в качестве стационарной фазы и смеси петролейного эфира (кипящего при 60-80C), и этилацетата или дихлорметана, и метанола подходящей полярности как подвижных фаз. Комнатная температура касается окружающей температуры (25-28C). Общая процедура для сочетания Сузуки. К раствору арилбромида (1 экв.) в диоксане и воде (5:1) добавляли арилбороновую кислоту или пинаконовый эфир арилбороновой кислоты (1,3 экв.), тетракис(трифенилфосфин)палладий(0) - (0,08 экв.) и карбонат калия (3,3 экв.). Данную смесь дегазировали N2 в течение 30 мин и кипятили с обратным холодильником до исчезновения обоих исходных материалов, что контролировалось методом тонкослойной жидкостной хроматографии (TLC). Обработка (H2O/AcOEt) и очистка дали необходимый продукт. Промежуточные соединения 1, 4-27, 32-54, 56-63, 65-84 и 86-89 были получены с использованием общей процедуры-1.( ppm, CDCl3, 400 MHz): 9.50 (d, J=2.6, 1H), 8.53 (dd, J=2.6, 8.8, 1H), 7.91 (d, J=8.8, 1H), 7.69-7.68 (m, 1H),7.63 (d, J=7.8, 1H), 7.44 (t, J=7.9, 1H), 7.08-7.05 (m, 1H), 3.91 (s, 3H). Промежуточное соединение 3. 6-(3-Метоксифенил)пиридин-3-амин. Порошок железа (739 мг, 13,24 ммоль) и хлорид аммония (100 мг, 3,18 ммоль) добавляли к раствору промежуточного соединения 2 (610 мг, 2,65 ммоль) в EtOH/H2O (2:1, 15 мл) и данную смесь кипятили с обратным холодильником в течение 1 ч. Данную смесь фильтровали через целит и целит промывали этанолом. Обработка (H2O/AcOEt) и концентрирование объединенных слоев дали промежуточное соединение 3 (330 мг) в виде воскоподобного твердого вещества. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 8.00 (d,J=2.7, 1H), 7.61 (d, J=8.5, 1H), 7.47-7.45 (m, 2H), 7.27 (t, J=8, 1H), 6.97 (dd, J=2.8, 8.5, 1H), 6.83-6.81 (m,1H), 5.46 (s, 2H), 3.78 (s, 3H). Промежуточное соединение 4. 3'-Этокси-3-фторбифенил-4-амин. Данное титульное соединение (1,34 г) получали из 2-фтор-4-броманилина (2,5 г, 13,1 ммоль) и 3 этоксифенилбороновой кислоты (2,8 г, 17,0T ммоль) в виде бледно-желтой жидкости. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.38-7.20 (m, 3H), 7.10 (d, J=7.9, 1H), 7.07-7.05 (m, 1H), 6.83-6.76 (m, 2 Н), 5.24 (s,2 Н), 4.06 (q, J=7, 2 Н), 1.32 (t, J=7, 3H). Промежуточное соединение 5. 3'-Этокси-3,5-дифторбифенил-4-амин. Титульное соединение (0,219 г) получали из 2,6-дифтор-4-броманилина (0,5 г, 2,4 ммоль) и 3 этоксифенилбороновой кислоты (0,517 г, 3,12 ммоль) в виде бледно-желтой жидкости. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.30-7.24 (m, 3H), 7.14 (d, J=7.9, 1H), 7.11 (s, 1H), 6.82 (dd, J=2.1, 8.1, 1H), 5.31 (s,2H), 4.07 (q, J=7, 2H), 1.32 (t, J=7, 3H). Промежуточное соединение 6. 2'-Хлор-3,5-дифторбифенил-4-амин. Титульное соединение (0,140 г) получали из 2,6-дифтор-4-бром анилина (0,22 г, 1,06 ммоль) и 2 хлорфенилбороновой кислоты (0,21 г, 1,38 ммоль) в виде белого твердого вещества. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.52-7.50 (m, 1H), 7.40-7.35 (m, 3H), 7.00 (d, J=2.1, 7.6, 2H), 5.39 (s, 2H). Промежуточное соединение 7. 3,5-Дифторбифенил-4-амин. Титульное соединение (0,401 г) получали из 2,6-дифтор-4-броманилина (0,5 г, 2,4 ммоль) и фенилбороновой кислоты (0,38 г, 3,12 ммоль) в виде белого твердого вещества. 1H-NMR ( ppm, ДМСО-d6, 400MHz): 7.60 (d, J=7.4, 2H), 7.38 (t, J=7.5, 2H), 7.30-7.25 (m, 3H), 5.33 (s, 2H). Промежуточное соединение 8. 3,5-Дифтор-3'-(трифторметокси)бифенил-4-амин. Титульное соединение (0,812 г) получали из 2,6-дифтор-4-броманилина (1 г, 4,8 ммоль) и 3(трифторметокси)фенилбороновой кислоты (1,28 г, 6,24 ммоль) в виде бесцветной жидкости. Промежуточное соединение 9. 3'-(Бензилокси)-3,5-дифторбифенил-4-амин. Титульное соединение (0,143 г) получали из 2,6-дифтор-4-броманилина (0,3 г, 1,4 ммоль) и 3(бензилокси)фенилбороновой кислоты (0,426 г, 1,8 ммоль) в виде бесцветной жидкости. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.49-7.44 (m, 2 Н), 7.39 (t, J=7.2, 2H), 7.35-7.26 (m, 4H), 7.24 (s, 1H), 7.18 (d, J=7.8,1H), 6.91 (dd, J=1.9, 8.0, 1H), 5.33 (s, 2H), 5.16 (s, 2H). Промежуточное соединение 10. 3-Хлор-3'-этокси-5-фторбифенил-4-амин. Титульное соединение (0,360 г) получали из 4-бром-2-хлор-6-фторанилина (0,5 г, 2,0 ммоль) и 3 этоксифенилбороновой кислоты (0,441 г, 2,65 ммоль) в виде желтой жидкости. 1H-NMR ( ppm, ДМСОd6, 400 MHz): 7.43-7.38 (m, 2 Н), 7.27 (t, J=7.9, 1H), 7.14 (d, J=7.9, 1H), 7.10 (s, 1H), 6.82 (dd, J=2.1, 8.1, 1H),5.51 (s, 2H), 4.07 (q, J=7, 2H), 1.32 (t, J=7, 3H). Промежуточное соединение 11. 3,5-Дихлор-3'-метоксибифенил-4-амин. Титульное соединение (0,550 г) получали из 2,6-дихлор-4-броманилина (0,5 г, 2,0 ммоль) и 3 метоксифенилбороновой кислоты (0,409 г, 2,69 ммоль) в виде белого твердого вещества. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.58 (s, 2 Н), 7.29 (t, J=7.8, 1H), 7.18-7.10 (m, 2H), 6.85 (dd, J=2, 8.1, 1H), 5.63 (s, 2H),3.81 (s, 3H). Промежуточное соединение 12. 3-Хлор-5-фтор-3'-пропоксибифенил-4-амин. Титульное соединение (0,273 г) получали из 4-бром-2-хлор-6-фторанилина (0,5 г, 2,2 ммоль) и 3 пропоксифенилбороновой кислоты (0,521 г, 2,9 ммоль) в виде желтой жидкости. 1H-NMR ( ppm, ДМСОd6, 400 MHz): 7.44-7.39 (m, 3H), 7.27 (t, J=7.9, 1H), 7.16-7.10 (m, 2H), 5.51 (s, 2H), 3.97 (t, J=6.5, 2H), 1.751.70 (m, 2H), 0.98 (t, J=7.9, 3H). Промежуточное соединение 13. 3-Хлор-2',5-дифторбифенил-4-амин. Титульное соединение (0, 392 г) получали из 4-бром-2-хлор-6-фторанилина (0,5 г, 2,2 ммоль) и 2 фторфенилбороновой кислоты (0,363 г, 2,6 ммоль) в виде бледно-желтой жидкости. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.51 (td, J=1.7, 7.8, 1H), 7.38-7.32 (m, 1H), 7.28 (s, 2H), 7.27-7.22 (m, 2H), 5.62 (s, 2H). Промежуточное соединение 14. 3,5-Дихлор-3'-этоксибифенил-4-амин. Титульное соединение (0,550 г) получали из 4-бром-2,6-дихлоранилина (0,5 г, 2,2 ммоль) и 3 этоксифенилбороновой кислоты (0,447 г, 2,7 ммоль) в виде желтой жидкости, которая имела чистоту приблизительно 70%, как установлено по данным 1H-NMR. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 7.56 (s,2H), 7.28 (s, 1H), 7.16-7.08 (m, 2H), 6.83 (dd, J=2, 8.1, 1H), 5.62 (s, 2H), 4.10 (q, J=7, 2H), 1.32 (t, J=7, 3H). Промежуточное соединение 15. 3-Фтор-3'-(трифторметокси)бифенил-4-амин. Титульное соединение (0,5 г) получали из 4-бром-2-фторанилина (1 г, 5,3 ммоль) и 3(трифторметокси)фенилбороновой кислоты (1,4 г, 6,8 ммоль) в виде желтой жидкости. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.62 (d, J=8, 1H), 7.53 (s, 1H), 7.48 (t, J=8, 1H), 7.42 (dd, J=2, 9.1, 1H), 7.28 (dd, J=2,8.3, 1H), 7.23 (d, J=11, 1H), 6.82 (t, J=8.5, 1H), 5.40 (s, 2H). Промежуточное соединение 16. 2'-Фтор-3-(трифторметокси)бифенил-4-амин. Титульное соединение (0,294 г) получали из 2-трифторметокси-4-бром анилина (0,5 г, 1,9 ммоль) и 2-фторфенилбороновой кислоты (0,345 г, 2,5 ммоль) в виде желтой жидкости. 1H-NMR ( ppm, ДМСО-d6,400 MHz): 7.47 (td, J=1.2, 4.7, 1H), 7.33-7.20 (m, 5H), 6.89 (d, J=8.8, 1H), 5.62 (s, 2H). Промежуточное соединение 17. 3,5-Дихлор-2'-фторбифенил-4-амин. Титульное соединение (0,367 г) получали из 4-бром-2,6-дихлор анилина (0,5 г, 1,9 ммоль) и 2 фторфенилбороновой кислоты (0,363 г, 2,6 ммоль) в виде белого твердого вещества. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.50 (t, J=6.3, 1H), 7.43 (s, 2H), 7.39-7.31 (m, 1H), 7.29-7.21 (m, 2H), 5.73 (s, 2H). Промежуточное соединение 18. 3,5-Дифтор-3'-изопропоксибифенил-4-амин. Титульное соединение (0,34 г) получали из 4-бром-2,6-дифторанилина (0,5 г, 2,4 ммоль) и 3 изопропоксифенилбороновой кислоты (0,337 г, 3,1 ммоль) в виде красной жидкости. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.30-7.22 (m, 3H), 7.16-7.07 (m, 2H), 6.89 (dd, J=2.3, 8.1, 1H), 5.32 (s, 2H), 4.68 (septet,J=6, 1H), 1.26 (d, J=6, 6H). Промежуточное соединение 19. 3,5-Дифтор-3'-пропоксибифенил-4-амин. Титульное соединение (0,3 г) получали из 4-бром-2,6-дифторанилина (0,5 г, 2,4 ммоль) и 3 пропоксифенилбороновой кислоты (0,337 г, 3,1 ммоль) в виде красной жидкости. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.30-7.24 (m, 3H), 7.18-7.10 (m, 2H), 6.86-6.80 (m, 1H), 5.31 (s, 2 Н), 3.97 (t, J=6.5,2H), 1.75-1.65 (m, 2H), 0.98 (t, J=7.4, 3H). Промежуточное соединение 20. 2',3-Дихлор-5-фторбифенил-4-амин. Титульное соединение (0,260 г) получали из 4-бром-2-хлор-6-фторанилина (0,5 г, 2,4 ммоль) и 2 хлорфенилбороновой кислоты (0,453 г, 2,9 ммоль) в виде белого твердого вещества. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.60 (d, J=7.3, 1H), 7.42-7.31 (m, 3H), 7.18-7.11 (m, 2H), 5.6 (s, 2H). Промежуточное соединение 21. 3'-Бутокси-3-хлор-5-фторбифенил-4-амин. Титульное соединение (0,190 г) получали из 4-бром-2-хлор-6-фторанилина (0,2 г, 0,89 ммоль) и 3 бутоксифенилбороновой кислоты (0,224 г, 1,16 ммоль) в виде желтого твердого вещества. 1H-NMR ((s, 2H), 4.01 (t, J=5.3, 2H), 1.72-1.65 (m, 2H), 1.50-1.41 (m, 2H), 0.93 (t, J=7.4, 3H). Промежуточное соединение 22. 3-Хлор-5-фтор-3'-изобутоксибифенил-4-амин. Титульное соединение (0,180 г) получали из 4-бром-2-хлор-6-фторанилина (0,2 г, 0,89 ммоль) и 3 изобутоксифенилбороновой кислоты (0,224 г, 1,16 ммоль) в виде желтого твердого вещества. 1H-NMR ((s, 2H), 3.83 (d, J=6.5, 2H), 2.07-1.97 (m, 1H), 1.00 (d, J=6.7, 6H). Промежуточное соединение 23. 2',3,5-Трифторбифенил-4-амин. Титульное соединение (0,492 г) получали из 4-бром-2,6-дифторанилина (0,5 г, 2,4 ммоль) и 2 фторфенилбороновой кислоты (0,436 г, 3,12 ммоль) в виде желтой жидкости. 1H-NMR ( ppm, ДМСО-d6,400 MHz): 7.51 (td, J=1.5, 7.9, 1H), 7.38-7.31 (m, 1H), 7.29-721 (m, 2H), 7.14 (d, J=8.6, 2H), 5.44 (s, 2H). Промежуточное соединение 24. 2',3,5-Трихлорбифенил-4-амин. Титульное соединение (0,4 г) получали из 4-бром-2,6-дихлоранилина (0,5 г, 2,1 ммоль) и 2 хлорфенилбороновой кислоты (0,421 г, 2,7 ммоль) в виде белого твердого вещества. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 7.55-7.50 (m, 1H), 7.40-7.32 (m, 3H), 7.29 (s, 2H), 5.72 (s, 2H). Промежуточное соединение 25. 3,5-Дифтор-3'-изобутоксибифенил-4-амин. Титульное соединение (0,16 г) получали из 4-бром-2,6-дифторанилина (0,2 г, 0,96 ммоль) и 3 изобутоксифенилбороновой кислоты (0,242 г, 1,2 ммоль) в виде желтой жидкости. Промежуточное соединение 26. 3,5-Дифтор-3'-бутоксибифенил-4-амин. Титульное соединение (0,104 г) получали из 4-бром-2,6-дифторанилина (0,2 г, 0,96 ммоль) и 3 бутоксифенилбороновой кислоты (0,242 г, 1,2 ммоль) в виде бесцветной жидкости.(s, 2H). Промежуточное соединение 28. 5-(Бензилокси)-1,3-дифтор-2-нитробензол. Карбонат калия (544 мг, 3,94 ммоль) и бензиловый спирт (0,3 мл, 2,8 ммоль) добавляли к раствору 2,4,6-трифторнитробензола (500 мг, 2,8 ммоль) в ДМФ (5 мл). Эту смесь перемешивали при комнатной температуре в течение ночи. Обработка (EtOAc/H2O) дала титульное соединение (521 мг) в виде желтой жидкости, которая использовалась на следующей стадии без дополнительной очистки. Промежуточное соединение 29. 4-(Бензилокси)-2,6-дифторанилин. Порошок железа (502 мг, 9 ммоль) и хлорид аммония (192 мг, 3,6 ммоль) добавляли к раствору промежуточного соединения 28 (500 мг, 1,8 ммоль) в EtOH/H2O (2:1, 15 мл) и данную смесь кипятили с обратным холодильником в течение 2 ч. Смесь фильтровали через целит и целит промывали этанолом. Обработка (H2O/AcOEt) объединенных фильтратов и очистка дала титульное соединение (24 мг) в виде бесцветной жидкости. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 7.42-7.36 (m, 3H), 7.35-7.28 (m, 2H), 6.68(dd, J=1.6, 8.8, 2H), 4.97 (s, 2H), 4.64 (s, 2H). Промежуточное соединение 30. 1-Бром-3-(циклопентилокси)бензол. Карбонат калия (400 мг, 2,8 ммоль) добавляли к 3-бромфенолу (500 мг, 2,8 ммоль), растворенному в ацетонитриле, и данную смесь кипятили с обратным холодильником в течение 1 ч и охлаждали до комнатной температуры. Добавляли циклопентилбромид (430 мг, 2,8 ммоль) и смесь вновь кипятили с обратным холодильником в течение ночи. Обработка (H2O/EtOAc) и очистка дала титульное соединение в виде бледно-желтой жидкости. 1H-NMR ( ppm, CDCl3, 400 MHz): 7.11 (t, J=8.3, 1H), 7.05-7.00 (m, 2H),6.82-6.76 (m, 1H), 4.76-4.68 (m, 1H), 1.94-1.73 (m, 6H), 1.65-1.54 (m, 2H). Промежуточное соединение 31. 2-(3-(Циклопентилокси)фенил)-4,4,5,5-тетраметил-1,3,2 диоксаборолан. Смесь промежуточного соединения 30 (335 мг, 1,4 ммоль), бис-(пинаколато)диборона (351 мг, 1,4 ммоль) и ацетата калия (450 мг, 4,6 ммоль) в диоксане дегазировали N2 в течение 30 мин. Добавляли тетракис(трифенилфосфин)палладий (0) (128 мг, 0,11 ммоль) и дегазирование вновь продолжали еще в течение 15 мин. Эту смесь кипятили с обратным холодильником в течение ночи. После завершения реакции обработка (H2O/EtOAc) и колоночная очистка дали титульное соединение (165 мг) в виде желтой жидкости. Промежуточное соединение 32. 3'-(Циклопентилокси)-3,5-дифторбифенил-4-амин. Титульное соединение (22 мг) получали из 4-бром-2,6-дифторанилина (165 мг, 0,6 ммоль) и промежуточного соединения 31 (120 мг, 0,6 ммоль) в виде бледно-желтой жидкости. 1H-NMR ( ppm, ДМСОd6, 400 MHz): 7.29-7.22 (m, 3H), 7.12 (d, J=8, 1H), 7.06 (s, 1H), 6.82-6.76 (m, 1H), 5.30 (s, 2H), 4.96-4.88 (m,1H), 1.96-1.82 (m, 2H), 1.75-1.65 (m, 4H), 1.60-1.51 (m, 2H). Промежуточное соединение 33. 3-Хлор-3'-(циклопентилокси)-5-фторбифенил-4-амин. Титульное соединение (450 мг) получали из 4-бром-2-хлор-6-фторанилина (600 мг, 2,7 ммоль) и промежуточного соединения 31 (1 г, 3,4 ммоль) в виде желтой жидкости. 1H-NMR ( ppm, ДМСО-d6, 400MHz): 7.42-7.36 (m, 2H), 7.26 (t, J=8, 1H), 7.11 (d, J=7.8, 1H), 7.08-7.05 (m, 1H), 6.80 (dd, J=2.3, 8.1, 1H),5.49 (s, 2H), 4.92-4.84 (m, 1H), 1.97-1.87 (m, 2H), 1.77-1.62 (m, 4H), 1.60-1.50 (m, 2H). Промежуточное соединение 34. 3'-(Дифторметокси)-3,5-дифторбифенил-4-амин. Титульное соединение (144 мг) получали из 4-бром-2,6-дифторанилина (200 мг, 0,96 ммоль) и 3(дифторметокси)фенилбороновой кислоты (234 мг, 1,25 ммоль) в виде белого твердого вещества. 1HNMR ( ppm, ДМСО-d6, 400 MHz): 7.49 (d, J=7.9, 1H), 7.43-7.39 (m, 2H), 7.38-7.30 (m, 2H), 7.32 (t, J=74,1H), 7.06 (dd, J=1.8, 7.9, 1H), 5.42 (s, 2H). Промежуточное соединение 35. 2-[3'-(Дифторметокси)-3,5-дифторбифенил-4-илкарбамоил]бензойная кислота. Титульное соединение (155 мг) получали из 4-бром-2-хлор-6-фторанилина (89 мг, 1,16 ммоль) и 3(дифторметокси)фенилбороновой кислоты (217 мг, 1,16 ммоль) в виде белого твердого вещества. 1HNMR ( ppm, ДМСО-d6, 400 MHz): 7.52-7.47 (m, 3H), 7.46-7.44 (m, 1H), 7.43-7.40 (m, 2H), 7.32 (t, J=74.2,1H), 5.60 (s, 2H). Промежуточное соединение 36. 2'-Хлор-3,5-дифтор-5'-метоксибифенил-4-амин. Титульное соединение (97 мг) получали из 4-бром-2,6-дифторанилина (100 мг, 0,48 ммоль) и 2 хлор-5-метоксифенилбороновой кислоты (116 мг, 0,62 ммоль) в виде желтого твердого вещества. 1HNMR ( ppm, ДМСО-d6, 400 MHz): 7.40 (d, J=9.6, 1H), 7.02 (d, J=7.7, 2H), 6.92 (s, 2H), 5.39 (s, 2H), 3.77 (s,3H). Промежуточное соединение 37. 3,3',5-Трифтор-5'-метоксибифенил-4-амин. Титульное соединение (51 мг) получали из 4-бром-2,6-дифторанилина (100 мг, 0,48 ммоль) и 3 фтор-5-метоксифенилбороновой кислоты (106 мг, 0,62 ммоль) в виде желтого твердого вещества. 1H- 23024702NMR ( ppm, ДМСО-d6, 400 MHz): 7.35 (dd, J=2.1, 8.1, 2H), 7.06 (d, J=10.2, 1H), 7.01 (s, 1H), 6.71 (dd, J=2,8.8, 1H), 5.42 (s, 2H), 3.81 (s, 3H). Промежуточное соединение 38. 4-(Бензо[d][1,3]диоксол-5-ил)-2,6-дифторанилин. Титульное соединение (143 мг) получали из 4-бром-2,6-дифторанилина (200 мг, 0,96 ммоль) и бензо[d][1,3]диоксол-5-илбороновой кислоты (207 мг, 1,25 ммоль) в виде белого твердого вещества. 1HNMR ( ppm, ДМСО-d6, 400 MHz): 7.23-7.18 (m, 3H), 7.08 (dd, J=1.8, 8.2, 1H), 6.91 (d, J=8.1, 1H), 6.01 (s,2H), 5.24 (s, 2H). Промежуточное соединение 39. 4-(Бензо[d][1,3]диоксол-5-ил)-2-хлор-6-фторанилин. Титульное соединение (143 мг) получали из 4-бром-2-хлор-6-фторанилина (200 мг, 0,89 ммоль) и бензо[d][1,3]диоксол-5-илбороновой кислоты (192 мг, 1,16 ммоль) в виде белого твердого вещества. 1HNMR ( ppm, ДМСО-d6, 400 MHz): 7.36-7.30 (m, 2H), 7.20 (d, J=1.7, 1H), 7.06 (dd, J=1.4, 8.1, 1H), 6.91 (d,J=8.1, 1H), 6.01 (s, 2H), 5.42 (s, 2H). Промежуточное соединение 40. 3,5-Дифтор-3',4'-диметоксибифенил-4-амин. Титульное соединение (39 мг) получали из 4-бром-2,6-дифторанилина (100 мг, 0,48 ммоль) и 3,4 диметоксифенилбороновой кислоты (113 мг, 0,62 ммоль) в виде бледно-желтого твердого вещества. 1HNMR ( ppm, ДМСО-d6, 400 MHz): 7.25 (dd, J=2, 8.3, 2H), 7.18-7.10 (m, 2H), 6.94 (d, J=8.4, 1H), 5.21 (s,2H), 3.81 (s, 3H), 3.75 (s, 3H). Промежуточное соединение 41. 3-Хлор-3',5-дифтор-5'-метоксибифенил-4-амин. Титульное соединение (71 мг) получали из 4-бром-2-хлор-6-фторанилина (100 мг, 0,44 ммоль) и 3 фтор-5-метоксифенилбороновой кислоты (97 мг, 0,57 ммоль) в виде бледно-желтого твердого вещества. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 7.51-7.45 (m, 2H), 7.05 (d, J=10.3, 1H), 7.00 (s, 1H), 6.73 (dd, J=2.1,4.2, 1H), 5.60 (s, 2H), 3.81 (s, 3H). Промежуточное соединение 42. 3,3'-Дихлор-5-фтор-5'-метоксибифенил-4-амин. Титульное соединение (41 мг) получали из 4-бром-2-хлор-6-фторанилина (100 мг, 0,44 ммоль) и 3 хлор-5-метоксифенилбороновой кислоты (107 мг, 0,57 ммоль) в виде бледно-желтого твердого вещества. Промежуточное соединение 43. 4-(2,3-Дигидробензофуран-5-ил)-2,6-дифторанилин. Титульное соединение (182 мг) получали из 4-бром-2,6-дифторанилина (200 мг, 0,96 ммоль) и 2,3 дигидробензофуран-5-илбороновой кислоты (204 мг, 1,25 ммоль) в виде белого твердого вещества. 1HNMR ( ppm, ДМСО-d6, 400 MHz): 7.46 (s, 1H), 7.30 (dd, J=1.8, 8.3, 1H), 7.16 (dd, J=2.1, 8.2, 2H), 6.75 (d,J=8.3, 1H), 5.18 (s, 2H), 4.52 (t, J=8.7, 2H), 3.18 (t, J=8.5, 2H). Промежуточное соединение 44. 2-Хлор-4-(2,3-дигидробензофуран-5-ил)-6-фторанилин. Титульное соединение (86 мг) получали из 4-бром-2-хлор-6-фторанилина (200 мг, 0,89 ммоль) и 2,3 дигидробензофуран-5-илбороновой кислоты (189 мг, 1,16 ммоль) в виде бледно-желтого твердого вещества. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 7.46 (s, 1H), 7.33-7.25 (m, 3H), 6.75 (d, J=8.3, 1H), 5.36 (s, 2H),4.52 (t, J=8.7, 2H), 3.18 (t, J=8.6, 2H). Промежуточное соединение 45. 4-(1,3-Диметил-1 Н-индазол-5-ил)-2,6-дифторанилин. Ацетат калия (0,344 г, 3,51 ммоль) и бис-(пинаколато)диборон (351 мг, 1,4 ммоль) добавляли к раствору 5-бром-1,3-диметил-1H-индазола (240 мг, 1,06 ммоль) в диоксане (10 мл) и смесь дегазировали азотом в течение 30 мин. Добавляли тетракис(трифенилфосфин) палладий(0) и дегазирование продолжали еще в течение 30 мин. Реакционную смесь кипятили с обратным холодильником в течение 2 ч. После завершения данной реакции обработка (AcOEt/H2O) с последующей колоночной очисткой дали 1,3 диметил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-индазол (85 мг) в виде белого твердого вещества. Титульное соединение (26 мг) получали из 4-бром-2,6-дифторанилина (50 мг, 0,24 ммоль) и 1,3 диметил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-индазола (85 мг, 0,31 ммоль) в виде белого твердого вещества. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 7.93 (s, 1H), 7.66 (dd, J=1.5, 8.8, 1H), 7.55 (d,J=8.8, 1H), 7.33 (dd, J=2, 8.2, 2H), 5.22 (s, 2H), 3.94 (s, 3H), 2.49 (s, 3H). Промежуточное соединение 46. 3'-Хлор-3,5-дифтор-5'-метоксибифенил-4-амин. Титульное соединение (39 мг) получали из 4-бром-2,6-дифторанилина (100 мг, 0,48 ммоль) и 3 хлор-5-метоксифенилбороновой кислоты (116 мг, 0,62 ммоль) в виде бледно-желтого твердого вещества. 1 Промежуточное соединение 50. 4'-Хлор-3,5-дифтор-3'-метоксибифенил-4-амин. Титульное соединение (81 мг) получали из 4-бром-2,6-дифторанилина (100 мг, 0,48 ммоль) и 4 хлор-5-метоксифенилбороновой кислоты (116 мг, 0,62 ммоль) в виде белого твердого вещества. Промежуточное соединение 51. 3,4'-Дихлор-5-фтор-3'-метоксибифенил-4-амин. Титульное соединение (82 мг) получали из 4-бром-2-хлор-6-фторанилина (100 мг, 0,44 ммоль) и 4 хлор-5-метоксифенилбороновой кислоты (107 мг, 0,62 ммоль) в виде бледно-желтого твердого вещества. Промежуточное соединение 52. 3-Хлор-2',5-дифтор-5'-метоксибифенил-4-амин. Титульное соединение (70 мг) получали из 4-бром-2-хлор-6-фторанилина (100 мг, 0,44 ммоль) и 2 фтор-5-метоксифенилбороновой кислоты (98 мг, 0,58 ммоль) в виде белого твердого вещества. 1H-NMR( ppm, ДМСО-d6, 400 MHz): 7.30-7.24 (m, 2H), 7.17 (t, J=9.1, 1H), 7.02-6.97 (m, 1H), 6.90-6.84 (m, 1H),5.61 (s, 2H), 3.77 (s, 3H). Промежуточное соединение 53. 3,4',5-Трифтор-3'-метоксибифенил-4-амин. Титульное соединение (480 мг) получали из 4-бром-2,6-дифторанилина (200 мг, 0,96 ммоль) и 4 фтор-5-метоксифенилбороновой кислоты (210 мг, 1,24 ммоль) в виде белого твердого вещества. 1H-NMR( ppm, ДМСО-d6, 400 MHz): 7.39-7.29 (m, 3H), 7.21-7.12 (m, 2H), 5.33 (s, 2H), 3.90 (s, 3H). Промежуточное соединение 54. 2,6-Дифтор-4-(3-метил-1 Н-индол-5-ил)анилин. Титульное соединение (68 мг) получали из 4-бром-2,6-дифторанилина (100 мг, 0,48 ммоль) и 3 метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-индола (160 мг, 0,62 ммоль) в виде белого твердого вещества. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 10.71 (s, 1H), 7.67 (s, 1H), 7.33-7.29 (m, 2H),7.28-7.21 (m, 2H), 7.09 (s, 1H), 5.12 (s, 2H), 2.27 (s, 3H). Промежуточное соединение 55. 2,6-Дифтор-4-(3-метил-1 Н-индазол-5-ил)анилин. Следуя общей процедуре-1, трет-бутил 5-(4-амино-3,5-дифторфенил)-3-метил-1H-индазол-1 карбоксилат (106 мг) был получен из 4-бром-2,6-дифторанилина (250 мг, 1,2 ммоль) и трет-бутил 3 метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-индазол-1-карбоксилата (559 мг, 1,56 ммоль) в виде белого твердого вещества. трет-Бутил 5-(4-амино-3,5-дифторфенил)-3-метил-1H-индазол-1 карбоксилат (205 мг) растворяли в дихлорметане (4 мл), добавляли трифторуксусную кислоту (0,8 мл) и перемешивали при комнатной температуре в течение 4 ч. Растворитель удаляли и остаток подвергали совместному выпариванию 4 раза с дихлорметаном. Полученное твердое вещество осушивали под высоким вакуумом с получением титульного соединения (243 мг) в виде белого твердого вещества. 1H-NMR(dd, J=2, 8.2, 2H), 5.22 (s, 2H), 2.50 (s, 3H). Промежуточное соединение 56. 3-Хлор-3'-этил-5-фторбифенил-4-амин. Титульное соединение (83 мг) было получено из 4-бром-2,6-дифторанилина (100 мг, 0,48 ммоль) и 3-этиленфенилбороновой кислоты (86 мг, 0,57 ммоль) в виде желтой жидкости. Промежуточное соединение 57. 3-Хлор-3'-этокси-2',5-дифторбифенил-4-амин. Титульное соединение (65 мг) получали из 4-бром-2-хлор-6-фторанилина (120 мг, 0,53 ммоль) и 3 этокси-2-фторфенилбороновой кислоты (120 мг, 0,69 ммоль) в виде бесцветной жидкости. Промежуточное соединение 58. 2-Хлор-4-(2,3-дигидробензо[b][1,4]диоксин-6-ил)-6-фторанилин. Титульное соединение (68 мг) получали из 4-бром-2,6-дифторанилина (100 мг, 0,48 ммоль) и 2,3 дигидробензо[b][1,4]диоксин-6-илбороновой кислоты (160 мг, 0,62 ммоль) в виде белого твердого вещества. Промежуточное соединение 59. 3-Хлор-5-фтор-3'-(2,2,2-трифторэтокси)бифенил-4-амин. Титульное соединение (85 мг) получали из 4-бром-2-хлор-6-фторанилина (100 мг, 0,44 ммоль) и 3(2,2,2-трифторэтокси)фенилбороновой кислоты (127 мг, 0,57 ммоль) в виде белого твердого вещества. 1 Промежуточное соединение 63. 3'-Циклопропокси-3,5-дифторбифенил-4-амин. Титульное соединение (170 мг) получали из 4-бром-2,6-дифторанилина (1,2 г, 5,76 ммоль) и 2-(3 циклопропоксифенил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан (1,5 г, 5,76 ммоль) в виде желтой жидкости. Промежуточное соединение 64. 3-Этил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-индол. 5-Бромизатин (5 г, 22,12 ммоль) добавляли по каплям к этилмагний йодиду, полученному из этилйодида (14 мл, 176,96 ммоль) и магния (8,6 г, 176,96 ммоль) в Et2O (50 мл), и перемешивали при комнатной температуре в течение ночи. Обработка (EtOAc/H2O) после добавления водн. 10% раствораNH4Cl и очистка дала 5-бром-3-этил-3-гидроксииндолин-2-он (1 г). К раствору этого промежуточного соединения (1 г, 3,93 ммоль) в ТГФ (40 мл) добавляли 2 M раствор боран-диметилсульфида в ТГФ (10 мл, 19,65 ммоль) и перемешивали при комнатной температуре в течение 3 ч. Обработка (EtOAc/H2O) и очистка дала 5-бром-3-этилиндол (800 мг). К раствору 5-бром-3-этил индола (800 мг, 3,57 ммоль) в диоксане (10 мл) добавляли бис-(пинаколато)диборон (1,078 г, 4,64 ммоль), ацетат калия (1,15 г, 11,78 ммоль) и [1,1'-бис-(дифенилфосфино)ферроцен]дихлор палладий(II).CH2Cl2, дегазировали в течение 30 мин и кипятили с обратным холодильником в течение ночи. Обработка с последующей очисткой дала титульное соединение (800 мг) в виде беловатого твердого вещества. Промежуточное соединение 65. 4-(3-Этил-1 Н-индол-5-ил)-2,6-дифторанилин. Титульное соединение (220 мг) получали из 4-бром-2,6-дифторанилина (662 мг, 2,57 ммоль) и промежуточного соединения 64 (440 мг, 1,78 ммоль) в виде желтой жидкости. 1H-NMR ( ppm, ДМСО-d6,400 MHz): 10.74 (s, 1H), 7.69 (s, 1H), 7.33-7.29 (m, 2H), 7.23 (dd, J=1.8, 8.3, 2H), 7.09 (s, 1H), 5.12 (s, 2H),2.73 (q, J=7.5, 2H), 1.27 (q, J=7.5, 3H). Промежуточное соединение 66. 3'-(Этилтио)-2,3,5,6-тетрафторбифенил-4-амин. Титульное соединение (280 мг) получали из 4-бром-2,3,5,6-тетрафторанилина (300 мг, 1,22 ммоль) и 3-(этилтио)фенилбороновой кислоты (291 мг, 1,6 ммоль) в виде бесцветной жидкости. Промежуточное соединение 67. 2'-Хлор-2-фтор-5'-метоксибифенил-4-амин. Титульное соединение (280 мг) получали из 4-бром-3-фторанилина (227 мг, 1,2 ммоль) и 2-хлор-5 метоксифенилбороновой кислоты (290 мг, 1,6 ммоль) в виде бледно-желтой жидкости. Промежуточное соединение 68. 3-Фтор-3'-пропоксибифенил-4-амин. Титульное соединение (280 мг) получали из 4-бром-2-фторанилина (390 мг, 1,6 ммоль) и 3 пропоксифенилбороновой кислоты (369 мг, 2 ммоль) в виде бесцветной жидкости. Промежуточное соединение 69. 3'-Пропоксибифенил-4-амин. Титульное соединение (280 мг) получали из 4-броманилина (300 мг, 1,7 ммоль) и 3 пропоксифенилбороновой кислоты (408 мг, 2,3 ммоль) в виде бесцветной жидкости. Промежуточное соединение 70. 3'-(Этилтио)-2-фторбифенил-4-амин. Титульное соединение (430 мг) получали из 4-бром-3-фторанилина (300 мг, 1,6 ммоль) и 3(этилтио)фенилбороновой кислоты (370 мг, 2,0 ммоль) в виде желтой жидкости. Промежуточное соединение 71. 3,5-Дифтор-3'-(2,2,2-трифторэтокси)бифенил-4-амин. Титульное соединение (89 мг) получали из 4-бром-2,6-дифторанилина (80 мг, 0,38 ммоль) и 3(2,2,2-трифторэтокси)фенилбороновой кислоты (108 мг, 0,5 ммоль) в виде бесцветной жидкости. Промежуточное соединение 72. 3'-Этил-3,5-дифторбифенил-4-амин. Титульное соединение (89 мг) получали из 4-бром-2,6-дифторанилина (100 мг, 0,48 ммоль) и 3 этилфенилбороновой кислоты (99 мг, 0,6 ммоль) в виде бесцветной жидкости. Промежуточное соединение 73. 2'-Хлорбифенил-4-амин. Титульное соединение (176 мг) получали из 4-броманилина (300 мг, 1,74 ммоль) и 2 хлорфенилбороновой кислоты (354 мг, 2,26 ммоль) в виде желтого твердого вещества. Промежуточное соединение 74. 3'-Метоксибифенил-4-амин. Титульное соединение (58 мг) получали из 4-броманилина (300 мг, 1,74 ммоль) и 3 метоксифенилбороновой кислоты (344 мг, 2,26 ммоль) в виде желтой жидкости. Промежуточное соединение 75. 3'-(Трифторметокси)бифенил-4-амин. Титульное соединение (280 мг) получали из 4-броманилина (300 мг, 1,74 ммоль) и 3(трифторметокси)фенилбороновой кислоты (466 мг, 2,26 ммоль) в виде бледно-желтой жидкости. Промежуточное соединение 76. 3'-(Этилтио)-2,6-дифторфенил-4-амин. Титульное соединение (500 мг) получали из 4-бром-3,5-дифторанилина (300 мг, 1,74 ммоль) и 3(этилтио)фенилбороновой кислоты (340 мг, 1,86 ммоль) в виде желтой жидкости. Промежуточное соединение 77. 3'-Этилбифенил-4-амин. Титульное соединение (300 мг) получали из 4-броманилина (270 мг, 1,56 ммоль) и 3 этилфенилбороновой кислоты (300 мг, 2,04 ммоль) в виде бесцветной жидкости. Промежуточное соединение 78. 3'-Бутокси-2,3,5,6-тетрафторбифенил-4-амин. Титульное соединение (250 мг) получали из 4-бром-2,3,5,6-тетрафторанилина (300 мг, 1,23 ммоль) и 3-бутоксифенилбороновой кислоты (310 мг, 1,59 ммоль) в виде желтой жидкости. Промежуточное соединение 79. 3'-Бутокси-3-фторбифенил-4-амин. Титульное соединение (170 мг) получали из 4-бром-2-фторанилина (240 мг, 1,26 ммоль) и 3- 26024702 бутоксифенилбороновой кислоты (310 мг, 1,59 ммоль) в виде желтой жидкости. Промежуточное соединение 80. 3'-Циклопропокси-3-фторбифенил-4-амин. Титульное соединение (230 мг) получали из 4-бром-2-фторанилина (1 г, 5,26 ммоль) и 3 изопропоксифенилбороновой кислоты (1,8 г, 6,84 ммоль) в виде желтой жидкости. Промежуточное соединение 81. 3'-Циклопропоксибифенил-4-амин. Титульное соединение (98 мг) получали из 4-броманилина (1 г, 5,81 ммоль) и 3 изопропоксифенилбороновой кислоты (1,96 г, 7,55 ммоль) в виде желтой жидкости. Промежуточное соединение 82. 3'-Бутокси-3-фторбифенил-4-амин. Титульное соединение (84 мг) получали из 4-броманилина (200 мг, 1,16 ммоль) и 3 бутоксифенилбороновой кислоты (293 мг, 1,5 ммоль) в виде желтой жидкости. Промежуточное соединение 83. 3'-Бутокси-2-фторбифенил-4-амин. Титульное соединение (241 мг) получали из 4-бром-3-фторанилина (200 мг, 1,05 ммоль) и 3 бутоксифенилбороновой кислоты (265 мг, 1,4 ммоль) в виде бесцветной жидкости. Промежуточное соединение 84. 3'-Бутокси-2,6-дифторбифенил-4-амин. Титульное соединение (172 мг) получали из 4-бром-3,5-дифторанилина (200 мг, 1 ммоль) и 3 бутоксифенилбороновой кислоты (242 мг, 1,2 ммоль) в виде бесцветной жидкости. Промежуточное соединение 85. 3-Пропил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Ниндол. Титульное соединение (500 мг) получали в виде бесцветной вязкой жидкости путем использования процедуры для промежуточного соединения 64 из пропилмагний бромида, полученного из пропилбромида (16,2 мл, 176,96 ммоль) и магния (4,3 г, 176,96 ммоль) в эфире (50 мл), 5-бромизатина (5 г, 22,12 ммоль), ТГФ (20 мл), 2 M боран-диметил сульфида в ТГФ (10 мл, 19,65 ммоль), бис(пинаколато)диборона (600 мг, 2,3 ммоль), ацетата калия (600 мг, 2,3 ммоль) и [1,1'-бис(дифенилфосфино)ферроцен]дихлор палладия(II).CH2Cl2 (44 мг, 0,03 ммоль) и диоксана (10 мл). Промежуточное соединение 86. 2,6-Дифтор-4-(3-пропил-1 Н-индол-5-ил)анилин. Титульное соединение (240 мг) получали из 4-бром-2,6-дифторанилина (400 мг, 1,55 ммоль) и промежуточного соединения 85 (500 мг, 2,11 ммоль) в виде бесцветной клейкой жидкости. Промежуточное соединение 87. 2-Хлор-4-(3-этил-1 Н-индол-5-ил)-6-фторанилин. Титульное соединение (60 мг) получали из 4-бром-2-хлор-6-фторанилина (300 мг, 1,1 ммоль) и промежуточного соединения 64 (316 мг, 1,42 ммоль) в виде коричневой вязкой жидкости. Промежуточное соединение 88. 2'-Хлор-3-фтор-5'-метоксибифенил-4-амино. Титульное соединение (134 мг) получали из 4-бром-2-фторанилина (150 мг, 0,79 ммоль) и 2-хлор-5 метоксифенилбороновой кислоты (191 мг, 1,02 ммоль) в виде бесцветной жидкости. Промежуточное соединение 89. 2'-Хлор-5'-метоксибифенил-4-амин. Титульное соединение (154 мг) получали из 4-броманилина (150 мг, 0,87 ммоль) и 2-хлор-5 метоксифенилбороновой кислоты (211 мг, 1,13 ммоль) в виде бесцветной вязкой жидкости. Общая процедура для получения амида. Процедура-1. Раствор ангидрида (1,3 экв.) и амина (1 экв.) растворяли в диоксане и кипятили с обратным холодильником в течение ночи. Диоксан выпаривали и результирующий остаток растворяли в AcOEt и экстрагировали в водн. 2 N NaHCO3 раствор. Водный слой подкисляли водн. 2 N HCl с получением твердого вещества, которое фильтровали и высушивали с получением необходимого амида. Примеры 1-11, 14, 1617 и 20 синтезировали с использованием общей процедуры-1. Процедура-2. Амин (1 экв.) растворяли в толуоле и порциями добавляли ангидрид (1 экв.), и данную смесь нагревали до 60 С в течение 4 ч. Затвердевший продукт фильтровали и промывали водн. 2 N HCl и высушивали под вакуумом с получением требуемого продукта. Примеры 12 и 13 синтезировали с использованием общей процедуры-2. Процедура-3. Амин (1 экв.) растворяли в уксусной кислоте и добавляли ангидрид (2 экв.), и данную смесь перемешивали при комнатной температуре в течение ночи. Отделившееся твердое вещество фильтровали и промывали петролейным эфиром и высушивали под вакуумом для получения требуемого продукта. Примеры 15, 18, 19, 21-35, 38-71 и 73-100 получали с использованием общей процедуры-3. Пример 1. 2-(3,5-Дифтор-3'-метоксибифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (52 мг) получали из промежуточного соединения 1 (150 мг, 0,64 ммоль) и фталевого ангидрида (189 мг) в виде белого твердого вещества. M.P.: 168-173C. 1H-NMR ( ppm,ДМСО-d6, 400 MHz): 13.05 (s, 1H), 10.19 (s, 1H), 7.83 (d, J=7.4, 1H), 7.69-7.63 (m, 1H), 7.62-7.52 (m, 4H),7.39 (t, J=7.9, 1H), 7.34-7.27 (m, 2H), 6.98 (d, J=6.8, 1H), 3.83 (s, 3H). MS (m/z): 381.55 ([M-H]-). Пример 2. 2-(3,5-Дифтор-3'-метоксибифенил-4-илкарбамоил)бензолсульфоновая кислота. Титульное соединение (64 мг) получали из промежуточного соединения 1 (150 мг, 0,64 ммоль) и 2 сульфобензойной кислоты циклического ангидрида (235 мг) в виде коричневого твердого вещества.([M-H]-). Пример 3. 2-(6-(3-Метоксифенил)пиридин-3-илкарбамоил)бензойная кислота. Титульное соединение (48 мг) получали из промежуточного соединения 3 (100 мг, 0,5 ммоль) и фталевого ангидрида (147 мг, 1 ммоль) в виде белого твердого вещества. M.P.: 194-199C. 1H-NMR (ppm, ДМСО-d6, 400 MHz): 13.17 (bs, 1H), 10.64 (s, 1H), 8.88 (d, 72, 1H), 8.22 (dd, J=2.2, 8.7, 1H), 7.97 (d,J=8.7, 1H), 7.90 (d, J=7, 1H), 7.70-7.66 (m, 1H), 7.63-7.56 (m, 4 Н), 7.38 (t, 78, 1H), 6.98-6.95 (m, 1H), 3.82 (s,3H). MS (m/z): 347.30 ([M-H]-). Пример 4. 2-(3'-Этокси-3-фторбифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (26 мг) получали из промежуточного соединения 4 (100 мг, 0,5 ммоль) и фталевого ангидрида (128 мг, 1 ммоль) в виде белого твердого вещества. M.P.: 151-157C. 1H-NMR (ppm, ДМСО-d6, 400 MHz): 13.06 (s, 1H), 10.22 (s, 1H), 7.95 (t, J=8.5, 1H), 7.89 (d, J=7.7, 1H), 7.68-7.52 (m,5H), 7.35 (t, J=7.9, 1H), 7.25 (d, J=8.2, 1H), 7.21 (s, 1H), 6.92 (d, J=8.4, 1H), 4.10 (q, J=7, 2 Н), 1.34 (t, J=7,3H). MS (m/z): 379.24 ([M]-). Пример 5. 2-(3'-Этокси-3,5-дифторбифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (15 мг) получали из промежуточного соединения 5 (100 мг, 0,43 ммоль) и фталевого ангидрида (118 мг, 0,86 ммоль) в виде белого твердого вещества. M.P.: 136-141 С. 1H-NMR ((m/z): 395.81 ([M-H]-). Пример 6. 3-(3,5-Дифтор-3'-метоксибифенил-4-илкарбамоил)пиразин-2-карбоновая кислота. Титульное соединение (270 мг) получали из промежуточного соединения 1 (150 мг, 0,64 ммоль) и 2,3-пиразиндикарбонового ангидрида (190 мг, 1,26 ммоль) в виде белого твердого вещества. M.P.: 180,1183,4C. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 13.82 (bs, 1H), 10.7 (s, 1H), 8.92 (d, J=5.7, 2H), 7.59 (d,J=9.1, 2H), 7.42-7.38 (m, 1H), 7.36-7.28 (m, 2H), 7.00 (d, J=8, 1H), 3.83 (s, 3H). MS (m/z): 384.05 ([M-H]-). Пример 7. 3-(3,5-Дифтор-3'-этоксибифенил-4-илкарбамоил)пиразин-2-карбоновая кислота. Титульное соединение (84 мг) получали из промежуточного соединения 5 (100 мг, 0,4 ммоль) и 2,3 пиразиндекарбонового ангидрида (120 мг, 0,8 ммоль) в виде белого твердого вещества. M.P.: 133,4137,3C. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 13.76 (s, 1H), 10.68 (s, 1H), 8.92 (dd, J=2.3, 7.7, 2H), 7.58 (d,J=9.2, 2H), 7.41-7.36 (m, 1H), 7.34-7.26 (m, 2H), 6.98 (d, J=8, 1H), 4.11 (q, J=6.9, 2H), 1.35 (t, J=6.9, 3H). MS(m/z): 398.19 ([M-H]-). Пример 8. 2-(2'-Хлор-3,5-дифторбифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (110 мг) получали из промежуточного соединения 6 (140 мг, 0,59 ммоль) и фталевого ангидрида (170 мг, 1,17 ммоль) в виде белого твердого вещества. M.P.: 143,5-145,1 C. 1HNMR ( ppm, ДМСО-d6, 400 MHz): 13.06 (s, 1H), 10.2 (s, 1H), 7.85 (d, J=7.6, 1H), 7.67 (t, J=7.3, 1H), 7.637.56 (m, 3H), 7.52-7.43 (m, 3H), 7.28 (d, J=8.4, 2H). MS (m/z): 386.15 ([M-H]-). Пример 9. 3-[3'-(Бензилокси)-3,5-дифторбифенил-4-илкарбамоил]пиразин-2-карбоновая кислота. Титульное соединение (42 мг) получали из промежуточного соединения 9 (65 мг, 0,21 ммоль) и 2,3 пиразиндикарбонового ангидрида (62 мг, 0,42 ммоль) в виде белого твердого вещества. M.P.: 142144,5C. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 13.77 (bs, 1H), 10.69 (s, 1H), 8.92 (dd, J=2.4, 7.7, 2H), 7.60(d, J=9.2, 2H), 7.48 (d, J=7.3, 2H), 7.44-7.32 (m, 6H), 7.07 (d, J=6.5, 1H), 5.20 (s, 2H). MS (m/z): 460.28 ([MH]-). Пример 10. 2-(3,5-Дифторбифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (85 мг) получали из промежуточного соединения 7 (100 мг, 0,48 ммоль) и фталевого ангидрида (144 мг, 0,86 ммоль) в виде белого твердого вещества. M.P.: 161,2-165,7C. 1H-NMR( ppm, ДМСО-d6, 400 MHz): 13.04 (s, 1H), 10.19 (s, 1H), 7.83 (d, J=7.6, 1H), 7.76 (d, J=7.4, 2H), 7.65 (d,J=8.2, 1H), 7.62-7.48 (m, 6H), 7.43 (d, J=7.2, 1H). MS (m/z): 352.06 ([M-H]-). Пример 11. 3-(3-Хлор-3'-этокси-5-фторбифенил-4-илкарбамоил)пиразин-2-карбоновая кислота. Титульное соединение (30 мг) получали из промежуточного соединения 10 (100 мг, 0,38 ммоль) и 2,3-пиразиндикарбонового ангидрида (112 мг, 0,75 ммоль) в виде белого твердого вещества. M.P.: 148153 C. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 13.74 (bs, 1H), 10.72 (s, 1H), 8.93 (dd, J=2.3, 6.4, 2H), 7.76 (s,1H), 7.70 (d, J=10.7, 1H), 7.42-7.36 (m, 1H), 7.34-7.26 (m, 2H), 6.98 (dd, J=1.8, 8.1, 1H), 4.12 (q, J=6.9, 2H),1.34 (t, J=6.9, 3H). MS (m/z): 414.01 ([M-H]-). Пример 12. 2-[3,5-Дифтор-3'-(трифторметокси)бифенил-4-илкарбамоил]бензойная кислота. Титульное соединение (15 мг) получали из промежуточного соединения 8 (100 мг, 0,34 ммоль) и фталевого ангидрида (50 мг, 0,34 ммоль) в виде белого твердого вещества. M.P.: 148,2-151,4C. 1H-NMR Пример 13. 2-[3'-(Бензилокси)-3,5-дифторбифенил-4-илкарбамоил]бензойная кислота. Титульное соединение (12 мг) получали из промежуточного соединения 9 (100 мг, 0,32 ммоль) и фталевого ангидрида (47 мг, 0,32 ммоль) в виде белого твердого вещества. M.P.: 140,3-143,4C. 1H-NMR(m/z): 457.83 ([M-H]-). Пример 14. 4,5-Дихлор-2-(3-хлор-3'-этокси-5-фторбифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (42 мг) получали из промежуточного соединения 10 (100 мг, 0,38 ммоль) и фталевого ангидрида (160 мг, 0,75 ммоль) в виде беловатого твердого вещества. M.P.: 260-265C. 1HNMR ( ppm, ДМСО-d6, 400 MHz): 15.33 (s, 1H), 8.16 (s, 1H), 7.96 (s, 1H), 7.71 (s, 1H), 7.64 (d, J=11, 1H),7.36 (t, J=7.8, 1H), 7.27-7.22 (m, 2H), 6.95 (dd, J=1.8, 8.1, 1H), 4.12 (d, J=7, 2H), 1.34 (t, J=7, 3H). MS (m/z): 481.02 ([M-H]-). Пример 15. 2-(3-Хлор-3'-этокси-5-фторбифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (86 мг) получали из промежуточного соединения 10 (145 мг, 0,55 ммоль) и фталевого ангидрида (160 мг, 1,1 ммоль) в виде белого твердого вещества. M.P.: 135-140C. 1H-NMR (ppm, ДМСО-d6, 400 MHz): 13.02 (s, 1H), 10.23 (s, 1H), 7.82 (d, J=7.6, 1H), 7.72 (s, 1H), 7.70-7.58 (m, 4H),7.38 (t, J=7.8, 1H), 7.33-7.26 (m, 2H), 6.97 (dd, J=2, 8.1, 1H), 4.12 (q, J=6.9, 2H), 1.35 (t, J=6.9, 3H). MS (m/z): 412.05 ([M-H]-). Пример 16. 4,5-Дихлор-2-(3,5-дифтор-3'-метоксибифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (95 мг) получали из промежуточного соединения 1 (100 мг, 0,42 ммоль) и 5,6-дихлоризобензофуран-1,3-диона (182 мг, 0,84 ммоль) в виде белого твердого вещества. M.P.: 158,6162,2C. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 13.58 (s, 1H), 10.40 (s, 1H), 7.57 (d, J=9.1, 2H), 8.03 (s, 1H),7.83 (s, 1H), 7.39 (t, J=7.9, 1H), 7.34-7.28 (m, 2H), 6.98 (dd, J=1.9,6.9, 1H), 3.83 (s, 3H). MS (m/z): 451.24([M-H]-). Пример 17. 4,5-Дихлор-2-(3'-этокси-3,5-дифторбифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (87 мг) получали из промежуточного соединения 5 (100 мг, 0,42 ммоль) и 5,6-дихлоризобензофуран-1,3-диона (173 мг, 0,8 ммоль) в виде белого твердого вещества. M.P.: 190,1192,4C. 1H-NMR ( ppm, ДМСО-d6, 400 MHz): 13.58 (s, 1H), 10.39 (s, 1H), 8.03 (s, 1H), 7.82 (s, 1H), 7.56(d, J=9.2, 2H), 7.37 (t, J=7.9, 1H), 7.33-7.26 (m, 2H), 6.97 (dd, J=1.8, 8.1, 1H), 4.11 (q, J=7, 2H), 1.34 (t, J=7,3H). MS (m/z): 464.92 ([M-H]-). Пример 18. 2-(3,5-Дихлор-3'-метоксибифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (20 мг) получали из промежуточного соединения 11 (150 мг, 0,56 ммоль) и фталевого ангидрида (165 мг, 1,12 ммоль) в виде белого твердого вещества. M.P.: 163-168C. 1H-NMR (([M-H]-). Пример 19. 2-(3-Хлор-5-фтор-3'-пропоксибифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (38 мг) получали из промежуточного соединения 12 (100 мг, 0,36 ммоль) и фталевого ангидрида (105 мг, 0,72 ммоль) в виде белого твердого вещества. M.P.: 144-148C. 1H-NMR (ppm, ДМСО-d6, 400 MHz): 13.03 (s, 1H), 10.24 (s, 1H), 7.82 (d, J=7.5, 1H), 7.73 (s, 1H), 7.70-7.57 (m, 4H),7.38 (t, J=7.7, 1H), 7.32-7.26 (m, 2H), 6.98 (d, J=8.1, 1H), 4.02 (t, J=6.5, 2H), 1.77-1.72 (m, 2H), 0.99 (t, J=7.4,3H). MS (m/z): 426.05 ([M-H]-). Пример 20. 2-(3-Хлор-2',5-дифторбифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (15 мг) получали из промежуточного соединения 13 (100 мг, 0,34 ммоль) и фталевого ангидрида (100 мг, 0,68 ммоль) в виде белого твердого вещества. M.P.: 163-167C. 1H-NMR (ppm, ДМСО-d6, 400 MHz): 13.05 (s, 1H), 10.3 (s, 1H), 7.83 (d, J=7.6, 1H), 7.70-7.58 (m, 5H), 7.57-7.46 (m,2H), 7.40-7.31 (m, 2H). MS (m/z): 386.15 ([M-H]-). Пример 21. 2-(3,5-Дихлор-3'-этоксибифенил-4-илкарбамоил)бензойная кислота. Титульное соединение (30 мг) получали из промежуточного соединения 14 (150 мг, 0,53 ммоль) и фталевого ангидрида (157 мг, 1,06 ммоль) в виде белого твердого вещества. M.P.: 135,9-138,2C. 1H-NMRMS (m/z): 429.30 ([M-H]-). Пример 22. 2-[3-Фтор-3'-(трифторметокси)бифенил-4-илкарбамоил]бензойная кислота. Титульное соединение (124 мг) получали из промежуточного соединения 15 (100 мг, 0,44 ммоль) и фталевого ангидрида (130 мг, 0,9 ммоль) в виде белого твердого вещества. M.P.: 128,3-132,1C. 1H-NMR( ppm, ДМСО-d6, 400 MHz): 13.07 (s, 1H), 10.28 (s, 1H), 7.99 (t, J=8.3, 1H), 7.88 (d, J=7.4, 1H), 7.77 (d, J=8,1H), 7.67 (s, 1H), 7.69-7.52 (m, 6H), 7.37 (d, J=8.2, 1H). MS (m/z): 417.86 ([M-H]-). Пример 23. 2-[2'-Фтор-3-(трифторметокси)бифенил-4-илкарбамоил]бензойная кислота. Титульное соединение (82 мг) получали из промежуточного соединения 16 (100 мг, 0,36 ммоль) и фталевого ангидрида (109 мг, 0,72 ммоль) в виде белого твердого вещества. M.P.: 142,2-148,1C. 1H-NMR
МПК / Метки
МПК: C07D 213/81, C07D 209/14, C07D 213/75, C07D 307/79, C07D 213/56, C07D 241/24
Метки: иммуномодуляторные, соединения, противовоспалительные, новые
Код ссылки
<a href="https://eas.patents.su/30-24702-novye-immunomodulyatornye-i-protivovospalitelnye-soedineniya.html" rel="bookmark" title="База патентов Евразийского Союза">Новые иммуномодуляторные и противовоспалительные соединения</a>
Предыдущий патент: Антитела, связывающие cd27 человека, и их применение
Следующий патент: Комбинация оланзапина и агониста taar1
Случайный патент: Способ и устройство для обработки табачных листьев при изготовлении резанного табака.