Производные фталазинонпирролопиримидинкарбоксамида
Номер патента: 23713
Опубликовано: 29.07.2016
Авторы: Фиртельхаус Мартин, Бенедиктус Эвальд, Дункерн Торстен, Канахер Тобиас, Флоккерци Дитер, Штадльвизер Йозеф, Цитт Кристоф, Тенор Германн, Паль Андреас, Манн Александер, Хуссонг Рагна, Штенгель Томас, Майер Томас, Хесслингер Кристиан, Хессманн Мануэла, Хольст Ханс Кристоф, Хатцельманн Армин, Хуммель Рольф-Петер
Формула / Реферат
1. Соединение формулы (1)
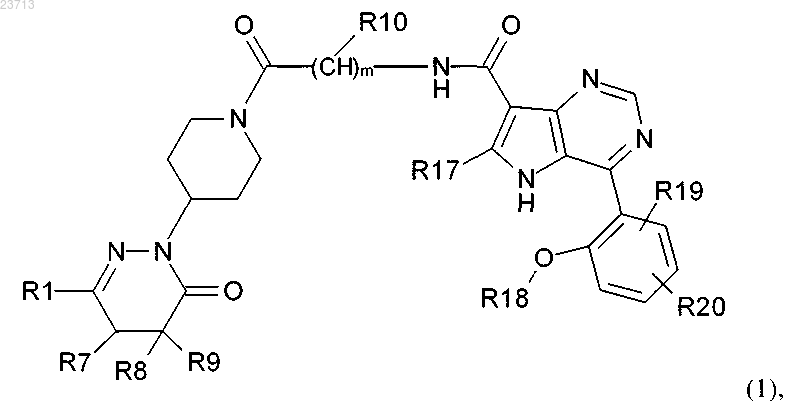
в которой R1 обозначает фенилпроизводное формул (а) или (b)

в которых R2 обозначает C1-C4-алкоксигруппу или C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором,
R3 обозначает C1-C4-алкоксигруппу, C3-C5-циклоалкоксигруппу, С3-С5-циклоалкоксиметоксигруппу или C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором,
R4 обозначает C1-C4-алкоксигруппу или C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором,
R5 обозначает C1-C4-алкил,
R6 обозначает водород или C1-C4-алкил,
или в которых R5 и R6, взятые вместе и с включением двух атомов углерода, к которым они присоединены, образуют спиросочлененное 5-, 6- или 7-членное углеводородное кольцо, в которое необязательно включен атом кислорода или серы,
R7 обозначает водород,
R8 обозначает C1-C4-алкил,
или R7 и R8 вместе образуют C3-C5-алкиленовую группу,
R9 обозначает водород или C1-C4-алкил,
или в которой R8 и R9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5-, 6- или 7-членное углеводородное кольцо,
m равно 1 или 2,
R10 независимо друг от друга обозначают водород, С5-С7-циклоалкил, C1-C6- алкил, -CH(CH3)-R11 или -CH2-R12,
где R11 обозначает незамещенный фенил или гидроксигруппу,
R12 обозначает гидроксигруппу, С5-С7-циклоалкил, -N-(C1-C2-алкил)2, -CH2-S-(C1-C2-алкил), бензил, незамещенный фенил, фенил, замещенный с помощью R13, фенил, замещенный с помощью R13 и R14,
где R13 обозначает галоген, C1-C4-алкоксигруппу, C1-C6-алкил, C1-C4-фторалкил, гидроксигруппу, фенил, -C(O)NH2, -CN, 2-оксоазетидин-1-ил или 2-оксопирролидин-1-ил,
R14 обозначает галоген, C1-C4-алкоксигруппу, С1-С6-алкил, C1-C4-фторалкил, гидроксигруппу, фенил, -C(O)NH2 или -CN,
или R12 выбран из группы, включающей имидазол-2-ил, имидазол-4-ил, пиразол-1-ил, тиофен-2-ил, тиофен-3-ил, тиазол-2-ил, тиазол-4-ил, тиазол-5-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, индол-2-ил, индол-3-ил, 1-метилиндол-2-ил или 1-метилиндол-3-ил, или
R12 обозначает -CH2-C(O)-R15,
где R15 обозначает гидроксигруппу, -N(R16)2, пиперидин-1-ил, пирролидин-1-ил или бензилоксигруппу,
где R16 независимо друг от друга обозначают водород или C1-C4-алкил,
R17 обозначает водород или метил,
R18 обозначает -CH2-C3-C6-циклоалкил,
R19 обозначает галоген, гидроксигруппу, C1-C4-алкоксигруппу, C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором, или C1-С4-фторалкил,
R20 обозначает галоген, гидроксигруппу, C1-C4-алкоксигруппу или C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором,
или R19 и R20 вместе образуют C1-C2-алкилендиоксигруппу,
или стереоизомер соединения, или соль соединения, или соль стереоизомера соединения.
2. Соединение формулы (1) по п.1, в которой R1 обозначает фенилпроизводное формул (а) или (b), в которых
R2 обозначает C1-C4-алкоксигруппу или C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором,
R3 обозначает C1-C4-алкоксигруппу или C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором,
R4 обозначает C1-C2-алкоксигруппу или C1-C2-алкоксигруппу, преимущественно или полностью замещенную фтором,
R5 обозначает C1-C2-алкил,
R6 обозначает водород или C1-C2-алкил,
или в которых R5 и R6, взятые вместе и с включением двух атомов углерода, к которым они присоединены, образуют спиросочлененное 5-, 6- или 7-членное углеводородное кольцо,
R7 обозначает водород,
R8 обозначает C1-C4-алкил,
или R7 и R8 вместе образуют C3-C5-алкиленовую группу,
R9 обозначает водород или C1-C4-алкил,
или в которой R8 и R9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5-, 6- или 7-членное углеводородное кольцо,
R10 независимо друг от друга обозначают водород, С5-С7-циклоалкил, C1-C4-алкил, -CH(CH3)-R11 или -СН2-R12,
где R11 обозначает незамещенный фенил или гидроксигруппу,
R12 обозначает гидроксигруппу, C5-C7-циклоалкил, -N-(C1-C2-алкил)2, -CH2-S-(C1-C2-алкил), бензил, незамещенный фенил, фенил, замещенный с помощью R13, фенил, замещенный с помощью R13 и R14,
где R13 обозначает галоген, C1-C4-алкоксигруппу, C1-C4-алкил, C1-C4-фторалкил, гидроксигруппу, фенил, -C(O)NH2, -CN, 2-оксоазетидин-1-ил или 2-оксопирролидин-1-ил,
R14 обозначает галоген, C1-C4-алкоксигруппу, C1-C4-алкил, C1-C4-фторалкил, гидроксигруппу, фенил, -C(O)NH2 или -CN,
или R12 выбран из группы, включающей имидазол-2-ил, имидазол-4-ил, пиразол-1-ил, тиофен-2-ил, тиофен-3-ил, тиазол-2-ил, тиазол-4-ил, тиазол-5-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, индол-2-ил, индол-3-ил, 1-метилиндол-2-ил или 1-метилиндол-3-ил,
или R12 обозначает -CH2-C(O)-R15,
где R15 обозначает гидроксигруппу, -N(R16)2, пиперидин-1-ил, пирролидин-1-ил или бензилоксигруппу,
где R16 независимо друг от друга обозначают водород или C1-C4-алкил,
R17 обозначает водород или метил,
R18 обозначает -CH2-C3-C6-циклоалкил,
R19 обозначает галоген, гидроксигруппу, C1-C4-алкоксигруппу, C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором, или C1-С4-фторалкил,
R20 обозначает галоген, гидроксигруппу, C1-C4-алкоксигруппу или C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором,
или R19 и R20 вместе образуют C1-C2-алкилендиоксигруппу,
или стереоизомер соединения или соль соединения, или соль стереоизомера соединения.
3. Соединение формулы (1) по п.1, в которой
R1 обозначает фенилпроизводное формул (а) или (b), в которых
R2 обозначает C1-C2-алкоксигруппу или C1-C2-алкоксигруппу, преимущественно или полностью замещенную фтором,
R3 обозначает C1-C2-алкоксигруппу или C1-C2-алкоксигруппу, преимущественно или полностью замещенную фтором,
R4 обозначает C1-C2-алкоксигруппу или C1-C2-алкоксигруппу, преимущественно или полностью замещенную фтором,
R5 обозначает C1-C2-алкил,
R6 обозначает водород или C1-C2-алкил,
или в которых R5 и R6, взятые вместе и с включением двух атомов углерода, к которым они присоединены, образуют спиросочлененное 5- или 6-членное углеводородное кольцо,
R7 обозначает водород,
R8 обозначает C1-C2-алкил,
или R7 и R8 вместе образуют C3-C5-алкиленовую группу,
R9 обозначает водород или C1-C2-алкил,
или в которой R8 и R9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5- или 6-членное углеводородное кольцо,
m равно 1 или 2,
R10 независимо друг от друга обозначают водород, С5-С7-циклоалкил, C1-C4-алкил, -CH(CH3)-R11 или -СН2-R12,
где R11 обозначает незамещенный фенил или гидроксигруппу,
R12 обозначает гидроксигруппу, С5-С7-циклоалкил, -N-(C1-C2-алкил)2, -CH2-S-(C1-C2-алкил), бензил, незамещенный фенил, фенил, замещенный с помощью R13, фенил, замещенный с помощью R13 и R14,
где R13 обозначает галоген, C1-C4-алкоксигруппу, C1-C4-алкил, C1-C4-фторалкил, гидроксигруппу, фенил, -C(O)NH2, -CN, 2-оксоазетидин-1-ил или 2-оксопирролидин-1-ил,
R14 обозначает галоген или C1-C4-алкоксигруппу, C1-C4-алкил, или R12 выбран из группы, включающей имидазол-2-ил, имидазол-4-ил, пиразол-1-ил, тиофен-2-ил, тиофен-3-ил, тиазол-2-ил, тиазол-4-ил, тиазол-5-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, индол-2-ил, индол-3-ил, 1-метилиндол-2-ил или 1-метилиндол-3-ил, или R12 обозначает -CH2-C(O)-R15,
где R15 обозначает гидроксигруппу, -N(R16)2, пиперидин-1-ил, пирролидин-1-ил или бензилоксигруппу,
где R16 независимо друг от друга обозначают водород или С1-С3-алкил,
R17 обозначает водород или метил,
R18 обозначает -СН2-С3-С5-циклоалкил,
R19 обозначает галоген или C1-C4-алкоксигруппу,
R20 обозначает галоген или C1-C4-алкоксигруппу,
или R19 и R20 вместе образуют C1-C2-алкилендиоксигруппу,
или стереоизомер соединения, или соль соединения, или соль стереоизомера соединения.
4. Соединение формулы (1) по п.1, в которой
R1 обозначает фенилпроизводное формул (а) или (b), в которых
R2 обозначает метоксигруппу,
R3 обозначает метоксигруппу,
R4 обозначает метоксигруппу,
R5 обозначает метил,
R6 обозначает водород,
R7 обозначает водород,
R8 обозначает C1-C2-алкил,
или R7 и R8 вместе образуют C3-C5-алкиленовую группу,
R9 обозначает водород или C1-C2-алкил, или в которой R8 и R9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5-членное углеводородное кольцо,
m равно 1 или 2,
R10 независимо друг от друга обозначают водород, C5-C7-циклоалкил, C1-C4-алкил, -CH(CH3)-R11 или -CH2-R12,
где R11 обозначает незамещенный фенил или гидроксигруппу,
R12 обозначает гидроксигруппу, С5-С7-циклоалкил, -N-(С1-С2-алкил)2, -CH2-S-(C1-C2-алкил), бензил, незамещенный фенил, фенил, замещенный с помощью R13, фенил, замещенный с помощью R13 и R14,
где R13 обозначает фтор, хлор, бром, C1-C2-алкоксигруппу, C1-C4-алкил, С1-С2-фторалкил, гидроксигруппу, фенил, -C(O)NH2, -CN, 2-оксоазетидин-1-ил или 2-оксопирролидин-1-ил,
R14 обозначает фтор, хлор, бром или C1-C2-алкоксигруппу, или R12 выбран из группы, включающей имидазол-2-ил, имидазол-4-ил, пиразол-1-ил, тиофен-2-ил, тиофен-3-ил, тиазол-2-ил, тиазол-4-ил, тиазол-5-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, индол-2-ил, индол-3-ил, 1-метилиндол-2-ил или 1-метилиндол-3-ил, или R12 обозначает -CH2-C(O)-R15,
где R15 обозначает гидроксигруппу, -N(R16)2, пиперидин-1-ил, пирролидин-1-ил или бензилоксигруппу, где
R16 независимо друг от друга обозначают водород или C1-C3-алкил,
R17 обозначает водород или метил,
R18 обозначает -CH2-C3-C4-циклоалкил,
R19 обозначает C1-C2-алкоксигруппу,
R20 обозначает фтор, хлор или бром,
или R19 и R20 вместе образуют метилендиоксигруппу,
или стереоизомер соединения, или соль соединения, или соль стереоизомера соединения.
5. Соединение формулы (1) по п.1, в которой
R1 обозначает фенилпроизводное формул (а) или (b), в которых
R2 обозначает метоксигруппу,
R3 обозначает метоксигруппу,
R4 обозначает метоксигруппу,
R5 обозначает метил,
R6 обозначает водород,
R7 обозначает водород,
R8 обозначает C1-C2-алкил,
или R7 и R8 вместе образуют C3- или С4-алкиленовую группу,
R9 обозначает водород или C1-C2-алкил,
или в которой R8 и R9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5-членное углеводородное кольцо,
m равно 1 или 2,
R10 независимо друг от друга обозначают водород, циклогексил, C1-C4-алкил, -CH(CH3)-R11 или -CH2-R12,
где R11 обозначает незамещенный фенил или гидроксигруппу,
R12 обозначает гидроксигруппу, циклогексил, -N-(CH3)2, -CH2-S-CH3, бензил, незамещенный фенил, фенил, замещенный с помощью R13, фенил, замещенный с помощью R13 и R14,
где R13 обозначает фтор, хлор, C1-C2-алкоксигруппу, метил, трет-бутил, трифторметил, гидроксигруппу, фенил, -C(O)NH2, -CN, 2-оксоазетидин-1-ил или 2-оксопирролидин-1-ил,
R14 обозначает фтор, хлор или метоксигруппу, или R12 выбран из группы, включающей имидазол-2-ил, имидазол-4-ил, пиразол-1-ил, тиофен-2-ил, тиофен-3-ил, тиазол-2-ил, тиазол-4-ил, тиазол-5-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, индол-2-ил, индол-3-ил, 1-метилиндол-2-ил или 1-метилиндол-3-ил, или R12 обозначает -CH2-C(O)-R15,
где R15 обозначает гидроксигруппу, -N(R16)2, пиперидин-1-ил, пирролидин-1-ил или бензилоксигруппу,
где R16 независимо друг от друга обозначают водород или изопропил,
R17 обозначает водород или метил,
R18 обозначает -CH2-C3-циклоалкил,
R19 обозначает метоксигруппу,
R20 обозначает фтор,
или R19 и R20 вместе образуют метилендиоксигруппу,
или стереоизомер соединения, или соль соединения, или соль стереоизомера соединения.
6. Соединение формулы (1) по п.5, которое выбрано из группы, включающей
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-3-(3,5-дифторфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4a,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4a,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(3-метилфенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(3-метилфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(3-метилфенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(4-трет-бутилфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(4-трет-бутилфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(4-карбамоилфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-этоксифенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-этоксифенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-этоксифенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(4-карбамоилфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(бифенил-4-ил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(бифенил-4-ил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(4-цианофенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-метилфенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(4-цианофенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(3-метилфенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-3-(3,4-дифторфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-3-(3,4-дифторфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(3-метилфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-метилфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[2-(циклопропилметокси)-4-фтор-5-метоксифенил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-3-(3,4-диметоксифенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(4-хлорфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-фторфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-метоксифенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(3-хлорфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-{(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-[2-(трифторметил)фенил]пропан-2-ил}-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-{(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-[2-(трифторметил)фенил]пропан-2-ил}-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(2-хлорфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(2-хлорфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R,3R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилбутан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(пиридин-2-ил)пропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(пиридин-2-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(пиридин-4-ил)пропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(пиридин-4-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(пиридин-3-ил)пропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(пиридин-3-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aR,8aS)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aR,8aS)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2R)-3-(4-трет-бутилфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-фторфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-3-(2,4-дихлорфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-{(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-[4-(трифторметил)фенил]пропан-2-ил}-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R,3R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилбутан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R,3R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилбутан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-гидроксифенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-гидроксифенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2S)-3-(2-хлорфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,7aR)-4-(3,4-диметоксифенил)-1-оксо-1,4а,5,6,7,7а-гексагидро-2Н-циклопента[d]пиридазин-2-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
N-[(2S)-3-(2-хлорфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(3-метилфенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(4-метоксифенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-(2-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-2-оксоэтил)-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-гидрокси-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S,3R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-гидрокси-1-оксобутан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксобутан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-4-фенилбутан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[3-(3,4-диметоксифенил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[3-(3,4-диметоксифенил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид;
4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-{4-[3-(3,4-диметоксифенил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид или
4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-{4-[3-(3,4-диметоксифенил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S,3S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-метил-1-оксопентан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
N-[(2S)-3-циклогексил-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
N-[(1R)-1-циклогексил-2-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-2-оксоэтил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
N-[(1S)-1-циклогексил-2-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-2-оксоэтил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(тиофен-2-ил)пропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(тиофен-2-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-(3-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-оксопропил)-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-4-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-4-оксо-1-фенилбутан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-4-{4-[3-(3,4-диметоксифенил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-4-оксо-1-фенилбутан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1,5-диоксо-5-(пиперидин-1-ил)пентан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1,5-диоксо-5-(пиперидин-1-ил)пентан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1,5-диоксо-5-(пиперидин-1-ил)пентан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(1,3-тиазол-4-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(1,3-тиазол-4-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(1,3-тиазол-4-ил)пропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(1H-пиразол-1-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(1Н-имидазол-4-ил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(1Н-имидазол-4-ил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(1H-индол-3-ил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(1Н-индол-3-ил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(1-метил-1H-индол-3-ил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
N-[(2S)-3-циклогексил-1-{4-[3-(3,4-диметоксифенил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-4-метил-1-оксопентан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(диметиламино)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(диметиламино)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-4-(метилсульфанил)-1-оксобутан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
N-[(2R)-3-(4-бромфенил)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
бензил-(4R)-4-[({4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-ил}карбонил)амино]-5-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-5-оксопентаноат,
(4R)-4-[({4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-ил}карбонил)амино]-5-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-5-оксопентановую кислоту,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1,5-диоксо-5-(пирролидин-1-ил)пентан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
(4S)-4-[({4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-ил}карбонил)амино]-5-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-5-оксопентановую кислоту,
бензил-(4S)-4-[({4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-ил}карбонил)амино]-5-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-5-оксопентаноат,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1,5-диоксо-5-(пирролидин-1-ил)пентан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1,5-диоксо-5-(пропан-2-иламино)пентан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1,5-диоксо-5-(пропан-2-иламино)пентан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[3-(3,4-димегоксифенил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-3-(4-фторфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-(пиридин-4-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[3-(3,4-диметоксифенил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[3-(3,4-диметоксифенил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-{(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-[4-(2-оксоазетидин-1-ил)фенил]пропан-2-ил)-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-{(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-[4-(2-оксопирролидин-1-ил)фенил]пропан-2-ил}-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[3-(7-метокси-2,2-диметил-2,3-дигидро-1-бензофуран-4-ил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-1-оксо-3-(пиридин-3-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[3-(7-метокси-2,2-диметил-2,3-дигидро-1-бензофуран-4-ил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[3-(3,4-диметоксифенил)-5,5-диэтил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-(2-{4-[3-(7-метокси-2,2-диметил-2,3-дигидро-1-бензофуран-4-ил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-2-оксоэтил)-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[3-(3,4-диметоксифенил)-5,5-диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил}-5-(диметиламино)-1,5-диоксопентан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-метил-1-оксобутан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-метил-1-оксобутан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3,3-диметил-1-оксобутан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-(2-{4-[9-(3,4-диметоксифенил)-6-оксо-7,8-диазаспиро[4.5]дец-8-ен-7-ил]пиперидин-1-ил}-2-оксоэтил)-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[9-(3,4-диметоксифенил)-6-оксо-7,8-диазаспиро[4.5]дец-8-ен-7-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид,
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[9-(3,4-диметоксифенил)-6-оксо-7,8-диазаспиро[4.5]дец-8-ен-7-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид и
4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-{4-[9-(3,4-диметоксифенил)-6-оксо-7,8-диазаспиро[4.5]дец-8-ен-7-ил]пиперидин-1-ил}-1-оксо-3-(пиридин-3-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид.
7. Соединение формулы (1) по п.1, которое представляет собой 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-3-(3-метилфенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид или его соль.
8. Соединение формулы (1) по п.1, которое представляет собой 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид или его соль.
9. Соединение формулы (1) по п.1, которое представляет собой 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-(2-{4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4а,5,6,7,8,8а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил}-2-оксоэтил)-5H-пирроло[3,2-d]пиримидин-7-карбоксамид или его соль.
10. Фармацевтическая композиция, включающая по меньшей мере одно из соединений формулы (1) или стереоизомер соединения, или его соль соединения, или соль стереоизомера соединения по любому из пп.1-9 вместе по меньшей мере с одним фармацевтически приемлемым вспомогательным веществом.
11. Фармацевтическая композиция по п.10 дополнительно включающая по меньшей мере одно терапевтическое средство, выбранное из группы, включающей кортикостероиды, антихолинергетики, агонисты β2-адренорецептора, антагонисты рецептора H1, антагонисты лейкотриенового рецептора, ингибиторы 5-липоксигеназы, антагонисты эндотелинового рецептора, простациклины, блокаторы кальциевых каналов, бета-блокаторы, ингибиторы фосфодиэстеразы типа 4, ингибиторы фосфодиэстеразы типа 5, иммуносупрессанты, аналоги витамина D, ингибиторы HMG-CoA редуктазы, легочные сурфактанты, антибиотики, активаторы/стимуляторы гуанилатциклазы, тетрагидробиоптерин и производные тетрагидробиоптерина, антикоагулянты, диуретики, пирфенидон и гликозиды дигиталиса и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
12. Применение соединения формулы (1), или стереоизомера соединения, или его соли соединения, или соли стереоизомера соединения по любому из пп.1-9 для приготовления фармацевтической композиции, ингибирующей фосфодиэстеразу типа 4 и типа 5.
13. Применение соединения формулы (1), или стереоизомера соединения, или его соли соединения, или соли стереоизомера соединения по любому из пп.1-9 для приготовления фармацевтической композиции, предназначенной для лечения или профилактики острого или хронического заболевания дыхательных путей.
14. Применение по п.13, в котором острое или хроническое заболевание дыхательных путей выбрано из группы, включающей интерстициальное заболевание легких, фиброз легких, муковисцидоз, бронхиальную астму, хронический бронхит, эмфизему, хроническое обструктивное заболевание легких (ХОЗЛ) и ХОЗЛ, связанное с легочной гипертензией.
Текст
В изобретении описаны соединения формулы (1) в которой R1, R7, R8, R9, R10, R17, R18, R19, R20 и m обладают значениями, приведенными в описании, которые являются новыми эффективными ингибиторами фосфодиэстеразы типа 4 и 5. Область техники, к которой относится изобретение Изобретение относится к новым производным фталазинонпирролопиримидинкарбоксамида, которые применяются в фармацевтической промышленности для производства фармацевтических композиций. Уровень техники В заявках на международные патенты WO 02/064584, WO 02/085906, WO 04/017974, WO 04/018449,WO 04/018451, WO 04/018457, WO 05/075456 и WO 05/075457 описаны производные фталазинона или пиридазинона, содержащие пиперидинильный заместитель, как ингибиторы фосфодиэстеразы типа 4. В заявках на международные патенты WO 2009106531 и WO 2011023693 описаны пирролопиримидинкарбоксамиды, являющиеся ингибиторами фосфодиэстеразы типа 5. Описание изобретения Согласно изобретению было установлено, что производные пиперидинилпиридазинонпирролопиримидинкарбоксамида, которые подробно описаны ниже, обладают неожиданными и особенно полезными характеристиками. Изобретение относится к соединению формулы (1) в которой R1 обозначает фенилпроизводное формул (а) или (b) в которых R2 обозначает С 1-С 4-алкоксигруппу или С 1-С 4-алкоксигруппу, преимущественно или полностью замещенную фтором,R3 обозначает С 1-С 4-алкоксигруппу, C3-C5-циклоалкоксигруппу, С 3-С 5-циклоалкоксиметоксигруппу или С 1-С 4-алкоксигруппу, преимущественно или полностью замещенную фтором,R4 обозначает C1-C4-алкоксигруппу или С 1-С 4-алкоксигруппу, преимущественно или полностью замещенную фтором,R5 обозначает C1-C4-алкил,R6 обозначает водород или C1-C4-алкил,или в которых R5 и R6, взятые вместе и с включением двух атомов углерода, к которым они присоединены, образуют спиросочлененное 5-, 6- или 7-членное углеводородное кольцо, в которое необязательно включен атом кислорода или серы,R7 обозначает водород,R8 обозначает С 1-С 4-алкил, или R7 и R8 вместе образуют C3-C5-алкиленовую группу,R9 обозначает водород или C1-C4-алкил, или в которой R8 и R9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5-, 6- или 7-членное углеводородное кольцо,m равно 1 или 2,R10 независимо друг от друга обозначают водород, С 5-С 7-циклоалкил, C1-C6-алкил, -CH(CH3)-R11 или -CH2-R12,где R11 обозначает незамещенный фенил или гидроксигруппу,R12 обозначает гидроксигруппу, С 5-С 7-циклоалкил, -N-(С 1-С 2-алкил)2, -CH2-S-(C1-C2-алкил), бензил,незамещенный фенил, фенил, замещенный с помощью R13, фенил, замещенный с помощью R13 и R14,где R13 обозначает галоген, C1-C4-алкоксигруппу, С 1-С 6-алкил, C1-C4-фторалкил, гидроксигруппу,фенил, -C(O)NH2, -CN, 2-оксоазетидин-1-ил или 2-оксопирролидин-1-ил,R14 обозначает галоген, C1-C4-алкоксигруппу, C1-C6-алкил, C1-C4-фторалкил, гидроксигруппу, фенил, -C(O)NH2 или -CN, или R12 выбран из группы, включающей имидазол-2-ил, имидазол-4-ил, пиразол-1-ил, тиофен-2-ил, тиофен-3-ил, тиазол-2-ил, тиазол-4-ил, тиазол-5-ил, пиридин-2-ил, пиридин-3-ил,пиридин-4-ил, индол-2-ил, индол-3-ил, 1-метилиндол-2-ил или 1-метилиндол-3-ил, или R12 обозначаетR16 независимо друг от друга обозначают водород или C1-C4-алкил,-1 023713R17 обозначает водород или метил,R18 обозначает -CH2-C3-C6-циклоалкил,R19 обозначает галоген, гидроксигруппу, C1-C4-алкоксигруппу, С 1-С 4-алкоксигруппу, преимущественно или полностью замещенную фтором, или С 1-С 4-фторалкил,R20 обозначает галоген, гидроксигруппу, С 1-С 4-алкоксигруппу или С 1-С 4-алкоксигруппу, преимущественно или полностью замещенную фтором,или R19 и R20 вместе образуют C1-C2-алкилендиоксигруппу,или к стереоизомеру соединения или к соли соединения, или к соли стереоизомера соединения.C1-C6-Алкил означает обладающую линейной или разветвленной цепью алкильную группу, содержащую от 1 до 6 атомов углерода. Примерами являются н-гексил, 2-метилгексил, 3-метилпентил,2,2-диметилбутил, 2,3-диметилбутил, н-пентил, 2-пентил, 3-пентил, 2-метилбутил, 3-метилбутил, 3 метилбут-2-ил, 2-метилбут-2-ил, 2,2-диметилпропил, бутил, изобутил, втор-бутил, трет-бутил, пропил,изопропил, этил и метил. С 1-С 4-Алкил означает обладающую линейной или разветвленной цепью алкильную группу, содержащую от 1 до 4 атомов углерода. Примерами являются бутил, изобутил, втор-бутил, трет-бутил, пропил, изопропил, этил и метил.C1-C3-Алкил означает обладающую линейной или разветвленной цепью алкильную группу, содержащую от 1 до 3 атомов углерода. Примерами являются пропил, изопропил, этил и метил. С 1-С 2-Алкил означает обладающую линейной цепью алкильную группу, содержащую от 1 до 2 атомов углерода. Примерами являются этил и метил. С 1-С 4-Алкоксигруппа означает группу, которая в дополнение к атому кислорода содержит обладающую линейной или разветвленной цепью алкильную группу, содержащую от 1 до 4 атомов углерода. Алкоксигруппами, содержащими от 1 до 4 атомов углерода, которые можно отметить в этом контексте,являются, например, бутоксигруппа, изобутоксигруппа, втор-бутоксигруппа, трет-бутоксигруппа, пропоксигруппа, изопропоксигруппа, этоксигруппа и метоксигруппа.C1-C2-Алкоксигруппа означает группу, которая в дополнение к атому кислорода содержит обладающую линейной цепью алкильную группу, содержащую от 1 до 2 атомов углерода. Примерами являются этоксигруппа и метоксигруппа.C1-C2-Алкилендиоксигруппа означает, например, метилендиоксигруппу [-О-CH2-O-] и этилендиоксигруппу [-O-CH2-CH2-O-]. С 1-С 4-Алкоксигруппа, которая полностью или преимущественно замещена фтором, представляет собой группу, которая в дополнение к атому кислорода содержит обладающую линейной или разветвленной цепью алкильную группу, содержащую от 1 до 4 атомов углерода, где один или большее количество атомов водорода алкильной группы заменены фтором. Примеры включают, но не ограничиваются только ими, трифторметоксигруппу, дифторметоксигруппу, фторметоксигруппу, перфторэтоксигруппу,1,1,1-трифтор-2-фторэтоксигруппу, 1,1,1-трифторэтоксигруппу, 1,1-дифтор-2,2-дифторэтоксигруппу,1,1-дифтор-2-фторэтоксигруппу, 1,1-дифторэтоксигруппу, 1-фтор-2,2-дифторэтоксигруппу, 1-фтор-2 фторэтоксигруппу, 1-фторэтоксигруппу, 2,2-дифторэтоксигруппу, 2-фторэтоксигруппу, 2,2,3,3,3 пентафторпропоксигруппу, н-перфторпропоксигруппу и н-перфторбутоксигруппу, из которых 1,1-дифтор-2,2-дифторэтоксигруппа, 1,1,1-трифторэтоксигруппа, трифторметоксигруппа и фторметоксигруппа являются предпочтительными. Наиболее предпочтительной является дифторметоксигруппа. "Преимущественно" в этом контексте означает, что более половины атомов водорода С 1-С 4-алкоксигруппы заменены атомами фтора.C1-C2-Алкоксигруппа, которая полностью или преимущественно замещена фтором, представляет собой группу, которая в дополнение к атому кислорода содержит обладающую линейной или разветвленной цепью алкильную группу, содержащую от 1 до 2 атомов углерода, где один или большее количество атомов водорода алкильной группы заменены фтором. Примеры включают, но не ограничиваются только ими, перфторэтоксигруппу, 1,1-дифтор-2,2-дифторэтоксигруппу, 1,2,2-тетрафторэтоксигруппу,1,1,1-трифторэтоксигруппу, трифторметоксигруппу и дифторметоксигруппу, из которых дифторметоксигруппа является предпочтительной. "Преимущественно" в этом контексте означает, что более половины атомов водорода C1-C2-алкоксигруппы заменены атомами фтора. С 1-С 4-Фторалкил означает обладающую линейной или разветвленной цепью алкильную группу, содержащую от 1 до 4 атомов углерода, где один или большее количество атомов водорода C1-C4-алкильной группы заменены фтором. Примеры включают, но не ограничиваются только ими, трифторметильную, дифторметильную, фторметильную, перфторэтильную, 1,1,1-трифтор-2-фторэтильную, 1,1,1 трифторэтильную, 1,1-дифтор-2,2-дифторэтильную, 1,1-дифтор-2-фторэтильную, 1,1-дифторэтильную,1-фтор-2,2-дифторэтильную, 1-фтор-2-фторэтильную, 1-фторэтильную, 2,2-дифторэтильную, 2 фторэтильную, н-перфторпропильную и н-перфторбутильную группу. C1-C4-фторалкил предпочтительно означает обладающую линейной или разветвленной цепью алкильную группу, содержащую от 1 до 4 атомов углерода, где от 1 до 3 атомов водорода С 1-С 4-алкильной группы заменены фтором. Примеры включают, но не ограничиваются только ими, трифторметильную, дифторметильную, фторметильную,перфторэтильную, 1,1,1-трифторэтильную, 1,1-дифтор-2-фторэтильную, 1,1-дифторэтильную, 1-фтор-2 023713 2,2-дифторэтильную, 1-фтор-2-фторэтильную, 1-фторэтильную, 2,2-дифторэтильную и 2-фторэтильную группу. С 1-С 2-Фторалкил означает обладающую линейной или разветвленной цепью алкильную группу, содержащую от 1 до 2 атомов углерода, где один или большее количество атомов водорода C1-C2-алкильной группы заменены фтором. Примеры включают, но не ограничиваются только ими, трифторметильную, дифторметильную, фторметильную, перфторэтильную, 1,1,1-трифтор-2-фторэтильную, 1,1,1 трифторэтильную, 1,1-дифтор-2,2-дифторэтильную, 1,1-дифтор-2-фторэтильную, 1,1-дифторэтильную,1-фтор-2,2-дифторэтильную, 1-фтор-2-фторэтильную, 1-фторэтильную, 2,2-дифторэтильную и 2 фторэтильную группу. C1-C2-фторалкил предпочтительно означает обладающую линейной или разветвленной цепью алкильную группу, содержащую от 1 до 2 атомов углерода, где от 1 до 3 атомов водорода С 1-С 2-алкильной группы заменены фтором. Примеры включают, но не ограничиваются только ими, трифторметильную, дифторметильную, фторметильную, перфторэтильную, 1,1,1-трифторэтильную,1,1-дифтор-2-фторэтильную, 1,1-дифторэтильную, 1-фтор-2,2-дифторэтильную, 1-фтор-2-фторэтильную,1-фторэтильную, 2,2-дифторэтильную и 2-фторэтильную группу.C3-C6-Циклоалкил означает циклоалкильную группу, содержащую от 3 до 6 атомов углерода, и означает циклопропил, циклобутилциклопентил или циклогексил. C3-C5-циклоалкил предпочтительно означает циклопропил, циклобутил или циклопентил, где C3-C4-циклоалкил более предпочтительно означает циклопропил и циклобутил. Наиболее предпочтительным циклоалкилом является циклопропил. Галоген означает фтор, хлор, бром или йод, причем фтор, хлор или бром являются предпочтительными, фтор и хлор являются более предпочтительными. В соответствии с определением группы -(CH)m-R10 эта группа может быть образована из альфааминокислот, таких как фенилаланин, тирозин, глицин, аланин, треонин или серии, или из бетааминокислот, таких как бета-аланин или бета-фенилаланин. Следует понимать, что, если R12 обозначает замещенное фенильное кольцо, то заместитель R13 может быть присоединен к фенильному кольцу в положении 2, в положении 3 или в положении 4. Кроме того,следует понимать, что заместители R13 и R14 фенильного кольца могут быть присоединены к фенильному кольцу в положениях 2 и 3, в положениях 2 и 4, в положениях 2 и 5, в положениях 2 и 6, в положениях 3 и 4, в положениях 3 и 5 и в положениях 3 и 6. Предпочтительно, если заместители R13 и R14 могут быть присоединены к фенильному кольцу в положениях 3 и 4, в положениях 3 и 5 и в положениях 2 и 4. Если R12 обозначает фенильное кольцо, которое замещено с помощью R13 или которое замещено с помощью R13 и R14, то типичными замещенными фенильными кольцами, которые можно отметить, являются 3-метилфенил, 4-метилфенил, 4-трет-бутилфенил, 4-бифенил, 4-метоксифенил, 4-этоксифенил, 2 трифторметилфенил, 4-трифторметилфенил, 2-хлорфенил, 3-хлорфенил, 4-хлорфенил, 4-фторфенил, 4 цианофенил, 4-гидроксифенил, 4-карбоксамидфенил, 3,4-дифторфенил, 3,5-дифторфенил, 2,4 дихлорфенил или 3,4-диметоксифенил. Кроме того, следует понимать, что заместители R19 и R20 могут быть присоединены к фенильному кольцу в положениях 4 и 5 и в положениях 5 и 6, предпочтительно, если R19 и R20 могут быть присоединены к фенильному кольцу в положениях 4 и 5. В случае, если R19 и R20 образуют С 1-С 2-алкилендиоксигруппу, то эта группа может быть присоединена к фенильному кольцу в положениях 4, 5 или в положениях 5, 6, предпочтительно в положениях 5, 6. Такое фенильное кольцо всегда содержит -O-CH2C3-C6-циклоалкильную группу, причем -O-CH2-циклопропильная группа является наиболее предпочтительной. Типичными фенильными кольцами, замещенными с помощью R19 и R20, которые можно отметить,являются 2-(циклопропилметокси)-5-фтор-4-метоксифенил, 2-(циклопропилметокси)-4-фтор-5-метоксифенил или 5-(циклопропилметокси)-1,3-бензодиоксол-4-ил. Соли соединений формулы (1) и их стереоизомеры включают все соли присоединения с неорганическими и органическими кислотами и соли с основаниями, предпочтительно все фармацевтически приемлемые соли присоединения с неорганическими и органическими кислотами и соли с основаниями, более предпочтительно все фармацевтически приемлемые соли присоединения с неорганическими и органическими кислотами и соли с основаниями, обычно использующиеся в фармацевтике. Примеры солей присоединения с кислотами включают, но не ограничиваются только ими, гидрохлориды, гидробромиды, фосфаты, нитраты, сульфаты, ацетаты, трифторацетаты, цитраты, глюконаты,включая D-глюконаты и L-глюконаты, глюконураты, включая D-глюконураты и L-глюконураты, бензоаты, 2-(4-гидроксибензоил)бензоаты, бутираты, салицилаты, сульфосалицилаты, малеаты, лаураты, малаты, включая L-малаты и D-малаты, лактаты, включая L-лактаты и D-лактаты, фумараты, сукцинаты, оксалаты, тартраты, включая L-тартраты, D-тартраты и мезо-тартраты, стеараты, бензолсульфонаты (без-3 023713 илаты), толуолсульфонаты (тозилаты), метансульфонаты (мезилаты), лаурилсульфонаты, 3-гидрокси-2 нафтоаты, лактобионаты (соли 4-О-бета-D-галактопиранозил-D-глюконовой кислоты), галактараты, эмбонаты и аскорбаты. Примеры солей с основаниями включают, но не ограничиваются только ими, соли лития, натрия,калия, кальция, алюминия, магния, титана, аммония, меглумина и гуанидиния. Соли включают нерастворимые в воде и, предпочтительно, растворимые в воде соли. Соединения формулы (1), их стереоизомеры, соли соединений формулы (1) или их стереоизомеры могут содержать, например, при выделении в кристаллической форме, различные количества растворителей. Поэтому в объем настоящего изобретения включены все сольваты соединений формулы (1), их стереоизомеры, соли соединений формулы (1) и их стереоизомеры. Гидраты являются предпочтительным примером сольватов."Стереоизомер" в качестве части выражения "или стереоизомер соединения" или выражения "или стереоизомер соли соединения" означает, что соединения формулы (1) содержат хиральные центры в положениях 4 а и 8 а в случае, если R7 и R8 вместе образуют C3-C5-алкиленовую группу. В случае, еслиR1 обозначает фенилпроизводное формулы (b), то в дигидрофурановом кольце содержится еще один хиральный центр, если заместители R5 и -CH2-R6 не являются одинаковыми. Предпочтительными являются соединения формулы (1), в которых атомы водорода в положениях 4 а и 8 а расположены в цисконфигурации, более предпочтительными являются соединения формулы (1), которые обладают S-конфигурацией в положении 4 а и R-конфигурацией в положении 8 а (в соответствии с правилам Кана, Ингольда и Прелога). Нумерация кольцевой системы, если R7 и R8 вместе образуют С 3-С 5-алкиленовую группу, представлена в приведенной ниже формуле (1). Обозначенное пунктирной линией кольцо показывает возможное замыкание R7 и R8 в кольцо. Однако предпочтительными являются такие соединения, в которых заместители R5 и -CH2-R6 являются одинаковыми или взятые вместе и с включением двух атомов углерода, к которым они присоединены, образуют спиросочлененное 5-, 6- или 7-членное углеводородное кольцо. Кроме того, соединения формулы (1) содержат дополнительный хиральный центр в положении 2 и, если R10 обозначает группу -CH(CH3)-R11, то содержится еще один хиральный центр. Все возможные стереоизомеры, т.е. чистые диастереоизомеры и чистые энантиомеры, а также все их смеси независимо от соотношения компонентов, включая рацематы, входят в объем настоящего изобретения (соответственно в объем конкретного пункта формулы изобретения). В предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1), в которой R1 обозначает фенилпроизводное формул (а) или (b), в которыхR2 обозначает C1-C4-алкоксигруппу или C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором,R3 обозначает C1-C4-алкоксигруппу или C1-C4-алкоксигруппу, преимущественно или полностью замещенную фтором,R4 обозначает C1-C2-алкоксигруппу или C1-C2-алкоксигруппу, преимущественно или полностью замещенную фтором,R5 обозначает C1-C2-алкил,R6 обозначает водород или C1-C2-алкил, или в которых R5 и R6, взятые вместе и с включением двух атомов углерода, к которым они присоединены, образуют спиросочлененное 5-, 6- или 7-членное углеводородное кольцо,R7 обозначает водород,R8 обозначает C1-C4-алкил, или R7 и R8 вместе образуют C3-C5-алкиленовую группу,R9 обозначает водород или C1-C4-алкил, или в которой R8 и R9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5-, 6- или 7-членное углеводородное кольцо,R10 независимо друг от друга обозначают водород, С 5-С 7-циклоалкил, С 1-С 4-алкил, -CH(CH3)-R11 или -CH2-R12, гдеR11 обозначает незамещенный фенил или гидроксигруппу,R12 обозначает гидроксигруппу, С 5-С 7-циклоалкил, -N-(С 1-С 2-алкил)2, -CH2-S-(C1-C2-алкил), бен-4 023713R16 независимо друг от друга обозначают водород или C1-C4-алкил,R17 обозначает водород или метил,R18 обозначает -CH2-C3-C6-циклоалкил,R19 обозначает галоген, гидроксигруппу, C1-C4-алкоксигруппу, С 1-С 4-алкоксигруппу, преимущественно или полностью замещенную фтором, или C1-С 4-фторалкил,R20 обозначает галоген, гидроксигруппу, C1-C4-алкоксигруппу или С 1-С 4-алкоксигруппу, преимущественно или полностью замещенную фтором,или R19 и R20 вместе образуют C1-C2-алкилендиоксигруппу,или к стереоизомеру соединения или к соли соединения, или к соли стереоизомера соединения. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1), в которой R1 обозначает фенилпроизводное формул (а) или (b), в которыхR2 обозначает C1-C2-алкоксигруппу или C1-C2-алкоксигруппу, преимущественно или полностью замещенную фтором,R3 обозначает С 1-С 2-алкоксигруппу или C1-C2-алкоксигруппу, преимущественно или полностью замещенную фтором,R4 обозначает C1-C2-алкоксигруппу или C1-C2-алкоксигруппу, преимущественно или полностью замещенную фтором, R5 обозначает C1-C2-алкил, R6 обозначает водород или C1-C2-алкил,или в которых R5 и R6, взятые вместе и с включением двух атомов углерода, к которым они присоединены, образуют спиросочлененное 5- или 6-членное углеводородное кольцо,R7 обозначает водород,R8 обозначает C1-C2-алкил,или R7 и R8 вместе образуют C3-C5-алкиленовую группу,R9 обозначает водород или C1-C2-алкил,или в которой R8 и R9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5- или 6-членное углеводородное кольцо,m равно 1 или 2,R10 независимо друг от друга обозначают водород, С 5-С 7-циклоалкил, С 1-С 4-алкил, -CH(CH3)-R11 или -CH2-R12, гдеR11 обозначает незамещенный фенил или гидроксигруппу,R12 обозначает гидроксигруппу, С 5-С 7-циклоалкил, -N-(С 1-С 2-алкил)2, -CH2-S-(С 1-С 2-алкил), бензил, незамещенный фенил, фенил, замещенный с помощью R13, фенил, замещенный с помощью R13 иR14,где R13 обозначает галоген, C1-C4-алкоксигруппу, C1-C4-алкил, C1-C4-фторалкил, гидроксигруппу,фенил, -C(O)NH2, -CN, 2-оксоазетидин-1-ил или 2-оксопирролидин-1-ил,R14 обозначает галоген или С 1-С 4-алкоксигруппу, C1-C4-алкил,или R12 выбран из группы, включающей имидазол-2-ил, имидазол-4-ил, пиразол-1-ил, тиофен-2-ил,тиофен-3-ил, тиазол-2-ил, тиазол-4-ил, тиазол-5-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, индол-2 ил, индол-3-ил, 1-метилиндол-2-ил или 1-метилиндол-3-ил, или R12 обозначает -CH2-C(O)-R15, гдеR16 независимо друг от друга обозначают водород или C1-C3-алкил,R17 обозначает водород или метил,R18 обозначает -CH2-C3-C5-циклоалкил,R19 обозначает галоген или С 1-С 4-алкоксигруппу,R20 обозначает галоген или C1-C4-алкоксигруппу,или R19 и R20 вместе образуют С 1-С 2-алкилендиоксигруппу,или к стереоизомеру соединения или к соли соединения, или к соли стереоизомера соединения. В еще одном предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1), в которой R1 обозначает фенилпроизводное формул (а) или (b), в которыхR4 обозначает метоксигруппу,R5 обозначает метил,R6 обозначает водород,R7 обозначает водород,R8 обозначает С 1-С 2-алкил,или R7 и R8 вместе образуют C3-C5-алкиленовую группу,R9 обозначает водород или C1-C2-алкил, или в которой R8 и R9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5-членное углеводородное кольцо, m равно 1 или 2,R10 независимо друг от друга обозначают водород, С 5-С 7-циклоалкил, С 1-С 4-алкил, -CH(CH3)-R11 или -CH2-R12,где R11 обозначает незамещенный фенил или гидроксигруппу,R12 обозначает гидроксигруппу, C5-C7-циклоалкил, -Н-(C1-C2-алкил)2, -CH2-S-(C1-C2-алкил), бензил, незамещенный фенил, фенил, замещенный с помощью R13, фенил, замещенный с помощью R13 иR16 независимо друг от друга обозначают водород или C1-C3-алкил,R17 обозначает водород или метил,R18 обозначает -CH2-C3-C4-циклоалкил,R19 обозначает C1-C2-алкоксигруппу,R20 обозначает фтор, хлор или бром,или R19 и R20 вместе образуют метилендиоксигруппу,или к стереоизомеру соединения или к соли соединения, или к соли стереоизомера соединения. В еще одном предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1), в которой R1 обозначает фенилпроизводное формул (а) или (b), в которыхR2 обозначает метоксигруппу,R3 обозначает метоксигруппу,R4 обозначает метоксигруппу,R5 обозначает метил,R6 обозначает водород,R7 обозначает водород,R8 обозначает C1-C2-алкил,или R7 и R8 вместе образуют C3- или С 4-алкиленовую группу,R9 обозначает водород или C1-C2-алкил,или в которой R8 и R9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5-членное углеводородное кольцо,m равно 1 или 2,R10 независимо друг от друга обозначают водород, циклогексил, C1-C4-алкил, -CH(CH3)-R11 илиR11 обозначает незамещенный фенил или гидроксигруппу,R12 обозначает гидроксигруппу, циклогексил, -N-(CH3)2, -CH2-S-CH3, бензил, незамещенный фенил, фенил, замещенный с помощью R13, фенил, замещенный с помощью R13 и R14, гдеR16 независимо друг от друга обозначают водород или изопропил,R17 обозначает водород или метил,R18 обозначает -CH2-C3-циклоалкил,R19 обозначает метоксигруппу,R20 обозначает фтор,-6 023713 или R19 и R20 вместе образуют метилендиоксигруппу,или к стереоизомеру соединения или к соли соединения, или к соли стереоизомера соединения. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 и R8 вместе образуютC3-C4-алкиленовую группу, предпочтительно С 4-алкиленовую группу, R9 обозначает водород и R1, R10,R17, R18, R19 и R20 являются такими, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 и R8 вместе образуютC3-C4-алкиленовую группу, предпочтительно С 4-алкиленовую группу, R9 обозначает водород и R1 обозначает фенильное производное формулы (а), в которой R2 обозначает С 1-С 4-алкоксигруппу и R3 обозначает С 1-С 4-алкоксигруппу, и R10, R17, R18, R19 и R20 являются такими, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 и R8 вместе образуютC3-C4-алкиленовую группу, предпочтительно С 4-алкиленовую группу, R9 обозначает водород и R1 обозначает фенильное производное формулы (а), в которой R2 обозначает С 1-С 4-алкоксигруппу и R3 обозначает С 1-С 4-алкоксигруппу, R18 обозначает -CH2-циклопропил, R19 обозначает С 1-С 4-алкоксигруппу или галоген, R20 обозначает С 1-С 4-алкоксигруппу или галоген или R19 и R20 вместе образуют C1-C2 алкилендиоксигруппу и R10 и R17 являются такими, как определено выше. Предпочтительно, если R2 обозначает C1-C2-алкоксигруппу, более предпочтительно метоксигруппу, R2 обозначает C1-C2-алкоксигруппу,более предпочтительно метоксигруппу, R16 обозначает -CH2-циклопропил, R19 обозначает C1-C2 алкоксигруппу, предпочтительно метоксигруппу, или галоген, предпочтительно фтор, хлор или бром, более предпочтительно фтор, R20 обозначает C1-C2-алкоксигруппу, предпочтительно метоксигруппу, или галоген, предпочтительно фтор, хлор или бром, более предпочтительно фтор, или R19 и R20 вместе предпочтительно образую метилендиоксигруппу и R10 и R17 являются такими, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 и R8 вместе образуютC3-C4-алкиленовую группу, предпочтительно C4-алкиленовую группу, R9 обозначает водород и R1 обозначает фенильное производное формулы (а), в которой R2 и R3 обозначают метоксигруппу, R18 обозначает -CH2-циклопропил, R19 и R20 вместе образуют метилендиоксигруппу, предпочтительно присоединенную к фенильному кольцу в положениях 5, 6, R10 обозначает водород, C1-C6-алкил, C5-C7 циклоалкил или -CH(CH3)-R11, R11 обозначает незамещенный фенил или гидроксигруппу и R17 является таким, как определено выше. Если R10 обозначает C1-C6-алкил, то им предпочтительно является метил, этил, изопропилизобутил, втор-бутил или трет-бутил и, если R10 обозначает С 5-C7-циклоалкил, то им предпочтительно является циклогексил. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 и R8 вместе образуютC3-C4-алкиленовую группу, предпочтительно С 4-алкиленовую группу, R9 обозначает водород и R1 обозначает фенильное производное формулы (а), в которой R2 и R3 обозначают метоксигруппу, R18 обозначает -CH2-циклопропил, R19 и R20 вместе образуют метилендиоксигруппу, предпочтительно присоединенную к фенильному кольцу в положениях 5, 6, R10 обозначает -CH2-R12, где R12 обозначает гидроксигруппу, С 5-С 7-циклоалкил, предпочтительно циклогексил, -N-(C1-C2-алкил)2, предпочтительно N(CH3)2, или -CH2-S-(C1-C2-алкил), предпочтительно -CH2-S-CH3, или бензил и R17 является таким, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 и R8 вместе образуютC3-C4-алкиленовую группу, предпочтительно C4-алкиленовую группу, R9 обозначает водород и R1 обозначает фенильное производное формулы (а), в которой R2 и R3 обозначают метоксигруппу, R18 обозначает -CH2-циклопропил, R19 и R20 вместе образуют метилендиоксигруппу, предпочтительно присоединенную к фенильному кольцу в положениях 5, 6, R10 обозначает -CH2-R12, где R12 выбран из группы,включающей имидазол-2-ил, имидазол-4-ил, пиразол-1-ил, тиофен-2-ил, тиофен-3-ил, тиазол-2-ил, тиазол-4-ил, тиазол-5-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, индол-2-ил, индол-3-ил, 1 метилиндол-2-ил или 1-метилиндол-3-ил, или R12 обозначает -CH2-C(O)-R15, где R15 обозначает гидроксигруппу, -N(R16)2, пиперидин-1-ил, пирролидин-1-ил или бензилоксигруппу, где R16 независимо друг от друга обозначают водород или C1-C4-алкил, предпочтительно C1-C3-алкил, более предпочтительно изопропил, и R17 является таким, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соедине-7 023713 нию формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 и R8 вместе образуют C3C4-алкиленовую группу, предпочтительно С 4-алкиленовую группу, R9 обозначает водород и R1 обозначает фенильное производное формулы (а), в которой R2 обозначает метоксигруппу и R3 обозначает метоксигруппу, R18 обозначает -CH2-циклопропил, R19 обозначает метоксигруппу или фтор, предпочтительно фтор, R20 обозначает метоксигруппу или фтор, предпочтительно метоксигруппу, или R19 и R20 вместе образуют метилендиоксигруппу, предпочтительно присоединенную к фенильному кольцу в положениях 5, 6, R10 обозначает -CH2-R12, где R12 обозначает незамещенный фенил и R17 является таким,как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно 1, R7 и R8 вместе образуют С 3-С 4-алкиленовую группу, предпочтительно С 4-алкиленовую группу, R9 обозначает водород и R1 обозначает фенильное производное формулы (а), в которой R2 и R3 обозначают метоксигруппу, R18 обозначает-CH2 циклопропил, R19 обозначает метоксигруппу или фтор, предпочтительно фтор, R20 обозначает метоксигруппу или фтор, предпочтительно метоксигруппу, или R19 и R20 вместе образуют метилендиоксигруппу, предпочтительно присоединенную к фенильному кольцу в положениях 5, 6, R10 обозначает -CH2R12, где R12 обозначает фенил, замещенный с помощью R13 или замещенный с помощью R13 и R14, гдеR13 и R14, а также R17 являются такими, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 и R8 вместе образуютC3-C4-алкиленовую группу, предпочтительно С 4-алкиленовую группу, R9 обозначает водород и R1 обозначает фенильное производное формулы (а), в которой R2 обозначает метоксигруппу и R3 обозначает метоксигруппу, R18 обозначает -CH2-циклопропил, R19 обозначает метоксигруппу или фтор, предпочтительно фтор, R20 обозначает метоксигруппу или фтор, предпочтительно метоксигруппу, или R19 и R20 вместе образуют метилендиоксигруппу, предпочтительно присоединенную к фенильному кольцу в положениях 5, 6, R10 обозначает -CH2-R12, где R12 обозначает фенил, замещенный с помощью R13 или замещенный с помощью R13 и R14, и R17 является таким, как определено выше. Если R12 обозначает фенил, замещенный с помощью R13, то R13 обозначает C1-C2-алкоксигруппу, C1-C4-алкил, С 1-С 2 фторалкил, фтор, хлор, бром, гидроксигруппу, фенил, -C(O)NH2 или -CN, предпочтительно, если R13 обозначает C1-C2-алкоксигруппу, метил, трет-бутил, трифторметил, фтор, хлор, гидроксигруппу, фенил,-C(O)NH2, -CN, 2-оксоазетидин-1-ил или 2-оксопирролидинил. Если R12 обозначает фенил, замещенный с помощью R13 и R14, то R13 и R14 независимо друг от друга обозначают C1-C2-алкоксигруппу, фтор,хлор или бром, предпочтительно метоксигруппу, фтор или хлор, более предпочтительно, если R13 и R14 оба обозначают метоксигруппу, фтор или хлор. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1, R7 и R8 вместе образуют C3-C4-алкиленовую группу, предпочтительно С 4-алкиленовую группу, R9 обозначает водород и R1 обозначает фенилпроизводное формулы (b), в которой R4 обозначает С 1-С 4-алкоксигруппу, предпочтительно C1-C2-алкоксигруппу, более предпочтительно метоксигруппу, R5 обозначает С 1-С 4-алкил, предпочтительно C1-C2-алкил, более предпочтительно метил,R6 обозначает водород или R5 и R6, взятые вместе и с включением двух атомов углерода, к которым они присоединены, образуют спиросочлененное 5- или 6-членное углеводородное кольцо, предпочтительно спиросочлененное 5- или 6-членное углеводородное кольцо, и R10, R17, R18, R19 и R20 являются такими, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 обозначает водород, R8 иR9 обозначают C1-C2-алкил, R1 обозначает фенильное производное формулы (а), в которой R2 обозначает С 1-С 4-алкоксигруппу и R3 обозначает С 1-С 4-алкоксигруппу, и R10, R17, R18, R19 и R20 являются такими, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 обозначает водород, R8 иR9 обозначают С 1-С 2-алкил, предпочтительно метил, R1 обозначает фенильное производное формулы(а), в которой R2 обозначает С 1-С 2-алкоксигруппу, предпочтительно метоксигруппу, и R3 обозначает С 1 С 2-алкоксигруппу, предпочтительно метоксигруппу, R10 обозначает -CH2-R12, где R12 обозначает незамещенный фенил или фенил, замещенный с помощью R13, где R13 обозначает галоген, предпочтительно фтор, хлор или бром, более предпочтительно фтор, R18 обозначает -CH2-циклопропил, R19 обозначает группу, или галоген, предпочтительно фтор, хлор или бром, более предпочтительно фтор, или R19 и R20 вместе образуют метилендиоксигруппу, которая предпочтительно присоединена к фенильному кольцу в положениях 5, 6, и R17 является таким, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 обозначает водород, R8 иR9 обозначают C1-C2-алкил, предпочтительно метил, R1 обозначает фенильное производное формулы-CH2-C(O)-R15, где R15 обозначает -N(R16)2, где R16 независимо друг от друга обозначают водород или С 1-С 4-алкил, предпочтительно водород или метил, R18 обозначает -CH2-циклопропил, R19 и R20 вместе образуют метилендиоксигруппу, которая предпочтительно присоединена к фенильному кольцу в положениях 5, 6, и R17 является таким, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 обозначает водород, R8 обозначает C1-C2-алкил, предпочтительно метил, R9 обозначает C1-C2-алкил, предпочтительно метил, иR1 обозначает фенилпроизводное формулы (b), в которой R4 обозначает C1-C4-алкоксигруппу, предпочтительно С 1-С 2-алкоксигруппу, более предпочтительно метоксигруппу, R5 обозначает С 1-С 4-алкил,предпочтительно C1-C2-алкил, более предпочтительно метил, R6 обозначает водород или R5 и R6, взятые вместе и с включением двух атомов углерода, к которым они присоединены, образуют спиросочлененное 5- или 6-членное углеводородное кольцо, предпочтительно спиросочлененное 5- или 6-членное углеводородное кольцо, и R10, R17, R18, R19 и R20 являются такими, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 обозначает водород, R8 обозначает C1-C2-алкил, предпочтительно метил, R9 обозначает C1-C2-алкил, предпочтительно метил, иR1 обозначает фенилпроизводное формулы (b), в которой R4 обозначает C1-C4-алкоксигруппу, предпочтительно C1-C2-алкоксигруппу, более предпочтительно метоксигруппу, R5 обозначает С 1-С 4-алкил,предпочтительно C1-C2-алкил, более предпочтительно метил, R6 обозначает водород и R10 обозначает водород, C1-C4-алкил, предпочтительно водород или C1-C2-алкил, более предпочтительно водород, илиR10 обозначает -CH2-R12, где R12 обозначает пиридин-2-ил, пиридин-3-ил или пиридин-4-ил, R18 обозначает -CH2-циклопропил, R19 и R20 вместе образуют метилендиоксигруппу, которая предпочтительно присоединена к фенильному кольцу в положениях 5, 6, и R17 является таким, как определено выше. В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы (1) или к стереоизомеру соединения, или к соли соединения, или к соли стереоизомера соединения, в которой m равно 1 или 2, предпочтительно, если m равно 1, R7 обозначает водород, R8 иR9, взятые вместе и с включением атома углерода, к которому они присоединены, образуют спиросочлененное 5-, 6- или 7-членное углеводородное кольцо, предпочтительно спиросочлененное 5-членное углеводородное кольцо, и R1 обозначает фенильное производное формулы (а), в которой R2 обозначаетR20 вместе образуют C1-C2-алкилендиоксигруппу и R10 и R17 являются такими, как определено выше. Предпочтительно, если R2 обозначает C1-C2-алкоксигруппу, более предпочтительно метоксигруппу, R2 обозначает C1-C2-алкоксигруппу, более предпочтительно метоксигруппу, R18 обозначает -CH2 циклопропил, R19 и R20 вместе образуют метилендиоксигруппу, R10 обозначает водород или -CH2-R12,где R12 обозначает незамещенный фенил, пиридин-2-ил, пиридин-3-ил или пиридин-4-ил, предпочтительно незамещенный фенил или пиридин-3-ил, и R17 является таким, как определено выше. Соединения, предлагаемые в настоящем изобретении, можно получить в соответствии со схемами реакций 1-3. Как показано на схеме реакций 1, соединения формулы 1, в которой R1, R7, R8, R9, R10, R17, R18,R19 и R20 обладают указанными выше значениями, можно получить по реакции сочетания карбоновой кислоты формулы (3) с первичным амином формулы (2) с использованием любой стандартной методики сочетания с образованием амидной связи, такой как например, использование реагентов сочетания, таких как HBTU, ГАТУ, TOTU, COMU, Т 3 Р, или использование активированных производных кислот, таких как имидазолиды. Обзор подходящих методик сочетания с образованием амидной связи приведен, например, в публикациях С.A.G.N. Montalbetti, V. Falque, Tetrahedron, 61 (2005), 10827-10852, и A. ElFaham, R.S. Funosas, R. Prohens, F. Albericio, Chemistry - A European Journal, 15 (2009), 9404-9416, и J. Соединения формулы (1b), (1c) и (1 е) также могут выступать в качестве исходных веществ для последующих реакций. Бензиловые эфиры соединений (1b) можно расщепить путем гидрогенолиза, который можно провести по стандартным методикам, известным специалисту в данной области техники,предпочтительно с использованием H2/Pd-C в спирте, таком как метанол или этанол, в качестве растворителя при температуре окружающей среды и при давлении водорода, равном атмосферному, и получить соответствующие производные карбоновой кислоты формулы (1 с). Соединения формулы (1d) можно получить по реакции сочетания производного карбоновой кислоты формулы (1 с) с первичным или вторичным амином формулы (7) с использованием любой стандартной методики сочетания с образованием амидной связи, такой как, например, использование реагентов сочетания, таких как HBTU, ГАТУ, TOTU или COMU. Альтернативный путь синтеза соединений формулы (1d) представлен на схеме 2 и он включает введение заместителей R22 и R23 в промежуточный продукт (2), который можно ввести в реакцию с соединением (3), и получить конечные соединения формулы (1d) в соответствии со схемой 1. Соединения формулы (1f) можно получить путем катализируемой палладием реакции сочетания соединений (1 е) и амидов формулы (8) с использованием Pd(dba)2 в качестве источника палладия, Xantphos в качестве лиганда, Cs2CO3 в качестве основания и 1,4-диоксана в качестве растворителя, при повышенных температурах (предпочтительно примерно при 140C) и, дополнительно, при нагревании микроволновым излучением. Получение карбоновых кислот формулы (3) описано в WO 2011/023693 и WO 2009/106531 или их можно получить по методикам, аналогичным описанным в настоящем изобретении. В случае, если Q обозначает имидазолил, методика получения этих соединений известно специалисту в данной области техники. На схеме реакций 2 представлен синтез соединений формулы (2). На первой стадии соединения формулы (4) вводят в реакцию с соединениями формулы (5) с использованием любой стандартной методики сочетания с образованием амидной связи, такой как например, использование реагентов сочетания,таких как HBTU, ГАТУ, TOTU, COMU, T3P, или использование активированных производных кислот,таких как имидазолиды. Обзор подходящих методик сочетания с образованием амидной связи приведен,например, в публикациях С.A.G.N. Montalbetti, V. Falque, Tetrahedron, 61 (2005), 10827-10852, и А. ElFaham, R.S. Funosas, R. Prohens, F. Albericio, Chemistry - A European Journal, 15 (2009), 9404-9416, и J.Glauder, Speciality Chemicals Magazine, 24(2004), 30-31. Первичный амин формулы (2) можно получить из соответствующих содержащих N-трет-бутоксикарбонильную защитную группу соединений формулы (6) с использованием стандартных условий удаления трет-бутоксикарбонильной группы, таких как, например, использование хлорида водорода или трифторуксусной кислоты в подходящем растворителе, таком как диоксан, тетрагидрофуран или дихлорметан. Соединения формулы (5) имеются в продаже или их можно получить из имеющихся в продаже предшественников по стандартным методикам, известным специалисту в данной области техники. Содержащие защитную группу N-Boc аминокислоты формулы (5 с) можно синтезировать с помощью двустадийной последовательности, проводя сначала реакцию образования амидной связи соединения (5 а) с первичным амином (14) с использованием любой стандартной методики сочетания с образованием амидной связи, такой как, например, использование реагентов сочетания, таких как HBTU, ГАТУ, TOTU или COMU, и затем расщепление бензилового эфира путем гидрогенолиза, который можно провести по стандартным методикам, известным специалисту в данной области техники, предпочтительно с использованием H2/Pd-С в спирте, таком как метанол или этанол, в качестве растворителя при температуре окружающей среды и при давлении водорода, равном атмосферному. Схема реакций 2 Синтез промежуточного продукта (9) представлен на схеме 3. Реакция Фриделя-Крафтса 1,2 диметоксибензола (10) с соединением (11) в присутствии хлорида алюминия дает -кетокислоту (12),которую можно ввести в реакцию с 4-гидразинилпиперидином (13) и получить соединение (9). Получение соединений формулы (4) описано в WO 2005075457 и WO 2005075456, или эти соединения можно получить по методикам, аналогичным описанным в настоящем изобретении. В ходе реакций сочетания с образованием амида с получением соединений формулы (6) и формулы(1) при использующихся условиях проведения реакций могут образовываться смеси диастереоизомеров или энантиомеров вследствие эпимеризации по стереогенному центру C-R10. Схема реакций 3 В соответствии с определением n и R10, R10 может быть образован из альфа-аминокислот, таких как фенилаланин, тирозин, глицин, серин, аланин и треонин, или из бета-аминокислот, таких как бетааланин или бета-фенилаланин. Исходными веществами, подходящими для синтеза R10, являются N-(трет-бутоксикарбонил)-3,5 дифтор-D-фенилаланин, N-(трет-бутоксикарбонил)-3-метил-L-фенилаланин, N-(трет-бутоксикарбонил)4-трет-бутил-D-фенилаланин, N-(трет-бутоксикарбонил)-4-карбамоил-D-фенилаланин, N-(трет-бутокси- 11023713 карбонил)-4-карбамоил-D-фенилаланин, N-(трет-бутоксикарбонил)-O-этил-D-тирозин, (2R)-3-(бифенил 4-ил)-2-[(трет-бутоксикарбонил)амино]пропановая кислота,N-(трет-бутоксикарбонил)-4-циано-Dфенилаланин, N-(трет-бутоксикарбонил)-4-метил-D-фенилаланин, N-(трет-бутоксикарбонил)-3-метил-Dфенилаланин,N-(трет-бутоксикарбонил)-3,4-дифтор-D-фенилаланин,N-(трет-бутоксикарбонил)-3 метокси-O-метил-L-тирозин,N-(трет-бутоксикарбонил)-4-хлор-D-фенилаланин,N-(трет-бутоксикарбонил)-4-фтор-D-фенилаланин, N-(трет-бутоксикарбонил)-O-метил-D-тирозин, N-(трет-бутоксикарбонил)-3-хлор-D-фенилаланин, N-(трет-бутоксикарбонил)-D-фенилаланин, N-(трет-бутоксикарбонил)-2(трифторметил)-D-фенилаланин, N-(трет-бутоксикарбонил)-2-хлор-D-фенилаланин, N-(трет-бутоксикарбонил)-L-фенилаланин, (бета-R)-N-(трет-бутоксикарбонил)-бета-метил-D-фенилаланин, N-(третбутоксикарбонил)-3-пиридин-2-ил-L-аланин, N-(трет-бутоксикарбонил)-3-пиридин-4-ил-L-аланин, N(трет-бутоксикарбонил)-3-пиридин-3-ил-L-аланин, N-(трет-бутоксикарбонил)-4-фтор-L-фенилаланин, N(трет-бутоксикарбонил)-2,4-дихлор-D-фенилаланин, N-(трет-бутоксикарбонил)-4-(трифторметил)-D-фенилаланин, N-(трет-бутоксикарбонил)-D-тирозин, N-(трет-бутоксикарбонил)-L-тирозин, N-(третбутоксикарбонил)-2-хлор-L-фенилаланин,N-(трет-бутоксикарбонил)-O-метил-D-тирозин,N-(третбутоксикарбонил)глицин, N-(трет-бутоксикарбонил)-L-серин, N-(трет-бутоксикарбонил)-L-аланин, N(трет-бутоксикарбонил)-D-аланин, N-(трет-бутоксикарбонил)-D-треонин, (2S)-2-[(трет-бутоксикарбонил)амино]бутановая кислота и (2R)-2-[(трет-бутоксикарбонил)амино]-4-фенилбутановая кислота. Специалисту в данной области техники известно, что, если в исходных или промежуточных соединениях имеется целый ряд реакционноспособных центров, то, чтобы реакция протекала именно по необходимому реакционноспособному центру, может быть необходимым временное блокирование одного или большего количества реакционноспособных центров с помощью защитных групп. Подробное описание использования известных защитных групп приведено, например, в публикациях Т.W. Greene, Protective Groups in Organic Synthesis, John WileySons, 1999, 3rd Ed., или Р. Kocienski, Protecting Groups,Thieme Medical Publishers, 2000. Соединения, предлагаемые в настоящем изобретении, выделяют и очищают по известным методикам, например, путем отгонки растворителя в вакууме и перекристаллизации полученного остатка из подходящего растворителя или использования одной из обычных методик очистки, таких как колоночная хроматография на подходящем носителе. Как должны понимать специалисты в данной области техники, настоящее изобретение не ограничивается конкретными вариантами осуществления, описанными в настоящем изобретении, а включает все модификации указанных вариантов осуществления, которые входят в сущность и объем настоящего изобретения, определенные прилагаемой формулой изобретения. Приведенные ниже примеры подробнее иллюстрируют настоящее изобретение без его ограничения. Дополнительные соединения, предлагаемые в настоящем изобретении, получение которых не описано подробно, можно получить аналогичным образом. Соединения, которые указаны в примерах, представляют собой предпочтительные варианты осуществления настоящего изобретения. Примеры Используются следующие аббревиатуры. КДИ: 1,1'-карбонил-бис-1 Н-имидазол;(об./об./об./об.): (объем/объем/объем/объем); ИЭР: ионизация электрораспылением; МС: масс-спектрометрия; МСВР: масс-спектрометрия высокого разрешения; ТСХ: тонкослойная хроматография; ВЭЖХ: высокоэффективная жидкостная хроматография. Если не указано иное, очистку соединений проводят с помощью колоночной флэш-хроматографии,препаративной ТСХ и препаративной ВЭЖХ. Очистку с помощью ВЭЖХ проводят с использованием колонки Phenomenex Gemini 5 мкм C18 (7530 мм) или Phenomenex Gemini 5 мкм C6-фенил (7530 мм) или Phenomenex Gemini 5 мкм C18 Axia (7530 мм), в двойном градиентном режиме (растворитель А: вода, растворитель В: ацетонитрил), при скорости потока, равной 40 мл/мин, с использованием в качестве буфера муравьиной кислоты или буферной системы, содержащей муравьиную кислоту и формиат аммония, и с УФ-детектированием при 240 нм. При использовании в настоящем изобретении термин "ЭИ" или "энантиомерный избыток" означает выраженный в процентах избыток одного энантиомера Е 1 в смеси обоих энантиомеров (Е 1+Е 2), рассчитанный по уравнению Энантиомерный избыток (ЭИ) определяли с помощью ВЭЖХ с использованием колонки ChiralcelOD-RH (1504,6 мм) [подвижная фаза: 100 мМ KPF6, pH 2/ацетонитрил (70/30)], при скорости потока,равной 0,6 мл/мин, и с УФ-детектированием при 220 и 316 нм. Все масс-спектры снимали с использованием методики ИЭР. Данные МСВР для примеров 1-125 приведены в виде МН+. Конечные продукты. Химические названия образованы с помощью программного обеспечения ACD/NAME Library DLL:NAMIPLIB.dll; Version: 11.1.0.22379. 1. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-3-(3,5-дифторфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (110 мг; соединение В 71) и ДИПЭА (0,20 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-2-1[(2R)-2-амино-3-(3,5-дифторфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-он (172 мг; соединение В 14) и COMU (146 мг) и реакционную смесь перемешивали при КТ в течение 4 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.); 2) силикагель, элюент: ДХМ/MeOH,98/2 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C48H49N7O8F2]: рассчитано: 890,3683; найдено: 890,3681. 2. 4-[2-(Циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(3-метилфенил)-1 оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (139 мг; соединение В 12) и ДИПЭА (0,25 мл) в ДХМ (2 мл) добавляли(4aS,8aR)-2-1-[(2S)-2-амино-3-(3-метилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-он (200 мг; соединение В 13) и COMU (177 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C50H56N7O7F]: рассчитано: 886,4298; найдено: 886,4297. 3. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(3-метилфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (71 мг; соединение В 71) и ДИПЭА (0,13 мл) в ДХМ (2 мл) добавляли (4aS,8aR)-2-1[(2S)-2-амино-3-(3-метилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-он (106 мг; соединение В 13) и COMU (94 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы су- 13023713 шили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C49H53N7O8]: рассчитано: 868,4028; найдено: 868,4025. 4. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(3-метилфенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (138 мг; соединение В 72) и ДИПЭА (0,25 мл) в ДХМ (3 мл) добавляли (4aS,8aR)2-1-[(2S)-2-амино-3-(3-метилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-он (200 мг; соединение В 13) и COMU (177 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C50H55N7O8]: рассчитано: 882,4185; найдено: 882,4176. 5. N-[(2R)-3-(4-трет-Бутилфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[2-(циклопропилметокси)-5-фтор-4 метоксифенил]-6-метил-5 Н-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (142 мг; соединение В 12) и ДИПЭА (0,25 мл) в ДХМ (3 мл) добавляли(4aS,8aR)-2-1-[(2R)-2-амино-3-(4-трет-бутилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-он (224 мг; соединение В 11) и COMU (180 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C53H62N7O7F]: рассчитано: 928,4768; найдено: 928,4763. 6. N-[(2R)-3-(4-трет-Бутилфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (71 мг; соединение В 71) и ДИПЭА (0,13 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-2-1[(2R)-2-амино-3-(4-трет-бутилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-он (115 мг; соединение В 11) и COMU (95 мг) и реакционную смесь перемешивали при КТ в течение 4 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C52H59N7O8]: рассчитано: 910,4498; найдено: 910,4492. 7. N-[(2R)-3-(4-Карбамоилфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (138 мг; соединение В 71) и ДИПЭА (0,26 мл) в ДХМ (3 мл) добавляли 4-[(2R)-2 амино-3-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-оксопропил]бензамид (220 мг; соединение В 9) и COMU (184 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и затем с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C49H52N8O9]: рассчитано: 897,3930; найдено: 897,3924. 8. 4-[2-(Циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(4-этоксифенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (144 мг; соединение В 12) и ДИПЭА (0,25 мл) в ДХМ (3 мл) добавляли(4aS,8aR)-2-1-[(2R)-2-амино-3-(4-этоксифенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-он (219 мг; соединение В 10) и COMU (183 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органиче- 14023713 ские фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C51H58N7O8F]: рассчитано: 916,4404; найдено: 916,4396. 9. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(4-этоксифенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (71 мг; соединение В 71) и ДИПЭА (0,13 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-21-[(2R)-2-амино-3-(4-этоксифенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-он (113 мг; соединение В 10) и COMU (95 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C50H55N7O9]: рассчитано: 898,4134; найдено: 898,4123. 10. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(4-этоксифенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (143 мг; соединение В 72) и ДИПЭА (0,25 мл) в ДХМ (3 мл) добавляли (4aS,8aR)2-1-[(2R)-2-амино-3-(4-этоксифенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-он (219 мг; соединение В 10) и COMU (183 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C51H57N7O9]: рассчитано: 912,4291; найдено: 912,4283. 11. N-[(2R)-3-(4-Карбамоилфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5 Н-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (144 мг; соединение В 72) и ДИПЭА (0,26 мл) в ДХМ (3 мл) добавляли 4-[(2R)-2 амино-3-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-оксопропил]бензамид (220 мг; соединение В 9) и COMU (184 мг) и реакционную смесь перемешивали при КТ в течение 5 ч. Дополнительно добавляли COMU (40 мг) и для завершения реакции реакционную смесь перемешивали в течение 12 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C50H54N8O9]: рассчитано: 911,4087; найдено: 911,4082. 12. N-[(2R)-3-(Бифенил-4-ил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (140 мг; соединение В 72) и ДИПЭА (0,25 мл) в ДХМ (3 мл) добавляли (4aS,8aR)2-1-[(2R)-2-амино-3-(бифенил-4-ил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-он (200 мг; соединение В 8) и COMU (179 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. MCBP [C55H57N7O8]: рассчитано: 944,4341; найдено: 944,4368. 13. N-[(2R)-3-(Бифенил-4-ил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (134 мг; соединение В 71) и ДИПЭА (0,25 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-21-[(2R)-2-амино-3-(бифенил-4-ил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-он (226 мг; соединение В 8) и HBTU (158 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Получен- 15023713 ный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.)] и дважды с помощью колоночной флэшхроматографии с использованием силикагеля [силикагель, элюент: ДХМ/MeOH, 98/2 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества.N-[(2R)-3-(4-Цианофенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (135 мг; соединение В 72) и ДИПЭА (0,24 мл) в ДХМ (3 мл) добавляли 4-[(2R)-2 амино-3-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-оксопропил]бензонитрил (200 мг; соединение В 3) и COMU (173 мг) и реакционную смесь перемешивали при КТ в течение 5 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.)] и затем с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C50H52N88]O: рассчитано: 893,3981; найдено: 893,3963. 15. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(4-метилфенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (129 мг; соединение В 72) и ДИПЭА (0,23 мл) в ДХМ (3 мл) добавляли (4aS,8aR)2-1-[(2R)-2-амино-3-(4-метилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-онгидрохлорид (200 мг; соединение В 5) и COMU (166 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Для завершения реакции дополнительно добавляли COMU(80 мг). Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВРN-[(2R)-3-(4-Цианофенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (130 мг; соединение В 71) и ДИПЭА (0,24 мл) в ДХМ (3 мл) добавляли 4-[(2R)-2-амино-34-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1 ил-3-оксопропил]бензонитрил (200 мг; соединение В 3) и COMU (173 мг) и реакционную смесь перемешивали при КТ в течение 2 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.); 2) силикагель, элюент: ДХМ/MeOH,98/2 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C49H50N8O8]: рассчитано: 879,3824; найдено: 879,3811. 17. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(3-метилфенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (129 мг; соединение В 72) и ДИПЭА (0,23 мл) в ДХМ (3 мл) добавляли (4aS,8aR)2-1-[(2R)-2-амино-3-(3-метилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-онгидрохлорид (200 мг; соединение В 4) и COMU (166 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C50H55N7O8]: рассчитано: 882,4185; найдено: 882,4176. 18. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-3-(3,4-дифторфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1 оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин- 16023713 7-карбоновой кислоты (124 мг; соединение В 72) и ДИПЭА (0,22 мл) в ДХМ (3 мл) добавляли (4aS,8aR)2-1-[(2R)-2-амино-3-(3,4-дифторфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорид (200 мг; соединение В 7) и COMU (159 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C49H51N7O8F2]: рассчитано: 904,3840; найдено: 904,3819. 19. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-3-(3,4-дифторфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1 оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (119 мг; соединение В 71) и ДИПЭА (0,22 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-2-1[(2R)-2-амино-3-(3,4-дифторфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-онгидрохлорид (200 мг; соединение В 7) и COMU (159 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C48H49N7O8F2]: рассчитано: 890,3683; найдено: 890,3680. 20. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(3-метилфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (124 мг; соединение В 71) и ДИПЭА (0,23 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-21-[(2R)-2-амино-3-(3-метилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-онгидрохлорид (200 мг; соединение В 4) и COMU (166 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.); 2) силикагель, элюент: ДХМ/MeOH, 98/2 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C49H53N7O8]: рассчитано: 868,4028; найдено: 868,4014. 21. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(4-метилфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (124 мг; соединение В 71) и ДИПЭА (0,23 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-21-[(2R)-2-амино-3-(4-метилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-онгидрохлорид (200 мг; соединение В 5) и COMU (166 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.); 2) силикагель, элюент: ДХМ/MeOH, 98/2 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C49H53N7O8]: рассчитано: 868,4028; найдено: 868,4021. 22. 4-[2-(Циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2 ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2R)-2-амино-3-фенилпропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (556 мг; соединение В 59), 4-[2(циклопропилметокси)-5-фтор-4-метоксифенил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (371 мг; соединение В 12) и ГАТУ (434 мг) в ДХМ (15 мл) добавляли ДИПЭА (0,49 мл) и смесь перемешивали при КТ в течение 75 мин. Затем добавляли насыщенный водный раствор бикарбоната натрия (10 мл) и ДХМ (15 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 100/0 до 95/5 (об./об.)] и получали искомое соединение в виде твердого вещества. МСВР [C49H55FN7O7]: рассчитано: 872,4142; найдено: 872,4147. 23. 4-[2-(Циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметокси- 17023713(250 мг; соединение В 17) и ГАТУ (319 мг) в ДХМ (15 мл) добавляли ДИПЭА (0,36 мл) и смесь перемешивали при КТ в течение 75 мин. Затем добавляли насыщенный водный раствор бикарбоната натрия (10 мл) и ДХМ (15 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: от смеси EtOAc/циклогексан до EtOAc и затем до смеси EtOAc/MeOH, от 1/1 до 95/5 (об./об.)] и получали искомое соединение в виде твердого вещества. МСВР [C48H53FN7O7]: рассчитано: 858,3985; найдено: 858,3996. 24. 4-[2-(Циклопропилметокси)-4-фтор-5-метоксифенил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2R)-2-амино-3-фенилпропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (278 мг; соединение В 59), 4-[2(циклопропилметокси)-4-фтор-5-метоксифенил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты(179 мг; соединение В 18) и ГАТУ (228 мг) в ДХМ (15 мл) добавляли ДИПЭА (0,31 мл) и смесь перемешивали при КТ в течение 75 мин. Затем добавляли насыщенный водный раствор бикарбоната натрия (10 мл) и ДХМ (15 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: от смеси EtOAc/циклогексан до EtOAc и затем до смеси EtOAc/MeOH, от 1/1 до 95/5 (об./об.)] и получали искомое соединение в виде твердого вещества. МСВР [C48H53FN7O7]: рассчитано: 858,3985; найдено: 858,3979. 25. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-3-(3,4-диметоксифенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1 оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (246 мг; соединение В 71) и ДИПЭА (0,46 мл) в ДХМ (5 мл) добавляли HBTU (291 мг). Реакционную смесь перемешивали при КТ в течение 0,5 ч и затем добавляли (4aS,8aR)-2-1-[(2S)-2 амино-3-(3,4-диметоксифенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорид (403 мг; соединение В 6) и реакционную смесь перемешивали при КТ в течение 2 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 100/0 до 98/2 (об./об.); 2) силикагель,элюирование в градиентном режиме: ДХМ/MeOH, от 98/2 до 95/5 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C50H56N7O10]: рассчитано: 914,4083; найдено: 914,4095. 26. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2R)-2-амино-3-фенилпропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-она(519 мг; соединение В 52),4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5 Н-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (368 мг; соединение В 72) и COMU (493 мг) в ДХМ (10 мл) добавляли ДИПЭА (162 мг) и смесь перемешивали при КТ в течение 1 ч. Дополнительно добавляли COMU (214 мг) и после перемешивания в течение 1,5 ч еще одну порцию COMU (428 мг) добавляли и для завершения реакции смесь перемешивали при КТ в течение 12 ч. Смесь экстрагировали насыщенным водным раствором бикарбоната натрия(35 мл) и фильтровали с помощью устройства для разделения фаз. Органический слой концентрировали в вакууме и полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: циклогексан/EtOAc/MeOH, от 100/0/0 до 0/100/0 и затем до 0/94/6 (об./об./об.)]. После лиофилизации из смеси ацетонитрил/вода (4/1(об./об. получали искомое соединение в виде твердого вещества. МСВР [C49H53N7O8]: рассчитано: 868,4028; найдено: 868,4017. 27. К суспензии (4aS,8aR)-2-1-[(2R)-2-амино-3-(4-хлорфенил)пропаноил]пиперидин-4-ил-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-она (1,51 г; соединение В 20), 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (967 мг; соединение В 71) и COMU (1,29 г) в ДХМ (25 мл) добавляли ДИПЭА (1,86 мл) и смесь перемешивали при КТ в течение 45 мин. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия (100 мл) и смесь экстрагировали с помощью ДХМ (2200 мл). Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток сначала очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: от циклогексана до EtOAc и затем до смеси EtOAc/MeOH, 9/1 (об./об.)], вторую очистку проводили с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: ДХМ/MeOH, от 1/0 до 9/1 (об./об.)], третью очистку проводили с помощью препаративной ТСХ [пластины для ТСХ 2020 см толщиной 2 мм, элюент: ДХМ/MeOH/NEt3, 87/10/3 (об./об./об.) и затем использовали элюент: ДХМ/EtOAc/MeOH, 80/12/8 (об./об./об.)] и заключительную очистку проводили с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C48H51ClN7O8]: рассчитано: 888,3482; найдено: 888,3494. 28. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(4-фторфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (1,05 г; соединение В 71) и ДИПЭА (1,94 г) в ДХМ (40 мл) добавляли COMU (1,39 г). После перемешивания в течение 5 мин добавляли (4aS,8aR)-2-1-[(2R)-2-амино-3-(4-фторфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорид(1,7 г; соединение В 26) и реакционную смесь перемешивали при КТ в течение 1 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент: ДХМ/MeOH,от 100/0 до 98/2 и затем до 97/3 (об./об./об.); 2) силикагель, элюент: ДХМ/MeOH, от 100/0 до 98/2 и затем до 97/3 (об./об./об.)]. Выделенный продукт растворяли в метаноле, обрабатывали древесным углем и фильтровали через слой целита. Растворитель удаляли в вакууме и после лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C48H51FN7O8]: рассчитано: 872,3778; найдено: 872,3777. 29. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(4-метоксифенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (490 мг; соединение В 71) и ДИПЭА (0,91 мл) в ДХМ (20 мл) добавляли HBTU (579 мг). После перемешивания в течение 5 мин добавляли (4aS,8aR)-2-1-[(2R)-2-амино-3-(4-метоксифенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорид (812 мг; соединение В 25) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент:EtOAc/MeOH, от 100/0 до 98/2 (об./об.); 2) силикагель, элюент: ДХМ/MeOH, от 100/0 до 98/2 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C49H54N7O9]: рассчитано: 884,3976; найдено: 884,3995. 30.N-[(2R)-3-(3-Хлорфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2R)-2-амино-3-(3-хлорфенил)пропаноил]пиперидин-4-ил-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-она (1,38 г; соединение В 19), 4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (879 мг; соединение В 71) и COMU (1,17 г) в ДХМ (25 мл) добавляли ДИПЭА (1,69 мл) и смесь перемешивали при КТ в течение 75 мин. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия (100 мл) и смесь экстрагировали с помощью ДХМ (2200 мл). Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток сначала очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: от циклогексана до EtOAc и затем до смеси EtOAc/MeOH, 9/1 (об./об.)], вторую очистку проводили с помощью колоночной флэш- 19023713 хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: ДХМ/MeOH, от 1/0 до 9/1 (об./об.)] и заключительную очистку проводили с помощью препаративной ТСХ [пластины для ТСХ 2020 см толщиной 2 мм, элюент: ДХМ/MeOH/NEt3, 87/10/3 (об./об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C48H51ClN7O8]: рассчитано: 888,3482; найдено: 888,3491. 31. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2R)-2-амино-3-фенилпропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-она (519 мг; соединение В 52), 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (353 мг; соединение В 71) и COMU (493 мг) в ДХМ (10 мл) добавляли ДИПЭА (162 мг) и смесь перемешивали при КТ в течение 1 ч. Дополнительно добавляли COMU (214 мг) и реакционную смесь перемешивали при КТ в течение еще 1,5 ч. Смесь экстрагировали насыщенным водным раствором бикарбоната натрия (35 мл) и фильтровали с помощью устройства для разделения фаз. Органический слой концентрировали в вакууме и полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: циклогексан/EtOAc/MeOH, от 100/0/0 до 0/100/0 и затем до 0/94/6 (об./об./об.)]. После лиофилизации из смеси ацетонитрил/вода (5/1 (об./об. получали искомое соединение в виде твердого вещества. МСВР [C48H51N7O8]: рассчитано: 854,3872; найдено: 854,3872. 32. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-[2-(трифторметил)фенил]пропан-2-ил-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-(1-(2R)-2-амино-3-[2-(трифторметил)фенил]пропаноилпиперидин-4-ил)4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (280 мг; соединение В 1), 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (165 мг; соединение В 72) и ГАТУ (190 мг) в ДХМ (4 мл) добавляли ДИПЭА (0,31 мл) и смесь перемешивали при КТ в течение 0,5 ч. Дополнительно добавляли (4aS,8aR)-2-(1-(2R)-2-амино-3[2-(трифторметил)фенил]пропаноилпиперидин-4-ил)-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорид (140 мг) и ГАТУ (95 мг) и для завершения реакции смесь перемешивали при КТ в течение 20 мин. Затем добавляли насыщенный водный раствор бикарбоната натрия (3 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 100/0 до 95/5 (об./об.)] и затем с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C50H53F3N7O8]: рассчитано: 936,3902; найдено: 936,3901. 33. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-[2-(трифторметил)фенил]пропан-2-ил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-(1-(2R)-2-амино-3-[2-(трифторметил)фенил]пропаноилпиперидин-4-ил)4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (280 мг; соединение В 1), 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (165 мг; соединение В 71) и ГАТУ (180 мг) в ДХМ (4 мл) добавляли ДИПЭА (0,31 мл) и смесь перемешивали при КТ в течение 1 ч. Затем добавляли насыщенный водный раствор бикарбоната натрия (3 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэш-хроматографии[модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 97/3 до 95/5 (об./об.)] и затем с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C49H51F3N7O8]: рассчитано: 922,3746; найдено: 922,3766. 34. N-[(2R)-3-(2-Хлорфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2R)-2-амино-3-(2-хлорфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (265 мг; соединение В 23), 4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (195 мг; соединение В 72) и COMU (289 мг) в ДХМ (10 мл) добавляли ДИПЭА (0,46 мл) и смесь перемешивали при КТ в течение 1 ч. Для завершения реакции дополнительно добавляли (4aS,8aR)-2-1[(2R)-2-амино-3-(2-хлорфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорид (106 мг; соединение В 23) и COMU (289 мг). Затем добавляли насыщенный водный раствор бикарбоната натрия (2,5 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [первая очистка: модифицированный аминогруппами силикагель, элюирование в градиентном режиме: от циклогексана до EtOAc и затем до смеси EtOAc/MeOH, 9/1 (об./об.); вторая очистка: от циклогексана до EtOAc и затем до смесиEtOAc/MeOH, 94/6 (об./об.)] и затем с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C49H53ClN7O8]: рассчитано: 902,3639; найдено: 902,3654. 35. N-[(2R)-3-(2-Хлорфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2R)-2-амино-3-(2-хлорфенил)пропаноил]пиперидин-4-ил-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (265 мг; соединение В 23), 4[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты(159 мг; соединение В 71) и COMU (289 мг) в ДХМ (10 мл) добавляли ДИПЭА (0,46 мл) и смесь перемешивали при КТ в течение 1 ч. Затем добавляли насыщенный водный раствор бикарбоната натрия (2,5 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэш-хроматографии[модифицированный аминогруппами силикагель, элюирование в градиентном режиме: от циклогексана до EtOAc и затем до смеси EtOAc/MeOH, 9/1 (об./об.)]. МСВР [C48H51ClN7O8]: рассчитано: 888,3482; найдено: 888,3483. 36. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии(4aS,8aR)-2-1-[(2S)-2-амино-3-фенилпропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (333 мг; соединение В 58), 4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (212 мг; соединение В 71) и HBTU (250 мг) в ДХМ (5 мл) добавляли ДИПЭА (0,42 мл) и смесь перемешивали при КТ в течение 45 мин. Затем к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия (10 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток сначала очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 95/5 до 90/10 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C48H52N7O8]: рассчитано: 854,3872; найдено: 854,3870. 37. 4-[2-(Циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R,3R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-фенилбутан-2 ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (114 мг; соединение В 12) и ДИПЭА (0,20 мл) в ДХМ (3 мл) добавляли(4aS,8aR)-2-1-[(2R,3R)-2-амино-3-фенилбутаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-он (164 мг; соединение В 40) и COMU (145 мг) и реакционную смесь перемешивали при КТ в течение 4 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь несколько раз экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.); 2) силикагель, элюент: ДХМ/MeOH, 98/2 (об./об.)] и с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C50H56N7O7F]: рассчитано: 886,4298; найдено: 886,4290. 38. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-(пиридин-2-ил)пропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2S)-2-амино-3-(пиридин-2-ил)пропаноил]пиперидин-4-ил-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (260 мг; соединение В 21), 4[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (184 мг; соединение В 72) и ГАТУ (175 мг) в ДХМ (4 мл) добавляли ДИПЭА (0,35 мл) и смесь перемешивали при КТ в течение 40 мин. Дополнительно добавляли ГАТУ (примерно 170 мг) и после перемешивания в течение 30 мин для завершения реакции дополнительно добавляли ГАТУ (примерно 170 мг), (4aS,8aR)-2-1-[(2S)-2-амино-3-(пиридин-2-ил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорид (260 мг) и ДИПЭА (примерно 0,18 мл). После перемешивания при КТ в течение 30 мин к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия (2 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Органический слой концентрировали при пониженном давлении и полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 100/0 до 93/7 (об./об.)] и затем с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C48H53N8O8]: рассчитано: 869,3981; найдено: 869,3983. 39. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-(пиридин-2-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2S)-2-амино-3-(пиридин-2-ил)пропаноил]пиперидин-4-ил-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (260 мг; соединение В 21), 4[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты(177 мг; соединение В 71) и COMU (236 мг) в ДХМ (3 мл) добавляли ДИПЭА (0,35 мл) и смесь перемешивали при КТ в течение 3 ч. Затем добавляли насыщенный водный раствор бикарбоната натрия (2 мл),фазы разделяли и органическую фазу сушили над сульфатом натрия. Органический слой концентрировали при пониженном давлении и полученный остаток сначала очищали с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме:EtOAc/MeOH, от 100/0 до 92,5/7,5 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C47H51N8O8]: рассчитано: 855,3824; найдено: 855,3822. 40. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-(пиридин-4-ил)пропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2S)-2-амино-3-(пиридин-4-ил)пропаноил]пиперидин-4-ил-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (545 мг; соединение В 64), 4[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (386 мг; соединение В 72) и COMU (493 мг) в ДХМ (4 мл) добавляли ДИПЭА (0,71 мл) и смесь перемешивали при КТ в течение. Для завершения реакции через 1 ч и через 3 ч дополнительно добавлялиCOMU (493 мг соответственно). Затем добавляли насыщенный водный раствор бикарбоната натрия (10 мл) и ДХМ (10 мл) и фазы разделяли и сушили над сульфатом натрия. Органический слой концентрировали при пониженном давлении и полученный остаток очищали с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме:EtOAc/MeOH, от 100/0 до 95/5 (об./об.)] и затем с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C48H53N8O8]: рассчитано: 869,3981; найдено: 869,4003. 41. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-(пиридин-4-ил)пропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2S)-2-амино-3-(пиридин-4-ил)пропаноил]пиперидин-4-ил-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (545 мг; соединение В 64), 4[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты(371 мг; соединение В 71) и COMU (493 мг) в ДХМ (4 мл) добавляли ДИПЭА (0,71 мл) и смесь перемешивали при КТ в течение 45 мин. Затем добавляли насыщенный водный раствор бикарбоната натрия (10 мл) и ДХМ (10 мл) и фазы разделяли с помощью устройства для разделения фаз. Органический слой концентрировали при пониженном давлении и полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 100/0 до от 95/5 до 90/10 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C47H51N8O8]: рассчитано: 855,3824; найдено: 855,3822. 42. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-(пиридин-3-ил)пропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2S)-2-амино-3-(пиридин-3-ил)пропаноил]пиперидин-4-ил-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-она (368 мг; соединение В 22), 4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (260 мг; соединение В 72) и HBTU (295 мг) в ДХМ (12 мл) добавляли ДИПЭА (0,48 мл) и смесь перемешивали при КТ в течение 1 ч. Затем добавляли ДХМ (25 мл) и насыщенный водный раствор бикарбоната натрия (10 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Органический слой концентрировали при пониженном давлении и полученный остаток очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюирование в градиентном режиме: от циклогексана до смесиEtOAc/MeOH, 92/8 (об./об.); 2) от циклогексана до смеси EtOAc/MeOH, 95/5 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР К суспензии (4aS,8aR)-2-1-[(2S)-2-амино-3-(пиридин-3-ил)пропаноил]пиперидин-4-ил-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-она (260 мг; соединение В 22), 4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (177 мг; соединение В 71) и HBTU (209 мг) в ДХМ (10 мл) добавляли ДИПЭА (0,34 мл) и смесь перемешивали при КТ в течение 1,5 ч. Затем добавляли ДХМ (15 мл) и насыщенный водный раствор бикарбоната натрия (5 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Органический слой концентрировали при пониженном давлении и полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: от циклогексана до EtOAc и затем до смесиEtOAc/MeOH, 90/10 (об./об.). После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C47H51N8O8]: рассчитано: 855,3824; найдено: 855,3827. 44. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aR,8aS)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aR,8aS)-2-1-[(2S)-2-амино-3-фенилпропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (550 мг; соединение В 67, 4-[5-(циклоропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (349 мг; соединение В 71) и ГАТУ (429 мг) в ДХМ (10 мл) добавляли ДИПЭА (0,48 мл) и смесь перемешивали при КТ в течение 12 ч. Затем добавляли насыщенный водный раствор бикарбоната натрия (8 мл) и ДХМ(20 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме:EtOAc/MeOH, от 100/0 до 95/5 (об./об.)] и получали искомое соединение в виде твердого вещества. МСВР [C48H51N7O8]: рассчитано: 854,3872; найдено: 854,3862. 45. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aR,8aS)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aR,8aS)-2-1-[(2R)-2-амино-3-фенилпропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-она (330 мг; чистота 78%, соединение В 70), 4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (177 мг; соединение В 71) и ГАТУ (202 мг) в ДХМ (10 мл) добавляли ДИПЭА (0,26 мл) и смесь перемешивали при КТ в течение примерно 1 ч. Затем добавляли насыщенный водный раствор бикарбоната натрия (10 мл) и ДХМ (25 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюирование в градиентном режиме EtOAc/MeOH, от 100/0 до 95/5 (об./об.); 2) EtOAc/MeOH, от 100/0 до 97/3 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода (30 мл, 1/1 (об./об. получали искомое соединение в виде твердого вещества. МСВР [C48H51N7O8]: рассчитано: 854,3872; найдено: 854,3862. 46. N-[(2R)-3-(4-трет-Бутилфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3 бензодиоксол-4-ил]-6-метил-5 Н-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (143 мг; соединение В 72) и ДИПЭА (0,25 мл) в ДХМ (3 мл) добавляли (4aS,8aR)2-1-[(2R)-2-амино-3-(4-трет-бутилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-он (224 мг; соединение В 11) и COMU (183 мг) и реакционную смесь перемешивали при КТ в течение 4 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C53H61N7O8]: рассчитано: 924,4654; найдено: 924,4656. 47. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(4-фторфенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (101 мг; соединение В 71) и ДИПЭА (0,19 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-2-1[(2S)-2-амино-3-(4-фторфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-он (154 мг; соединение В 15) и COMU (135 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C48H50N7O8F]: рассчитано: 872,3778; найдено: 872,3772. 48. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-3-(2,4-дихлорфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (102 мг; соединение В 71) и ДИПЭА (0,19 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-2-1[(2R)-2-амино-3-(2,4-дихлорфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 агексагидрофталазин-1(2H)-он (170 мг; соединение В 16) и COMU (136 мг) и реакционную смесь перемешивали при КТ в течение 2 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.); 2) силикагель, элюент: ДХМ/MeOH, 98/2(об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C48H49N7O8Cl2]: рассчитано: 922,3092; найдено: 922,3086. 49. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-[4-(трифторметил)фенил]пропан-2-ил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (116 мг; соединение В 71) и ДИПЭА (0,22 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-2-(1(2R)-2-амино-3-[4-(трифторметил)фенил]пропаноилпиперидин-4-ил)-4-(3,4-диметоксифенил)4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-он (193 мг; соединение В 24) и COMU (155 мг) и реакционную смесь перемешивали при КТ в течение 2 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C49H50N7O8F3]: рассчитано: 922,3746; найдено: 922,3749. 50. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R,3R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-фенилбутан-2 ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (113 мг; соединение В 71) и ДИПЭА (0,21 мл) в ДХМ (3 мл) добавляли (4aS,8aR)-21-[(2R,3R)-2-амино-3-фенилбутаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-он (170 мг; соединение В 40) и COMU (151 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.); 2) силикагель, элюент: ДХМ/MeOH, 98/2 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C49H53N7O8]: рассчитано: 868,4028; найдено: 868,4026. 51. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R,3R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-3-фенилбутан-2 ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (138 мг; соединение В 72) и ДИПЭА (0,25 мл) в ДХМ (3 мл) добавляли (4aS,8aR)2-1-[(2R,3R)-2-амино-3-фенилбутаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-он (200 мг; соединение В 40) и COMU (177 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь дважды экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C50H55N7O8]: рассчитано: 882,4185; найдено: 882,4181. 52. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(4-гидроксифенил)-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. Смесь (4aS,8aR)-2-1-[(2R)-2-амино-3-(4-гидроксифенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (300 мг; соединение В 54), 4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-ил(1 Н-имидазол-1 ил)метанона (212 мг; соединение В 53) и ДИПЭА (204 мг) в ДХМ (15 мл) перемешивали при КТ в течение 10 мин, затем при кипячении с обратным холодильником в течение примерно 15 ч и затем при КТ в течение примерно 2 дней. Затем добавляли ДХМ (35 мл) и смесь экстрагировали насыщенным водным раствором бикарбоната натрия (310 мл). Органическую фазу концентрировали при пониженном давлении и полученный остаток обрабатывали с помощью ДХМ и фильтровали через слой силикагеля (элюент: EtOAc). Растворитель удаляли в вакууме и остаток дважды очищали с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюент для первой очистки: циклогексан/EtOAc/MeOH, от 100/0/0 до 0/100/0 и затем до 0/90/10 (об./об./об.), элюент для второй очистки: циклогексан/EtOAc/MeOH, от 100/0/0 до 0/100/0 и затем до 0/95/5 (об./об./об.)]. После лиофилизации из смеси ацетонитрил/вода (20 мл, 1/1 (об./об. получали искомое соединение в виде твердого вещества. МСВР(202 мг; соединение В 53) и ДИПЭА (162 мг) в ДХМ (10 мл) перемешивали при кипячении с обратным холодильником в течение 7,5 ч и затем при КТ в течение примерно 18 ч. Затем добавляли ДХМ (10 мл) и смесь экстрагировали насыщенным водным раствором бикарбоната натрия (35 мл). Органическую фазу концентрировали при пониженном давлении и полученный остаток четырежды очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюент для первой очистки: EtOAc/MeOH, 9/1; элюирование в градиентном режиме для второй очистки: EtOAc/MeOH, от 1/0 до 98/2 и затем до 95/5 (об./об./об.); элюент для третьей очистки: EtOAc/MeOH, 9/1, элюент для четвертой очистки: ДХМ/MeOH, 95/5]. После лиофилизации из смеси ацетонитрил/вода (15 мл, 4/1 (об./об. получали искомое соединение в виде твердого вещества. МСВР [C48H51N7O9]: рассчитано: 870,3821; найдено: 870,3817. 54. N-[(2S)-3-(2-Хлорфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. Смесь (4aS,8aR)-2-1-[(2S)-2-амино-3-(2-хлорфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-она (277 мг; соединение В 74), 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (177 мг; соединение В 71), HBTU (380 мг) и ДИПЭА (259 мг) в ДХМ (7,5 мл) перемешивали при КТ в течение 2,5 ч. Затем добавляли насыщенный водный раствор бикарбоната натрия (5 мл) и органическую фазу отделяли с помощью устройства для разделения фаз. Органическую фазу концентрировали при пониженном давлении и полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме для первой очистки: циклогексан/EtOAc/MeOH, от 1/0/0 до 0/9/1 (об./об./об.); силикагель, элюирование в градиентном режиме для второй очистки: циклогексан/EtOAc/ДХМ/MeOH, от 1/0/0/0 до 0/9/1/0 и затем до 0/8/1/1 (об./об./об./об.)]. После лиофилизации из смеси ацетонитрил/вода (10 мл, 1/1 (об./об. получали искомое соединение в виде твердого вещества. МСВР [C48H50N7O8Cl]: рассчитано: 888,3482; найдено: 888,3473. 55. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,7aR)-4-(3,4-диметоксифенил)-1-оксо-1,4 а,5,6,7,7 а-гексагидро-2 Н-циклопента[d]пиридазин-2-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси(4aS,7aR)-2-1-[(2R)-2-амино-3-фенилпропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-2,4 а,5,6,7,7 а-гексагидро-1 Н-циклопента[d]пиридазин-1-онгидрохлорида (171 мг; соединение В 90) и ДИПЭА (123 мг) в ДХМ (10 мл) добавляли 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5Hпирроло[3,2-d]пиримидин-7-ил(1 Н-имидазол-1-ил)метанон (212 мг; соединение В 53) и реакционную смесь перемешивали при 45C в течение 48 ч и при КТ в течение 72 ч. Затем растворитель выпаривали и остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 1/0 до 9/1 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода (6 мл, 4/1 (об./об. получали искомое соединение в виде твердого вещества. МСВР [C47H49N7O8]: рассчитано: 840,3715; найдено: 840,3712. 56. N-[(2S)-3-(2-Хлорфенил)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. Смесь(4aS,8aR)-2-1-[(2S)-2-амино-3-(2-хлорфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-она (277 мг; соединение В 74) 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (184 мг; соединение В 72), HBTU (380 мг) и ДИПЭА (259 мг) в ДХМ (7,5 мл) перемешивали при КТ в течение 2,5 ч. Затем добавляли насыщенный водный раствор бикарбоната натрия (5 мл) и органическую фазу отделяли с помощью устройства для разделения фаз. Органическую фазу концентрировали при пониженном давлении и полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме для первой очистки: циклогексан/EtOAc/MeOH, от 1/0/0 до 0/1/0 и затем до 0/9/1 (об./об./об.); силикагель, элюирование в градиентном режиме для второй очистки: циклогексан/EtOAc/ДХМ/MeOH, от 1/0/0/0 до 0/9/1/0 и затем до 0/8/1/1(об./об./об./об.); силикагель, элюирование в градиентном режиме для третьей очистки: циклогексан/EtOAc/MeOH, от 1/0/0 до 2/8/0, затем до 0/1/0 и затем до 0/9,5/0,5 (об./об./об.)]. После лиофилизации из смеси ацетонитрил/вода (15 мл, 2/1 (об./об. получали искомое соединение в виде твердого вещества.(4aS,8aR)-2-1-[(2R)-2-амино-3-(3-метилфенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорид (173 мг; соединение В 4) и COMU (143 мг) и реакционную смесь перемешивали при КТ в течение 2,5 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия, смесь дважды экстрагировали с помощью ДХМ и растворитель удаляли в вакууме. Остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.); 2) силикагель, элюирование в градиентном режиме: ДХМ/MeOH, от 97/3 до 98/2 (об./об.)] и, в заключение, с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. MCBP [C50H56N7O7F]: рассчитано: 886,4298; найдено: 886,4296. 58. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-(4-метоксифенил)-1-оксопропан-2-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (107 мг; соединение В 72) и ДИПЭА (0,19 мл) в ДХМ (3 мл) добавляли (4aS,8aR)2-1-[(2R)-2-амино-3-(4-метоксифенил)пропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорид (171 мг; соединение В 25) и COMU (138 мг) и реакционную смесь перемешивали при КТ в течение 4 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия, смесь дважды экстрагировали с помощью ДХМ и растворитель удаляли в вакууме. Остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. MCBP [C50H55N7O9]: рассчитано: 898,4134; найдено: 898,4129. 59. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-(2-4-[(4aS,8aR)-4-(3,4-диметоксифенил)1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-2-оксоэтил)-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (2,30 г; соединение В 71), (4aS,8aR)-2-[1-(аминоацетил)пиперидин-4-ил]-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (2,80 г; соединение В 80) иHBTU (2,71 г) в ДХМ (50 мл) добавляли ДИПЭА (4,5 мл) и реакционную смесь перемешивали при КТ в течение 30 мин. Затем добавляли насыщенный водный раствор бикарбоната натрия (30 мл), органическую фазу отделяли, сушили над сульфатом натрия и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме для первой очистки:EtOAc/MeOH, от 98/2 до 90/10 (об./об.), элюент для второй очистки: EtOAc/MeOH, 90/10 (об./об.)]. Органический растворитель, находящийся во всех содержащих искомое соединение фракциях, удаляли в вакууме и полученный остаток обрабатывали диэтиловым эфиром (20 мл), отфильтровывали и промывали этиловым эфиром и, в заключение, сушили в вакууме и получали искомое соединение в виде твердого вещества. MCBP [C41H45N7O8]: рассчитано: 764,3402; найдено: 764,3398. 60. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-гидрокси-1-оксопропан-2 ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. Раствор 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (2,47 г; соединение В 71), TOTU (2,30 г), НОАТ (952 мг) и ДИПЭА (3,6 мл) в ДМФ (50 мл) перемешивали при КТ в течение 30 мин и затем добавляли (4aS,8aR)-2-1-[(2S)-2-амино-3 гидроксипропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)онтрифторацетат (3,21 г; соединение В 78). Реакционную смесь перемешивали при КТ в течение 1,5 ч,затем все летучие вещества удаляли в вакууме и полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 100/0 до 90/10 (об./об.)] и получали искомое соединение в виде твердого вещества. МСВР [C42H47N7O9]: рассчитано: 794,3508; найдено: 794,3517. 61. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметокси- 26023713 фенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-5Hпирроло[3,2-d]пиримидин-7-карбоксамид. Смесь 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (2,41 г; соединение В 71), (4aS,8aR)-2-1-[(2S)-2-аминопропаноил]пиперидин-4-ил-4-(3,4 диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-она (3,02 г; соединение В 82), HBTU (2,85 г) и ДИПЭА (15,91 мл) в ДХМ (120 мл) перемешивали при КТ в течение 2 ч. Затем смесь экстрагировали насыщенным водным раствором бикарбоната натрия (50 мл), и затем отделенную органическую фазу экстрагировали разбавленным вдвое насыщенным раствором лимонной кислоты (75 мл) и затем рассолом и разбавленным вдвое насыщенным раствором бикарбоната натрия. Органическую фазу обрабатывали древесным углем (8 г) и с помощью ДХМ (100 мл) и фильтровали через слой целита. Растворитель удаляли в вакууме и полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: ДХМ/циклогексан/EtOAc/MeOH, от 1/0/0/0 до 1/1/0/0, затем до 0/1/0/0, затем до 1/0/0/0 и затем до 0/0/9/1 (об./об./об./об.)] и получали искомое соединение в виде твердого вещества. МСВР [C42H47N7O8]: рассчитано: 778,3559; найдено: 778,3556. 62. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (212 мг; соединение В 71), (4aS,8aR)-2-1-[(2R)-2-аминопропаноил]пиперидин-4 ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (266 мг; соединение В 62) и HBTU (250 мг) в ДХМ (5 мл) добавляли ДИПЭА (0,42 мл) и реакционную смесь перемешивали при КТ в течение 30 мин. Затем добавляли насыщенный водный раствор бикарбоната натрия (3 мл),органическую фазу отделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме:EtOAc/MeOH, от 95/5 до 90/10 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода (20 мл, 3/1(об./об. получали искомое соединение в виде твердого вещества. МСВР [C42H47N7O8]: рассчитано: 778,3559; найдено: 778,3561. 63. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S,3R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-гидрокси-1-оксобутан-2 ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (2,47 г; соединение В 71) 4aS,8aR)-2-1-[(2S,3R)-2-амино-3-гидроксибутаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (3,31 г; соединение В 2) и HBTU (2,92 г) в ДХМ (50 мл) добавляли ДИПЭА (4,9 мл) и реакционную смесь перемешивали при КТ в течение 30 мин. Затем к смеси добавляли насыщенный водный раствор бикарбоната натрия (20 мл), органическую фазу отделяли, сушили над сульфатом натрия и концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме:EtOAc/MeOH, от 95/5 до 90/10 (об./об.)]. Фракции, содержащие продукт, собирали, растворитель удаляли в вакууме и остаток обрабатывали этиловым эфиром. Суспензию фильтровали и осадок на фильтре сушили в вакууме и получали искомое соединение в виде твердого вещества. МСВР [C43H49N7O9]: рассчитано: 808,3665; найдено: 808,3662. 64. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксобутан-2-ил]-6-метил 5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5 Н-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (147 мг; соединение В 72), (4aS,8aR)-2-1-[(2S)-2-аминобутаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (147 мг; соединение В 51) и HBTU (167 мг) в ДХМ (4 мл) добавляли ДИПЭА (0,28 мл) и реакционную смесь перемешивали при КТ в течение 30 мин. Дополнительно добавляли 4-[5-(циклопропилметокси)-1,3 бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновую кислоту (75 мг; соединение В 72) и HBTU (85 мг) и реакционную смесь перемешивали при КТ в течение 48 ч. Затем к смеси добавляли насыщенный водный раствор бикарбоната натрия (2 мл) и органическую фазу отделяли с помощью устройства для разделения фаз. Органический слой концентрировали при пониженном давлении и полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 97/3 до 95/5 (об./об.)] и с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР 65. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксо-4-фенилбутан-2-ил]5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (799 мг; соединение В 71) и ДИПЭА (1,48 мл) в ДХМ (30 мл) добавляли HBTU (943 мг) и суспензию перемешивали при КТ в течение 30 мин. Затем добавляли (4aS,8aR)-2-1-[(2R)-2-амино-4 фенилбутаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорид (1,29 г; соединение В 85) и реакционную смесь перемешивали при КТ в течение 2 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия, смесь дважды экстрагировали с помощью ДХМ и органическую фазу сушили над сульфатом магния. Органический слой концентрировали при пониженном давлении и полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 100/0 до 98/2 (об./об.); 2) силикагель, элюирование в градиентном режиме: ДХМ/MeOH, от 100/0 до 98/2 (об./об.)]. Выделенный продукт растворяли в ацетонитриле и обрабатывали древесным углем и фильтровали через слой целита. Очистка с помощью колоночной флэшхроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме:EtOAc/MeOH, от 100/0 до 98/2 (об./об.)] и последующая лиофилизация из смеси ацетонитрил/вода давали искомое соединение в виде твердого вещества. МСВР [C49H54N7O8]: рассчитано: 868,4028; найдено: 868,4026. 66. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[3-(3,4-диметоксифенил)-5,5 диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]-6-метил 5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин 7-карбоновой кислоты (153 мг; соединение В 72) и ДИПЭА (0,27 мл) в ДХМ (3 мл) добавляли 2-1-[(2R)2-амино-3-фенилпропаноил]пиперидин-4-ил-6-(3,4-диметоксифенил)-4,4-диметил-4,5-дигидропиридазин-3(2H)-он (205 мг; соединение В 87) и COMU (196 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь экстрагировали с помощью ДХМ. Объединенные органические фазы сушили над сульфатом магния и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР[C47H51N7O8]: рассчитано: 842,3872; найдено: 842,3874. 67. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2R)-1-4-[3-(3,4-диметоксифенил)-5,5 диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]-5Hпирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (273 мг; соединение В 71) и ДИПЭА (0,51 мл) в ДХМ (5 мл) добавляли 2-1-[(2R)-2 амино-3-фенилпропаноил]пиперидин-4-ил-6-(3,4-диметоксифенил)-4,4-диметил-4,5-дигидропиридазин 3(2H)-он (380 мг; соединение В 87) и HBTU (322 мг) и реакционную смесь перемешивали при КТ в течение 2 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь экстрагировали с помощью ДХМ. Органический слой концентрировали при пониженном давлении и полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [1) модифицированный аминогруппами силикагель, элюент: EtOAc/MeOH, 98/2 (об./об.); 2) силикагель, элюент: ДХМ/MeOH, 98/2 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C46H49N7O8]: рассчитано: 828,3715; найдено: 828,3713. 68. 4-[2-(Циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-4-[3-(3,4-диметоксифенил)-5,5 диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]-5Hпирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-5H-пирроло[3,2-d]пиримидин-7 карбоновой кислоты (250 мг; соединение В 17) и ДИПЭА (0,13 мл) в ДХМ (2 мл) добавляли 2-1-[(2R)-2 амино-3-фенилпропаноил]пиперидин-4-ил-6-(3,4-диметоксифенил)-4,4-диметил-4,5-дигидропиридазин 3(2H)-он (98,5 мг; соединение В 87) и COMU (94,2 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь экстрагировали с помощью ДХМ. Органический слой концентрировали при пониженном давлении и полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C46H50FN7O7]: рассчитано: 832,3829; найдено: 832,3817. 69. 4-[2-(Циклопропилметокси)-5-фтор-4-метоксифенил]-N-[(2R)-1-4-[3-(3,4-диметоксифенил)-5,5 диметил-6-оксо-5,6-дигидропиридазин-1(4H)-ил]пиперидин-1-ил-1-оксо-3-фенилпропан-2-ил]-6-метил 5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К смеси 4-[2-(циклопропилметокси)-5-фтор-4-метоксифенил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (155 мг; соединение В 12) и ДИПЭА (0,27 мл) в ДХМ (3 мл) добавляли 21-[(2R)-2-амино-3-фенилпропаноил]пиперидин-4-ил-6-(3,4-диметоксифенил)-4,4-диметил-4,5-дигидропиридазин-3(2H)-он (205 мг; соединение В 87) и COMU (196 мг) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли разбавленный вдвое насыщенный водный раствор бикарбоната натрия и смесь экстрагировали с помощью ДХМ. Органический слой концентрировали при пониженном давлении и полученный остаток очищали с помощью препаративной ВЭЖХ и получали искомое соединение в виде твердого вещества. МСВР [C47H52FN7O7]: рассчитано: 846,3985; найдено: 846,3978. 70. N-[(2S)-3-Циклогексил-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-1-оксопропан-2-ил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол 4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2S)-2-амино-3-циклогексилпропаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (253 мг; соединение В 93), 4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-6-метил-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (165 мг; соединение В 72) и ГАТУ (190 мг) в ДХМ (4 мл) добавляли ДИПЭА (0,31 мл) и смесь перемешивали при КТ в течение 30 мин. Дополнительно добавляли ГАТУ (85 мг) и для завершения реакции реакционную смесь перемешивали в течение 20 мин. Затем смесь экстрагировали насыщенным водным раствором бикарбоната натрия (3 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 100/0 до 95/5 (об./об.)]. После лиофилизации из смеси ацетонитрил/вода получали искомое соединение в виде твердого вещества. МСВР [C49H60N7O8]: рассчитано: 874,4498; найдено: 874,4507. 71. 4-[5-(Циклопропилметокси)-1,3-бензодиоксол-4-ил]-N-[(2S,3S)-1-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-3-метил-1-оксопентан-2 ил]-5H-пирроло[3,2-d]пиримидин-7-карбоксамид. К суспензии (4aS,8aR)-2-1-[(2S,3S)-2-амино-3-метилпентаноил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (194 мг; соединение В 95), 4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-карбоновой кислоты (141 мг; соединение В 71) и HBTU (167 мг) в ДХМ (4 мл) добавляли ДИПЭА (0,28 мл) и смесь перемешивали при КТ в течение 20 мин. Дополнительно добавляли HBTU (75 мг) и для завершения реакции реакционную смесь перемешивали в течение 30 мин. Затем смесь экстрагировали насыщенным водным раствором бикарбоната натрия (2 мл), фазы разделяли с помощью устройства для разделения фаз и органический слой концентрировали при пониженном давлении. Полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [первая колонка: модифицированный аминогруппами силикагель,элюирование в градиентном режиме: EtOAc/MeOH, от 97/3 до 95/5 (об./об.); вторая колонка: модифицированный аминогруппами силикагель, элюирование в градиентном режиме: EtOAc/MeOH, от 100/0 до 90/10 (об./об.)] и получали искомое соединение в виде твердого вещества. МСВР [C45H53N7O8]: рассчитано: 820,4028; найдено: 820,4032. 72.(4aS,8aR)-2-1-[(2R)-2-амино-2-циклогексилацетил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (175 мг; соединение В 97), 4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5H-пирроло[3,2-d]пиримидин-7-ил(1H-имидазол-1-ил)-метанона (129 мг; соединение В 53) и ДИПЭА (124 мг) в ДХМ (10 мл) перемешивали при КТ в течение 2 дней и при 45C в течение 20 ч. Смесь экстрагировали насыщенным водным раствором бикарбоната натрия (35 мл). Органическую фазу концентрировали при пониженном давлении и полученный остаток дважды очищали с помощью колоночной флэш-хроматографии [первая колонка: силикагель, элюирование в градиентном режиме: EtOAc/н-гексан, от 70/30 до 100/0 (об./об.); вторая колонка: модифицированный аминогруппами силикагель, элюирование в градиентном режиме: циклогексан/EtOAc/MeOH, от 100/0/0 до 0/100/0 и затем до 0/90/10 (об./об./об.)]. После лиофилизации из смеси ацетонитрил/вода (20 мл, 8/2(об./об. получали искомое соединение в виде твердого вещества. МСВР [C47H55N7O8]: рассчитано: 846,4185; найдено: 846,4183. 73. N-[(1S)-1-Циклогексил-2-4-[(4aS,8aR)-4-(3,4-диметоксифенил)-1-оксо-4 а,5,6,7,8,8 а-гексагидрофталазин-2(1H)-ил]пиперидин-1-ил-2-оксоэтил]-4-[5-(циклопропилметокси)-1,3-бензодиоксол-4-ил]5H-пирроло[3,2-d]пиримидин-7-карбоксамид. Смесь 4aS,8aR)-2-1-[(2S)-2-амино-2-циклогексилацетил]пиперидин-4-ил-4-(3,4-диметоксифенил)-4 а,5,6,7,8,8 а-гексагидрофталазин-1(2H)-онгидрохлорида (356 мг; соединение В 99), 4-[5(циклопропилметокси)-1,3-бензодиоксол-4-ил]-5 Н-пирроло[3,2-d]пиримидин-7-ил(1 Н-имидазол-1-ил)метанона (262 мг; соединение В 53) и ДИПЭА (252 мг) в ДХМ (15 мл) перемешивали при КТ в течение примерно 2 дней и при 45C в течение 2 дней. Смесь экстрагировали насыщенным водным раствором бикарбоната натрия (320 мл). Органическую фазу концентрировали при пониженном давлении и полученный остаток очищали с помощью колоночной флэш-хроматографии [модифицированный аминогруппами силикагель, элюирование в градиентном режиме: циклогексан/EtOAc/MeOH, от 100/0/0 до 0/100/0 и
МПК / Метки
МПК: A61K 31/519, C07D 487/04, A61P 11/00
Метки: фталазинонпирролопиримидинкарбоксамида, производные
Код ссылки
<a href="https://eas.patents.su/30-23713-proizvodnye-ftalazinonpirrolopirimidinkarboksamida.html" rel="bookmark" title="База патентов Евразийского Союза">Производные фталазинонпирролопиримидинкарбоксамида</a>
Предыдущий патент: Комбинации активных соединений, содержащие производное соединение (тио)карбоксамида и фунгицидное соединение
Следующий патент: Катализатор на основе алюмината цинка и марганца, используемый для дегидрирования алканов
Случайный патент: Блистерная упаковка для применения в ингаляторах












