Производные пиримидина в качестве ингибиторов фосфодиэстеразы pde10
Номер патента: 23685
Опубликовано: 30.06.2016
Авторы: Кокс Кристофер Д., Рахим Иззат Т., Лейтон Марк Э., Керн Джеффри, Дудкин Вадим
Формула / Реферат
1. Соединение формулы I
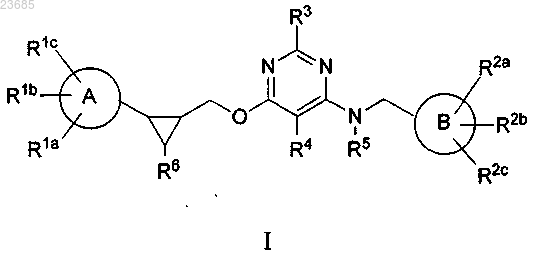
где А выбирают из:
(1) пиридила,
(2) хинолинила,
(3) нафтиридинила,
(4) тиазолила,
(5) пиридазинила,
(6) оксазолила,
(7) пиразолила,
(8) дигидропирролопиразолила,
(9) дигидроциклопентапиридинила,
(10) имидазопиридазинила и
(11) пиразолопиримидинила;
В выбирают из:
(1) тиазолила,
(2) пиразолила,
(3) тиадиазолила,
(4) изоксазолила,
(5) изотиазолила,
(6) пиридила и
(7) пиримидинила;
R1a, R1b и R1c независимо выбирают из:
(1) водорода,
(2) галогена,
(3) гидроксила,
(4) -(С=O)m-On-С1-6алкила, где алкил не замещен или замещен одним или несколькими заместителями, выбранными из R13,
(5) -(С=О)m-On-С3-6циклоалкила, где циклоалкил не замещен или замещен одним или несколькими заместителями, выбранными из R13,
(6) -(С=О)m-С2-4алкенила, где алкенил не замещен или замещен одним или несколькими заместителями, выбранными из R13,
(7) -(С=О)m-С2-4алкинила, где алкинил не замещен или замещен одним или несколькими заместителями, выбранными из R13,
(8) -(С=О)m-On-фенила или -(С=O)m-On-нафтила, где фенил или нафтил не замещен или замещен одним или несколькими заместителями, выбранными из R13,
(9) -(C=O)m-NR10R11,
(10) -S(O)2-NR10R11,
(11) -S(O)q-R12, где R12 представляет собой R10 или R11,
(12) -СО2Н,
(13) -CN и
(14) -NO2;
R2a, R2b и R2c независимо выбирают из:
(1) водорода,
(2) галогена,
(3) гидроксила,
(4) -(С=О)m-On-С1-6алкила, где алкил не замещен или замещен одним или несколькими заместителями, выбранными из R13,
(5) -(С=О)m-On-С3-6циклоалкила, где циклоалкил не замещен или замещен одним или несколькими заместителями, выбранными из R13,
(6) -(С=О)m-С2-4алкенила, где алкенил не замещен или замещен одним или несколькими заместителями, выбранными из R13,
(7) -(С=О)m-С2-4алкинила, где алкинил не замещен или замещен одним или несколькими заместителями, выбранными из R13,
(8) -(С=О)m-On-фенила или -(С=О)m-On-нафтила, где фенил или нафтил не замещен или замещен одним или несколькими заместителями, выбранными из R13,
(9) -(C=O)m-NR10R11,
(10) -S(O)2-NR10R11,
(11) -S(O)q-R12,
(12) -СО2Н,
(13) -CN и
(14) -NO2;
R3 выбирают из:
(1) СН3,
(2) CF3,
(3) CH2F,
(4) CH2CH3 ,
(5) циклопропила,
(6) цианогруппы,
(7) водорода,
(8) NH2,
(9) C(O)OR5,
(10) -О-С1-6алкила,
(11) -(CO)NH2,
(12) С1-6алкил-OH,
(13) С(О)С1-6алкила и
(14) галогена;
R4 выбирают из:
(1) водорода,
(2) галогена,
(3) -С1-6алкила и
(4) цианогруппы;
R5 выбирают из:
(1) водорода и
(2) С1-6алкила;
R6 выбирают из:
(1) водорода,
(2) С1-6алкила и
(3) OC1-6алкила;
R10 и R11 независимо выбирают из:
(a) водорода,
(b) С1-6алкила, который является незамещенным или замещеннным заместителем R14,
(c) С3-6алкенила, который не замещен или замещен заместителем R14,
(d) С3-6алкинила, который не замещен или замещен заместителем R14,
(e) С3-6циклоалкила, который не замещен или замещен заместителем R14,
(f) С1-6алкоксила, который не замещен или замещен заместителем R14, и
(g) фенила, который не замещен или замещен заместителем R14;
R13 выбирают из:
(1) галогена,
(2) гидроксила,
(3) -(С=O)m-On-С1-6алкила, где алкил не замещен или замещен одним или несколькими заместителями, выбранными из R14,
(4) -On-(С1-3)перфторалкила,
(5) -(С=O)m-On-С3-6циклоалкила, где циклоалкил не замещен или замещен одним или несколькими заместителями, выбранными из R14,
(6) -(С=O)m-С2-4алкенила, где алкенил не замещен или замещен одним или несколькими заместителями, выбранными из R14,
(7) -(С=O)m-С2-4алкинила, где алкинил не замещен или замещен одним или несколькими заместителями, выбранными из R14,
(8) -(С=O)m-On-фенила или -(С=O)m-On-нафтила, где фенил или нафтил не замещен или замещен одним или несколькими заместителями, выбранными из R14,
(9) -(C=O)m-NR10R11,
(10) -S(O)-NR10R11,
(11) -S(O)q-R12,
(12) -СО2Н,
(13) -CN и
(14) -NO2;
R14 выбирают из:
(1) гидроксила,
(2) галогена,
(3) -С1-6алкила,
(4) -С3-6циклоалкила,
(5) -О-С1-6алкила,
(6) -(С=О)-С1-6алкила,
(7) -NH-C1-6алкила,
(8) фенила,
(9) -СО2Н и
(10) -CN;
и где m имеет значение 0 или 1, n имеет значение 0 или 1 (где если m равно 0 или n равно 0, то имеется связь), q имеет значение 0, 1 или 2,
или его фармацевтически приемлемая соль.
2. Соединение по п.1 формулы Ia
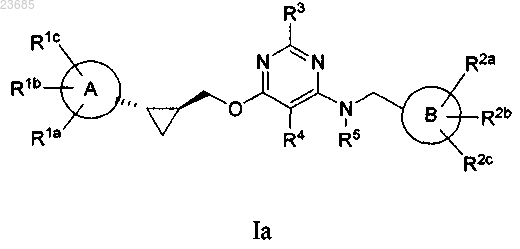
или его фармацевтически приемлемая соль.
3. Соединение по п.1 или его фармацевтически приемлемая соль, где А выбирают из:
(1) пиридила,
(2) хинолинила и
(3) нафтиридинила.
4. Соединение по п.1 или его фармацевтически приемлемая соль, где В выбирают из:
(1) тиазолила,
(2) пиразолила и
(3) тиадиазолила.
5. Соединение по п.1 или его фармацевтически приемлемая соль, где В выбирают из группы, состоящей из
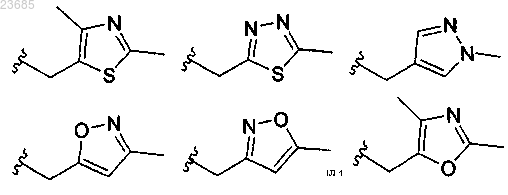
6. Соединение по п.1 или его фармацевтически приемлемая соль, где R1a, R1b, R1c выбирают из:
(1) C1-6алкила, который не замещен или замещен галогеном или гидроксилом,
(2) -О-С1-6алкила, который не замещен или замещен галогеном или гидроксилом,
(3) фенила, который не замещен или замещен галогеном, гидроксилом, -NH2, -NH-C1-6алкилом или -N(C1-6алкил)(C1-6алкил), -O-C1-6алкилом или -C1-6алкилом, который не замещен или замещен фтором, и
(4) -О-фенила, который не замещен или замещен галогеном, гидроксилом, -NH2, -NH-C1-6алкилом или -N(C1-6алкил)(C1-6алкил), -O-C1-6алкилом или -C1-6алкилом, который не замещен или замещен фтором.
7. Соединение по п.6 или его фармацевтически приемлемая соль, где R1a, R1b и R1c выбирают из:
(1) водорода,
(2) хлора,
(3) фтора,
(4) брома,
(5) метила,
(6) метоксигруппы,
(7) (метил)циклопропила-,
(8) циклопропила,
(9) (метокси)фенила- и
(10) (метил)фенила-.
8. Соединение по п.1 или его фармацевтически приемлемая соль, где R2a, R2b, R2c независимо выбирают из:
(1) водорода,
(2) галогена,
(3) гидроксила,
(4) C1-6алкила, который не замещен или замещен галогеном, гидроксилом или фенилом или нафтилом,
(5) -О-C1-6алкила, который не замещен или замещен галогеном, гидроксилом или фенилом, и
(6) фенила, который не замещен или замещен галогеном, гидроксилом, -C1-6алкилом, -O-C1-6алкилом или -NO2.
9. Соединение по п.8 или его фармацевтически приемлемая соль, где R2c представляет собой водород и R2a и R2b независимо выбирают из:
(1) водорода,
(2) хлора,
(3) фтора,
(4) брома,
(5) метила,
(6) циклопропила,
(7) изопропоксигруппы,
(8) метоксигруппы и
(9) трет-бутоксигруппы.
10. Соединение по п.1 или его фармацевтически приемлемая соль, где R3 выбирают из СН3, CF3 или CH2F.
11. Соединение по п.1 или его фармацевтически приемлемая соль, где R5 выбирают из водорода или метила.
12. Соединение, выбранное из
2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
2-метил-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-метил-6-{[(1S,2S)-2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-2-метил-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-2-метил-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-2-метил-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
S,S-N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-2-метил-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-2-метил-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
S,S-N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-2-метил-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-2-метилпиримидин-4-амина;
S,S-N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-2-метилпиримидин-4-амина;
N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-2-метил-6-[(2-пиридин-2-илциклопропил)метокси}пиримидин-4-амина;
S,S-N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
S,S-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]пиримидин-4-амина;
S,S-6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]пиримидин-4-амина;
S,S-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
6-{[2-(3-метоксипиридин-2-ил)циклопропил]метокси}-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]пиримидин-4-амина;
6-{[2-(5-фторпиридин-2-ил)циклопропил]метокси}-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]пиримидин-4-амина;
S,S-6-{[2-(5-фторпиридин-2-ил)циклопропил]метокси}-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]пиримидин-4-амина;
6-({2-[5-(фторметил)пиридин-2-ил]циклопропил}метокси)-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]пиримидин-4-амина;
6-({2-[5-(дифторметил)пиридин-2-ил]циклопропил}метокси)-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]пиримидин-4-амина;
2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-({2-[5-(трифторметил)пиридин-2-ил]циклопропил}метокси)пиримидин-4-амина;
2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-{[2-(1,3-тиазол-4-ил)циклопропил]метокси}пиримидин-4-амина;
2-метил-N-[(2-метил-1,3-тиазол-5-ил)метил]-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-метил-N-[(2-метил-1,3-тиазол-5-ил)метил]-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
2-метил-N-[(2-метил-1,3-тиазол-5-ил)метил]-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
S,S-2-метил-N-[(2-метил-1,3-тиазол-5-ил)метил]-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
2-метил-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(2-метил-1,3-тиазол-5-ил)метил]пиримидин-4-амина;
S,S-2-метил-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(2-метил-1,3-тиазол-5-ил)метил]пиримидин-4-амина;
6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-2-метил-N-[(2-метил-1,3-тиазол-5-ил)метил]пиримидин-4-амина;
S,S-6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-2-метил-N-[(2-метил-1,3-тиазол-5-ил)метил]пиримидин-4-амина;
2-метил-N-[(2-метил-1,3-тиазол-5-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-метил-N-[(2-метил-1,3-тиазол-5-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
2-метил-N-[(2-метил-1,3-тиазол-5-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-метил-N-[(2-метил-1,3-тиазол-5-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
S,S-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
S,S-6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
6-{[2-(5-фторпиридин-2-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
S,S-6-{[2-(5-фторпиридин-2-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
6-({2-[5-(фторметил)пиридин-2-ил]циклопропил}метокси)-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
6-({2-[5-(дифторметил)пиридин-2-ил]циклопропил}метокси)-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-метил-6-{[2-(6-метилпиридазин-3-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
S,S-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-(2-метил-1,3-тиазол-4-ил)циклопропил]метокси}пиримидин-4-амина;
2-метил-6-{[2-(2-метил-1,3-оксазол-4-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-метил-6-{[2-(1-метил-1Н-пиразол-3-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
N-[(5-циклопропил-1,3,4-тиадиазол-2-ил)метил]-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-[(5-циклопропил-1,3,4-тиадиазол-2-ил)метил]-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амина;
N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
S,S-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
S,S-6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
S,S-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-2,4-диамина;
S,S-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-2,4-диамина;
2-метокси-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-метокси-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
2,5-диметил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2,5-диметил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-2,5-диметил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-2,5-диметил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
N-6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-2-(трифторметил)пиримидин-4-амина;
S,S-N-6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-2-(трифторметил)пиримидин-4-амина;
6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-2-(трифторметил)пиримидин-4-амина;
S,S-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-2-(трифторметил)пиримидин-4-амина;
N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]-2-(трифторметил)пиримидин-4-амина;
S,S-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]-2-(трифторметил)пиримидин-4-амина;
N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]-2-(трифторметил)пиримидин-4-амина;
S,S-N-[(5-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]-2-(трифторметил)пиримидин-4-амина;
6-{[2-(5,6-дигидро-4Н-пирроло[1,2-b]пиразол-2-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
6-{[(1S,2S)-2-(5,6-дигидро-4Н-пирроло[1,2-b]пиразол-2-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
S,S-6-{[(1S,2S)-2-(5-метоксипиридин-2-ил)циклопропил]метокси}-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-пиразоло[1,5-а]пиримидин-2-илциклопропил]метокси}пиримидин-4-амина;
2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[(1S,2S)-2-пиразоло[1,5-а]пиримидин-2-илциклопропил]метокси}пиримидин-4-амина;
2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-пиразоло[1,5-а]пиримидин-5-илциклопропил]метокси}пиримидин-4-амина;
2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[(1S,2S)-2-пиразоло[1,5-а]пиримидин-5-илциклопропил]метокси}пиримидин-4-амина;
6-{[2-(5-бромпиридин-2-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
S,S-6-{[(1S,2S)-2-(5-бромпиридин-2-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-метил-6-{[2-(2-метилимидазо[1,2-b]пиридазин-6-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-метил-6-{[(1S,2S)-2-(2-метилимидазо[1,2-b]пиридазин-6-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
5-хлор-2-метил-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
S,S-5-хлор-2-метил-6-{[(1S,2S)-2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-этил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-5-фтор-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-5-фтор-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-5-фтор-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-5-фтор-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
5-фтор-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-5-фтор-2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
5-фтор-2-метил-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
S,S-5-фтор-2-метил-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-(фторметил)-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-(фторметил)-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-2-этил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-2-этил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
2-этил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-этил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
2-циклопропил-N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-циклопропил-N-[(2,4-диметил-1,3-тиазол-5-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
2-циклопропил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-2-циклопропил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
5-фтор-6-{[2-(5-метоксипиридин-2-ил)циклопропил]метокси}-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
5-фтор-6-{[(1S,2S)-2-(5-метоксипиридин-2-ил)циклопропил]метокси}-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
5-фтор-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-2,4-диамина;
5-фтор-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[(1S,2S)-2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-2,4-диамина;
5-фтор-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
5-фтор-6-{[(1S,2S)-2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
5-фтор-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-пиридин-2-илциклопропил]метокси}пиримидин-2,4-диамина;
5-фтор-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[(1S,2S)-2-пиридин-2-илциклопропил]метокси}пиримидин-2,4-диамина;
5-фтор-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-пиридин-2-илциклопропил]метокси}пиримидин-2,4-диамина;
5-фтор-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[(1S,2S)-2-пиридин-2-илциклопропил]метокси}пиримидин-2,4-диамина;
N-4-(2,4-диметоксибензил)-5-фтор-6-{[2-пиридин-2-илциклопропил]метокси}пиримидин-2,4-диамина;
N-4-(2,4-диметоксибензил)-5-фтор-6-{[(1S,2S)-2-пиридин-2-илциклопропил]метокси}пиримидин-2,4-диамина;
6-{[2-(5-хлорпиридин-2-ил)циклопропил]метокси}-5-фтор-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
6-{[(lS,2S)-2-(5-хлорпиридин-2-ил)циклопропил]метокси}-5-фтор-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
5-фтор-6-{[2-(5-фторпиридин-2-ил)циклопропил]метокси}-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
5-фтор-6-{[(1S,2S)-2-(5-фторпиридин-2-ил)циклопропил]метокси}-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
5-хлор-6-{[2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
5-хлор-6-{[(1S,2S)-2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
6-{[2-(4,5-диметилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
6-{[(1S,2S)-2-(4,5-диметилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамина;
6-((2-(5,6-дигидро-4Н-пирроло[1,2-b]пиразол-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
6-(((1S,2S)-2-(5,6-дигидро-4Н-пирроло[1,2-b]пиразол-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)-6-((2-(6-метилпиридин-2-ил)циклопропил)метокси)пиримидин-2,4-диамина;
5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)-6-(((1S,2S)-2-(6-метилпиридин-2-ил)циклопропил)метокси)пиримидин-2,4-диамина;
6-((2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
S,S-6-(((1S,2S)-2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
6-((2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
S,S-6-(((1S,2S)-2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
6-((2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
S,S-6-(((1S,2S)-2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
6-((2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
S,S-6-(((1S,2S)-2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
6-((2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
S,S-6-(((1S,2S)-2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
6-((2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
S,S-6-(((1S,2S)-2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
6-((2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
S,S-6-(((1S,2S)-2-(6,7-дигидро-5Н-циклопента[b]пиридин-2-ил)циклопропил)метокси)-5-фтор-N-4-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-2,4-диамина;
6-бром-N-((2,4-диметилтиазол-5-ил)метил)-2-метил-6-((2-(пиридин-2-ил)циклопропил)метокси)пиримидин-4-амина;
4-((2,4-диметилтиазол-5-ил)метиламино)-2-метил-6-((2-(пиридин-2-ил)циклопропил)метокси)пиримидин-5-карбонитрила;
2-метил-4-((1-метил-1Н-пиразол-4-ил)метиламино)-6-((2-(пиридин-2-ил)циклопропил)метокси)пиримидин-5-карбонитрила;
4-((1-метил-1Н-пиразол-4-ил)метиламино)-6-((2-(пиридин-2-ил)циклопропил)метокси)пиримидин-2-карбоксамида;
4-((1-метил-1Н-пиразол-4-ил)метиламино)-6-((2-(пиридин-2-ил)циклопропил)метокси)пиримидин-2-карбонитрила;
2-метил-N-((5-метил-1,3,4-тиадиазол-2-ил)метил)-6-((2-(5-(тиазол-4-ил)пиридин-2-ил)циклопропил)метокси)пиримидин-4-амина;
6-{[2-(2,3'-бипиридин-6'-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-({2-[5-(1,3-тиазол-5-ил)пиридин-2-ил]циклопропил}метокси)пиримидин-4-амина;
6-{[2-(3,4'-бипиридин-6-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-({2-[5-(1,3-тиазол-2-ил)пиридин-2-ил]циклопропил}метокси)пиримидин-4-амина;
6-{[2-(3,3'-бипиридин-6-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-(5-пиридазин-4-илпиридин-2-ил)циклопропил]метокси}пиримидин-4-амина;
6-((2-(5-этилпиридин-2-ил)циклопропил)метокси)-2-метил-N-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-4-амина;
6-{[2-(5-циклопропилпиридин-2-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амина;
6-((2-(5-(1Н-пиразол-1-ил)пиридин-2-ил)циклопропил)метокси)-2-метил-N-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-4-амина;
6-(2-((2-метил-6-((5-метил-1,3,4-тиадиазол-2-ил)метиламино)пиримидин-4-илокси)метил)циклопропил)никотинонитрила;
2-метил-N-((5-метилизоксазол-3-ил)метил)-6-((2-(пиридин-2-ил)циклопропил)метокси)пиримидин-4-амина;
N-[(2-фтор-5-метилпиридин-3-ил)метил]-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
S,S-N-(изотиаазол-5-илметил)-2-метил-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
2-метил-N-[(5-метилпиразин-2-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амина;
2-метил-6-[(2-пиридин-2-илциклопропил)метокси]-N-(пиримидин-5 -илметил)пиримидин-4-амина;
2-метил-6-[(2-пиридин-2-ил)циклопропил)метокси)-N-(пиридин-4-илметил)пиримидин-4-амина;
2-метил-6-[(2-пиридин-2-илциклопропил)метокси]-N-(пиридин-3-илметил)пиримидин-4-амина;
2-метил-N-((3-метилпиридин-4-ил)метил)-6-((2-(пиридин-2-ил)циклопропил)метокси)пиримидин-4-амина;
6-(2-((2-метил-6-((5-метил-1,3,4-тиадиазол-2-ил)метиламино)пиримидин-4-илокси)метил)циклопропил)пиридина;
2-амино-4-{[(1S,2S)-2-(5-метилпиридин-2-ил)циклопропил]метокси}-6-{[(5-метил-1,3,4-тиадиазол-2-ил)метил]амино}пиримидин-5-карбонитрила;
2-амино-4-{[(1S,2S)-2-(5-метилпиридин-2-ил)циклопропил]метокси}-6-{[(5-метил-1,3,4-тиадиазол-2-ил)метил]амино}пиримидин-5-карбонитрила;
S,S-2-амино-4-{[(1S,2S)-2-(5-метилпиридин-2-ил)циклопропил]метокси}-6-{[(5-метил-1,3,4-тиадиазол-2-ил)метил]амино}пиримидин-5-карбонитрила;
2-амино-4-{[(1S,2S)-2-(5-метоксипиридин-2-ил)циклопропил]метокси}-6-{[(5-метил-1,3,4-тиадиазол-2-ил)метил]амино}пиримидин-5-карбонитрила;
S,S-2-амино-4-{[(1S,2S)-2-(5-метоксипиридин-2-ил)циклопропил]метокси}-6-{[(5-метил-1,3,4-тиадиазол-2-ил)метил]амино}пиримидин-5-карбонитрила;
N-метокси-N-метил-5-((2-метил-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-иламино)метил)-1,3,4-тиадиазол-2-карбоксамида;
1-(5-((2-метил-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-иламино)метил)-1,3,4-тиадиазол-2-ил)этанона;
1-(5-((2-метил-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-иламино)метил)-1,3,4-тиадиазол-2-ил)этанола;
4-((5-метил-1,3,4-тиадиазол-2-ил)метиламино)-6-(((1R,2R)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-2-карбоновой кислоты;
этил 4-((5-метил-1,3,4-тиадиазол-2-ил)метиламино)-6-(((1R,2R)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-2-карбоксилата;
2-(5-((2-метил-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-иламино)метил)-1,3,4-тиадиазол-2-ил)пропан-2-ола;
2-(6-((1S,2S)-2-((2-метил-6-((5-метил-1,3,4-тиадиазол-2-ил)метиламино)пиримидин-4-илокси)метил)циклопропил)пиридин-3-ил)пропан-2-ола;
метил 5-((2-метил-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-иламино)метил)-1,3,4-тиадиазол-2-карбоксилата;
5-((2-метил-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-иламино)метил)-1,3,4-тиадиазол-2-карбонитрила;
5-((2-метил-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-иламино)метил)-1,3,4-тиадиазол-2-карбоксамида;
6-(((1S,3S)-2-трет-бутокси-3-(5-метилпиридин-2-ил)циклопропил)метокси)-2-метил-N-((5-метил-1,3,4-тиадиазол-2-ил)метил)пиримидин-4-амина;
2-этил-N-((5-метил-1,3,4-тиадиазол-2-ил)метил)-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-амина;
2-(4-((5-метил-1,3,4-тиадиазол-2-ил)метиламино)-6-(((1R,2R)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-2-ил)пропан-2-ола;
N-((5-трет-бутил-1,3,4-тиадиазол-2-ил)метил)-2-метил-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-амина;
1-(4-((5-метил-1,3,4-тиадиазол-2-ил)метиламино)-6-(((1R,2R)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-2-ил)этанона;
2-метил-N-((5-метил-1,3,4-тиадиазол-2-ил)метил)-6-(((1R,2R)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-амина;
1-(5-((2-метил-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-иламино)метил)-1,3,4-тиадиазол-2-ил)этанола;
2-хлор-N-((5-метил-1,3,4-тиадиазол-2-ил)метил)-6-(((1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин-4-амина;
или его фармацевтически приемлемая соль.
13. Соединение, представляющее собой 2-метил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амин или его фармацевтически приемлемую соль.
14. Соединение, представляющее собой 2-метил-6-{[(1S,2S)-2-(5-метилпиридин-2-ил)циклопропил]метокси}-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амин или его фармацевтически приемлемую соль.
15. Соединение, представляющее собой S,S-N-[(1,3-диметил-1Н-пиразол-5-ил)метил]-2-метил-6-[(2-хинолин-2-илциклопропил)метокси]пиримидин-4-амин или его фармацевтически приемлемую соль.
16. Соединение, представляющее собой S,S-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]-6-{[2-(1,5-нафтиридин-2-ил)циклопропил]метокси}пиримидин-4-амин или его фармацевтически приемлемую соль.
17. Соединение, представляющее собой S,S-6-{[(1S,2S)-2-(5-метоксипиридин-2-ил)циклопропил]метокси}-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамин или его фармацевтически приемлемую соль.
18. Соединение, представляющее собой 2-этил-N-[(1-метил-1Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амин или его фармацевтически приемлемую соль.
19. Соединение, представляющее собой 5-фтор-6-{[(1S,2S)-2-(5-метоксипиридин-2-ил)циклопропил]метокси}-N-4-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-2,4-диамин или его фармацевтически приемлемую соль.
20. Соединение, представляющее собой 6-{[2-(3,3'-бипиридин-6-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амин или его фармацевтически приемлемую соль.
21. Соединение, представляющее собой 6-{[2-(5-циклопропилпиридин-2-ил)циклопропил]метокси}-2-метил-N-[(5-метил-1,3,4-тиадиазол-2-ил)метил]пиримидин-4-амин или его фармацевтически приемлемую соль.
22. Соединение, представляющее собой 2-метил-N-((5-метилизоксазол-3-ил)метил)-6-((2-(пиридин-2-ил)циклопропил)метокси)пиримидин-4-амин или его фармацевтически приемлемую соль.
23. Соединение, представляющее собой 2-амино-4-{[(1S,2S)-2-(5-метилпиридин-2-ил)циклопропил]метокси}-6-{[(5-метил-1,3,4-тиадиазол-2-ил)метил]амино}пиримидин-5-карбонитрил или его фармацевтически приемлемую соль.
24. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении фосфодиэстеразы 10, содержащая фармацевтически приемлемый носитель и соединение по п.1 или его фармацевтически приемлемую соль.
25. Применение соединения или его фармацевтически приемлемой соли по п.1 для лечения неврологического или психиатрического расстройства, связанного с дисфункцией фосфодиэстеразы 10 у пациента-млекопитающего, нуждающегося в таком лечении.
26. Применение соединения по п.1 или его фармацевтически приемлемой соли в изготовлении лекарственного препарата для лечения расстройства, выбранного из психотических расстройств, бредовых расстройств и вызванного действием лекарственных средств психоза; тревожных расстройств, двигательных расстройств, аффективных расстройств и нейродегенеративных расстройств.
27. Способ лечения неврологического или психиатрического расстройства, связанного с дисфункцией фосфодиэстеразы 10 у пациента-млекопитающего, нуждающегося в таком лечении, включающий введение пациенту терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли.
28. Способ лечения неврологического или психиатрического расстройства, связанного с гипофункцией стриатума или с дисфункцией базальных ганглий (ядер) у пациента-млекопитающего, нуждающегося в таком лечении, включающий введение пациенту терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли.
29. Способ лечения шизофрении у пациента-млекопитающего, нуждающегося в таком лечении, включающий введение пациенту терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли.
Текст
ПРОИЗВОДНЫЕ ПИРИМИДИНА В КАЧЕСТВЕ ИНГИБИТОРОВ ФОСФОДИЭСТЕРАЗЫ PDE10 Изобретение направлено на пиримидиновые соединения, которые являются полезными в качестве терапевтических средств лечения расстройств центральной нервной системы, связанных с фосфодиэстеразой 10 (PDE10). Изобретение также относится к применению таких соединений для лечения неврологических и психиатрических расстройств, таких как шизофрения, психоз или болезнь Хантингтона, и расстройств, связанных с гипофункцией стриатума или с дисфункцией базальных ганглий (ядер). Область техники, к которой относится изобретение Изобретение в целом, относится к соединениям, которые действуют в качестве ингибиторов фермента фосфодиэстеразы (PDE) 10, к их композициям и терапевтическим применениям. Предпосылки создания изобретения Шизофрения представляет собой инвалидизирующее расстройство, поражающее психиатрические и моторные функции мозга. Ее обычно диагностируют у индивидуумов в возрасте от 20-23 до 24-26 лет,и симптомы включают галлюцинации и бредовые идеи или, как крайность, ангедонию или социальную самоизоляцию. По всему спектру расстройств симптомы указывают на ухудшение когнитивных функций и на функциональную недееспособность. Несмотря на улучшения антипсихотических методов лечения,текущие методы терапии, включая типичные (галоперидол) и атипичные (клозапин или оланзапин) антипсихотические средства, являются не особо пригодными и дают в результате чрезвычайно высокую степень нарушения режима терапии и прекращения приема лекарственного препарата. Неудовлетворенность терапией относят к недостатку эффективности или к непереносимым и неприемлемым побочным эффектам. Побочные эффекты были связаны со значительными метаболическими, экстрапирамидальными, prolactic и кардиологическими нежелательными явлениями. См. Lieberman et al., N. Engl. J. Med.(2005) 353:1209-1223. Хотя полагают, что в патогенезе шизофрении участвуют многочисленные пути, приводящие к психозу и к нарушениям когнитивной способности, основное внимание фокусируется на роли дисфункции глутамат/NMDA, связанной с уровнями циклического гуанозин-монофосфата (cGMP), и на роли допаминового (D2) рецептора, связанного с циклическим аденозин-монофосфатом (сАМР). Эти убиквитарные вторичные мессенджеры ответственны за изменение функции многих внутриклеточных белков. Циклический AMP, как полагают, регулирует активность сАМР-зависимой протеинкиназы (PKA), которая, в свою очередь, фосфорилирует и регулирует многие типы белков, включающие ионные каналы,ферменты и факторы транскрипции. Аналогично, cGMP также ответственен за прямую регуляцию киназ и ионных каналов. Один путь влияния на уровни циклических нуклеотидов, таких как сАМР и cGMP, представляет собой изменение или регуляцию ферментов, которые разлагают эти ферменты, известных как специфичные фосфодиэстеразы (PDE) 3',5'-циклических нуклеотидов. Суперсемейство PDE включает в себя двадцать один ген, которые кодируют одиннадцать семейств PDE. Эти семейства дополнительно подразделяютсся на группы на основе гомологии каталитических доменов и специфичности субстратов и включают 1) сАМР-специфичную группу, PDE 4A-D, 7 А и 7 В и 8 А и 8 В, 2) cGMP-специфичную группу, PDE 5 А, 6 А-С и 9 А, и 3) группу, которая имеет субстрат с двойной специфичностью, PDE 1 А-C, 2 А, 3 А и 3 В,10 А и 11 А. Гомология семейств, находящаяся в диапазоне 20-45%, позволяет предположить, что можно разработать селективные ингибиторы для каждого из этих подтипов. Были сделаны независимые сообщения об идентификации PDE10 по трем группам и было показано отличие от других PDE на основе ее аминокислотной последовательности, функциональных свойств и распределения в тканях (Fujishige et al., J. Biol. Chem. (1999) 274:18438-18445; Loughney et al., Gene(1999) 234:109-117; Soderling et al., PNAS, USA (1999) 96:7071-7076). Подтип PDE10 на сегодняшний день состоит из единственного члена, PDE10A, имеющего альтернативные сплайс-варианты как на Nконце (три варианта), так и на С-конце (два варианта), но это не влияет на домен GAF на N-конце или на каталитический центр на С-конце. Сплайс-варианты N-конца, PDE10A1 и PDE10A2, отличаются тем, что вариант А 2 имеет центр фосфорилирования PKA, который при активации, то есть фосфорилированияPKA в ответ на повышенные уровни сАМР, дает в результате внутриклеточные изменения в локализации фермента. PDE10A отличается от других семейств PDE, также имеющих консервативный домен GAF,тем, что ее лиганд представляет собой сАМР, тогда как в случае других имеющих GAF-домен PDE лиганд представляет собой cGMP (Kehler et al., Expert Opin. Ther. Patents (2007) 17(2):147-158). PDE10A имеет ограниченную, но высокую экспрессию в мозге и в яичках. Высокая экспрессия в мозге и, в частности, в нейронах стриатума, присущая PDE10, позволяет предположить, что ингибиторы также могут быть пригодны для лечения неврологических и психиатрических расстройств и состояний. Полагают, что ингибирование PDE10 является полезным в лечении шизофрении и широкого ряда состояний или расстройств, которое могло бы давать положительный эффект в результате увеличения уровней сАМР и/или cGMP в нейронах, включая ряд неврологических, психотических, тревожных и/или двигательных расстройств. В соответствии с этим средства, которые ингибируют PDE10 и, в частности,PDE10A, могли бы быть желательны в качестве терапевтических средств для лечения неврологических и психиатрических расстройств. Краткое изложение сущности изобретения Настоящее изобретение направлено на пиримидиновые соединения, которые являются полезными в качестве терапевтических средств для лечения расстройств центральной нервной системы, связанных с фосфодиэстеразой 10 (PDE10). Настоящее изобретение также относится к применению таких соединений для лечения неврологических и психиатрических расстройств, таких как шизофрения, психоз или болезнь Хантингтона, и расстройств, связанных с гипофункцией стриатума или с дисфункцией базальных ганглий (ядер). Подробное описание изобретения Настоящее изобретение направлено на соединения формулы I(1) водорода,(2) галогена,(3) гидроксила,(4) -(C=O)m-On-C1-6 алкила, где алкил незамещен или замещен одним или несколькими заместителями, выбранными из R13,(5) -(C=O)m-On-C3-6 циклоалкила, где циклоалкил незамещен или замещен одним или несколькими заместителями, выбранными из R13,(6) -(С=О)m-С 2-4 алкенила, где алкенил незамещен или замещен одним или несколькими заместителями, выбранными из R13,(7) - (С=О)m-С 2-4 алкинила, где алкинил незамещен или замещен одним или несколькими заместителями, выбранными из R13,(8) -(C=O)m-On-фенила или -(C=O)m-On-нафтила, где фенил или нафтил незамещен или замещен одним или несколькими заместителями, выбранными из R13,(9) -(C=O)m-NR10R11,(10) -S(O)2-NR10R11,(11) -S(O)q-R12, где R12 представляет собой R10 или R11,(12) -СО 2 Н,(13) -CN и(1) водорода,(2) галогена,(3) гидроксила,(4) -(С=O)m-On-С 1-6 алкила, где алкил незамещен или замещен одним или несколькими заместителями, выбранными из R13,(5) -(C=O)m-On-C3-6 циклоалкила, где циклоалкил незамещен или замещен одним или несколькими заместителями, выбранными из R13,(6) -(С=O)m-С 2-4 алкенила, где алкенил незамещен или замещен одним или несколькими заместителями, выбранными из R13,(7) -(С=O)m-С 2-4 алкинила, где алкинил незамещен или замещен одним или несколькими заместителями, выбранными из R13,-2 023685(8) -(C=O)m-On-фенила или -(C=O)m-On-нафтила, где фенил или нафтил незамещен или замещен одним или несколькими заместителями, выбранными из R13,(9) -(C=O)m-NR10R11,(10) -S(O)2-NR10R11,(11) -S(O)q-R12,(12) -СО 2 Н,(13) -CN и(a) водорода,(b) C1-6 алкила, который является незамещенным или замещеннным заместителем R14,(c) С 3-6 алкенила, который незамещен или замещен заместителем R14,(d) C3-6 алкинила, который незамещен или замещен заместителем R14,(e) С 3-6 циклоалкила, который незамещен или замещен заместителем R14,(f) C1-6 алкоксила, который незамещен или замещен заместителем R14, и(g) фенила, который незамещен или замещен заместителем R14;(1) галогена,(2) гидроксила,(3) -(С=O)m-On-С 1-6 алкила, где алкил незамещен или замещен одним или несколькими заместителями, выбранными из R14,(4) -On-(C1-3) перфторалкила,(5) -(С=O)m-On-C3-6 циклоалкила, где циклоалкил незамещен или замещен одним или несколькими заместителями, выбранными из R14,(6) -(С=O)m-С 2-4 алкенила, где алкенил незамещен или замещен одним или несколькими заместителями, выбранными из R14,(7) -(С=О)m-С 2-4 алкинила, где алкинил незамещен или замещен одним или несколькими заместителями, выбранными из R14,(8) -(C=O)m-On-фенила или -(C=O)m-On-нафтила, где фенил или нафтил незамещен или замещен одним или несколькими заместителями, выбранными из R14,(9) -(C=O)m-NR10R11,(10) -S(O)2-NR10R11,(11) -S(O)q-R12,(12) -СО 2 Н,(13) -CN и(10) -CN; и где m имеет значение 0 или 1, n имеет значение 0 или 1 (где, если m равно 0 или n равно 0, то имеется связь), q имеет значение 0, 1 или 2, или его фармацевтически приемлемая соль. Вариант осуществления настоящего изобретения включает соединения формулы Ia где А, В, R1a, R1b, R1c, R2a, R2b, R2c, R3, R4 и R5 определены в этом документе; или их фармацевтически приемлемая соль. Один из вариантов осуществления настоящего изобретения включает соединения, где А выбирают из(3) нафтиридинила. Один из вариантов осуществления настоящего изобретения включает соединения, где А выбирают из Один из вариантов осуществления настоящего изобретения включает соединения, где А представляет собой пиридил. Один из вариантов осуществления настоящего изобретения включает соединения,где А представляет собой хинолинил. Один из вариантов осуществления настоящего изобретения включает в себя соединения, где А представляет собой нафтиридинил. Один из вариантов осуществления настоящего изобретения включает соединения, где В выбирают из(3) тиадиазолила. Один из вариантов осуществления настоящего изобретения включает соединения, где В представляет собой тиазолил. Один из вариантов осуществления настоящего изобретения включает соединения,где В представляет собой пиразолил. Один из вариантов осуществления настоящего изобретения включает соединения, где В представляет собой тиадиазолил. Один из вариантов осуществления настоящего изобретения включает соединения, где В выбирают из Один из вариантов осуществления настоящего изобретения включает соединения, где В выбирают из группы, состоящей из Один из вариантов осуществления настоящего изобретения включает соединения, где В представляет собой Один из вариантов осуществления настоящего изобретения включает соединения, где В представляет собой Один из вариантов осуществления настоящего изобретения включает соединения, где В представляет собой Один из вариантов осуществления настоящего изобретения включает соединения, где R1a, R1b, R1c выбирают из(1) C1-6 алкила, который незамещен или замещен галогеном или гидроксилом,(2) -O-С 1-6 алкила, который незамещен или замещен галогеном или гидроксилом,(3) фенила, который незамещен или замещен галогеном, гидроксилом, -NH2, -NH-C1-6 алкилом или-N(C1-6 алкил)(С 1-6 алкил), -O-C1-6 алкилом или -C1-6 алкилом, который незамещен или замещен фтором, и(4) -О-фенила, который незамещен или замещен галогеном, гидроксилом, -NH2, -NH-C1-6 алкилом или -N(С 1-6 алкил)(С 1-6 алкил), -O-С 1-6 алкилом или -С 1-6 алкилом, который незамещен или замещен фтором. Один из вариантов осуществления настоящего изобретения включает соединения, где R1a, R1b и R1c выбирают из(10) (метил)фенила-. Один из вариантов осуществления настоящего изобретения включает соединения, где R2a, R2b, R2c независимо выбирают из группы, состоящей из 1) водорода,(2) галогена,(3) гидроксила,(4) C1-6 алкила, который незамещен или замещен галогеном, гидроксилом или фенилом или нафтилом,(5) -О-С 1-6 алкила, который незамещен или замещен галогеном, гидроксилом или фенилом, и(6) фенила, который незамещен или замещен галогеном, гидроксилом, -С 1-6 алкилом, -O-С 1-6 алкилом или -NO2. Один из вариантов осуществления настоящего изобретения включает соединения, где R2c представляет собой водород и R2a и R2b независимо выбирают из(9) трет-бутоксигруппы. Один из вариантов осуществления настоящего изобретения включает соединения, где R2c представ-5 023685 ляет собой водород и R2a и R2b независимо выбирают из группы, состоящей из(6) циклопропила. Один из вариантов осуществления настоящего изобретения включает соединения, где R2c представляет собой водород, R2b представляет собой водород или метил и R2a представляет собой метил или циклопропил. Один из вариантов осуществления настоящего изобретения включает соединения, где R3 выбирают из СН 3, CF3 или CH2F. Один из вариантов осуществления настоящего изобретения включает соединения, где R3 представляет собой СН 3. Один из вариантов осуществления настоящего изобретения включает соединения, где R5 выбирают из водорода и метила. Один из вариантов осуществления настоящего изобретения включает соединения,где R5 представляет собой водород. Конкретные варианты осуществления настоящего изобретения включают соединение, которое выбирают из заявленных соединений из представленных в этом документе примеров и их фармацевтически приемлемых солей и их отдельных энантиомеров и диастереомеров. Как оценено специалистами в данной области, используемые в этом документе термины галоген или гало предназначены для включения фтора, хлора, брома и йода. Подобно этому, "алкил", так же как другие группы, имеющие префикс "алк", такие как алкоксигруппа, алканоил, означает углеродные цепи,которые могут быть линейными или разветвленными или могут представлять собой их комбинации. С 1-6,как в С 1-6 алкиле, определяют для идентификации группы, которая имеет 1, 2, 3, 4, 5 или 6 углеродов в линейном или разветвленном расположении, такой как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил и тому подобное. "Алкилен" означает прямую или разветвленную цепь углеродных атомов с группой, замещенной по обоим концам, таким как -СН 2 СН 2- и-СН 2 СН 2 СН 2-. "Алкенил" означает углеродную цепь, которая содержит по меньшей мере одну углеродуглеродную двойную связь и которая может быть линейной или разветвленной или может представлять собой их комбинации, так что С 2-6 алкенил определяют для идентификации группы, которая имеет 2, 3, 4,5 или 6 углеродов и которая включает по меньшей мере одну двойную связь, которая может находиться в Е- или Z-расположении, включая винил, аллил, изопропенил, пентенил, гексенил, гептенил, 1-пропенил,2-бутенил, 2-метил-2-бутенил и тому подобное. "Алкинил" означает углеродную цепь, которая содержит по меньшей мере одну углерод-углеродную тройную связь и которая может быть линейной или разветвленной или может представлять собой их комбинацию, такую как этинил, пропаргил, 3-метил-1 пентинил, 2-гептинил и тому подобное. "Циклоалкил" означает моно-, би- или трициклическую структуру, необязательно соединенную с линейными или разветвленными структурами, имеющую указанное число углеродных атомов, такую как циклопропил, циклопентил, циклогептил, адамантил, циклододецилметил, 2-этил-1-бицикло[4.4.0]децил и тому подобное. "Алкокси" означает алкоксигруппу с прямой или с разветвленной цепью, имеющей указанное число атомов углерода. С 1-6 алкоксигруппа, например,включает метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу и тому подобное. Термин"гетероциклил", как используют в этом документе, включает как ненасыщенные гетероциклические фрагменты, содержащие моно- или бициклические ароматические кольца, где по меньшей мере одно кольцо содержит гетероатом, выбранный из N, О и S, и каждое кольцо содержит 5 или 6 атомов (то есть"гетероарил"), так и насыщенные гетероциклические фрагменты, содержащие моно- или бициклические насыщенные кольца, где по меньшей мере одно кольцо содержит гетероатом, выбранный из N, О и S, и каждое кольцо содержит 3, 5 или 6 атомов. Примеры "гетероарила" включают бензимидазолил, бензимидазолонил, бензофуранил, бензофуразанил, бензопиразолил, бензотиазолил, бензотриазолил, бензотиофенил, бензоксазепин, бензоксазолил, карбазолил, карболинил, циннолинил, фуранил, фуро(2,3b)пиридил, имидазолил, индолинил, индолил, дигидроиндолил, индолазинил, индазолил, изобензофуранил, изоиндолил, изохинолил, изотиазолил, изоксазолил, нафтпиридинил, оксадиазолил, оксазолил, оксазолин, изоксазолин, оксетанил, пиразинил, пиразолил, пиридазинил, пиридопиридинил, пиридазинил,пиридил, пиримидил, пирролил, хиназолинил, хинолил, хиноксалинил, тетрагидрохиноксалинил, тетразолил, тетразолопиридил, тиадиазолил, тиазолил, тиенил, триазолил и их N-оксиды. Примеры насыщенных гетероциклических фрагментов включают азетидинил, 1,4-диоксанил, гексагидроазепинил, пиперазинил, пиперидинил, пиридин-2-онил, пирролидинил, морфолинил, тетрагидрофуранил, тиоморфолинил и тетрагидротиенил, и их N-оксиды. Группа, которую принимают в качестве замещенной заместителями, может быть замещена любым числом таких заместителей. Группа, которую принимают в качестве независимо замещенной заместителями, может быть независимо замещена любым числом таких заместителей. Термин "замещенный" означает, что один или более водородов на означенной группе заменен(ы) группой, которую выбирают из упомянутой группы, при условии, что нормальная валентность означенной группы в существующих обстоятельствах не превышается, и что замещение приводит к стабильному соединению. Комбинации заместителей и/или переменных параметров допустимы только в том случае, если такие комбинации при-6 023685 водят к стабильным соединениям. Упоминание "стабильного соединения" или "стабильной структуры" означает, что соединение является достаточно устойчивым, чтобы сохраниться при выделении с полезной степенью чистоты из реакционной смеси, и чтобы сохраниться при приготовлении состава с эффективным терапевтическим средством. Соединения по настоящему изобретению могут содержать один или более стереогенных центров и,соответственно, могут находиться в виде рацематов, рацемических смесей, отдельных энантиомеров,диастереомерных смесей и отдельных диастереомеров. Дополнительные центры асимметрии могут присутствовать в зависимости от природы различных заместителей в молекуле. Каждый такой центр асимметрии будет независимо производить два оптических изомера, и подразумевается, что все возможные оптические изомеры и диастереомеры в смесях и в чистом виде или в виде частично очищенных соединений включаются в объем этого изобретения. Любые формулы, структуры или названия соединений,приведенные в этом описании изобретения, которые не устанавливают точно конкретную стереохимию,как подразумевается, охватывают любые и все существующие изомеры, которые описаны выше, и их смеси в любой пропорции. При точном описании стереохимии, подразумевается, что изобретение охватывает тот конкретный изомер в чистом виде или в виде части смеси с другими изомерами в любой пропорции. Независимый синтез этих диастереомеров или их хроматографические разделения могут быть осуществлены известным в данной области способом в результате соответствующей модификации методологии, раскрытой в этом документе. Их абсолютная стереохимия может быть определена рентгеноструктурной кристаллографией кристаллических продуктов или кристаллических промежуточных веществ, из которых получают производные, при необходимости, с помощью реагента, содержащего центр асимметрии с известной абсолютной конфигурацией. При желании, рацемические смеси соединений могут быть разделены, чтобы выделить индивидуальные энантиомеры. Разделение может быть выполнено известными в данной области способами, такими как реакция сочетания рацемической смеси соединений с энантиомерно чистым соединением с образованием диастереомерной смеси, с последующим разделением индивидуальных диастереомеров стандартными способами, такими как фракциональная кристаллизация и хроматография. Реакция сочетания часто представляет собой образование солей с использованием энантиомерно чистой(ого) кислоты или основания. Диастереомерные производные затем могут быть превращены в чистые энантиомеры отщеплением добавленного хирального остатка. Рацемическая смесь соединений также может быть разделена непосредственно хроматографическими способами с применением хиральных стационарных фаз, где способы хорошо известны в данной области. Альтернативно,любой энантиомер соединения может быть получен в ходе стереоселективного синтеза с использованием оптически чистых исходных веществ или реагентов известной конфигурации посредством способов, которые хорошо известны в данной области. Рентгеновская кристаллическая структура небольших молекул соединения примера 2-29 показала, что в 1 и 2 положениях циклопропильного кольца абсолютное стереохимическое обозначение было (S,S). Абсолютное стереохимическое обозначение для всех других соединений в примерах было присвоено на основе этого структурного определения соединения примера 229. Настоящее изобретение также включает все фармацевтически приемлемые изотопные варианты соединения формулы I, в которой один или более атомов заменен(ы) атомами, имеющими одинаковое атомное число, но атомную массу или массовое число, отличающиеся от атомной массы или массового числа, обычно встречающихся в природе. Примеры изотопов, подходящих для включения в соединения по изобретению, включают в себя изотопы водорода, такие как 2 Н и 3 Н, изотопы углерода, такие как 11 С,13 С и 14 С, изотопы азота, такие как 13N и 15N, изотопы кислорода, такие как 15O, 17O и 18O, изотоп фосфора, такой как 32 Р, изотоп серы, такой как 35S, изотоп фтора, такой как 18F, изотопы йода, такие как 123I и 125I, и изотоп хлора, такой как 36Cl. Некоторые изотопно-меченые соединения формулы I, например соединения, включающие радиоактивный изотоп, являются полезными в изучении распределения в тканях лекарственного средства и/или субстрата. Радиоактивные изотопы тритий, то есть 3 Н, и углерод-14, то есть 14 С, являются особенно полезными для этой цели с точки зрения легкости их введения и готового средства обнаружения. Замещение более тяжелыми изотопами, такими как дейтерий, то есть 2 Н, может предоставить некоторые терапевтические преимущества, получающиеся в результате большей метаболической стабильности, например увеличенный период полураспада (полувыведения) in vivo или сниженные требования к дозировкам, и значит может быть предпочтительным при некоторых обстоятельствах. Замещение позитронно-активными изотопами, такими как 11 С, 18F, 15O и 13N, может быть полезным в изучениях методом позитронно-эмиссионной томографии (PET) с целью исследования степени занятости рецептора субстратом. Изотопно-меченые соединения формулы I, как правило, получают по обычно применяемым методикам, известным специалистам в данной области, или с помощью процессов, аналогичных процессам, описанным в прилагаемых примерах, с применением соответствующих изотопномеченых реагентов вместо немеченного реагента, применяемого прежде. Будет ясно, что используемые в этом документе примеры соединений по настоящему изобретению предназначены также для включения фармацевтически приемлемых солей, а также солей, которые не являются фармацевтически приемлемыми, в том случае, когда они используются в качестве веществ-7 023685 предшественников свободных соединений или в других синтетических манипуляциях. Соединения по настоящему изобретению могут быть введены в форме фармацевтически приемлемой соли. Термин"фармацевтически приемлемые соли" относится к солям, приготовленным из фармацевтически приемлемых нетоксичных оснований или кислот. Если соединение по данному изобретению является кислотным,то его соответствующая соль может быть удобно приготовлена из фармацевтически приемлемых нетоксичных оснований, включающих неорганические основания и органические основания. Соли, получаемые из таких неорганических оснований, включают соли алюминия, аммония, кальция, меди (двух- и одновалентной), железа (трех- и двухвалентного), лития, магния, марганца (четырех-, трех- и двухвалентного), калия, натрия, цинка и подобные соли. Конкретные варианты осуществления включают соли аммония, кальция, марганца четырехвалентного, калия и натрия. Соли в твердой форме могут иметь две или более кристаллических структур, и также могут находиться в форме гидратов. Соли, получаемые из фармацевтически приемлемых органических нетоксичных оснований, включают соли первичных, вторичных и третичных аминов, замещенных аминов, в том числе замещенных аминов природного происхождения, циклических аминов и основных ионообменных смол, таких как аргинин, бетаин, кофеин,холин, N,N'-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, морфолин, пиперазин, пиперидин, полиаминные смолы,прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин, трометамин и тому подобное. Если соединения по данному изобретению являются основными, то их соответствующие соли могут быть приготовлены из фармацевтически приемлемых нетоксичных кислот, включающих неорганические и органические кислоты. Такие кислоты включают уксусную, бензолсульфоновую, бензойную, камфорсульфоновую, лимонную, этансульфоновую, фумаровую, глюконовую, глутаминовую, бромистоводородную, хлористоводородную, изэтионовую, молочную, малеиновую, яблочную, миндальную, метансульфоновую, слизевую, азотную, памовую, пантотеновую, фосфорную, янтарную, серную, винную, птолуолсульфоновую кислоту и тому подобное. Конкретные варианты осуществления включают лимонную, бромисто-водородную, хлористо-водородную, малеиновую, фосфорную, серную, фумаровую и винную кислоты. Будет ясно, что используемые в этом документе упоминания соединений по настоящему изобретению, как подразумевается, также включают фармацевтически приемлемые соли. Иллюстрацию изобретения осуществляют с помощью примеров конкретных соединений, раскрытых в примерах и в этом документе. Заявленные соединения являются полезными в способе лечения неврологического или психиатрического расстройства, связанного с дисфункцией PDE10 у пациента, такого как млекопитающее, нуждающегося в таком ингибировании, включающем введение эффективного количества соединения. В дополнение к приматам, в частности людям, разнообразные другие млекопитающие могут быть вылечены в соответствии со способом по настоящему изобретению. Заявленные соединения являются полезными в способе ингибирования активности PDE10 у пациента, такого как млекопитающее, нуждающегося в таком ингибировании, включающем введение эффективного количества соединения. Целевые соединения также полезны в лечении неврологического или психиатрического расстройства, связанного с гипофункцией стриатума или с дисфункцией базальных ганглий (ядер) у пациента-млекопитающего, нуждающегося в таком лечении. В дополнение к приматам, в частности людям, разнообразные другие млекопитающие могут быть вылечены в соответствии со способом по настоящему изобретению. Настоящее изобретение направлено на соединение по настоящему изобретению или на его фармацевтически приемлемую соль для применения в лекарственном препарате. Настоящее изобретение дополнительно направлено на применение соединения по настоящему изобретению или его фармацевтически приемлемой соли в изготовлении лекарственного препарата для лечения неврологического или психиатрического расстройства, связанного с дисфункцией PDE10 у пациента-млекопитающего, нуждающегося в таком лечении. Настоящее изобретение дополнительно направлено на применение соединения по настоящему изобретению или его фармацевтически приемлемой соли в изготовлении лекарственного препарата для лечения неврологического или психиатрического расстройства, связанного с гипофункцией стриатума или с дисфункцией базальных ганглий (ядер) у пациента-млекопитающего, нуждающегося в таком лечении."Лечение" или "процедура лечения" болезненного состояния включает: 1) предотвращение болезненного состояния, то есть оказывание содействия тому, чтобы клинические симптомы болезненного состояния не развились у субъекта, который может быть незащищен от возникновения болезненного состояния или предрасположен болезненному состоянию, но еще не испытывает или не проявляет симптомы болезненного состояния; 2) ингибирование болезненного состояния, то есть остановку развития болезненного состояния или его клинических симптомов; 3) или облегчение болезненного состояния, то есть вызывание временного или постоянного обратного развития болезненного состояния или ослабления его клинических симптомов. Субъект, подлежащий лечению способами по настоящему изобретению, как правило, представляет собой млекопитающее, в частности, человеческое существо мужского или женского пола, для которого желательна терапия. Термин "терапевтически эффективное количество" означает количество заявленного-8 023685 соединения, которое будет вызывать биологическую или соматическую реакцию в ткани, в системе у животного или человека, которая является желаемой у исследователя, ветеринара, лечащего врача или другого врача-клициниста. Ясно, что специалист в данной области может оказывать воздействие на неврологические и психиатрические расстройства посредством лечения пациента, страдающего на данный момент от расстройств, или посредством профилактического лечения пациента, испытывающего такие расстройства, с применением эффективного количества соединения по настоящему изобретению. Как используют в этом документе, термины "лечение" и "проведение лечения" относятся ко всем процессам,где может быть отмечено замедление, прерывание, остановка, контролирование или прекращение прогрессирования неврологических и психиатрических расстройств, описанных в этом документе, но не обязательно может быть показано полное устранение всех симптомов расстройства, а также к профилактической терапии с достижением торможения прогрессирования или снижения риска возникновения отмеченных состояний, в особенности у пациента, который предрасположен к такому заболеванию или расстройству. Авторы данной заявки предполагают, что ингибиторы PDE10 и, в частности, ингибиторы PDE10A могут обеспечивать терапевтическую пользу тем индивидуумам, которые страдают от психиатрических и когнитивных расстройств. Единственно возможное и особое распределение PDE10A в средних проекционных шипиковых нейронах стриатума, которые образуют основной центр для вхождения кортикальных и дофаминергических нейронов в базальные ганглии, позволяет предположить, что может быть возможным и желательным выявление ингибиторов PDE10 для уменьшения интенсивности или для устранения нежелательной клеточной сигнализации в пределах этого центра. Не желая быть связанными какой-либо теорией, авторы заявки полагают, что ингибирование PDE10A в стриатуме может приводить к увеличению сигнализации cAMP/cGMP и стриарного продукта, что имеет потенциал для восстановления угнетенного поведения, которое ухудшается при когнитивном заболевании, таком как шизофрения. Регуляция и интеграция вхождения глутаматергических и дофаминергических нейронов могут улучшить когнитивное поведение, при одновременном подавлении или снижении нежелательного поведения. Таким образом, в одном из вариантов осуществления, соединения по этому изобретению обеспечивают способ лечения или уменьшения интенсивности симптомов заболеваний или состояний, в которых гипофункция стриатума является постоянно проявляющимся признаком, или заболеваний или состояний, в которых дисфункция базальных ганглий играет определенную роль, например, таких как болезнь Паркинсона, болезнь Хантингтона, шизофрения, обсессивно-компульсивные нарушения, привыкание к лекарственным или наркотическим средствам и психоз. Другие состояния, для которых ингибиторы, описанные в этом документе, могут иметь желательный и полезный эффект, включают состояния, требующие снижение активности и пониженной реакции в отношении психомоторных стимулянтов, или где было бы желательно снизить реакции условного избегания, что часто можно спрогнозировать по клинической антипсихотической активности. Как используют в этом документе, термин "селективный ингибитор PDE10" относится к органической молекуле, которая эффективно ингибирует фермент из семейства PDE10 в большей степени, чем ферменты из семейств PDE1-9 или PDE11. В одном из вариантов осуществления селективный ингибиторPDE10 представляет собой органическую молекулу, имеющую Ki для ингибирования PDE10, значение которого меньше или приблизительно равно одной десятой значения Ki для вещества, которое является ингибитором для другого фермента PDE. Иными словами, органическая молекула ингибирует активность PDE10 в той же самой степени при концентрации, составляющей одну десятую или менее, чем концентрация, необходимая для любого другого фермента PDE. Предпочтительно селективный ингибитор PDE10 представляет собой органическую молекулу, имеющую Ki для ингибирования PDE10, значение которого меньше или приблизительно равно одной сотой значения Ki для вещества, которое является ингибитором для другого фермента PDE. Иными словами, органическая молекула ингибирует активность PDE10 в той же степени при концентрации, составляющей приблизительно одну сотую или менее,чем концентрация, необходимая для любого другого фермента PDE. "Селективный ингибитор PDE10" может быть выявлен, например, в результате сравнения способности органической молекулы ингибировать активность PDE10 с ее способностью ингибировать ферменты PDE из других семейств PDE. Например, органическая молекула может быть изучена в отношении ее способности ингибировать активность PDE10, а также активность PDE1A, PDE1B, PDE1C, PDE2A, PDE3A, PDE3B, PDE4A, PDE4B,PDE4C, PDE4D, PDE5A, PDE6A, PDE6B, PDE6C, PDE7A, PDE7B, PDE8A, PDE8B, PDE9A и/илиPDE11A. Ферменты фосфодиэстеразы, включая PDE10, вовлечены в широкий ряд биологических функций. Это позволило предположить потенциальную роль для этих ферментов в разнообразных процессах, протекающих во время заболеваний у людей или других видов. Соединения по настоящему изобретению имеют полезность в лечении разнообразных неврологических и психиатрических расстройств. В одном из конкретных вариантов осуществления соединения по настоящему изобретению обеспечивают способ лечения шизофрении или психоза, включающий введение пациенту, нуждающемуся в лечении, эффективного количества соединения по настоящему изобретению. Диагностическое и статистическое руководство по психиатрическим расстройствам (Diagnostic and Statistical Manual of MentalDisorders), четвертая редакция, пересмотренная (DSM-IV-TR) (2000, American Psychiatric Association,Washington DC) предоставляет средство диагностики психиатрических расстройств, которые включают параноидную, гебефреническую, кататоническую или недифференцированную шизофрению и вызванные действием химических веществ психотические расстройства. Как используется в этом документе,термин "шизофрения или психоз" включает в себя диагноз и классификацию этих душевных расстройств, что описано в DSM-IV-TR, и термин предназначен для включения подобных расстройств, описанных в других источниках. Расстройства и состояния, охваченные в этом документе, включают состояния или заболевания, такие как шизофрения или психоз, включая шизофрению (параноидного, гебефренического, кататонического, недифференцированного или резидуального типа), шизофреноформное расстройство, шизоаффективное расстройство, например, бредового типа или депрессивного типа,бредовое расстройство, психотическое расстройство, кратковременное психотическое расстройство, индуцированное психотическое расстройство, психотическое расстройство, обусловленное соматическим заболеванием, и вызванное действием химического вещества или вызванное действием лекарственного средства (например, психоз, вызванный алкоголем, амфетамином, каннабисом, кокаином, галлюциногенами, ингалянтами, опиоидами, фенциклидином, кетамином и другими диссоциированными анестетиками, и другими психостимуляторами), психоз (психотическое расстройство), психоз, сопутствующий аффективным расстройствам, кратковременный реактивный психоз, шизоаффективный психоз, расстройства "шизофренического спектра", такие как шизоидные или шизотипические расстройства личности,расстройство личности параноидного типа, расстройство личности шизоидного типа, болезнь, сопутствующая психозу (такая как большая депрессия, маниакально-депрессивное (биполярное аффективное) расстройство, болезнь Альцгеймера и посттравматический стрессовый синдром), включая как позитивные, так и негативные симптомы шизофрении и других психозов, но не ограничиваются этим. В другом конкретном варианте осуществления соединения по настоящему изобретению обеспечивают способ лечения когнитивных расстройств, включающий введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения по настоящему изобретению. Диагностическое и статистическое руководство по психиатрическим расстройствам, четвертая редакция, пересмотренная(DSM-IV-TR), также предоставляет средство диагностики психиатрических заболеваний, которые включают когнитивные расстройства, в том числе деменцию, острый алкогольный бред, алкогольные амнестические расстройства и возрастное снижение когнитивных способностей. Как используют в этом документе, термин "когнитивные расстройства" включает в себя диагноз и классификацию этих расстройств, что описано в DSM-IV-TR, и термин предназначен для включения подобных расстройств, описанных в других источниках. Расстройства и состояния, охваченные в этом документе, включают расстройства, которые имеют в качестве симптома дефицит внимания и/или восприятия, такие как деменция(сопутствующая болезни Альцгеймера, ишемии, мультиинфарктной деменции, травме, внутричерепным опухолям, черепно-мозговой травме, сосудистым проблемам или инсульту, алкогольной деменции или другой связанной с действием лекарственного средства деменции, синдрому СПИД, заболеванию ВИЧ,болезни Паркинсона, болезни Хантингтона, болезни Пика, болезни Крейтцфельдта-Якоба, перинатальной гипоксии, другим соматическим заболеваниям или злоупотреблению различными веществами), болезнь Альцгеймера, мультиинфарктная деменция, СПИД-ассоциированная деменция и лобно-височная деменция, бредовое состояние, амнестические расстройства или возрастное снижение когнитивных способностей, но не ограничиваются этим. В другом конкретном варианте осуществления соединения по настоящему изобретению обеспечивают способ лечения тревожных расстройств, включающий введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения по настоящему изобретению. Диагностическое и статистическое руководство по психиатрическим расстройствам, четвертая редакция, пересмотренная (DSMIV-TR), также предоставляет средство диагностики психиатрических заболеваний, которые включают тревожные расстройства в виде генерализованного тревожного расстройства, обсессивнокомпульсивного расстройства и панической атаки. Как используют в этом документе, термин "тревожные расстройства" включает в себя диагноз и классификацию этих душевных расстройств, что описано вDSM-IV-TR, и термин предназначен для включения подобных расстройств, описанных в других источниках. Расстройства и состояния, охваченные в этом документе, включают тревожные расстройства, такие как острое стрессовое расстройство, агорафобия (патологическая боязнь открытых пространств), генерализованное тревожное расстройство, обсессивно-компульсивное расстройство, паническая атака,паническое расстройство, посттравматическое стрессовое расстройство, тревожное расстройство, вызванное разлукой, социофобия, специфическая фобия, вызванное химическим веществом тревожное расстройство и тревога вследствие соматического заболевания, но не ограничиваются этим. В другом конкретном варианте осуществления соединения по настоящему изобретению обеспечивают способ лечения связанных с действием химических веществ расстройств и аддиктивного поведения, включающий введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения по настоящему изобретению. Диагностическое и статистическое руководство по психиатрическим расстройствам, четвертая редакция, пересмотренная (DSM-IV-TR), также предоставляет средство диагностики заболеваний, которые включают персистирующую деменцию, персистирующее амнестическое- 10023685 расстройство, психотическое расстройство или тревожное расстройство, вызванное злоупотреблением различными веществами и переносимостью веществ, которыми злоупотребляют, зависимостью от веществ, которыми злоупотребляют, или отказом от веществ, которыми злоупотребляют. Как используют в этом документе, термин "связанные с действием химических веществ расстройства и аддиктивное поведение" включает в себя диагноз и классификацию этих душевных расстройств, что описано в DSM-IVTR, и термин предназначен для включения подобных расстройств, описанных в других источниках. Расстройства и состояния, охваченные в этом документе, включают в себя связанные с действием химических веществ расстройства и аддиктивное поведение, такие как делирий (бредовое состояние), вызванный различными веществами, персистирующая деменция, персистирующее амнестическое расстройство,психотическое расстройство или тревожное расстройство, привыкание к приему лекарственных средств,переносимость лекарственных средств, и зависимость или синдром отказа от веществ, включающих спирт, амфетамины, каннабис, кокаин, галлюциногены, ингалянты, никотин, опиоиды, фенциклидин,седативные средства, гипнотические средства или анксиолитические средства (транквилизаторы), но не ограничиваются этим. В другом конкретном варианте осуществления соединения по настоящему изобретению обеспечивают способ лечения ожирения или нарушения пищевого поведения, связанные с избыточным приемом пищи, и осложнения, связанные с этим, включающий введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения по настоящему изобретению. В настоящее время ожирение включено в десятую редакцию международной Классификации болезней и связанных со здоровьем проблем (ICD-10) (Всемирная организация здоровья, 1992) в качестве соматического заболевания. Диагностическое и статистическое руководство по психиатрическим расстройствам, четвертая редакция, пересмотренная (DSM-IV-TR), также предоставляет средство диагностики заболеваний, которые включают ожирение при наличии психологических факторов, влияющих на медицинское состояние. Как используют в этом документе, термин "ожирение или нарушения пищевого поведения, связанные с избыточным приемом пищи" включает в себя диагноз и классификацию этих медицинских состояний и расстройств,описанных в ICD-10 и DSM-IV-TR, и термин предназначен для включения подобных расстройств, описанных в других источниках. Расстройства и состояния, охваченные в этом документе, включают ожирение, нейрогенную булимию и навязчивые расстройства пищевого поведения, но не ограничиваются этим. В еще одном конкретном варианте осуществления соединения по настоящему изобретению обеспечивают способ лечения аффективных и депрессивных расстройств, включающий введение пациенту,нуждающемуся в таком лечении, эффективного количества соединения по настоящему изобретению. Как используют в этом документе, термин "аффективные и депрессивные расстройства" включает диагноз и классификацию этих медицинских состояний и расстройств, что описано в руководстве DSM-IV-TR, и термин предназначен для включения подобных расстройств, описанных в других источниках. Расстройства и состояния, охваченные в этом документе, включают биполярные расстройства, аффективные расстройства, в том числе депрессивные расстройства, основной депрессивный эпизод легкого, умеренного или тяжелого типа, аффективный эпизод маниакального или смешанного типа, гипоманиакальный аффективный эпизод, депрессивный эпизод с атипичными признаками, депрессивный эпизод с меланхолическими признаками, депрессивный эпизод с кататоническими признаками, аффективный эпизод с послеродовым проявлением, постинсультную депрессию; большое депрессивное расстройство, дистимическое расстройство, малое депрессивное расстройство, предменструальное дисфорическое расстройство,постпсихотическое депрессивное расстройство, развивающееся при шизофрении, большое депрессивное расстройство, наложенное на психотическое расстройство, такое как бредовое расстройство или шизофрения, биполярное расстройство, например биполярное расстройство I типа, биполярное расстройство II типа, циклотимическое расстройство, депрессию, в том числе униполярную депрессию, сезонную депрессию и послеродовую депрессию, предменструальный синдром (PMS) и предменструальное дисфорическое расстройство (PDD), аффективные расстройства вследствие соматического заболевания и вызванные действием различных веществ аффективные расстройства, но не ограничиваются этим. В другом конкретном варианте осуществления соединения по настоящему изобретению обеспечивают способ лечения боли, включающий введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения по настоящему изобретению. Конкретные варианты боли представляют собой костную и суставную боль (остеоартрит), повторяющуюся при движении боль, зубную боль, боль,связанную с раковым заболеванием, миофасциальный болевой синдром (повреждение мышц, фибромиалгию), периоперативную боль (общую хирургическую, гинекологическую), хроническую боль и нейропатическую боль. В других конкретных вариантах осуществления соединения по настоящему изобретению обеспечивают способы лечения других типов расстройств, связанных с когнитивными способностями, со способностями к обучению и с психической деятельностью, включающих нарушения способности к обучению,такие как нарушение способности к чтению, нарушение способности к математике или нарушение способности к написанию выражения, синдром гиперактивности с дефицитом внимания, возрастное снижение когнитивных способностей, первазивное расстройство развития, в том числе аутическое расстройство, расстройства внимания, такие как синдром гиперактивности с дефицитом внимания (ADHD) и кон- 11023685 дуктивное расстройство; расстройство, связанное с рецептором NMDA, такое как аутизм, депрессия,беспамятство в легкой форме, детские нарушения способности к обучению и закрытую травму черепа; нейродегенеративное расстройство или состояние, такое как нейродегенерация, сопутствующая черепномозговой травме, инсульту, церебральному инфаркту, эпилептическому приступу, отравлению нейротоксинами или нейродегенерации, вызванной гипокликемией; мультисистемную атрофию; двигательные расстройства, такие как акинезии и акинетико-ригидные синдромы (в том числе болезнь Паркинсона,паркинсонизм, вызванный действием лекарственных средств, постэнцефалитический паркинсонизм,прогрессирующий надъядерный паралич, множественная системная атрофия, кортикобазальная дегенерация, комплексное протекание паркинсонизма-бокового амиотрофического склероза (ALS) - деменции и кальцификация базальных ядер головного мозга), паркинсонизм, вызванный действием медикаментов(такой как паркинсонизм, вызванный действием нейролептиков, злокачественный нейролептический синдром, острая дистония, вызванная действием нейролептиков, острая акатизия, вызванная действием нейролептиков, поздняя дискинезия, вызванная действием нейролептиков и постуральный тремор, вызванный действием медикаментов), болезнь Хантингтона, дискинезия, сопутствующая терапии агонистами дофамина, синдром Жилль де ла Туретта, эпилепсия, мышечные спазмы и расстройства, связанные с мышечной спастичностью или вялостью, включая тремор; дискинезии, включая тремор (такой как тремор в состоянии покоя, постуральный тремор, интенционное дрожание и эссенциальный тремор), синдром беспокойных ног, хорею (такую как хорея Сиденгама, болезнь Хантингтона, доброкачественная наследственная хорея, нейроакантоцитоз, симптоматическая хорея, хорея и гемибаллизм, вызванные действием лекарственных средств), миоклонию (в том числе генерализованную миоклонию и фокальную миоклонию), тики (включая простые тики, комбинированные тики и симптоматические тики), дистонию(в том числе генерализованную, идиопатическую, вызванную действием лекарственных средств, симптоматическую, пароксимальную и фокальную (такую как блефароспазм, оромандибулярная дистония,спазматическая дистония, спастическая кривошея, аксиальная дистония, гемиплегический и дистонический графоспазм; недержание мочи; нейрональное повреждение (в том числе поражение зрения, ретинопатию или макулярную дегенерацию глаза, тиннитус, ухудшение и потерю слуха, и отек головного мозга); рвоту; и нарушения сна, включая бессонницу и нарколепсию, но не ограниченными этим. Из вышеупомянутых расстройств лечение шизофрении, биполярного расстройства, депрессии, в том числе униполярной депрессии, сезонной депрессии и послеродовой депрессии, предменструального синдрома(PMS) и предменструального дисфорического расстройства (PDD), нарушений способности к обучению,первазивных расстройств развития, в том числе аутического расстройства, расстройств внимания, в том числе синдрома гиперактивности с дефицитом внимания (ADHD), аутизма, тикозных расстройств, в том числе синдрома Туретта, тревожных расстройств, в том числе фобии и посттравматического стрессового расстройства, когнитивных расстройств, сопутствующих деменции, деменции при СПИД, болезни Альцгеймера, Паркинсона, Хантингтона, спастичности, миоклонии, мышечного спазма, тиннитуса и ухудшения и потери слуха представляет собой особую важность. Активность соединений согласно настоящему изобретению в качестве ингибиторов PDE10 может быть легко определена без лишнего экспериментирования с использованием методики флуоресцентной поляризации (FP), которая хорошо известна в данной области (Huang, W., et al., J. Biomol. Screen., 2002,7:215). В частности, соединения следующих примеров имели активность в контрольных пробах, показывая способность ингибировать гидролиз фосфатной сложноэфирной связи циклического нуклеотида. Любое соединение, демонстрирующее значение Ki (константа ингибирования) ниже 1 мкМ, могло бы считаться ингибитором PDE10, который определен в этом документе. В обычном эксперименте ингибирующая активность в отношении PDE10 для соединений по настоящему изобретению была определена в соответствии со следующей методикой проведения эксперимента. PDE10A2 была амплифицирована из кДНК головного мозга эмбриона человека (Clontech, Mountain View, CA) с использованием прямого праймера, соответствующего нуклеотидам 56-77 PDE10A2 человека (номер доступа AF1274806 Genbank Identifier 4894716), содержащего обобщающую типичную последовательность Kozak, и обратного праймера, соответствующего нуклеотидам 2406-2413 PDE10A2(номер доступа AF127480, Genbank Identifier 4894716). Амплификацию посредством полимеразы Easy-A(Stratagene, La Jolla, CA) проводили при 95 С в течение 2 мин с последующим проведением тридцати трех циклов при 95 С в течение 40 с, при 55 С в течение 30 с и при 72 С в течение 2 мин 48 с. Конечное удлинение проводили при 72 С в течение 7 мин. Продукт ПЦР подвергали ТА-клонированию вpcDNA3.2-ТОРО (Invitrogen, Carlsbad, CA) согласно стандартному протоколу. Клетки AD293 с 70-80% конфлюэнтностью были временно трансфицированы посредством PDE10A2/pcDNA3.2-ТОРО человека с применением липофектамина 2000 в соответствии с указаниями изготовителя (Invitrogen, Carlsbad, CA). Клетки собирали через 48 ч после трансфекции и лизировали соникацией (осаждение: 3, 105 с импульсы) в буферном растворе, содержащем 20 мМ HEPES (N-2-гидроксиэтилпиперазин-N-2-этансульфоновая кислота), 1 мМ EDTA (этилендиаминтетрауксусная кислота) и коктейль ингибиторов протеаз (Roche). Лизат собирали центрифугированием при 75000g в течение 20 мин. Супернатант, содержащий цитоплазматическую фракцию, использовали для оценивания активности PDE10A2. Анализ методом флуо- 12023685 ресцентной поляризации фосфодиэстераз циклических нуклеотидов выполняли с использованием набораIMAP FP, поставляемого из Molecular Devices, Sunnyvale, СА (продуктR8139). Технологию IMAP применяли ранее в анализе фосфодиэстераз (Huang, W., et al., J. Biomol. Screen, 2002, 7:215). Исследования проводили при комнатной температуре в 384-луночных микротитрационных планшетах с объемом инкубирования 20,2 мкл. Растворы испытуемых соединений приготавливали в ДМСО (диметилсульфоксиде) и подвергали серийному разведению в ДМСО, что дало в результате по 8 мкл каждого из 10 растворов, отличающихся трехкратно по концентрации, по 32-серийного разведения на планшет. 100%-ное ингибирование определяют с применением известного ингибитора PDE10, который может представлять собой любое соединение, которое присутствует с 5000-кратным своим значением Ki в пробе, описание которой приводится ниже, как, например, папаверин (см. Siuciak, et al. Neuropharmacology (2006) 51:386396; Becker, et al. Behav. Brain Res. (2008) 186 (2):155-60; Threlfell, et al., J. Pharmacol. Exp. Ther. (2009) 328Labcyte Echo 555 (Labcyte, Sunnyvale, CA) используют для дозирования 200 нл из каждой лунки титрационного планшета в 384-луночный аналитический планшет. Раствор фермента (разведение 1/1600 из аликвот; достаточное для получения 20%-й конверсии субстрата) и отдельный раствор FAM-меченнойcAMP-PDE (цАМФ-зависимая фосфодиэстераза) из Molecular Devices (продуктR7506) в конечной концентрации 50 нМ изготавливают в аналитическом буферном растворе (10 мМ Трис-HCl, рН 7,2, 10 мМ MgCl2, 0,05% NaN3, 0,01% Твин-20 и 1 мМ DTT (дитиотреитол. Фермент и субстрат затем добавляют в аналитические планшеты двумя последовательными добавлениями по 10 мкл и затем встряхивают для смешивания. Реакцию оставляют протекать при комнатной температуре в течение 30 мин. Затем изготавливают из компонентов набора связывающий раствор, состоящий из 80% раствора А, 20% раствора В и связывающего реагента в объеме 1/600 относительно итогового связывающего раствора. Ферментативную реакцию останавливают добавлением 60 мкл связывающего раствора в каждую лунку аналитических планшетов и планшеты герметизируют и встряхивают в течение 10 с. Планшет инкубируют при комнатной температуре в течение по меньшей мере 1 ч перед измерением методом флуоресцентной поляризации (FP). Параллельную и перпендикулярную флуоресценцию каждой лунки планшета измеряют с помощью планшет-ридера Perkin Elmer EnVision (Waltham, MA). Флуоресцентную поляризацию (mP) вычисляют по параллельной (S) и перпендикулярной (Р) флуоресценции лунки каждого образца и по аналогичным значениям для медианной контрольной лунки, содержащей только субстрат (So и Ро), с использованием следующего уравнения: Поляризация (mP)=1000(S/So-P/Po)/(S/So+P/Po). Профили доза-ингибирование для каждого соединения охарактеризовывают подгонкой данных mP к четырехпараметровому уравнению, приведенному ниже. Кажущуюся константу ингибирования (Ki),максимальное ингибирование на низком плато относительно "контроля 100%-го ингибирования" (Imax; например, 1 совпадает с этим контролем), минимальное ингибирование на высоком плато относительно"контроля 0%-го ингибирования (Imin, например, 0 совпадает с контролем без лекарственного средства) и наклон кривой (nH) определяют в результате построения кривой нелинейным методом наименьших квадратов по значениям mP в виде функции зависимости от дозы соединения с использованием программного обеспечения для внутреннего пользования на основе методик, описанных Mosser et al., JALA,2003, 8:54-63, по следующему уравнению:"контрольных образцов 100%-го ингибирования" (100% mP) представляют собой константы, определяемые для контрольных образцов, размещенных в колонках 1-2 и 23-24 каждого аналитического планшета. Кажущееся значение (Km) для FAM-меченного сАМР (циклический аденозин-монофосфат), равное 150 нМ, определяют в отдельных экспериментах с использованием параллельной вариации субстрата (Substrate) и концентраций выбираемого лекарственного средства (Drug). Селективность в отношении PDE10, в сравнении с другими семействами PDE, оценивают с использованием технологии IMAP. Фермент PDE2A3 макаки-резуса и фермент PDE10A2 человека получают из цитозольных фракций временно трансфицированных клеток HEK. Все другие PDE представляют собой фермент человека GST(Кат.60010), PDE3A (Кат.60030), PDE4A1A (Кат.60040), PDE5A1 (Кат.60050), PDE6C (Кат.60060), PDE7A (Кат.60070), PDE8A1 (Кат.60080), PDE9A2 (Кат.60090), PDE11A4 (Кат.60110). Анализ PDE1-11 проводят параллельно при комнатной температуре в 384-луночных микротитрационных планшетах с инкубационным объемом 20,2 мкл. Растворы испытуемых соединений получают в ДМСО и подвергают серийному разведению посредством ДМСО, что дает по 30 мкл каждого из 10 растворов, отличающихся трехкратно по концентрации, по 32-серийного разведения на планшет. 100%-ное ингибирование определяют в результате добавления буферного раствора вместо фермента, и 0%-ное ингибирование определяют с использованием ДМСО (1% конечные концентрации). Labcyte POD 810 (Labcyte, Sunnyvale, CA) используют для дозирования 200 нл из каждой лунки титрационного планшета для приготовления одиннадцати копий аналитического планшета для каждой титрации, по одной копии для каждого фермента PDE. Раствор каждого фермента (разведение из аликвот; достаточное для получения 20%-й конверсии субстрата) и отдельный раствор FAM-меченного сАМР или FAM-меченного cGMP изMolecular Devices (Sunnyvale, CA, продуктR7506 или cGMPR7508) в конечной концентрации 50 нМ изготавливают в аналитическом буферном растворе (10 мМ Трис-HCl, рН 7,2, 10 мМ MgCl2, 0,05% NaN3,0,01% Твин-20 и 1 мМ DTT (дитиотреитол. Следует отметить, что субстрат для PDE2 представляет собой 50 нМ FAM-cAMP, содержащий 1000 нМ cGMP. Фермент и субстрат затем добавляют в аналитические планшеты двумя последовательными добавлениями по 10 мкл и затем встряхивают для смешивания. Реакцию оставляют протекать при комнатной температуре в течение 60 мин. Затем изготавливают из компонентов набора связывающий раствор, состоящий из 80% раствора А, 20% раствора В и связывающего реагента в объеме 1/600 относительно итогового связывающего раствора. Ферментативную реакцию останавливают добавлением 60 мкл связывающего раствора в каждую лунку аналитических планшетов. Планшеты герметизируют и встряхивают в течение 10 с. Планшет инкубируют при комнатной температуре в течение 1 ч, затем измеряют параллельную и перпендикулярную флуоресценцию с помощью планшет-ридера Тесап Genios Pro (Тесап, Switzerland). Кажущиеся константы ингибирования для соединений в отношении всех 11 PDE вычисляют по показаниям параллельной и перпендикулярной флуоресценции, что описано для анализа методом FP (флуоресцентной поляризации) PDE10 с использованием следующих кажущихся значений KM для каждой комбинации фермента и субстрата: PDE1A(FAM-cAMP) 150 нМ, PDE8A1 (FAM-cAMP) 50 нМ, PDE9A2 (FAM-cGMP) 60 нМ, PDE10A2 (FAMcAMP) 150 нМ, PDE11A4 (FAM-cAMP) 1000 нМ. Собственная ингибирующая активность соединения в отношении PDE10, которое может быть использовано в соответствии с настоящим изобретением, может быть определена с помощью этих проб. Все конечные соединения следующих примеров имеют активность в ингибировании ферментаPDE10 человека в вышеупомянутых пробах, как правило, со значением Ki, равным менее приблизительно 1 мкМ. В частности, все конечные соединения следующих примеров имеют активность в ингибировании фермента PDE10 человека в вышеупомянутых пробах, как правило, со значением Ki, равным менее приблизительно 0,1 мкМ. Дополнительные данные приводятся в следующих примерах. Такой результат служит показателем собственной активности соединений при использовании в качестве ингибиторов фермента PDE10. В общем, один из специалистов в данной области мог бы оценить, что вещество считается эффективным в ингибировании активности PDE10, если оно имеет значение Ki, равное менее или приблизительно 1 мкМ, предпочтительно менее или приблизительно 0,1 мкМ. Настоящее изобретение также включает соединения в рамках основного объема изобретения, которые обладают активностью в качестве ингибиторов других ферментов фосфодиэстеразы. Что касается 2-алкоксипиримидиновых соединений, данные соединения показывают неожиданные свойства, например, касающиеся увеличенных эффективности, пероральной биологической доступности, метаболической стабильности и/или сниженной нецелевой активности. Заявленные соединения являются, кроме того, полезными в способе предотвращения, лечения, контролирования, уменьшения интенсивности симптомов или снижения риска заболеваний, расстройств и состояний, отмеченных в этом документе. Заявленные соединения, кроме того, являются полезными в способе предотвращения, лечения, контролирования, уменьшения интенсивности симптомов или снижения риска вышеупомянутых заболеваний, расстройств и состояний в комбинации с другими средствами. Соединения по настоящему изобретению могут быть использованы в комбинации с одним или более другими лекарственными средствами в лечении, предотвращении, контролировании, уменьшении интенсивности симптомов или снижении риска заболеваний или состояний, для которых соединения по настоящему изобретению или другие лекарственные средства могут иметь полезность, где комбинация лекарственных средств, взятых вместе, является безопаснее или более эффективной, чем любое лекарственное средство как таковое. Такое(ие) другое(ие) лекарственное(ые) средство(а) может/могут быть введено(ы) путем и в количестве, обычно используемыми для этого, одновременно или последовательно с соединением по настоящему изобретению. В том случае, когда соединение по настоящему изобретению используют одновременно с одним или более другими лекарственными средствами, может быть жела- 14023685 тельна фармацевтическая композиция в стандартной лекарственной форме, содержащей такие другие лекарственные средства и соединение по настоящему изобретению. Однако комбинированная терапия также может включать виды терапии, в которых соединение по настоящему изобретению и одно или более других лекарственных средств вводят по различным перекрывающимся схемам. Также предусматривается, что, при использовании в комбинации с одним или более другими активнодействующими ингредиентами, соединения по настоящему изобретению и другие активнодействующие ингредиенты могут быть использованы в более низких дозах, чем при отдельном использовании каждого из них. В соответствии с этим фармацевтические композиции по настоящему изобретению включают фармацевтические композиции, которые содержат один или более других активнодействующих ингредиентов, в дополнение к соединению по настоящему изобретению. Вышеупомянутые комбинации включают комбинации соединения по настоящему изобретению не только с одним другим активнодействующим соединением,но также и с двумя или более другими активнодействующими соединениями. Аналогично, соединения по настоящему изобретению могут быть использованы в комбинации с другими лекарственными средствами, которые применяются в предотвращении, лечении, контролировании, уменьшении интенсивности симптомов или в снижении риска возникновения заболеваний или состояний, в отношении которых соединения по настоящему изобретению являются полезными. Такие другие лекарственные средства могут быть введены, путем и в количестве, обычно используемыми для этого, одновременно или последовательно с соединением по настоящему изобретению. В соответствии с этим фармацевтические композиции по настоящему изобретению включают фармацевтические композиции, которые также содержат один или более других активнодействующих ингредиентов, в дополнение к соединению по настоящему изобретению. Массовое отношение соединения по настоящему изобретению ко второму активнодействующему ингредиенту может варьироваться и будет зависеть от эффективной дозы каждого ингредиента. Как правило, будет использоваться эффективная доза каждого ингредиента. Так, например, если соединение по настоящему изобретению комбинируют с другим средством, массовое отношение соединения по настоящему изобретению к другому средству будет, как правило, находиться в диапазоне от приблизительно 1000:1 до приблизительно 1:1000, как, например, от приблизительно 200:1 до приблизительно 1:200. Комбинации соединения по настоящему изобретению и других активнодействующих ингредиентов будут, как правило, также находиться в пределах вышеупомянутого диапазона, но в каждом случае должна быть использована эффективная доза каждого активнодействующего ингредиента. В таких комбинациях соединение по настоящему изобретению и другие активнодействующие средства могут быть введены отдельно или вместе. Кроме того, введение одного компонента может происходить до введения, одновременно с введением или после введения других(ого) средств(а). В соответствии с вышеизложенным заявленные соединения могут быть использованы как таковые или в комбинации с другими средствами, которые известны как благотворно действующие в отношении заявленных показаний, или с другими лекарственными средствами, которые оказывают действие на рецепторы или ферменты, которые либо повышают эффективность, безопасность, удобство применения,либо снижают нежелательные побочные эффекты или токсичность соединений по настоящему изобретению. Заявленное соединение и другое средство могут быть введены совместно, либо в ходе сопутствующей терапии, либо при использовании комбинированного препарата. В одном из вариантов осуществления заявленное соединение может быть применено в комбинации со средствами против болезни Альцгеймера, ингибиторами -секретазы, ингибиторами -секретазы, ингибиторами редуктазы HMG-CoA, нестероидными противовоспалительными лекарственными средствами, включающими ибупрофен, витамином Е и антиамилоидными антителами. В другом варианте осуществления заявленное соединение может быть применено в комбинации с седативными средствами, снотворными средствами, анксиолитическими средствами, антипсихотическими средствами, успокоительными препаратами, циклопирролонами, имидазопиридинами, пиразолопиримидинами, транквилизаторами, агонистами и антагонистами мелатонина, мелатонергическими средствами, бензодиазепинами, барбитуратами, антагонистами 5 НТ-2 и с тому подобным, таким как адиназолам, аллобарбитал, алонимид, алпразолам, амисульприд, амитриптилин, амобарбитал, амоксапин, арипипразол, атипичные антипсихотические средства, бентазепам, бензоктамин, бротизолам, бупропион,бусприон, бутабарбитал, буталбитал, капурид, карбоклорал, хлоральбетаин, хлоральгидрат, кломипрамин, клоназепам, клоперидон, клоразепат, хлордиазепоксид, клоретат, хлорпромазин, клозапин, ципразепам, дезипрамин, декскламол, диазепам, дихлоральфеназон, дивалпроекс, дифенгидрамин, доксепин,эстазолам, этхлорвинол, этомидат, фенобам, флунитразепам, флупентиксол, флуфеназин, флуразепам,флувоксамин, флуоксетин, фосазепам, глутетимид, галазепам, галоперидол, гидроксизин, имипрамин,литий, лоразепам, лорметазепам, мапротилин, меклоквалон, мелатонин, мефобарбитал, мепробамат, метаквалон, мидафлур, мидазолам, нефазодон, низобамат, нитразепам, нортриптилин, оланзапин, оксазепам, паральдегид, пароксетин, пентобарбитал, перлапин, перфеназин, фенелзин, фенобарбитал, празепам,прометазин, пропофол, протриптилин, квазепам, кветиапин, реклазепам, рисперидон, ролетамид, секобарбитал, сертралин, супроклон, темазепам, тиоридазин, тиотиксен, траказолат, транилципромин, тразодон, триазолам, трепипам, трицетамид, триклофос, трифлуоперазин, триметозин, тримипрамин, улдазепам, венлафаксин, залеплон, зипрасодон, золазепам, золпидем, и с их солями и их комбинациями, и с- 15023685 тому подобным, или заявленное соединение может быть введено в сочетании с применением физических методов, таких как фототерапия или электростимуляция. В другом варианте осуществления заявленное соединение может быть применено в комбинации с леводопа (с селективным экстрацеребральным ингибитором декарбоксилазы, таким как карбидопа или бенсеразид, или без него), антихолинергиками, такими как бипериден (необязательно, в виде его гидрохлоридной или лактатной соли) и тригексифенидил (бензгексол) гидрохлорид, ингибиторами СОМТ (катехол-О-метилтрансферазы), такими как энтакапон, ингибиторами МОА-В, антиоксидантами, антагонистами рецептора А 2 а аденозина, холинергическими агонистами, антагонистами рецептора NMDA, антагонистами рецептора серотонина и агонистами рецептора допамина, такими как алентемол, бромокриптин, фенолдопам, лизурид, наксаголид, перголид и прамипексол. Будет ясно, что агонист допамина может находиться в форме фармацевтически приемлемой соли, например алентемол-гидробромида, бромокриптин-мезилата, фенолдопам-мезилата, наксаголид-гидрохлорида и перголид-мезилата. Лизурид и прамипексол обычно используются в несолевой форме. В другом варианте осуществления заявленное соединение может использоваться в комбинации с соединением из фенотиазинового, тиоксантенового, гетероциклического дибензазепинового, бутирофенонового, дифенилбутилпиперидинового и индолонового классов нейролептических веществ. Подходящие примеры фенотиазинов включают хлорпромазин, мезоридазин, тиоридазин, ацетофеназин, флуфеназин, перфеназин и трифлуоперазин. Соответствующие примеры тиоксантенов включают хлорпротиксен и тиотиксен. Пример дибензазепина представляет собой клозапин. Пример бутирофенона представляет собой галоперидол. Пример дифенилбутилпиперидина представляет собой пимозид. Пример индолона представляет собой молиндолон. Другие нейролептические вещества включают локсапин, сульпирид и рисперидон. Будет понятно, что нейролептические вещества, когда используются в комбинации с заявленным соединением, могут находиться в форме фармацевтически приемлемой соли, например хлорпромазин-гидрохлорида, мезоридазин-безилата, тиоридазин-гидрохлорида, ацетофеназин-малеата, флуфеназин-гидрохлорида, флурфеназин-энатата, флуфеназин-деканоата, трифлуоперазин-гидрохлорида,тиотиксен-гидрохлорида, галоперидол-деканоата, локсапин-сукцината и молиндон-гидрохлорида. Перфеназин, хлорпротиксен, клозапин, галоперидол, пимозид и рисперидон обычно используются в несолевой форме. Таким образом, заявленное соединение может применяться в комбинации с ацетофеназином,алентемолом, арипипразолом, амисульпридом, бензгексолом, бромокриптином, бипериденом, хлорпромазином, хлорпротиксеном, клозапином, диазепамом, фенолдопамом, флуфеназином, галоперидолом,леводопа, леводопа с бенсеразидом, леводопа с карбидопа, лизуридом, локсапином, мезоридазином, молиндолоном, наксаголидом, оланзапином, перголидом, перфеназином, пимозидом, прамипексолом, кветиапином, рисперидоном, сульпиридом, тетрабеназином, тригексифенидилом, тиоридазином, тиотиксеном, трифлуоперазином или зипразидоном. В другом варианте осуществления заявленное соединение может использоваться в комбинации с антидепрессантом или с успокоительным средством, включая ингибиторы обратного захвата норэпинефрина (включая трициклические соединения третичных аминов и трициклические соединения вторичных аминов), селективные ингибиторы обратного захвата серотонина (SSRI), ингибиторы моноаминоксидазы(MAOI); обратимые ингибиторы моноаминоксидазы (RIMA), ингибиторы обратного захвата серотонина и норадреналина (SNRI), антагонисты фактора высвобождения кортикотропина (CRF), антагонисты адренорецепторов, антагонисты рецептора нейрокинина-1, атипичные антидепрессанты, бензодиазепины, агонисты или антагонисты 5-HT1a, в частности частичные агонисты 5-HT1a, и антагонисты фактора высвобождения кортикотропина (CRF). Конкретные средства включают амитриптилин, кломипрамин,доксепин, имипрамин и тримипрамин; амоксапин, дезипрамин, мапротилин, нортриптилин и протриптилин; флуоксетин, флувоксамин, пароксетин и сертралин; изокарбоксазид, фенелзин, транилципромин и селегилин; моклобемид; венлафаксин; дулоксетин; апрепитант; бупропион, литий, нефазодон, тразодон и вилоксазин; альпразолам, хлордиазепоксид, клоназепам, хлоразепат, диазепам, галазепам, лоразепам,оксазепам и празепам; буспирон, флезиноксан, гепирон и ипсапирон, и их фармацевтически приемлемые соли. Соединения по настоящему изобретению могут быть введены посредством перорального, парентерального (например, внутримышечно, внутрибрюшинно, внутривенно, ICV (через церебральные вены),интрацистернальной инъекцией или вливанием, подкожной инъекцией или вживлением имплантата),посредством ингаляционного, назального, вагинального, ректального, сублингвального или местного способа введения и могут быть приготовлены по отдельности или совместно, в составах с соответствующими дозированными единицами, содержащих обычные нетоксичные фармацевтически приемлемые носители, вспомогательные вещества и среды для лекарственного вещества, соответствующие каждому способу введения. В дополнение к лечению теплокровных животных, таких как мыши, крысы, лошади,крупный рогатый скот, овцы, собаки, кошки, обезьяны и тому подобное, соединения по настоящему изобретению являются эффективными для использования на людях. Термины "введение" и/или "вводимое" соединение следует понимать как обозначающие предоставление соединения по изобретению или пролекарства соединения по изобретению индивидууму, нуждающемуся в лечении. Термин "композиция", как используется в этом документе, предназначается для охвата продукта,- 16023685 содержащего указанные ингредиенты в заданных количествах или пропорциях, а также любого продукта, который получается, непосредственно или опосредованно, в результате объединения указанных ингредиентов в указанных количествах. Этот термин в связи с фармацевтической композицией предназначен для охвата продукта, содержащего активный(е) ингредиент(ы) и инертный(е) ингредиент(ы), которые составляют носитель, а также любого продукта, который получается, непосредственно или опосредованно, в результате объединения, комплексообразования или агрегации любых двух или более ингредиентов или в результате диссоциации одного или нескольких ингредиентов, или в результате протекания других типов реакций или взаимодействий одного или более ингредиентов. В целом, фармацевтические композиции получают посредством приведения активного ингредиента к однородной и тесной ассоциации с жидким носителем или мелкодисперсным твердым носителем, или с тем и с другим, и затем,при необходимости, формования продукта в виде желаемого состава. В фармацевтическую композицию активное заявленное соединение включается в количестве, достаточном для оказания желаемого влияния на ход заболеваний или на состояние пациента при данных заболеваниях. Соответственно, фармацевтические композиции по настоящему изобретению охватывают любую композицию, полученную посредством смешивания соединения по настоящему изобретению и фармацевтически приемлемого носителя. Фармацевтические композиции, предназначенные для перорального использования, могут быть приготовлены в соответствии с любым способом, известным в области изготовления фармацевтических композиций, и такие композиции могут содержать одно или несколько веществ, выбранных из группы,состоящей из подслащивающих веществ, ароматизирующих веществ, красящих веществ и консервирующих веществ, с обеспечением фармацевтически элегантных и приятных на вид и вкус препаратов. Таблетки содержат активный ингредиент, находящийся в смеси с нетоксичными фармацевтически приемлемыми эксципиентами, которые являются пригодными для производства таблеток. Таблетки могут не иметь покрытия, или они могут быть покрыты оболочкой с помощью известных технологий, для замедления разрушения и всасывания в желудочно-кишечном тракте, и обеспечения посредством этого пролонгированного действия в течение более длительного периода. Композиции для перорального использования могут также быть представлены в виде твердых желатиновых капсул, где активные ингредиенты смешаны с инертным твердым разбавителем, например с карбонатом кальция, фосфатом кальция или каолином, или в виде мягких желатиновых капсул, где активный ингредиент смешан с водой или масляной средой, например с арахисовым маслом, жидким парафином или оливковым маслом. Водные суспензии, масляные суспензии, диспергируемые порошки или гранулы, эмульсии типа "масло-в-воде" и стерильная водная или маслянистая суспензия для инъекций могут быть получены с помощью стандартных способов, известных в данной области. Под "фармацевтически приемлемый" понимают носитель,разбавитель или зксципиент, который должен быть совместим с другими ингредиентами состава и не должен оказывать вредное действие на пациента, принимающего данный препарат. Заявленные соединения, кроме того, являются полезными в способе предупреждения, лечения, контролирования, уменьшения интенсивности симптомов или снижения риска возникновения заболеваний,расстройств и состояний, отмеченных в этом документе. Дозировка активного ингредиента в композициях по этому изобретению может варьироваться, однако необходимо, чтобы количество активного ингредиента было таким, которое позволяет получить подходящую лекарственную форму. Активный ингредиент может быть введен пациентам (животным и человеку), нуждающимся в таком лечении, дозировками,которые будут обеспечивать оптимальную фармацевтическую эффективность. Выбираемая дозировка зависит от желаемого терапевтического эффекта, от пути введения и от длительности лечения. Доза будет варьироваться от пациента к пациенту в зависимости от природы и тяжести заболевания, массы пациента, специальных диет, которых придерживается пациент, сопутствующего медикаментозного лечения и других факторов, которые будут понятны специалистам в данной области. Как правило, пациенту,например, людям и людям в пожилом возрасте, вводят дозировки на уровне между 0,001 и 10 мг/кг массы тела в сутки. Диапазон дозировок, как правило, будет составлять 0,5 мг - 1,0 г на пациента в сутки,которые могут быть введены разовой дозой или многократными дозами. В одном из вариантов осуществления диапазон дозировок будет составлять приблизительно 0,5-500 мг на пациента в сутки; в другом варианте осуществления приблизительно 0,5-200 мг на пациента в сутки и в еще одном варианте осуществления приблизительно 5-50 мг на пациента в сутки. Фармацевтические композиции по настоящему изобретению могут быть обеспечены в твердой дозированной лекарственной форме, например, содержащей приблизительно 0,5-500 мг активного ингредиента или содержащей приблизительно 1-250 мг активного ингредиента. Фармацевтическая композиция может быть обеспечена в твердей дозированной лекарственной форме, содержащей приблизительно 1, 5,10, 25, 50, 100, 200 или 250 мг активного ингредиента. В случае перорального введения композиции могут быть обеспечены в форме таблеток, содержащих 1,0-1000 мг активного ингредиента, как, например,1, 5, 10, 15, 20, 25, 50, 75, 100, 150, 200, 250, 300, 400, 500, 600, 750, 800, 900 и 1000 мг активного ингредиента, для симптоматической корректировки дозировки для пациента, подлежащего лечению. Соединения могут быть введены по схеме 1-4 раза в день, как, например, однократно или двукратно в сутки. Несколько способов получения соединений по настоящему изобретению проиллюстрировано на следующих далее схемах и в примерах. Исходные материалы и необходимые промежуточные соедине- 17023685 ния в некоторых случаях являются коммерчески доступными или же могут быть получены в соответствии с известными из литературы методиками или в соответствии с тем, как проиллюстрировано в описании. Соединения по настоящему изобретению могут быть получены посредством использования реакций, которые показаны на следующих далее схемах, в дополнение к другим стандартным манипуляциям,которые известны из литературы или приведены в качестве примера в экспериментальных методиках. Нумерация заместителей, которая показана на схемах, необязательно коррелирует с нумерацией, используемой в формуле изобретения, и часто, для ясности, показан один заместитель, присоединенный к соединению там, где возможно много заместителей, в соответствии с определениями, приведенными выше. Реакции, используемые для получения соединений по настоящему изобретению, осуществляют посредством использования реакций, которые показаны на схемах ипримерах в этом документе, в дополнение к другим стандартным манипуляциям, таким как сложноэфирный гидролиз, отщепление защитных групп и тому подобное, которые могут быть известны из литературы или приведены в качестве иллюстрации в экспериментальных методиках. Исходные вещества изготавливают согласно методикам, которые известны в данной области или проиллюстрированы в этом документе. В этом документе используют следующие сокращения: Me - метил; Et - этил; t-Bu - грет-бутил; Ar - арил; Ph - фенил; Bn - бензил; Ас - ацетил;HOBt - гидроксибензотриазолгидрат; TEA - триэтиламин; DMF - N,N-диметилформамид; к.т. - комнатная температура; HPLC - высокоэффективная жидкостная хроматография; ЯМР - ядерный магнитный резонанс; TLC - тонкослойная хроматография. В некоторых случаях конечный продукт может быть дополнительно модифицирован, например, посредством манипуляции с заместителями. Эти манипуляции могут включать реакции восстановления,окисления, алкилирования, ацилирования и гидролиза, которые обычно известны специалистам в данной области, но не ограничиваются этим. В некоторых случаях порядок выполнения указанных выше схем реакций может быть изменен для облегчения протекания реакции или для исключения нежелательных продуктов реакции. Следующие примеры приводятся для того, чтобы можно было бы прийти к более полному пониманию настоящего изобретения. Эти примеры являются только иллюстративными и не должны рассматриваться как ограничивающие настоящее изобретение каким-либо образом. Реакционная схема А(1,973 мл, 19,02 ммоль) и перемешивают при кипячении с обратным холодильником в течение ночи. Смесь концентрируют в вакууме и остаток очищают градиентным элюированием на силикагеле (0-50%EtOAc в гексане), что сопровождается элюированием пика 1 (А-1-транс) (1,6 г, 44%), затем градиент растворителей увеличивают до 100% EtOAc, что сопровождается элюированием пика 2 (А-2-цис). (914 мг,25%), в обоих случаях в виде масел желтого цвета. Энантиомеры А-1-транс могут быть разделены с помощью хиральной препаративной сверхкритической флюидной хроматографии (SFC) (внутренний диаметр 3,0 см 25 см ChiralTech IC, 7% EtOH/CO2, 70 мл/мин) и проанализированы с помощью хиральной аналитической SFC (внутренний диаметр 4,6 мм 25 см ChiralTech IC, 7% EtOH/CO2, 2,4 мл/мин): энт 1=3,6 мин, энт 2 = 4,1 мин, что дает указанное в заглавии соединение. 1 Н ЯМР(500 МГц, CDCl3): 8,44 (м, 1 Н), 7,56 (тд, J=7,6, 1,7 Гц, 1 Н), 7,22 (дд, J=7,8, 1,0 Гц, 1 Н),7,08 (ддд, J=7,6, 4,9, 1,2 Гц, 1 Н), 4,17 (кв., J=7,3 Гц, 2 Н), 2,58 (ддд, J=10,0, 6,1, 3,9 Гц, 1 Н), 2,25 (ддд,J=9,5, 5,6, 3,9 Гц, 1 Н), 1,61 (м, 2 Н), 1,28 (т, J=7,1 Гц, 3 Н) ; LRMS (ES) (масс-спектрометрия низкого разрешения с ионизацией электрораспылением): вычислено М+Н для C11H13NO2S: 192,2; найдено: 192,1.(S,S) [транс 2-(пиридин-2-ил)циклопропил]метанол (А-4). Раствор А-1-транс (751 мг, 3,93 ммоль) в THF (20 мл) охлаждают до 0 С и медленно обрабатывают литийалюмогидридом (3,93 мл, 3,93 ммоль, 1 М раствор в THF). Раствор нагревают до комнатной температуры и перемешивают в течение 20 мин. Реакционную смесь затем повторно охлаждают до 0 С и обрабатывают по каплям последовательно посредством 0,15 мл воды, 0,15 мл 15%-го раствора NaOH и 0,45 мл воды. К смеси добавляют сульфат натрия. После перемешивания при комнатной температуре в течение 10 мин смесь фильтруют через слой Целита и фильтрат концентрируют в вакууме с получением ука- 18023685 занного в заглавии соединения в виде масла бледно-желтого цвета. Вещество является достаточно чистым для использования на последующей стадии без дополнительной очистки. 1 Н ЯМР (500 МГц, CDCl3):8,41 (д, J=4,2 Гц, 1 Н), 7,52 (тд, J=7,6, 1,7 Гц, 1 Н), 7,10 (д, J=7,8 Гц, 1 Н),7,03 (ддд, J=7,3, 4,9, 0,7 Гц, 1 Н), 3,72 (дд, J=11,2, 6,4 Гц, 1 Н), 3,57 (дд, J=11,2, 7,1 Гц, 1 Н), 2,26 (шир. с,1 Н), 1,98 (м, 1 Н), 1,74 (м, 1 Н), 1,25 (м, 1 Н), 0,96 (м, 1 Н) м.д.; LRMS (ES) (масс-спектрометрия низкого разрешения с ионизацией электрораспылением): вычислено М+Н для C9H11NO: 150,2; найдено: 150,1. В качестве альтернативного средства разделения энантиомеров с этим элементарным звеном, энантиомер А-4 отделяют от его соответствующего энантиомера с помощью хиральной препаративной сверхкритической флюидной хроматографии (SFC) (внутренний диаметр 3,0 см 25 см ChiralPak AD-H,MeCN/MeOH/CO2 3:7:90, 70 мл/мин) и анализируют с помощью хиральной аналитической SFC (внутренний диаметр 4,6 мм 25 см ChiralPak AD-H, MeCN/MeOH/CO2 3:7:90, 2,4 мл/мин): энт 1=7,5 мин,энт 2=8,4 мин. С использованием этого способа определяют, что энантиомер (S,S) дает второй пик элюирования и выделяется с энантиомерным избытком 98,7%. Реакционная схема В 2-Винилхинолин (В-1). Раствор 2-хлорхинолина (1 г, 6,11 ммоль) и винилтрибутилолова (2,69 мл, 9,17 ммоль) в толуоле (30 мл) обрабатывают посредством Pd(PPh3)4 (0,706 г, 0,611 ммоль) и нагревают и кипятят с обратным холодильником в течение 1,5 ч. Реакционную смесь концентрируют и получающийся в результате материал очищают непосредственно градиентным элюированием на силикагеле (0-25% EtOAc в гексане) с получением указанного в заглавии соединения в виде бесцветного масла (941 мг, 99%). LRMS m/z (M+H) 156,1: найдено, 156,2: рассчитано. Этил 2-(хинолин-2-ил)циклопропанкарбоксилат (В-2-транс). Раствор В-1 (941 мг, 6,06 ммоль) в толуоле (20 мл) обрабатывают этилдиазоацетатом (0,629 мл, 6,06 ммоль) и перемешивают при кипячении с обратным холодильником в течение ночи. Смесь концентрируют и остаток очищают градиентным элюированием на силикагеле (0-30% EtOAc в гексане), что сопровождается элюированием пика 1 (транс-диастереомер). Затем градиент растворителей увеличивают (до 50% EtOAc в гексане), что сопровождается элюированием пика 2 (цис-диастереомер). Это дает указанное в заглавии соединение в виде масла бледно-желтого цвета (706 мг, 40%, степень чистоты приблизительно 70%), которое можно использовать на следующей стадии без дополнительной очистки, LRMS m/z(S,S) [2-(хинолин-2-ил)циклопропил]метанол (В-4). Раствор В-2-транс (200 мг, 0,829 ммоль) в THF (20 мл) охлаждают до 0 С и медленно обрабатывают посредством 1 М раствора LiAlH4 в THF (0,829 мл, 0,829 ммоль). Раствор нагревают до комнатной температуры и перемешивают в течение 20 мин. Смесь повторно охлаждают до 0 С и обрабатывают по каплям последовательно посредством 0,03 мл воды, 0,03 мл 15%-го раствора NaOH и 0,09 мл воды. К смеси добавляют сульфат натрия и после перемешивания при комнатной температуре в течение 10 мин смесь фильтруют через слой Целита с исчерпывающим элюированием посредством CH2Cl2 и МеОН. Фильтрат концентрируют в вакууме и получающийся в результате остаток очищают градиентным элюированием на силикагеле (0-100% EtOAc в гексане) с получением указанного в заглавии соединения в виде бесцветного масла (130 мг, 79%). 1 Н ЯМР (500 МГц, CDCl3):7,93 (д, J=3,5 Гц, 1 Н), 7,90 (д, J=3,5 Гц, 1 Н), 7,67 (д, J=8,1 Гц, 1 Н), 7,59(дд, J=11,4, 7,2 Гц, 1 Н), 2,15 (дт, J=8,5, 4,4 Гц, 1 Н), 1,84 (м, 1 Н), 1,33 (дт, J=8,6, 4,4 Гц, 1 Н), 1,01 (ддд,J=10,4, 5,9, 1,1 Гц, 1 Н) м.д.; LRMS (ES) (масс-спектрометрия низкого разрешения с ионизацией электрораспылнием) m/z (M+H) 200,1 найдено, 200,2 рассчитано. Энантиомер В-4 отделяют от его соответствующего энантиомера с помощью хиральной препаративной сверхкритической флюидной хроматографии (SFC) (внутренний диаметр 3,0 см 25 см ChiralPak AD-H, 30% МеОН/СО 2 + 0, 1% DEA, 70 мл/мин)- 19023685 и анализируют с помощью хиральной аналитической SFC (внутренний диаметр 4,6 мм 25 см ChiralPakAD-H, 30% МеОН/СО 2+0,1 DEA, 2,4 мл/мин): энт 1=2,8 мин, энт 2=3,5 мин. С использованием этого способа определяют, что энантиомер (S,S) дает первый пик элюирования и выделяется с энантиомерным избытком 99%. Реакционная схема С Этил 3-(1,5-нафтиридин-2-ил)проп-2-еноат (С-1). 2-Хлор-1,5-нафтиридин (101 мг, 0,614 ммоль), сложный эфир бороновой кислоты X1 (195 мг, 0,920 ммоль), S-Phos (25,2 мг, 0,061 ммоль), K3PO4 (391 мг, 1,84 ммоль) и PdOAc2 (6,89 мг, 0,031 ммоль) объединяют в 5-миллилитровом флаконе, пригодном для использования в условиях микроволнового излучения, в THF (2,5 мл) и воде (500 мкл). Реакционную смесь нагревают при 100 С в течение 15 мин. Реакционную смесь разбавляют посредством EtOAc (20 мл), промывают насыщенным водным растворомNaHCO3 (25 мл) и насыщенным солевым раствором (25 мл), сушат над MgSO4, фильтруют и концентрируют в вакууме. Получающийся в результате остаток очищают градиентным элюированием на силикагеле (10-100%EtOAc в гексане) с получением указанного в заглавии соединения в виде твердого вещества бледнооранжевого цвета (118 мг, 90%). 1 Н ЯМР (500 МГц, ДМСО):9,02 (дд, J=4,1, 1,6 Гц, 1 Н), 8,48 (д, J=8,8 Гц, 1 Н), 8,48-8,42 (м, 1 Н),8,25 (д, J=8,7 Гц, 1 Н), 7,84-7,79 (м, 2 Н), 7,13 (д, J=16,0 Гц, 1 Н), 4,25 (кв., J=7,1 Гц, 2 Н), 1,30 (т, J=7,1 Гц,3 Н) м.д.; LRMS (ES) (масс-спектрометрия низкого разрешения с ионизацией электрораспылением) m/z(M+H) 229,2 найдено, 229,1 рассчитано. Этил 2-(1,5-нафтиридин-2-ил)циклопропанкарбоксилат (С-2). В 5-миллилитровый герметизированный флакон добавляют триметилсульфоксониййодид (170 мг,0,770 ммоль), ДМСО (2567 мкл) и NaH (26,7 мг, 0,668 ммоль). Эту смесь перемешивают в течение 40 мин при 50 С. Реакционную смесь затем охлаждают до комнатной температуры и к ней добавляют раствор С 1 (110 мг, 0,513 ммоль) в ДМСО (1,5 мл). Реакционную смесь перемешивают при комнатной температуре в течение 5 мин, затем разбавляют посредством EtOAc (75 мл) и промывают насыщенным водным раствором NaHCO3 (420 мл). Органическую часть сушат над MgSO4, фильтруют и концентрируют в вакууме. Получающийся в результате остаток очищают градиентным элюированием на силикагеле (20100% EtOAc в гексане) с получением указанного в заглавии соединения (67 мг, 57%). 1 Н ЯМР (500 МГц, CDCl3):8,89 (дд, J=4,2, 1,6 Гц, 1 Н), 8,28 (д, J=8,6 Гц, 1 Н), 8,23 (д, J=8,6 Гц, 1 Н),7,60-7,57 (м, 2 Н), 4,20 (кв., J=7,1 Гц, 2 Н), 2,82-2,77 (м, 1 Н), 2,47-2,42 (м, 1 Н), 1,79 (ддд, J=8,6, 6,0, 3,8 Гц,1 Н), 1,71 (ддд, J=8,9, 5,6, 3,8 Гц, 1 Н), 1,29 (т, J=7,2 Гц, 3 Н) м.д.; LRMS (ES) (масс-спектрометрия низкого разрешения с ионизацией электрораспылением) m/z (M+H) 243,3 найдено, 243,3 рассчитано.(S,S) [2-(1,5-нафтиридин-2-ил)циклопропил]метанол (С-4). Указанное в заглавии соединение получают из С-2 в соответствии с протоколом, представленным на схеме А, с получением указанного в заглавии соединения в виде камеди коричневого цвета. 1 Н ЯМР (500 МГц, CDCl3):8,86 (дд, J=4,2, 1,6 Гц, 1 Н), 8,21-8,26 (м, 2 Н), 7,57 (дд, J=8,5, 4,2 Гц,1 Н), 7,44 (д, J=8,7 Гц, 1 Н), 3,77 (дд, J=11,3, 6,3 Гц, 1 Н), 3,68 (дд, J=113, 6,9 Гц, 1 Н), 2,21 (дт, J=8,6, 4,5 Гц,1 Н), 1,99-1,92 (м, 1 Н), 1,48-1,42 -(м, 1 Н), 1,16-1,10 (м, 1 Н); LRMS (ES) (масс-спектрометрия низкого разрешения с ионизацией электрораспылением) m/z (M+H) 201,3 найдено, 201,2 рассчитано. Энантиомер С 4 отделяют от его соответствующего энантиомера с помощью хиральной препаративной сверхкритической флюидной хроматографии (SFC) (внутренний диаметр 3,0 см 25 см ChiralPak AD-H, 30% МеОН/СО 2 + 0,1% DEA, 70 мл/мин) и анализируют с помощью хиральной аналитической SFC (внутренний диаметр 4,6 мм 25 см ChiralPak AD-H, 30% МеОН/СО 2+0,1% DEA, 2,4 мл/мин): энт 1=3,4 мин,энт 2=4,7 мин. С использованием этого способа определяют, что энантиомер (S,S) дает второй пик элюирования и выделяется с энантиомерным избытком 99%. Этил 3-(5-метоксипиридин-2-ил)проп-2-еноат (D-1). В 25-миллилитровый флакон, пригодный для использования в условиях микроволнового излучения,добавляют 2-бром-5-метоксипиридин (1,88 г, 10 ммоль), этилакрилат (5,44 мл, 50,0 ммоль), Pd(OAc)2(0,225 г, 1,000 ммоль), K2CO3 (4,15 г, 30,0 ммоль) и гидрат трет-бутиламмонийхлорида (2,96 г, 10,00 ммоль). Суспензию нагревают в микроволновой печи при 160 С в течение 1 ч. При охлаждении до комнатной температуры смесь разбавляют посредством EtOAc (100 мл) и промывают насыщенным водным раствором NaHCO3 (100 мл). Водный слой экстрагируют дополнительным EtOAc (250 мл). Объединенные органические слои затем промывают водой и насыщенным солевым раствором, сушат над Na2SO4, фильтруют и концентрируют в вакууме. Получающийся в результате остаток очищают градиентным элюированием на силикагеле (0-50% EtOAc в гексане) с получением указанного в заглавии соединения (1,5 г,72%). 1 Н ЯМР (500 МГц, CDCl3):8,35 (д, J=3,0 Гц, 1 Н), 7,65 (д, J=15,7 Гц, 1 Н), 7,38 (д, J=8,6 Гц, 1 Н),7,18 (дд, J=8,6, 3,0 Гц, 1 Н), 6,76 (д, J=15,7 Гц, 1 Н), 4,26 (кв., J=7,1 Гц, 2 Н), 3,89 (с, 3 Н), 1,33 (т, J=7,1 Гц,3 Н) м.д.; LRMS (ES) (масс-спектрометрия низкого разрешения с ионизацией электрораспылением) m/z(M+H) 208,0 найдено, 208,2 рассчитано. Этил 2-(5-метоксипиридин-2-ил)циклопропанкарбоксилат (D-2). Указанное в заглавии соединение получают из D-1 в соответствии с указанным на схеме С протоколом с получением D-2 в виде твердого вещества светло-желтого цвета. 1 Н ЯМР (500 МГц, CDC13) :8,15 (д, J=2,9 Гц, 1 Н), 7,14 (д, J=8,0 Гц, 1 Н), 7,10 (дд, J=8,0, 2,9 Гц,1 Н), 4,16 (кв., J=7,1 Гц, 2 Н, 3,82 (с, 3 Н), 2,58-2,52 (м, 1 Н), 2,18-2,12 (м, 1 Н), 1,56 (м, 1 Н), 1,54 (м, 1 Н), 1,27(S,S) [2-(5-метоксипиридин-2-ил)циклопропил]метанол (D-4). Указанное в заглавии соединение получают из D-2 в соответствии с протоколом, указанным на схеме А, с получением D-4 в виде масла светло-желтого цвета. 1 Н ЯМР (500 МГц, CDCl3):8,14 (д, J=2,9 Гц, 1 Н), 7,09 (дд, J=8,6, 2,9 Гц, 1 Н, 7,04 (д, J=8,6 Гц, 1 Н),3,82 (с, 3 Н), 3,72-3,66 (м, 1 Н), 3,61-3,55 (м, 1 Н), 1,97-1,91 (м, 1 Н), 1,69-1,62 (м, 1 Н), 1,20-1,14 (м, 1 Н), 0,91(1 Н, дт, J=8,71, 5,06 Гц) м.д.; LRMS (масс-спектрометрия низкого разрешения) m/z (M+H) 180,1 найдено,180,1 рассчитано. Энантиомер D-4 отделяют от его соответствующего энантиомера с помощью хиральной препаративной сверхкритической флюидной хроматографии (SFC) (внутренний диаметр 3,0 см 25 см ChiralPak AD-H, MeCN/MeOH/CO2 6,7/13,3/80, +0,1% DEA, 70 мл/мин) и анализируют с помощью хиральной аналитической SFC (внутренний диаметр 4,6 мм 25 см ChiralPak AD-H, MeCN/MeOH/CO2 6,7/13,3/80, +0,1% DEA, 2,4 мл/мин): энт 1=3,7 мин, энт 2 = 4,4 мин. С использованием этого способа определяют, что энантиомер (S,S) дает второй пик элюирования и выделяется с энантиомерным избытком 99%. Реакционная схема Е 2-Бром-5-(фторметил)пиридин (Е-1). К перемешанному раствору 2-бром-5-метилпиридина (23,8 г, 138,0 ммоль) и винилтрифторбората калия (20,39 г, 152,0 ммоль) в диоксане (235 мл) под азотом добавляют Pd(dppf)2Cl2 (11,30 г, 13,8 ммоль),карбонат цезия (135,0 г, 415,0 ммоль) и воду (41,5 мл). Получающуюся в результате смесь нагревают до 100 С в течение 2 ч. Реакционная смесь разделяется на этилацетат и насыщенный раствор бикарбоната натрия. Органическую фазу концентрируют, и разделение на флэш-колонке с использованием градиента- 21023685 этилацетат/гексан 0-30% дает Е-1 в виде летучего масла, которое переносят непосредственно на следующую стадию. Этил 2-(5-метилпиридин-2-ил)циклопропанкарбоксилат (Е-2-транс). К перемешанному раствору Е-1 (16,44 г, 138,0 ммоль) в толуоле (300 мл) добавляют этилдиазоацетат (42,9 мл, 414,0 ммоль) и получающуюся в результате смесь нагревают до 100 С в течение 3 ч. Смесь оставляют остыть и разделиться на этилацетат и насыщенный раствор бикарбоната натрия. Органическую фазу концентрируют, и разделение на флэш-колонке с использованием градиента этилацетат/гексан 0-20% дает Е-2-транс в виде масла (11,7 г, 41%). LRMS (ES) (М+Н)+: найдено 206,2, вычислено 2 06,2.(S,S) [2-(5-метилпиридин-2-ил)циклопропил]метанол (Е-3). Раствор Е-2-транс (5,0 г, 24,36 ммоль) в THF (80 мл) охлаждают до 0 С и медленно обрабатывают литийалюмогидридом (55,0 мл, 55,0 ммоль, 1 М раствор в THF). Раствор перемешивают в течение 30 мин при 0 С. Реакционную смесь затем обрабатывают по каплям последовательно посредством 2,0 мл воды,2,0 мл 15%-го раствора NaOH и 6,0 мл воды. Сульфат натрия добавляют к смеси. После перемешивания при комнатной температуре в течение 4 ч, смесь фильтруют и фильтрат концентрируют в вакууме с получением указанного в заглавии соединения в виде масла бледно-желтого масла (3,4 г, 85,4%). LRMS(ES) (М+Н)+: найдено 164,2, вычислено 164,2. 1 Н ЯМР (400 МГц, ДМСО-d6):8,21 (м, 1 Н), 7,41 (м, 1 Н), 7,12 (м, 1 Н), 4,57 (м, 1 Н), 3,44 (м, 1 Н),3,33 (м, 1 Н), 2,21 (с, 3 Н), 1,88 (м, 1 Н), 1,44 (м, 1 Н), 0,98 (м, 1 Н), 0,81 (м, 1 Н). Энантиомер Е-3 отделяют от его соответствующего энантиомера с помощью хиральной препаративной сверхкритической флюидной хроматографии (SFC) (внутренний диаметр 3,0 см 25 см ChiralPak AS-H, 10% iPrOH/CO2 + 0, 1% DEA,80 мл/мин) и анализируют с помощью хиральной аналитической SFC (внутренний диаметр 4,6 мм 15 см ChiralPak AS-H, 15% iPrOH/CO2 + 0, 1% DEA, 2,4 мл/мин): энт 1=3,7 мин, энт 2=4,5 мин, что дает указанное в заглавии соединение. С использованием этого способа определяют, что энантиомер (S,S) дает второй пик элюирования и выделяется с энантиомерным избытком 99%. Реакционная схема F 2-Бром-5-(фторметил)пиридин (F-1). К перемешанному раствору (6-бромпиридин-3-ил)метанола (1,00 г, 5,32 ммоль) в дихлорметане (25 мл) при 0 С добавляют DAST (0,70 мл, 5,32 ммоль) и получающийся в результате раствор перемешивают при 0 С в течение 1 ч. Смесь промывают насыщенным раствором бикарбоната натрия и концентрируют. Разделение на флэш-колонке с использованием градиента этилацетата/гексана 0-10% дает F-1 (0,37 г, 37%). LRMS (ES) (М+Н)+: найдено 190,0/192,0, вычислено 190,0/192,0. 5-(Фторметил)-2-винилпиридин (F-2). К перемешанному раствору F-1 (1,09 г, 5,74 ммоль) и винилтрифторбората калия (1,54 г, 11,47 ммоль) в диоксане (9,75 мл) под азотом добавляют Pd(dppf)2Cl2 (0,47 г, 0,57 ммоль), карбонат цезия (5,61 г, 17,21 ммоль) и воду (1,72 мл). Получающуюся в результате смесь нагревают до 100 С в течение 90 мин. Реакционная смесь разделяется на этилацетат и насыщенный раствор бикарбоната натрия. Органическую фазу концентрируют, и разделение на флэш-колонке с использованием градиента этилацетат/гексан 0-15% дает F-2 в виде масла (0,53 г, 61%). LRMS (ES) (М+Н)+: найдено 138,0, вычислено 138,1. Этил 2-(5-(фторметил)пиридин-2-ил)циклопропанкарбоксилат (F-3-транс). Указанное в заглавии соединение получают из F-2 в соответствии с протоколом, указанным на схеме А, в итоге получают в форме транс-рацемата без хирального разделения F-3-транс в виде масла коричневого цвета. LRMS (ES) (M+H)+: найдено 224,2, вычислено 224,2. 2-(5-(Фторметил)пиридин-2-ил)циклопропил)метанол (F-4). Указанное в заглавии соединение получают из F-3-транс в соответствии с протоколом, указанным на схеме А, с получением F-4 в виде масла желтого цвета. LRMS (ES) (M+H)+: найдено 182,2, вычислено 182,2. 2-Хлор-5-(дифторметил)пиридин (G-1). Указанное в заглавии соединение получают из 2-хлор-5-пиридинкарбоксальдегида в соответствии с протоколом, указанным на схеме F, с получением G-l. LRMS (ES) (М+Н)+: найдено 164.1, вычислено 164,5. 5-(Дифторметил)-2-винилпиридин (G-2). Указанное в заглавии соединение получают из G-1 в соответствии с протоколом, указанным на схеме F, с получением G-2 в виде масла. LRMS (ES) (М+Н)+: найдено 156,1, вычислено 156,1. Этил 2-(5-(дифторметил)пиридин-2-ил)циклопропанкарбоксилат (G-3-транс). Указанное в заглавии соединение получают из G-2 в соответствии с протоколом, указанным на схеме А, в итоге получают в форме транс-рацемата без хирального разделения G-3-транс в виде масла.LRMS (ES) (M+H)+: найдено 242,2, вычислено 242,2. 2-(5-(Дифторметил)пиридин-2-ил)циклопропил)метанол (G-4). Указанное в заглавии соединение получают из G-3-транс в соответствии с протоколом, указанным на схеме А, с получением G-4 в виде масла желтого цвета. LRMS (ES) (M+H)+: найдено 200,2, вычислено 200,2. Реакционная схема Н 3-Метил-6-винилпиридазин (Н-1). Указанное в заглавии соединение получают из 3-хлор-6-метилпиридазина в соответствии с протоколом, указанным на схеме F, с получением Н-1 в виде масла. LRMS (ES) (M+H)+: найдено 121,1, вычислено 121,1. Этил 2-(6-метилпиридазин-3-ил)циклопропанкарбоксилат (Н-2-транс). Указанное в заглавии соединение получают из Н-1 в соответствии с протоколом, указанным на схеме А, в итоге получают в форме транс-рацемата без хирального разделения Н-2-транс в виде масла.LRMS (ES) (М+Н)+: найдено 207,2, вычислено 207,2. 2-(6-Метилпиридазин-3-ил)циклопропил)метанол (Н-3). Указанное в заглавии соединение получают из Н-2-транс в соответствии с протоколом, указанным на схеме А, с получением Н-3 в виде масла. LRMS (ES) (М+Н)+: найдено 165,2, вычислено 165,2. Реакционная схема I 5-Бром-2-винилпиридин (I-1). Указанное в заглавии соединение получают из 2,5-дибромпиридина в соответствии с протоколом,указанным на схеме F, с получением I-1 в виде масла. LRMS (ES) (M+H)+: найдено 184,0/186,0, вычислено 184,0/186,0. Этил 2-(5-бромпиридин-2-ил)циклопропанкарбоксилат (I-2-транс). Указанное в заглавии соединение получают из I-1 в соответствии с протоколом, указанным на схеме А, в итоге получают в форме транс-рацемата без хирального разделения I-2-транс в виде масла. LRMS(ES) (M+H)+: найдено 270,1/272,1, вычислено 270,1/272,1. 2-(5-Бромпиридин-2-ил)циклопропил)метанол (I-3). Указанное в заглавии соединение получают из I-2-транс в соответствии с протоколом, указанным на схеме А, с получением I-3 в виде масла. LRMS (ES) (M+H)+: найдено 228,1/230,1, вычислено 228,1/230,1. Реакционная схема J Этил 2-(5-фторпиридин-2-ил)циклопропанкарбоксилат (J-2-транс). 2-Бром-5-фторпиридин используют для получения J-1 в соответствии с протоколом, указанным на схеме F. J-1 используют непосредственно для получения указанного в заглавии соединения в соответствии с протоколом, указанным на схеме А, с получением J-2-транс в виде масла. LRMS (ES) (М+Н)+: найдено 210,2, вычислено 210,2. 2-(5-Фторпиридин-2-ил)циклопропил)метанол (J-4). Указанное в заглавии соединение получают из J-2-транс в соответствии с протоколом, указанным на схеме А, с получением J-4 в виде масла. LRMS (ES) (М+Н)+: найдено 168,0, вычислено 168,2. Реакционная схема K 5-(Трифторметил)-2-винилпиридин (K-1). Указанное в заглавии соединение получают из 2-бром-5-трифторметилпиридина в соответствии с протоколом, указанным на схеме F, с получением K-1 в виде масла. LRMS (ES) (M+H)+: найдено 174,0,вычислено 174,1. Этил 2-(5-(трифторметил)пиридин-2-ил)циклопропанкарбоксилат (K-2-транс). Указанное в заглавии соединение получают из K-1 в соответствии с протоколом, указанным на схеме А, в итоге получают в форме транс-рацемата без хирального разделения K-3-транс в виде масла.LRMS (ES) (М+Н)+: найдено 260,1, вычислено 2 60,2. 2-(5-(Трифторметил)пиридин-2-ил)циклопропил)метанол (K-3). Указанное в заглавии соединение получают из K-3-транс в соответствии с протоколом, указанным на схеме А, с получением K-4 в виде масла. LRMS (ES) (М+Н)+: найдено 218,1, вычислено 218,2. Реакционная схема L 3-Фтор-5-метил-2-винилпиридин (L-1). Указанное в заглавии соединение получают из 2-хлор-3-фтор-5-метилпиридина в соответствии с протоколом, указанным на схеме F, с получением L-2 в виде масла. LRMS (ES) (M+H)+: найдено 138,0,вычислено 138,1. Этил 2-(3-фтор-5-метилпиридин-2-ил)циклопропанкарбоксилат (L-2-транс).- 24023685 Указанное в заглавии соединение получают из L-1 в соответствии с протоколом, указанным на схеме А, в итоге получают в форме транс-рацемата без хирального разделения L-2-транс в виде масла.LRMS (ES) (M+H)+: найдено 224,2, вычислено 224,2. 2-(3-Фтор-5-метилпиридин-2-ил)циклопропил)метанол (L-3). Указанное в заглавии соединение получают из L-2-транс в соответствии с протоколом, указанным на схеме А, с получением L-3 в виде масла. LRMS (ES) (M+H)+: найдено 182,1, вычислено 182,2. Реакционная схема М(Е)-этил 3-(пиразоло[1,5-а]пиридин-2-ил)акрилат (М-1). Указанное в заглавии соединение получают из 2-хлорпиразоло[1,5-а]пиридина в соответствии с протоколом, указанным на схеме С, с получением М-1 в виде масла. LRMS (ES) (М+Н)+: найдено 203,2,вычислено 203,2. Этил 2-(пиразоло[1,5-а])пиридин-2-ил)циклопропанкарбоксилат (М-2-транс). Указанное в заглавии соединение получают из М-1 в соответствии с протоколом, указанным на схеме С, в итоге получают в форме транс-рацемата без хирального разделения М-2-транс в виде твердого вещества. LRMS (ES) (М+Н)+: найдено 217,1, вычислено 217,2. 2-(Пиразоло[1,5-а]пиридин-2-ил)циклопропил)метанол (М-3). Указанное в заглавии соединение получают из М-2-транс в соответствии с протоколом, указанным на схеме А, с получением М-3 в виде масла. LRMS (ES) (M+H)+: найдено 189,2, вычислено 189,2. Реакционная схема N Этил 3-(2-метилтиазол-4-ил)акрилат (N-1). К перемешанному раствору гидрида натрия (1,04 г, 26,0 ммоль) в THF (47,2 мл) добавляют порциями триэтил-фосфоноацетат (5,19 мл, 26,0 ммоль) при комнатной температуре. Получающуюся в результате смесь перемешивают в течение 30 мин при комнатной температуре. К этой смеси добавляют раствор 2-метилтиазол-4-карбальдегида (3,0 г, 23,6 ммоль), растворенного в THF (30 мл) при энергичном перемешивании. Реакционную смесь перемешивают в течение 1 ч, и она разделяется на этилацетат и насыщенный раствор бикарбоната натрия. Органическую фазу промывают насыщенным солевым раствором,сушат над сульфатом натрия и концентрируют, что дает указанное в заглавии соединение в виде масла желтого цвета (4,3 г, 92%). LRMS (ES) (М+Н)+: найдено 198,1, вычислено 198,2. Этил 2-(2-метилтиазол-4-ил)циклопропанкарбоксилат (N-2-транс). Указанное в заглавии соединение получают из N-1 в соответствии с протоколом, указанным на схеме С, с получением N-2-транс. LRMS (ES) (М+Н)+: найдено 212,2, вычислено 212,2. 2-(2-Метилтиазол-4-ил)циклопропил)метанол (N-4). Указанное в заглавии соединение получают из N-2-транс в соответствии с протоколом, указанным на схеме А, с получением N-4 в виде твердого вещества. LRMS (ES) (M+H)+: найдено 170,1, вычислено 170,2.(Е)-Этил 3-(2-метилоксазол-4-ил)акрилат (O-2). Указанное в заглавии соединение получают из О-1 в соответствии с протоколом, указанным на схеме N, с получением O-2. LRMS (ES) (М+Н)+: найдено 182,1, вычислено 182,1. Этил 2-(2-метилоксазол-4-ил)циклопропанкарбоксилат (O-3-транс). Указанное в заглавии соединение получают из O-2 в соответствии с протоколом, указанным на схеме С, в итоге получают в форме транс-рацемата без хирального разделения O-3-транс в виде масла.LRMS (ES) (М+Н)+: найдено 196,2, вычислено 196,2. 2-(2-Метилоксазол-4-ил)циклопропил)метанол (O-4). Указанное в заглавии соединение получают из O-3-транс в соответствии с протоколом, указанным на схеме А, с получением O-4 в виде твердого вещества. LRMS (ES) (M+H)+: найдено 154,1, вычислено 154,1. Реакционная схема Р(Е)-Этил 3-(3-метоксипиридин-2-ил)акрилат (Р-2). Указанное в заглавии соединение получают из Р-1 в соответствии с протоколом, указанным на схеме N, с получением Р-2. LRMS (ES) (М+Н)+: найдено 208,1, вычислено 208,2. Этил 2-(3-метоксипиридин-2-ил)циклопропанкарбоксилат (Р-3-транс). Указанное в заглавии соединение получают из Р-2 в соответствии с протоколом, указанным на схеме С, в итоге получают в форме транс-рацемата без хирального разделения Р-3-транс в виде масла.LRMS (ES) (M+H)+: найдено 222,2, вычислено 222,2. 2-(3-Метоксипиридин-2-ил)циклопропил)метанол (Р-4). Указанное в заглавии соединение получают из Р-3-транс в соответствии с протоколом, указанным на схеме А, с получением Р-4 в виде твердого вещества. LRMS (ES) (М+Н)+: найдено 180,2, вычислено 180,2. Реакционная схема Q Этил 2-(1-метил-1 Н-пиразол-3-ил)циклопропанкарбоксилат (Q-2-транс). Указанное в заглавии соединение приготавливают из 1-метил-1 Н-пиразол-3-карбальдегида в соответствии с протоколом, указанным на схеме N, с получением соединения Q-1, которое используют непосредственно далее с применением протокола, указанного на схеме С, и в итоге получают в форме трансрацемата без хирального разделения Q-2-транс в виде масла. LRMS (ES) (М+Н)+: найдено 195,3, вычислено 195,2.- 26023685 2-(1-Метил-1 Н-пиразол-3-ил)циклопропил)метанол (Q-3). Указанное в заглавии соединение получают из Q-2-транс в соответствии с протоколом, указанным на схеме А, с получением Q-3 в виде твердого вещества. LRMS (ES) (M+H)+: найдено 153,2, вычислено 153,2. Реакционная схема R(Е)-этил 3-(тиазол-4-ил)акрилат (R-1). Указанное в заглавии соединение получают из тиазол-4-карбальдегида в соответствии с протоколом, указанным на схеме N, с получением R-2. LRMS (ES) (М+Н)+: найдено 184,1, вычислено 184,2. Этил 2-(тиазол-4-ил)циклопропанкарбоксилат (R-2-транс). Указанное в заглавии соединение приготавливают из R-1 в соответствии с протоколом, указанным на схеме С, в итоге получают в форме транс-рацемата без хирального разделения R-2-транс. LRMS (ES)(М+Н)+: найдено 198,1, вычислено 198,2. 2-(Тиазол-4-ил)циклопропил)метанол (R-3). Указанное в заглавии соединение получают из R-2-транс в соответствии с протоколом, указанным на схеме А, с получением R-3. LRMS (ES) (М+Н)+: найдено 156,1, вычислено 156,2. Реакционная схема S трет-Бутилдиметил(проп-2-инилокси)силан (S-1). К смеси проп-2-ин-1-ола (168 г, 3 моль), Et3N (412 г, 4,08 моль) в CH2Cl2 (3500 мл) добавляют раствор TBSCl (543 г, 3,45 моль) в CH2Cl2 (500 мл) при 0 С. Затем реакционную смесь нагревают вплоть до комнатной температуры и перемешивают в течение ночи. Смесь промывают водой (3000 мл), сушат надNa2SO4 и концентрируют, что дает сырой продукт, который очищают флэш-хроматографией (петролейный эфир) и дистилляцией, что дает соединение S-1 в виде жидкости желтого цвета (110 г, 43%).(Е)-трет-бутилдиметил(3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)аллилокси)силан (S-2). Смесь гидрида бис(циклопентадиенил)цирконийхлорида (16,2 г, 0,062 моль), пинаколборана (160,5 г, 1,25 моль) и TEA (8,7 мл, 0,062 моль) в THF (1200 мл) нагревают до 50 С в течение 10 мин и добавляют соединение S-1 (106 г, 0,62 моль). Затем смесь перемешивают при 50 С в течение ночи. Реакционную смесь охлаждают, гасят водой и концентрируют с удалением большей части THF. Остаток экстрагируют этилацетатом (2000 мл). Органический слой промывают насыщенным солевым раствором, сушат над безводным Na2SO4 и концентрируют в вакууме, что дает сырой продукт, который очищают флэшхроматографией (петролейный эфир) с получением соединения S-2 в виде жидкости желтого цвета (139 г, 74,7%). трет-Бутилдиметил 2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)циклопропил)метокси)силан(S-3). К смеси соединения S-2 (65 г, 0,218 моль) и Pd(OAc)2 (5 г, 0,0218 моль) в THF (200 мл) добавляют раствор CH3N2 (свежеприготовленный, 2,18 моль) в простом эфире (1200 мл) при -78 С. Затем реакционную смесь нагревают до комнатной температуры и перемешивают в течение ночи. Смесь фильтруют и фильтрат концентрируют, что дает сырой продукт, который очищают флэш-хроматографией (петролейный эфир) с получением соединения S-3 в виде масла желтого цвета (27,5 г, 40%). 2-трет-Бутилдиметилсилилокси)метил)циклопропилбороновая кислота (S-4).- 27023685 К смеси соединения S-3 (36 г, 0,115 моль) в ацетоне (360 мл) и воде (180 мл) добавляют NaIO4 (148 г, 0,69 моль) и NaOAc (53,2 г, 0,69 моль) при комнатной температуре. Затем реакционную смесь перемешивают при 25 С в течение ночи. Смесь фильтруют и фильтрат концентрируют с удалением ацетона,экстрагируют этилацетатом (600 мл). Органический слой промывают водой, насыщенным солевым раствором, сушат над Na2SO4 и концентрируют, что дает сырой продукт, который очищают хроматографией(петролейный эфир/этилацетат = 10:1-4:1 и затем MeOH/CH2Cl2 = 25:1), что дает S-4 в виде жидкости желтого цвета (19,3 г, 73%). 2-(2-трет-Бутилдиметилсилилокси)метил)циклопропил)-6,7-дигидро-5 Н-циклопента[b]пиридин(S-5). К перемешанному раствору соединения S-4 (3,0 г, 13,0 моль) в толуоле (50 мл) добавляют 2-хлор 6,7-дигидро-5 Н-циклопента[b]пиридин (2,0 г, 13,0 ммоль), ацетат палладия (0,29 г, 1,30 ммоль), ди(1 адамантил)-н-бутилфосфин (1,40 г, 3,91 ммоль), карбонат цезия (12,74 г, 39,10 ммоль) и воду (16,6 мл). Получающуюся в результате смесь нагревают до 100 С в течение ночи. Реакционная смесь разделяется на этилацетат и насыщенный раствор бикарбоната натрия. Органическую фазу концентрируют, и разделение на флэш-колонке с использованием градиента этилацетат/гексан 0-10% дает S-5 в виде масла (3,19 г, 65%). 1S,2S)-2-(6,7-дигидро-5 Н-циклопента[b]пиридин-2-ил)циклопропил)метанол (S-6). К перемешанному раствору соединения S-5 (3,19 г, 10,5 ммоль) в THF (40 мл) добавляют 1 М раствор тетрабутиламмонийфторида (10,5 мл, 10,5 ммоль). Получающуюся в результате смесь перемешивают 2 ч при комнатной температуре и концентрируют. Разделение на флэш-колонке с использованием градиента этилацетат/гексан 10-100% дает S-6 в виде масла (1,44 г, 72%). Пример 1 6-Хлор-2-метил-N-1-метил-1 Н-пиразол-4-ил)метил)пиримидин-4-амин (1-1). К перемешанному раствору 4,6-дихлор-2-метилпиримидина (100 мг, 0,61 ммоль) в диоксане (1 мл) добавляют триэтиламин (0,3 мл, 2,15 ммоль) и (1-метил-1 Н-пиразол-4-ил)метанамин (68 мг, 0,61 ммоль). Получающуюся в результате смесь подвергают воздействию микроволнового излучения при 150 С в течение 30 мин. Реакционную смесь разбавляют этилацетатом и промывают насыщенным раствором бикарбоната натрия. Органическую фазу концентрируют, и разделение на флэш-колонке с использованием градиента этилацетат/гексан 10-100% дает соединение 1-1 в виде твердого вещества белого цвета (121 мг, 83%). MS (масс-спектрометрия) (М+Н)+: найдено 238,0857, вычислено 238,0854. 2-Метил-N-[(1-метил-1 Н-пиразол-4-ил)метил]-6-[(2-пиридин-2-илциклопропил)метокси]пиримидин-4-амин (1-2). К перемешанному раствору А-4 (188 мг, 1,26 ммоль) в THF (2,5 мл) добавляют 60% дисперсию гидрида натрия (74 мг, 1,85 ммоль) и получающийся в результате раствор перемешивают при комнатной температуре в течение 20 мин. К этому добавляют соединение 1-1 (200 мг, 0,84 ммоль) и получающуюся в результате смесь подвергают воздействию микроволнового излучения при 100 С в течение 90 мин. Реакционную смесь концентрируют и очищают с использованием обращенно-фазовой хроматографии (1030%, 0,1% TFA в смеси H2O/ацетонитрил), что дает соединение 1-2 в виде твердого вещества белого цвета (231 мг, 78%). MS (M+H)+: найдено 351,1927, вычислено 351,1928. Пример 2- 28023685 4-Хлор-2-метил-6-1S,2S)-2-(5-метилпиридин-2-ил)циклопропил)метокси)пиримидин (2-1). К суспензии гидрида натрия (103 мг, 2,57 ммоль) в THF (6,0 мл) добавляют соединение (S,S) Е-3(350 мг, 2,14 ммоль). Получающуюся в результате смесь перемешивают в течение 30 мин перед добавлением 4,6-дихлор-2-метилпиридина (419 мг, 2,57 ммоль). После нагревания при 80 С в течение 1 ч реакционную смесь разбавляют этилацетатом и промывают водой и насыщенным солевым раствором. Органическую фазу концентрируют, и хроматография на флэш-колонке с использованием градиента этилацетат/гексан 0-40% дает соединение 2-1 в виде бесцветного масла (453 мг, 73%). MS (M+H)+: найдено 290,35, вычислено 290,10. трет-Бутил 5-метил-1,3,4-тиадиазол-2-ил)метил)(2-метил-6-1S,2S)-2-(5-метилпиридин-2-ил) циклопропил)метокси)пиримидин-4-ил)карбамат (2-2). Раствор соединения 2-1 (100 мг, 0,35 ммоль), трет-бутил 5-метил-1,3,4-тиадиазол-2-ил)метил) карбамата (119 мг, 0,52 ммоль; для приготовления, см. D.C. Pryde et al. J. Med. Chem. 2006, 49, 4409-4424),1M трет-бутоксида калия (1,03 мл в THF) и 2-ди-трет-бутилфосфино-2',4',6'-триизопропилбифенила (14,6 мг, 0,035 ммоль) в 2-метил-2-бутаноле (1,7 мл) продувают посредством N2 в течение 5 мин. Добавляют трис(дибензилиденацетон)дипалладий(0) (31,6 мг, 0,035 ммоль) и смесь нагревают при 60 С в течение 1 ч. Реакционную смесь охлаждают до комнатной температуры и разбавляют этилацетатом и насыщенным раствором NaHCO3. Органическую фазу промывают водой, насыщенным солевым раствором и концентрируют. Остаток очищают хроматографией на флэш-колонке с использованием градиента этилацетат/гексан 20-60%, что дает соединение 2-2 в виде бесцветного масла (117 мг, 70%). MS (M+H)+: найдено 483,10, вычислено 483,21. 2-Метил-6-[(1S,2S)-2-(5-метилпиридин-2-ил)циклопропил]метокси-N-[(5-метил-1,3,4-тиадиазол 2-ил)метил]пиримидин-4-амин (2-3"). К раствору соединения 2-2 (51,0 мг, 0,11 ммоль) в МеОН (0,53 мл) добавляют K2CO3 (17,5 мг, 0,13 ммоль). Полученную суспензию перемешивают при 70 С в течение 2 ч. Смесь разбавляют посредствомEtOAc, затем экстрагируют 1 н. раствором HCl. Водный слой подщелачивают 5 н. раствором NaOH и экстрагируют посредством DCM три раза. Объединенные DCM-слои сушат над Na2SO4 и концентрируют,что дает соединение 2-3" в виде твердого вещества грязно-белого цвета (29 мг, 72%). MS (массспектрометрия) (М+Н)+: найдено 383,1654, вычислено 383,1649. 1(д, J=7,7 Гц, 1 Н), 5,64 (с, 1 Н), 4,76 (д, J=5,0 Гц, 2 Н), 4,23 (м, 1 Н), 4,14 (м, 1 Н), 2,65 (с, 3 Н), 2,31 (с, 3 Н),2,22 (с, 3 Н), 2,09 (м, 1 Н), 1,71 (м, 1 Н), 1,12 (м, 1 Н), 0,98 (м, 1 Н). Таблица 1 Следующие соединения получают способом, аналогичным способу примеров 1 и 2, с использованием соответственно замещенных 4,6-дихлорпиримидина, амина и спиртов, описанным выше на схемах AR. Исходные вещества, не проиллюстрированные выше, являются доступными для приобретения, описаны в литературе или могут быть легко синтезированы специалистом в области органического синтеза без лишнего экспериментирования.
МПК / Метки
МПК: C07D 239/47
Метки: пиримидина, производные, pde10, фосфодиэстеразы, ингибиторов, качестве
Код ссылки
<a href="https://eas.patents.su/30-23685-proizvodnye-pirimidina-v-kachestve-ingibitorov-fosfodiesterazy-pde10.html" rel="bookmark" title="База патентов Евразийского Союза">Производные пиримидина в качестве ингибиторов фосфодиэстеразы pde10</a>


































