Модуляторы глюкагонового рецептора
Номер патента: 23517
Опубликовано: 30.06.2016
Авторы: Ли Эстер Чэн Йинь, Эспнес Гэри Эрик, Пфефферкорн Джеффри Аллен, Дайдьюк Мэри Тереса, Филипски Кевин Джеймс, Гусман-Перес Энджел, Ту Мейхуа Майк, Стивенс Бенджамин Доусон
Формула / Реферат
1. Соединение формулы I
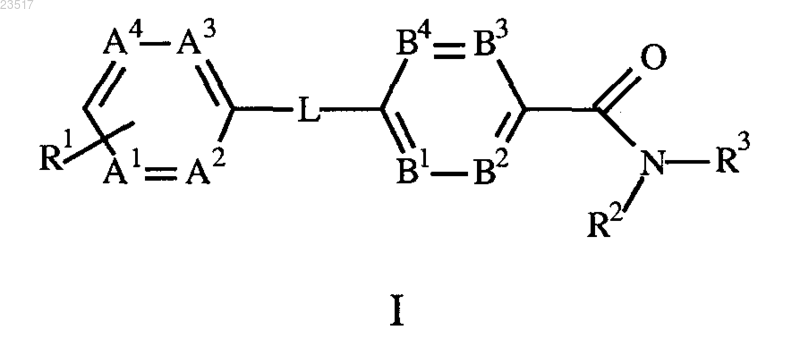
или его фармацевтически приемлемая соль,
где R1 представляет собой 5-членную гетероарильную группу, содержащую от 1 до 4 гетероатомов, выбранных из N и О, присоединенную по атому углерода или азота и возможно конденсированную с (С4-С7)циклоалкилом или фенилом; где возможно конденсированный 5-членный гетероарил возможно замещен заместителями в количестве от одного до четырех, каждый из которых независимо выбран из галогена, группы -S-(С1-С3)алкил, гидрокси, (С3-С5)циклоалкила, циано, фенила, пиридинила, (С1-С6)алкила, возможно замещенного фтором в количестве от одного до трех, или (С1-С6)алкокси, возможно замещенного фтором в количестве от одного до трех;
R2 представляет собой H или метил;
R3 представляет собой -(СН2)2СО2Н;
каждый из А1, А2, А3 и А4 независимо представляет собой CR4 или N при условии, что не более двух из А1, А2, А3 и А4 представляют собой N;
R4 в каждом случае независимо представляет собой Н, галоген, (С1-С3)алкил или (С1-С3)алкокси;
L представляет собой -X-CH(R5)- или -CH(R5)-X-;
X представляет собой СН2, О или NH;
R5 представляет собой (С1-С6)алкил, возможно замещенный фтором в количестве от одного до трех; (С3-С7)циклоалкил, возможно замещенный (С1-С3)алкилом в количестве от одного до двух, который возможно замещен фтором в количестве от одного до трех, где один атом углерода в (С3-С7)циклоалкиле может быть заменен на NH, О или S; или (С3-С7)циклоалкил-(С1-С6)алкил, где (С3-С7)циклоалкильная группа указанного (С3-С7)циклоалкил-(С1-С6)алкила возможно замещена (С1-С3)алкилом в количестве от одного до двух, который возможно замещен фтором в количестве от одного до трех;
каждый из В1, В2, В3 и В4 независимо представляет собой CR6 или N при условии, что не более двух из В1, В2, В3 и В4 представляют собой N;
R6 в каждом случае независимо представляет собой Н, галоген, (С1-С3)алкил или (С1-С3)алкокси.
2. Соединение по п.1 или его фармацевтически приемлемая соль, где R1 представляет собой 5-членный гетероарил, содержащий от 1 до 4 гетероатомов, выбранных из N и О, присоединенный через атом азота к атому углерода между А1 и А4 кольца, содержащего А1, А2, А3 и А4; R2 представляет собой водород и R3 представляет собой -(CH2)2CO2H.
3. Соединение по п.1 или 2 или его фармацевтически приемлемая соль, где X представляет собой О.
4. Соединение по п.1 или 2 или его фармацевтически приемлемая соль, где X представляет собой NH.
5. Соединение по п.1 или 2 или его фармацевтически приемлемая соль, где X представляет собой СН2.
6. Соединение по п.3 или 4 или его фармацевтически приемлемая соль, где L представляет собой -X-CH(R5)-; каждый из А1, А2, А3 и А4 независимо представляет собой CR4; или А4 представляет собой N и каждый из А1, А2 и А3 представляет собой CR4; или каждый из А1 и А4 представляет собой N и каждый из А2 и А3 представляет собой CR4; или каждый из А2 и А4 представляет собой N и каждый из А1 и А3 представляет собой CR4; R4 в каждом случае независимо представляет собой H или метил; каждый из В1, В2, В3 и В4 представляет собой CR6; или В1 представляет собой N и каждый из В2, В3 и В4 представляет собой CR6; или каждый из В2 и В3 представляет собой N и каждый из В1 и В4 представляет собой CR6; или каждый из В1 и В4 представляет собой N и каждый из В2 и В3 представляет собой CR6; R6 в каждом случае представляет собой Н.
7. Соединение по п.3 или его фармацевтически приемлемая соль, где L представляет собой -X-CH(R5)-; каждый из А1, А2, А3 и А4 представляет собой CR4; или А4 представляет собой N и каждый из А1, А2 и А3 представляет собой CR4; или каждый из А1 и А4 представляет собой N и каждый из А2 и А3 представляет собой CR4; или каждый из А2 и А4 представляет собой N и каждый из А1 и А3 представляет собой CR4; R4 в каждом случае независимо представляет собой H или метил; каждый из В1, В2, В3 и В4 представляет собой CR6; R6 в каждом случае независимо представляет собой H или метил.
8. Соединение по п.4 или его фармацевтически приемлемая соль, где R2 представляет собой водород; R3 представляет собой -(CH2)2CO2H; L представляет собой -CH(R5)-X-; A4 представляет собой N и каждый из А1, А2 и А3 представляет собой CR4; или каждый из А1 и А4 представляет собой N и каждый из А2 и А3 представляет собой CR4; или каждый из А2 и А4 представляет собой N и каждый из А1 и А3 представляет собой CR4; R4 в каждом случае независимо представляет собой H или метил; каждый из В1, В2, В3 и В4 представляет собой CR6; R6 в каждом случае независимо представляет собой H или метил.
9. Соединение по п.4 или его фармацевтически приемлемая соль, где R2 представляет собой водород; R3 представляет собой -(CH2)2CO2H; L представляет собой -CH(R5)-X-; каждый из А1, А2, А3 и А4 независимо представляет собой CR4; R4 в каждом случае независимо представляет собой H или метил; один из В1, В2, В3 и В4 представляет собой N, а остальные представляют собой CR6; R6 в каждом случае независимо представляет собой H или метил.
10. Соединение по пп.6-8 или 9 или его фармацевтически приемлемая соль, где R5 представляет собой этил, пропил, изопропил, изобутил, неопентил, циклопропил, циклобутил, диметилциклобутил, циклопентил или циклопропилметил.
11. Соединение по п.10 или его фармацевтически приемлемая соль, где R1 представляет собой имидазолил, пиразолил, триазолил или индазолил, возможно замещенные заместителями в количестве от одного до двух, каждый из которых независимо выбран из метила, трифторметила, этила, пропила, изопропила, бутила, трет-бутила, метокси, этокси, циано, хлора или фтора.
12. Соединение по п.1 или его фармацевтически приемлемая соль, где R1 представляет собой имидазолил, пиразолил, триазолил или индазолил, возможно замещенные заместителями в количестве от одного до двух, каждый из которых независимо выбран из метила, трифторметила, этила, пропила, изопропила, бутила, трет-бутила, метокси, этокси, циано, хлора или фтора; L представляет собой -X-CHR5-; X представляет собой О; R5 представляет собой этил, пропил, изопропил, изобутил, неопентил, циклопропил, циклобутил, диметилциклобутил, циклопентил или циклопропилметил.
13. Соединение по п.1 или его фармацевтически приемлемая соль, где R1 представляет собой имидазолил, пиразолил, триазолил или индазолил, возможно замещенные заместителями в количестве от одного до двух, каждый из которых независимо выбран из метила, трифторметила, этила, пропила, изопропила, бутила, трет-бутила, метокси, этокси, циано, хлора или фтора; L представляет собой -CHR5-X-; Х представляет собой NH и R5 представляет собой этил, пропил, изопропил, изобутил, неопентил, циклопропил, циклобутил, диметилциклобутил, циклопентил или циклопропилметил.
14. Соединение по п.12 или 13 или его фармацевтически приемлемая соль, где R1 представляет собой 4-трифторметилпиразол-1-ил или 4-трифторметилимидазол-1-ил.
15. Соединение по п.1, выбранное из группы, состоящей из
(+/-)-3-(4-(1-(3-метил-4-(4-(трифторметил)-1H-имидазол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(3-метил-1-(4-(4-(трифторметил)-1H-имидазол-1-ил)фенил)бутокси)бензамидо)пропионовой кислоты;
(+/-)-3-(6-(1-(4-(4-(трифторметил)-1Н-пиразол-1-ил)фенокси)бутил)никотинамидо)пропионовой кислоты;
(+/-)-3-(4-(4-метил-1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фенил)пентан-2-ил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(R)-3-(4-(1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(S)-3-(4-(1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(циклопентил(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(R)-3-(4-(1-(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(S)-3-(4-(1-(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(3,5-димегил-4-(4-(трифторметил)-1H-пиразол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(R)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(S)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-(трифторметил)-1Н-имидазол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(R)-3-(4-(1-(4-(4-(трифторметил)-1Н-имидазол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(S)-3-(4-(1-(4-(4-(трифторметил)-1H-имидазол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-(трифторметил)-1H-имидазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-(метилтио)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3-трет-бутил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-хлор-3-метил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-хлор-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-этил-3-метил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3,5-диэтил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-метил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3-изопропил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-фтор-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3-метил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(2Н-1,2,3-триазол-2-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3-бутил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(5-этокси-3-метил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(5-метокси-3-метил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-бутил-1Н-имидазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(2-циано-3,4,5-триметил-1Н-пиррол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3-циано-2,4-диметил-1Н-пиррол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(2-циано-3-метил-1Н-пиррол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(6-(1-(4-(3-пропил-1H-пиразол-1-ил)фенокси)бутил)никотинамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3,4-диметил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(1H-имидазо[1,2-b]пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3-этил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-хлор-5-метил-1H-имидазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4,5-диэтил-1H-имидазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3,5-диметил-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3-метил-1H-1,2,4-триазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(1H-1,2,4-триазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(2-бутил-1H-имидазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4,5-диметил-1H-имидазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(1-пропил-1H-пиразол-4-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(1H-пиразол-3-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3,5-диметилизоксазол-4-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(1-метил-3-(трифторметил)-1H-пиразол-5-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(1-метил-1H-пиразол-4-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(1,5-диметил-1H-пиразол-4-ил)фенокси)бутил)бензамидо)пропионовой кислоты
(+/-)-3-(4-(1-(4-(1H-пиразол-4-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(1-метил-1H-пиразол-5-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(1,3,5-триметил-1H-пиразол-4-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(R)-3-(4-(1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(S)-3-(4-(1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(6-(4-фенил-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-фтор-1H-пиразол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(6-(3-метил-1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фенил)бутиламино)никотинамидо)пропионовой кислоты;
(+/-)-3-(4-(2-циклопропил-1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)этил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(циклопентил(4-(4-(трифторметил)-1Н-пиразол-1-ил)фенокси)метил)бензамидо)пропионовой кислоты;
(R)-3-(4-(циклопентил(4-(4-(трифторметил)-1Н-пиразол-1-ил)фенокси)метил)бензамидо)пропионовой кислоты;
(S)-3-(4-(циклопентил(4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(циклобутил(4-(4-(трифторметил)-1Н-пиразол-1-ил)фенокси)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(3,3-диметил-1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-метил-3-(трифторметил)-1Н-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3-(трифторметил)-1H-1,2,4-триазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(3-метил-4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(2-метил-4-(трифторметил)-1H-имидазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(циклопропил(4-(4-(трифторметил)-1Н-пиразол-1-ил)фенокси)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(2-метил-1-(4-(4-(трифторметил)-1Н-пиразол-1-ил)фенокси)пропил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)пропил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(3-метил-1-(4-(4-(трифторметил)-1H-имидазол-1-ил)фенил)бутокси)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(3-метил-1-(4-(4-(трифторметил)-1Н-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1Н-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(S)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(R)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(5-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-2-илокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-илокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-илокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-циано-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4,5,6,7-тетрагидро-2H-индазол-2-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(5,6-дигидроциклопента[с]пиразол-2(4H)-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(2Н-индазол-2-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-метил-1H-1,2,3-триазол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(2-(3-метил-1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фенил)бутиламино)пиримидин-5-карбоксамидо)пропионовой кислоты;
(+/-)-3-(4-(циклопентил(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(R)-3-(4-(циклопентил(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(S)-3-(4-(циклопентил(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(R)-3-(4-(циклопентил(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(S)-3-(4-(циклопентил(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(2-(циклогексил(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-ил)метиламино)никотинамидо)пропионовой кислоты;
(+/-)-3-(4-(3,3-диметил-1-(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(циклогексил(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(6-(3-метил-1-(5-метил-6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)бутил)никотинамидо)пропионовой кислоты;
(R)-3-(4-(1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты;
(S)-3-(4-(1-(4-(4-(трифторметил)-1H-пиразол-1-ил)фениламино)бутил)бензамидо)пропионовой кислоты,
или его фармацевтически приемлемая соль.
16. Соединение по п.1, выбранное из группы, состоящей из
(+/-)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(S)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(R)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(циклопентил(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(R)-3-(4-(циклопентил(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(S)-3-(4-(циклопентил(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты,
или его фармацевтически приемлемая соль.
17. Соединение, выбранное из группы, состоящей из
(+/-)-3-(4-(3-метил-1-(5-метил-6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(циклобутил(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(2-циклопропил-1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)этил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(3-метил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+)-3-(3-фтор-4-(1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(-)-3-(3-фтор-4-(1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+)-3-(3-метил-4-(1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(-)-3-(3-метил-4-(1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+)-3-(4-(1-(2-(4-(трифторметил)-1H-пиразол-1-ил)пиримидин-5-иламино)бутил)бензамидо)пропионовой кислоты;
(+)-3-(4-((3,3-диметилциклобутил)(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(-)-3-(4-((3,3-диметилциклобутил)(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
3-(4-(1-(4-(2H-индазол-2-ил)-3-метилфенокси)бутил)бензамидо)пропионовой кислоты;
(+)-3-(6-(циклогексил(2-метил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенил)метиламино)никотинамидо)пропионовой кислоты;
(-)-3-(6-(циклогексил(2-метил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенил)метиламино)никотинамидо)пропионовой кислоты;
(+/-)-3-(4-((4-(2H-индазол-2-ил)фенокси)(циклопентил)метил)бензамидо)пропионовой кислоты;
(+)-3-(4-((6-(4-хлор-1H-имидазол-1-ил)пиридин-3-иламино)(циклопентил)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(2,2,2-трифтор-1-(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)этил)бензамидо)пропионовой кислоты;
3-(4-((6-(4-трет-бутил-1Н-имидазол-1-ил)пиридин-3-иламино)(циклопентил)метил)бензамидо)пропионовой кислоты;
3-(4-(циклопентил(6-(4-изопропил-1Н-имидазол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(+)-3-(4-(1-(4-(2-индазол-2-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
3-(4-(1-(4-(7-метил-2H-индазол-2-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
3-(4-(1-(4-(6-метил-2H-индазол-2-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
3-(4-(1-(4-(4-метил-2H-индазол-2-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
3-(4-(1-(4-(5-метил-2H-индазол-2-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
3-(4-(1-(6-(4-фенил-1H-имидазол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-хлор-1Н-пиразол-1-ил)-3,5-диметилфенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(циклопентил(3,5-диметил-4-(4-(трифторметил)-1H-имидазол-1-ил)фенокси)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(6-(1-(6-(4-фенил-1H-пиразол-1-ил)пиридин-3-иламино)бутил)никотинамидо)пропионовой кислоты;
(+/-)-3-(6-(1-(6-(4-фенил-1H-пиразол-1-ил)пиридин-3-илокси)бутил)бензамидо)пропионовой кислоты;
(+)-3-(4-((3,3-диметилциклобутил)(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(-)-3-(4-((3,3-диметилциклобутил)(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(+)-3-(4-(1-(6-(4-трет-бутил-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(-)-3-(4-(1-(6-(4-трет-бутил-1Н-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+)-3-(4-(циклобутил(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)метил)бензамидо)пропионовой кислоты;
(-)-3-(4-(циклобутил(3,5-димегил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(7-хлор-2Н-индазол-2-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(5-хлор-2H-индазол-2-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1H-имидазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+)-3-(6-(3-метил-1-(6-(4-(трифторметил)-1Н-пиразол-1-ил)пиридин-3-ил)бутиламино)никотинамидо)пропионовой кислоты;
(-)-3-(6-(3-метил-1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-ил)бутиламино)никотинамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(4-циклопропил-1H-пиразол-1-ил)-3,5-диметилфенокси)бутил)бензамидо)пропионовой кислоты;
3-(4-(1-(4-(4-хлор-1H-пиразол-1-ил)-3,5-диметилфенокси)бутил)бензамидо)пропионовой кислоты;
(+)-3-(4-(циклогексил(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(-)-3-(4-(циклогексил(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1Н-1,2,3-триазол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(2-(4-(трифторметил)-1H-пиразол-1-ил)пиримидин-5-илокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(5-метил-6-(4-(трифторметил)-1Н-пиразол-1-ил)пиридин-3-илокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(циклобутил(3,5-диметил-4-(4-(трифторметил)-1Н-пиразол-1-ил)фенокси)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-((3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)(3,3-диметилциклобутил)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(3-метокси-5-метил-4-(4-(трифторметил)-1Н-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-((3,3-дифторциклобутил)(6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовой кислоты;
(+)-3-(4-((3,3-диметилциклобутил)(2-(4-(трифторметил)-1Н-пиразол-1-ил)пиримидин-5-илокси)метил)бензамидо)пропионовой кислоты;
(-)-3-(4-((3,3-диметилциклобутил)(2-(4-(трифторметил)-1H-пиразол-1-ил)пиримидин-5-илокси)метил)бензамидо)пропионовой кислоты;
(+)-3-(4-((3,3-диметилциклобутил)(2-(4-(трифторметил)-1Н-пиразол-1-ил)пиримидин-5-иламино)метил)бензамидо)пропионовой кислоты;
(-)-3-(4-((3,3-диметилциклобутил)(2-(4-(трифторметил)-1Н-пиразол-1-ил)пиримидин-5-иламино)метил)бензамидо)пропионовой кислоты;
3-(4-(1-(2-метил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовой кислоты;
(+)-3-(4-(1-(6-(4-фенил-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(-)-3-(4-(1-(6-(4-фенил-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(6-(4-фенил-1H-имидазол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-((6-(4-хлор-3-метил-1H-пиразол-1-ил)пиридин-3-иламино)(циклопентил)метил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(6-(4-(пиридин-2-ил)-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(N-метил-4-(1-(6-(4-фенил-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(+)-3-(4-(1-(6-(4-этил-3-метил-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(-)-3-(4-(1-(6-(4-этил-3-метил-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовой кислоты;
(R)-3-(6-((1-(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенил)-3-метилбутил)амино)никотинамидо)пропионовой кислоты;
(S)-3-(6-((1-(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенил)-3-метилбутил)амино)никотинамидо)пропионовой кислоты;
(+)-(3-(6-((циклопентил(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенил)метил)амино)никотинамидо)пропионовой кислоты;
(-)-3-(6-((циклопентил(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенил)метил)амино)никотинамидо)пропионовой кислоты;
(+)-N-{4-[4,4,4-трифтор-1-({6-[4-(трифторметил)-1Н-пиразол-1-ил]пиридин-3-ил}амино)бутил]бензоил}-бета-аланина;
(-)-N-{4-[4,4,4-трифтор-1-({6-[4-(трифторметил)-1H-пиразол-1-ил]пиридин-3-ил}амино)бутил]бензоил}-бета-аланина;
(+)-N-{4-[{[6-(4-циклопропил-1Н-пиразол-1-ил)пиридин-3-ил]амино}(3,3-диметилциклобутил)метил]бензоил}-бета-аланина;
(-)-N-{4-[{[6-(4-циклопропил-1Н-пиразол-1-ил)пиридин-3-ил]амино}(3,3-диметилциклобутил)метил]бензоил}-бета-аланина;
(+/-)-N-[4-(1-{[6-(4-циклопропил-1Н-пиразол-1-ил)пиридин-3-ил]амино}бутил)бензоил]-бета-аланина;
(±)-3-(4-((тетрагидро-2Н-пиран-4-ил)((6-(4-(трифторметил)-1Н-пиразол-1-ил)пиридин-3-ил)амино)метил)бензамидо)пропионовой кислоты;
(±)-3-(4-(2,2-диметил-1-((6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-ил)амино)пропил)бензамидо)пропионовой кислоты;
(+)-3-(4-(2,2-диметил-1-((6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-ил)амино)пропил)бензамидо)пропионовой кислоты;
(-)-3-(4-(2,2-диметил-1-((6-(4-(трифторметил)-1Н-пиразол-1-ил)пиридин-3-ил)амино)пропил)бензамидо)пропионовой кислоты;
(±)-3-(4-(2,2-диметил-1-((6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-ил)амино)пропил)бензамидо)пропионовой кислоты;
(+)-3-(4-(2,2-диметил-1-((6-(4-(трифторметил)-1Н-имидазол-1-ил)пиридин-3-ил)амино)пропил)бензамидо)пропионовой кислоты;
(-)-3-(4-(2,2-диметил-1-((6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-ил)амино)пропил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-{1-[3,5-дифтор-4-(4-трифторметилпиразол-1-ил)фенокси]бутил}бензоиламино)пропионовой кислоты;
(+/-)-3-(4-{1-[4-(5-фториндазол-2-ил)фенокси]бутил}бензоиламино)пропионовой кислоты;
(+/-)-3-(4-{1-[4-(6-фториндазол-2-ил)фенокси]бутил}бензоиламино)пропионовой кислоты;
(S)-3-(4-(1-(4-(2Н-индазол-2-ил)-3,5-диметилфенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-((3,3-диметилциклобутил)(6-(4-(трифторметил)-1Н-имидазол-1-ил)пиридин-3-иламино)ме-тил)бензамидо)пропионовой кислоты;
(+/-)-3-(4-(1-(4-(2Н-индазол-2-ил)-3,5-диметилфенокси)бутил)бензамидо)пропионовой кислоты;
(+/-)-3-(6-(1-(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-ил)бутиламино)никотинамидо)пропионовой кислоты;
(+)-3-(4-((6-(4-хлор-3-метил-1H-пиразол-1-ил)пиридин-3-иламино)(циклопентил)метил)бензамидо)про-пионовой кислоты;
(-)-3-(4-((6-(4-хлор-3-метил-1H-пиразол-1-ил)пиридин-3-иламино)(циклопентил)метил)бензамидо)пропионовой кислоты;
3-(4-(циклопентил(2-(4-(трифторметил)-1H-имидазол-1-ил)пиримидин-5-иламино)метил)бензамидо)пропионовой кислоты,
или его фармацевтически приемлемая соль.
18. Фармацевтическая композиция, действующая в качестве глюкагонового антагониста, содержащая (1) терапевтически эффективное количество соединения по любому из пп.1-17 или его фармацевтически приемлемой соли и (2) фармацевтически приемлемый эксципиент, разбавитель или носитель.
19. Способ лечения или замедления развития или возникновения сахарного диабета II типа и связанных с диабетом расстройств у животных, включающий стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-18.
20. Способ лечения или замедления развития или возникновения сахарного диабета II типа и связанных с диабетом расстройств у животных, включающий стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции по п.18.
21. Соединение по п.1, представляющее собой (S)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1H-пиразол-1-ил)фенокси)бутил)бензамидо)пропионовую кислоту, или его фармацевтически приемлемая соль.
22. Соединение по п.1, представляющее собой 3-(4-(циклопентил(6-(4-(трифторметил)-1H-пиразол-1-ил)пиридин-3-иламино)метил)бензамидо)пропионовую кислоту, изомер 1, или его фармацевтически приемлемая соль.
23. Соединение по п.1, представляющее собой 3-(4-(1-(6-(4-трет-бутил-1H-пиразол-1-ил)пиридин-3-иламино)бутил)бензамидо)пропионовую кислоту, изомер 2, или его фармацевтически приемлемая соль.
24. Соединение по п.1, представляющее собой 3-(4-((3,3-диметилциклобутил)(2-(4-(трифторметил)-1Н-пиразол-1-ил)пиримидин-5-илокси)метил)бензамидо)пропионовую кислоту, изомер 1, или его фармацевтически приемлемая соль.
Текст
В изобретении предложено соединение формулы I или его фармацевтически приемлемая соль, гдеR1, R2, R3, A1, A2, A3, A4, L, В 1, В 2, В 3 и В 4 являются такими, как здесь определено. Обнаружено, что соединения формулы I действуют в качестве глюкагоновых антагонистов или обратных агонистов. Следовательно, соединения формулы I и их фармацевтические композиции полезны для лечения заболеваний, расстройств или состояний, опосредованных глюкагоном. Эспнес Гэри Эрик, Дайдьюк Мэри Тереса, Филипски Кевин Джеймс,Гусман-Перес Энджел, Ли Эстер Чэн Йинь, Пфефферкорн Джеффри Аллен, Стивенс Бенджамин Доусон,Ту Мейхуа Майк (US) Поликарпов А.В. (RU) Область изобретения Настоящее изобретение относится к соединениям, представляющим собой антагонисты, смешанные агонисты/антагонисты, частичные агонисты, отрицательные аллостерические модуляторы или обратные агонисты глюкагонового рецептора, фармацевтическим композициям, содержащим указанные соединения, и применениям соединений или композиций. Предшествующий уровень техники Сахарный диабет представляет собой серьезную проблему здравоохранения из-за его увеличивающейся распространенности и связанного с ним риска для здоровья. Это заболевание характеризуется нарушениями метаболизма при образовании и потреблении углеводов, что приводит в результате к нарушению поддержания требуемых уровней глюкозы крови. Различают две основные формы сахарного диабета. Сахарный диабет I типа или инсулинозависимый сахарный диабет (IDDMT1DM) является результатом абсолютного дефицита инсулина. Сахарный диабет II типа или инсулинонезависимый сахарный диабет (NIDDMT2DM) часто возникает при нормальных или даже повышенных уровнях инсулина и, повидимому, представляет собой результат неспособности тканей и клеток соответствующим образом отвечать на инсулин. Активный контроль над NIDDMT2DM посредством медикаментозного лечения является важным; иначе он может прогрессировать до недостаточности -клеток и зависимости от инсулина. Глюкагон представляет собой пептид, состоящий из двадцати девяти аминокислот, который секретируется -клетками поджелудочной железы в печеночную портальную вену, таким образом приводя к тому, что печень подвергается воздействию более высоких уровней этого гормона по сравнению с тканями, отличными от печеночных. Уровни глюкагона в плазме крови уменьшаются в ответ на гипергликемию, гиперинсулинемию, повышенные уровни неэтерифицированнных жирных кислот и соматостатина в плазме крови, тогда как секреция глюкагона увеличивается в ответ на гипогликемию и повышенные уровни аминокислот в плазме крови. Глюкагон посредством активации своего рецептора представляет собой сильный активатор продукции глюкозы печенью, активируя гликогенолиз и глюконеогенез. Глюкагоновый рецептор представляет собой белок массой 62 кДа, который активируется глюкагоном и представляет собой класс В семейства рецепторов, связанных с G-белком. Другие близкородственные связанные с G-белком рецепторы включают рецептор глюкагоноподобного пептида 1 (GLP-1),рецептор глюкагоноподобного пептида 2 (GLP-2) и рецептор гастроингибиторного полипептида. Глюкагоновый рецептор у людей кодируется геном GCGR, и эти рецепторы главным образом экспрессируются в печени, тогда как меньшие количества обнаруживаются в почках, сердце, жировой ткани, селезенке,тимусе, надпочечниках, поджелудочной железе, коре головного мозга и желудочно-кишечном тракте. Стимуляция глюкагонового рецептора приводит в результате к активации аденилатциклазы и увеличенным уровням внутриклеточного сАМР. Сообщается о том, что необычная миссенс-мутация в гене GCGR коррелирует с сахарным диабетомII типа, и сообщается о том, что инактивирующая глюкагоновый рецептор мутация у людей вызывает резистентность к глюкагону и ассоциируется с гиперплазией -клеток поджелудочной железы, незидиобластозом, гиперглюкагонемией и нейроэндокринными опухолями поджелудочной железы. В исследованиях на грызунах с использованием нокаутированных по GCGR мышей и мышей, обработанных антисмысловыми GCGR олигонуклеотидами, мыши продемонстрировали улучшение уровня глюкозы натощак, толерантности к глюкозе и функции -клеток поджелудочной железы. Как у здоровых контрольных животных, так и в животных моделях сахарного диабета I и II типов удаление глюкагона из системы кровообращения с использованием селективных и специфических антител привело в результате к сокращению гликемического уровня. Конкретнее, показано, что обработка обеих мышей и яванского макака антителами, оказывающими антагонистические действия против GCGR (mAb В и mAb Ac), улучшает гликемический контроль, не вызывая гипогликемию. Недавние исследования на мышах дополнительно продемонстрировали, что антагонизм глюкагонового рецептора приводит в результате к улучшенному глюкозному гомеостазу посредством механизма, который требует функционального рецептора GLP-1. Антагонизм глюкагонового рецептора приводил в результате к компенсационной сверхпродукции GLP-1, вероятно -клетками поджелудочной железы, и последнее может играть важную роль во внутриостровковой регуляции и поддержании функции -клеток. Многообещающая область исследования сахарного диабета включает использование низкомолекулярных антагонистов, смешанных агонистов/антагонистов, частичных агонистов, отрицательных аллостерических модуляторов или обратных агонистов глюкагонового рецептора, чтобы понизить уровень глюкагона в системе кровообращения и, таким образом, понизить гликемический уровень. Терапевтически, ожидается, что инактивация глюкагонового рецептора может представлять собой эффективную стратегию для понижения уровня глюкозы крови путем сокращения объемов продукции глюкозы в печени и нормализации стимулированной глюкозой секреции инсулина. Следовательно, глюкагоновый антагонист, смешанный агонист/антагонист, частичный агонист, отрицательный аллостерический модулятор или обратный агонист могут обеспечивать терапевтическое лечение NTDDMT2DM и ассоциированных осложнений, среди прочего, гипергликемии, дислипидемии, синдрома инсулинорезистентности, гиперинсулинемии, гипертензии и ожирения.-1 023517 Несколько лекарственных средств в пяти основных категориях, каждое из которых действует в соответствии с различными механизмами, доступны для лечения гипергликемии и, как следствие,NIDDMT2DM (Moller, D.E., "New drug targets for Type 2 diabetes and the metabolic syndrome" Nature 414; 821-827, (2001. (А) Агенты, усиливающие секрецию инсулина, включая сульфонилмочевину (например,глипизид, глимепирид, глибурид) и меглитиниды (например, натеглидин и репаглинид), улучшают секрецию инсулина, действуя на -клетки поджелудочной железы. В то время как эта терапия может уменьшать уровень глюкозы крови, она обладает ограниченной эффективностью и переносимостью, вызывает увеличение массы и часто вызывает гипогликемию. (Б) Полагают, что бигуаниды (например,метформин) действуют преимущественно путем уменьшения продукции глюкозы в печени. Бигуаниды часто вызывают желудочно-кишечные расстройства и лактацидоз, что дополнительно ограничивает их применение. (В) Ингибиторы альфы-глюкозидазы (например, акарбоза) уменьшают поглощение глюкозы кишечником. Эти агенты часто вызывают желудочно-кишечные расстройства. (Г) Тиазолидиндионы (например, пиоглитазон, розиглитазон) действуют в отношении определенного рецептора (гамма-рецептор,активируемый пролифератором пероксисом) в печени, мышце и жировых тканях. Они регулируют липидный метаболизм, впоследствии увеличивая ответ этих тканей на действия инсулина. Частое использование этих лекарств может приводить к увеличению массы тела и может вызывать отек и анемию. (Д) Инсулин используется в более серьезных случаях, как самостоятельно, так и в комбинации с вышеупомянутыми агентами. Идеально, эффективное новое лечение NIDDMT2DM может удовлетворять следующим критериям:(а) оно не обладает существенными побочными действиями, включающими индукцию гипогликемии; (б) не вызывает увеличение массы тела; (в) по меньшей мере, частично заменяет инсулин, действуя через механизм(ы), которые не зависят от действий инсулина; (г) желательно является метаболически стабильным, давая возможность для менее частого применения; и (д) пригоден к применению в комбинации с переносимыми количествами любой из категорий перечисленных здесь лекарств. Появилось множество публикаций, которые раскрывают непептидные соединения, которые действуют в отношении глюкагонового рецептора. Например, каждый из WO 03/048109, WO 2004/002480, WO 2005/123668, WO 2005/118542, WO 2006/086488, WO 2006/102067, WO 2007/106181, WO 2007/114855,WO 2007/120270, WO 2007/123581 и Kurukulasuriya et al. BioorganicMedicinal Chemistry Letters, 2004,14(9), 2047-2050 раскрывает непептидные соединения, которые действуют в качестве антагонистов глюкагонового рецептора. Хотя исследования проводятся в настоящее время, сохраняется потребность в более эффективном и безопасном терапевтическом лечении сахарного диабета, в частности NIDDM. Краткое описание графических материалов На чертеже изображена дифракция рентгеновских лучей на порошке для приведенного в примере соединения, как указано. Краткое изложение сущности изобретения В настоящем изобретении предложены соединения формулы I, действующие в качестве модуляторов глюкагонового рецептора, в частности глюкагоновые антагонисты; таким образом, они могут быть использованы в лечении заболеваний, опосредованных таким антагонизмом (например, заболеваний,связанных с сахарным диабетом II типа, и сопутствующих заболеваний, связанных с сахарным диабетом и ожирением). Первое воплощение настоящего изобретения представляют собой соединение формулы I или его фармацевтически приемлемую соль,где R1 представляет собой 5-членную гетероарильную группу, содержащую от 1 до 4 гетероатомов,выбранных из N и О, присоединенную по атому углерода или азота и возможно конденсированную с (С 4 С 7)циклоалкилом или фенилом; где возможно конденсированный 5-членный гетероарил возможно замещен заместителями в количестве от одного до четырех, каждый из которых независимо выбран из галогена, группы -S-(С 1-С 3)алкил, гидрокси, (С 3-С 5)циклоалкила, циано, фенила, пиридинила, (С 1-С 6)алкила,возможно замещенного фтором в количестве от одного до трех, или (C1-С 6)алкокси, возможно замещенного фтором в количестве от одного до трех;R3 представляет собой -(CH2)2 СО 2 Н; каждый из А 1, А 2, А 3 и А 4 независимо представляет собой CR4 или N при условии, что не более двух из А 1, А 2, А 3 и А 4 представляют собой N;R4 в каждом случае независимо представляет собой Н, галоген, (С 1-С 3)алкил или (С 1-С 3)алкокси;X представляет собой СН 2, О или NH;R5 представляет собой (С 1-С 6)алкил, возможно замещенный фтором в количестве от одного до трех;(С 3-С 7)циклоалкил, возможно замещенный (С 1-С 3)алкилом в количестве от одного до двух, который возможно замещен фтором в количестве от одного до трех, и где один атом углерода в (С 3-С 7)циклоалкиле может быть заменен на NH, О или S; или (С 3-С 7)циклоалкил-(С 1-С 6)алкил, где (С 3-С 7)циклоалкильная группа указанного (С 3-С 7)циклоалкил-(С 1-С 6)алкила возможно замещена (С 1-С 3)алкилом в количестве от одного до двух, который возможно замещен фтором в количестве от одного до трех; каждый из В 1, В 2, В и В 4 независимо представляет собой CR6 или N при условии, что не более двух 1 из В , В 2, В 3 и В 4 представляют собой N;R6 в каждом случае независимо представляет собой Н, галоген, (С 1-С 3)алкил или (С 1-С 3)алкокси. Второе воплощение настоящего изобретения представляет собой соединение в соответствии с первым воплощением или его фармацевтически приемлемую соль, где R1 представляет собой 5-членный гетероарил, присоединенный через атом азота к углероду между А 1 и А 4 кольца, содержащего А 1, А 2, А 3 и А 4; R2 представляет собой водород и R3 представляет собой -(СН 2)2 СО 2 Н. Третье воплощение настоящего изобретения представляет собой соединение в соответствии с первым или вторым воплощениями или его фармацевтически приемлемую соль, где X представляет собой О. Четвертое воплощение настоящего изобретения представляет собой соединение в соответствии с первым или вторым воплощениями или его фармацевтически приемлемую соль, где X представляет собойNH. Пятое воплощение настоящего изобретения представляет собой соединение в соответствии с первым или вторым воплощениями или его фармацевтически приемлемую соль, где X представляет собой СН 2. Шестое воплощение настоящего изобретения представляет собой соединение в соответствии с третьим или четвертым воплощениями или его фармацевтически приемлемую соль, где L представляет собой -X-CH(R5)-; каждый из A1, A2, A3 и A4 независимо представляет собой CR4; или A4 представляет собой N, и каждый из A1, A2 и A3 представляет собой CR4; или каждый из A1 и A4 представляет собой N, и каждый из А 2 и A3 представляет собой CR4; или каждый из А 2 и A4 представляет собой N, и каждый из A1 и A3 представляет собой CR4; R4 в каждом случае независимо представляет собой H или метил; каждый из В 1, В 2, В 3 и В 4 представляет собой CR6; или В 1 представляет собой N, и каждый из В 2, В 3 и В 4 представляет собой CR6; или каждый из В 2 и В 3 представляет собой N, и каждый из В 1 и В 4 представляет собой CR6; или каждый из В 1 и В 4 представляет собой N; и каждый из В 2 и В 3 представляет собой CR6; и R6 в каждом случае представляет собой Н. Седьмое воплощение настоящего изобретения представляет собой соединение в соответствии с третьим воплощением или его фармацевтически приемлемую соль, где L представляет собой -X-CH(R5)-; каждый из А 1, А 2, А 3 и А 4 представляет собой CR4; или А 4 представляет собой N, и каждый из А 1, А 2 и А 3 представляет собой CR4; или каждый из А 1 и А 4 представляет собой N, и каждый из А 2 и А 3 представляет собой CR4; или каждый из А 2 и А 4 представляет собой N, и каждый из А 1 и А 3 представляет собой CR4;R4 в каждом случае независимо представляет собой H или метил; каждый из В 1, В 2, В 3 и В 4 представляет собой CR6; и R6 в каждом случае независимо представляет собой H или метил. Восьмое воплощение настоящего изобретения представляет собой соединение в соответствии с четвертым воплощением или его фармацевтически приемлемую соль, где R2 представляет собой водород; R3 представляет собой -(СН 2)2 СО 2 Н; L представляет собой -CH(R5)-X-; A4 представляет собой N, и каждый из А 1, А 2 и А 3 представляет собой CR4; или каждый из А 1 и А 4 представляет собой N, и каждый из А 2 и А 3 представляет собой CR4; или каждый из А 2 и А 4 представляет собой N, и каждый из А 1 и А 3 представляет собой CR4; R4 в каждом случае независимо представляет собой H или метил; каждый из В 1,В 2, В 3 и В 4 представляет собой CR6; и R6 в каждом случае независимо представляет собой H или метил. Девятое воплощение настоящего изобретения представляет собой соединение в соответствии с четвертым воплощением или его фармацевтически приемлемую соль, где R2 представляет собой водород; R3 представляет собой -(СН 2)2 СО 2 Н; L представляет собой -CH(R5)-X-; каждый из А 1, А 2, А 3 и А 4 независимо представляет собой CR4; R4 в каждом случае независимо представляет собой H или метил; один из В 1,В 2, В 3 и В 4 представляет собой N, а остальные представляют собой CR6; и R6 в каждом случае независимо представляет собой H или метил. Десятое воплощение настоящего изобретения представляет собой соединение в соответствии с воплощениями с шестое по девятое или его фармацевтически приемлемую соль, где R5 представляет собой этил, пропил, изопропил, изобутил, неопентил, циклопропил, циклобутил, диметилциклобутил, циклопентил или циклопропилметил. Одиннадцатое воплощение настоящего изобретения представляет собой соединение в соответствии с десятым воплощением или его фармацевтически приемлемую соль, где R1 представляет собой имидазолил, пиразолил, триазолил или индазолил, возможно замещенные заместителями в количестве от одного до двух, каждый из которых независимо выбран из метила, трифторметила, этила, пропила, изопропила, бутила, трет-бутила, метокси, этокси, циано, хлора или фтора. Двенадцатое воплощение настоящего изобретения представляет собой соединение в соответствии с первым воплощением или его фармацевтически приемлемую соль, где R1 представляет собой имидазолил, пиразолил, триазолил или индазолил, возможно замещенные заместителями в количестве от одного до двух, каждый из которых независимо выбран из метила, трифторметила, этила, пропила, изопропила,-3 023517 бутила, трет-бутила, метокси, этокси, циано, хлора или фтора; L представляет собой -X-CHR5-; X представляет собой О; и R5 представляет собой этил, пропил, изопропил, изобутил, неопентил, циклопропил,циклобутил, диметилциклобутил, циклопентил или циклопропилметил. Тринадцатое воплощение настоящего изобретения представляет собой соединение в соответствии с первым воплощением или его фармацевтически приемлемую соль, где R1 представляет собой имидазолил, пиразолил, триазолил или индазолил, возможно замещенные заместителями в количестве от одного до двух, каждый из которых независимо выбран из метила, трифторметила, этила, пропила, изопропила,бутила, трет-бутила, метокси, этокси, циано, хлора или фтора; L представляет собой -CHR5-X-; X представляет собой NH; и R5 представляет собой этил, пропил, изопропил, изобутил, неопентил, циклопропил, циклобутил, диметилциклобутил, циклопентил или циклопропилметил. Четырнадцатое воплощение настоящего изобретения представляет собой соединение в соответствии с двенадцатым или тринадцатым воплощениями или его фармацевтически приемлемую соль, где R1 представляет собой 4-трифторметилпиразол-1-ил или 4-трифторметилимидазол-1-ил. Пятнадцатое воплощение настоящего изобретения представляет собой соединение, выбранное из группы, состоящей из или его фармацевтически приемлемую соль. Шестнадцатое воплощение настоящего изобретения представляет собой соединение, выбранное из группы, состоящей из или его фармацевтически приемлемую соль.-8 023517 Семнадцатое воплощение настоящего изобретения представляет собой соединение, выбранное из группы, состоящей из или его фармацевтически приемлемую соль. Еще одно воплощение настоящего изобретения представляет собой соединение в соответствии с первым воплощением, представляющее собой (S)-3-(4-(1-(3,5-диметил-4-(4-(трифторметил)-1 Н-пиразол 1-ил)фенокси)бутил)бензамидо)пропионовую кислоту, или его фармацевтически приемлемую соль. Еще одно воплощение настоящего изобретения представляет собой соединение в соответствии с первым воплощением, представляющее собой 3-(4-(циклопентил(6-(4-(трифторметил)-1 Н-пиразол-1 ил)пиридин-3-иламино)метил)бензамидо)пропионовую кислоту, изомер 1, или его фармацевтически приемлемую соль.- 12023517 Еще одно воплощение настоящего изобретения представляет собой соединение в соответствии с первым воплощением, представляющее собой 3-(4-(1-(6-(4-трет-бутил-1H-пиразол-1-ил)пиридин-3 иламино)бутил)бензамидо)пропионовую кислоту, изомер 2, или его фармацевтически приемлемую соль. Еще одно воплощение настоящего изобретения представляет собой соединение в соответствии с первым воплощением, представляющее собой 3-(4-3,3-диметилциклобутил)(2-(4-(трифторметил)-1Hпиразол-1-ил)пиримидин-5-илокси)метил)бензамидо)пропионовую кислоту, изомер 1, или его фармацевтически приемлемую соль. Еще один аспект настоящего изобретения представляет собой фармацевтическую композицию,действующую в качестве глюкагонового антагониста, содержащую (1) терапевтически эффективное количество соединения по настоящему изобретению или его фармацевтически приемлемой соли и (2) фармацевтически приемлемый эксципиент, разбавитель или носитель. Еще один аспект настоящего изобретения представляет собой способ лечения или замедления развития или возникновения сахарного диабета II типа и связанных с диабетом расстройств у животных,включающий стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по настоящему изобретению или его фармацевтически приемлемой соли. Еще один аспект настоящего изобретения представляет собой способ лечения или замедления развития или возникновения сахарного диабета II типа и связанных с диабетом расстройств у животных,включающий стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества фармацевтической композиции по настоящему изобретению. Определения Использованный здесь термин "алкил" относится к углеводородному радикалу общей формулыCnH2n+1-алкановый радикал может быть прямолинейным или разветвленным. Например, термин "(С 1 С 6)алкил" относится к одновалентной прямолинейной или разветвленной алифатической группе, содержащей от 1 до 6 атомов углерода (например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, вторбутил, трет-бутил, н-пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, неопентил, 3,3-диметилпропил,гексил, 2-метилпентил и т.п). Аналогично, алкиленовый фррагмент (т.е. алкильная группировка) группы алкокси, ацильной (например, алканоильной), алкиламино, диалкиламино, алкилсульфонильной и алкилтио имеют то же самое определение, как выше. Когда указано, что алкановый радикал или алкильная группировка являются "возможно замещенными", тогда они могут быть незамещенными или замещенными одним или более чем одним заместителем (как правило, от одного до трех заместителей, за исключением случая галогеновых заместителей, таких как перхлор или перфторалкилы). Термин "циклоалкил" относится к неароматическим кольцам, полностью гидрированным, и которые могут существовать в виде единичного кольца, бициклического кольца или спирального кольца. Если не указано иное, то карбоциклическое кольцо, как правило, представляет собой 3-8-членное кольцо. Например, (С 3-С 7)циклоалкил включает группы, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, циклогептил, норборнил (бицикло[2.2.1]гептил) и т.п. В некоторых воплощениях один или больше чем один атом углерода в циклоалкиле могут быть заменены на указанный гетероатом, такой как О, S, NH или N-алкил. Фраза "5-членный гетероарил" или "6-членный гетероарил" обозначает радикал соответственно 5 или 6-членного гетероароматического кольца. Гетероароматическое кольцо может соержать от 1 до 4 гетероатомов, выбранных из N, О и S. 5-6-Членные гетероарильные группы включают пирролил, фуранил, тиенил, имидазолил, тиазолил, оксазолил, триазолил, тетразолил, пиридинил, пиримидинил, пиразинил, триазинил и т.п. Предпочтительные 5-6-членные гетероарильные группы включают пиразолил,имидазолил, пиридинил, пиримидинил или пиразинил. Гетероарильная группа, если указано, может быть конденсированный с еще одним кольцом. Например, 5-членный гетероарил, такой как пиразол, может быть конденсирован с фенилом с получением индазола. Фраза "терапевтически эффективное количество" обозначает количество соединения по настоящему изобретению, которое (1) лечит или предупреждает конкретное заболевание, состояние или расстройство, (2) смягчает, уменьшает интенсивность или устраняет один или более чем один симптом конкретного заболевания, состояния или расстройства, или (3) предупреждает или задерживает начало одного или более чем одного симптома конкретного описанного здесь заболевания, состояния или расстройства. Термин "животное" относится к людям (мужчине или женщине), животным-компаньонам (например, собакам, кошкам и лошадям), сельскохозяйственным животным, животным, содержащимся в зоопарке, морским животным, птицам или другим похожим видам животных. "Пригодные в пищу животные" относятся к сельскохозяйственным животным, таким как коровы, свиньи, овцы и домашняя птица. Фраза "фармацевтически приемлемый" указывает на то, что вещество или композиция должна быть совместима химически и/или токсикологически с другими ингредиентами, входящими в состав композиции, и/или животным, которого им лечат. Термины "лечение", "лечить" или "процесс лечения" включают как предупредительное, т.е. профилактическое, так и паллиативное лечение. Использованные здесь термины "модулированный" или "модулирующий", или "модулируют(ет)",если не указано иное, относятся к изменениям активности глюкагонового рецептора в результате дейст- 13023517 вия соединений по настоящему изобретению. Использованные здесь термины "опосредованный" или "опосредующий", или "опосредуют(ет)", если не указано иное, относятся к лечению или предупреждению конкретного заболевания, состояния или расстройства, (2) смягчению, уменьшению интенсивности или устранению одного или более чем одного симптома конкретного заболевания, состояния или расстройства, или (3) предупреждению или замедлению возникновения одного или более чем одного симптома конкретного описанного здесь заболевания,состояния или расстройства путем модуляции глюкагона. Термин "соединения по настоящему изобретению" (если конкретно не указано иное) относится к соединениям формулы I и любым фармацевтически приемлемым солям соединений, а также ко всем стереоизомерам (включая диастереоизомеры и энантиомеры), таутомерам, конформационным изомерам и изотопно меченым соединениям. Гидраты и сольваты соединений по настоящему изобретению рассматриваются как композиции по настоящему изобретению, где соединение находится в ассоциации с водой или растворителем соответственно. Подробное описание изобретения Соединения по настоящему изобретению могут быть синтезированы посредством путей синтеза,которые включают способы, аналогичные способам, хорошо известным в химической области техники, в особенности в свете содержащегося здесь описания. Исходные материалы обычно доступны из коммерческих источников, таких как Aldrich Chemicals (Milwaukee, WI), или могут быть легко получены способами хорошо известными специалистам в данной области техники (например, способами, в общем описанными в Louis F. Fieser and Mary Fieser, Reagents for Organic Synthesis, v. 1-19, Wiley, New York (19671999 d.), или Beilsteins Handbuch der organischen Chemie, 4, Aufl. ed. Springer-Verlag, Berlin, включая приложения (также доступные через интерактивную базу данных Beilstein. Для иллюстративных задач изображенные ниже схемы взаимодействий предлагают возможные способы пути синтеза соединений по настоящему изобретению, а также ключевых промежуточных соединений. Более подробное описание отдельных стадий взаимодействий смотри в нижеприведенном разделе Примеры. Специалистам в данной области техники понятно, что другие пути синтеза можно использовать для синтеза соединений по изобретению. Хотя специфические исходные материалы и реагенты приведены на схемах и обсуждаются ниже, можно легко заменить их другими исходными материалами и реагентами с получением различных производных и/или условий реакции. Кроме того, многие соединения, получаемые с помощью способов, описанных ниже, могут быть дополнительно модифицированы в свете этого описания с использованием обычной химии, хорошо известной специалистам в данной области техники. При получении соединений по настоящему изобретению может быть необходима защита удаленной функциональной группы (например, первичного или вторичного амина) промежуточных соединений. Необходимость такой защиты будет изменяться в зависимости от природы удаленной функциональной группы и условий способов получения. Подходящие защитные группы амино (NH-Pg) включают ацетил,трифторацетил, трет-бутоксикарбонил (ВОС), бензилоксикарбонил (CBz) и 9-флуоренилметиленоксикарбонил (Fmoc). Аналогично, "защитная группа гидрокси" относится к заместителю группы гидрокси, которая блокирует или защищает гидроксильную функциональную группу. Подходящие защитные группы гидроксила (O-Pg) включают, например, аллил, ацетил, силил, бензил, параметоксибензил, тритил и т.п. Необходимость такой защиты легко определяется специалистами в данной области техники. Общее описание защитных групп и их применения смотри в T.W. Greene, Protective Groups in OrganicSynthesis. John WileySons, New York, 1991. Реакционная схема I раскрывает общие способы, которые могут быть использованы при получении соединений формулы I по настоящему изобретению. Реакционная схема I- 14023517 Реакционная схема I предлагает общий путь, который может быть использован для получения соединений формулы I. Более конкретная подробная информация об изображенных превращениях приведена на реакционных схемах II-VII ниже. Понятно, что реакционные схемы являются иллюстративными,и их не следует рассматривать как ограничивающие каким-либо образом. На стадии один реакционной схемы I соединение R1-М формулы VII и соединение формулы VI подвергают реакции сочетания. В соединении формулы VII R1 представляет собой 5-членную возможно конденсированную и возможно замещенную гетероарильную группу. Группа M может представлять собой либо водород, когда он присоединен по азоту в гетероарильной группе R1, или подходящие виды металлов, прикрепленные к углероду в гетероарильной группе R1. Когда M представляет собой металл, присоединенный по углероду в группеR1, тогда реакцию сочетания можно проводить с использованием палладия, катализирующего реакцию сочетания. Когда M представляет собой водород, присоединенный по азоту в гетероарильной группе R1,тогда реакцию нуклеофильного замещения с образованием соединения формулы V можно проводить в подходящем растворителе в присутствии основания. В соединении формулы I Lg представляет собой подходящую уходящую группу, такую как галогенид или трифлат. Соединение формулы V может затем взаимодействовать с соединением формулы IV с получением соединения формулы III. В соединении формулы V L' представляет собой группу-предшественник, которая вместе с R" в соединении формулыIV превращается в линкер L в соединении формулы III. Соединение формулы III можно затем гидролизировать с получением свободной кислоты формулы II, которую можно затем подвергнуть реакции амидного сочетания с амином R3' R2 NH с последующим удалением защиты, если необходимо получить соединение формулы I. Группа R3 в амине R3R2NH может представлять собой сам R3 или защищенный вариант R3, защита с которого затем может быть удалена с получением R3. Реакционная схема II раскрывает еще один общий способ, который может быть использован для получения соединений по настоящему изобретению формулы I. Реакционная схема II Эфирное соединение формулы III можно получить путем взаимодействия подходящего гетероарильного соединения R1-H или металлированного гетероарильного соединения R1-М с соединением формулы IIIa. Взаимодействие с R1-H может быть использовано, когда водород, изображенный в R1-H, присоединен по азоту в гетероарильной группе R1. Взаимодействие может быть осуществлено в подходящем растворителе, таком как диметилсульфоксид, и основании, таком как карбонат калия, в присутствии йодида меди(I). Взаимодействие между соединением формулы IIIa и R1-М можно осуществить с помощью катализируемой палладием реакции сочетания. Предпочтительно взаимодействие осуществляют между боронатным эфиром R1-M (где M представляет собой ВOR')2 R' представляет собой H или низший алкил, или оба R' вместе образуют подходящую циклическую группу) и соединением формулы IIIa (где Lg представляет собой OSO2CF3, Cl, Br или I) с использованием подходящего палладиевого катализатора,подходящего фосфинового лиганда и подходящего основания в присутствии подходящего растворителя при температуре, находящейся типично в диапазоне от комнатной температуры до приблизительно температуры дефлегмации (или при температурах выше температуры кипения растворителя, например 120 С, с использованием условий микроволнового реактора). Подходящий палладиевый катализатор представляет собой трис-(дибензилиденацетон)дипалладий,бис-(дибензилиденацетон)палладий,ацетат палладия или(1,1'-бис-(дифенилфосфино)ферроцен)дихлорпалладий. Подходящий фосфиновый лиганд представляет собой трициклогексилфосфин,трифенилфосфин или 2-дициклогексилфосфин-2',6'-диметоксилбифенил. Подходящее основание представляет собой карбонат натрия, карбонат калия, фосфат калия или гидрокарбонат натрия, а растворители представляют собой DME (диметиловый эфир), 1,4-диоксан или THF (тетрагидрофуран)/вода. Альтернативно, перекрестное сочетание можно проводить между триметилстаннаном общей формулы R1-M (где M представляет собой SnMe3) и соединением формулы IIIa с использованием подходящего катализатора, такого как тетракис(трифенилфосфин)палладий, представляющий собой возможный источник меди(I), такой как хлорид меди(I), подходящего основания, такого как фторид цезия, и подходящего растворителя, такого как N,N-диметилформамид, при температуре обычно приблизительно от 80 до 120 С. Кроме того, также могут быть использованы альтернативные способы с использованием ме- 15023517 таллированных соединений R1-M (где M представляет собой MgX' или ZnX', a X' представляет собой галогенид) с производным IIIa с использованием подходящего палладиевого катализатора, подходящего фосфинового основания и возможного источника меди(I), а также подходящего основания в присутствии подходящего растворителя при температуре обычно составляющей приблизительно температуру дефлегмации. Подходящие палладиевые катализаторы представляют собой трис-(дибензилиденацетон)дипалладий, бис-(дибензилиденацетон)палладий, ацетат палладия или (1,1'-бис-(дифенилфосфино)ферроцен)дихлорпалладий. Подходящие фосфиновые основания представляют собой трициклогексилфосфин или 2-дициклогексилфосфин-2',6'-диметоксилбифенил. Подходящий источник меди(I) представляет собой хлорид меди(I). Подходящие основания представляют собой карбонат калия и гидрокарбонат натрия. Подходящие растворители представляют собой DME, 1,4-диоксан или THF/вода. Соединение формулы III затем подвергают гидролизу с получением соединения формулы II. В зависимости от того, какая R группа присутствует в сложном эфире формулы III, гидролиз, катализируемый подходящей кислотой или основанием, может быть осуществлен для получения соответствующей свободной кислоты в соединении формулы II. Например, когда R представляет собой метил, тогда гидролиз обычно осуществляют с водным раствором гидроксида натрия или гидроксида лития в смеси с метанолом и тетрагидрофураном при температуре от комнатной до 80 С в течение 15 мин-24 ч. Превращение соединения формулы II с получением соединения формулы I можно осуществлять с использованием условий стандартного амидного сочетания. Амидное сочетание осуществляют с использованием стандартных условий, описанных в литературе. Кислота формулы II может быть превращена в соответствующий хлорангидрид с использованием подходящего хлорирующего агента, такого как оксалилхлорид или тионилхлорид, в подходящем растворителе, таком как дихлорметан или толуол, возможно в присутствии каталитического DMF (диметилформамид), при подходящей температуре, обычно между 0 С и комнатной температурой. Хлорангидрид может затем взаимодействовать с амином общей формулы R3-NH2 в присутствии основания, такого как триэтиламин или диизопропилэтиламин, в подходящем растворителе, таком как дихлорметан или толуол, при температуре от 0 С до комнатной. R3' может представлять собой сам R3 или защищенный вариант R3, защита с которого затем может быть удалена с получением R3. Альтернативно, кислота формулы II может быть превращена в подходящие активированные частицы со связывающим агентом, таким как EDCIHCl, HBTU, HATU, PyBop, DCC или CDI, в подходящем растворителе, таком как дихлорметан, ацетонитрил или DMF. В присутствии EDCIHCl обычно добавляют НОВТ. EDCI представляет собой 1-этил-3-(3-диметиламинопропил)карбодиимид;HBTU представляет собой О-бензотриазол-N,N,N',N'-тетраметилуронийгексафторфосфат; HATU представляет собой O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуронийгексафторфосфат; РуВор представляет собой бензотриазол-1-илокситрипирролидинфосфоний гексафторфосфат; DCC представляет собой дициклогексилкарбодиимид; CDI представляет собой N,N'-карбонилдиимидазол, и НОВТ представляет собой 1-гидроксибензотриазол. Также применяют подходящее основание, такое как триэтиламин или диизопропилэтиламин, а взаимодействие обычно проводят при комнатной температуре. В случае, когда R3 представляет собой защищенный вариант R3, тогда последующее удаление защиты можно провести с помощью способов, известных в данной области техники, с получением R3. Например, еслиR3 является сложным эфиром, то можно проводить гидролиз, катализируемый подходящей кислотой или основанием, с получением соответствующей свободной кислоты в соединении формулы I. Реакционная схема III раскрывает основные способы, которые можно использовать для получения соединений формулы Ia по настоящему изобретению. Соединения формулы Ia представляют собой соединения формулы I, где L представляет собой -C(R5)-Х-, X представляет собой NH и R2 представляет собой Н. Реакционная схема III Нитрил формулы Va взаимодействует с подходящим реактивом Гриньяра R5-M, где M представляет- 16023517 собой галогенид магния, такой как хлорид магния или бромид магния. Взаимодействие осуществляют в подходящем растворителе, таком как тетрагидрофуран, или смесь тетрагидрофурана и диэтилового эфира. Взаимодействие типично осуществляют при температуре от 0 до 100 С, и предпочтительно микроволновое облучение реакционной смеси. После завершения реакции Гриньяра реакционную смесь затем подвергают восстановлению с использованием подходящего восстановителя, такого как борогидрид натрия, в подходящем растворителе, таком как метанол, с получением аминового соединения формулы IVa. Соединение формулы IVa затем превращают в соединение формулы Ia, как описано ранее на реакционной схеме II. На реакционной схеме IV предложено получение соединений, где L представляет собой -XCHR5- и Амин формулы IVb может быть получен путем восстановления, такого как путем гидрирования соответствующего нитропроизводного. Амин формулы IVb может быть превращен в соединение формулыIIIb при помощи двух способов. Первый способ включает взаимодействие амина с альдегидом формулыIVb' с последующим алкилированием получающегося в результате альдимина подходящим алкилирующим реагентом R5-М формулы IVb". Взаимодействие амина формулы IVb с альдегидом формулы IVb' с получением соответствующего альдимина осуществляют в подходящем растворителе, таком как толуол,обычно в присутствии молекулярных сит, при температуре от комнатной до 100 С в течение 1-24 ч. Реакционную смесь, содержащую альдимин, можно фильтровать и концентрировать. Полученный остаток затем может быть снова повторно растворен в растворителе, подходящем для реакции алкилирования,таком как тетрагидрофуран. Как правило, используют подходящий металлированный алкилирующий агент, такой как реактив Гриньяра R5-М формулы IVb", где M представляет собой металл, такой как галогенид магния. Реакцию алкилирования можно проводить при температуре от 0 до 60 С в течение 1-24 ч с получением соединения формулы IIIb. Когда R5-M представляет собой реактив Гриньяра, может быть желательно добавление хлорида цинка в реакционную смесь для увеличения выхода соединения формулы IIIb (смотри Ishihara, K. et al.; JACS, 2006, 128, 9998. Альтернативно, соединение формулы IIIb может быть получено путем взаимодействия амина формулы IVb и кетона формулы IVb'" с последующим восстановлением получающегося в результате имина. Взаимодействие может быть осуществлено в типичных условиях восстановительного аминирования с получением соединения формулы IIIb. Например, амин формулы IVb и кетон IVb'" в подходящем растворителе, таком как диметоксиэтан, и в присутствии молекулярных сит и пара-толуолсульфоновой кислоты, может взаимодействовать при температуре от комнатной до 120 С (в запаянной пробирке) в течение 1-24 ч. Реакционную смесь затем можно оставить остывать при комнатной температуре и затем обработать подходящим восстановителем, таким как цианоборогидрид натрия в метаноле, а также в присутствии уксусной кислоты в течение 1-24 ч с получением соединения формулы IIIb. Соединение формулы IIIb может быть гидролизовано с получением свободной кислоты соединения формулы IIb при помощи способов, ранее описанных для получения соединения формулы IIa на реакционной схеме II. Свободнокислотное соединение формулы IIb затем может претерпеть амидное сочетание с последующим удалением защиты при необходимости с получением соединения формулы Ib, как описано ранее для превращения соединения формулы IIa в формулу Ia на реакционной схеме II. Реакционная схема V раскрывает основные способы, которые могут быть использованы для получения соединений формулы Ic по настоящему изобретению. Соединения формулы Ic представляют собой соединения формулы I, где L представляет собой -X-C(R5)-, X представляет собой О и R2 представляет собой Н. Соединение формулы IVc получают путем взаимодействия альдегида формулы Vc с подходящим металлированным алкилированным соединением R5-M (Vc'). Как правило, R5-M представляет собой реактив Гриньяра, в котором M представляет собой галогенид магния, такой как хлорид магния или бромид магния. Взаимодействие осуществляют в подходящем растворителе, таком как тетрагидрофуран, при температуре от приблизительно -78 С до комнатной в течение периода времени от 15 мин до 24 ч с получением спирта формулы IVc. Спирт IVc затем сочетают с фенолом формулы IVc' с использованием фенольного эфира в условиях реакции Митсунобу (смотри, например, Mitsunobu, О.; Synthesis, 1981, 1;Lepore, S.D. et al. J. Org. Chem, 2003, 68(21), 8261-8263) с получением соединения формулы IIIc. Взаимодействие обычно осуществляют в подходящем растворителе, таком как тетрагидрофуран, в присутствии подходящего связывающего агента, такого как диэтилазодикарбоксилат (DEAD) или диизопропилазодикарбоксилат (DIAD), и фосфинового лиганда, такого как трифенилфосфин. Взаимодействие обычно осуществляют при температуре от 0 С до комнатной в течение 1-24 ч. Соединение IIIc затем может быть гидролизовано до соединения формулы IIc с последующими образованием амида и удалением защиты,при необходимости, с получением соединения формулы Ic, как описано ранее для соответствующих стадий на реакционной схеме II. На реакционной схеме VI раскрыты основные способы, которые могут быть использованы для получения соединений формулы Id по настоящему изобретению. Соединения формулы Id представляют собой соединения формулы I, где L представляет собой -C(R5)-Х-, X представляет собой О, a R2 представляет собой Н. Реакционная схема VI Соединение формулы Id получают по аналогии с получением соединения формулы Ic на реакционной схеме V путем замены соединения формулы Vd, Vd', IVd, IVd', IIId и IId на соединения Vc, Vc', IVc,IVc', IIIc и IIc, как описано ранее. На реакционной схеме VII раскрыты общие способы, которые можно использовать для получения соединения формулы Ia по настоящему изобретению. Соединения формулы Ia представляют собой соединения формулы I, где R1 находится в положении пара, L представляет собой -X-C(R5)-, X представляет собой СН 2 и R2 представляет собой Н. Соединение бромида фосфония формулы VIIe можно обработать подходящим основанием и затем провести взаимодействие с кетоновым производным формулы VIIe' с получением олефинового соединения формулы VIe. Соединение формулы VIIe, как правило, обрабатывают основанием, таким как литий бис-(триметилсилил)амид (LHMDS) в подходящем растворителе, таком как толуол, при температуре от-78 С до комнатной. Другие основания, которые могут быть использованы, включают амиды лития, такие как литий диизопропиламид (LDA), литий 2,2,6,6-тетраметилпиперидид (LiTMP) или литий диэтиламид, а также алкил литий, такой как метиллитий или н-бутиллитий. Соединение формулы VI затем может взаимодействовать с гетероарильным соединением R1-M(VIe', где M представляет собой водород, присоединенный по азоту или подходящий металл, присоединенный по углероду). Когда M представляет собой металл, присоединенный по углероду в гетероариле,представленном R1, тогда взаимодействие обычно представляет собой катализируемую палладием реакцию сочетания, как описано ранее для первой стадии реакционной схемы II, с получением соединения формулы Ve. Когда M представляет собой водород, присоединенный по азоту в гетероариле R1, тогда реакцию нуклеофильного замещения обычно осуществляют в подходящем растворителе в присутствии основания. Соединение формулы Ve затем подвергают гидролизу, обычно в метаноле и тетрагидрофуране, с использованием гидроксида натрия в качестве основания при температуре от 0 С до комнатной в течение 1-24 ч с получением свободной кислоты формулы IVe. Свободная кислота формулы IVe затем может взаимодействовать с амином R3'-NH2 с использованием условий амидного спаривания, описанных ранее для реакционной схемы II, с получением соединения формулы IIIe. Соединение формулы IIIe затем подвергают гидрированию для восстановления олефиновой группировки и получения соединения формулы IIe. Гидрирование обычно осуществляют в присутствии подходящего гидрирующего катализатора,такого как 10% палладий на углероде (Pd/C), в пригодном растворителе, таком как метанол, при температуре от комнатной до 50 С. На этой стадии можно использовать аппарат для гидрирования, такой как гидрогенизатор ThalesNano H-Cube (ThalesNano, Budapest, Hungary) с 10% Pd/C картриджем. Защита с соединения формулы IIe затем при необходимости может быть удалена, как описано ранее для реакционной схемы II, с получением соединения формулы Ie. На реакционной схеме VIII раскрыт еще один общий способ, который может быть использован для получения соединений формулы Ic по настоящему изобретению. Соединения формулы Ic представляют собой соединения формулы I, где L представляет собой -X-C(R5)-, X представляет собой О и R2 представляет собой Н. Реакционная схема VIII Соединение формулы Vf, где Lg представляет собой подходящий галогенид, предпочтительно йодид, и R3' представляет собой защищенную группу R3 (такую как сложный эфир подходящей группы- 19023517 карбоновой кислоты R3), может быть обработано магнием в подходящем растворителе с получением соответствующего реагента Гриньяра. Реагент Гриньяра затем может быть приведен во взаимодействие с альдегидом R5-CHO с получением соединения формулы IVf. Соединение формулы IVf может претерпевать сочетание Митсунобу с соединением формулы IVc', как описано ранее для реакционной схемы V, с получением соединения формулы IIIf. Удаление защиты с соединения формулы IIIf, например, путем гидролиза ранее описанного сложного эфира затем позволяет получить соединение формулы Ic. Соединения по настоящему изобретению могут быть выделены и использованы сами по себе или по возможности в форме их фармацевтически приемлемой соли. Термин "соли" относится к неорганическим и органическим солям соединений по настоящему изобретению. Эти соли могут быть получены insitu во время окончательного выделения и очистки соединения или путем отдельного взаимодействия соединения с подходящей органической или неорганической кислотой или основанием и выделения образующейся таким образом соли. Типичные соли включают соли гидробромид, гидрохлорид, йодгидрат,сульфат, бисульфат, нитрат, ацетат, трифторацетат, оксалат, безилат, пальмитат, памоат, малонат, стеарат, лаурат, малат, борат, бензоат, лактат, фосфат, гексафторфосфат, бензолсульфонат, тозилат, формиат,цитрат, малеат, фумарат, сукцинат, тартрат, нафтилат, мезилат, глюкогептаноат, лактобионат и лаурилсульфонат и т.п. Они могут включать катионы, основанные на щелочных и щелочно-земельных металлах, таких как натрий, литий, калий, кальций, магний, и т.п., а также нетоксичные ионы аммония, четвертичного аммония и амина, включая аммоний, тетраметиламмоний, тетраэтиламмоний, метиламин, диметиламин, триметиламин, триэтиламин, этиламин и т.п, но не ограничивающиеся ими; смотри, например,Berge, et al., J. Pharm. Sci., 66, 1-19 (1977). Соединения по настоящему изобретению могут содержать асимметрические или хиральные центры, и, таким образом, существовать в различных стереоизомерных формах. Если не указано иное, то предполагается, что все стереоизомерные формы соединений по настоящему изобретению, а также их смеси, включая рацемические смеси, образуют часть настоящего изобретения. Дополнительно, настоящее изобретение охватывает все геометрические и позиционные изомеры. Например, если соединение по настоящему изобретению включает двойную связь или конденсированное кольцо, то цис- и трансформы, а также смеси входят в объем изобретения. Дииастереоизомерные смеси могут быть разделены на индивидуальные диастереоизомеры на основе их физико-химических различий способами, хорошо известными специалистам в данной области техники, такими как хроматография и/или фракционная кристаллизация. Энантиомеры могут быть разделены превращением энантиомерной смеси в диастереоизомерную смесь путем взаимодействия с подходящим оптически активным соединением (например, хиральным вспомогательным соединением, таким как хиральный спирт или хлорангидрид Мошера), разделения диастереоизомеров и превращения (например,гидролиза) индивидуальных диастереоизомеров в соответствующие чистые энантиомеры. Кроме того,некоторые из соединений по настоящему изобретению могут представлять собой атропизомеры (например, замещенные биарилы) и рассматриваются как часть изобретения. Энантиомеры также могут быть разделены путем применения колонки для хиральной ВЭЖХ (высокоэффективная жидкостная хроматография). Альтернативно, специфические стереоизомеры могут быть синтезированы путем использования оптически активного исходного вещества, путем асимметрического синтеза с использованием оптически активных реагентов, субстратов, катализаторов или растворителей, или путем превращения одного стереоизомера в другой путем асимметрического превращения. Также возможно, чтобы промежуточные соединения и соединения по настоящему изобретению могли существовать в различных таутомерных формах, и все такие формы входят в объем изобретения. Термин "таутомер" или "таутомерная форма" относится к структурным изомерам с различными энергиями, которые являются взаимопревращаемыми через низкоэнергетический барьер. Например, протонные таутомеры (также известные как прототропные таутомеры) включают взаимопревращения путем перемещения протона, такие как кето-энольные и имин-энаминовые изомеризации. Конкретный пример протонного таутомера представляет собой имидазольную группировку, где протон может мигрировать между двумя кольцевыми азотами. Валентные таутомеры включают взаимопревращения путем реорганизации некоторых из связывающих электронов. Например, пиримидоновое кольцо по настоящему изобретению также может существовать в своей гидроксипиримидиновой форме. Обе такие формы включены в соединения формулы I. Некоторые соединения по настоящему изобретению могут существовать в различных стабильных конформационных формах, которые могут быть разделяемыми. Торсионная асимметрия вследствие ограниченного вращения вокруг асимметрической простой связи, например, из-за стерической затрудненности или напряжения кольца может дать возможность для разделения различных конформеров. Настоящее изобретение также охватывает изотопно меченые соединения по настоящему изобретению, идентичные перечисленным здесь, но за исключением того, что один или более чем один атом заменен на атом, имеющий атомную массу или массовый номер, отличающиеся от атомной массы или массового числа, обычно обнаруживаемого в природе. Примеры изотопов, которые могут быть включены в соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора,серы, фтора, йода и хлора, такие как 2 Н, 3 Н, 11 С, 13 С, 14 С, 13N, 15N, 15O, 17O, 18O, 31 Р, 32 Р, 35S, 18F, 123I, 125I иCl соответственно. Некоторые изотопно меченые соединения по настоящему изобретению (например, меченые 3 Н и 14 С) полезны в анализах тканевого распределения соединения и/или субстрата. Особенно предпочтительны тритированные (т.е. 3 Н) и углерод-14 (т.е. 14 С) изотопы ввиду легкости их получения и обнаружения. Дополнительно, замещение более тяжелыми изотопами, такими как дейтерий (т.е. 2 Н) может обеспечить некоторые терапевтические преимущества, возникающие в результате большей метаболической стабильности (например, увеличенного периода полувыведения in vivo или уменьшенной потребности в дозах), и, следовательно, может быть предпочтительным в некоторых случаях. Позитронно-активные изотопы, такие как 15 О, 13N, 11 С, и 18F, полезны для исследований путем позитронно-эмиссионной томографии (PET), для исследования путем занятости субстрата. Изотопно-меченые соединения по настоящему изобретению в общем могут быть получены следующими способами, аналогичными описанным на схемах и/или ниже в примерах путем замены изотопно меченного реагента на не меченный изотопом реагент. Некоторые соединения по настоящему изобретению могут существовать в более чем одной кристаллической форме (в общем называемой "полиморфы"). Полиморфы могут быть приготовлены путем кристаллизации в различных состояниях, например, с использованием различных растворителей или различных смесей растворителей для перекристаллизации; кристаллизации при различных температурах; и/или различных режимов охлаждения, находящихся в диапазоне от очень быстрого до очень медленного охлаждения во время кристаллизации. Полиморфы также могут быть получены путем нагревания или плавления соединение по настоящему изобретению, а затем постепенного или быстрого охлаждения. Присутствие полиморфов может быть определено ЯМР (ядерный магнитный резонанс) спектроскопией твердого тела, ИК (инфракрасной) спектроскопией, дифференциальной сканирующей калориметрией,дифракцией рентгеновских лучей на порошке или другими такими способами. Соединения настоящего изобретения полезны для лечения заболеваний, состояний и/или расстройств, модулированных глюкагоном; таким образом, еще одно воплощение настоящего изобретения представляет собой фармацевтическая композиция, содержащая терапевтически эффективное количество соединения по настоящему изобретению и фармацевтически приемлемый эксципиент, разбавитель или носитель. Соединения по настоящему изобретению (включающие использованные здесь композиции и способы) также могут быть использованы в приготовлении лекарственного средства для описанных здесь терапевтических применений. Типичную композицию готовят путем смешивания соединения по настоящему изобретению и носителя, разбавителя или эксципиента. Подходящие носители, разбавители и эксципиенты хорошо известны специалистам в данной области техники и включают материалы, такие как углеводы, воски, водорастворимые и/или набухающие полимеры, гидрофильные или гидрофобные материалы, желатин,масла, растворители, воду и т.п. Конкретный используемый носитель, разбавитель или эксципиент зависит от способов и задачи, для которой применяется соединение по настоящему изобретению. Растворители, как правило, выбирают из числа растворителей, которые специалист в данной области техники рассматривает в общем как безопасные (GRAS) при введении млекопитающему. В общем, безопасные растворители представляют собой нетоксичные водные растворители, такие как воду и другие нетоксичные растворители, растворимые в воде или смешивающиеся с водой. Подходящие водные растворители включают воду, этанол, пропиленгликоль, полиэтиленгликоль (например, PEG400, PEG300) и т.д. и их смеси. Композиции также могут включать один или более чем один буфер, стабилизатор, поверхностноактивное вещество, увлажнители, смазывающие агенты, эмульгаторы, суспендирующие агенты, консерванты, антиоксиданты, агенты, придающие непрозрачность, скользящие вещества, технологические добавки, красители, подсластители, ароматизаторы, корригенты и другие известные добавки для получения наилучшей композиции лекарства (т.е. соединения по настоящему изобретению или его фармацевтической композиции) или облегчения приготовления фармацевтического продукта (т.е. лекарственного средства). Композиции могут быть приготовлены с использованием обычных способов растворения и смешивания. Например, партию лекарственного вещества (т.е. соединения по настоящему изобретению или стабилизированной формы соединения (например, комплекса с циклодекстриновым производным или другим известным комплексообразователем растворяют в подходящем растворителе в присутствии одного или более чем одного вышеописанного эксципиента. Соединение по настоящему изобретению,как правило, готовят в фармацевтических лекарственных формах с достижением легко контролируемой дозы лекарства и обеспечением пациента превосходным продуктом, легким в обращении. Фармацевтические композиции также включают сольваты и гидраты соединений формулы I. Термин "сольват" относится к молекулярному комплексу соединения формулы I (включающего его фармацевтически приемлемые соли) с одной или более чем одной молекулой растворителя. Такие молекулы растворителя представляют собой молекулы, обычно используемые в фармацевтической области, которые, как известно, являются безвредными для реципиента, например воду, этанол, этиленгликоль и т.п. Термин "гидрат" относится к комплексу, в котором молекула растворителя представляет собой воду. Сольваты и/или гидраты предпочтительно существуют в кристаллической форме. Другие растворители- 21023517 могут быть использованы в качестве сольватов-промежуточных соединений при получении более желательных сольватов, такие как метанол, метил трет-бутиловый эфир, этилацетат, метил ацетат, (S)пропиленгликоль, (R)-пропиленгликоль, 1,4-бутин-диол и т.п. Фармацевтическая композиция (или препарат) для применения могут быть упакованы множеством путей в зависимости от способа, используемого для введения лекарства. Как правило, изделие для распространения включает контейнер, в котором расположена фармацевтическая композиция в подходящей форме. Подходящие контейнеры хорошо известны специалистам в данной области техники и включают материалы, такие как флаконы (пластиковые и стеклянные), саше, ампулы, пластиковые контейнеры,металлические цилиндры и т.п. Контейнер также может включать защищенную от вскрытия конструкцию для предотвращения неосторожного доступа к содержимому контейнера. Кроме того, на контейнере имеется этикетка, на которой описано содержимое контейнера. Этикетка также может содержать соответствующие предупреждения. В настоящем описании изобретения раскрыт способ лечения заболеваний, состояний и/или расстройств, модулируемых глюкагоном, у животного, при котором животному, нуждающемуся в таком лечении, вводят терапевтически эффективное количество соединения по настоящему изобретению или фармацевтической композиции, содержащей эффективное количество соединения по настоящему изобретению, и фармацевтически приемлемый эксципиент, разбавитель или носитель. Этот способ особенно полезен для лечения заболеваний, состояний и/или расстройств, при которых благоприятно модулирование глюкагона, которые включают: пищевые расстройства (например, компульсивное переедание, анорексия, булимия, потеря массы тела или контроль массы тела и ожирение),предупреждение ожирения и инсулинорезистентность. В описании раскрыто лечение ожирения и связанных с ожирением расстройств (например, избыточной массы тела, набора массы тела или удерживания массы тела). Ожирение и избыточная масса тела, как правило, определяются при помощи индекса массы тела(BMI), который коррелирует с общим содержанием жира в организме и оценивает относительный риск заболевания. BMI рассчитывается по массе в килограммах, деленной на площадь в квадратных метрахReport, Washington, DC: U.S. Department of Health and Human Services, NIH publication no. 98-4083 (1998). Один аспект настоящего изобретения представляет собой лечение или замедление развития или возникновения сахарного диабета или связанных с сахарным диабетом расстройств, включая сахарный диабет I типа (инсулинозависимый сахарный диабет, также названный "IDDM") и II типа (инсулинонезависимый сахарный диабет, также названный "NIDDM"), нарушение толерантности к глюкозе, инсулинорезистентность, гипергликемию и диабетические осложнения (такие как атеросклероз, ишемическая болезнь сердца, инсульт, заболевание периферических сосудов, нефропатия, гипертензия, нейропатия и ретинопатия). В описании изобретения также раскрыто лечение сахарного диабета или связанных с ожирением осложнений, таких как метаболический синдром. Метаболический синдром включает заболевания, состояния или расстройства, такие как дислипидемия, гипертензия, инсулинорезистентность, сахарный диабет (например, сахарный диабет II типа), увеличение массы тела, ишемическая болезнь сердца и сердечная недостаточность. Более подробную информацию о метаболическом синдроме можно найти, например, в Zimmet, P.Z., et al., "The Metabolic Syndrome: Perhaps an Etiologic Mystery but Far From a Myth - WhereDoes the International Diabetes Federation Stand", DiabetesEndocrinology. 7(2), (2005); and Alberti, K.G., et al.,"The Metabolic Syndrome - A New Worldwide Definition," Lancet, 366, 1059-62 (2005). Предпочтительно введение соединений по настоящему изобретению обеспечивает статистически знначимое (р 0,05) уменьшение по меньшей мере одного фактора риска сердечно-сосудистого заболевания, такое как уменьшение лептина плазмы крови, С-реактивного белка (CRP) и/или холестерина, по сравнению с растворителем без лекарства в качестве контроля. Введение соединений по настоящему изобретению также может обеспечить статистически значимое (р 0,05) уменьшение уровней глюкозы в сыворотке крови. В описании настоящего изобретения состояние, которое лечат, представляет собой нарушение толерантности к глюкозе, гипергликемию, осложнения сахарного диабета, такие как сахарные катаракты,диабетическая нейропатия, диабетическая нефропатия, диабетическая ретинопатия и диабетическая кардиомиопатия, нервную анорексию, булимию, кахексию, гиперурикемию, гиперинсулинемию, гиперхолестеринемию, гиперлипидемию, дислипидемию, смешанную дислипидемию, гипертриглицеридемию,неалкогольную жировую печень, атеросклероз, артериосклероз, острую сердечную недостаточность, застойную сердечную недостаточность, ишемическую болезнь сердца, кардиомиопатию, инфаркт миокарда, стенокардию, гипертензию, гипотензию, инсульт, ишемию, ишемическое реперфузионное повреждение, аневризму, рестеноз, сосудистый стеноз, солидные опухоли, рак кожи, меланому, лимфому, рак молочной железы, рак легкого, колоректальный рак, рак желудка, рак пищевода, рак поджелудочной железы, рак предстательной железы, рак почки, рак печени, рак мочевого пузыря, рак шейки матки, рак мат- 22023517 ки, рая семенника и рак яичника. Настоящее изобретения также относится к терапевтическим способам лечения вышеописанных состояний у млекопитающего, включающего человека, где соединение формулы I по изобретению вводят в качестве компонента подходящей схемы введения доз с получением преимущества терапии. Подходящая схема введения доз, количество каждой вводимой дозы и интервалы между дозами соединения зависят от используемого соединения формулы (I) по изобретению, типа используемой фармацевтической композиции, показателей субъекта, которого лечат, и тяжести состояния. Как правило, эффективная доза соединений по настоящему изобретению находится в диапазоне от 0,01 до 30 мг/кг/сутки, предпочтительно от 0,01 до 5 мг/кг/сутки активного соединения в виде разовой или дробных доз. Тем не менее, может потребоваться некоторая вариабельность в общем диапазоне доз в зависимости от возраста и массы субъекта, которого лечат, предполагаемого пути введения, конкретного вводимого соединения и т.п. Определение схемы введения доз и оптимальных доз для конкретного пациента находится в пределах знаний специалиста в данной области техники с учетом преимуществ от настоящего описания. Практическим врачам понятно, что "кг" относится к массе пациента, измеряемой в килограммах. Соединения или композиции по изобретению могут быть введены в виде разовой (например, один раз в сутки) или дробных доз или путем постоянной инфузии. Соединения по изобретению также могут быть введены самостоятельно или в комбинации с фармацевтически приемлемыми носителями, растворителями или разбавителями в разовых или дробных дозах. Подходящие фармацевтические носители,растворители и разбавители включают инертные твердые разбавители или наполнители, стерильные водные растворы и различные органические растворители. Соединения или композиции по настоящему изобретению могут быть введены субъекту, нуждающемуся в лечении, посредством различных путей введения, включая пероральный и парентеральный(например, внутривенный, подкожный или интрамедуллярный) пути. Дополнительно, фармацевтические композиции по изобретению могут быть введены интраназально, в виде суппозитория или с использованием "флэш" композиции, т.е. возможность для растворения лекарственного средства во рту без необходимости использовать воду. Также следует отметить, что соединения по настоящему изобретению могут быть использованы в композициях с длительным высвобождением, контролируемым высвобождением и замедленным высвобождением, которые также хорошо известны специалистам в данной области техники. Соединения по изобретению также могут быть использованы в сочетании с другими фармацевтическими агентами для лечения описанных здесь заболеваний, состояний и/или расстройств. Таким образом,также раскрыты способы лечения, включающие введение соединений по настоящему изобретению в комбинации с другими фармацевтическими агентами. Подходящие фармацевтические агенты, которые могут быть использованы в комбинации с соединениями по настоящему изобретению, включают агенты против ожирения (включая агенты, подавляющие аппетит), противодиабетические агенты, антигипергликемические агенты, гиполипидемиечские агенты и антигипертензивные агенты. Подходящие противодиабетические агенты включают ингибитор ацетил-СоА карбоксилазы-2(АСС-2), ингибитор диацилглицерол-О-ацилтрансферазы 1 (DGAT-1), ингибитор фосфодиэстеразы(PDE)-10, сульфонилмочевину (например, ацетогексамид, хлорпропамид, диабинез, глибенкламид,глипизид, глибурид, глимепирид, гликлазид, глипентид, гликвидон, глизоламид, толазамид и толбутамид), меглитинид, ингибитор -амилазы (например, тендамистат, трестатин и AL-3688), ингибитор глюкозид гидролазы (например, акарбоза), ингибитор -глюкозидазы (например, адипозин, камиглибоза,эмиглитат, миглитол, воглибоза, прадимицин-Q и сальбостатин), агонист PPARyyyy (рецептора, активируемого пролифератором пероксисом) (например, балаглитазон, циглитазон, дарглитазон, энглитазон,изаглитазон, пиоглитазон, розиглитазон и троглитазон), агонист PPAR / (например, CLX-0940, GW1536, GW-1929, GW-2433, KRP-297, L-796449, LR-90, МК-0767 и SB-219994), бигуанид (например, метформин), агонист глюкагоноподобного пептида 1 (GLP-1) (например, эксендин-3 и эксендин-4), ингибитор белка тирозинфосфатазы-1 В (РТР-1B) (например, тродусквемин, экстракт гиртиозал и соединения,раскрытые Zhang, S., et al., Drug Discovery Today, 12(9/10), 373-381 (2007, ингибитор SIRT-1 (например,ресвератрол), ингибитор дипептидил пептидазы IV (DPP-IV) (например, ситаглиптин, вилдаглиптин,алоглиптин и саксаглиптин), ингибитор SGLT1 (натрий-зависимый переносчик глюкозы), ингибиторSGLT2 (например, дапаглифлозин, ремоглифлозин, серглифлозин и AVE2268), агент, усиливающий секрецию инсулина, ингибитор окисления жирных кислот, антагонист А 2, ингибитор c-jun аминоконцевой киназы (JNK), инсулин, инсулиновый миметик, ингибитор гликогенфосфорилазы и агонист рецептораVPAC2. Предпочтительные противодиабетические агенты для комбинированных аспектов представляют собой метформин, ингибитор SGLT2 (например, дапаглифлозин, ремоглифлозин, серглифлозин иAVE2268) и ингибиторы DPP-IV (например, ситаглиптин, вилдаглиптин, алоглиптин и саксаглиптин). Предпочтительные комбинации включают соединения формулы I с метформином и ингибитор DPP-IV или с метформином и ингибитором SGLT2. Подходящие агенты против ожирения включают ингибиторы 110-гидроксистероиддегидрогеназы-1(11-HSD тип I), ингибитор стеароил-СоА десатуразы-1 (SCD-1), агонисты MCR-4, агонисты холецистокинина-А (CCK-А), ингибиторы обратного захвата моноамина (такие как сибутрамин), симпатомиметики, 3-адренергические агонисты, дофаминовые агонисты (таких как бромкриптин), аналоги меланоцитстимулирующего гормона, агонисты 5 НТ 2 с (5-гидрокситриптамин), антагонисты меланинконцентрирующего гормона, лептин (белок ОВ), лептиновые аналоги, лептиновые агонисты, галаниновые антагонисты, ингибиторы липазы (такие как тетрагидролипстатин, т.е. орлистат), аноректические агенты (такие как агонист бомбезина), антагонисты нейропептида-Y (например, антагонисты NPY Y5), PYY3-36 (включая его аналоги), тиреомиметики, дегидроэпиандростерон или его аналог, глюкокортикоидные агонисты или антагонисты, орексиновые антагонисты, агонисты глюкагоноподобного пептида-1, цилиарные нейтротрофические факторы (такие как Axokine, доступный от Regeneron Pharmaceuticals, Inc., Tarrytown,NY and ProcterGamble Company, Cincinnati, ОН), ингибиторы человеческого агути-связанного пептида(AGRP), грелиновые антагонисты, антагонисты или обратные агонисты гистамина 3, агонисты нейромедина U, ингибиторы МТР/АроВ (например, селективные для кишечника МТР (микросомальный переносящий белок) ингибиторы, такие как дирлотапид), опиоидный антагонист, орексиновый антагонист и т.п. Предпочтительные агенты против ожирения для применения в комбинированных аспектах по настоящему изобретению включают селективные для кишечника МТР ингибиторы (например, дирлотапид,митратапид и имплитапид, R56918 (CAS No. 403987) и CAS No. 913541-47-6), агонисты ССКа (холецистокинина А) (например, N-бензил-2-[4-(1-индол-3-илметил)-5-оксо-1-фенил-4,5-дигидро-2,3,6,10bтетрааза-бензо[е]азулен-6-ил]-N-изопропил-ацетамид, описанный в публикации РСТWO 2005/116034 или публикации США 2005-0267100 A1), агонисты 5 НТ 2 с (например, лоркасерин), агонист MCR4(например, соединения, описанные в патенте США 6818658), липазный ингибитор (например, цетилистат), PYY3-36 (используемый здесь "PYY3-36" включает аналоги, такие как ПЭГилированный PYY3-36,например, описанный в публикации США 2006/0178501), опиоидные антагонисты (например, налтрексон), олеоил-эстрон (CAS180003-17-2), обинепитид (ТМ 30338), прамлинтид (Symlin), тезофензин(NS2330), лептин, лираглутид, бромкриптин, орлистат, экзеенатид (Byetta), AOD-9604 (CAS22123110-3) и сибутрамин. Предпочтительно соединения по настоящему изобретению и комбинированные терапевтические композиции вводят в сочетании с физическими упражнениями и рациональной диетой. Все приведенные выше патенты США и публикации включены сюда путем ссылки. Воплощения настоящего изобретения проиллюстрированы в следующих примерах. Тем не менее,понятно, что воплощения изобретения не ограничены конкретными деталями этих примеров, поскольку известны другие их вариации или они станут понятны в свете настоящего описания специалистам в данной области техники. Примеры Если не указано иное, то исходные вещества, как правило, доступны из коммерческих источников,таких как Aldrich Chemicals Co. (Milwaukee, WI), Lancaster Synthesis, Inc. (Windham, NH), Acros OrganicsVarian Inc., Palo Alto, CA) при комнатной температуре при 400 МГц для протона. Химические сдвиги выражены в миллионных доляхотносительно остаточного растворителя в качестве внутреннего стандарта. Формы пиков обозначены следующим образом: s, синглет; d, дублет; dd, двойной дублет; t, триплет; q, квартет; m, мультиплет; bs, широкий синглет; 2s, два синглета. Масс-спектры с химической ионизацией при атмосферном давлении (APCI) регистрировали на спектрометре Fisons Platform II (газноситель: ацетонитрил: доступен из Micromass Ltd, Manchester, UK). Масс-спектры с химической ионизацией (CI) получали на приборе Hewlett-Packard 5989 (ионизация аммиаком, PBMS: доступен изHewlett-Packard Company, Palo Alto, CA). Масс-спектры с ионизацией путем распыления электронов (ES) получали на приборе Waters ZMD (газ-носитель: ацетонитрил: доступен из Waters Corp., Milford, MA). Масс-спектры высокого разрешения (HRMS) получены на Agilent Model 6210 с использованием способа времяпролетной масс-спектрометрии. Когда описана интенсивность хлор-или бромсодержащих ионов, тогда обнаружено ожидаемое отношение интенсивностей (приблизительно 3:1 для 35Cl/37Clсодержащих ионов и 1:1 для 79Br/81Br-содержащих ионов) и приведена интенсивность только меньшего масс-иона. В некоторых случаях приведены только типичные пики 1H ЯМР. Оптические вращения определяли на поляриметре PerkinElmer 241 (доступен из PerkinElmer Inc., Wellesley, MA) с использованием натриевой D-линии (=589 нм) при указанной температуре и представлены следующим образом[]Dtemp, концентрация (с=г/100 мл) и растворитель. Колоночную хроматографию осуществляли с использованием силикагеля Baker (40 мкм; J.T.Baker, Phillipsburg, NJ) или Silica Gel 50 (EM Sciences, Gibbstown, NJ) в стеклянных колонках или в колонках Flash 40 Biotage (ISC, Inc., Shelton, CT), или картриджах Biotage SNAP KPsil или Redisep Rfsilica (от Teledyne Isco) при низком давлении азота. Хиральную SFC (суперкритическая жидкостная- 24023517 хроматография) осуществляли на указанных хиральных колонках. Некоторые растворители и реагенты могут быть названы с использованием общепринятых сокращений, таких как, например, DCM для дихлорметана, DMF для диметилформамида, EtOH для этанола,EtOAc для этилацетата и МеОН для метанола. Получение исходных веществ и промежуточных соединений Следующие исходные материалы доступны из соответствующих источников: (Z)-N-(3(диметиламино)-2-(трифторметил)аллилиден)-N-метилметанаминий гексафторфосфат - Anichem LLC(East Brunswick, NJ, USA); 3-(трифторметил)-1H-1,2,4-триазол - Beta Pharma Inc. (Branford, CT, USA); 2 метил-4-(трифторметил)-1 Н-имидазол - APAC Pharmaceutical LLC (Columbia, MA, USA); этил 2 хлорпиримидин-5-карбоксилат - Ark Pharm Inc. (Libertyville, IL, USA); 2-циклопропилацетальдегид - Anichem LLC (North Brunswick, NJ, USA); 4-хлор-3-метил-1 Н-пиразол - Oakwood Products, Inc. (West Columbia, SC, USA); 2-(1H-пиразол-4-ил)пиридин - Oakwood Products, Inc. (West Columbia, SC, USA) и 4 этил-3-метил-1H-пиразол - Aces Pharma, Inc. (Branford, CT, USA). Получение промежуточных соединений Промежуточное соединение (1). (4-(4-(Трифторметил-1H-пиразол-1-ил)фенил)метанол Смесь (4-йодфенил)метанола (1030 мг, 4,41 ммоль), 4-(трифторметил)-1 Н-пиразола (600 мг, 4,41 ммоль), йодида меди(I) (168 мг, 0,882 ммоль), транс-4-гидрокси-L-пролина (231 мг, 1,76 ммоль) и карбоната цезия (2900 мг, 8,82 ммоль) в диметилсульфоксиде (7,5 мл) нагревали до 85 С в течение 20 ч. Смесь разбавляли водой и дважды экстрагировали этилацетатом. Объединенные органические слои сушили над сульфатом натрия, фильтровали и концентрировали. Очистка путем колоночной хроматографии (0-45% этилацетат в гептане) позволила получить (4-(4-(трифторметил)-1H-пиразол-1-ил)фенил)метанол. 1 Н ЯМР (400 МГц, CDCl3, ): 8.16 (s, 1H), 7.89 (s, 1H), 7.65 (d, J=8,39 Гц, 2H), 7.47 (d, J=8,39 Гц, 2H), 4.74 (d,J=5,66 Гц, 2H), 1.85 (t, J=5,86 Гц, 1 Н). Промежуточное соединение (2). 4-(4-(Трифторметил)-1H-пиразол-1-ил)бензальдегид Смесь промежуточного соединения (1) (230 мг, 0,95 ммоль), диметилсульфоксида (1,35 мл) и триэтиламина (0,662 мл, 4,75 ммоль) в дихлорметане (3,5 мл) охлаждали до 0 С. Порциями добавляли комплекс триоксида серы с пиридином (0,454 г, 2,85 ммоль), и смесь перемешивали при 0 С в течение 2 ч. Реакционную смесь разбавляли этилацетатом, промывали насыщенным хлоридом аммония и рассолом,сушили над сульфатом натрия, фильтровали и концентрировали с получением 4-(4-(трифторметил)-1Hпиразол-1-ил)бензальдегида. 1 Н ЯМР (400 МГц, CDCl3, ): 10.04 (s, 1H), 8.29 (s, 1H), 7.99-8.05 (m, 2H),7.95 (s, 1H), 7.87-7.92 (m, 2H). Промежуточное соединение (3). 1-(2-Метил-4-нитрофенил)-4-(трифторметил)-1 Н-имидазол Смесь 4-(трифторметил)-1 Н-имидазола (198 мг, 1,46 ммоль), 1-фтор-2-метил-4-нитробензола (216 мг, 1,53 ммоль) и карбоната калия (402 мг, 2,91 ммоль) в ацетонитриле (1,5 мл) нагревали до 85 С в течение 24 ч. Смесь разбавляли водой и насыщенным хлоридом аммония, и дважды экстрагировали этилацетатом. Объединенные органические слои сушили над сульфатом натрия, фильтровали и концентрировали. Очистка путем колоночной хроматографии (0-50% этилацетат в гептане) позволила получить 1-(2 метил-4-нитрофенил)-4-(трифторметил)-1 Н-имидазол. 1 Н ЯМР (500 МГц, CDCl3, ): 8.30 (d, J=2,44 Гц,1H), 8.21-8.25 (m, 1H), 7.70 (s, 1H), 7.45-7.49 (m, 2H), 2.38 (s, 3H). В смесь промежуточного соединения (3) (325 мг, 1,20 ммоль) и 10 мас.% палладия на углероде (40 мг) в этаноле (6 мл) нагнетали до 48 фунт/кв.дюйм (330900 Па) водород и встряхивали в течение 6 ч. Смесь фильтровали через целит, промывали этилацетатом и метанолом. Фильтрат концентрировали с получением 3-метил-4-(4-(трифторметил)-1 Н-имидазол-1-ил)бензоламина. 1 Н ЯМР (500 МГц, CDCl3, ): 7.56 (s, 1H), 7.32 (s, 1H), 7.01 (d, J=8,54 Гц, 1H), 6.62 (d, J=2,68 Гц, 1H), 6.57 (dd, J=8,29, 2,44 Гц, 1H), 3.85 При -40 С изопропилмагний хлорид литий хлорид (15,3 мл, 1,3 M в THF (тетрагидрофуран), 19,9 ммоль) по каплям добавляли к раствору этил-4-йодбензоата (5000 мг, 18,11 ммоль) в тетрагидрофуране(30 мл). Раствор перемешивали при -40 С в течение 40 мин. Добавляли масляный альдегид (1830 мг, 25,4 ммоль). Смесь оставляли нагреваться до комнатной температуры в течение 3 ч. Реакционную смесь гасили 1 н. HCl и трижды экстрагировали этилацетатом. Объединенные органические слои сушили над сульфатом натрия, фильтровали и концентрировали с получением этил 4-(1-гидроксибутил)бензоата. 1 Н ЯМР(400 МГц, CDCl3, ): 8.02 (d, J=8,6 Гц, 2 Н), 7.41 (d, J=8,0 Гц, 2 Н), 4.83-4.66 (m, 1H), 4.38 (q, J=7,2 Гц, 2 Н),1.86 (d, J=3,7 Гц, 1H), 1.83-1.61 (m, 2H), 1.51-1.42 (m, 1H), 1.39 (t, J=7,2 Гц, 3 Н), 1.36-1.23 (m, 1H), 0.94 (t,J=7,6 Гц, 3 Н). Смесь неочищенного спирта (1,0 г, 4,5 ммоль) в дихлорметане (16,7 мл), диметилсульфоксид (4,79 мл) и триэтиламин (2,28 г, 22,5 ммоль) охлаждали до 0 С. Порциями добавляли комплекс триоксида серы с пиридином (2,15 г, 13,5 ммоль), и смесь перемешивали при 0 С в течение 1 ч. Реакционную смесь затем оставляли нагреваться до комнатной температуры и перемешивали в течение 2 ч. Реакционную смесь гасили рассолом и разбавляли дихлорметаном. Слои разделяли, и водный слой вновь экстрагировали дихлорметаном. Объединенные органические слои сушили над сульфатом натрия, фильтровали и концентрировали. Очистка путем колоночной хроматографии (0-30% этилацетат в гептане) позволила получить этил 4-бутирилбензоат. 1 Н ЯМР (400 МГц, CDCl3, ): 8.05-8.17 (m, 2H), 8.04-7.92 (m, 2H), 4.40 (q,J=7,15 Гц, 2H), 2.96 (t, J=7,22 Гц, 2H), 1.86-1.69 (m, 2H), 1.40 (t, J=7,12 Гц, 3 Н), 1.00 (t, J=7,22 Гц, 3H). Промежуточное соединение (6). 6-(4-(Трифторметил)-1 Н-имидазол-1-ил)пиридин-3-амин Смесь 4-(трифторметил)-1H-имидазола (2000 мг, 14,70 ммоль), 2-хлор-5-нитропиридина (2330 мг,14,70 ммоль) и карбоната калия (4060 мг, 29,4 ммоль) в ацетонитриле (14,7 мл) нагревали при 85 С в течение ночи. Реакционную смесь разбавляли водой и трижды экстрагировали этилацетатом. Объединенные органические слои промывали рассолом, сушили над сульфатом натрия, фильтровали и концентрировали. Неочищенный остаток растворяли в этаноле (20 мл) и этилацетате (15 мл). К раствору добавляли 10 мас.% палладия на углероде (500 мг). В смесь нагнетали до 50 фунт/кв.дюйм (344700 Па) водород и встряхивали в течение 5 ч. Реакционную смесь фильтровали через целит, промывали метанолом. Фильтрат концентрировали с получением 6-(4-(трифторметил)-1H-имидазол-1-ил)пиридин-3-амина. 1 Н ЯМР Фосфорил хлорид (18,0 мл, 200 ммоль) добавляли в капельной воронке в течение 30 мин к безводному диметилформамиду (40,0 мл) при 0 С. После завершения добавления светло-розовый раствор нагревали до комнатной температуры, и 3,3,3-трифторпропионовую кислоту (8,90 мл, 101 ммоль) по каплям добавляли в течение 10 мин. Раствор затем нагревали до 55 С и перемешивали в течение 4 ч при 55 С. Ярко-желтый раствор охлаждали до комнатной температуры и медленно добавляли в течение 30- 26023517 мин к охлажденному до 0 С раствору гексафторфосфата натрия (19,0 г, 110 ммоль) в воде (250 мл), поддерживая внутреннюю температуру ниже 10 С. Желтый осадок собирали путем вакуумного фильтрования и промывали охлажденной на льду водой (3X150 мл). Желтое твердое вещество сушили в вакууме и затем дважды подвергали азеотропной перегонке с толуолом и вновь сушили в вакууме с получением(Z)N-(3-(диметиламино)-2-(трифторметил)аллилиден)-N-метилметанаминий гексафторфосфата (V) в виде желтого твердого вещества (22,0 г, 64%). 1 Н ЯМР (400 МГц, CD3CN, ): 7.72 (s, 2H), 3.41 (s, 6H), 3.23 (d,J=1,4 Гц, 6H). Промежуточное соединение (7B). 1-(4-Бром-2.6-диметилфенил)гидразин хлоргидрат В трехгорлую круглодонную колбу объемом 3 л, оборудованную магнитной мешалкой, добавляли концентрированную соляную кислоту (125 мл) и воду (250 мл). Медленно при 0 С добавляли 4-бром-2,6 диметилбензоламин (100 г, 500 ммоль). Перемешивание продолжали в течение еще 15 мин, получая в результате густую белую суспензию. К суспензии по каплям добавляли свежеприготовленный раствор нитрита натрия (34,5 г, 500 ммоль) в воде (100 мл), поддерживая внутреннюю температуру ниже 5 С. После перемешивания в течение 30 мин образовывался темно-оранжевый раствор. По каплям добавляли олова (II) хлорид дегидрат (282 г, 1250 ммоль) в 1:1 концентрированную соляную кислоту: воду (300 мл),поддерживая внутреннюю температуру между 0-5 С. Образующуюся в результате смесь перемешивали при 0 С в течение 1 ч и затем нагревали до комнатной температуры и перемешивали в течение 15 ч. Реакционную смесь фильтровали и промывали диэтиловым эфиром. Твердое вещество медленно добавляли к водному 10 M раствору гидроксида натрия (1 л) при температуре 0-10 С и экстрагировали этилацетатом (3 Х 800 мл). Органический слой дважды промывали рассолом, сушили над безводным сульфатом натрия и концентрировали с получением 1-(4-бром-2,6-диметилфенил)гидразина (76,0 г, 353 ммоль). Гидразин растворяли в этилацетате (800 мл), к которому добавляли соляную кислоту/метанол (88,2 мл). Смесь перемешивали в течение 25 мин. Реакционную смесь фильтровали, промывали этилацетатом до тех пор, пока твердое вещество не становилось белым. Белое твердое вещество сушили в вакууме с получением 1-(4-бром-2,6-диметилфенил)гидразина хлоргидрата (80,0 г, 64%). 1 Н ЯМР (400 МГц, DMSO(3000 мг, 8,819 ммоль) и 1-(4-бром-2,6-диметилфенил)гидразин хлоргидрат (2480 мг, 9,84 ммоль) суспендировали в тетрагидрофуране. Суспензию охлаждали до 0 С. Натрий метоксид (551 мг, 9,7 ммоль) одной порцией добавляли в виде твердого вещества. Ледяную баню удаляли, и смесь нагревали до комнатной температуры и перемешивали в течение 48 ч. Затем при комнатной температуре добавляли трифторуксусную кислоту (3 мл). Реакционную смесь нагревали до 80 С в течение 5 ч, разбавляли этилацетатом и дважды промывали насыщенным бикарбонатом натрия. Объединенные водные промывки экстрагировали этилацетатом. Объединенные органические слои промывали рассолом, сушили над сульфатом натрия, фильтровали и концентрировали. Очистка путем колоночной хроматографии (0-20% этилацетат в гептане) позволила получить 1-(4-бром-2,6-диметилфенил)-4-(трифторметил)-1H-пиразол в виде масла. 1 Н ЯМР (400 МГц, CDCl3, ): 7.93 (s, 1H), 7.71 (s, 1H), 7.31 (s, 2H), 1.99 (s, 6H). Промежуточное соединение (8). 3,5-Диметил-4-(4-(трифторметил)-1 Н-пиразол-1-ил)бензоламин Флакон, содержащий промежуточное соединение (7) (1200 мг, 3,76 ммоль), йодид меди(I) (143 мг,0,75 ммоль), транс-4-гидрокси-L-пролин (197 мг, 1,50 ммоль) и карбонат калия (1570 мг, 11,3 ммоль) продували азотом. Добавляли диметилсульфоксид (7,5 мл), а затем аммиак (3,73 мл, приблизительно 28% водный). Флакон запаивали и нагревали до 75 С в течение 20 ч. Реакционную смесь охлаждали до комнатной температуры, разбавляли водой и дважды экстрагировали этилацетатом. Объединенные органические слои сушили над сульфатом натрия, фильтровали и концентрировали с получением 3,5-диметил- 27023517 4-(4-(трифторметил)-1H-пиразол-1-ил) бензоламина. 1H ЯМР (400 МГц, CDCl3, ): 7.84 (s, 1H), 7.65 (s,1H), 6.37 (s, 2H), 3.82-3.47 (br s, 2H), 1.85 (s, 6H). MS (M+H+CH3CN): 297,2. Промежуточное соединение (9). (+/-)-Метил-4-(1-гидрокси-3-метилбутил)бензоат Раствор 4-формилбензойной кислоты метилового эфира (1,56 г, 9,50 ммоль) в тетрагидрофуране (53 мл) охлаждали до 0 С. Затем по каплям в течение 15 мин добавляли изобутилмагний хлорид (4,75 мл, 2 М в THF). Реакционную смесь перемешивали при 0 С в течение 1 ч. Ледяную баню удаляли, и реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 1 ч. Реакционную смесь гасили путем осторожного добавления 1 н. HCl. Реакционную смесь разбавляли водой и диэтиловым эфиром, и слои разделяли. Водный слой еще трижды экстрагировали диэтиловым эфиром. Объединенные органические вещества сушили над сульфатом магния, фильтровали и концентрировали. Очистка путем колоночной хроматографии (0-40% этилацетат в гептане) позволила получить (+/-)метил-4-(1-гидрокси-3-метилбутил)бензоат (404,6 мг, 19%) в виде прозрачного бесцветного масла. 1 Н ЯМР (400 МГц, CDCl3, ): 7.99 (d, J=8,2 Гц, 2 Н), 7.40 (d, J=8,2 Гц, 2 Н), 4.79 (br. s., 1H), 3.89 (s, 3 Н), 1.94 Промежуточное соединение (9) (404,6 мг, 1,820 ммоль) растворяли в дихлорметане (6,07 мл) и охлаждали до 0 С. Добавляли пиридиний хлорхромат (785 мг, 3,64 ммоль). Ледяную баню удаляли и реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 48 ч. Реакционную смесь разбавляли дихлорметаном и добавляли сульфат магния. Эту смесь перемешивали в течение 10 мин и затем фильтровали и концентрировали. Очистка путем колоночной хроматографии (030% этилацетат в гептане) позволила получить метил-4-(3-метилбутаноил)бензоат (363,7 мг, 91%) в виде прозрачного бесцветного масла. 1 Н ЯМР (400 МГц, CDCl3, ): 8.07-8.13 (m, 2H), 7.95-8.00 (m, 2H), 3.93 (s,3 Н), 2.82-2.86 (m, 2 Н), 2.28 (dt, J=13,4, 6,8 Гц, 1H), 0.99 (d, 6H). Промежуточное соединение (11). 4-Фтор-1-(4-нитрофенил)-1H-пиразол К раствору 4-фтор-1H-пиразола (250 мг, 2,90 ммоль) и карбоната калия (803 мг, 5,81 ммоль) в ацетонитриле (3 мл) добавляли 4-фторнитробензол (430 мг, 3,05 ммоль). Образующуюся в результате смесь перемешивали при 70 С в течение 2 ч. Реакционную смесь затем фильтровали и концентрировали. Очистка путем колоночной хроматографии позволила получить 4-фтор-1-(4-нитрофенил)-1 Н-пиразол (400 мг, 67%). 1 Н ЯМР (400 МГц, CDCl3, ): 8.34 (d, 2H), 7.91 (d, 1H), 7.81 (d, 2H), 7.67 (d, 1H). Промежуточное соединение (12). 4-(4-Фтор-1 Н-пиразол-1-ил)анилин В смесь промежуточного соединения (11) (200 мг, 0,965 ммоль) и 10 мас.% палладия на углероде(100 мг) в этаноле (10 мл) нагнетали до 15 фунт/кв.дюйм (103400 Па) водород и перемешивали при 35 С в течение ночи. Реакционную смесь фильтровали и концентрировали. Очистка путем колоночной хроматографии позволила получить 4-(4-фтор-1 Н-пиразол-1-ил)анилин (150 мг, 88%). 1 Н ЯМР (400 МГц,CDCl3, ): 7.65 (d, 1 Н), 7.50 (d, 1H), 7.37 (d, 2H), 6.72 (d, 2H), 3.76 (br s, 2H). К охлажденному до 0 С раствору 4-(трифторметил)-1H-пиразола (1 г, 7 ммоль) в N,Nдиметилформамиде (10 мл) добавляли 60 мас.% гидрид натрия (132 мг, 3,31 ммоль). Смесь перемешивали при 0 С в течение 30 мин. Добавляли 4-фторбензонитрил (979 мг, 8,08 ммоль), и реакционную смесь нагревали до 80 С в течение ночи. Добавляли насыщенный хлорид аммония, и смесь экстрагировали этилацетатом. Органический слой сушили над сульфатом натрия, фильтровали и концентрировали. Очистка путем колоночной хроматографии позволила получить 4-(4-(трифторметил)-1H-пиразол-1 ил)бензонитрил (1,2 г, 72%). 1 Н ЯМР (400 МГц, CD3OD, ): 8.84 (s, 1H), 7.96 (s, 1H), 7.95 (d, 2H), 7.78 (d,2H). Промежуточное соединение Во флакон для микроволнового реактора загружали промежуточное соединение (13) (300 мг, 1,26 ммоль) и тетрагидрофуран (5 мл). Добавляли изобутилмагний бромид (1,90 мл, 2 М в THF, 3,80 ммоль). Образующуюся в результате смесь нагревали до 100 С при микроволновом излучении в течение 1 ч. Смесь осторожно добавляли к раствору боргидрида натрия (95,7 мг, 2,53 ммоль) в метаноле (5 мл) при комнатной температуре. После перемешивания в течение 5 мин реакционную смесь концентрировали досуха. Очистка путем колоночной хроматографии позволила получить (+/-)-3-метил-1-(4-(4(трифторметил)-1H-пиразол-1-ил)фенил)бутан-1-амин (250 мг, 67%). 1 Н ЯМР (400 МГц, CD3OD, ): 8.69 К охлажденному до -20 С раствору промежуточного соединения 30 (1,28 г, 4,26 ммоль) в тетрагидрофуране (20 мл) добавляли изобутилмагний бромид (2,13 мл, 2 М в THF, 4,26 ммоль). Реакционную смесь нагревали до комнатной температуры и перемешивали в течение 5 ч. Добавляли насыщенный хлорид аммония, и смесь экстрагировали этилацетатом. Объединенные органические слои сушили над сульфатом магния, фильтровали и концентрировали. Очистка путем колоночной хроматографии позволила получить (+/-)-трет-бутил-3-(N-трет-бутил-4-(1-гидрокси-3-метилбутил)бензамидо)пропаноат (400 мг, 24%). 1 Н ЯМР (400 МГц, CD3OD, ): 7.45-7.43 (m, 2H), 7.35-7.33 (m, 2H), 4.73 (m, 1H), 3.62-3.58 (m,2H), 2.48-2.45 (m, 2H), 1.72-1.67 (m, 2 Н), 1.57 (s, 9 Н), 1.50-1.47 (m, 1 Н), 1.36 (s, 9H), 0.97-0.96 (m, 6H). Промежуточное соединение (16). (+/-)-Метил-4-(2-циклопропил-1-гидроксиэтил)бензоат К охлажденному до -40 С раствору метил-4-йодбензоата (0,39 г, 1,5 ммоль) в тетрагидрофуране (7,5 мл) по каплям добавляли изопропилмагний хлорид литий хлорид (1,5 мл, 1,3 M в THF, 1,95 ммоль). После перемешивания в течение 30 мин при -40 С по каплям добавляли 2-циклопропилацетальдегид (190 мг, 2,26 ммоль). Образующуюся в результате смесь затем перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь гасили насыщенным хлоридом аммония, и она распределялась между водой и этилацетатом. Слои разделяли, и водный слой вновь экстрагировали этилацетатом. Объединенные органические слои сушили над сульфатом натрия, фильтровали и концентрировали. Очистка путем колоночной хроматографии позволила получить (+/-)-метил-4-(2-циклопропил-1-гидроксиэтил)бензоат
МПК / Метки
МПК: C07D 231/18, C07D 249/08, C07D 233/61, C07D 233/70, C07D 207/34, C07D 231/12, C07D 261/08, C07D 231/56, C07D 233/84, C07D 233/64, C07D 231/14, C07D 231/16, C07D 233/68, C07D 249/06, C07D 231/54
Метки: рецептора, глюкагонового, модуляторы
Код ссылки
<a href="https://eas.patents.su/30-23517-modulyatory-glyukagonovogo-receptora.html" rel="bookmark" title="База патентов Евразийского Союза">Модуляторы глюкагонового рецептора</a>
Предыдущий патент: Арматурный элемент для заливки, состоящий из кольцевых частей, и арматура из таких элементов
Следующий патент: Профиль для облицовки откосов
Случайный патент: Способ регулирования газожидкостного двигателя внутреннего сгорания












