Гетероциклические ингибиторы глутаминилциклазы (qc, ec 2.3.2.5)
Номер патента: 22420
Опубликовано: 30.12.2015
Авторы: Демут Ханс-Ульрих, Хайзер Ульрих, Гэртнер Ульф-Торстен
Формула / Реферат
1. Соединение формулы (I)
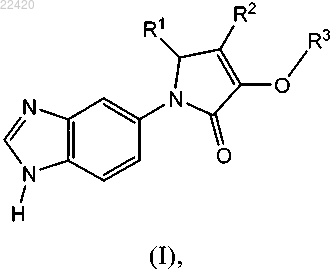
или его фармацевтически приемлемая соль или полиморф, включая все его стереоизомеры, в которой
R1 обозначает -C1-С6алкил, -C6-С8арил, -C3-С6циклоалкил, -хинолин, -C3-С6гетероциклил, -C3-С6циклоалкил, замещенный фенилом, -C3-С6циклоалкил, замещенный феноксигруппой, -фенил, замещенный C3-С6циклоалкилом, -фенил, замещенный фенилом, C3-С6гетероциклил, замещенный фенилом, фенил, замещенный C3-С6гетероциклилом, фенил, замещенный -O-C3-С6циклоалкилом, или фенил, замещенный
-C3-С6циклоалкил-C3-С6гетероциклилом,
где любой из вышеуказанных C3-С6гетероциклилов содержит один или два гетероатома, выбранных из N и О, где любая из вышеуказанных C6-С8арильных, C3-С6циклоалкильных, C3-С6гетероциклильных, фенильных или феноксигрупп необязательно может быть замещена 1, 2 или 3 группами, выбранными из C1-С6алкила и галогена;
R2 обозначает -С1-С6алкил, C1-С6галогеналкил, -C6-С8арил,
где вышеуказанная арильная группа необязательно может быть замещена 1, 2 или 3 группами галогена; и
R3 обозначает C1-С6алкил или С1-С6галогеналкил.
2. Соединение по п.1, в котором R1 обозначает -C1-С6алкил, -С6-С8арил, -С3-С6циклоалкил, -C3-С6циклоалкил, замещенный фенилом, -C3-С6циклоалкил, замещенный феноксигруппой, -фенил, замещенный C3-С6циклоалкилом, -фенил, замещенный фенилом, C3-С6гетероциклил, замещенный фенилом, фенил, замещенный C3-С6гетероциклилом, фенил, замещенный -O-C3-С6циклоалкилом, или фенил, замещенный -C3-С6циклоалкил-С3-С6гетероциклилом.
3. Соединение по п.2, в котором R1 обозначает -C1-С6алкил, -C6-С8арил, -С3-С6циклоалкил, -C3-С6гетероарил, -фенил, замещенный фенилом, фенил, замещенный C3-С6гетероциклилом, или фенил, замещенный -O-C3-С6циклоалкилом, где указанная фенильная группа необязательно замещена 1, 2 или 3 группами галогена, где указанная гетероциклильная группа необязательно замещена 1, 2 или 3 C1-С6алкильными группами и где указанная циклоалкильная группа необязательно замещена 1, 2 или 3 группами галогена.
4. Соединение по п.3, в котором R1 обозначает фенил, необязательно замещенный 1, 2 или 3 группами галогена, такой как 2,3-дифторфенил.
5. Соединение по одному из пп.1-4, в котором R2 обозначает метил, этил, пропил, изопропил, трифторметил или фенил, необязательно замещенный 1, 2 или 3 группами галогена.
6. Соединение по п.5, в котором R2 обозначает метил или незамещенный фенил.
7. Соединение по одному из пп.1-6, в котором R3 обозначает метил.
8. Соединение по одному из пп.1-7, в котором R3 обозначает 2,2,2-трифторэтил или 2,2,3,3-тетрафторпропил.
9. Соединение по одному из примеров 1-35 или его фармацевтически приемлемая соль или стереоизомер.
10. Соединение по п.1, которое представляет собой 1-(1H-бензо[d]имидазол-6-ил)-5-(2,3-дифторфенил)-3-метокси-4-метил-1H-пиррол-2(5H)-он или его фармацевтически приемлемую соль или полиморф.
11. Применение соединения по пп.1-10 в качестве лекарственного средства, обладающего ингибирующей активностью в отношении глутаминилциклазы.
12. Фармацевтическая композиция, содержащая соединение по одному из пп.1-10 в комбинации с одним или несколькими терапевтически приемлемыми разбавителями или носителями.
13. Фармацевтическая композиция по п.12, которая дополнительно содержит по меньшей мере одно соединение, выбранное из группы, включающей нейрозащитные средства, ингибиторы отложения амилоидного белка и ингибиторы синтеза бета-амилоида.
14. Фармацевтическая композиция по п.12 или 13, которая дополнительно содержит по меньшей мере одно соединение, выбранное из группы, включающей антитела к бета-амилоиду; ингибиторы ацетилхолинэстеразы (АСЕ), ингибиторы бета-секретаз, ингибиторы гамма-секретаз и антагонисты рецептора NMDA.
15. Применение соединения по одному из пп.1-10 или фармацевтической композиции по одному из пп.12-14 для лечения заболевания, выбранного из группы, включающей болезнь Кеннеди, рак двенадцатиперстной кишки, сопровождающийся или не сопровождающийся инфекциями Helicobacter pylori, колоректальный рак, синдром Золлигера-Эллисона, рак желудка, сопровождающийся или не сопровождающийся инфекциями Helicobacter pylori, патогенные психотические состояния, шизофрению, бесплодие, неоплазию, воспалительные ответы организма, рак, злокачественные метастазы, меланому, псориаз, нарушенные гуморальные и клеточно-опосредуемые иммунные ответы, процессы адгезии и миграции лейкоцитов в эндотелии, нарушенное всасывание пищи, нарушения сна-бодрствования, нарушенную гомеостатическую регуляцию энергетического метаболизма, нарушенную функцию вегетативной нервной системы, нарушенный гормональный баланс или нарушенную регуляцию жидкостей организма, рассеянный склероз, синдром Гийена-Барре и хроническую воспалительную демиелинизирующую полирадикулоневропатию.
16. Применение соединения по одному из пп.1-10 или фармацевтической композиции по одному из пп.12-14 для лечения заболевания, выбранного из группы, включающей умеренное когнитивное нарушение, болезнь Альцгеймера, семейную британскую деменцию, семейную датскую деменцию, нейродегенерацию при синдроме Дауна и болезнь Гентингтона.
17. Применение соединения по одному из пп.1-10 или фармацевтической композиции по одному из пп.12-14 для лечения заболевания, выбранного из группы, включающей ревматоидный артрит, атеросклероз, панкреатит и рестеноз.
18. Способ лечения или предупреждения заболевания, выбранного из группы, включающей болезнь Кеннеди, язвенное заболевание, рак двенадцатиперстной кишки, сопровождающийся или не сопровождающийся инфекциями Helicobacter pylori, колоректальный рак, синдром Золлигера-Эллисона, рак желудка, сопровождающийся или не сопровождающийся инфекциями Helicobacter pylori, патогенные психотические состояния, шизофрению, бесплодие, неоплазию, воспалительные ответы организма, рак, злокачественные метастазы, меланому, псориаз, нарушенные гуморальные и клеточно-опосредуемые иммунные ответы, процессы адгезии и миграции лейкоцитов в эндотелии, нарушенное всасывание пищи, нарушения сна-бодрствования, нарушенную гомеостатическую регуляцию энергетического метаболизма, нарушенную функцию вегетативной нервной системы, нарушенный гормональный баланс или нарушенную регуляцию жидкостей организма, рассеянный склероз, синдром Гийена-Барре и хроническую воспалительную демиелинизирующую полирадикулоневропатию, включающий введение субъекту соединения по одному из пп.1-10 или фармацевтической композицию по одному из пп.12-14 в эффективном количестве.
19. Способ лечения или предупреждения заболевания, выбранного из группы, включающей умеренное когнитивное нарушение, болезнь Альцгеймера, семейную британскую деменцию, семейную датскую деменцию, нейродегенерацию при синдроме Дауна и болезнь Гентингтона, включающий введение субъекту соединения по одному из пп.1-10 или фармацевтической композиции по одному из пп.12-14 в эффективном количестве.
20. Способ лечения или предупреждения заболевания, выбранного из группы, включающей ревматоидный артрит, атеросклероз, панкреатит и рестеноз, включающий введение субъекту соединения по одному из пп.1-10 или фармацевтической композиции по одному из пп.12-14 в эффективном количестве.
Текст
ГЕТЕРОЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ ГЛУТАМИНИЛЦИКЛАЗЫ (QC, EC 2.3.2.5) Изобретение относится к новым гетероциклическим производным формулы (I) в качестве ингибиторов глутаминилциклазы (QC, ЕС 2.3.2.5). QC катализирует внутримолекулярную циклизацию N-концевых глутаминовых остатков с образованием пироглутаминовой кислоты (5-оксопролил, pGlu) с выделением в свободном состоянии аммиака, и внутримолекулярную циклизацию N-концевых глутаматных остатков с образованием пироглутаминовой кислоты с выделением в свободном состоянии воды. Область техники, к которой относится изобретение Настоящее изобретение относится к новым гетероциклическим производным, являющимся ингибиторами глутаминилциклазы (QC, ЕС 2.3.2.5). Глутаминилциклаза (QC, ЕС 2.3.2.5) катализирует внутримолекулярную циклизацию N-концевых глутаминовых остатков с образованием пироглутаминовой кислоты (5-оксопролил, pGlu) с выделением в свободном состоянии аммиака и внутримолекулярную циклизацию N-концевых глутаматных остатков с образованием пироглутаминовой кислоты с выделением в свободном состоянии воды. Предпосылки создания изобретения Глутаминилциклаза (QC, ЕС 2.3.2.5) катализирует внутримолекулярную циклизацию N-концевых глутаминовых остатков с образованием пироглутаминовой кислоты (pGlu) с выделением в свободном состоянии аммиака. QC впервые была выделена Messer из латекса тропического растения Carica papaya в 1963 г. (Messer M., Nature 4874, 1963, с. 1299). Спустя 24 г соответствующая ферментативная активность была обнаружена в гипофизе животных (Busby W.H.J. и др., J Biol Chem 262, 1987, cc. 8532-8536; FischerGln в pGlu с помощью QC было обнаружено для предшественников TRH (тиреолиберин) и GnRH (гонадолиберин) (Busby W.H.J. и др., J Biol Chem 262, 1987, cc. 8532-8536; Fischer W.H. и Spiess J., Proc NatlAcad Sci USA 84, 1987, cc. 3628-3632). Кроме того, первые эксперименты по установлению локализацииQC позволили обнаружить ее совместную локализацию с предполагаемыми продуктами катализа в бычьем гипофизе, что является дополнительным доказательством ее функции в синтезе пептидных гормонов (Bockers Т.М. и др., J. Neuroendocrinol 7, 1995, cc. 445-453). В противоположность этому физиологическая функция растительной QC все еще остается невыясненной. Предполагается, что фермент из С.papaya играет роль в защите растений от патогенных микроорганизмов (El Moussaoui А. и др., Cell MolLife Sci 58, 2001, cc. 556-570). В настоящее время на основе сравнительного анализа последовательностей были выявлены предполагаемые QC из других растений (Dahl S.W. и др., Protein Expr Purif 20, 2000,cc. 27-36). Однако физиологическая функция этих ферментов все еще остается невыясненной. Известные выделенные из растений и животных QC обладают строгой специфичностью в отношении L-глутамина вN-концевом положении субстратов, и установлено, что их кинетические характеристики описываются уравнением Михаэлиса-Ментен (Pohl Т. и др., Proc Natl Acad Sci USA 88, 1991, cc. 10059-10063; ConsalvoA. P. и др., Anal Biochem 175, 1988, cc. 131-138; Gololobov M. Y. и др., Biol Chem Hoppe Seyler 377, 1996,cc. 395-398). Однако сравнение первичных структур QC из С. papaya и высококонсервативных QC млекопитающих не выявило никакой гомологии их последовательностей (Dahl S. W. и др., Protein Expr Purif 20, 2000, cc. 27-36). В то время как растительные QC, по-видимому, принадлежат к новому семейству ферментов (Dahl S. W. и др., Protein Expr Purif 20, 2000, cc. 27-36), было установлено, что QC млекопитающих обладают выраженной гомологией последовательностей с бактериальными аминопептидазами(Bateman R. С. и др., Biochemistry 40, 2001, cc. 11246-11250), это позволило сделать заключение о различном эволюционном происхождении QC из растений и QC из животных. В настоящее время установлено, что рекомбинантная человеческая QC, a также активность QC в экстрактах, выделенных из головного мозга, катализирует циклизацию как N-концевого глутаминила,так и глутамата. Более конкретно установлено, что для катализируемого циклазой Glu1-превращения оптимальным является значение pH, близкое к 6,0, а для Gln1-превращения в pGlu-производные оптимальным является значение pH, близкое к 8,0. Поскольку образование пептидов, родственных pGlu-A, можно подавлять путем ингибирования рекомбинантной человеческой QC и QC-активности, присутствующей в экстрактах, выделенных из гипофиза свиньи, то фермент QC является мишенью при разработке лекарственных средств, предназначенных для лечения болезни Альцгеймера. Ингибиторы QC описаны в WO 2004/098625, WO 2004/098591, WO 2005/039548, WO 2005/075436,WO 2008/055945, WO 2008/055947, WO 2008/055950 и WO 2008/065141. В заявке EP 02011349.4 описаны полинуклеотиды, кодирующие глутаминилциклазу насекомых, а также кодируемые ими полипептиды, и их применение в способах скрининга агентов, снижающих глутаминилциклазную активность. Такие агенты можно применять в качестве пестицидов. Определения Понятия "ki" или "KI" и "KD" относятся к константам связывания, которые характеризуют связывание ингибитора с ферментом и последующее отщепление от фермента. Другой мерой является значение"IC50", отражающее концентрацию ингибитора, которая при данной концентрации субстрата приводит к 50%-ному ингибированию активности фермента. Понятие "DPIV-ингибитор" или "ингибитор дипептидилпептидазы IV" хорошо известно специалисту в данной области и обозначает ингибиторы ферментов, которые ингибируют каталитическую активность DPIV или DPIV-подобных ферментов."DPIV-активность" представляет собой каталитическую активность дипептидилпептидазы IV(DPIV) и DPIV-подобных ферментов. Указанные ферменты представляют собой сериновые протеазы,производящие расщепление после остатка пролина (и в меньшей степени после аланина, после серина или после глицина), которые присутствуют в различных тканях организма млекопитающего, включая почки, печень и тонкий кишечник, где они обеспечивают высокоспецифичное удаление дипептидов с N-1 022420 конца биологически активных пептидов, если пролин или аланин являются остатками, примыкающими кN-концевой аминокислоте в последовательности указанных пептидов. Понятие "РЕР-ингибитор" или "ингибитор пролилэндопептидазы" хорошо известно специалисту в данной области и обозначает ингибиторы ферментов, которые ингибируют каталитическую активность пролилэндопептидазы (PEP, пролилолигопептидаза, POP)."РЕР-активность" представляет собой каталитическую активность эндопротеазы, которая обладает способностью гидролизовать присутствующие после пролина связи в пептидах или белках, в которых пролин находится в положении 3 или далее от N-конца аминокислотной последовательности пептида или белкового субстрата. Понятие "QC" в настоящем изобретении обозначает глутаминилциклазу (QC) и QC-подобные ферменты. QC и QC-подобные ферменты имеют идентичную или сходную ферментативную активность,обозначенную далее как QC-активность. Следует отметить, что QC-подобные ферменты могут принципиально отличаться от QC по своей молекулярной структуре. Примерами QC-подобных ферментов являются глутаминилпептидциклотрансфераза-подобные белки (QPCTL), присутствующие в организме человека (GenBank NM017659), мыши (GenBank BC058181), Масаса fascicularis (GenBank АВ 168255),Масаса mulatta (GenBank XM001110995), Canis familiaris (GenBank XM541552), RattUSnorvegicUS(GenBank XM001066591), MUSmusculUS(GenBank BC058181) и Bos taurUS(GenBankBT026254). В частности, понятие "QC-активность" в настоящем изобретении обозначает внутримолекулярную циклизацию N-концевых остатков глутамина с образованием пироглутаминовой кислоты (pGlu) или Nконцевого L-гомоглутамина или L-P-гомоглутамина с образованием циклического пирогомоглутаминового производного с выделением в свободном состоянии аммиака (см. ниже схемы 1 и 2). Схема 1. Циклизация глутамина с помощью QC Понятие "ЕС" в настоящем изобретении относится к активности QC и QC-подобных ферментов, таких как глутаматциклаза (ЕС), которая обозначена далее как ЕС-активность. Понятие "ЕС-активность" в настоящем изобретении обозначает внутримолекулярную циклизациюN-концевых глутаматных остатков с образованием пироглутаминовой кислоты (pGlu) с помощью QC(см. ниже схему 3). Схема 3. N-Концевая циклизация незаряженных глутамильных пептидов с помощью QC (ЕС) Понятие "QC-ингибитор" или "ингибитор глутаминилциклазы" хорошо известно специалисту в данной области и означает ингибиторы ферментов, которые ингибируют каталитическую активность глутаминилциклазы (QC) или активность глутамилциклазы (ЕС). Эффективность ингибирования ОС С точки зрения ингибирования QC в предпочтительных вариантах осуществления изобретения,способе и при медицинском применении используют агент, ингибирование которым QC характеризуется значением IC50, составляющим 10 мкм или менее, более предпочтительно 1 мкМ или менее, еще более предпочтительно 0,1 мкМ или менее, или 0,01 мкМ или менее, или наиболее предпочтительно 0,001 мкМ или менее. Фактически рассматриваются ингибиторы, для которых значения Ki находятся в нижнем микромолярном, предпочтительно в наномолярном и еще более предпочтительно в пикомолярном диапазоне. При этом, хотя представленные в настоящем описании активные агенты для удобства обозначены как"QC-ингибиторы", должно быть очевидно, что такая номенклатура не ограничивает рассматриваемое изобретение каким-либо конкретным механизмом действия. Молекулярная масса ингибиторов ОС В целом ингибиторы QC, которые используют в способе, предлагаемом в настоящем изобретении,или при медицинском применении, представляют собой небольшие молекулы, например с молекулярной массой 500 г/моль или менее, 400 г/моль или менее, предпочтительно 350 г/моль или менее, еще более предпочтительно 300 г/моль или менее, и даже 250 г/моль или менее. Понятие "субъект" в настоящем изобретении относится к животному, предпочтительно млекопитающему, наиболее предпочтительно человеку, которого подвергают лечению, наблюдению или экспериментальной обработке. Понятие "терапевтически эффективное количество" в настоящем изобретении означает количество действующего вещества или фармацевтического агента, вызывающее биологический или медицинский ответ в тканевой системе животного или человека, который требуется получить исследователю, ветеринару или врачу или другому клиницисту, включающий облегчение симптомов заболевания или нарушения, подлежащего лечению. В настоящем изобретении понятие "фармацевтически приемлемый" относится к применению как для лечения человека, так и в ветеринарии: например, к "фармацевтически приемлемым" относятся приемлемое для ветеринарии соединение или соединение, приемлемое для медицины и медико-санитарной помощи человеку. В настоящем изобретении, если специально не указано иное, понятие "алкил" обозначает C1 С 12 алкильную группу, предпочтительно C1-С 8 алкильную группу, например C1-С 12 алкильную группу,например C1-С 4 алкильную группу. Алкильные группы могут быть с прямой цепью или разветвленными. Пригодными алкильными группами являются, например метил, этил, пропил (например, н-пропил и изопропил), бутил (например, н-бутил, изобутил, втор-бутил и трет-бутил), пентил (например, н-петил), гексил (например, н-гексил), гептил (например н-гептил) и октил (например н-октил). Понятие "алк", например, используемое в понятиях "алкоксигруппа", "галогеналкил" и "тиоалкил"., следует интерпретировать в соответствии с понятием "алкил". Примерами алкоксигрупп являются метоксигруппа, этоксигруппа, пропоксигруппа (например, н-пропоксигруппа), бутоксигруппа (например, н-бутоксигруппа), пентоксигруппа (например, н-пентоксигруппа), гексоксигруппа (например, н-гексоксигруппа), гептоксигруппа(например н-гептоксигруппа) и октоксигруппа (например н-октоксигруппа). Примерами тиоалкильных групп являются метилтиогруппы. Примером галогеналкильных групп является фторалкильная группа,например, CF3. Понятие "алкенил", если специально не указано иное, обозначает C2-С 12 алкенильную группу, предпочтительно C2-С 6 алкенильную группу, например, C2-С 4 алкенильную группу, которая содержит по меньшей мере одну двойную связь в любом требуемом положении и которая не содержит никаких тройных связей. Алкенильные группы могут быть с прямой или разветвленной цепью. Примерами алкенильных групп, имеющих одну двойную связь, являются пропенил и бутенил. Примером алкенильных групп,имеющих две двойные связи, является пентадиенил, например (1E,3E)-пентадиенил. Понятие "алкинил", если не указано иное, обозначает C2-С 12 алкинильную группу, предпочтительноC2-С 6 алкинильную группу, например,C2-С 4 алкинильную группу, которая содержит по меньшей мере одну тройную связь в любом требуемом положении и которая может содержать также одну или несколько двойных связей или может не содержать их. Алкинильные группы могут быть с прямой или разветвленной цепью. Примерами алкенильных групп являются пропинил и бутинил. Понятие "алкилен" обозначает цепь формулы -(CH2)n-, в которой n представляет собой целое число,например, 2-5, если специально не указано иное. Понятие "циклоалкил", если специально не указано иное, обозначает C3-С 12 циклоалкильную группу(т.е. содержащую от 3 до 10 кольцевых атомов углерода), более предпочтительно C3-С 8 циклоалкильную группу, например, C3-С 6 циклоалкильную группу. Примерами циклоалкильных групп являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Наиболее предпочтительно количество кольцевых атомов углерода составляет от трех до шести. Понятие "гетероциклический", если специально не указано иное, обозначает карбоциклильную группу, в которой один или несколько (например, 1, 2 или 3) кольцевых атома замещены гетероатомами,выбранными из N, S или O. Конкретным примером гетероциклильной группы является циклоалкильная группа (например, циклопентил или более предпочтительно циклогексил), в которой один или несколько(например, 1, 2 или 3, предпочтительно 1 или 2, наиболее предпочтительно 1) кольцевых атома замещены гетероатомами, выбранными из N, S или O. Примерами гетероциклильных групп, содержащих один гетероатом, являются пирролидин, тетрагидрофуран и пиперидин, а примерами гетероциклильных групп, содержащих два гетероатома, являются морфолин, пиперазин, диоксолан и диоксан. Другим конкретным примером гетероциклильной группы является циклоалкенильная группа (например, циклогексинильная группа), в которой один или несколько (например, 1, 2 или 3, предпочтительно 1 или 2, наиболее предпочтительно 1) кольцевых атома замещены гетероатомами, выбранными из N, S или O. Примером такой группы является дигидропиранил (например, 3,4-дигидро-2H-пиран-2-ил-). Понятие "арил", если специально не указано иное, обозначает C6-С 12 арильную группу, предпочти-3 022420 тельно C6-С 10 арильную группу, более предпочтительно C6-С 8 арильную группу. Арильные группы могут содержать по меньшей мере одно ароматическое кольцо (например, одно, два или три кольца). Примером типичной арильной группы с одним ароматическим кольцом является фенил. Примером типичной арильной группы с двумя ароматическими кольцами является нафтил. Понятие "гетероарил", если специально не указано иное, обозначает арильный фрагмент, в котором один или несколько (например 1, 2, 3 или 4, предпочтительно 1, 2 или 3) кольцевых атома замещены гетероатомами, выбранными из N, S и O, или 5-членное ароматическое кольцо, содержащее один или несколько (например 1, 2, 3 или 4, предпочтительно 1, 2 или 3) кольцевых атома, выбранных из N, S и O. Примерами моноциклических гетероарильных групп, содержащих один гетероатом, являются: пятичленные кольца (например, пиррол, фуран, тиофен); и шестичленные кольца (например, пиридин, такой как пиридин-2-ил, пиридин-3-ил и пиридин-4-ил). Примерами моноциклических гетероарильных групп,содержащих два гетероатома, являются: пятичленные кольца (например, пиразол, оксазол, изоксазол,тиазол, изотиазол, имидазол, такой как имидазол-1-ил, имидазол-2-ил, имидазол-4-ил); шестичленные кольца (например, пиридазин, пиримидин, пиразин). Примерами моноциклических гетероарильных групп, содержащих три гетероатома, являются: 1,2,3-триазол и 1,2,4-триазол. Примером моноциклических гетероарильных групп, содержащих четыре гетероатома, является тетразол. Примерами бициклических гетероарильных групп являются: индол (например, индол-6-ил), бензофуран, бензтиофен, хинолин,изохинолин, индазол, бензимидазол, бензтиазол, хиназолин и пурин. Понятие "-алкиларил", если специально не указано иное, обозначает арильный остаток, который связан через алкиленовый остаток, например,C1-4 алкиленовый остаток. Понятие "-алкилгетероарил", если специально не указано иное, обозначает гетероарильный остаток,который связан через алкиленовый остаток, например, C1-4 алкиленовый остаток. Понятие "галоген" или "гало" включает фтор (F), хлор (Cl) и бром (Br). Понятие "амино" относится к группе -NH2. Понятие "фенил, замещенный фенилом" относится к бифенилу. Понятие обозначает простую связь, при этом стереохимия не определена. Когда бензимидазол представляет собой бензимидазол-5-ил, который изображают в виде то специалисту в данной области должно быть очевидно, что бензимидазол-6-ил, который изображают в виде имеет эквивалентную структуру. В настоящем описании обе формы бензимидазола обозначают одним понятием бензимидазол-5-ил". Стереоизомеры Под объем настоящего изобретения подпадают все возможные стереоизомеры соединений, предлагаемых в изобретении. Если соединения, предлагаемые в изобретении, имеют по меньшей мере один хиральный центр, то они могут находиться в виде энантиомеров. Если соединения имеют два или большее количество хиральных центра, то они могут кроме того находиться в виде диастереоизомеров. Следует иметь ввиду,что все такие изомеры и их смеси подпадают под объем настоящего изобретения. Получение и выделение стереоизомеров Если способы получения соединений, предлагаемых в изобретении, приводят к получению смеси стереоизомеров, эти изомеры можно разделять с помощью общепринятых методов, таких как препаративная хроматография. Соединения можно получать в рацемической форме или в виде индивидуальных энантиомеров с помощью либо энантиомерного синтеза, либо путем разделения. Соединения, например,можно разделять на компоненты-энантиомеры с помощью стандартных методов, таких как формирование диастереомерных пар посредством солеобразования с использованием оптически активной кислоты,такой как (-)-ди-пара-толуол-d-винная кислота и/или (+)-ди-пара-толуол-1-винная кислота с осуществлением последующей фракционированной кристаллизации и регенерации свободного основания. Соединения можно разделять также путем формирования диастереомерных сложных эфиров или амидов с последующим хроматографическим разделением и удалением хиральных вспомогательных веществ. В альтернативном варианте соединения можно разделять с использованием хиральной ЖХВР-колонки. Фармацевтически приемлемые соли Принимая во внимание близкое сходство соединений в свободной форме и соединений в форме их солей или сольватов, подразумевается, что когда в настоящем описании упоминается соединение, то при этом подразумевается также соответствующая соль, сольват или полиморф, при условии, что возможно их образование в конкретных условиях. Соли и сольваты соединений формулы (I) и их физиологически функциональные производные, пригодные для применения в медицине, представляют собой соединения, в которых противоион или связанный растворитель являются фармацевтически приемлемыми. Однако под объем настоящего изобретения подпадают также соли или сольваты, содержащие неприемлемые с фармацевтической точки зрения противоионы и связанные растворители, например в качестве промежуточных продуктов при получении других соединений и их фармацевтически приемлемых солей и сольватов. Пригодными солями, которые можно применять согласно настоящему изобретению, являются соли образованные как с органическими, так и с неорганическими кислотами или основаниями. К фармацевтически приемлемым кислотно-аддитивным солям относятся соли, образованные с такими кислотами как соляная, бромисто-водородная, серная, азотная, лимонная, винная, фосфорная, молочная, пировиноградная, уксусная, трифторуксусная, трифенилуксусная, сульфамовая, сульфаниловая, янтарная, щавелевая,фумаровая, малеиновая, яблочная, миндальная, глутамовая, аспарагиновая, щавелевоуксусная, метансульфоновая, этансульфоновая, арилсульфоновая (например паратолуолсульфоновая, бензолсульфоновая, нафталинсульфоновая или нафталиндисульфоновая), салициловая, глутаровая, глюконовая, трикарбаллиловая, коричная, замещенная коричная (например коричная кислота, замещенная фенилом, метилом, метоксигруппой или галогеном, включая 4-метил- и 4-метоксикоричную кислоту), аскорбиновая,олеиновая, нафтойная, гидроксинафтойная (например 1- или 3-гидрокси-2-нафтойная), нафталинакриловая (например нафталин-2-акриловая), бензойная, 4-метоксибензойная, 2- или 4-гидроксибензойная, 4 хлорбензойная, 4-фенилбензойная, бензолакриловая (например 1,4-бензолдиакриловая) кислота, изетионовые кислоты, перхлорная, пропионовая, гликолевая, гидроксиэтансульфоновая, памовая, циклогексансульфамовая, салициловая, сахариновая и трифторуксусная кислота. К фармацевтически приемлемым солям присоединения оснований относятся аммониевые соли, соли щелочных металлов, таких как натрий и калий, щелочно-земельных металлов, таких как кальций и магний, и соли присоединения органических оснований, таких как дициклогексиламин и N-метил-D-глюкамин. Подразумевается, что все соединения, предлагаемые в настоящем изобретении, в форме фармацевтически приемлемых кислотно-аддитивных солей подпадают под объем настоящего изобретения. Полиморфные кристаллические формы Кроме того, некоторые кристаллические формы соединений могут существовать в виде полиморфов, и они подпадают под объем настоящего изобретения. Дополнительно, некоторые соединения могут образовывать также сольваты с водой (т.е. гидраты) или с обычными органическими растворителями, и подразумевается, что такие сольваты также подпадают под объем настоящего изобретения. Соединения,включая их соли, можно получать также в форме их гидратов, или в форме, включающей другие растворители, применяемые для кристаллизации. Пролекарства Кроме того, под объем настоящего изобретения подпадают пролекарства соединений, предлагаемых здесь. Как правило, такие пролекарства представляют собой функциональные производные соединений, которые легко превращаются in vivo в требуемое обладающее терапевтической активностью соединение. Таким образом, в этих случаях подразумевается, что в способах лечения, предлагаемых в настоящем изобретении, понятие "введение" включает лечение различных указанных нарушений с помощью представляющих собой пролекарства вариантов одного или нескольких заявленных соединений,которые превращаются в указанное выше соединение in vivo после введения субъекту. Стандартные процедуры выбора и получения пригодных производных, представляющих собой пролекарства, описаны,например в "Design of Prodrugs", под ред. Н. Bundgaard, изд-во Elsevier, 1985. Защитные группы В процессе получения соединений, предлагаемых в настоящем изобретении, может оказаться необходимым и/или целесообразным защищать чувствительные или реактивные группы на любых рассматриваемых молекулах. Это можно осуществлять с использованием стандартных защитных групп, таких,которые описаны в Protective Groups in Organic Chemistry, под ред. J.F.W. McOmie, изд-во Plenum Press,1973; и у T.W. GreeneP.G.M. Wuts, Protective Groups in Organic Synthesis, изд-во John WileySons,1991, указанные публикации полностью включены в настоящее описание в качестве ссылки. Защитные группы можно удалять на соответствующей последующей стадии с помощью методов, известных в данной области. В настоящем изобретении подразумевается, что понятие "композиция" включает продукт, содержащий заявленные соединения в терапевтически эффективных количествах, а также любой продукт, который образуется непосредственно или опосредованно из комбинаций соединений, предлагаемых в настоящем изобретении. Носители и добавки для галеновых препаративных форм Для жидких препаратов, предназначенных для орального введения, таких, например, как суспензии,эликсиры и растворы, пригодные носители и добавки предпочтительно могут представлять собой воду,гликоли, масла, спирты, ароматизаторы, консерванты, красители и т.п.; для твердых препаратов, предназначенных для орального введения, таких, например, как порошки, капсулы, желатиновые капсулы и таблетки, пригодными носителями и добавками являются крахмалы, сахара, разбавители, агенты, способствующие грануляции, замасливатели, связующие вещества, разрыхлители и т.п. Носители, которые можно добавлять к смеси, содержат необходимые и инертные фармацевтические эксципиенты, включая (но не ограничиваясь только ими) пригодные связующие вещества, суспендирующие агенты, замасливатели, корригенты, подслащивающие вещества, консерванты, покрытия, разрыхлители, пигменты и окрашивающие вещества. К растворимым полимерам, которые можно применять в качестве носителей доставляемого к мишени лекарственного средства, относятся поливинилпирролидон, пирановый сополимер, полигидроксипропил-метакриламидофенол, полигидроксиэтиласпартамидфенол, или полиэтиленоксидполилизин, замещенный пальмитоильным фрагментом. Кроме того, соединения, предлагаемые в настоящем изобретении, можно соединять с классом биоразлагаемых полимеров, применяемых для достижения контролируемого высвобождения лекарственного средства, таких, например, как полимолочная кислота, полиэпсилонкапролактон, полигидроксимасляная кислота, сложные полиортоэфиры, полиацетали, полидигидропираны, полицианакрилаты и сшитые или амфипатические блок-сополимеры гидрогелей. Пригодными связующими веществами являются (но не ограничиваясь только ими) крахмал, желатин, натуральные сахара, такие как глюкоза или бета-лактоза, подслащивающие вещества из кукурузы,натуральные и синтетические камеди, такие как аравийская камедь, трагакант или олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п. В качестве разрыхлителей можно применять (но не ограничиваясь только ими) крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и т.п. Краткое изложение сущности изобретения Настоящее изобретение относится к соединению формулы (I) или его фармацевтически приемлемой соли или полиморфу, включая все его стереоизомеры, в которойR1 обозначает -С 1-С 6 алкил, -С 6-С 8 арил, -С 3-С 6 циклоалкил, -хинолин, -C3-С 6 гетероциклил, -C3-С 6 циклоалкил, замещенный фенилом, -C3-С 6 циклоалкил, замещенный феноксигруппой, -фенил, замещенный С 3-С 6 циклоалкилом, -фенил, замещенный фенилом, С 3-С 6 гетероциклил, замещенный фенилом, фенил, замещенный С 3-С 6 гетероциклилом, фенил, замещенный -O-С 3-С 6 циклоалкилом, или фенил, замещенный -C3-С 6 циклоалкил-С 3-С 6 гетероциклилом, где любой из вышеуказанных C3-С 6 гетероциклилов содержит один или два гетероатома, выбранных из N и О; и где любая из вышеуказанных C6-С 8 арильных, С 3-С 6 циклоалкильных, C3-С 6 гетероциклильных, фенильных или феноксигрупп необязательно может быть замещена 1, 2 или 3 группами, выбранными из C1 С 6 алкила и галогена;R2 обозначает -С 1-С 6 алкил, С 1-С 6 галогеналкил, -С 6-С 8 арил; и где вышеуказанная арильная группа необязательно может быть замещена 1, 2 или 3 группами галогена; иR3 обозначает C1-С 6 алкил или C1-С 6 галогеналкил. Подробное описание изобретения В том случае, когда циклоалкил и гетероциклил являются замещенными, они, как правило, замещены 1 или 2 заместителями (например, 1 заместителем). Как правило, заместитель представляет собой C1 С 6 алкил (например, метил) или галоген (например, хлор или фтор). Более предпочтительно циклоалкильные и гетероциклильные группы являются незамещенными. В том случае, когда арил и гетероарил являются замещенными, они, как правило, замещены 1, 2 или 3 (например, 1 или 2) заместителями. Заместители для арила и гетероарила выбирают из группы, включающей C1-С 6 алкил (например, метил), галоген (например, фтор, хлор, бром). Когда R1 или R2 обозначает арил, то арил предпочтительно обозначает необязательно замещенный фенил. Примерами замещенных фенильных групп, входящих в R1 или R2, являются 2-бромфенил, 2 бром-4-фторфенил-, 2-бром-5-фторфенил-, 2-фтор-5-бромфенил, 2-хлорфенил-, 2-фторфенил-, 3 хлорфенил-, 3-бромфенил-, 3-фторфенил-, 4-хлорфенил-, 4-фторфенил-, 4-бромфенил-, 4-бром-2 фторфенил, 2-хлор-3,6-дифторфенил), 2,3-дихлорфенил-, 2,3-дифторфенил-, 2,3,4-трифторфенил, 2,3,5 трифторфенил, 2,4-дихлорфенил-, 2,4-дифторфенил-, 2,4,6-трифторфенил-, 2,5-дихлорфенил-, 2,6 дихлорфенил-, 2,6-дифторфенил-, 3,4-дихлорфенил-, 3,4-дифторфенил-, 3,5-дифторфенил-, 2,4,5 трифторфенил-, 3,4,5-трифторфенил-, 2,4-диметилфенил-, 3-метилфенил-, 3,4-диметилфенил-, 4 метилфенил-,4-изопропилфенил-,4-трет-бутилфенил-,2,4,6-триметилфенил-,2-изопропил-6 метилфенил-, 2-(трифторметил)фенил-, 4-(трифторметил)фенил-, 2,4-бис(трифторметил)фенил-, 3,5-6 022420 бис(трифторметил)фенил-. В альтернативном варианте R2 может представлять собой незамещенный фенил-. Другими примерами замещенных фенильных групп являются 2,3-дифтор-4-метилфенил, 2-фтор-3(метил)фенил-, 4-хлор-3-метилфенил, 4-бром-4-этилфенил. Когда R1 или R2 обозначает циклоалкил, то циклоалкил предпочтительно представляет собой необязательно замещенный циклоалкил. Примерами циклоалкила являются циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Примерами замещенного карбоциклила являются 2 метилциклогексил-, 3-метилциклогексил-, 4-метилциклогексил- и 4,4-дифторциклогексил. Когда R1 или R2 обозначает гетероциклил (который необязательно может быть замещен), то его примерами могут служить тетрагидрофуранил, морфолинил, пиперидинил, 3,4-дигидро-2H-пиранил, тетрагидропиранил, пирролидинил, метилтетрагидрофуранил- (например, 5-метилтетрагидрофуран-2-ил-). Когда R1 обозначает фенил замещенный фенилом или фенил замещенный гетероциклилом (таким как моноциклический гетероциклил), в котором любая из вышеуказанных фенильных и гетероциклильных групп необязательно может быть замещена, то, как правило, фенильное кольцо, непосредственно связанное с атомом азота, является незамещенным и концевое фенильное кольцо или гетероциклильное кольцо необязательно замещено одним, двумя или тремя заместителями (например, одним или двумя,например, одним заместителем). Как правило, концевая фенильная или моноциклическая гетероциклильная группа является незамещенной. Как правило, концевая фенильная или моноциклическая гетероциклильная группа является заместителем в арильном кольце (т.е. в фениле) в положении 4. Когда R1 обозначает фенил, замещенный фенилом, в котором любая из вышеуказанных фенильных групп необязательно может быть замещена, то его примером может служить -бифенил-4-ил. Когда R1 обозначает фенил, замещенный моноциклической гетероциклильной группой, в котором любая из вышеуказанных фенильных и гетероциклильных групп необязательно может быть замещена, то его примерами являются 4-морфолинофенил-, 4-(пиперидин-1-ил)фенил-, 4-(1-метилпиперидин-4 ил)фенил- и 4-(тетрагидро-2H-пиран-4-ил)фенил-. Когда R1 обозначает -циклоалкил, замещенный фенилом, в котором любая из вышеуказанных циклоалкильных и фенильных групп необязательно может быть замещена, то его примером является 4 фенилциклогексил-. Когда R1 обозначает -циклоалкил, замещенный феноксигруппой, в котором любая из вышеуказанных циклоалкильных и феноксигрупп необязательно может быть замещена, то его примером является 4 феноксициклогексил-. Когда R1 обозначает -гетероциклил, замещенный фенилом, в котором любая из вышеуказанных фенильных и гетероциклильных групп необязательно может быть замещена, то его примером является 1 фенилпиперидин-4-ил-. Когда R1 обозначает фенил, замещенный -O-циклоалкилом, в котором любая из вышеуказанных фенильных и циклоалкильных групп необязательно может быть замещена, то его примером является 4 циклогексилоксифенил-. Когда R1 обозначает -фенил, замещенный циклоалкилом, в котором любая из вышеуказанных фенильных и циклоалкильных групп необязательно может быть замещена, то его примерами являются 4 циклогексилфенил- или 4,4-дифторциклогексилфенил-. Когда R1 обозначает фенил, замещенный -циклоалкилгетероциклилом, в котором любая из вышеуказанных фенильных, циклоалкильных и гетероциклильных групп необязательно может быть замещена,то его примером является (4-морфолиноциклогексил)фенил-. В одном из вариантов осуществления настоящего изобретения, R1 обозначает -C1-С 6 алкил (например, изопропил), -арил (например, фенил), -циклоалкил (например, циклогексил), - хинолинил,-циклоалкил, замещенный фенилом (например, -циклогексилфенил), -циклоалкил, замещенный феноксигруппой (например, -циклогексил-O-фенил), -фенил, замещенный циклоалкилом (например,-фенилциклогексил), -фенил, замещенный фенилом (например, -фенилфенил), гетероциклил, замещенный фенилом (например, -пиперидинилфенил), фенил, замещенный гетероциклилом (например,-фенилморфолинил, -фенилпиперидинил или -фенилтетрагидропиранил), фенил, замещенный -Oциклоалкилом (например, -фенил-O-циклогексил) или фенил, замещенный -циклоалкилгетероциклилом(например, -фенилциклогексилморфолинил); где фенильная группа необязательно замещена одной или несколькими группами галогена (например, фтором, бромом или хлором); где гетероциклильная группа необязательно замещена одной или несколькими C1-С 6 алкильными группами (например, метилом); и где циклоалкильная группа необязательно замещена одной или несколькими группами галогена (например,фтором). В другом варианте осуществления изобретения R1 обозначает -C1-С 6 алкил (например, изопропил),-арил (например, фенил), -циклоалкил (например, циклогексил), -хинолинил, -фенил, замещенный фенилом (например, -фенилфенил), фенил, замещенный гетероциклилом (например, -фенилморфолинил или-фенилпиперидинил) или фенил, замещенный -O-циклоалкилом (например, -фенил-O-циклогексил); где фенильная группа необязательно замещена одной или несколькими группами галогена (например, фтором, бромом или хлором). В следующем варианте осуществления изобретения, R1 обозначает -арил (например, фенил), необя-7 022420 зательно замещенный одной или несколькими группами галогена (например, фтором, бромом или хлором). Еще в одном варианте осуществления изобретения, R1 обозначает фенил, замещенный одной или несколькими группами, представляющими собой фтор (например, 2,3-дифторфенил). Предпочтительно, R2 обозначает -C1-С 6 алкил или -арил. В одном из вариантов осуществления настоящего изобретения R2 обозначает -C1-С 6 алкил (например, метил, этил, пропил или изопропил), C1-С 6 галогеналкил (например, трифторметил) или -арил (например, фенил); где фенильная группа необязательно замещена одной или несколькими группами галогена (например, фтором). В другом варианте осуществления настоящего изобретения, R2 обозначает -C1 С 6 алкил (например, метил, этил, пропил или изопропил) или -арил (например, фенил), необязательно замещенный одной или несколькими группами галогена (например, фтором). В следующем варианте осуществления настоящего изобретения, R2 обозначает метил или фенил, необязательно замещенный одной или несколькими группами, представляющими собой фтор. Еще в одном варианте осуществления настоящего изобретения R2 обозначает метил. Предпочтительно R3 обозначает C1-С 6 алкил. В одном из вариантов осуществления настоящего изобретения, R3 обозначает C1-С 6 алкил (например, метил или этил). В другом варианте осуществления настоящего изобретения, R3 обозначает C1 С 6 алкил (например, метил). Предпочтительно R3 обозначает C1-С 6 галогеналкил. В одном из вариантов осуществления настоящего изобретения, R3 обозначает C1-С 6 галогеналкил(например, 2,2,2-трифторэтил или 2,2,3,3-тетрафторпропил). В одном из вариантов осуществления настоящего изобретения, соединение формулы (I) представляет собой соединение, описанное в любом из примеров 1-32. или его фармацевтически приемлемую соль или полиморф, включая все стереоизомеры. В другом варианте осуществления настоящего изобретения, соединение формулы (I) представляет собой соединение, описанное в любом из примеров 1-35,или его фармацевтически приемлемую соль или полиморф, включая все стереоизомеры. В следующем варианте осуществления настоящего изобретения, соединение формулы (I) представляет собой 1-(1H-бензо[d]имидазол-6-ил)-5-(2,3-дифторфенил)-3-метокси-4-метил-1H-пиррол-2(5 Н)-он или его фармацевтически приемлемую соль или полиморф. Способы Другим объектом изобретения является способ получения соединения формулы (I), который включает:(а) получение соединения формулы (I) из соединения формулы (II) в которой R1 и R2 имеют значения, указанные выше для соединении формулы (I). Стадия способа(а), как правило, включает реакцию в диазометане в пригодном растворителе, таком как метанол. Неограничивающий пример осуществления стадии способа (а), приведен в настоящем описании как "Способ 1";(b) взаимное превращение соединений формулы (I); и/или(c) удаление защитных групп из защищенного соединения формулы (I). Соединения формулы (I) и промежуточные соединения можно получать также с помощью методик, аналогичным известных специалисту в данной области технике, или представленным в настоящем описании. В частности, соединения формулы (II) описаны в WO 2008/055945 или их можно получать аналогично методам, описанным вWO 2008/055945. Новые промежуточные продукты являются объектом настоящего изобретения. Терапевтическое применение Физиологическими субстратами для QC (ЕС) в организме млекопитающих являются, например,пептиды амилоида бета (3-40), (3-42), (11-40 и 11-42), ABri, ADan, гастрин, нейротензин, FPP, CCL 2,CCL 7, CCL 8, CCL 16, CCL 18, фракталкин, орексин A, [Gln3]-глюкагон(3-29), [Gln5]-субстанция Р(5-11) и пептид QYNAD. Более подробное описание указанных субстанций приведено в табл. 1. Соединения и/или комбинации, предлагаемые в настоящем изобретении, и фармацевтические композиции, содержащие по меньшей мере один ингибитор QC (ЕС), можно применять для лечения состояний, которые можно лечить путем модуляции QC-активности. Таблица 1. Аминокислотные последовательности обладающих физиологической активностью пептидов,содержащих N-концевой глутаминовый остаток, которые можно подвергать циклизации с получением в качестве конечного продукта pGlu Было установлено, что глутамат присутствует в положениях 3, 11 и 22 амилоидного -пептида. Кроме того, было описано, что мутация, заключающаяся в замене глутаминовой кислоты (E) на глутаминP05067), представляет собой мутацию, обусловливающую так называемый цереброартериальный амилоидоз датского типа. Было установлено, что -амилоидные пептиды, содержащие остаток пироглутамовой кислоты в положении 3,11 и/или 22, обладают более высокой цитотоксичностью и гидрофобностью, чем амилоидные-пептиды 1-40(42/43) (Saido Т.С., Medical Hypotheses 54(3), 2000, cc. 427-429). Можно создавать многочисленные N-концевые вариации, например, Абета(3-40), Абета(3-42), Абета(11-40) и Абета (11-42), посредством расщепления в различных сайтах с помощью фермента Р- 11022420J.T. и др., J. Biol. Chem. 277 (18), 2002, cc. 16278-16284), и/или путем процессинга полноразмерных пептидов Абета(1-40) и Абета(1-42) с помощью аминопептидазы или дипептидиламинопептидазы. Во всех случаях последующая циклизация N-концевого остатка глутаминовой кислоты катализируется QC. Клетки, обладающие способностью к транедукции через эпителий, прежде всего несущие гастрин(G) клетки, осуществляют координацию секреции желудочной кислоты с поступающей в желудок пищей. В современных исследованиях установлено, что из предшественника гастрина образуются продукты, обладающие несколькими видами активности, и что существует целый ряд важных моментов (контрольных точек) в биосинтезе гастрина. Участвующие в биосинтезе предшественники и промежуточные продукты (прогастрин и Gly-гастрины), возможно, представляют собой факторы роста; их продукты,амидированные гастрины, регулируют пролиферацию эпителиальных клеток, дифференцировку продуцирующих кислоту париетальных клеток и секретирующих гистамин энтерохромаффиноподобных клеток (ECL-клетки), и экспрессию генов, связанных с синтезом и хранением гистамина в ECL-клетках, а также острую стимуляцию секреции кислоты. Гастрин стимулирует также производство представителей семейства эпидермального фактора роста (EGF), которые в свою очередь ингибируют функцию париетальных клеток, но стимулируют рост поверхностных эпителиальных клеток. Концентрации гастрина в плазме у пациентов, зараженных Helicobacter pylori, у которых, как известно, существует повышенный риск возникновения язвенной болезни двенадцатиперстной кишки и рака желудка, повышены (DockrayG.J., J Physiol, 15, 1999, cc. 315-324). Известно, что пептидный гормон гастрин, который выделяется из антральных G-клеток, стимулирует синтез и высвобождение гистамина из ECL-клеток в кислородпродуцирующую слизистую черезCCK-2-рецепторы. Мобилизованный гистамин индуцирует секрецию кислоты в результате связывания с Н(2)-рецепторами, локализованными на париетальных клетках. В современных исследованиях высказано предположение о том, что гастрин, как в виде полностью амидированной, так и в виде менее процессированных форм (прогастрин и удлиненный глицином гастрин), также является фактором роста в желудочно-кишечном тракте. Было установлено, что основное трофическое действие амидированного гастрина связано с кислородпродуцирующей слизистой оболочкой желудка, где он вызывает повышенную пролиферацию стволовых клеток желудка и ECL-клеток, что приводит к увеличению массы париетальных иECL-клеток. С другой стороны, основной мишенью трофического действия менее процессированного гастрина (например, удлиненного глицином гастрина), вероятно, является слизистая оболочка ободочной кишки (Koh T.J. и Chen D., Regul Pept 93, 2000, cc. 337-344). Нейротензин (NT) представляет собой нейропептид, участвующий в патофизиологии шизофрении,который специфически модулирует системы нейротрансмиттеров (нейромедиаторов), регуляция которых, как продемонстрировано ранее, нарушается при этом заболевании. Клинические исследования, при которых определяли концентрации NT в спинно-мозговой жидкости (CSF), позволили выявить группу страдающих шизофренией пациентов с пониженными концентрациями NT в CSF, которые восстанавливались при эффективном лечении с помощью антипсихотических лекарственных средств. Известны также данные, которые подтверждают роль NT-систем в механизме действия антипсихотических лекарственных средств. Поведенческие и биохимические реакции при введении NT в центральную нервную систему очень сходны с реакциями на системное введение антипсихотических лекарственных средств, и антипсихотические лекарственные средства повышают нейротрансмиссию NT. Совокупность этих данных привела к гипотезе о том, что NT функционирует в качестве эндогенного антипсихотического агента. Кроме того, обычные и атипичные антипсихотические лекарственные средства по-разному изменяют нейротрансмиссию NT в области черного тела и в мезолимбических допаминсодержащих конечных областях, и эти явления свидетельствуют о чувствительности к вызыванию побочных действий и эффективности соответственно (Binder Е. В. и др., Biol Psychiatry, 50, 2001, cc. 856-872). Стимулирующий оплодотворение пептид (FPP), трипептид, родственный тиреотропин-рилизинггормону (TRH), обнаружен в семенной плазме. Современные исследования in vitro и in vivo позволили установить, что FPP играет важную роль в регуляции фертильности спермы. В частности, FPP стимулирует прежде всего "включение" неспособных к оплодотворению (неактивных) сперматозоидов и существенно быстрее делает их фертильными, а затем поддерживает эту способность посредством того, что сперматозоиды не подвергаются спонтанной потере акросомы и вследствие этого не теряют способность к оплодотворению. Аденозин, который, как известно, регулирует путь трансдукции сигнала аденилилциклазы (АС)/сАМР, приводит к аналогичным реакциям и фактически усиливает их. Установлено, что иFPP, и аденозин стимулируют производство сАМР в неактивных клетках, но ингибируют его в активных клетках, причем FPP-рецепторы каким-то образом взаимодействуют с аденозиновыми рецепторами и Gбелками для осуществления регуляции АС. Эти события влияют на состояние фосфорилирования тирозина различных белков, некоторые из которых важны для начального "включения", другие, вероятно,участвуют в самой реакции акросомы. Кальцитонин и ангиотензин II, также обнаруженные в семенной плазме, оказывают аналогичные действия in vitro на неактивные сперматозоиды и могут усиливать реакции на FPP. Эти молекулы проявляют аналогичные действия in vivo, оказывая влияние на фертильность путем стимуляции и затем поддержания способности к оплодотворению. Любое уменьшение доступно- 12022420 сти FPP, аденозина, кальцитонина и ангиотензина II или дефекты в их рецепторах приводят к развитию мужского бесплодия (Fraser L.R. и Adeoya-Osiguwa S. A., Vitam Horm 63, 2001, cc. 1-28).CCL2 (MCP-1), CCL7, CCL8, CCL16, CCL18 и фракталкин играют важную роль в таких патофизиологических состояниях, как подавление пролиферации миелодных клеток-предшественников, неоплазии,воспалительные реакции хозяина, рак, псориаз, ревматоидный артрит, атеросклероз, васкулит, гуморальные и клеточно-опосредуемые иммунные ответы, процессы адгезии и миграции лейкоцитов в эндотелии,воспалительное заболевание кишечника, рестеноз, фиброз легкого, легочная гипертензия, фиброз печени,цирроз печени, нефросклероз, ремоделирование желудочков, сердечная недостаточность, артериопатия после трансплантации органов и снижение функции венозных трансплантатов. Во многих исследованиях подчеркивалась решающая роль MCP-1 в развитии атеросклероза (Gu L. и др., Mol.Cell 2, 1998, cc. 275-281; Gosling J. и др., J Clin.Invest 103, 1999, cc. 773-778); ревматоидного артрита (Gong J. H. и др., J Exp.Med 186, 1997, cc. 131-137; Ogata Н. и др., J Pathol. 182, 1997, cc. 106-114); панкреатита (Bhatia М. и др., Am. J Physiol Gastrointest.Liver Physiol 288, 2005, cc. G1259-G1265); болезни Альцгеймера (Yamamoto M. и др., Am.J Pathol. 166, 2005, cc. 1475-1485); фиброза легкого (Inoshima I. и др., Am.J Physiol Lung Cell Mol.Physiol 286, 2004, cc. L1038-L1044); фиброза почек (Wada Т. и др., JVase. Biol. 24, 2004, cc. 1886-1890). Кроме того, MCP-1 может играть роль при гестозе (Katabuchi H. и др., Med Electron Microsc. 36, 2003, cc. 253-262), действовать в качестве паракринного фактора при развитии опухоли (Ohta М. и др., Int.J Oncol. 22, 2003, cc. 773-778; Li S. и др., J Exp.Med 202, 2005, cc. 617624), участвовать в развитии невропатической боли (White F.A. и др., Proc. Natl. Acad.Sci.U.S.A., 2005) и СПИДа (Park I. W., Wang J. F. и Groopman J. E. Blood 97, 2001, cc. 352-358; Coll В. и др., Cytokine 34, 2006, cc. 51-55). Установлено, что уровни MCP-1 повышены в CSF страдающих AD пациентов и пациентов, имеющих умеренные когнитивные нарушения (MCI) (Galimberti D. и др., Arch.Neurol. 63, 2006, cc. 538-543). Кроме того, установлено, что уровень MCP-1 повышен в сыворотке пациентов с MCI и AD на ранней стадии (Clerici F. и др., Neurobiol.Aging 27, 2006, cc. 1763-1768). В настоящее время в клинических опытах изучено несколько цитотоксических вакцин на основе Tлимфоцитарных пептидов против гепатита B, вируса иммунодефицита человека и меланомы. Одной из перспективных вакцин против меланомы, которую применяют индивидуально или в сочетании с другими опухолевыми антигенами, является декапептид ELA. Этот пептид является аналогом иммунодоминантного пептида антигена Melan-A/MART-1, который несет N-концевую глутаминовую кислоту. Известно, что аминогруппа и гамма-карбоксильная группа глутаминовых кислот, а также аминогруппа и гамма-карбоксамидная группа глутаминов легко конденсируются с образованием пироглутаминовых производных. Для решения указанных проблем, связанных со стабильностью, было разработано несколько пептидов, представляющих интерес с фармацевтической точки зрения, которые содержали пироглутаминовую кислоту вместо N-концевого глутамина или глутаминовой кислоты без потери фармакологических свойств. Однако по сравнению с ELA у производного пироглутаминовой кислоты(PyrELA), а также N-концевого кэппированного ацетилом производного (AcELA) не удалось сохранить цитотоксическую активность, присущую T-лимфоцитам (CTL). Несмотря на то, что в PyrELA и AcELA были внесены кажущиеся очень небольшими модификации, эти два производных, вероятно, обладают более низкой аффинностью по сравнению с ELA к специфическому классу I главного комплекса гистосовместимости. Следовательно, для того, чтобы полностью сохранить активность ELA, следует избегать образования PyrELA (Beck А. и др., J Pept Res 57, 2001, cc. 528-538). Орексин А представляет собой нейропептид, который играет важную роль в регуляции всасывания пищи и нарушении сна, вероятно, в результате координации комплекса поведенческих и физиологических реакций этих комплементарных связанных с гомеостазом функций. Он играет также определенную роль в связанной с гомеостазом регуляции энергетического метаболизма, функции вегетативной нервной системы, гормональном балансе и регуляции общей воды организма. В настоящее время установлено, что в спинно-мозговой жидкости (CSF) пациентов, страдающих рассеянным склерозом или синдромом Гильена-Барре, присутствуют более высокие уровни пентапептида QYNAD, чем у здоровых субъектов (Brinkmeier Н. и др., Nature Medicine б, 2000, cc. 808-811). Из литературы известно, что имеются существенные различия в точках зрения на механизм действия пентапептида Gln-Tyr-Asn-Ala-Asp (QYNAD), прежде всего касательно эффективности его взаимодействия с натриевыми каналами и способности блокировать их, что приводит к усилению дисфункции аксонов,участвующих в воспалительных аутоиммунных заболеваниях центральной нервной системы. Но в последнее время было продемонстрировано, что не QYNAD, а его циклизованная пироглутаматная форма,pEYNAD, представляет собой активную форму, которая блокирует натриевые каналы, приводит к усилению дисфункции аксонов. Натриевые каналы экспрессируются с высокой плотностью в миелинированных аксонах и выполняют необходимую функцию, заключающуюся в проведении потенциалов действия вдоль аксонов в головном и спинном мозге млекопитающих. Таким образом, можно предположить, что они участвуют в некоторых аспектах патофизиологии воспалительных аутоиммунных заболеваний, прежде всего рассеянного склероза, синдрома Гийена-Барре и хронической воспалительной демиелинизи- 13022420 рующей полирадикулоневропатии. Кроме того, QYNAD является субстратом для фермента глутаминилциклазы (QC, ЕС 2.3.2.5), которая также присутствует в головном мозге млекопитающих, прежде всего в головном мозге человека. Глутаминилциклаза эффективно катализирует образование pEYNAD из его предшественника QYNAD. Таким образом, в настоящем изобретении предложено применение соединений формулы (I) для получения лекарственного средства, предназначенного для предупреждения или облегчения, или для лечения заболевания, выбранного из группы, включающей умеренное когнитивное нарушение, болезнь Альцгеймера, семейную британскую деменцию, семейную датскую деменцию, нейродегенерацию при синдроме Дауна, болезнь Гентингтона, болезнь Кеннеди, язвенное заболевание, рак двенадцатиперстной кишки, сопровождающийся или не сопровождающийся инфекциями Helicobacter pylori, колоректальный рак, синдром Золлигера-Эллисон, рак желудка, сопровождающийся или не сопровождающийся инфекциями Helicobacter pylori, патогенные психотические состояния, шизофрению, бесплодие, неоплазию,воспалительные ответы организма, рак, злокачественные метастазы, меланому, псориаз, ревматоидный артрит, атеросклероз, панкреатит, рестеноз, нарушенные гуморальные и клеточно-опосредуемые иммунные ответы, процессы адгезии и миграции лейкоцитов в эндотелии, нарушенное всасывание пищи, нарушения сна-бодрствования, нарушенную гомеостатическую регуляцию энергетического метаболизма,нарушенную функцию вегетативной нервной системы, нарушенный гормональный баланс или нарушенную регуляцию жидкостей организма, рассеянный склероз, синдром Гийена-Барре и хроническую воспалительную демиелинизирующую полирадикулоневропатию. Кроме того, путем введения млекопитающему соединения, предлагаемого в настоящем изобретении, можно стимулировать пролиферацию миелоидных клеток-предшественников. Кроме того, введение ингибитора QC, предлагаемого в настоящем изобретении, может приводить к подавлению мужской фертильности. Предпочтительный вариант осуществления настоящего изобретения относится к применению ингибиторов активности QC (ЕС) в сочетании с другими агентами, прежде всего для лечения нервных заболеваний, атеросклероза и рассеянного склероза. В настоящем изобретении предложен также способ лечения вышеуказанных заболеваний, заключающийся в том, что млекопитающему, предпочтительно человеку, вводят по меньшей мере одно соединение формулы (I) в терапевтически активном количестве. В наиболее предпочтительном варианте осуществления изобретения указанный способ и соответствующие применения относятся к лечению заболевания, выбранного из группы, включающей умеренное когнитивное нарушение, болезнь Альцгеймера, семейную британскую деменцию, семейную датскую деменцию, нейродегенерацию при синдроме Дауна, болезнь Паркинсона и хорею Гентингтона, которые включают введение млекопитающему, предпочтительно человеку, по меньшей мере одного соединения формулы (I) в терапевтически активном количестве. Еще более предпочтительный вариант осуществления настоящего изобретения относится к способу лечения и соответствующим применениям для лечения ревматоидного артрита, атеросклероза, панкреатита и рестеноза. Фармацевтические комбинации Предпочтительный вариант осуществления настоящего изобретения относится к композиции,предпочтительно к фармацевтической композиции, которая содержит по меньшей мере один ингибиторQC необязательно в комбинации по меньшей мере с одним другим агентом, выбранным из группы,включающей ноотропные средства, нейрозащитные средства, лекарственные средства против болезни Паркинсона, ингибиторы отложения амилоидного белка, ингибиторы синтеза бета-амилоида, антидепрессанты, анксиолитические лекарственные средства, антипсихотические лекарственные средства и лекарственные средства против рассеянного склероза. Наиболее предпочтительно ингибитор QC представляет собой соединение формулы (I), предлагаемое в настоящем изобретении. Более конкретно, вышеуказанный другой агент выбирают из группы, включающей антитела к бетаамилоиду, ингибиторы цистеинпротеазы, PEP-ингибиторы, LiCl, ингибиторы ацетилхолинэстеразы(AChE), усилители PIMT (протеинизоаспартаткарбоксиметилтрансфераза), ингибиторы бета-секретаз,ингибиторы гамма-секретаз, ингибиторы аминопептидаз, предпочтительно ингибиторы дипептидилпептидаз, наиболее предпочтительно ингибиторы DP IV; ингибиторы нейтральной эндопептидазы, ингибиторы фосфодиэстеразы-4 (PDE-4), ингибиторы TNF-альфа, антагонисты мускаринового рецептора M1,антагонисты рецептора NMDA, ингибиторы рецептора сигма-1, антагонисты гистамина H3, иммуномодуляторные средства, иммуносупрессорные средства, антагонисты MCP-1 или агент, выбранный из группы, включающей антегрен (натализумаб), неурелан (фампридин-SR), кампат (алемтузумаб), IR 208,NBI 5788/MSP 771 (типлимотид), паклитаксел, Anergix.MS (AG 284), SH636, дифферин (CD 271, адапален), BAY 361677 (интерлейкин-4), ингибиторы матриксных металлопротеиназ (например, ВВ 76163),интерферон-тау (трофобластин) и SAIK-MS. Кроме того, другой агент может представлять собой, например, успокоительное лекарственное средство (анксиолитик) или антидепрессант, выбранный из группы, включающей:(b) избирательные ингибиторы повторного захвата серотонина (SSRI), например циталопрам, флуоксетин, флуоксамин, эсциталопрам, сертралин, пароксетин;(f) ингибиторы повторного захвата серотонина-норэпинефрина (SNRI), например венлафаксин, дулоксетин;(h) ингибиторы повторного захвата норэпинефрина (NRI), например ребоксетин;(l) лиганды NPY-рецептора: агонисты или антагонисты NPY. В другом варианте осуществления настоящего изобретения другой агент может представлять собой,например, лекарственное средство против рассеянного склероза, выбранное из группы, включающей(d) антитела, например AGT-1, моноклональное антитело к колониестимулирующему фактору гранулоцитов-макрофагов (GM-CSF), модуляторы рецептора Nogo, ABT-874, алемтузумаб (САМРАТН),антитело к ОХ 40, CNTO-1275, DN-1921, натализумаб (синоним AN-100226, антегрен, МАт VLA-4, дакслизумаб (синоним зенепакс, Ro-34-7375, SMART анти-Тас), J-695, приликсимаб (синоним центара, CEN000029, cM-T412), MRA, дантес, антитело к IL-12,(e) препараты пептидной нуклеиновой кислоты (PNA), например ретиколос;(f) интерферон альфа, например альфаферон, человеческий альфа интерферон (синоним омниферон,альфа лейкоферон);(g) интерферон бета, например фрон, подобный интеферону бета-1 а авонекс, бетрон (ребиф), аналоги интерферона бета, слитый белок интерферон бета-трансферрин, рекомбинантный подобный интерферону бета-1b препарат бетасерон;(i) пептиды, например АТ-008, AnergiX.MS, иммунокин (альфа-иммунокин-NNSO3), циклические пептиды типа ZD-7349;(k) плазмиду, кодирующую специфический для рассеянного склероза аутоантиген, и плазмиду, кодирующую цитокин, например ВНТ-3009;(r) аналоги обеспечивающего направленный перенос в нейроны белка, осуществляющего транспорт через мембраны таурина и полученного из растений ингибитора калпаина леупептина, например нейродура;(w) тозил-пролин-фенилаланиновые низкомолекулярые антагонисты взаимодействия VLA4/VCAM, например ТВС-3342;(x) ингибиторы молекул клеточной адгезии, например ТВС-772;(z) антагонисты свободных легких цепей иммуноглобулинов (IgLC), связывающихся с рецепторами тучных клеток, например F-991;(cc) сополимер L-тирозина, L-лизина, L-глутаминовой кислоты и L-аланина, например глатирамера ацетат (синоним копаксон, СОР-1, сополимер-1);(oo) ингибиторы фосфорилазы пуриновых нуклеозидов, например 9-(3-пиридилметил)-9 деазагуанин, пелдезин (синоним ВСХ-34, ТО-200);(tt) вакцины, содержащие белки теплового шока, например HSPPC-96;(uu) нейрегулиновые факторы роста, например GGF-2 (синоним нейрегулин, глиальный ростовой фактор 2);(xx) ингибиторы моноцитарного хемоаттрактантного белка-1, например бензимидазолы типа ингибиторов MCP-1, LKS-1456, PD-064036, PD-064126, PD-084486, PD-172084, PD-172386. Кроме того, настоящее изобретение относится к фармацевтическим композициям, предназначенным, например для парентерального, энтерального или орального введения, которые содержат по меньшей мере один ингибитор QC необязательно в сочетании по меньшей мере с одним другим вышеуказанным средством. Эти комбинации обладают особенно благоприятным действием. Таким образом, установлено, что указанные комбинации являются эффективными и пригодными для лечения вышеуказанных болезней,таким образом, изобретение относится к способу лечения указанных состояний. Способ заключаются в том, что вводят либо одновременно, либо последовательно по меньшей мере один ингибитор QC и по меньшей мере одно другое средство. Совместное введение предусматривает введение препаративной формы, которая содержит по меньшей мере один ингибитор QC и по меньшей мере одно другое средство, или практически одновременное введение отдельных препаративных форм каждого средства. Антитела к бета-амилоиду и содержащие их композиции описаны, например в Антитела к бета-амилоиду можно выбирать, например, из поликлональных, моноклональных, химерных или гуманизированных антител. Кроме того, указанные антитела можно применять для осуществления активной и пассивной иммунных терапий, т.е. с использованием вакцин и моноклональных антител. Приемлемыми примерами антител к бета-амилоиду являются ACU-5A5, huC091 (фирма Acumen/Merck); PF-4360365, М-1014, RI-1219, RI-409, RN-1219 (фирма Rinat Neuroscience Corp (Pfizer Inc; терапевтические нанотела фирмы Ablynx/Boehringer Ingelheim; специфические для бета-амилоида гуманизированные моноклональные антитела фирмы Intellect Neurosciences/IBL; m266, m266.2 (фирма EliMindset BioPharmaceuticals Inc. Наиболее предпочтительными являются антитела, которые распознают N-конец Ар-пептида. Приемлемым антителом, которое распознает N-конец A, является, например, Acl-24 (фирма AC immuneCA). Моноклональное антитело к бета-амилоиду описано в WO 2007/068412. Соответствующие химерные и гуманизированные антитела описаны в WO 2008/011348. Способ получения композиции вакцины,предназначенной для лечения ассоциированных с амилоидом болезней, описан в WO 2007/068411. Приемлемыми ингибиторами цистеиновой протеазы являются, например, ингибиторы катепсина В. Ингибиторы катепсина В и композиции, содержащие указанные ингибиторы, описаны, например в Примерами приемлемых усилителей PIMT являются 10-аминоалифатилдибенз[b,f]оксепины, описанные в WO98/15647 и WO03/057204 соответственно. Пригодными согласно настоящему изобретению являются также модуляторы активности PIMT, описанные в WO2004/039773. Ингибиторы бета-секретазы и композиции, содержащие указанные ингибиторы, описаны, например, в Приемлемыми примерами ингибиторов бета-секретазы, которые можно применять согласно настоящему изобретению, являются WY-25105 (фирма Wyeth); посифен, (+)-фенсерин (фирма TorreyPines / Пригодными для применения согласно настоящему изобретению ингибиторами гамма-секретазы являются GSI-953, WAY-GSI-A, WAY-GSI-B (фирма Wyeth); MK-0752, MRK-560, L-852505, L-685-458,- 17022420 Пригодными для цели настоящего изобретения ингибиторами DPIV являются, например, ситаглиптин, дес-фтор-ситаглиптин (MerckCo. Inc.); вилдаглиптин, DPP-728, SDZ-272-070 (Novartis); ABT-279,ABT-341 (Abbott Laboratories); денаглиптин, ТА-6666 (GlaxoSmithKline plc.); SYR-322 (Takeda San DiegoNordisk A/S). Другими предпочтительными ингибиторами DPIV являются:(i) дипептидподобные соединения, описанные в WO 99/61431, например N-валилпролил, Oбензоилгидроксиламин, аланилпирролидин, подобные изолейцилтиазолидину L-аллоизолейцилтиазолидин, L-треоизолейцилпирролидин и их соли, прежде всего фумаровые соли, и Lаллоизолейцилпирролидин и его соли;(v) обладающие активностью при местном применении ингибиторы DP IV, описанные в WO 01/14318;(vii) ингибиторы DP IV на основе глутаминила, описанные в WO 03/072556 и WO 2004/099134. Пригодными для целей настоящего изобретения ингибиторами синтеза бета-амилоида являются,например биснорцимсерин (фирма Axonyx Inc.); (R)-флурбипрофен (МСР-7869; флуризан) (фирма Myriad Genetics); нитрофлурбипрофен (фирма NicOx); BGC-20-0406 (фирма Sankyo Co. Ltd.) и BGC-20-0466(фирма BTG plc.). Приемлемыми ингибиторами отложения амилоидного белка, которые можно применять согласно настоящему изобретению, являются, например SP-233 (фирма Samaritan Pharmaceuticals); AZD-103Ltd.); CHF-5022, CHF-5074, CHF-5096 и CHF-5105 (фирма Chiesi Farmaceutici SpA.). Приемлемыми ингибиторами PDE-4, которые можно применять согласно настоящему изобретению,являются, например, доксофиллин (фирма Instituto Biologico Chemioterapica ABC SpA.); глазные капли идудиласта, типелукаст, ибудиласт (фирма Kyorin Pharmaceutical Co. Ltd.); теофиллин (фирма Elan Приемлемыми ингибиторами МАО, которые можно применять согласно настоящему изобретению,являются, например линезолид (фирма Pharmacia Corp.); RWJ-416457 (фирма RW Johnson Pharmaceuticalof Jerusalem); сафинамид (фирма Pfizer) и NW-1048 (фирма Newron Pharmaceuticals SpA). Приемлемыми ингибиторами гистамина H3, которые можно применять согласно настоящему изобретению, являются, например АВТ-239, АВТ-834 (фирма Abbott Laboratories); 3874-H1 (фирма Aventis Приемлемыми ингибиторами пролилэндопептидазы, которые можно применять согласно настоящему изобретению, являются, например Fmoc-Ala-Pyrr-CN, Z-Phe-Pro-бензотиазол (фирма Probiodrug),Z-321 (фирма Zeria Pharmaceutical Co Ltd.); ONO-1603 (фирма Ono Pharmaceutical Co Ltd); JTP-4819(фирма Japan Tobacco Inc.) и S-17092 (фирма Servier). Другими приемлемыми соединениями, которые можно применять согласно настоящему изобретению в сочетании с ингибиторами QC, являются NPY, миметик NPY или агонист или антагонист NPY,или лиганд NPY-рецепторов. Предпочтительными согласно настоящему изобретению являются антагонисты NPY-рецепторов. Приемлемыми лигандами или антагонистами NPY-рецепторов являются соединения, которые представляют собой производные 3a,4,5,9b-тетрагидро-1h-бенз[е]индол-2-иламина, описанные в WO 00/68197. Антагонисты NPY-рецептора, которые следует упомянуть, включают описанные в европейских заявках на патент публикациях международных заявок в патентах заявке на японский патент JP 09157253; публикациях международных заявок WO 94/00486, WO 93/12139, WO 95/00161 и WO 99/15498; патенте US 5328899; немецкой заявке на патент DE 3939797; европейских заявках на патент ЕР 355794 и ЕР 355793; и заявках на японский патент JP 06116284 и JP 07267988. Предпочтительными антагонистами NPY являются соединения, конкретно описанные в этих патентных документах. Более предпочтительными соединениями являются аминокислотные и имеющие непептидную основу антагонисты NPY. Аминокислотные и имеющие непептидную основу антагонистыNPY, которые следуют упомянуть, включают описанные в европейских заявках на патент международных заявках на патент Патентах заявке на японский патент JP09157253. Предпочтительные аминокислотные и имеющие непептидную основу антагонисты NPY представ- 20022420 ляют собой соединения, конкретно описанные в этих патентных документах. Наиболее предпочтительными соединениями являются имеющие аминокислотную основу антагонисты NPY. Имеющие аминокислотную основу соединения, которые следует упомянуть, включают соединения, описанные в международных заявках на патент WO 94/17035, WO 97/19911, WO 97/19913, WO 97/19914 или предпочтительно WO 99/15498. Предпочтительными имеющими аминокислотную основу антагонистами NPY являются соединения, конкретно описанные в этих патентных документах, напримерBIBP3226 и прежде всего амид (R)-N2-(дифенилацетил)-(R)-N-[1-(4-гидроксифенил)этил]аргинина (пример 4 международной заявки на патент WO 99/15498). Агонисты M1-рецептора и композиции, содержащие такие ингибиторы, описаны, например в WO 2004/087158, WO 91/10664. Приемлемыми антагонистами М 1-рецептора, которые можно применять согласно настоящему изобретению, являются, например CDD-0102 (фирма Cognitive Pharmaceuticals); цевимелин (эвоксак) (фирма Приемлемыми ингибиторами ацетилхолинэстеразы, которые можно применять согласно настоящему изобретению, являются, например донепезил (фирма Eisai Co. Ltd.); ривастигмин (фирма Novartis Приемлемыми антагонистами NMDA-рецептора, которые можно применять согласно настоящему изобретению, являются, например мемантин (фирма MerzCo. GmbH); топирамат (фирма JohnsonCR-3991, CR-2249, CR-3394 (фирма Rottapharm SpA.); AV-101 (4-С 1-кинуренин (4-C1-KYN, 7-хлоркинуреиновая кислота (7-C1-KYNA) (фирма VistaGen); NPS-1407 (фирма NPS Pharmaceuticals Inc.); YT1006 (фирма Yaupon Therapeutics Inc.); ED-1812 (фирма Sosei RD Ltd.); химантан (гидрохлорид N-2(адамантил)гексаметиленимина) (RAMS); ланцицемин (AR-R-15896) (фирма AstraZeneca); EVT-102, Ro25-6981 и Ro-63-1908 (фирма Hoffmann-La Roche AG/Evotec). Кроме того, настоящее изобретение относится к комбинированным терапиям, которые можно применять для лечения атеросклероза, рестеноза или артрита, заключающимся в том, что вводят ингибиторQC в сочетании с другим терапевтическим средством, выбранным из группы, включающей ингибиторы ангиотензинпревращающего фермента (АСЕ); блокаторы рецептора ангиотензина II; диуретики; блокаторы кальциевых каналов (ССВ); бета-блокаторы; ингибиторы агрегации тромбоцитов; модуляторы абсорбции холестерина; ингибиторы HMG-Co-A-редуктазы; соединения, повышающие уровень липопротеидов высокой плотности (ЛПВП); ингибиторы ренина; ингибиторы IL-6; противовоспалительные кортикостероиды; антипролиферативные средства; доноры оксида азота; ингибиторы синтеза внеклеточного матрикса; ингибиторы трансдукции сигналов факторов роста или цитокинов; антагонисты MCP-1 и ингибиторы тирозинкиназ, которые обладают благоприятным или синергетическим действием по сравнению с индивидуальным применением каждого компонента для монотерапии. Под блокаторами рецептора ангиотензина II подразумеваются действующие вещества, которые связываются с подтипом AT1-рецептора ангиотензина II, но не вызывают активацию рецептора. Благодаря их способности вызывать блокаду AT1-рецептора эти антагонисты можно применять, например, в качестве гипотензивных средств. Приемлемые блокаторы рецептора ангиотензина II, которые можно применять в комбинации, предлагаемой в настоящем изобретении, являются антагонисты AT1-рецептора, имеющие различные структурные особенности, предпочтительно имеющие непептидные структуры. Например, следует упомянуть соединения, выбранные из группы, включающей валсартан (EP443983), лосартан (EP253310), кандесартан (EP459136), эпросартан (EP403159), ирбесартан (EP454511), олмесартан (EP503785), тазосартан или во всех случаях их фармацевтически приемлемую соль. Предпочтительными антагонистами AT1-рецептора являются разрешенные к применению и поступающие в продажу средства, наиболее предпочтительным является валсартан или его фармацевтически приемлемая соль. Препятствующие ферментативному расщеплению ангиотензина с образованием ангиотензина II ингибиторы АСЕ представляют собой эффективный вариант средств регуляции кровяного давления, и их применение является приемлемым терапевтическим методом лечения гипертензии. Приемлемые ингибиторы АСЕ, которые можно применять в комбинации, предлагаемой в настоящем изобретении, представляют собой, например, соединение, выбранное из группы, включающей алацеприл, беназеприл, беназеприлат; каптоприл, церонаприл, цилазаприл, делаприл, эналаприл, энаприлат,фозиноприл, имидаприл, лизиноприл, мовелтоприл, периндоприл, квинаприл, рамиприл, спираприл, темокаприл и трандолаприл, или во всех случаях их фармацевтически приемлемую соль. Предпочтительными ингибиторами АСЕ являются поступающие в продажу средства, наиболее предпочтительными являются беназеприл и эналаприл. Диуретик представляет собой, например, тиазидное производное, выбранное из группы, включающей хлортиазид, гидрохлортиазид, метилклотиазид и хлорталидон. Наиболее предпочтительным диуретиком является гидрохлортиазид. К диуретиком относятся также калийсберегающие диуретики, такие как амилорид или триаметерин или их фармацевтически приемлемая соль. К классу ССВ относятся прежде всего дигидропиридины (DHP) и не-DHP, такие как ССВ дилтиа- 22022420 земового типа и верапамилового типа. ССВ, которые можно применять в комбинации, предпочтительно являются представителями классаDHP, выбранными из группы, включающей амлодипин, фелодипин, риосидин, исрадипин, лацидипин,никардипин, нифедипин, нигулдипин, нилудипин, нимодипин, нисолдипин, нитрендипин и нивалдипин,и они предпочтительно являются представителями класса не-DHP, выбранными из группы, включающей флунаризин, прениламин, дилтиазем, фендилин, галлопамил, мибефрадил, анипамил, тиапамил и верапамил, и во всех случаях их фармацевтически приемлемую соль. Все эти ССВ имеют терапевтическое применение, например, в качестве гипотензивных средств, средств против стенокардии или антиаритмических лекарственных средств. Предпочтительными ССВ являются амлодипин, дилтиазем, иерадипин, никардипин, нифедипин,нимодипин, нисолдипин, нитрендипин и верапамил или, например, в зависимости от конкретного ССВ,его фармацевтически приемлемая соль. Наиболее предпочтительным в качестве DHP является амлодипин или его фармацевтически приемлемая соль, прежде всего безилат. Наиболее предпочтительным в качестве не-DHP является верапамил или его фармацевтически приемлемая соль, прежде всего гидрохлорид. Бета-блокаторы, которые можно применять согласно настоящему изобретению, являются бетаадренергические блокаторы (бета-блокаторы), которые конкурируют с эпинефрином за бетаадренергические рецепторы и оказывают воздействие на активность эпинефрина. Предпочтительно бетаблокаторы обладают избирательным действием в отношении бета-адренергического рецептора по сравнению с альфа-адренергическими рецепторами и поэтому не обладают существенным альфаблокирующим действием. Приемлемыми бета-блокаторами являются соединения, выбранные из группы,включающей ацебутолол, атенолол, бетаксолол, бисопролол, картеолол, карведилол, эсмолол, лабеталол,метопролол, надолол, окспренолол, пенбутолол, пиндолол, пропранолол, соталол и тимолол. Если бетаблокатор представляет собой кислоту или основание или если он благодаря другим особенностям может образовывать фармацевтически приемлемые соли или пролекарства, то эти формы также подпадают под объем изобретения, и, как должно быть очевидно, соединения можно вводить в свободной форме или в форме фармацевтически приемлемой соли или пролекарства, такого как гидролизуемый в физиологических условиях и физиологически приемлемый сложный эфир. Например, метопролол можно вводить в форме тартрата, пропранолол можно вводить в форме гидрохлорида и т.д. Ингибиторы агрегации тромбоцитов представляют собой PLAVIX (клопидогрела бисульфат),PLETAL (цилостазол) и аспирин. Модуляторы абсорбции холестерина представляют собой ZETIA (эзетимиб) и KT6-971 (фирмаKotobuki Pharmaceutical Co. Japan). Подразумевается, что ингибиторы HMG-Co-A-редуктазы (называемые также ингибиторами бетагидрокси-бета-метилглутарил-кофермент-А-редуктазы или статины) представляют собой действующие вещества, которые можно применять для снижения уровня липидов, включая холестерин, в крови. Класс ингибиторов HMG-Co-A-редуктаз включает соединения, которые обладают различными структурными особенностями. Например, следует упомянуть соединения, выбранные из группы, включающей аторвастатин, церивастатин, флувастатин, ловастатин, питавастатин, правастатин, росувастатин и симвастатин, или во всех случаях их фармацевтически приемлемую соль. Предпочтительными ингибиторами HMG-Co-A-редуктазы являются соединения, которые поступают в продажу, наиболее предпочтительным является аторвастатин, питавастатин или симвастатин, или их фармацевтически приемлемая соль. Соединения, повышающие уровень ЛПВП, включают, но не ограничиваясь только ими, ингибиторы белка-транспортера сложного эфира холестерина (СЕТР). Примерами ингибиторов СЕТР является соединение JTT7O5, описанное в примере 26 US6426365, выданного 30 июля 2002 г., и его фармацевтически приемлемые соли. Ингибирование опосредуемого интерлейкином 6 воспаления можно достигать опосредованно путем регуляции эндогенного синтеза холестерина и истощения изопреноидов или путем непосредственного ингибирования пути трансдукции сигнала с помощью ингибитора/антитела к интерлейкину 6, ингибитора/антитела к рецептору интерлейкина 6, антисмыслового олигонуклеотида интерлейкина 6 (ASON), ингибитора/антитела к белку gp130, ингибиторов/антител к тирозинкиназе, ингибиторов/антител к сериновой/треониновой киназе, ингибиторов/антител к активируемой митогеном протеин-(МАР)-киназе, ингибиторов/антител к фосфатидилинозитол-3-киназе (PI3K), ингибиторов/антител к ядерному фактору каппаВ (NF-B), ингибиторов/антител к IB-киназе (IKK), ингибиторов/антител к активатору белка-1 (АР 1), ингибиторов/антител к факторам транскрипции STAT, с помощью измененного IL-6, неполных пептидов IL-6 или рецептора IL-6, или белка SOCS (супрессоры передачи сигналов цитокинами), активаторов/лигандов PPAR гамма и/или PPAR бета/дельта или их функциональных фрагментов. Приемлемым противовоспалительным кортикостероидом является дексаметазон. Приемлемыми антипролиферативными средствами являются кладрибин, рапамицин, винкристин и таксол. Приемлемым ингибитором синтеза внеклеточного матрикса является галофугинон. Приемлемым ингибитором трансдукции сигналов факторов роста или цитокинов является, например ингибитор ras R115777. Приемлемым ингибитором тирозинкиназы является тирфостин. Приемлемые ингибиторы ренина описаны, например, в WO 2006/116435. Предпочтительным ингибитором ренина является алискирен, предпочтительно в форме полуфумарата. Антагонисты MCP-1 можно выбирать, например, из антител к MCP-1, предпочтительно моноклональных или гуманизированных моноклональных антител, ингибиторов экспрессии MCP-1, антагонистов CCR2, ингибиторов TNF-альфа, ингибиторов экспрессии гена VCAM-1 и моноклональных антител к С 5 а. Антагонисты MCP-1 и композиции, содержащие указанные ингибиторы, описаны, например вNovartis AG); CC-11006 (Celgene Corp.); SSR-150106 (фирма Sanofi-Aventis); MLN-1202 (фирма Millenium Pharmaceuticals Inc.); AGI-1067, AGIX-4207, AGI-1096 (фирма AtherioGenics Inc.); PRS-211095, PRS211092 (фирма Pharmos Corp.); моноклональные антитела к С 5 а, например нейтразумаб (фирма G2 Therapies Ltd.); AZD-6942 (фирма AstraZeneca plc.); 2-меркаптоимидазолы (фирма JohnsonJohnson); TEIE00526, TEI-6122 (фирма Deltagen); RS-504393 (фирма Roche Holding AG); SB-282241, SB-380732, ADR7 (фирма GlaxoSmithKline); моноклональные антитела к MCP-1 (фирма JohnsonJohnson). Комбинации ингибиторов QC с антагонистами MCP-1 можно применять для лечения воспалительных заболеваний в целом, включая нейродегенеративные болезни. Комбинации ингибиторов QC с антагонистами MCP-1 предпочтительно применяют для лечения болезни Альцгеймера. Наиболее предпочтительно ингибитор QC объединяют с одним или несколькими соединениями,выбранными из следующей группы: PF-4360365, m266, бапинеузумаб, R-1450, посифен, (+)-фенсерин,MK-0752, LY-450139, Е-2012, (R)-флурбипрофен, AZD-103, ААВ-001 (бапинеузумаб), трамипросат,EGb-761, TAK-070, доксофиллин, теофиллин, циломиласт, тофимиласт, рофлумиласт, тетомиласт, типелукаст, ибудиласт, HT-0712, МЕМ-1414, оглемиласт, линезолид, будипин, изокарбоксазид, фенелзин,транилципромин, индантодол, моклобемид, расагилин, ладостигил, сафинамид, АВТ-239, АВТ-834,GSK-189254A, ципроксифан, JNJ-17216498, Fmoc-Ala-Pyrr-CN, Z-Phe-Pro-бензотиазол, Z-321, ONO-1603,JTP-4819, S-17092, BIBP3226; амид (R)-N2-(дифенилацетил)-(R)-N-[1-(4-гидроксифенил)этил]аргинина,цевимелин, сабкомелин, (PD-151832), донепезил, ривастигмин, (-)-фенсерин, ладостигил, галантамин,такрин, метрифонат, мемантин, топирамат, AVP-923, EN-3231, нерамексан, валсартан, беназеприл, эналаприл, гидрохлортиазид, амлодипин, дилтиазем, исрадипин, никардипин, нифедипин, нимодипин, нисолдипин, нитрендипин, верапамил, амлодипин, ацебутолол, атенолол, бетаксолол, бисопролол, картеолол, карведилол, эсмолол, лабеталол, метопролол, надолол, окспренолол, пенбутолол, пиндолол, пропранолол, соталол, тимолол, PLAVIX (клопидогрела бисульфат), PLETAL (цилостазол), аспирин,ZETIA (эзетимиб) и KT6-971, статины, аторвастатин, питавастатин или симвастатин; дексаметазон,кладрибин, рапамицин, винкристин, таксол, алискирен, С-243, ABN-912, SSR-150106, MLN-1202 и бетаферон. В частности, изобретение относится к следующим комбинациям: ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с аторвастатином для лечения и/или предупреждения атеросклероза; ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с иммунодепрессантами, предпочтительно с рапамицином, для предупреждения и/или лечения рестеноза; ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с иммунодепрессантами, предпочтительно с паклитакселом, для предупреждения и/или лечения рестеноза,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с ингибиторами AChE,предпочтительно с донепезилом, для предупреждения и/или лечения болезни Альцгеймера,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,- 24022420 выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с интерферонами, предпочтительно с аронексом, для предупреждения и/или лечения рассеянного склероза,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с интерферонами, предпочтительно с бетафероном, для предупреждения и/или лечения рассеянного склероза,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с интерферонами, предпочтительно с ребифом, для предупреждения и/или лечения рассеянного склероза,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с копаксоном, для предупреждения и/или лечения рассеянного склероза,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с дексаметазоном, для предупреждения и/или лечения рестеноза,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с дексаметазоном, для предупреждения и/или лечения атеросклероза,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с дексаметазоном, для предупреждения и/или лечения ревматоидного артрита,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с ингибиторами HMGCo-A-редуктазы для предупреждения и/или лечения рестеноза, где ингибитор HMG-Со-А-редуктазы выбран из аторвастатина, церивастатина, флувастатина, ловастатина, питавастатина, правастатина, росувастатина и симвастатина,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с ингибиторами HMGCo-A-редуктазы для предупреждения и/или лечения атеросклероза, где ингибитор HMG-Co-A-редуктазы выбран из аторвастатина, церивастатина, флувастатина, ловастатина, питавастатина, правастатина, росувастатина и симвастатина,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с ингибиторами HMGCo-A-редуктазы для предупреждения и/или лечения ревматоидного артрита, где ингибитор HMG-Co-Aредуктазы выбран из аторвастатина, церивастатина, флувастатина, ловастатина, питавастатина, правастатина, росувастатина и симвастатина. ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с антителами к амилоиду бета для предупреждения и/или лечения умеренного когнитивного нарушения, где антитело к амилоиду бета представляет собой Acl-24,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с антителами к амилоиду бета для предупреждения и/или лечения болезни Альцгеймера, где антитело к амилоиду бета представляет собой Acl-24,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с антителами к амилоиду бета для предупреждения и/или лечения нейродегенерации при синдроме Дауна, где антитело к амилоиду бета представляет собой Acl-24,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с ингибиторами бетасекретазы для предупреждения и/или лечения умеренного когнитивного нарушения, где ингибитор бетасекретазы выбран из WY-25105, GW-840736X и CTS-21166,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с ингибиторами бетасекретазы для предупреждения и/или лечения болезни Альцгеймера, где ингибитор бета-секретазы выбран из WY-25105, GW-840736X и CTS-21166,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с ингибиторами бетасекретазы для предупреждения и/или лечения нейродегенерации при синдроме Дауна, где ингибитор бета-секретазы выбран из WY-25105, GW-840736X и CTS-21166,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с ингибиторами гаммасекретазы для предупреждения и/или лечения умеренного когнитивного нарушения, где ингибитор гам- 25022420 ма-секретазы выбран из LY-450139, LY-411575 и AN-37124,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с ингибиторами гаммасекретазы для предупреждения и/или лечения болезни Альцгеймера, где ингибитор гамма-секретазы выбран из LY-450139, LY-411575 и AN-37124,ингибитор QC, предпочтительно ингибитор QC формулы (I), более предпочтительно ингибитор QC,выбранный из числа ингибиторов, представленных в примерах 1-35, в сочетании с ингибиторами гаммасекретазы для предупреждения и/или лечения нейродегенерации при синдроме Дауна, где ингибитор гамма-секретазы выбран из LY-450139, LY-411575 и AN-37124. Указанную комбинированную терапию предпочтительно применяют при AD, FAD, FDD и нейродегенерации при синдроме Дауна, а также атеросклерозе, ревматоидном артрите, рестенозе и панкреатите. Указанные комбинированные терапии могут приводить к улучшенному терапевтическому действию (снижение пролиферации, а также уменьшение воспаления, стимула пролиферации), чем при индивидуальном применении любого из средств. Описание конкретной комбинации ингибиторов QC и других соединений приведено, в частности, в заявке WO 2004/098625, которая включена в настоящее описание в качестве ссылки. Фармацевтические композиции Для получения фармацевтических композиций, предлагаемых в настоящем изобретении, можно применять в качестве действующих(его) веществ(а) по меньшей мере одно соединение формулы (I) необязательно в сочетании по меньшей мере с одним из других вышеуказанных агентов. Действующее(ие) вещество(а) тщательно смешивают с фармацевтическим носителем согласно общепринятым методам приготовления фармацевтических препаратов, при этом носитель может находиться в широком разнообразии форм в зависимости от формы препарата, которая требуется для введения, например, орального или парентерального, такого как внутримышечное введение. Для приготовления композиций в виде оральной лекарственной формы можно использовать любые обычно применяемые в фармацевтике среды. Так, для жидких предназначенных для орального введения препаратов, таких, например, как суспензии, эликсиры и растворы, в качестве пригодных носителей и добавок можно использовать воду, гликоли, масла, спирты, ароматизаторы, консерванты, красители и т.п.; для твердых предназначенных для орального введения препаратов, таких, например, как порошки, капсулы, желатиновые капсулы и таблетки, в качестве пригодных носителей и добавок можно использовать крахмалы, сахара, разбавители,гранулирующие средства, замасливатели, связующие вещества, разрыхлители и т.п. Благодаря простоте их введения таблетки и капсулы являются наиболее предпочтительными оральными стандартными формами лекарственного средства, очевидно, что в этом случае применяют твердые фармацевтические носители. При необходимости на таблетки можно наносить с помощью стандартных методов сахарное покрытие или энтеросолюбильное покрытие. Для вводимых парентеральным путем лекарственных средств носитель, как правило, содержит стерильную воду, хотя можно включать и другие ингредиенты, например, для повышения растворимости или с целью консервации. Можно приготавливать также предназначенные для инъекции суспензии, в этом случае можно применять соответствующие жидкие носители, суспендирующие агенты и т.п. Фармацевтические композиции, представленные в настоящем описании, должны содержать в пересчете на стандартную дозу лекарственного средства, например, таблетку, капсулу, порошок, инъекционный объем, чайную ложку и т.п., действующее(ие) вещество(а) в количестве, необходимом для введения описанной выше эффективной дозы. Фармацевтические композиции, представленные в настоящем описании, должны содержать в пересчете на стандартную дозу лекарственного средства, например, таблетку, капсулу, порошок, инъекционный объем, суппозиторий, чайную ложку и т.п., каждое действующее вещество или их комбинацию в количестве, составляющем примерно от 0,03 до 100 мг/кг (предпочтительно 0,1-30 мг/кг), и их можно вводить в дозе, составляющей примерно 0,1-300 мг/кг в день (предпочтительно 1-50 мг/кг в день). Однако дозы можно варьировать в зависимости от требований пациента, серьезности состояния, подлежащего лечению и применяемого соединения. Можно применять либо ежедневное введение, либо последующее периодическое введение. Предпочтительно указанные композиции находятся в виде стандартных форм лекарственного средства, таких как таблетки, пилюли, капсулы, порошки, гранулы, стерильные растворы или суспензии для парентерального введения, дозируемые аэрозоли или жидкие спреи, капли, ампулы, автоматические инъекционные устройства или суппозитории; которые предназначены для орального, парентерального, интраназального, подъязычного или ректального введения, или для введения путем ингаляции или инсуффляции. В альтернативном варианте композиции могут находиться в форме, пригодной для введения один раз в неделю или один раз в месяц; например, в виде нерастворимой соли обладающего активностью соединения, такой как деканоат, они могут быть приспособлены для приготовления препарата в виде депо, предназначенного для внутримышечной инъекции. Для приготовления твердых композиций,таких как таблетки, основное действующее вещество смешивают с фармацевтическим носителем, например, с обычными применяемыми при таблетировании ингредиентами, такими как кукурузный крахмал, лактоза, сахароза, сорбит, тальк, стеариновая кислота, стеарат магния, вторичный кислый фосфат кальция или камеди, и другими фармацевтическими разбавителями, например, с водой, до образования твердой предварительной формы композиции, содержащей в виде гомогенной смеси соединение, предлагаемое в настоящем изобретении, или его фармацевтически приемлемую соль. Когда указывается, что эти предварительные формы композиции являются гомогенными, это означает, что действующее вещество равномерно диспергировано в композиции, что позволяет легко разделять композицию на части для получения обладающих одинаковой эффективностью форм лекарственного средства, таких как таблетки,пилюли и капсулы. Затем указанную твердую предварительную форму композиции разделяют на стандартные формы лекарственного средства описанного выше типа, которые содержат каждое из действующих веществ или их комбинаций, предлагаемых в настоящем изобретении, в количестве, составляющем от 0,1 до примерно 500 мг. На таблетки или пилюли, которые содержат композиции, предлагаемые в настоящем изобретении,можно наносить покрытие или обрабатывать иным образом для получения лекарственных форм, обладающих преимуществом, заключающемся в пролонгированном действии. Например, таблетка или пилюля может иметь внутренний содержащий дозу компонент и внешний содержащий дозу компонент, где последний присутствует в форме оболочки, находящейся над первым компонентом. Два компонента могут быть разделены энтеросолюбильным слоем, который служит для того, чтобы препятствовать распаду в желудке, и позволяет внутреннему компоненту проходит в интактном виде в двенадцатиперстную кишку или который позволяет замедлять высвобождение. Для таких энтеросолюбильных слоев или покрытий можно применять разнообразные материалы, к указанным материалам относятся многочисленные полимерные кислоты в сочетании с такими материалами, как шеллак, цетиловый спирт и ацетат целлюлозы. К указанным жидким формам, в которые можно включать композиции, предлагаемые в настоящем изобретении, с целью введения оральным путем или с помощью инъекции, относятся водные растворы,соответствующим образом ароматизированные сиропы, водные или масляные суспензии и ароматизированные эмульсии, приготовленные с использованием съедобных масел, таких как хлопковое масло, кунжутное масло, кокосовое масло или арахисовое масло, а также эликсиры и сходные фармацевтические наполнители. Пригодными диспергирующими или суспендирующими средствами для водных суспензий могут служить синтетические и природные камеди, такие как трагакант, аравийская камедь, альгинат,декстран, натриевая соль карбоксиметилцеллюлозы, метилцеллюлоза, поливинилпирролидон или желатин. Фармацевтическая композиция может содержать от примерно 0,01 до 100 мг, предпочтительно примерно 5-50 мг каждого соединения, и она может быть включена в любую форму, пригодную для выбранного пути введения. Носители представляют собой необходимые и инертные фармацевтические эксципиенты, включая (но не ограничиваясь только ими) связующие вещества, суспендирующие агенты,замасливатели, корригенты, подслащивающие вещества, консерванты, красители и покрытия. Композиции, пригодные для орального введения, включают твердые формы, такие как пилюли, таблетки, каплетки, капсулы (каждая из указанных форм включает формы с быстрым высвобождением, контролируемым высвобождением и пролонгированным высвобождением), гранулы и порошки, и жидкие формы, такие как растворы, сиропы, эликсиры, эмульсии и суспензии. Формы, которые можно применять для парентерального введения, включают стерильные растворы, эмульсии и суспензии. Предпочтительно соединения, предлагаемые в настоящем изобретении, следует вводить в виде однократной суточной дозы, или общую суточную дозу можно вводить в виде разделенных доз два, три или четыре раза в день. Кроме того, соединения, предлагаемые в настоящем изобретении, можно вводить в интраназальной форме посредством местного применения с использованием пригодных устройств для интраназального введения, или с помощью трансдермальных кожных пластырей, как это хорошо известно обычному специалисту в данной области. При введении в форме трансдермальной системы введения введение дозы следует, естественно, осуществлять непрерывно, а не с перерывами в процессе выполнения схемы приема лекарственного средства. Например, для орального введения в форме таблетки или капсулы компонент, представляющий собой действующее вещество, можно объединять с пригодным для орального введения нетоксичным фармацевтически приемлемым инертным носителем, таким как этанол, глицерин, вода и т.п. Кроме того,если это необходимо или целесообразно, в смесь можно включать также пригодные связующие вещества, замасливатели, разрыхлители и красители. Пригодными связующими веществами являются (но не ограничиваясь только ими) крахмал, желатин, природные сахара, такие как глюкоза или бета-лактоза,подслащивающие вещества из кукурузы, природные и синтетические камеди, такие как аравийская камедь, трагакант, или олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п. Разрыхлители включают (но не ограничиваясь только ими) крахмал, метилцеллюлозу, агар,бентонит, ксантановая камедь и т.п. Жидкие формы приготавливают в пригодных ароматизированных суспендирующих или диспергирующих веществах, таких как синтетические или природные камеди, например, трагакант, аравийская камедь, метилцеллюлоза и т.п. Для парентерального введения требуются стерильные суспензии и растворы. В том случае, когда требуется применять внутривенное введение, используют изотонические пре- 27022420 параты, которые, как правило, содержат пригодные консерванты. Соединения или комбинации, предлагаемые в настоящем изобретении, можно вводить также в форме липосомных систем введения, таких как малые однослойные (моноламеллярные) везикулы, большие однослойные везикулы и многослойные (мультиламеллярные) везикулы. Липосомы можно приготавливать из различных фосфолипидов, таких как холестерин, стеариламин или фосфатидилхолины. Соединения или комбинации, предлагаемые в настоящем изобретении, можно вводить также с использованием моноклональных антител в качестве индивидуальных носителей, с которыми связаны молекулы соединения. Соединения, предлагаемые в настоящем изобретении, можно связывать также с растворимыми полимерами, выполняющими функцию носителей, способных осуществлять направленный перенос лекарственного средства. В качестве таких полимеров можно применять поливинилпирролидон,сополимер пирана, полигидроксипропилметакриламидфенол, полигидроксиэтиласпартамидфенол или полиэтиленоксидполилизин, замещенный остатком пальмитоила. Кроме того, соединения, предлагаемые в настоящем изобретении, можно связывать с классом биоразлагаемых полимеров, которые можно применять для достижения контролируемого высвобождения лекарственного средства, например, с полимолочной кислотой, поли-эпсилон-капролактоном, полигидроксимасляной кислотой, сложными полиортоэфирами, полиацеталями, полидигидропиранами, полицианоакрилатами и сшитыми или амфипатическими блок-сополимерами гидрогелей. Соединения или комбинации, предлагаемые в настоящем изобретении, можно вводить в виде любой из вышеуказанных композиций и согласно схемам приема лекарственного средства, принятым в данной области в каждом случае, когда требуется осуществлять лечение рассматриваемого нарушения. Суточная доза продуктов может варьироваться в широких пределах от 0,01 до 1000 мг на млекопитающее в день. Для орального введения композиции предпочтительно приготавливают в форме таблеток,содержащих 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200, 250 и 500 мг каждого из действующих веществ или их комбинаций для симптоматического регулирования дозы для пациента,подлежащего лечению. Эффективное количество лекарственного средства обычно поступает в организм при уровне доз от примерно 0,1 до примерно 300 мг/кг веса тела в день. Предпочтительно диапазон составляет от примерно 1 до примерно 50 мг/кг веса тела в день. Соединения или комбинации можно вводить согласно схеме приема, предусматривающей 1-4 введения в день. Специалисты в данной области легко могут определять оптимальные предназначенные для введения дозы, которые должны варьироваться в зависимости от конкретного применяемого соединения, пути введения, эффективности препарата и прогрессирования болезненного состояния. Кроме того, учет факторов, ассоциированных с характеристиками конкретного пациента, подлежащего лечению, включая возраст пациента, вес, диету и продолжительность введения, может привести к необходимости осуществлять регулировку доз. Следующим объектом изобретения является также способ получения фармацевтической композиции, содержащей по меньшей мере одно соединение формулы (I) необязательно в сочетании по меньшей мере с одним из перечисленных других агентов и фармацевтически приемлемым носителем. Композиции предпочтительно присутствуют в стандартной форме лекарственного средства в количестве, соответствующем требуемой суточной дозе. Пригодные дозы, в том числе прежде всего стандартные дозы соединений, предлагаемых в настоящем изобретении, представляют собой известные дозы, в том числе стандартные дозы этих соединений,которые описаны или на которые даны ссылки в справочниках, таких как Британская Фармакопея и Фармакопея США, Remington's Pharmaceutical Sciences (изд-во Mack Publishing Co.), Martindale The ExtraPharmacopoeia (изд-во The Pharmaceutical Press, London) (например, см. 31-е изд., с. 341 и процитированные на ней ссылки) или в вышеуказанных публикациях. Примеры
МПК / Метки
МПК: A61P 29/00, A61K 31/4709, C07D 401/04, C07D 403/14, A61P 31/04, A61K 31/4184, A61P 35/00, A61K 31/5377, A61P 25/18, A61P 1/04, C07D 405/10, C07D 403/04, A61K 31/454, C07D 403/10, A61P 25/28
Метки: глутаминилциклазы, гетероциклические, 2.3.2.5, ингибиторы
Код ссылки
<a href="https://eas.patents.su/30-22420-geterociklicheskie-ingibitory-glutaminilciklazy-qc-ec-2325.html" rel="bookmark" title="База патентов Евразийского Союза">Гетероциклические ингибиторы глутаминилциклазы (qc, ec 2.3.2.5)</a>
Предыдущий патент: Легковесная строительная конструкция, изготовленная с применением строительного раствора, и способ изготовления
Следующий патент: Штамповая сталь
Случайный патент: Лифт и тормозное устройство лифта












