Хиназолиновые соединения
Номер патента: 20330
Опубликовано: 30.10.2014
Авторы: Мюррей Питер Джон, Харди Джордж, Кинг-Андервуд Джон, Брукфилд Фредерик Артур, Ито Кадзухиро, Браун Кристофер Джон
Формула / Реферат
1. Соединение формулы (I)
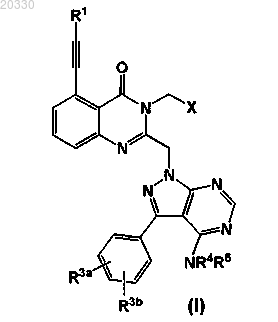
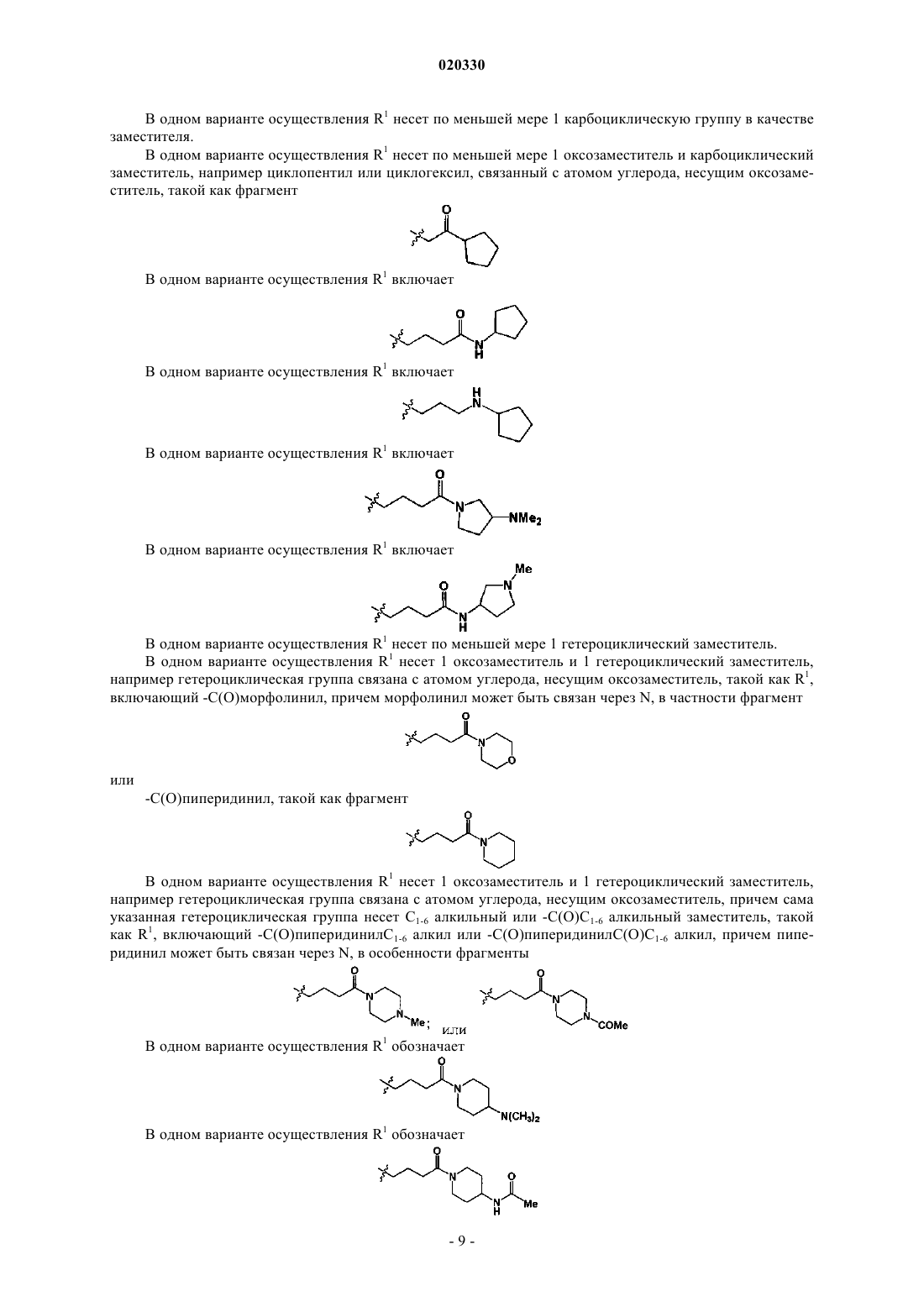
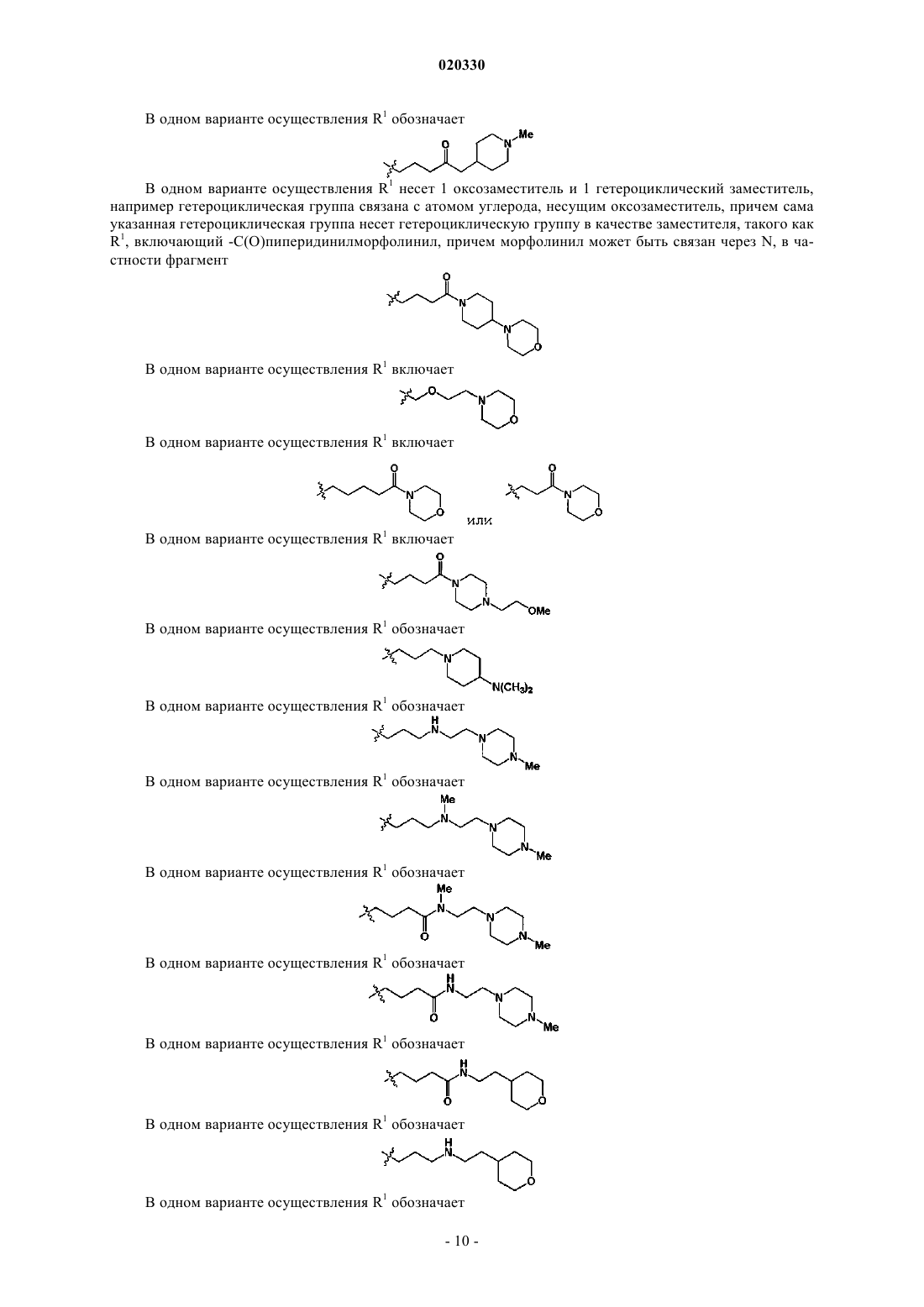
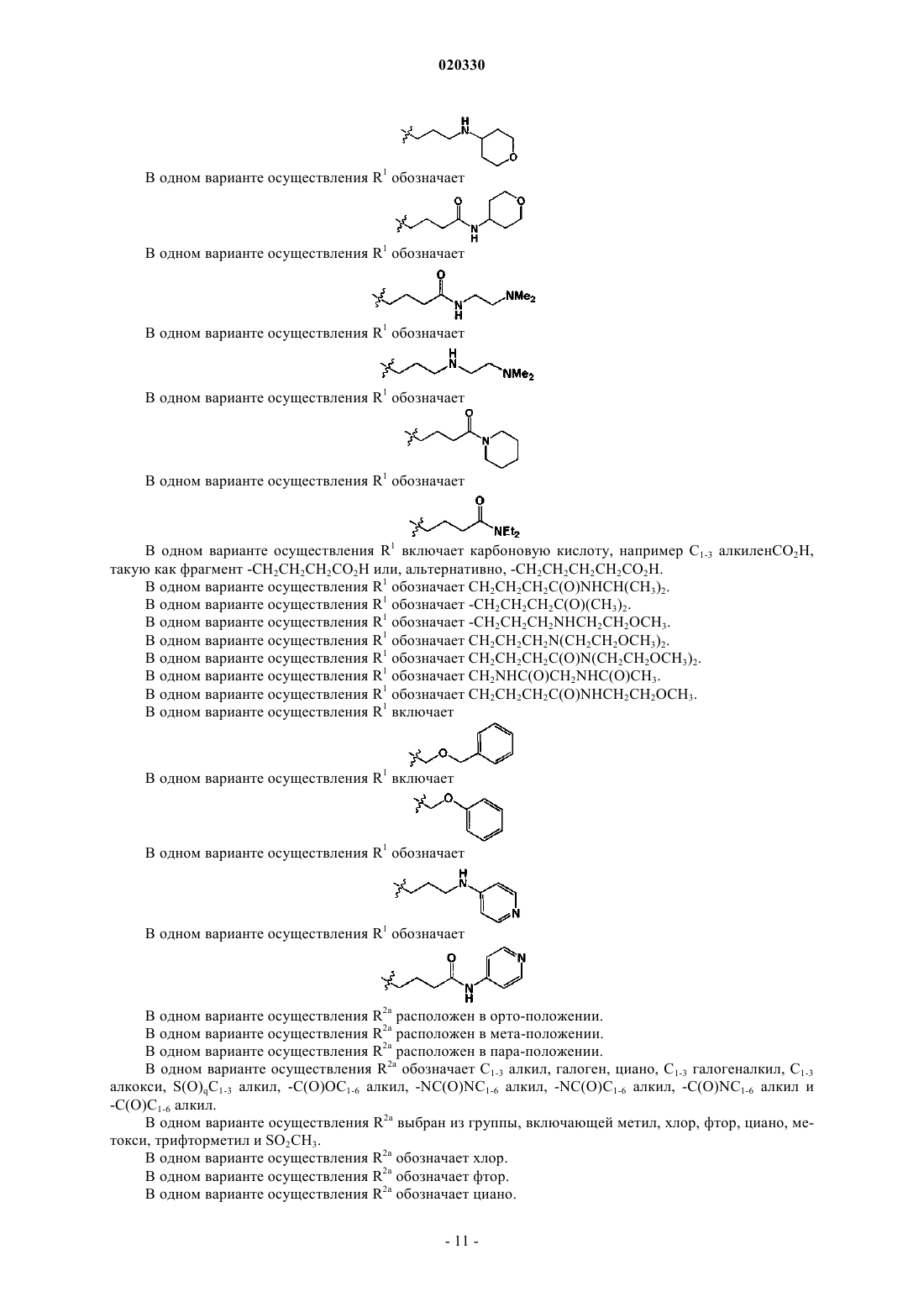
в которой R1 выбран из группы, состоящей из
-H;
разветвленной или неразветвленной C1-10 алкильной цепи, в которой по меньшей мере 1 атом углерода заменен кислородом;
-CH2CH2CH2OH;
-CH2OCH2CH2OCH2CH2OH;
-CH2NHCONH2;
-C1-3 алкиленСО2Н;
-CH2CH2CH2CH2CO2H;
-CH2CH2CH2C(O)NHCH(CH3)2;
-CH2CH2CH2C(O)(CH3)2;
-CH2CH2CH2NHCH2CH2OCH3;
-CH2CH2CH2N(CH2CH2OCH3)2;
-CH2CH2CH2C(O)N(CH2CH2OCH3)2;
-CH2NHC(O)CH2NHC(O)CH3;
-CH2CH2CH2C(O)NHCH2CH2OCH3;
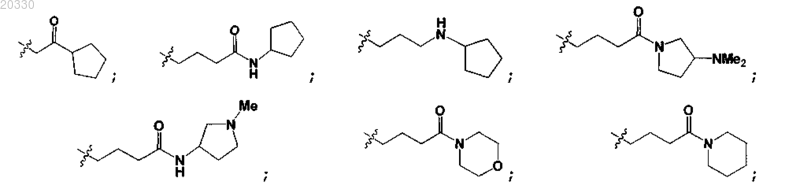
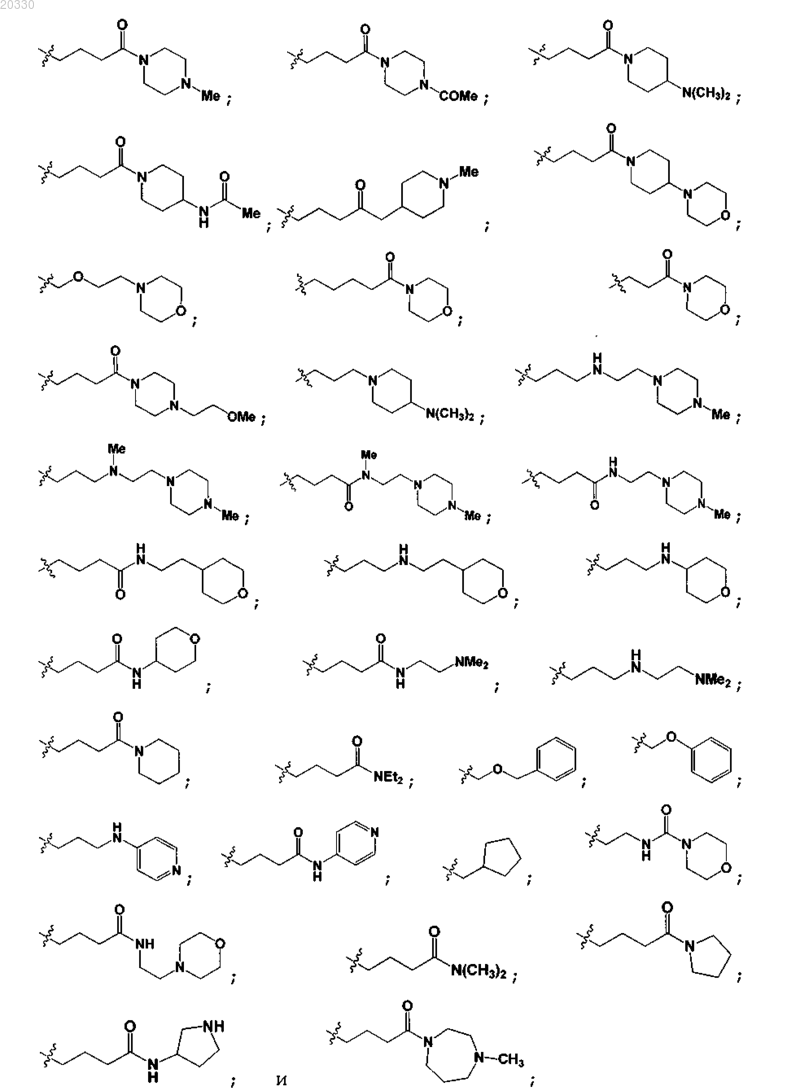
X обозначает фенил или C5-9 гетероарил, каждый из которых замещен R2a и R2b; причем R2a выбран из водорода, -C1-3 алкила, галогена, гидроксила, циано, -C1-3 галогеналкила, -C1-3 алкокси, -S(O)qC1-3 алкила, C(O)OC1-6алкила, -NC(O)NC1-6 алкила, -NC(O)C1-6 алкила, -C(O)NC1-6 алкила и -C(O)C1-6 алкила; и R2b выбран из водорода, C1-3 алкила, галогена, гидроксила, циано, -C1-3 галогеналкила, -C1-3 алкокси и -C0-6 алкил -S(O)qC1-3 алкила;
R3a обозначает гидроксил;
R3b выбран из водорода, галогена и -C1-3 алкокси;
R4 обозначает водород;
R5 обозначает водород;
q означает 0 или целое число 1 или 2;
или его фармацевтически приемлемая соль, включая все стереоизомеры, таутомеры и изотопные производные.
2. Соединение формулы (I) по п.1, в котором R1 обозначает водород или -CH2CH2CH2C(O)OH.
3. Соединение формулы (I) по п.1, в котором R1 обозначает -CH2CH2CH2C(O)N(CH2CH2OCH3)2.
4. Соединение формулы (I) по п.1, в котором R1 обозначает -CH2OCH2CH2OCH2CH2OCH3.
5. Соединение формулы (I) по любому из пп.1-4, в котором R2a выбран из группы, включающей хлор, фтор, циано, метокси, трифторметил и SO2CH3.
6. Соединение формулы (I) по любому из пп.1-5, в котором R2a находится в орто-положении.
7. Соединение формулы (I) по любому из пп.1-6, в котором R3 находится в мета-положении.
8. Соединение формулы (I) по любому из пп.1-7, в котором R3 находится в пара-положении.
9. Соединение формулы (I) по любому из пп.1-8, в котором гетероарил представляет собой С5-9-членное ароматическое карбоциклическое кольцо или бициклическую кольцевую систему, включающую 1 или более (например, 1, 2, 3 или 4) гетероатомов, независимо выбранных из О, N и S.
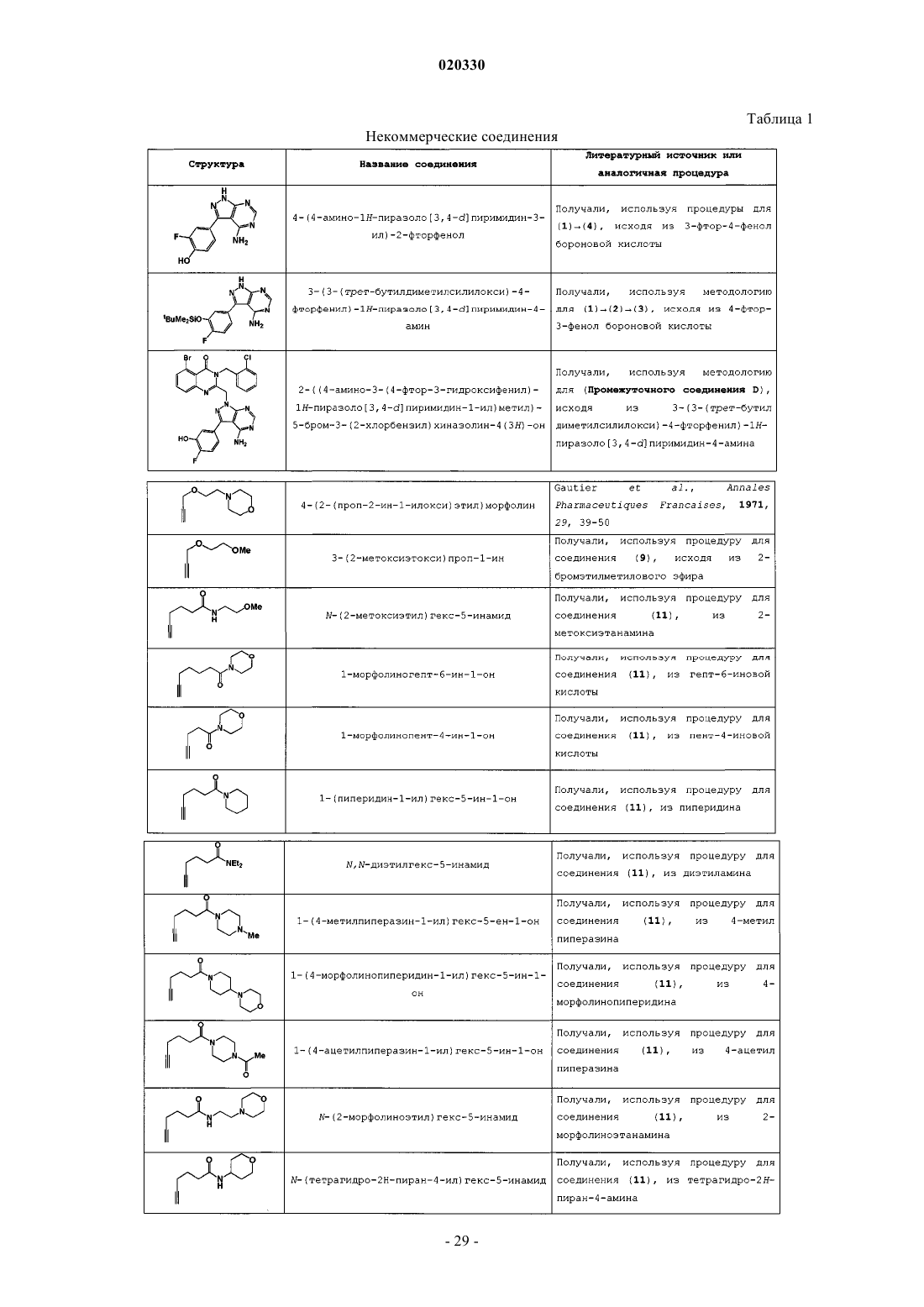
10. Соединение формулы (I) по п.1, причем соединение выбрано из следующих соединений:
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(3-(2-(2-метоксиэтокси)этокси)проп-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)гекс-5-иновая кислота;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
3-((2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-(3-(2-(2-гидроксиэтокси)этокси)проп-1-ин-1-ил)-4-оксохиназолин-3(4H)-ил)метил)бензонитрил;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(5-(циклопентиламино)пент-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(3-(2-морфолиноэтокси)проп-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(3-хлорбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(3-хлорбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(2-фторбензил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(2-фторбензил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(3-метоксибензил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(3-метоксибензил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(3-(трифторметил)бензил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(3-(трифторметил)бензил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(4-хлорбензил)-5-этинил хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(4-(метилсульфонил)бензил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(4-(метилсульфонил)бензил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(4-(трифторметил)бензил)хиназолин-4(3H)-он;
3-((2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-4-оксохиназолин-3(4H)-ил)метил)бензонитрил;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(3-(метилсульфонил)бензил)хиназолин-4(3H)-он;
3-((2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-4-оксохиназолин-3(4H)-ил)метил)бензонитрил;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(4-хлорбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(4-хлорбензил)-5-(3-метоксипроп-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(3-метоксибензил)-5-(3-метоксипроп-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(3-метоксипроп-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(4-(трифторметил)бензил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(3-(2-метоксиэтокси)проп-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-((5-метилизоксазол-3-ил)метил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-((5-метилизоксазол-3-ил)метил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(3-хлор-2-фторбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2,6-дифторбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(4-хлор-2-фторбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(3-фтор-4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-(3-метоксипроп-1-инил)-3-(3-(трифторметил)бензил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(4-фторбензил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(3-циклопентилпроп-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-(3-(бензилокси)проп-1-инил)-3-(2-хлорбензил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(5-гидроксипент-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(2-фтор-5-метоксибензил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(3,4-дихлорбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-бензил-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(2-трифторметилбензил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(4-метоксибензил)хиназолин-4(3H)-он;
4-((2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-4-оксохиназолин-3(4H)-ил)метил)бензонитрил;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-этинил-3-(2-фтор-4-метоксибензил)хиназолин-4(3H)-он;
1-(3-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)проп-2-инил)карбамид;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-фторбензил)-5-(3-(2-(2-метоксиэтокси)этокси)проп-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-фтор-3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-этинилхиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(3-феноксипроп-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-фторбензил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
6-(2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-(2-метоксиэтил)гекс-5-инамид;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(7-морфолино-7-оксогепт-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(5-морфолино-5-оксопент-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-((5-метилпиразин-2-ил)метил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-оксо-6-(пиперидин-1-ил)гекс-1-ин-1-ил)хиназолин-4(3H)-он;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N,N-диэтилгекс-5-инамид;
7-(2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)гепт-6-иновая кислота;
2-ацетамидо-N-(3-(2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)проп-2-ин-1-ил)ацетамид;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(3-метокси-5-(трифторметил)бензил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-метоксифенетил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(бензо[b]тиофен-2-илметил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-фтор-3-метоксибензил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
3-((2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)-4-оксохиназолин-3(4H)-ил)метил)метилбензоат;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-((1-метил-1H-пиразол-4-ил)метил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(бензофуран-5-илметил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-((2-метилтиазол-4-ил)метил)-5-(6-морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-(4-метилпиперазин-1-ил)-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-(4-морфолинопиперидин-1-ил)-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он;
5-(6-(4-ацетилпиперазин-1-ил)-6-оксогекс-1-ин-1-ил)-2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)хиназолин-4(3H)-он;
N-(4-(2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)бут-3-ин-1-ил)морфолин-4-карбоксамид;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-(5-(бис-(2-метоксиэтил)амино)пент-1-инил)-3-(2-хлорбензил)хиназолин-4(3H)-он;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-циклопентилгекс-5-инамид;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-(тетрагидро-2H-пиран-4-ил)гекс-5-инамид;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-(2-морфолиноэтил)гекс-5-инамид;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-(4-(2-метоксиэтил)пиперазин-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-(2-(диметиламино)этил)гекс-5-инамид;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-(пиридин-4-ил)гекс-5-инамид;
6-(2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-(пиридин-4-ил)гекс-5-инамид;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-(4-(диметиламино)пиперидин-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N,N-бис-(2-метоксиэтил)гекс-5-инамид;
6-(2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N,N-бис-(2-метоксиэтил)гекс-5-инамид;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-(2-(4-метилпиперазин-1-ил)этил)гекс-5-инамид;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-метил-N-(2-(4-метилпиперазин-1-ил)этил)гекс-5-инамид;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-изопропилгекс-5-инамид;
6-(2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-изопропилгекс-5-инамид;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N,N-диметилгекс-5-инамид;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-оксо-6-(пирролидин-1-ил)гекс-1-ин-1-ил)хиназолин-4(3H)-он;
6-(2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4-оксо-3,4-дигидрохиназолин-5-ил)-N-(пирролидин-3-ил)гекс-5-инамид;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-(3-(диметиламино)пирролидин-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-(3-(диметиламино)пирролидин-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он;
2-((4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-(4-метил-1,4-диазепан-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он,
2-((4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-(4-метил-1,4-диазепан-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он,
2-((4-амино-3-(4-гидрокси-3-метоксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-морфолино-6-оксогекс-1-инил)хиназолин-4(3H)-он;
или его фармацевтически приемлемая соль, включая все стереоизомеры, таутомеры и изотопные производные.
11. Фармацевтическая композиция, включающая соединение по любому из пп.1-10, в комбинации с 1 или более фармацевтически приемлемых разбавителей или носителей.
12. Применение соединения формулы (I) по любому из пп.1-10 в качестве лекарственного средства.
13. Применение соединения формулы (I) по любому из пп.1-10 в лечении или профилактике состояния, выбранного из
COPD (включая хронический бронхит и эмфизему), астмы, детской астмы, муковисцидоза, саркоидоза, идиопатического легочного фиброза, аллергического ринита, ринита, синусита, аллергического конъюнктивита, конъюнктивита, аллергического дерматита, контактного дерматита, псориаза, язвенного колита, воспаления сустава, вторичного по отношению к ревматоидному артриту или остеоартриту, ревматоидного артрита, панкреатита, кахексии, ингибирования роста и метастаза опухолей, включая немелкоклеточный рак легкого, рак молочной железы, рак желудка, колоректальный рак и злокачественную меланому.
14. Применение соединения формулы (I) по любому из пп.1-10 для получения лекарственного средства для лечения или профилактики состояния, выбранного из
COPD (включая хронический бронхит и эмфизему), астмы, детской астмы, муковисцидоза, саркоидоза, идиопатического легочного фиброза, аллергического ринита, ринита, синусита, аллергического конъюнктивита, конъюнктивита, аллергического дерматита, контактного дерматита, псориаза, язвенного колита, воспаления сустава, вторичного по отношению к ревматоидному артриту или остеоартриту, ревматоидного артрита, панкреатита, кахексии, ингибирования роста и метастаза опухолей, включая немелкоклеточный рак легкого, рак молочной железы, рак желудка, колоректальный рак и злокачественную меланому.
15. Способ лечения состояния, выбранного из
COPD (включая хронический бронхит и эмфизему), астмы, детской астмы, муковисцидоза, саркоидоза, идиопатического легочного фиброза, аллергического ринита, ринита, синусита, аллергического конъюнктивита, конъюнктивита, аллергического дерматита, контактного дерматита, псориаза, язвенного колита, воспаления сустава, вторичного по отношению к ревматоидному артриту или остеоартриту, ревматоидного артрита, панкреатита, кахексии, ингибирования роста и метастаза опухолей, включая немелкоклеточный рак легкого, рак молочной железы, рак желудка, колоректальный рак и злокачественную меланому,
который включает введение пациенту эффективного количества соединения формулы (I) по любому из пп.1-10 или фармацевтической композиции по п.11.
16. Промежуточное соединение формулы (VI)
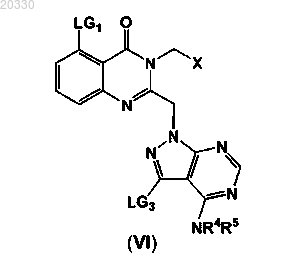
в которой LG1 и LG3 независимо обозначают галоген и X, R4 и R5 имеют значения, определенные в п.1.
17. Промежуточное соединение формулы (II)
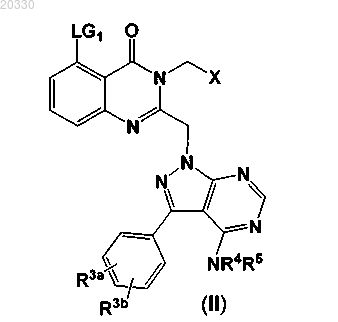
в которой LG1 обозначает галоген и X, R3a, R3b, R4 и R5 имеют значения, определенные в п.1.
18. Промежуточное соединение по п.16 или 17, в котором LG1 обозначает бром.
Текст
Кинг-Андервуд Джон, Ито Кадзухиро,Мюррей Питер Джон, Харди Джордж,Брукфилд Фредерик Артур, Браун Кристофер Джон (GB) и к композициям, включающим эти соединения, и к применению этих соединений и их композиций в лечении, например в лечении воспалительных заболеваний, в частности респираторного воспалительного заболевания. Изобретение также распространяется на способы получения указанных соединений. Область изобретения Изобретение относится к соединениям, которые являются ингибиторами фосфоинозитид 3-киназ (киназы PI3). В особенности изобретение относится к соединениям, которые ингибируют подтип дельта киназы PI3 и, в некоторых случаях, кроме того, подтипы гамма и альфа, и к их применению в терапии, включая применение в фармацевтических комбинациях, особенно в лечении воспалительных заболеваний, включая воспалительные заболевания легкого, такие как COPD и астма. Раскрытие также распространяется на способы получения указанных соединений и фармацевтические композиции, включающие эти соединения. Уровень техники Липидкиназы катализируют фосфорилирование липидов с получением веществ, участвующих в регуляции разнообразных физиологических процессов, включая миграцию и адгезию клеток. PI3-киназы принадлежат к этому классу ферментов и представляют собой мембраносвязанные белки, которые катализируют фосфорилирование липидов, которые сами связаны с мембранами клеток. Изозим дельта PI3 киназы(киназа PI3 ) является одной из четырех изоформ типа 1 киназы PI3, ответственных за формирование различных 3'-фосфорилированных фосфоинозитидов, которые опосредуют клеточную трансдукцию сигналов и участвуют во множестве клеточных процессов, таких как воспаление, трансдукция сигналов факторов роста, злокачественная трансформация и иммунитет (см. Review by Rameh, L.E. andCantley, L.C., J. Biol. Chem., 1999, 274:8347-8350). Участие киназ PI3 в контроле воспаления было подтверждено в нескольких моделях с использованием ингибиторов пан-PI3 киназ, таких как LY-294002 и вортманнин (Ito, K. et al., J. Pharmacol. Exp.Ther., 2007, 321:1-8). Недавние исследования проводили, используя либо селективные ингибиторы киназы PI3, либо на нокаут-мышах, у которых отсутствовала специфическая изоформа фермента. Эти исследования продемонстрировали роль путей, контролируемых ферментами киназы PI3, в воспалении. Было обнаружено, что селективный ингибитор киназы PI3IC-87114 ингибирует гиперчувствительность дыхательных путей, высвобождение IgE, экспрессию провоспалительных цитокинов, аккумуляцию воспалительных клеток в легком и сосудистую проницаемость у сенсибилизированных овальбумином и подвергнутых провокации овальбумином мышей (Lee, K.S. et al., J. Allergy Clin. Immunol., 2006, 118:403-409,and Lee, K.S. et al., FASEB J., 2006, 20:455-65). Кроме того, IC-87114 снижал аккумуляцию нейтрофилов в легких мышей и функцию нейтрофилов, стимулируемую TNF (Sadhu, C. et al., BioCHem. Biophys. Res.Commun., 2003, 308:764-9). Изоформакиназы PI3 активируется инсулином и другими факторами роста,а также сигналами белка, связанного с G-белком, и воспалительными цитокинами. Недавно сообщалось,что двойной ингибитор / киназ PI3 TG100-115 ингибирует легочную эозинофилию, аккумуляцию интерлейкина 13, а также муцина и гиперчувствительность дыхательных путей на мышиной модели при введении в форме аэрозоля. Те же самые авторы также сообщали, что соединение было в состоянии ингибировать легочный нейтрофиллез, вызываемый как LPS, так и сигаретным дымом (Doukas, J. et al., J.Pharmacol. Exp. Ther., 2009, 328:758-765). Поскольку она также активируется окислительным стрессом, киназа PI3, изоформа , вероятно,окажется релевантной как мишень для терапевтического вмешательства при тех заболеваниях, в которых участвует высокий уровень окислительного стресса. Даунстрим-медиаторы трансдукции сигналов киназы PI3 включают Akt (серин/треонин протеинкиназа) и мишень рапамицина у млекопитающих, ферментrmTOR. В недавней работе было сделано предположение, что активация киназы PI3 , приводящая к фосфорилированию Akt, может вызывать состояние резистентности к кортикостероидам в обычно чувствительных к кортикостероидам клетках (To, Y. et al., Am. J. Respir. Crit. Care Med., 2010, 182:897-904). Эти наблюдения привели к гипотезе, что этот сигнальный каскад может быть одним механизмом, ответственным за нечувствительность к кортикостероидам при воспалении, наблюдаемом в легких пациентов,страдающих COPD, а также курящих астматиков, таким образом подвергая их легкие повышенному окислительному стрессу. Действительно, было сделано предположение, что теофиллин, соединение, используемое в лечении как COPD, так и астмы, обращает нечувствительность к стероидам через механизмы, включающие взаимодействие с путями, контролируемыми киназой PI3(To, Y. et al., Am. J. Respir.Crit. Care Med., 2010, 182:897-904). В настоящее время основным лечением как астмы, так и COPD является ингаляционная терапия с использованием комбинации кортикостероидов, мускариновых антагонистов и 2-агонистов, являющейся, согласно клинической оценке, адекватной. Один способ ответить на неразрешенные медицинские потребности при COPD и астме состоит в том, чтобы идентифицировать новые терапевтические средства, например, подходящие для использования в качестве лекарственных средств для ингаляции, которые имеют потенциал по обеспечению значительной выгоды при использовании как монотерапии или в комбинации с одним или более лекарственными средствами из этих трех фармакологических классов. Поэтому сохраняется потребность идентифицировать и разрабатывать изоформ-селективные ингибиторы киназы PI3, которые имели бы потенциал по обеспечению повышенной терапевтической эффективности при астме, COPD и других воспалительных заболеваниях. Сущность изобретения Изобретение относится к соединению формулы (I)R1 обозначает H, насыщенную или ненасыщенную, разветвленную или неразветвленную C1-15 алкильную цепь, в которой 1 или более атомов углерода (например, 1, 2 или 3 атома углерода, предпочтительно 1 или 2, в частности 1) могут быть заменены гетероатомом, выбранным из O, N, S(O)p (например,группа CH2 может быть заменена O, или NH, или S, или SO2 или группа -CH3 на конце цепи или на разветвлении может быть заменена OH или NH2), причем указанная цепь может быть замещена 1 или более группами (например, от 1 до 3, например 2 группами), независимо выбранными из оксо, галогена, арила,гетероарила, карбоциклила или гетероциклила, причем каждый арил, гетероарил, карбоциклил или гетероциклил несет от 0 до 3 заместителей, выбранных из галогена, гидроксила, -C1-6 алкила, -C1-6 алкокси, -C2-3 алкоксиOC1-3 алкила, -C2-3 алкилOC1-3 алкила, -C1-3 гидроксиалкила, -C1-6 галогеналкила, амино, -C1-4 моно- или -C2-8 диалкиламино, -C1-4 моно- или -C2-8 диациламино, -C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилS(O)pNR6R7, -C0-6 алкилNR8C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилC(O)OC0-6 алкила, -NR8C0-6 алкилC(O)NR6R7, -NR8C0-6 алкилC(O)C0-6 алкила, -С 0-6 алкилC(O)NR6R7 и -C0-6 алкилC(O)C1-6 алкила; и/или один арил, гетероциклил или карбоциклил;X обозначает C6-10 арил или C5-9 гетероарил, каждый из которых замещен R2a и R2b; причем R2a выбран из водорода, -C1-3 алкила, галогена, гидроксила, циано, -C1-3 галогеналкила, -C1-3 алкокси, -C2-3 алкоксиOC1-3 алкила, -C2-3 алкилOC1-3 алкила, -C1-3 гидроксиалкила, -C0-6 алкилS(O)qC1-3 алкила, -C0-6 алкилS(O)pNR6R7, -C0-6 алкилNR8 С 0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилC(O)OH, -C0-6 алкилC(O)OC1-6 алкила, -NR8C0-6 алкилC(O)NR6R7, -NR8C0-6 алкилC(O)C1-6 алкила, -C0-6 алкилC(O)NR6R7 иR4 обозначает водород или -C1-3 алкил;R5 обозначает водород или -C1-3 алкил;R6 обозначает водород или -C1-6 алкил;R7 обозначает водород или -C1-6 алкил;R8 обозначает водород или -C1-6 алкил;p означает 0 или целое число 1 или 2;q означает 0 или целое число 1 или 2; или к его фармацевтически приемлемой соли, включая все стереоизомеры, таутомеры и изотопные производные. В одном варианте осуществления R1 обозначает Н, насыщенную или ненасыщенную, разветвленную или неразветвленную C1-12 алкильную цепь, в которой 1 или более атомов углерода (например, 1, 2 или 3 атома углерода, предпочтительно 1 или 2, в частности 1) могут быть заменены гетероатомом, выбранным из O, N, S(O)p (например, группа CH2 может быть заменена O, или NH, или S, или SO2 или группа -CH3 на конце цепи или на разветвлении может быть заменена ОН или NH2), причем указанная цепь может быть замещена 1 или более группами (например, от 1 до 3, например 2 группами), независимо выбранными из оксо, галогена, арила, гетероарила, карбоциклила или гетероциклила, причем каждый арил, гетероарил, карбоциклил или гетероциклил несет от 0 до 3 заместителей, выбранных из галогена, гидроксила, -C1-6 алкила, -C1-6 алкокси, -C2-3 алкилOC1-3 алкила, -C2-3 алкоксиOC1-3 алкила, -C1-3 гидроксиалкила, -C1-6 галогеналкила, амино, -C1-4 моноили -C2-8 диалкиламино, -C1-4 моно- или -C2-8 диациламино, -C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилS(O)pNR6R7, -C0-6 алкилNR8C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилC(O)OC0-6 алкила, NR8C0-6 алкилC(O)NR6R7, -NR8C0-6 алкилC(О)C0-6 алкила, -С 0-6 алкилC(O)NR6R7 и -C0-6 алкилC(O)C1-6 алкила; и/или один арил, гетероциклил или карбоциклил. В одном варианте осуществления изобретение относится к соединению формулы (I)R1 обозначает Н, насыщенную или ненасыщенную, разветвленную или неразветвленную C1-10 алкильную цепь, в которой 1 или более атомов углерода (например, 1, 2 или 3 атома углерода, предпочтительно 1 или 2, в частности 1) могут быть заменены гетероатомом, выбранным из О, N, S(O)p (например,группа CH2 может быть заменена О, или NH, или S, или SO2 или группа -CH3 на конце цепи или на разветвлении может быть заменена ОН или NH2), причем указанная цепь может быть замещена 1 или более группами (например, от 1 до 3, например 2 группами), независимо выбранными из оксо, галогена, арила,гетероарила, карбоциклила или гетероциклила, причем каждый арил, гетероарил, карбоциклил или гетероциклил несет от 0 до 3 заместителей, выбранных из галогена, -C1-6 алкила, -C1-6 алкокси, -C2-3 алкоксиOC1-3 алкила,-C1-6 галогеналкила, амино, -C1-4 моно- или -C2-8 диалкиламино, -C1-4 моно- или -C2-8 диациламино, -C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилS(O)pNR6R7, -C0-6 алкилNR8C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилC(О)OC0-6 алкила, -NC0-6 алкилC(O)NR6R7, -NC0-6 алкилC(O)C0-6 алкила, -C0-6 алкилC(O)NR6R7 иX обозначает C6-10 арил или C5-9 гетероарил, каждый из которых замещен R2a и, в ряде случаев, R2b,причем R2a обозначает водород, -C1-3 алкил, галоген, гидроксил, циано, -C1-3 галогеналкил, -C1-3 алкокси,-C2-3 алкоксиOC1-3 алкил, -C1-3 гидроксиалкил, -C0-6 алкилS(O)qC1-3 алкил, -C0-6 алкилS(O)pNR6R7, -C0-6 алкилNR8C0-6 алкилS(O)pC1-6 алкил, -C0-6 алкилC(O)OH, -C0-6 алкилC(O)OC1-6 алкил, -NC0-6 алкилС(O)NR6R7, -NR8C0-6 алкилC(O)C1-6 алкил, -C0-6 алкилC(O)NR6R7 и -C0-6 алкилC(O)C1-6 алкил; иR4 обозначает водород или -C1-3 алкил;R5 обозначает водород или -C1-3 алкил;R6 обозначает водород или -C1-6 алкил;R7 обозначает водород или -C1-6 алкил;R8 обозначает водород или -C1-6 алкил;p означает 0 или целое число 1 или 2;q означает 0 или целое число 1 или 2; или к его фармацевтически приемлемой соли, включая все стереоизомеры, таутомеры и изотопные производные. В одном варианте осуществления настоящее раскрытие относится к соединению формулы (IA')R1 обозначает H, насыщенную или ненасыщенную, разветвленную или неразветвленную C1-15 алкильную цепь, в которой 1 или более атомов углерода (например, 1, 2 или 3 атома углерода, предпочтительно 1 или 2, в частности 1) могут быть заменены гетероатомом, выбранным из O, N, S(O)p (например,группа CH2 может быть заменена О, или NH, или S, или SO2 или группа -CH3 на конце цепи или на раз-3 020330 ветвлении может быть заменена ОН или NH2), причем указанная цепь может быть замещена 1 или более группами (например, от 1 до 3, например 2 группами), независимо выбранными из оксо, галогена, арила,гетероарила, карбоциклила или гетероциклила, причем каждый арил, гетероарил, карбоциклил или гетероциклил несет от 0 до 3 заместителей, выбранных из галогена, гидроксила, -C1-6 алкила, -C1-6 алкокси, -C2-3 алкоксиOC1-3 алкила, -C2-3 алкилOC1-3 алкила, -C1-3 гидроксиалкила, -C1-6 галогеналкила, амино, -C1-4 моноили -C2-8 диалкиламино, -C1-4 моно- или -C2-8 диациламино, -C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилS(O)pNR6R7, -C0-6 алкилNR8C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилC(O)OC0-6 алкила, -NR8C0-6 алкилС(O)NR6R7, -NR8C0-6 алкилC(O)C0-6 алкила, -C0-6 алкилC(O)NR6R7 и -C0-6 алкилC(O)C1-6 алкила; и/или один арил, гетероциклил или карбоциклил;R4 обозначает водород или -C1-3 алкил;R5 обозначает водород или -C1-3 алкил;R6 обозначает водород или -C1-6 алкил;R7 обозначает водород или -C1-6 алкил;R8 обозначает водород или -C1-6 алкил;p означает 0 или целое число 1 или 2;q означает 0 или целое число 1 или 2; или к его фармацевтически приемлемой соли, включая все стереоизомеры, таутомеры и изотопные производные. В одном варианте осуществления настоящее раскрытие относится к соединению формулы (IA)R1 обозначает H, насыщенную или ненасыщенную, разветвленную или неразветвленную C1-15 алкильную цепь (такую, как C1-12 алкильная цепь или C1-10 алкильная цепь), в которой 1 или более атомов углерода (например, 1, 2 или 3 атома углерода, предпочтительно 1 или 2, в частности 1) могут быть заменены гетероатомом, выбранным из О, N, S(O)p (например, группа СН 2 может быть заменена О, илиNH, или S, или SO2 или группа -CH3 на конце цепи или на разветвлении может быть заменена OH илиNH2), причем указанная цепь может быть замещена 1 или более группами, независимо выбранными из оксо, галогена, арила, гетероарила, карбоциклила или гетероциклила, причем каждый арил, гетероарил,карбоциклил или гетероциклил несет от 0 до 3 заместителей, выбранных из галогена, -C1-6 алкила, -C1-6 алкокси, -C2-3 алкоксиOC1-3 алкила, -C1-6 галогеналкила, амино, -C1-4 моно- или -C2-8 диалкиламино, -C1-4 моно- или -C2-8 диациламино,-C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилS(O)pNR6R7, -C0-6 алкилNR8C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилC(O)OC0-6 алкила, -NC0-6 алкилC(O)NR6R7, -NC0-6 алкилC(O)C0-6 алкила, -C0-6 алкилC(O)NR6R7 и -C0-6 алкилC(O)C1-6 алкила; и/или один арил, гетероциклил или карбоциклил;R4 обозначает водород или -C1-3 алкил;R5 обозначает водород или -C1-3 алкил;R6 обозначает водород или -C1-6 алкил;R7 обозначает водород или -C1-6 алкил;R8 обозначает водород или -C1-6 алкил;p означает 0 или целое число 1 или 2;q означает 0 или целое число 1 или 2; или к его фармацевтически приемлемой соли, включая все стереоизомеры, таутомеры и изотопные производные. Изобретение относится к соединению формулы (IB')R1 обозначает Н, насыщенную или ненасыщенную, разветвленную или неразветвленную C1-15 алкильную цепь, в которой 1 или более атомов углерода (например, 1, 2 или 3 атома углерода, предпочтительно 1 или 2, в частности 1) могут быть заменены гетероатомом, выбранным из О, N, S(O)p (например,группа CH2 может быть заменена О, или NH, или S, или SO2 или группа -CH3 на конце цепи или на разветвлении может быть заменена ОН или NH2), причем указанная цепь может быть замещена 1 или более группами (например, от 1 до 3, например 2 группами), независимо выбранными из оксо, галогена, арила,гетероарила, карбоциклила или гетероциклила, причем каждый арил, гетероарил, карбоциклил или гетероциклил несет от 0 до 3 заместителей, выбранных из галогена, гидроксила, -C1-6 алкила, -C1-6 алкокси, -C2-3 алкоксиOC1-3 алкила, -C2-3 алкилOC1-3 алкила, -C1-3 гидроксиалкила, -C1-6 галогеналкила, амино, -C1-4 моноили -C2-8 диалкиламино, -C1-4 моно- или -C2-8 диациламино, -C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилS(O)pNR6R7, -C0-6 алкилNR8 С 0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилC(O)OC0-6 алкила, -NR8C0-6 алкилC(O)NR6R7, -NR8C0-6 алкилC(O)C0-6 алкила, -C0-6 алкилC(O)NR6R7 и -C0-6 алкилC(O)C1-6 алкила; и/или один арил, гетероциклил или карбоциклил;R4 обозначает водород или -C1-3 алкил;R5 обозначает водород или C1-3 алкил;R6 обозначает водород или -C1-6 алкил;R7 обозначает водород или -C1-6 алкил;R8 обозначает водород или -C1-6 алкил;p означает 0 или целое число 1 или 2;q означает 0 или целое число 1 или 2,или к его фармацевтически приемлемой соли, включая все стереоизомеры, таутомеры и изотопные производные. Изобретение относится к соединению формулы (IB)R1 обозначает Н, насыщенную или ненасыщенную, разветвленную или неразветвленную C1-15 алкильную цепь (такую, как C1-12 алкильная цепь или C1-10 алкильная цепь), в которой 1 или более атомов углерода (например, 1, 2 или 3 атома углерода, предпочтительно 1 или 2, в частности 1) могут быть заменены гетероатомом, выбранным из О, N, S(O)p (например, группа СН 2 может быть заменена О, илиNH, или S, или SO2 или группа -CH3 на конце цепи или на разветвлении может быть заменена ОН илиNH2), причем указанная цепь может быть замещена 1 или более группами, независимо выбранными из оксо, галогена, арила, гетероарила, карбоциклила или гетероциклила, причем каждый арил, гетероарил,карбоциклил или гетероциклил несет от 0 до 3 заместителей, выбранных из галогена, -C1-6 алкила, -C1-6 алкокси, -C2-3 алкоксиOC1-3 алкила, -C1-6 галогеналкила, амино, -C1-4 моно- или -C2-8 диалкиламино, -C1-4 моно- или -С 2-8 диациламино,-C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилS(O)pNR6R7, -C0-6 алкилNR8C0-6 алкилS(O)pC1-6 алкила, -C0-6 алкилC(O)OC0-6 алкила, -NC0-6 алкилC(O)NR6R7, -NC0-6 алкилC(O)C0-6 алкила, -C0-6 алкилC(O)NR6R7 и -C0-6 алкилC(O)C1-6 алкила; и/или один арил, гетероциклил или карбоциклил;R4 обозначает водород или -C1-3 алкил;R5 обозначает водород или -C1-3 алкил;R6 обозначает водород или -C1-6 алкил;R7 обозначает водород или -C1-6 алкил;R8 обозначает водород или -C1-6 алкил;p означает 0 или целое число 1 или 2;q означает 0 или целое число 1 или 2; или к его фармацевтически приемлемой соли, включая все стереоизомеры, таутомеры и изотопные производные. В одном варианте осуществления изобретение относится к соединению формулы (IC) в которой R1, R3a, R3b, R4 и R5 имеют значения, определенные выше для соединений формулы (I). В одном варианте осуществления изобретение относится к соединению формулы (ID) в которой R1, R2a, R2b, R3a, R3b, R4 и R5 имеют значения, определенные выше для соединений формулы (I). В одном варианте осуществления изобретение относится к соединению формулы (IE) в которой R1, R3a, R3b, R4 и R5 имеют значения, определенные выше для соединений формулы (I). В одном варианте осуществления изобретение относится к соединению формулы (IF) в которой R1, R2a, R3a, R3b, R4 и R5 имеют значения, определенные выше для соединений формулы (I). В одном варианте осуществления изобретение относится к соединению формулы (IG) в которой R1, R2a, R3a, R3b, R4 и R5 имеют значения, определенные выше для соединений формулы (I). Соединения согласно настоящему раскрытию являются, по меньшей мере, ингибиторами дельтаPI3K. Некоторые соединения согласно раскрытию могут быть ингибиторами альфа и дельта PI3K. Некоторые соединения согласно раскрытию могут быть ингибиторами дельта и гамма PI3K. Некоторые соединения могут быть ингибиторами изозима альфа и гамма. Другие соединения могут быть ингибиторами подтипа альфа, дельта и гамма. Предложено, чтобы различные биологические профили могли быть связаны с этими различными профилями ингибирования, что может быть выгодным в путях нацеливания для различных заболеваний. Ингибитор в рамках изобретения относится к соединению, которое уменьшает (например, по меньшей мере на 50%) или устраняет биологическую активность мишени, например дельта PI3K, в ферментном тесте in vitro. Соединения согласно настоящему раскрытию активны в клеточных системах скрининга и таким образом демонстрируют, что они обладают подходящими свойствами для проникновения в клетки. Общая ссылка на соединения формулы (I) включает ссылку на соединения формул (IA)-(IG), если из контекста не следует иное. Алкил в рамках изобретения относится к алкилу с прямой или разветвленной цепью, такому как,без ограничения, метил, этил, пропил, изопропил, бутил и трет-бутил. В одном варианте осуществления алкил относится к алкилу с прямой цепью. Алкокси в рамках изобретения относится к алкокси с прямой или разветвленной цепью, например метокси, этокси, пропокси, бутокси. Алкокси в рамках изобретения также распространяется на варианты осуществления, в которых атом кислорода расположен в пределах алкильной цепи, например-(CH2)nOCH3-. В одном варианте осуществления алкокси связан с остатком молекулы через кислород. В одном варианте осуществления алкокси связан с остатком молекулы через углерод. В одном варианте осуществления раскрытие относится к алкокси с прямой цепью.-C2-3 АлкоксиOC1-3 алкил в рамках изобретения относится к -C2-3 алкокси, связанному с остатком молекулы через кислород с образованием цепи кислород-алкилен-кислород-алкил. Карбоциклил в рамках изобретения относится к насыщенным или частично насыщенным C3-10 карбоциклическим кольцевым системам, например циклопропилу, циклобутилу, циклопентилу и циклогексилу. Гетероарил представляет собой С 5-9-членное ароматическое карбоциклическое кольцо или бициклическую кольцевую систему, включающую 1 или более (например, 1, 2, 3 или 4) гетероатомов, независимо выбранных из О, N и S. Примеры гетероарилов включают пиррол, оксазол, тиазол, изотиазол, имидазол, пиразол, изоксазол, пиридазин, пиримидин, пиразин, бензотиофен, бензофуран или 1,2,3- и 1,2,4 триазол. В бициклической кольцевой системе определение гетероарила будет удовлетворено, если по меньшей мере одно кольцо содержит гетероатом и по меньшей мере одно кольцо является ароматическим. Гетероарил может быть связан с остатком молекулы через карбоциклическое кольцо или кольцо,включающее гетероатом. В бициклической системе определение ароматического будет удовлетворено ароматической природой по меньшей мере одного кольца в системе. Гетероциклические группы в рамках изобретения относятся к 5-10-членным кольцевым системам,которые являются насыщенными или частично ненасыщенными и которые являются неароматическими,включающим 1 или более (например, 1, 2 или 3, в частности 1 или 2) гетероатомов, независимо выбранных из О, N и S, например 5-, или 6-, или 7-членным кольцам, включая пирролидин, тетрагидрофуран,тетрагидротиофен, пиперидин, пиперазин, морфолин, 1,4-диоксан, пирролидин и оксоимидазолидин,таким как пирролидин, тетрагидрофуран, тетрагидротиофен, пиперидин, пиперазин, морфолин и 1,4 диоксан, и в частности пиперидин, пиперазин и морфолин. Примером насыщенных 7-членных гетероциклических колец является 1,4-диазепановое кольцо, и примером частично ненасыщенных 7-членных колец является 2,3,4,5-тетрагидро-1,4-оксазепин. Гетероциклическая группа может быть связана, например, с алкильной цепью, через углерод или подходящий гетероатом, такой как N. Оксо в рамках изобретения относится к группе =O, и эта группа может быть присоединена к атому углерода с образованием C=O или гетероатому с образованием, например, S=O или SO2. Галогеналкил в рамках изобретения относится к группе, имеющей от 1 до 6 атомов галогена, например от 1 до 5 атомов галогена. В одном варианте осуществления галогеналкил представляет собой пергалогеналкил, например перфторалкил, такой как CF2CF3 и CF3. Галоген представляет собой бром, хлор или фтор.C1-4 моно- или C2-8 диацил относятся к -C(O)C1-4 алкилу и -(COC1-4 алкил)2, соответственно. Арил в рамках изобретения относится, например, к C6-14 моно- или полициклическим группам (таким, как C6-10 моно- или бициклические группы), имеющим от 1 до 3 колец, причем по меньшей мере 1 кольцо является ароматическим, включая фенил, нафтил, антраценил, 5,6,7,8-тетрагидронафтил и т.п.,такой как фенил и нафтил. В одном варианте осуществления X обозначает фенил. В одном варианте осуществления X обозначает C5-9-членный гетероарил. В одном варианте осуществления X обозначает пиразинил, такой как пиразин-2-ил, в частности метилпиразин-2-ил, более конкретно 5-метилпиразин-2-ил. В одном варианте осуществления X обозначает бензотиофенил, например бензотиофен-2-ил. В одном варианте осуществления X обозначает бензофуранил, например бензофуран-5-ил. В одном варианте осуществления X обозначает тиазолил, например тиазол-4-ил. В одном варианте осуществления X обозначает изоксазолил, например изоксазол-3-ил, такой как 5 метилизоксазол-3-ил. В R1 подходящий гетероатом может заменить любой атом углерода, включая связующий атом углерода, атом углерода разветвления или концевой атом углерода, и атом(ы) водорода может(гут) заполнить оставшиеся валентности, если требуется. В одном варианте осуществления R1 обозначает Н. В другом варианте осуществления R1 обозначает разветвленную или неразветвленную C1-10 алкильную цепь, в которой по меньшей мере 1 атом углерода (например, 1, 2 или 3 атома углерода) заменен кислородом, например С 9 алкил, включающий 1, 2 или 3 атома кислорода, такой какCH2OCH2CH2OCH2CH2OCH3. В одном варианте осуществления R1 обозначает -CH2OCH3. В одном варианте осуществления R1 обозначает -CH2CH2CH2OH. В одном варианте осуществления R1 обозначает CH2OCH2CH2OCH2CH2OH. В одном варианте осуществления R1 несет по меньшей мере 1 оксозаместитель. В одном варианте осуществления R1 обозначает -CH2NHCONH2.-8 020330 В одном варианте осуществления R1 несет по меньшей мере 1 карбоциклическую группу в качестве заместителя. В одном варианте осуществления R1 несет по меньшей мере 1 оксозаместитель и карбоциклический заместитель, например циклопентил или циклогексил, связанный с атомом углерода, несущим оксозаместитель, такой как фрагмент В одном варианте осуществления R1 включает В одном варианте осуществления R1 включает В одном варианте осуществления R1 включает В одном варианте осуществления R1 включает В одном варианте осуществления R1 несет по меньшей мере 1 гетероциклический заместитель. В одном варианте осуществления R1 несет 1 оксозаместитель и 1 гетероциклический заместитель,например гетероциклическая группа связана с атомом углерода, несущим оксозаместитель, такой как R1,включающий -C(O)морфолинил, причем морфолинил может быть связан через N, в частности фрагмент В одном варианте осуществления R1 несет 1 оксозаместитель и 1 гетероциклический заместитель,например гетероциклическая группа связана с атомом углерода, несущим оксозаместитель, причем сама указанная гетероциклическая группа несет C1-6 алкильный или -C(O)C1-6 алкильный заместитель, такой как R1, включающий -C(O)пиперидинилC1-6 алкил или -C(O)пиперидинилC(O)C1-6 алкил, причем пиперидинил может быть связан через N, в особенности фрагменты В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает-9 020330 В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 несет 1 оксозаместитель и 1 гетероциклический заместитель,например гетероциклическая группа связана с атомом углерода, несущим оксозаместитель, причем сама указанная гетероциклическая группа несет гетероциклическую группу в качестве заместителя, такого какR1, включающий -C(O)пиперидинилморфолинил, причем морфолинил может быть связан через N, в частности фрагмент В одном варианте осуществления R1 включает В одном варианте осуществления R1 включает В одном варианте осуществления R1 включает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 включает карбоновую кислоту, например C1-3 алкиленСО 2 Н,такую как фрагмент -CH2CH2CH2CO2H или, альтернативно, -CH2CH2CH2CH2CO2H. В одном варианте осуществления R1 обозначает CH2CH2CH2C(O)NHCH(CH3)2. В одном варианте осуществления R1 обозначает -CH2CH2CH2C(O)(CH3)2. В одном варианте осуществления R1 обозначает -CH2CH2CH2NHCH2CH2OCH3. В одном варианте осуществления R1 обозначает CH2CH2CH2N(CH2CH2OCH3)2. В одном варианте осуществления R1 обозначает CH2CH2CH2C(O)N(CH2CH2OCH3)2. В одном варианте осуществления R1 обозначает CH2NHC(O)CH2NHC(O)CH3. В одном варианте осуществления R1 обозначает CH2CH2CH2C(O)NHCH2CH2OCH3. В одном варианте осуществления R1 включает В одном варианте осуществления R1 включает В одном варианте осуществления R1 обозначает В одном варианте осуществления R1 обозначает В одном варианте осуществления R2a расположен в орто-положении. В одном варианте осуществления R2a расположен в мета-положении. В одном варианте осуществления R2a расположен в пара-положении. В одном варианте осуществления R2a обозначает C1-3 алкил, галоген, циано, C1-3 галогеналкил, C1-3 алкокси, S(O)qC1-3 алкил, -C(O)OC1-6 алкил, -NC(O)NC1-6 алкил, -NC(O)C1-6 алкил, -C(O)NC1-6 алкил и-C(O)C1-6 алкил. В одном варианте осуществления R2a выбран из группы, включающей метил, хлор, фтор, циано, метокси, трифторметил и SO2CH3. В одном варианте осуществления R2a обозначает хлор. В одном варианте осуществления R2a обозначает фтор. В одном варианте осуществления R2a обозначает циано.- 11020330 В одном варианте осуществления R2a обозначает метокси. В одном варианте осуществления R2a обозначает метил. В одном варианте осуществления R2a обозначает SO2CH3. В одном варианте осуществления R2a обозначает -C(O)OCH3. В одном варианте осуществления R2a обозначает CF3. В одном варианте осуществления R2b обозначает водород. В одном варианте осуществления R2b обозначает хлор. В одном варианте осуществления R2b обозначает -OCH3-. В одном варианте осуществления R2a и R2b находятся в положениях 2,3, или 2,4, или 3,4, или 3,5,соответственно. В одном варианте осуществления R2a обозначает CF3 и R2b обозначает метокси.R3a находится предпочтительно в орто-, мета- или пара-положении, таком как орто- или параположение. В одном варианте осуществления R3b обозначает водород. В одном варианте осуществления R3b обозначает фтор или хлор, например, в положении 4. В одном варианте осуществления R3a и R3b находятся в положении 3,4, соответственно. В одном варианте осуществления R4 обозначает H. В одном варианте осуществления R5 обозначает H. В одном варианте осуществления p=2. В одном варианте осуществления q=2. В одном варианте осуществления изобретение относится к фармацевтически приемлемой соли присоединения с кислотой соединения формулы (I). Фармацевтически приемлемые соли присоединения с кислотой, как упомянуто выше, включают терапевтически активные нетоксичные формы соли присоединения с кислотой, которые могут образовывать соединения формулы (I). Эти фармацевтически приемлемые соли присоединения с кислотой могут быть получены обработкой формы основания такой подходящей кислотой. Подходящие кислоты включают, например, неорганические кислоты, такие как галогеноводородные кислоты, например хлористоводородная или бромисто-водородная кислота, серная, азотная, фосфорная и т.п. кислоты; или органические кислоты, такие как, например, уксусная, пропионовая, гидроксиуксусная, молочная, пировиноградная, щавелевая (т.е. этановая дикислота), малоновая, янтарная (т.е. бутановая дикислота), малеиновая,фумаровая, яблочная, винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, птолуолсульфоновая, цикламовая, салициловая, парааминосалициловая, памовая кислоты и т.п. Примеры солей соединения (I) включают все фармацевтически приемлемые соли, такие как, без ограничения, соли присоединения с неорганическими кислотами, такие как соли HCl и HBr, и соли присоединения с органическими кислотами, такие как соль метансульфоновой кислоты. Раскрытие также распространяется на сольваты соединений по изобретению. Примеры сольватов включают гидраты. Соединения согласно раскрытию включают такие, в которых определенный атом представляет собой природный или неприродный изотоп. В одном варианте осуществления изотоп представляет собой стабильный изотоп. Таким образом, соединения согласно раскрытию включают, например, такие, которые содержат 1 или более атомов дейтерия вместо атомов водорода, и т.п. Соединения, описанные здесь, могут включать 1 или более хиральных центров, и раскрытие включает рацематы, оба энантиомера (например, каждый из которых, в основном, не содержит другого энантиомера) и все возможные стереоизомеры. В одном варианте осуществления одна энантиомерная форма присутствует в очищенной форме, которая, в основном, не содержит соответствующей энантиомерной формы. Раскрытие также распространяется на все полиморфные формы соединений, определенных здесь. В одном аспекте соединение формулы (I) представляет собой одно из следующих соединений: 2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5 этинилхиназолин-4(3H)-он; 2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(3(2-(2-метоксиэтокси)этокси)проп-1-ин-1-ил)хиназолин-4(3H)-он; 2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6 морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)гекс-5-иновая кислота; 2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6 морфолино-6-оксогекс-1-ин-1-ил)хиназолин-4(3H)-он; 3-2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-(3-(2-(2-гидроксиэтокси)этокси)проп-1-ин-1-ил)-4-оксохиназолин-3(4H)-ил)метил)бензонитрил; 2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(3(2-морфолиноэтокси)проп-1-инил)хиназолин-4(3H)-он;N-(4-(2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)4-оксо-3,4-дигидрохиназолин-5-ил)бут-3-ин-1-ил)морфолин-4-карбоксамид; 2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-(5-(бис-(2-метоксиэтил)амино)пент-1-инил)-3-(2-хлорбензил)хиназолин-4(3H)-он; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-циклопентилгекс-5-инамид ; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-(тетрагидро-2 Н-пиран-4-ил)гекс-5-инамид; 6-(2-4-амино-3-(4-гидроксифенил)-1 Н-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-(2-морфолиноэтил)гекс-5-инамид; 2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6(4-(2-метоксиэтил)пиперазин-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-(2-(диметиламино)этил)гекс-5-инамид; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-(пиридин-4-ил)гекс-5-инамид; 6-(2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-(пиридин-4-ил)гекс-5-инамид; 2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6(4-(диметиламино)пиперидин-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N,N-бис(2-метоксиэтил)гекс-5-инамид; 6-(2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N,N-бис (2-метоксиэтил) гекс-5-инамид; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-(2-(4-метилпиперазин-1-ил)этил)гекс-5-инамид; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-метил-N-(2-(4-метилпиперазин-1-ил)этил)гекс-5-инамид; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-изопропилгекс-5-инамид; 6-(2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-изопропилгекс-5-инамид; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N,N-диметилгекс-5-инамид; 2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6 оксо-6-(пирролидин-1-ил)гекс-1-ин-1-ил)хиназолин-4(3H)-он; 6-(2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-4 оксо-3,4-дигидрохиназолин-5-ил)-N-(пирролидин-3-ил)гекс-5-инамид; 2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6(3-(диметиламино)пирролидин-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он; 2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6(3-(диметиламино)пирролидин-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он; 2-4-амино-3-(4-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6(4-метил-1,4-диазепан-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он,2-4-амино-3-(3-гидроксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6(4-метил-1,4-диазепан-1-ил)-6-оксогекс-1-инил)хиназолин-4(3H)-он,2-4-амино-3-(4-гидрокси-3-метоксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(6-морфолино-6-оксогекс-1-инил)хиназолин-4(3H)-он,или его фармацевтически приемлемую соль, включая все стереоизомеры, таутомеры и изотопные производные. Соединения формулы (I) могут быть получены способом, включающим введение в реакцию соединения формулы (II) или его защищенного производного, в которой X, R3a, R3b, R4 и R5 имеют значения, определенные выше для соединений формулы (I), и LG1 обозначает уходящую группу, такую как галоген, в частности бром, с соединением формулы (III) или его защищенным производным, в которой R1 имеет значения, определенные выше для соединений формулы (I), в присутствии подходящего катализатора, органического основания и полярного апротонного растворителя, в инертной атмосфере; и в случае необходимости удаление защитной группы, с получением соединения формулы (I); и, в случае необходимости, превращение одного соединения формулы(I) в другое соединение формулы (I) обычными превращениями функциональных групп. Подходящие катализаторы включают катализаторы на основе палладия, такие как бис-(трифенилфосфин)палладий(II) дихлорид, в присутствии йодида меди. Подходящим полярным апротонным растворителем является DMF. Подходящей инертной атмосферой является азот. Реакция может быть осуществлена с использованием облучения, например с использованием микроволнового облучения при 120C и мощности 200 Вт. Удаление защитной группы с получением соединения формулы (I), где, например, R1 обозначает H и защитная группа представляет собой силильную группу, может быть осуществлено обработкой таким реагентом, как тетрабутиламмоний хлорид, в присутствии полярного апротонного растворителя, такого как DMF. Реакция может быть осуществлена при пониженной температуре, такой как приблизительно 0C. Соединения формулы (I), в которой R1 включает группу карбоновой кислоты, могут быть превращены в другие соединения формулы (I) обычными методиками, например амидным сочетанием. Другие примеры превращения соединения формулы (I) в другие соединения формулы (I) представлены теми соединениями формулы (I), в которых R1 включает первичный спирт. Такие соединения могут быть превращены в соединения формулы (I), в которых R1 включает первичный галогеналкил, и затем,путем последующей реакции с первичным или вторичным амином, в соединение формулы (I), в которомR1 включает алкиламин. Соединения формулы (II) могут быть получены реакцией соединения формулы (IV) или его защищенного производного, в которой LG1 и X имеют значения, определенные выше для соединений формулы (II), и LG2 обозначает уходящую группу, например галоген, такой как хлор, с соединением формулы (V) или его защищенным производным, в которой R3a, R3b, R4 и R5 имеют значения, определенные выше для соединений формулы (I), в присутствии основания, в полярном апротонном растворителе. Подходящие защитные группы для соединений формулы (V), в которой R3a является гидроксилом,включают трет-бутилдиметилсилиловый эфир. Подходящие основания включают карбонат калия. Подходящим полярным апротонным растворителем является DMF. Альтернативно соединения формулы (II) могут быть получены реакцией соединения формулы (VI) или его защищенного производного, в которой LG1, X, R4 и R5 имеют значения, определенные выше для соединений формулы (II), и LG3 обозначает уходящую группу, такую как галоген, в частности йод, с соединением формулы (VII) или его защищенным производным, в которой R3a и R3b имеют значения, определенные выше для соединений формулы (I), в присутствии подходящего катализатора на основе благородного металла, неорганического основания и полярного протонного растворителя, в инертной атмосфере; с последующим, если необходимо, удалением защитных групп от групп R3a, и/или R3b, и/или X. Подходящим катализатором является тетракис(трифенилфосфин)палладий(0). Подходящим неорганическим основанием является карбонат натрия. Подходящим полярным протонным растворителем является этанол. Реакция может быть осуществлена при повышенной температуре, например при 85C, в течение нескольких дней, например в течение 3 дней, перед охлаждением до температуры окружающей среды. Соединения формулы (VI) могут быть получены реакцией соединения формулы (IV) или его защищенного производного, в которой LG1, LG2 и X имеют значения, определенные выше, с соединением формулы (VIII) или его защищенным производным, в которой R4 и R5 имеют значения, определенные выше для соединений формулы (I), и LG3 обозначает уходящую группу, например атом галогена, в частности йод. Реакцию предпочтительно проводят в полярном апротонном растворителе и в присутствии неорганического основания при температуре окружающей среды, такой как комнатная температура, и в темноте. Подходящим неорганическим основанием является карбонат натрия. Подходящим полярным апротонным растворителем является DMF. Соединения формулы (V), в которой R3a, R3b, R4 и R5 имеют значения, определенные выше, могут быть получены реакцией соединения формулы (VIII), в которой LG3, R4 и R5 имеют значения, определенные выше, с соединением формулы (VII) или его защищенным производным, в которой R3a и R3b имеют значения, определенные выше для соединений формулы (I). Соединения формулы (IV) могут быть получены реакцией соединения формулы (IX) или его защищенного производного, в которой LG1 имеет значения, определенные выше для соединений формулы (II), и LG4 обозначает уходящую группу, например галоген, такой как хлор или гидрокси, с соединением формулы (X) или его защищенным производным, в которой X, R2a и R2b имеют значения, определенные выше для соединений формулы (II), в присутствии подходящего реагента, такого как тригалогенид фосфора, органического основания и неполярного растворителя. Подходящим тригалогенидом фосфора является трихлорид фосфора. Подходящим неполярным растворителем является толуол. Подходящим органическим основанием является триэтиламин. Защита гидроксила может, например, быть произведена с использованием TBDMSCI в подходящем растворителе, например DMF, в присутствии подходящего основания, такого как имидазол. Соединения формулы (IX) могут быть получены реакцией соединения формулы (XI) или его защищенного производного, в которой LG1 имеет значения, определенные выше для соединений формулы (II), с соединением формулы (XII) в которой LG5 и LG6 обозначают уходящие группы, например галоген, такой как хлор, в присутствии подходящего растворителя и подходящего основания. Подходящим растворителем является толуол, и подходящим основанием является пиридин. Защитные группы могут потребоваться для защиты химически чувствительных групп в ходе одной или более реакций, описанных выше, для гарантии эффективности процесса. Таким образом, если желательно или необходимо, промежуточные соединения могут быть защищены при помощи обычных защитных групп. Защитные группы и средства для их удаления описаны в "Protective Groups in OrganicSynthesis", Theodora W. Greene and Peter G.M. Wuts, опубликовано John WileySons Inc.; 4th Rev. Ed.,2006, ISBN-10: 0471697540. Новые промежуточные соединения заявлены как один аспект изобретения. Соединения формул (III), (VII), (VIII), (X), (XI) и (XII), как определено выше, либо являются коммерчески доступными, либо могут быть легко получены из коммерчески доступных исходных материалов с использованием обычных опубликованных методик (см. например, табл. 1). Отбор соединений формулы (I), раскрытых здесь, осуществляли путем скрининга с использованием ВЭЖХ с хиральной стационарной фазой на наличие взаимонепревращаемых вращательных изомеров,иначе известных как атропизомеры. Атропизомерия является результатом затрудненного вращения вокруг простой связи, где торсионный энергетический барьер на пути свободного вращения достаточно высок для значительного замедления взаимного превращения не накладывающихся друг на друга конформеров. Аналитические и препаративные способы, раскрытые ниже, использовались для разделения отдельных атропизомеров множества раскрытых в публикациях ингибиторов PI3K, показывая, что они обычно встречаются в виде смесей стереоизомеров, обладающих очень длительным периодом полужизни (месяцы или годы) в физиологических условиях. (См. экспериментальный раздел в отношении деталей.) Наличие атропизомеризи представляет собой дополнительную сложность для разработки таких соединений в качестве терапевтических средств, так как отдельные стереоизомеры обычно являются чрезвычайно предпочтительными по сравнению со смесями, такими как рацематы. Анализ выбранных примеров с использованием хроматографических способов, раскрытых здесь, не предоставил какоголибо доказательства того, что соединения формулы (I) демонстрируют атропизомерию. В отсутствие дополнительных признаков, известных как дающие начало стереоизомерам, например стереогенный центр, текущее раскрытие относится к соединениям, которые предпочтительно существуют как единственные отдельные молекулы. Таким образом, соединения согласно настоящему раскрытию особенно пригодны как терапевтически активные средства в фармацевтических композициях и в лечении. В одном аспекте соединения могут быть использованы в лечении, например, COPD и/или астмы. Соединения PI3K, разработанные до настоящего времени, обычно предназначены для перорального введения. Обычно эта стратегия включает оптимизацию фармакокинетического профиля соединения для достижения нужной продолжительности действия. Таким образом, между дозами устанавливается и поддерживается достаточно высокая концентрация лекарственного средства, чтобы обеспечить непре- 18020330 рывную клиническую выгоду. Неизбежным и часто нежелательным последствием этого подхода является то, что нецелевые ткани организма, особенно печень и кишечник, могут подвергаться действию фармакологически активных концентраций лекарственного средства. Альтернативная стратегия состоит в разработке режимов лечения, в которых лекарственное средство вводят непосредственно в воспаленный орган (например, топическая терапия). Хотя этот подход не является подходящим для лечения всех хронических воспалительных состояний, он экстенсивно эксплуатировался в лечении заболеваний легких (астма, COPD), поражений кожи (атопический дерматит и псориаз), заболеваний носа (аллергический ринит) и желудочно-кишечных расстройств (язвенный колит). В топической терапии желаемая эффективность может иногда достигаться за счет обеспечения пролонгированной продолжительности действия лекарственного средства и его сохранения преимущественно в целевом органе, таким образом минимизируя риски системной токсичности. Альтернативно, может использоваться подходящий состав, который создает "резервуар" активного лекарственного средства,которое становится тогда доступным для поддержания желательных эффектов. Первый подход иллюстрируется использованием антихолинергического лекарственного средства тиотропий бромида (SpirivaHandiHaler), который вводят топически в легкое для лечения COPD. Это соединение имеет исключительно высокое сродство с его целевым рецептором, что приводит к очень медленной скорости выведения (скорости диссоциации) и, соответственно, длительной продолжительности действия. Согласно одному аспекту настоящего раскрытия изобретение относится к применению соединения состава в качестве ингибитора киназы PI3, например, вводимого топически в легкое. В одном аспекте раскрытия соединения по изобретению являются особенно подходящими для топической доставки, такой как топическая доставка в легкие, в частности, для лечения COPD. Таким образом, согласно одному аспекту изобретение относится к применению соединений формулы (I) для лечения COPD и/или астмы, в частности COPD или тяжелой астмы, ингаляцией, т.е. топическим введением в легкое. Предпочтительно введение в легкое позволяет реализовать у пациентов благоприятные эффекты соединений, минимизируя побочные эффекты. В одном варианте осуществления соединения являются подходящими для сенсибилизации пациентов к лечению кортикостероидом. Соединения по изобретению могут также быть использованы для лечения ревматоидного артрита. Далее, настоящее изобретение относится к фармацевтической композиции, включающей соединение согласно раскрытию, в случае необходимости в комбинации с одним или более фармацевтически приемлемыми разбавителями или носителями. Разбавители и носители могут включать подходящие для парентерального, перорального, топического, мукозального и ректального введения и могут различаться в зависимости от пути введения. В одном варианте осуществления композиции могут быть получены, например, для парентерального, подкожного, внутримышечного, внутривенного, внутрисуставного или околосуставного введения,особенно в форме жидких растворов или суспензий; для перорального введения, особенно в форме таблеток или капсул; для топического, например легочного или внутриносового введения, особенно в форме порошков, носовых капель или аэрозолей, и чрескожного введения; для мукозального введения, например через щечную, подъязычную или влагалищную слизистую оболочку, и для ректального введения,например, в форме суппозитория. Композиции могут вводиться в стандартных лекарственных формах и могут быть получены любым из способов, известных в области фармации, например, как описано в Remington's PharmaceuticalSciences, 17th ed., Mack Publishing Company, Easton, PA., (1985). Составы для парентерального введения могут содержать в качестве эксципиентов стерилизованную воду или солевой раствор, алкиленгликоли, такие как пропиленгликоль, полиалкиленгликоли, такие как полиэтиленгликоль, масла растительного происхождения, гидрированные нафталины и т.п. Составы для носового введения могут быть твердыми и могут содержать эксципиенты, например лактозу или декстран, или могут быть водными или масляными растворами для использования в форме носовых капель или мерного спрея. Для буккального введения типичные эксципиенты включают сахара,стеарат кальция, стеарат магния, предварительно желированный крахмал и т.п. Композиции, подходящие для перорального введения, могут включать один или более физиологически совместимых носителей и/или эксципиентов и могут быть в твердой или жидкой форме. Таблетки и капсулы могут быть получены со связующими, например сиропом, гуммиарабиком, желатином, сорбитом, трагакантом или поливинилпирролидоном; наполнителями, такими как лактоза, сахароза, кукурузный крахмал, фосфат кальция, сорбит или глицин; лубрикантами, такими как стеарат магния, тальк, полиэтиленгликоль или диоксид кремния; и поверхностно-активными веществами, такими как лаурилсульфат натрия. Жидкие композиции могут содержать обычные добавки, такие как суспендирующие агенты, например сироп сорбита, метилцеллюлоза, сахарный сироп, желатин, карбоксилметилцеллюлоза или пищевые жиры; эмульгаторы, такие как лецитин или гуммиарабик; растительные масла, такие как миндальное масло, кокосовое масло, жир печени трески или арахисовое масло; консерванты, такие как бутилированный гидроксианизол (BHA) и бутилированный гидрокситолуол (BHT). Жидкие композиции могут быть инкапсулированы, например, в желатине с получением стандартной лекарственной формы. Твердые пероральные лекарственные формы включают таблетки, твердые капсулы из двух составных частей и мягкие эластичные желатиновые (SEG) капсулы. Сухой состав капсулы обычно включает приблизительно от 40 до 60% концентрации желатина,приблизительно от 20 до 30% концентрации мягчителя (такого, как глицерин, сорбит или пропиленгликоль) и приблизительно от 30 до 40% концентрации воды. Другие материалы, такие как консерванты,красители, замутнители и ароматизаторы, также могут присутствовать. Жидкий заполняющий материал включает твердое лекарственное средство, которое было растворено, солюбилизировано или диспергировано (с суспендирующими агентами, такими как пчелиный воск, гидрированное касторовое масло или полиэтиленгликоль 4000), или жидкое лекарственное средство в носителях или комбинациях носителей,таких как минеральное масло, растительные масла, триглицериды, гликоли, многоатомные спирты и поверхностно-активные средства. Предпочтительно соединение формулы (I) вводят топически в легкое. Следовательно, в одном варианте осуществления изобретение относится к фармацевтической композиции, включающей соединение согласно раскрытию, в случае необходимости в комбинации с одним или более топически приемлемых разбавителей или носителей. Топическое введение в легкое может быть осуществлено при помощи состава аэрозоля. Составы аэрозоля обычно включают активный ингредиент, суспендированный или растворенный в подходящем аэрозольном пропелленте, таком как хлорфторуглерод (CFC) или гидрофторуглерод (HFC). Подходящие пропелленты CFC включают трихлорфторметан (пропеллент 11), дихлортетрафторметан (пропеллент 114) и дихлордифторметан (пропеллент 12). Подходящие пропеллентыHFC включают тетрафторэтан (HFC-134a) и гептафторпропан (HFC-227). Пропеллент обычно составляет от 40 до 99,5%, например от 40 до 90%, от общей массы всей композиции для ингаляции. Состав может включать эксципиенты, включая совместные растворители (например, этанол) и поверхностно-активные вещества (например, лецитин, сорбитан триолеат и т.п.). Составы аэрозоля упаковываются в канистры, и подходящая доза выдается посредством дозирующего клапана (например, поставляемого Bespak, Valois или 3 М). Топическое введение в легкое может также быть осуществлено при помощи неаэрозольного состава, такого как водный раствор или суспензия. Он может вводиться посредством небулайзера. Топическое введение в легкое может также быть осуществлено при помощи сухого порошкового состава. Сухой порошковый состав содержит соединение согласно раскрытию в тонкораздробленной форме, обычно с массовым средним диаметром (MMAD) 1-10 мкм. Состав обычно содержит топически приемлемый разбавитель, такой как лактоза, обычно имеющий большую величину частиц, например массовый средний диаметр (MMAD) 100 мкм или больше. Примеры сухих порошковых систем доставки включаютSPINHALER, DISKHALER, TURBOHALER, DISKUS, SKYEHALER, ACCUHALER и CLICKHALER. В одном варианте осуществления изобретение относится к соединению в форме измельченного сухого порошкового состава, например, включающего лактозу подходящей марки, заполненного в устройство, такое как DISKUS. Соединения согласно раскрытию имеют терапевтическую активность. В следующем аспекте настоящее изобретение относится к соединению согласно раскрытию для применения в качестве лекарственного средства. Соединения согласно раскрытию могут также быть использованы в лечении респираторных нарушений, включая COPD (включая хронический бронхит и эмфизему), астму, детскую астму, муковисцидоз, саркоидоз, идиопатический легочный фиброз, аллергический ринит, ринит, синусит, особенно астму,хронический бронхит и COPD. Соединения согласно раскрытию могут также ресенсибилизировать состояние пациента к лечению кортикостероидом, когда состояние пациента стало устойчивым к нему. Одно или более соединений согласно раскрытию могут демонстрировать противовирусную активность и оказаться полезными в лечении вирусных обострений астмы и/или COPD. Соединения согласно настоящему раскрытию могут также быть использованы в профилактике, лечении или облегчении заболеваний, вызванных вирусом гриппа, риновирусом и/или респираторным синцитиальным вирусом. Также ожидается, что соединения согласно раскрытию могут быть использованы в лечении некоторых состояний, которые могут излечиваться топической или местной терапией, включая аллергический конъюнктивит, конъюнктивит, аллергический дерматит, контактный дерматит, псориаз, язвенный колит,воспаление суставов, вторичное по отношению к ревматоидному артриту или остеоартриту. В одном варианте осуществления соединения формулы (I), как считается, являются пригодными для использования в лечении гепатита C и/или ВИЧ при введении подходящим путем. Подходящие пути введения могут включать пероральную, внутривенную инъекцию или инфузию. В одном варианте осуществления соединение формулы (I) для лечения гепатита C доставляют в кровь перед ее поступлением в печень. Также ожидается, что соединения согласно раскрытию могут быть использованы в лечении некоторых других состояний, включая ревматоидный артрит, панкреатит, кахексию, ингибирование роста и метастаза опухолей, включая немелкоклеточный рак легкого, рак молочной железы, рак желудка, коло- 20020330 ректальный рак и злокачественную меланому. Таким образом, в следующем аспекте настоящее изобретение относится к соединению, как описано здесь, для применения в лечении одного или более вышеупомянутых состояний. В следующем аспекте настоящее изобретение относится к применению соединения, как описано здесь, для получения лекарственного средства для лечения одного или более вышеупомянутых состояний. В следующем аспекте настоящее изобретение относится к способу лечения вышеупомянутых состояний, который включает введение пациенту эффективного количества соединения согласно раскрытию или его фармацевтической композиции. Соединения, описанные здесь, могут также использоваться в получении лекарственного средства для лечения одного или более идентифицированных выше заболеваний. Слово "лечение" охватывает как профилактику, так и терапевтическое лечение. Соединение согласно раскрытию может также вводиться в комбинации с одним или более другими активными ингредиентами, например активными ингредиентами, подходящими для лечения вышеупомянутых состояний. Например, возможные комбинации для лечения респираторных нарушений включают комбинации со стероидами (например, будезонидом, беклометазон дипропионатом, флутиказон пропионатом, мометазон фуроатом, флутиказон фуроатом), бета-агонистами (например, тербуталином,салбутамолом, салметеролом, формотеролом, индакатеролом) и/или ксантинами (например, теофиллином), мускариновыми антагонистами (например, ипратропием) и/или ингибитором p38 MAP киназы. В одном варианте осуществления соединение согласно раскрытию вводят в комбинации с противовирусным агентом, например ацикловиром, тамифлю, реленца или интерфероном. В одном варианте осуществления комбинация активных ингредиентов содержится в совместном составе. В одном варианте осуществления комбинацию активных ингредиентов просто вводят совместно. Экспериментальный раздел Аббревиатуры Аббревиатуры, используемые здесь, имеют значения, определенные ниже в таблице. Любые аббревиатуры, имеющиеся в тексте, которые не были определены, имеют общепринятое значение. АсОН - ледяная уксусная кислота Водн. - водный Ас - ацетил АТФ - аденозин-5'-трифосфатCOPD - хроническая обструктивная болезнь легкихFCS - зародышевая телячья сыворотка г - грамм(ы)HOBt - 1-гидроксибензотриазол ВЭЖХ - высокоэффективная жидкостная хроматография ВЭЖХ-MS - высокоэффективная жидкостная хроматография с масс-спектрометрией ч - час(ы)KHMDS - гексаметилдисилазан калия мкл - микролитр(ы)MeOD - дейтерийсодержащий метанол мг - миллиграмм(ы) МГц - мегагерц мин - минута(ты) мл - миллилитр(ы) мМ - миллимоль мм - миллиметр ммоль - миллимольNMP - 1-метилпирролидин-2-он (N-метил-2-пирролидон) ЯМР - ядерный магнитный резонанс (спектроскопия)PBS - фосфатный буферный солевой растворPIP3 - фосфатидилинозитол 3,4,5-трифосфат РМА - форбол миристат ацетат Ро - пероральное введениеRP-ВЭЖХ - высокоэффективная жидкостная хроматография с обратной фазойSCX - катионообменная смола на твердой подложкеTLC - тонкослойная хроматография ТМВ - 3,3',5,5'-тетраметилбензидинTNF - фактор некроза опухоли альфаTR-FRET - резонансный перенос энергии флуоресценции с временным разрешением об. - объемVT - вариабельная температура Вт - Ватт Общие процедуры Промежуточные соединения и полученные на заказ химические строительные блоки, не доступные из коммерческих источников, были получены согласно процедурам, раскрытым здесь, или с использованием описанных в литературе способов. Все другие исходные материалы и растворители (качества ВЭЖХ) были получены из коммерческих источников и использовались без дальнейшей очистки. Где это указано, реакционные среды дегазировали, пропуская через них поток азота в течение по меньшей мере 10 мин. Микроволновые реакции осуществляли, используя сфокусированные микроволновые приборы СЕМ Discover или Explorer. Органические растворы высушивали, используя сульфат магния или сульфатSiliaFlash P60 (230-400 меш) или Biotage Isolute SPE, предварительно заполненной Flash Si II. Аналитические методы Анализ методом тонкослойной хроматографии (TLC) осуществляли на Kieselgel 60 с планшетами с флуоресцентным индикатором УФ 254 и визуализировали, используя УФ-свет, или окрашивали стандартными растворами для окрашивания для TLC или йодом. Аналитическая высокоэффективная жидкостная хроматография с масс-спектрометрией. Все образцы анализировали обычным образом с помощью ВЭЖХ-MS, используя аппаратуру и условия, описанные ниже. Если не указано иное, конечное соединение подвергали анализу, используя способ В, и промежуточные звенья проанализировали, используя способ А. Способ А осуществляли на системах Agilent HP1 100 и Shimadzu 2010, используя колонки с обратной фазой Atlantis dC18 (5 мкм, 2,150 мм), градиент 5-100% В (А=вода/0,1% муравьиной кислоты,В=ацетонитрил/0,1% муравьиной кислоты) за 3 мин, объем инъекции 3 мкл, поток=1,0 мл/мин. УФспектры регистрировали при 215 нм, используя УФ-детектор двойной длины волны Waters 2487 или систему Shimadzu 2010. Масс-спектры получали в диапазоне m/z от 150 до 850 на частоте отбора пробы 2 сканирования в секунду, используя Waters ZMD, или в диапазоне m/z от 100 до 1000 на частоте отбора пробы 2 Гц, используя ионизацию с электрораспылением, с помощью системы Shimadzu 2010 LC-MS. Способ В осуществляли на системах Agilent HP1 100 и Shimadzu 2010, используя колонки с обратной фазой Atlantis dCl8 (3 мкм, 2,1100 мм), градиент 5-100% В (А=вода/0,1% муравьиной кислоты,В=ацетонитрил/0,1% муравьиной кислоты) за 7 мин, объем инъекции 3 мкл, поток=0,6 мл/мин. УФспектры регистрировали при 215 нм, используя светодиодную матрицу Waters 2996, или на системе Shimadzu 2010. Масс-спектры получали в диапазоне m/z от 150 до 850 на частоте отбора пробы 2 сканирования в секунду, используя Waters ZQ, или в диапазоне m/z от 100 до 1000 на частоте отбора пробы 2 Гц,используя ионизацию с электрораспылением, с помощью системы Shimadzu 2010 LC-MS. Способ С осуществляли на системах Agilent HP1100, используя колонки с обратной фазой Phenomenex Gemini dC18 (3 мкм, 2,050 мм), градиент 1-100% В (А=2 мМ бикарбоната аммония pH 10,В=ацетонитрил) за 3,5 мин, объем инъекции 3 мкл, поток=1,0 мл/мин. УФ-спектры регистрировали при 215 нм, используя УФ-детектор двойной длины волны Waters 2487 или светодиодную матрицу Waters 2996. Масс-спектры получали в диапазоне m/z от 150 до 850 на частоте отбора пробы 2 сканирования в секунду, используя Waters ZMD или Waters ZQ. Способ D осуществляли на системах Agilent HP1200, используя колонки Agilent Extend C18 (1,8 мкм,4,630 мм) при 40C и объемной скорости потока 2,5-4,5 мл/мин-1, элюируя с градиентом H2O-MeCN,содержащим 0,1% об./об. муравьиной кислоты, в течение 4 мин. Информация градиента: 0-3,00 мин, изменение от 95% Н 2 О-5% MeCN до 5% Н 2 О-95% MeCN; 3,00-3,01 мин, поддержание при 5% Н 2 О-95%MeCN, объемная скорость потока увеличилась до 4,5 мл/мин-1; 3,01-3,50 мин поддержание при 5% Н 2 О 95% MeCN; 3,50-3,60 мин возвращение к 95% Н 2 О-5% MeCN; объемная скорость потока уменьшилась до 3,50 мл/мин-1; 3,60-3,90 мин поддержание при 95% H2O-5% MeCN; 3,90-4,00 мин поддержание при 95% Н 2 О-5% MeCN, объемная скорость потока уменьшилась до 2,5 мл/мин-1. УФ-детекцию осуществляли при 254 нм, используя детектор переменной длины волны Agilent G1314B. Масс-спектры получали в диапазоне m/z от 60 до 2000 на частоте отбора пробы 1,6 с/цикл с использованием Agilent G1956B. Аналитическую ВЭЖХ с хиральной стационарной фазой осуществляли, используя колонки Daicel(5 мкм 5 см 4,6 мм), содержащие одну из следующих стационарных фаз: Chiralpak AD-H, Chiralcel ODH, Chiralcel OJ-H и Chiralpak AS-H. Использовали объемную скорость потока 1 мл/мин, элюируя в изократических условиях за 6-20 мин с использованием одной из следующих мобильных фаз: 70:30 гептан:IPA (об./об.), 85:15 гептан:EtOH (об./об.), 50:50 MeOH:EtOH (об./об.) и ацетонитрил; УФ-детекцию использовали при 254 нм. Каждая из этих мобильных фаз совместима с наполнителями колонки, упомянутыми выше, что обеспечивает 16 различных сочетаний растворителей и стационарных фаз. Модификаторы, такие как триэтиламин (0,1%), муравьиная кислота (0,1%), могут быть добавлены для улучшения разрешения. Полупрепаративную ЖХ-УФ с хиральной стационарной фазой осуществляли на препаративной модульной системе Gilson, используя полупрепаративную колонку Daicel CHiralpak AD (10 мм, 20250 мм) и объемную скорость потока 18 мл/мин, элюируя изократическим способом в течение 20 мин, используя 70:20 гептан:IPA и 0,1% триэтиламина, с использованием объема инъекции 1,0 мл. УФ-спектры регистрировали и фракции анализировали на аккумуляцию при 215 нм с УФ-детектором Gilson 119. Данные интегрировали и представляли с использованием программного обеспечения OpenLynx иOpenLynx Browser или программного обеспечения Shimadzu PsiPort. 1 Н ЯМР-спектроскопия: спектры получали на спектрометре Bruker DPX 250 МГц, Bruker Avance III 400 МГц или Bruker DRX 500 МГц, используя остаточные протонированные резонансы дейтеризованного растворителя в качестве внутреннего стандарта. Получение некоммерческих промежуточных соединений 3-(3-(трет-бутилдиметилсилилокси)фенил)1 Н-пиразоло[3,4-d]пиримидин-4-амин (3). К перемешиваемой суспензии 3-йод-1 Н-пиразоло[3,4-d]пиримидин-4-амина (1) (8,22 г, 31,5 ммоль),3-фенолбороновой кислоты (13,0 г, 94,5 ммоль) и фосфата калия (10,0 г, 47,3 ммоль) в дегазированной смеси DMF/вода (3:2, 140 мл) добавляли [dppf] дихлорид палладия(II) (13,0 г, 15,7 ммоль). Реакционную смесь промывали азотом, нагревали при 120C в течение 2 ч и затем давали охладиться до температуры окружающей среды. Реакционную смесь разбавляли EtOAc (500 мл) и водным раствором соляной кислоты (2 М, 500 мл) и полученную суспензию фильтровали. Фильтрат экстрагировали водным раствором соляной кислоты (2 М, 2500 мл). Объединенные водные экстракты подщелачивали насыщенным водным раствором карбоната натрия до pH 10. Образовавшийся осадок фильтровали и фильтрат экстрагировалиEtOAc (31 л). Объединенные органические экстракты высушивали, фильтровали и растворитель удаляли в вакууме, получая твердое вещество серого цвета. Все твердые материалы, полученные в ходе процедуры обработки, объединяли и растирали с DCM, получая 3-(4-амино-1 Н-пиразоло[3,4-d]пиримидин-3 ил)фенол (2) (6,04 г, 84%) в форме твердого вещества серого цвета: m/z 228 (М+Н)+ (ES+). К перемешиваемому раствору соединения (2) (4,69 г, 20,66 ммоль) и имидазола (2,10 г, 30,99 ммоль) в сухом DMF (100 мл) добавляли TBDMSCI (4,70 г, 30,99 ммоль). Через 16 ч добавляли дополнительные аликвоты имидазола (2,10 г, 30,99 ммоль) и TBDMSCI (4,70 г, 30,99 ммоль) и смесь перемешивали в течение 48 ч. Реакционную смесь разбавляли водой (120 мл) и экстрагировали DCM (2200 мл). Объединенные органические экстракты промывали водой (2200 мл), высушивали, фильтровали и объем уменьшали приблизительно до 100 мл упариванием в вакууме. Полученную суспензию фильтровали и твердое вещество промывали гептаном (50 мл), получая целевое соединение (3) (6,05 г, 85%) в форме твердого вещества грязно-белого цвета: m/z 343 (М+Н)+ (ES+). 3-(4-(трет-Бутилдиметилсилилокси)фенил)-1 Н-пиразоло[3,4-d]пиримидин-4-амин (5).DMF (90 мл) добавляли водный раствор гидроксида натрия (1 М, 76,0 мл, 76,8 ммоль). Реакционную смесь промывали азотом и нагревали при 120C в течение 18 ч. Реакционной смеси давали охладиться до температуры окружающей среды и разбавляли водой (200 мл). Полученный осадок собирали фильтрацией и промывали водой (200 мл) и затем DCM, пока фильтрат не становился бесцветным, получая 4-(4 амино-1 Н-пиразоло[3,4-d]пиримидин-3-ил)фенол (4) (5,25 г, 60%) в форме твердого вещества коричневого цвета: m/z 228 (М+Н)+ (ES+). К перемешиваемому раствору соединения (4) (5,25 г, 23,1 ммоль) и имидазола (3,85 г, 57,8 ммоль) в сухом DMF (70 мл) добавляли TBDMSCI (4,19 г, 27,7 ммоль). Через 16 ч добавляли дополнительные аликвоты имидазола (1,93 г, 28,9 ммоль) и TBDMSCI (2,10 г, 13,9 ммоль) и смесь перемешивали в течение 4 ч. Реакционную смесь разбавляли водой (200 мл) и полученный осадок собирали фильтрацией,промывали водой (200 мл) и гептаном (300 мл), получая целевое соединение (5) (7,31 г, 93%) в форме твердого вещества коричневого цвета: m/z 344 (М+Н)+ (ES+). 5-Бром-3-(2-хлорбензил)-2-(хлорметил)хиназолин-4(3H)-он (8). хлорацетил хлорида (2,26 мл, 28,4 ммоль) в толуоле (75 мл) по каплям за 1 ч. Реакционной смеси давали нагреться до температуры окружающей среды, нагревали при 115C в течение 3 ч и затем давали охладиться до температуры окружающей среды. Объем растворителя уменьшали наполовину упариванием в вакууме. После отстаивания в течение ночи продукт осаждали и собирали фильтрацией, получая 2-бром 6-(2-хлорацетамидо)бензойную кислоту (7 а) (1,44 г) в форме твердого вещества белого цвета: m/z 290/292 (М+Н)+ (ES+). Фильтрат концентрировали в вакууме и остаток растирали со смесью этанол/гептан,получая 2-бром-6-(2-гидроксиацетамидо)бензойную кислоту (7b) (1,02 г, объединенный выход 59%): m/z 274/276 (М+Н)+ (ES+). Как 7 а, так и 7b может использоваться без дальнейшей очистки на следующей стадии. К перемешиваемой смеси соединения (7 а) (7,50 г, 27,4 ммоль), 2-хлорбензиламина (5,00 мл, 41,05 ммоль) и триэтиламина (5,70 мл, 41,1 ммоль) в толуоле (250 мл) добавляли по каплям за 1 ч раствор трихлорида фосфора (2,60 мл, 30,1 ммоль) в толуоле (250 мл). Реакционную смесь нагревали до 110C в течение 24 ч, после чего горячий раствор декантировали и концентрировали в вакууме. Остаток растирали с пропан-2-олом (50 мл), получая целевое соединение (8) (6,41 г, 59%) в форме твердого вещества желтого цвета: m/z 397/399 (М+Н)+ (ES+). 3-(2-(2-Метоксиэтокси)этокси)проп-1-ин (9). К перемешиваемой суспензии гидрида натрия (3,12 г, 78,0 ммоль) в THF (100 мл), охлажденной до 5C в ванне со льдом, добавляли по каплям раствор пропаргилового спирта (4,60 г, 78,0 ммоль) в THF (20 мл). Смесь перемешивали при 5C в течение 30 мин и затем давали нагреться до температуры окружающей среды и обрабатывали по каплям 1-бром-2-(2-метоксиэтокси)этаном (7,00 мл, 52,0 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 16 ч и затем разбавляли водой (100 мл) и экстрагировали простым диэтиловым эфиром (2100 мл). Объединенные органические экстракты высушивали, фильтровали и упаривали в вакууме. Остаток очищали флэш-хроматографией на колонке,элюируя 30%-м EtOAc в гептане, получая целевое соединение (9) (250 мг, 9%) в форме бесцветного масла: 1 Н ЯМР (500 МГц, MeOD) : 4,18 (2 Н, дд), 3,66-3,69 (2 Н, м), 3,60-3,66 (4 Н, м), 3,52-3,56 (2 Н, м), 3,36 К перемешиваемой суспензии трет-бутоксида калия (1,06 г, 9,42 ммоль) в THF (300 мл), охлажденной до 0C в ванне со льдом, добавляли раствор 2,2'-диэтанолгликоля (4,60 г, 78,0 ммоль) в THF (10 мл). Смесь перемешивали при 0C в течение 30 мин и затем давали нагреться до температуры окружающей среды и обрабатывали по каплям бромидом пропаргила (1,68 мл 80%-го раствора в толуоле, 11,30 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 16 ч, и разбавляли солевым раствором и водой (5:1, 50 мл), и экстрагировали EtOAc (3500 мл). Объединенные органические экстракты высушивали, фильтровали и упаривали в вакууме. Остаток очищали флэш-хроматографией на колонке,элюируя 25-60%-м EtOAc в гептане, получая целевое соединение (10) (410 мг, 30%) в форме желтого масла: 1H ЯМР (250 МГц, CDCl3) : 2,22 (1 Н, с), 2,45 (1 Н, т), 3,58-3,66 (2 Н, м), 3,67-3,79 (6 Н, м), 4,22 (2 Н, д). 1-Морфолиногекс-5-ин-1-он (11).EDC (940 мг, 4,90 ммоль) в DCM (10 мл) добавляли морфолин (391 мкл, 4,46 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение ночи и затем разбавляли DCM (50 мл). Полученный раствор промывали водой (310 мл), солевым раствором (10 мл) и водным раствором соляной кислоты (2 М, 220 мл) и затем высушивали, фильтровали и упаривали в вакууме, получая целевое соединение (11) (808 мг, 100%) в форме желтого масла: 1H ЯМР (500 МГц, CDCl3) : 3,65-3,71 (4 Н, м),3,63 (2 Н, д), 3,45-3,54 (2 Н, м), 2,46 (2 Н, т), 2,26-2,33 (2 Н, м), 1,98 (1 Н, т), 1,88 (2 Н, квинтет). 2-Ацетамидо-N-(проп-2-инил)ацетамид (12).(360 мг, 1,88 ммоль) в DCM (10 мл) добавляли пропаргиламин (109 мкл, 1,71 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение ночи и затем упаривали в вакууме. Остаток очищали флэш-хроматографией на колонке, элюируя от 0 до 5% метанола в DCM, получая целевое соединение (12) (218 мг, 83%) в форме твердого вещества белого цвета: 1 Н ЯМР (500 МГц, CDCl3) : 2,07 К суспензии бут-3-ин-1-амин гидрохлорида (200 мг, 1,89 ммоль) и триэтиламина (425 мкл, 3,78 ммоль) в DCM (60 мл) добавляли морфолин-4-карбонил хлорид (218 мкл, 1,89 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение ночи и затем промывали водным раствором соляной кислоты (2 М, 220 мл), насыщенным водным раствором бикарбоната натрия (220 мл), высушивали, фильтровали и упаривали в вакууме. Остаток очищали флэш-хроматографией на колонке, элюируя 0-100% этилацетата в гептане, получая целевое соединение (13) (164 мг, 48%) в форме твердого вещества белого цвета: 1H ЯМР (500 МГц, ДМСО-d6) : 2,28 (2 Н, тд), 2,82 (1 Н, т), 3,09-3,18 (2 Н, м), 3,203,27 (4 Н, м), 3,48-3,57 (4 Н, м), 6,74 (1 Н, т). К перемешиваемому раствору гидрокарбоната натрия (2,73 г, 32,5 ммоль) в воде (50 мл) частями за 30 мин добавляли гидрохлорид гидроксиламина (2,30 г, 33,2 ммоль). Полученный раствор добавляли к энергично перемешиваемой суспензии 2-фтор-3-метоксибензальдегида (5,00 г, 32,5 ммоль) в этаноле (45 мл) и реакционную смесь перемешивали при температуре окружающей среды в течение 16 ч. Полученный осадок удаляли фильтрацией, промывали водой (3100 мл) и затем давали высохнуть на воздухе,получая 2-фтор-3-метоксибензальдегид оксим (14) (4,69 г, 85%) в форме кристаллического твердого вещества белого цвета: m/z 170 (М+Н)+ (ES+). К перемешиваемому раствору оксима (14) (1,50 г, 8,86 ммоль) в этаноле (70 мл) под азотом добавляли 10%-й палладий на углероде (100 мг). Реакционную смесь помещали в атмосферу водорода и перемешивали при температуре окружающей среды в течение 2 ч. Реакционную смесь фильтровали через Целит и затем упаривали в вакууме, чтобы удалить этанол. Полученный сырой остаток разделяли между этилацетатом(50 мл) и водным раствором соляной кислоты (2 М, 50 мл). Водный слой отделяли, нейтрализовали насыщенным раствором гидрокарбоната натрия, и затем повторно экстрагировали этилацетатом (70 мл), затем смесью 2-пропанола и хлороформа (1:1, 270 мл). Экстракты пропанола/хлороформа высушивали, фильтровали и упаривали в вакууме отдельно, получая целевое соединение (15) в двух загрузках (загрузка 1: 346 мг,25%; загрузка 2: 370 мг, 27%) в форме твердых частиц белого цвета: m/z 156 (М+Н)+ (ES+) (способ С). 2-4-Амино-3-йод-1 Н-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-бром-3-(2-хлорбензил)хиназолин 4(3H)-он: промежуточное соединение А. 30,7 ммоль) и 3-йод-1 Н-пиразоло[3,4-d]пиримидин-4-амина (1) (8,09 г, 30,7 ммоль) в DMF (300 мл) добавляли карбонат калия (6,36 г, 46,0 ммоль) и реакцию поддерживали при температуре окружающей среды в темноте в течение 24 ч. Смесь лили на воду (4,0 л) и полученную суспензию перемешивали при температуре окружающей среды в течение 1 ч. Осадок отделяли фильтрацией и высушивали в вакууме,получая целевое соединение, промежуточное соединение А, в форме бесцветного твердого вещества К перемешиваемой смеси соединения (8) (100 мг, 0,25 ммоль) и карбоната калия (42 мг, 0,30 ммоль) в DMF (2,5 мл) добавляли раствор соединения (3) (94 мг, 0,28 ммоль) в DMF (2,5 мл) и реакционную смесь перемешивали при температуре окружающей среды в течение 18 ч. Карбонат калия (335 мг, 0,75 ммоль) добавляли в 3 частях за 30 ч. Растворитель удаляли в вакууме и сырой материал очищали флэшхроматографией на колонке, элюируя 4,5% метанола в DCM, получая целевое соединение (промежуточное соединение В) (94 мг, 64%) в форме твердого вещества грязно-белого цвета: m/z 588/590 (М+Н)+ Путь А. Тщательно перемолотую смесь промежуточного соединения (10,0 г, 15,3 ммоль), Na2CO310H2O (9,60 г,33,6 ммоль), 4-гидроксифенилбороновой кислоты (4,21 г, 30,5 ммоль), и Pd(Ph3)4 (1,32 г, 1,14 ммоль) вEtOH (300 мл) продували азотом и затем перемешивали при 85C в течение 3 дней. Смесь охлаждали до температуры окружающей среды и осадок отделяли фильтрацией и промывали EtOH (100 мл). Твердое вещество повторно суспендировали в воде (100 мл) и перемешивали в течение еще 30 мин, затем отделяли фильтрацией, промывали EtOH (50 мл) и высушивали в вакууме, получая целевое соединение, промежуточное соединение С, в форме твердого вещества грязно-белого цвета (4,86 г, 51%): m/z 588/590 (М+Н)+ (ES+). Путь В. К перемешиваемой смеси соединения (8) (100 мг, 0,25 ммоль) и карбоната калия (42 мг, 0,30 ммоль) в DMF (2,5 мл) добавляли раствор соединения (5) (94 мг, 0,28 ммоль) в DMF (2,5 мл) и реакционную смесь перемешивали при температуре окружающей среды в течение 18 ч. Растворитель удаляли в вакууме и сырой материал очищали флэш-хроматографией на колонке, элюируя 4,5% метанола в DCM, получая целевое соединение, промежуточное соединение С (82 мг, 55%), в форме твердого вещества кремового цвета: m/z 588/590 (М+Н)+ (ES+) (способ В). 2-4-Амино-3-(3-фтор-4-гидроксифенил)-1 Н-пиразоло[3,4-d]пиримидин-1-ил)метил)-5-бром-3-(2 хлорбензил)хиназолин-4(3H)-он: промежуточное соединение D. К перемешиваемой смеси соединения (8) (200 мг, 0,502 ммоль) и карбоната калия (83 мг, 0,60 ммоль) в DMF (2,0 мл) добавляли раствор 4-(4-амино-1 Н-пиразоло[3,4-d]пиримидин-3-ил)-2-фторфенола (см. табл. 1 ниже) (148 мг, 0,602 ммоль) в DMF (2,0 мл) и реакционную смесь перемешивали при температуре окружающей среды в течение 18 ч. Растворитель удаляли в вакууме и сырой материал очищали флэшхроматографией на колонке, элюируя 5%-м метанолом в DCM, получая целевое соединение, промежуточное соединение D (81 мг, 27%), в форме твердого вещества грязно-белого цвета: m/z 606/608 (М+Н)+ Смесь промежуточного соединения А (400 мг, 0,630 ммоль), 2-метокси-4-(4,4,5,5-тетраметил-1,3,2 диоксаборолан-2-ил)фенола (189 мг, 0,755 ммоль), Na2CO310H2O (396 мг, 1,39 ммоль) и Pd(Ph3)4 (55 мг,0,047 ммоль) в EtOH (12 мл) очищали азотом и затем перемешивали при 85C в течение 24 ч. Смесь охлаждали и упаривали в вакууме и остаток очищали флэш-хроматографией на колонке (SiO2, 80 г, MeOH вCH2Cl2, элюирование с градиентом 0-10%), получая целевое соединение, промежуточное соединение Е, в форме твердого вещества светло-коричневого цвета (225 мг, 56%): m/z 618/620 (М+Н)+ (ES+). 2-4-Амино-3-(4-гидроксифенил)-1 Н-пиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5(5-йодпент-1-инил)хиназолин-4(3H)-он: промежуточное соединение F. К смеси промежуточного соединения С (503 мг, 0,854 ммоль), йодида меди(I) (17 мг, 0,089 ммоль) и дихлорида бис-(трифенилфосфин)палладия(II) (64 мг, 0,089 ммоль) в диэтиламине (3,2 мл, 31 ммоль) добавляли пент-4-ин-1-ол (157 мкл, 1,70 ммоль). Реакционную смесь дегазировали N2, и нагревали при 60C в течение 2,5 ч, и затем охлаждали до температуры окружающей среды. Полученную смесь упаривали в вакууме и остаток растирали с EtOAc (5,0 мл) и высушивали в вакууме, получая 2-4-амино-3-(4-гидроксифенил)-1 Нпиразоло[3,4-d]пиримидин-1-ил)метил)-3-(2-хлорбензил)-5-(5-гидроксипент-1-инил)хиназолин-4(3H)-он (16) в форме твердого вещества коричневого цвета (488 мг, чистота 92%, 89%): m/z 590/592 (М+Н)+ (ES+) (способ D). К перемешиваемой суспензии спирта (16) (162 мг, чистота 92%, 0,252 ммоль) в DCM (8,0 мл) добавляли йод (121 мг, 0,477 ммоль), трифенилфосфин (115 мг, 0,438 ммоль) и имидазол (35 мг, 0,51 ммоль) и смесь поддерживали при температуре окружающей среды в течение 2 ч. Реакционную смесь упаривали в вакууме и остаток очищали флэш-хроматографией на колонке (SiO2, 40 г, MeOH в DCM, элюирование с градиентом 0-10%), получая промежуточное соединение F (109 мг, 73%, чистые, 45,0%) в форме твердого вещества желтого цвета: m/z 702/704 (М+Н)+ (ES+) (способ D), которое использовали без дальнейшей очистки в последующих превращениях. Дополнительные промежуточные соединения и некоммерческие строительные блоки, показанные на реакционных схемах, которые следуют далее, получали, используя процедуры, описанные выше для аналогичных производных, или способами, описанными в цитируемых литературных ссылках (табл. 1).
МПК / Метки
МПК: A61P 11/00, A61K 31/519, A61P 35/00, A61P 17/00, A61P 19/02, A61P 11/06, C07D 487/04
Метки: хиназолиновые, соединения
Код ссылки
<a href="https://eas.patents.su/30-20330-hinazolinovye-soedineniya.html" rel="bookmark" title="База патентов Евразийского Союза">Хиназолиновые соединения</a>
Предыдущий патент: Плазменная печь
Следующий патент: Способ производства фармацевтического препарата, содержащего алискирен
Случайный патент: Способ получения диарилкарбоната