Производные рифамицина
Номер патента: 20201
Опубликовано: 30.09.2014
Авторы: Кампана Мануэла, Росини Гоффредо, Канната Винченцо, Фолегатти Маена, Вискоми Джузеппе Клаудио, Риги Паоло
Формула / Реферат
1. Соединение формулы I
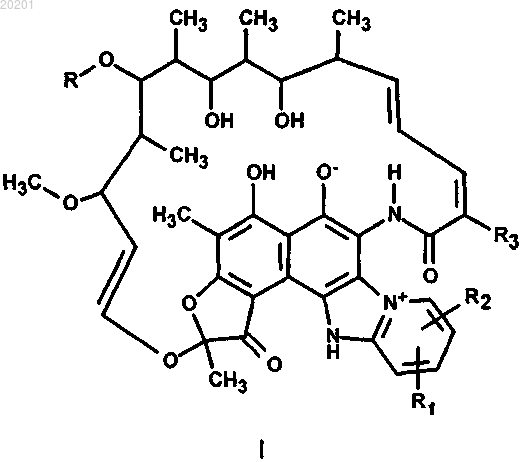
где R представляет собой водород или ацетил;
каждый из R1 и R2 независимо выбран из группы, состоящей из водорода, (С1-4)алкила, (С1-3)алкокси(С1-4)алкила, гидроксиметила, гидрокси(С2-4)алкила; или
R1 и R2, взятые вместе с двумя последовательными атомами углерода пиридинового кольца, образуют бензольное кольцо, незамещенное или моно- или дизамещенное одной или двумя метильными или этильными группами; и
R3 представляет собой гидрокси(С1-4)алкил.
2. Соединение по п.1, где R представляет собой ацетильную группу; R1 и R2 независимо представляют собой водород или метил и R3 представляет собой гидрокси(С1-4)алкил.
3. Соединение по п.2, где R представляет собой ацетильную группу; R1 представляет собой водород; R2 представляет собой п-метил и R3 представляет собой гидроксиметил, имеющее название (16Z,18E,28E)-25-(ацетилокси)-5,21,23-тригидрокси-16-(гидроксиметил)-27-метокси-2,4,11,20,22,24,26-гептаметил-1,15-диоксо-1,13-дигидро-2Н-2,7-(эпоксипента-дека[1,11,13]триенимино)фуро[2",3":7',8']нафто[1',2':4,5]имидазо[1,2-а]пиридин-8-ий-6-олят.
4. Способ получения соединения формулы II
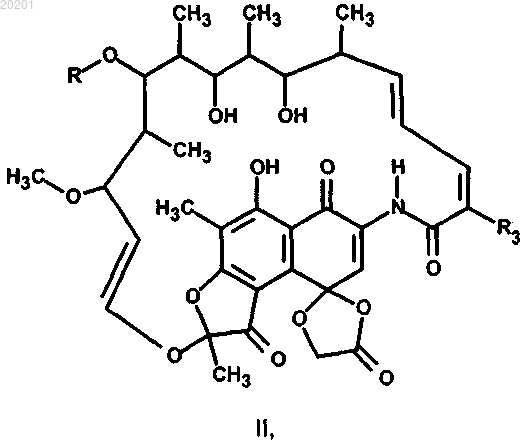
где R представляет собой водород или ацетил и
R3 представляет собой гидрокси(С1-4)алкил,
включающий
получение биологической культуры, содержащей в водном растворе микроорганизм, выбранный из Streptomyces mediterranei и Nocardia mediterranea, и питательные агенты; и
окисление полученной культуры окислителем,
где окислитель выбран из одного или более чем одного из нитрита натрия, водного раствора дихромата калия, персульфата аммония или периодата натрия.
5. Способ по п.4, где R представляет собой ацетил и R3 представляет собой гидроксиметил.
6. Способ синтеза соединения по п.1, включающий взаимодействие соединения формулы II

где R представляет собой водород или ацетил и
R3 представляет собой гидрокси(С1-4)алкил,
с соединением формулы III
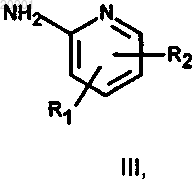
где каждый из R1 и R2 независимо выбран из группы, состоящей из водорода, (С1-4)алкила, (С1-3)алкокси(С1-4)алкила, гидроксиметила, гидрокси(С2-4)алкила; или
R1 и R2, взятые вместе с двумя последовательными атомами углерода пиридинового кольца, образуют бензольное кольцо, незамещенное или моно- или дизамещенное одной или двумя метильными или этильными группами,
в присутствии органического растворителя, смеси из более чем одного органического растворителя или смеси органического растворителя с водой при температуре от температуры окружающей среды до 60°C в течение 1-100 ч, где органический растворитель выбран из группы, состоящей из ароматических углеводородов, выбранных из толуола и бензола, низших галогенированных углеводородов, выбранных из метиленхлорида, хлороформа, 1,2-дихлорэтана, низших алканолов, выбранных из метанола, этанола, пропанола, изопропанола или н-бутанола, ацетонитрила, диоксана, тетрагидрофурана и их комбинаций или смеси с водой в различных объемных соотношениях.
7. Способ по п.6, где на каждый молярный эквивалент соединения формулы II используют от примерно 0,1 до примерно 1 мол.экв. йода или комбинации йод/окислитель.
8. Способ по п.6, где соединение формулы III представляет собой 2-амино-4-метилпиридин.
9. Способ синтеза соединения формулы I

включающий
получение биологической культуры, содержащей в водном растворе микроорганизм, выбранный из Streptomyces mediterranei и Nocardia mediterranea, и питательные агенты;
окисление полученной культуры окислителем с получением окисленного продукта формулы II

где R представляет собой водород или ацетил и
R3 представляет собой гидрокси(С1-4)алкил, и
взаимодействие соединения формулы II с производным 2-аминопиридина формулы III

где R1 и R2 такие, как определено в п.6.
10. Антибактериальная фармацевтическая композиция, содержащая терапевтически эффективное количество соединения формулы I в комбинации с одним или более чем одним фармацевтически приемлемым ингредиентом.
11. Применение антибактериальной фармацевтической композиции, содержащей одно или более чем одно соединение формулы I и фармацевтически приемлемый эксципиент, для лечения, предотвращения или ослабления чрезмерного развития микрофлоры у пациента, страдающего связанным с пищеварительным трактом расстройством.
12. Применение антибактериальной фармацевтической композиции, содержащей одно или более чем одно соединение формулы I в комбинации с одним или более чем одним соединением формулы II и фармацевтически приемлемый эксципиент, для лечения, предотвращения или ослабления чрезмерного развития микрофлоры у пациента, страдающего связанным с пищеварительным трактом расстройством.
13. Применение по п.11, где композиция дополнительно содержит рифаксимин или неомицин.
Текст
Раскрыты соединения, представляющие собой производные рифамицина формулы I, гдеR представляет собой водород или ацетил; R1 и R2 независимо выбраны из группы, состоящей из водорода, (С 1-4)алкила, (С 1-3)алкокси(С 1-4)алкила, гидроксиметила, гидрокси(С 2-4)алкила; или R1 иR2, взятые вместе с двумя последовательными атомами углерода пиридинового кольца, образуют бензольное кольцо, незамещенное или моно- или дизамещенное одной или двумя метильными или этильными группами; и R3 представляет собой гидрокси(С 1-4)алкил. Раскрытые соединения обладают антибактериальной активностью. Также описаны способы синтеза этих соединений,фармацевтическая композиция, содержащая соединение формулы I, и применение такой композиции. Область изобретения Настоящее изобретение относится к области фармацевтических композиций, в частности к области пероральных препаратов, для лечения воспалительных заболеваний пищеварительного тракта. Предшествующий уровень техники Рифаксимин (rifaximin, INN; см. The Merck Index, XIII Ed., 8304), антибиотик, принадлежащий к классу рифамицинов, представляет собой пиридоимидазорифамицин, описанный и заявленный в патенте Италии IT 1154655. В европейском патенте ЕР 0161534 описан способ его получения, начиная с рифамицина О (The Merck Index, XIII Ed., 8301). Способы получения полиморфных форм рифаксимина описаны в публикации заявки на патент США 2008-0262232 (Viscomi et al.), которая в полном объеме включена в данный документ посредством ссылки. Рифаксимин используют для лечения острых и хронических кишечных инфекций, вызванных грамположительными и грамотрицательными бактериями, а также в качестве вспомогательного средства при терапии гипераммониемии. Рифаксимин продается в США как XIFAXAN для лечения диареи путешественников, вызванной неинвазивными штаммами Escherichia coli. Также рифаксимин используют для лечения диареи, ассоциированной с Clostridum difficile, болезни Крона, дивертикулита, печеночной энцефалопатии, инфекционной диареи, синдрома раздраженной толстой кишки, паучита, гипертрофии тонкой кишки, диареи путешественников, неспецифического язвенного колита, а также для эрадикации Helicobacter pylori и профилактики после желудочно-кишечной хирургии. В уровне техники известны производные рифамицина, несущие гетероциклическое кольцо, конденсированное в 3,4-положении. Например, в патентах США 4263404 и 4341785 описаны производные рифамицина и имидазорифамицина. Рифамицины обладают антибактериальной активностью и их получают из вторичных метаболитов культур микроорганизмов, полезных для лечения инфекций, в частности туберкулеза, как описано Sensi P. вFarmaco [Sci], (1959); 14:146-7 и Mitnick C.D. et al. в Expert Opin. Pharmacother. (2009); 10:381-401. Недавно были идентифицированы производные рифамицина, являющиеся активаторами рецептора X прегнана (PXR), члена семейства ядерных рецепторов, который регулирует экспрессию метаболического фермента, вовлеченную в реакции млекопитающих на химическую стимуляцию, как описано в Natl.Acad. Sci. USA (1998), 95:12208-12213. Рифамицины характеризуются химической структурой, состоящей из одного или более конденсированных ароматических колец, образующих циклическую структуру с алифатическим кольцом, как описано Prelong, V. et al. в Helv. Chim. Acta (1973); 56:2279. Аналоги рифамицина получают химической модификацией ароматической или алифатической части молекулы, как описано Sensi P. в ResearchMartinelli E. et al. описывают в J. Antibiot. 31 (10), 949, 1978 рифамицин R, полученный от мутантного продуцента рифомицина Nocardia mediterranea, но о биологической активности этого соединения не сообщается. Рифамицин является антибиотиком, использующимся в терапии туберкулеза, и важно располагать новыми антибиотиками без какой-либо антибиотической резистентности к рифамицину. Настоящее изобретение решает проблему получения нового замещенного рифаксимина, производного рифамицина О, но обладающего отличающейся от него антибиотической активностью. Описание изобретения В данном документе раскрыто соединение формулы I где R представляет собой водород или ацетил; каждый из R1 и R2 независимо выбран из группы, состоящей из водорода, (С 1-4)алкила,(С 1-3)алкокси(С 1-4)алкила, гидроксиметила, гидрокси(С 2-4)алкила; илиR1 и R2, взятые вместе с двумя последовательными атомами углерода пиридинового кольца, образуют бензольное кольцо, которое является незамещенным или моно- или дизамещенным одной или двумя метильными или этильными группами; и-1 020201 В некоторых воплощениях R представляет собой ацетильную группу; R1 и R2 независимо представляют собой водород или метил и R3 представляет собой гидрокси(С 1-4)алкил. В других воплощениях R представляет собой ацетильную группу; R1 представляет собой водород; R2 представляет собой параметил и R3 представляет собой гидроксиметил (т.е. соединение (16Z,18 Е,28 Е)-25-(ацетилокси)-5,21,23 тригидрокси-16-(гидроксиметил)-27-метокси-2,4,11,20,22,24,26-гептаметил-1,15-диоксо-1,13-дигидро 2 Н-2,7-(эпоксипента-дека[1,11,13]триенимино)фуро[2",3":7',8']нафто[1',2':4,5]имидазо[1,2-а]пиридин-8 ий-6-олят). В другом аспекте раскрыт способ получения соединения формулы II где R представляет собой водород или ацетил;Streptomyces mediterranea и Nocardia mediterranea, в водном растворе и питательные вещества и окисление полученной культуры окислителем,где окислитель выбран из одного или более чем одного из следующих соединений: нитрит натрия,водный раствор дихромата калия, персульфат аммония или периодат натрия. В определенных воплощениях R представляет собой ацетил и R3 представляет собой гидроксиметил. В другом аспекте раскрыт способ синтезирования соединения по п.1, включающий взаимодействие соединения формулы II где R представляет собой водород или ацетил и R3 представляет собой гидрокси(С 1-4)алкил, с соединением формулы III где каждый из R1 и R2 независимо выбран из группы, состоящей из водорода, (С 1-4)алкила,(С 1-3)алкокси(С 1-4)алкила, гидроксиметила, гидрокси(С 2-4)алкила; илиR1 и R2, взятые вместе с двумя последовательными атомами углерода пиридинового кольца, образуют бензольное кольцо, которое является незамещенным или моно- или дизамещенным одной или двумя метильными или этильными группами,в присутствии органического растворителя, смеси более чем одного органического растворителя или смеси органического растворителя с водой при температуре от температуры окружающей среды до 60 С в течение периода времени от 1 до 100 ч, где органический растворитель выбран из группы, состоящей из ароматических углеводородов, выбранных из толуола или бензола, низших галогенированных углеводородов, выбранных из метиленхлорида, хлороформа, 1,2-дихлорэтана, низших алканолов,выбранных из метанола, этанола, пропанола, изопропанола или н-бутанола, ацетонитрила, диоксана, тетрагидрофурана и их комбинации или в смеси с водой в различных объемных соотношениях.-2 020201 В определенных воплощениях на каждый молярный эквивалент соединения формулы II используют от примерно 0,1 до примерно 1 мол.экв. йода или комбинации йод/окислитель. В других воплощениях соединение формулы III представляет собой 2-амино-4-метилпиридин. В другом аспекте раскрыт способ синтезирования соединения по п.1, включающий получение биологической культуры, содержащей микроорганизм, выбранный из Streptomycesmediterranei и Nocardia mediterranea, в водном растворе и питательные вещества; окисление полученной культуры окислителем с получением окисленного продукта формулы II где R представляет собой водород или ацетил;R3 представляет собой гидрокси(С 1-4)алкил,и взаимодействие соединения формулы II с производным 2-аминопиридина формулы III где R1 и R2 такие, как определено выше. Еще один аспект касается антибактериальной фармацевтической композиции, содержащей терапевтически эффективное количество соединения формулы I в комбинации с одним или более чем одним фармацевтически приемлемым ингредиентом. В другом аспекте изобретения раскрыто применение антибактериальной фармацевтической композиции, содержащей одно или более чем одно соединение формулы I и фармацевтически приемлемый эксципиент, для лечения, предотвращения или ослабления чрезмерного развития микрофлоры у пациента, страдающего связанным с пищеварительным трактом расстройством. В еще одном аспекте изобретения раскрыто применение антибактериальной фармацевтической композиции, содержащей одно или более чем одно соединение формулы I в комбинации с одним или более чем одним соединением формулы II и фармацевтически приемлемый эксципиент, для лечения,предотвращения или ослабления чрезмерного развития микрофлоры у пациента, страдающего связанным с пищеварительным трактом расстройством. В некоторых воплощениях изменение уровня чрезмерного развития микрофлоры отражает эффективность лечения, где снижение уровня чрезмерного развития микрофлоры свидетельствует об эффективности лечения или где изменение уровня чрезмерного развития микрофлоры является признаком того, что субъект, вероятно, проявляет благоприятную клиническую реакцию на лечение. В одном воплощении изобретения применяемая композиция дополнительно содержит рифаксимин или неомицин. В определенных воплощениях соединение формулы I присутствует в соотношении от примерно 0,01 до 100% (мас./мас.) относительно рифаксимина. Краткое описание графических материалов На фиг. 1 показана ВЭЖХ хроматограмма соединения формулы II, где R представляет собой ацетил и R3 представляет собой гидроксиметил [(12'Z,14'Е,24'Е)-5',17',19'-тригидрокси-12'-(гидроксиметил)-23'метокси-2',4',16',18',20',22'-гексаметил-1',4,6',11'-тетраоксо-1',2'-дигидро-6'Н-спиро[1,3-диксолан-2,9'[2,7]-(эпоксипента-дека[1,11,13]триенимино)нафто[2,1-b]фуран]-21'-илацетат]. На фиг. 2 показан 1 Н ЯМР спектр соединения формулы II, где R представляет собой ацетил и R3 представляет собой гидроксиметил [(12'Z,14'Е,24'Е)-5',17',19'-тригидрокси-12'-(гидроксиметил)-23'метокси-2',4',16',18',20',22'-гексаметил-1',4,6',11'-тетраоксо-1',2'-дигидро-6'Н-спиро[1,3-диксолан-2,9'[2,7]-(эпоксипента-дека[1,11,13]триенимино)нафто[2,1-b]фуран]-21'-илацетат]. На фиг. 3 показана ВЭЖХ хроматограмма соединения формулы I, где R представляет собой ацетил;R1 представляет собой водород; R2 представляет собой метил и R3 представляет собой гидроксиметил-3 020201 На фиг. 4 показан ИК-спектр соединения формулы I, где R представляет собой ацетил; R1 представляет собой водород; R2 представляет собой метил и R3 представляет собой гидроксиметил[(16Z,18 Е,28 Е)-25-(ацетилокси)-5,21,23-тригидрокси-16-(гидроксиметил)-27-метокси-2,4,11,20,22,24,26 гептаметил-1,15-диоксо-1,13-дигидро-2 Н-2,7-(эпоксипента-дека[1,11,13]триенимино)фуро[2",3":7',8']нафто[1',2':4,5]имидазо[1,2-а]пиридин-8-ий-6-олят]. На фиг. 5 показан 1 Н ЯМР спектр соединения формулы I, где R представляет собой ацетил; R1 представляет собой водород; R2 представляет собой метил и R3 представляет собой гидроксиметил[(16Z,18E,28E)-25-(ацетилокси)-5,21,23-тригидрокси-16-(гидроксиметил)-27-метокси-2,4,11,20,22,24,26 гептаметил-1,15-диоксо-1,13-дигидро-2 Н-2,7-(эпоксипента-дека[1,11,13]триенимино)фуро[2",3":7',8']нафто[1',2':4,5]имидазо[1,2-а]пиридин-8-ий-6-олят]. На фиг. 6 показан 13 С ЯМР спектр полученного соединения формулы I, где R представляет собой ацетильную группу; R1 представляет собой водород; R2 представляет собой метил и R3 представляет собой гидроксиметил[(16Z,18 Е,28 Е)-25-(ацетилокси)-5,21,23-тригидрокси-16-(гидроксиметил)-27 метокси-2,4,11,20,22,24,26-гептаметил-1,15-диоксо-1,13-дигидро-2 Н-2,7-(эпоксипента-дека[1,11,13]триенимино)фуро[2",3":7',8']нафто[1',2':4,5]имидазо[1,2-а]пиридин-8-ий-6-олят]. На фиг. 7 показан спектр МС-ИЭУ (масс-спектроскопия с ионизацией электронным ударом) соединения формулы I, где R представляет собой ацетильную группу; R1 представляет собой водород;R2 представляет собой метил и R3 представляет собой гидроксиметил. Подробное описание изобретения В одном аспекте раскрыты производные рифамицина формулы I где R представляет собой водород или ацетил; каждый из R1 и R2 независимо выбран из группы, состоящей из водорода, (С 1-4)алкила,(С 1-3)алкокси(С 1-4)алкила, гидроксиметила, гидрокси(С 2-4)алкила; илиR1 и R2, взятые вместе с двумя последовательными атомами углерода пиридинового кольца, образуют бензольное кольцо, где бензольное кольцо является незамещенным, монозамещенным или дизамещенным метилом или этилом; иR3 представляет собой гидрокси(С 1-4)алкил. В одном воплощении соединений формулы I R представляет собой ацетил; каждый из R1 и R2 независимо выбран из водорода или метила и R3 представляет собой (С 1-4)гидроксиалкил. Другой аспект включает соединение формулы I, где R представляет собой ацетил; R1 представляет собой водород; R2 представляет собой п-метил и R3 представляет собой гидроксиметил, имеющее название(16Z,18E,28E)-25-(ацетилокси)-5,21,23-тригидрокси-16-(гидроксиметил)-27-метокси 2,4,11,20,22,24,26-гептаметил-1,15-диоксо-1,13-дигидро-2 Н-2,7-(эпоксипентадека[1,11,13]триенимино)фуро[2",3":7',8']нафто[1',2':4,5]имидазо[1,2-а]пиридин-8-ий-6-олят. В данном документе термины (С 1-3)алкил, (С 2-4)алкил и (С 1-4)алкил идентифицируют линейные или разветвленные алкильные радикалы, содержащие от 1 до 3, или от 2 до 4, или от 1 до 4 углеродных атомов соответственно, такие как, например, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил или трет-бутил, тогда как термин (С 1-3)алкокси, по существу, относится к группам метокси, этокси,пропокси или изопропокси. Представленные здесь соединения могут быть получены согласно способам, которые зависят от типа соединений, которые требуется получить. Так, например, соединения формулы I, где R и R3 являются такими, как определено выше, могут быть получены посредством взаимодействия соединений формулыII, полученных как промежуточный продукт в способе, аналогичном способу, описанному в патенте США 4263404, с незамещенными или замещенными 2-аминопиридиновыми соединениями формулы III,как определено ниже: где R1, R2 и R3 имеют такое же значение, как определено выше. Соединения формулы II могут быть получены из подходящей биологической культуры микроорганизмов, таких как Streptomyces mediterranei или Nocardia mediterranea, в присутствии окислителя, такого как нитрит натрия, дихромат калия, персульфат аммония, периодат натрия. В общем соединения формулы II, в частности, когда R1 представляет собой Н; R2 представляет собой метил; R представляет собой ацетил и R3 представляет собой гидроксиметил, могут быть получены в результате процесса очистки смеси, полученной из вышеуказанной биологической культуры. Метод очистки может представлять собой, например, хроматографию, кристаллизацию и экстракцию органическим растворителем. Аналитические методы, полезные для идентификации, и характеристики полученных соединений включают 1 Н ЯМР, ИК-спектроскопию, масс-спектроскопию с ионизацией электронным ударом (МС-ИЭУ) и хроматографию (ВЭЖХ). Полученные соединения формулы II могут взаимодействовать с молярным избытком выбранного производного аминопиридина формулы III в подходящей системе растворителей, из которой требуемый конечный продукт соединений формулы I извлекают с помощью известных специалистам способов. Молярный избыток варьирует от примерно 2 до примерно 8 или более эквивалентов, рассчитанных по соединению формулы II. Взаимодействие может быть осуществлено, например, в присутствии растворителя или системы растворителей, которые обычно выбирают из растворителей, обычно использующихся в химии рифамицинов. Например, могут быть использованы ароматические углеводороды, такие как бензол или толуол,низшие галогенированные углеводороды, такие как метиленхлорид, хлороформ, 1,2-дихлорэтан или т.п.,низшие алканолы, такие как метанол, этанол, пропанол, изопропанол или н-бутанол. Также пригодны для применения низшие алкильные эфиры низшей алифатической кислоты, гликоли, ацетонитрил, диоксан и тетрагидрофуран. Эти растворители могут быть использованы по отдельности или в виде смеси,содержащей два или более чем два вышеуказанных растворителя, а также в смеси с водой в различных объемных соотношениях. Предпочтительные растворители включают бензол, толуол, низшие галогенированные углеводороды, низшие алканолы сами по себе или в смеси с водой, ацетонитрил, гликоли, диоксан и тетрагидрофуран, используемые сами по себе, или в комбинации, или в смеси с водой. Взаимодействие может происходить при давлении окружающей среды и в широком интервале температур, например от комнатной температуры до температуры кипения реакционной смеси. Было обнаружено, что для получения описанных здесь соединений полезен диапазон температур от комнатной температуры, например 20C, до примерно 60C. Реакция завершалась в течение периода времени, который варьировал в зависимости от природы аминопиридинового субстрата формулы III и условий, в которых проводилась реакция. Обычно для получения конечных продуктов формулы I с желательными выходами требовалось от примерно 1 до примерно 100 ч. Было обнаружено, что протеканию реакции способствует проведение взаимодействия в присутствии йода или подходящей комбинации йод/окислитель; где йод может представлять собой, например, йодид щелочного или щелочно-земельного металла и гидроиодид того же самого исходного производного пиридина, а окислитель может представлять собой агент, способный в условиях реакции окислять ион йода с высвобождением йода в реакционную смесь. Йод или йод/окислитель могут присутствовать в реакционной смеси соответственно в количествах от примерно 0,1 до примерно 1 мол.экв. йода на каждый моль исходного соединения, представленного формулой II. В этом случае, однако, реакционный раствор может быть впоследствии обработан подходящим восстановителем, например аскорбиновой кислотой, изоаскорбиновой кислотой или дигидроксиацетоном. Полученные соединения могут быть подвергнуты дальнейшим химическим взаимодействиям для получения других соединений формулы I. Так, например, соединение формулы I, где R, R1, R2 и R3 являются такими, как определено выше, может быть получено посредством обработки полученного соединения подходящим восстановителем, таким как, например, (L-)аскорбиновая кислота.-5 020201 Соединения формулы I, где R представляет собой водород, могут быть получены посредством гидролиза в щелочных условиях соответствующего соединения, где R представляет собой ацетил. Представленные здесь соединения могут быть извлечены из реакционной среды, например, с помощью способов, известных квалифицированным специалистам. Эти способы включают экстракцию подходящим органическим растворителем, например этилацетатом, хлороформом, метиленхлоридом и их аналогами или их смесью, выпаривание досуха органического экстракта и перенос остатка в подходящий растворитель, из которого выделяют конечный продукт. Альтернативно, смесь может быть непосредственно выпарена досуха и полученный остаток, в свою очередь, перенесен в подходящий растворитель, из которого выделяют конечный продукт кристаллизацией или хроматографией. Растворители, которые можно успешно применять, выбирают из воды, метанола этанола, н-пропанола, изопропанола,н-гексана, этилацетата, метилена хлороформа, монометилового эфира этиленгликоля или их смеси. Представленные здесь соединения могут быть получены из продукта реакции, например, с чистотой выше чем 90%, с помощью известных в уровне техники способов очистки, таких как хроматография. Представленные здесь соединения полезны в качестве антибактериальных агентов. Они обладают активностью in vitro против как грамположительных, так и грамотрицательных бактерий. Соединения оказывают антибактериальное действие на бактерии, выделенные из клинических препаратов, которые могут быть обнаружены в кишечной бактериальной флоре при патологических состояниях. Антибактериальная активность соединений формулы I была показана с помощью измерения минимальной концентрации активного вещества, способной ингибировать рост патогенных бактерий in vitro(МИК). Ее выражают в миллиграммах вещества на 1 л культуральной среды. Антибактериальная активность одного из наиболее репрезентативных соединений формулы I, гдеR представляет собой ацетильную группу, R1 и R2 независимо представляют собой водород или метильную группу и R3 представляет собой гидроксиметил, была измерена для большого количества штаммов бактерий, принадлежащих к различным семействам, таким как Enterobacteriaceae, грамотрицательным не-Enterobacteriaceae, Staphylococcus. Значения МИК находятся в пределах от 0,06 до 128 мг/л, и эти значения показывают антибактериальную эффективность соединения формулы I. В другом аспекте представленные здесь соединения могут быть использованы в качестве антибактериальных агентов, включая их введение в состав фармацевтических композиций. Эти соединения могут быть использованы по отдельности или в комбинации с другими антибиотиками, такими как рифампицин, рифамицин, неомицин и/или рифаксимин, и в широком диапазоне массовых соотношений, предпочтительно от 0,01 до 100 мас.%. В другом аспекте фармацевтический препарат содержит соединения формулы I с фармацевтически приемлемым носителем, разбавителем или эксципиентом. Тем самым представленные здесь соединения могут быть введены различными путями, например перорально, местно или парентерально. Для такого введения соединения воплощают в виде общепринятых фармацевтических дозированных композиций. Эти композиции могут содержать соединения формулы I по отдельности или в смеси с соединением формулы II или другим фармацевтически активным ингредиентом вместе с обычными добавками, такими как, например, подсластители, корригенты, красители, покрывающие вещества, консерванты, инертные разбавители, такие как, например, карбонат кальция или натрия, лактоза и тальк, связывающие агенты, например крахмал, желатин и поливинилпирролидон,суспендирующие агенты, например метилцеллюлоза или гидроксиэтилцеллюлоза, и увлажняющие агенты, такие как, например, лецитин, стеараты полиоксиэтилена и сорбитанмоноолеат полиоксиэтилена. Препараты, полезные для местного и парентерального введения, могут содержать активные ингредиенты, растворенные или суспендированные в дистиллированной и апирогенной воде, в смеси с обычно используемыми фармацевтическими носителями. Другим аспектом настоящего изобретения является применение соединения формулы I отдельно,или в комбинации с другим соединением формулы I, или в комбинации с соединением формулы II, или в комбинации с другими фармацевтически активными агентами для лечения или предотвращения бактериальных инфекций. В частности, раскрытые здесь фармацевтические композиции могут быть использованы для лечения пациента, страдающего связанным с пищеварительным трактом расстройством, включая одно или более чем одно из следующего: синдром раздраженной толстой кишки, диарею, диарею, ассоциированную с микроорганизмами, диарею, ассоциированную с Clostridum difficile, диарею путешественников, чрезмерное развитие микрофлоры тонкого кишечника, болезнь Крона, хронический панкреатит, недостаточность поджелудочной железы, колит, печеночную энцефалопатию, дивертикулез и паучит, но ограничиваясь ими. В другом аспекте настоящего изобретения раскрытые здесь соединения обладают антибактериальной активностью и играют роль в активации прегнанового X рецептора (PRX), ядерного рецептора, регулирующего гены, вовлеченные в отложение ксенобиотиков и частично эндобиотиков и детоксикацию. В данном документе предложены способы лечения, предотвращения или ослабления связанных с пищеварительным трактом расстройств, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества одного или более чем одного соединения, раскрытого здесь. Связанные с пищеварительным трактом расстройства включают одно или более чем одно из следующего: син-6 020201 дром раздраженной толстой кишки, диарею, диарею, ассоциированную с микроорганизмами, диарею,ассоциированную с Clostridum difficile, диарею путешественников, чрезмерное развитие микрофлоры тонкого кишечника, болезнь Крона, хронический панкреатит, недостаточность поджелудочной железы,колит, печеночную энцефалопатию, дивертикулез и паучит. Продолжительность лечения для конкретного расстройства, связанного с пищеварительным трактом, будет зависеть, в частности, от расстройства. Например, диарея путешественников может потребовать лечения длительностью всего от 12 до примерно 72 ч, тогда как болезнь Крона может потребовать лечения в течение от примерно 2 дней до 3 месяцев. Дозировка также будет зависеть от болезненного состояния. Подходящие диапазоны доз предложены в данном документе ниже. В данном документе предложены способы лечения или предотвращения патологического состояния у пациента с подозрением на воздействие на него средств биологической войны. Идентификация пациентов, требующих профилактического лечения связанного с пищеварительным трактом расстройства, находится в пределах компетенции и знаний специалиста в данной области. В медицинской практике приняты определенные способы идентификации пациентов с повышенным риском развития связанного с пищеварительным трактом расстройства, которое можно лечить раскрытыми здесь способами, такие как семейный анамнез, история путешествий и планы предполагаемых путешествий, наличие факторов риска, связанных с развитием этого болезненного состояния у данного пациента. Практикующий врач, являющийся специалистом в данной области, может легко идентифицировать таких потенциальных пациентов с помощью, например, клинических тестов, медицинского осмотра, общего и семейного анамнеза, истории поездок. Способ оценки эффективности лечения субъекта включает определение долечебного уровня чрезмерного развития кишечной микрофлоры способами, хорошо известными из уровня техники (например,с помощью водородного дыхательного теста, биопсии, взятия проб кишечных бактерий и т.д.), и затем введение субъекту терапевтически эффективного количества представленных здесь соединений. Через подходящий период времени с момента введения соединения (например, после начального периода лечения), например через 2, 4, 8, 12 или 72 ч, снова определяют уровень чрезмерного развития микрофлоры. Изменение бактериального уровня показывает эффективность лечения. В ходе лечения уровень чрезмерного развития бактериальной микрофлоры можно измерять периодически. Например, чрезмерное развитие микрофлоры можно контролировать каждые несколько часов, дней или недель для оценки дальнейшей эффективности лечения. Снижение уровня чрезмерного развития микрофлоры свидетельствует об эффективности лечения. Описанный способ может быть использован для скрининга или отбора пациентов, на которых лечение представленными здесь соединениями может оказать благоприятное воздействие. Еще один аспект составляет способ лечения субъекта, страдающего или восприимчивого к расстройству пищеварительного тракта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества представленных здесь соединений с целью его лечения. После идентификации субъекта, страдающего или восприимчивого к расстройству пищеварительного тракта, например СРТК, вводят одно или более чем одно представленное здесь соединение. В одном аспекте способы оценки эффективности лечения субъекта с помощью представленного здесь соединения или его смеси с другими активными ингредиентами, включают определение долечебного уровня чрезмерного развития бактериальной микрофлоры, введение субъекту терапевтически эффективного количества соединения формул I или II, либо по отдельности, либо в комбинации с другими активными ингредиентами и определение чрезмерного развития бактериальной микрофлоры у субъекта после начального периода лечения представленными здесь соединениями, где изменение уровня чрезмерного развития микрофлоры показывает эффективность антибактериального лечения. Эффективность лечения может быть измерена, например, по снижению уровня чрезмерного развития бактериальной микрофлоры. Также эффективность может быть измерена, исходя из ослабления симптомов, ассоциированных с расстройством пищеварительного тракта, стабилизации симптомов или исчезновения симптомов, ассоциированных с расстройством пищеварительного тракта, например ослабления тошноты, метеоризма, диареи и тому подобных симптомов. В одном аспекте способы контроля состояния субъекта в ходе лечения с помощью представленных здесь соединений включают определение долечебного уровня чрезмерного развития микрофлоры, введение субъекту терапевтически эффективного количества представленного здесь соединения и определение чрезмерного развития микрофлоры у субъекта после начального периода лечения представленными здесь соединениями, где изменение уровня чрезмерного развития микрофлоры показывает эффективность антибактериального лечения. Другой аспект настоящего изобретения составляют фармацевтические препараты, содержащие, например, эффективное количество производного рифамицина отдельно или в комбинации с другими фармацевтически активными ингредиентами в фармацевтически приемлемом носителе. В следующем воплощении эффективное количество является эффективным для лечения бактериальной инфекции, например чрезмерного развития микрофлоры тонкого кишечника, болезни Крона, печеночной энцефалопатии, колита, обусловленного антибиотиками и/или дивертикулеза.-7 020201 Примеры применения для лечения диареи путешественников приведены в Infante R.M., EricssonDiarrhea With Rifaximin on Various Continents. The American Journal of Gastroenterology. May 2003, volume 98, Number 5, которые в полном объеме включены в данный документ посредством ссылок. Фармацевтические композиции могут содержать одно или более чем одно соединение формул I илиII или могут содержать смесь более чем одного соединения, представленного одной и той же формулой,или смесь соединений формулы I с соединениями формулы II, или смесь с другими фармацевтически активными ингредиентами. Смеси могут быть выбраны, например, исходя из необходимого уровня системной адсорбции, профиля растворения, участка пищеварительного тракта, требующего лечения и тому подобных факторов. Фармацевтические композиции могут содержать носитель, например один или более чем один из следующего: разбавитель, связывающий агент, смазывающий агент, разрыхлитель, краситель, корригент или подсластитель. Композиции могут быть составлены для выбранных таблеток с оболочкой или без оболочки, твердых и мягких желатиновых капсул, покрытых сахаром пилюль, леденцов, облаток, пеллет и порошков в запечатанных пакетах. Например, композиции могут быть составлены для местного применения в виде, например, мазей, помад, кремов, гелей и лосьонов. Производные рифамицина вводят субъекту, используя фармацевтически приемлемую композицию,например фармацевтически приемлемую композицию, которая обеспечивает длительную доставку субъекту в течение по меньшей мере 12, 24, 36, 48 ч, одной, двух, трех или четырех недель после введения субъекту фармацевтически приемлемой композиции. Эти фармацевтические композиции пригодны для местного или перорального введения субъекту. В других воплощениях, как подробно описано ниже, представленные здесь фармацевтические композиции могут быть специально составлены для введения в твердой или жидкой форме, включая композиции,адаптированные для следующих способов введения: (1) перорального введения, например в виде микстур (водные или неводные растворы или суспензии), таблеток, болюсов, порошков, гранул, паст; (2) парентерального введения, например подкожной, внутримышечной или внутривенной инъекцией, например в виде стерильного раствора или суспензии; (3) местного введения, например в виде крема, мази или спрея, наносимого на кожу; (4) интравагинального или интраректального введения, например в виде пессария, крема или пены; или (5) аэрозольного введения, например в виде водного аэрозоля,липосомального препарата или твердых частиц, содержащих соединение. Термин "фармацевтически приемлемый" относится к тем представленным здесь соединениям, композициям, содержащим такие соединения, и/или лекарственным формам, которые в рамках тщательной медицинской оценки признаны пригодными для использования в контакте с тканями человека и животных с разумным соотношением пользы и риска без чрезмерной токсичности, раздражения и аллергической реакции или других проблем или осложнений Термин "фармацевтически приемлемый носитель" включает фармацевтически приемлемое вещество, композицию или носитель, такие как жидкий или твердый наполнитель, разбавители, эксципиенты,растворители или инкапсулирующий материал, вовлеченные в перенос или транспортировку целевого химического вещества от одного органа или части тела к другому органу или части тела. Все носители предпочтительно "приемлемы" в смысле совместимости с другими ингредиентами композиции и не вредны для пациента. Некоторые примеры веществ, которые могут служить фармацевтически приемлемыми носителями, включают: (1) сахара, такие как лактоза, глюкоза и сахароза; (2) крахмалы, такие как кукурузный крахмал и картофельный крахмал; (3) целлюлозу и ее производные, такие как натрийкарбоксиметилцеллюлоза, этилцеллюлоза и ацетат целлюлозы; (4) порошкообразный трагакант;(5) солод; (6) желатин; (7) тальк; (8) эксципиенты, такие как масло какао и воски для суппозиториев;(9) масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; (10) гликоли, такие как пропиленгликоль;(11) полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; (12) сложные эфиры, такие как этилолеат и этиллаурат; (13) агар; (14) забуферивающие агенты, такие как гидроксид магния и гидроксид алюминия; (15) альгиновая кислота; (16) апирогенная вода; (17) изотонический раствор;(18) раствор Рингера; (19) этиловый спирт; (20) растворы фосфатного буфера и (21) другие нетоксичные совместимые вещества, применяемые в фармацевтических композициях. Кроме того, в композиции могут входить увлажнители, эмульгаторы и смазывающие вещества, такие как лаурилсульфат натрия и стеарат магния, а также красители, регуляторы высвобождения, покрывающие вещества, подсластители, вкусовые и ароматизирующие добавки, консерванты и антиоксиданты. Примеры фармацевтически приемлемых антиоксидантов включают: (1) растворимые в воде антиоксиданты, такие как аскорбиновая кислота, гидрохлорид цистеина, бисульфат натрия, метабисульфит натрия, сульфит натрия и тому подобные соединения; (2) растворимые в масле антиоксиданты, такие как аскорбилпальмитат, бутилгидроксианизол (ВНА), бутилгидрокситолуол (ВНТ), лецитин, пропилгаллат,альфа-токоферол и тому подобные соединения; (3) металл-хелатирующие агенты, такие как лимонная-8 020201 кислота, этилендиаминтетрауксусная кислота (EDTA), сорбит, винная кислота, фосфорная кислота и тому подобные соединения. Композиции, содержащие производные рифамицина, включают композиции, пригодные для перорального, назального, местного (включая трансбуккальное и сублингвальное), ректального, вагинального, аэрозольного и/или парентерального введения. Композиции могут быть удобным образом представлены в виде стандартных лекарственных форм и могут быть изготовлены любыми методами, общеизвестными в современной фармацевтике. Количество активного ингредиента, которое может быть объединено с материалом носителя для получения единичной лекарственной формы, будет варьировать в зависимости от реципиента, проходящего лечение, и конкретного пути введения. Количество активного ингредиента, которое может быть объединено с материалом носителя для получения единичной лекарственной формы, в общем случае будет таким количеством соединения, которое обеспечивает терапевтический эффект. Как правило, из 100% это количество будет меняться от примерно 1 до примерно 99% активного ингредиента, предпочтительно от примерно 5 до примерно 70%, наиболее предпочтительно от примерно 40 до примерно 70%. Способы изготовления этих композиций могут включать стадию объединения производных рифамицина, отдельно или в смеси с другими активными ингредиентами, с носителем и возможно с одним или более чем одним вспомогательным ингредиентом. В общем композиции изготавливают путем однородного и равномерного объединения производных рифамицина, отдельно или в смеси с другими активными ингредиентами, с жидкими носителями или тонкоизмельченными твердыми носителями или с теми и другими, и затем, если необходимо, формуя конечный продукт. Представленные здесь композиции, пригодные для перорального введения, могут быть в форме капсул, облаток, пилюль, таблеток, леденцов (с использованием корригированной основы, обычно сахарозы с акацией или трагакантом), порошков, гранул или в виде раствора или суспензии в водной или неводной жидкости, или в виде эмульсии "масло-в-воде" или "вода-в-масле", или в виде эликсира или сиропа, или в виде пастилок (с использованием инертной основы, такой как желатин и глицерин или сахароза и акация), и/или в виде полосканий для рта и тому подобных форм, каждая из которых содержит заранее установленное количество производных рифамицина формулы I отдельно или в смеси с другими активными ингредиентами. Соединение также может быть введено в форме болюса, электуария или пасты. Производное рифамицина может быть преимущественно использовано в производстве лекарственных препаратов, обладающих антибиотической активностью, предназначенных как для перорального,так и для местного применения. Лекарственные препараты для перорального применения вместе с обычными эксципиентами могут содержать, например, разбавители, такие как маннит, лактоза и сорбит; связывающие агенты, такие как крахмалы, желатины, сахара, производные целлюлозы, натуральные смолы и поливинилпирролидон; смазывающие агенты, такие как тальк, стеараты, гидрогенизированные растительные масла, полиэтиленгликоль и коллоидный диоксид кремния; разрыхлители, такие как крахмалы,целлюлозы, альгинаты, смолы и сетчатые полимеры; красители, корригенты и подсластители. Представленные здесь соединения включают твердые препараты, вводимые пероральным путем,например в виде таблеток с оболочкой или без оболочки, твердых и мягких желатиновых капсул, покрытых сахаром пилюль, леденцов, облаток, пеллет и порошков в запечатанных пакетах или другой упаковке. Лекарственные препараты для местного применения могут содержать производные рифамицина формулы I по отдельности, или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами вместе с обычными эксципиентами, такими как белый вазелин, белый воск, ланолин и его производные, стеариловый спирт, пропиленгликоль, лаурилсульфат натрия, простые эфиры жирных полиоксиэтиленовых спиртов, сложные эфиры жирных полиоксиэтиленовых кислот, моностеарат сорбитана, глицерилмоностеарат, моностеарат пропиленгликоля, полиэтиленгликоли, метилцеллюлоза, гидроксиметилпропилцеллюлоза, натрий-карбоксиметилцеллюлоза, коллоидный алюминий и силикат магния, альгинат натрия. Представленные здесь соединения могут быть изготовлены в виде различных препаратов, например местных препаратов, например мазей, помад, кремов, гелей и лосьонов. В представленных здесь твердых лекарственных формах для перорального введения (капсулы, таблетки, пилюли, драже, порошки, гранулы и тому подобные формы) активный ингредиент смешан с одним или более чем одним фармацевтически приемлемым носителем, таким как цитрат натрия или гидрофосфат кальция, и/или любым из следующего: (1) наполнители или добавки, такие как крахмалы, лактоза, сахароза, глюкоза, маннит и/или кремниевая кислота; (2) связывающие вещества, такие как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и/или акация;(3) влагоудерживающие вещества, такие как глицерин; (4) разрыхлители, такие как агар-агар, карбонат кальция, картофельный или тапиоковый крахмал, альгиновая кислота, определенные силикаты и карбонат натрия; (5) замедлители растворения, такие как парафин; (6) ускорители абсорбции, такие как четвертичные аммониевые соединения; (7) увлажнители, такие как, например, цетиловый спирт и моностеарат глицерина; (8) абсорбенты, такие как каолин и бентонитовая глина; (9) смазывающие вещества, такие-9 020201 как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси; и (10) красители. В случае капсул, таблеток и пилюль фармацевтические композиции могут также содержать буферные агенты. Твердые композиции подобного типа также можно применять в качестве наполнителей в мягких и твердых желатиновых капсулах, используя такие эксципиенты, как лактоза или молочные сахара, а также высокомолекулярные полиэтиленгликоли и тому подобные соединения. Таблетка может быть изготовлена прессованием или формованием, возможно с одним или более чем одним вспомогательным ингредиентом. Прессованные таблетки могут быть изготовлены с применением связывающего вещества (например, желатина или гидроксипропилметилцеллюлозы), смазывающего вещества, инертного разбавителя, консерванта, разрыхлителя (например, крахмалгликолята натрия или сшитой карбоксиметилцеллюлозы натрия), поверхностно-активного или диспергирующего агента. Формованные таблетки могут быть изготовлены формованием в соответствующей машине смеси порошкообразного активного ингредиента, увлажненного инертным жидким разбавителем. Таблетки и другие твердые лекарственные формы фармацевтических композиций, содержащих представленные здесь соединения, такие как драже, капсулы, пилюли и гранулы, возможно могут иметь насечки или могут быть изготовлены с покрытиями и оболочками, такими как кишечно-растворимые покрытия и другие покрытия, общеизвестные в современном фармацевтическом производстве. Они могут быть также составлены таким образом, чтобы обеспечивать замедленное или контролируемое высвобождение активного ингредиента, с применением для этого, например, гидроксипропилметилцеллюлозы в различных пропорциях для получения желательного профиля высвобождения, других полимерных матриц, липосом и/или микросфер. Они могут быть стерилизованы при помощи, например, фильтрации через фильтр, задерживающий бактерии, или введения стерилизующих агентов в форму стерильной твердой композиции, которая может быть растворена в стерильной воде или в некоторых других стерильных инъекционных средах непосредственно перед использованием. Эти композиции также возможно могут содержать замутнители и могут иметь такой состав, чтобы высвобождать активный(е) ингредиент(ы) только, или преимущественно, в определенной части желудочно-кишечного тракта, возможно, в замедленном режиме. Примеры инкапсулирующих композиций, которые могут быть использованы,включают полимерные вещества и воски. Если это целесообразно, активный ингредиент также может быть в микроинкапсулированной форме с одним или более чем одним эксципиентом, описанным выше. Жидкие лекарственные формы для перорального введения производных рифамицина формулы I по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами включают фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активному ингредиенту, жидкие лекарственные формы могут содержать инертные разбавители, обычно используемые в данной области, такие как, например, вода или другие растворители, солюбилизаторы и эмульгаторы, такие как этиловый спирт, изопропиловый спирт,этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, масла (в частности, хлопковое, арахисовое, кукурузное, оливковое, касторовое, кунжутное масло и масло ростков пшеницы), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли, сложные эфиры жирных кислот и сорбитана и смеси вышеуказанных соединений. В дополнение к инертному разбавителю, пероральные композиции могут содержать адъюванты, такие как увлажнители, эмульгаторы, суспендирующие агенты, подсластители, корригенты, красители,ароматизаторы и консерванты. Суспензии, в дополнение к активным производным рифамицина формулы I по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами,могут содержать суспендирующие агенты, такие как, например, этоксилированные изостеариловые спирты, сложные эфиры полиоксиэтиленсорбита и сорбитана, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар, трагакант и смеси вышеуказанных соединений. Представленные в этом документе фармацевтические композиции для ректального и вагинального введения могут представлять собой суппозитории, которые могут быть изготовлены смешиванием одного или более чем одного производного рифамицина по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами, с одним или более чем одним подходящим, нераздражающим эксципиентом или носителем, представляющим собой, например, масло какао, полиэтиленгликоль, воск для суппозиториев или салицилат, и который при комнатной температуре представляет собой твердое вещество, а при температуре тела становится жидким, и вследствие этого будет расплавляться в полости прямой кишки или влагалища и высвобождать активный агент. Представленные здесь композиции, пригодные для вагинального введения, также включают пессарии, тампоны, кремы, гели, пасты, пены или спреи, содержащие носители, которые общеизвестны в данной области как подходящие для этих лекарственных форм. Лекарственные формы производных рифамицина для местного или трансдермального введения включают порошки, спреи, мази, пасты, кремы, лосьоны, гели, растворы, пластыри и ингаляторы. Активные производные рифамицина могут быть смешаны в стерильных условиях с фармацевтически приемлемым носителем и с любыми консервантами, буферами или пропеллентами, которые могут быть необходимы.- 10020201 Мази, пасты, кремы и гели могут содержать, в дополнение к представленным здесь производным рифамицина, эксципиенты, такие как животные и растительные жиры, масла, воски, парафин, крахмал,трагакант, производные целлюлозы, полиэтиленгликоли, силиконы, бентониты, кремниевую кислоту,тальк и оксид цинка, или смеси вышеуказанных соединений. Порошки и спреи могут содержать, в дополнение к производным рифамицина по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами,эксципиенты, такие как лактоза, тальк, кремниевая кислота, гидроксид алюминия, силикат кальция и порошкообразный полиамид, или смеси этих веществ. Спреи могут дополнительно содержать обычные пропелленты, такие как хлорфторуглеводороды и летучие незамещенные углеводороды, такие как бутан и пропан. Альтернативно, производные рифамицина по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами могут быть введены в виде аэрозоля. Для этого изготавливают водные аэрозоли, липосомные препараты или твердые частицы, содержащие соединение. Может быть использована неводная суспензия (например, фторуглеродный пропеллент). Предпочтительны ультразвуковые небулайзеры, так как они минимизируют воздействие на агент усилия сдвига, которое может приводить к распаду соединения. Обычно водный аэрозоль изготавливают, объединяя водный раствор или суспензию агента с общепринятыми фармацевтически приемлемыми носителями и стабилизаторами. Носители и стабилизаторы варьируются в зависимости от требований конкретного соединения, но обычно включают неионогенные поверхностно-активные вещества (твины, плюроники или полиэтиленгликоль), безвредные белки, подобные сывороточному альбумину, эфиры сорбитана, олеиновую кислоту, лецитин, аминокислоты, такие как глицин, буферы, соли, сахара или сахарные спирты. Аэрозоли, как правило, изготавливают из изотонических растворов. Трансдермальные пластыри имеют дополнительные преимущества в обеспечении контролируемой доставки в организм производных рифамицина по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами. Такие лекарственные формы могут быть изготовлены растворением или диспергированием агента в подходящей среде. Также могут быть использованы усилители абсорбции для увеличения потока активного ингредиента через кожу. Скорость такого потока можно контролировать либо с помощью регулирующей скорость мембраны, либо за счет диспергирования активного ингредиента в полимерной матрице или геле. Предполагается, что офтальмологические препараты, глазные мази, порошки, растворы и тому подобные формы, также входят в объем представленного здесь изобретения. Представленные здесь фармацевтические композиции, пригодные для парентерального введения,содержат одно или более чем одно производное рифамицина по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами, в комбинации с одним или более чем одним фармацевтически приемлемым стерильным изотоническим водным или неводным раствором, дисперсией, суспензией или эмульсией, или стерильным порошком, который может быть восстановлен до стерильного инъекционного раствора или дисперсии непосредственно перед применением, возможно содержащим антиокислители, буферы, бактериостатики, растворенные вещества, делающие препарат изотоничным крови предполагаемого реципиента, суспендирующие агенты или загустители. Примеры подходящих водных и неводных носителей, которые могут быть использованы в представленных здесь фармацевтических композициях, включают воду, этанол, полиолы (такие как глицерин,пропиленгликоль, полиэтиленгликоль и тому подобные соединения) и их подходящие смеси, растительные масла, такие как оливковое масло, и инъекционные органические эфиры, такие как этилолеат. Подходящая текучесть может быть обеспечена, например, при помощи покрывающих веществ, таких как лецитин, поддержанием необходимого размера частиц в случае дисперсий и за счет применения поверхностно-активных веществ. Эти композиции также могут содержать адъюванты, такие как консерванты, увлажнители, эмульгаторы и диспергирующие агенты. Предотвращение действия микроорганизмов может быть обеспечено за счет включения различных антибактериальных и противогрибковых средств, например парабена, хлорбутанола, фенола, сорбиновой кислоты и тому подобных соединений. Также может быть желательным включение в композиции изотонических агентов, таких как сахара, хлорид натрия и тому подобные соединения. Кроме того, пролонгированная абсорбция инъекционной фармацевтической формы может быть достигнута за счет включения агентов, которые замедляют абсорбцию, таких как моностеарат алюминия и желатин. В некоторых случаях для увеличения продолжительности действия лекарственного средства желательно замедлить абсорбцию лекарственного средства после подкожного или внутримышечного введения. Инъекционные формы депо изготавливают путем формирования матриц микроинкапсулированных производных рифамицина по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами, в биоразрушаемых полимерах, таких как сополимер полилактид-полигликолид. Скорость высвобождения лекарственного средства можно контролировать с по- 11020201 мощью соотношения лекарственного средства и полимера и природы конкретного применяемого полимера. Примеры других биоразрушаемых полимеров включают поли(ортоэфиры) и поли(ангидриды). Инъекционные депо-препараты также изготавливают, заключая лекарственное средство в липосомы или микроэмульсии, совместимые с тканями организма. При введении производных рифамицина формулы I по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами, в качестве лекарственных препаратов людям и животным они могут применяться в чистом виде или в виде фармацевтической композиции, содержащей, например, 0,1-99,5% (более предпочтительно 0,5-90%) активного ингредиента в комбинации с фармацевтически приемлемым носителем. Независимо от выбранного способа введения, производные рифамицина формулы I по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами, которые могут применяться в подходящей гидратированной форме, и/или представленные здесь фармацевтические композиции изготавливают в виде фармацевтически приемлемых лекарственных форм общепринятыми способами, которые известны специалистам. Фактические уровни дозировки и режим введения активных ингредиентов для представленных здесь фармацевтических композиций могут варьироваться таким образом, чтобы получить количество активного ингредиента, которое эффективно для достижения желаемой терапевтической реакции для данного пациента, композиции и способа введения, но не является токсичным для пациента. Типичная доза находится в пределах от 1 до 3000 мг/день. Предпочтительная доза представленных здесь производных рифамицина формулы I представляет собой максимальную дозу, которую пациент может перенести без развития серьезных побочных эффектов. В одном воплощении представленные здесь производные рифамицина вводят в концентрации от примерно 1 до примерно 200 мг/кг массы тела, от примерно 10 до примерно 100 мг/кг массы тела или от примерно 40 до примерно 80 мг/кг массы тела. Промежуточные по отношению к вышеперечисленным значениям диапазоны также входят в объем изобретения. При комбинированном терапевтическом лечении как представленные здесь соединения, так и другое лекарственное(ые) средство(а) вводят млекопитающим (например, людям мужского или женского пола) общепринятыми способами. Агенты могут быть введены в виде единой лекарственной формы или в виде раздельных лекарственных форм. Эффективные количества других терапевтических агентов общеизвестны специалистам в данной области. Однако определение оптимального эффективного диапазона доз другого(их) терапевтического(их) агента(ов) находится в пределах компетенции практикующего специалиста. В одном представленном здесь воплощении, в котором другой терапевтический агент вводят животному, эффективное количество представленного здесь соединения меньше, чем его эффективное количество в случае, когда другой терапевтический агент не вводят. В другом воплощении эффективное количество традиционного агента меньше, чем его эффективное количество в случае, когда не вводят представленное здесь соединение. Таким образом, могут быть минимизированы нежелательные побочные эффекты, ассоциированные с высокими дозами любого агента. Другие возможные преимущества (включая улучшенный режим введения и/или снижение стоимости лекарственного средства, но не ограничиваясь ими) очевидны специалистам в данной области. В различных воплощениях лекарственные средства (например, профилактические или терапевтические агенты) вводят с интервалом меньше чем 5 мин, меньше чем 30 мин, 1 ч, примерно 1 ч, от примерно 1 до примерно 2 ч, от примерно 2 до примерно 3 ч, от примерно 3 до примерно 4 ч, от примерно 4 до примерно 5 ч, от примерно 5 до примерно 6 ч, от примерно 6 до примерно 7 ч, от примерно 7 до примерно 8 ч, от примерно 8 до примерно 9 ч, от примерно 9 до примерно 10 ч, от примерно 10 до примерно 11 ч, от примерно 11 до примерно 12 ч, от примерно 12 до 18 ч, от 18 до 24 ч, от 24 до 36 ч, от 36 до 48 ч, от 48 до 52 ч, от 52 до 60 ч, от 60 до 72 ч, от 72 до 84 ч, от 84 до 96 ч или от 96 до 120 ч. В предпочтительном воплощении два или более чем два средства вводят в течение одного и того же визита пациента. В определенных воплощениях одно или более чем одно представленное здесь соединение и одно или более чем одно другое лекарственное средство (например, профилактические или терапевтические агенты) вводят циклически. Циклическая терапия включает введение в течение периода времени первого средства (например, первого профилактического или терапевтического агента) с последующим введением в течение периода времени второго средства (например, второго профилактического или терапевтического средства), за которым возможно следует введение в течение периода времени третьего средства(например, профилактического или терапевтического агента) и так далее и затем повторение этого последовательного введения, т.е. цикл, предназначенный для замедления развития резистентности к одному из средств, предотвращения или снижения побочных эффектов одного из средств и/или повышения эффективности средств. В определенных воплощениях введение одного и того же представленного здесь соединения может быть повторено и интервал между введениями может составлять по меньшей мере 1, 2, 3, 5, 10, 15, 30, 45 дней, 2 месяца, 75 дней, 3 месяца или по меньшей мере 6 месяцев. В других воплощениях введение одного и того же лекарственного средства (например, профилактического или терапевтического агента), от- 12020201 личающегося от производных рифамицина, может быть повторено, и интервал между введениями может составлять по меньшей мере 1, 2, 3, 5, 10, 15, 30, 45 дней, 2 месяца, 75 дней, 3 месяца или по меньшей мере 6 месяцев. Определенные показания могут потребовать более продолжительного лечения. Например, лечение диареи путешественников может продолжаться всего от 12 до примерно 72 ч, тогда как лечение болезни Крона может занять от примерно 1 дня до примерно 3 месяцев. В данном документе также предложены наборы, например наборы для лечения у субъекта расстройства пищеварительного тракта. Наборы могут содержать, например, одно или более чем одно производное рифамицина по отдельности или в их смеси, или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами и инструкцию по применению. Инструкции по применению могут содержать указания по применению препарата, информацию о дозировке, правила хранения и тому подобную информацию. Также предложены упакованные композиции, которые могут содержать терапевтически эффективное количество одного или более чем одного производного рифамицина по отдельности или в их смеси,или в смеси с соединениями формулы II, или в смеси с другими активными ингредиентами, и фармацевтически приемлемый носитель или разбавитель, где композиция составлена для лечения субъекта, страдающего или восприимчивого к расстройству пищеварительного тракта, и упакована вместе с инструкцией по лечению субъекта, страдающего или восприимчивого к расстройству пищеварительного тракта. Пример 1. Синтез(12'Z,14'Е,24'Е)-5',17',19'-тригидрокси-12'-(гидроксиметил)-23'-метокси-2',4',16',18',20',22'гексаметил-1',4,6',11'-тетраоксо-1',2'-дигидро-6'Н-спиро[1,3-диксолан-2,9'-[2,7]-(эпоксипентадека[1,11,13]триенимино)нафто[2,1-b]фуран]-21'-илацетата. Этот пример предлагает один из способов получения соединения формулы II, где R представляет собой ацетил; R1 представляет собой водород; R2 представляет собой параметил и R3 представляет собой гидроксиметил. Культуру Nocardia mediterranea (ATCC 31064) выращивали в течение 6-8 дней на агаре Беннета и инкубировали при 28C. В стерильных условиях две колбы Эрленмейера объемом 500 мл инокулировали культурой, полученной на скошенном агаре. Колбы содержали 100 мл ростовой среды, состав которой описан в табл. 1. Таблица 1 Величину рН доводили до 7,3 с помощью 1 М NaOH. Инокулированные таким образом колбы помещали на орбитальную качалку на 72 ч при 28C. Содержимое двух колб Эрленмейра использовали как инокулюм, сливая их в 10-литровый предварительный ферментатор, содержащий 4 л вышеупомянутой роствой среды. Инкубацию проводили при 28C, перемешивании со скоростью 300 об/мин и аэрации 1 об./об./мин. После 48 ч выращивания получали объем 7-10% осажденных клеток. На следующей стадии клетки использовали как инокулюм в 10-литровом стеклянном ферментаторе, содержащем 4 л среды, состав которой описан в табл. 2. Величину рН доводили до 7,8 с помощью NaOH и стерилизовали в течение 60 мин при 120C. После стерилизации рН составлял 6,4. В качестве инокулюма использовали содержимое предварительного ферментатора в количестве, равном 5% содержимого ферментатора. Ферментацию проводили при 28C,перемешивании со скоростью 750 об/мин и аэрации с интенсивностью 1 об./об/мин. В качестве пеногасителя использовали силикон А. В ходе ферментации культуральный бульон приобретал характерный красно-коричневый цвет. Объем осажденных клеток получали после 200 ч выращивания. рН культурального бульона составлял 7,5, и затем культуральный бульон собирали для отделения клеток. Мицелий удаляли фильтрованием и отбрасывали. рН фильтрата доводили до 2,0 с помощью 10%(об./об.) соляной кислоты и экстрагировали три раза равным объемом этилацетата. Объединенные экстракты концентрировали досуха под вакуумом при 35C и остаток растворяли в 0,005 М натрийфосфатном буфере с рН 7,5. Добавляли нитрит натрия до получения конечной концентрации 0,2%(мас./об.). После перемешивания в течение 30 мин при комнатной температуре буферный раствор экстрагировали три раза равным объемом этилацетата. Объединенные органические экстракты концентрировали досуха под вакуумом при 35C. Экстракт очищали колоночной хроматографией на силикагеле в условиях изократического элюирования смесью растворителей дихлорметан/метанол в соотношении 40:1(об./об.) с линейной скоростью 2,65 см/мин и емкостью загрузки 1 г смеси для разделения в 13 мм стационарной фазы. Полученное соединение анализировали с помощью ВЭЖХ, используя колонку Hypersil ODS длиной 250 мм и диаметром 4,4 мм, элюированную в изократических условиях системой ацетонитрил/0,025 М натрий-дигидрофосфатный буфер (рН 7,0) в соотношении 1:1 (об./об.) при скорости потока 1 мл/мин. Собирали хроматографическую фракцию чистотой выше 90% и растворитель концентрировали досуха под вакуумом. На фиг. 1 показан хроматографический профиль соединения формулы II, гдеR представляет собой ацетил; R1 представляет собой водород; R2 представляет собой п-метил и R3 представляет собой гидроксиметил, характеризующегося временем удерживания (RT) 7,45 мин. Соединение идентифицировали с помощью 1 Н ЯМР, спектр показан на фиг. 2. Пример 2. Синтез(16Z,18 Е,28 Е)-25-(ацетилокси)-5,21,23-тригидрокси-16-(гидроксиметил)-27-метокси 2,4,11,20,22,24,26-гептаметил-1,15-диоксо-1,13-дигидро-2 Н-2,7-(эпоксипентадека[1,11,13]триенимино)фуро[2",3":7',8']нафто[1',2':4,5]имидазо[1,2-а]пиридин-8-ий-6-олята Это соединение представляет собой соединение формулы I, где R представляет собой ацетил;R1 представляет собой водород; R2 представляет собой п-метил и R3 представляет собой гидроксиметил. К раствору 200 мг (12'Z,14'Е,24'Е)-5',17',19'-тригидрокси-12'-(гидроксиметил)-23'-метокси 2',4',16',18',20',22'-гексаметил-1',4,6',11'-тетраоксо-1',2'-дигидро-6'Н-спиро[1,3-диксолан-2,9'-[2,7](эпоксипента-дека[1,11,13]триенимино)нафто[2,1-b]фуран]-21'-илацетата, полученного, как описано в примере 1, в 0,6 мл дистиллированной воды и 0,5 мл этанола добавляли при перемешивании при комнатной температуре 82 мг 2-амино-4-метилпиридина. Реакционную смесь выдерживали при 47C в течение примерно 5 ч до полного исчезновения реагента формулы II по результатам ВЭЖХ анализа, который выполняли так же, как описано в примере 1. Раствор приводили к температуре окружающей среды и добавляли 5 мг аскорбиновой кислоты. Раствор подкисляли концентрированной HCl до рН 2,0 и после это- 14020201 го экстрагировали двумя аликвотами по примерно 1,0 мл этилацетата. Объединенные органические фазы сушили над сульфатом натрия, фильтровали и выпаривали досуха. Полученное соединение, проанализированное с помощью ВЭЖХ при таких же условиях, как и в примере 1, характеризуется временем удерживания 6,2 мин. с чистотой, соответствующей 95%, хроматограмма показана на фиг. 3. Полученное соединение идентифицировали с помощью ИК-СФ (инфракрасная спектроскопия с преобразованием Фурье), 1 Н ЯМР и 13 С ЯМР спектроскопии, молекулярную массу определяли с помощью МС-ИЭУ спектроскопии. ИК-спектр. Характеристические полосы поглощения, полученные на пленке NaCl, наблюдали на следующих частотах (см-1): 3400, 2972, 2929.6, 1717.7, 1654.3, 1690.0, 1543.6, 1508.5, 1475.7, 1454.5,1373.8, 1322.9, 1233.4, 1157.3, 1106.4, 1059.7, 1021.5, 974.8, 949.3, 877.2, 800.8, 732.8. Спектр показан на фиг. 4, и данные согласуются с предложенной структурой. 1 Н ЯМР спектр. Наблюдали следующие характеристические резонансные пики (выраженные как м.д.): 0.34 (d, 3H), 0.76 (d, 3H), 0.97 (d, 3H), 1.27 (m, 1H) 1.44 (m, 1H), 1.63 (m, 1H), 1.89 (s, 3H), 1.99 (s,3H), 2.09 (s, 3H), 2.32 (m, 1H), 2.59 (s, 3H), 2.91 (m, 1H), 3.02 (s, 3H), 3.37 (d, 1H), 3.73 (m, 2H), 3.95 (m,2H), 4.50 (d, 1H), 4.63 (d, 1H), 4.95 (d, 1H), 5.01 (d, 1H), 6.06 (d, 1H), 6.18 (d, 1H), 6.49 (d, 1H), 6.92 (d, 1H),7.05 (d, 1H), 7.39 (s, 1H), 8.53 (d, 1H), 9.13 (s, 1H), 14.73 (s, 1H), 16.89 (s, 1H), где s = синглет, d = дублет,m = мультиплет. Спектр показан на фиг. 5, и данные согласуются с предложенной структурой. 13 С ЯМР спектр. Наблюдали следующие характеристические резонансные пики (выраженные как м.д.): 7.14, 7.47, 8.75, 10.90, 17.25, 20.79, 22.33, 32.81, 36.87, 38.14, 38.35, 57.24, 65.13, 72.35, 74.31, 77.16,77.62, 97.51, 103.98, 104.53, 108.43, 109.58, 111.77, 114.29, 114.29, 114.37, 117.74, 119.09, 122.77, 125.39,129,26, 139,09, 139.28, 141.15, 144.54, 147.93, 153.59, 169.05, 172.08, 172.14, 181.82, 189.19. Спектр показан на фиг. 6, и данные согласуются с предложенной структурой. МС-ИЭУ. Молекулярную массу определяли с настроечными параметрами ESI+ и ESI- с напряжением на капилляре 3 кВ, на конусе 25 В и на экстракторе 3 кВ. Спектр показан на фиг. 7, и полученное соединение имело молекулярную массу, соответствующую значению 801. Пример 3. Минимальная концентрация активного вещества, способная ингибировать рост патогенных бактерий in vitro. Минимальную концентрацию активного вещества, способную ингибировать рост патогенных бактерий in vitro (МИК), определяли способом микроразведений, как описано Национальным комитетом для клинических лабораторный стандартов (National Committee for Clinical laboratory Standards NCCLS,2003), а в качестве контрольного стандарта были включены Е.coli (АТСС 25922), P.aeruginosa (АТСС 27853), S.aureus (АТСС 29213), Е.faecalis (АТСС 29212). В табл. 3 представлены результаты определения минимальных концентраций ингибирования ростаin vitro различных штаммов грамотрицательных бактерий. В табл. 4 представлены результаты определения минимальных концентраций ингибирования роста
МПК / Метки
МПК: C07D 493/20, C07D 498/22, A61P 31/00, A61K 31/437, A61K 31/357
Метки: производные, рифамицина
Код ссылки
<a href="https://eas.patents.su/30-20201-proizvodnye-rifamicina.html" rel="bookmark" title="База патентов Евразийского Союза">Производные рифамицина</a>












