Лактамные соединения и их применение в качестве фармацевтических препаратов
Номер патента: 19747
Опубликовано: 30.06.2014
Авторы: Яо Вэньцин, Меткаф Брайан В., Чжо Цзиньцун, Бернс Дэвид, Цянь Дин-Цюань, Сюй Мэйчжун, Хэ Чуньхун, Чжан Колин
Формула / Реферат
1. Соединение формулы I
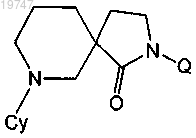
или его фармацевтически приемлемая соль, где
Су представляет собой арил или гетероарил, каждый необязательно замещенный 1, 2, 3, 4 или 5 -W-X-Y-Z;
-W-X-Y-Z, каждый независимо, представляют собой атом галогена, CN, NO2, С1-4алкокси, гетероарилокси, C2-6алкинил, C1-4галогеналкокси, NRcC(O)Rd, NRcC(O)ORa, C(O)NRcRd, NRcRd, NReS(O)2Rb,
C1-4галогеналкил, C1-6алкил, гетероциклоалкил, арил или гетероарил, где каждый упомянутый C1-6алкил, арил или гетероарил необязательно замещен 1, 2 или 3 атомами галогена, C1-6алкилом, C1-4галогеналкилом, CN, NO2, ORa, SRa, C(O)NRcRd, NRcC(O)Rd или COORa;
Q представляет собой циклогексил, замещенный в 4-м положении по меньшей мере одним -W'-X'-Y'-Z';
-W'-X'-Y'-Z', каждый независимо, представляют собой ОН, C1-4алкокси, CN, C1-4алкил, -О-гетероарил, -(C1-4алкил)-CN, COORa, C(O)NRcRd или NRcC(O)ORa;
Ra представляет собой атом водорода, C1-6алкил, C1-6галогеналкил, C2-6алкенил, C2-6алкинил, арил, циклоалкил, гетероарил или гетероциклоалкил, где упомянутые C1-6алкил, C1-6галогеналкил, С2-6алкенил, С2-6алкинил, арил, циклоалкил, гетероарил или гетероциклоалкил необязательно замещены атомом водорода, ОН, амино, атомом галогена, C1-6алкилом, C1-6галогеналкилом, арилом, арилалкилом, гетероарилом, гетероарилалкилом, циклоалкилом или гетероциклоалкилом;
Rb представляет собой атом водорода, С1-6алкил, C1-6галогеналкил, C2-6алкенил, С2-6алкинил, арил, циклоалкил, гетероарил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил, где упомянутые C1-6алкил, C1-6галогеналкил, С2-6алкенил, С2-6алкинил, арил, циклоалкил, гетероарил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил необязательно замещены атомом водорода, ОН, амино, атомом галогена, C1-6алкилом, C1-6галогеналкилом, арилом, арилалкилом, гетероарилом, гетероарилалкилом, циклоалкилом или гетероциклоалкилом;
Rc и Rd, каждый независимо, представляют собой атом водорода, C1-10алкил, C1-6галогеналкил, C2-6алкенил, C2-6алкинил, арил, гетероарил, циклоалкил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил, где упомянутые C1-10алкил, C1-6галогеналкил, С2-6алкенил, С2-6алкинил, арил, гетероарил, циклоалкил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил необязательно замещены атомом водорода, ОН, амино, атомом галогена, C1-6алкилом, C1-6галогеналкилом, арилом, арилалкилом, гетероарилом, гетероарилалкилом, циклоалкилом или гетероциклоалкилом; или
Rc и Rd совместно с атомом азота, к которому они присоединены, образуют 4-, 5-, 6- или 7-звенную гетероциклоалкильную группу;
Re представляет собой атом водорода, C1-10алкил, C1-6галогеналкил, C2-6алкенил, C2-6алкинил, арил, гетероарил, циклоалкил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил, где упомянутые C1-10алкил, C1-6галогеналкил, С2-6алкенил, С2-6алкинил, арил, гетероарил, циклоалкил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил необязательно замещены атомом водорода, ОН, амино, атомом галогена, C1-6алкилом, C1-6галогеналкилом, арилом, арилалкилом, гетероарилом, гетероарилалкилом, циклоалкилом или гетероциклоалкилом;
где каждый арил выбирают из фенила и нафтила;
каждый циклоалкил выбирают из группы, состоящей из циклопропила, циклобутила, циклопентила, циклогексила, циклогептила, циклопентенила, циклогексенила, циклогексадиенила, циклогептатриенила, норборнила, норпинила, норкарнила и адамантила;
каждый гетероарил выбирают из группы, состоящей из пиридила, пиримидинила, пиразинила, пиридазинила, триазинила, фурила, хинолила, изохинолила, тиенила, имидазолила, тиазолила, индолила, пиррила, оксазолила, бензофурила, бензотиенила, бензтиазолила, изоксазолила, пиразолила, триазолила, тетразолила, индазолила, 1,2,4-тиадиазолила, изотиазолила, бензотиенила, пуринила, карбазолила, бензимидазолила, индолинила, хиназолинила, пирроло[2,3-d]пиримидинила и 1,3-бензотиазолила;
каждый гетероциклоалкил выбирают из группы, состоящей из морфолино, тиоморфолино, пиперазинила, тетрагидрофуранила, тетрагидротиенила, 2,3-дигидробензофурила, 1,3-бензодиоксола, бензо-1,4-диоксана, пиперидинила, пирролидинила, изоксазолидинила, изотиазолидинила, пиразолидинила, оксазолидинила, тиазолидинила, имидазолидинила, 1,2,3,6-тетрагидропиридинила, 2-оксо-(2Н)-пиридинила, 2-оксо[1,3]оксазолидинила, 2-оксопирролидинила, 2-оксопиперидинила и 2-оксо[1,3]оксазинанила;
каждый арилалкил представляет собой C1-6алкил, замещенный арилом;
каждый гетероарилалкил представляет собой C1-6алкил, замещенный гетероарилом.
2. Соединение по п.1 или его фармацевтически приемлемая соль, в котором Су представляет собой фенил, нафтил, пиридил, пиримидинил, триазинил, фуранил, тиазолил, пиразинил, пуринил, хиназолинил, хинолинил, изохинолинил, пирроло[2,3-d]пиримидинил или 1,3-бензотиазолил, каждый необязательно замещенный 1, 2, 3, 4 или 5 -W-X-Y-Z.
3. Соединение по п.1 или его фармацевтически приемлемая соль, в котором Су представляет собой фенил, нафтил, пиридил, пиримидинил, триазинил, фуранил или тиенил, каждый необязательно замещенный 1, 2, 3, 4 или 5 -W-X-Y-Z.
4. Соединение по п.1 или его фармацевтически приемлемая соль, в котором Су представляет собой фенил, нафтил, пиридил, пиримидинил, триазинил, фуранил, тиазолил, пиразинил, пуринил, хиназолинил, хинолинил, изохинолинил, пирроло[2,3-d]пиримидинил или 1,3-бензотиазолил, каждый необязательно замещенный 1, 2, 3 или 4 атомами галогена, CN, NO2, C1-4алкокси, гетероарилокси, С2-6алкинил, C1-4галогеналкокси, NRcC(O)Rd, NRcC(O)ORa, C(O)NRcRd, NRcRd, NReS(O)2Rb, C1-4галогеналкил, C1-6алкил, гетероциклоалкил, арил или гетероарил, где каждый из упомянутых C1-6алкила, арила или гетероарила необязательно замещен 1, 2 или 3 атомами галогена, C1-6алкилом, C1-4галогеналкилом, CN, NO2, ORa, SRa, C(O)NRcRd, NRcC(O)Rd или COORa.
5. Соединение по п.1 или его фармацевтически приемлемая соль, в котором Су представляет собой фенил, нафтил, пиридил, пиримидинил, триазинил, фуранил, тиенил, тиазолил, пиразинил, пуринил, хиназолинил, хинолинил, изохинолинил, пирроло[2,3-d]пиримидинил или 1,3-бензотиазолил, каждый необязательно замещенный 1, 2, 3 или 4 заместителями, независимо выбранными из атома галогена, CN, NO2, C1-4алкокси, пиридин-2-илокси, пиридин-3-илокси, пиридин-4-илокси, С2-6алкинила, C1-4галогеналкокси, NRcC(O)Rd, NRcC(O)ORa, C(O)NRcRd, NRcRd, NReS(O)2Rb, C1-4галогеналкила, C1-6алкила, фенила, пиридила, пиримидинила, изоксазолила, пиразолила, 1,2,3,6-тетрагидропиридинила, 2-оксо-(2Н)-пиридинила, 2-оксо[1,3]оксазолидинила, 2-оксопирролидинила, пирролидинила, 2-оксопиперидинила и 2-оксо[1,3]оксазинанила; где каждый из упомянутых C1-6алкила, фенила, пиридила, пиримидинила, изоксазолила, пиразолила, 1,2,3,6-тетрагидропиридинила, 2-оксо-(2Н)-пиридинила, 2-оксо[1,3]оксазолидинила, 2-оксопирролидинила, пирролидила, 2-оксопиперидинила или 2-оксо[1,3]оксазинанила необязательно замещен 1, 2 или 3 атомами галогена, C1-6алкилом, C1-4галогеналкилом, CN, NO2, ORa, SRa, C(O)NRcRd, NRcC(O)Rd или COORa.
6. Соединение по п.1 или его фармацевтически приемлемая соль, в котором Су представляет собой фенил, нафтил, пиридил, пиримидинил, триазинил, фуранил или тиенил, каждый необязательно замещенный 1, 2 или 3 атомами галогена, CN, C1-4алкокси, C1-4галогеналкокси, C1-6алкилом или арилом, где упомянутый C1-6алкил или арил необязательно замещен 1, 2 или 3 атомами галогена, C1-6алкилом, C1-4галогеналкилом, CN, NO2, ORa или SRa.
7. Соединение по п.1 или его фармацевтически приемлемая соль, в котором Су представляет собой фенил, нафтил, пиридил, пиримидинил, триазинил, фуранил или тиенил, каждый необязательно замещенный 1, 2 или 3 атомами галогена, CN, C1-4алкокси, C1-4галогеналкокси, С1-6алкилом или арилом, где упомянутый C1-6алкил или арил необязательно замещен 1, 2 или 3 атомами галогена или C1-6алкилом.
8. Соединение по п.1 или его фармацевтически приемлемая соль, в котором Су представляет собой фенил, пиридил, пиримидинил, хинолинил или изохинолинил, каждый необязательно замещенный 1, 2, 3, 4 или 5
-W-X-Y-Z.
9. Соединение по п.1, в котором Су представляет собой фенил, пиридил, пиримидинил, хинолинил или изохинолинил, каждый необязательно замещенный 1, 2 или 3 атомами галогена, CN, C1-6алкилом, C1-4галогеналкилом, C1-4алкокси, NRcC(O)ORa или C(O)NRcRd.
10. Соединение, выбранное из
7-(4-фторфенил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она;
7-(3-фторфенил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-фенил-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-[5-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]декан-1-она;
6-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]никотинонитрила;
2-(транс-4-гидроксициклогексил)-7-(6-метоксипиридин-2-ил)-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-(6-метилпиридин-2-ил)-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-(5-метилпиридин-2-ил)-2,7-диазаспиро[4.5]декан-1-она;
7-(5-фторпиридин-2-ил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-[6-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]декан-1-она;
(5S)-2-(транс-4-гидроксициклогексил)-7-[5-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]декан-1-она;
(5R)-2-(транс-4-гидроксициклогексил)-7-[5-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]декан-1-она;
7-(6-фторпиридин-2-ил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-(3-метилпиридин-2-ил)-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-(4-метоксипиридин-2-ил)-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-пиридин-2-ил-2,7-диазаспиро[4.5]декан-1-она;
7-[3-хлор-5-(трифторметил)пиридин-2-ил]-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она;
4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]бензонитрила;
2-(транс-4-гидроксициклогексил)-7-[4-(трифторметил)фенил]-2,7-диазаспиро[4.5]декан-1-она;
3-фтор-4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]бензонитрила;
изопропил {4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]фенил}карбамата;
проп-2-ин-1-ил {4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]фенил}карбамата;
метил {4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]фенил}карбамата;
N-{4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]фенил}ацетамида;
N-{4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]фенил}циклопропанкарбоксамида;
изопропил {3-фтор-4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]фенил}карбамата;
проп-2-ин-1-ил {3-фтор-4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]фенил}карбамата;
метил {3-фтор-4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]фенил}карбамата;
N-{3-фтор-4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]фенил}циклопропанкарбоксамида;
7-(4-хлорпиримидин-2-ил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-[4-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-[6-метил-4-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]декан-1-она;
метил 6-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]никотината;
2-(транс-4-гидроксициклогексил)-7-изохинолин-1-ил-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-хинолин-2-ил-2,7-диазаспиро[4.5]декан-1-она;
N-{3-фтор-4-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]фенил}ацетамида;
4-{1-оксо-7-[5-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]дек-2-ил}циклогексанкарбонитрила;
4-{1-оксо-7-[4-(трифторметил)фенил]-2,7-диазаспиро[4.5]дек-2-ил}циклогексанкарбонитрила;
4-{7-[3-хлор-5-(трифторметил)пиридин-2-ил]-1-оксо-2,7-диазаспиро[4.5]дек-2-ил}циклогексанкарбонитрила;
4-[7-(3,5-дихлорпиридин-2-ил)-1-оксо-2,7-диазаспиро[4.5]дек-2-ил]циклогексанкарбонитрила;
4-[7-(6-фторпиридин-2-ил)-1-оксо-2,7-диазаспиро[4.5]дек-2-ил]циклогексанкарбонитрила;
(транс-4-{1-оксо-7-[5-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]дек-2-ил}циклогексил)ацетонитрила;
(транс-4-{1-оксо-7-[4-(трифторметил)фенил]-2,7-диазаспиро[4.5]дек-2-ил}циклогексил)ацетонитрила;
(транс-4-{7-[3-хлор-5-(трифторметил)пиридин-2-ил]-1-оксо-2,7-диазаспиро[4.5]дек-2-ил}циклогексил)ацетонитрила;
{транс-4-[7-(3,5-дихлорпиридин-2-ил)-1-оксо-2,7-диазаспиро[4.5]дек-2-ил]циклогексил}ацетонитрила;
{транс-4-[7-(6-фторпиридин-2-ил)-1-оксо-2,7-диазаспиро[4.5]дек-2-ил]циклогексил}ацетонитрила;
7-(2-фтор-4-нитрофенил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она;
2-(транс-4-гидроксициклогексил)-7-[6-метил-4-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]декан-1-она;
7-(5-этилпиримидин-2-ил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она;
7-(2-хлорпиримидин-4-ил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она;
6-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]-N,N-диметилникотинамида;
или его фармацевтически приемлемая соль.
11. Фармацевтическая композиция для модулирования активности 11βHSD1 или MR, включающая в себя соединение по любому из пп.1-10 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
12. Способ лечения болезни у пациента, в котором упомянутая болезнь представляет собой ожирение, диабет, нарушение толерантности к глюкозе, резистентность к инсулину, гипергликемию, гипертонию, гиперлипемию, расстройство познавательной функции, депрессию, деменцию, глаукому, сердечно-сосудистые расстройства, остеопороз, воспаление, сердечно-сосудистое, почечное или воспалительное заболевание, сердечную недостаточность, атеросклероз, артериосклероз, коронарную недостаточность, тромбоз, ангину, болезнь периферических сосудов, повреждение сосудистой стенки, инсульт, дислипидемию, гиперлипопротеинемию, диабетическую дислипидемию, смешанную дислипидемию, гиперхолестеринемию, гипертриглицеридемию, метаболический синдром или общее альдостероновое повреждение органа-мишени, включающий введение соединений по пп.1-10.
13. Способ лечения у пациента диабета типа 2, содержащий введение указанному пациенту терапевтически эффективного количества соединения по любому из пп.1-10 или его фармацевтически приемлемую соль.
14. Применение соединения по любому из пп.1-10 или его фармацевтически приемлемой соли для производства лекарственного средства для лечения ожирения, диабета, нарушения толерантности к глюкозе, резистентности к инсулину, гипергликемии, гипертонии, гиперлипемии, расстройства познавательной функции, депрессии, деменции, глаукомы, сердечно-сосудистых расстройств, остеопороза, воспаления, сердечно-сосудистого, почечного или воспалительного заболевания, сердечной недостаточности, атеросклероза, артериосклероза, коронарной недостаточности, тромбоза, ангины, болезни периферических сосудов, повреждения сосудистой стенки, инсульта, дислипидемии, гиперлипопротеинемии, диабетической дислипидемии, смешанной дислипидемии, гиперхолестеринемии, гипертриглицеридемии, метаболического синдрома или общего альдостеронового повреждения органа-мишени.
15. Применение соединения по любому из пп.1-10 или его фармацевтически приемлемой соли для производства лекарственного средства для лечения диабета типа 2.
16. Применение соединения по любому из пп.1-10 или его фармацевтически приемлемой соли для лечения ожирения, диабета, нарушения толерантности к глюкозе, резистентности к инсулину, гипергликемии, гипертонии, гиперлипемии, расстройства познавательной функции, депрессии, деменции, глаукомы, сердечно-сосудистых расстройств, остеопороза, воспаления, сердечно-сосудистого, почечного или воспалительного заболевания, сердечной недостаточности, атеросклероза, артериосклероза, коронарной недостаточности, тромбоза, ангины, болезни периферических сосудов, повреждения сосудистой стенки, инсульта, дислипидемии, гиперлипопротеинемии, диабетической дислипидемии, смешанной дислипидемии, гиперхолестеринемии, гипертриглицеридемии, метаболического синдрома или общего альдостеронового повреждения органа-мишени.
17. Применение соединения по любому из пп.1-10 или его фармацевтически приемлемой соли для лечения диабета типа 2.
Текст
Настоящее изобретение относится к ингибиторам 11 гидроксистероиддегидрогеназы 1-го типа,антагонистам минералокортикоидного рецептора (MR), и их фармацевтическим композициям. Соединения формулы I могут быть применены для лечения различных болезней, опосредованных с экспрессией или активностью 11 гидроксистероиддегидрогеназы 1-го типа, и/или болезней, ассоциированных с избытком альдостерона. Область техники, к которой относится изобретение Настоящее изобретение относится к модуляторам 11 гидроксистероиддегидрогеназы 1-го типа(11HSD1) и/или минералокортикоидного рецептора (MR), их композициям и способам их применения. Уровень техники Глюкокортикоиды представляют собой стероидные гормоны, которые регулируют жировой метаболизм, функцию и распределение. У позвоночных глюкокортикоиды оказывают сильные и разнообразные физиологические воздействия на развитие, нейробиологию, воспаление, кровяное давление, метаболизм и апоптоз клеток. У людей первичный эндогенно образующийся глюкокортикоид представляет собой кортизол. Кортизол синтезируется в пучковой зоне коры надпочечников под контролем быстродействующей цепи нейроэндокринной обратной связи, обозначаемой как гипоталамо-гипофизарнонадпочечниковая (НРА) ось. Продуцирование кортизола в надпочечниках протекает под контролем адренокортикотропного гормона (АСТН), фактора, образуемого и секретируемого аденогипофизом. Продукция АСТН в аденогипофизе является высокорегулируемой и управляется кортиколиберином (CRH),продуцируемом в паравентрикулярном ядре гипоталамуса. НРА ось поддерживает циркулирование концентраций кортизола в определенных пределах, с продвижением вверх во время дневного максимума или при стрессах, и быстро ослабляется через петлю отрицательной обратной связи, возникающей из способности кортизола подавлять продукцирование АСТН в аденогипофизе и продукцию CRH в гипоталамусе. Альдостерон представляет собой другой гормон, продуцируемый корой надпочечников; альдостерон регулирует гомеостаз натрия и калия. 50 лет назад роль избытка альдостерона в болезни человека обнаружили при описании синдрома первичного альдостеризма (Conn (1955), J. Lab. Clin. Med. 45: 6-17). Сейчас очевидно, что повышенные уровни альдостерона ассоциированы с повреждающими эффектами сердца и почек и являются основным фактором вклада в заболеваемость и смертность как при сердечной недостаточности, так и гипертонии. Два представителя надсемейства ядерно-гормонального рецептора, глюкокортикоидный рецептор(GR) и минералокортикоидный рецептор (MR), опосредуют функцию кортизола in vivo, в то время как первичным внутриклеточным рецептором альдостерона является MR. Эти рецепторы также обозначаются как лиганд-зависимые факторы транскрипции, так как их функциональность зависит от рецептора,связывающегося с его лигандом (например, кортизолом); от связывания лиганда этими рецепторами,прямомодулирующего транскрипцию через связывающие ДНК цинковые штифтовые домены и домены транскрипционной активации. Исторически основные детерминанты глюкокортикоидного действия были приписаны трем первичным факторам: 1) циркулированию уровеней глюкокортикоида (управляемого в основном НРА осью),2) белковому связыванию глюкокортикоидов и 3) плотности внутриклеточного рецептора внутри тканей-мишеней. Недавно была идентифицирована четвертая детерминанта глюкокортикоидной функции: тканеспецифический дорецепторный метаболизм глюкокортикоид-активирующих и -инактивирующих энзимов. Эти 11-бета-гидроксистероидные дегидрогеназы (11HSD) действуют как энзимы дорецепторного контроля, которые модулируют активацию GR и MR путем регуляции глюкокортикоидных гормонов. К настоящему времени были клонированы и охарактеризованы два различных изофермента 11-бета-HSD: 11HSD1 (также известный как 11-бета-HSD типа 1, 11HSD1, HSD11B1, HDL и HSD11L) и 11HSD2. 11HSD1 и 11HSD2 катализируют взаимопревращение гормонально активного кортизола (кортикостерона у грызунов) и неактивного кортизона (11-дегидрокортикостерона у грызунов). 11HSD1 широко распространен в тканях крысы и человека; экспрессия энзима и соответствующей мРНК обнаружена в легком, яичке и наиболее обильно в печени и жировой ткани. 11HSD1 катализирует как 11-бетадегидрирование, так и обратную реакцию 11-оксовосстановления, хотя 11HSD1 действует преимущественно как NADPH-зависимая оксоредуктаза в интактных клетках и тканях, катализируя активацию кортизола из инертного кортизона (Low et al. (1994), J. Mol. Endocrin. 13: 167-174) и описана регуляция глюкокортикоидного доступа к GR. Обратно, экспрессия 11HSD2 обнаружена главным образом в минералокортикоидных тканях-мишенях, таких как почка, плацента, толстая кишка и слюнная железа, которая действует как NAD-зависимая дегидрогеназа, катализирующая инактивацию кортизола в кортизон (Albiston et al. (1994), Mol. Cell. Endocrin. 105: R11-R17), и, как было установлено, защищает MR от избытка глюкокортикоида, такого как высокие уровни рецептор-активного кортизола (Blum et al. (2003), Prog.In vitro MR связывает кортизол и альдостерон с равным сродством. Тканеспецифичная активность альдостерона, однако, сопоставима с экспрессией 11HSD2 (Funder et al. (1988), Science 242: 583-585). Дезактивация кортизола в кортизон под действием 11HSD2 на сайте MR делает возможным связывание альдостерона с этим рецептором in vivo. Связывание альдостерона с MR приводит к диссоциации лиганд-активированного MR из мультибелкового комплекса, содержащего шаперонные белки, транслокацию MR в ядро и его связывание с элементами гормонального ответа в регуляторных регионах промоте-1 019747 ров генов-мишеней. В пределах периферического нефрона почки индукция сыворотки и экспрессия глюкокортикоид-индуцируемой киназы-1 (sgk-1) ведет к абсорбции ионов Na+ и воды через эпителиальный натриевый канал, а также выделение калия с последующим объемным расширением и гипертонией(Bhargava et al. (2001), Endo. 142: 1587-1594). У людей повышенные концентрации альдостерона ассоциированы с эндотелиальной дифункцией,инфарктом миокарда, левожелудочковой атрофией и смертью. При попытках модулировать эти болезненные эффекты принимались разнообразные стратегии воздействия для контроля гиперактивности альдостерона и уменьшения конечной гипертонии и взаимосвязанных с ней сердечно-сосудистых последствий. Ингибирование ангиотензин-конвертующего энзима (АСЕ) и блокада ангиотензинового рецептора 1-го типа (AT1R) являются двумя стратегиями, которые прямо влияют на систему реннин-ангиотензинальдостерон (RAAS). Однако, хотя АСЕ ингибирование и AT1R антагонизм изначально уменьшают концентрации альдостерона, циркулирование концентраций этого гормона возвращается к исходным уровням при продолжительной терапии (известно как "падение альдостерона"). Важно, что совместное назначение антагонистов MR спиронолактона или эплеренона прямо блокирует повреждающие эффекты этого механизма падения и впечатляюще уменьшает смертность пациентов (Pitt et al., New England J.Med. (1999), 341: 709-719; Pitt et al., New England J. Med. (2003), 348: 1309-1321). Следовательно, MR антагонизм может быть важной стратегией лечения для многочисленных пациентов с гипертонией и сердечно-сосудистой болезнью, особенно страдающих гипертонией пациентов с риском повреждения органа-мишени. Мутации в любом из генов, кодирующих 11-бета-HSD энзимы, ассоциированы с патологиями человека. Например, 11HSD2 экспрессирована в альдостерон-чувствительных тканях, таких как периферический нефрон, слюнная железа и слизистая толстой кишки, где активность кортизол-дегидрогеназы служит для защиты от запрещенного замещения кортизолом MR, по существу неселективного (Edwardset al. (1988), Lancet 2: 986-989). Индивидуумы с мутациями в 11HSD2 имеют недостаточность этой кортизол-дезактивирующей активности и, как результат, синдром очевидного избытка минералокортикоида(также обозначаемый как "SAME"), характеризующийся гипертонией, калиевой недостаточностью и удержанием натрия (Wilson et al. (1998), Proc. Natl. Acad. Sci. 95: 10200-10205). Подобным образом, мутации в 11HSD1, первичном регуляторе тканеспецифической биодоступности глюкокортикоида, в генном кодировании солокализованного NADPH-образующего энзима, дегидрогеназы гексозы-6-фосфата(H6PD), могут приводить к дефициту кортизонредуктазы (CRD), при котором активация кортизона в кортизол не протекает, что приводит к адренокортикотропин-опосредованному избытку андрогенного гормона. CRD пациенты выделяют фактически все глюкокортикоиды как метаболиты кортизона (тетрагидрокортизон) с низкой или отсутствующей концентрацией метаболитов кортизола (тетрагидрокортизолы). При пероральном поступлении кортизона CRD пациенты проявляют ненормально низкую плазменную концентрацию кортизолов. У этих индивидуумов присутствует АСТН-опосредованный избыток андрогенного гормона (гирсутизм, менструальная неравномерность, гиперандрогенизм), фенотип, сходный с синдромом поликистозного яичника (PCOS) (Draper et al. (2003), Nat. Genet. 34: 434-439). Важность НРА оси в контролировании глюкокортикоидных отклонений очевидна из того факта,что разрыв гомеостаза в НРА оси под действием или избыточной, или недостаточной секреции или действия приводит соответственно к болезни Иценко-Кушинга или болезни Аддисона (Miller и Chrousos(2001), Endocrinology and Metabolism, eds. Felig и Frohman (McGraw-Hill, New York), 4th Ed.: 387-524). Пациенты с болезнью Иценко-Кушинга (редкая болезнь, характеризуемая системным избытком глюкокортикоида, возникающим вследствие надпочечной или гипофизарной опухоли) или получающие глюкокортикоидную терапию проявляют обратимое внутреннее ожирение. Интересно, что фенотип пациентов с болезнью Иценко-Кушинга близко сходен с метаболическим синдромом Ривена (Reaven) (также известным как Х-синдром или синдром резистентности к инсулину), симптомы которого включают внутреннее ожирение, толерантность к глюкозе, резистентность к инсулину, гипертонию, диабет 2-го типа и гиперлипемию (Reaven (1993), Ann. Rev. Med. 44: 121-131). Однако роль глюкокортикоидов в преобладающих формах человеческого ожирения остается малоизученной, так как циркулирующие концентрации глюкокортикоида не являются повышенными у большинства пациентов с метаболическим синдромом. В действительности, было показано, что действие глюкокортикоида на целевую ткань зависит не только от циркулирующих уровней, но также от внутриклеточной концентрации, локально усиленного действия глюкокортикоидов в жировой ткани и скелетных мышцах при метаболическом синдроме. Накапливается понимание того, что энзиматическая активность 11HSD1, которая регенерирует активные глюкокортикоиды из неактивных форм и играет центральную роль при регулировании внутриклеточной концентрации глюкокортикоида, обычно повышена в жировых скоплениях в тучных индивидуумах. Это предполагает роль локальной реактивации глюкокортикоида при ожирении и метаболическом синдроме. При данной способности 11HSD1 к регенерации кортизола из инертного циркулирующего кортизона уделялось значительное внимание к ее роли в усилении глюкокортикоидной функции. 11HSD1 экспрессирована в многомедиаторных GR-обогащенных тканях, включая ткани значительной метаболи-2 019747 ческой важности, такой как печень, жировая ткань и скелетная мышца, и, как таковое, было постулировано как содействующее в тканеспецифическом потенцировании глюкокортикоид-опосредованного противодействия инсулиновой функции. Обсуждение а) фенотипического сходства между глюкокортикоидным избытком (болезнь Иценко-Кушинга) и метаболическим синдромом с нормальной циркуляцией глюкокортикоидов при последнем, также как b) способностью 11HSD1 к генерации активного кортизола из неактивного кортизона тканеспецифический способом, привело к предположению, что общее ожирение и ассоциированное метаболическое осложнение в Х-синдроме возникает из возрастания активности 11HSD1 в пределах жировой ткани, приводя к "болезни Иценко-Кушинга в сальнике" (Bujalska et al.(1997), Lancet 349: 1210-1213). Действительно, было показано, что 11HSD1 регулирован на повышение в жировой ткани у тучных грызунов и людей (Livingstone et al. (2000), Endocrinology 131: 560-563; Rask etal. (2001), J. Clin. Endocrinol. Metab. 86: 1418-1421; Lindsay et al. (2003), J. Clin. Endocrinol. Metab. 88: 2738-2744; Wake et al. (2003), J. Clin. Endocrinol. Metab. 88: 3983-3988). Дополнительная поддержка этой точки зрения была получена в исследованиях на моделях трансгенных мышей. Жироспецифическая гиперэкспрессия 11HSD1 под контролем промотера аР 2 в мыши продуцирует фенотип, удивительно напоминающий человеческий метаболический синдром (Masuzaki etal. (2001), Science 294: 2166-2170; Masuzaki et al. (2003), J. Clinical Invest. 112: 83-90). Важно, что этот фенотип имеет место без прироста общего циркулирующего кортикостерона, но далее управляется локальной продукцией кортикостерона в пределах жировых депо. Увеличенная активность 11HSD1 в этих мышах (2-3-кратная) очень подобна той, что наблюдается при человеческом ожирении (Rask et al. (2001),J. Clin. Endocrinol. Metab. 86: 1418-1421). Это допускает, что локальная 11HSD1-опосредованная конверсия инертного глюкокортикоида в активный глюкокортикоид может иметь сильные влияния на чувствительность к инсулину по всему телу. Основываясь на этих данных, было предсказано, что потеря 11HSD1 будет вести к возрастанию чувствительности к инсулину и толерантности к глюкозе благодаря тканеспецифической недостаточности уровней активного глюкокортикоида. В действительности это случай показаний в исследованиях с 11HSD1-дефицитными мышами, получаемыми гомологичной рекомбинацией (Kotelevstev et al. (1997),Proc. Natl. Acad. Sci. 94: 14924-14929; Morton et al. (2001), J. Biol. Chem. 276: 41293-41300; Morton et al.(2004), Диабет 53: 931-938). Эти мыши полностью лишены активности 11-кеторедуктазы, подтверждая,что 11HSD1 определяет только активность, способную к генерации активного кортикостерона из инертного 11-дегидрокортикостерона. 11HSD1-дефицитные мыши являются устойчивыми к гипергликемии, вызванной диетой и стрессом, проявляют уменьшенную индукцию печеночных глюконеогенных энзимов (PEPCK, G6P), показывают увеличенную чувствительность к инсулину в пределах жировой ткани и имеют неустановленный липидный профиль (уменьшенные концентрации триглицеридов и увеличенные кардиопротекторного HDL). Кроме того, эти животные обнаруживают устойчивость к ожирению, спровоцированному высококалорийной диетой. Взятые совместно, эти исследования на трансгенных мышах подтверждают роль локальной реактивации глюкокортикоидов в контроле печеночной и периферической чувствительности к инсулину и допускают, что ингибирование активности 11HSD1 может предоставлять преимущество при лечении ряда глюкокортикоид-зависимых расстройств, включая ожирение, резистентность к инсулину, гипергликемию и гиперлипемию. Были опубликованы данные в поддержку этой гипотезы. Недавно было сообщено, что 11HSD1 играет роль в патогенезе общего ожирения и появлении метаболического синдрома у людей. Повышенная экспрессия гена 11HSD1 ассоциирована с метаболическими ненормальностями у тучных женщин и повышенная экспрессия этого гена предположительно вносит вклад в повышенную локальную конверсию кортизона в кортизол в жировой ткани тучных индивидуумов (Engeli et al. (2004), Obes. Res. 12: 9-17). Было показано, что новый класс ингибиторов 11HSD1, арилсульфонамидотиазолы, улучшают чувствительность печени к инсулину и понижают уровни глюкозы в крови при гипергликемических напряжениях мыши (Barf et al. (2002), J. Med. Chem. 45: 3813-3815; Alberts et al. Endocrinology (2003), 144: 4755-4762). Кроме того, недавно было сообщено, что селективные ингибиторы 11HSD1 могут улучшать тяжелую гипергликемию в генетически диабетических тучных мышах. Таким образом, 11HSD1 является многообещающей фармацевтической мишенью для лечения метаболического синдрома (Masuzaki etal. (2003), Curr. Drug Targets Immune Endocr. Metabol. Disord. 3: 255-62). А. Ожирение и метаболический синдром. Как описано выше, множество линий доказательства предполагают, что ингибирование активности 11HSD1 может быть эффективно для уменьшения ожирения и/или признаков метаболического синдрома, включая толерантность к глюкозе, резистентность к инсулину, гипергликемии, гипертонии и/или гиперлипемии. Глюкокортикоиды являются известными антагонистами действия инсулина и уменьшения локальных уровней глюкокортикоида ингибированием внутриклеточной конверсии кортизона в кортизол, которые могут увеличивать печеночную и/или периферическую чувствительность к инсулину и потенциально уменьшать внутреннее ожирение. Как описано выше, мыши с отключенным 11HSD1 являются устойчивыми к гипергликемии, проявляют ослабленную индукцию ключевых печеночных глюко-3 019747 неогенных энзимов, показывают заметно повышенную чувствительность к инсулину в пределах жировой ткани и имеют улучшенный липидный профиль. Кроме того, эти животные обнаруживают устойчивость к ожирению, вызванному высококалорийной диетой (Kotelevstev et al. (1997), Proc. Natl. Acad. Sci. 94: 14924-14929; Morton et al. (2001), J. Biol. Chem. 276: 41293-41300; Morton et al. (2004), Diabet 53: 931-938). Так, предполагают, что ингибирование 11HSD1 имеет множественные положительные эффекты в печени, жировой ткани и/или скелетной мышце, особенно относящееся к облегчению компонент(ов) метаболического синдрома и/или ожирения.B. Панкреатическая функция. Известно, что глюкокортикоиды ингибируют стимулированное глюкозой выделение инсулина из панкреатических бета-клеток (Billaudel и Sutter (1979), Horm. Metab. Res. 11: 555-560). Как в болезни Иценко-Кушинга, так и диабетических fa/fa крысах Цукера (Zucker), стимулированное глюкозой выделение инсулина заметно уменьшается (Ogawa et al. (1992), J. Clin. Invest. 90: 497-504). Сообщалось, что мРНК 11HSD1 и активность в панкреатических островковых клетках ob/ob мышей и ингибирование этой активности действием ингибитора 11HSD1 карбеноксолона улучшает стимулированное глюкозой выделение инсулина (Davani et al. (2000), J. Biol. Chem. 275: 34841-34844). Так, предсказано, что ингибирование 11HSD1 имеет положительные эффекты на поджелудочную железу, включая увеличение стимулированного глюкозой выделения инсулина.C. Когнитивная способность и деменция. Легкое расстройство познавательных функций является обычным признаком старения, что может быть в конечном счете отнесено к прогрессу деменции. Как у стареющих животных и людей, межиндивидуальные различия в общей познавательной функции связаны с вариабельностью в долгосрочном воздействии глюкокортикоидов (Lupien et al. (1998), Nat. Neurosci. 1: 69-73). Предполагают, что дисрегуляция НРА оси, приводящая к хроническому воздействию избытка глюкокортикоида в определенных подразделах мозга, вносит вклад в снижении познавательной функции (McEwen и Sapolsky (1995), Curr.Early Edition: 1-6). Обработка первичных клеток гиппокампа ингибитором 11HSD1 карбеноксолоном защищает клетки от глюкокортикоид-опосредованного обострения возбуждающей аминокислотной нейротоксичности (Rajan et al. (1996), J. Neurosci. 16: 65-70). Кроме того, 11HSD1-дефицитные мыши защищены от глюкокортикоид-ассоциированной дисфункции гиппокампа, которая ассоциирована со старением (Yau et al. (2001), Proc. Natl. Acad. Sci. 98: 4716-4721). В дважды рандомизированных, двойных слепых, плацебо-контролируемых перекрестных исследованиях, назначение карбеноксолона улучшало словесную беглость и словесную память (Sandeep et al. (2004), Proc. Natl. Acad. Sci. Early Edition: 1-6). Таким образом, предполагают, что ингибирование 11HSD1 уменьшает воздействие глюкокортикоидов в мозгу и защищает от повреждающих эффектов глюкокортикоида на нейрональную функцию, включая познавательный упадок, деменцию и/или депрессию.D. Внутриглазное давление. Глюкокортикоиды могут быть применены локально и системно для широкого диапазона состояний в клинической офтальмологии. Одно особенное осложнение при этих схемах лечения представляет собой кортикостероид-индуцированную глаукому. Эта патология характеризуется значительным увеличением внутриглазного давления (IOP). В его наиболее продвинутой и нелеченной форме IOP может вести к частичной потере поля зрения и в конечном счете слепоте. IOP возникает из взаимосвязи между накоплением влаги и ее выделением. Накопление влаги имеет место в непигментированных клетках эпителия(NPE) и ее выделение проходит через клетки трабекулярной сети. 11HSD1 локализован в NPE клеткахSci. 42: 2037-2042) и его функция, вероятно, существенна для усиления глюкокортикоидной активности в пределах этих клеток. Это мнение подтверждается наблюдением такого факта, что свободная концентрация кортизола значительно превышает концентрацию кортизона в жидкости (отношение 14:1). Функциональную значимость 11HSD1 в глазу исследовали с применением ингибитора карбеноксолона на здоровых добровольцах (Rauz et al. (2001), Invest. Ophthalmol. Vis. Sci. 42: 2037-2042). После семи дней лечения карбеноксолоном, IOP уменьшалось на 18%. Таким образом, считается, что ингибирование 11HSD1 в глазу уменьшает локальные глюкокортикоидные концентрации и IOP, приводя к благотворным эффектам в управлении глаукомой и другими глазными расстройствами. Е. Гипертония. Гипертензивные вещества, произведенные из адипоцита, такие как лептин и ангиотензиноген, как было предположено, вовлечены в патогенез гипертонии, связанной с ожирением (Matsuzawa et al. (1999),Ann. N. Y. Acad. Sci. 892: 146-154; Wajchenberg (2000), Endocr. Rev. 21: 697-738). Лептин, который секретируется в избытке в aP2-11HSD1 трансгенной мыши (Masuzaki et al. (2003), J. Clinical Invest. 112: 8390), может активировать различные пути симпатической нервной системы, включая те, что регулируют кровяное давление (Matsuzawa et al. (1999), Ann. N. Y. Acad. Sci. 892: 146-154). Кроме того, система ре-4 019747 нин-ангиотензин (RAS), как было показано, является основной детерминантой кровяного давления(Walker et al. (1979), Hypertension 1: 287-291). Ангиотензиноген, который имеет место в печени и жировой ткани, является ключевым субстратом для ренина и управляет активацией RAS. Плазменные уровни ангиотензиногена значительно повышены в aP2-11HSD1 трансгенной мыши, как ангиотензина II и альдостерона (Masuzaki et al. (2003), J. Clinical Invest. 112: 83-90). Эти силы аналогично управляют повышенным кровяным давлением, наблюдаемым в aP2-11HSD1 трансгенной мыши. Лечение этих мышей низкими дозами антагониста рецептора ангиотензина II ликвидируют эту гипертонию (Masuzaki et al.(2003), J. Clinical Invest. 112: 83-90). Эти данные иллюстрируют важность локальной реактивации глюкокортикоида в жировой ткани и печени и позволяют допустить, что гипертония может быть вызвана или обострена активностью 11HSD1. Таким образом, ингибирование 11HSD1 и уменьшение уровеней глюкокортикоидов жировой ткани и/или печени, как предсказывается, имеет благотворные эффекты на гипертонию и связанные с гипертонией сердечно-сосудистые расстройства.F. Костная болезнь. Глюкокортикоиды могут иметь неблагоприятные воздействия на скелетные ткани. Продолжительное воздействие даже умеренных доз глюкокортикоида может приводить к остеопорозу (Cannalis (1996),J. Clin. Endocrinol. Metab. 81: 3441-3447) и повышенному риску переломов. Эксперименты in vitro подтверждают разрушающее влияние глюкокортикоидов как на клетки, разрушающие костную ткань (также известные как остеокласты), так и клетки, формирующие костную ткань (остеобласты). 11HSD1, как было показано, присутствует в культурах человеческих первичных остеобластов, также как клетках из взрослой кости, подобной смеси остеокластов и остеобластов (Cooper et al. (2000), Bone 27: 375-381); ингибитор 11HSD1, карбеноксолон, как было показано, ослабляет отрицательные эффекты глюкокортикоидов на образование узелков кости (Bellows et al. (1998), Bone 23: 119-125). Таким образом, ингибирование 11HSD1, как считается, уменьшает локальную концентрацию глюкокортикоида в пределах остеобластов и остеокластов, приводя к благотворным эффектам при различных формах костной болезни,включая остеопороз. В настоящее время развиваются низкомолекулярные ингибиторы 11HSD1 для лечения или предотвращения 11HSD1-опосредованных заболеваний, такие как описанные выше. Например, определенные основанные на амиде ингибиторы описаны в WO 2004/089470, WO 2004/089896,WO 2004/056745 и WO 2004/065351. Антагонисты 11HSD1 были исследованы в клинических испытаниях на людях (Kurukulasuriya etal. (2003), Curr. Med. Chem. 10: 123-53). В свете экспериментальных данных, показывающих роль 11HSD1 в таких расстройствах опосредованных глюкокортикоидом, как метаболический синдром, гипертония, ожирение, резистентность к инсулину, гипергликемия, гиперлипемия, диабет 2-го типа, избыток андрогенного гормона (гирсутизм,менструальная неравномерность, гиперандрогенизм) и синдром поликистозного яичника (PCOS), желательны терапевтические агенты, направленные на увеличение или подавление этих метаболических путей модулированием уровня 11HSD1 глюкокортикоидной сигнальной трансдукции. Кроме того, так как MR связывается с альдостероном (его природным лигандом) и кортизолом с равными величинами сродства, соединения, которые создаются для взаимодействия с активным сайтом 11HSD1 (который связывается с кортизоном/кортизолом) также могут взаимодействовать с MR и действовать как антагонисты. Так как MR вовлечен в сердечную недостаточность, гипертонию и родственные патологии, включая атеросклероз, артериосклероз, болезнь коронарных артерий, тромбоз, ангину,болезнь периферических сосудов, повреждение сосудистой стенки и инсульт, MR антагонисты желательны и также могут быть применены для лечения сложных сердечно-сосудистых, почечных и воспалительных патологий, включая расстройства липидного метаболизма, включая дислипидемию или гиперлипопротеиномию, диабетическую дислипидемию, смешанную дислипидемию, гиперхолестеринемию,гипертриглицеридемию, также как заболевания, ассоциированные с диабетом 1-го типа, диабетом 2-го типа, ожирением, метаболический синдромом, резистентностью к инсулину и общим зависимым от альдостерона повреждением органа-мишени. Как здесь доказано, существует продолжающаяся необходимость в новых и улучшенных лекарствах, которые нацелены на 11HSD1 и/или MR. Описанные здесь соединения, композиции и способы помогают решить эту и другие задачи. Сущность изобретения Настоящее изобретение предоставляет, в частности, соединения формулы I или их фармацевтически приемлемые соли, для которых здесь определены составляющие фрагменты. Настоящее изобретение далее предоставляет композиции, включающие в себя соединения по изобретению и фармацевтически приемлемый носитель. Настоящее изобретение далее предоставляет способы модулирования 11HSD1 или MR контактированием 11HSD1 или MR с соединением по изобретению. Настоящее изобретение далее предоставляет способы ингибирования 11HSD1 или MR контактированием 11HSD1 или MR с соединением по изобретению. Настоящее изобретение далее предоставляет способы ингибирования конверсии кортизона в кортизол в клетке контактированием клетки с соединением по изобретению. Настоящее изобретение далее предоставляет способы ингибирования продукции кортизола в клетке контактированием клетки с соединением по изобретению. Настоящее изобретение далее предоставляет способы лечения болезней, ассоциированных с активностью или экспрессией 11HDS1 или MR. Настоящее изобретение далее предоставляет соединение или композицию по изобретению для применения в терапии. Настоящее изобретение далее предоставляет соединение по изобретению для применения в лечении болезни, ассоциированной с экспрессией или активностью 11HSD1 или MR. Настоящее изобретение далее предоставляет соединение или композицию для применения при получении лекарства для лечения болезни, ассоциированной с экспрессией или активностью 11HSD1 илиMR. Подробное описание предпочтительного варианта осуществления Настоящее изобретение предоставляет, в частности, соединения формулы I или их фармацевтически приемлемые соли,где Су представляет собой арил или гетероарил, каждый необязательно замещенный 1, 2, 3, 4 или 5-W-X-Y-Z, каждый независимо, представляют собой атом галогена, CN, NO2, С 1-4 алкокси, гетероарилокси, С 2-6 алкинил, C1-4 галогеналкокси, NRcC(O)Rd, NRcC(O)ORa, C(O)NRcRd, NRcRd, NReS(O)2Rb,C1-4 галогеналкил, C1-6 алкил, гетероциклоалкил, арил или гетероарил, где каждый упомянутый C1-6 алкил,арил или гетероарил необязательно замещен 1, 2 или 3 атомами галогена, C1-6 алкилом,C1-4 галогеналкилом, CN, NO2, ORa, SRa, -C(O)NRcRd, NRcC(O)Rd или COORa;Q представляет собой циклогексил, замещенный в 4-м положении по меньшей мере одним -W'-X'Y'-Z';Ra представляет собой атом водорода, C1-6 алкил, C1-6 галогеналкил, C2-6 алкенил, C2-6 алкинил, арил,циклоалкил, гетероарил или гетероциклоалкил, где упомянутые C1-6 алкил, C1-6 галогеналкил, C2-6 алкенил,C2-6 алкинил, арил, циклоалкил, гетероарил или гетероциклоалкил необязательно замещены атомом водорода, ОН, амино, атомом галогена, C1-6 алкилом, C1-6 галогеналкилом, арилом, арилалкилом, гетероарилом, гетероарилалкилом, циклоалкилом или гетероциклоалкилом;Rb представляет собой атом водорода, C1-6 алкил, C1-6 галогеналкил, C2-6 алкенил, C2-6 алкинил, арил,циклоалкил, гетероарил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил, где упомянутые C1-6 алкил, C1-6 галогеналкил, C2-6 алкенил, C2-6 алкинил, арил, циклоалкил, гетероарил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил необязательно замещены атомом водорода, ОН, амино, атомом галогена, C1-6 алкилом,C1-6 галогеналкилом, арилом, арилалкилом, гетероарилом, гетероарилалкилом, циклоалкилом или гетероциклоалкилом;Rc и Rd, каждый независимо, представляют собой атом водорода, C1-10 алкил, C1-6 галогеналкил,C2-6 алкенил, C2-6 алкинил, арил, гетероарил, циклоалкил, гетероциклоалкил, арилалкил, гетероарилалкил,циклоалкилалкил или гетероциклоалкилалкил, где упомянутые C1-10 алкил, C1-6 галогеналкил, C2-6 алкенил,С 2-6 алкинил, арил, гетероарил, циклоалкил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил необязательно замещены атомом водорода, ОН, амино, атомом гало-6 019747Re представляет собой атом водорода, C1-10 алкил, C1-6 галогеналкил, C2-6 алкенил, C2-6 алкинил, арил,гетероарил, циклоалкил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил, где упомянутые C1-10 алкил, C1-6 галогеналкил, C2-6 алкенил, C2-6 алкинил, арил, гетероарил, циклоалкил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил или гетероциклоалкилалкил необязательно замещены атомом водорода, ОН, амино, атомом галогена, C1-6 алкилом,C1-6 галогеналкилом, арилом, арилалкилом, гетероарилом, гетероарилалкилом, циклоалкилом или гетероциклоалкилом; где каждый арил выбирают из фенила и нафтила; каждый циклоалкил выбирают из группы, состоящей из циклопропила, циклобутила, циклопентила,циклогексила, циклогептила, циклопентенила, циклогексенила, циклогексадиенила, циклогептатриенила,норборнила, норпинила, норкарнила и адамантила; каждый гетероарил выбирают из группы, состоящей из пиридила, пиримидинила, пиразинила, пиридазинила, триазинила, фурила, хинолила, изохинолила, тиенила, имидазолила, тиазолила, индолила,пиррила, оксазолила, бензофурила, бензотиенила, бензтиазолила, изоксазолила, пиразолила, триазолила,тетразолила, индазолила, 1,2,4-тиадиазолила, изотиазолила, бензотиенила, пуринила, карбазолила, бензимидазолила, индолинила, хиназолинила, пирроло[2,3-d]пиримидинила и 1,3-бензотиазолила; каждый гетероциклоалкил выбирают из группы, состоящей из морфолино, тиоморфолино, пиперазинила, тетрагидрофуранила, тетрагидротиенила, 2,3-дигидробензофурила, 1,3-бензодиоксола, бензо-1,4 диоксана, пиперидинила, пирролидинила, изоксазолидинила, изотиазолидинила, пиразолидинила, оксазолидинила, тиазолидинила, имидазолидинила, 1,2,3,6-тетрагидропиридинила, 2-оксо-(2H)-пиридинила,2-оксо[1,3]оксазолидинила, 2-оксопирролидинила, 2-оксопиперидинила и 2-оксо[1,3]оксазинанила; каждый арилалкил представляет собой C1-6 алкил, замещенный арилом; каждый гетероарилалкил представляет собой C1-6 алкил, замещенный гетероарилом. В предпочтительном варианте Су представляет собой фенил, нафтил, пиридил, пиримидинил, триазинил, фуранил, тиазолил, пиразинил, пуринил, хиназолинил, хинолинил, изохинолинил, пирроло[2,3d]пиримидинил или 1,3-бензотиазолил, каждый необязательно замещенный 1, 2, 3, 4 или 5 -W-X-Y-Z. В более предпочтительном варианте Су представляет собой фенил, нафтил, пиридил, пиримидинил,триазинил, фуранил или тиенил, каждый необязательно замещенный 1, 2, 3, 4 или 5 -W-X-Y-Z. В еще более предпочтительном варианте Су представляет собой фенил, нафтил, пиридил, пиримидинил, триазинил, фуранил, тиазолил, пиразинил, пуринил, хиназолинил, хинолинил, изохинолинил,пирроло[2,3-d]пиримидинил или 1,3-бензотиазолил, каждый необязательно замещенный 1, 2, 3 или 4 атомами галогена, CN, NO2, C1-4 алкокси, гетероарилокси, C2-6 алкинил, C1-4 галогеналкокси, NRcC(O)Rd,NRcC(O)ORa, C(O)NRcRd, NRcRd, NReS(O)2Rb, C1-4 галогеналкил, C1-6 алкил, гетероциклоалкил, арил или гетероарил, где каждый из упомянутых C1-6 алкила, арила или гетероарила необязательно замещен 1, 2 или 3 атомами галогена, C1-6 алкилом, C1-4 галогеналкилом, CN, NO2, ORa, SRa, C(O)NRcRd, NRcC(O)Rd илиCOORa. В наиболее предпочтительном варианте Су представляет собой фенил, нафтил, пиридил, пиримидинил, триазинил, фуранил, тиенил, тиазолил, пиразинил, пуринил, хиназолинил, хинолинил, изохинолинил, пирроло[2,3-d]пиримидинил или 1,3-бензотиазолил, каждый необязательно замещенный 1, 2, 3 или 4 заместителями, независимо выбранными из атома галогена, CN, NO2, C1-4 алкокси, пиридин-2 илокси, пиридин-3-илокси, пиридин-4-илокси, С 2-6 алкинила, C1-4 галогеналкокси, NRcC(O)Rd,NRcC(O)ORa, C(O)NRcRd, NRcRd, NReS(O)2Rb, C1-4 галогеналкила, C1-6 алкила, фенила, пиридила, пиримидинила, изоксазолила, пиразолила, 1,2,3,6-тетрагидропиридинила, 2-оксо-(2 Н)-пиридинила, 2 оксо[1,3]оксазолидинила,2-оксопирролидинила,пирролидинила,2-оксопиперидинила и 2 оксо[1,3]оксазинанила; где каждый из упомянутых C1-6 алкила, фенила, пиридила, пиримидинила, изоксазолила, пиразолила, 1,2,3,6-тетрагидропиридинила, 2-оксо-(2 Н)-пиридинила, 2-оксо[1,3]оксазолидинила,2-оксопирролидинила, пирролидила, 2-оксопиперидинила или 2-оксо[1,3]оксазинанила необязательно замещен 1, 2 или 3 атомами галогена, C1-6 алкилом, C1-4 галогеналкилом, CN, NO2, ORa, SRa, C(O)NRcRd,NRcC(O)Rd или COORa. В более предпочтительном варианте Су представляет собой фенил, нафтил, пиридил, пиримидинил,триазинил, фуранил или тиенил, каждый необязательно замещенный 1, 2 или 3 атомами галогена, CN,C1-4 алкокси, C1-4 галогеналкокси, C1-6 алкилом или арилом, где упомянутый C1-6 алкил или арил необязательно замещен 1, 2 или 3 атомами галогена, C1-6 алкилом, C1-4 галогеналкилом, CN, NO2, ORa или SRa. В еще более предпочтительном варианте Су представляет собой фенил, нафтил, пиридил, пиримидинил, триазинил, фуранил или тиенил, каждый необязательно замещенный 1, 2 или 3 атомами галогена,CN, C1-4 алкокси, C1-4 галогеналкокси, C1-6 алкилом или арилом, где упомянутый C1-6 алкил или арил необязательно замещен 1, 2 или 3 атомами галогена или C1-6 алкилом. В частном воплощении изобретение относится к соединению, в котором Су представляет собой фе-7 019747 нил, пиридил, пиримидинил, хинолинил или изохинолинил, каждый необязательно замещенный 1, 2, 3, 4 или 5 -W-X-Y-Z. В другом частном воплощении изобретение относится к соединению, в котором Су представляет собой фенил, пиридил, пиримидинил, хинолинил или изохинолинил, каждый необязательно замещенный 1, 2 или 3 атомами галогена, CN, C1-6 алкилом, С 1-4 галогеналкилом, C1-4 алкокси, NRcC(O)ORa илиC(O)NRcRd. В частном варианте изобретение относится к соединениям, выбранным из 7-(4-фторфенил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она; 7-(3-фторфенил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она; 2-(транс-4-гидроксициклогексил)-7-фенил-2,7-диазаспиро[4.5]декан-1-она; 2-(транс-4-гидроксициклогексил)-7-[5-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]декан-1 она; 6-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]никотинонитрила; 2-(транс-4-гидроксициклогексил)-7-(6-метоксипиридин-2-ил)-2,7-диазаспиро[4.5]декан-1-она; 2-(транс-4-гидроксициклогексил)-7-(6-метилпиридин-2-ил)-2,7-диазаспиро[4.5]декан-1-она; 2-(транс-4-гидроксициклогексил)-7-(5-метилпиридин-2-ил)-2,7-диазаспиро[4.5]декан-1-она; 7-(5-фторпиридин-2-ил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она; 2-(транс-4-гидроксициклогексил)-7-[6-(трифторметил)пиридин-2-ил]-2,7-диазаспиро[4.5]декан-1 она;(транс-4-7-[3-хлор-5-(трифторметил)пиридин-2-ил]-1-оксо-2,7-диазаспиро[4.5]дек-2 илциклогексил)ацетонитрила; транс-4-[7-(3,5-дихлорпиридин-2-ил)-1-оксо-2,7-диазаспиро[4.5]дек-2 ил]циклогексилацетонитрила; транс-4-[7-(6-фторпиридин-2-ил)-1-оксо-2,7-диазаспиро[4.5]дек-2-ил]циклогексилацетонитрила; 7-(2-фтор-4-нитрофенил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она; 2-(транс-4-гидроксициклогексил)-7-[6-метил-4-(трифторметил)пиридин-2-ил]-2,7 диазаспиро[4.5]декан-1-она; 7-(5-этилпиримидин-2-ил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она; 7-(2-хлорпиримидин-4-ил)-2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она; 6-[2-(транс-4-гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]дек-7-ил]-N,Nдиметилникотинамида; или их фармацевтически приемлемым солям. Настоящее изобретение также относится к фармацевтическим композициям для модулирования активности 11HSD1 или MR, включающим в себя соединение формулы I или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель. Настоящее изобретение также относится к способу лечения болезни у пациента, в котором упомянутая болезнь представляет собой ожирение, диабет, нарушение толерантности к глюкозе, резистентность к инсулину, гипергликемию, гипертонию, гиперлипемию, расстройство познавательной функции,депрессию, деменцию, глаукому, сердечно-сосудистые расстройства, остеопороз, воспаление, сердечнососудистое, почечное или воспалительное заболевание, сердечную недостаточность, атеросклероз, артериосклероз, коронарную недостаточность, тромбоз, ангину, болезнь периферических сосудов, повреждение сосудистой стенки, инсульт, дислипидемию, гиперлипопротеинемию, диабетическую дислипидемию, смешанную дислипидемию, гиперхолестеринемию, гипертриглицеридемию, метаболический синдром или общее альдостероновое повреждение органа-мишени. В частном воплощении изобретение относится к способу лечения у пациента диабета типа 2, включающему введение указанному пациенту терапевтически эффективного количества соединения формулыI или его фармацевтически приемлемой соли. Настоящее изобретение также раскрывает применение соединения формулы I или его фармацевтически приемлемой соли для производства лекарственного средства для лечения ожирения, диабета, нарушения толерантности к глюкозе, резистентности к инсулину, гипергликемии, гипертонии, гиперлипемии, расстройства познавательной функции, депрессии, деменции, глаукомы, сердечно-сосудистые расстройства, остеопороза, воспаления, сердечно-сосудистого, почечного или воспалительного заболевания,сердечной недостаточности, атеросклероза, артериосклероза, коронарной недостаточности, тромбоза,ангины, болезни периферических сосудов, повреждения сосудистой стенки, инсульта, дислипидемии,гиперлипопротеинемии, диабетической дислипидемии, смешанной дислипидемии, гиперхолестеринемии, гипертриглицеридемии, метаболического синдрома или общего альдостеронового повреждения органа-мишени. В частном варианте изобретение относится к применению соединения формулы I или его фармацевтически приемлемой соли для производства лекарственного средства для лечения диабета типа 2. В другом частном воплощении изобретение относится к применению соединения формулы I или его фармацевтически приемлемой соли для лечения ожирения, диабета, нарушения толерантности к глюкозе, резистентности к инсулину, гипергликемии, гипертонии, гиперлипемии, расстройства познавательной функции, депрессии, деменции, глаукомы, сердечно-сосудистые расстройства, остеопороза, воспаления, сердечно-сосудистого, почечного или воспалительного заболевания, сердечной недостаточности, атеросклероза, артериосклероза, коронарной недостаточности, тромбоза, ангины, болезни периферических сосудов, повреждения сосудистой стенки, инсульта, дислипидемии, гиперлипопротеинемии,диабетической дислипидемии, смешанной дислипидемии, гиперхолестеринемии, гипертриглицеридемии,метаболического синдрома или общего альдостеронового повреждения органа-мишени. В частном варианте изобретение относится к применению соединения формулы I или его фармацевтически приемлемой соли для лечения диабета типа 2. В различных местах в настоящем описании заместители в соединениях по изобретению объединены в группы или в диапазоны. Специально предполагается, что изобретение включает каждый член таких групп и диапазонов и любую индивидуальную подкомбинацию. Например, термин "C1-6 алкил" специально предназначен впер-9 019747 вые описывать по отдельности метил, этил, С 3 алкил, С 4 алкил, С 5 алкил и С 6 алкил. Далее, будет принято во внимание, что определенные черты изобретения, которые, для ясности,описаны в контексте раздельных вариантов осуществления, также могут быть представлены в комбинации в отдельном варианте осуществления. Обратно, различные черты изобретения, которые, для краткости, описаны в контексте отдельного варианта осуществления, могут также быть представлены по отдельности или в любой пригодной подкомбинации. Термин "n-звенный", где n представляет собой целое число, типично описывает число циклообразующих атомов в фрагменте, где число циклообразующих атомов равно n. Например, пиперидинил представляет собой пример 6-звенного гетероциклоалкильного цикла и 1,2,3,4-тетрагидронафталин представляет собой пример 10-звенной циклоалкильной группы. Применяемый здесь термин "алкил" должен обозначать насыщенную углеводородную группу, которая является линейной или разветвленной. Примеры алкильных групп включают в себя метил (Me),этил (Et), пропил (например, N-пропил и изопропил), бутил (например, N-бутил, изобутил, трет-бутил),пентил (например, N-пентил, изопентил, неопентил) и подобные. Алкильная группа может содержат от 1 до приблизительно 20, от 2 до приблизительно 20, от 1 до приблизительно 10, от 1 до приблизительно 8,от 1 до приблизительно 6, от 1 до приблизительно 4 или от 1 до приблизительно 3 атомов углерода. Термин "алкандиил" относится к двухвалентной алкильной связывающей группе. Применяемый здесь термин "алкенил" относится к алкильной группе, имеющей одну или несколько двойных углерод-углеродных связей. Примеры алкенильных групп включают в себя этенил, пропенил,циклогексенил и подобные. Термин "алкендиил" относится к двухвалентной связывающей алкенильной группе. Применяемый здесь термин "алкинил" относится к алкильной группе, имеющий одну или несколько тройных углерод-углеродных связей. Примеры алкинильных групп включают в себя этинил, пропинил и подобные. Термин "алкиндиил" относится к двухвалентной связывающей алкинильной группе. Применяемый здесь термин "галогеналкил" относится к алкильной группе, имеющий один или несколько галогенных заместителей. Примеры галогеналкильных групп включают в себя CF3, C2F5, CHF2,CCl3, CHCl2, C2Cl5 и подобные. Применяемый здесь термин "арил" относится к моноциклическим или полициклическим (например,имеющим 2, 3 или 4 конденсированных цикла) ароматическим углеводородам, таким как, например, фенил, нафтил, антраценил, фенантренил, инданил, инденил и подобным. В некоторых вариантах осуществления арильные группы имеют от 6 до приблизительно 20 атомов углерода. Применяемый здесь термин "циклоалкил" относится к неароматическим циклическим углеводородам, включая циклические алкильные, алкенильные и алкинильные группы. Циклоалкильная группа может включать моно- или полициклические (например, имеющие 2, 3 или 4 конденсированных цикла) группы. Циклообразующие атомы углерода циклоалкильной группы могут быть необязательно замещены оксо- или сульфидогруппой. Примеры циклоалкильных групп включают в себя циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклопентенил, циклогексенил, циклогексадиенил, циклогептатриенил, норборнил, норпинил, норкарнил, адамантил и подобные. Также в определение циклоалкила включены фрагменты, которые имеют один или несколько ароматических циклов, конденсированных (т.е. имеющие связь одновременно с) с циклоалкильным циклом, например бензо- или тиенильные производные пентана, пентена, гексана и подобные. Применяемый здесь термин "гетероарил" относится к ароматическому гетероциклу, имеющему по меньшей мере один гетероатом среди циклических атомов, такой как сера, кислород или азот. Гетероарильные группы включают моноциклические и полициклические (например, имеющие 2, 3 или 4 конденсированных циклов) системы. Примеры гетероарильных групп включают в себя, без ограничения,пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, фурил, хинолил, изохинолил, тиенил,имидазолил, тиазолил, индолил, пиррил, оксазолил, бензофурил, бензотиенил, бензтиазолил,изоксазолил, пиразолил, триазолил, тетразолил, индазолил, 1,2,4-тиадиазолил, изотиазолил, бензотиенил,пуринил, карбазолил, бензимидазолил, индолинил и подобные. В некоторых вариантах осуществления гетероарильная группа имеет от 1 до приблизительно 20 атомов углерода и в следующих вариантах осуществления от около 3 до приблизительно 20 атомов углерода. В некоторых вариантах осуществления гетероарильная группа содержит от 3 до приблизительно 14, от 4 до приблизительно 14, от 3 до приблизительно 7 или от 5 до 6 циклообразующих атомов. В некоторых вариантах осуществления гетероарильная группа имеет от 1 до приблизительно 4, от 1 до приблизительно 3 или от 1 до 2 гетероатомов. Применяемый здесь термин "гетероциклоалкил" относится к неароматическим гетероциклам,включая циклические алкильные, алкенильные и алкинильные группы, в которых один или несколько циклообразующих атомов углерода заменены гетероатомом, таким как атом кислорода, азота или серы. Гетероциклоалкильные группы включают в себя моноциклические и полициклические (например, имеющие 2, 3 или 4 конденсированных цикла) системы. Примеры "гетероциклоалкильных" групп включают в себя морфолино, тиоморфолино, пиперазинил, тетрагидрофуранил, тетрагидротиенил, 2,3 дигидробензофурил, 1,3-бензодиоксол, бензо-1,4-диоксан, пиперидинил, пирролидинил, изоксазолидинил, изотиазолидинил, пиразолидинил, оксазолидинил, тиазолидинил, имидазолидинил и подобные. Циклообразующие атомы углерода и гетероатомы гетероциклоалкильной группы могут быть необязательно замещены оксо- или сульфидогруппой. Также включены в определение гетероциклоалкила фрагменты, которые имеют один или несколько ароматических циклов, конденсированных (т.е. имеющих связь одновременно с) с неароматическим гетероциклическим циклом, например фталимидил, нафталимидил, и бензопроизводные гетероциклов, такие как индоленовые и изоиндоленовые группы. В некоторых вариантах осуществления гетероциклоалкильная группа имеет от 1 до приблизительно 20 атомов углерода и в следующих вариантах осуществления от около 3 до приблизительно 20 атомов углерода. В некоторых вариантах осуществления гетероциклоалкильная группа содержит от 3 до приблизительно 14,от 4 до приблизительно 14, от 3 до приблизительно 7 или 5-6 циклообразующих атомов. В некоторых вариантах осуществления гетероциклоалкильная группа имеет от 1 до приблизительно 4, от 1 до приблизительно 3 или от 1 до 2 гетероатомов. В некоторых вариантах осуществления гетероциклоалкильная группа содержит 0-3 двойных или тройных связи. В некоторых вариантах осуществления гетероциклоалкильная группа содержит 0-2 двойных или тройных связи. Применяемый здесь термин "атом галогена" или "галоген" включает в себя фтор, хлор, бром и йод. Применяемый здесь термин "алкокси" относится к -О-алкильной группе. Примеры алкоксигрупп включают в себя метокси, этокси, пропокси (например, N-пропокси и изопропокси), трет-бутокси и подобные. Применяемый здесь термин "галогеналкокси" относится к -О-галогеналкильной группе. Примером галогеналкоксигруппы является OCF3. Применяемый здесь термин "гетероарилокси" относится к -О-гетероарилу. Примером гетероарилокси является пиридин-2-илокси [т.е. -О-(пиридин-2-ил)]. Применяемый здесь термин "арилалкил" относится к алкилу, замещенному арилом и "циклоалкилалкил" относится к алкилу, замещенному циклоалкилом. Примером арилалкильной группы является бензил. Применяемый здесь термин "амино" относится к NH2. Применяемый здесь термин "алкиламино" относится к аминогруппе, замещенной алкильной группой. Применяемый здесь термин "диалкиламино" относится к аминогруппе, замещенной двумя алкильными группами. Соединения, описанные здесь, могут быть асимметрическими (например, имеющими один или несколько стереоцентров). Подразумеваются все стереоизомеры, такие как энантиомеры и диастереомеры,пока не указано иное. Соединения по настоящему изобретению, которые содержат асимметрически замещенные атомы углерода, могут быть выделены в оптически активной или рацемической формах. В технике известны способы, как получить оптически активные формы из оптически активных исходных веществ, такие как метод расщепления рацемической смеси или путь стереоселективного синтеза. Много геометрических изомеров олефинов, C=N двойных связей и подобного, также могут присутствовать в соединениях, описанных здесь, и все такие стабильные изомеры рассматриваются в настоящем изобретении. Цис- и транс-геометрические изомеры соединений по настоящему изобретению описаны и могут быть выделены в виде смеси изомеров или как отдельные изомерные формы. Расщепление рацемических смесей соединений может быть проведено по любому из многочисленных способов, известных в технике. Пример способа включает в себя фракционную перекристаллизацию с применением хиральной расщепляющей кислоты, которая оптически активна, солеобразующей органической кислоты. Приемлемые расщепляющие агенты для способов фракционной перекристаллизации представляет собой, например, оптически активные кислоты, такие как D- и L-формы винной кислоты,диацетилвинной кислоты, дибензоилвинной кислоты, миндальной кислоты, яблочной кислоты, молочной кислоты или различных оптически активных камфорсульфоновых кислот, таких как камфорсульфоновая кислота. Другие расщепляющие агенты, пригодные для способов фракционной кристаллизации, включают стереоизомерно чистые формы альфа-метилбензиламина (например, S- и Rформы или диастереомерно чистые формы), 2-фенилглицинол, норэфедрин, эфедрин, N-метилэфедрин,циклогексилэтиламин, 1,2-диаминоциклогексан и подобные. Расщепление рацемических смесей также может быть проведено путем элюирования, на колонке,заполненной оптически активным расщепляющим агентом (например, динитробензоилфенилглицином). Приемлемая элюирующая композиция растворителей может быть определена специалистом в данной области. Соединения по изобретению также включают в себя таутомерные формы, такие как кетоенольные таутомеры. Соединения по изобретению далее включают в себя гидраты и сольваты, также как безводные и несольватированные формы. Соединения по изобретению также могут включать все изотопы атомов, присутствующих в полупродуктах или конечных соединениях. Изотопы включают в себя атомы, имеющие те же атомные номера, но различные массовые числа. Например, изотопы водорода включают в себя тритий и дейтерий. Фраза "фармацевтически приемлемый" здесь используется для обозначения тех соединений, ве- 11019747 ществ, композиций и/или форм дозировки, которые, в пределах установленного врачом диагноза, приемлемы для применения в контакте с тканями пациентов и животных без избыточной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, что соответствует значительному отношению преимущество-риск. Настоящее изобретение также включает в себя фармацевтически приемлемые соли соединений,описанных здесь. Применяемый здесь термин "фармацевтически приемлемые соли" относится к производным впервые описанных соединений, где исходное соединение модифицируется путем конвертирования существующей кислоты или основания в его солевую форму. Примеры фармацевтически приемлемых солей включают в себя, без ограничения, соли минеральной или органической кислоты с основными остатками, такими как амины; щелочные или органические соли с кислотным остатком, таким как карбоновые кислоты и подобные. Фармацевтически приемлемые соли по настоящему изобретению включают в себя традиционные нетоксичные соли или четвертичные аммониевые соли исходного соединения, образуемые, например, из нетоксичных неорганических или органических кислот. Фармацевтически приемлемые соли по настоящему изобретению могут быть синтезированы из исходного соединения,которое содержит основной или кислотный фрагмент традиционными химическими способами. В целом,такие соли могут быть получены по реакции кислоты или основания в свободных формах этих соединений со стехиометрическим количеством соответствующего основания или кислоты в воде или в органическом растворителе или в их смеси; в целом, неводные среды, подобные простому эфиру, этилацетату,этанолу, изопропанолу или ацетонитрилу, являются предпочтительными. Перечень пригодных солей приведен в Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, Pa., 1985. p. 1418 и Journal of Pharmaceutical Science, 66. 2 (1977), каждый из которых включен сюда в качестве ссылки. Настоящее изобретение также включает в себя пролекарства описанных здесь соединений. Применяемый здесь термин "пролекарства" относится к любым ковалентно связанным носителям, которые высвобождают активное исходное лекарство при назначении млекопитающему субъекту. Пролекарства могут быть получены модифицированием функциональных групп, присутствующих в соединениях, таким способом, что модифицирующие группы отщепляются, или в стандартных превращениях, или invivo, до исходных соединений. Пролекарства включают в себя соединения, в которых гидроксильные,амино, сульфгидридные или карбоксильные группы связываются с любой группой таким образом, что при назначении млекопитающему субъекту расщепляются с образованием соответственно свободной гидроксильной, амино, сульфгидридной или карбоксильной группы. Примеры пролекарств включают в себя, без ограничения, ацетатные, формиатные и бензоатные производные спиртовой и аминной функциональных групп в соединениях по изобретению. Получение и применение пролекарств обсуждаются в Т. Higuchi и V. Stella, "Pro-drugs as Novel Delivery Systems", vol. 14 of A.C.S. Symposium Series, и в Bioreversible Carriers In Drug Design, ed. Edward B. Roche, American Pharmaceutical Association и PergamonPress, 1987; оба из которых включены в качестве ссылки. Синтез. Новые соединения по настоящему изобретению могут быть получены разнообразными путями, известными для специалиста в области органического синтеза. Соединения по настоящему изобретению могут быть синтезированы с применением способов, которые далее описаны ниже, совместно с синтетическими способами, известными в области синтетической органической химии или варьированием их,что будет высоко оценено специалистами в данной области. Соединения по этому изобретению могут быть получены из легко доступных исходных веществ с применением следующих общих способов и методик. Будет высоко оценено, что если даны типичные или предпочтительные условия процесса (т.е. температуры реакции, время, мольные отношения реактантов, растворителей, давления, и т.д.), то другие условия процесса также могут быть применены, пока не указано иное. Оптимальные реакционные условия могут варьировать в зависимости от особенностей реактантов или примененного растворителя, но такие условия могут быть определены специалистом в данной области стандартными процедурами оптимизации. Способы, описанные здесь, могут контролироваться согласно любому пригодному способу, известному в технике. Например, образование продукта может контролироваться спектроскопическими методами, такими как спектроскопия ядерного магнитного резонанса (например, 1 Н- или 13 С-), инфракрасной спектроскопией, спектрометрией (например, в ультрафиолетовом и видимом диапазонах) или массспектрометрией или методом хроматографии, такой как жидкостная хроматография высокого разрешения (HPLC) или тонкослойной хроматографией. Получение соединений может включать защиту и удаление различных химических групп. Необходимость для защиты, удаления и выбора соответствующих защитных групп могут быть легко определены специалистом в данной области. Химия защитных групп может быть найдена, например, в Greene, etal., Protective Groups in Organic Synthesis, 2d. Ed., WileySons, 1991; которая включена в качестве ссылки. Реакции в способах, описанных здесь, могут быть проведены в пригодных растворителях, которые могут быть легко выбраны специалистом в области органического синтеза. Пригодные растворители мо- 12019747 гут быть, по существу, нереакционноспособны с исходными веществами (реактантами), интермедиатами или продуктами при температурах, при которых проводятся реакции, т.е. температуры, которые могут находиться в диапазоне от температуры замерзания растворителя до температуры его кипения. Данная реакция может быть проведена в одном растворителе или смеси более чем одного растворителя. В зависимости от особенностей реакционной стадии могут быть выбраны растворители, пригодные для отдельной реакционной стадии. Соединения по изобретению могут быть получены, например, с применением реакционных путей и методик, описанных ниже. Соединения по изобретению могут быть стандартно получены способом, представленным на схеме 1. Реагенты формулы 1-1 (X представляет собой уходящую группу, такую как атом галогена) могут быть введены в реакцию с аминами формулы 1-2 (или их солями) в соответствующем растворителе (например,CH2Cl2) и необязательно в присутствии основания, такого как диизопропилэтиламин для получения желаемых продуктов 1-3. Например, сульфонилхлориды формулы 1-4 могут быть введены в реакцию с аминами формулы 1-2 для получения сульфонилзамещенных соединений формулы 1-5. Схема 1 Серии спироциклических аминов формулы 2-8 могут быть получены согласно методике, представленной на схеме 2. N-защищенный 2-1 (Pr представляет собой амино-защитную группу, такую как Boc) могут быть обработаны основанием, таким как LDA, при низкой температуре в растворителе, таком как тетрагидрофуран, с последующим добавлением 1-бром-3-метил-2-бутена (2-2). Полученный интермедиат(2-3) может быть обработан озоном и затем восстановлен метилсульфидом для получения альдегида 2-4. Восстановительное аминирование 2-4 с аминами 2-5 может быть проведено в растворителе, таком как метанол, и с применением восстанавливающего агента, такого как триацетоксиборогидрид натрия, и продукт 2-6 может быть циклизован в присутствии основания, такого как изопропилмагнийбромид для получения лактама 2-7, который при кислотном отщеплении Вос-группы приводит к требуемому амину 2-8. Серии аминов формулы 3-7 могут быть получены согласно методике, представленной на схеме 3. Обработка Вос-защищенного этилового эфира нипекотиновой кислоты 3-1 основанием, таким как LDA,при низкой температуре в растворителе, таком как тетрагидрофуран, с последующим добавлением 1 бром-3-метил-2-бутена, может приводить к интермедиату 3-2, который может быть обработан озоном с последующим восстановлением метилсульфидом для получения альдегида 3-3. Восстановительное аминирование 3-3 с аминами 3-4 (где Q1, например, представляет собой замещенный или незамещенный циклоалкил или арил) может быть проведено в растворителе, таком как метанол и с применением восстанавливающего агента, такого как триацетоксиборогидрид натрия. Полученный интермедиат 3-5 может быть циклизован в присутствии основания, такого как изопропилмагний бромид для получения лактама 3-6, который при кислотном отщеплении Вос-группы приводит к требуемому пиперидину 3-7. Схема 3 Серии пиперидинов 4-4 могут быть получены способом, представленным на схеме 4. Соединение 41 может быть легко конвертировано в спирогидантоин 4-2 в условиях Бухерера-Бергса, с применением,например, карбоната аммония и цианида натрия или цианида калия в водном этаноле. Алкилирование соединения 4-2 одним эквивалентом алкилгалогенида QX (X представляет собой уходящую группу, такую как атом галогена) в присутствии карбоната калия в DMF, с последующим вторым алкилированием действием R3cX (X представляет собой уходящую группу, такую как атом галогена), в присутствии гидрида натрия в DMF, приводит к замещенным гидантоинам 4-3, которые при кислотном отщеплении Восгруппы приводят к желаемым пиперидинам 4-4. Альтернативно, обработка соединения 5-1 алкиламинами R3cNH2 и цианидом натрия может приводить к алкилированным производным гидантоина 5-2. Ароматические замещенные гидантоины 5-4 могут быть получены сочетанием с соединениями 5-2 с ароматическими бороновыми кислотами или ароматическими галогенидами 5-3 в присутствии катализатора. Кислотное расщепление Вос-группы приводит к желаемым пиперидинам 5-4 (схема 5). Схема 5 В следующем альтернативном пути пиперидины 6-6 также могут быть получены способом, представленным на схеме 6. Защищенная аминокислота 6-1 может сочетаться с амином Q-NH2 с применением сшивающего агента, такого как ВОР, для получения соединения 6-2, которое, в свою очередь, может быть прогидрировано в присутствии Pd-катализатора для получения соединения 6-3. Соединение 6-3 может быть обработано метилхлорформиатом и основанием, таким как триэтиламин в CH2Cl2, для завершения закрытия цикла и образования гидантоина 6-4. Как описано ранее, N-алкилирование R3cX (X представляет собой уходящую группу, такую как атом галогена) может приводить к соединениям формулы 6-5 и кислотное расщепление может приводить к соединениям формулы 6-6. Схема 6 Способы Соединения по изобретению могут модулировать активность 11HSD1 и/или MR. Термин "модулировать" обозначает способность увеличивать или уменьшать активность энзима или рецептора. Согласно этому соединения по изобретению могут быть применены в способах модулирования 11HSD1 и/илиMR контактированием энзима или рецептора с любым одним или несколькими описанными здесь соединениями или композициями. В некоторых вариантах осуществления соединения по настоящему изобре- 15019747 тению могут действовать как ингибиторы 11HSD1 и/или MR. В следующих вариантах осуществления соединения по изобретению могут быть применены для модулирования активности 11HSD1 и/или MR у пациента, имеющего необходимость модулирования энзима или рецептора, путем назначения модулирующего количества соединения по изобретению. Настоящее изобретение далее предоставляет способы ингибирования конверсии кортизона в кортизол в клетке или ингибирования продукции кортизола в клетке, где конверсия в или продукция кортизола являются опосредованными, по меньшей мере частично, активностью 11HSD1. Способы измерения скоростей конверсии кортизона в кортизол и обратно, также как способы измерения уровней кортизона и кортизола в клетках, является стандартной процедурой в технике. Настоящее изобретение далее предоставляет способы увеличения чувствительности клетки к инсулину контактированием клетки с соединением по изобретению. Способы измерения чувствительности к инсулину являются стандартной процедурой в технике. Настоящее изобретение далее предоставляет способы лечения болезни, ассоциированной с активностью или экспрессией, включая ненормальную активность и сверхэкспрессию, 11HSD1 и/или MR у индивидуума (например, пациента) назначением пациенту, нуждающемуся в лечении, терапевтически эффективного количества или дозы соединения по настоящему изобретению или его фармацевтический композиции. Примеры болезней могут включать любую болезнь, расстройство или состояние, т.е. прямо или опосредованно связанные с экспрессией или активностью энзима или рецептора. 11HSD1 ассоциированная болезнь также может включать в себя любую болезнь, расстройство или состояние,которое может быть предотвращено, улучшено или остановлено в развитии модулированием энзиматической активности. Примеры 11HSD1-ассоциированных болезней включают в себя ожирение, диабет, толерантность к глюкозе, резистентность к инсулину, гипергликемию, гипертонию, гиперлипемию, познавательный упадок, деменцию, депрессию (например, психотическую депрессию), глаукому, сердечно-сосудистые расстройства, остеопороз и воспаление. Далее, примеры 11HSD1-ассоциированных болезней включают в себя метаболический синдром, диабет 2-го типа, избыток андрогенного гормона (гирсутизм, менструальная неравномерность, гиперандрогенизм) и синдром поликистозного яичника (PCOS). Настоящее изобретение далее предоставляет способы модулирования MR-активности контактированием MR с соединением по изобретению, его фармацевтически приемлемой солью, пролекарством или их композицией. В некоторых вариантах осуществления модулирование может представлять собой ингибирование. В следующих вариантах осуществления представлены способы ингибирования связывания альдостерона с MR (необязательно в клетке). Способы измерения MR-активности и ингибирования связывания альдостерона являются стандартной процедурой в технике. Настоящее изобретение далее предоставляет способы лечения болезни, ассоциированный с активностью или экспрессией MR. Примеры болезней, ассоциированных с активностью или экспрессией MR,включают в себя, без ограничения, гипертонию, также как сердечно-сосудистые, почечные и воспалительные патологии, такие как сердечная недостаточность, атеросклероз, артериосклероз, болезнь коронарных артерий, тромбоз, ангина, болезнь периферических сосудов, повреждение сосудистой стенки,инсульт, дислипидемия, гиперлипопротеиномия, диабетическая дислипидемия, смешанная дислипидемия, гиперхолестеринемия, гипертриглицеридемия, и заболевания, связанные с диабетом 1-го типа, диабетом 2-го типа, метаболическим синдромом ожирения, резистентностью к инсулину и общим альдостерон-опосредованным повреждением органа-мишени. Применяемый здесь термин "клетка" предназначен обозначать клетку, которая находится in vitro, exvivo или in vivo. В некоторых вариантах осуществления ex vivo клетка может быть частью тканевого образца, извлеченного из организма, такого как млекопитающее. В некоторых вариантах осуществления invitro клетка может быть клеткой в клеточной культуре. В некоторых вариантах осуществления in vivo клетка представляет собой клетку, живущую в организме, таком как млекопитающее. В некоторых вариантах осуществления клетка представляет собой адипоцит, панкреатическую клетку, гепатоцит, нейрон или клетку, формирующую глаз. Применяемый здесь термин "контактирование" относится к связыванию совместно указанных фрагментов в in vitro системе или in vivo системе. Например, "контактирование" 11HSD1 энзима с соединением по изобретению включает в себя назначение соединения по настоящему изобретению индивидууму или пациенту, такому как человек, имеющему 11HSD1, также как, например, введение соединения по изобретению в образец, содержащий клеточный или очищенный препарат, содержащий 11HSD1 энзим. Применяемый здесь термин "индивидуум" или "пациент", которые применяются, заменяя друг друга, относится к любому животному, включая млекопитающих, предпочтительно мышей, крыс, других грызунов, кроликов, собак, кошек, свиней, крупных рогатых, овец, лошадей или приматов и наиболее предпочтительно людей. Применяемая здесь фраза "терапевтически эффективное количество" относится к количеству активного соединения или фармацевтического агента, которое проявляет биологическую или медицинскую реакцию в ткани, системе, животном, индивидууме или человеке, которая является искомой исследователем, ветеринаром, практикующим врачом или другим клиницистом, что включает в себя один или несколько из следующих пунктов:(1) предотвращение болезни, например предотвращение болезни, состояния или расстройства у индивидуума, который может быть предрасположен болезни, состоянию или расстройству, но оно пока не имеет места или не показывает патологии или симпатологии болезни (неограничивающими примерами являются предотвращение метаболического синдрома, гипертонии, ожирения, резистентности к инсулину, гипергликемии, гиперлипидемии, диабета 2-го типа, избытка андрогенного гормона (гирсутизм, менструальная неравномерность, гиперандрогенизм) и синдрома поликистозного яичника (PCOS;(2) блокирование болезни, например блокирование болезни, состояния или расстройства у индивидуума, который испытывает или проявляет патологию или симпатологию болезни, состояния или расстройства (т.е. остановка дальнейшего развития патологии и/или симпатологии), такое как блокирование развития метаболического синдрома, гипертонии, ожирения, резистентности к инсулину, гипергликемии,гиперлипемии, диабета 2-го типа, избытка андрогенного гормона (гирсутизм, менструальная неравномерность, гиперандрогенизм) или синдрома поликистозного яичника (PCOS), стабилизации от вирусной нагрузки в случае вирусной инфекции; и(3) ослабление болезни, например ослабление болезни, состояния или расстройства у индивидуума,который испытывает или проявляет патологию или симпатологию болезни, состояния или расстройства(т.е. обращение патологии и/или симпатологии), такое как уменьшение тяжести метаболического синдрома, гипертонии, ожирения, резистентности к инсулину, гипергликемии, гиперлипидемии, диабета 2 го типа, избытка андрогенного гормона (гирсутизм, менструальная неравномерность, гиперандрогенизм) и синдрома поликистозного яичника (PCOS) или уменьшение вирусной нагрузки в случае вирусной инфекции. Фармацевтические рецептуры и формы дозировки. При применении в качестве фармацевтических препаратов, соединения формулы I могут назначаться в форме фармацевтических композиций. Эти композиции могут быть получены способом, хорошо известным в фармацевтической технике, и могут быть назначены разнообразными путями, в зависимости от того, желательно ли местное или системное лечение и от области, подвергающейся лечению. Назначение может быть местным (включая глазной и к слизистым оболочкам, включая внутриносовое, вагинальное и ректальное поступление), легочное (например, путем ингаляции или инсуффляции порошков или аэрозолей, включая действием распылителя; внутритрахеальным, внутриносовым, эпидермальным и чрескожным), глазное, оральное или парентеральное. Способы глазного поступления могут включать местное назначение (глазные капли), субконъюнктивальное, периокулярное, инъекцию в стекловидное тело или введение посредством катетера-баллона или глазной вкладки, хирургически помещаемых в конъюнктивальный мешок. Парентеральное назначение включает в себя внутривенную, внутриартериальную, подкожную, внутрибрюшную или внутримышечную инъекцию или инфузию; или внутричерепное, например интратекальное или интравентрикулярное назначение. Парентеральное назначение может быть в форме одиночной шариковой дозы или может быть, например, в форме постоянного перфузионного насоса. Фармацевтические композиции и рецептуры для местного назначения могут включать чрескожный пластыри, мази, лосьоны, кремы, гели, капли, суппозитории, спреи, жидкости и порошки. Традиционные фармацевтические носители, водные, порошковые или масляные основания, загустители и подобные могут быть необходимы или желательны. Это изобретение также включает в себя фармацевтические композиции, которые содержат в качестве активного компонента один или несколько вышеупомянутых соединений по изобретению в комбинации с одним или несколькими фармацевтически приемлемыми носителями. При приготовлении композиций по изобретению типично активный компонент смешивается с наполнителем, разбавляется наполнителем или заключается в объем носителя в форме, например, капсулы, маленького пакета, бумажного или другого контейнера. Когда наполнитель служит разжижителем, он может представлять собой твердое, полутвердое или жидкое вещество, которое действует как носитель, переносчик или среда для активного компонента. Так, композиции могут быть в форме таблеток, пилюль, порошков, ромбов, малых пакетов, капсул, эликсиров, суспензий, эмульсий, растворов, сиропов, аэрозолей (как твердая или жидкая среда), мазей, содержащих, например, до 10% по массе активного соединения, мягких и жестких желатиновых капсул, суппозиториев, стерильных инъецируемых растворов и стерильных комплексных порошков. При приготовлении рецептуры активное соединение может быть размолото для получения соответствующего размера частиц перед соединением с другими компонентами. Если активное соединение является существенно нерастворимым, оно может быть размолото до размера частиц менее чем 200 меш. Если активное соединение является существенно водорастворимым, размер частиц может быть установлен путем размалывания для получения существенно единообразного распределения в рецептуре, например, около 40 меш. Некоторые примеры приемлемых наполнителей включают лактозу, декстрозу, сахарозу, сорбит,маннит, крахмалы, смолу акации, фосфат кальция, альгинаты, трагакант, желатин, силикат кремния,- 17019747 микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, воду, сироп и метилцеллюлозу. Рецептуры могут, кроме того, включать смазывающие агенты, такие как тальк, стеарат магния и минеральное масло; смачивающие агенты; эмульгирующие и суспендирующие агенты; консервирующие агенты, такие как метил- и пропилгидроксибензоаты; подсластители и отдушки. Композиции по изобретению могут быть рецептурированы для того, чтобы обеспечить быстрое, продолжительное или замедленное высвобождение активного компонента после назначения пациенту с использованием методик,известных в технике. Композиции могут быть сформированы в форме дозировки со стандартным элементом, каждая дозировка содержит от около 5 до приблизительно 100 мг, более обычно от около 10 до приблизительно 30 мг активного компонента. Термин "формы дозировки со стандартным элементом" относится к физически отдельным элементам, пригодным как единичные дозировки для людей и других млекопитающих,каждый элемент содержит предварительно определенное количество активного вещества, рассчитанное для получения желаемого терапевтического эффекта, в соединении с пригодным фармацевтическим наполнителем. Активное соединение может быть эффективным в широком диапазоне дозировки и обычно назначается в фармацевтически эффективном количестве. Будет понятно, однако, что количество соединения,действительно назначенного, будет обычно определяться врачом, согласно существенным обстоятельствам, включая излечиваемое состояние, выбранный способ применения, назначенное соединение, возраст,массу и реакции индивидуального пациента, тяжести симптомов пациента и подобного. Для приготовления твердых композиций, таких как таблетки, основной активный компонент смешивается с фармацевтическим наполнителем для образования твердой, заранее сформованной композиции, содержащей гомогенную смесь соединения по настоящему изобретению. Когда эти заранее формованные композиции обозначаются как гомогенные, активный компонент типично диспергирован равномерно по композиции, так что композиция может быть легко разделена в равно эффективные формы дозировки со стандартным элементом, такие как таблетки, пилюли и капсулы. Эта твердая пререцептура затем подразделяется в формы дозировки со стандартным элементом типа описанных выше, содержащих от, например, 0,1 до приблизительно 500 мг активного компонента по настоящему изобретению. Таблетки или пилюли по настоящему изобретению могут быть покрыты или иначе компаундированы для получения формы дозировки, имеющей преимущество продолжительного действия. Например,таблетка или пилюля может включать в себя внутреннюю дозировку и внешний компонент дозировки,последний находится в форме конверта вокруг первого. Два компонента могут быть разделены посредством энтерального слоя, который служит для защиты от разрушения в желудке и позволяет внутреннему компоненту проходить неповрежденным в двенадцатиперстную кишку или иметь задержку в высвобождении. Разнообразные вещества могут быть применены для таких энтеральных слоев или покрытий,включая ряд полимерных кислот и смесей полимерных кислот с такими веществами, как шеллак, цетиловый спирт и ацетат целлюлозы. Жидкие формы, в которые могут быть включены соединения и композиции по настоящему изобретению, для назначение перорально или путем инъекции, включают в себя водные растворы, сиропы с хорошей отдушкой, водные или масляные суспензии, и эмульсии с отдушкой съедобными маслами, такими как хлопковое масло, кунжутное масло, кокосовое масло или арахисовое масло, также как эликсиры и подобные фармацевтические носители. Композиции для ингаляции или инсуффляции включают в себя растворы и суспензии в фармацевтически приемлемых, водных или органических растворителях или их смесях, и порошки. Жидкие или твердые композиции могут содержат пригодные фармацевтически приемлемые наполнители, как описано ранее. В некоторых вариантах осуществления композиции назначаются оральным или назальным дыхательным путем для локального или системного эффекта. Композиции могут быть распылены с применением инертных газов. Распыленные растворы могут вдыхаться прямо из распыляющего устройства или распыляющее устройство может быть присоединено к дыхательной маске или дыхательному аппарату прерывистого положительного давления. Растворенные, суспендированные или порошковые композиции могут назначаться перорально или назально из устройств, которые доставляют рецептуру соответствующим способом. Количество соединения или композиции, назначенных пациенту, будет варьировать в зависимости от того, что назначается, цели назначения, такой как профилактика или терапия, состояния пациента,способа применения и подобных. В терапевтических применениях композиции могут назначаться пациенту, уже страдающему от болезни, в количестве, достаточном для остановки в развитии или, по меньшей мере, частичной остановки симптомов болезни и ее осложнений. Эффективные дозы будут зависеть от состояния болезни, которая излечивается, также как от диагноза лечащего врача в зависимости от факторов, таких как тяжесть болезни, возраст, масса и общее состояние пациента и подобного. Композиции, назначенные пациенту, могут быть в форме фармацевтических композиций, описанных выше. Эти композиции могут быть стерилизованы традиционными методиками стерилизации или могут быть стерильно отфильтрованы. Водные растворы могут быть упакованы для применения "как есть" или в лиофилизированном виде, с объединением лиофилизированного препарата с стерильным водным носителем перед назначением. рН препаратов соединения типично будет находиться между 3 и 11, более предпочтительно из 5 до 9 и наиболее предпочтительно от 7 до 8. Будет понятно, что применение определенных вышеупомянутых наполнителей, носителей или стабилизаторов будет приводить к образованию фармацевтических солей. Терапевтическая дозировка соединений по настоящему изобретению может варьировать согласно,например, особенности применения, для которого производится лечение, способа назначения соединения, здоровья и состояния пациента, и диагноза предписывающего врача. Количественное соотношение или концентрация соединения по изобретению в фармацевтической композиции может варьировать в зависимости от ряда факторов, включая дозировку, химические характеристики (например, гидрофобность) и способы применения. Например, соединения по изобретению могут быть предоставлены в водном физиологическом буферном растворе, содержащем от около 0,1 до приблизительно 10 мас./об.% соединения для парентерального назначения. Некоторые типичные диапазоны дозы составляют от около 1 мкг/кг до около 1 г/кг массы тела в день. В некоторых вариантах осуществления диапазон дозы составляет от около 0,01 до приблизительно 100 мг/кг массы тела в день. Подобным образом, дозировки зависят от таких факторов, как тип и динамика болезни или расстройства, общего состояния здоровья отдельного пациента, относительной биологической эффективности выбранного соединения, рецептуры наполнителя и его способа применения. Эффективные дозы могут быть экстраполированы из кривых зависимости доза-эффект, полученных из in vitro или тестовых модельных систем на животных. Соединения по изобретению также могут быть рецептурированы в комбинации с одним или несколькими добавочными активными компонентами, которые могут включать любой фармацевтический агент, такой как антивирусные агенты, антитела, иммунноподавители, противовоспалительные агенты и подобные. Меченые соединения и способы исследования. Другой аспект настоящего изобретения относится к меченым соединениям по изобретению (радиомеченным, флуоресцентно-меченным, и т.д.), которые могут быть применены не только в радиовидении,но также в исследованиях как in vitro, так и in vivo, для локализации и количественного определения энзима в образцах ткани, включая человека, и для идентификации лигандов ингибированием связывания меченого соединения. Согласно этому настоящее изобретение включает в себя энзиматические исследования, которые содержат такие меченые соединения. Настоящее изобретение далее включает в себя изотопно-меченные соединения по изобретению."Изотопно-" или "радиомеченное" соединение представляет собой соединение по изобретению, где один или несколько атомов заменены или замещены атомом, имеющий атомную массу или массовое число,отличающееся от атомной массы или массового числа, типично находимого в природе (т.е. природное распределение). Пригодные радионуклиды, которые могут быть включены в соединения по настоящему изобретению, включают, без ограничения, 2 Н (также обозначаемый как D для дейтерия), 3 Н (также обозначаемый как Т для трития), 11C, 13C, 14 С, 13N, 15N, 15O, 17O, 18O, 18F, 35S, 36Cl, 82Br, 75Br, 76Br, 77Br, 123I, 124I,125I и 131I. Радионуклид, т.е. включенный в текущие радиомеченные соединения, будет зависеть от специфического применения этого радиомеченного соединения. Например, для метки рецептора in vitro и исследований по конкурентному вытеснению, соединения, которые содержат 3 Н, 14 С, 82Br, 125I, 131I или 35S, обычно будут наиболее применимыми. Для радиовидения использование 11 С, 18F, 125I, 123I, 124I, 131I,75Br, 76Br или 77Br обычно будет наиболее применимым. Понятно, что "радиомеченное соединение" представляет собой соединение, которое содержит по меньшей мере один радионуклид. В некоторых вариантах осуществления радионуклид является выбранным из группы, состоящей из 3 Н, 14 С, 125I, 35S и 82Br. В некоторых вариантах осуществления меченые соединения по настоящему изобретению содержат флуоресцентную метку. Синтетические способы для включения радиоизотопов и флуоресцентных меток в органические соединения являются хорошо известными в технике. Меченое соединение по изобретению (радиомеченный, флуоресцентный-меченный и т.д.) может применяться в скриннинг-исследовании для идентификации/исследования соединений. Например, вновь синтезированное или идентифицированное соединение (т.е. тестовое соединение), которое является меченым, может быть исследовано на его способность связывать 11HSD1 или MR методом мониторинга варьирования его концентрации при контактировании с 11HSD1 или MR, через отслеживание меток. В качестве другого примера тестовое соединение (меченное) может быть исследовано на его способность уменьшать связывание другого соединения, которое, как известно, связывается с 11HSD1 или MR (т.е. стандартного соединения). Согласно этому способность тестового соединения конкурировать со стандартным соединением при связывании с 11HSD1 или MR прямо коррелирует с его связывающей способностью. Обратно, в некоторых других скрининг-тестах, помечается стандартное соединение, а тестовые соединения являются немечеными. Согласно этому концентрация меченого стандартного соединения отслеживается для того, чтобы исследовать конкуренцию между стандартным соединением и тестовым соединением, и, таким образом, определяется относительная связывающая способность тестового соединения. Комплекты. Настоящее изобретение также включает в себя фармацевтические комплекты, которые могут быть применены, например, при лечении или предотвращении упоминаемых здесь 11HSD1- или MRассоциированных болезней или расстройств, ожирения, диабета и других болезней, которые включают один или несколько контейнеров, содержащих фармацевтическую композицию, включающую в себя терапевтически эффективное количество соединения по изобретению. Такие комплекты могут далее включать, если желательно, один или несколько различных традиционных компонентов фармацевтического комплекта, такого как, например, контейнеры с одним или несколькими фармацевтически приемлемыми носителями, добавочные контейнеры и т.д., как будет легко очевидно для специалистов в данной области. Инструкции, или как вставки или как наклейки, показывающие количества назначаемых компонентов, инструкции для назначения, и/или указания для смешения компонентов, также могут быть включены в комплект. Изобретение будет описано более подробно посредством специфических примеров. Последующие примеры предложены с иллюстративными целями и не предназначены ограничивать, любым способом,изобретение. Специалисты в данной области легко осознают разнообразные некритические параметры,которые могут быть изменены или модифицированы для получения по существу тех же результатов. Было найдено, что соединения из примеров являются ингибиторами 11HSD1 и/или MR согласно одному или нескольким исследованиям, предоставленным здесь. Примеры Пример 1. К раствору 1-трет-бутил 3-этил пиперидин-1,3-дикарбоксилата (2,6 г, 10,0 ммоль) в THF (30 мл) медленно добавляли LDA (6,7 мл, 12,0 ммоль, 1,8 M раствор в смеси гептан/тетрагидрофуран/этилбензол) при -78 С и смесь медленно отогревали до -55 С в течение 1 ч. К этой смеси медленно добавляли 1-бром-3-метил-2-бутен (1,55 г, 10,5 ммоль) и реакцию отогревали до комнатной температуры и перемешивали в течение 4 ч. Смесь тушили насыщенным NH4Cl и экстрагировали диэтиловым эфиром; объединенный экстракт промывали насыщенным солевым раствором, высушивали и концентрировали. Продукт (2,75 г, 85%) очищали методом комбифлэш-хроматографии при элюировании смесью гексан/этилацетат. Стадия 2. 1-трет-Бутил 3-этил 3-(2-оксоэтил)пиперидин-1,3-дикарбоксилатCH2Cl2 (100 мл) охлаждали до -78 С и в реакционную смесь пропускали озон, пока наблюдался слегка голубой цвет (около 15 мин). Затем через раствор пропускали азот для удаления избытка озона. Добавляли диметилсульфид (10 мл) и реакцию медленно отогревали до комнатной температуры и перемешивали в течение ночи. Затем реакционную смесь промывали водой и насыщенным солевым раствором, высушивали и концентрировали, что дало продукт (2,5 г).DIPEA (1,05 экв.) добавляли к раствору гидрохлорида транс-4-аминоциклогексанола (0,080 г, 0,53 ммоль) в метаноле (2,0 мл) и перемешивали в течение 5 мин, к этому раствору добавляли 1-трет-бутил 3 этил 3-(2-оксоэтил)пиперидин-1,3-дикарбоксилат (0,15 г, 0,5 ммоль), затем триацетоксиборогидрид натрия (0,21 г, 1,0 ммоль) и смесь перемешивали в течение 2 ч. Реакционную смесь подкисляли добавлением АсОН, разбавляли водой и экстрагировали эфиром, водную фазу подщелачивали добавлением 1 н.NaOH и экстрагировали этилацетатом, который затем промывали водой, насыщенным солевым раствором, высушивали и концентрировали, что приводило к требуемому продукту (0,17 г, 85%). Изопропилмагний бромид (1,0 М в THF, 1,5 мл) медленно добавляли к раствору 1-трет-бутил 3-этил 3-2-[(цис-4-гидроксициклогексил)амино]этилпиперидин-1,3-дикарбоксилата (0,15 г, 0,38 ммоль) при 0 С и смесь перемешивали при этой температуре в течение 1 ч. Затем реакционную смесь выливали в холодную воду и экстрагировали этилацетатом, высушивали и концентрировали, что приводило к требуемому продукту (0,11 г, 85%). Хлористый водород (2,0 мл, 4,0 М в 1,4-диоксане) добавляли к раствору трет-бутил 2-(цис-4 гидроксициклогексил)-1-оксо-2,7-диазаспиро[4.5]декан-7-карбоксилата (0,10 г) в этилацетате (0,5 мл) при комнатной температуре и смесь перемешивали в течение 1 ч. Затем растворитель удаляли в вакууме,что приводило к продукту.LC-MS: 253,2 (М+Н)+. Стадия 6. 7-[(3-Хлор-2-метилфенил)сульфонил]-2-(цис-4-гидроксициклогексил)-2,7 диазаспиро[4.5]декан-1-он. Раствор 3-хлор-2-метилбензолсульфонилхлорида (0,050 г, 0,22 ммоль) в CH2Cl2 (1,0 мл) медленно добавляли к смеси гидрохлорида 2-(цис-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она (0,060 г,0,2 ммоль) и DIPEA (0,10 мл, 0,6 ммоль) в CH2Cl2 (1,0 мл) при 0 С и реакцию перемешивали в течение 1 ч. Смесь разбавляли этилацетатом и затем промывали разбавленной HCl, водой и насыщенным солевым раствором, высушивали и концентрировали. Продукт очищали методом комбифлэш-хроматографии с элюированием смесью CH2Cl2/EtOAc. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением методик, аналогичных методике примера 1. Это соединение получали с применением хиральной колонки для разделения энантиомеров примера 6. Это соединение получали с применением методик, аналогичных методикам синтеза в примере 1. Это соединение получали с применением методик, аналогичных методикам синтеза в примере 1. Это соединение получали с применением методик, аналогичных описанным для синтеза в примере 1, стадии 1-5, продолженных затем методикой амин/арильного сочетания, индуцируемого микроволновым излучением. Смесь гидрохлорида 2-циклогексил-2,7-диазаспиро[4.5]декан-1-она (0,025 г, 0,000092 моль), 1 бром-2-фторбензола (0,032 г, 0,00018 моль) и трет-бутоксида натрия (0,026 г, 0,00027 моль) в DMSO (0,5 мл) облучали в микроволновой области при 180 С в течение 5 мин. После охлаждения реакционной смеси до температуры внешней среды сырой продукт очищали препаративной HPLC. Это соединение получали с применением методик, аналогичных методике синтеза в примере 17. Это соединение получали с применением методик, аналогичных методике синтеза в примере 17. Это соединение получали с применением методик, аналогичных методике синтеза в примере 17. Это соединение получали с применением методик, аналогичных методике синтеза в примере 17. Это соединение получали с применением методик, аналогичных методике синтеза в примере 17. Это соединение получали с применением методик, аналогичных методике синтеза в примере 17. Это соединение получали с применением методик, аналогичных описанным для синтеза в примере 1, стадии 1-3, продолженных затем восстановительным аминированием с циклизацией и процедурой амин/арильного сочетания. 1-Аминоциклопропанкарбоновую кислоту (0,10 г, 0,00099 моль) в МеОН (3 мл) с 4 н. HCl (1,5 мл) перемешивали при комнатной температуре в течение 2 ч. LCMS анализ показал, что карбоновая кислота успешно конвертирована в метиловый эфир (m/z 116,3). Летучие продукты удаляли в вакууме, что дало 150 мг метилового эфира в виде соли с HCl. К этому метиловому эфиру добавляли 1-трет-бутил 3-этил 3(2-оксоэтил)пиперидин-1,3-дикарбоксилат (0,25 г, 0,00084 моль) и триэтиламин (190 мкл, 0,0013 моль) в 1,2-дихлорэтане (1,5 мл, 0,019 моль) и перемешивали при комнатной температуре в течение 30 мин. При перемешивании к смеси добавляли триацетоксиборогидрид натрия (0,35 г, 0,0017 моль). После перемешивания при комнатной температуре в течение 2 ч реакционную смесь нагревали до 70 С и перемешивали в течение 16 ч. Данные LCMS показали, что спиропродукт образовался и метиловый эфир гидролизован (m/z 283,0 (M-Bu + 2 Н)+). Реакционную смесь разбавляли этилацетатом и органический раствор промывали 1 н. HCl, водой, насыщенным солевым раствором и высушивали над Na2SO4. После фильтрования фильтрат концентрировали для получения 300 мг неочищенного вещества. Остаток перемешивали с раствором МеОН (2 мл) в 4 н. HCl-диоксановом растворе в течение 2 ч для образования метилового эфира. Летучие продукты удаляли в вакууме для получения 268 мг желаемого продукта. Это соединение получали с применением методик, аналогичных описанным для синтеза в примере 1, стадии 1-5, продолженных затем процедурой амин/арильного сочетания, индуцированного микроволновым излучением. Смесь гидрохлорида 2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она (5 мг,0,00002 моль), 2-хлор-5-(трифторметил)пиридина (6 мг, 0,00003 моль) и триэтиламина (20 мкл, 0,0001 моль) в N-метилпирролидиноне (800 мкл, 0,008 моль) облучали микроволновым излучением при 180 С в течение 10 мин. После охлаждения смесь очищали препаративной HPLC, что дало 1,7 мг желаемого продукта. Это соединение получали с применением методик, аналогичных тем, что описаны для синтеза в примере 27. Это соединение получали с применением методик, аналогичных описанным для синтеза в примере 1, стадии 1-5, продолженных затем процедурой амин/арильного сочетания, индуцированного микроволновым излучением. Смесь гидрохлорида 2-(транс-4-гидроксициклогексил)-2,7-диазаспиро[4.5]декан-1-она (35 мг,0,00012 моль), 2-бром-6-метоксипиридина (34 мг, 0,00018 моль), триэтиламина (200 мкл, 0,001 моль) и иодида меди(I) (28 мг, 0,00014 моль) в N-метилпирролидиноне (1,0 мл, 0,010 моль) облучали микроволновым излучением при 180 С в течение 20 мин. После самопроизвольного охлаждения реакционной смеси до комнатной температуры сырую смесь очищали препаративной HPLC, что дало 8,3 мг желаемого продукта. Это соединение получали с применением методик, аналогичных тем, что описаны для синтеза в примере 29. Это соединение получали с применением методик, аналогичных тем, что описаны для синтеза в примере 29. Это соединение получали с применением методик, аналогичных тем, что описаны для синтеза в примере 29. Это соединение получали с применением методик, аналогичных тем, что описаны для синтеза в примере 29. Это соединение получали хиральным разделением примера 27. Это соединение получали хиральным разделением примера 27. Это соединение получали с применением методик, аналогичных тем, что описаны для синтеза в примере 29. Это соединение получали с применением методик, аналогичных тем, что описаны для синтеза в примере 29. Это соединение получали с применением методик, аналогичных тем, что описаны для синтеза в примере 29.
МПК / Метки
МПК: C07D 471/10, A61K 31/438, C07D 221/20
Метки: качестве, лактамные, фармацевтических, препаратов, применение, соединения
Код ссылки
<a href="https://eas.patents.su/30-19747-laktamnye-soedineniya-i-ih-primenenie-v-kachestve-farmacevticheskih-preparatov.html" rel="bookmark" title="База патентов Евразийского Союза">Лактамные соединения и их применение в качестве фармацевтических препаратов</a>
Предыдущий патент: Противомикробная композиция, содержащая эвгенол, терпинеол и тимол, и способ дезинфицирования поверхности
Следующий патент: Антибактериальные композиции
Случайный патент: Энтомопатогенный препарат против личинок комаров на основештамма bacillus thuringiensis var. israelensis h-14 вкпм в-7572