Замещенные глицинамиды с антитромботическим и ингибирующим фактор хa действием
Номер патента: 15188
Опубликовано: 30.06.2011
Авторы: Герлах Кай, Пфау Роланд, Припке Хеннинг, Шулер-Метц Аннетте, Винен Вольфганг, Нар Герберт, Хандшух Зандра, Даманн Георг
Формула / Реферат
1. Соединения общей формулы (I)
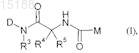
в которой D обозначает замещенную бициклическую систему формулы (II)
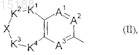
где K1и K4 независимо друг от друга обозначают -CH2-, -CHR7a-, -CR7bR7c- или -C(O)-группу, где
R7a, R7b, R7c независимо друг от друга обозначают атом фтора, гидроксигруппу, C1-C5-алкилоксигруппу, тетрагидрофуранил, оксетанил, аминогруппу, C1-C5-алкиламиногруппу, ди(C1-C5-алкил)аминогруппу, C3-C5-циклоалкилениминогруппу, C1-C5-алкилкарбониламиногруппу, C1-C5-алкил, который может быть замещен 1-3 атомами фтора, гидрокси-C1-C5-алкил, C1-C5-алкилокси-C1-C5-алкил, амино-C1-C5-алкил, C1-C5-алкиламино-C1-C5-алкил, ди(C1-C5-алкил)амино-C1-C5-алкил, C4-C7-циклоалкиленимино-C1-C5-алкил, карбокси-C0-C5-алкил, C1-C5-алкилоксикарбонил-C0-C5-алкил, аминокарбонил-C0-C5-алкил, C1-C5-алкиламинокарбонил-C0-C5-алкил, ди(C1-C5-алкил)аминокарбонил-C0-C5-алкил, C4-C7-циклоалкилениминокарбонил-C0-C5-алкил, фенил или 5- либо 6-членный гетероарил, который может быть замещен 1-2 заместителями, выбранными из нитрогруппы, аминогруппы, гидроксигруппы, метоксигруппы, цианогруппы, C1-C5-алкила и атомов фтора, хлора и брома,
при этом оба остатка R7b, R7c не могут быть одновременно присоединены через гетероатом к кольцевому атому углерода, за исключением случая, когда -C(R7bR7c)- соответствует -CF2-группе, или два остатка R7b, R7c совместно с кольцевым атомом углерода могут образовывать 3-, 4-, 5-, 6- либо 7-членный насыщенный карбоцикл или циклопентеновое, циклогексеновое, оксетановое, азетидиновое, тиетановое, тетрагидрофурановое, пирролидиновое, тетрагидротиофеновое, тетрагидропирановое, пиперидиновое, пентаметиленсульфидное, гексаметилениминовое, 1,3-диоксолановое, 1,4-диоксановое, гексагидропиридазиновое, пиперазиновое, тиоморфолиновое, морфолиновое, 2-имидазолидиноновое, 2-оксазолидиноновое, тетрагидро-2(1H)-пиримидиноновое либо [1,3]оксазинан-2-оновое кольцо, метиленовые группы которого могут быть замещены 1-2 C1-C3-алкильными или CF3-группами, и/или метиленовые группы которого, если они не присоединены к гетероатому, могут быть замещены 1-2 атомами фтора, и/или в котором -CH2-группа рядом с N-атомом может быть заменена на -CO-группу, и/или каждая из иминогрупп которого может быть замещена C1-C3-алкилом или C1-C3-алкилкарбонилом, и/или в котором атом серы может быть окислен до сульфоксида или сульфоновой группы;
K2 и K3независимо друг от друга обозначают -CH2-, -CHR8a-, -CR8bR8c- или -C(O)-группу, где
R8a, R8b, R8c независимо друг от друга обозначают C1-C5-алкил, который может быть замещен 1-3 атомами фтора, гидрокси-C1-C5-алкил, C1-C5-алкилокси-C1-C5-алкил, амино-C1-C5-алкил, C1-C5-алкиламино-C1-C5-алкил, ди(C1-C5-алкил)амино-C1-C5-алкил, C4-C7-циклоалкиленимино-C1-C5-алкил, карбокси-C0-C5-алкил, C1-C5-алкилоксикарбонил-C0-C5-алкил, аминокарбонил-C0-C5-алкил, C1-C5-алкиламинокарбонил-C0-C5-алкил, ди(C1-C5-алкил)аминокарбонил-C0-C5-алкил или C4-C7-циклоалкилениминокарбонил-C0-C5-алкил или два остатка R8b, R8cсовместно с кольцевым атомом углерода могут образовывать 3-, 4-, 5-, 6- либо 7-членный насыщенный карбоцикл или циклопентеновое, циклогексеновое, оксетановое, азетидиновое, тиетановое, тетрагидрофурановое, пирролидиновое, тетрагидротиофеновое, тетрагидропирановое, пиперидиновое, пентаметиленсульфидное, гексаметилениминовое, гексагидропиридазиновое, тетрагидро-2(1H)-пиримидиноновое либо [1,3]оксазинан-2-оновое кольцо, метиленовые группы которого могут быть замещены 1-2 C1-C3-алкильными или CF3-группами, и/или метиленовые группы которого, если они не присоединены к гетероатому, могут быть замещены 1-2 атомами фтора, и/или в котором -CH2-группа рядом с атомом азота может быть заменена на -CO-группу, и/или каждая из иминогрупп которого может быть замещена C1-C3-алкилом или C1-C3-алкилкарбонилом, и/или в котором атом серы может быть окислен до сульфоксида или сульфоновой группы,
при условии, что введенный в составе R8bили R8c гетероатом не может быть отделен от заместителя X в формуле (I) только одним атомом углерода и что в целом в формуле (II) могут присутствовать максимум четыре остатка, выбранных из R7a, R7b, R7c, R8a, R8b и R8c;
X обозначает атом кислорода либо серы, сульфеновую группу, сульфоновую группу или NR1-группу, в которой
R1 представляет собой атом водорода, гидроксигруппу, C1-C3-алкилоксигруппу, аминогруппу, C1-C3-алкиламиногруппу, ди(C1-C3-алкил)аминогруппу, C1-C5-алкил, C2-C5-алкенил-CH2-группу, C2-C5-алкинил-CH2-группу, C3-C6-циклоалкил, C4-C6-циклоалкенил, оксетан-3-ил, тетрагидрофуран-3-ил, бензил, C1-C5-алкилкарбонил, трифторметилкарбонил, C3-C6-циклоалкилкарбонил, C1-C5-алкилсульфонил, C3-C6-циклоалкилсульфонил, аминокарбонил, C1-C5-алкиламинокарбонил, ди(C1-C5-алкил)аминокарбонил, C1-C5-алкилоксикарбонил или C4-C7-циклоалкилениминокарбонил, при этом присутствующие в вышеуказанных группах метиленовые и метильные группы дополнительно могут быть замещены C1-C3-алкилом, карбоксигруппой либо C1-C5-алкоксикарбонилом или могут быть замещены гидроксигруппой, C1-C5-алкилоксигруппой, аминогруппой, C1-C5-алкиламиногруппой, C1-C5-диалкиламиногруппой либо C4-C7-циклоалкилениминогруппой, если такие метиленовые или метильные группы не присоединены непосредственно к гетероатому из группы, включающей O, N и S, и/или 1-3 атома водорода могут быть заменены на атомы фтора, если такие метиленовые или метильные группы не присоединены непосредственно к гетероатому из группы, включающей O, N и S;
A1 обозначает N или CR10;
A2 обозначает N или CR11;
A3 обозначает N или CR12, где
R10, R11 и R12 независимо друг от друга обозначают атом водорода, фтора, хлора, брома либо йода, C1-C5-алкил, CF3-группу, C2-C5-алкенил, C2-C5-алкинил, цианогруппу, карбоксигруппу, C1-C5-алкилоксикарбонил, гидроксигруппу, C1-C3-алкилоксигруппу, CF3O-группу, CHF2O-группу, CH2FO-группу, аминогруппу, C1-C5-алкиламиногруппу, ди(C1-C5-алкил)аминогруппу или C4-C7-циклоалкилениминогруппу, или
D представляет собой одну из четырех групп (II-1), (II-2), (II-3) и (II-4)
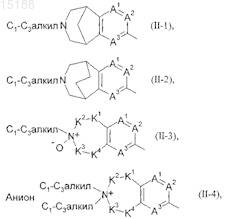
где остатки A1, A2, A3, K1, K2, K3, K4 имеют указанные выше значения;
Анион в группе формулы (II-4) обозначает фторид, хлорид, бромид, иодид, сульфат, гидросульфат, фосфат, гидрофосфат, бензоат, салицилат, сукцинат, цитрат или тартрат;
R3 обозначает атом водорода или C1-C3-алкил;
R4 и R5независимо друг от друга обозначают атом водорода, линейную либо разветвленную C1-C6-алкильную, C2-C6-алкенильную или C2-C6-алкинильную группу,
при этом атомы водорода метиленовых и/или метильных фрагментов линейной или разветвленной C1-C6-алкильной, C2-C6-алкенильной или C2-C6-алкинильной группы необязательно могут быть полностью или частично заменены на атомы фтора и/или один или два атома водорода линейной или разветвленной C1-C6-алкильной, C2-C6-алкенильной или C2-C6-алкинильной группы в ее метиленовых и/или метильных фрагментах необязательно могут быть независимо друг от друга заменены на C3-C7-циклоалкил, нитрил, гидроксигруппу, C1-C5-алкилоксигруппу, атомы водорода которой необязательно могут быть полностью или частично заменены атомами фтора, аллилоксигруппу, пропаргилоксигруппу, фенилметилоксигруппу, фенетилоксигруппу, C1-C5-алкилкарбонилоксигруппу, C1-C5-алкилоксикарбонилоксигруппу, карбокси-C1-C5-алкилоксигруппу, C1-C5-алкилоксикарбонил-C1-C5-алкилоксигруппу, C1-C5-алкилокси-C2-C5-алкилоксигруппу, меркаптогруппу, C1-C5-алкилсульфанил, C1-C5-алкилсульфинил, C1-C5-алкилсульфонил, карбоксигруппу, C1-C5-алкилоксикарбонил, аминокарбонил, C1-C5-алкиламинокарбонил, ди(C1-C5-алкил)аминокарбонил, C1-C5-алкиламинокарбонилоксигруппу, ди(C1-C5-алкил)аминокарбонилоксигруппу, C4-C7-циклоалкилениминокарбонил, аминосульфонил, C1-C5-алкиламиносульфонил, ди(C1-C5-алкил)аминосульфонил, C4-C7-циклоалкилениминосульфонил, ди(C1-C5-алкил)фосфорил, аминогруппу, C1-C5-алкиламиногруппу, ди(C1-C5-алкил)аминогруппу, C1-C5-алкилкарбониламиногруппу, трифторацетиламиногруппу, C1-C5-алкилокси-C1-C5-алкилкарбониламиногруппу, фенилкарбониламиногруппу, C1-C5-алкиламинокарбониламиногруппу, ди(C1-C5-алкил)аминокарбониламиногруппу, C1-C5-алкилоксикарбониламиногруппу, фенилметилоксикарбониламиногруппу, C1-C5-алкилокси-C2-C5-алкилокси-C1-C2-алкилкарбониламиногруппу, C1-C5-алкилсульфониламиногруппу, N-(C1-C5-алкилсульфонил)-C1-C5-алкиламиногруппу, C3-C6-циклоалкилкарбониламиногруппу, 4-морфолинокарбониламиногруппу, морфолинил, тиоморфолинил, пирролидинил, пиперидинил, пиперазинил, тетрагидрофуранил или тетрагидропиранил, где каждый из вышеуказанных карбо- и гетероциклов может быть замещен в кольце 1-4 C1-C3-алкильными или C1-C3-алкилкарбонильными группами или 1 или 2 оксогруппами и/или вышеуказанные фенильные и гетероарильные остатки могут быть заменены на 1 или 2 заместителя, выбранных из атомов фтора, хлора и брома, метила, метоксигруппы, аминогруппы и трифторметила, или два смежных атома углерода фенильного кольца могут быть замещены -CH2-O-CH2-группой и/или вышеуказанные алкильные группы могут быть замещены циано-C1-C5-алкилоксикарбонилом или карбоксигруппой, а вышеуказанные карбокс- или сульфонамиды необязательно дополнительно могут быть замещены у атома азота C1-C5-алкилом, и/или атомы водорода, соединенные с sp2-гибридизированными атомами углерода линейной или разветвленной C2-C6-алкенильной группы, необязательно могут быть полностью или частично заменены на атомы фтора,
или обозначают карбоксигруппу, аминокарбонил, C1-C5-алкиламинокарбонил, C3-C6-циклоалкиламинокарбонил, ди(C1-C5-алкил)аминокарбонил, C1-C5-алкилоксикарбонил, C4-C7-циклоалкилениминокарбонил либо фенильную, моно- либо бициклическую гетероарильную, фенил-C1-C5-алкильную или моно- либо бициклическую гетероарил-C1-C5-алкильную группу, при этом указанная группа в фенильной или гетероарильной части необязательно может быть одно-трехзамещенной идентичными или разными заместителями, выбранными из группы, включающей атомы фтора, хлора, брома и йода, C1-C5-алкил, трифторметил, бензил, аминогруппу, нитрогруппу, C1-C5-алкиламиногруппу, ди(C1-C5-алкил)аминогруппу, гидроксигруппу, C1-C5-алкилоксигруппу, моно-, ди- и трифторметоксигруппу, карбоксигруппу и C1-C5-алкилоксикарбонил, или два смежных атома углерода фенильного кольца могут быть замещены -CH2-O-CH2-группой, или обозначают C3-C7-циклоалкильную, морфолинильную, тиоморфолинильную, пирролидинильную, пиперидинильную, пиперазинильную, тетрагидрофуранильную либо тетрагидропиранильную группу, которая необязательно может быть замещена одним или двумя остатками, независимо друг от друга выбранными из C1-C3-алкила, ацетила, C1-C5-алкилоксикарбонила и гидроксикарбонила, или
R4 и R5совместно с атомом углерода, к которому они присоединены, образуют C3-C7-циклоалкильную или C5-C7-циклоалкенильную группу, при этом одна из метиленовых групп C4-C7-циклоалкильной группы может быть заменена на атом кислорода либо серы, -NH-группу, -N(C1-C5-алкил), -N(C1-C4-алкилкарбонил), -N(C1-C4-алкилоксикарбонил), карбонил, сульфинил или сульфонил и/или две непосредственно смежные друг с другом метиленовые группы C4-C7-циклоалкильной группы совместно могут быть заменены на
-C(O)NH-группу, -C(O)N(C1-C5-алкил), -S(O)2NH-группу или -S(O)2N(C1-C5-алкил) и/или 1-3 атома углерода C3-C7-циклоалкильной группы необязательно могут быть независимо друг от друга замещены соответственно одним либо двумя атомами фтора или одной либо двумя C1-C5-алкильными группами или гидроксигруппой, C1-C5-алкилоксигруппой, формилоксигруппой, C1-C5-алкилкарбонилоксигруппой, C1-C5-алкилсульфанилом, C1-C5-алкилсульфонилом, аминосульфонилом, C1-C5-алкиламиносульфонилом, ди(C1-C5-алкил)аминосульфонилом, C4-C7-циклоалкилениминосульфонилом, аминогруппой, C1-C5-алкиламиногруппой, ди(C1-C5-алкил)аминогруппой, C1-C5-алкилкарбониламиногруппой, C1-C5-алкилсульфониламиногруппой, N-(C1-C5-алкилсульфонил)-C1-C5-алкиламиногруппой, C3-C6-циклоалкилкарбониламиногруппой, нитрилом, карбокси-C1-C5-алкилом, C1-C5-алкилоксикарбонил-C1-C5-алкилом, карбоксигруппой, C1-C5-алкилоксикарбонилом, аминокарбонилом, C1-C5-алкиламинокарбонилом, ди(C1-C5-алкил)аминокарбонилом или C4-C7-циклоалкилениминокарбонилом и/или 1 либо 2 атома углерода C5-C7-циклоалкенильной группы необязательно могут быть независимо друг от друга замещены соответственно C1-C5-алкилом, нитрилом, карбокси-C1-C5-алкилом, C1-C5-алкилоксикарбонил-C1-C5-алкилом, карбоксигруппой, C1-C5-алкилоксикарбонилом, аминокарбонилом, C1-C5-алкиламинокарбонилом, ди(C1-C5-алкил)аминокарбонилом, C3-C6-циклоалкилениминокарбонилом, аминосульфонилом, C1-C5-алкиламиносульфонилом, ди(C1-C5-алкил)аминосульфонилом, C3-C6-циклоалкилениминосульфонилом или 1 либо 2 атомами фтора и/или 1 либо 2 атома углерода C4-C7-циклоалкенильной группы, которые соединены с другим атомом углерода не двойной связью, необязательно могут быть независимо друг от друга замещены гидроксигруппой, C1-C5-алкилоксигруппой, C1-C5-алкилкарбонилоксигруппой, C1-C5-алкилсульфанилом, C1-C5-алкилсульфонилом, аминогруппой, C1-C5-алкиламиногруппой, ди(C1-C5-алкил)аминогруппой, C1-C5-алкилкарбониламиногруппой, C1-C5-алкилсульфониламиногруппой, N-(C1-C5-алкилсульфонил)-C1-C5-алкиламиногруппой или C3-C6-циклоалкилкарбониламиногруппой, при условии, что подобная, образованная совместно остатками R4 и R5 C3-C7-циклоалкильная или C5-C7-циклоалкенильная группа, в которой 2 гетероатома в цикле из группы, включающей атом кислорода и атом азота, отделены друг от друга точно одной необязательно замещенной -CH2-группой и/или одна или обе метиленовые группы цикла, которые непосредственно соединены с атомом углерода, к которому присоединены остатки R4и R5, заменены на гетероатом из группы, включающей атом кислорода, атом азота и атом серы, и/или присоединенный к циклической группе заместитель, который отличается тем, что гетероатом из группы, включающей атом кислорода, атом азота, атом серы и атом фтора, непосредственно присоединен к циклической группе, отделен от другого гетероатома из группы, включающей атом кислорода, атом азота и атом серы, за исключением сульфоновой группы, точно одной необязательно замещенной метиленовой группой и/или два атома в кольце образуют -O-O- или -S-O-связь, исключена из объема изобретения;
M представляет собой тиофеновое кольцо формулы (III)
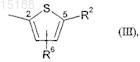
которое через положение 2 присоединено к карбонильной группе в формуле (I) и в положении 5 замещено остатком R2 и необязательно дополнительно замещено остатком R6 и в котором
R2 обозначает атом водорода, фтора, хлора, брома либо йода, метоксигруппу, C1-C2-алкил, формил, NH2CO-группу или этинил;
R6 обозначает атом водорода, фтора, хлора, брома либо йода, C1-C2-алкил или аминогруппу,
при этом под упомянутым выше в определениях заместителей выражением "гетероарильная группа" или "гетероарил" подразумевается, если не указано иное, моноциклическая 5- или 6-членная гетероарильная группа, которая, если она является 6-членной, содержит один, два или три атома азота, а если является 5-членной, либо содержит необязательно замещенную C1-C3-алкилом иминогруппу, атом кислорода или серы, либо содержит необязательно замещенную C1-C3-алкилом иминогруппу или атом кислорода или серы и дополнительно один или два атома азота, либо содержит необязательно замещенную C1-C3-алкилом иминогруппу и три атома азота и с которой, кроме того, через два смежных атома углерода может быть сконденсировано необязательно замещенное атомом фтора, хлора либо брома, C1-C3-алкилом, гидроксигруппой, C1-C3-алкилоксигруппой, аминогруппой, C1-C3-алкиламиногруппой, ди(C1-C3-алкил)аминогруппой или C3-C6-циклоалкилениминогруппой фенильное кольцо и которая далее присоединена через атом азота или через атом углерода гетероциклической части или сконденсированного фенильного кольца, под упомянутым выше в определениях заместителей выражением "атом галогена" подразумевается, если не указано иное, атом из группы, включающей фтор, хлор, бром и йод, упомянутые выше в определениях заместителей алкильные, алкенильные, алкинильные и алкилоксигруппы, содержащие более двух атомов углерода, могут, если не указано иное, иметь прямую или разветвленную цепь, а алкильные группы в указанных выше диалкилированных остатках, например диалкиламиногруппах, могут быть идентичными или разными и атомы водорода упомянутых выше в определении заместителей метильных или этильных групп могут быть, если не указано иное, полностью или частично заменены на атомы фтора,
их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли.
2. Соединения общей формулы (I) по п.1, где
D обозначает замещенную бициклическую систему формулы (II)
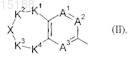
в которой K1 и K4независимо друг от друга обозначают -CH2-, -CHR7a-, -CR7bR7c- или -C(O)-группу, где
R7a, R7b, R7c независимо друг от друга обозначают атом фтора, гидроксигруппу, C1-C5-алкилоксигруппу, C1-C5-алкил, который может быть замещен 1-3 атомами фтора, гидрокси-C1-C5-алкил, C1-C5-алкилокси-C1-C5-алкил, фенил, который может быть замещен 1-2 заместителями, выбранными из нитрогруппы, аминогруппы, гидроксигруппы, метоксигруппы, цианогруппы, C1-C5-алкила и атомов фтора, хлора и брома, или 5- либо 6-членную гетероарильную группу,
при этом оба остатка R7b, R7c не могут быть одновременно присоединены через гетероатом к кольцевому атому углерода, за исключением случая, когда -C(R7bR7c)- соответствует -CF2-группе, или
два остатка R7b, R7c совместно с кольцевым атомом углерода могут образовывать 3-, 4-, 5-, 6- либо 7-членный насыщенный карбоцикл или циклопентеновое, циклогексеновое, оксетановое, тетрагидрофурановое либо тетрагидропирановое кольцо, метиленовые группы которого могут быть замещены 1 или 2 C1-C3-алкильными группами или CF3-группами и/или метиленовые группы которого, если они не присоединены к гетероатому, могут быть замещены 1 или 2 атомами фтора;
K2 и K3независимо друг от друга обозначают -CH2-, -CHR8a-, -CR8bR8c- или -C(O)-группу, где
R8a, R8b, R8c независимо друг от друга обозначают C1-C5-алкил, который может быть замещен 1-3 атомами фтора, гидрокси-C1-C5-алкил или C1-C5-алкилокси-C1-C5-алкил или
два остатка R8b, R8c совместно с кольцевым атомом углерода могут образовывать 3-, 4-, 5-, 6- либо 7-членный карбоцикл или циклопентеновое, циклогексеновое, оксетановое, тетрагидрофурановое либо тетрагидропирановое кольцо, метиленовые группы которого могут быть замещены 1 или 2 C1-C3-алкильными группами или CF3-группами и/или метиленовые группы которого, если они не присоединены к гетероатому, могут быть замещены 1 или 2 атомами фтора,
при условии, что введенный в составе R8bили R8c гетероатом не может быть отделен от заместителя X в формуле (I) только одним атомом углерода и что в целом в формуле (II) могут присутствовать максимум четыре остатка, выбранных из R7a, R7b, R7c, R8a, R8b и R8c;
X обозначает атом кислорода либо серы, сульфеновую группу, сульфоновую группу или NR1-группу, в которой
R1 представляет собой атом водорода, C1-C5-алкил, C2-C5-алкенил-CH2-группу, C2-C5-алкинил-CH2-группу, C3-C6-циклоалкил, C4-C6-циклоалкенил, оксетан-3-ил, тетрагидрофуран-3-ил, бензил, C1-C5-алкилкарбонил, трифторметилкарбонил, C3-C6-циклоалкилкарбонил, C1-C5-алкилсульфонил, C3-C6-циклоалкилсульфонил, аминокарбонил, C1-C5-алкиламинокарбонил, ди(C1-C5-алкил)аминокарбонил, C1-C5-алкилоксикарбонил или C4-C7-циклоалкилениминокарбонил, при этом присутствующие в вышеуказанных группах метиленовые и метильные группы дополнительно могут быть замещены C1-C3-алкилом, карбоксигруппой или C1-C5-алкоксикарбонилом либо могут быть замещены гидроксигруппой, C1-C5-алкилоксигруппой, аминогруппой, C1-C5-алкиламиногруппой, C1-C5-диалкиламиногруппой или C4-C7-циклоалкилениминогруппой, если такие метиленовые или метильные группы не присоединены непосредственно к гетероатому из группы, включающей O, N и S, и/или 1-3 атома водорода могут быть заменены на атомы фтора, если такие метиленовые или метильные группы не присоединены непосредственно к гетероатому из группы, включающей O, N и S;
A1, A2и A3 имеют указанные для каждого из них в п.1 значения, или
D представляет собой одну из четырех групп (II-1а), (II-2а), (II-3) или (II-4)
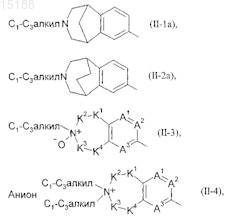
где остатки A1, A2, A3, K1, K2, K3, K4 имеют указанные выше значения;
Анион в группе формулы (II-4) обозначает фторид, хлорид, бромид, иодид, сульфат, гидросульфат, фосфат, гидрофосфат, бензоат, салицилат, сукцинат, цитрат или тартрат;
R3 обозначает атом водорода;
R4, R5и M имеют указанные для каждого из них в п.1 значения,
их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли.
3. Соединения общей формулы (I) по п.1 или 2, где
D обозначает замещенную бициклическую систему формулы (II)
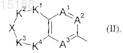
где K1, K2, K3и K4 имеют указанные для них в п.1 или 2 значения;
X обозначает NR1-группу, в которой
R1 представляет собой атом водорода, C1-C5-алкил, C2-C5-алкенил-CH2-группу, C2-C5-алкинил-CH2-группу, C3-C6-циклоалкил или C4-C6-циклоалкенил, при этом присутствующие в вышеуказанных группах метиленовые и метильные группы дополнительно могут быть замещены C1-C3-алкилом, карбоксигруппой или C1-C5-алкоксикарбонилом либо могут быть замещены гидроксигруппой, C1-C5-алкилоксигруппой, аминогруппой, C1-C5-алкиламиногруппой, C1-C5-диалкиламиногруппой или C4-C7-циклоалкилениминогруппой, если такие метиленовые или метильные группы не присоединены непосредственно к гетероатому из группы, включающей O, N и S, и/или 1-3 атома водорода могут быть заменены на атомы фтора, если такие метиленовые или метильные группы не присоединены непосредственно к атому азота;
A1 обозначает N или CR10;
A2 обозначает N или CR11;
A3 обозначает N или CR12, где
R10, R11 и R12 независимо друг от друга обозначают атом водорода, фтора, хлора либо брома, C1-C5-алкил, CF3-группу, цианогруппу, карбоксигруппу, C1-C5-алкилоксикарбонил, гидроксигруппу, C1-C3-алкилоксигруппу, CF3O-группу, CHF2O-группу или CH2FO-группу, или
D представляет собой одну из четырех групп (II-1а), (II-2а), (II-3) или (II-4)

где остатки A1, A2, A3, K1, K2, K3, K4 имеют указанные выше значения;
Анион в группе формулы (II-4) может быть выбран из группы, включающей фторид, хлорид, бромид, иодид, сульфат, фосфат, бензоат, салицилат, сукцинат, цитрат и тартрат;
R3, R4, R5 и M имеют указанные для каждого из них в п.1 или 2 значения, при этом R6 представляет собой атом водорода,
их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли.
4. Соединения общей формулы (I) по одному из пп.1-3, где
D, R3 и M имеют указанные для каждого из них в одном из пп.1-3 значения;
R4 обозначает линейную либо разветвленную C3-C6-алкенильную либо C3-C6-алкинильную группу, линейную либо разветвленную C1-C6-алкильную группу, атомы водорода которой необязательно могут быть полностью или частично заменены на атомы фтора и в которой один или два атома водорода необязательно могут быть независимо друг от друга заменены на C3-C7-циклоалкил, гидроксигруппу, C1-C5-алкилоксигруппу, фенилметилоксигруппу, фенетилоксигруппу, карбокси-C1-C5-алкилоксигруппу, C1-C5-алкилоксикарбонил-C1-C5-алкилоксигруппу, C1-C5-алкилокси-С2-С5алкилоксигруппу, C1-C5-алкилсульфанил, C1-C5-алкилсульфинил, C1-C5-алкилсульфонил, карбоксигруппу, C1-C5-алкилоксикарбонил, аминокарбонил, C1-C5-алкиламинокарбонил, ди(C1-C5-алкил)аминокарбонил, C1-C5-алкиламинокарбонилоксигруппу, ди(C1-C5-алкил)аминокарбонилоксигруппу, C4-C7-циклоалкилениминокарбонил, аминогруппу, C1-C5-алкиламиногруппу, ди(C1-C5-алкил)аминогруппу, C1-C5-алкилкарбониламиногруппу, трифторацетиламиногруппу, C1-C5-алкилокси-C1-C5-алкилкарбониламиногруппу, фенилкарбониламиногруппу, C1-C5-алкиламинокарбониламиногруппу, ди(C1-C5-алкил)аминокарбониламиногруппу, C1-C5-алкилоксикарбониламиногруппу, фенилметилоксикарбониламиногруппу, C1-C5-алкилокси-C2-C5-алкилокси-C1-C2-алкилкарбониламиногруппу, C1-C5-алкилсульфониламиногруппу, C3-C6-циклоалкилкарбониламиногруппу или 4-морфолинокарбониламиногруппу,
где каждый из вышеуказанных карбо- и гетероциклов может быть замещен в кольце 1-4 C1-C3-алкильными либо C1-C3-алкилкарбонильными группами или 1 или 2 оксогруппами и/или вышеуказанные фенильные и гетероарильные остатки могут быть заменены на 1 или 2 заместителя, выбранных из фтора, хлора, брома, метила, метоксигруппы и трифторметила, или два смежных атома углерода фенильного кольца могут быть замещены -CH2-O-CH2-группой и/или вышеуказанные алкильные группы могут быть замещены циано-C1-C5-алкилоксикарбонилом или карбоксигруппой, а вышеуказанные карбокс- или сульфонамиды необязательно дополнительно могут быть замещены у атома азота C1-C5-алкилом,
или обозначает фенильную, фенил-C1-C2-алкильную, гетероарил-C1-C2-алкильную или C-связанную гетероарильную группу, где гетероарильная группа выбрана из группы, включающей имидазолил, фуранил, тиофенил, тиазолил, пиразолил, тетразолил, бензимидазолил, индолил, пиримидинил, пиразинил, оксазолил, 1,2,4-триазолил и пиридинил, и где указанная группа в фенильной или гетероарильной части необязательно может быть одно- или двузамещена одинаковыми или разными заместителями, выбранными из атомов хлора и фтора, C1-C3-алкила, бензила, гидроксигруппы, аминогруппы, CF3-группы, CH3O-группы и CHF2O-группы;
R5 обозначает атом водорода, линейную либо разветвленную C1-C4-алкильную группу, атомы водорода которой необязательно могут быть полностью или частично заменены на атомы фтора, или обозначает пропаргил или C1-C3-алкилокси-C1-C3-алкил или
R4 и R5совместно с атомом углерода, к которому они присоединены, образуют C5-C6-циклоалкенильную или C3-C7-циклоалкильную группу, при этом одна из метиленовых групп C4-C7-циклоалкильной группы может быть заменена на атом кислорода либо серы, -NH-группу, -N(C1-C5-алкил), -N(C1-C4-алкилкарбонил), карбонил, сульфинил или сульфонил или две непосредственно смежные друг с другом метиленовые группы C4-C7-циклоалкильной группы совместно могут быть заменены на -C(O)NH-группу, -C(O)N(C1-C5-алкил),
-S(O)2NH-группу или -S(O)2N(C1-C5-алкил) и/или 1 или 2 атома углерода C3-C7-циклоалкильной группы необязательно могут быть независимо друг от друга замещены соответственно одним или двумя атомами фтора или одной или двумя C1-C5-алкильными группами либо гидроксигруппой, C1-C5-алкилоксигруппой, формилоксигруппой, аминогруппой, C1-C5-алкиламиногруппой, ди(C1-C5-алкил)аминогруппой, C1-C5-алкилкарбониламиногруппой, C3-C6-циклоалкилкарбониламиногруппой, нитрилом, карбоксигруппой, C1-C5-алкилоксикарбонилом, аминокарбонилом, C1-C5-алкиламинокарбонилом, ди(C1-C5-алкил)аминокарбонилом или C4-C7-циклоалкилениминокарбонилом, при условии, что подобная, образованная совместно остатками R4 и R5 C3-C7-циклоалкильная группа, в которой два гетероатома в цикле из группы, включающей атом кислорода и атом азота, отделены друг от друга точно одной необязательно замещенной -CH2-группой и/или одна или обе метиленовые группы цикла, которые непосредственно соединены с атомом углерода, к которому присоединены остатки R4и R5, заменены на гетероатом из группы, включающей атом кислорода, атом азота и атом серы, и/или присоединенный к циклической группе заместитель, который отличается тем, что гетероатом из группы, включающей атом кислорода, атом азота, атом серы и атом фтора, непосредственно присоединен к циклической группе, отделен от другого гетероатома из группы, включающей атом кислорода, атом азота и атом серы, точно одной необязательно замещенной метиленовой группой и/или два атома в кольце образуют -O-O- или -S-O-связь, исключена из объема изобретения,
их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли.
5. Соединения общей формулы (I) по одному из пп.1-4, где
D обозначает замещенную бициклическую систему формулы (II)
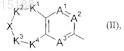
где K1и K4 независимо друг от друга обозначают -CH2-, -CHR7a- или -CR7bR7c-группу, где
R7a, R7b, R7c независимо друг от друга обозначают C1-C2-алкил или фенил, который может быть замещен 1 или 2 заместителями, выбранными из нитрогруппы, аминогруппы, гидроксигруппы, метоксигруппы, цианогруппы, C1-C5-алкила, атома фтора, атома хлора и атома брома;
K2 и K3, каждый, обозначают -CH2-группу;
X обозначает NR1-группу, в которой
R1 представляет собой атом водорода, C1-C5-алкил, C2-C4-алкенил-CH2-группу, C2-C4-алкинил-CH2-группу или C3-C6-циклоалкил, при этом присутствующие в вышеуказанных C2-C5-алкильных группах метиленовые и метильные группы могут быть замещены 1-3 атомами фтора, если такие метиленовые или метильные группы не присоединены непосредственно к атому азота;
A1 обозначает N или CR10;
A2 обозначает N или CR11;
A3 обозначает N или CR12, где
R10, R11 и R12 независимо друг от друга обозначают атом водорода, фтора либо хлора, C1-C3-алкил, CF3-группу, гидроксигруппу или CH3O-группу, или
D обозначает одну из групп (II-3) или (II-4)
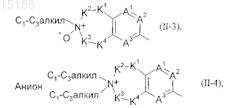
где остатки A1, A2, A3, K1, K2, K3, K4 имеют указанные выше значения;
Анион в группе формулы (II-4) может быть выбран из группы, включающей фторид, хлорид, бромид, иодид, сульфат, фосфат, бензоат, салицилат, сукцинат, цитрат и тартрат;
R3 обозначает атом водорода;
R4 обозначает линейную либо разветвленную C3-C6-алкенильную или C3-C6-алкинильную группу, линейную либо разветвленную C1-C4-алкильную группу, атомы водорода которой необязательно частично могут быть заменены на один-четыре атома фтора и в которой один или два атома водорода необязательно могут быть независимо друг от друга заменены на C3-C7-циклоалкил, гидроксигруппу, C1-C5-алкилоксигруппу, фенилметилоксигруппу, C1-C5-алкилсульфанил, C1-C5-алкилсульфинил, C1-C5-алкилсульфонил, карбоксигруппу, C1-C5-алкилоксикарбонил, аминокарбонил, C1-C5-алкиламинокарбонил, ди(C1-C5-алкил)аминокарбонил, C4-C7-циклоалкилениминокарбонил, аминогруппу, C1-C5-алкиламиногруппу, ди(C1-C5-алкил)аминогруппу, C1-C5-алкилкарбониламиногруппу, карбокси-C1-C5-алкилкарбониламиногруппу или C1-C5-алкилоксикарбонил-C1-C5-алкилкарбониламиногруппу,
где вышеуказанные фенильные остатки могут быть заменены на 1 или 2 заместителя, выбранных из фтора, хлора, брома, метила, метоксигруппы и трифторметила, или вышеуказанные карбоксамиды необязательно дополнительно могут быть замещены у атома азота C1-C5-алкилом,
или обозначает фенильную, фенил-C1-C2-алкильную, гетероарил-C1-C2-алкильную или C-связанную гетероарильную группу, при этом гетероарильная группа выбрана из группы, включающей имидазолил, фуранил, тиофенил, тиазолил, пиразолил, тетразолил, бензимидазолил, индолил, пиримидинил, пиразинил, оксазолил и пиридинил, и указанная группа необязательно может быть одно- или двузамещена в фенильной или гетероарильной части одинаковыми или разными заместителями, выбранными из атомов хлора и фтора, C1-C3-алкила, CF3-группы, HO-группы, CH3O-группы и CHF2O-группы;
R5 обозначает атом водорода, линейную либо разветвленную C1-C4-алкильную группу, пропаргил или C1-C3-алкилокси-C1-C3-алкил или
R4 и R5совместно с атомом углерода, к которому они присоединены, образуют C5-C6-циклоалкенильную или C3-C7-циклоалкильную группу, при этом одна из метиленовых групп C4-C7-циклоалкильной группы может быть заменена на атом кислорода либо серы или сульфонил или 1 или 2 атома углерода C3-C7-циклоалкильной группы необязательно могут быть независимо друг от друга замещены соответственно одним или двумя атомами фтора или одной или двумя C1-C5-алкильными группами либо гидроксигруппой, C1-C5-алкилоксигруппой, формилоксигруппой, нитрилом, карбоксигруппой, C1-C5-алкилоксикарбонилом, аминокарбонилом, C1-C5-алкиламинокарбонилом, ди(C1-C5-алкил)аминокарбонилом или C4-C7-циклоалкилениминокарбонилом, при условии, что подобная, образованная совместно остатками R4 и R5 C3-C7-циклоалкильная группа, в которой одна из метиленовых групп цикла, которая непосредственно соединена с атомом углерода, к которому присоединены остатки R4 и R5, заменена на атом кислорода либо серы, исключена из объема изобретения;
M представляет собой тиофеновое кольцо формулы (III)
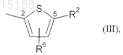
которое через положение 2 присоединено к карбонильной группе в формуле (I) и в положении 5 замещено остатком R2 и в котором
R2 обозначает атом хлора либо брома или этинил;
R6 обозначает атом водорода,
при этом упомянутые выше в определениях заместителей алкильные, алкенильные, алкинильные и алкилоксигруппы, содержащие более двух атомов углерода, могут, если не указано иное, иметь прямую или разветвленную цепь, а алкильные группы в указанных выше диалкилированных остатках, например диалкиламиногруппах, могут быть идентичными или разными,
их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли.
6. Соединения общей формулы (I) по одному из пп.1-5, где
D обозначает замещенную бициклическую систему формулы (II)
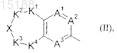
где K1и K4 независимо друг от друга обозначают -CH2-, -CHR7a- или -CR7bR7c-группу, где
R7a, R7b, R7c независимо друг от друга обозначают C1-C2-алкил;
K2 и K3, каждый, обозначают -CH2-группу;
X обозначает NR1-группу, в которой
R1 представляет собой атом водорода или C1-C5-алкильную либо C3-C6-циклоалкильную группу, при этом в присутствующих в вышеуказанных группах метиленовых и метильных группах 1-3 атома водорода могут быть заменены на атомы фтора, если такие метиленовые или метильные группы не присоединены непосредственно к атому азота;
А1 обозначает CR10;
А2 обозначает CR11;
А3 обозначает CR12, где
R10, R11 и R12 независимо друг от друга обозначают атом водорода, фтора либо хлора, C1-C3-алкил, CF3-группу, HO-группу или CH3O-группу, или
D обозначает группу (II-4)
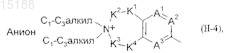
где остатки A1, A2, A3, K1, K2, K3, K4 имеют указанные выше значения;
Анион может быть выбран из группы, включающей фторид, хлорид, бромид, иодид, сульфат, фосфат, бензоат, салицилат, сукцинат, цитрат и тартрат,
их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли.
7. Соединения общей формулы (I) по одному из пп.1-6, в которых ни R4, ни R5 не могут обозначать атом водорода, их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли.
8. Соединения общей формулы (I) по одному из пп.1-6, в которых R4 и R5 совместно с атомом углерода, к которому они присоединены, образуют C5-C6-циклоалкенильную или C3-C7-циклоалкильную группу, при этом одна из метиленовых групп C4-C7-циклоалкильной группы может быть заменена на атом кислорода либо серы, при условии, что подобная, образованная совместно остатками R4и R5 C3-C7-циклоалкильная группа, в которой одна из метиленовых групп цикла, которая непосредственно соединена с атомом углерода, к которому присоединены остатки R4и R5, заменена на атом кислорода либо серы, исключена из объема изобретения, их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли.
9. Соединение общей формулы (I) по п.1, выбранное из группы, включающей
амид 3-[(5-бромтиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ил)тетрагидрофуран-3-карбоновой кислоты,
амид 3-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ил)тетрагидрофуран-3-карбоновой кислоты,
N-[1-(3-этил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)-1-метилэтил]амид 5-хлортиофен-2-карбоновой кислоты,
амид 5-этинил-N-[1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]тиофен-2-карбоновой кислоты,
N-[1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5-хлортиофен-2-карбоновой кислоты,
N-[1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5-бромтиофен-2-карбоновой кислоты,
N-[2-метокси-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5-хлортиофен-2-карбоновой кислоты,
амид 1-[(5-бромтиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ил)циклопентан-1-карбоновой кислоты,
амид 1-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ил)циклопентан-1-карбоновой кислоты,
амид 3-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ил)тетрагидротиофен-3-карбоновой кислоты,
амид 1-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ил)циклобутан-1-карбоновой кислоты,
амид 1-[(5-бромтиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ил)циклопент-3-ен-1-карбоновой кислоты,
амид 1-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ил)циклогексан-1-карбоновой кислоты,
N-[2-бензилокси-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
N-[2-бензилокси-1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5-хлортиофен-2-карбоновой кислоты,
N-[2-гидрокси-1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
N-[3-гидрокси-1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)пропил]амид 5-бромтиофен-2-карбоновой кислоты,
N-[1-метил-3-диметиламинокарбонил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)пропил]амид 5-хлортиофен-2-карбоновой кислоты,
N-[2-(4-гидроксифенил)-1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил] амид 5-хлортиофен-2-карбоновой кислоты,
N-[1-метил-1-(3,5-диметил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5-хлортиофен-2-карбоновой кислоты,
N-{1-метил-1-[3-метил-5-(4-аминофенил)-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил]этил}амид 5-хлортиофен-2-карбоновой кислоты,
N-[2-этокси-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5-хлортиофен-2-карбоновой кислоты,
N-[3-метокси-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)пропил]амид 5-хлортиофен-2-карбоновой кислоты,
N-[2-изопропилокси-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5-хлортиофен-2-карбоновой кислоты,
N-[3-бензилокси-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)пропил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
амид 1-[(5-хлортиофен-2-ил)карбониламино]-3,4-диметокси-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ил)циклопентан-1-карбоновой кислоты,
N-[C-(1-метилпиразол-3-ил)-C-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)метил]амид 5-хлортиофен-2-карбоновой кислоты,
N-[2-фенил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
N-[2-(фуран-2-ил)-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
N-[2-(4-метоксифенил)-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5-хлортиофен-2-карбоновой кислоты,
N-[2-(4-гидрокси-3-нитрофенил)-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил] амид 5-хлортиофен-2-карбоновой кислоты,
N-[2-(4-гидроксифенил)-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
N-[2-циклогексил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
N-[3-аминокарбонил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)пропил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
N-[2-ацетиламино-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
N-[2-бензоиламино-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-бромтиофен-2-карбоновой кислоты,
N-[2-(2-гидроксикарбонилэтил)карбониламино-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
N-[2-(2-гидроксикарбонилэтил)карбониламино-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
N-[2-(4-метоксикарбонилбутил)карбониламино-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5-хлортиофен-2-карбоновой кислоты,
иодид N-[1-метил-1-(3,3-диметил-2,3,4,5-тетрагидро-1H-бензо[d]азепиний-7-илкарбамоил)этил]амида 5-хлортиофен-2-карбоновой кислоты,
амид 3-[(5-хлортиофен-2-ил)карбониламино]-N-(3,5-диметил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-ил)тетрагидрофуран-3-карбоновой кислоты и
их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли.
10. Физиологически совместимые соли соединений по одному из пп.1-9.
11. Лекарственное средство, содержащее соединение по одному из пп.1-9 или физиологически совместимую соль по п.10 и необязательно один или несколько инертных носителей и/или разбавителей.
12. Применение соединения по одному из пп.1-9 или физиологически совместимой соли по п.10 для приготовления лекарственного средства, обладающего ингибирующим действием на фактор Xa и/или на родственные серинпротеазы.
13. Способ приготовления лекарственного средства по п.11, отличающийся тем, что соединение по одному из пп.1-9 или физиологически совместимую соль по п.10 не химическим путем объединяют с одним или несколькими инертными носителями и/или разбавителями.
Текст
В изобретении описаны новые, обладающие ценными свойствами замещенные глицинамиды общей формулы (I) в которой D, M, R3, R4 и R5 имеют указанные в описании изобретения значения, их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли, прежде всего их физиологически совместимые соли с неорганическими или органическими кислотами или основаниями.(71)(73) Заявитель и патентовладелец: БРИНГЕР ИНГЕЛЬХАЙМ ИНТЕРНАЦИОНАЛЬ ГМБХ (DE) 015188 Настоящее изобретение относится к новым, обладающим ценными свойствами замещенным глицинамидам общей формулы (I) их таутомерам, их энантиомерам, их диастереомерам, их смесям и их солям, прежде всего их физиологически совместимым солям с неорганическими или органическими кислотами или основаниями. Соединения приведенной выше общей формулы (I), а также их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли, прежде всего их физиологически совместимые соли с неорганическими или органическими кислотами или основаниями, и их стереоизомеры обладают ценными фармакологическими свойствами, прежде всего антитромботическим действием и ингибирующим действием на фактор Xa. Объектами настоящего изобретения являются в соответствии с этим новые соединения приведенной выше общей формулы (I), их получение, содержащие эти фармакологически активные соединения лекарственные средства, их получение и применение. В 1-м варианте осуществления настоящего изобретения предлагаются соединения общей формулыD обозначает замещенную бициклическую систему формулы (II) в которой K1 и K4 независимо друг от друга обозначают -CH2-, -CHR7a-, -CR7bR7c- или -C(O)-группу, гдеR7a, R7b, R7c независимо друг от друга обозначают атом фтора, гидроксигруппу, C1-C5 алкилоксигруппу, тетрагидрофуранил, оксетанил, аминогруппу, C1-C5-алкиламиногруппу, ди(C1-C5 алкил)аминогруппу, C3-C5-циклоалкилениминогруппу, C1-C5-алкилкарбониламиногруппу, C1-C5-алкил,который может быть замещен 1-3 атомами фтора, гидрокси-C1-C5-алкил, C1-C5-алкилокси-C1-C5-алкил,амино-C1-C5-алкил,C1-C5-алкиламино-C1-C5-алкил,ди(C1-C5-алкил)амино-C1-C5-алкил,C4-C7 циклоалкиленимино-C1-C5-алкил, карбокси-C0-C5-алкил, C1-C5-алкилоксикарбонил-C0-C5-алкил, аминокарбонил-C0-C5-алкил, C1-C5-алкиламинокарбонил-C0-C5-алкил, ди(C1-C5-алкил)аминокарбонил-C0-C5 алкил, C4-C7-циклоалкилениминокарбонил-C0-C5-алкил, фенил или 5- либо 6-членный гетероарил, который может быть замещен 1-2 заместителями, выбранными из нитрогруппы, аминогруппы, гидроксигруппы, метоксигруппы, цианогруппы, C1-C5-алкила и атомов фтора, хлора и брома,при этом оба остатка R7b, R7c не могут быть одновременно присоединены через гетероатом к кольцевому атому углерода, за исключением случая, когда -C(R7bR7c)- соответствует -CF2-группе, или два остатка R7b, R7c совместно с кольцевым атомом углерода могут образовывать 3-, 4-, 5-, 6- либо 7-членный насыщенный карбоцикл или циклопентеновое, циклогексеновое, оксетановое, азетидиновое, тиетановое,тетрагидрофурановое, пирролидиновое, тетрагидротиофеновое, тетрагидропирановое, пиперидиновое,пентаметиленсульфидное, гексаметилениминовое, 1,3-диоксолановое, 1,4-диоксановое, гексагидропиридазиновое,пиперазиновое,тиоморфолиновое,морфолиновое,2-имидазолидиноновое,2 оксазолидиноновое, тетрагидро-2(1H)-пиримидиноновое либо [1,3]оксазинан-2-оновое кольцо, метиленовые группы которого могут быть замещены 1-2 C1-C3-алкильными или CF3-группами, и/или метиленовые группы которого, если они не присоединены к гетероатому, могут быть замещены 1-2 атомами фтора, и/или в котором -CH2-группа рядом с N-атомом может быть заменена на -CO-группу, и/или каждая из иминогрупп которого может быть замещена C1-C3-алкилом или C1-C3-алкилкарбонилом, и/или в котором атом серы может быть окислен до сульфоксида или сульфоновой группы;K2 и K3 независимо друг от друга обозначают -CH2-, -CHR8a-, -CR8bR8c- или -C(O)-группу, гдеR8a, R8b, R8c независимо друг от друга обозначают C1-C5-алкил, который может быть замещен 1-3 атомами фтора, гидрокси-C1-C5-алкил, C1-C5-алкилокси-C1-C5-алкил, амино-C1-C5-алкил, C1-C5 алкиламино-C1-C5-алкил, ди(C1-C5-алкил)амино-C1-C5-алкил, C4-C7-циклоалкиленимино-C1-C5-алкил,карбокси-C0-C5-алкил, C1-C5-алкилоксикарбонил-C0-C5-алкил, аминокарбонил-C0-C5-алкил, C1-C5 алкиламинокарбонил-C0-C5-алкил, ди(C1-C5-алкил)аминокарбонил-C0-C5-алкил или C4-C7-циклоалкилениминокарбонил-C0-C5-алкил или два остатка R8b, R8c совместно с кольцевым атомом углерода могут образовывать 3-, 4-, 5-, 6- либо 7-членный насыщенный карбоцикл или циклопентеновое, циклогексеновое, оксетановое, азетидиновое,тиетановое, тетрагидрофурановое, пирролидиновое, тетрагидротиофеновое, тетрагидропирановое, пиперидиновое, пентаметиленсульфидное, гексаметилениминовое, гексагидропиридазиновое, тетрагидро 2(1H)-пиримидиноновое либо [1,3]оксазинан-2-оновое кольцо, метиленовые группы которого могут быть замещены 1-2 C1-C3-алкильными или CF3-группами, и/или метиленовые группы которого, если они не присоединены к гетероатому, могут быть замещены 1-2 атомами фтора, и/или в котором -CH2-группа рядом с атомом азота может быть заменена на -CO-группу, и/или каждая из иминогрупп которого может-1 015188 быть замещена C1-C3-алкилом или C1-C3-алкилкарбонилом, и/или в котором атом серы может быть окислен до сульфоксида или сульфоновой группы,при условии, что введенный в составе R8b или R8c гетероатом не может быть отделен от заместителяX в формуле (I) только одним атомом углерода и что в целом в формуле (II) могут присутствовать максимум четыре остатка, выбранных из R7a, R7b, R7c, R8a, R8b и R8c;X обозначает атом кислорода либо серы, сульфеновую группу, сульфоновую группу или NR1 группу, в которойR1 представляет собой атом водорода, гидроксигруппу, C1-C3-алкилоксигруппу, аминогруппу, C1C3-алкиламиногруппу, ди(C1-C3-алкил)аминогруппу, C1-C5-алкил, C2-C5-алкенил-CH2-группу, C2-C5 алкинил-CH2-группу, C3-C6-циклоалкил, C4-C6-циклоалкенил, оксетан-3-ил, тетрагидрофуран-3-ил, бензил, C1-C5-алкилкарбонил, трифторметилкарбонил, C3-C6-циклоалкилкарбонил, C1-C5-алкилсульфонил,C3-C6-циклоалкилсульфонил,аминокарбонил,C1-C5-алкиламинокарбонил,ди(C1-C5 алкил)аминокарбонил, C1-C5-алкилоксикарбонил или C4-C7-циклоалкилениминокарбонил, при этом присутствующие в вышеуказанных группах метиленовые и метильные группы дополнительно могут быть замещены C1-C3-алкилом, карбоксигруппой либо C1-C5-алкоксикарбонилом или могут быть замещены гидроксигруппой,C1-C5-алкилоксигруппой,аминогруппой,C1-C5-алкиламиногруппой,C1-C5 диалкиламиногруппой либо C4-C7-циклоалкилениминогруппой, если такие метиленовые или метильные группы не присоединены непосредственно к гетероатому из группы, включающей O, N и S, и/или 1-3 атома водорода могут быть заменены на атомы фтора, если такие метиленовые или метильные группы не присоединены непосредственно к гетероатому из группы, включающей O, N и S;R10, R11 и R12 независимо друг от друга обозначают атом водорода, фтора, хлора, брома либо йода,C1-C5-алкил, CF3-группу, C2-C5-алкенил, C2-C5-алкинил, цианогруппу, карбоксигруппу, C1-C5 алкилоксикарбонил, гидроксигруппу, C1-C3-алкилоксигруппу, CF3O-группу, CHF2O-группу, CH2FOгруппу,аминогруппу,C1-C5-алкиламиногруппу,ди(C1-C5-алкил)аминогруппу илиC4-C7 циклоалкилениминогруппу,или D представляет собой одну из четырех групп (II-1), (II-2), (II-3) и (II-4) где остатки A1, A2, A3, K1, K2, K3, K4 имеют указанные выше значения; Анион в группе формулы (II-4) обозначает фторид, хлорид, бромид, иодид, сульфат, гидросульфат,фосфат, гидрофосфат, бензоат, салицилат, сукцинат, цитрат или тартрат;R3 обозначает атом водорода или C1-C3-алкил;R4 и R5 независимо друг от друга обозначают атом водорода, линейную либо разветвленную C1-C6 алкильную, C2-C6-алкенильную или C2-C6-алкинильную группу,при этом атомы водорода метиленовых и/или метильных фрагментов линейной или разветвленной C1-C6 алкильной, C2-C6-алкенильной или C2-C6-алкинильной группы необязательно могут быть полностью или частично заменены на атомы фтора и/или один или два атома водорода линейной или разветвленной C1C6-алкильной, C2-C6-алкенильной или C2-C6-алкинильной группы в ее метиленовых и/или метильных фрагментах необязательно могут быть независимо друг от друга заменены на C3-C7-циклоалкил, нитрил,гидроксигруппу, C1-C5-алкилоксигруппу, атомы водорода которой необязательно могут быть полностью или частично заменены атомами фтора, аллилоксигруппу, пропаргилоксигруппу, фенилметилоксигруппу, фенетилоксигруппу, C1-C5-алкилкарбонилоксигруппу, C1-C5-алкилоксикарбонилоксигруппу, карбоксиC1-C5-алкилоксигруппу,C1-C5-алкилоксикарбонил-C1-C5-алкилоксигруппу,C1-C5-алкилокси-C2-C5 алкилоксигруппу, меркаптогруппу, C1-C5-алкилсульфанил, C1-C5-алкилсульфинил, C1-C5-алкилсульфонил, карбоксигруппу, C1-C5-алкилоксикарбонил, аминокарбонил, C1-C5-алкиламинокарбонил,ди(C1-C5-алкил)аминокарбонил, C1-C5-алкиламинокарбонилоксигруппу, ди(C1-C5-алкил)аминокарбонил-2 015188 оксигруппу, C4-C7-циклоалкилениминокарбонил, аминосульфонил, C1-C5-алкиламиносульфонил, ди(C1C5-алкил)аминосульфонил, C4-C7-циклоалкилениминосульфонил, ди(C1-C5-алкил)фосфорил, аминогруппу, C1-C5-алкиламиногруппу, ди(C1-C5-алкил)аминогруппу, C1-C5-алкилкарбониламиногруппу, трифторацетиламиногруппу, C1-C5-алкилокси-C1-C5-алкилкарбониламиногруппу, фенилкарбониламиногруппу,C1-C5-алкиламинокарбониламиногруппу, ди(C1-C5-алкил)аминокарбониламиногруппу, C1-C5-алкилоксикарбониламиногруппу, фенилметилоксикарбониламиногруппу, C1-C5-алкилокси-C2-C5-алкилокси-C1-C2 алкилкарбониламиногруппу, C1-C5-алкилсульфониламиногруппу, N-(C1-C5-алкилсульфонил)-C1-C5 алкиламиногруппу, C3-C6-циклоалкилкарбониламиногруппу, 4-морфолинокарбониламиногруппу, морфолинил, тиоморфолинил, пирролидинил, пиперидинил, пиперазинил, тетрагидрофуранил или тетрагидропиранил, где каждый из вышеуказанных карбо- и гетероциклов может быть замещен в кольце 1-4 C1C3-алкильными или C1-C3-алкилкарбонильными группами либо 1 или 2 оксогруппами и/или вышеуказанные фенильные и гетероарильные остатки могут быть заменены на 1 или 2 заместителя, выбранных из атомов фтора, хлора и брома, метила, метоксигруппы, аминогруппы и трифторметила, или два смежных атома углерода фенильного кольца могут быть замещены -CH2-O-CH2-группой и/или вышеуказанные алкильные группы могут быть замещены циано-C1-C5-алкилоксикарбонилом или карбоксигруппой, а вышеуказанные карбокс- или сульфонамиды необязательно дополнительно могут быть замещены у атома азота C1-C5-алкилом, и/или атомы водорода, соединенные с sp2-гибридизированными атомами углерода линейной или разветвленной C2-C6-алкенильной группы, необязательно могут быть полностью или частично заменены на атомы фтора,или обозначают карбоксигруппу,аминокарбонил,C1-C5-алкиламинокарбонил,C3-C6 циклоалкиламинокарбонил,ди(C1-C5-алкил)аминокарбонил,C1-C5-алкилоксикарбонил,C4-C7 циклоалкилениминокарбонил либо фенильную, моно- либо бициклическую гетероарильную, фенил-C1C5-алкильную или моно- либо бициклическую гетероарил-C1-C5-алкильную группу, при этом указанная группа в фенильной или гетероарильной части необязательно может быть замещена 1-3 идентичными или разными заместителями, выбранными из группы, включающей атомы фтора, хлора, брома и йода,C1-C5-алкил, трифторметил, бензил, аминогруппу, нитрогруппу, C1-C5-алкиламиногруппу, ди(C1-C5 алкил)аминогруппу, гидроксигруппу, C1-C5-алкилоксигруппу, моно-, ди- и трифторметоксигруппу, карбоксигруппу и C1-C5-алкилоксикарбонил, или два смежных атома углерода фенильного кольца могут быть замещены -CH2-O-CH2-группой, или обозначают C3-C7-циклоалкильную, морфолинильную, тиоморфолинильную, пирролидинильную, пиперидинильную, пиперазинильную, тетрагидрофуранильную либо тетрагидропиранильную группу, которая необязательно может быть замещена одним или двумя остатками, независимо друг от друга выбранными из C1-C3-алкила, ацетила, C1-C5-алкилоксикарбонила и гидроксикарбонила, илиR4 и R5 совместно с атомом углерода, к которому они присоединены, образуют C3-C7 циклоалкильную или C5-C7-циклоалкенильную группу, при этом одна из метиленовых групп C4-C7 циклоалкильной группы может быть заменена на атом кислорода либо серы, -NH-группу, -N(C1-C5 алкил), -N(C1-C4-алкилкарбонил), -N(C1-C4-алкилоксикарбонил), карбонил, сульфинил или сульфонил,и/или две непосредственно смежные друг с другом метиленовые группы C4-C7-циклоалкильной группы совместно могут быть заменены на -C(O)NH-группу, -C(O)N(C1-C5-алкил), -S(O)2NH-группу или-S(O)2N(C1-C5-алкил), и/или 1-3 атома углерода C3-C7-циклоалкильной группы необязательно могут быть независимо друг от друга замещены соответственно одним либо двумя атомами фтора или одной либо двумя C1-C5-алкильными группами или гидроксигруппой, C1-C5-алкилоксигруппой, формилоксигруппой,C1-C5-алкилкарбонилоксигруппой, C1-C5-алкилсульфанилом, C1-C5-алкилсульфонилом, аминосульфонилом, C1-C5-алкиламиносульфонилом, ди(C1-C5-алкил)аминосульфонилом, C4-C7-циклоалкилениминосульфонилом, аминогруппой, C1-C5-алкиламиногруппой, ди(C1-C5-алкил)аминогруппой, C1-C5 алкилкарбониламиногруппой, C1-C5-алкилсульфониламиногруппой, N-(C1-C5-алкилсульфонил)-C1-C5 алкиламиногруппой, C3-C6-циклоалкилкарбониламиногруппой, нитрилом, карбокси-C1-C5-алкилом,C1-C5-алкилоксикарбонил-C1-C5-алкилом, карбоксигруппой, C1-C5-алкилоксикарбонилом, аминокарбонилом, C1-C5-алкиламинокарбонилом, ди(C1-C5-алкил)аминокарбонилом или C4-C7-циклоалкилениминокарбонилом, и/или 1 либо 2 атома углерода C5-C7-циклоалкенильной группы необязательно могут быть независимо друг от друга замещены соответственно C1-C5-алкилом, нитрилом, карбокси-C1-C5-алкилом,C1-C5-алкилоксикарбонил-C1-C5-алкилом, карбоксигруппой, C1-C5-алкилоксикарбонилом, аминокарбонилом, C1-C5-алкиламинокарбонилом, ди(C1-C5-алкил)аминокарбонилом, C3-C6-циклоалкилениминокарбонилом, аминосульфонилом, C1-C5-алкиламиносульфонилом, ди(C1-C5-алкил)аминосульфонилом,C3-C6-циклоалкилениминосульфонилом или 1 либо 2 атомами фтора и/или 1 либо 2 атома углерода C4C7-циклоалкенильной группы, которые соединены с другим атомом углерода не двойной связью, необязательно могут быть независимо друг от друга замещены гидроксигруппой, C1-C5-алкилоксигруппой, C1C5-алкилкарбонилоксигруппой, C1-C5-алкилсульфанилом, C1-C5-алкилсульфонилом, аминогруппой, C1C5-алкиламиногруппой, ди(C1-C5-алкил)аминогруппой, C1-C5-алкилкарбониламиногруппой, C1-C5 алкилсульфониламиногруппой,N-(C1-C5-алкилсульфонил)-C1-C5-алкиламиногруппой илиC3-C6 циклоалкилкарбониламиногруппой, при условии, что подобная, образованная совместно остатками R4 иR5 C3-C7-циклоалкильная или C3-C7-циклоалкенильная группа, в которой два гетероатома в цикле из-3 015188 группы, включающей атом кислорода и атом азота, отделены друг от друга точно одной необязательно замещенной -CH2-группой и/или одна или обе метиленовые группы цикла, которые непосредственно соединены с атомом углерода, к которому присоединены остатки R4 и R5, заменены на гетероатом из группы, включающей атом кислорода, атом азота и атом серы, и/или присоединенный к циклической группе заместитель, который отличается тем, что гетероатом из группы, включающей атом кислорода,атом азота, атом серы и атом фтора, непосредственно присоединен к циклической группе, отделен от другого гетероатома из группы, включающей атом кислорода, атом азота и атом серы, за исключением сульфоновой группы, точно одной необязательно замещенной метиленовой группой и/или два атома в кольце образуют -O-O- или -S-O-связь, исключена из объема изобретения;M представляет собой тиофеновое кольцо формулы (III) которое через положение 2 присоединено к карбонильной группе в формуле (I) и в положении 5 замещено остатком R2 и необязательно дополнительно замещено остатком R6 и в которомR6 обозначает атом водорода, фтора, хлора, брома либо йода, C1-C2-алкил или аминогруппу,при этом под упомянутым выше в определениях заместителей выражением "гетероарильная группа" или "гетероарил" подразумевается, если не указано иное, моноциклическая 5- или 6-членная гетероарильная группа, которая, если она является 6-членной, содержит один, два или три атома азота, а если является 5-членной, либо содержит необязательно замещенную C1-C3-алкилом иминогруппу, атом кислорода или серы, либо содержит необязательно замещенную C1-C3-алкилом иминогруппу или атом кислорода или серы и дополнительно один или два атома азота, либо содержит необязательно замещеннуюC1-C3-алкилом иминогруппу и три атома азота и с которой, кроме того, через два смежных атома углерода может быть сконденсировано необязательно замещенное атомом фтора, хлора либо брома, C1-C3 алкилом, гидроксигруппой, C1-C3-алкилоксигруппой, аминогруппой, C1-C3-алкиламиногруппой, ди(C1C3-алкил)аминогруппой или C3-C6-циклоалкилениминогруппой фенильное кольцо и которая далее присоединена через атом азота или через атом углерода гетероциклической части или сконденсированного фенильного кольца, под упомянутым выше в определениях заместителей выражением "атом галогена" подразумевается, если не указано иное, атом из группы, включающей фтор, хлор, бром и йод, упомянутые выше в определениях заместителей алкильные, алкенильные, алкинильные и алкилоксигруппы, содержащие более двух атомов углерода, могут, если не указано иное, иметь прямую или разветвленную цепь, а алкильные группы в указанных выше диалкилированных остатках, например диалкиламиногруппах, могут быть идентичными или разными и атомы водорода упомянутых выше в определении заместителей метильных или этильных групп могут быть, если не указано иное, полностью или частично заменены на атомы фтора,их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли. В качестве примера моноциклических гетероарильных групп можно назвать пиридил,N-оксипиридил, пиразолил, пиридазинил, пиримидинил, пиразинил, [1,2,3]триазинил, [1,3,5]триазинил,[1,2,4]триазинил, пирролил, имидазолил, [1,2,4]триазолил, [1,2,3]триазолил, тетразолил, фуранил, изоксазолил, оксазолил, [1,2,3]оксадиазолил, [1,2,4]оксадиазолил, фуразанил, тиофенил, тиазолил, изотиазолил,[1,2,3]тиадиазолил, [1,2,4]тиадиазолил или [1,2,5]тиадиазолил. В качестве примера бициклических гетероарильных групп можно назвать бензимидазолил, бензофуранил, бензо[c]фуранил, бензотиофенил, бензо[c]тиофенил, бензотиазолил, бензо[c]изотиазолил, бензо[d]изотиазолил, бензооксазолил, бензо[c]изоксазолил, бензо[d]изоксазолил, бензо[1,2,5]оксадиазолил,бензо[1,2,5]тиадиазолил, бензо[1,2,3]тиадиазолил, бензо[d][1,2,3]триазинил, бензо[1,2,4]триазинил, бензотриазолил,циннолинил,хинолинил,N-оксихинолинил,изохинолинил,хиназолинил,N-оксихиназолинил, хиноксалинил, фталазинил, индолил, изоиндолил или 1-окса-2,3-диазаинденил. В качестве примера упомянутых выше в определении заместителей C1-C6-алкильных групп можно назвать метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, 1-пентил, 2-пентил, 3-пентил,неопентил, 3-метил-2-бутил, 1-гексил, 2-гексил, 3-гексил, 3-метил-2-пентил, 4-метил-2-пентил, 3-метил 3-пентил, 2-метил-3-пентил, 2,2-диметил-3-бутил или 2,3-диметил-2-бутил. В качестве примера упомянутых выше в определении заместителей C1-C5-алкилоксигрупп можно назвать метилокси-, этилокси-, 1-пропилокси-, 2-пропилокси-, н-бутилокси-, втор-бутилокси-, третбутилокси-, 1-пентилокси-, 2-пентилокси-, 3-пентилокси- или неопентилоксигруппу. В качестве примера упомянутых выше в определении заместителей C2-C5-алкенильных групп можно назвать этенил, 1-пропен-1-ил, 2-пропен-1-ил, 1-бутен-1-ил, 2-бутен-1-ил, 3-бутен-1-ил, 1-пентен-1 ил, 2-пентен-1-ил, 3-пентен-1-ил, 4-пентен-1-ил, 1-гексен-1-ил, 2-гексен-1-ил, 3-гексен-1-ил, 4-гексен-1 ил, 5-гексен-1-ил, бут-1-ен-2-ил, бут-2-ен-2-ил, бут-1-ен-3-ил, 2-метилпроп-2-ен-1-ил, пент-1-ен-2-ил,пент-2-ен-2-ил, пент-3-ен-2-ил, пент-4-ен-2-ил, пент-1-ен-3-ил, пент-2-ен-3-ил, 2-метилбут-1-ен-1-ил, 2-4 015188 метилбут-2-ен-1-ил, 2-метилбут-3-ен-1-ил или 2-этилпроп-2-ен-1-ил. В качестве примера упомянутых выше в определении заместителей C2-C5-алкинильных групп можно назвать этинил, 1-пропинил, 2-пропинил, 1-бутин-1-ил, 1-бутин-3-ил, 2-бутин-1-ил, 3-бутин-1-ил,1-пентин-1-ил, 1-пентин-3-ил, 1-пентин-4-ил, 2-пентин-1-ил, 2-пентин-3-ил, 3-пентин-1-ил, 4-пентин-1 ил, 2-метил-1-бутин-4-ил, 3-метил-1-бутин-1-ил или 3-метил-1-бутин-3-ил. Во 2-м варианте осуществления настоящего изобретения предлагаются соединения общей формулыD обозначает замещенную бициклическую систему формулы (II) в которой K1 и K4 независимо друг от друга обозначают -CH2-, -CHR7a-, -CR7bR7c- или -C(O)-группу, гдеR7a, R7b, R7c независимо друг от друга обозначают атом фтора, гидроксигруппу, C1-C5 алкилоксигруппу, C1-C5-алкил, который может быть замещен 1-3 атомами фтора, гидрокси-C1-C5-алкил,C1-C5-алкилокси-C1-C5-алкил, фенил, который может быть замещен 1-2 заместителями, выбранными из нитрогруппы, аминогруппы, гидроксигруппы, метоксигруппы, цианогруппы, C1-C5-алкила и атомов фтора, хлора и брома, или 5- либо 6-членную гетероарильную группу,при этом оба остатка R7b, R7c не могут быть одновременно присоединены через гетероатом к кольцевому атому углерода, за исключением случая, когда -C(R7bR7c)- соответствует -CF2-группе, или два остатка R7b, R7c совместно с кольцевым атомом углерода могут образовывать 3-, 4-, 5-, 6- либо 7-членный насыщенный карбоцикл или циклопентеновое, циклогексеновое, оксетановое, тетрагидрофурановое либо тетрагидропирановое кольцо, метиленовые группы которого могут быть замещены 1 или 2 C1-C3 алкильными группами или CF3-группами и/или метиленовые группы которого, если они не присоединены к гетероатому, могут быть замещены 1 или 2 атомами фтора;K2 и K3 независимо друг от друга обозначают -CH2-, -CHR8a-, -CR8bR8c- или -C(O)-группу, гдеR8a, R8b, R8c независимо друг от друга обозначают C1-C5-алкил, который может быть замещен 1-3 атомами фтора, гидрокси-C1-C5-алкил или C1-C5-алкилокси-C1-C5-алкил или два остатка R8b, R8c совместно с кольцевым атомом углерода могут образовывать 3-, 4-, 5-, 6- либо 7-членный карбоцикл или циклопентеновое, циклогексеновое, оксетановое, тетрагидрофурановое либо тетрагидропирановое кольцо, метиленовые группы которого могут быть замещены 1 или 2 C1-C3 алкильными группами или CF3-группами и/или метиленовые группы которого, если они не присоединены к гетероатому, могут быть замещены 1 или 2 атомами фтора,при условии, что введенный в составе R8b или R8c гетероатом не может быть отделен от заместителяX в формуле (I) только одним атомом углерода и что в целом в формуле (II) могут присутствовать максимум четыре остатка, выбранных из R7a, R7b, R7c, R8a, R8b и R8c;X обозначает атом кислорода либо серы, сульфеновую группу, сульфоновую группу или NR1 группу, в которойR1 представляет собой атом водорода, C1-C5-алкил, C2-C5-алкенил-CH2-группу, C2-C5-алкинил-CH2 группу, C3-C6-циклоалкил, C4-C6-циклоалкенил, оксетан-3-ил, тетрагидрофуран-3-ил, бензил, C1-C5 алкилкарбонил, трифторметилкарбонил, C3-C6-циклоалкилкарбонил, C1-C5-алкилсульфонил, C3-C6 циклоалкилсульфонил, аминокарбонил, C1-C5-алкиламинокарбонил, ди(C1-C5-алкил)аминокарбонил,C1-C5-алкилоксикарбонил или C4-C7-циклоалкилениминокарбонил, при этом присутствующие в вышеуказанных группах метиленовые и метильные группы дополнительно могут быть замещены C1-C3 алкилом, карбоксигруппой или C1-C5-алкоксикарбонилом либо могут быть замещены гидроксигруппой,C1-C5-алкилоксигруппой, аминогруппой, C1-C5-алкиламиногруппой, C1-C5-диалкиламиногруппой или C4C7-циклоалкилениминогруппой, если такие метиленовые или метильные группы не присоединены непосредственно к гетероатому из группы, включающей O, N и S, и/или 1-3 атома водорода могут быть заменены на атомы фтора, если такие метиленовые или метильные группы не присоединены непосредственно к гетероатому из группы, включающей O, N и S;A1, A2 и A3 имеют указанные для каждого из них при описании 1-го варианта значения, илиD представляет собой одну из четырех групп (II-1a), (II-2a), (II-3) или (II-4) где остатки A1, A2, A3, K1, K2, K3, K4 имеют указанные выше значения; Анион в группе формулы (II-4) обозначает фторид, хлорид, бромид, иодид, сульфат, гидросульфат,фосфат, гидрофосфат, бензоат, салицилат, сукцинат, цитрат или тартрат;R3 обозначает атом водорода иR4, R5 и M имеют указанные для каждого из них при описании 1-го варианта значения,их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли. В 3-м варианте осуществления настоящего изобретения предлагаются соединения общей формулыD обозначает замещенную бициклическую систему формулы (II) в которой K1, K2, K3 и K4 имеют указанные для каждого из них при описании 1-го или 2-го варианта значения;R1 представляет собой атом водорода, C1-C5-алкил, C2-C5-алкенил-CH2-группу, C2-C5-алкинил-CH2 группу, C3-C6-циклоалкил или C4-C6-циклоалкенил, при этом присутствующие в вышеуказанных группах метиленовые и метильные группы дополнительно могут быть замещены C1-C3-алкилом, карбоксигруппой или C1-C5-алкоксикарбонилом либо могут быть замещены гидроксигруппой, C1-C5 алкилоксигруппой, аминогруппой, C1-C5-алкиламиногруппой, C1-C5-диалкиламиногруппой или C4-C7 циклоалкилениминогруппой, если такие метиленовые или метильные группы не присоединены непосредственно к гетероатому из группы, включающей O, N и S, и/или 1-3 атома водорода могут быть заменены на атомы фтора, если такие метиленовые или метильные группы не присоединены непосредственно к атому азота;R10, R11 и R12 независимо друг от друга обозначают атом водорода, фтора, хлора либо брома, C1-C5 алкил, CF3-группу, цианогруппу, карбоксигруппу, C1-C5-алкилоксикарбонил, гидроксигруппу, C1-C3 алкилоксигруппу, CF3O-группу, CHF2O-группу или CH2FO-группу, илиD представляет собой одну из четырех групп (II-1 а), (II-2a), (II-3) или (II-4)-6 015188 где остатки A1, A2, A3, K1, K2, K3, K4 имеют указанные выше значения; Анион в группе формулы (II-4) может быть выбран из группы, включающей фторид, хлорид, бромид, иодид, сульфат, фосфат, бензоат, салицилат, сукцинат, цитрат и тартрат;R3, R4, R5 и M имеют указанные для каждого из них при описании 1-го или 2-го варианта значения,при этом R6 представляет собой атом водорода,их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли. В 4-м варианте осуществления настоящего изобретения предлагаются соединения общей формулыD, R3 и M имеют указанные для каждого из них при описании 1-го, 2-го или 3-го варианта значения;R4 обозначает линейную либо разветвленную C3-C6-алкенильную либо C3-C6-алкинильную группу,линейную либо разветвленную C1-C6-алкильную группу, атомы водорода которой необязательно могут быть полностью или частично заменены на атомы фтора и в которой один или два атома водорода необязательно могут быть независимо друг от друга заменены на C3-C7-циклоалкил, гидроксигруппу, C1C5-алкилоксигруппу, фенилметилоксигруппу, фенетилоксигруппу, карбокси-C1-C5-алкилоксигруппу, C1C5-алкилоксикарбонил-C1-C5-алкилоксигруппу, C1-C5-алкилокси-C2-C5-алкилоксигруппу, C1-C5-алкилсульфанил, C1-C5-алкилсульфинил, C1-C5-алкилсульфонил, карбоксигруппу, C1-C5-алкилоксикарбонил,аминокарбонил,C1-C5-алкиламинокарбонил,ди(C1-C5-алкил)аминокарбонил,C1-C5-алкиламинокарбонилоксигруппу, ди(C1-C5-алкил)аминокарбонилоксигруппу, C4-C7-циклоалкилениминокарбонил,аминогруппу, C1-C5-алкиламиногруппу, ди(C1-C5-алкил)аминогруппу, C1-C5-алкилкарбониламиногруппу,трифторацетиламиногруппу, C1-C5-алкилокси-C1-C5-алкилкарбониламиногруппу, фенилкарбониламиногруппу, C1-C5-алкиламинокарбониламиногруппу, ди(C1-C5-алкил)аминокарбониламиногруппу, C1-C5 алкилоксикарбониламиногруппу,фенилметилоксикарбониламиногруппу,C1-C5-алкилокси-C2-C5 алкилокси-C1-C2-алкилкарбониламиногруппу, C1-C5-алкилсульфониламиногруппу, C3-C6-циклоалкилкарбониламиногруппу или 4-морфолинокарбониламиногруппу,где каждый из вышеуказанных карбо- и гетероциклов может быть замещен в кольце 1-4 C1-C3 алкильными либо C1-C3-алкилкарбонильными группами или 1 или 2 оксогруппами и/или вышеуказанные фенильные и гетероарильные остатки могут быть заменены на 1 или 2 заместителя, выбранных из фтора,хлора, брома, метила, метоксигруппы и трифторметила, или два смежных атома углерода фенильного кольца могут быть замещены -CH2-O-CH2-группой и/или вышеуказанные алкильные группы могут быть замещены циано-C1-C5-алкилоксикарбонилом или карбоксигруппой, а вышеуказанные карбокс- или сульфонамиды необязательно дополнительно могут быть замещены у атома азота C1-C5-алкилом,или обозначает фенильную, фенил-C1-C2-алкильную, гетероарил-C1-C2-алкильную или C-связанную гетероарильную группу, где гетероарильная группа выбрана из группы, включающей имидазолил, фуранил, тиофенил, тиазолил, пиразолил, тетразолил, бензимидазолил, индолил, пиримидинил, пиразинил,оксазолил, 1,2,4-триазолил и пиридинил, и где указанная группа в фенильной или гетероарильной части необязательно может быть одно- или двузамещена одинаковыми или разными заместителями, выбранными из атомов хлора и фтора, C1-C3-алкила, бензила, гидроксигруппы, аминогруппы, CF3-группы,CH3O-группы и CHF2O-группы;R5 обозначает атом водорода, линейную либо разветвленную C1-C4-алкильную группу, атомы водорода которой необязательно могут быть полностью или частично заменены на атомы фтора, или обозначает пропаргил или C1-C3-алкилокси-C1-C3-алкил илиR4 и R5 совместно с атомом углерода, к которому они присоединены, образуют C5-C6 циклоалкенильную или C3-C7-циклоалкильную группу, при этом одна из метиленовых групп C4-C7 циклоалкильной группы может быть заменена на атом кислорода либо серы, -NH-группу, -N(C1-C5 алкил), -N(C1-C4-алкилкарбонил), карбонил, сульфинил или сульфонил или две непосредственно смежные друг с другом метиленовые группы C4-C7-циклоалкильной группы совместно могут быть заменены на -C(O)NH-группу, -C(O)N(C1-C5-алкил), -S(O)2NH-группу или -S(O)2N(C1-C5-алкил) и/или 1 или 2 атома углерода C3-C7-циклоалкильной группы необязательно могут быть независимо друг от друга замещены соответственно одним или двумя атомами фтора или одной или двумя C1-C5-алкильными группами либо гидроксигруппой, C1-C5-алкилоксигруппой, формилоксигруппой, аминогруппой, C1-C5 алкиламиногруппой,ди(C1-C5-алкил)аминогруппой,C1-C5-алкилкарбониламиногруппой,C3-C6 циклоалкилкарбониламиногруппой, нитрилом, карбоксигруппой, C1-C5-алкилоксикарбонилом, аминокарбонилом,C1-C5-алкиламинокарбонилом,ди(C1-C5-алкил)аминокарбонилом илиC4-C7 циклоалкилениминокарбонилом, при условии, что подобная, образованная совместно остатками R4 и R5C3-C7-циклоалкильная группа, в которой два гетероатома в цикле из группы, включающей атом кислорода и атом азота, отделены друг от друга точно одной необязательно замещенной -CH2-группой и/или одна или обе метиленовые группы цикла, которые непосредственно соединены с атомом углерода, к которому присоединены остатки R4 и R5, заменены на гетероатом из группы, включающей атом кислорода,атом азота и атом серы, и/или присоединенный к циклической группе заместитель, который отличается тем, что гетероатом из группы, включающей атом кислорода, атом азота, атом серы и атом фтора, непосредственно присоединен к циклической группе, отделен от другого гетероатома из группы, включающей атом кислорода, атом азота и атом серы, точно одной необязательно замещенной метиленовой груп-7 015188 пой и/или два атома в кольце образуют -O-O- или -S-O-связь, исключена из объема изобретения,их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли. В 5-м варианте осуществления настоящего изобретения предлагаются соединения общей формулыD обозначает замещенную бициклическую систему формулы (II) в которой K1 и K4 независимо друг от друга обозначают -CH2-, -CHR7a- или -CR7bR7c-группу, гдеR7a, R7b, R7c независимо друг от друга обозначают C1-C2-алкил или фенил, который может быть замещен 1 или 2 заместителями, выбранными из нитрогруппы, аминогруппы, гидроксигруппы, метоксигруппы, цианогруппы, C1-C5-алкила, атома фтора, атома хлора и атома брома;R1 представляет собой атом водорода, C1-C5-алкил, C2-C4-алкенил-CH2-группу, C2-C4-алкинил-CH2 группу или C3-C6-циклоалкил, при этом присутствующие в вышеуказанных C2-C5-алкильных группах метиленовые и метильные группы могут быть замещены 1-3 атомами фтора, если такие метиленовые или метильные группы не присоединены непосредственно к атому азота;R10, R11 и R12 независимо друг от друга обозначают атом водорода, фтора либо хлора, C1-C3-алкил,CF3-группу, гидроксигруппу или CH3O-группу, илиD обозначает одну из групп (II-3) или (II-4) где остатки A1, A2, A3, K1, K2, K3, K4 имеют указанные выше значения; Анион в группе формулы (II-4) может быть выбран из группы, включающей фторид, хлорид, бромид, иодид, сульфат, фосфат, бензоат, салицилат, сукцинат, цитрат и тартрат;R4 обозначает линейную либо разветвленную C3-C6-алкенильную или C3-C6-алкинильную группу,линейную либо разветвленную C1-C4-алкильную группу, атомы водорода которой необязательно частично могут быть заменены на один-четыре атома фтора и в которой один или два атома водорода необязательно могут быть независимо друг от друга заменены на C3-C7-циклоалкил, гидроксигруппу, C1-C5 алкилоксигруппу, фенилметилоксигруппу, C1-C5-алкилсульфанил, C1-C5-алкилсульфинил, C1-C5-алкилсульфонил, карбоксигруппу, C1-C5-алкилоксикарбонил, аминокарбонил, C1-C5-алкиламинокарбонил,ди(C1-C5-алкил)аминокарбонил, C4-C7-циклоалкилениминокарбонил, аминогруппу, C1-C5-алкиламиногруппу, ди(C1-C5-алкил)аминогруппу, C1-C5-алкилкарбониламиногруппу, карбокси-C1-C5-алкилкарбониламиногруппу или C1-C5-алкилоксикарбонил-C1-C5-алкилкарбониламиногруппу,где вышеуказанные фенильные остатки могут быть заменены на 1 или 2 заместителя, выбранных из фтора, хлора, брома, метила, метоксигруппы и трифторметила, или вышеуказанные карбоксамиды необязательно дополнительно могут быть замещены у атома азота C1-C5-алкилом,или обозначает фенильную, фенил-C1-C2-алкильную, гетероарил-C1-C2-алкильную или C-связанную гетероарильную группу, при этом гетероарильная группа выбрана из группы, включающей имидазолил,фуранил, тиофенил, тиазолил, пиразолил, тетразолил, бензимидазолил, индолил, пиримидинил, пиразинил, оксазолил и пиридинил, и указанная группа необязательно может быть одно- или двузамещена в фенильной или гетероарильной части одинаковыми или разными заместителями, выбранными из атомов хлора и фтора, C1-C3-алкила, CF3-группы, HO-группы, CH3O-группы и CHF2O-группы;R5 обозначает атом водорода, линейную либо разветвленную C1-C4-алкильную группу, пропаргил или C1-C3-алкилокси-C1-C3-алкил илиR4 и R5 совместно с атомом углерода, к которому они присоединены, образуют C5-C6 циклоалкенильную или C3-C7-циклоалкильную группу, при этом одна из метиленовых групп C4-C7 циклоалкильной группы может быть заменена на атом кислорода либо серы или сульфонил или 1 или 2 атома углерода C3-C7-циклоалкильной группы необязательно могут быть независимо друг от друга замещены соответственно одним или двумя атомами фтора или одной или двумя C1-C5-алкильными груп-8 015188 пами либо гидроксигруппой, C1-C5-алкилоксигруппой, формилоксигруппой, нитрилом, карбоксигруппой, C1-C5-алкилоксикарбонилом, аминокарбонилом, C1-C5-алкиламинокарбонилом, ди(C1-C5-алкил)аминокарбонилом или C4-C7-циклоалкилениминокарбонилом, при условии, что подобная, образованная совместно остатками R4 и R5 C3-C7-циклоалкильная группа, в которой одна из метиленовых групп цикла,которая непосредственно соединена с атомом углерода, к которому присоединены остатки R4 и R5, заменена на атом кислорода либо серы, исключена из объема изобретения;M представляет собой тиофеновое кольцо формулы (III) которое через положение 2 присоединено к карбонильной группе в формуле (I) и в положении 5 замещено остатком R2 и в которомR2 обозначает атом хлора либо брома или этинил;R6 обозначает атом водорода,при этом упомянутые выше в определениях заместителей алкильные, алкенильные, алкинильные и алкилоксигруппы, содержащие более двух атомов углерода, могут, если не указано иное, иметь прямую или разветвленную цепь, а алкильные группы в указанных выше диалкилированных остатках, например диалкиламиногруппах, могут быть идентичными или разными,их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли. В 6-м варианте осуществления настоящего изобретения предлагаются соединения общей формулыD обозначает замещенную бициклическую систему формулы (II) в которой K1 и K4 независимо друг от друга обозначают -CH2-, -CHR7a- или -CR7bR7c-группу, гдеR7a, R7b, R7c независимо друг от друга обозначают C1-C2-алкил;R1 представляет собой атом водорода или C1-C5-алкильную либо C3-C6-циклоалкильную группу,при этом присутствующие в вышеуказанных группах метиленовые и метильные группы 1-3 атома водорода могут быть заменены на атомы фтора, если такие метиленовые или метильные группы не присоединены непосредственно к атому азота ( Прим. перев. - Так указано в оригинале на с. 30, строки 17-21);R10, R11 и R12 независимо друг от друга обозначают атом водорода, фтора либо хлора, C1-C3-алкил,CF3-группу, HO-группу или CH3O-группу, или где остатки A1, A2, A3, K1, K2, K3, K4 имеют указанные выше значения; Анион может быть выбран из группы, включающей фторид, хлорид, бромид, иодид, сульфат, фосфат, бензоат, салицилат, сукцинат, цитрат и тартрат,их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли. В 7-м варианте осуществления настоящего изобретения предлагаются соединения общей формулы(I) согласно варианту 1-5 или 6, в которых ни R4, ни R5 не могут обозначать атом водорода, их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли. В 8-м варианте осуществления настоящего изобретения предлагаются соединения общей формулы(I) согласно варианту 1-5 или 6, где R4 и R5 совместно с атомом углерода, к которому они присоединены,образуют C5-C6-циклоалкенильную или C3-C7-циклоалкильную группу, при этом одна из метиленовых групп C4-C7-циклоалкильной группы может быть заменена на атом кислорода либо серы, при условии,что подобная, образованная совместно остатками R4 и R5 C3-C7-циклоалкильная группа, в которой одна из метиленовых групп цикла, которая непосредственно соединена с атомом углерода, к которому присоединены остатки R4 и R5, заменена на атом кислорода либо серы, исключена из объема изобретения, их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли.-9 015188 В качестве наиболее предпочтительных примеров циклических групп, которые могут быть образованы остатками R4, R5 и атомом углерода, к которому они присоединены, можно назвать следующие циклические системы: В качестве примера предпочтительных соединений общей формулы (I), включая их таутомеры, их энантиомеры, их диастереомеры, их смеси и их соли, следует назвать следующие: амид 3-[(5-бромтиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7 ил)тетрагидрофуран-3-карбоновой кислоты,амид 3-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7 ил)тетрагидрофуран-3-карбоновой кислоты,N-[1-(3-этил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)-1-метилэтил]амид 5-хлортиофен-2-карбоновой кислоты,амид 5-этинил-N-[1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]тиофен-2-карбоновой кислоты,N-[1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5 хлортиофен-2-карбоновой кислоты,N-[1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5 бромтиофен-2-карбоновой кислоты,N-[2-метокси-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5 хлортиофен-2-карбоновой кислоты,амид 1-[(5-бромтиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7 ил)циклопентан-1-карбоновой кислоты,амид 1-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7 ил)циклопентан-1-карбоновой кислоты,амид 3-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7 ил)тетрагидротиофен-3-карбоновой кислоты,амид 1-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7 ил)циклобутан-1-карбоновой кислоты,амид 1-[(5-бромтиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7 ил)циклопент-3-ен-1-карбоновой кислоты,амид 1-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7 ил)циклогексан-1-карбоновой кислоты,N-[2-бензилокси-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид (R)-5 хлортиофен-2-карбоновой кислоты,N-[2-бензилокси-1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амид 5-хлортиофен-2-карбоновой кислоты,N-[2-гидрокси-1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амидN-[1-метил-1-(3,3-диметил-2,3,4,5-тетрагидро-1H-бензо[d]азепиний-7-илкарбамоил)этил]амида 5-хлортиофен-2-карбоновой кислоты,амид 3-[(5-хлортиофен-2-ил)карбониламино]-N-(3,5-диметил-2,3,4,5-тетрагидро-1H-бензо[d]азепин 7-ил)тетрагидрофуран-3-карбоновой кислоты. Объектом изобретения являются также физиологически совместимые соли соединений, представленных в приведенных выше вариантах осуществления изобретения и примерах. Еще одним объектом изобретения являются лекарственные средства, содержащие одно из представленных в приведенных выше вариантах осуществления изобретения и примерах соединений или его физиологически совместимую соль и необязательно один или несколько инертных носителей и/или разбавителей. Объектом изобретения является, кроме того, применение одного из представленных в приведенных выше вариантах осуществления изобретения и примерах соединений или его физиологически совместимой соли для приготовления лекарственного средства, обладающего ингибирующим действием на фактор Xa и/или ингибирующим действием на родственные серинпротеазы. Следующим объектом изобретения является способ приготовления лекарственного средства, отличающийся тем, что одно из представленных в приведенных выше вариантах осуществления изобретения и примерах соединений или его физиологически совместимую соль не химическим путем объединяют с одним или несколькими инертными носителями и/или разбавителями. Согласно изобретению соединения общей формулы (I) получают известными способами, например следующими способами.(a) Соединение общей формулы (Ia) где A1-A3, K1-K4, X и R1-R6 имеют указанные в описании 1-го варианта осуществления изобретения значения и присутствующие в котором аминогруппы, гидроксигруппы, карбоксигруппы или тиольные группы при необходимости можно защищать обычными защитными группами, такими, например, как описанные у T.W. Greene, P.G.M. Wuts в "Protective Groups in Organic Synthesis", которые по завершении химических превращений можно вновь отщеплять известными из литературы методами, получают описанными в примерах осуществления изобретения способами или можно получать, например, в соответствии с одной из приведенных ниже реакционных схем 1 и 2. На приведенных выше схемах Q обозначает гидроксигруппу, C1-C4-алкилоксигруппу, атом галогена, алкилоксикарбонилоксигруппу или ацилоксигруппу, а PG представляет собой атом водорода или известную из литературы защитную группу для функциональной аминогруппы, такую, например, как третбутоксикарбонильную, бензилоксикарбонильную или трифторацетильную группу. Представленные на схемах 1 и 2 реакционные стадии I)-III) можно проводить в соответствии с описанными в примерах методами или в соответствии с известными из литературы условиями, например,следующим путем. Стадия I). Ацилирование амина (IV) или (VII) взаимодействием при необходимости с активированной карбоновой кислотой (V), соответственно (VI) или (VIII). Подобное ацилирование целесообразно проводить взаимодействием с соответствующим галогенидом или ангидридом в растворителе, таком как метиленхлорид, хлороформ, четыреххлористый углерод,диэтиловый эфир, тетрагидрофуран, диоксан, бензол, толуол, ацетонитрил, диметилформамид, раствор едкого натра или сульфолан, необязательно в присутствии неорганического или органического основания, при температуре в пределах от -20 до 200C, предпочтительно, однако, от -10 до 160C. Однако указанное ацилирование можно проводить и взаимодействием со свободной кислотой, необязательно в присутствии активатора кислоты или обезвоживающего средства, например в присутствии изобутилового эфира хлормуравьиной кислоты, тионилхлорида, триметилхлорсилана, хлористого водорода, серной кислоты, метансульфоновой кислоты, паратолуолсульфоновой кислоты, трихлорида фосфора, пентаоксида фосфора, 2-этокси-1-этоксикарбонил-1,2-дигидрохинолина (ЭЭДХ), N,N'-дициклогексилкарбодиимида, N,N'-дициклогексилкарбодиимида/камфорсульфоновой кислоты, N,N'-дициклогексилкарбодиимида/N-гидроксисукцинимида, 1-гидроксибензотриазола, N,N'-карбонилдиимидазола,тетрафторбората O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония/N-метилморфолина, тетрафторбо- 12015188 рата O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония/N-этилдиизопропиламина, гексафторфосфата Oпентафторфенил-N,N,N',N'-тетраметилурония/триэтиламина, N,N'-тионилдиимидазола или трифенилфосфина/четыреххлористого углерода, при температуре в пределах от -20 до 200C, предпочтительно,однако, от -10 до 160C. Ацилирование можно также проводить взаимодействием с эфиром карбоновой кислоты (V) или(VI) и с амином (IV) путем активирования триметилалюминием. Однако ацилирование соединения общей формулы (IV) можно также проводить взаимодействием с реакционноспособным производным карбоновой кислоты общей формулы (IX) в которой R4-R6 и R2 имеют указанные в описании 1-го варианта осуществления изобретения значения. В этом случае ацилирование целесообразно проводить в растворителе, таком, например, как толуол,тетрагидрофуран или диметилформамид, с добавлением кислоты, такой как уксусная кислота или камфорсульфоновая кислота, или при необходимости в присутствии кислоты Льюиса, такой как хлорид цинка или хлорид меди(II), и при необходимости при добавлении аминовых оснований, таких, например, как диизопропилэтиламин, триэтиламин или N-метилморфолин, при температуре в пределах от -10 до 100C,например, с применением микроволновой печи или метода, описанного у P. Wipf и др., Helvetica ChimicaActa, 69, 1986, с. 1153. Соединения общей формулы (IX) можно получать из соединений общей формулы (V), предпочтительно проведением реакции в растворителе или смеси растворителей, таких как дихлорметан, трихлорметан, четыреххлористый углерод, бензол, хлорбензол, толуол, ксилол, гексаметилдисилоксан, диэтиловый эфир, тетрагидрофуран, диоксан, ацетонитрил, пиридин, необязательно в присутствии N,N'дициклогексилкарбодиимида, N,N'-дициклогексилкарбодиимида/N-гидроксисукцинимида, 1-гидроксибензотриазола, N,N'-карбонилдиимидазола, тетрафторбората O-(бензотриазол-1-ил)-N,N,N'N'-тетраметилурония/N-метилморфолина,тетрафторборатаO-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония/N-этилдиизопропиламина, или в уксусном ангидриде при температуре в пределах от -20 до 200C, предпочтительно, однако, при температуре в пределах от -10 до 100C. Другие методы амидного сочетания описаны, например, у P.D. Bailey, I.D. Collier, K.M. Morgan вHouben-Weyl Ergnzungsband 22, изд-во Thieme Verlag, 2003, и цитируемой в этих публикациях литературе. Стадия II), соответственно III). Отщепление защитной группы. Использовавшуюся на время протекания реакции защитную группу в последующем при необходимости отщепляют, например, гидролитическим путем в водном растворителе, например в воде, изопропаноле/воде, тетрагидрофуране/воде или диоксане/воде, в присутствии кислоты, такой как трифторуксусная кислота, соляная кислота или серная кислота, либо в присутствии основания щелочного металла,такого как гидроксид лития, гидроксид натрия или гидроксид калия, или путем отщепления простого эфира, например, в присутствии иодтриметилсилана, при температуре в пределах от 0 до 100C, предпочтительно при температуре в пределах от 10 до 50C. Однако бензильную, метоксибензильную или бензилоксикарбонильную группу отщепляют, например, путем гидрогенолиза, в частности, с использованием водорода в присутствии катализатора, такого как палладий на угле, в пригодном для этой цели растворителе, таком как метанол, этанол, этилацетат,диметилформамид, диметилформамид/ацетон или ледяная уксусная кислота, необязательно с добавлением кислоты, такой как соляная кислота, при температуре в пределах от 0 до 50C, предпочтительно, однако, при комнатной температуре, и при давлении водорода в интервале от 1 до 7 бар, но предпочтительно в интервале от 1 до 5 бар. Защитную группу можно также отщеплять методами, описанными у T.W. Greene, P.G.M. Wuts в(а) Структурные фрагменты общей формулы где A1, A2, A3, K1, K2, K3, K4, X и R3 имеют указанные в описании 1-го варианта осуществления изобретения значения и присутствующие в которых аминогруппы, гидроксигруппы, карбоксигруппы или тиольные группы при необходимости можно защищать обычными защитными группами, такими, например,как описанные у T.W. Greene, P.G.M. Wuts в "Protective Groups in Organic Synthesis", которые в ходе выполнения последовательности реакций по синтезу соединений формулы (I) можно вновь отщеплять известными из литературы методами, известны из литературы или же могут быть синтезированы методами, описанными в примерах осуществления изобретения, либо, например, известными из литературы- 13015188 методами или по аналогии с известными из литературы методами, такими, например, как описанные в(II-4) в том случае, когда они представляют собой бензазепиновые соединения, можно получать из приемлемых бензазепиновых предшественников, например, окислением с помощью мета-хлорпербензойной кислоты, соответственно алкилированием алкилгалогенидом, как это описано ниже в экспериментальной части. Так, например, соединение общей формулы (IV), в которой R3 обозначает атом водорода, а A1, A2,3A , K1, K2, K3, K4 и X имеют указанные в описании 1-го варианта осуществления изобретения значения,можно получать восстановлением нитрогруппы в соединении общей формулы (III) в которой A1, A2, A3, K1, K2, K3, K4 и X имеют указанные в описании 1-го варианта осуществления изобретения значения, описанным ниже методом. Подобное восстановление нитрогруппы целесообразно проводить в растворителе или смеси растворителей, таких как вода, водный раствор хлорида аммония, соляная кислота, серная кислота, фосфорная кислота, муравьиная кислота, уксусная кислота, уксусный ангидрид, например, взаимодействием с неблагородными металлами, такими как железо, цинк, олово, или с серосодержащими соединениями, такими как сульфид аммония, сульфид натрия или дитионит натрия, либо каталитическим гидрированием водородом, например, под давлением от 0,5 до 100 бар, предпочтительно, однако, от 1 до 50 бар, гидразином в качестве восстановителя, предпочтительно в присутствии катализатора, такого как никель Ренея,палладий на угле, оксид платины, платина на минеральных волокнах или родий, либо комплексными гидридами, такими как алюмогидрид лития, борогидрид натрия, цианборогидрид натрия, диизобутилалюмогидрид, предпочтительно в растворителе или смеси растворителей, таких как вода, метанол, этанол,изопропанол, пентан, гексан, циклогексан, гептан, бензол, толуол, ксилол, этилацетат, метилпропионат,гликоль, диметиловый эфир гликоля, диметиловый эфир диэтиленгликоля, диоксан, тетрагидрофуран, Nметилпирролидинон или же N-этилдиизопропиламин, N-C1-C5-алкилморфолин, N-C1-C5-алкилпиперидин, N-C1-C5-алкилпирролидин, триэтиламин, пиридин, например, при температуре в пределах от(б) Структурные фрагменты общей формулы в которых R4, R5, R6 и R2 имеют указанные в описании 1-го варианта осуществления изобретения значения, а Q обозначает гидроксигруппу, C1-C4-алкилоксигруппу, атом галогена, алкилоксикарбонилоксигруппу или ацилоксигруппу и присутствующие в которых аминогруппы, гидроксигруппы, карбоксигруппы или тиольные группы при необходимости можно защищать обычными защитными группами,такими, например, как описанные у T.W. Greene, P.G.M. Wuts в "Protective Groups in Organic Synthesis",которые в ходе выполнения последовательности реакций по синтезу соединений формулы (I) можно вновь отщеплять известными из литературы методами, известны из литературы или же могут быть синтезированы методами, описанными в примерах осуществления изобретения, либо известными из литературы методами или по аналогии с известными из литературы методами, такими, например, как описанные в WO 04/46138. Схема 3- 14015188 Так, например, указанные структурные фрагменты можно также получать в соответствии с приведенной выше схемой 3 взаимодействием соединения (VIII) с амином (VI-1), где Q обозначает гидроксигруппу, C1-C4-алкилоксигруппу, атом галогена, алкилоксикарбонилоксигруппу или ацилоксигруппу, aQ-I обозначает гидрокси- или C1-C4-алкилоксигруппу, которую после стадии ацилирования можно при необходимости путем омыления и активирования по описанной выше методике переводить в группу Q. Ацилирование можно проводить в соответствии с уже рассмотренными выше условиями ацилирования. Аминокислотные производные (VI-1) известны из литературы или же могут быть получены из имеющихся в продаже аминокислотных производных по аналогии с известными из литературы методами,описанными, в частности, в примерах. При проведении описанных выше реакций присутствующие при определенных условиях реакционноспособные группы, такие как гидрокси-, карбокси-, амино-, алкиламино- или иминогруппы, можно защищать на время протекания реакции обычными защитными группами, которые можно вновь отщеплять по завершении реакции. В качестве примера защитной группы для гидроксигруппы можно назвать метоксигруппу, бензилоксигруппу, триметилсилильную группу, ацетильную группу, бензоильную группу, трет-бутильную группу, тритильную группу, бензильную группу или тетрагидропиранильную группу. В качестве примера защитной группы для карбоксильной группы можно назвать триметилсилильную, метильную, этильную, трет-бутильную, бензильную или тетрагидропиранильную группу. В качестве примера защитной группы для амино-, алкиламино- или иминогруппы можно назвать ацетильную, трифторацетильную, бензоильную, этоксикарбонильную, трет-бутоксикарбонильную, бензилоксикарбонильную, бензильную, метоксибензильную или 2,4-диметоксибензильную группу, а для аминогруппы - дополнительно фталильную группу. В качестве примера защитной группы для этинильной группы можно назвать триметилсилильную,дифенилметилсилильную, трет-бутилдиметилсилильную или 1-гидрокси-1-метилэтильную группу. Другие возможные защитные группы и методы их отщепления описаны у T.W. Greene, P.G.M. Wuts в "Protective Groups in Organic Synthesis", изд-во Wiley, 1991 и 1999. Использовавшуюся на время протекания реакции защитную группу в последующем при необходимости можно отщеплять, например, гидролитическим путем в водном растворителе, например в воде,изопропаноле/воде, тетрагидрофуране/воде или диоксане/воде, в присутствии кислоты, такой как трифторуксусная кислота, соляная кислота или серная кислота, либо в присутствии основания щелочного металла, такого как гидроксид лития, гидроксид натрия или гидроксид калия, или путем отщепления простого эфира, например, в присутствии иодтриметилсилана, при температуре в пределах от 0 до 100C,предпочтительно при температуре в пределах от 10 до 50C. Однако бензильную, метоксибензильную или бензилоксикарбонильную группу отщепляют, например, путем гидрогенолиза, в частности, с использованием водорода в присутствии катализатора, такого как палладий на угле, в пригодном для этой цели растворителе, таком как метанол, этанол, этилацетат,диметилформамид, диметилформамид/ацетон или ледяная уксусная кислота, необязательно с добавлением кислоты, такой как соляная кислота, при температуре в пределах от 0 до 50C, предпочтительно, однако, при комнатной температуре, и при давлении водорода в интервале от 1 до 7 бар, предпочтительно,однако, от 1 до 5 бар. Метоксибензильную группу можно отщеплять также в присутствии окислителя, такого как аммонийнитрат церия(IV), в растворителе, таком как метиленхлорид, ацетонитрил или ацетонитрил/вода, при температуре в пределах от 0 до 50C, предпочтительно, однако, при комнатной температуре. Метоксигруппу целесообразно отщеплять в присутствии трибромида бора в растворителе, таком как метиленхлорид, при температуре в пределах от -35 до -25C. 2,4-Диметоксибензильную группу предпочтительно отщеплять, однако, в трифторуксусной кислоте в присутствии анизола. трет-Бутильную или трет-бутилоксикарбонильную группу предпочтительно отщеплять обработкой кислотой, такой как трифторуксусная кислота или соляная кислота, необязательно с использованием растворителя, такого как метиленхлорид, диоксан или диэтиловый эфир. Фталильную группу предпочтительно отщеплять в присутствии гидразина или первичного амина,такого как метиламин, этиламин или н-бутиламин, в растворителе, таком как метанол, этанол, изопропанол, толуол/вода или диоксан, при температуре в пределах от 20 до 50C. Аллилоксикарбонильную группу отщепляют обработкой каталитическим количеством тетракис(трифенилфосфин)палладия(0), предпочтительно в растворителе, таком как тетрагидрофуран, и предпочтительно в присутствии избытка основания, такого как морфолин или 1,3-димедон, при температуре в пределах от 0 до 100C, предпочтительно при комнатной температуре, и в атмосфере инертного газа либо обработкой каталитическим количеством хлорида трис-(трифенилфосфин)родия(I) в растворителе,таком как водный этанол, и необязательно в присутствии основания, такого как 1,4 диазабицикло[2.2.2]октан, при температуре в пределах от 20 до 70C.- 15015188 Помимо этого полученные соединения общей формулы (I) можно разделять на их энантиомеры и/или диастереомеры. Так, например, полученные соединения общей формулы (I), которые образуются в виде рацематов,можно разделять по известным методам (см. N.L. Allinger и E.L. Eliel, "Topics in Stereochemistry", изд-воWiley Interscience, 1971, т. 6) на их оптические антиподы, а соединения общей формулы (I) по меньшей мере с 2 асимметрическими атомами углерода можно на основе различий физико-химических свойств таких соединений разделять по известным методам, например хроматографией и/или фракционной кристаллизацией, на их диастереомеры, которые при их образовании в рацемической форме в последующем можно разделять, как указано выше, на энантиомеры. Разделение на энантиомеры предпочтительно осуществлять путем колоночного разделения на хиральных фазах либо путем перекристаллизации из оптически активного растворителя или взаимодействием с оптически активным веществом, которое с рацемическим соединением образует соли или производные, такие как сложные эфиры или амиды, прежде всего взаимодействием с кислотами и их активированными производными или спиртами, и разделением полученной в результате смеси диастереомерных солей или производных, например, на основе различий в их растворимости, при этом из чистых диастереомерных солей или производных можно высвобождать свободные антиподы воздействием пригодного для этой цели средства. В качестве примера наиболее часто используемых в вышеуказанных целях оптически активных кислот можно назвать D- и L-формы винной кислоты либо дибензоилвинной кислоты, ди-о-толилвинной кислоты, яблочной кислоты, миндальной кислоты, камфорсульфоновой кислоты,глутаминовой кислоты, аспарагиновой кислоты или хинной кислоты. В качестве примера оптически активного спирта можно назвать (+)- или (-)-ментол, а в качестве примера оптически активного ацильного остатка в амидах можно назвать (+)- или (-)-ментилоксикарбонильный остаток. Полученные соединения формулы (I) можно, кроме того, переводить в их соли, прежде всего для фармацевтического применения - в их физиологически совместимые соли, с неорганическими или органическими кислотами. В качестве примера пригодных для этой цели кислот можно назвать соляную кислоту, бромисто-водородную кислоту, серную кислоту, метансульфоновую кислоту, фосфорную кислоту, фумаровую кислоту, янтарную кислоту, молочную кислоту, лимонную кислоту, винную кислоту или малеиновую кислоту. Кроме того, полученные таким путем новые соединения формулы (I), если они содержат карбоксигруппу, в последующем при необходимости можно переводить в их соли с неорганическими или органическими основаниями, прежде всего для фармацевтического применения - в их физиологически совместимые соли. В качестве примера пригодных для этой цели оснований можно назвать гидроксид натрия,гидроксид калия, циклогексиламин, этаноламин, диэтаноламин и триэтаноламин. Соединения общей формулы (I), а также их таутомеры, их энантиомеры, их диастереомеры и их физиологически совместимые соли обладают, как уже указывалось в начале описания, ценными фармакологическими свойствами, прежде всего антитромботическим действием, которое основано преимущественно на влияющем на тромбин или фактор Xa действии, например, на ингибирующем тромбин или фактор Xa действии, на удлиняющем частичное активированное тромбопластиновое время действии и на ингибирующем действии на родственные серинпротеазы, такие, например, как урокиназа, фактор VIIa,фактор IX, фактор XI и фактор XII. Ингибирующее действие представленных ниже в разделе "Экспериментальная часть" соединений на фактор Xa исследовали по описанной ниже методике. Методика. Исследование кинетики ферментов проводят с использованием хромогенного субстрата. Высвобождающееся из бесцветного хромогенного субстрата под действием человеческого фактора Xa количество паранитроанилина (пНА) определяют фотометрически при 405 нм. Это количество пропорционально активности используемого фермента. Ингибирование ферментативной активности тестируемым веществом (в сравнении с растворителем в качестве контроля) определяют при различных концентрациях тестируемого вещества и на основе полученных данных рассчитывают значение IC50, которое соответствует той концентрации тестируемого вещества, при которой оно ингибирует активность фактора Xa на 50%. Материалы. трис-(Гидроксиметил)аминометановый буфер (100 ммоль) и хлорид натрия (150 ммоль), pH 8,0,плюс фракция V человеческого альбумина в концентрации 1 мг/мл, без протеаз. Фактор Xa (фирма Calbiochem): удельная активность 217 МЕ/мг, конечная концентрация 7 МЕ/мл в каждой реакционной смеси. Субстрат S 2765 (фирма Chromogenix): конечная концентрация 0,3 мМ/л (1 KM) в каждой реакционной смеси. Тестируемое вещество: конечная концентрация 100, 30, 10, 3, 1, 0,3, 0,1, 0,03, 0,01, 0,003,0,001 мкмоль/л. Проведение экспериментов. 10 мкл исходного раствора тестируемого вещества в 23,5-кратной концентрации, соответственно растворитель (контроль), 175 мкл трис/ЧСА-буфера и 25 мкл рабочего раствора фактора Xa в концентра- 16015188 ции 65,8 ед./л инкубируют в течение 10 мин при 37C. После добавления 25 мкл рабочего раствора субстрата S 2765 (2,82 ммоль/л) образец в течение 600 с анализируют при 37C в фотометре (SpectraMax 250) при 405 нм. Анализ и обработка результатов. 1. Определяют максимальное увеличение (ОП/мин) по 21 экспериментальной точке. 2. Определяют ингибирование в % в сравнении с растворителем, используемым в качестве контроля. 3. Строят кривую доза-эффект (график зависимости ингибирования в % от концентрации тестируемого вещества). 4. Определяют концентрацию IC50 путем интерполяции значения по оси X (соответствует концентрации тестируемого вещества) кривой доза-эффект при значении по оси Y, соответствующем ингибированию активности фактора Xa на 50%. Значения IC50 у всех соединений, которые тестировали в этом опыте, составили менее 100 мкмоль/л. Предлагаемые в изобретении соединения обладают в целом хорошей переносимостью. Благодаря своим фармакологическим свойствам предлагаемые в изобретении новые соединения и их физиологически совместимые соли пригодны для профилактики и лечения тромботических заболеваний вен и артерий, например, для профилактики и лечения тромбозов глубоких вен нижних конечностей,для предотвращения реокклюзии сосудов после наложения анастомоза или ангиопластики (чрескожной катетерной коронаропластики (ЧК(К)А, а также окклюзии при заболеваниях периферийных артерий,для профилактики и лечения эмболии легочной артерии, распространенного внутрисосудистого свертывания крови и тяжелого сепсиса, для предотвращения и профилактики тромбозов глубоких вен у пациентов с обострением хронического обструктивного заболевания легких, для лечения язвенного колита, для профилактики и лечения коронарных тромбозов, для профилактики апоплексического удара и для предотвращения окклюзии шунтов. Предлагаемые в изобретении соединения пригодны также для антитромботической поддерживающей терапии при тромболитической терапии, например, альтеплазой, ретеплазой, тенектеплазой, стафилокиназой или стрептокиназой, для предотвращения длительного рестеноза после ЧК(К)А, для профилактики и лечения случаев ишемии у пациентов со всеми формами коронарной болезни сердца, для предотвращения метастазирования и роста опухолей и распространения воспалительных процессов, например, при лечении пневмосклероза, для профилактики и лечения ревматоидного артрита, для предупреждения или предотвращения фибринзависимого спайкообразования и/или образования рубцовой ткани, а также для стимуляции процессов заживления ран Благодаря своим фармакологическим свойствам предлагаемые в изобретении новые соединения и их физиологически совместимые соли пригодны, кроме того, для лечения болезни Альцгеймера и болезни Паркинсона. Логическое обоснование этому вытекает, например, из следующих фактов, которые позволяют сделать вывод о том, что ингибиторы тромбина, соответственно ингибиторы фактора Xa, благодаря своей способности подавлять образование тромбина, соответственно его активность, могут представлять собой ценные лекарственные вещества, пригодные для терапии болезни Альцгеймера и болезни Паркинсона. Результаты клинических и экспериментальных исследований дают все основания предполагать, что нейротоксические механизмы, например обусловленное активацией протеаз каскада свертывания крови воспаление, участвуют в гибели нейронов вследствие травмы головного мозга. Данные различных исследований указывают на участие тромбина в нейродегенеративных процессах, например,вследствие апоплексического удара, повторного наложения анастомоза или травматических повреждений головного мозга. Повышенную активность тромбина можно было обнаружить, например, даже по истечении нескольких дней после повреждения периферических нервов. Помимо этого было установлено, что тромбин вызывает ретракцию нейритов (аксонов), а также пролиферацию нейроглиальных клеток и апоптоз в первичных культурах нейронов и нейробластов (обзорную информацию см. Neurobiol. Aging 25(6), 2004, c. 783-793). Кроме того, результаты различных исследований in vitro на головном мозге пациентов, страдающих болезнью Альцгеймера, свидетельствуют о том, что тромбин играет определенную роль в патогенезе этой болезни (Neurosci. Lett. 146, 1992, c. 152-154). В нейритных бляшках в головном мозге пациентов, страдающих болезнью Альцгеймера, удалось обнаружить накопление иммунореактивного тромбина. В исследованиях in vitro было установлено, что тромбин играет также определенную роль в регуляции и стимуляции продуцирования белка-предшественника амилоида (APP-белка, от англ."amyloid precursor protein"), а также в расщеплении APP-белка на фрагменты, которые можно было обнаружить в амилоидных бляшках в головном мозге пациентов, страдающих болезнью Альцгеймера. Помимо этого было установлено, что индуцированная тромбином активация микроглии in vivo ведет к дегенерации нигральных допаминергических нейронов. Эти факты позволяют сделать вывод о том, что активация микроглии, вызванная эндогенным(и) веществом(ами), например тромбином, участвует в невропатологическом процессе гибели допаминергических нейронов, который встречается у пациентов, страдающих болезнью Паркинсона (J. Neurosci., 23, 2003, c. 5877-5886).- 17015188 Для достижения соответствующего действия предлагаемые в изобретении соединения целесообразно применять от 1 до 4 раз в день в дозе, которая при внутривенном введении составляет от 0,01 до 3 мг/кг, предпочтительно от 0,03 до 1,0 мг/кг, а при пероральном введении составляет от 0,03 до 30 мг/кг,предпочтительно от 0,1 до 10 мг/кг. С этой целью предлагаемые в изобретении соединения формулы (I), необязательно в сочетании с другими действующими веществами, перерабатывают совместно с одним или несколькими обычными инертными носителями и/или разбавителями, например с кукурузным крахмалом, лактозой, тростниковым сахаром, микрокристаллической целлюлозой, стеаратом магния, поливинилпирролидоном, лимонной кислотой, винной кислотой, водой, водой/этанолом, водой/глицерином, водой/сорбитом, водой/полиэтиленгликолем, пропиленгликолем, цетилстеариловым спиртом, карбоксиметилцеллюлозой или жиросодержащими веществами, такими как отвержденный жир, или их приемлемыми смесями, в обычные галеновы препараты, такие как таблетки, драже, капсулы, порошки, суспензии или суппозитории. Предлагаемые в изобретении новые соединения и их физиологически совместимые соли могут использоваться в терапевтических целях в сочетании с ацетилсалициловой кислотой, с ингибиторами агрегации тромбоцитов, такими как антагонисты фибриногенового рецептора (например, абциксимаб, эптифибатид, тирофибан, роксифибан), с физиологическими активаторами и ингибиторами системы свертывания крови и их рекомбинантными аналогами (например, протеином C, TFPI, антитромбином), с ингибиторами АДФ-индуцированной агрегации (например, клопидогрелем, тиклопидином), с антагонистамиP2T-рецептора (например, кангрелором) или с комбинированными антагонистами тромбоксанового рецептора/ингибиторами синтетазы (например, тербогрелем). Экспериментальная часть. Ниже изобретение более подробно рассмотрено на примерах, которые, однако, не ограничивают его объем. Для полученных в рассмотренных ниже примерах соединений обычно имеются данные об их температуре плавления и/или ИК-спектре, УФ-спектре, 1H-ЯМР-спектре и/или масс-спектре. Если не указано иное, для определения значений Rf использовали готовые пластины для тонкослойной хроматографии(ТСХ) типа "Силикагель 60 F254" (фирма Е. Merck, Дармштадт, артикул 1.05714) без насыщения в камере. Значения Rf, которые определяли с использованием материала, обозначенного как "алокс", получали с применением готовых пластин для ТСХ типа "Оксид алюминия 60 F254" (фирма E. Merck, Дармштадт, артикул 1.05713) без насыщения в камере. Значения Rf, которые определяли с использованием материала, обозначенного как "RP-8" (обращенная фаза), получали с применением готовых пластин для ТСХ типа "RP-8 F254s" (фирма Е. Merck, Дармштадт, артикул 1.15684) без насыщения в камере. Указанные в примерах для систем растворителей (элюентов) соотношения между их компонентами относятся к единицам объема соответствующего растворителя. В качестве силикагеля для хроматографической очистки использовали силикагель, выпускаемый фирмой Millipore (MATREX, 35-70 мкм) и RPматериал фирмы Varian (Microsorb, 60-8 мкм; C18 Dynamax). При отсутствии более подробных данных о конфигурации того или иного соединения остается открытым вопрос о том, идет ли речь о чистых энантиомерах или смесях энантиомеров/диастереомеров. В последующей экспериментальной части описания используются следующие сокращения: ВОС - трет-бутоксикарбонил; ДИПЭА - N-этилдиизопропиламин; ДМФ - N,N-диметилформамид; насыщ. - насыщенный; ч - час(ы); ГАТУ - гексафторфосфат O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония; Все свободные валентности у атома азота в приведенных структурных формулах, по умолчанию,подразумевают соответствующее количество атомов водорода.- 18015188 Данные ЖХВР-МС получали с использованием следующих условий и оборудования. Метод 1. Масс-спектрометр Waters ZQ2000, автоматическое устройство для ввода проб Gilson 215, ЖХВРхроматограф HP1100, детектор на диодной матрице. В качестве подвижной фазы использовали следующую: А: вода с 0,10% ТФУК; Б: ацетонитрил с 0,10% ТФУК. В качестве неподвижной фазы использовали колонку X-Terra MS C18, 3,5 мкм, 4,650 мм. Обнаружение детектором на диодной матрице проводили в диапазоне длин волн от 210 до 500 нм. Метод 2. Спектрометр Waters Alliance 2695, детектор PDA 2996, ZQ 2002. В качестве подвижной фазы использовали следующую: А: вода с 0,10% ТФУК; Б: ацетонитрил с 0,10% ТФУК. В качестве неподвижной фазы использовали колонку Waters X-Terra MS C18, 2,5 мкм, 4,630 мм. Метод 3. Спектрометр Waters Alliance 2695, детектор PDA 2996. В качестве подвижной фазы использовали следующую: А: вода с 0,13% ТФУК; Б: ацетонитрил с 0,10% ТФУК. В качестве неподвижной фазы использовали колонку Varian Microsorb 100 C18; 3,5 мкм; 4,650 мм. Метод 3a. Спектрометр Waters Alliance 2695, детектор PDA 2996. В качестве подвижной фазы использовали следующую: А: вода с 0,1% ТФУК; Б: ацетонитрил с 0,1% ТФУК. В качестве неподвижной фазы использовали колонку Varian Microsorb 100 C18; 2,5 мкм; 4,630 мм. Метод 4.Agilent 1100. В качестве подвижной фазы использовали следующую: А: вода с 0,10% муравьиной кислоты; Б: ацетонитрил с 0,10% муравьиной кислоты. В качестве неподвижной фазы использовали колонку Zorbax StableBond C18; 3,5 мкм; 4,675 мм.- 19015188 Метод 5. Спектрометр Waters Alliance 2695, детектор PDA 2996. В качестве подвижной фазы использовали следующую: А: вода с 0,1% ТФУК; Б: ацетонитрил с 0,1% ТФУК. В качестве неподвижной фазы использовали колонку Interchim HS Strategy 5 C18-2; 5 мкм; 4,650 мм. Метод 6. Спектрометр Waters Alliance 26905, детектор PDA 996. В качестве подвижной фазы использовали следующую: А: вода с 0,1% ТФУК; Б: ацетонитрил с 0,1% ТФУК. В качестве неподвижной фазы использовали колонку MerckChromolith SpeedRod RP-18e; 4,650 мм. Пример 1. Амид 3-[(5-бромтиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7 ил)тетрагидрофуран-3-карбоновой кислоты(а) 7-Нитро-2,3,4,5-тетрагидро-1H-бензо[d]азепин. 8,4 г (29,0 ммоль) 3-трифторацетил-7-нитро-2,3,4,5-тетрагидро-1H-бензо[d]азепина в атмосфере азота суспендируют в 80 мл метанола, смешивают с 5 мл раствора NaOH (50%-го) и в течение 2 ч перемешивают при 70C. Затем метанол отгоняют на ротационном испарителе, остаток смешивают с водой и экстрагируют трет-бутилэтиловым эфиром. Органическую фазу промывают раствором NaOH (50%-ным) и насыщ. раствором хлорида натрия, сушат над сульфатом натрия и досуха концентрируют в вакууме. Выход: 5,1 г (91%). Значение Rf: 0,28 (оксид алюминия; дихлорметан/этанол в соотношении 95:5).(б) 3-Метил-7-нитро-2,3,4,5-тетрагидро-1H-бензо[d]азепин. 5,0 г (26,0 ммоль) 7-нитро-2,3,4,5-тетрагидро-1H-бензо[d]азепина при перемешивании и при комнатной температуре смешивают в 9,8 мл (260,1 моль) муравьиной кислоты с 15,5 мл (208,1 ммоль) раствора формалина в воде (37%-ного) и оставляют перемешиваться на ночь при 70C. Затем реакционную смесь при охлаждении на ледяной бане подщелачивают раствором NaOH (50%-ным) и экстрагируют трет-бутилметиловым эфиром. Органическую фазу сушат над сульфатом натрия и досуха концентрируют в вакууме. Выход: 4,8 г (90%). Значение Rf: 0,65 (оксид алюминия; дихлорметан/этанол в соотношении 95:5).(в) 3-Метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-иламин. 4,8 г (23,2 ммоль) 3-метил-7-нитро-2,3,4,5-тетрагидро-1H-бензо[d]азепина растворяют в 45 мл метанола и смешивают с 400 мг 10%-ного Pd/C. После этого в течение 5 ч гидрируют в аппарате Парра при комнатной температуре и при давлении водорода 3 бар. Затем катализатор отфильтровывают и фильтрат концентрируют в вакууме. Выход: 3,9 г (96%). Значение Rf: 0,36 (оксид алюминия; дихлорметан/этанол в соотношении 98:2).(г) Гидрохлорид 3-аминотетрагидрофуран-3-карбоновой кислоты. 3,5 г (15,1 ммоль) 3-трет-бутоксикарбониламинотетрагидрофуран-3-карбоновой кислоты растворяют в 150 мл 1-молярной соляной кислоты и в течение 1 ч перемешивают при комнатной температуре. После этого реакционную смесь лиофилизируют. Выход: 2,5 г (100%).(д) 3-[(5-Бромтиофен-2-ил)карбониламино]тетрагидрофуран-3-карбоновая кислота. 3,1 г (14,9 ммоль) 5-бромтиофен-2-карбоновой кислоты при перемешивании и при комнатной температуре смешивают в 50 мл дихлорметана с 5,4 мл (74,6 ммоль) тионилхлорида и перемешивают в течение 3,5 ч при нагревании с обратным холодильником. После этого реакционную смесь концентрируют досуха. 2,5 г (14,9 ммоль) гидрохлорида 3-аминотетрагидрофуран-3-карбоновой кислоты растворяют в 2,0 мл (14,9 ммоль) ТЭА и 150 мл ацетонитрила, при перемешивании смешивают с 5,9 мл (22,4 ммоль)N,О-бис-(триметилсилил)трифторацетамида и в течение 4 ч перемешивают при нагревании с обратным холодильником. Далее реакционную смесь смешивают с 4,1 мл (29,8 ммоль) ТЭА и раствором полученного хлорангидрида кислоты в 50 мл ацетонитрила, в течение 15 мин перемешивают при нагревании с обратным холодильником и затем медленно охлаждают до комнатной температуры. После этого досуха концентрируют в вакууме, остаток смешивают с водой и 2-молярным раствором карбоната натрия и промывают диэтиловым эфиром. Водную фазу подкисляют 20 мл конц. соляной кислоты до pH 1, осадок отделяют вакуум-фильтрацией и сушат в вакуумном сушильном шкафу при 50C. Выход: 3,6 г (75%).(е) Амид 3-[(5-бромтиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин 7-ил)тетрагидрофуран-3-карбоновой кислоты. 700,0 мг (2,19 ммоль) 3-[(5-бромтиофен-2-ил)карбониламино]тетрагидрофуран-3-карбоновой кислоты при перемешивании и при комнатной температуре смешивают в 10 мл ДМФ с 890,0 мг(2,34 ммоль) ГАТУ и 601,0 мкл (5,47 ммоль) N-MM и перемешивают в течение 10 мин. После этого добавляют 385,0 мг (2,19 ммоль) 3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-иламина и смесь оставляют перемешиваться на ночь при 65C. Далее реакционную смесь смешивают с водой и насыщ. раствором гидрокарбоната натрия, осадок отфильтровывают и очищают хроматографией на оксиде алюминия(а) Бензиловый эфир 3-[(5-хлортиофен-2-ил)карбониламино]тетрагидрофуран-3-карбоновой кислоты. 1,59 г (9,8 ммоль) 5-хлортиофен-2-карбоновой кислоты растворяют в 30 мл ДМФ и при комнатной температуре в течение 20 ч перемешивают с 3,61 г (10,7 ммоль) бензилового эфира 3 аминотетрагидрофуран-3-карбоновой кислоты, 3,46 г (10,8 ммоль) ТБТУ и 4,3 мл (39 ммоль) N-MM. После этого концентрируют и очищают хроматографией на силикагеле (элюент: дихлорметан/этанол в соотношении от 100:0 до 94:6). Выход: количественный. Значение Rf: 0,59 (силикагель; дихлорметан/этанол в соотношении 9:1).(б) 3-[(5-Хлортиофен-2-ил)карбониламино]тетрагидрофуран-3-карбоновая кислота. 3,6 г (9,8 ммоль) бензилового эфира 3-[(5-хлортиофен-2-ил)карбониламино]тетрагидрофуран-3 карбоновой кислоты растворяют в 60 мл этанола, смешивают с 39,1 мл (39,1 ммоль) 1-молярного водного раствора едкого натра и в течение 6 ч перемешивают при комнатной температуре. После концентрирования в вакууме остаток при охлаждении на ледяной бане смешивают с 1-молярной водной соляной кислотой, осадок отделяют вакуум-фильтрацией и сушат в вакуумном сушильном шкафу при 60C.(в) Амид 3-[(5-хлортиофен-2-ил)карбониламино]-N-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин 7-ил)тетрагидрофуран-3-карбоновой кислоты. Указанное соединение получают аналогично примеру 2(a) из 3-[(5-хлортиофен-2 ил)карбониламино]тетрагидрофуран-3-карбоновой кислоты и 3-метил-2,3,4,5-тетрагидро-1Hбензо[d]азепин-7-иламина с использованием ТБТУ и ТЭА в ТГФ при комнатной температуре с последующей очисткой хроматографией на оксиде алюминия (элюент: дихлорметан/этанол в соотношении от 100:0 до 97:3). Выход: 67%. Значение Rf: 0,63 (оксид алюминия; дихлорметан/этанол в соотношении 95:5).(а) 2-(5-Хлортиофен-2-ил)-4,4-диметил-4H-оксазол-5-он. 1,0 г (4,0 ммоль) 2-[(5-хлортиофен-2-ил)карбониламино]-2-метилпропионовой кислоты в 30 мл уксусного ангидрида в течение 1 ч перемешивают при 85C. После этого реакционную смесь концентрируют досуха. Выход: 927,3 мг (100%).(10,0 мкмоль) ДИПЭА, после чего нагревают до 80C, оставляют на ночь при этой температуре и затем оставляют стоять в течение 2 дней при комнатной температуре. Далее реакционный раствор фильтруют через основный оксид алюминия и фильтрат концентрируют в вакууме. Выход: количественный. Значение Rt: 3,31 мин (ЖХВР-МС, метод 1).(а) 2-[(5-Хлортиофен-2-ил)карбониламино]-2-метилпропионовая кислота. 4,5 г (27,7 ммоль) 5-хлортиофен-2-карбоновой кислоты при перемешивании и при комнатной температуре смешивают в 250 мл дихлорметана с 8,0 мл (110,7 ммоль) тионилхлорида и в течение 3 ч перемешивают при нагревании с обратным холодильником. После этого реакционную смесь концентрируют досуха. 2,9 г (27,7 ммоль) 2-аминоизомасляной кислоты при перемешивании смешивают в 300 мл ацетонитрила с 8,0 мл (30,4 ммоль) N,O-бис-(триметилсилил)трифторацетамида и в течение 3,5 ч перемешивают при нагревании с обратным холодильником. Далее реакционную смесь смешивают с 8,5 мл(60,9 ммоль) ТЭА и раствором полученного хлорангидрида кислоты в 75 мл ацетонитрила, после чего перемешивают в течение 15 мин при нагревании с обратным холодильником и затем медленно охлаждают до комнатной температуры. Далее реакционную смесь досуха концентрируют в вакууме, остаток смешивают с водой и 2-молярным раствором карбоната натрия и промывают диэтиловым эфиром. Водную фазу подкисляют с помощью 20 мл конц. соляной кислоты до pH 1, осадок отделяют вакуум- 22015188 фильтрацией и сушат в вакуумном сушильном шкафу при 50C. Выход: 5,9 г (86%).(б) N-1-Метил-1-[3-(2,2,2-трифторацетил)-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил]этиламид 5-хлортиофен-2-карбоновой кислоты. Указанное соединение получают аналогично примеру 2(в) из 2-[(5-хлортиофен-2 ил)карбониламино]-2-метилпропионовой кислоты и 3-(2,2,2-трифторацетил)-2,3,4,5-тетрагидро-1Hбензо[d]азепин-7-иламина с использованием ТБТУ и N-MM в ДМФ при комнатной температуре с последующей фильтрацией через оксид алюминия. Выход: (95%). Значение Rf: 0,65 (силикагель; дихлорметан/этанол в соотношении 9:1). 500,0 мг (1,03 ммоль) N-1-метил-1-[3-(2,2,2-трифторацетил)-2,3,4,5-тетрагидро-1H-бензо[d]азепин 7-илкарбамоил]этиламида 5-хлортиофен-2-карбоновой кислоты при перемешивании и при комнатной температуре смешивают в 15 мл метанола и 10 мл воды с 637,0 мг (4,61 ммоль) карбоната калия и в течение 3 ч перемешивают при нагревании с обратным холодильником. Далее реакционную смесь концентрируют в вакууме, остаток смешивают с водой, осадок отфильтровывают и сушат в вакуумном сушильном шкафу при 50C. Выход: 340,0 мг (85%). Значение Rf: 0,20 (силикагель; дихлорметан/метанол/конц. раствор аммиака в соотношении 80:20:2). 100,0 мг (0,26 ммоль) N-[1-метил-1-(2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амида 5-хлортиофен-2-карбоновой кислоты при перемешивании и при комнатной температуре смешивают в 5 мл ТГФ с 43,0 мкл (0,31 ммоль) ТЭА и 27,0 мкл (0,29 ммоль) уксусного ангидрида и в течение 2 ч перемешивают при комнатной температуре. Далее реакционную смесь смешивают с водой,осадок отфильтровывают и сушат в вакуумном сушильном шкафу при 50C. Выход: 80,0 мг (72%). Значение Rf: 0,90 (силикагель; дихлорметан/метанол/конц. раствор аммиака в соотношении 80:20:2). 100,0 мг (0,26 ммоль) N-[1-метил-1-(2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]амида 5-хлортиофен-2-карбоновой кислоты в 5 мл ацетона при перемешивании и при комнатной температуре смешивают с 74,0 мг (0,54 ммоль) карбоната калия и 21,0 мкл (0,26 ммоль) иодэтана и в течение 3 ч перемешивают при нагревании с обратным холодильником. Далее реакционную смесь при комнатной температуре смешивают с водой, осадок отфильтровывают и сушат в вакуумном сушильном шкафу при 50C.(а) Этиловый эфир 5-триметилсилилэтинилтиофен-2-карбоновой кислоты. Раствор 32,5 г (138,0 ммоль) этилового эфира 5-бромтиофен-2-карбоновой кислоты в 320 мл ацетонитрила и 640 мл ТГФ при перемешивании смешивают в атмосфере аргона с 1,3 г (7,0 ммоль) иодида меди(I) и 39,0 г (276,0 ммоль) триметилсилилацетилена, перемешивают в течение 5 мин и затем добавляют 5,6 г (7,0 ммоль) 1,1-бис-(дифенилфосфино)ферроцендихлорпалладий(II)-PdCl2 в комплексе сCH2Cl2 в соотношении 1:1 и 57,4 мл (414,0 ммоль) ТЭА. Далее реакционную смесь оставляют перемешиваться на ночь при комнатной температуре, после чего концентрируют в вакууме, остаток смешивают с этилацетатом и промывают раствором аммиака (5%-ным) и водой. Органическую фазу сушат над сульфатом натрия и досуха концентрируют в вакууме. Остаток смешивают с диэтиловым эфиром, осадок отделяют вакуум-фильтрацией и сушат. Выход: количественный. Значение Rf: 0,71 (силикагель; петролейный эфир/этилацетат в соотношении 8:2).(б) 5-Этинилтиофен-2-карбоновая кислота. Раствор 36,2 г (114,0 ммоль) этилового эфира 5-триметилсиланилэтинилтиофен-2-карбоновой кислоты в 185 мл этанола смешивают с 730,0 мл (1,46 моль) 2-молярного водного раствора едкого натра и оставляют перемешиваться на ночь при 50C. Далее реакционную смесь досуха концентрируют в вакууме, остаток смешивают с водой и промывают дихлорметаном. Водную фазу при охлаждении на ледяной бане подкисляют 6-молярной водной соляной кислотой, осадок отфильтровывают и сушат в вакуумном сушильном шкафу при 50C. Выход: 8,9 г (41%). Значение Rf: 0,64 (RP-8; метанол/раствор NaCl (5%-ный) в соотношении 6:4).(в) Метиловый эфир 2-[(5-этинилтиофен-2-ил)карбониламино]-2-метилпропионовой кислоты. Раствор 6,0 г (39,4 ммоль) 5-этинилтиофен-2-карбоновой кислоты в 180 мл ТГФ при перемешивании смешивают с 20,6 мл (118,3 ммоль) ДИПЭА и 13,9 г (43,3 ммоль) ТБТУ и перемешивают в течение 10 мин. Затем добавляют 6,1 г (39,4 ммоль) гидрохлорида метилового эфира 2-аминоизомасляной кислоты и оставляют перемешиваться на ночь при комнатной температуре. Далее реакционную смесь досуха концентрируют в вакууме, остаток смешивают с этилацетатом и промывают водой и раствором гидрокарбоната натрия (5%-ным). Органическую фазу сушат над сульфатом натрия и концентрируют в вакууме. Выход: 9,3 г (94%). Значение Rf: 0,71 (силикагель; дихлорметан/этанол в соотношении 9:1).(г) 2-[(5-Этинилтиофен-2-ил)карбониламино]-2-метилпропионовая кислота. 9,3 г (37,1 ммоль) метилового эфира 2-[(5-этинилтиофен-2-ил)карбониламино]-2-метилпропионовой кислоты растворяют в 550 мл воды и 370 мл ТГФ, смешивают с 74,2 мл (74,2 ммоль) 1-молярного водного раствора гидроксида лития и в течение 2 ч перемешивают при комнатной температуре. После этого ТГФ отгоняют в вакууме и экстрагируют дихлорметаном. Водную фазу подкисляют 3-молярной водной соляной кислотой, осадок отфильтровывают и сушат в вакуумном сушильном шкафу при 50C. Выход: 8,4 г (95%). Значение Rf: 0,20 (силикагель; дихлорметан/этанол в соотношении 9:1).(д) 2-(5-Этинилтиофен-2-ил)-4,4,-диметил-4H-оксазол-5-он. Указанное соединение получают аналогично примеру 3(а) из 2-[(5-этинилтиофен-2 ил)карбониламино]-2-метилпропионовой кислоты в уксусном ангидриде при 65C с последующей очи- 24015188 сткой хроматографией на силикагеле (элюент: петролейный эфир/этилацетат в соотношении 2:1). Выход: 3,1 г (84%). Значение Rf: 0,67 (силикагель; петролейный эфир/этилацетат в соотношении 7:3).(е) Амид 5-этинил-N-[1-метил-1-(3-метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)этил]тиофен-2-карбоновой кислоты. Раствор 150,0 мг (0,7 ммоль) 2-(5-этинилтиофен-2-ил)-4,4,-диметил-4H-оксазол-5-она в 7,5 мл толуола и 850,0 мкл уксусной кислоты при перемешивании смешивают с раствором 134,2 мг (0,8 ммоль) 3 метил-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-иламина в 8,5 мл ДМФ и оставляют перемешиваться на ночь при 65C. Далее реакционную смесь досуха концентрируют в вакууме, остаток растворяют в дихлорметане и этаноле и фильтруют через оксид алюминия. Фильтрат смешивают с водой, осадок отделяют вакуум-фильтрацией и сушат в вакуумном сушильном шкафу при 55C. Выход: 260,0 мг (96%). Значение Rf: 0,43 (RP-8; метанол/раствор NaCl (5%-ный) в соотношении 6:4).(а) 3-Трифторацетил-7-нитро-2,3,4,5-тетрагидро-1H-бензо[d]азепин. 12,5 г (51,39 ммоль) 3-трифторацетил-2,3,4,5-тетрагидро-1H-бензо[d]азепина в 30 мл уксусного ангидрида растворяют в 18,9 мл (352,0 ммоль) серной кислоты (конц.) и при температуре в пределах от -5 до 0C медленно смешивают с 3,6 мл (51,39 ммоль) азотной кислоты (65%), после чего перемешивают в течение 1 ч при 0C. Далее реакционную смесь сливают в воду, экстрагируют этилацетатом, органическую фазу сушат над сульфатом натрия и концентрируют досуха. Остаток перекристаллизовывают из этанола. Выход: 10,4 г (70%). Значение Rf: 0,78 (силикагель; дихлорметан/этанол в соотношении 95:5).(б) трет-Бутиловый эфир 7-нитро-2,3,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты. 5,0 г (17,34 ммоль) 3-трифторацетил-7-нитро-2,3,4,5-тетрагидро-1H-бензо[d]азепина в 50 мл ТГФ смешивают с 10,4 мл (20,81 ммоль) 2-молярного раствора едкого натра и в течение 30 мин перемешивают при комнатной температуре. Далее реакционный раствор смешивают с 1,88 г (17,69 ммоль) карбоната натрия и 5,0 мл воды, после чего при охлаждении на ледяной бане дозируют раствор 3,98 г (18,21 ммоль) ди-трет-бутилдикарбоната в 15 мл ТГФ и перемешивают в течение 1 ч при комнатной температуре. Затем отфильтровывают нарастворившееся вещество, фильтрат смешивают с этилацетатом и промывают насыщ. раствором хлорида натрия. Органическую фазу сушат над сульфатом натрия и фильтрат досуха концентрируют в вакууме. Выход: количественный. Значение Rf: 0,81 (силикагель; дихлорметан/этанол в соотношении 95:5).(в) 8-Нитро-1,3,4,5-тетрагидробензо[d]азепин-2-он и 7-нитро-1,3,4,5-тетрагидробензо[d]азепин-2-он. 5,1 г (17,3 ммоль) трет-бутилового эфира 7-нитро-2,3,4,5-тетрагидробензо[d]азепин-3-карбоновой кислоты в 50 мл этилацетата и 70 мл воды при интенсивном перемешивании смешивают с 8,9 г(41,63 ммоль) метапериодата натрия и 0,54 г (2,60 ммоль) хлорида рутенияH2O и в течение 3,5 ч пере- 25015188 мешивают при комнатной температуре. Затем отфильтровывают нарастворившееся вещество, фильтрат смешивают с этилацетатом и промывают раствором дисульфита натрия (10%-ным) и насыщ. раствором хлорида натрия. Органическую фазу сушат над сульфатом натрия и фильтрат досуха концентрируют в вакууме. Остаток растворяют в 60 мл дихлорметана, добавляют 6,0 мл ТФУК и оставляют перемешиваться на ночь. Далее реакционный раствор досуха концентрируют в вакууме, остаток смешивают с дихлорметаном, промывают водой и насыщ. раствором гидрокарбоната натрия, сушат над сульфатом натрия и досуха концентрируют в вакууме. Выход: 2,3 г (65%). Значение Rf: 0,52 (силикагель; дихлорметан/этанол в соотношении 9:1).(г) 8-Амино-1,3,4,5-тетрагидробензо[d]азепин-2-он и 7-амино-1,3,4,5-тетрагидробензо[d]азепин-2-он. 2,3 г (11,2 ммоль) 8-нитро-1,3,4,5-тетрагидробензо[d]азепин-2-она/7-нитро-1,3,4,5-тетрагидробензо[d]азепин-2-она растворяют в 40 мл метанола и смешивают с 300 мг 10%-ного Pd/C. После этого в течение 17 ч гидрируют в аппарате Парра при комнатной температуре и при давлении водорода 3 бара. Затем катализатор отфильтровывают и фильтрат концентрируют в вакууме. Выход: 1,51 г (77%). Значение Rf: 0,10 (силикагель; дихлорметан/этанол в соотношении 95:5).(д) N-[1-Метил-1-(4-оксо-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7-илкарбамоил)-1-метилэтил]амид 5-хлортиофен-2-карбоновой кислоты и N-[1-метил-1-(2-оксо-2,3,4,5-тетрагидро-1H-бензо[d]азепин-7 илкарбамоил)-1-метилэтил]амид 5-хлортиофен-2-карбоновой кислоты. Указанные соединения получают аналогично примеру 1 из 2-(5-хлортиофен-2-ил)карбониламино-2 метилпропионовой кислоты с использованием ГАТУ,N-MM и 8-амино-1,3,4,5 тетрагидробензо[d]азепин-2-она/7-амино-1,3,4,5-тетрагидробензо[d]азепин-2-она в ДМФ с последующей очисткой хроматографией на силикагеле (элюент: дихлорметан/этанол в соотношении от 100:0 до 92:8). Выход: количественный. Значение Rf: 0,40 (силикагель; дихлорметан/этанол в соотношении 9:1).C19H20ClN3O3S (405,90). Масс-спектр: (M+H)+=406/408 (изотопы хлора). Аналогично примеру 1 можно получить следующие соединения. Аналогично примеру 2 можно получить следующие соединения.
МПК / Метки
МПК: C07D 471/04, A61P 29/00, A61P 35/00, A61K 31/55, C07D 409/14, C07D 409/12, C07D 417/14, C07D 413/04, A61P 9/00, C07D 487/04
Метки: ингибирующим, глицинамиды, замещенные, фактор, действием, антитромботическим
Код ссылки
<a href="https://eas.patents.su/30-15188-zameshhennye-glicinamidy-s-antitromboticheskim-i-ingibiruyushhim-faktor-ha-dejjstviem.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные глицинамиды с антитромботическим и ингибирующим фактор хa действием</a>
Предыдущий патент: Гидромеханический щелевой перфоратор
Следующий патент: Ингибиторы киназы
Случайный патент: Производные пиримидинилпиридазинона












