Производные тиола, обладающие (ace/nep) ингибирующим действием на металлопептидазу
Номер патента: 2339
Опубликовано: 25.04.2002
Авторы: Сантанджело Франческо, Романьяно Стефано, Семераро Клаудио, Норчини Габриеле, Пеллачини Франко
Формула / Реферат
1. Соединение формулы
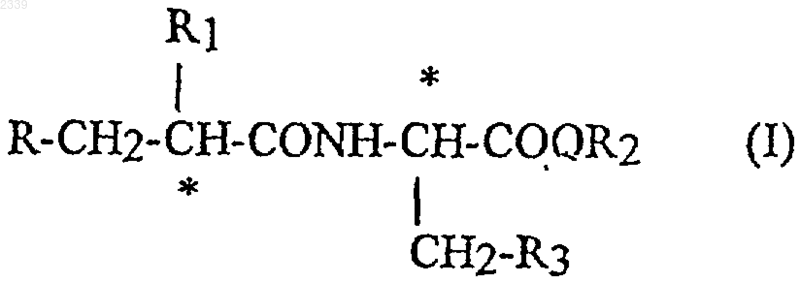
где R обозначает меркаптогруппу или группу R4COS, которая превращается в организме в меркаптогруппу,
R1 обозначает С2-С4алкильную группу с прямой или разветвленной цепью или арильную или арилалкильную группу, имеющую от 1 до 6 атомов углерода в алкильном фрагменте, где арил обозначает фенил или 5- или 6-членный ароматический гетероцикл с одним или двумя гетероатомами, выбранными из группы, включающей азот, кислород и серу, необязательно замещенный одним или несколькими одинаковыми или различными заместителями, выбранными из группы, включающей атомы галогена, гидроксигруппы, алкокси-, алкил-, алкилтио-, алкилсульфонил- или алкоксикарбонильные группы, которые имеют от 1 до 6 атомов углерода в алкильном фрагменте, С1-С3алкильные группы, которые содержат один или несколько атомов фтора, карбоксигруппы, нитрогрулпы, амино- или аминокарбонильные группы, ациламиногруппы, аминосульфонильные группы, моно- или диалкиламино- или моно- или диалкиламинокарбонильные группы, имеющие от 1 до 6 атомов в алкильном фрагменте,
R2 обозначает водород, С1-C4алкильную группу с прямой или разветвленной цепью или бензильную группу,
R3 обозначает 5- или 6-членный ароматический гетероцикл, который содержит один или два гетероатома, выбранных из группы, включающей азот, кислород и серу, необязательно сконденсированный с бензольным кольцом, необязательно замещенный фенильной группой, где фенильная и гетероциклическая группа необязательно замещены одним или двумя одинаковыми или различными заместителями, выбранными из группы, включающей атомы галогена, алкил-, алкокси-, алкилтио- или алкоксикарбонильные группы, которые имеют от 1 до 3 атомов углерода в алкильном фрагменте,
R4 обозначает С1-С4алкильную группу с прямой или разветвленной цепью или фенильную группу,
атомы углерода, помеченные звездочкой, являются стереогенными центрами,
и его фармацевтически приемлемые соли, при условии, что R3 не обозначает имидазолильную или индолильную группу.
2. Соединение формулы I по п.1, где R3 обозначает 5- или 6-членную ароматическую гетероциклическую группу, которая содержит один или два гетероатома, выбранных из группы, включающей азот, кислород и серу.
3. Соединение формулы I по п.2, где R1 обозначает фенилалкильную группу, необязательно замещенную одним или несколькими одинаковыми или различными заместителями, выбранными из группы, включающей атомы галогена, гидрокси-, алкил- или алкоксигруппы.
4. Соединение формулы I по п.1 в форме соли с щелочным металлом, выбранным из группы, включающей натрий, литий и калий.
5. Способ получения соединения формулы I по п.1, включающий взаимодействие между соединением формулы
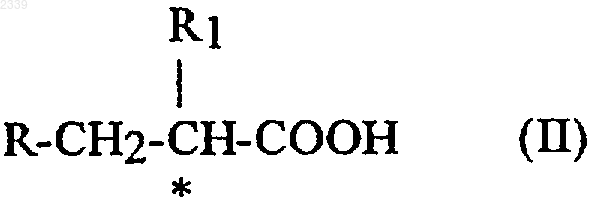
где R и R1 имеют значения, указанные в п.1, и производным аланина формулы

где R2 и R3 имеют значения, указанные в п.1.
6. Фармацевтическая композиция, содержащая терапевтически эффективное количество соединения формулы I по п.1 в смеси с носителем, предназначенная для фармацевтического применения.
7. Фармацевтическая композиция по п.6, предназначенная для лечения сердечно-сосудистых заболеваний.
8. Способ лечения сердечно-сосудистых заболеваний, включающий введение терапевтически эффективного количества соединения формулы I по п.1.
9. Метиловый эфир N-(3-фенилкарбонилтио-2-фенилметилпропионил)(4-тиазолил)-L-аланина.
10. Метиловый эфир N-(3-фенилкарбонилтио-2-фенилметилпропионил)(2-тиенил)-L-аланина.
11. Метиловый эфир N-(3-фенилкарбонилтио-2-фенилметилпропионил)(2-пиридил)-L-аланина.
12. N-(2-фенилметил-3-меркаптопропионил)(4-тиазолил)-L-аланин.
13. N-(2-фенилметил-3-меркаптопропионил)(2-тиенил)-L-аланин.
14. N-(2-фенилметил-3-меркаптопропионил)(2-пиридил)-L-аланин.
Текст
1 Настоящее изобретение относится к тиольным производным, обладающим ингибирующей активностью в отношении металлопептидаз, и в частности оно относится к производным N-меркаптоацилаланина, пригодным для лечения сердечно-сосудистых заболеваний. Интерес к изучению молекул, обладающих способностью ингибировать металлопептидазы,с точки зрения фармакологии обусловлен ролью указанных ферментов, проявляющейся на уровне сердечно-сосудистой системы. Хорошо известным является тот факт, что соединения, которые обладают ингибирующей активностью в отношении ангиотензинпревращающего фермента (АСЕ), весьма перспективны для лечения гипертензии, сердечной недостаточности и постинфарктного состояния благодаря тому, что они ингибируют образование ангиотензина II, представляеющего собой вещество, которое оказывает различные воздействия,в том числе увеличивает кровяное давление. Соединения, обладающие ингибирующей активностью в отношении эндотелинпревращающего фермента (ЕСЕ), пригодны в качестве антисосудосуживающих агентов, поскольку они ингибируют образование эндотелина, представляющего собой пептид, состоящий из 21 аминокислоты и обладающий сосудосуживающей активностью. И наоборот, соединения, обладающие ингибирующей активностью в отношении фермента нейтральная эндопептидаза (NEP), который также называют энкефалиназой, пригодны в качестве сосудорасширяющих агентов, поскольку фермент NEP ответственен за инактивацию не только эндогенного энкефалина, но также и некоторых натрийуретических факторов, среди которых, например, следует отметить предсердный фактор (предсердный натрийуретический фактор, ANF), гормон, секретируемый сердцем, который увеличивает расширение кровеносных сосудов и на почечном уровне повышает диурез и натрийурез. Таким образом, с учетом их разных механизмов действия на сердечно-сосудистую систему, соединения, обладающие ингибирующей активностью в отношении металлопептидаз,обычно используются по отдельности или в комбинации для лечения гипертензии, почечной недостаточности, застойной сердечной недостаточности и ишемических кардиопатологий. Из тиольных производных, обладающих ингибирующей активностью в отношении металлопептидаз, в качестве соединений-аналогов для NEP-ингибиторов и АСЕ-ингибиторов соответственно рассматривают тиорфан [(DL)-(3 меркапто-2-бензилпропаноил)глицин], впервые описанный Request и др. в Nature, том 288, стр. 286-288 (1980), и каптоприл (The Merck Index,XI изд.,1773, стр. 267) соответственно. В литературе описаны другие имеющие тиольное строение молекулы, которые обладаютN-Меркаптоацильные дипептиды, обладающие ингибирующей активностью в отношении ЕСЕ, в частности N-меркаптоацильные производные триптофана, описаны у S.R. Bertenshaw и др. в BioorganicMedicinal ChemistrySons, Inc.) описаны меркаптоалканоильные аминокислоты, обладающие ингибирующей активностью в отношении энкефалиназы. В патенте США 4199512 (E.R. SquibbSons, Inc.) описаны меркаптоалканоильные аминокислоты, обладающие ингибирующей активностью в отношении АСЕ. В европейской заявке 0566157 (ScheringCorporation) описаны N-меркаптоапильные производные аланина, обладающие ингибирующей активностью в отношении NEP. В европейской заявке 0449523 (E.R. SquibbSons, Inc.) описаны меркапто- или ацилтиотрифторметиламиды, обладающие ингибирующей активностью в отношении NEP. В европейской заявке 0524553 [Institut National de la Sante et de la Recherche Medicale(INSERM)] описаны ацилмеркаптоалканоилдипептиды, обладающие ингибирующей активностью в отношении нейтральной эндопептидазы и пептидилпептидазы А. В международной заявке WO 93/08162ACE/NEP-ингибирующей активностью. В европейской заявке 0419327 (Societe Civile Bioproject) описаны производные аминокислот, такие как, например, N-меркаптоацильные производные фенилаланина, гистидина и триптофана, обладающие ингибирующей активностью в отношении энкефалиназы и в отношении АСЕ.-Меркаптоацильные дипептиды, обладающие ингибирующей активностью в отношении АСЕ и NEP, также описаны у S.S. Bhagwat и др. в BioorganicMedicinal Chemistry Letters, 7,735-738, 1995. В этой последней работе авторами сделано заключение, что присутствие бифенилметильной группы придает представляющую интерес смешанную ACE/NEP-ингибирующую активность молекулам, имеющим строение меркаптоацильного дипептида, замещение бифенильной группы такими группами, как - или-нафтил, приводит к существенному снижению активности. Согласно настоящему изобретению были обнаружены производные N-меркаптоацилаланина, которые обладают выраженной ингибирующей активностью в отношении ангиотен 3 зинпревращающего фермента, а также фермента нейтральная эндопептидаза (двойная ACE/NEPингибирующая активность), что делает их особенно пригодными для лечения сердечнососудистых патологий. Таким образом, объектом настоящего изобретения являются соединения формулы где R обозначает меркаптогруппу или группуR4COS, которая превращается в организме в меркаптогруппу,R1 обозначает С 2-С 4 алкильную группу с прямой или разветвленной цепью или арильную или арилалкильную группу, имеющую от 1 до 6 атомов углерода в алкильном фрагменте, где арил обозначает фенил или 5- или 6-членный ароматический гетероцикл с одним или двумя гетероатомами, выбранными из группы, включающей азот, кислород и серу, необязательно замещенный одним или несколькими одинаковыми или различными заместителями, выбранными из группы, включающей атомы галогена,гидроксигруппы, алкокси-, алкил-, алкилтио-,алкилсульфонил- или алкоксикарбонильные группы, которые имеют от 1 до 6 атомов углерода в алкильном фрагменте, C1-С 3 алкильные группы, которые содержат один или несколько атомов фтора, карбоксигруппы, нитрогруппы,амино- или аминокарбонильные группы, ациламиногруппы, аминосульфонильные группы,моно- или диалкиламино- или моно- или диалкиламинокарбонильные группы, имеющие от 1 до 6 атомов в алкильном фрагменте,R2 обозначает водород, С 1-С 4 алкильную группу с прямой или разветвленной цепью или бензильную группу,R3 обозначает 5- или 6-членный ароматический гетероцикл, который содержит один или два гетероатома, выбранных из группы, включающей азот, кислород и серу, необязательно замещенный фенильной группой, где фенильная и гетероциклическая группа необязательно замещены одним или двумя одинаковыми или различными заместителями, выбранными из группы, включающей атомы галогена, алкил-,алкокси-, алкилтио- или алкоксикарбонильные группы, которые имеют от 1 до 3 атомов углерода в алкильном фрагменте,R4 обозначает С 1-С 4 алкильную группу с прямой или с разветвленной цепью или фенильную группу,атомы углерода, помеченные звездочкой, являются стереогенными центрами,и их фармацевтически приемлемые соли,при условии, что R3 не обозначает имидазолильную или индолильную группу. Соединения формулы I содержат два стереогенных центра и поэтому могут находиться в форме стереоизомеров. 4 Таким образом, объектом настоящего изобретения являются соединения формулы I в форме стереоизомерной смеси, а также в форме отдельных стереоизомеров. Соединения формулы I по изобретению обладают двойной ACE/NEP-ингибирующей активностью и пригодны для лечения сердечнососудистых заболеваний. В контексте настоящего описания, если не указано иное, под понятием "алкильная группа с прямой или разветвленной цепью" подразумевают алкил, такой как метил, этил, н-пропил,изопропил, н-бутил, втор-бутил, трет-бутил,изобутил, н-пентил, 2-пентил, 3-пентил, изопентил, трет-пентил, н-гексил и изогексил; под понятием "алкоксигруппа с прямой или разветвленной цепью" подразумевают алкоксигруппу,такую как метокси, этокси, н-пропокси и изопропокси; под понятием "атом галогена" подразумевают атом фтора, хлора, брома или йода; под понятием "ацил" подразумевают ацильную группу, происходящую из алифатической или ароматической карбоновой кислоты, такой как уксусная, пропионовая, масляная и бензойная кислота; под понятием "5- или 6-членный ароматический гетероцикл с 1 или 2 гетероатомами, выбранными из группы, включающей азот,кислород и серу", подразумевают такую группу,как тиазол, изоксазол, оксазол, изотиазол, пиразол, имидазол, тиофен, пиррол, пиридин, пиримидин, пиразин, пиридазин и фуран, необязательно сконденсированный с бензольным кольцом. Примерами фармацевтически приемлемых солей соединений формулы I являются соли щелочных или щелочно-земельных металлов и соли фармацевтически приемлемых органических оснований. Предпочтительными соединениями формулы I являются соединения, в которых R3 обозначает 5- или 6-членную ароматическую гетероциклическую группу, которая содержит один или два гетероатома, выбранных из группы,включающей азот, кислород и серу. Еще более предпочтительными соединениями в этом классе являются соединения формулы I, у которых R1 обозначает фенилалкильную группу, необязательно замещенную одним или несколькими одинаковыми или различными заместителями, выбранными из группы, включающей атомы галогена, гидрокси-, алкил- или алкоксигруппы. Предпочтительными примерами фармацевтически приемлемых солей соединений формулы I являются соли щелочных металлов,таких как натрий, литий и калий. Для специалиста в данной области очевидно, что соединения формулы I, у которых R обозначает группу R4COS, обладают способностью превращаться в организме в соединения, у которых R обозначает меркаптогруппу, а соединения формулы I, у которых R2 обозначает алкильную 5 или бензильную группу, являются биологическими предшественниками (пролекарствами) соответствующих соединений формулы I, у которых R обозначает меркаптогруппу (R=SH) или R2 обозначает атом водорода (R2=Н) соответственно. Конкретные примеры предпочтительных соединений формулы I по изобретению включают метиловый эфир N-(3-фенилкарбонилтио 2-фенилметилпропионил)(2-тиенил)аланина; метиловый эфир N-(3-фенилкарбонилтио 2-фенилметилпропионил)(4-тиазолил)аланина; метиловый эфир N-(3-фенилкарбонилтио 2-фенилметилпропионил)(2-пиридил)аланина; метиловый эфир N-(3-фенилкарбонилтио 2-фенилметилпропионил)(3-пиридил)аланина; метиловый эфир N-(3-фенилкарбонилтио 2-фенилметилпропионил)(2-фурил)аланина;(2-фурил)аланин. Получение предлагаемых соединений формулы I проводят в соответствии со способом синтеза, включающим взаимодействие между соединением формулы где R и R1 имеют указанные выше значения, и производным аланина формулы где R2 и R3 имеют указанные выше значения. Реакцию конденсации проводят в соответствии со способами, общепринятыми в химии пептидов. До проведения реакции может оказаться полезным соответствующим образом защитить необязательные функциональные группы, которые могут мешать взаимодействию. Необязательную защиту проводят общепринятыми способами. В отношении соединений, у которых R обозначает группу R4COS, предпочтительно использовать в качестве промежуточных веществ соединения формулы II, получая, таким образом, соответствующие соединения формулы I, у которых R обозначает группу R4COS, из которых путем гидролиза могут быть получены соединения формулы I, у которых R обозначает группу SH. Оценка пригодности необязательной защиты, а также выбор приемлемого типа защиты, 002339 6 соответствующего проводимой реакции и функциональным группам, подлежащим защите, хорошо известны специалистам в данным области. Удаление необязательных защитных групп проводят в соответствии с общепринятыми способами. Общие примеры применения защитных групп в органической химии можно найти уSons, Inc., 2 изд., 1991. Соединения формул II и III являются известными или легко могут быть получены общепринятыми способами. Например, соединения формулы II могут быть получены согласно описанию к патенту Великобритании 1576161, выданному на имяE.R. SquibbSons, Inc. Соединения формулы I в форме отдельных стереоизомеров получают путем стереоселективного синтеза или разделения стереоизомерной смеси в соответствии с общепринятыми способами. Получение солей предлагаемых соединений формулы I также проводят в соответствии с общепринятыми способами. Соединения формулы I по изобретению проявляют двойную ACE/NEP-ингибирующую активность и пригодны для лечения сердечнососудистых заболеваний. Ингибирующую активность соединений формулы I оценивали в опытах in vitro. В частности, ингибирующую активность соединений формулы I оценивали в сравнении с вышеуказанными тиорфаном и каптоприлом. Обнаруженная ингибирующая активностьin vitro соединений формулы I, выраженная в виде значения IC50, является важной с фармакологической точки зрения, поскольку проявляется в наномолярных концентрациях. Обнаруженная ингибирующая активность в отношении АСЕ оказалась сопоставимой с активностью каптоприла, а ингибирующая активность в отношении NEP оказалась сопоставимой с активностью тиорфана. Для практического применения в терапии на основе соединений формулы I могут быть изготовлены твердые или жидкие фармацевтические композиции, пригодные для орального или парентерального введения. Таким образом, фармацевтические композиции, содержащие терапевтически эффективное количество соединения формулы I в смеси с носителем, предназначенные для фармацевтического применения, являются еще одним объектом настоящего изобретения. Конкретными примерами фармацевтических композиций по настоящему изобретению являются таблетки, таблетки с покрытием, капсулы, грануляты, растворы и суспензии, пригодные для орального введения, а также раство 7 ры и суспензии, пригодные для парентерального введения. Фармацевтические композиции по изобретению получают в соответствии с общепринятыми способами. Суточная доза соединения формулы I или соответствующего пролекарства может зависеть от ряда факторов, таких как серьезность заболевания, индивидуальная реакция пациента или тип композиции, но она обычно находится в диапазоне от 0,1 до 10 мг на кг веса тела и может применяться в виде однократной дозы или может быть разделена на несколько суточных доз. Ниже изобретение проиллюстрировано на примерах. Если не указано иное, быструю хроматографию проводили с использованием силикагеля для быстрой хроматографии фирмы Baker(код 7024-00). Пример 1. Получение метилового эфира N(3-фенилкарбонилтио-2-фенилметилпропионил)(4-тиазолил)-L-аланина (соединение 1). Раствор гидроксибензотриазола (1,25 г; 9,25 ммоля) в тетрагидрофуране (30 мл), а затем раствор дициклогексилкарбодиимида (1,81 г; 9,25 ммоля) в метиленхлориде (10 мл) добавляли при перемешивании при 0 С к смеси, содержащей 3-фенилкарбонилтио-2-фенилметилпропионовую кислоту (2,78 г; 9,25 ммоля), метиловый эфир (4-тиазолил)-L-аланина (2,40 г; 9,25 ммоля), полученный обработкой метилового эфира N-трет-бутоксикарбонил-(4-тиазолил)-Lаланина (поставляемого фирмой Sinthetech Inc.(25 мл) и в метиленхлориде (40 мл). Реакционную смесь выдерживали при перемешивании при комнатной температуре в течение 20 ч, затем отфильтровывали дициклогексилмочевину и растворитель выпаривали при пониженном давлении. Остаток собирали этилацетатом и раствор промывали 20%-ным водным раствором хлорида натрия, 5%-ным раствором бикарбоната натрия и еще раз 20%-ным раствором хлорида натрия. После разделения фаз и упаривания органической фазы образовавшееся твердое вещество очищали экспресс-хроматографией (силикагель, элюент этилацетат:гексан в соотношении 1:1, давление азота 0,1 атм.), получая таким образом метиловый эфир N-(3 фенилкарбонилтио-2-фенилметилпропионил)(4 тиазолил)-L-аланина (3,85 г; выход 88%) в виде маслянистого продукта. После обработки маслянистого продукта этиловым эфиром и гексаном и последующей фильтрации получали требуемый продукт в виде твердого вещества (2,2 г; соотношение стереоизомеров 2S:2R = 85:15). 1 8 6,53 (s, 1 Н, NH); 7,15-7,90 (m, 10 Н, фенил); 6,928,51 (m, 2H, тиазолил). Из маточных растворов выделяли дополнительную фракцию соединения 1 (1,5 г; соотношение стереоизомеров 2S:2R = 65:35) в виде маслянистого продукта. Аналогичным путем получали следующие соединения: метиловый эфир N-(3-фенилкарбонилтио 2-фенилметилпропионил)(2-тиенил)-L-аланина(соединение 4). Метиловый эфир N-(3-фенилкарбонилтио 2-фенилметилпропионил)(4-тиазолил)-L-аланина (1,20 г; 2,56 ммоля), полученный согласно примеру 1, суспендировали в этаноле (30 мл),дегазировали, барботируя азотом, для удаления кислорода. К суспензии при 0 С добавляли в атмосфере азота по каплям водный дегазированный 1 н. раствор гидроксида натрия (7,68 мл). Реакционную смесь выдерживали при перемешивании в течение 4 ч при комнатной температуре, затем охлаждали до 0 С и подкисляли 10%-ным раствором соляной кислоты (5 мл) и предварительно дегазированной водой (5 мл). Реакционную смесь упаривали досуха при пониженном давлении и остаток собирали ацетонитрилом и еще раз упаривали досуха. Остаток,собранный смесью метанол:метиленхлорид в соотношении 1:1 (15 мл), фильтровали с целью удаления неорганических солей и раствор упаривали досуха при пониженном давлении. Затем остаток собирали водой, содержащей соляную кислоту (20 мл) и метиленхлорид (20 мл). Фазы разделяли и органическую фазу упаривали досуха при пониженном давлении, получая остаток (0,81 г), из которого после обработки третбутиловым эфиром, фильтрации и сушки получили N-(2-фенилметил-3-меркаптопропионил)(m, 1H, CHCOO); 6,51 (d, 1H, JHH=5,8 Гц,CONH); 7,09=7,30 [m, 6H, фенил, СН(тиазолил)]; 8,85 [d, 1H, JHH=2,0 Гц, СН(тиазолил)]. Аналогичным путем получали следующие соединения:(част./млн): 1,78-1,86 (m, 1H, SH); 2,20-2,89 (m,5 Н, СH2-СН-СH2); 2,95-3,26 (m, 2H, СH2 пиридил); 4,64-4,75 (m, 1H, СНСОО); 8,33 (d,1H, JHH=8,1 Гц, NH); 7,10-8,47 (m, 9H, ароматич.); 12,7 (bs, 1H, СООН). Пример 3. Оценка фармакологической активности in vitro. а) Ингибирующая активность в отношенииNEP оценивали на мембранах коркового слоя почки крыс, полученных в соответствии со способом, описанным у Т. Maeda и др. в Biochim.Biophys. Acta 1983, 731(1), 115-120. У самцов крыс линии Sprague-Dawley весом примерно 300 г удаляли почки и выдерживали при 4 С. Корковый слой почки осторожно выделяли, тонко измельчали и суспендировали в гомогенизирующем буфере (10 мМ фосфат натрия, рН 7,4, содержащий 1 мМ MgCl2, 30 мМNaCl, 0,02% NаN3) в концентрации 1:15 мас./об. Затем ткань гомогенизировали на холоде в течение 30 с с использованием гомогенизатора типа Ultra-Turrax. Приблизительно 10 мл гомогената наслаивали на 10 мл сахарозы (41% мас./об.) и центрифугировали при 31200 об./мин в течение 30 мин при 4 С с фиксированным углом ротора. Мембраны собирали с поверхности буфера/сахарозы, дважды промывали 50 мМ трис-НСl-буфером (рН 7,4) и ресуспендировали в этом же буфере для хранения до использования в виде аликвотных количеств при -80 С. Ингибирующую активность в отношении NEP оценивали в соответствии с методом, описанным у С.Llorens и др. в Eur. J. Pharmacol. 69,(1981), 113-116, как представлено в данном описании. Аликвотные количества суспензии мембран, полученные по описанной выше методике,(концентрация протеинов 5 мкг/мл) предварительно инкубировали в присутствии ингибитора аминопептидазы (Бестатин -1 мМ) в течение 10 мин при 30 С. Добавляли [3 Н] [Leu5]-энкефалин(15 нМ) и трис-НСl-буфер, рН 7,4 (50 мМ), таким образом, чтобы получить конечный объем 100 мкл. Через 20 мин инкубацию при 30 С прекращали, добавляя 0,1 M HCl (100 мкл). Образование метаболита [3H]Tyr-Gly-Gly количественно оценивали после отделения непрореагировавшего субстрата с помощью хроматографии на полистироловых колонках (Porapak Q),измеряя относительную радиоактивность с помощью жидкостного сцинтиляционного счетчика. Процент ингибирования образования метаболита в препаратах мембран, обработанных соединениями формулы I и соединениямиэталонами, по сравнению с необработанными препаратами мембран выражали в виде значения IС 50 (нМ). б) Ингибирующая активность в отношении АСЕ. Ингибирующую активность в отношении АСЕ оценивали в соответствии с методом, известным из литературы [B.Holmquist и др. Analytical Biochemistry, 95, 540-548 (1979)]. 50 мкМ АСЕ (250 миллиед./мл, выделенный из легкого кролика, КФ 3.4.15.1, фирмаSIGMA) предварительно инкубировали в термостатированных кюветах при 37 С с 50 мкл соединения формулы I или соединения-эталона,или соответствующего носителя. Реакцию начинали добавлением 500 мкл 0,8 мМ фурилакрилоилфенилаланилглицилглицина(FAPGGSIGMA). Одновременно с помощью спектрофотометра типа Beckman DU-50, снабженного программой для расчета дельта А/мин и коэффициентов регрессии кривых, описывающих кинетику фермента, непрерывно в течение 5 мин регистрировали поглощение при 340 нм. Процент ингибирования фермента в препаратах, обработанных соединениями формулыI или соединениями-эталонами, по сравнению с препаратами, которые инкубировали с носителем, выражали в виде значения IC50 (нМ). Ниже в таблице приведены значения IC50 Данные, приведенные в таблице, показывают, что предлагаемые соединения формулы I обладают выраженной двойной ACE/NEPингибирующей активностью. Выявленная активность сопоставима с активностью каптоприла в отношении АСЕ-ингибирующей активности и с активностью тиорфана в отношении где R обозначает меркаптогруппу или группуR4COS, которая превращается в организме в меркаптогруппу,R1 обозначает С 2-С 4 алкильную группу с прямой или разветвленной цепью или арильную или арилалкильную группу, имеющую от 1 до 6 атомов углерода в алкильном фрагменте, где арил обозначает фенил или 5- или 6-членный ароматический гетероцикл с одним или двумя гетероатомами, выбранными из группы, включающей азот, кислород и серу, необязательно замещенный одним или несколькими одинаковыми или различными заместителями, выбранными из группы, включающей атомы галогена,гидроксигруппы, алкокси-, алкил-, алкилтио-,алкилсульфонил- или алкоксикарбонильные группы, которые имеют от 1 до 6 атомов углерода в алкильном фрагменте, С 1-С 3 алкильные группы, которые содержат один или несколько атомов фтора, карбоксигруппы, нитрогрулпы,амино- или аминокарбонильные группы, ациламиногруппы, аминосульфонильные группы,моно- или диалкиламино- или моно- или диалкиламинокарбонильные группы, имеющие от 1 до 6 атомов в алкильном фрагменте,R2 обозначает водород, С 1-C4 алкильную группу с прямой или разветвленной цепью или бензильную группу,R3 обозначает 5- или 6-членный ароматический гетероцикл, который содержит один или два гетероатома, выбранных из группы, включающей азот, кислород и серу, необязательно сконденсированный с бензольным кольцом, необязательно замещенный фенильной группой,где фенильная и гетероциклическая группа необязательно замещены одним или двумя одинаковыми или различными заместителями, выбранными из группы, включающей атомы галогена, алкил-, алкокси-, алкилтио- или алкоксикарбонильные группы, которые имеют от 1 до 3 атомов углерода в алкильном фрагменте,R4 обозначает С 1-С 4 алкильную группу с прямой или разветвленной цепью или фенильную группу, 12 атомы углерода, помеченные звездочкой, являются стереогенными центрами,и его фармацевтически приемлемые соли,при условии, что R3 не обозначает имидазолильную или индолильную группу. 2. Соединение формулы I по п.1, где R3 обозначает 5- или 6-членную ароматическую гетероциклическую группу, которая содержит один или два гетероатома, выбранных из группы, включающей азот, кислород и серу. 3. Соединение формулы I по п.2, где R1 обозначает фенилалкильную группу, необязательно замещенную одним или несколькими одинаковыми или различными заместителями,выбранными из группы, включающей атомы галогена, гидрокси-, алкил- или алкоксигруппы. 4. Соединение формулы I по п.1 в форме соли с щелочным металлом, выбранным из группы, включающей натрий, литий и калий. 5. Способ получения соединения формулыI по п.1, включающий взаимодействие между соединением формулы где R2 и R3 имеют значения, указанные в п.1. 6. Фармацевтическая композиция, содержащая терапевтически эффективное количество соединения формулы I по п.1 в смеси с носителем, предназначенная для фармацевтического применения. 7. Фармацевтическая композиция по п.6,предназначенная для лечения сердечнососудистых заболеваний. 8. Способ лечения сердечно-сосудистых заболеваний, включающий введение терапевтически эффективного количества соединения формулы I по п.1. 9. Метиловый эфир N-(3-фенилкарбонилтио-2-фенилметилпропионил)(4-тиазолил)-Lаланина. 10. Метиловый эфир N-(3-фенилкарбонилтио-2-фенилметилпропионил)(2-тиенил)-Lаланина. 11. Метиловый эфир N-(3-фенилкарбонилтио-2-фенилметилпропионил)(2-пиридил)-Lаланина. 12. N-(2-фенилметил-3-меркаптопропионил)(4-тиазолил)-L-аланин. 13. N-(2-фенилметил-3-меркаптопропионил)(2-тиенил)-L-аланин. 14. N-(2-фенилметил-3-меркаптопропионил)(2-пиридил)-L-аланин.
МПК / Метки
МПК: A61P 9/00, A61K 31/425, C07D 275/02
Метки: производные, ингибирующим, металлопептидазу, действием, тиола, обладающие
Код ссылки
<a href="https://eas.patents.su/7-2339-proizvodnye-tiola-obladayushhie-ace-nep-ingibiruyushhim-dejjstviem-na-metallopeptidazu.html" rel="bookmark" title="База патентов Евразийского Союза">Производные тиола, обладающие (ace/nep) ингибирующим действием на металлопептидазу</a>
Предыдущий патент: Сосуд для напитков
Следующий патент: Способ получения кислотных солей тровафлоксацина
Случайный патент: Управление трафиком в спутниковой системе передачи данных











