Замещенные индолиноны с ингибирующим действием по отношению к киназам и циклин/cdk-комплексам
Номер патента: 3532
Опубликовано: 26.06.2003
Авторы: Хеккель Армин, Вальтер Райнер, Редеманн Норберт, Грелль Вольфганг, Ван-Мэл Якобус К.А.
Формула / Реферат
1. Замещенные индолиноны общей формулы

в которой X обозначает атом кислорода,
R1 обозначает атом водорода или C1-C4алкоксикарбонильную группу,
R2 обозначает карбокси-, C1-C4алкоксикарбонильную или аминокарбонильную группу, где аминовый фрагмент может быть замещен одной либо двумя C1-C3алкильными группами и заместители могут быть идентичными или разными,
R3 обозначает необязательно замещенную атомом фтора, хлора либо брома, метильной, циано- или аминометильной группой фенильную группу,
R4 обозначает атом водорода или метильную группу и
R5 обозначает атом водорода,
необязательно замещенную карбокси- или C1-C3алкоксикарбонильной группой C1-C5алкильную группу или бензильную группу,
необязательно замещенную метильной группой C3-C7циклоалкильную группу,
необязательно замещенную метильной группой инданильную, пиридильную, оксазолильную, тиазолильную или имидазолильную группу, с которыми соответственно дополнительно через два смежных атома углерода может быть сконденсировано фенильное кольцо,
необязательно замещенную атомом фтора, хлора либо брома, метокси-, карбокси-, C1-C3алкилоксикарбонильной, нитро- или аминосульфонильной группой метилфенильную группу или диметоксифенильную группу, соединенную через атом углерода пирролидинильную или пиперидинильную группу, которые соответственно по атому азота замещены C1-C3алкильной группой,
фенильную группу, замещенную
трифторметоксигруппой, атомом фтора, хлора, брома либо иода, C1-C3алкоксигруппой, которая в положении 2 или 3 может быть замещена амино-, C1-C3алкиламино-, ди(C1-C3алкил)амино-, фенил-C1-C3алкиламино-, N-(C1-C3алкил)фенил-C1-C3алкиламино-, пирролидиновой или пиперидиновой группой, фенил-C1-C3алкиламино-C1-C3алкильной группой, которая замещена в фенильном ядре атомом фтора, хлора, брома либо иода, C1-C5алкильной, C1-C3алкокси- или трифторметильной группой и дополнительно по атому азота амина замещена C1-C3алкильной группой, в которой атомы водорода, начиная с положения 2, могут быть полностью либо частично заменены на атомы фтора, C1-C5алкильной, фенильной, имидазолильной, C3-C7циклоалкильной, C1-C3алкокси-C1-C3алкокси-, фенил-C1-C3алкокси-, карбокси-C1-C3алкильной, C1-C3алкоксикарбонил-C1-C3алкильной, карбокси-, C1-C3алкоксикарбонильной, аминокарбонильной, C1-C3алкиламинокарбонильной, ди(C1-C3алкил)аминокарбонильной, фенил-C1-C3алкиламинокарбонильной, N-(C1-C3алкил)фенил-C1-C3алкиламинокарбонильной, пиперазинокарбонильной, N-(C1-C3алкил)пиперазинокарбонильной, нитро-, амино-, C1-C3алкиламино-, ди(C1-C3алкил)амино-, пирролидиновой, пиперидиновой, морфолиновой, C2-C4алканоиламино-, N-(C1-C3алкил)-C2-C4алканоиламино-, бензоиламино- или N-(C1-C3алкил)бензоиламиногруппой,
N-(C1-C3алкил)-C2-C4алканоиламиногруппой, которая в алкильном фрагменте дополнительно замещена карбокси- либо C1-C3алкоксикарбонильной группой,
C1-C3алкиламинокарбонильной либо ди(C1-C3алкил)аминокарбонильной группой, в которых один алкильный фрагмент дополнительно замещен ди(C1-C3алкил)аминогруппой, или
N-(C1-C3алкил)-C1-C3алкилсульфониламино- либо N-(C1-C3алкил)фенилсульфониламиногруппой, в которых алкильный фрагмент дополнительно может быть замещен циано-, карбокси-, C1-C3алкоксикарбонильной, C1-C3алкиламино-, ди(C1-C3алкил)амино-, аминокарбонильной, C1-C3алкиламинокарбонильной, ди(C1-C3алкил)аминокарбонильной, пиперидинокарбонильной или 2-[ди(C1-C3алкиламино)]этиламинокарбонильной группой,
необязательно замещенную C1-C3алкильной группой фенильную группу, в которой алкильный фрагмент замещен гидрокси-, C1-C3алкокси-, карбокси-, C1-C3алкоксикарбонильной, амино-, C1-C5алкиламино-, ди(C1-C5алкил)амино-, C2-C4алканоиламино-, N-(C1-C3алкил)-C2-C4алканоиламино-, пирролидиновой, дегидропирролидиновой, пиперидиновой, дегидропиперидиновой, 3-гидроксипиперидиновой, 4-гидроксипиперидиновой, гексаметиленимино-, морфолиновой, тиоморфолиновой, пиперазиновой, 4-(C1-C3алкил)пиперазиновой, 4-фенилпиперазиновой, 4-(C2-C4алканоил)пиперазиновой, 4-бензоилпиперазиновой или имидазолильной группой,
при этом вышеуказанные насыщенные циклоалкилениминовые кольца, C1-C5алкиламино- или ди(C1-C5алкил)аминогруппы дополнительно могут быть замещены одной либо двумя C1-C5алкильными группами, C3-C7циклоалкильной, гидрокси-, C1-C3алкокси-, карбокси-, C1-C3алкоксикарбонильной, аминокарбонильной, C1-C3алкиламинокарбонильной или ди(C1-C3алкил)аминокарбонильной группой, в фенильном ядре - необязательно атомами фтора, хлора, брома либо иода, одно- либо двузамещенными C1-C3алкильными или цианогруппами фенил-C1-C3алкильной или фенильной группой, при этом заместители могут быть идентичными или разными, или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на карбонильную либо сульфонильную группу, а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома, метильной, амино-, C1-C3алкиламино- или ди(C1-C3алкил)аминогруппой,
или с одним из вышеуказанных незамещенных циклоалкилениминовых колец через два смежных атома углерода может быть сконденсировано необязательно замещенное одной либо двумя C1-C3алкоксигруппами фенильное кольцо,
а также их изомеры и их соли.
2. Замещенные индолиноны общей формулы I по п.1,
в которых X обозначает атом кислорода,
R1 обозначает атом водорода,
R2 обозначает карбокси-, C1-C4алкоксикарбонильную или аминокарбонильную группу, в которой аминовый фрагмент может быть замещен одной либо двумя C1-C3алкильными группами и заместители могут быть идентичными либо разными,
R3 обозначает необязательно замещенную метильной группой фенильную группу,
R4 обозначает атом водорода или метильную группу и
R5 обозначает атом водорода,
C1-C3алкильную группу, бензильную группу или замещенную карбокси-
либо C1-C3алкоксикарбонильной группой метильную или этильную группу,
необязательно замещенную метильной группой C3-C7циклоалкильную группу,
необязательно замещенную метильной группой инданильную, пиридильную, оксазолильную, тиазолильную шыш имидазолильную группу, с которыми соответственно дополнительно через два смежных атома углерода может быть сконденсировано фенильное кольцо,
необязательно замещенную атомом фтора, хлора либо брома, метокси-, карбокси-, C1-C3алкилоксикарбонильной, нитро- или аминосульфонильной группой метилфенильную либо диметоксифенильную группу,
3-пирролидинильную или 4-пиперидинильную группу, которые соответственно по атому азота замещены C1-C3алкильной группой,
фенильную группу, замещенную
трифторметокси-, бензилокси-, циано- или нитрогруппой, атомом фтора, хлора либо брома,
C1-C3алкоксигруппой, причем этокси- и н-пропоксигруппа, каждая соответственно, в концевом положении может быть замещена диметиламино-, диэтиламино-, N-этилметиламино-, N-бензилметиламино- либо пиперидиновой группой,
фенил-C1-C3алкиламино-C1-C3алкильной группой, которая может быть замещена в фенильном ядре атомом фтора, хлора, брома либо иода, метильной, метокси- или трифторметильной группой и дополнительно по атому аминного азота амина может быть замещена C1-C5алкильной либо 2,2,2-трифторэтильной группой, C1-C4алкильной, фенильной, имидазолильной, циклогексильной, метоксиметильной, карбоксиметильной, C1-C3алкоксикарбонилметильной, карбокси-, C1-C3алкоксикарбонильной, аминокарбонильной, C1-C3алкиламинокарбонильной, ди(C1-C3алкил)аминокарбонильной, фенил-C1-C3алкиламинокарбонильной, N-(C1-C3алкил)фенил-C1-C3алкиламинокарбонильной, пиперазинокарбонильной, N-(C1-C3алкил)пиперазинокарбонильной, амино-, C1-C3алкиламино-, ди(C1-C3алкил)амино-, пирролидиновой, пиперидиновой, морфолиновой, С2-C4алканоиламино-, N-(C1-C3алкил)-C2-C4алканоиламино-, бензоиламино- или N-(C1-C3)бензоиламиногруппой,
N-(C1-C3алкил)-C2-C4алканоиламиногруппой, которая в алкильном фрагменте дополнительно замещена карбокси- либо C1-C3алкоксикарбонильной группой,
C1-C3алкиламинокарбонильной или ди(C1-C3алкил)аминокарбонильной группой, в которых один алкильный фрагмент дополнительно замещен ди(C1-C3алкил)аминогруппой, или N-(C1-C3алкил)-C1-C3алкилсульфониламино- либо N-(C1-C3алкил)фенилсульфониламиногруппой, в которых алкильный фрагмент дополнительно может быть замещен циано-, карбокси-, C1-C3алкоксикарбонильной, C1-C3алкиламино-, ди(C1-C3алкил)амино-, аминокарбонильной, C1-C3алкиламинокарбонильной, ди(C1-C3алкил)аминокарбонильной, пиперидинокарбонильной или 2-[ди(C1-C3алкиламино)]этиламинокарбонильной группой, необязательно замещенную C1-C3алкильной группой фенильную группу, в которой алкильная группа замещена гидрокси-, C1-C3алкокси-, карбокси-, C1-C3алкоксикарбонильной, амино-, C1-C5алкиламино-, ди(C1-C5алкил) амино-, C2-C4алканоиламино-, N-(C1-C3алкил)-C2-C4алканоиламино-, пирролидиновой, дегидропирролидиновой, пиперидиновой, дегидропиперидиновой, 4-гидроксипиперидиновой, гексаметиленимино-, морфолиновой, тиоморфолиновой, пиперазиновой, 4-(C1-C3алкил)пиперазиновой, 4-фенилпиперазиновой, 4-(C2-C4алканоил)пиперазиновой, 4-бензоилпиперазиновой или имидазолильной группой,
при этом вышеуказанные насыщенные циклоалкилениминовые кольца дополнительно могут быть замещены фенильной группой либо одной или двумя метильными группами,
вышеуказанные C1-C5алкиламино- и ди(C1-C5алкил)аминогруппы дополнительно могут быть замещены одной либо двумя C1-C3алкильными группами, циклогексильной, гидрокси-, C1-C3алкокси-, карбокси-, C1-C3алкоксикарбонильной, аминокарбонильной, C1-C3алкиламинокарбонильной либо ди(C1-C3алкил)аминокарбонильной группой, необязательно замещенной в фенильном ядре атомом фтора, хлора, брома либо иода, метильной или цианогруппой фенил-C1-C3алкильной либо фенильной группой, или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на карбонильную либо сульфонильную группу, а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома, метильной, амино-, C1-C3алкиламино- или ди(C1-C3алкил)аминогруппой, или с одним из вышеуказанных незамещенных циклоалкилениминовых колец через два смежных атома углерода может быть сконденсировано необязательно замещенное одной или двумя C1-C3алкоксигруппами фенильное кольцо,
а также их изомеры и их соли.
3. Замещенные индолиноны общей формулы I по п.1,
в которых X обозначает атом кислорода,
R1 обозначает атом водорода,
R2 обозначает карбокси- или аминокарбонильную группу, в которой аминовый фрагмент может быть замещен одной либо двумя C1-C3алкильными группами и заместители могут быть идентичными либо разными,
R3 обозначает необязательно замещенную метильной группой фенильную группу,
R4 обозначает атом водорода и
R5 обозначает атом водорода,
3-пирролидинильную либо 4-пиперидинильную группу, замещенные соответственно по атому азота C1-C3алкильной группой,
фенильную группу, замещенную C1-C3алкоксигруппой, причем этокси- и н-пропоксигруппа, каждая соответственно, в концевом положении может быть замещена диметиламино-, диэтиламино-, N-этилметиламино-, N-бензилметиламино- либо пиперидиновой группой,
фенил-C1-C3алкиламино-C1-C3алкильной группой, которая может быть замещена в фенильном ядре атомом фтора, хлора, брома либо иода, метильной, метокси- или трифторметильной группой и дополнительно по атому азота амина также C1-C5алкильной либо 2,2,2-трифторэтильной группой,
необязательно замещенную C1-C3алкильной группой фенильную группу, в которой алкильная группа замещена гидрокси-, C1-C3алкокси-, карбокси-, C1-C3алкоксикарбонильной, амино-, C1-C5алкиламино-, ди(C1-C5алкил)амино-, C2-C4алканоиламино-, N-(C1-C3алкил)-C2-C4алканоиламино-, пирролидиновой, дегидропирролидиновой, пиперидиновой, дегидропиперидиновой, 4-гидроксипиперидиновой, гексаметиленимино-, морфолиновой, тиоморфолиновой, пиперазиновой, 4-(C1-C3алкил)пиперазиновой, 4-фенилпиперазиновой, 4-(C2-C4алканоил)пиперазиновой, 4-бензоилпиперазиновой или имидазолильной группой,
при этом вышеуказанные насыщенные циклоалкилениминовые кольца дополнительно могут быть замещены фенильной группой либо одной или двумя метильными группами,
вышеуказанные C1-C5алкиламино- и ди(C1-C5алкил)аминогруппы дополнительно могут быть замещены одной либо двумя C1-C3алкильными группами, циклогексильной, гидрокси-, C1-C3алкокси-, карбокси-, C1-C3алкоксикарбонильной, аминокарбонильной, C1-C3алкиламинокарбонильной лшсю ди(C1-C3алкил)аминокарбонильной группой, необязательно замещенной в фенильном ядре атомом фтора, хлора, брома либо иода, метильной или цианогруппой фенил-C1-C3алкильной либо фенильной группой, или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на карбонильную либо сульфонильную группу, а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома, метильной, амино-, C1-C3алкиламино- или ди(C1-C3алкил)аминогруппой, или с одним из вышеуказанных незамещенных циклоалкилениминовых колец через два смежных атома углерода может быть сконденсировано необязательно замещенное одной или двумя C1-C3алкоксигруппами фенильное кольцо,
а также их изомеры и их соли.
4. Замещенные индолиноны общей формулы I по любому из пп.1-3, в которых остаток R2 находится в положении 5.
5. Замещенные индолиноны общей формулы I по п.1, выбранные из группы, включающей
(а) 3-Z-[1-(4-аминометилфениламино)-1-фенилметилен]-5-амидо-2-индолинон,
(б) 3-Z-[1-фениламино-1-фенилметилен]-5-амидо-2-индолинон,
(в) 3-Z-[1-(4-бромфениламино)-1-фенилметилен]-5-амидо-2-индолинон,
(г) 3-Z-[1-(4-диметиламинометил)фениламино-1-фенилметилен]-5-амидо-2-индолинон,
(д) 3-Z-[1-(4-пирролидинометилфениламино)-1-фенилметилен]-5-амидо-2-индолинон,
(е) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-амидо-2-индолинон,
(ж) 3-Z-[1-(4-гексаметилениминометилфениламино)-1-фенилметилен]-5-амидо-2-индолинон,
(з) 3-Z-[1-(4-(4-бензилпиперидинометил)фениламино)-1-фенилметилен]-5-амидо-2-индолинон,
(и) 3-Z-[1-(4-(N-бутиламинометил)фениламино)-1-фенилметилен]-5-амидо-2-индолинон,
(к) 3-Z-[1-(4-(N-(фенилметил)аминометил)фениламино)-1-фенилметилен]-5-амидо-2-индолинон,
(л) 3-Z-[1-(4-(N-метил-N-бензиламинометил)фениламино)-1-фенилметилен]-5-амидо-2-индолинон,
(м) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-диметилкарбамоил-2-индолинон,
(н) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-диэтилкарбамоил-2-индолинон,
(о) 3-Z-[1-(4-(3-диэтиламинопропокси)фениламино)-1-фенилметилен]-5-амидо-2-индолинон,
и их соли.
6. Физиологически приемлемые соли соединений по любому из пп.1-5.
7. Лекарственные средства, содержащие в своем составе соединение по любому из пп.1-5 или соль по п.6 при необходимости наряду с одним либо несколькими инертными носителями и/или разбавителями.
8. Применение соединения по любому из пп.1-5 или соли по п.6 для изготовления соответствующего лекарственного средства, предназначенного для лечения избыточной или аномальной пролиферации клеток.
9. Способ получения лекарственного средства по п.7, отличающийся тем, что соединение по любому из пп.1-5 или соль по п.6 нехимическим путем вводят в один либо несколько инертных носителей и/или растворителей.
10. Способ получения соединений по любому из пп.1-6, отличающийся тем, что
а) соединение общей формулы
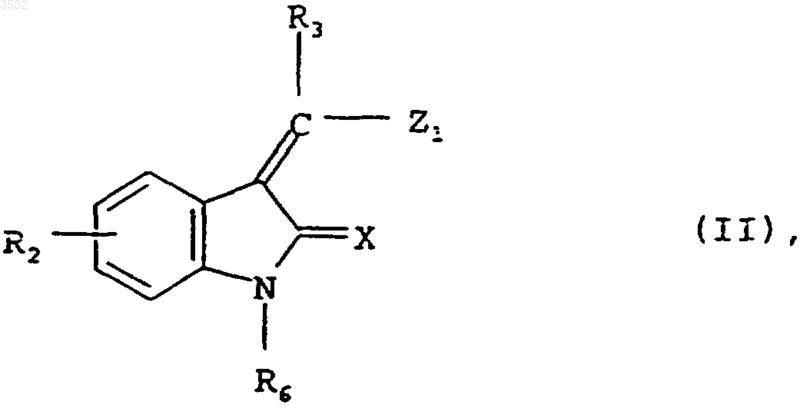
в которой X, R2 и R3 имеют значения, указанные в пп.1-6, R6 обозначает атом водорода, защитную группу для атома азота лактамовой группы или представляет собой связь с твердой фазой, a Z1 обозначает атом галогена, гидрокси-, алкокси- или аралкоксигруппу, подвергают взаимодействию с амином общей формулы

в которой R4 и R5 имеют значения, указанные в пп.1-6, и затем при необходимости отщепляют используемую для защиты атома азота лактамовой группы защитную группу или полученное таким путем соединение отщепляют от твердой фазы, или
б) для получения соединения общей формулы I, которое содержит аминометильную группу, а X представляет собой атом кислорода, восстанавливают соединение общей формулы
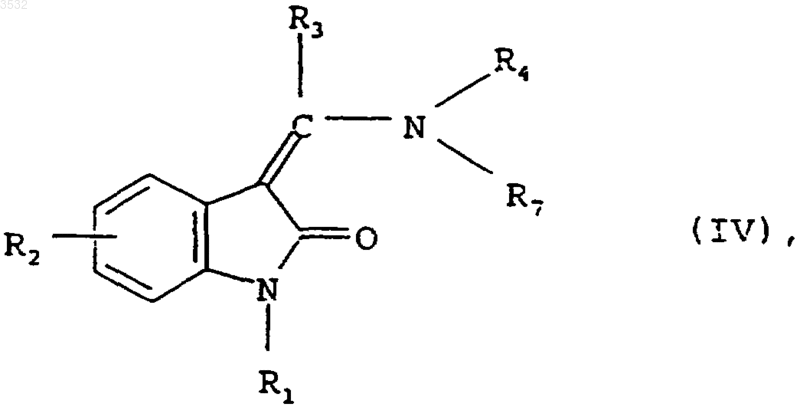
в которой R1-R4 имеют значения, указанные в пп.1-6, a R7 имеет значения, идентичные значениям R5, указанным в пп.1-6, при условии, что R5 содержит цианогруппу, и затем при необходимости полученное таким образом соединение общей формулы I, содержащее алкоксикарбонильную группу, путем гидролиза переводят в соответствующее карбоксисоединение, или полученное таким образом соединение общей формулы I, содержащее амино- или алкиламиногруппу, путем алкилирования либо восстановительного алкилирования, переводят в соответствующее алкиламино- либо диалкиламиносоединение, или
полученное таким образом соединение общей формулы I, содержащее амино- или алкиламиногруппу, путем ацилирования переводят в соответствующее ацильное соединение, или
полученное таким образом соединение общей формулы I, содержащее карбоксигруппу, путем этерификации либо амидирования переводят в соответствующее сложноэфирное либо аминокарбонильное соединение, или
при необходимости используемую во время реакций для защиты реакционноспособных групп защитную группу отщепляют, или
при необходимости полученное таким образом соединение общей формулы I разделяют затем на его стереоизомеры, или
полученное таким образом соединение общей формулы I переводят в его соли, прежде всего, в его физиологически приемлемые для применения в фармацевтике соли с неорганическими или органическими кислотами либо основаниями.
Текст
1 Настоящее изобретение относится к новым замещенным индолинонам общей формулы к их изомерам, их солям, прежде всего к их физиологически приемлемым солям, каковые соединения обладают ценными свойствами. Указанные соединения общей формулы I, в которой R1 обозначает атом водорода или пролекарственный остаток, обладают ценными фармакологическими свойствами, в частности ингибирующим действием по отношению к различным киназам, в первую очередь по отношению к комплексам CDK (CDK1, CDK2, CDK3,CDK4, CDK6, CDK7, CDK8 и CDK9) с их специфическими циклинами (A, B1, B2, С, D1, D2,D3, Е, F, G1, G2, Н, I и К) и по отношению к вирусному циклину (см. L. Mengtao в Journ. Virology 71(3), стр. 1984-1991 (1997, а остальные соединения приведенной выше общей формулыI, в которой R1 имеет значения, отличные от атома водорода и пролекарственного остатка,представляют собой ценные промежуточные продукты для получения соединений, названных первыми. Объектом настоящего изобретения являются в соответствии с этим вышеуказанные соединения общей формулы I, при этом соединения, в которых R1 обозначает атом водорода или пролекарственный остаток, обладают ценными фармакологическими свойствами, содержащие эти фармакологически эффективные соединения лекарственные средства, их применение и способ их получения. В вышеприведенной общей формуле I Х обозначает атом кислорода или серы, R1 обозначает атом водорода, С 1-С 4 алкоксикарбонильную или С 2-С 4 алканоильную группу,R2 обозначает карбокси-, С 1-С 4 алкоксикарбонильную или аминокарбонильную группу, где аминовый фрагмент может быть замещен одной либо двумя С 1-С 3 алкильными группами и заместители могут быть идентичными или разными,R3 обозначает фенильную либо нафтильную группу, которые могут быть замещены атомами фтора, хлора или брома, С 1-С 3 алкильными, С 1-С 3 алкокси-, циано-, трифторметильными, нитро-, амино-, С 1-С 3 алкиламино-, ди(С 1 С 3 алкил)амино-, С 2-С 4 алканоиламино-, N-(С 1 С 3 алкил)-С 2-С 4 алканоиламино-,N-(С 1-С 3 алкил)-С 2-С 4 алканоиламино-, С 1-С 3 алкилсульфониламино-, амино-С 1-С 3 алкильными, С 1-С 3 алкиламино-С 1-С 3 алкильными,ди(С 1-С 3 алкил) амино-С 1-С 3 алкильными,N-(С 2-С 4 алканоил) амино-С 1-С 3 алкильными или N-(С 2-С 4 алканоил)-С 1-С 3 алкиламино-С 1-С 3 алкильными группа 003532 2 ми и заместители могут быть идентичными или разными,R4 обозначает атом водорода или С 1-С 3 алкильную группу иR5 обозначает атом водорода,необязательно замещенную фенильной,карбокси- или С 1-С 3 алкоксикарбонильной группой С 1-С 5 алкильную группу, необязательно замещенную С 1-С 3 алкильной группой С 3-С 7 циклоалкильную группу,необязательно замещенную С 1-С 3 алкильной группой инданильную группу, 5-членную гетероарильную группу, содержащую необязательно замещенную С 1-С 3 алкильной группой иминогруппу, атом кислорода или серы либо необязательно замещенную С 1-С 3 алкильной группой иминогруппу и атом кислорода, серы или азота либо два атома азота, или обозначает 6-членную гетероарильную группу, содержащую 1-3 атома азота, при этом через два смежных атома углерода или через один атом углерода и смежную иминогруппу в составе вышеуказанных 5- и 6-членных гетероарильных групп дополнительно может быть присоединен 1,3-бутадиениленовый мостик, а углеродный скелет вышеуказанных моно- и бициклических колец может быть одно- либо двузамещенным атомами фтора, хлора, брома или иода, С 1 С 5 алкильными или цианогруппами и заместители могут быть идентичными или разными, соединенную через атом углерода пирролидинильную либо пиперидинильную группу, которая соответственно по атому азота может быть замещена С 1-С 3 алкильной группой,необязательно двузамещенную атомами фтора, хлора, брома или иода, С 1-С 5 алкильными, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильными, аминосульфонильными, нитроили цианогруппами фенильную группу, при этом заместители могут быть идентичными или разными, фенильную, пиридильную, пиримидильную или тиенильную группу, каждая из которых замещена соответственно трифторметоксигруппой, атомом фтора,хлора, брома либо иода,С 1-С 3 алкоксигруппой, которая в положении 2 или 3 может быть замещена амино-, С 1-С 3 алкиламино-, ди(С 1-С 3 алкил)амино-, фенил-С 1 С 3 алкиламино-, N-(С 1-С 3 алкил)фенил-С 1-С 3 алкиламино-, пирролидиновой или пиперидиновой группой, фенил-С 1-С 3 алкиламино-С 1-С 3 алкильной группой, которая может быть однолибо двузамещенной в фенильном ядре трифторметильной группой, атомами фтора, хлора,брома либо иода, С 1-С 5 алкильными или С 1 С 3 алкоксигруппами, при этом заместители могут быть идентичными или разными, и дополнительно по атому азота амина замещена С 1 С 3 алкильной группой, в которой атомы водорода, начиная с положения 2, могут быть частично либо полностью заменены на атомы фтора, 3 С 1-С 5 алкильной, фенильной, имидазолильной, С 3-С 7 циклоалкильной, С 1-С 3 алкокси-С 1 С 3 алкокси-, фенил-С 1-С 3 алкокси-, карбокси-С 1 С 3 алкильной,С 1-С 3 алкоксикарбонил-С 1-С 3 алкильной, карбокси-, С 1-С 3 алкоксикарбонильной,аминокарбонильной,С 1-С 3 алкиламинокарбонильной,ди(С 1-С 3 алкил)аминокарбонильной,фенил-С 1-С 3 алкиламинокарбонильной, N-(С 1 С 3 алкил)фенил-С 1-С 3 алкиламинокарбонильной,пиперазинокарбонильной, N-(С 1-С 3 алкил)пиперазинокарбонильной, нитро-, амино-, С 1-С 3 алкиламино-, ди(С 1-С 3 алкил)амино-, пирролидиновой, пиперидиновой, морфолиновой, С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)-С 2-С 4 алканоиламино-, бензоиламино- или N-(С 1-С 3 алкил)бензоиламиногруппой,N-(С 1-С 3 алкил)-С 2-С 4 алканоиламиногруппой, которая в алкильном фрагменте дополнительно замещена карбокси- либо С 1-С 3 алкоксикарбонильной группой,С 1-С 3 алкиламинокарбонильной либо ди(С 1-С 3 алкил)аминокарбонильной группой, в которых один алкильный фрагмент дополнительно замещен ди(С 1-С 3 алкил)аминогруппой,илиN-(С 1-С 3 алкил)-С 1-С 3 алкилсульфониламино- либо N-(С 1-С 3 алкил)фенилсульфониламиногруппой, в которых алкильный фрагмент дополнительно может быть замещен циано-,карбокси-,С 1-С 3 алкоксикарбонильной,С 1 С 3 алкиламино-, ди(С 1-С 3 алкил)амино-, аминокарбонильной, С 1-С 3 алкиламинокарбонильной,ди(С 1-С 3 алкил)аминокарбонильной, пиперидинокарбонильной или 2-[ди(С 1-С 3 алкиламино)] этиламинокарбонильной группой, замещенную С 1-С 3 алкильной группой фенильную или тиенильную группу, в которой алкильный фрагмент замещен гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, амино-, С 1 С 5 алкиламино-, ди(С 1-С 5 алкил)амино-, С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)-С 2-С 4 алканоиламино-, пирролидиновой, дегидропирролидиновой, пиперидиновой, дегидропиперидиновой, 3 гидроксипиперидиновой, 4-гидроксипиперидиновой, гексаметиленимино-, морфолиновой,тиоморфолиновой, пиперазиновой, 4-(С 1-С 3 алкил)пиперазиновой, 4-фенилпиперазиновой, 4(С 2-С 4 алканоил)пиперазиновой,4-бензоилпиперазиновой или имидазолильной группой,при этом вышеуказанные насыщенные циклоалкилениминовые кольца, С 1-С 5 алкиламино- или ди(С 1-С 5 алкил)аминогруппы дополнительно могут быть замещены одной либо двумя С 1-С 5 алкильными группами, С 3-С 7 циклоалкильной, гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1-С 3 алкиламинокарбонильной или ди(С 1-С 3 алкил)аминокарбонильной группой, в фенильном ядре - необязательно атомами фтора,хлора, брома либо иода, одно- либо двузамещенными С 1-С 3 алкильными или цианогруппами фенил-С 1-С 3 алкильной или фенильной группой,при этом заместители могут быть идентичными 4 или разными, или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на карбонильную либо сульфонильную группу, а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома, метильной,амино-, С 1-С 3 алкиламино- или ди(С 1-С 3 алкил)аминогруппой, или с одним из вышеуказанных незамещенных циклоалкилениминовых колец через два смежных атома углерода может быть сконденсировано необязательно замещенное одной либо двумя С 1-С 3 алкоксигруппами фенильное кольцо,при этом указанные при расшифровке вышеназванных остатков карбоксигруппы дополнительно могут быть заменены на группу, переводимую in vivo в карбоксигруппу, а указанные при расшифровке вышеназванных остатков амино- и иминогруппы дополнительно могут быть замещены отщепляемым in vivo остатком. Кроме того, указанные выше насыщенные алкильные и алкоксильные фрагменты в составе соединений, которые содержат более двух атомов углерода, включают также их разветвленные изомеры, как, например, изопропильную,трет-бутильную, изобутильную группу и т.п. К предпочтительным соединениям общей формулы I относятся те из них, в которых Х обозначает атом кислорода или серы,R1 обозначает атом водорода, С 1-С 4 алкоксикарбонильную или С 2-С 4 алканоильную группу,R2 обозначает карбокси-,С 1 С 4 алкоксикарбонильную или аминокарбонильную группу, где аминовый фрагмент может быть замещен одной либо двумя С 1 С 3 алкильными группами и заместители могут быть идентичными или разными,R3 обозначает фенильную либо нафтильную группу, которые могут быть замещены атомами фтора, хлора или брома, С 1-С 3 алкильными, С 1-С 3 алкокси-, циано-, трифторметильными, нитро-, амино-, С 1-С 3 алкиламино-, ди(С 1 С 3 алкил)амино-, С 2-С 4 алканоиламино-, N-(С 1 С 3 алкил)-С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)С 2-С 4 алканоиламино-,С 1-С 3 алкилсульфониламино-, амино-С 1-С 3 алкильными, С 1-С 3 алкиламино-С 1-С 3 алкильными, ди(С 1-С 3 алкил)аминоС 1-С 3 алкильными, N-(С 2-С 4 алканоил)амино-С 1 С 3 алкильными или N-(С 2-С 4 алканоил)-С 1-С 3 алкиламино-С 1-С 3 алкильными группами и заместители могут быть идентичными или разными,R4 обозначает атом водорода или С 1 С 3 алкильную группу иR5 обозначает атом водорода,необязательно замещенную фенильной,карбокси- или С 1-С 3 алкоксикарбонильной группой С 1-С 5 алкильную группу, 5 необязательно замещенную С 1 С 3 алкильной группой С 3-С 7 циклоалкильную группу,необязательно замещенную С 1-С 3 алкильной группой инданильную группу, 5 членную гетероарильную группу, содержащую необязательно замещенную С 1-С 3 алкильной группой иминогруппу, атом кислорода или серы либо необязательно замещенную С 1-С 3 алкильной группой иминогруппу и атом кислорода, серы или азота либо два атома азота, или обозначает 6-членную гетероарильную группу,содержащую 1-3 атома азота, при этом через два смежных атома углерода или через один атом углерода и смежную иминогруппу в составе вышеуказанных 5- и 6-членных гетероарильных групп дополнительно может быть присоединен 1,3-бутадиениленовый мостик, а углеродный скелет вышеуказанных моно- и бициклических колец может быть одно- либо двузамещенным атомами фтора, хлора, брома или иода, С 1 С 5 алкильными или цианогруппами и заместители могут быть идентичными или разными, соединенную через атом углерода пирролидинильную либо пиперидинильную группу, которая соответственно по атому азота может быть замещена С 1-С 3 алкильной группой,необязательно одно- либо двузамещенную атомами фтора, хлора, брома или иода, С 1-С 5 алкильными или цианогруппами фенильную группу, при этом заместители могут быть идентичными или разными, фенильную, пиридильную, пиримидильную или тиенильную группу,каждая из которых замещена соответственно С 3-С 7 циклоалкильной, С 1-С 3 алкокси-, фенил-С 1-С 3 алкокси-, карбокси-С 1-С 3 алкильной,С 1-С 3 алкоксикарбонил-С 1-С 3 алкильной, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1-С 3 алкиламинокарбонильной, ди(С 1 С 3 алкил)аминокарбонильной, нитро-, амино-,С 1-С 3 алкиламино-, ди(С 1-С 3 алкил)амино-, С 2 С 4 алканоиламиноилиN-(С 1-С 3 алкил)-С 2 С 4 алканоиламиногруппой,С 1-С 3 алкиламинокарбонильной группой, в которой алкильный фрагмент дополнительно замещен ди(С 1-С 3 алкил)аминогруппой, илиN-(С 1-С 3 алкил)-С 1 С 3 алкилсульфониламиногруппой, в которой алкильный фрагмент дополнительно может быть замещен циано-, карбокси-, С 1-С 3 алкоксикарбонильной, С 1-С 3 алкиламино- либо ди(С 1 С 3 алкил)аминокарбонильной группой,замещенную С 1-С 3 алкильной группой фенильную или тиенильную группу, в которой алкильный фрагмент замещен гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, амино-, С 1-С 5 алкиламино-, ди(С 1-С 5 алкил) амино-, С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)С 2-С 4 алканоиламино-, пирролидиновой, пиперидиновой, гексаметиленимино-, морфолиновой,пиперазиновой, 4-(С 1-С 3 алкил)пиперазиновой, 003532 6 4-(С 2-С 4 алканоил)пиперазиновой, 4-бензоилпиперазиновой или имидазолильной группой,при этом вышеуказанные циклоалкилениминовые кольца, С 1-С 5 алкиламино- или ди(С 1 С 5 алкил)аминогруппы дополнительно могут быть замещены С 1-С 5 алкильной, С 3-С 7 циклоалкильной,гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1-С 3 алкиламинокарбонильной или ди(С 1-С 3 алкил)аминокарбонильной группой, в фенильном ядре - необязательно атомами фтора, хлора, брома либо иода, одно- либо двузамещенной С 1-С 3 алкильными или цианогруппами фенил-С 1 С 3 алкильной или фенильной группой, при этом заместители могут быть идентичными или разными,или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на карбонильную либо сульфонильную группу, а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома или метильной группой,прежде всего, такие соединения общей формулы I, в которых Х обозначает атом кислорода,R1 обозначает атом водорода или С 1-С 4 алкоксикарбонильную группу, R2 обозначает карбокси-, С 1-С 4 алкоксикарбонильную или аминокарбонильную группу, где аминовый фрагмент может быть замещен одной либо двумя С 1 С 3 алкильными группами и заместители могут быть идентичными или разными, R3 обозначает необязательно замещенную атомом фтора, хлора либо брома, метильной, циано- или аминометильной группой фенильную группу, R4 обозначает атом водорода или метильную группу и R5 обозначает атом водорода,необязательно замещенную карбокси- или С 1-С 3 алкоксикарбонильной группой С 1 С 5 алкильную группу или бензильную группу,необязательно замещенную метильной группой С 3-С 7 циклоалкильную группу,необязательно замещенную метильной группой инданильную, пиридильную, оксазолильную,тиазолильную или имидазолильную группу, с которыми соответственно дополнительно через два смежных атома углерода может быть сконденсировано фенильное кольцо, необязательно замещенную атомом фтора, хлора либо брома, метокси-, карбокси-, С 1-С 3 алкилоксикарбонильной, нитро- или аминосульфонильной группой метилфенильную группу или диметоксифенильную группу, соединенную через атом углерода пирролидинильную или пиперидинильную группу, которые соответственно по атому азота замещены С 1-С 3 алкильной группой, фенильную группу, замещенную трифторметоксигруппой, атомом фтора, хлора, брома либо иода, С 1-С 3 алкоксигруппой, которая в положении 2 или 3 может быть замещена амино-, С 1-С 3 алкиламино-, ди(С 1-С 3 алкил)амино-, 7 фенил-С 1-С 3 алкиламино-, N-(С 1-С 3 алкил)фенилС 1-С 3 алкиламино-, пирролидиновой или пиперидиновой группой, фенил-С 1-С 3 алкиламино-С 1 С 3 алкильной группой, которая в фенильном ядре замещена атомом фтора, хлора, брома либо иода,С 1-С 5 алкильной, С 1-С 3 алкокси- или трифторметильной группой и дополнительно по атому азота амина замещена С 1-С 3 алкильной группой, в которой атомы водорода, начиная с положения 2, могут быть полностью либо частично заменены на атомы фтора,С 1-С 5 алкильной, фенильной, имидазолильной, С 3-С 7 циклоалкильной, С 1-С 3 алкокси-С 1-С 3 алкокси-, фенил-С 1-С 3 алкокси-, карбокси-С 1-С 3 алкильной, С 1-С 3 алкоксикарбонил-С 1-С 3 алкильной,карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1-С 3 алкиламинокарбонильной, ди(С 1 С 3 алкил)аминокарбонильной, фенил-С 1-С 3 алкиламинокарбонильной, N-(С 1-С 3 алкил)фенил-С 1-С 3 алкиламинокарбонильной, пиперазинокарбонильной,N-(С 1-С 3 алкил)пиперазинокарбонильной,нитро-, амино-, С 1-С 3 алкиламино-, ди(С 1-С 3 алкил) амино-, пирролидиновой, пиперидиновой, морфолиновой, С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)С 2-С 4 алканоиламино-, бензоиламино- или N-(С 1 С 3 алкил)бензоиламиногруппой,N-(С 1-С 3 алкил)-С 2-С 4 алканоиламиногруппой, которая в алкильном фрагменте дополнительно замещена карбокси- либо С 1-С 3 алкоксикарбонильной группой,С 1-С 3 алкиламинокарбонильной либо ди(С 1-С 3 алкил)аминокарбонильной группой, в которых один алкильный фрагмент дополнительно замещен ди(С 1-С 3 алкил)аминогруппой,илиN-(С 1-С 3 алкил)-С 1-С 3 алкилсульфониламино- либо N-(С 1-С 3 алкил)фенилсульфониламиногруппой, в которых алкильный фрагмент дополнительно может быть замещен циано-,карбокси-, С 1-С 3 алкоксикарбонильной, С 1-С 3 алкиламино-, ди(С 1-С 3 алкил)амино-, аминокарбонильной, С 1-С 3 алкиламинокарбонильной, ди(С 1 С 3 алкил)аминокарбонильной, пиперидинокарбонильной или 2-[ди(С 1-С 3 алкиламино)]этиламинокарбонильной группой, необязательно замещенную С 1-С 3 алкильной группой фенильную группу, в которой алкильный фрагмент замещен гидрокси-, С 1-С 3 алкокси-, карбокси-,С 1-С 3 алкоксикарбонильной, амино-, С 1-С 5 алкиламино-, ди(С 1-С 5 алкил)амино-, С 2-С 4 алканоиламино-,N-(С 1-С 3 алкил)-С 2-С 4 алканоиламино-, пирролидиновой, дегидропирролидиновой,пиперидиновой, дегидропиперидиновой, 3-гидроксипиперидиновой, 4-гидроксипиперидиновой, гексаметиленимино-, морфолиновой, тиоморфолиновой, пиперазиновой, 4-(С 1-С 3 алкил) пиперазиновой, 4-фенилпиперазиновой, 4-(С 2 С 4 алканоил)пиперазиновой,4-бензоилпиперазиновой или имидазолильной группой, при этом вышеуказанные насыщенные циклоалкилениминовые кольца, С 1-С 5 алкиламино- или ди(С 1-С 5 алкил)аминогруппы дополнительно 8 могут быть замещены одной либо двумя С 1-С 5 алкильными группами, С 3-С 7 циклоалкильной,гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1 С 3 алкиламинокарбонильной или ди(С 1-С 3 алкил)аминокарбонильной группой, в фенильном ядре - необязательно атомами фтора, хлора,брома либо иода, одно- либо двузамещенными С 1-С 3 алкильными или цианогруппами фенил-С 1 С 3 алкильной или фенильной группой, при этом заместители могут быть идентичными или разными, или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на карбонильную либо сульфонильную группу, а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома, метильной, амино-,С 1-С 3 алкиламиноили ди(С 1 С 3 алкил)аминогруп-пой, или с одним из вышеуказанных незамещенных циклоалкилениминовых колец через два смежных атома углерода может быть сконденсировано необязательно замещенное одной либо двумя С 1 С 3 алкоксигруппами фенильное кольцо, а также их изомеры и их соли. Особенно предпочтительными соединениями вышеприведенной общей формулы I являются те из них, в которых Х обозначает атом кислорода, R1 обозначает атом водорода, R2 обозначает карбокси-,С 1-С 4 алкоксикарбонильную или аминокарбонильную группу, в которой аминовый фрагмент может быть замещен одной либо двумя С 1-С 3 алкильными группами и заместители могут быть идентичными либо разными, R3 обозначает необязательно замещенную метильной группой фенильную группу, R4 обозначает атом водорода или метильную группу и R5 обозначает атом водорода,С 1-С 3 алкильную группу,бензильную группу или замещенную карбокси- либо С 1-С 3 алкоксикарбонильной группой метильную или этильную группу,необязательно замещенную метильной группой С 3-С 7 циклоалкильную группу,необязательно замещенную метильной группой инданильную, пиридильную, оксазолильную, тиазолильную или имидазолильную группу,с которыми соответственно дополнительно через два смежных атома углерода может быть сконденсировано фенильное кольцо,необязательно замещенную атомом фтора,хлора либо брома, метокси-, карбокси-, С 1 С 3 алкилоксикарбонильной, нитро- или аминосульфонильной группой метилфенильную либо диметоксифенильную группу,3-пирролидинильную или 4-пиперидинильную группу, которые соответственно по атому азота замещены С 1-С 3 алкильной группой, 9 фенильную группу, замещенную трифторметокси-, бензилокси-, циано- или нитрогруппой, атомом фтора, хлора либо брома,С 1-С 3 алкоксигруппой, причем этокси- и нпропоксигруппа, каждая соответственно в концевом положении может быть замещена диметиламино-, диэтиламино-, N-этилметиламино-,N-бензилметиламино- либо пиперидиновой группой,фенил-С 1-С 3 алкиламино-С 1-С 3 алкильной группой, которая может быть замещена в фенильном ядре атомом фтора, хлора, брома либо иода, метильной, метокси- или трифторметильной группой и дополнительно по атому азота амина может быть замещена С 1-С 5 алкильной либо 2,2,2-трифторэтильной группой, С 1 С 4 алкильной, фенильной, имидазолильной, циклогексильной, метоксиметильной, карбоксиметильной, С 1-С 3 алкоксикарбонилметильной, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной,С 1-С 3 алкиламинокарбонильной,ди(С 1-С 3 алкил)аминокарбонильной, фенил-С 1 С 3 алкиламинокарбонильной, N-(С 1-С 3 алкил)фенил-С 1-С 3 алкиламинокарбонильной, пиперазинокарбонильной,N-(С 1-С 3 алкил)пиперазинокарбонильной,амино-,С 1-С 3 алкиламино-,ди(С 1-С 3 алкил)амино-, пирролидиновой, пиперидиновой, морфолиновой, С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)-С 2-С 4 алканоиламино-,бензоиламино- или N-(С 1-С 3)бензоиламиногруппой,N-(С 1-С 3 алкил)-С 2-С 4 алканоиламиногруппой, которая в алкильном фрагменте дополнительно замещена карбокси- либо С 1-С 3 алкоксикарбонильной группой,С 1-С 3 алкиламинокарбонильной или ди(С 1 С 3 алкил)аминокарбонильной группой, в которых один алкильный фрагмент дополнительно замещен ди(С 1-С 3 алкил)аминогруппой, или N(С 1-С 3 алкил)-С 1-С 3 алкилсульфониламино- либоN-(С 1-С 3 алкил)фенилсульфониламиногруппой,в которых алкильный фрагмент дополнительно может быть замещен циано-, карбокси-, С 1-С 3 алкоксикарбонильной, С 1-С 3 алкиламино-, ди(С 1 С 3 алкил)амино-, аминокарбонильной, С 1-С 3 алкиламинокарбонильной, ди(С 1-С 3 алкил)аминокарбонильной, пиперидинокарбонильной или 2[ди(С 1-С 3 алкиламино)]этиламинокарбонильной группой, необязательно замещенную С 1-С 3 алкильной группой фенильную группу, в которой алкильная группа замещена гидрокси-, С 1 С 3 алкокси-,карбокси-,С 1-С 3 алкоксикарбонильной, амино-, С 1-С 5 алкиламино-, ди 10 при этом вышеуказанные насыщенные циклоалкилениминовые кольца дополнительно могут быть замещены фенильной группой либо одной или двумя метильными группами,вышеуказанные С 1-С 5 алкиламино- и ди(С 1 С 5 алкил)аминогруппы дополнительно могут быть замещены одной либо двумя С 1-С 3 алкильными группами, циклогексильной, гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1-С 3 алкиламинокарбонильной либо ди(С 1 С 3 алкил)аминокарбонильной группой, необязательно замещенной в фенильном ядре атомом фтора, хлора, брома либо иода, метильной или цианогруппой фенил-С 1-С 3 алкильной либо фенильной группой, или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на карбонильную либо сульфонильную группу,а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома, метильной,амино-, С 1-С 3 алкиламино- или ди(С 1-С 3 алкил)аминогруппой, или с одним из вышеуказанных незамещенных циклоалкилениминовых колец через два смежных атома углерода может быть сконденсировано необязательно замещенное одной или двумя С 1-С 3 алкоксигруппами фенильное кольцо, а также их изомеры и их соли. К наиболее предпочтительным относятся такие соединения вышеприведенной формулы I,в которых Х обозначает атом кислорода, R1 обозначает атом водорода, R2 обозначает карбоксиили аминокарбонильную группу, в которой аминовый фрагмент может быть замещен одной либо двумя С 1-С 3 алкильными группами и заместители могут быть идентичными либо разными, R3 обозначает необязательно замещенную метильной группой фенильную группу,R4 обозначает атом водорода и R5 обозначает атом водорода,3-пирролидинильную либо 4-пиперидинильную группу, замещенные соответственно по атому азота С 1-С 3 алкильной группой,фенильную группу, замещенную С 1 С 3 алкоксигруппой, причем этокси- и нпропоксигруппа, каждая соответственно в концевом положении может быть замещена диметиламино-, диэтиламино-, N-этилметиламино-,N-бензилметиламино- либо пиперидиновой группой, фенил-С 1-С 3 алкиламино-С 1-С 3 алкильной группой, которая может быть замещена в фенильном ядре атомом фтора, хлора, брома либо иода, метильной, метокси- или трифторметильной группой и дополнительно по атому азота амина также С 1-С 5 алкильной либо 2,2,2 трифторэтильной группой,необязательно замещенную С 1-С 3 алкильной группой фенильную группу, в которой алкильная группа замещена гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, 11 амино-, С 1-С 5 алкиламино-, ди(С 1-С 5 алкил)амино-, С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)-С 2 С 4 алканоиламино-, пирролидиновой, дегидропирролидиновой, пиперидиновой, дегидропиперидиновой, 4-гидроксипиперидиновой, гексаметиленимино-, морфолиновой, тиоморфолиновой, пиперазиновой, 4-(С 1-С 3 алкил)пиперазиновой, 4-фенилпиперазиновой, 4-(С 2-С 4 алканоил)пиперазиновой, 4-бензоилпиперазиновой или имидазолильной группой,при этом вышеуказанные насыщенные циклоалкилениминовые кольца дополнительно могут быть замещены фенильной группой либо одной или двумя метильными группами,вышеуказанные С 1-С 5 алкиламино- и ди(С 1 С 5 алкил)аминогруппы дополнительно могут быть замещены одной либо двумя С 1 С 3 алкильными группами, циклогексильной,гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1 С 3 алкиламинокарбонильной либо ди(С 1 С 3 алкил)аминокарбонильной группой, необязательно замещенной в фенильном ядре атомом фтора, хлора, брома либо иода, метильной или цианогруппой фенил-С 1-С 3 алкильной либо фенильной группой, или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на карбонильную либо сульфонильную группу,а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома, метильной,амино-, С 1-С 3 алкиламино- или ди(С 1-С 3 алкил)аминогруппой, или с одним из вышеуказанных незамещенных циклоалкилениминовых колец через два смежных атома углерода может быть сконденсировано необязательно замещенное одной или двумя С 1-С 3 алкоксигруппами фенильное кольцо, а также их изомеры и их соли. Особенно предпочтительны указанные выше соединения, в которых остаток R2 находится в положении 5, прежде всего, следующие соединения:(и) 3-Z-[1-(4-(N-бутиламинометил)фениламино)-1-фенилметилен]-5-амидо-2-индолинон,(к) 3-Z-[1-(4-(N-(фенилметил)аминометил)фениламино)-1-фенилметилен]-5-амидо-2 индолинон,(л) 3-Z-[1-(4-(N-метил-N-бензиламинометил)фениламино)-1-фенилметилен]-5-амидо-2 индолинон,(м) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-диметилкарбамоил-2 индолинон,(н) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-диэтилкарбамоил-2 индолинон,(о) 3-Z-[1-(4-(3-диэтиламинопропокси)фениламино)-1-фенилметилен]-5-амидо-2-индолинон и их соли. Согласно изобретению новые соединения можно получать, например, по следующим способам, в принципе известным из литературы. а) Взаимодействием соединения общей формулы в которой X, R2 и R3 имеют указанные выше значения, R6 обозначает атом водорода, защитную группу для атома азота лактамовой группы или связь с твердой фазой, a Z1 обозначает атом галогена, гидрокси-, алкокси- либо аралкоксигруппу, например атом хлора или брома, метокси-, этокси- либо бензилоксигруппу, с амином общей формулы в которой R4 и R5 имеют указанные выше значения, и при необходимости последующим отщеплением используемой защитной группы для атома азота лактамовой группы или отщеплением от твердой фазы. В качестве защитной группы для атома азота лактамовой группы приемлемы, например,ацетильная, бензоильная, этоксикарбонильная,трет-бутоксикарбонильная или бензилоксикарбонильная группа, а в качестве твердой фазы смола Ринка или смола Зибера. Реакцию осуществляют предпочтительно в растворителе, таком как диметилформамид, толуол, ацетонитрил, тетрагидрофуран, диметилсульфоксид, метиленхлорид, либо в их смесях,необязательно в присутствии инертного основания, такого как триэтиламин, N-этилдиизопропиламин или гидрокарбонат натрия, при температурах в интервале от 20 до 175 С, при этом используемую защитную группу можно одновременно отщеплять в результате переамидирования. 13 Если Z1 в соединении общей формулы II обозначает атом галогена, то реакцию предпочтительно проводят в присутствии инертного основания при температурах в интервале от 20 до 120 С. Если же Z1 в соединении общей формулыII обозначает гидрокси-, алкокси- или аралкоксигруппу, то реакцию предпочтительно проводят при температурах в интервале от 20 до 200 С. Последующее отщепление необязательно используемой защитной группы целесообразно осуществлять либо гидролитическим путем в водном или спиртовом растворителе, например,в смеси метанол/вода, этанол/вода, изопропанол/вода, тетрагидрофуран/вода, диоксан/вода,диметилформамид/вода, в метаноле или этаноле, в присутствии основания щелочного металла, такого как гидроксид лития, гидроксид натрия или гидроксид калия, при температурах в интервале от 0 до 100 С, предпочтительно при температурах в интервале от 10 до 50 С, либо предпочтительно путем переамидирования с помощью первичного или вторичного органического основания, такого как аммиак, метиламин,бутиламин, диметиламин или пиперидин, в растворителе, таком как метанол, этанол, диметилформамид и в их смесях, или же с использованием избытка применяемого амина при температурах в интервале от 0 до 100 С, предпочтительно при температурах в интервале от 10 до 50 С. Отщепление от используемой твердой фазы предпочтительно осуществлять с помощью трифторуксусной кислоты и воды в присутствии диалкилсульфида, такого как диметилсульфид,при температурах в интервале от 0 до 35 С,предпочтительно при комнатной температуре. б) Для получения соединения общей формулы I, содержащего аминометильную группу, а Х представляет собой атом кислорода: восстановлением соединения общей формулы в которой R1-R4 имеют указанные выше значения, a R7 имеет значение, идентичное из указанных для R5, при условии, что R5 обозначает цианогруппу. Восстановление предпочтительно проводят путем каталитического гидрирования с помощью водорода в присутствии катализатора,такого как палладий на угле или платина, в растворителе, таком как метанол, этанол, этиловый эфир уксусной кислоты, диметилформамид,смесь диметилформамид/ацетон или ледяная уксусная кислота, необязательно с добавками 14 кислоты, такой как соляная кислота, при температурах в интервале от 0 до 50 С, предпочтительно, однако, при комнатной температуре, и при давлении водорода от 1 до 7 бар, предпочтительно от 3 до 5 бар. В случае получения согласно изобретению соединения общей формулы I, содержащего алкоксикарбонильную группу, его можно посредством гидролиза переводить в соответствующее карбоксисоединение, или в случае получения соединения общей формулы I, содержащего амино- или алкиламиногруппу, его можно путем алкилирования либо восстановительного алкилирования переводить в соответствующее алкиламино-, соответственно диалкиламиносоединение, или в случае получения соединения общей формулы I, содержащего амино- или алкиламиногруппу, его можно путем ацилирования переводить в соответствующее ацильное соединение, или в случае получения соединения общей формулы I, содержащего карбоксигруппу, его можно путем этерификации или амидирования переводить в соответствующее сложноэфирно- или аминокарбонильное соединение. Последующий гидролиз осуществляют предпочтительно в водном растворителе, например в воде, смеси изопропанол/вода, тетрагидрофуран/вода или диоксан/вода, в присутствии кислоты, такой как трифторуксусная кислота, соляная кислота или серная кислота, либо в присутствии основания щелочного металла, такого как гидроксид лития, гидроксид натрия или гидроксид калия, при температурах в интервале от 0 до 100 С, предпочтительно при температурах в интервале от 10 до 50 С. Последующее восстановительное алкилирование осуществляют предпочтительно в соответствующем растворе, таком как метанол,смесь метанол/вода, метанол/вода/аммиак, этанол, простой эфир, тетрагидрофуран, диоксан или диметилформамид, необязательно с добавками кислоты, такой как соляная кислота, в присутствии каталитически инициированного водорода, например водорода в присутствии никеля Ренея, платины или палладия на угле,либо в присутствии гидрида металла, такого как борогидрид натрия, борогидрид лития или алюмогидрид лития, при температурах в интервале от 0 до 100 С, предпочтительно при температурах в интервале от 20 до 80 С. Последующее алкилирование осуществляют с помощью соответствующего алкилирующего агента, такого как алкилгалогенид или диалкилсульфат, как например метилиодид, диметилсульфат или пропилбромид, предпочтительно в растворителе, таком как метанол, этанол, метиленхлорид, тетрагидрофуран, толуол,диоксан, диметилсульфоксид или диметилформамид, необязательно в присутствии неорганического либо третичного органического основания, такого как триэтиламин, N-этилдиизо 15 пропиламин или диметиламинопиридин, предпочтительно при температурах в интервале от 20 С до температуры кипения используемого растворителя. Последующее ацилирование осуществляют предпочтительно в растворителе, таком как метиленхлорид, диэтиловый эфир, тетрагидрофуран, толуол, диоксан, ацетонитрил, диметилсульфоксид или диметилформамид, необязательно в присутствии неорганического либо третичного органического основания, предпочтительно при температурах в интервале от 20 С до температуры кипения используемого растворителя. При этом ацилирование целесообразно проводить с помощью соответствующей кислоты, предпочтительно в присутствии отбирающего воду (обезвоживающего) агента, например в присутствии изобутилового эфира хлормуравьиной кислоты, тетраэтилового эфира ортоугольной кислоты, триметилового эфира ортоуксусной кислоты, 2,2-диметоксипропана, тетраметоксисилана, тионилхлорида, триметилхлорсилана, трихлорида фосфора, пентоксида фосфора,N,N'-дициклогексилкарбодиимида, смеси N,N'дициклогексилкарбодиимида и N-гидроксисукцинимида, N,N'-дициклогексилкарбодиимида и 1-гидроксибензтриазола, тетрафторбората 2(1 Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония, смеси тетрафторбората 2-(1 Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония и 1-гидроксибензтриазола, N,N'-карбонилдиимидазола или смеси трифенилфосфина и тетрахлорметана, и необязательно с добавками основания, такого как пиридин, 4-диметиламинопиридин, Nметилморфолин или триэтиламин, при температурах в интервале от 0 до 150 С, предпочтительно при температурах в интервале от 0 до 100 С, а ацилирование с помощью соответствующего реакционноспособного соединения, в частности его ангидрида, сложного эфира, имидазолидов или галогенидов, целесообразно проводить при необходимости в присутствии третичного органического основания, такого как триэтиламин, N-этилдиизопропиламин либо Nметилморфолин, при температурах в интервале от 0 до 150 С, предпочтительно при температурах в интервале от 50 до 100 С. Последующую этерификацию или последующее амидирование целесообразно осуществлять взаимодействием соответствующего реакционноспособного производного карбоновой кислоты с соответствующим спиртом или амином, описанным выше. При проведении описанных выше реакций необязательно имеющиеся реакционноспособные группы, такие как карбокси-, амино-, алкиламино- или иминогруппы, можно защищать в ходе реакции обычными защитными группами,а по завершении реакции снова отщеплять их. Так, например, для защиты карбоксильной группы может использоваться триметилсилильная, метильная, этильная, трет-бутильная, бен 003532 16 зильная либо тетрагидропиранильная группа, а для защиты амино-, алкиламино- или иминогруппы пригодны ацетильная, трифторацетильная, бензоильная, этоксикарбонильная, третбутоксикарбонильная, бензилоксикарбонильная,бензильная, метоксибензильная либо 2,4 диметоксибензильная группа, а для защиты аминогруппы - дополнительно фталильная группа. Последующее отщепление необязательно используемой защитной группы осуществляют,например, гидролитическим путем в водном растворителе, например в воде, в смеси изопропанол/вода, тетрагидрофуран/вода или диоксан/вода, в присутствии кислоты, такой как трифторуксусная кислота, соляная кислота или серная кислота, либо в присутствии основания щелочного металла, такого как гидроксид лития,гидроксид натрия или гидроксид калия, при температурах в интервале от 0 до 100 С, предпочтительно при температурах в интервале от 10 до 50 С. Отщепление же бензильной, метоксибензильной или бензилоксикарбонильной группы осуществляют, например, путем гидрогенолиза,в частности с помощью водорода в присутствии катализатора, такого как палладий на угле, в растворителе, таком как метанол, этанол, этиловый эфир уксусной кислоты, диметилформамид,смесь диметилформамида и ацетона или ледяная уксусная кислота, необязательно с добавками кислоты, такой как соляная кислота или ледяная уксусная кислота, при температурах в интервале от 0 до 50 С, предпочтительно, однако, при комнатной температуре и давлении водорода от 1 до 7 бар, предпочтительно от 3 до 5 бар. Отщепление метоксибензильной группы может проводиться также в присутствии окислителя, такого как церий (IV)-аммонийнитрат, в растворителе, таком как метиленхлорид, ацетонитрил или смесь ацетонитрил/вода, при температурах в интервале от 0 до 50 С, предпочтительно, однако, при комнатной температуре. Отщепление 2,4-диметоксибензильной группы целесообразно осуществлять в трифторуксусной кислоте в присутствии анизола. Отщепление трет-бутильной или третбутилоксикарбонильной группы предпочтительно осуществлять путем обработки кислотой,такой как трифторуксусная кислота либо соляная кислота, необязательно с использованием растворителя, такого как метиленхлорид, диоксан, уксусный эфир или простой эфир. Отщепление фталильной группы предпочтительно осуществлять в присутствии гидразина или первичного амина, такого как метиламин,этиламин либо н-бутиламин, в растворителе,таком как метанол, этанол, изопропанол, смесь толуол/вода или диоксан, при температурах в интервале от 20 до 50 С. 17 Далее, полученные хиральные соединения общей формулы I могут разделяться на их энантиомеры и/или диастереомеры. Так, например,полученные соединения общей формулы I, образующиеся в форме рацематов, по известным методам (см. Allinger N.L. и Eliel E.L. в "Topicsin Stereochemistry", том 6, изд-во Wiley Interscience, 1971) можно разделять на их оптические антиподы, а соединения общей формулы I,по меньшей мере, c 2 асимметричными атомами углерода благодаря их физико-химическим различиям по известным методам, например посредством хроматографии и/или путем фракционированной кристаллизации, можно разделять на их диастереомеры, которые в случае их получения в рацемической форме можно разделять, как описано выше, на энантиомеры. Предпочтительно разделять энантиомеры посредством колоночной хроматографии по хиральным фазам либо путем перекристаллизации из оптически активного растворителя, либо взаимодействием с оптически активной субстанцией, образующей с рацемическим соединением соли или производные, например сложные эфиры или амиды, прежде всего, с кислотами и их активированными производными или спиртами, а разделение полученной таким образом смеси диастереомерных солей или производных осуществлять, например, исходя из различной степени их растворимости, при этом из чистых диастереомерных солей или производных действием соответствующих средств могут высвобождаться свободные антиподы. К наиболее приемлемым оптически активным кислотам относятся среди прочих D- и L-формы винной кислоты, дибензоилвинной кислоты, ди-отолилвинной кислоты, яблочной кислоты, миндальной кислоты, камфорсульфоновой кислоты,глутаминовой кислоты, N-ацетилглутаминовой кислоты,аспарагиновой кислоты,Nацетиласпарагиновой кислоты или хинной кислоты. В качестве оптически активного спирта можно использовать, например, (+)- или (-)ментол, а в качестве оптически активной ацильной группы в амидах можно применять, например, (+)- или (-)-метилоксикарбонил. Далее, получаемые соединения формулы I можно переводить в их соли, прежде всего для применения в фармацевтике - в их физиологически приемлемые соли с органическими или неорганическими кислотами. Такими кислотами в этих целях могут служить среди прочих соляная кислота, бромисто-водородная кислота, серная кислота, фосфорная кислота, фумаровая кислота, янтарная кислота, молочная кислота,лимонная кислота, винная кислота, малеиновая кислота или метансульфокислота. Кроме того, получаемые описанным выше путем новые соединения формулы I, если они содержат карбоксигруппу, при необходимости могут переводиться затем в их соли с органическими или неорганическими основаниями, пре 003532 18 жде всего для применения в фармацевтике - в их физиологически приемлемые соли. Такими основаниями в этих целях могут служить среди прочих гидроксид натрия, гидроксид калия,циклогексиламин, этаноламин, диэтаноламин и триэтаноламин. Используемые в качестве исходных продуктов соединения общих формул I-VIII частично известны из литературы либо их можно получать по методам, известным из литературы,или же по технологии, описанной в примерах. Как уже указывалось выше, новые соединения общей формулы I, в которой R1 представляет собой атом водорода или пролекарственный остаток, обладают ценными фармакологическими свойствами, прежде всего ингибирующим действием по отношению к различным киназам и комплексам циклин/CDK, а также подавляют пролиферацию культивированных раковых клеток человека и рост опухолей после орального введения у лишенных волосяного покрова мышей, инфицированных раковыми клетками человека. Представленные в качестве примеров в табл. 1 соединения испытывали на их биологическую эффективность следующим образом: Тест 1. Ингибирoвание ферментативной активности комплекса циклин/CDK in vitro. Для продуцирования активных человеческих холоферментов циклин/CDK использовали клетки насекомых High Five (BTI-TN-5B1-4),которые инфицировали высоким титром рекомбинантного бакуловируса. С использованием бакуловирусного вектора, содержащего два промотора (энхансерный промотор полиэдрина,Р 10-энхансерный промотор), экспрессировали в одной и той же клетке меченные с помощьюCDK6). Активный холофермент выделяли с помощью аффинной хроматографии на сефарозе,содержащей глутатион. Рекомбинантный pRB,меченый с помощью GST (аминокислотные остатки в положениях 379-928), продуцировали в Е. coli и очищали с помощью аффинной хроматографии на сефарозе, содержащей глутатион. Применяемые для анализа киназной активности субстраты выбирали в зависимости от конкретных киназ. В качестве субстрата для комплексов циклин E/CDK2, циклин A/CDK2,циклин B/CDK1 и v-циклин/СDК 6 использовали гистон H1 (фирма Sigma). В качестве субстрата для комплексов циклин D1/CDK4, циклин(аминокислотные остатки в положениях 379928). Лизаты рекомбинантных инфицированных бакуловирусами клеток насекомых или также рекомбинантные киназы (полученные путем 19 очистки из лизатов) вместе с несущим радиоактивную метку АТФ инкубировали в 1%-ном растворе ДМСО (диметилсульфоксид) в течение 45 мин при 30 С в присутствии пригодного субстрата с различными концентрациями ингибитора. Протеины субстрата со связанной радиоактивностью осаждали с помощью 5%-ной ТХК(трихлоруксусная кислота) в гидрофобные многолуночные титрационные микропланшеты из поливинилиденфторида (фирма Millipore) или с помощью 0,5%-ного раствора фосфорной кислоты осаждали на фильтры типа Whatman P81. После добавления сцинтилляционной жидкости измеряли радиоактивность с помощью жидкостного сцинтилляционного счетчика типаWallace 1450 Microbeta. Для каждой концентрации вещества измерения проводили в двух повторностях; вычисляли значения IС 50, характеризующие ингибирование фермента. Тест 2. Ингибирование пролиферации культивируемых клеток опухоли человека. Клетки опухоли лейомиосаркомы линииSK-UT-1B (полученные из Американской коллекции типовых культур (АТСC) культивировали в минимальной эссенциальной среде, содержащей заменимые аминокислоты (фирмаGibco), дополненной пируватом натрия (1 ммоль), глутамином (2 ммоля) и 10% фетальной бычьей сыворотки (фирма Gibco), и собирали на логарифмической фазе роста. Затем клетки линии SK-UT-1B вносили в лунки многолуночного планшета типа Cytostar (фирма Amersham) с плотностью 4000 клеток на лунку и инкубировали в термостате в течение ночи. К клеткам добавляли соединения в различных концентрациях (растворенные в ДМСО; конечная концентрация: 1%). После инкубации в течение 48 ч в каждую лунку добавляли 14 С-тимидин (фирмаAmersham) и инкубировали еще в течение 24 ч. Количество 14 С-тимидина, включенного в присутствии ингибитора в клетки опухоли, и количество клеток, находящихся на S-фазе (фаза синтеза) клеточного роста, измеряли с помощью жидкостного сцинтилляционного счетчика типаWallace 1450 Microbeta. Значения IC50, характеризующие ингибирование пролиферации (ингибирование встраивания 14 С-тимидина), вычисляли с поправкой на фоновое излучение. Все измерения проводили в двух повторностях. Тест 3. Исследование действия in vivo на лишенных волосяного покрова (бестимусных) мышах, имеющих опухоли. Самцам и/или самкам бестимусных мышей(мыши линии NMRI nu/nu; вес 25-35 г; количество особей в группе N=10-20) путем подкожной инъекции объемом 0,1 мл вводили по 106 клеток [клетки линии SK-UT-1B или немелкоклеточного рака легкого линии NCI-H460 (полученные из АТСС]; в альтернативном варианте подкожно имплантировали небольшие кусочки опухолевой ткани в виде скоплений клеток линии SK-UT-1B или линии NCI-H460. По истече 003532 20 нии 1-3 недель после инъекции, соответственно имплантации животным ежедневно на протяжении 2-4 недель вводили орально (с помощью желудочного зонда) ингибитор киназы. Рост опухоли измеряли трижды в неделю с помощью цифрового штангенциркуля. Действие ингибитора киназы на рост опухоли выражали в виде процента ингибирования по сравнению с контрольной группой, обработанной плацебо. В приведенной ниже таблице представлены результаты, полученные в тесте 2 in vitro. Соединение Ингибирование пролиферацииSK-UT-1B IC50 [мкМ] 4 (2) 0,17 4 (14) 0,18 4 (62) 0,05 4 (53) 0,01 4 (54) 0,03 4 (60) 0,03 4 (120) 0,04 4 (122) 0,04 4 (94) 0,03 3 (3) 0,01 3 (7) 0,01 4 (129) 0,04 Благодаря их биологическим свойствам новые соединения общей формулы I, их изомеры и их физиологически приемлемые соли пригодны для лечения заболеваний, связанных с избыточной либо аномальной пролиферацией клеток. К таким заболеваниям относятся (но не ограничиваясь только ими) вирусные инфекции(например, ВИЧ-инфекция и саркома Капоши),воспаления и аутоиммунные заболевания (например, колит, артрит, болезнь Альцгеймера,гломерулонефрит и заживление ран), бактериальные, грибковые и/или паразитарные инфекции, лейкозы, лимфома и солидные опухоли,кожные заболевания (например, псориаз), остеопатия, заболевания сердечно-сосудистой системы (например, рестеноз и гипертрофия). Кроме того, они могут применяться для защиты быстро разрастающихся клеток (например волосковых, интестинальных клеток, клеток крови и клеток-предшественников) от ДНКповреждения, обусловленного радиацией, УФоблучением и/или лечением с использованием цитостатиков. Новые соединения могут быть раcсчитаны на краткий либо длительный курс лечения вышеназванных заболеваний, при необходимости в сочетании с другими известными соединениями, в частности с другими цитостатиками. Требуемая для достижения соответствующего эффекта дозировка составляет предпочтительно при внутривенном введении от 0,1 до 30 мг/кг, предпочтительно от 0,3 до 10 мг/кг, а при оральном введении - от 0,1 до 100 мг/кг, предпочтительно от 0,3 до 30 мг/кг, соответственно 21 при 1-4-разовом приеме в день. В этих целях из получаемых согласно изобретению соединений формулы I, при необходимости в сочетании с другими активными веществами, совместно с одним либо несколькими обычными инертными носителями и/или разбавителями, такими, например, как кукурузный крахмал, молочный сахар, сахароза, микрокристаллическая целлюлоза, стеарат магния, поливинилпирролидон,лимонная кислота, винная кислота, вода/этанол,вода/глицерин, вода/сорбит, вода/полиэтиленгликоль, пропиленгликоль, цетилстеариловый спирт, карбоксиметилцеллюлоза или жирные субстанции, такие как твердый жир, либо их соответствующие смеси, можно изготавливать обычные галеновые композиции в форме таблеток, драже, капсул, порошков, суспензий, свечей или в виде растворов для инъекций либо вливания. Ниже изобретение более подробно поясняется на примерах. Пример 1. Метиловый эфир 1-ацетил-2 индолинон-5-карбоновой кислоты. 10,5 г метилового эфира 2-индолинон-5 карбоновой кислоты (получение аналогичноOgawa и др., Сhеm. Pharm. Bull 36, стр. 22532258 (1988 перемешивают в 30 мл ацетангидрида в течение 4 ч при 140 С. Затем смеси дают остыть, сливают на ледяную воду и осадок отфильтровывают с помощью вакуум-фильтра. Продукт повторно промывают водой, после чего растворяют с помощью метиленхлорида, сушат над сульфатом натрия и концентрируют. Выход: 11 г (86% от теории).Rf-значение: 0,63 (силикагель, метиленхлорид/метанол 50:1). Пример 2. Метиловый эфир 1-ацетил-3-(1 этокси-1-фенилметилен)-2-индолинон-5-карбоновой кислоты. 11 г метилового эфира 1-ацетил-2 индолинон-5-карбоновой кислоты перемешивают в 110 мл ацетангидрида и 30 мл триэтилового эфира ортобензойной кислоты в течение 2 ч при 100 С. Затем центрифугируют, остаток промывают простым эфиром и отфильтровывают с помощью вакуум-фильтра. Выход: 11,5 г (67% от теории).Novobiochem) помещают в 330 мл диметилформамида для набухания. Затем добавляют 330 мл 30%-ного пиперидина в диметилформамиде и встряхивают в течение 7 мин с целью отщепления защитной Fmoc-группы, после чего смолу несколько раз промывают диметилформамидом. Далее добавляют 7,3 г 2-индолинон-5-карбоновой кислоты, 5,6 г гидроксибензотриазола,13,3 г тетрафторбората O-(бензотриазол-1-ил)N,N,N',N'-тетраметилурония и 5,7 мл N-этил 003532 22 диизопропиламина в 300 мл диметилформамида и встряхивают в течение 1 ч. Затем раствор отфильтровывают с помощью вакуум-фильтра и смолу пять раз промывают 300 мл диметилформамида и трижды 300 мл метиленхлорида. Для сушки через смолу пропускают поток азота. Выход: 28 г насыщенной смолы. Пример 4. 5 г полученной согласно примеру 3 насыщенной смолы перемешивают в 15 мл ацетангидрида при 80 С в течение 1 ч. Затем добавляют 15 мл триэтилового эфира ортобензойной кислоты и встряхивают в течение последующих 3 ч при 110 С. После этого смолу отфильтровывают с помощью вакуум-фильтра и промывают последовательно диметилформамидом, метанолом и метиленхлоридом. Выход: 7 г влажной смолы. Пример 5. 4-(Этиламинометил)нитробензол. 6 г 4-нитробензилбромида растворяют в 25 мл этанола, смешивают с 25 мл 10%-ного раствора этиламина в этаноле и в течение 2 ч нагревают с обратным холодильником. Затем смесь центрифугируют, остаток растворяют с помощью метиленхлорида и промывают разбавленным едким натром. В завершение органическую фазу концентрируют. Выход: 2,3 г (46% от теории).Rf-значение: 0,2 (силикагель, метиленхлорид/метанол 9:1). Аналогичным путем получают следующие соединения: 4-[N-(4 хлорфенилметил)аминометил]нитробензол,4-(N-циклогексиламинометил)нитробензол,4-(N-изопропиламинометил)нитробензол,4-(N-бутиламинометил)нитробензол,4-(N-метоксикарбонилметиламинометил) нитробензол,4-(N-(фенилметил)аминометил)нитробензол,4-(пирролидинометил)нитробензол,4-(морфолинометил)нитробензол,4-(пиперидинометил)нитробензол,4-(гексаметиленимино)нитробензол,4-(4-гидроксипиперидинометил)нитробензол,4-(4-метилпиперидинометил)нитробензол,4-(4-этилпиперидинометил)нитробензол,4-(4-изопропилпиперидинометил)нитробензол,4-(4-фенилпиперидинометил)нитробензол,4-(4-бензилпиперидинометил)нитробензол,4-(4-этоксикарбонилпиперидинометил)нитробензол,4-(диметиламинометил)нитробензол,4-(дипропиламинометил)нитробензол,4-(4-трет-бутилоксикарбонилпиперазинометил)нитробензол,3-(диметиламинометил)нитробензол, 23 4-(2-диэтиламиноэтил)нитробензол,4-(2-морфолинилэтил)нитробензол,4-(2-пирролидинилэтил)нитробензол,4-(2-пиперидинилэтил)нитробензол,4-(N-этил-N-бензиламинометил)нитробензол,4-(N-пропил-N-бензиламинометил)нитробензол,4-[N-метил-N-(4-хлорфенилметил)амино метил]нитробензол,4-[N-метил-N-(4-бромфенилметил)аминометил]нитробензол,4-[N-метил-N-(3-хлорфенилметил)аминометил]нитробензол,4-[N-метил-N-(3,4-диметоксифенил)аминометил]нитробензол,4-[N-метил-N-(4-метоксифенилметил)аминометил]нитробензол,4-[N-2,2,2-трифторэтил-N-(фенилметил) аминометил]нитробензол,4-[N-2,2,2-трифторэтил-N-(4-хлорфенилметил)аминометил]нитробензол. Пример 6. 4-(N-этил-N-трет-бутоксикарбониламинометил)нитробензол. 2,2 г 4-(этиламинометил)нитробензола растворяют в 50 мл уксусного эфира и в течение 30 мин перемешивают при комнатной температуре с 2,6 г ди-трет-бутилдикарбоната. Затем раствор промывают водой и концентрируют. Выход: 3,4 г.Rf-значение: 0,9 (силикагель, метиленхлорид/метанол 9:1). Аналогичным путем получают следующие соединения: 4-[N-(4-хлорфенилметил)-N-трет-бутоксикарбониламинометил]нитробензол,4-(N-циклогексил-N-трет-бутоксикарбониламинометил)нитробензол,4-(N-изопропил-N-трет-бутоксикарбониламинометил)нитробензол,4-(N-бутил-N-трет-бутоксикарбониламинометил)нитробензол,4-(N-метоксикарбонилметил-N-тpeт-бутоксикарбониламиномeтил)нитробензол,4-(N-(фенилметил)-N-трет-бутоксикарбониламинометил)нитробензол. Пример 7. 4-(N-этил-N-трет-бутоксикарбониламинометил)анилин. 6,4 г 4-(N-этил-N-трет-бутоксикарбониламинометил)нитробензола растворяют в 60 мл метанола и гидрируют в присутствии 1,5 г никеля Ренея при комнатной температуре и давлении 3 бара. Затем катализатор отфильтровывают и раствор концентрируют. Выход: 4,78 г.Rf-значение: 0,7 (силикагель, метиленхлорид/метанол 50:1). Аналогичным путем получают следующие соединения: 4-[N-(4-хлорфенилметил)-N-трет-бутоксикарбониламинометил]анилин, 003532 24 4-(N-циклогексил-N-трет-бутоксикарбониламинометил)анилин,4-(N-изопропил-N-трет-бутоксикарбониламинометил)анилин,4-(N-бутил-N-трет-бутоксикарбониламинометил)анилин,4-(N-метоксикарбонилметил-N-трет-бутоксикарбониламинометил)анилин,4-(N-(фенилметил)-N-трет-бутоксикарбониламинометил)анилин,4-(пирролидинометил)анилин,4-(морфолинометил)анилин,4-(пиперидинометил)анилин,4-(гексаметилениминометил)анилин,4-(4-гидроксипиперидинометил)анилин,4-(4-метилпиперидинометил)анилин,4-(4-этилпиперидинометил)анилин,4-(4-изопропилпиперидинометил)анилин,4-(4-фенилпиперидинометил)анилин,4-(4-бензилпиперидинометил)анилин,4-(4-этоксикарбонилпиперидинометил) анилин,4-(2-морфолинилэтил)анилин,4-(2-пирролидинилэтил)анилин,4-(2-пиперидинилэтил)анилин,4-(N-этил-N-бензиламинометил)анилин,4-(N-пропил-N-бензиламинометил)анилин,4-[N-метил-N-(4-хлорфенилметил)аминометил]анилин,4-[N-метил-N-(4-бромфенилметил)аминометил]анилин,4-[N-метил-N-(3-хлорфенилметил)аминометил]анилин,4-[N-метил-N-(3,4-диметоксифенилметил) аминометил]анилин,4-[N-метил-N-(4-метоксифенилметил)аминометил]анилин,4-[N-2,2,2-трифторэтил-N-(фенилметил) аминометил]анилин,4-[N-2,2,2-трифторэтил-N-(4-хлорфенилметил)аминометил]анилин. Получение конечных продуктов. Пример 1. Метиловый эфир 3-Z-[1-(1-метилпиперидин-4-иламино)-1-фенилметилен]-2-индолинон-5-карбоновой кислоты. 11,5 г метилового эфира 1-ацетил-3-(1 этокси-1-фенилметилен)-2-индолинон-5-карбоновой кислоты растворяют в 115 мл метиленхлорида и перемешивают в течение 5 ч при комнатной температуре с 10,8 г 4-амино-Nметилпиперидина. Затем добавляют 20 мл аммиака в метаноле и выдерживают в течение ночи. В завершение раствор упаривают и остаток промывают простым эфиром. Выход: 11,9 г (97% от теории).Rf-значение: 0,20 (силикагель, метиленхлорид/метанол 9:1),C23H25N3 О 3,масс-спектр: m/z=391 (М+). Аналогичным путем получают следующие соединения:(6) метиловый эфир 3-Z-(1-фениламино-1 фенилметилен)-2-индолинон-5-карбоновой кислоты. Пример 2. 3-Z-[1-(1-метилпиперидин-4 иламино)-1-фенилметилен]-2-индолинон-5 карбоновая кислота. 11,9 г метилового эфира 3-Z-[1-(1 метилпиперидин-4-иламино)-1-фенилметилен]2-индолинон-5-карбоновой кислоты нагревают в течение 4 ч в 300 мл метанола и 150 мл 1 н. едкого натра с обратным холодильником. Затем нейтрализуют 150 мл 1 н. соляной кислоты и концентрируют досуха. Остаток несколько раз промывают водой и сушат. Выход: 86% от теории.Rf-значение: 0,17 (силикагель, метиленхлорид/метанол 4:1),C22H23N3O3,масс-спектр: m/z=377 (М+). Аналогичным путем получают следующие соединения:(6) 3-Z-[1-фениламино-1-фенилметилен]-2 индолинон-5-карбоновую кислоту. Пример 3. 3-Z-[1-(1-метилпиперидин-4 иламино)-1-фенилметилен]-5-диметилкарбамоил-2-индолинон. 2 г 3-Z-[1-(1-метилпиперидин-4-иламино)1-фенилметилен]-2-индолинон-5-карбоновой кислоты нагревают с 5 мл тионилхлорида в течение 2 ч с обратным холодильником. Затем центрифугируют и остаток промывают простым эфиром. 0,5 г этого хлорангидрида кислоты без последующей очистки растворяют с помощью 5 мл метиленхлорида и смешивают с 0,5 мл диметиламина в 5 мл метиленхлорида, после чего перемешивают в течение ночи при комнатной температуре. В завершение продукт хроматографируют на силикагельной колонке, используя систему растворителей метиленхлорид/метанол/аммиак в соотношении 4:1:0,1. Выход: 50% от теории. Назначение: 0,14 (силикагель, метиленхлорид/метанол 9:1),C24H28N4O2,масс-спектр:m/z=404 (M+). Аналогичным путем получают следующие соединения:(3) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-диметилкарбамоил-2 индолинон: получение: из 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-2-индолинон-5 карбоновой кислоты и диметиламина или путем перемешивания в течение 20 ч при комнатной температуре 0,64 г Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-2-индолинонкарбо 27 новой кислоты, 0,34 г гидрохлорида диметиламина, 0,9 г тетрафторобората O-бензотриазол-1 ил-N,N,N',N'-тетраметилурония, 0,4 г 1-гидрокси-1 Н-бензтриазола и 2,9 г диизопропилэтиламина в 20 мл диметилформамида, после чего концентрируют и остаток суспендируют в воде; осадок отфильтровывают с помощью вакуумфильтра,выход: 600 мг (88% от теории),Rf-значение: 0,2 (силикагель, метиленхлорид/этанол 9:1),C30H32N4O2,масс-спектр:(4) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-метилкарбамоил-2-индолинон: получение: из 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-2-индолинон-5-карбоновой кислоты и метиламина аналогично примеру 3 (3),Rf-значение: 0,2 (силикагель, метиленхлорид/этанол 9:1),C29H30N4O2,масс-спектр:(5) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-метилэтилкарбамоил-2 индолинон: получение: из 3-Z-[1-(4 пиперидинометилфениламино)-1 фенилметилен]-2-индолинон-5-карбоновой кислоты и метилэтиламина аналогично примеру 3(6) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-пропилкарбамоил-2 индолинон: получение: из 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-2-индолинон-5 карбоновой кислоты и пропиламина аналогично примеру 3 (3),Rf-значение: 0,31 (силикагель, метиленхлорид/этанол 9:1),C31H34N4O2,масс-спектр:(7) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-диэтилкарбамоил-2-индолинон: получение: из 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-2-индолинон-5 карбоновой кислоты и диэтиламина аналогично примеру 3 (3),Rf-значение: 0,55 (силикагель, метиленхлорид/этанол 9:1),C32H36N4O2,масс-спектр:(32) 3-Z-(1-фениламино-1-фенилметилен)5-дипропилкарбамоил-2-индолинон. Пример 4. 3-Z-[1-(4-аминофениламино)-1 фенилметилен]-5-амидо-2-индолинон. 800 мг полученной согласно примеру 4 смолы суспендируют в 4 мл метиленхлорида и встряхивают с 0,8 г 1,4-фенилендиамина в течение 16 ч при комнатной температуре. Затем отфильтровывают и смолу несколько раз промывают метиленхлоридом, метанолом и диметилформамидом. Далее для удаления ацетильной группы добавляют в течение 2 ч 3 мл аммиака в метаноле. После повторной промывки добавляют в течение 90 мин 4 мл 10%-ной трифторуксусной кислоты в метиленхлориде, смолу отделяют и раствор концентрируют. Остаток растворяют в небольшом количестве 1 н. едкого натра и экстрагируют метиленхлоридом. Органическую фазу сушат над сульфатом натрия и центрифугируют. Выход: 45 мг (30% от теории по завершении всех стадий),Rf-значение: 0,26 (силикагель, метиленхлорид/метанол 9:1),C22H18N4O2,масс-спектр: m/z=370 (M+). Аналогичным путем получают следующие соединения:(143) 3-Z-[1-(4-(N-трифторэтил-N-(4-хлорфенилметил)аминометил)фениламино)-1 фенилметилен]-5-амидо-2-индолинон. Пример 5. 3-Z-[1-(4-(4-ацетилпиперазинилметил)фениламино)-1-фенилметилен]-5-амидо 2-индолинон. 25 мг 3-Z-[1-(4-пиперазинилметил)фениламино)-1-фенилметилен]-5-амидо-2-индолинона и 0,02 г триэтиламина растворяют в 10 мл метиленхлорида и смешивают с 5 мг ацетилхлорида,после чего раствор перемешивают в течение 16 ч при комнатной температуре. Затем промывают водой и в завершение органическую фазу центрифугируют. выход: 15 мг (68% от теории),С 29 Н 29N5O3,масс-спектр: m/z=495 (M+). 43 Аналогичным путем получают следующее соединение:(1) 3-Z-[1-(4-(4-бензоилпиперазинилметил) фениламино)-1-фенилметилен]-5-амидо-2 индолинон: получение: из 3-Z-[1-(4-(пиперазинилметил)фениламино)-1-фенилметилен]-5-амидо-2 индолинона и бензоилхлорида,выход: 91% от теории,C34H31N5 О 3,масс-спектр: m/z=557 (М+). Пример 6. 3-Z-[1-(4-диэтилкарбамоилфениламино)-1-фенилметилен]-5-амидо-2-индолинон. 7 г смолы из стадии IV подвергают аналогично примеру 4 взаимодействию с этиловым эфиром 4-аминобензойной кислоты. Влажную насыщенную смолу суспендируют в 30 мл диоксана и 30 мл метанола и перемешивают совместно с 25 мл 1 н. едкого натра в течение 40 ч. Затем нейтрализуют разбавленной соляной кислотой и промывают метиленхлоридом, метанолом и диметилформамидом. Далее 300 мг смолы суспендируют в 3 мл диметилформамида и вместе с 0,2 мл диэтиламина, 0,5 г тетрафторбората О-(бензотриазол-1-ил)-N,N,N',N'тетраметилурония и 0,8 мл этилдиизопропиламина выдерживают в течение 60 ч при комнатной температуре. В завершение продукт, аналогичный описанному в примере 4, отщепляют от смолы. Выход: 29 мг,Rf-значение: 0,46 (силикагель, метиленхлорид/метанол 9:1),C27H26N4O3,масс-спектр: m/z=454 (М+). Аналогичным путем получают следующие соединения:Rf-значение: 0,48 (силикагель, метиленхлорид/метанол 9:1),C30H24N4O3,масс-спектр: m/z=488 (M+). Пример 7. 3-Z-[1-(4-(N-метилбензоиламино)фениламино)-1-фенилметилен]-5-амидо-2 индолинон. 4,5 г смолы из стадии IV подвергают аналогично примеру 4 взаимодействию с 3,4 г 4(9 Н-флуорен-9-илметоксикарбонил)метиламино)анилина в диметилформамиде. Затем защитную группу 9 Н-флуорен отщепляют с помощью 4 мл 30%-ного пиперидина в диметилформамиде и смолу несколько раз промывают. Далее 400 мг смолы суспендируют в 4 мл диметилформамида и 0,3 мл триэтиламина, после чего подвергают взаимодействию с 0,3 мл бензоилхлорида в течение 1 ч при комнатной температуре. В завершение продукт, аналогичный описанному в примере 4, отщепляют от смолы. Выход: 33 мг,Rf-значение: 0,45 (силикагель, метиленхлорид/метанол 9:1),C30H24N4O3,масс-спектр: m/z=488 (М+). Аналогичным путем получают следующие соединения:Rf-значение: 0,53 (силикагель, метиленхлорид/метанол 9:1),С 29 Н 24N4O4S,масс-спектр: m/z=524 (М+). Пример 8. Ампула с сухим препаратом,содержащим 75 мг активного вещества из расчета на 10 мл. Состав: активное вещество 75,0 мг маннит 50,0 мг вода для инъекционных целей до 10,0 мл Получение. Активное вещество и маннит растворяют в воде. После заполнения ампулы проводят сушку вымораживанием. Для приготовления готового к использованию раствора разбавляют специальной водой для инъекционных целей. Пример 9. Ампула с сухим препаратом,содержащим 35 мг активного вещества из расчета на 2 мл. Состав: активное вещество 35,0 мг маннит 100,0 мг вода для инъекционных целей до 2,0 мл Получение. Активное вещество и маннит растворяют в воде. После заполнения ампулы проводят сушку вымораживанием. Для приготовления готового к использованию раствора разбавляют специальной водой для инъекционных целей. Пример 10. Таблетка, содержащая 50 мг активного вещества. Состав:(5) стеарат магния 2,0 мг 215,0 мг Изготовление. Ингредиенты (1), (2) и (3) смешивают и гранулируют с использованием водного раствора ингредиента (4). К высушенному грануляту примешивают ингредиент (5). Из этой смеси прессуют таблетки в форме биплана с односторонней фасеткой и насечкой с обеих сторон. Диаметр таблеток: 9 мм. Пример 11. Таблетка, содержащая 350 мг активного вещества. Состав: 46 Изготовление. Ингредиенты (1), (2) и (3) смешивают и гранулируют с использованием водного раствора ингредиента (4). К высушенному грануляту примешивают ингредиент (5). Из этой смеси прессуют таблетки в форме биплана с односторонней фасеткой и насечкой с обеих сторон. Диаметр таблеток 12 мм. Пример 12. Капсулы, содержащие 50 мг активного вещества. Состав:(2) кукурузный крахмал высушенный 58,0 мг(3) молочный сахар порошкообразный 50,0 мг(4) стеарат магния 2,0 мг 160,0 мг Изготовление. Ингредиент (1) растирают вместе с ингредиентом (3). Эту растертую массу добавляют при интенсивном перемешивании к смеси из ингредиентов (2) и (4). В завершение эту порошковую смесь с помощью соответствующего дозирующего устройства расфасовывают в капсулы размером 3 с твердым желатиновым покрытием. Пример 13. Капсулы, содержащие 350 мг активного вещества. Состав:(2) кукурузный крахмал высушенный 46,0 мг(3) молочный сахар порошкообразный 30,0 мг(4) стеарат магния 4,0 мг 430,0 мг Изготовление. Ингредиент (1) растирают вместе с ингредиентом (3). Эту растертую массу добавляют при интенсивном перемешивании к смеси из ингредиентов (2) и (4). В завершение эту порошковую смесь с помощью соответствующего дозирующего устройства расфасовывают в капсулы размером 0 с твердым желатиновым покрытием. Пример 14. Суппозитории, содержащие 100 мг активного вещества. Одна свеча содержит: активное вещество 100,0 мг полиэтиленгликоль (мол.масса 1500) 600,0 мг полиэтиленгликоль (мол.масса 6000) 460,0 мг полиэтиленсорбитанмоностеарат 840,0 мг 2000,0 мг Изготовление. Полиэтиленгликоль расплавляют совместно с полиэтиленсорбитанмоностеаратом. При температуре 40 С измельченную активную субстанцию диспергируют в расплаве до достижения гомогенности. Затем охлаждают до 38 С и разливают в предварительно слегка охлажденные формы. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Замещенные индолиноны общей формулы в которой Х обозначает атом кислорода,R1 обозначает атом водорода или С 1 С 4 алкоксикарбонильную группу,R2 обозначает карбокси-, С 1-С 4 алкоксикарбонильную или аминокарбонильную группу,где аминовый фрагмент может быть замещен одной либо двумя С 1-С 3 алкильными группами и заместители могут быть идентичными или разными,R3 обозначает необязательно замещенную атомом фтора, хлора либо брома, метильной,циано- или аминометильной группой фенильную группу,R4 обозначает атом водорода или метильную группу иR5 обозначает атом водорода,необязательно замещенную карбокси- или С 1-С 3 алкоксикарбонильной группой С 1-С 5 алкильную группу или бензильную группу, необязательно замещенную метильной группой С 3 С 7 циклоалкильную группу,необязательно замещенную метильной группой инданильную, пиридильную, оксазолильную, тиазолильную или имидазолильную группу, с которыми соответственно дополнительно через два смежных атома углерода может быть сконденсировано фенильное кольцо,необязательно замещенную атомом фтора, хлора либо брома, метокси-, карбокси-, С 1 С 3 алкилоксикарбонильной, нитро- или аминосульфонильной группой метилфенильную группу или диметоксифенильную группу, соединенную через атом углерода пирролидинильную или пиперидинильную группу, которые соответственно по атому азота замещены С 1 С 3 алкильной группой,фенильную группу, замещенную трифторметоксигруппой, атомом фтора,хлора, брома либо иода, С 1-С 3 алкоксигруппой,которая в положении 2 или 3 может быть замещена амино-, С 1-С 3 алкиламино-, ди(С 1-С 3 алкил)амино-, фенил-С 1-С 3 алкиламино-, N-(С 1-С 3 алкил)фенил-С 1-С 3 алкиламино-, пирролидиновой или пиперидиновой группой, фенил-С 1 С 3 алкиламино-С 1-С 3 алкильной группой, которая замещена в фенильном ядре атомом фтора, хлора, брома либо иода, С 1-С 5 алкильной, С 1 С 3 алкокси- или трифторметильной группой и дополнительно по атому азота амина замещена С 1-С 3 алкильной группой, в которой атомы водорода, начиная с положения 2, могут быть полностью либо частично заменены на атомы фтора, С 1-С 5 алкильной, фенильной, имидазолильной, С 3-С 7 циклоалкильной, С 1-С 3 алкоксиС 1-С 3 алкокси-, фенил-С 1-С 3 алкокси-, кapбoкcиС 1-С 3 алкильной,С 1-С 3 алкоксикарбонил-С 1 003532 48 С 3 алкильной,карбокси-,С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1-С 3 алкиламинокарбонильной, ди(С 1-С 3 алкил)аминокарбонильной, фенил-С 1-С 3 алкиламинокарбонильной, N-(С 1-С 3 алкил)фенил-С 1-С 3 алкиламинокарбонильной, пиперазинокарбонильной, N-(С 1 С 3 алкил)пиперазинокарбонильной, нитро-, амино-, С 1-С 3 алкиламино-, ди(С 1-С 3 алкил)амино-,пирролидиновой, пиперидиновой, морфолиновой, С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)-С 2 С 4 алканоиламино-, бензоиламино- или N-(С 1 С 3 алкил)бензоиламиногруппой,N-(С 1-С 3 алкил)-С 2-С 4 алканоиламиногруппой, которая в алкильном фрагменте дополнительно замещена карбокси- либо С 1-С 3 алкоксикарбонильной группой,С 1-С 3 алкиламинокарбонильной либо ди(С 1-С 3 алкил)аминокарбонильной группой, в которых один алкильный фрагмент дополнительно замещен ди(С 1-С 3 алкил)аминогруппой, илиN-(С 1-С 3 алкил)-С 1-С 3 алкилсульфониламино- либо N-(С 1-С 3 алкил)фенилсульфониламиногруппой, в которых алкильный фрагмент дополнительно может быть замещен циано-, карбокси-,С 1-С 3 алкоксикарбонильной,С 1-С 3 алкиламино-, ди(С 1-С 3 алкил)амино-, аминокарбонильной, С 1-С 3 алкиламинокарбонильной, ди(С 1 С 3 алкил)аминокарбонильной, пиперидинокарбонильной или 2-[ди(С 1-С 3 алкиламино)]этиламинокарбонильной группой,необязательно замещенную С 1 С 3 алкильной группой фенильную группу, в которой алкильный фрагмент замещен гидрокси-,С 1-С 3 алкокси-,карбокси-,С 1 С 3 алкоксикарбонильной, амино-, С 1-С 5 алкиламино-, ди(С 1-С 5 алкил)амино-, С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)-С 2-С 4 алканоиламино-,пирролидиновой, дегидропирролидиновой, пиперидиновой, дегидропиперидиновой, 3-гидроксипиперидиновой, 4-гидроксипиперидиновой, гексаметиленимино-, морфолиновой, тиоморфолиновой, пиперазиновой, 4-(С 1-С 3 алкил)пиперазиновой, 4-фенилпиперазиновой, 4(С 2-С 4 алканоил)пиперазиновой, 4-бензоилпиперазиновой или имидазолильной группой,при этом вышеуказанные насыщенные пиклоалкилениминовые кольца, С 1-С 5 алкиламино- или ди(С 1-С 5 алкил)аминогруппы дополнительно могут быть замещены одной либо двумя С 1-С 5 алкильными группами, С 3-С 7 циклоалкильной, гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1-С 3 алкиламинокарбонильной или ди(С 1-С 3 алкил)аминокарбонильной группой, в фенильном ядре - необязательно атомами фтора,хлора, брома либо иода, одно- либо двузамещенными С 1-С 3 алкильными или цианогруппами фенил-С 1-С 3 алкильной или фенильной группой,при этом заместители могут быть идентичными или разными, или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на 49 карбонильную либо сульфонильную группу, а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома, метильной,амино-, С 1-С 3 алкиламино- или ди(С 1-С 3 алкил) аминогруппой,или с одним из вышеуказанных незамещенных циклоалкилениминовых колец через два смежных атома углерода может быть сконденсировано необязательно замещенное одной либо двумя С 1-С 3 алкоксигруппами фенильное кольцо, а также их изомеры и их соли. 2. Замещенные индолиноны общей формулы I по п.1,в которых Х обозначает атом кислорода,R1 обозначает атом водорода,R2 обозначает карбокси-, С 1-С 4 алкоксикарбонильную или аминокарбонильную группу,в которой аминовый фрагмент может быть замещен одной либо двумя С 1-С 3 алкильными группами и заместители могут быть идентичными либо разными,R3 обозначает необязательно замещенную метильной группой фенильную группу,R4 обозначает атом водорода или метильную группу иR5 обозначает атом водорода,С 1-С 3 алкильную группу,бензильную группу или замещенную карбоксилибо С 1-С 3 алкоксикарбонильной группой метильную или этильную группу,необязательно замещенную метильной группой С 3-С 7 циклоалкильную группу,необязательно замещенную метильной группой инданильную, пиридильную, оксазолильную, тиазолильную или имидазолильную группу,с которыми соответственно дополнительно через два смежных атома углерода может быть сконденсировано фенильное кольцо,необязательно замещенную атомом фтора,хлора либо брома, метокси-, карбокси-, С 1-С 3 алкилоксикарбонильной, нитро- или аминосульфонильной группой метилфенильную либо диметоксифенильную группу,3-пирролидинильную или 4-пиперидинильную группу, которые соответственно по атому азота замещены С 1-С 3 алкильной группой,фенильную группу, замещенную трифторметокси-, бензилокси-, циано- или нитрогруппой, атомом фтора, хлора либо брома,С 1-С 3 алкоксигруппой, причем этокси- и нпропоксигруппа, каждая соответственно в концевом положении может быть замещена диметиламино-, диэтиламино-, N-этилметиламино-,N-бензилметиламино- либо пиперидиновой группой,фенил-С 1-С 3 алкиламино-С 1-С 3 алкильной группой, которая может быть замещена в фенильном ядре атомом фтора, хлора, брома либо иода, метильной, метокси- или трифторметиль 003532 50 ной группой и дополнительно по атому аминного азота амина может быть замещена С 1 С 5 алкильной либо 2,2,2-трифторэтильной группой, С 1-С 4 алкильной, фенильной, имидазолильной, циклогексильной, метоксиметильной, карбоксиметильной, С 1-С 3 алкоксикарбонилметильной, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1-С 3 алкиламинокарбониль-ной,ди(С 1-С 3 алкил)аминокарбонильной,фенил-С 1 С 3 алкиламинокарбонильной, N-(С 1-С 3 алкил) фенил-С 1-С 3 алкиламинокарбонильной, пиперазинокарбонильной,N-(С 1-С 3 алкил)пиперазинокарбонильной, амино-, С 1-С 3 алкиламино-, ди(С 1 С 3 алкил)амино-, пирролидиновой, пиперидиновой, морфолиновой, С 2-С 4 алканоиламино-, N(С 1-С 3 алкил)-С 2-С 4 алканоиламино-, бензоиламино- или N-( С 1-С 3)бензоиламиногруппой,N-(С 1-С 3 алкил)-С 2-С 4 алканоиламиногруппой, которая в алкильном фрагменте дополнительно замещена карбокси- либо С 1-С 3 алкоксикарбонильной группой,С 1-С 3 алкиламинокарбонильной или ди(С 1 С 3 алкил)аминокарбонильной группой, в которых один алкильный фрагмент дополнительно замещен ди(С 1-С 3 алкил)аминогруппой, или N(С 1-С 3 алкил)-С 1-С 3 алкилсульфониламино- либоN-(С 1-С 3 алкил)фенилсульфониламиногруппой,в которых алкильный фрагмент дополнительно может быть замещен циано-, карбокси-, С 1-С 3 алкоксикарбонильной, С 1-С 3 алкиламино-, ди(С 1 С 3 алкил)амино-, аминокарбонильной, С 1-С 3 алкиламинокарбонильной, ди(С 1-С 3 алкил)аминокарбонильной, пиперидинокарбонильной или 2[ди(С 1-С 3 алкиламино)]этиламинокарбонильной группой, необязательно замещенную С 1 С 3 алкильной группой фенильную группу, в которой алкильная группа замещена гидрокси-,С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, амино-, С 1-С 5 алкиламино-, ди(С 1-С 5 алкил) амино-, С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)-С 2-С 4 алканоиламино-,пирролидиновой,дегидропирролидиновой, пиперидиновой, дегидропиперидиновой,4-гидроксипиперидиновой, гексаметиленимино-, морфолиновой,тиоморфолиновой, пиперазиновой, 4-(С 1-С 3 алкил) пиперазиновой, 4-фенилпиперазиновой, 4(С 2-С 4 алканоил)пиперазиновой,4-бензоилпиперазиновой или имидазолильной группой,при этом вышеуказанные насыщенные циклоалкилениминовые кольца дополнительно могут быть замещены фенильной группой либо одной или двумя метильными группами,вышеуказанные С 1-С 5 алкиламино- и ди(С 1 С 5 алкил)аминогруппы дополнительно могут быть замещены одной либо двумя С 1 С 3 алкильными группами, циклогексильной, гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1-С 3 алкиламинокарбонильной либо ди(С 1-С 3 алкил)аминокарбонильной группой, необязательно замещенной в фенильном ядре атомом фтора, 51 хлора, брома либо иода, метильной или цианогруппой фенил-С 1-С 3 алкильной либо фенильной группой, или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на карбонильную либо сульфонильную группу, а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома, метильной, амино-,С 1-С 3 алкиламино- или ди(С 1-С 3 алкил)аминогруппой, или с одним из вышеуказанных незамещенных циклоалкилениминовых колец через два смежных атома углерода может быть сконденсировано необязательно замещенное одной или двумя С 1-С 3 алкоксигруппами фенильное кольцо,а также их изомеры и их соли. 3. Замещенные индолиноны общей формулы I по п.1,в которых Х обозначает атом кислорода,R1 обозначает атом водорода,R2 обозначает карбокси- или аминокарбонильную группу, в которой аминовый фрагмент может быть замещен одной либо двумя С 1 С 3 алкильными группами и заместители могут быть идентичными либо разными, R3 обозначает необязательно замещенную метильной группой фенильную группу,R4 обозначает атом водорода и R5 обозначает атом водорода,3-пирролидинильную либо 4-пиперидинильную группу, замещенные соответственно по атому азота С 1-С 3 алкильной группой, фенильную группу, замещенную С 1-С 3 алкоксигруппой, причем этокси- и нпропоксигруппа, каждая соответственно в концевом положении может быть замещена диметиламино-, диэтиламино-, N-этилметиламино-,N-бензилметиламино- либо пиперидиновой группой,фенил-С 1-С 3 алкиламино-С 1-С 3 алкильной группой, которая может быть замещена в фенильном ядре атомом фтора, хлора, брома либо иода, метильной, метокси- или трифторметильной группой и дополнительно по атому азота амина также С 1-С 5 алкильной либо 2,2,2 трифторэтильной группой,необязательно замещенную С 1-С 3 алкильной группой фенильную группу, в которой алкильная группа замещена гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной,амино-, С 1-С 5 алкиламино-, ди(С 1-С 5 алкил)амино-, С 2-С 4 алканоиламино-, N-(С 1-С 3 алкил)-С 2-С 4 алканоиламино-, пирролидиновой, дегидропирролидиновой, пиперидиновой, дегидропиперидиновой, 4-гидроксипиперидиновой, гексаметиленимино-, морфолиновой, тиоморфолиновой,пиперазиновой, 4-(С 1-С 3 алкил)пиперазиновой,4-фенилпиперазиновой, 4-(С 2-С 4 алканоил)пиперазиновой, 4-бензоилпиперазиновой или имидазолильной группой, 003532 52 при этом вышеуказанные насыщенные циклоалкилениминовые кольца дополнительно могут быть замещены фенильной группой либо одной или двумя метильными группами,вышеуказанные С 1-С 5 алкиламино- и ди(С 1 С 5 алкил)аминогруппы дополнительно могут быть замещены одной либо двумя С 1-С 3 алкильными группами, циклогексильной, гидрокси-, С 1-С 3 алкокси-, карбокси-, С 1-С 3 алкоксикарбонильной, аминокарбонильной, С 1-С 3 алкиламинокарбонильной либо ди(С 1-С 3 алкил) аминокарбонильной группой, необязательно замещенной в фенильном ядре атомом фтора,хлора, брома либо иода, метильной или цианогруппой фенил-С 1-С 3 алкильной либо фенильной группой, или смежная с атомом азота метиленовая группа в вышеуказанных циклоалкилениминовых кольцах может быть заменена на карбонильную либо сульфонильную группу, а вышеуказанные однозамещенные фенильные группы дополнительно могут быть замещены атомом фтора, хлора либо брома, метильной, амино-,С 1-С 3 алкиламино- или ди(С 1-С 3 алкил)аминогруппой, или с одним из вышеуказанных незамещенных циклоалкилениминовых колец через два смежных атома углерода может быть сконденсировано необязательно замещенное одной или двумя С 1-С 3 алкоксигруппами фенильное кольцо, а также их изомеры и их соли. 4. Замещенные индолиноны общей формулы I по любому из пп.1-3, в которых остаток R2 находится в положении 5. 5. Замещенные индолиноны общей формулы I по п.1, выбранные из группы, включающей(м) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-диметилкарбамоил-2 индолинон,(н) 3-Z-[1-(4-пиперидинометилфениламино)-1-фенилметилен]-5-диэтилкарбамоил-2-индолинон,(о) 3-Z-[1-(4-(3-диэтиламинопропокси)фениламино)-1-фенилметилен]-5-амидо-2-индолинон,и их соли. 6. Физиологически приемлемые соли соединений по любому из пп.1-5. 7. Лекарственные средства, содержащие в своем составе соединение по любому из пп.1-5 или соль по п.6 при необходимости наряду с одним либо несколькими инертными носителями и/или разбавителями. 8. Применение соединения по любому из пп.1-5 или соли по п.6 для изготовления соответствующего лекарственного средства, предназначенного для лечения избыточной или аномальной пролиферации клеток. 9. Способ получения лекарственного средства по п.7, отличающийся тем, что соединение по любому из пп.1-5 или соль по п.6 нехимическим путем вводят в один либо несколько инертных носителей и/или растворителей. 10. Способ получения соединений по любому из пп.1-6, отличающийся тем, что а) соединение общей формулы в которой X, R2 и R3 имеют значения, указанные в пп.1-6, R6 обозначает атом водорода, защитную группу для атома азота лактамовой группы или представляет собой связь с твердой фазой, a в которой R4 и R5 имеют значения, указанные в пп.1-6, и затем при необходимости отщепляют используемую для защиты атома азота лактамовой группы защитную группу или полученное 54 таким путем соединение отщепляют от твердой фазы, или б) для получения соединения общей формулы I, которое содержит аминометильную группу, а Х представляет собой атом кислорода,восстанавливают соединение общей формулы в которой R1-R4 имеют значения, указанные в пп.1-6, a R7 имеет значения, идентичные значениям R5, указанным в пп.1-6, при условии,что R5 содержит цианогруппу, и затем при необходимости полученное таким образом соединение общей формулы I, содержащее алкоксикарбонильную группу, путем гидролиза переводят в соответствующее карбоксисоединение,или полученное таким образом соединение общей формулы I, содержащее амино- или алкиламиногруппу, путем алкилирования либо восстановительного алкилирования, переводят в соответствующее алкиламино- либо диалкиламино-соединение, или полученное таким образом соединение общей формулы I, содержащее амино- или алкиламиногруппу, путем ацилирования переводят в соответствующее ацильное соединение,или полученное таким образом соединение общей формулы I, содержащее карбоксигруппу,путем этерификации либо амидирования переводят в соответствующее сложноэфирное либо аминокарбонильное соединение, или при необходимости используемую во время реакций для защиты реакционноспособных групп защитную группу отщепляют, или при необходимости полученное таким образом соединение общей формулы I разделяют затем на его стереоизомеры, или полученное таким образом соединение общей формулы I переводят в его соли, прежде всего, в его физиологически приемлемые для применения в фармацевтике соли с неорганическими или органическими кислотами либо основаниями.
МПК / Метки
МПК: A61K 31/40, C07D 209/34, A61P 25/28
Метки: отношению, индолиноны, киназам, ингибирующим, замещенные, действием
Код ссылки
<a href="https://eas.patents.su/28-3532-zameshhennye-indolinony-s-ingibiruyushhim-dejjstviem-po-otnosheniyu-k-kinazam-i-ciklin-cdk-kompleksam.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные индолиноны с ингибирующим действием по отношению к киназам и циклин/cdk-комплексам</a>
Предыдущий патент: Моноклональное антитело s19 к поверхностному антигену сперматозоидов, антиген, выявляемый таким антителом, и содержащие его вакцина и спермицид
Следующий патент: Высокоскоростной транспортный модуль
Случайный патент: Малогабаритный шкаф комплектного распределительного устройства с воздушной изоляцией












