Производные пиримидина и их применение в качестве модуляторов cb2
Номер патента: 12703
Опубликовано: 30.12.2009
Авторы: Слингсби Брайан Питер, Ролингз Дерек Энтони, Грин Ричард Ховард, Уиттингтон Эндрю Ричард, Митчелл Уилльям Леонард, Нейлор Алан, Итертон Эндрю Джон, Гиблин Джерард Мартин Пол
Формула / Реферат
1. Соединение формулы (I)
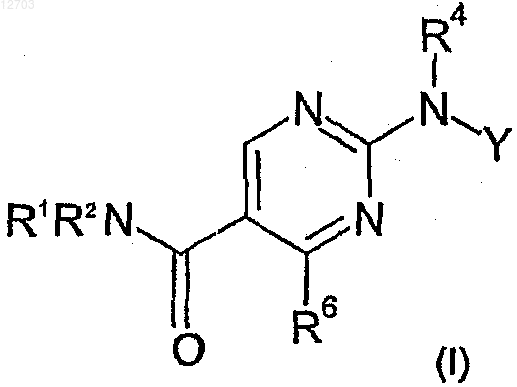
где Y представляет собой фенил, необязательно замещенный одним, двумя или тремя заместителями, независимо выбранными из C1-6-алкила, галогензамещенного C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена, C1-6-алкилсульфонильной группы, -CONH2, -NHCOCH3 и -СООН, галогензамещенного С1-6-алкокси и SO2NR8aR8b, и SC1-6-алкил;
R1 выбирают из водорода, C1-6-алкила, C3-6-циклоалкила и галогензамещенного C1-6-алкила;
R2 представляет собой (CH2)mR3, где m равен 0 или 1;
или R1 и R2 вместе с N, к которому они присоединены, образуют необязательно замещенный 4-8-членный неароматический гетероциклильный цикл, содержащий 1-4 дополнительных гетероатома, выбранных из кислорода, азота и серы, причем заместители независимо выбраны из C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена, сульфонильной группы, метилсульфонила, NR8aR8b, NHCOCH3, (=O) и -CONHCH3;
R3 представляет собой необязательно замещенную 4-8-членную неароматическую гетероциклильную группу, содержащую 1-4 гетерогруппу, выбранную из кислорода, азота и серы, необязательно замещенную C3-8-циклоалкильную группу, необязательно замещенный линейный или разветвленный C1-10-алкил, С5-7-циклоалкенил или R5, причем заместители независимо выбраны из C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена, сульфонильной группы, метилсульфонила, NR8aR8b, NHCOCH3, (=O) и -CONHCH3;
R4 выбирают из водорода, C1-6-алкила, C3-6-циклоалкила или галогензамещенного C1-6-алкила, COCH3 и SO2Me;
R5 представляет собой
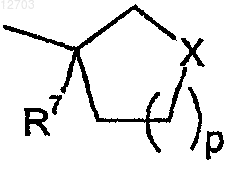
где р равен 0, 1 или 2 и X представляет собой CH2 или О;
R6 представляет собой метил, хлор или CHxFn, где n равен 1, 2 или 3, х равен 0, 1 или 2 и сумма n и х составляет 3;
R7 представляет собой ОН, C1-6-алкокси, NR8aR8b, NHCOR9, NHSO2R9, SOqR9;
R8a представляет собой Н или C1-6-алкил;
R8b представляет собой Н или C1-6-алкил;
R9 представляет собой C1-6-алкил;
q равен 0, 1 или 2;
или его фармацевтически приемлемое производное.
2. Соединение по п.1, где Y представляет собой замещенный фенил.
3. Соединение по п.1, где соединение имеет формулу (Ia)
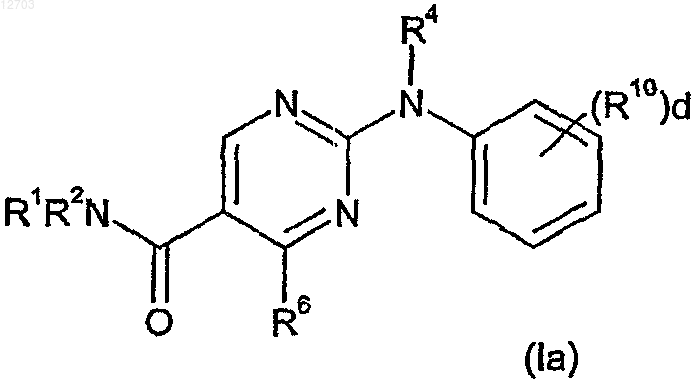
где R1 выбирают из водорода, C1-6-алкила, C3-6-циклоалкила и галогензамещенного C1-6-алкила;
R2 представляет собой (CH2)mR3, где m равен 0 или 1;
или R1 и R2 вместе с N, к которому они присоединены, образуют 4-8-членный неароматический цикл, выбранный из азетидинила, пирролидинила, морфолинила, пиперазинила, пиперидинила, тетрагидропиридинила, азапина, оксапина, азациклооктанила, азаоксациклооктанила и азатиациклооктанила, любой из которых может быть незамещенным или замещен одним, двумя или тремя заместителями, выбранными из C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена, сульфонильной группы, метилсульфонила, NR8aR8b, NHCOCH3, (=O) и -CONHCH3;
R3 представляет собой 2- или 3-азетидинил, оксетанил, тиоксетанил, тиоксетанил-s-оксид, тиоксетанил-s,s-диоксид, диоксаланил, пирролидинил, тетрагидрофуранил, тетрагидротиофенил, морфолинил, пиперидинил, пиперазинил, тетрагидропиранил, тетрагидротиопиранил, тиоморфолинил, тиоморфолинил-s,s-диоксид, тетрагидропиридинил, азапин, оксапин, азациклооктанил, азаоксациклооктанил, азатиациклооктанил, оксациклооктанил, тиациклооктанил, C3-8-циклоалкильную группу, линейный или разветвленный C1-10-алкил, С5-7-циклоалкенил или R5, любой из которых может быть незамещенным или замещен одним, двумя или тремя заместителями, выбранными из C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена, сульфонильной группы, метилсульфонила, NR8aR8b, NHCOCH3, (=O) и -CONHCH3;
R10 выбирают из C1-6-алкила, галогензамещенного C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена, C1-6-алкилсульфонильной группы, -CONH2, -NHCOCH3, -COOH, галогензамещенного C1-6-алкокси, SC1-6-алкила и SO2NR8aR8b;
R4 выбирают из водорода, C1-6-алкила, C3-6-циклоалкила или галогензамещенного C1-6-алкила, COCH3 и SO2Me;
R5 представляет собой
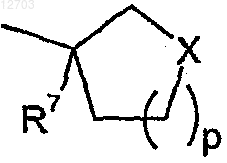
где р равен 0, 1 или 2 и X представляет собой СН2 или О;
R6 представляет собой метил, хлор или CHxFn, где n равен 1, 2 или 3, х равен 0, 1 или 2 и сумма n и х составляет 3;
R7 представляет собой ОН, С1-6-алкокси, NR8aR8b, NHCOR9, NHSO2R9, SOqR9;
R8a представляет собой Н или C1-6-алкил;
R8b представляет собой Н или C1-6-алкил;
R9 представляет собой C1-6-алкил;
q равен 0, 1 или 2;
d равен 0, 1, 2 или 3;
или его фармацевтически приемлемое производное.
4. Соединение по любому из пп.1-3, где R4 представляет собой C1-6-алкил или водород.
5. Соединение по любому из пп.1-4, где R6 представляет собой CF3.
6. Соединение по любому из пп.1-3, выбранное из следующих соединений:
1-[2-(3-хлорфениламино)-4-трифторметилпиримидин-5-ил]-1-пиперидин-1-илметанон;
циклопентилметиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
1-[2-(3-хлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон;
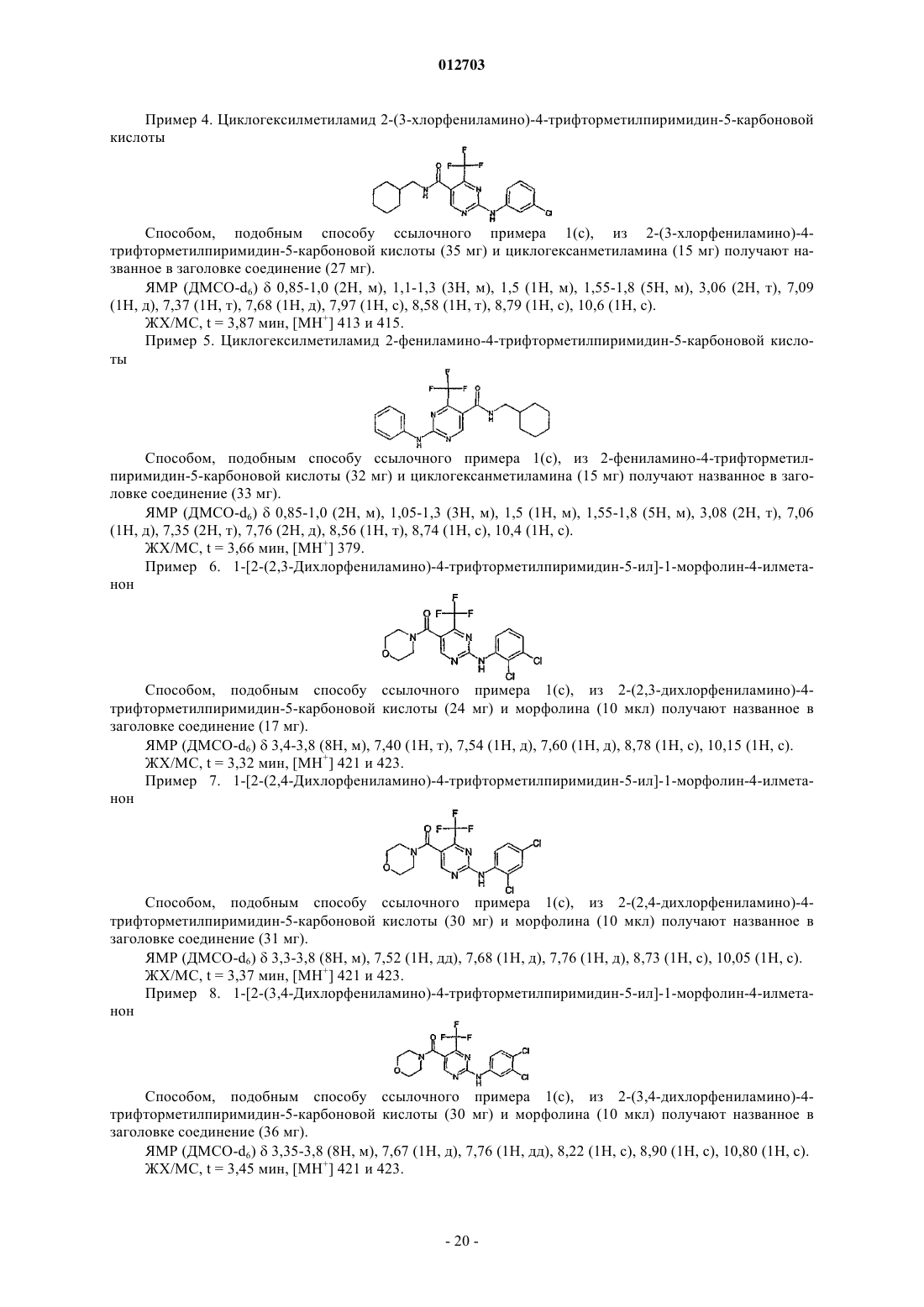
циклогексилметиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
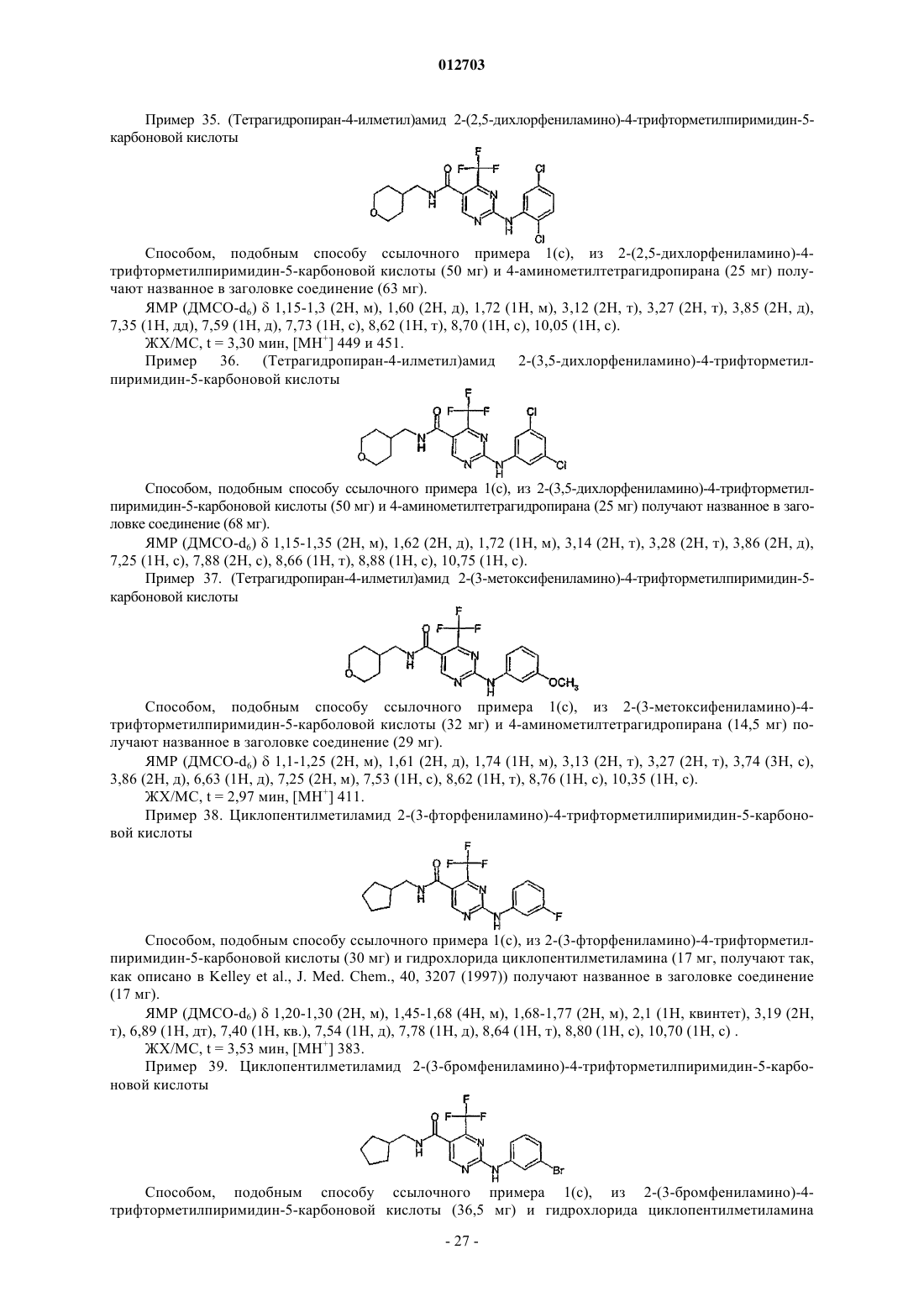
циклогексилметиламид 2-фениламино-4-трифторметилпиримидин-5-карбоновой кислоты;
1-[2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон;
1-[2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон;
1-[2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон;
1-[2-(2,5-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон;
1-[2-(3-фторфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон;
1-[2-(3-бромфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон;
1-[2-(3-бромфениламино)-4-трифторметилпиримидин-5-ил]-1-пиперидин-4-илметанон;
1-[2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон;
циклопентиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин -5-карбоновой кислоты;
циклогексилметиламид 2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2,6-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3-метоксифениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(циклопентилметил)амид 2-(3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(циклопентилметил)амид 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(2,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(2,6-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(3-метоксифениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутиламид 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутиламид 2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутиламид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутиламид 2-(2,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутиламид 2-(2,6-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты
циклобутиламид 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутиламид 2-(3-метоксифениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2,6-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
1-[2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-(морфолин-4-ил)метанон;
циклогексилметиламид 2-(3-метоксифениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(1-гидроксициклогексилметил)амид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(1-гидроксициклогексилметил)амид 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(3-хлор-4-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(3-хлор-2-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(5-хлор-2-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(3,5-дифторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(4-хлор-2-трифторметилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(3-цианофениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3-цианофениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(3-цианофениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(4-цианофениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(4-цианофениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(4-цианофениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3-метокси-5-(трифторметил)фениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3,5-бис-трифторметилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3-бром-5-(трифторметил)фениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3-фтор-5-(трифторметил)фениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-фтор-3-(трифторметил)фениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-метилтио-3-(трифторметил)фениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(циклопентилметил)амид 2-(5-хлор-2-метилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3-хлор-4-метилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3-хлор-2-метилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(4-хлор-3-метоксифениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(4-хлор-3-метилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметилметиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметилметиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметилметиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(5-хлор-2-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3,5-дифторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3-хлор-4-трифторметоксифениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3-хлор-4-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3-хлор-2-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3-фтор-4-трифторметилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3-хлор-4-цианофениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2,6-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3-метоксифениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентиламид 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентиламид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопропиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(3,3-диметилбутил)амид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)аьшф 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-фтор-3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-фтор-5-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3,5-дифторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(4-фтор-3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(4-трифторметокси-3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(4-циано-3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(4-трифторметил-3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(4-циано-3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(1,1-диоксогексагидро-1l6-тиопиран-4-ил)амид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2,4-дифторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2-хлор-4-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2,4-дифторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2-хлор-4-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2-хлор-4-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2-фтор-4-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2-хлор-4-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2-фтор-4-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2-фтор-4-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2-бром-4-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2-фтор-4-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-фтор-4-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-хлор-4-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-хлор-4-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-хлор-4-цианофениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-хлор-4-трифторметилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2-хлор-4-цианофениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2-бром-4-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-бром-4-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопропилметиламид 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопропилметиламид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2,3-дифторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2-фтор-3-трифторметилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(2-хлор-4-метилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(4-хлор-3-метоксифениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклогексилметиламид 2-(5-хлор-2-метилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(3-хлор-4-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(3-хлор-2-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(2-хлор-5-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклопентилметиламид 2-(фениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
циклобутилметиламид 2-(2-фтор-3-трифторметилфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидропиран-4-илметил)амид 2-(2-трифторметил-4-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидротиопиран-4-илметил)амид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(тетрагидротиопиран-4-илметил)амид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(2-оксопропил)амид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(диоксогексагидро-1l6-тиопиран-4-илметил)амид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;
(диоксогексагидро-1l6-тиопиран-4-илметил)амид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты,
или его фармацевтически приемлемое производное.
7. Циклопентилметиламид 2-(3-хлор-4-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты или его фармацевтически приемлемое производное.
8. Циклопентилметиламид 2-(3-хлор-4-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты.
9. Соединение по любому из пп.1-8 в форме наночастиц.
10. Фармацевтическая композиция, включающая соединение по любому из пп.1-9 или его фармацевтически приемлемое производное.
11. Фармацевтическая композиция по п.10, дополнительно включающая фармацевтически приемлемый носитель или разбавитель.
12. Способ лечения человека или животного, страдающего от состояния, опосредованного активностью рецепторов каннабиноида 2, включающий введение субъекту терапевтически эффективного количества соединения формулы (I) по любому из пп.1-9 или его фармацевтически приемлемого производного.
13. Способ по п.12, в котором состоянием является иммунное расстройство, воспалительное расстройство, боль, ревматоидный артрит, рассеянный склероз, остеоартрит или остеопороз.
14. Способ по п.13, где боль выбрана из воспалительной боли, висцеральной боли, раковой боли, невропатической боли, боли в нижнем отделе спины, мышечной боли, послеоперационной боли, острой боли или мигрени.
15. Способ по п.13, где воспалительное расстройство представляет собой расстройство желудочно-кишечного тракта, такое как болезнь Крона или язвенный колит.
Текст
012703 Настоящее изобретение относится к новым производным пиримидина, фармацевтическим композициям, содержащим такие соединения, и их применению при лечении болезней, в частности боли, вызванных непосредственно или косвенно повышением или понижением активности каннабиноидных рецепторов. Каннабиноиды представляют собой специфический класс психотропных соединений, присутствующих в конопле индийской (Cannabis sativa), включающих примерно шестьдесят различных молекул,причем наиболее характерными являются каннабиол, каннабидиол и некоторые изомеры тетрагидроканнабинола. Знания о терапевтической активности конопли восходят к древним династиям Китая, где 5000 лет назад коноплю использовали для лечения астмы, мигрени и некоторых гинекологических расстройств. Позднее такие применения утвердились настолько, что около 1850 г. экстракты конопли были включены в Фармакопею США и оставались там до 1947 г. Известно, что каннабиноиды оказывают различное действие на разные системы и/или органы, причем наиболее важным является действие на центральную нервную систему и на сердечно-сосудистую систему. Такое действие включает изменения в памяти и познавательной способности, эйфорию и седативный эффект. Также наблюдают периферическое действие, связанное с сужением бронхов, иммуномодуляцией и воспалением. Также подтверждена документально способность каннабиноидов снижать внутриглазное давление и воздействовать на дыхательную и эндокринную системы. См., например, L.E.Hollister, Health Aspects of Cannabis, Pharmacological Reviews, Vol. 38, pp. 1-20 (1986). Позднее обнаружилось, что каннабиноиды подавляют клеточные и гуморальные иммунные реакции и проявляют противовоспалительные свойства. Wirth et al., Antiinflammatory Properties of Cannabichrome, Life Science, Vol. 26,pp. 1991-1995 (1980). Несмотря на вышеописанные преимущества, терапевтическое применение конопли является спорным как из-за связанного с ним психотропного действия (по причине зависимости и аддикции), так и из-за разнообразных побочных действий, которые пока не совсем ясны. Хотя работа в данной области продолжается непрерывно с 1940-х, доказательства, указывающие на то, что периферические эффекты каннабиноидов опосредуются прямо, а не вторично действием на ЦНС, ограничены за отсутствием характеризации рецепторов, отсутствием информации, касающейся андогенного лиганда каннабиноидов, и до недавних пор отсутствием соединений, селективных для подтипов рецепторов. Обнаружено, что первый каннабиноидный рецептор локализуется, главным образом, в головном мозге, в линиях нейральных клеток и только в меньшей степени на периферическом уровне. С учетом его локализации его назвали центральным рецептором ("СВ 1"). См. Matsuda et al., "Structure of a CannabinoidReceptor and Functional Expression of the Cloned cDNA", Nature, Vol. 346, pp. 561-564 (1990). Второй каннабиноидный рецептор ("CB2") идентифицирован в селезенке и оценен как модулирующий непсихотропное действие каннабиноидов. См. Munro et al., "Molecular Characterization of a Peripheral Receptor forCannabinoids", Nature, Vol. 365, pp. 61-65 (1993). Недавно получен ряд соединений, которые способны действовать как агонисты в отношении обоих каннабиноидных рецепторов. Например, известно применение производных дигидроксипиррол-(1,2,3d,е)-1,4-бензоксазина при лечении глаукомы и применение производных 1,5-дифенилпиразола в качестве иммуномодуляторов или психотропных средств при лечении различных невропатологий, мигрени, эпилепсии, глаукомы и т.д. См. патент США 5112820 и ЕР 576357 соответственно. Однако, поскольку указанные соединения активны в отношении как рецептора СВ 1, так и рецептора СВ 2, их применение может привести к серьезному психотропному действию. Описанные выше показания и преимущественная локализация рецептора СВ 2 в иммунной системе подтверждают специфическую роль СВ 2 в модуляции иммунной и противовоспалительной реакции на стимулирование различных источников. Общее количество людей, страдающих от боли, огромно (почти 300 млн), с преобладанием людей,страдающих от боли в спине, остеоартрической боли и послеоперационной боли. Невропатическая боль(связанная с повреждениями нейронов, такими как повреждения, вызванные диабетом, ВИЧ, герпесной инфекцией или ударом) имеет место с меньшим, но все еще существенным, преобладанием над болью при раковых заболеваниях. Патогенные механизмы, приводящие к болевым симптомам, можно отнести к двум основным категориям: механизмы, являющиеся компонентами воспалительной реакции ткани (воспалительная боль); и механизмы, являющиеся результатом повреждения нейронов определенной формы (невропатическая боль). Хроническую воспалительную боль составляют преимущественно остеоартрит, хроническая боль в нижней части спины и ревматоидный артрит. Боль является результатом внезапного или постоянного повреждения и/или воспаления. Такая боль может быть спонтанной или спровоцированной. В основе лежит патологическая гиперчувствительность как результат физиологической гипервозбудимости и высвобождения медиаторов воспаления, которые затем потенцируют такую гипервозбудимость. Рецепторы СВ 2 экспрессируются на клетках зоны воспаления (Т-клетки, В-клетки, макрофаги,тучные клетки) и опосредуют иммунную супрессию через ингибирование высвобождения медиаторов-1 012703 клеточного взаимодействия/воспаления. Рецепторы СВ 2 также могут экспрессироваться на сенсорных нервных окончаниях и, следовательно, ингибировать гипералгезию непосредственно. Теперь проверяется роль СВ 2 при иммуномодуляции, воспалении, остеопорозе, сердечнососудистых заболеваниях, болезнях почек и других болезненных состояниях. С учетом того факта, что каннабиноиды действуют на рецепторы, способные модулировать различные функциональные действия,и с учетом низкой гомологии между СВ 2 и СВ 1 важность разработки класса лекарственных средств, селективных для специфического рецептора, очевидна. Природные и синтетические каннабиноиды, доступные в настоящее время, не выполняют указанной функции, поскольку они активны в отношении обоих рецепторов. На основании вышеизложенного существует потребность в соединениях, способных селективно модулировать рецепторы для каннабиноидов и, следовательно, патологий, связанных с такими рецепторами. Таким образом, модуляторы СВ 2 являются уникальным подходом к фармакотерапии иммунных расстройств, воспаления, остеопороза, почечной ишемии и других патофизиологических состояний. Настоящее изобретение относится к новым производным пиримидина формулы (I) и их фармацевтически приемлемым производным, фармацевтическим композициям, содержащим такие соединения или производные, и их применению в качестве модуляторов рецептора СВ 2, которые полезны при лечении различных расстройств. Настоящее изобретение также относится к способу лечения болезни, опосредованной рецепторами СВ 2, у животного, включая человека, включающему введение животному, нуждающемуся в этом, эффективного количества соединения формулы (I) или его фармацевтически приемлемого производного. Изобретение относится к соединениям формулы (I) где Y представляет собой фенил, необязательно замещенный одним, двумя или тремя заместителями;R1 и R2 вместе с N, к которому они присоединены, образуют необязательно замещенный 4-8 членный неароматический гетероциклильный цикл;R3 представляет собой необязательно замещенную 4-8-членную неароматическую гетероциклильную группу, необязательно замещенную С 3-8-циклоалкильную группу, необязательно замещенный линейный или разветвленный C1-10-алкил, С 5-7-циклоалкенил или R5; где р равен 0, 1 или 2, и X представляет собой СН 2 или О;q равен 0, 1 или 2; и их фармацевтически приемлемым производным. В одном отдельном воплощении Y представляет собой замещенный фенил. В одном отдельном воплощении Y замещен 1 или 2 заместителями. Если Y является монозамещенным, в одном отдельном воплощении заместитель находится в положении 3. Если Y является дизамещенным, в одном отдельном воплощении заместители находятся в положениях 2 и 4. Когда Y является замещенным, заместитель или заместители предпочтительно выбирают изC1-6-алкила, галогензамещенного C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена,C1-6-алкилсульфонильной группы, -CONH2, -NHCOCH3 и -СООН. Кроме того, заместитель или заместители можно выбрать из галогензамещенного C1-6-алкокси и SO2NR8aR8b, где R8a и R8b имеют значения,указанные выше. Кроме того, заместитель или заместители могут представлять собой SC1-6-алкил. В одном отдельном воплощении Y замещен хлором, фтором, бромом, циано, CF3, метилом,CF3O- или SCH3 и метокси; предпочтительнее галогеном, циано или метокси.-2 012703 В одном отдельном воплощении соединение формулы (I) представляет собой соединение формулыR1 и R2 вместе с N, к которому они присоединены, образуют 4-8-членный неароматический цикл,выбранный из азетидинила, пирролидинила, морфолинила, пиперазинила, пиперидинила, тетрагидропиридинила, азапина, оксапина, азациклооктанила, азаоксациклооктанила и азатиациклооктанила, любой из которых может быть незамещенным или замещен одним, двумя или тремя заместителями, выбранными из C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена, сульфонильной группы, метилсульфонила, NR8aR8b, NHCOCH3, (=O) и -CONHCH3;R3 представляет собой 2- или 3-азетидинил, оксетанил, тиоксетанил, тиоксетанил-s-оксид, тиоксетанил-s,s-диоксид, диоксаланил, пирролидинил, тетрагидрофуранил, тетрагидротиофенил, морфолинил,пиперидинил, пиперазинил, тетрагидропиранил, тетрагидротиопиранил, тиоморфолинил, тиоморфолинил-s,s-диоксид, тетрагидропиридинил, азапин, оксапин, азациклооктанил, азаоксациклооктанил, азатиациклооктанил, оксациклооктанил, тиациклооктанил, C3-8-циклоалкильную группу, линейный или разветвленный C1-10-алкил, С 5-7-циклоалкенил или R5, любой из которых может быть незамещенным или замещен одним, двумя или тремя заместителями, выбранными из C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена, сульфонильной группы, метилсульфонила, NR8aR8b, NHCOCH3, (=O) и где р равен 0, 1 или 2, и X представляет собой СН 2 или О;d равен 0, 1, 2 или 3; и его фармацевтически приемлемые производные. В одном отдельном воплощении R1 представляет собой водород. В одном отдельном воплощении R4 представляет собой C1-6-алкил или водород, предпочтительнее метил или водород, даже предпочтительнее водород. С другой стороны, R1 и R2 вместе с N, к которому они присоединены, образуют необязательно замещенный 5- или 6-членный неароматический гетероциклильный цикл. Когда R1 и R2 вместе с N, к которому они присоединены, образуют 4-8-членный неароматический гетероциклильный цикл, который является замещенным, или когда R3 является замещенным, заместитель или заместители предпочтительно выбирают из C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена или сульфонильной группы. Кроме того, необязательный(ые) заместитель(и) можно выбрать из метилсульфонила, NR8aR8b, NHCOCH3, (=O) или -CONHCH3,В одном отдельном воплощении R6 представляет собой CHxFn, например CF3, CHF2, CH2F, предпочтительно CF3. В одном отдельном воплощении R5 представляет собой где р равен 0, 1 или 2. В одном отдельном воплощении R7 представляет собой ОН.-3 012703 В одном отдельном воплощении R3 представляет собой необязательно замещенную 4-8-членную неароматическую гетероциклильную группу, необязательно замещенную C3-8-циклоалкильную группу,необязательно замещенный линейный или разветвленный C1-10-алкил или R5. В одном отдельном воплощении, когда R3 представляет собой необязательно замещенную С 3-8-циклоалкильную группу или необязательно замещенный 4-8-членный неароматический гетероциклил, m равен 1. В одном отдельном воплощении R3 представляет собой необязательно замещенную С 3-6-циклоалкильную группу или необязательно замещенный 4- или 6-членный неароматический гетероциклил. В одном отдельном воплощении R1 и R2 вместе с N, к которому они присоединены, образуют 4-8-членный неароматический гетероциклильный цикл, который выбирают из пирролидинила, морфолинила, пиперазинила, пиперидинила и тетрагидропиридинила. В одном отдельном воплощении, когда R3 представляет собой неароматический гетероциклил, его выбирают из пирролидинила, тетрагидрофуранила, тетрагидротиофенила, морфолинила, пиперидинила,пиперазинила, тетрагидропиранила, тетрагидротиопиранила, тиоморфолинила, тиоморфолинил-s,sдиоксида, тетрагидропиридинила. В одном отдельном воплощении соединение формулы (I) представляет собой соединение формулы где R3 представляет собой пирролидинил, тетрагидрофуранил, тетрагидротиофенил, морфолинил,пиперидинил, пиперазинил, тетрагидропиранил, тетрагидротиопиранил, тиоморфолинил, тиоморфолинил-s,s-диоксид, тетрагидропиридинил, C3-8-циклоалкильную группу, любой из которых может быть незамещенньм или замещен одним, двумя или тремя заместителями, выбранными из C1-6-алкила,C1-6-алкокси, гидроксигруппы, цианогруппы, галогена, сульфонильной группы, метилсульфонила,NR8aR8b, NHCOCH3, (=O) и -CONHCH3;R4 выбирают из водорода или метила;d равен 0, 1, 2 или 3; и его фармацевтически приемлемые производные. В одном отдельном воплощении m равен 1. В одном отдельном воплощении соединение формулы (I) представляет собой соединение формулы где R1 и R2 вместе с N, к которому они присоединены, образуют 5-6-членный неароматический цикл, выбранный из пирролидинила, морфолинила, пиперазинила, пиперидинила и тетрагидропиридинила, любой из которых может быть незамещенным или замещен одним, двумя или тремя заместителями, выбранными из C1-6-алкила, C1-6-алкокси, гидроксигруппы, цианогруппы, галогена, сульфонильной группы, метилсульфонила, NR8aR8b, NHCOCH3, (=O) и -CONHCH3;R4 представляет собой водород или метил;d равен 0, 1, 2 или 3; и его фармацевтически приемлемые производные. В одном отдельном воплощении соединения являются селективными для СВ 2 по сравнению с СВ 1. Предпочтительно соединения являются 100-кратно селективными, т.е. соединения формулы (I) имеют величину ЕС 50 для клонированного человеческого каннабиноидного рецептора СВ 2 по меньшей мере 100-кратную относительно величины ЕС 50 для клонированного человеческого каннабиноидного рецептора СВ 1 или имеют менее чем 10% эффективность для рецептора СВ 1.-4 012703 Изобретение описывается с использованием приведенных далее определений, если не указывается иное. Термин "фармацевтически приемлемое производное" обозначает любые фармацевтически приемлемые соли, сложные эфиры, соли таких эфиров или сольваты соединений формулы (I) или любого другого соединения, которые после введения реципиенту способны дать (прямо или косвенно) соединение формулы (I) или его активный метаболит или остаток. Специалистам в данной области техники следует иметь в виду, что для получения их фармацевтически приемлемых производных соединения формулы (I) можно модифицировать по любым функциональным группам в соединениях и что соединения формулы (I) можно дериватизировать по нескольким положениям. Следует иметь в виду, что для фармацевтического применения соли, о которых речь шла выше, будут физиологически приемлемыми солями, но и другие соли могут найти применение, например, при получении соединений формулы (I) и их физиологически приемлемых солей. Фармацевтически приемлемые соли включают соли, описанные в Berge, Bighley и Monkhouse, J. Pharm. Sci., 1977, 66, 1-19. Термин "фармацевтически приемлемые соли" относится к солям, полученным из фармацевтически приемлемых нетоксичных оснований, в том числе неорганических оснований и органических оснований. Соли,полученные из неорганических оснований, включают соли алюминия, аммония, кальция, меди, железа(3), железа(2), лития, магния, марганца(3), марганца(2), калия, натрия, цинка и т.п. Соли, образованные с фармацевтически приемлемыми нетоксичными органическими основаниями, включают соли первичных, вторичных и третичных аминов, замещенных аминов, в том числе встречающихся в природе замещенных аминов, циклических аминов и основных ионообменных смол, таких как аргинин, бетаин, кофеин, холин, N,N'-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, морфолин, пиперазин, пиперидин, полиаминовые смолы,прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин, трометамин и подобные основания. Когда соединение настоящего изобретения является основанием, соли можно получить с фармацевтически приемлемыми нетоксичными кислотами, в том числе неорганическими и органическими кислотами. К таким кислотам относятся уксусная, бензолсульфоновая, бензойная, камфарсульфоновая,лимонная, этансульфоновая, фумаровая, глюконовая, глутаминовая, бромо-водородная, хлороводородная, изэтионовая, молочная, малеиновая, яблочная, миндальная, метансульфоновая, слизевая,азотная, памовая, пантотеновая, фосфорная, янтарная, серная, винная, п-толуолсульфоновая кислота и подобные кислоты. Предпочтительные примеры фармацевтически приемлемых солей включают аммониевые, кальциевые, магниевые, калиевые и натриевые соли и соли, образованные с малеиновой, фумаровой, бензойной,аскорбиновой, памовой, янтарной, хлоро-водородной, серной, бис-метиленсалициловой, метансульфоновой, этандисульфоновой, пропионовой, винной, салициловой, лимонной, глюконовой, аспарагиновой,стеариновой, пальмитиновой, итаконовой, гликолевой, п-аминобензойной, глутаминовой, бензолсульфоновой, циклогексилсульфаминовой, фосфорной и азотной кислотами. Термин "галоген" используется для обозначения фтора, хлора, брома или иода. Термин "алкил" как обозначение группы или части группы подразумевает алкильную группу с линейной или разветвленной цепью или их комбинацию, например метил, этил, н-пропил, изопропил,н-бутил, втор-бутил, трет-бутил, пентил, гексил, 1,1-диметилэтил или их комбинация. Термин "алкокси" как обозначение группы или части группы подразумевает линейную, разветвленную или циклическую алкильную группу с атомом кислорода, присоединенным к цепи, например метокси, этокси, н-пропокси, изопропокси, н-бутокси, втор-бутокси, трет-бутоксигруппу, пентокси, гексилоксигруппу, циклопентокси- или циклогексилоксигруппу. Термин "циклоалкил" обозначает замкнутый неароматический цикл, например циклобутил, циклопентил, циклогексил, или циклогептил, или циклооктил. Термин "циклоалкенил" как обозначение группы или части группы подразумевает неароматический цикл, содержащий по меньшей мере одну группу СН=СН, например циклобутенил, циклопентенил, циклогексенил, или циклогептенил, или циклооктенил. Когда R1 и R2, взятые вместе с N, к которому они присоединены, образуют необязательно замещенный гетероциклильный цикл, такой цикл может необязательно содержать дополнительные 1, 2, 3 или 4 гетероатома. Цикл может быть насыщенным или ненасыщенным. Предпочтительно дополнительные гетероатомы выбирают из атомов кислорода, азота или серы. Примером 4-членного гетероциклила является азетидинил. Примеры 5-членных гетероциклилов включают пирролидинил. Примерами 6-членных гетероциклилов являются морфолинил, пиперазинил или пиперидинил. Другим примером является тетрагидропиридинил. Примерами 7-членных гетероциклилов являются азапин или оксапин. Примерами 8-членных гетероциклилов являются азациклооктанил, азаоксациклооктанил или азатиациклооктанил. Когда R3 представляет собой необязательно замещенную неароматическую гетероциклильную группу, цикл может содержать 1, 2, 3 или 4 гетероатома. Предпочтительно гетероатомы выбирают из атомов кислорода, азота или серы. Примерами 4-членных групп являются 2- или 3-азитидинил, оксета-5 012703 нил, тиоксетанил, тиоксетанил-s-оксид, тиоксетанил-s,s-диоксид. Примеры 5-членных гетероциклильных групп в данном случае включают диоксаланил, пирролидинил, или тетрагидрофуранил, или тетрагидротиофенил. Примерами 6-членных гетероциклильных групп являются морфолинил, пиперидинил, пиперазинил, тетрагидропиранил, тетрагидротиопиранил, тиоморфолинил или тиоморфолинил-s,s-диоксид. Другим примером является тетрагидропиридинил. Примерами 7-членных гетероциклильных групп являются азапин и оксапин. Примерами 8-членных гетероциклильных групп являются азациклооктанил, азаоксациклооктанил или азатиациклооктанил, оксациклооктанил или тиациклооктанил. В одном отдельном воплощении соединения настоящего изобретения можно выбрать из группы, в которую входят 1-[2-(3-хлорфениламино)-4-трифторметилпиримидин-5-ил]-1-пиперидин-1-илметанон; циклопентилметиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты; 1-[2-(3-хлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-1-илметанон; циклогексилметиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты; циклогексилметиламид 2-фениламино-4-трифторметилпиримидин-5-карбоновой кислоты; 1-[2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон; 1-[2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон; 1-[2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон; 1-[2-(2,5-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон; 1-[2-(3-фторфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон; 1-[2-(3-бромфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон; 1-[2-(3-бромфениламино)-4-трифторметилпиримидин-5-ил]-1-пиперидин-4-илметанон; 1-[2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон; циклопентиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты; циклогексилметиламид 2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты; циклогексилметиламид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты; циклогексилметиламид 2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты; циклогексилметиламид 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты; циклогексилметиламид 2-(3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты; циклогексилметиламид 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты; циклогексилметиламид 2-(2,6-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты;(тетрагидротиопиран-4-илметил)амид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5 карбоновой кислоты; и их фармацевтически приемлемые производные. Соединения формулы (I) можно получить так, как указано на схемах, приведенных далее. Схема 1 В приведенных формулах L представляет собой удаляемую группу, например галоген, PG представляет собой защитную группу, например метил, этил или бензил, X представляет собой удаляемую группу, например галоген, OC1-6-алкил, например O-метил или O-этил, или NRaRb, где Ra и Rb выбирают независимо из C1-6-алкила, например метила, и R1, R2, R4, R6 и Y имеют значения, указанные при определении соединений формулы (I). Схема 2 В приведенных формулах L1 и L2 представляют собой удаляемые группы, выбранные независимо из галогена, например хлора, и R1, R2, R4, R6 и Y имеют значения, указанные при определении соединений формулы (I). Следует иметь в виду, что настоящее изобретение охватывает все изомеры соединений формулы (I) и их фармацевтически приемлемых производных, включая все геометрические, таутомерные и оптические формы, и их смеси (например, рацемические смеси). Когда в соединениях формулы (I) присутствуют дополнительные хиральные центры, настоящее изобретение включает в свой объем все возможные диастереоизомеры, в том числе их смеси. Различные изомерные формы можно расщепить или отделить одну от другой обычными способами или любой данный изомер можно получить обычными синтетическими способами или стереоспецифическим, или асимметричным синтезом. Предметом изобретения также являются соединения, меченные радиоактивными изотопами, которые идентичны соединениям, описываемым формулой I и последующими формулами, но в которых в действительности один или несколько атомов заменены атомом с атомной массой или массовым числом, отличающимися от атомной массы или массового числа, обычно обнаруживаемых в природе. Примеры изотопов, которые можно вводить в соединения изобретения, включают изотопы водорода, углерода, азота, кислорода, фосфора,- 10012703 фтора, иода и хлора, такие как 3 Н, 11 С, 14 С, 8F, 123I и 125I. Соединения настоящего изобретения и фармацевтически приемлемые соли указанных соединений,содержащие вышеуказанные изотопы и/или другие изотопы других атомов, входят в объем настоящего изобретения. Меченные изотопами соединения настоящего изобретения, например соединения, в которые внедрены радиоактивные изотопы, такие как 3 Н, 14 С, пригодны в анализах лекарственного средства и/или распределения в тканевом субстрате. Изотопы трития, т.е. 3 Н, и углерода-14, т.е. 14 С, особенно предпочтительны для легкости получения и обнаружения. Изотопы 11 С и 8F особенно пригодны в PET(позитронная эмиссионная томография), и изотоп 125I особенно пригоден в SPECT (эмиссионная компьютерная томография одиночных фотонов), и все пригодны при визуализации головного мозга. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2 Н, может дать некоторые лечебные преимущества, являющиеся результатом большей метаболической устойчивости, например повышенного полупериода существования in vivo или при необходимости пониженных дозировок, и, следовательно, предпочтительно при некоторых обстоятельствах. Меченные изотопами соединения формулы I и другие соединения данного изобретения, как правило, можно получить, осуществляя процедуры, описанные на схемах и/или ниже в примерах, путем замещения легко доступным меченным изотопами реагентом реагента, не меченного изотопами. Соединения формулы (I) можно получить в кристаллической или некристаллической форме, и, если форма кристаллическая, они могут быть необязательно гидратированными или сольватированными. Данное изобретение включает в свой объем стехиометрические гидраты или сольваты, а также соединения, содержащие переменные количества воды и/или растворителя. Соединения изобретения связываются селективно с рецептором СВ 2 и, следовательно, являются пригодными при лечении болезни, опосредованной рецептором СВ 2. В связи с их способностью связываться с рецептором СВ 2 соединения изобретения могут быть пригодны при лечении расстройств, перечисленных далее. Так, соединения формулы (I) могут быть пригодны в качестве аналгетиков. Например, они могут быть пригодны при лечении хронической воспалительной боли (например, боли, связанной с ревматоидным артритом, остеоартритом, ревматоидным спондилитом, подагрическим артритом и ювенильным артритом), включая свойство модифицировать болезнь и сохранять структуру сустава; боли в скелетных мышцах; боли в нижней части спины и шее; растяжений и напряжений; невропатической боли; симпатически поддерживаемой боли; миозита; боли, связанной с раковым заболеванием и фибромиалгией; боли, связанной с мигренью; боли, связанной с гриппом или другими вирусными инфекциями, такими как насморк; ревматической лихорадки; боли, связанной с функциональными расстройствами кишечника, такими как неязвенная диспепсия, экстракардиальная боль в грудной клетке и синдром разраженной толстой кишки; боли, связанной с миокардиальной ишемией; послеоперационной боли; головной боли; зубной боли и дисменореи. Соединения изобретения также могут быть пригодны для изменения болезни или сохранения структуры сустава при рассеянном склерозе, ревматоидном артрите, остеоартрите, ревматоидном спондилите, подагрическом артрите и ювенильном артрите. Соединения изобретения могут быть пригодны, в частности, при лечении невропатической боли. Синдромы невропатической боли могут развиваться после повреждений нейронов, и в результате такая боль может сохраняться на протяжении месяцев или лет даже после заживления начального повреждения. Повреждение нейронов может иметь место в периферических нервах, спинных корешках, спинном мозге или некоторых участках головного мозга. Синдромы невропатической боли традиционно классифицируют по заболеванию или событию, вызвавшему их. Синдромы невропатической боли включают диабетическую невропатию; ишиалгию; неспецифическую боль в нижней части спины; боль при рассеянном склерозе; фибромиалгию; невропатию, связанную с ВИЧ; постгерпетическую невралгию; тригеминальную невралгию и боль в результате физической травмы, ампутации, рака, токсинов или хронического воспаления. Такие состояния трудно лечить, и хотя известны некоторые лекарственные средства с ограниченной эффективностью, полного контроля над болью достигают редко. Симптомы невропатической боли поразительно неоднородны и часто описываются как спонтанная стреляющая и режущая боль или постоянная обжигающая боль. Кроме того, существует боль, связанная с обычно безболезненными ощущениями, такая как "булавки и иголки" (парестезия и дизестезия), повышенная чувствительность зубов (гиперестезия), болезненное ощущение после безвредного раздражения (динамическая, статическая или тепловая аллодиния), повышенная чувствительность к вредным разражителям (тепловая, холодовая, механическая гипералгезия), длительное ощущение боли после устранения раздражения (гиперпатия) или отсутствие или нехватка селективных сенсорных проводящих путей (гипоалгезия). Соединения формулы (I) также могут быть пригодны при лечении лихорадки. Соединения формулы (I) также могут быть пригодны при лечении воспаления, например при лечении кожных болезней (например, солнечных ожогов, ожогов, экземы, дерматита, псориаза); глазных болезней, таких как глаукома, ретинит, ретинопатия, увеит и острое повреждение глазной ткани (например,конъюнктивит); легочных расстройств (например, астмы, бронхита, эмфиземы, аллергического ринита,респираторного дистресс-синдрома, болезни голубятников, легкого "фермера", хронической обструктивной болезни легких (COPD); расстройств желудочно-кишечного тракта (например, афтозной язвы, бо- 11012703 лезни Крона, атопического гастрита, разных форм гастрита, неспецифического язвенного колита, кишечного инфантилизма, регионарного илеита, синдрома раздраженной толстой кишки, воспалительного заболевания пищеварительного тракта, гастроэзофагиального рефлюкса); при пересадке органов; других состояний с воспалительным компонентом, таких как сосудистая болезнь, мигрень, нодозный периартрит, тиреоидит, апластическая анемия, болезнь Ходжкина, склерома, тяжелая псевдопаралитическая миастения, рассеянный склероз, соркоидоз, нефротический синдром, синдром Бехчета, полимиозит, гингивит, миокардиальная ишемия, пирексия, системная красная волчанка, тендинит, бурсит и синдром Шегрена. Соединения формулы (I) также пригодны при лечении различных иммунологических заболеваний,таких как аутоиммунные болезни, болезни иммунологического дефицита или пересадки органов. Соединения формулы (I) также эффективны при повышении латентного периода ВИЧ-инфекции. Соединения формулы (I) также пригодны при лечении болезней аномальной функции тромбоцитов(например, окклюзивных сосудистых болезней). Соединения формулы (I) также пригодны для получения лекарственного средства с диуретическим действием. Соединения формулы (I) также пригодны при лечении импотенции и эриктильной дисфункции. Соединения формулы (I) также пригодны для ослабления гемодинамического побочного действия нестероидных противовоспалительных лекарственных средств (NSAID) и ингибиторов циклооксигеназы-2 (СОХ-2). Соединения формулы (I) также пригодны при лечении нейродегенеративных болезней и нейродегенерации, такой как деменция, в частности дегенеративная деменция (в том числе, сенильная деменция,болезнь Альцгеймера, болезнь Пика, хорея Гентингтона, болезнь Паркинсона и болезнь КрейтцфельдаЯкоба, моторная нейронная деменция), сосудистая деменция (в том числе деменция множественного инфаркта), а также деменция, связанная с повреждениями, занимающими интракраниальное пространство; травм; инфекций и родственных состояний (в том числе ВИЧ-инфекции); деменции при болезни Паркинсона; метаболизма; отравления токсинами; аноксии и при дефиците витаминов; и умеренного ухудшения познавательной способности, связанного со старением, в частности ухудшения памяти, связанного с возрастом. Соединения также могут быть пригодными для лечениия бокового амиотрофного склероза (ALS) и нейровоспаления. Соединения формулы (I) также пригодны при нейропротекции и при лечении нейродегенерации после удара, остановки сердца, легочного шунтирования, травматического повреждения головного мозга,повреждения спинного мозга или подобного повреждения. Соединения формулы (I) также пригодны при лечении тиннита. Соединения формулы (I) также пригодны при лечении психической болезни, например шизофрении, депрессии (этот термин, используемый в данном случае, включает биполярную депрессию, униполярную депрессию, одиночные или рецидивные большие депрессивные эпизоды без или с психотическими признаками, кататоническими признаками, меланхолическими признаками, атипичными признаками, или послеродовое начальное, сезонное аффективное расстройство, дистимические расстройства с ранним или поздним началом и без или с атипичными признаками, невротическую депрессию и социальные фобии, депрессию, сопровождающую деменцию, например деменцию типа по Альцгеймеру, шизоаффективное расстройство или депрессивного типа, и депрессивные расстройства, являющиеся результатом общего медицинского состояния, в том числе, но не ограничиваясь этим, инфаркта миокарда, диабета, выкидыша или аборта и т.д.), тревожных расстройств (в том числе генерализованного общего расстройства и социального тревожного расстройства), панической атаки, агорафобии, социальной фобии,обсессивно-компульсивного расстройства и посттравматического стресса, расстройства памяти, в том числе деменции, амнезийных расстройств и ухудшения памяти, связанного с возрастом, расстройств пищевого поведения, в том числе нервно-психической анорексии и нервно-психической булимии, половой дисфункции, расстройств сна (в том числе нарушений циркадного ритма, диссомнии, инсомнии, апноэ во сне и нарколепсии), состояния отвыкания от злоупотребления лекарственными средствами, такими как кокаин, этанол, никотин, бензодиазепины, алкоголь, кофеин, фенилциклидин (фенилциклидиноподобные соединения), опиаты (например, героин, морфин), амфетамин или родственные амфетамину лекарственные средства (например, декстроамфетамин, метиламфетамин) или их сочетания. Соединения формулы (I) также пригодны при предупреждении или ослаблении зависимости от или при предупреждении или ослаблении толерантности или возвратной толерантности к средству, вызывающему зависимость. Примерами средств, вызывающих зависимость, являются опиаты (например,морфин), ЦНС-депрессанты (например, этанол), психостимуляторы (например, кокаин) и никотин. Соединения формулы (I) также пригодны при лечении почечной дисфункции (нефрита, в частности,мезангиального пролиферативного гломерулонефрита, нефритического синдрома), дисфункции печени(гепатита, цирроза), гастроинтестинальной дисфункции (диареи) и рака толстой кишки. Следует иметь в виду, что ссылки на лечение включают как лечение установленных симптомов, так и профилактическое лечение, если явно не указано иное. Согласно другому аспекту изобретение относится к соединению формулы (I) или его фармацевти- 12012703 чески приемлемому производному для применения в медицине или ветеринарии. Согласно другому аспекту изобретение относится к соединению формулы (I) или его фармацевтически приемлемому производному для применения при лечении состояния, которое опосредуется активностью каннабиноидных рецепторов 2. Согласно другому аспекту изобретение относится к способу лечения субъекта - человека или животного, страдающего от состояния, которое опосредуется активностью каннабиноидных рецепторов 2,включающему введение указанному субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемого производного. Согласно другому аспекту изобретение относится к способу лечения субъекта - человека или животного, страдающего от иммунного расстройства, воспалительного расстройства, боли, ревматоидного артрита, рассеянного склероза, остеоартрита или остепороза, включающему введение указанному субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемого производного. Предпочтительно боль выбирают из воспалительной боли, висцеральной боли, боли при раковом заболевании, боли в нижней части спины, боли в скелетных мышцах, послеоперационной боли, острой боли и мигрени. Предпочтительнее воспалительная боль является болью, связанной с ревматоидным артритом или остеоартритом. Согласно еще одному аспекту изобретение относится к применению соединения формулы (I) или его фармацевтически приемлемого производного для получения лечебного средства для лечения или предупреждения состояния, такого как иммунное расстройство, воспалительное расстройство, боль, ревматоидный артрит, рассеянный склероз, остеоартрит или остеопороз. Предпочтительно боль выбирают из воспалительной боли, висцеральной боли, боли при раковом заболевании, невропатической боли, боли в нижней части спины, боли в скелетных мышцах, послеоперационной боли, острой боли и мигрени. Предпочтительнее воспалительная боль является болью, связанной с ревматоидным артритом или остеоартритом. Для того чтобы применять соединение формулы (I) или его фармацевтически приемлемое производное для лечения людей и других млекопитающих, его обычно вводят в состав, который получают согласно обычной фармацевтической практике как фармацевтическую композицию. Поэтому в другом аспекте изобретение относится к фармацевтической композиции, содержащей соединение формулы (I) или его фармацевтически приемлемое производное, адаптированные для применения в медицине или ветеринарии. Используемый в данном описании термин "модулятор" обозначает как антагониста, так и частичного или полного агониста и инверсного агониста. В одном воплощении модуляторы настоящего изобретения являются агонистами. Используемый в данном описании термин "лечение" или "лечащий" включает лечение установленных расстройств, а также включает их профилактику. В данном описании термин "профилактика" используется для обозначения предупреждения симптомов у уже пораженного субъекта или предупреждения рецидива симптомов у пораженного субъекта и не ограничивается полным предупреждением поражения. Соединения формулы (I) и их фармацевтически приемлемые производные для лечения указанных заболеваний можно вводить стандартными способами, например перорально, парентерально, подъязычно, дермально, интраназально, трансдермально, ректально, ингаляцией или буккальным введением. Соединения формулы (I) и их фармацевтически приемлемые производные, активные при пероральном введении, можно вводить в композиции в виде сиропов, таблеток, капсул и пастилок. Композиция в виде сиропа, как правило, будет состоять из суспензии или раствора соединения или его соли в жидком носителе, например этаноле, арахисовом масле, глицерине или воде, с добавлением корригента или красителя. Когда композиция имеет форму таблетки, можно использовать любой фармацевтически приемлемый носитель, обычно используемый для получения твердых составов. Примеры таких носителей включают стеарат магния, каолин, тальк, желатин, аравийскую камедь, стеариновую кислоту, крахмал, лактозу и сахарозу. Когда композиция имеет форму капсулы, подходящим является любое инкапсулирование, например, с использованием вышеуказанных носителей в капсуле с твердой желатиновой оболочкой. Когда композиция имеет форму капсулы с мягкой желатиновой оболочкой,можно рассматривать любой фармацевтический носитель, обычно используемый для получения дисперсий или суспензий, например водные смолы, целлюлозы, силикаты или масла, и вносить их в капсулу с мягкой желатиновой оболочкой. Типичные парентеральные композиции состоят из раствора или суспензии соединения или его производного в стерильном водном или неводном носителе, необязательно содержащем парентерально приемлемое масло, например полиэтиленгликоль, поливинилпирролидон, лецитин, арахисовое масло или сезамовое масло. Типичные композиции для ингаляции имеют форму раствора, суспензии или эмульсии, которые можно вводить в виде сухого порошка или в форме аэрозоля с использованием обычного пропеллента,такого как дихлордифторметан или трихлорфторметан.- 13012703 Типичная композиция суппозитория содержит соединение формулы (I) или его фармацевтически приемлемое производное, активное при введении указанным способом, в смеси со связующим веществом и/или смазывающим веществом, например полигликолями, желатином, маслом какао или другими низкоплавкими растительными восками, или жирами, или их синтетическими аналогами. Типичные дермальные и трансдермальные композиции содержат обычный водный или неводный наполнитель, как, например, крем, мазь, лосьон или паста, или имеют форму содержащего лекарственное средство пластыря, пэтча или пленки. Предпочтительно композиция находится в стандартной лекарственной форме, например таблетки,капсулы или установленной дозы аэрозоля, так что пациент может ввести однократную дозу. Каждая стандартная лекарственная форма для перорального введения содержит, соответственно, от 0,01 до 500 мг/кг, например от 0,1 мг до 500 мг/кг, и предпочтительно от 0,01 до 100 мг/кг, например от 1 до 100 мг/кг, и каждая стандартная лекарственная форма для парентерального введения содержит, соответственно, от 0,1 до 100 мг/кг соединения формулы (I) или его фармацевтически приемлемого производного в расчете на свободную кислоту. Каждая стандартная лекарственная форма для интраназального введения содержит, соответственно, 1-400 мг и предпочтительно 10-200 мг на человека. Местная композиция содержит, соответственно, 0,01-5,0% соединения формулы (I). Ежесуточная схема приема лекарственного средства в случае перорального введения составляет,соответственно, примерно от 0,01 до 40 мг/кг соединения формулы (I) или его фармацевтически приемлемого производного в расчете на свободную кислоту. Ежесуточная схема приема лекарственного средства в случае парентерального введения составляет, соответственно, примерно от 0,001 до 40 мг/кг соединения формулы (I) или его фармацевтически приемлемого производного в расчете на свободную кислоту. Ежесуточная схема приема лекарственного средства в случае интраназального введения и оральной ингаляции составляет, соответственно, от примерно 10 мг до примерно 550 мг на человека. Активный ингредиент можно вводить от 1 до 6 раз в сутки - достаточно для проявления нужной активности. Может оказаться выгодным получать соединения настоящего изобретения в виде наночастиц. Так можно улучшить пероральную биологическую доступность соединений. Для целей настоящего изобретения "наночастицы" определяются как твердые частицы, 50% которых имеют размер менее 1 мкм,предпочтительнее менее примерно 0,75 мкм. Размер твердых частиц соединения (I) можно определить методом дифракции лучей лазера. Подходящим прибором для определения размера частиц методом дифракции лучей лазера является лазерный анализатор размера частиц Lecotrac с использованием оптической скамьи HELOS, снабженной диспергирующим устройством QUIXEL. Известны многие способы синтеза твердых частиц в форме наночастиц. Типично такие способы включают процесс перемалывания, предпочтительно мокрого перемалывания, в присутствии вещества,модифицирующего поверхность, которое ингибирует агрегацию и/или рост кристаллов только что созданных наночастиц. С другой стороны, такие способы могут включать процесс осаждения, предпочтительно процесс осаждения в водной среде из раствора лекарственного средства в неводном растворителе. Характерные способы получения твердых частиц в форме наночастиц описаны в патентах и публикациях, перечисленных ниже. Патент США 4826689, ViolantoFischer; патент США 5145684, Liversidge et al.; патент США 5298262, NaRajagopalan; патент США 5302401, Liversidge et al.; патент США 5336507, Naal.; патент США 5560931, Eickhoff et al.; патент США 5560932, Bagchi et al.; патент США 5565188, Wong et al.; патент США 5571536, Eickhoff et al.; патент США 5573783, DesienoStetsko; патент США 5580579, Ruddy et al.; патент США 5585108, Ruddy et al.; патент США 5587143,Wong; патент США 5591456, Freinson et al.; патент США 5622938, Wong; патент США 5662883,Bagchi et al.; патент США 5665331, Bagchi et al.; патент США 5718919, Ruddy et al.; патент США 5747001, Wiedmann et al.; WO 93/25190, 96/24336, 97/14407, 98/35666, 99/65469,00/18374, 00/27369, 00/30615 и 01/41760. Такие способы можно легко приспособить для получения соединения (I) в форме наночастиц. Такие способы образуют еще один аспект изобретения. В способе настоящего изобретения, для того чтобы получить форму наночистиц соединения, используют предпочтительно стадию мокрого перемалывания, осуществляемую в мельнице, такой как дисперсионная мельница. Настоящее изобретение можно осуществить с использованием обычного метода мокрого перемалывания, такого как метод, описанный в Lachmann et al., The Theory and Practice ofIndustrial Pharmacy, Chapter 2, "Milling", p/45 (1986). В дополнительное уточнение в WO 02/00196 (SmithKline Beecham plc) для применения при получении твердых частиц лекарственного вещества в форме наночастиц описывается процедура мокрого пе- 14012703 ремалывания с использованием мельницы, в которой, по меньшей мере, некоторые поверхности изготовлены из нейлона (полиамида), содержащего одну или несколько внутренних смазок. В другом аспекте настоящее изобретение относится к способу получения соединений в форме наночастиц, включающему мокрое перемалывание суспензии соединения в мельнице, имеющей по меньшей мере одну камеру и средства для перемешивания, причем указанная(ые) камера(ы) и/или указанные средства для перемешивания содержат содержащий смазку нейлон, описанный в WO 02/00196. Суспензия соединения изобретения для применения при мокром перемалывании типично представляет собой жидкую суспензию грубо измельченного соединения в жидкой среде. Термин "суспензия" означает, что соединение, по существу, является нерастворимым в жидкой среде. Представленная жидкая среда включает водную среду. Используя способ настоящего изобретения, средний размер частиц соединения по изобретению, по существу, составляет до 1 мм в диаметре. При этом выгодно устраняется необходимость предварительно обрабатывать соединение. В другом аспекте изобретения водная среда, подвергаемая обработке в мельнице, содержит соединение (I), присутствующее в количестве от примерно 1 до примерно 40 мас./мас.%, предпочтительно от примерно 10 до примерно 30 мас./мас.%, предпочтительнее примерно 20 мас./мас.%. Водная среда также может содержать один или несколько фармацевтически приемлемых водорастворимых носителей, подходящих для стерической стабилизации и последующей переработки для фармацевтической композиции соединения (I) после перемалывания, например распылительной сушки. Фармацевтически приемлемыми эксципиентами, наиболее подходящими для стерической стабилизации и распылительной сушки, являются поверхностно-активные вещества, такие как полоксамеры,лаурилсульфат натрия и полисорбаты, и т.д.; стабилизаторы, такие как целлюлозы, например гидроксипропилметилцеллюлоза; и носители, такие как углеводы, например маннит. В другом аспекте изобретения водная среда, подвергаемая обработке в мельнице, также может содержать гидроксипропилметилцеллюлозу (НРМС), присутствующую в количестве от примерно 0,1 до примерно 10 мас./мас.%. Способ настоящего изобретения может включать последующую стадию сушки соединения изобретения с образованием порошка. Соответственно, в другом аспекте настоящее изобретение относится к способу получения фармацевтической композиции, содержащей соединение настоящего изобретения, включающему получение соединения формулы (I) в форме наночастиц, необязательно с последующей сушкой с получением порошка. Другим аспектом изобретения является фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемое производное, в которой соединение формулы (I) или его фармацевтически приемлемое производное находятся в виде твердых частиц в форме наночастиц в смеси с фармацевтически приемлемыми носителями или эксципиентами."Сушкой" называют удаление воды или другого жидкого носителя, используемого в способе для сохранения соединения формулы (I) в жидкой суспензии или растворе. Такая стадия сушки может представлять собой любой способ сушки, известный в технике, в том числе сушку вымораживанием, грануляционную сушку или распылительную сушку. Из указанных способов особенно предпочтительна распылительная сушка. Все такие методы хорошо известны в технике. Распылительную сушку/грануляцию в псевдоожиженном слое размолотых композиций наиболее удобно осуществлять с использованием распылительной сушилки, такой как Mobile Minor Spray Dryer [Niro, Denmark], или сушилки с псевдоожиженным слоем, такие как изготовляет Glatt, Германия. В другом аспекте изобретение относится к фармацевтической композиции, как она определена ранее, в форме сухого порошка, который можно получить мокрым перемалыванием твердых частиц соединения формулы (I) с последующей распылительной сушкой полученной суспензии. Предпочтительно фармацевтическая композиция, как она определена ранее, содержит НРМС в количестве менее примерно 15 мас./мас.%, предпочтительно в количестве в интервале от 0,1 до 10 мас./мас.%. Соединения для рецепторов СВ 2 для применения в данном изобретении можно использовать в сочетании с другими лечебными средствами, например ингибиторами СОХ-2, такими как целекоксиб, деракоксиб, рофекоксиб, валдекоксиб, парекоксиб или СОХ-189; ингибиторами 5-липоксигеназы; NSAID,такими как аспирин, диклофенак, индометацин, набуметон или ибупрофен; антагонистами лейкотриеновых рецепторов; DMARD, такими как метотрексат; агонистами аденозинового рецептора А 1; блокираторами натриевых каналов, такими как ламотригин; модуляторами рецепторов NMDA, такими как антагонисты глициновых рецепторов; габапентином и родственными соединениями; трициклическими антидепрессантами, такими как амитриптилин; нейронстабилизирующими противоэлиптическими лекарственными средствами; ингибиторами моноаминергического поглощения, такими как венлафаксин; опиатными аналгетиками; местными анестетиками; агонистами 5HT1, такими как триптаны, например суматриптан, наратриптан, золмитриптан, элетриптан, фроватриптан, алмотриптан или ризатриптан; лигандами рецептора EP1, лигандами рецептора ЕР 4; лигандами рецептора ЕР 2; лигандами рецептора ЕР 3; антагонистами ЕР 4; антагонистами ЕР 2 и антагонистами ЕР 3; лигандами брадикининовых рецепторов и лигандом- 15012703 ваниллоидного рецептора; лекарственными средствами против ревматоидного артрита, например лекарственными средствами против TNF, например энбрелом, ремикадом, лекарственными средствами противIL-1 или DMARD, например лефлунамидом. Когда соединения используют в сочетании с другими лечебными средствами, соединения можно вводить или последовательно, или одновременно любым удобным способом. Другие ингибиторы СОХ-2 описаны в патентах США 5474995, 5633272, 5466823, 6310099 и 6291523, и в WO 96/25405, 97/38986, 98/03484, 97/14691, 99/12930, 00/26216, 00/52008, 00/38311,01/58881 и 02/18374. Соединение настоящего изобретения можно вводить в сочетании с другими активными веществами, такими как антагонисты 5 НТ 3, антагонисты NK-1, агонисты серотонина, селективные ингибиторы повторного поглощения серотонина (SSRI), ингибиторы повторного поглощения норадреналина (SNRI),трициклические антидепрессанты и/или допаминергические антидепрессанты. Подходящие антагонисты 5 НТ 3, которые можно использовать в сочетании с соединением изобретения, включают, например, онданстерон, гранистерон, метоклопрамид. Подходящие агонисты серотонина, которые можно использовать в сочетании с соединением изобретения, включают суматриптан, рауволсцин, иохимбин, метоклопрамид. Подходящие SSRI, которые можно использовать в сочетании с соединением изобретения, включают флуоксетин, циталопрам, фемоксетин, флувоксамин, пароксетин, индалпин, сертралин, цимелдин. Подходящие SNRI, которые можно использовать в сочетании с соединением изобретения, включают венлафаксин и ребоксетин. Подходящие трициклические антидепрессанты, которые можно использовать в сочетании с соединением изобретения, включают имипрамин, амитриптилин, хломипрамин и нортриптилин. Подходящие допаминергические антидепрессанты, которые можно использовать в сочетании с соединением изобретения, включают бупропион и аминептин. Следует иметь в виду, что соединения любых вышеуказанных сочетаний и композиций можно вводить одновременно (или в единой, или в разных фармацевтических композициях), раздельно или последовательно. Таким образом, в еще одном аспекте изобретение относится к сочетанию, включающему соединение формулы (I) или его фармацевтически приемлемое производное, наряду с другим лечебным средством или средствами. Сочетания, указанные выше, для применения можно удобно представить в форме фармацевтической композиции, и, таким образом, фармацевтические композиции, содержащие сочетание, указанное выше, вместе с фармацевтически приемлемым носителем или эксципиентом составляют дополнительный аспект изобретения. Отдельные компоненты таких сочетаний можно вводить или последовательно,или одновременно в отдельных или комбинированных фармацевтических композициях. Когда соединение формулы (I) или его фармацевтически приемлемое производное используют в сочетании с другим лечебным средством, активным против того же болезненного состояния, доза каждого соединения может отличаться от дозы, когда соединение вводят одно. Соответствующие дозы могут быть легко установлены специалистами в данной области техники. Определение активности агониста каннабиноидного рецептора СВ 1. Активность агонистов каннабиноидного рецептора СВ 1 соединений формулы (I) определяют согласно экспериментальному методу, описанному далее. Экспериментальный метод. Клетки дрожжей (Saccharomyces cerevisiae), экспрессирующие человеческий каннабиноидный рецептор СВ 1, получают путем интеграции экспрессирующих кассет в хромосомный локус ura3 штамма дрожжей MMY23. Такая кассета состоит из последовательности ДНК, кодирующей человеческий рецептор СВ 1, фланкированной дрожжевым промотором GPD по 5'-концу СВ 1 и транскрипционной концевой последовательностью дрожжей по 3'-концу СВ 1. MMY23 экспрессирует альфа-субъединицу химерногоG-белка дрожжей/млекопитающего, в которой 5 С-концевых аминокислот Gpa1 заменены 5 С-концевыми аминокислотами человеческого Gi3 (как описано в Brown et al. (2000), Yest, 16:11-22). Клетки выращивают при 30 С в жидких синтетических полных (SC) дрожжевых средах (Guthrie and Fink(1991), Methods in Enzymology, Vol. 194), лишенных урацила, триптофана, аденина и лейцина, до поздней логарифмической фазы (приблизительно 6 OD600/мл). Агонисты получают в виде 10 мМ исходных растворов в ДМСО. Величины ЕС 50 (концентрация,необходимая для получения 50% максимальной реакции) оценивают с использованием 3-5-кратных разведений (BiomekFX, Beckman) в ДМСО. Растворы агонистов в ДМСО (1% от конечного объема смеси для анализа) переносят в темные с прозрачным дном титрационные микропланшеты от NUNC (96- или 384-луночные). Клетки суспендируют при плотности 0,2 OD600/мл в SC средах, лишенных гистидина,урацила, триптофана, аденина и лейцина, и с добавлением 10 мМ 3-аминотриазола, 0,1 М фосфата натрия, рН 7,0, и 20 мкМ флуоресцеина диD-глюкопиранозида (FDGlu). Полученную смесь (50 мкл на лунку для 384-луночных планшетов, 200 мкл на лунку для 96-луночных планшетов) добавляют к агони- 16012703 сту в аналитических планшетах (Multidrop 384, Labsystems). После инкубации при 30 С в течение 24 ч определяют с использованием аппарата для считывания титрационных микропланшетов Spectrofluor(Tecan; длина волны возбуждения 485 нм; длина волны испускания 535 нм) флуоресценцию, являющуюся результатом разложения флуоресцентного красителя FDGlu до экзоглюканазы - эндогенного дрожжевого фермента, продуцируемого во время роста клеток, стимулированного агонистом. Флуоресценцию откладывают на графике против концентрации соединения, и итеративно вычерчивают кривую с использованием соответствия четырех параметров для получения величины влияния концентрации. Эффективность (Emax) вычисляют из уравнения где Мах [соединение X] и Min [соединение X] являются максимумом и минимумом, соответственно, найденными из кривой влияния концентрации для соединения X, и Max[HU210] и Min[HU210] являются максимумом и минимумом,соответственно, найденными из кривой влияния концентрации для (6aR,10aR)-3-(1,1'-диметилгептил)6 а,7,10,10 а-тетрагидро-1-гидрокси-6,6-диметил-6H-дибензо[b,d]пиран-9-метанола (HU210, доступен от Tocris). Величины равноэффективного молярного отношения (EMR) вычисляют из уравнения где ЕС 50[соединение X] представляет собой ЕС 50 соединения X, и ЕС 50[HU210] представляет собой ЕС 50HU210. Соединения примеров, испытанные согласно такому методу, имеют величины ЕС 50 2000 нМ и/или величины эффективности 50% для клонированного каннабиноидного рецептора СВ 1. Определение активности агониста каннабиноидного рецептора СВ 2. Активность агонистов каннабиноидного рецептора СВ 2 соединений формулы (I) определяют согласно экспериментальному методу, описанному далее. Экспериментальный метод. Клетки дрожжей (Saccharomyces cerevisaiae), экспрессирующие человеческий каннабиноидный рецептор СВ 2, получают путем интеграции экспрессирующих кассет в хромосомный локус ura3 штамма дрожжей MMY23. Такая кассета состоит из последовательности ДНК, кодирующей человеческий рецептор СВ 2, фланкированной дрожжевым промотором GPD по 5'-концу СВ 2 и транскрипционной концевой последовательностью дрожжей по 3'-концу СВ 2. MMY23 экспрессирует альфа-субъединицу химерногоG-белка дрожжей/млекопитающего, в которой 5 С-концевых аминокислот Gpa1 заменены 5 С-концевыми аминокислотами человеческого Gi3 (как описано в Brown et al. (2000), Yest, 16:11-22). Клетки выращивают при 30 С в жидких синтетических полных (SC) дрожжевых средах (Guthrie and Fink(1991), Methods in Enzymology, Vol. 194), лишенных урацила, триптофана, аденина и лейцина, до поздней логарифмической фазы (приблизительно 6 OD600/мл). Агонисты получают в виде 10 мМ исходных растворов в ДМСО. Величины ЕС 50 (концентрация,необходимая для получения 50% максимальной реакции) оценивают с использованием 3-5-кратных разведений (BiomekFX, Beckman) в ДМСО. Растворы агонистов в ДМСО (1% от конечного объема смеси для анализа) переносят в темные с прозрачным дном титрационные микропланшеты от NUNC (96- или 384-луночные). Клетки суспендируют при плотности 0,2 OD600/мл в SC средах, лишенных гистидина,урацила, триптофана, аденина и лейцина, и с добавлением 10 мМ 3-аминотриазола, 0,1 М фосфата натрия, рН 7,0 и 20 мкМ флуоресцеина диD-глюкопиранозида (FDGlu). Полученную смесь (50 мкл на лунку для 384-луночных планшетов, 200 мкл на лунку для 96-луночных планшетов) добавляют к агонисту в аналитических планшетах (Multidrop 384, Labsystems). После инкубации при 30 С в течение 24 ч определяют, с использованием аппарата для считывания титрационных микропланшетов Spectrofluor(Tecan; длина волны возбуждения 485 нм; длина волны испускания 535 нм), флуоресценцию, являющуюся результатом разложения флуоресцентного красителя FDGlu до экзоглюканазы - эндогенного дрожжевого фермента, продуцируемого во время роста клеток, стимулированного агонистом. Флуоресценцию откладывают на графике против концентрации соединения, и итеративно вычерчивают кривую с использованием соответствия четырех параметров для получения величины влияния концентрации. Эффективность (Emax) вычисляют из уравнения где Мах [соединение X] и Min [соединение X] являются максимумом и минимумом, соответственно, найденными из кривой влияния концентрации для соединения X, и Мах[HU210] и Min[HU210] являются максимумом и минимумом,соответственно, найденными из кривой влияния концентрации для (6aR,10aR)-3-(1,1'-диметилгептил)6 а,7,10,10 а-тетрагидро-1-гидрокси-6,6-диметил-6H-дибензо[b,d]пиран-9-метанола (HU210, доступен от Tocris). Величины равноэффективного молярного отношения (EMR) вычисляют из уравнения где ЕС 50[соединение X] представляет собой ЕС 50 соединения X, и EC50[HU210] представляет собой ЕС 50HU210. Соединения примеров 1-23, 31-56, 68 и 163-256, испытанные согласно такому методу, имеют величины ЕС 50 20-300 нМ и величины эффективности 50% для клонированного каннабиноидного рецептора СВ 2.- 17012703 Соединения примеров 24-30, 73-113 и 257-259, испытанные согласно такому методу, имеют величины ЕС 50 300-1000 нМ и величины эффективности 50% для клонированного каннабиноидного рецептора СВ 2. Соединения примеров 57-67, 69-72, 114-162 и 260-265, испытанные согласно такому методу, имеют величины ЕС 50 1000 нМ и величины эффективности 50% для клонированного каннабиноидного рецептора СВ 2. Приведенные далее примеры являются пояснительными, но не ограничивающими воплощения настоящего изобретения. Все экспериментальные результаты ЯМР регистрируют при 400 МГц. Условия, приборы и программное обеспечение, используемые для масс-направленной автоматической очистки. Приборы. Градиентный насос Waters 600, система управления для образцов Waters 2700, система управления для реагентов Waters, масс-спектрометр Micromass ZMD, коллектор фракций Gilson 202, коллектор отходов Gilson Aspec. Программное обеспечение.Micromass Masslynx, версия 3,5. Колонка. Используемая колонка типично является колонкой Supelco ABZ+ с размерами внутреннего диаметра 10 мм и длиной 100 мм. Размер частиц неподвижной фазы 5 мкм. Растворители.B. Органический растворитель = MeCN:вода (95:5) + 0,05% муравьиной кислоты. Кондиционный растворитель = МеОН:вода (80:20) + 50 ммоль ацетата аммония. Растворитель для промывания иглы = МеОН:вода:ДМСО (80:10:10). Методы. Используют пять методов в зависимости от аналитического времени удерживания интересующего соединения. Во всех методах скорость потока 20 мл/мин и время прогона 15 мин, в которое входят 10-минутный градиент и последующие 5 мин на промывку колонки и стадию повторного уравновешивания. Метод 1. MDP 1,5-2,2 = 0-30% В Метод 2. MDP 2,0-2,8 = 5-30% В Метод 3. MDP 2,5-3,0 = 15-55% В Метод 4. MDP 2,8-4,0 = 30-80% В Метод 5. MDP 3,8-5,5 = 50-90% В Ссылочный пример 1. Бензиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты(а) К раствору бензил 2-хлор-4-трифторметилпиримидин-5-карбоксилата (0,50 г, обр. от Maybridge) в 1,4-диоксане (5 мл) добавляют 3-хлоранилин (0,85 мл) и раствор перемешивают при комнатной температуре в течение 15 ч. 1,4-Диоксан удаляют при пониженном давлении и добавляют этилацетат (15 мл). Раствор последовательно промывают 2 N соляной кислотой (10 мл) и водой (310 мл), сушат (MgSO4),упаривают, остаток обрабатывают гексаном, и получают бензил-2-(3-хлорфениламино)-4 трифторметилпиримидин-5-карбоксилат (524 мг). ЯМР (ДМСО-d6)5,35 (2 Н, с), 7,14 (1 Н, д), 7,35-7,45 (6 Н, м), 7,68 (1 Н, м), 7,98 (1 Н, с), 9,13 (1 Н, с),10,95 (1 Н, с). ЖХ/МС, t = 3,70 мин, [МН+] 408 и 410.(b) К раствору бензил 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоксилата (0,50 г) в этаноле (15 мл) добавляют раствор гидроксида калия (205 мг) в этаноле (10 мл), и раствор перемешивают при кипячении с обратным холодильником в течение 15 ч. Этанол удаляют при пониженном давлении и добавляют воду (15 мл). Раствор промывают эфиром и добавляют концентрированную соляную кислоту для доведения до кислотности с рН 1. Выпавшее в осадок твердое вещество отфильтровывают, промывают водой и сушат в вакууме при 50 С, и получают 2-(3-хлорфениламино)-4-трифторметилпиримидин 5-карбоновую кислоту (366 мг). ЯМР (ДМСО-d6)7,49 (1 Н, д), 7,71 (1 Н, т), 7,98 (1 Н, д), 8,33 (1 Н, с), 9,42 (1 Н, с), 11,15 (1 Н, с), 14,0(15 мкл), гидрат 1-гидроксибензотриазола (23 мг) и гидрохлорид 1-(3-диметиламинопропил)-3 этилкарбодиимида (25 мг). Раствор перемешивают в течение 3 ч и оставляют на ночь. Диметилформамид удаляют при пониженном давлении и добавляют этилацетат (5 мл). Раствор последовательно промывают 5% раствором бикарбоната натрия (2,5 мл), водой (2,5 мл), 5% раствором лимонной кислоты (2,5 мл) и рассолом (22,5 мл), сушат (MgSO4), упаривают и получают названное в заголовке соединение (45 мг). ЯМР (ДМСО-d6)4,47 (2 Н, д), 7,10 (1 Н, д), 7,25 (1 Н, м), 7,36 (5 Н, м), 7,69 (1 Н, д), 7,98 (1 Н, с),8,89 (1 Н, с), 9,12 (1 Н, т), 10,65 (1 Н, с). ЖХ/МС, t = 3,23 мин, [МН+] 407 и 409. Способом, подобным способу ссылочного примера 1(c), из 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и пиперидина (13 мкл) получают названное в заголовке соединение (38 мг). ЯМР (ДМСО-d6)1,3-1,65 (6 Н, м), 3,28 (2 Н, с), 3,6 (2 Н, ушир.с), 7,10 (1 Н, д), 7,37 (1 Н, т), 7,68 (1 Н,д), 7,96 (1 Н, с), 8,78 (1 Н, с), 10,55 (1 Н, с). ЖХ/МС, t = 3,63 мин, [МН+] 385 и 387. Пример 2. Циклопентилметиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(3-хлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (100 мг) и гидрохлорида циклопентилметиламина Способом, подобным способу ссылочного примера 1(c), из 2-(3-хлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (35 мг) и морфолина (11,5 мкл) получают названное в заголовке соединение (43 мг). ЯМР (ДМСО-d6)3,4-3,75 (8 Н, м), 7,10 (1 Н, д), 7,38 (1 Н, т), 7,68 (1 Н, д), 7,98 (1 Н, с), 8,80 (1 Н, с),10,60 (1 Н, с). ЖХ/МС, t = 3,29 мин, [МН+] 387 и 389. Способом, подобным способу ссылочного примера 1(c), из 2-(3-хлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (35 мг) и циклогексанметиламина (15 мг) получают названное в заголовке соединение (27 мг). ЯМР (ДМСО-d6)0,85-1,0 (2 Н, м), 1,1-1,3 (3H, м), 1,5 (1 Н, м), 1,55-1,8 (5 Н, м), 3,06 (2 Н, т), 7,09 Способом, подобным способу ссылочного примера 1(c), из 2-фениламино-4-трифторметилпиримидин-5-карбоновой кислоты (32 мг) и циклогексанметиламина (15 мг) получают названное в заголовке соединение (33 мг). ЯМР (ДМСО-d6)0,85-1,0 (2 Н, м), 1,05-1,3 (3H, м), 1,5 (1 Н, м), 1,55-1,8 (5 Н, м), 3,08 (2 Н, т), 7,06 Способом, подобным способу ссылочного примера 1(c), из 2-(2,3-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (24 мг) и морфолина (10 мкл) получают названное в заголовке соединение (17 мг). ЯМР (ДМСО-d6)3,4-3,8 (8 Н, м), 7,40 (1 Н, т), 7,54 (1 Н, д), 7,60 (1 Н, д), 8,78 (1 Н, с), 10,15 (1 Н, с). ЖХ/МС, t = 3,32 мин, [МН+] 421 и 423. Пример 7. 1-[2-(2,4-Дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон Способом, подобным способу ссылочного примера 1(c), из 2-(2,4-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (30 мг) и морфолина (10 мкл) получают названное в заголовке соединение (31 мг). ЯМР (ДМСО-d6)3,3-3,8 (8 Н, м), 7,52 (1 Н, дд), 7,68 (1 Н, д), 7,76 (1 Н, д), 8,73 (1 Н, с), 10,05 (1 Н, с). ЖХ/МС, t = 3,37 мин, [МН+] 421 и 423. Пример 8. 1-[2-(3,4-Дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон Способом, подобным способу ссылочного примера 1(с), из 2-(3,4-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (30 мг) и морфолина (10 мкл) получают названное в заголовке соединение (36 мг). ЯМР (ДМСО-d6)3,35-3,8 (8 Н, м), 7,67 (1 Н, д), 7,76 (1 Н, дд), 8,22 (1 Н, с), 8,90 (1 Н, с), 10,80 (1 Н, с). ЖХ/МС, t = 3,45 мин, [МН+] 421 и 423. Способом, подобным способу ссылочного примера 1(c), из 2-(2,5-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (35 мг) и морфолина (14,5 мкл) получают названное в заголовке соединение (27 мг). ЯМР (ДМСО-d6)3,4-3,75 (8 Н, м), 7,32 (1 Н, дд), 7,66 (1 Н, д), 7,78 (1 Н, д), 8,71 (1 Н, с), 10,05 (1 Н, с). ЖХ/МС, t = 3,31 мин, [МН+] 421 и 423. Пример 10. 1-[2-(3-Фторфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон Способом, подобным способу ссылочного примера 1(c), из 2-(3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и морфолина (12 мкл) получают названное в заголовке соединение (31 мг). ЯМР (ДМСО-d6)3,4-3,8 (8 Н, м), 6,85 (1 Н, тд), 7,37 (1 Н, кв.), 7,52 (1 Н, д), 7,77 (1 Н, дт), 8,80 (1 Н, с),10,65 (1 Н, с). ЖХ/МС, t = 3,06 мин, [МН+] 371. Пример 11. 1-[2-(3-Бромфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон Способом, подобным способу ссылочного примера 1(с), из 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и морфолина (10 мкл) получают названное в заголовке соединение (31 мг). ЯМР (ДМСО-d6)3,4-3,8 (8 Н, м), 7,22 (1 Н, д), 7,30 (1 Н, т), 7,71 (1 Н, д), 8,11 (1 Н, с), 8,81 (1 Н, с),10,60 (1 Н, с). ЖХ/МС, t = 3,25 мин, [МН+] 431 и 433. Пример 12. 1-[2-(3-Бромфениламино)-4-трифторметилпиримидин-5-ил]-1-пиперидин-4-илметанон Способом, подобным способу ссылочного примера 1(c), из 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и пиперидина (12 мкл) получают названное в заголовке соединение (31 мг). ЯМР (ДМСО-d6)1,3-1,7 (6 Н, м), 3,26 (2 Н, с), 3,60 (2 Н, ушир.с), 7,21 (1 Н, д), 7,30 (1 Н, т), 7,70 (1 Н,д), 8,11 (1 Н, с), 8,78 (1 Н, с), 10,55 (1 Н, с). ЖХ/МС, t = 3,57 мин, [МН+] 429 и 431. Пример 13. 1-[2-(3,5-Дихлорфениламино)-4-трифторметилпиримидин-5-ил]-1-морфолин-4-илметанон Способом, подобным способу ссылочного примера 1(c), из 2-(3,5-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (35 мг) и морфолина (14,5 мкл) получают названное в заголовке соединение (42 мг). ЯМР (ДМСО-d6)3,4-3,75 (8 Н, м), 7,35 (1 Н, с), 7,89 (2 Н, с), 8,87 (1 Н, с), 10,80 (1 Н, с). ЖХ/МС, t = 3,52 мин, [МН+] 421 и 423. Способом, подобным способу ссылочного примера 1(c), из 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и циклопентиламина (13 мкл) получают названное в заголовке соединение (34 мг). ЯМР (ДМСО-d6)1,5 (4 Н, м), 1,65 (2 Н, м), 1,85 (2 Н, м), 4,15 (1 Н, м), 7,09 (1 Н, д), 7,36 (1 Н, т), 7,67 Способом, подобным способу ссылочного примера 1(c), из 2-(2,3-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (35 мг) и циклогексанметиламина (16 мкл) получают названное в заголовке соединение (30 мг). ЯМР (ДМСО-d6)0,85-1,0 (2 Н, м), 1,1-1,3 (3H, м), 1,45 (1 Н, м), 1,55-1,8 (5 Н, м), 3,05 (2 Н, т), 7,40 Способом, подобным способу ссылочного примера 1(c), из 2-(2,4-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (35 мг) и циклогексанметиламина (16 мкл) получают названное в заголовке соединение (14 мг). ЯМР (ДМСО-d6)0,85-1,0 (2 Н, м), 1,1-1,3 (3H, м), 1,45 (1 Н, м), 1,55-1,75 (5 Н, м), 3,05 (2 Н, т), 7,46 Способом, подобным способу ссылочного примера 1(c), из 2-(3,4-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (35 мг) и циклогексанметиламина (16 мкл) получают названное в заголовке соединение (31 мг). ЯМР (ДМСО-d6)0,8-1,0 (2 Н, м), 1,1-1,3 (3H, м), 1,5 (1 Н, м), 1,55-1,8 (5 Н, м), 3,06 (2 Н, т),7,62 (1 Н, д), 7,69 (1 Н, д), 8,18 (1 Н, с), 8,59 (1 Н, т), 8,82 (1 Н, с), 10,70 (1 Н, с). ЖХ/МС, t = 4,01 мин, [МН+] 447 и 449. Пример 18. Циклогексилметиламид 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5 карбоновой кислоты Способом, подобным способу ссылочного примера 1 (с), из 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и циклогексанметиламина (16 мкл) получают названное в заголовке соединение (30 мг). ЯМР (ДМСО-d6)0,85-1,0 (2 Н, м), 1,1-1,3 (3H, м), 1,5 (1 Н, м), 1,55-1,8 (5 Н, м), 3,07 (2 Н, т), 7,26 Способом, подобным способу ссылочного примера 1(c), из 2-(3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и циклогексанметиламина (18 мкл) получают названное в заголовке соединение (38 мг). ЯМР (ДМСО-d6)0,85-1,0 (2 Н, м), 1,1-1,3 (3H, м), 1,5 (1 Н, м), 1,55-1,8 (5 Н, м), 3,09 (2 Н, т), 6,87 Способом, подобным способу ссылочного примера 1(c), из 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и циклогексанметиламина (15 мкл) получают названное в заголовке соединение (36 мг). ЯМР (ДМСО-d6)0,85-1,0 (2 Н, м), 1,1-1,3 (3H, м), 1,5 (1 Н, м), 1,55-1,8 (5 Н, м), 3,08 (2 Н, т), 7,23 Способом, подобным способу ссылочного примера 1(c), из 2-(2,6-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (33 мг) и циклогексанметиламина (15 мкл) получают названное в заголовке соединение (9 мг). ЯМР (ДМСО-d6)0,85-1,0 (2 Н, м), 1,05-1,25 (3H, м), 1,46 (1 Н, м), 1,55-1,8 (5 Н, м), 3,04 (2 Н, т), 7,39 Способом, подобным способу ссылочного примера 1(c), из 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (30 мг) и 4-аминометилтетрагидропирана (13 мг) получают названное в заголовке соединение (25 мг). ЯМР (ДМСО-d6)1,15-1,3 (2 Н, м), 1,62 (2 Н, д), 1,74 (1 Н, м), 3,13 (2 Н, т), 3,27 (2 Н, т), 3,86 (2 Н, д),7,10 (1 Н, д), 7,37 (1 Н, т), 7,66 (1 Н, д), 7,97 (1 Н, с), 8,63 (1 Н, т), 8,82 (1 Н, с), 10,60 (1 Н, с). ЖХ/МС, t = 3,22 мин, [МН+] 415 и 417. Пример 23. Циклобутиламид 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(3-хлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и циклобутиламина (10 мкл) получают названное в заголовке(1 Н, т), 7,67 (1 Н, д), 7,96 (1 Н, с), 8,82 (2 Н, с), 10,60 (1 Н, с). ЖХ/МС, t = 3,45 мин, [МН+] 371 и 373. Примеры 24-30. В табл. 1 приводятся примеры 24-30, в колонке 1 указываются предшественники, которые вводят во взаимодействие с метил-2-хлор-4-трифторметилпиримидин-5-карбоксилатом способом, подобным способу ссылочного примера 1(a). Способом, подобным способу ссылочного примера 1(b), получают эфир полученной карбоновой кислоты. Наконец, способом, подобным способу ссылочного примера 1(c), полученный из кислоты продукт вводят во взаимодействие с предшественником из колонки 2, и получают конечный продукт, указанный в колонке 3. Таблица 1 Способом, подобным способу ссылочного примера 1(c), из 2-(3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и 4-аминометилтетрагидропирана (16 мг) получают названное в заголовке соединение (38 мг). ЯМР (ДМСО-d6)1,15-1,3 (2 Н, м), 1,63 (2 Н, д), 1,75 (1 Н, м), 3,15 (2 Н, т), 3,29 (2 Н, т), 3,86 (2 Н, д),6,88 (1 Н, тд), 7,38 (1 Н, кв.), 7,51 (1 Н, д), 7,76 (1 Н, дт), 8,64 (1 Н, т), 8,82 (1 Н, с), 10,60 (1 Н, с). ЖХ/МС, t = 3,08 мин, [МН+] 399. Способом, подобным способу ссылочного примера 1(c), из 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и 4-аминометилтетрагидропирана (13,5 мг) получают названное в заголовке соединение (36 мг). ЯМР (ДМСО-d6)1,15-1,3 (2 Н, м), 1,62 (2 Н, д), 1,74 (1 Н, м), 3,13 (2 Н, т), 3,27 (2 Н, т), 3,86 (2 Н, д),7,23 (1 Н, д), 7,31 (1 Н, т), 7,71 (1 Н, д), 8,11 (1 Н, с), 8,63 (1 Н, т), 8,82 (1 Н, с), 10,60 (1 Н, с). ЖХ/МС, t = 3,26 мин, [МН+] 459 и 461. Пример 33. (Тетрагидропиран-4-илметил)амид 2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5 карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (30 мг) и 4-аминометилтетрагидропирана (12 мг) получают названное в заголовке соединение (25 мг). ЯМР (ДМСО-d6)1,1-1,25 (2 Н, м), 1,60 (2 Н, д), 1,72 (1 Н, м), 3,11 (2 Н, т), 3,26 (2 Н, т), 3,85 (2 Н, д),7,40 (1 Н, т), 7,55 (2 Н, д), 8,60 (1 Н, т), 8,66 (1 Н, с), 10,10 (1 Н, с). ЖХ/МС, t = 3,29 мин, [МН+] 449 и 451. Пример 34. (Тетрагидропиран-4-илметил) амид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (30 мг) и 4-аминометилтетрагидропирана (12 мг) получают названное в заголовке соединение (34 мг). ЯМР (ДМСО-d6)1,1-1,25 (2 Н, м), 1,59 (2 Н, д), 1,72 (1 Н, м), 3,11 (2 Н, т), 3,26 (2 Н, т), 3,85 (2 Н, д),7,47 (1 Н, дд), 7,57 (1 Н, д), 7,72 (1 Н, с), 8,60 (1 Н, т), 8,65 (1 Н, с), 10,05 (1 Н, с). ЖХ/МС, t = 3,33 мин, [МН+] 449 и 451. Дополнительный синтез примера 34. (Тетрагидропиран-4-илметил)амид 2-(2,4-дихлорфениламино)4-трифторметилпиримидин-5-карбоновой кислоты(а) К раствору метил 2-хлор-4-трифторметилпиримидин-5-карбоксилата (0,50 г, обр. от Maybridge) в 1,4-диоксане (5 мл) добавляют 2,4-дихлоранилин (1,7 г) и раствор перемешивают при кипячении с обратным холодильником в течение 7 ч. 1,4-Диоксан удаляют при пониженном давлении и добавляют этилацетат (15 мл). Раствор последовательно промывают 2 N соляной кислотой (10 мл) и водой (310 мл), сушат(MgSO4), упаривают, остаток обрабатывают гексаном и получают метил-2-(2,4-дихлорфениламино)-4 трифторметилпиримидин-5-карбоксилат (358 мг). ЯМР(CDCl3)3,95 (3H, с), 7,30 (1 Н, дд), 7,45 (1 Н, д), 8,00 (1 Н, с), 8,5 (1 Н, д), 9,05 (1 Н, с). ЖХ/МС, t = 3,74 мин, [МН+] 366.(0,358 г) в этаноле (8 мл) добавляют раствор гидроксида калия (190 мг) в этаноле (8 мл) и раствор перемешивают при кипячении с обратным холодильником в течение 24 ч. Этанол удаляют при пониженном давлении и добавляют воду (15 мл). Раствор промывают эфиром и добавляют концентрированную соляную кислоту для доведения до кислотности с рН 1. Выпавшее в осадок твердое вещество отфильтровывают, промывают водой и сушат в вакууме при 50 С, и получают 2-(2,4-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновую кислоту (262 мг).(20 мг). Раствор перемешивают в течение 3 ч и оставляют на ночь. Диметилформамид удаляют при пониженном давлении и добавляют этилацетат (5 мл). Раствор последовательно промывают 5% раствором бикарбоната натрия (2,5 мл), водой (2,5 мл), 5% раствором лимонной кислоты (2,5 мл) и рассолом (22,5 мл), сушат (MgSO4), упаривают и получают названное в заголовке соединение (34 мг). ЯМР (ДМСО-d6)1,20 (2 Н, м), 1,58 (2 Н, д), 1,70 (1 Н, м), 3,10 (2 Н, т), 3,23 (2 Н, т), 3,84 (2 Н, дд), 7,46 Дополнительный синтез примера 34. (Тетрагидропиран-4-илметил)амид 2-(2,4-дихлорфениламино)4-трифторметилпиримидин-5-карбоновой кислоты(a) К раствору метил 2-хлор-4-трифторметилпиримидин-5-карбоксилата (70 г, обр. от Maybridge 22 г, обр. от Fluorochem 48 г) в 1,4-диоксане (100 мл) добавляют 2,4-дихлоранилин (142 г), и раствор перемешивают при кипячении с обратным холодильником в течение 10,5 ч. 1,4-Диоксан удаляют при пониженном давлении (приблизительно 50 мл) и добавляют 2 N HCl (800 мл). Смесь перемешивают подвесной мешалкой в течение 3 ч и полученное твердое вещество отфильтровывают на керамическом фильтре. Твердое вещество промывают 2 N HCl (2300 мл) и водой (4400 мл), затем сушат над гидроксидом натрия в вакууме при 50 С и получают метил 2-(2,4-дихлорфениламино)-4 трифторметилпиримидин-5-карбоксилат. Твердое вещество содержит приблизительно 5% 2,4 дихлоранилина. ЯМР (ДМСО-d6)3,84 (3H, с), 7,47 (1 Н, дд), 7,49 (1 Н, д), 7,74 (1 Н, д), 8,96 (1 Н, с), 10,45 (1 Н, с). ЖХ/МС, t = 3,66 мин, [МН+] 366.(b) К раствору метил 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоксилата (107 г) в метаноле (700 мл) добавляют раствор гидроксида калия (50 г) в метаноле (700 мл) и раствор перемешивают при кипячении с обратным холодильником в течение 24 ч. Метанол удаляют при пониженном давлении и добавляют воду (800 мл). Раствор промывают эфиром (3400 мл, который удаляет оставшийся 2,4-дихлоранилин) и добавляют концентрированную соляную кислоту для доведения до кислотности с рН 1. Выпавшее в осадок твердое вещество отфильтровывают, промывают 2 N HCl и водой до тех пор,пока рН фильтрата не будет нейтральным. Твердое вещество сушат в вакууме при 50 С и получают 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновую кислоту (86,9 г). ЯМР (ДМСО-d6)7,48 (1 Н, дд), 7,60 (1 Н, д), 7,73 (1 Н, д), 8,95 (1 Н, с), 10,3 (1 Н, с), 13,6 (1 Н, с). ЖХ/МС, t = 4,35 мин, [МН+] 352.(с) К раствору 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (86 г) в диметилформамиде (800 мл) последовательно добавляют N-этилморфолин (93 мл),4-аминометилтетрагидропиран (29,5 г), гидрат 1-гидроксибензотриазола (51,5 г) и гидрохлорид 1-(3 диметиламинопропил)-3-этилкарбодиимида (56,2 г). Раствор перемешивают в течение 24 ч. Диметилформамид частично удаляют (приблизительно 650 мл) при пониженном давлении и добавляют 5% раствор бикарбоната натрия (3500 мл, добавляют частями, контролируя выделение диоксида углерода). Смесь перемешивают подвесной мешалкой в течение 3 ч и полученное твердое вещество отфильтровывают на керамическом фильтре. Твердое вещество промывают 5% раствором бикарбоната натрия(4400 мл) и водой (3400 мл), сушат над гидроксидом натрия в вакууме при 50 С и получают названное в заголовке соединение (109,1 г). ЯМР (ДМСО-d6)1,20 (2 Н, м), 1,58 (2 Н, д), 1,70 (1 Н, м), 3,10 (2 Н, т), 3,23 (2 Н, т), 3,84 (2 Н, дд), 7,46 Способом, подобным способу ссылочного примера 1(c), из 2-(2,5-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (50 мг) и 4-аминометилтетрагидропирана (25 мг) получают названное в заголовке соединение (63 мг). ЯМР (ДМСО-d6)1,15-1,3 (2 Н, м), 1,60 (2 Н, д), 1,72 (1 Н, м), 3,12 (2 Н, т), 3,27 (2 Н, т), 3,85 (2 Н, д),7,35 (1 Н, дд), 7,59 (1 Н, д), 7,73 (1 Н, с), 8,62 (1 Н, т), 8,70 (1 Н, с), 10,05 (1 Н, с). ЖХ/МС, t = 3,30 мин, [МН+] 449 и 451. Пример 36. (Тетрагидропиран-4-илметил)амид 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (50 мг) и 4-аминометилтетрагидропирана (25 мг) получают названное в заголовке соединение (68 мг). ЯМР (ДМСО-d6)1,15-1,35 (2 Н, м), 1,62 (2 Н, д), 1,72 (1 Н, м), 3,14 (2 Н, т), 3,28 (2 Н, т), 3,86 (2 Н, д),7,25 (1 Н, с), 7,88 (2 Н, с), 8,66 (1 Н, т), 8,88 (1 Н, с), 10,75 (1 Н, с). Пример 37. (Тетрагидропиран-4-илметил)амид 2-(3-метоксифениламино)-4-трифторметилпиримидин-5 карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(3-метоксифениламино)-4 трифторметилпиримидин-5-карболовой кислоты (32 мг) и 4-аминометилтетрагидропирана (14,5 мг) получают названное в заголовке соединение (29 мг). ЯМР (ДМСО-d6)1,1-1,25 (2 Н, м), 1,61 (2 Н, д), 1,74 (1 Н, м), 3,13 (2 Н, т), 3,27 (2 Н, т), 3,74 (3H, с),3,86 (2 Н, д), 6,63 (1 Н, д), 7,25 (2 Н, м), 7,53 (1 Н, с), 8,62 (1 Н, т), 8,76 (1 Н, с), 10,35 (1 Н, с). ЖХ/МС, t = 2,97 мин, [МН+] 411. Пример 38. Циклопентилметиламид 2-(3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(3-фторфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (30 мг) и гидрохлорида циклопентилметиламина (17 мг, получают так,как описано в Kelley et al., J. Med. Chem., 40, 3207 (1997 получают названное в заголовке соединение Способом, подобным способу ссылочного примера 1(c), из 2-(3-бромфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (36,5 мг) и гидрохлорида циклопентилметиламина Способом, подобным способу ссылочного примера 1(c), из 2-(2,3-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (32 мг) и гидрохлорида циклопентилметиламина (15 мг) получают названное в заголовке соединение (30 мг). ЯМР (ДМСО-d6)1,15-1,30 (2 Н, м), 1,44-1,78 (6 Н, м), 2,10 (1 Н, квинтет), 3,16 (2 Н, т), 7,41 (2 Н, т),7,54 (1 Н, м), 8,58 (1 Н, ушир.т), 8,78 (1 Н, с), 10,10 (1 Н, с). ЖХ/МС, t= 3,71 мин, [МН+] 433 и 435. Пример 41. Циклопентилметиламид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5 карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (32 мг) и гидрохлорида циклопентилметиламина (15 мг) получают названное в заголовке соединение (27 мг). ЯМР (ДМСО-d6)1,2-1,3 (2 Н, м), 1,4-1,79 (6 Н, м), 2,10 (1 Н, квинтет), 3,17 (2 Н, т), 7,50 (1 Н, д), 7,60 Способом, подобным способу ссылочного примера 1(c), из 2-(2,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты. (32 мг) и гидрохлорида циклопентилметиламина (15 мг) получают названное в заголовке соединение (23 мг). ЯМР (ДМСО-d6)1,15-1,30 (2 Н, м), 1,45-1,79 (6 Н, м), 2,08 (1 Н, квинтет), 3,18 (2 Н, т), 7,38 (1 Н, д),7,62 (1 Н, д), 7,75 (1 Н, с), 8,61 (1 Н, ушир.т), 8,71 (1 Н, с), 10,05 (1 Н, с). ЖХ/МС, t = 3,76 мин, [МН+] 433 и 435. Пример 43. Циклопентилметиламид 2-(2,6-дихлорфениламино)-4-трифторметилпиримидин-5 карбоновой кислоты Способом, подобным способу ссылочного примера 1(с), из 2-(2,6-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (32 мг) и гидрохлорида циклопентилметиламина (15 мг) получают названное в заголовке соединение (25 мг). ЯМР (ДМСО-d6)1,15-1,30 (2 Н, м), 1,45-1,78 (6 Н, м), 2,08 (1 Н, квинтет), 3,15 (2 Н, т), 7,4 (1 Н, т),7,6-7,68 (2 Н, м), 8,5-8,7 (2 Н, м), 10,20 (1 Н, с). ЖХ/МС, t = 3,49 мин, [МН+] 433 и 435. 2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5 Способом, подобным способу ссылочного примера 1(c), из 2-(3,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (32 мг) и гидрохлорида циклопентилметиламина (15 мг) получают названное в заголовке соединение (29 мг). ЯМР (ДМСО-d6)1,12-1,3 (2 Н, м), 1,44-1,8 (6 Н, м), 2,1 (1 Н, квинтет), 3,17 (2 Н, т), 7,62 (1 Н,ушир.д), 7,72 (1 Н, д), 8,18 (1 Н, д), 8,60-8,69 (1 Н, ушир.т), 8,83 (1 Н, с), 10,80 (1 Н, с). ЖХ/МС, t = 3,87 мин, [МН+] 433 и 435. Пример 45. Циклопентилметиламид 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5 карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (32 мг) и гидрохлорида циклопентилметиламина (15 мг) получают названное в заголовке соединение (27 мг) . ЯМР (ДМСО-d6)1,14-1,34 (2 Н, м), 1,45-1,8 (6 Н, м), 2,10 (1 Н, квинтет), 3,20 (2 Н, т), 7,28 (1 Н, с),7,91 (2 Н, с), 8,6-8,7 (1 Н, ушир.т), 8,9 (1 Н, с), 10,75 (1 Н, с). ЖХ/МС, t = 3,94 мин, [МН+] 433 и 435. Пример 46. Циклопентилметиламид 2-(3-метоксифениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(3-метоксифениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (3,2 мг) и гидрохлорида циклопентилметиламина (17 мг) получают названное в заголовке соединение (21 мг). ЯМР (ДМСО-d6)1,25-1,38 (2 Н, м), 1,50-1,85 (6 Н, м), 2,15 (1 Н, квинтет), 3,25 (2 Н, т), 3,85 (3H, с),6,70 (1 Н, ушир.д), 7,26-7,37 (2 Н, м), 7,60 (1 Н, м), 8,68 (1 Н, т), 8,80 (1 Н, с), 10,50 (1 Н, с). ЖХ/МС, t = 3,46 мин, [МН+] 395. Пример 47. Циклобутиламид 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(3-бромфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (35 мг) и циклобутиламина (10 мкл) получают названное в заголовке соединение (30 мг). ЯМР (ДМСО-d6)1,70 (2 Н, м), 1,97 (2 Н, м), 2,22 (2 Н, м), 4,32 (1 Н, м), 7,22-7,33 (2 Н, м), 7,70 (1 Н, д),8,10 (1 Н, с), 8,81-8,83 (2 Н, м), 10,60 (1 Н, с). ЖХ/МС, t = 3,47 мин, [МН+] 415 и 417. Пример 48. Циклобутиламид 2-(2,3-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(2,3-дихлорфениламино)-4-трифтор- 29012703 метилпиримидин-5-карбоновой кислоты (25 мг) и циклобутиламина (10 мкл) получают названное в заголовке соединение (20 мг). ЯМР (ДМСО-d6)1,70 (2 Н, м), 1,97 (2 Н, м), 2,22 (2 Н, м), 4,32 (1 Н, м), 7,38-7,56 (3H, м), 8,65 (1 Н, с),8,80 (1 Н, д), 10,10 (1 Н, с). ЖХ/МС, t = 3,48 мин, [МН+] 405 и 407. Пример 49. Циклобутиламид 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(2,4-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (30 мг) и циклобутиламина (10 мкл) получают названное в заголовке соединение (26 мг). ЯМР (ДМСО-d6)1,70 (2 Н, м), 1,97 (2 Н, м), 2,22 (2 Н, м), 4,32 (1 Н, м), 7,46-7,72 (3H, м), 8,64 (1 Н, с),8,80 (1 Н, д), 10,00 (1 Н, с). ЖХ/МС, t = 3,54 мин, [МН+] 405 и 407. Пример 50. Циклобутиламид 2-(2,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(2,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты (50 мг) и циклобутиламина (19 мкл) получают названное в заголовке соединение (56 мг). ЯМР (ДМСО-d6)1,70 (2 Н, м), 1,97 (2 Н, м), 2,22 (2 Н, м), 4,30 (1 Н, м), 7,33-7,73 (3H, м), 8,70 (1 Н, с),8,80 (1 Н, д), 10,00 (1 Н, с). ЖХ/МС, t = 3,52 мин, [МН+] 405 и 407. Пример 51. Способом, подобным способу ссылочного примера 1(c), из 2-(2,6-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (30 мг) и циклобутиламина (10 мкл) получают названное в заголовке соединение (34 мг). ЯМР (ДМСО-d6)1,70 (2 Н, м), 1,97 (2 Н, м), 2,22 (2 Н, м), 4,30 (1 Н, м), 7,36-7,60 (3H, м), 8,59 (1 Н, с),8,80 (1 Н, д), 10,15 (1 Н, с). ЖХ/МС, t = 3,24 мин, [МН+] 405 и 407. Пример 52. Циклобутиламид 2-(3,5-дихлорфениламино)-4-трифторметилпиримидин-5-карбоновой кислоты Способом, подобным способу ссылочного примера 1(c), из 2-(3,5-дихлорфениламино)-4 трифторметилпиримидин-5-карбоновой кислоты (50 мг) и циклобутиламина (19 мкл) получают названное в заголовке соединение (56 мг). ЯМР (ДМСО-d6)1,70 (2 Н, м), 1,97 (2 Н, м), 2,22 (2 Н, м), 4,32 (1 Н, м), 7,25-7,87 (3H, м), 8,85 (1 Н, д),8,88 (1 Н, с), 10,80 (1 Н, с). ЖХ/МС, t = 3,73 мин, [МН+] 405 и 407.
МПК / Метки
МПК: C07D 409/12, C07D 401/06, A61K 31/506, A61K 31/505, C07D 239/42, C07D 405/12, C07D 403/06
Метки: пиримидина, качестве, производные, модуляторов, применение
Код ссылки
<a href="https://eas.patents.su/30-12703-proizvodnye-pirimidina-i-ih-primenenie-v-kachestve-modulyatorov-cb2.html" rel="bookmark" title="База патентов Евразийского Союза">Производные пиримидина и их применение в качестве модуляторов cb2</a>
Предыдущий патент: Замещённые индазолы, композиции, содержащие указанные индазолы, способ их получения и применение
Следующий патент: Новые фармацевтические соединения
Случайный патент: Способ и установка для удаления диоксида углерода из сырьевого газа