Производные триазолопиримидина в качестве ингибиторов киназы гликогенсинтазы-3
Номер патента: 11300
Опубликовано: 27.02.2009
Авторы: Эмбрехтс Вернер Констант Йохан, Коиманс Людвиг Поль, Виллемс Марк, Бейнстерс Петер Якобус Йоханнес Антониус, Лав Кристофер Джон, Фрейн Эдди Жан Эдгар, Вандермасен Неле
Формула / Реферат
1. Производные триазолопиримидина формулы
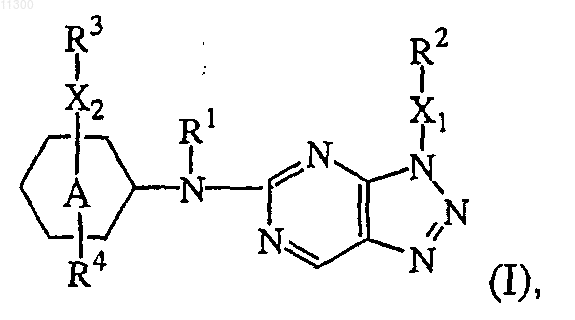
и его фармацевтически приемлемая аддитивная соль, где
кольцо A представляет собой фенил;
R1 представляет собой водород или C1-6алкил;
X1 представляет собой прямую связь или -(CH2)n3-, причем n3 означает целое число, равное 1, 2 или 3;
R2 представляет собой C3-7циклоалкил; фенил; 6-членный моноциклический гетероцикл, содержащий N, который может быть замещен C1-6-алкоксикарбонилом; или радикал формулы
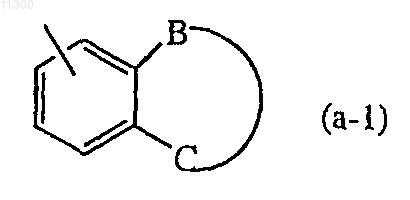
где -B-C- представляет собой бивалентный радикал формулы
| -CH2-CH2-CH2-; | (b-1) |
| -X3-CH2-(CH2)n-X3- | (b-4) |
или
| -CH=N-X3-, | (b-6) |
причем X3 представляет собой O или NR5;
n означает целое число, равное 1;
где указанный фенил, где возможно, может быть необязательно замещенным по крайней мере одним заместителем, выбранным из галогена; C1-4алкила, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси, циано, C1-4алкилокси, C1-4алкилкарбонила, C1-4алкилоксиC1-4алкилокси, NR6R7 или -C(=O)-NR6R7; полигалогенC1-6алкила; C1-6алкилокси, необязательно замещенного C1-4алкилокси; C1-6алкилтио; арилтио; арилкарбонила; NR6R7; -C(=O)-NR6R7; -S(=O)n1-R8; или имидазолила, необязательно замещенного C1-4алкилом;
X2 представляет собой прямую связь; -NR1-; -O-(CH2)n3-; -C(=O)-; -C(=O)-NR5-(CH2)n3-; -(CH2)n3-; -S(=O)n1-NR5-(CH2)n3-NR5-;
R3 представляет собой насыщенный или ароматический 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, или ароматический 9-членный бициклический гетероцикл, содержащий два гетероатома, выбранных из O или N, где указанный заместитель R3, где возможно, может быть замещен галогеном; гидрокси; C1-6алкилом, оксогруппой или -NR6R7;
R4 представляет собой водород, нитро, карбоксил;
R5 представляет собой водород;
R6 и R7, каждый независимо, представляют собой водород; C1-6алкил; C1-6алкилкарбонил, необязательно замещенный C1-4алкилокси; C1-6алкилоксикарбонил; C3-7циклоалкилкарбонил; циано; адамантанилкарбонил;
R8 представляет собой NR6R7;
n1 означает целое число, равное 2;
где арил представляет собой фенил или фенил, замещенный по крайней мере одним заместителем, выбранным из галогена, C1-6алкила, C3-7циклоалкила, C1-6алкилокси, циано, нитро, полигалогенC1-6алкила или полигалогенC1-6алкилокси.
2. Соединение по п.1, где
R2 представляет собой C3-7циклоалкил; фенил или 6-членный моноциклический гетероцикл, содержащий N, который может быть замещен C1-6-алкоксикарбонилом; или радикал формулы
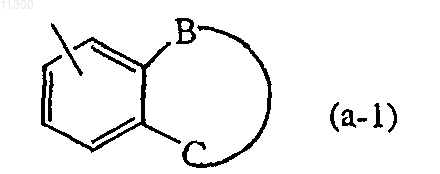
где -B-C- представляет собой бивалентный радикал формулы
| -CH2-CH2-CH2-; | (b-1) |
| -X3-CH2-(CH2)n-Х3-, | (b-4) |
причем X3 представляет собой O или NR5; n означает число, равное 1;
где указанный фенил, где возможно, может быть необязательно замещен по крайней мере одним заместителем, выбранным из галогена; C1-4алкила, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси, циано, C1-4алкилокси, NR6R7 или -C(=O)-NR6R7; -S(=O)n1-R8; полигалогенC1-6алкила; C1-6алкилокси; C1-6алкилтио; NR6R7; -C(=O)-NR6R7;
X2 представляет собой прямую связь; -NR1-; -C(=O)-; (CH2)n3-;
R3 представляет собой 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, где указанный заместитель R3, где возможно, может быть необязательно замещен по крайней мере одним заместителем, выбранным из галогена; гидрокси; C1-6алкила или -NR6R7; и в случае, когда R3 представляет собой насыщенный 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, указанный R3 может быть также замещен по крайней мере одной оксогруппой;
R5 представляет собой водород;
R6 и R7, каждый независимо, представляют собой водород, циано, C1-6алкилкарбонил, C1-4алкил;
R8 представляет собой NR6R7.
3. Соединение по п.1, где
кольцо A представляет собой фенил;
R1 представляет собой водород или C1-6алкил;
X1 представляет собой прямую связь или -(CH2)n3-;
R2 представляет собой C3-7циклоалкил, фенил, 6-членный моноциклический гетероцикл, содержащий N, который может быть замещен C1-6-алкоксикарбонилом; или радикал формулы
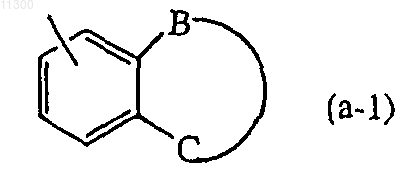
где -B-C- представляет собой бивалентный радикал формулы
| -CH2-CH2-CH2-; | (b-1) |
| -X3-CH2-(CH2)n-X3-; | (b-4) |
| -CH=N-X3-, | (b-6) |
причем X3 представляет собой O или NR5;
n означает целое число, равное 1;
где указанный фенил, где возможно, может быть необязательно замещен по крайней мере одним заместителем, выбранным из галогена; полигалогенC1-6алкила; C1-6алкилокси, необязательно замещенного C1-4алкилокси; C1-6алкилтио; NR6R7; -C(=O)NR6R7; -S(=O)n1-R8; имидазолила, необязательно замещенного C1-4алкилом; арилтио; арилкарбонила; или C1-4алкила, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси, циано, C1-4алкилокси, C1-4алкилоксиC1-4алкилокси, NR6R7 или -C(=O)-NR6R7;
X2 представляет собой прямую свячь; -NR1-; -O-(CH2)n3-; -C(=O)-; -C(=O)-NR5-(CH2)n3-; -(CH2)n3- или -S(=O)n1-NR5-(CH2)n3-NR5-;
R3 представляет собой 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, где указанный заместитель R3, где возможно, может быть необязательно замещен по крайней мере одним заместителем, выбранным из галогена; гидрокси; C1-6алкила; или NR6R7; и в случае, когда R3 представляет собой насыщенный 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, указанный R3 может быть также замещен по крайней мере одной оксогруппой;
R4 представляет собой водород, нитро или карбоксил;
R5 представляет собой водород;
R6 и R7, каждый независимо, представляют собой водород; циано; C1-6алкилкарбонил, необязательно замещенный C1-4алкилокси; C1-6алкилоксикарбонил; C3-7циклоалкилкарбонил; адамантанилкарбонил или C1-6алкил;
R8 представляет собой NR6R7;
n1 означает целое число, равное 2;
арил представляет собой фенил.
4. Соединение по любому из пп.1-3, где
кольцо A представляет собой фенил;
R1 представляет собой водород;
X1 представляет собой прямую связь или -(CH2)n3-;
R2 представляет собой инданил; 2,3-дигидро-1,4-бензодиоксанил; фенил, необязательно замещенный 1 или 2 заместителями, при этом каждый независимо выбран из C1-6алкилокси; галогена; полигалогенC1-6алкила; NR6R7; -S(=O)n1-R8; -C(=O)NR6R7; или C1-6алкила, который может быть необязательно замещен гидрокси, циано, C1-4алкилокси, C1-4алкилоксиC1-4алкилокси, NR6R7 или -C(=O)NR6R7; X2 представляет собой прямую связь; -NR1-, -O-(CH2)n3-, -C(=O)-, -C(=O)-NR5-(CH2)n3-; или -(CH2)n3-;
R3 представляет собой тетразолил; пиперазинил; имидазолил; оксазолил; пиримидинил; тиазолил; триазолил; пиридил; пиперидинил; пиразинил; пиразолил или морфолинил; и эти указанные кольца, представляющие собой R3, могут быть необязательно замещены одним заместителем, выбранным из C1-6алкила; NR6R7; гидрокси; галогена; и в случае когда R3 представляет собой насыщенную или частично насыщенную циклическую структуру, указанный R3 может быть также замещен по крайней мере одной оксогруппой;
R4 представляет собой водород;
R6 и R7, каждый независимо, представляют собой водород; циано; C1-6алкилкарбонил, необязательно замещенный C1-4алкилокси; C1-6алкилоксикарбонил; C3-7циклоалкилкарбонил или C1-6алкил;
R8 представляет собой NR6R7.
5. Соединение по любому из пп.1-4, где заместитель R3 связан с кольцом A в мета-положении относительно линкера NR1.
6. Соединение по любому из пп.1-4, где заместитель R3 связан с кольцом A в пара-положении относительно линкера NR1.
7. Соединение по любому из пп.1-6, где заместитель R3 представляет собой необязательно замещенный насыщенный 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N.
8. Соединение по любому из пп.1-7, где X1 представляет собой прямую связь.
9. Соединение по любому из пп.1, 5-8, где R2 представляет собой C3-7циклоалкил; фенил; 6-членный моноциклический гетероцикл, содержащий N; или радикал формулы (а-1); где указанный фенил замещен по крайней мере одним заместителем, выбранным из полигалогенC1-6алкила, C1-6алкилокси, NR6R7; или C1-6алкила, замещенного NR6R7.
10. Соединение по любому из пп.1, 5, 6, 8 или 9, где R3 представляет собой 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, или 9-членный бициклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O или N, где указанный заместитель R3 замещен по крайней мере одним заместителем, выбранным из C1-6алкила или NR6R7.
11. Соединение по любому из пп.1, 5-8 или 10, где R2 представляет собой C3-7циклоалкил; фенил; 6-членный моноциклический гетероцикл, содержащий N; или радикал формулы (а-1), где указанный фенил замещен по крайней мере одним заместителем, выбранным из галогена; полигалогенC1-6алкила.
12. Соединение по п.1, выбранное из
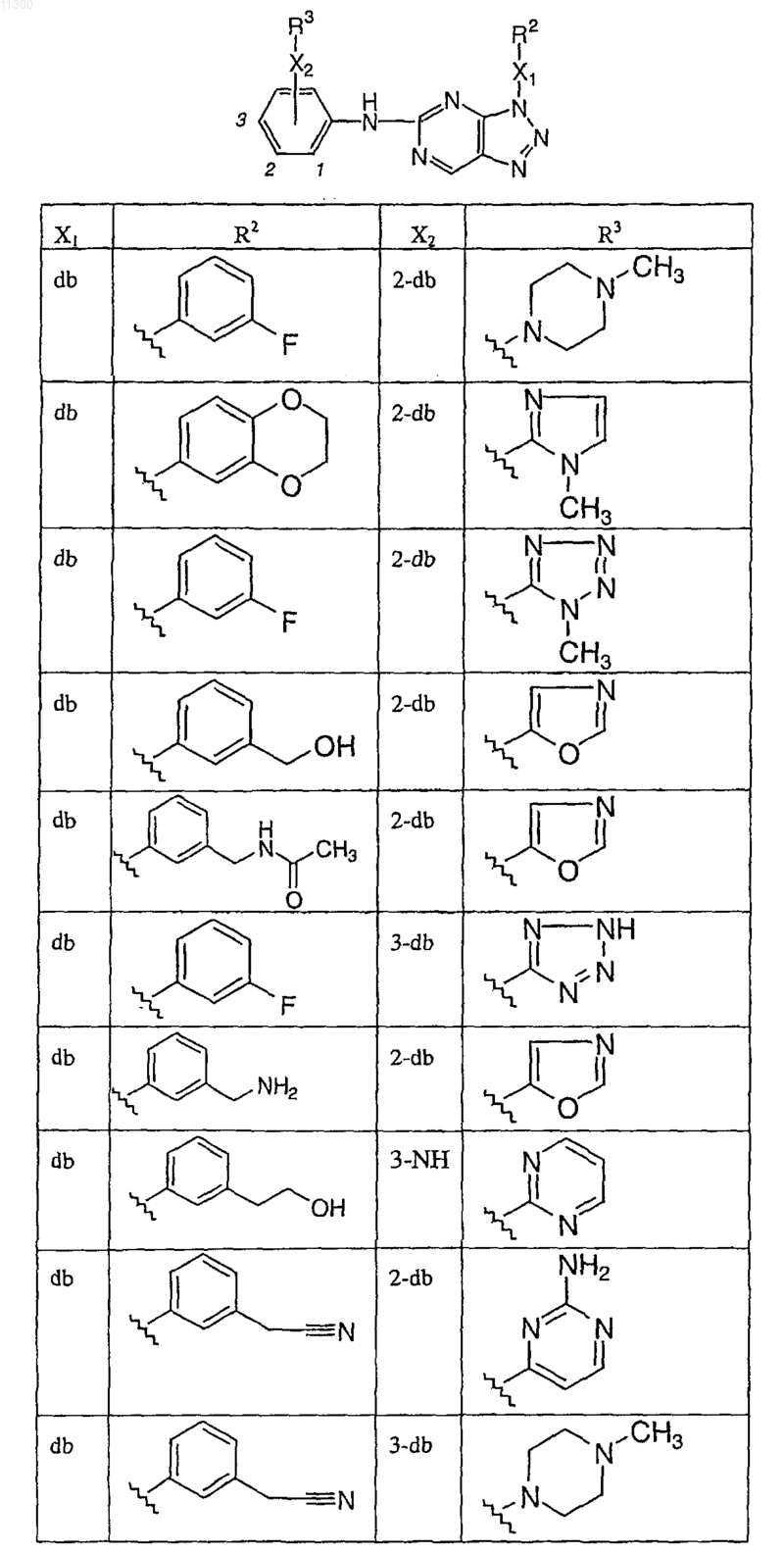
и его фармацевтически приемлемой соли.
13. Соединение по п.1, выбранное из
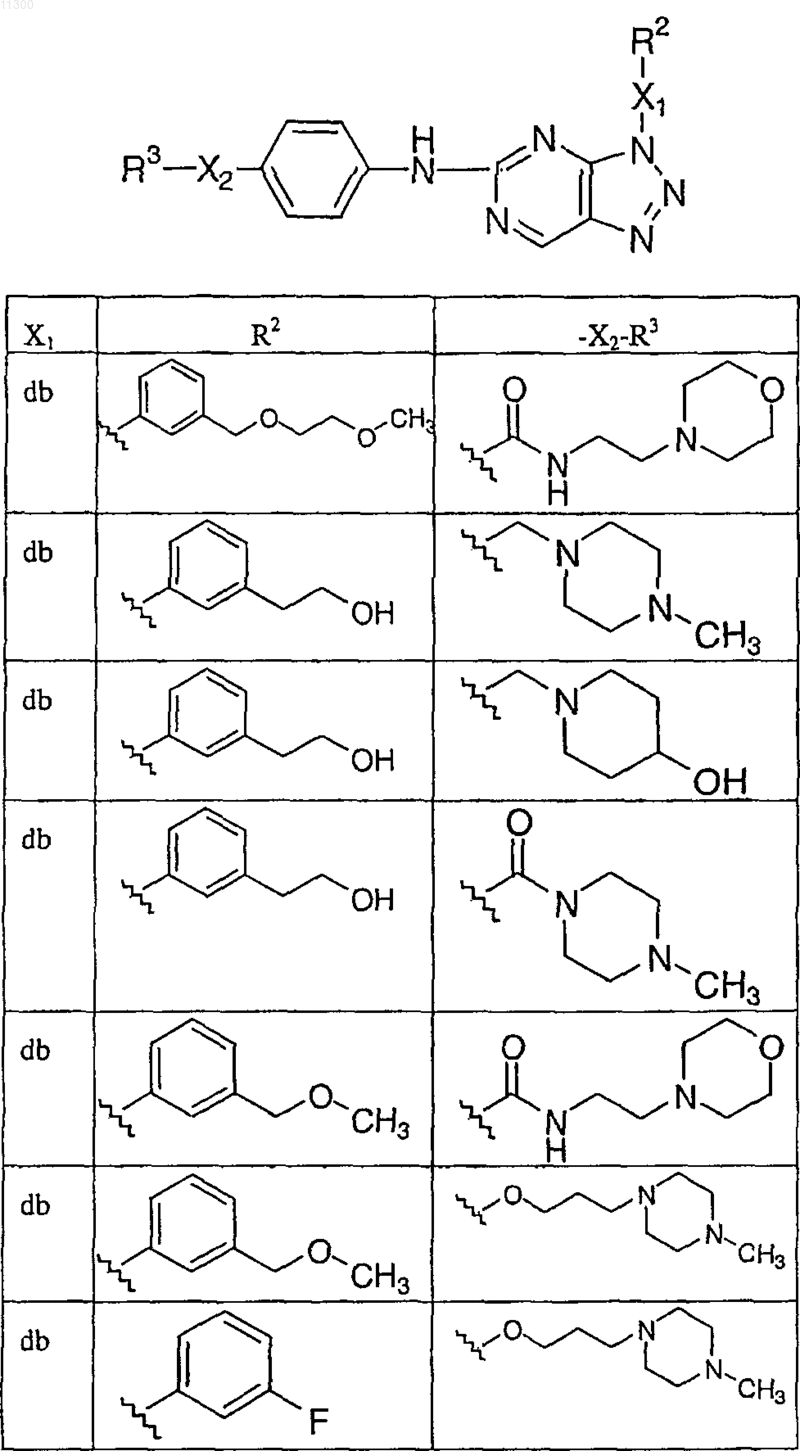
и его фармацевтически приемлемой соли.
14. Применение соединения по любому из пп.1-13 для получения лекарственного средства для профилактики или лечения заболеваний, опосредованных GSK-3.
15. Применение соединения по любому из пп.1-13 для получения лекарственного средства для профилактики или лечения диабета, болезни Альцгеймера и боли.
16. Фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и в качестве активного компонента терапевтически эффективное количество соединения по любому из пп.1-13.
17. Способ получения фармацевтической композиции по п.16, отличающийся тем, что терапевтически эффективное количество соединения по любому из пп.1-13 смешивают с фармацевтически приемлемым носителем с образованием однородной смеси.
18. Способ получения соединения по п.1, включающий циклизацию промежуточного соединения формулы (II) в присутствии нитритной соли, подходящего растворителя и подходящей кислоты
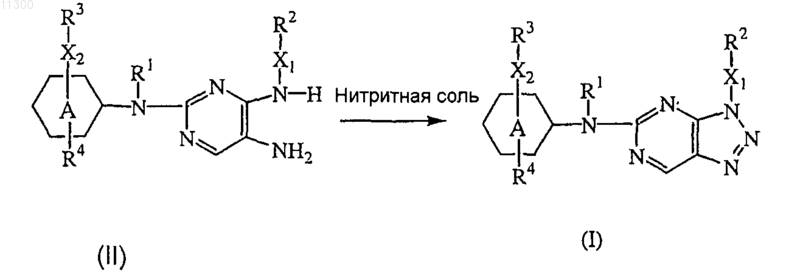
где кольцо A, R1-R4, X1 и X2 такие, как определено в п.1;
или, при желании, превращение соединений формулы (I) друг в друга, следуя известным в данной области преобразованиям, и, кроме того, при желании, превращение соединений формулы (I) в терапевтически активную нетоксичную аддитивную соль кислоты путем обработки кислотой или в терапевтически активную нетоксичную аддитивную соль основания обработкой основанием либо, наоборот, превращение формы аддитивной соли кислоты в свободное основание путем обработки щелочью или превращение аддитивной соли основания в свободную кислоту обработкой кислотой.
19. Способ получения соединения по п.1, включающий взаимодействие промежуточного соединения формулы (III) с промежуточным соединением формулы (IV) в присутствии подходящего растворителя
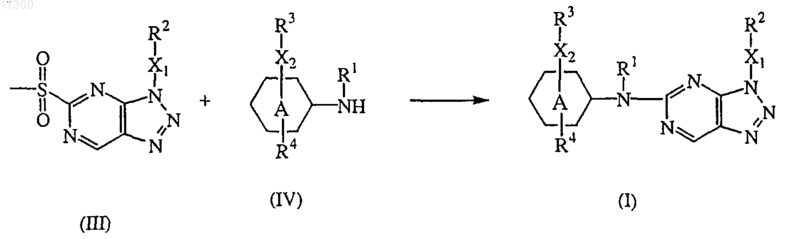
где кольцо A, R1-R4, X1 и X2 такие, как определено в п.1;
или, при желании, превращение соединений формулы (I) друг в друга, следуя известным в данной области преобразованиям, и, кроме того, при желании, превращение соединений формулы (I) в терапевтически активную нетоксичную аддитивную соль кислоты путем обработки кислотой или в терапевтически активную нетоксичную аддитивную соль основания обработкой основанием либо, наоборот, превращение формы аддитивной соли кислоты в свободное основание путем обработки щелочью или превращение аддитивной соли основания в свободную кислоту обработкой кислотой.
Текст
011300 Настоящее изобретение относится к новой группе соединений, их применению в качестве лекарственного средства, их применению для получения лекарственного средства для лечения заболеваний, опосредованных через киназу гликогенсинтазы-3 (GSK-3), в частности киназы гликогенсинтазы-3 и -3; способам их получения и фармацевтическим композициям, их содержащим. В международной публикации WO 00/62778 описываются циклические ингибиторы протеинтирозинкиназы. В частности, в этой публикации раскрываются тиазолильные производные, содержащие бициклическую структуру. В международной публикации WO 01/44246 описываются бициклические соединения на основе пиримидина и пиридина, имеющие ингибирующую активность в отношении GSK-3. В международной публикации WO 99/65897 описываются соединения на основе пиримидина и пиридина, имеющие ингибирующую активность в отношении GSK-3. В международной публикации WO 02/04450 описываются производные пурина, имеющие активность ингибирования образования -амилоида либо стимулирования образования белка-предшественника -амилоида. В международной публикации WO 02/50073 описываются пиразоло[3,4-с]пиридины в качестве ингибиторов GSK-3. Международная публикация WO 2004/018473 относится к ди- и тризамещенным производным 8-азапурина как ингибиторам циклинзависимой киназы. В патенте Японии 59062594 описываются 3,5-дизамещенные соединения триазолопиримидина. Настоящее изобретение относится к соединениям, которые отличаются от соединений предшествующего уровня техники по структуре, фармакологической активности, эффективности, селективности,растворимости, проницаемости, метаболической стабильности. Настоящее изобретение относится к соединению формулы его фармацевтически приемлемой аддитивной соли,в которой кольцо A представляет собой фенил;R1 представляет собой водород или C1-6 алкил;X1 представляет собой прямую связь или -(CH2)n3-; причем n3 означает целое число, равное 1, 2 или 3;R2 представляет собой C3-7 циклоалкил; фенил; 6-членный моноциклический гетероцикл, содержащий N, который может быть замещен C1-6-алкоксикарбонилом; или радикал формулы где -B-C- представляет собой бивалентный радикал формулыn означает целое число, равное 1; где указанный фенил, где возможно, может быть необязательно замещенным по крайней мере одним заместителем, выбранным из галогена; C1-4 алкила, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси, циано, C1-4 алкилокси,C1-4 алкилкарбонила, C1-4 алкилоксиC1-4 алкилокси, NR6R7 или -C(=O)-NR6R7; полигалогенC1-6 алкила;X2 представляет собой прямую связь; -NR1-; -O-(CH2)n3-; -C(=O)-; -C(=O)-NR5-(CH2)n3-; -(CH2)n3-;R3 представляет собой насыщенный или ароматический 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, или ароматический 9-членный бициклический гетероцикл, содержащий два гетероатома, выбранных из O или N, где указанный заместитель R3, где возможно, может быть замещен галогеном; гидрокси; C1-6 алкилом, оксогруппой или -NR6R7;n1 означает целое число, равное 2; где арил представляет собой фенил или фенил, замещенный по крайней мере одним заместителем, выбранным из галогена, C1-6 алкила, C3-7 циклоалкила, C1-6 алкилокси,циано, нитро, полигалогенC1-6 алкила или полигалогенC1-6 алкилокси. Настоящее изобретение также относится к применению соединения формулы (I) для получения лекарственного средства для профилактики или лечения заболеваний, опосредованных GSK-3. Используемый здесь термин C1-3 алкил в качестве группы или части группы означает насыщенные углеводородные радикалы с прямой или разветвленной цепью, имеющие от 1 до 3 углеродных атомов,такие как метил, этил, пропил, 1-метилэтил; C1-4 алкил как группа или часть группы означает насыщенные углеводородные радикалы с прямой или разветвленной цепью, имеющие от 1 до 4 углеродных атомов, такие как группы, определенные для C1-3 алкила, и бутил; C1-6 алкил как группа или часть группы означает насыщенные углеводородные радикалы с прямой или разветвленной цепью, имеющие от 1 до 6 углеродных атомов, такие как группы, определенные для C1-4 алкила, и пентил, гексил, 2-метилбутил и т.п.; C2-4 алкенил как группа или часть группы означает углеводородные радикалы с прямой или разветвленной цепью, имеющие от 2 до 4 углеродных атомов, содержащие двойную связь, такие как этенил,пропенил, бутенил и т.п.; C2-6 алкенил как группа или часть группы означает углеводородные радикалы с прямой или разветвленной цепью, имеющие от 2 до 6 углеродных атомов, содержащие двойную связь,такие как группы, определенные для C2-4 алкенила, и пентенил, гексенил и т.п.; C2-4 алкинил как группа или часть группы означает углеводородные радикалы с прямой или разветвленной цепью, имеющие от 2 до 4 углеродных атомов, содержащие тройную связь, такие как этинил, пропинил, бутинил и т.п.;C2-6 алкинил как группа или часть группы означает углеводородные радикалы с прямой или разветвленной цепью, имеющие от 2 до 6 углеродных атомов, содержащие тройную связь, такие как группы, определенные для C2-4 алкинила, и пентинил, гексинил и т.п.; термин C3-7 циклоалкил характерен для циклопропила, циклобутила, циклопентила, циклогексила и циклогептила; 4-, 5-, 6- или 7-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, N или S, включает насыщенные, частично насыщенные или ароматические 4-, 5-, 6- или 7-членные моноциклические гетероциклы, содержащие по крайней мере один гетероатом, выбранный из O, N или S; насыщенные гетероциклы представляют собой гетероциклы, содержащие только простые (ординарные) связи; частично насыщенные гетероциклы представляют собой гетероциклы, содержащие по крайней мере одну двойную связь при условии, что циклическая структура не является ароматической циклической структурой; термин "ароматический" является общеизвестным для специалиста в данной области и означает циклически сопряженные системы с ароматической стабильностью при числе -электронов, равном 4n'+2, т.е. с 6, 10,14 и т.д. -электронами (правило Хюккеля; при этом n' равно 1, 2, 3 и т.д.). Конкретными примерами 4-, 5-, 6- или 7-членных насыщенных моноциклических гетероциклов являются азетидинил, оксетанил, тетрагидрофуранил, пирролидинил, диоксоланин, имидазолидинил, тиазолидинил, тетрагидротиенил, дигидрооксазолил, изотиазолидинил, изоксазолидинил, оксадиазолидинил, триазолидинил, тиадиазолидинил, пиразолидинил, пиперидинил, гексагидропиримидинил, гексагидропиридазинил, диоксанил, морфолинил, дитианил, тиоморфолинил, пиперазинил, гомопиперидинил(азепанил), [1,3]диазепанил, гомопиперазинил ([1,4]диазепанил), [1,2]диазепанил, оксепанил, диоксепанил. Конкретными примерами 5- или 6-членных частично насыщенных гетероциклов являются пирролинил, имидазолинил, пиразолинил и т.д. Конкретными примерами 4-, 5-, 6- или 7-членных ароматических моноциклических гетероциклов являются пирролил, фурил, тиенил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, триазолил, тиадиазолил, оксадиазолил, тетразолил, пиридил, пиримидинил, пиразинил, пиридазинил. Используемый здесь ранее фрагмент (=O) образует часть карбонила, когда связан с атомом углерода, часть сульфоксида, когда связан с атомом серы, и часть сульфонила, когда два указанных термина связаны с атомом серы. Примерами R3, представляющего собой насыщенный 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, где указанный R3 замещен по крайней мере одной оксо (группой), являются, например, циклогексанон или тетрагидро-1,1 диоксид-2 Н-тиопиран. Термин "гало" является характерным для фтора, хлора, брома и йода. Используемые ранее и в дальнейшем термины полигалогенC1-4 алкил и полигалогенC1-6 алкил в качестве группы или части группы определяют как моно- или полигалогензамещенный C1-4 алкил или C1-6 алкил, например метил, замещенный одним или несколькими атомами фтора, дифторметил или трифторметил, 1,1-дифторэтил и т.п. В случае,когда с алкильной группой связан больше чем один атом галогена, что не выходит за пределы определения полигалогенC1-4 алкила или полигалогенC1-6 алкила, эти атомы галогена могут быть одинаковыми или различными.-2 011300 Подразумевается, что термин гетероцикл в определении, например, R2 или R3 включает все возможные изомерные формы гетероциклов, например пирролил также включает 2 Н-пирролил. Вышеупомянутые гетероциклы могут быть присоединены к остатку молекулы формулы (I) посредством любого кольцевого углерода или гетероатома по обстановке, если не оговорено иначе. Так, например, когда 5- или 6-членный гетероцикл представляет собой имидазолил, он может представлять собой 1-имидазолил, 2-имидазолил, 4-имидазолил и т.п. В тех случаях, когда любая переменная (например, R6, R7 и т.д.) встречается больше чем один раз в какой-либо составляющей, каждое определение является независимым. Линии, начерченные в направлении от заместителей внутрь циклической структуры, указывают на то, что связь может быть присоединена к любому из подходящих атомов кольца циклической структуры. Например, в случае радикала формулы (a-1), указанный радикал может быть присоединен к остатку соединения формулы (I) через атом углерода фенильной части или через атом углерода или гетероатом части -B-C-. Для терапевтического применения соли соединений формулы (I) представляют собой соли, в которых противоион является фармацевтически приемлемым. Однако соли кислот и оснований, которые не являются фармацевтически приемлемыми, могут также найти применение, например, для получения или очистки фармацевтически приемлемого соединения. Все соли, независимо от того, являются ли они фармацевтически приемлемыми или нет, входят в объем настоящего изобретения. Подразумевается, что вышеупомянутые фармацевтически приемлемые аддитивные соли включают терапевтически активные нетоксичные формы аддитивных солей кислоты, которые способны образовывать соединения формулы (I). Последние можно получить, обрабатывая основную форму (соединения) соответствующими кислотами, как, например, неорганическими кислотами, такими как, например, галогенводородные кислоты, например хлористо-водородная, бромисто-водородная и т.п.; серная кислота,азотная кислота, фосфорная кислота и т.п.; или органическими кислотами, такими как, например, уксусная, пропановая, оксиуксусная (гликолевая), 2-оксипропановая, 2-оксопропановая, щавелевая, малоновая, янтарная, малеиновая, фумаровая, яблочная, винная, 2-гидрокси-1,2,3-пропантрикарбоновая, метансульфоновая, этансульфоновая, бензолсульфоновая, 4-метилбензолсульфоновая, циклогексансульфаминовая, 2-гидроксибензойная, 4-амино-2-гидроксибензойная и т.п. кислоты. С другой стороны, солевая форма может быть превращена обработкой щелочью в форму свободного основания. Соединения формулы (I), содержащие кислые протоны, могут быть превращены в их терапевтически активные нетоксичные формы аддитивной соли металла или амина обработкой соответствующими органическими и неорганическими основаниями. Соответствующие формы солей основания включают,например, соли аммония, соли щелочных и щелочно-земельных металлов, например, соли лития, натрия,калия, магния, кальция и т.п., соли с органическими основаниями, например первичными, вторичными и третичными алифатическими и ароматическими основаниями, такими как метиламин, этиламин, пропиламин, изопропиламин, четыре изомера бутиламина, диметиламин, диэтиламин, диэтаноламин, дипропиламин, диизопропиламин, ди-н-бутиламин, пирролидин, пиперидин, морфолин, триметиламин, триэтиламин, трипропиламин, хинуклидин, пиридин, хинолин и изохинолин, бензатин, N-метил-Dглюкамин, 2-амино-2-(гидроксиметил)-1,3-пропандиол, гидрабамин, и соли с аминокислотами, такими как, например, аргинин, лизин и т.п. С другой стороны, солевую форму можно превратить обработкой кислотой в форму свободной кислоты. Термин "аддитивная соль" также включает гидраты и аддитивные формы растворителя, которые способны образовывать соединения формулы (I). Примерами таких форм являются гидраты, алкоголяты и т.п. Используемый ранее термин "кватернизованный (четвертичный) амин" означает соли кватернизованного амина, которые способны образовывать соединения формулы (I) путем взаимодействия основного азота соединения формулы (I) с соответствующим кватернизирующим агентом, таким как, например, необязательно замещенный алкилгалогенид, арилгалогенид или арилалкилгалогенид, например метилоидид или бензилоид. Могут быть также использованы другие реагенты с легко отщепляемыми группами, такие как алкилтрифторметансульфонаты, алкилметансульфонаты и алкил-п-толуолсульфонаты. Кватернизованный амин имеет положительно заряженный азот. Фармацевтически приемлемые противоионы включают хлор, бром, йод, трифторацетат и ацетат. Предпочтительный противоион может быть введен, используя ионообменные смолы (иониты). Подразумевается, что N-оксидные формы заявляемых соединений включают соединения формулы(I), в которых один или несколько третичных атомов азота окислены в так называемый N-оксид. Используемый ранее термин "стереохимически изомерные формы" охватывает все возможные стереоизомерные формы, которые могут иметь соединения формулы (I), и их N-оксиды, аддитивные соли,кватернизованные амины или физиологически функциональные производные. Если не оговорено иначе,химическое название соединений обозначает смесь всех возможных стереохимически изомерных форм,при этом указанные смеси включают в себя все диастереомеры и энантиомеры основной молекулярной структуры, а также каждую из индивидуальных изомерных форм формулы (I) и их N-оксидов, солей,сольватов или кватернизованных аминов, в основном свободную, т.е. ассоциированную меньше чем с-3 011300 10%, предпочтительно меньше чем 5%, в частности меньше чем 2% и наиболее предпочтительно меньше чем 1% других изомеров. В частности, стереогенные центры могут иметь R- или S-конфигурацию; заместители на бивалентных циклических (частично) насыщенных радикалах могут иметь цис- либо трансконфигурацию. Соединения, заключающие в себе двойные связи, могут иметь E- илиZ-стереохимию при указанной двойной связи. Подразумевается, что стереохимически изомерные формы соединений формулы (I) также не выходят за рамки объема данного изобретения. Некоторые из соединений формулы (I) могут также существовать в их таутомерных формах (например, кетоенольный таутомеризм). Подразумевается, что указанные формы, хотя они явно не указаны в вышеупомянутой формуле, входят в объем настоящего изобретения. Термин "соединения формулы (I)", всякий раз при использовании в дальнейшем, как подразумевается, также включает их N-оксидные формы, их соли, их кватернизованные амины и их стереохимически изомерные формы. Особый интерес представляют собой те соединения формулы (I), которые являются стереохимически чистыми. Первый вариант настоящего изобретения представляет собой соединения формулы (I), где кольцо A представляет собой фенил, пиридил, пиримидинил, пиридазинил или пиразинил;X1 представляет собой прямую связь: -(CH2)n3- или -(CH2)n4-X1a-X1b-; при этом n3 означает целое число, равное 1, 2, 3 или 4;X1b представляет собой прямую связь или C1-2 алкил;R2 представляет собой C3-7 циклоалкил; фенил или 4-, 5-, 6-или 7-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N; или радикал формулы где -B-C- представляет собой бивалентный радикал формулыn' означает целое число, равное 0 или 1; где указанный заместитель R2, где это возможно, может быть необязательно замещен по крайней мере одним заместителем, выбранным из галогена; гидрокси; C1-6 алкила, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси, циано, карбоксила, C1-4 алкилокси,C1-4 алкилкарбонила,C1-4 алкилоксикарбонила,C1-4 алкилкарбонилокси,NR6R7,-C(=O)-NR6R7,5 6 7 8 5 8-NR -C(=O)-NR R , -S(=O)n1-R или -NR -S(=O)n1-R ; C2-6 алкенила или C2-6 алкинила, каждый необязательно замещенный по крайней мере одним заместителем, выбранным из гидрокси, циано, карбоксила,C1-4 алкилокси,C1-4 алкилкарбонила,C1-4 алкилоксикарбонила,C1-4 алкилкарбонилокси,NR6R7,6 7 5 6 7 8 5 8X2 представляет собой прямую связь; -NR-1-; -O-; -C(=O)-; -C(=S)-; -S-; -S(-O)n1-; -(CH2)n3- илиR3 представляет собой 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, где указанный заместитель R3, где возможно, может быть необязательно замещен по крайней мере одним заместителем, выбранным из галогена; гидрокси;C1-6 алкила, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси,-4 011300 циано, карбоксила, C1-4 алкилокси, C1-4 алкилкарбонила, C1-4 алкилоксикарбонила, C1-4 алкилкарбонилокси,NR6R7, -C(=O)-NR6R7, -NR5-C(=O)-NR6R7, -S(=O)n1-R8 или -NR5-S(=O)n1-R8; C2-6 алкенила илиC2-6 алкинила, каждый необязательно замещенный по крайней мере одним заместителем, выбранным из гидрокси, циано, карбоксила, C1-4 алкилокси, C1-4 алкилкарбонила, C1-4 алкилоксикарбонила, C1-4 алкилкарбонилокси, NR6R7, -C(=O)-NR6R7, -NR5-C(=O)-NR6R7, -S(=O)n1-R8 или -NR5-S(=O)n1-R8; полигалогенC1-6 алкила; C1-6 алкилокси, необязательно замещенного карбоксилом; полигалогенC1-6 алкилокси; C1-6 алкилтио; полигалогенC1-6 алкилтио; C1-6 алкилоксикарбонила; C1-6 алкилкарбонилокси;-NR5-CN; или и в случае, когда R3 представляет собой насыщенный 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, указанный R3 может быть также замещен по крайней мере одной оксогруппой;R4 представляет собой водород; галоген; гидрокси; C1-4 алкил, необязательно замещенный по крайней мере одним заместителем, выбранным из гидрокси, циано, карбоксила, C1-4 алкилокси,C1-4 алкилкарбонила, C1-4 алкилоксикарбонила, C1-4 алкилкарбонилокси, NR9R10, -C(=O)-NR9R10,-NR5-C(=O)-NR9R10, -S(=O)n1-R11 или -NR5-S(=O)n1-R11; C2-4 алкенил или C2-4 алкинил, каждый необязательно замещенный по крайней мере одним заместителем, выбранным из гидрокси, циано, карбоксила,C1-4 алкилокси,C1-4 алкилкарбонила,C1-4 алкилоксикарбонила,C1-4 алкилкарбонилокси,NR9R10,9 10 5 9 10 11 5 11R5 представляет собой водород или C1-4 алкил;n1 означает целое число, равное 1 или 2; арил представляет собой фенил или фенил, замещенный по крайней мере одним заместителем, выбранным из галогена, C1-6 алкила, C3-7 циклоалкила, C1-6 алкилокси, циано, нитро, полигалогенC1-6 алкила или полигалогенC1-6 алкилокси. Вторым представляющим интерес вариантом настоящего изобретения являются соединения формулы (I), где кольцо A представляет собой фенил;R1 представляет собой водород или C1-6 алкил;X1 представляет собой прямую связь или -(CH2)n3-;R2 представляет собой C3-7 циклоалкил; фенил; 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N; бензоксазолил; или радикал формулы где -B-C- представляет собой бивалентный радикал формулыn означает целое число, равное 1; где указанный заместитель R2, где возможно, может быть необязательно замещен по крайней мере одним заместителем, в частности 1 или 2 заместителями, выбранными из галогена; C1-6 алкила, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси, циано, C1-4 алкилокси, C1-4 алкилоксиC1-4 алкилокси, NR6R7 или -C(=O)-NR6R7; полигалогенC1-6 алкила; C1-6 алкилокси, необязательно замещенного C1-4 алкилокси; C1-6 алкилтио; C1-6 алкилоксикарбонила; циано; арилтио; арилокси; арилкарбонила; NR6R7; -C(=O)-NR6R7; -S(=O)n1-R8 или имидазолила, необязательно замещенногоX2 представляет собой прямую связь; -NR1-; -O-(CH2)n3-; -C(=O)-; -C(=O)-NR5-(CH2)n3-; -(CH2)n3- илиR3 представляет собой 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, где указанный заместитель R3, где возможно, может быть необязательно замещен по крайней мере одним заместителем, выбранным из галогена; гидрокси;C1-6 алкила; NR6R7; и в случае, когда R3 представляет собой насыщенный или частично насыщенный 5 или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, указанный R3 может быть также замещен по крайней мере одной оксогруппой; в частности, R3 представляет собой имидазолил, оксазолил, тиазолил, пирролил, пиразолил, триазолил, тетразолил, морфолинил, пиридил, пиперидинил, пиримидинил, пиразинил или пиперазинил, где указанный заместитель R3, где возможно, может быть необязательно замещен по крайней мере одним заместителем,выбранным из галогена; гидрокси; C1-6 алкила или NR6R7; и в случае, когда R3 представляет собой насыщенный или частично насыщенный 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, указанный R3 может быть также замещен по крайней мере одной оксогруппой;n1 означает целое число, равное 2; арил представляет собой фенил. Третий представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где заместитель Х 2-R3 связан с кольцом A в мета-положении относительно линкера NR1. Четвертый представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где заместитель Х 2-R3 связан с кольцом A в пара-положении относительно линкера NR1. Пятый представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где заместитель R4 связан с кольцом A в пара-положении относительно линкераNR1. Шестой представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где заместитель -X1-R2 является незамещенным или замещен 1, 2 или 3 заместителями, в частности заместитель R2 является незамещенным или замещен 1 или 2 заместителями, и, в особенности, где заместитель -X1-R2 замещен 1 заместителем, и предпочтительно указанный заместитель расположен в мета- или пара-положении по сравнению со связью заместителя -X1-R2 с азотом части триазола триазолпиримидиновой циклической структуры. Седьмой представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где заместитель R3 является незамещенным или замещен 1, 2 или 3 заместителями, в частности заместитель R3 является незамещенным или замещен 1 заместителем. Восьмой представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где заместитель R3 является необязательно замещенным насыщенным 5 или 6-членным моноциклическим гетероциклом, содержащим по крайней мере один гетероатом, выбранный из O, S или N; более предпочтительно заместитель R3 представляет собой необязательно замещенный насыщенный 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N; наиболее предпочтительно заместитель R3 представляет собой пиперазинил. Девятый представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где R3 представляет собой 5- или 6-членный моноциклический гетероцикл,содержащий по крайней мере один гетероатом, выбранный из O, S или N, или 9- или 10-членный бициклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, где указанный заместитель R3, где возможно, может быть необязательно замещен по крайней мере одним заместителем, выбранным из галогена; гидрокси; C1-6 алкила, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси, циано, карбоксила, C1-4 алкилокси, C1-4 алкилоксиC1-4 алкилокси, C1-4 алкилкарбонила, C1-4 алкилоксикарбонила, C1-4 алкилкарбонилокси, NR6R7, -C(=O)-NR6R7,-NR5-C(=O)-NR6R7, -S(=O)n1-R8 или -NR5-S(=O)n1-R8; C2-6 алкенила или C2-6 алкинила, каждый необязательно замещенный по крайней мере одним заместителем, выбранным из гидрокси, циано, карбоксила,C1-4 алкилокси,C1-4 алкилкарбонила,C1-4 алкилоксикарбонила,C1-4 алкилкарбонилокси,NR6R7,6 7 5 6 7 8 5 8-C(=O)-NR R , -NR -C(=O)-NR R , -S(=O)n1-R или -NR -S(=O)n1-R ; полигалогенC1-6 алкила; C1-6 алкилокси, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси, циано,карбоксила, C1-4 алкилокси, C1-4 алкилкарбонила, C1-4 алкилоксикарбонила, C1-4 алкилкарбонилокси, NR6R7,-C(=O)-NR6R7, -NR5-C(=O)-NR6R7, -S(=O)n1-R8 или -NR5-S(=O)n1-R8; полигалогенC1-6 алкилокси;-NR -C(=O)-NR R ; -NR -C(=O)-R ; -S(=O)n1-R ; -NR -S(=O)n1-R ; -S-CN; -NR -CN; и в случае, когда R3 представляет собой насыщенный или частично насыщенный 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, указанный R3 может быть также замещен по крайней мере одной оксогруппой. Десятый представляющий интерес вариант настоящего изобретения представляет собой соединения формулы (I), где кольцо A представляет собой фенил;X1 представляет собой прямую связь или -(CH2)n3-;R2 представляет собой инданил; 2,3-дигидро-1,4-бензодиоксанил; фенил, необязательно замещенный 1 или 2 заместителями, каждый независимо выбранный из C1-6 алкила, который может быть необязательно замещен гидрокси, циано, C1-4 алкилокси, C1-4 алкилоксиC1-4 алкилокси, NR6R7 или -C(=O)-NR6R7,где указанный C1-6 алкил представляет собой предпочтительно метил; C1-6 алкилокси, в частности метокси; галоген, в частности фтор; полигалогенC1-6 алкил, в частности трифторметил; циано; NR6R7;R3 представляет собой тетразолил; пиперазинил; имидазолил; оксазолил; пиримидинил; тиазолил; триазолил; пиридил; пиперидинил; пиразинил; пиразолил; морфолинил; и эти указанные циклы, представляющие собой R3, могут быть необязательно замещены одним заместителем, выбранным изC1-6 алкила, в частности метила; NR6R7; гидрокси; галогена; и в случае, когда R3 представляет собой насыщенную или частично насыщенную циклическую структуру, указанный R3 может быть также замещен по крайней мере одной оксогруппой;R8 представляет собой NR6R7. Одиннадцатый представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где кольцо A представляет собой фенил;X1 представляет собой прямую связь или -(CH2)n3-;R2 представляет собой фенил, необязательно замещенный 1 или 2 заместителями, и этот каждый заместитель независимо выбран из C1-6 алкила, который может быть необязательно замещенным гидрокси или циано, где указанный C1-6 алкил представляет собой предпочтительно метил; галоген, в частности фтор; C(=O) NR6R7;X2 представляет собой прямую связь;R3 представляет собой тетразолил; имидазолил; оксазолил; пиримидинил; морфолинил; и эти указанные циклы, представляющие собой R3, могут быть необязательно замещенными одним заместителем,выбранным из C1-6 алкила, в частности метила; или NR6R7;R6 и R7, каждый независимо, представляют собой водород или C1-6 алкилкарбонил. Двенадцатый представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где кольцо A представляет собой фенил;X1 представляет собой прямую связь;R2 представляет собой 2,3-дигидро-1,4-бензодиоксанил или фенил, замещенный 1 заместителем,выбранным из галогена, в частности фтором; или C1-6 алкил, замещенный гидрокси, циано, C1-4 алкилокси,C1-4 алкилоксиC1-4 алкилокси или NR6R7; Х 2 представляет собой прямую связь; -NR1-; -O-(CH2)n3-; -C(=O)-; -C(=O)-NR5-(CH2)n3- или -(CH2)n3-;R3 представляет собой тетразолил; пиперазинил; имидазолил; оксазолил; пиримидинил; морфолинил или пиперидинил; и эти указанные циклы, представляющие собой R3, могут быть необязательно замещенными одним заместителем, выбранным из C1-6 алкила, в частности метилом; NR6R7; или гидрокси;R6 и R7, каждый независимо, представляют собой водород или C1-6 алкилкарбонил. Тринадцатый представляющий интерес вариант воплощения настоящего изобретения представляет собой такие соединения формулы A, где X1 представляет собой прямую связь. Четырнадцатый представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где R2 представляет собой фенил; 4-, 5-, 6- или 7-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N; бензок-7 011300 сазолил или радикал формулы где указанный R2 может быть необязательно замещенным, как определено выше. Пятнадцатый представляющий интерес вариант воплощения настоящего изобретения представляет собой соединения формулы (I), где R2 представляет собой C3-7 циклоалкил; фенил; 4-, 5-, 6-или 7-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N; бензоксазолил или радикал формулы (а-1), где указанный заместитель R2 является замещенным по крайней мере одним заместителем, выбранным из C1-6 алкила, замещенного NR6R7; C2-6 алкенила илиC2-6 алкинила, каждый замещенный NR6R7; полигалогенC1-6 алкила, замещенного NR6R7; C1-6 алкилокси,замещенного NR6R7; полигалогенC1-6 алкилокси, замещенного NR6R7; или NR6R7. Шестнадцатым представляющим интерес вариантом воплощения настоящего изобретения являются соединения формулы (I), где R2 представляет собой 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, или 9- или 10-членный бициклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, где указанный заместитель R3 является замещенным по крайней мере одним заместителем, выбранным изC1-6 алкилокси, замещенного NR6R7; или NR6R7. Семнадцатый представляющий интерес вариант воплощения настоящего изобретения представляет собой такие соединения формулы (I), где R2 представляет собой C3-7 циклоалкил; фенил; 4-, 5-, 6- или 7-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный изO, S или N; бензоксазолил или радикал формулы (а-1), где указанный заместитель R2 является замещенным по крайней мере одним заместителем, выбранным из C1-6 алкила, замещенного NR6R7; C2-6 алкенила или C2-6 алкинила, каждый замещенный NR6R7; полигалогенC1-6 алкила, замещенного NR6R7;C1-6 алкилокси, замещенного NR6R7; полигалогенC1-6 алкилокси, замещенного NR6R7; или NR6R7; и где R3 представляет собой 5- или 6-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, или 9- или 10-членный бициклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный из O, S или N, где указанный заместитель R3 является замещенным по крайней мере одним заместителем, выбранным из C1-6 алкила, замещенного NR6R7;NR6R7. Восемнадцатый представляющий интерес вариант воплощения настоящего изобретения представляет собой такие соединения формулы (I), где R1 представляет собой водород. Девятнадцатый представляющий интерес вариант воплощения настоящего изобретения представляет собой такие соединения формулы (I), где R2 представляет собой C3-7 циклоалкил; фенил; 4-, 5-, 6- или 7-членный моноциклический гетероцикл, содержащий по крайней мере один гетероатом, выбранный изO, S или N; бензоксазолил или радикал формулы (а-1), и этот указанный заместитель R2 является замещенным по крайней мере одним заместителем, выбранным из галогена, в частности по крайней мере одним атомом фтора; полигалогенC1-6 алкила, в частности C1-6 алкила, замещенного одним-тремя атомами фтора, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси, циано, карбоксила, C1-4 алкилокси, C1-4 алкилоксиC1-4 алкилокси, C1-4 алкилкарбонила, C1-4 алкилоксикарбонила, C1-4 алкилкарбонилокси, NR6R7, -C(=O)-NR6R7, -NR5-C(=O)-NR6R7, -S(=O)n1-R8 или-NR5-S(=O)n1-R8; полигалогенC1-6 алкилокси, в частности C1-6 алкилокси, замещенного одним-тремя атомами фтора, необязательно замещенного по крайней мере одним заместителем, выбранным из гидрокси,циано, карбоксила, C1-4 алкилокси, C1-4 алкилоксиC1-4 алкилокси, C1-4 алкилкарбонила, C1-4 алкилоксикарбонила, C1-4 алкилкарбонилокси, NR6R7, -C(=O)-NR6R7, -NR5-C(=O)-NR6R7, -S(=O)n1-R8 или-NR5-S(=O)n1-R8. Двадцатый представляющий интерес вариант воплощения настоящего изобретения представляет собой те соединения формулы (I), где X1-R2 представляет собой 3-фторфенил или 4-фторфенил. Предпочтительными соединениями формулы (I) являются соединения 17, 3, 24, 14, 65, 33, 22, 35, 9,23, 1, 32, 52, 30, 21, 2, 29, 26, 128, 151, 73, 145, 117, 115, 138, 76, 125, 84, 152, 86, 108, 112, 80, 94, 7, 31, 20,27, 28, 96, 97, 87, 85, перечисленные в табл. 1-5, их N-оксиды, фармацевтически приемлемые аддитивные соли, их кватернизованные амины и стереохимически изомерные формы. Более предпочтительными соединениями формулы (I) являются соединения 7, 31, 20, 27, 28, 96, 97,87, 85, перечисленные в табл. 1-5, их N-оксиды, фармацевтически приемлемые аддитивные соли, их кватернизованные амины и стереохимически изомерные формы. Наиболее предпочтительными соединениями формулы (I) являются соединения 36, 66, 28, 96, 115,138, 114, 84, 87, 88, 112, 78, 79, 80, 104, 106, 143, перечисленные в табл. 1-5, их N-оксиды, фармацевтически приемлемые аддитивные соли, их кватернизованные амины и стереохимически изомерные формы. Соединения формулы (I) могут быть получены циклизацией промежуточного соединения формулы Вышеприведенная реакция может быть также использована для получения соединений формулы(I), где R4 представляет собой либо водород, либо нитро, и эти указанные соединения, представляемые формулой (I-а) и (I-b), получают из промежуточного соединения формулы (II), где R4 представляет собой водород, и это указанное промежуточное соединение представлено формулой (II-а) Вышеприведенная реакция может быть также использована для получения соединения формулы (I),где R2 представляет собой фенильное кольцо, замещенное аминокарбонилом, и это указанное соединение, представленное формулой (I-c), получают из промежуточного соединения (II), в котором R2 представляет фенильное кольцо, замещенное частью имидазола, и это указанное промежуточное соединение представлено ниже формулой (II-b) Кроме того, соединения формулы (I) можно получить взаимодействием промежуточного соединения формулы (III) с промежуточным соединением формулы (IV) в присутствии подходящего растворителя, такого как, например, (CH3)2N-C(=O)H, диметилсульфоксид, CH3-O-CH2-CH2-OH, спирт, например 2-пропанол и т.п., необязательно в присутствии подходящего основания, такого как, например,N,N-диизопропилэтанамин, NaH или 2,6-диметилпиридин Соединения формулы (I) можно также получить взаимодействием промежуточного соединения(III') с промежуточным соединением формулы (IV) в присутствии подходящего растворителя, такого как,например, (CH3)2N-C(=O)H, диметилсульфоксид, CH3-O-CH2-CH2-OH, спирт, например 2-пропанол и т.п.,необязательно в присутствии подходящего основания,такого как,например,N,N-диизопропилэтанамин, NaH или 2,6-диметилпиридин В двух вышеприведенных реакциях полученное соединение формулы (I) может быть выделено и,при необходимости, очищено согласно методам, общеизвестным в данной области техники, таким как,например, экстракция, кристаллизация, дистилляция, растирание и хроматография. В случае, когда соединение формулы (I) кристаллизуется, его можно выделить фильтрованием. В противном случае кристаллизацию можно вызвать добавлением соответствующего растворителя, такого как, например, вода; ацетонитрил; спирт, такой как, например, метанол; и комбинаций указанных растворителей. Альтернативно, реакционную смесь можно также упарить досуха с последующей очисткой остатка методом хроматографии (например, ВЭЖХ с обращенной фазой, флэш-хроматография и т.п.). Реакционная смесь может быть также подвергнута очистке хроматографией без предварительного выпаривания растворителя. Кроме того, соединение формулы (I) можно выделить выпариванием растворителя с последующей перекристаллизацией в подходящем растворителе, таком как, например, вода; ацетонитрил; спирт, такой как, например, метанол; и комбинациях из указанных растворителей. Специалисту в данной области очевидно, какой метод должен быть использован, какой растворитель является наиболее подходящим для использования или это является результатом общепринятого (рутинного) экспериментирования с целью нахождения наиболее подходящего способа выделения. Соединения формулы (I), где Х 2-R3 представляет собой где Rb представляет собой водород, C1-4 алкил или циано и Rc представляет собой водород илиC1-4 алкил. Эти указанные соединения, представленные формулой (I-d), можно получить взаимодействием промежуточного соединения формулы (XV) с промежуточным соединением формулы (XVI) в присутствии подходящего растворителя, такого как, например, CH3-CH2-O-CH2-CH2-OH, и подходящей соли, такой как, например, метанолят натрия представленные формулой (I-е), можно получить взаимодействием промежуточного соединения формулы (XV) с гидразином в присутствии подходящего растворителя, такого как, например,CH3-CH2-O-CH2-CH2-OH В этом и нижеследующих получениях соединений продукты реакции могут быть выделены из реакционной среды и, если необходимо, дополнительно очищены методами, общеизвестными в данной- 10011300 области, такими как, например, экстракция, кристаллизация, дистилляция, растирание и хроматография. Кроме того, соединения формулы (I) можно получить путем превращения соединений формулы (I) друг в друга согласно известным в данной области реакциям трансформации групп. Соединения формулы (I) могут быть превращены в соответствующие N-оксидные формы, следуя общеизвестным способам превращения тривалентного азота в его N-оксидную форму. Указанная реакция N-окисления может быть, как правило, осуществлена взаимодействием исходного продукта формулы (I) с подходящим органическим или неорганическим пероксидом. Подходящие неорганические пероксиды включают, например, пероксид водорода, пероксиды щелочных или щелочно-земельных металлов, например пероксид натрия, пероксид калия; подходящие органические пероксиды могут включать пероксикислоты (надкислоты), такие как, например, бензолкарбопероксовая кислота или галогензамещенная бензолкарбопероксовая кислота, например 3-хлорпероксибензойная кислота, пероксиалкановые кислоты, например пероксиуксусная кислота, алкилгидропероксиды, например трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие спирты, например этанол и т.п.,углеводороды, например толуол, кетоны, например 2-бутанон, галогенированные углеводороды, например дихлорметан, и смеси из вышеуказанных растворителей. Соединения формулы (I), где R2 представляет собой циклическую систему, замещенную галогеном,например бромом, могут быть превращены в соединение формулы (I), где указанный заместитель R2 является незамещенным, в присутствии H2 и в присутствии подходящего катализатора, такого как, например, палладий на углероде, подходящего каталитического яда, такого как, например, раствор тиофена,подходящего основания, такого как, например, N,N-диэтилэтанамин, и подходящего растворителя, такого как, например, тетрагидрофуран. Соединения формулы (I), где R2 замещен галогеном, можно также превратить в соединение формулы (I), где R2 замещен C1-6 алкилтио, взаимодействием с реагентом формулы щелочной металл+N,N-диметилсульфоксид. Последние соединения могут быть далее превращены в соединение формулы(I), где R2 замещен C1-6 алкил-S(=O)-, реакцией с подходящим окислителем, таким как пероксид, например 3-хлорпероксибензойная кислота, в присутствии подходящего растворителя, такого как спирт, например этанол. Соединения формулы (I), где R3 и/или R2 замещен галогеном, могут быть превращены в соединение формулы (I), где R3 и/или R2 замещен C1-6 алкилокси, реакцией с алкоголятной солью, такой как, например, LiOC1-6 алкил, в присутствии подходящего растворителя, такого как спирт, например метанол. Соединения формулы (I), где R3 и/или R2 замещен галогеном, могут быть также превращены в соединение формулы (I), где R3 и/или R2 замещен гидрокси, реакцией с подходящим карбоксилатом, например ацетатом натрия, в подходящем инертном к протеканию реакции растворителе, таком как, например, N,N-диметилсульфоксид, с последующей обработкой полученного реакционного продукта подходящим основанием, таким как пиридин. Соединения формулы (I), где R3 и/или R2 замещен хлором,могут быть превращены в соединение формулы (I), где R3 и/или R2 замещен фтором, реакцией с подходящей фторидной солью, такой как, например, фторид калия, в присутствии подходящего растворителя,например сульфолан. Соединения формулы (I), где R3 и/или R2 замещен C1-4 алкилоксиC1-6 алкилом, могут быть превращены в соединение формулы (I), где R3 и/или R2 замещен гидроксиC1-6 алкилом, путем деалкилирования простого эфира в присутствии подходящего деалкилирующего агента, такого как, например, трибромборан, и подходящего растворителя, такого как метиленхлорид. Соединения формулы (I), где R3 и/или R2 замещен C1-6 алкилоксикарбонилом, могут быть превращены в соединение формулы (I), где R3 и/или R2 замещен аминокарбонилом или моно- или ди(C1-6 алкил)аминокарбонилом, реакцией с подходящим агентом, таким как аммиак, NH2(C1-6 алкил),AlCH3[N(C1-6 алкил)2]Cl, необязательно в присутствии подходящей кислоты, такой как, например, хлористо-водородная кислота, и в присутствии подходящего растворителя, такого как спирт, например метанол; тетрагидрофуран; N,N-диизопропилэтан. Соединения формулы (I), где R3 и/или R2 замещен C1-6 алкилоксикарбонилом, могут быть также превращены в соединение формулы (I), где R3 и/или R2 замещен карбоксилом, реакцией с подходящим основанием, таким как, например, гидроксид натрия, в присутствии подходящего растворителя, такого как, например, диоксан или N,N-диметилсульфоксид. Соединения формулы (I), где R2 является незамещенным, могут быть превращены в соединение, где 2R является замещенным галогеном, реакцией с подходящим галогенирующим агентом, таким как, например, Br2 или 1-(хлорметил)-4-фтор-1,4-диазониабицикло[2,2,2]октан-бис-[тетрафторборат], в присутствии подходящего растворителя, такого как тетрагидрофуран, вода, ацетонитрил, хлороформ, и необязательно в присутствии подходящего основания, такого как N,N-диэтилэтанамин. Соединения формулы (I), где R3 и/или R2 является замещенным C1-6 алкилоксикарбонилом, могут быть превращены в соединение формулы (I), где R3 и/или R2 замещен гидроксиметилом, путем реакции с подходящим восстановителем, таким как, например, LiAlH4.- 11011300 Соединения формулы (I), где R3 и/или R2 является замещенным NH2, могут быть превращены в соединение формулы (I), где R3 и/или R2 является замещенным NH-S(=O)2-NR6R7, путем реакции сW1-S(-O)2-NR6R7, где W1 представляет собой подходящую отщепляемую группу, такую как, например,атом галогена, например хлор, в присутствии подходящего растворителя, такого как, например,N,N-диметилацетамид, и подходящего основания, такого как, например, N,N-диэтилэтанамин. Соединения формулы (I), где R3 и/или R2 замещен NH-C(=O)-C1-6 алкилом, NH-C(=O)-O-C1-6 алкилом, C1-6 алкилом, замещенным NH-C(=O)-C1-6 алкилом или NH-C(=O)-O-C1-6 алкилом, могут быть превращены в соединение формулы (I), где R3 и/или R2 замещен NH2 или C1-6 алкилом, замещенным NH2,реакцией с подходящей кислотой, такой как, например, HCl, в присутствии подходящего растворителя,такого как, например, диоксан или спирт, например этанол, метоксиэтанол, 2-пропанол. Соединения формулы (I), где R3 и/или R2 является замещенным NH-S(=O)n1-R8, могут быть превращены в соединение формулы (I), где R3 и/или R2 является замещенным N(C2-4 алкенил)-S(=O)n1-R8, путем реакции с C2-4 алкенил-W1, где W1 представляет собой подходящую отщепляемую группу, такую как, например, галоген, например бром и т.п., в присутствии NaH и подходящего растворителя, такого как, например, N,N-диметилформамид. Соединения формулы (I), где R3 и/или R2 является замещенным NH2 или C1-6 алкилом, замещеннымNH2, могут быть превращены в соединение формулы (I), где R3 и/или R2 является замещенным N (CH2)2 или C1-6 алкилом, замещенным N(CH3)2, восстановительным алкилированием [-O-CH2-]n в присутствииH2, подходящего катализатора, такого как, например, палладий на углероде, подходящего каталитического яда, такого как, например, раствор тиофена, и подходящего растворителя, такого как, например, спирт,например метанол. Соединения формулы (I), где R1 представляет собой водород, могут быть превращены в соединение формулы (I), где R1 представляет собой этил, реакцией с N,N-диэтиламином в присутствии подходящего растворителя, такого как, например, N,N-диметилформамид. Соединения формулы (I), где R2 и/или R3 является замещенным C(=O)-C1-6 алкилом, могут быть превращены в соединение формулы (I), где R2 и/или R3 замещен C(=O)-N(CH3)2, путем реакции с N,N-диметилформамидом. Некоторые из соединений формулы (I) и некоторые из промежуточных соединений в настоящем изобретении могут состоять из смеси стереохимически изомерных форм. Чистые стереохимически изомерные формы указанных соединений и указанных промежуточных соединений можно получить посредством применения известных в данной области методов. Например, диастереоизомеры могут быть разделены физическими методами, такими как селективная кристаллизация, или хроматографическими методами, такими как, например, противоточное распределение, жидкостная хроматография и т.п. методы. Энантиомеры можно получить из рацемических смесей, сначала превращая указанные рацемические смеси с помощью подходящих разделяющих агентов, таких как, например, хиральные кислоты, в смеси диастереомерных солей или соединений; затем разделяя указанные смеси диастереомерных солей или соединений физическими методами путем, например, селективной кристаллизации или хроматографическими методами, например с помощью жидкостной хроматографии, и т.п. методами; и, наконец, превращая указанные разделенные диастереомерные соли или соединения в соответствующие энантиомеры. Кроме того, чистые стереохимически изомерные формы можно получить из чистых стереохимически изомерных форм подходящих промежуточных соединений и исходных продуктов при условии, что происходящие реакции протекают стереоспецифически. Альтернативный способ разделения энантиомерных форм соединений формулы (I) и промежуточных соединений включает жидкостную хроматографию, в частности жидкостную хроматографию с использованием хиральной стационарной (неподвижной) фазы. Некоторые из промежуточных соединений и исходных продуктов представляют собой известные соединения и могут быть коммерчески доступными или их можно получить в соответствии с известными в данной области способами. Промежуточные соединения формулы (II) можно получить путем восстановления промежуточного соединения формулы (V) подходящим восстановителем, таким как, например, Н 2, в присутствии подходящего катализатора, такого как, например, платина на углероде или палладий на углероде, необязательно в присутствии подходящего каталитического яда, такого как, например, раствор тиофена, необязательно в присутствии NH2-NH2, в присутствии подходящего растворителя, такого как, например,N,N-диметилацетамид, тетрагидрофуран, N,N-диметилформамид или подходящего спирта, такого как,например, метанол, этанол и т.п., и необязательно в присутствии подходящего основания, такого как,например, N,N-диэтилэтанамин Промежуточные соединения формулы (V) можно получить взаимодействием промежуточного соединения формулы (VI), где W1 представляет собой подходящую отщепляемую группу, такую как, например, галоген, например хлор и т.п., с промежуточным соединением формулы (VII) в присутствии подходящего растворителя, такого как, например, N,N-диметилацетамид или спирт, например этанол и т.п., и необязательно в присутствии основания, такого как, например, N,N-диизопропилэтанамин Промежуточные соединения формулы (V) могут быть получены взаимодействием промежуточного соединения формулы (VIII), где W2 представляет собой подходящую отщепляемую группу, такую как,например, галоген, например хлор и т.п., с промежуточным соединением формулы (IV) в присутствии подходящего основания, такого как, например, N,N-диизопропилэтанамин или N,N-диэтилэтанамин, и необязательно в присутствии подходящего растворителя, такого как, например, N,N-диметилацетамид,N,N-диметилформамид, 1,4-диоксан представляют собой один Промежуточные соединения формулы (V), где R2-X1-NH- и часть и тот же заместитель, который представлен формулой Ra-NH-, и эти указанные промежуточные соединения представлены ниже формулой (V-a), могут быть получены взаимодействием промежуточного соединения формулы (IX), где W2 такой, как определено выше, с Ra-NH2 в присутствии подходящего основания, такого как, например, N,N-диизопропилэтанамин, и подходящего растворителя, такого как, например, N,N-диметилацетамид, N,N-диметилформамид или CH2Cl2 Промежуточные соединения формулы (V) могут быть также получены взаимодействием промежуточного соединения формулы (IV) с промежуточным соединением формулы (VII) и промежуточным соединением формулы (IX) в присутствии подходящего растворителя, такого как, например,N,N-диметилформамид- 13011300 Промежуточные соединения формулы (VI), где W1 представляет собой хлор, и эти указанные промежуточные соединения представлены ниже формулой (VI-а), могут быть получены взаимодействием промежуточного соединения формулы (X) с POCl3 Промежуточные соединения формулы (X) могут быть получены взаимодействием промежуточного соединения формулы (IV) с промежуточным соединением формулы (XI), где W3 представляет собой подходящую отщепляемую группу, такую как, например, галоген, например, хлор, в присутствии подходящего растворителя, такого как, например, тетрагидрофуран и вода, или CH3-O-(CH2)2-OH, и необязательно в присутствии подходящего основания, такого как, например, N,N-диизопропилэтанамин Промежуточные соединения формулы (IV), где R1 представляет собой водород, и эти указанные промежуточные соединения представлены ниже формулой (IV-a), можно получить взаимодействием промежуточного соединения формулы (IV-b) с подходящим восстановителем, таким как, например, Н 2, в присутствии подходящего катализатора, такого как, например, платина на углероде или палладий на углероде, необязательно подходящего каталитического яда, такого как, например, раствор тиофена,подходящего растворителя, такого как, например, N,N-диметилацетамид, тетрагидрофуран,N,N-диметилформамид или подходящего спирта, такого как, например, метанол, и необязательно в присутствии подходящего основания, такого как, например, N,N-диэтилэтанамин Промежуточные соединения формулы (IV-b), где X2 представляет собой прямую связь и R3 представляет собой и эти указанные промежуточные соединения представлены ниже формулой (IV-b-1), могут быть получены взаимодействием промежуточного соединения формулы (IV-c) с CH3O-C(=O)-NH-NH2, в присутствии подходящего растворителя, такого как, например, спирт, например этанол и т.п., и подходящего алкоголята, такого как, например, этанолят натрия и т.п. Промежуточные соединения формулы (IV-b), где X2 представляет собой -S(=O)n1-NR5-(CH2)n3-, и эти промежуточные соединения представлены ниже формулой (IV-b-2), могут быть получены взаимодействием промежуточного соединения формулы (IV-d), где W3 такой, как определен выше, с промежуточным соединением формулы (XIX) в присутствии подходящего основания, такого как, например,NaHCO3, и подходящего растворителя, такого как, например, вода и спирт, например 2-пропанола и т.п. Промежуточные соединения формулы (IV), где X2 представляет собой NR1, и эти указанные промежуточные соединения представлены ниже формулой (IV-e), могут быть получены взаимодействием промежуточного соединения формулы (XX) с промежуточным соединением формулы (XXI), где W4 представляет собой подходящую отщепляемую группу, такую как, например, галоген, например хлор, в присутствии CaO и подходящего растворителя, такого как, например, тетрагидрофуран. Промежуточные соединения формулы (VIII) могут быть получены взаимодействием промежуточного соединения формулы (VII) с промежуточным соединением формулы (IX) в присутствии подходящего растворителя, такого как, например, N,N-диметилацетамид, N,N-диметилформамид, CH2Cl2 или 1,4-диоксан, и необязательно в присутствии подходящего основания, такого как, например,N,N-диизопропилэтанамин Промежуточные соединения формулы (VII) можно получить путем восстановления промежуточного соединения формулы (VII-a) в присутствии Fe и раствора хлорида аммония Промежуточные соединения формулы (III) могут быть получены взаимодействием промежуточного соединения формулы (XII) с подходящим окислителем, таким как, например, KMnO4, в присутствии подходящего растворителя, такого как, например, вода, и подходящей кислоты, такой как, например, уксусная кислота. Альтернативным подходящим окислителем является мета-хлорпербензойная кислота, в подходящем растворителе, таком как, например, CH2Cl2 и спирт, например метанол и т.п., необязательно в присутствии морфолинометилполистирол HL смолы и смолы бикарбоната (полистирилметил)триметиламмония Промежуточные соединения формулы (III), где R2 замещен C1-6 алкилом, замещенным NR6H, и эти указанные промежуточные соединения представлены ниже формулой (III-а), могут быть получены взаимодействием промежуточного соединения формулы (XII), где R2 замещен C1-6 алкилом, замещеннымNH2, и это указанное промежуточное соединение представлено ниже формулой (XII-а), с промежуточным соединением формулы (XXII), где W5 представляет собой подходящую отщепляемую группу, такую как, например, галоген, например хлор, в присутствии подходящего окислителя, такого как, например,мета-хлорпербензойная кислота, подходящего растворителя, такого как, например, CH2Cl2 и спирт, например метанол и т.п., необязательно в присутствии морфолинометилполистирол HL смолы и смолы бикарбоната (полистирилметил)триметиламмония Промежуточные соединения формулы (XII) можно получить взаимодействием промежуточного соединения формулы (XIII) с нитритной солью, такой как NaNO2, в присутствии подходящего растворителя, такого как, например, вода, и подходящей кислоты, такой как, например, 6 н. или 1 н. хлористоводородная кислота и/или уксусная кислота и т.п. Промежуточные соединения формулы (XII-а) могут быть получены взаимодействием промежуточного соединения формулы (XII-b) с подходящей кислотой, такой как, например, HCl и т.п., в присутствии подходящего растворителя, такого как, например, вода Промежуточные соединения формулы (XIII) могут быть получены взаимодействием промежуточного соединения формулы (XIV) с подходящим восстановителем, таким как, например, H2, в присутствии подходящего катализатора, такого как, например, платина на углероде или палладий на углероде,необязательно подходящего каталитического яда, такого как, например, раствор тиофена, подходящего растворителя, такого как, например, N,N-диметилацетамид, тетрагидрофуран, N,N-диметилформамид или подходящего спирта, такого как, например, метанол, и необязательно в присутствии подходящего основания, такого как, например, N,N-диэтилэтанамин Промежуточные соединения формулы (XIV) можно получить взаимодействием промежуточного соединения формулы (VIII) в присутствии NaS-CH3 в воде Промежуточные соединения формулы (XIV) можно также получить взаимодействием промежуточного соединения формулы (IX) с промежуточным соединением формулы (VII) в присутствии NaCH2SH и подходящего растворителя, такого как, например, N,N-диметилформамид Промежуточные соединения формулы (XV) могут быть получены взаимодействием промежуточного соединения формулы (XVII) с N,N-диметилформамидом (DMF) в присутствии подходящего основания, такого как, например, диэтиламин Промежуточные соединения формулы (XV), где R1 представляет собой этил, и эти указанные промежуточные соединения представлены ниже формулой (XV-a), могут быть получены взаимодействием промежуточного соединения формулы (XV), где R1 представляет собой водород, и это промежуточное соединение представлено ниже формулой (XV-b), в присутствии N,N-диэтилэтанамина, и подходящего растворителя, такого как, например, N,N-диметилформамид Промежуточные соединения формулы (XVII) можно получить взаимодействием промежуточного соединения формулы (III) с промежуточным соединением формулы (XVIII) в присутствии подходящего растворителя, такого как, например, диметилсульфоксид, CH3-O-CH2-CH2-OH или (CH3)2N-C(=O)H в присутствии NaH Промежуточные соединения формулы (III') могут быть получены путем циклизации промежуточного соединения формулы (XXIII) в присутствии нитритной соли, такой как, например, NaNO2, подходящей кислоты, такой как, например, хлористо-водородная кислота, например, 6 н. HCl или 1 н. HCl,и/или уксусная кислота и т.п., и необязательно в присутствии подходящего растворителя, такого как,например, вода Промежуточные соединения формулы (XXIII) могут быть получены взаимодействием промежуточного соединения формулы (XXIV) с подходящим восстановителем, таким как, например, H2, в присутствии подходящего катализатора, такого как, например, платина на углероде, в присутствии подходящего каталитического яда, такого как, например, раствор тиофена, в присутствии подходящего растворителя,такого как, например, N,N-диметилацетамид, тетрагидрофуран, N,N-диметилформамид, или подходяще- 17011300 го спирта, такого как, например, метанол, этанол и т.п., и в присутствии подходящего основания, такого как, например, N,N-диэтилэтанамин Промежуточные соединения формулы (XXIV) могут быть получены взаимодействием промежуточного соединения формулы (VII) с промежуточным соединением формулы (IX), где W2 представляет собой галоген, и это указанное промежуточное соединение представлено ниже формулой (IX-а), в присутствии подходящего растворителя, такого как, например, метиленхлорид, и подходящего основания,такого как, например, N,N-диметилбензоламин Соединения формулы (I) ингибируют киназу гликогенсинтазы-3 (GSK-3), в частности киназу гликогенсинтазы-3 (GSK-3) и/или киназу гликогенсинтазы-3 (GSK-3). Указанные соединения являются селективными ингибиторами киназы гликогенсинтазы-3. Конкретные ингибирующие соединения являются превосходными терапевтическими средствами, поскольку они характеризуются более высокой эффективностью и более низкой токсичностью благодаря своей селективности. Синонимами GSK-3 являются -протеинкиназа I (TPK I), FA (фактор A) киназа, киназа FA и киназаATP-цитрат-лиазы (ACLK). Киназа гликогенсинтазы-3 (GSK-3), которая существует в двух изоформах, как уже заявлено выше,т.е. GSK-3 и GSK-3, представляет собой пролиннаправленную серин/треониновую киназу, первоначально идентифицированную как фермент, который фосфорилирует гликогенсинтазу. Однако было показано, что GSK-3 фосфорилирует многие белки in vitro, такие как гликогенсинтаза, ингибитор 1-2 фосфатазы, субъединица типа-II cAMP-зависимой протеинкиназы, G-субъединица фосфатазы-1,ATP-цитрат-лиаза, ацетилкофермент A-карбоксилаза, основной миелиновый белок; белок, ассоциируемый с микроканальцами; белок нейрофиламента, акцепторная молекула клеток N-CAM, рецептор фактора роста нервов, фактор транскрипции c-Jun, фактор транскрипции JunD, фактор транскрипции c-Myb,фактор транскрипции с-Мус, фактор транскрипции L-Myc, супрессорный белок аденоматозной полипозной кишечной опухоли, -белок и -катенин. Вышеуказанное многообразие белков, которые могут быть фосфорилированы GSK-3, подразумевает участие GSK-3 в разнообразных метаболических и регуляторных процессах, происходящих в клетках. Поэтому ингибиторы GSK-3 могут быть использованы для предотвращения или лечения заболеваний, опосредованных через активность GSK-3, таких как диабет, болезнь Альцгеймера, боль, в частности нейропатическая боль. Ингибиторы GSK-3 могут быть также использованы для ингибирования подвижности сперматозоидов и поэтому могут быть использованы в качестве контрацептивов для мужчин. В частности, соединения по данному изобретению используют для профилактики или лечения болезни Альцгеймера; диабета, в основном диабета типа 2 (инсулиннезависимый диабет); биполярных расстройств; рака; боли, в особенности нейропатической боли; депрессии; воспалительных заболеваний. В особенности, соединения по данному изобретению являются полезными для профилактики или лечения диабета, в основном диабета типа 2 (инсулиннезависимого диабета); боли, особенно нейропатической боли; депрессии; воспалительных заболеваний. Основными нейропатологическими признаками болезни Альцгеймера являются потеря нейронов,отложение амилоидных волокон и конъюгированных спиралевидных филаментов (PHF) или нейрофибриллярных сплетений (NFT). Образование сплетений, по-видимому, является следствием накопления аномально фосфорилированного -белка. Это аномальное фосфорилирование дестабилизирует цитоскелет нейронов, что ведет к нарушению (снижению) аксонального транспорта, недостаточности функционирования и, в конечном счете, гибели нейронов. Как было показано, между плотностью нейрофибриллярных сплетений и длительностью и серьезностью заболевания Альцгеймера существует соответствие. Снижение степени -фосфорилирования может обусловливать нейрозащиту и может предотвратить развитие или способствовать лечению болезни Альцгеймера или может замедлить прогрессирование заболевания. Как было упомянуто выше, GSK-3 фосфорилирует -белок. Поэтому соединения, имеющие ингибирующую активность в отношении GSK-3, могут быть полезными для профилактики или лечения- 18011300 болезни Альцгеймера. Инсулин регулирует накопление полисахаридов и синтез гликогена. Стадия, лимитирующая скорость синтеза гликогена, катализируется ферментом, гликогенсинтазой. Считают, что гликогенсинтаза ингибируется фосфорилированием и что инсулин стимулирует гликогенсинтазу, вызывая тем самым снижение фосфорилирования этого фермента. Таким образом, чтобы активировать гликогенсинтазу, инсулин должен либо активировать фосфатазы, либо ингибировать киназы, либо и то и другое. Считают, что гликогенсинтаза является субстратом для киназы гликогенсинтазы-3 и что инсулин инактивирует GSK-3, способствуя тем самым дефосфорилированию гликогенсинтазы. Помимо роли GSK-3 в инсулин-индуцируемом синтезе гликогена, GSK-3 может также играть роль в инсулинорезистентности. Считают, что фосфорилирование GSK-3-зависимого инсулин-рецепторного субстрата-1 способствует инсулинорезистентности. Поэтому ингибирование GSK-3 может привести к увеличению депонирования гликогена и сопутствующему снижению уровня глюкозы в крови, имитируя тем самым гипогликемический эффект инсулина. Ингибирование GSK-3 обеспечивает альтернативную терапию, позволяющую регулировать инсулинорезистентность, обычно наблюдаемую при инсулиннезависимом сахарном диабете и ожирении. Ингибиторы GSK-3 могут таким образом обеспечить новый способ терапевтического воздействия на диабет типа 1 и типа 2. Ингибиторы GSK-3 могут быть также предназначены для использования для профилактики или лечения боли, в особенности нейропатической боли. После аксотомии или повреждения в результате хронического сдавливания нервные клетки (нейроны) погибают в результате апоптоза, и морфологические изменения коррелируют с началом гипералгезии и/или аллодинии. Индуцирование апоптоза, вероятно, инициировано снижением доставки нейротрофических факторов, поскольку временная потеря нейронов (период действия нейронной утраты) позитивно изменяется при введении нейротрофинов. GSK, как было показано, вовлечена в инициирование каскада апоптоза и изъятие трофических факторов стимулирует GSK-3 путь апоптоза. С учетом вышеизложенного ингибиторы GSK-3 могли бы ослабить сигналы или даже предотвратить уровни нейропатической боли. Благодаря своим ингибирующим свойствам в отношении GSK-3, соединения формулы (I), ихN-оксиды, фармацевтически приемлемые аддитивные соли, кватернизованные амины и их стереохимически изомерные формы являются полезными для предотвращения или лечения GSK-3-опосредованных заболеваний, таких как биполярное расстройство (в частности, маниакальная депрессия), диабет, болезнь Альцгеймера, лейко(цито)пения, FTDP-17 (лобно-височная деменция, ассоциируемая с болезнью Паркинсона), кортико-базальная дегенерация, прогрессирующий надъядерный паралич, множественная системная атрофия, болезнь Пика, болезнь Ниманна-Пика типа C, деменция Pugilistica, дименция, связанная с образованием только нейрофибриллярных сплетений; деменция, связанная с образованием нейрофибриллярных сплетений и кальцификацией; синдром Дауна, миотоническая дистрофия, комплекс Паркинсонизма-деменции Гуама, деменция, связанная с использованием вспомогательных средств (например,слухового аппарата); постэнцефалитический паркинсонизм; прионовые заболевания, связанные с образованием нейрофибриллярных сплетений; подострый склерозирующий панэнцефалит, дегенерация лобной доли (головного мозга) (FLD), аргирофильная гранулезная болезнь, подострый склеротизирующий панэнцефалит (SSPE) (позднее осложнение вирусных инфекций в центральной нервной системе), воспалительные заболевания, депрессия, рак, дерматологические расстройства, такие как алопеция, нейрозащита,шизофрения, боль, в особенности нейропатическая боль. Настоящие соединения также являются полезными в качестве контрацептивов для мужчин. В общем, соединения по данному изобретению могут быть использованы для лечения млекопитающих, страдающих заболеванием, опосредованным GSK-3, или они могут быть использованы для профилактической терапии млекопитающих с целью предотвращения заболевания, опосредованного GSK-3. В особенности соединения по данному изобретению могут быть использованы для лечения млекопитающих, страдающих болезнью Альцгеймера; диабетом, особенно диабетом типа 2; раком, воспалительными заболеваниями; биполярным расстройством; депрессией; болью, особенно страдающих нейропатической болью. Наиболее предпочтительно соединения по данному изобретению могут быть использованы для лечения млекопитающих, страдающих диабетом, в особенности диабетом типа 2; воспалительными заболеваниями; депрессией; болью, в особенности нейропатической болью. Принимая во внимание вышеописанные фармакологические свойства, соединения формулы (I) или их любая подгруппа, их N-оксиды, фармацевтически приемлемые аддитивные соли, их кватернизованные амины и стереохимически изомерные формы могут быть использованы в качестве лекарственного средства. В частности, предлагаемые соединения могут быть использованы для получения лекарственного средства для лечения или предотвращения заболеваний, опосредованных GSK-3. В особенности предлагаемые соединения могут быть использованы для получения лекарственного средства для лечения или профилактики возникновения болезни Альцгеймера; диабета, особенно диабета типа 2; рака; воспалительных заболеваний; биполярного расстройства; депрессии; боли, особенно нейропатической боли.- 19011300 Наиболее предпочтительно заявляемые соединения могут быть использованы для получения лекарственного средства для лечения или профилактики диабета, в особенности диабета типа 2; воспалительных заболеваний; депрессии; боли, в особенности нейропатической боли. Ввиду полезности соединений формулы (I) предлагается способ лечения млекопитающих, включая людей, страдающих заболеваниями, опосредованными GSK-3, или способ предотвращения у млекопитающих, включая людей, GSK-3-опосредованных заболеваний, в особенности способ лечения или профилактики болезни Альцгеймера; диабета, особенно диабета типа 2; рака; воспалительных заболеваний; биполярного расстройства; депрессии; боли, в частности нейропатической боли, наиболее предпочтительно диабета, в частности диабета типа 2; воспалительных заболеваний; депрессии; боли, в частности нейропатической боли. Указанный способ включает введение, предпочтительно пероральное введение,млекопитающим, включая людей, эффективного количества соединения формулы (I), его N-оксидной формы, фармацевтически приемлемой аддитивной соли, кватернизованного амина или его возможной стереохимически изомерной формы. Кроме того, настоящее изобретение предлагает композиции для профилактики или лечения заболеваний, опосредованных GSK-3, содержащие терапевтически эффективное количество соединения формулы (I), его N-оксида, его фармацевтически приемлемой аддитивной соли, его кватернизованного амина и стереохимически изомерной соли, и фармацевтически приемлемый носитель или разбавитель. Соединения по данному изобретению или любая их подгруппа могут быть формулированы в различные фармацевтические лекарственные формы, предназначенные для введения. В качестве подходящих композиций могут быть цитированы все типы композиций, обычно используемые для системного введения лекарственных средств. Для приготовления фармацевтических композиций по данному изобретению эффективное количество конкретного соединения, необязательно в форме аддитивной соли, в качестве активного компонента смешивают с фармацевтически приемлемым носителем с образованием однородной (гомогенной) смеси и этот носитель может принимать разнообразные формы в зависимости от формы препарата, требуемой для введения. Желательно, чтобы эти фармацевтические композиции находились в унитарной (единичной) лекарственной форме, подходящей, в частности, для введения пероральным ректальным, чрескожным путем или с помощью парентеральной инъекции. Например, для получения композиций в пероральной лекарственной форме может быть использована любая из обычных фармацевтических сред, например, таких как вода, гликоли, масла, спирты и т.п., в случае пероральных жидких препаратов, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, разбавители, смазки, связующие, дезинтегрирующие средства и т.п., в случае порошков, пилюль, капсул и таблеток. Из-за удобства при введении таблетки и капсулы представляют собой наиболее предпочтительные пероральные дозированные лекарственные формы,и в этом случае очевидно использование твердых фармацевтических носителей. Для парентеральных композиций носитель обычно включает стерильную воду, по крайней мере в значительной степени, хотя могут быть включены и другие компоненты, например, которые способствуют улучшению растворимости. Можно получить, например, инъецируемые растворы, в которых носитель включает физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Можно получить также инъецируемые суспензии и в этом случае могут быть использованы соответствующие жидкие носители, суспендирующие средства и т.п. Также включены препараты в твердой форме, которые, как предполагается, превращают, непосредственно перед применением, в препараты в жидкой форме. Для композиций, подходящих для чрескожного введения, носитель необязательно включает средство, усиливающее проникновение, и/или подходящее увлажняющее средство, необязательно комбинированное с подходящими вспомогательными веществами любой природы в незначительных пропорциях, которые не оказывают существенного вредного воздействия на кожу. Указанные вспомогательные вещества могут облегчать введение в кожу и/или могут быть полезными для приготовления желательных композиций. Вышеуказанные композиции могут вводиться различными способами, например в виде трансдермального пластыря, в виде нанесения пятна (капли), в виде мази. Соединения по данному изобретению можно также вводить путем ингаляции или инсуффляции посредством способов и препаратов, используемых в данной области для введения таким путем. Так, например, в общем, соединения по данному изобретению могут быть введены в легкие в форме раствора, суспензии или сухого порошка. Любая система, разработанная для доставки растворов, суспензий или сухих порошков путем пероральной или назальной ингаляции или инсуффляции, является пригодной для введения предлагаемых соединений. Особенно целесообразно составлять вышеупомянутые фармацевтические композиции в виде дозированной (разовой) лекарственной формы по причине легкости введения последней и достижения единообразия дозировки при ее использовании. Используемый здесь термин "дозированная лекарственная форма" относится к физически дискретным единицам, подходящим в качестве унитарных доз, при этом каждая единица содержит предварительно установленное количество активного компонента, обеспечивающее, исходя из расчета, проявление желаемого терапевтического действия в сочетании с требуемым фармацевтическим носителем. Примерами таких дозированных лекарственных форм являются таблетки(включая таблетки с насечкой или покрытые оболочкой таблетки), капсулы, пилюли, пакетики с порошком, облатки, суппозитории, инъецируемые растворы или суспензии и т.п. и их отдельные кратные еди- 20011300 ницы. Настоящие соединения представляют собой перорально активные соединения и их предпочтительно вводят оральным путем. Как хорошо известно специалистам в данной области, точная доза, терапевтически эффективное количество и частота введения препарата зависят от конкретно используемого соединения формулы (I); конкретного состояния, подлежащего лечению; серьезности состояния, подлежащего лечению; возраста,массы тела, пола, степени расстройства и общего физического состояния конкретного пациента, а также природы другого лекарственного средства, которое может принимать индивидуум. Кроме того, очевидно, что указанная эффективная суточная доза может быть снижена или увеличена в зависимости от реакции на нее лечимого субъекта и/или в зависимости от оценки лечащего врача, прописывающего прием соединений по данному изобретению. При использовании в качестве лекарственного средства для профилактики или лечения болезни Альцгеймера соединения формулы (I) могут быть использованы в комбинации с другими традиционными лекарственными средствами для борьбы с болезнью Альцгеймера, такими как галантамин, донепезил,ривастигмин или такрин. Поэтому настоящее изобретение также относится к комбинации соединения формулы (I) и другого средства, способного предотвращать или лечить болезнь Альцгеймера. Указанная комбинация может быть использована в качестве лекарственного средства. Настоящее изобретение также относится к продукту, содержащему (а) соединение формулы (I) и (b) другое средство, способное предотвращать или лечить болезнь Альцгеймера, как комбинированному препарату для одновременного,раздельного или последовательного применения для профилактики или лечения болезни Альцгеймера. Различные лекарственные средства могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями. При использовании в качестве лекарственного средства для профилактики или лечения диабета типа 2 соединения формулы (I) могут быть использованы в комбинации с другими традиционными лекарственными средствами для борьбы с диабетом типа 2, такими как глибенкламид, хлорпропамид, гликлазид, глипизид, глихидон, толбутамид, метформин, акарбоза, миглитол, натеглинид, репаглинид, ацетогексамид, глимепирид, глибурид, толазамид, троглитазон, розиглитазон, пиоглитазон, изаглитазон. Таким образом, настоящее изобретение также относится к комбинации соединения формулы (I) и другого средства, способного предотвращать или лечить диабет типа 2. Указанная комбинация может быть использована в качестве лекарственного средства. Настоящее изобретение также относится к продукту, содержащему (а) соединение формулы (I) и (b) другое средство, способное предотвращать или лечить диабет типа 2, как комбинированному препарату для одновременного, отдельного или последовательного применения для профилактики или лечения диабета типа 2. Различные лекарственные средства могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями. При использовании в качестве лекарственного средства для профилактики или лечения рака соединения формулы (I) могут быть использованы в комбинации с другими традиционными лекарственными средствами, используемыми для борьбы с раком, такими как координационные соединения платины,например цисплатин или карбоплатин; соединения таксана, например паклитаксел или доцетаксел; соединения камптотецина, например иринотекан или топотекан; противоопухолевые алкалоиды барвинка,например винбластин, винкристин или винорелбин; противоопухолевые нуклеозидные производные,например 5-фторурацил, гемцитабин или капецитабин; алкилирующие средства азотистых секретов или нитрозомочевины, например циклофосфамид, хлорамбуцил, кармустин или ломустин; противоопухолевые производные антрациклина, например даунорубицин, доксорубицин или идарубицин; антителаHER2, например трастзумаб; и противоопухолевые производные подофиллотоксина, например этопозид или тенипозид; и противоэстрогенные средства, включая антагонисты рецептора эстрогена и селективные модуляторы рецептора эстрогена, предпочтительно тамоксифен, или альтернативно торемифен, дролоксифен, фаслодекс и ралоксифен; ингибиторы ароматазы, такие как эксеместан, анастрозол, летразол и ворозол; дифференциирующие средства, например ретиноиды, витамин В и ингибиторы ДНКметилтрансфераз, например азацитидин; ингибиторы киназы, например флавоперидол и иматинибмезилат, или ингибиторы фарнезилтрансфераз, например R115777. Таким образом, настоящее изобретение также относится к комбинации соединения формулы (I) и другого средства, способного предотвращать или лечить рак. Указанная комбинация может быть использована в качестве лекарственного средства. Настоящее изобретение также относится к продукту, содержащему (а) соединение формулы (I) и (b) другое средство, способное предотвращать или лечить рак, как комбинированному препарату для одновременного, отдельного или последовательного применения для профилактики или лечения рака. Различные лекарственные средства могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями. При использовании в качестве лекарственного средства для профилактики или лечения биполярного расстройства соединения формулы (I) могут быть использованы в комбинации с другими традиционными лекарственными средствами для борьбы с биполярным расстройством, такими как нейролептики,атипичные антипсихотические средства, противоэпилептические средства, бензодиазепины, соли лития,например оланзапин, рисперидон, карбамазепин, валпроат, топирамат.- 21011300 Таким образом, настоящее изобретение также относится к комбинации соединения формулы (I) и другого средства, способного предотвращать или лечить биполярное расстройство. Указанная комбинация может быть использована в качестве лекарственного средства. Настоящее изобретение также относится к продукту, содержащему (а) соединение формулы (I) и (b) другое средство, способное предотвращать или лечить биполярное расстройство, как комбинированному препарату для одновременного, отдельного или последовательного применения для профилактики или лечения биполярного расстройства. Различные лекарственные средства могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями. При использовании в качестве лекарственного средства для профилактики или лечения воспалительных заболеваний соединения формулы (I) могут быть использованы в комбинации с другими традиционными лекарственными средствами, используемыми для борьбы с воспалительными заболеваниями,такими как стероиды, ингибиторы циклооксигеназы-2, нестероидные противовоспалительные лекарственные средства, антитела TNF-, такие как, например, ацетилсалициловая кислота, буфексамак, калийдиклофенак, сулиндак, натрий-диклофенак, кеторолак трометамол, толметин, ибупрофен, напроксен,натрий-напроксен, тиапрофен(овая) кислота, флурбипрофен, мефенамовая кислота, нифлуминовая кислота, меклофенамат, индометацин, проглуметацин, кетопрофен, набуметон, парацетамол, пироксикам,теноксикам, нимесулид, фенилбутазон, трамадол, беклометазон-дипропионат, бетаметазон, бекламетазон, будезонид, флутиказон, мометазон, дексаметазон, гидрокортизон, метилпреднизолон, преднизолон,преднизон, триамцинолон, целекоксиб, рофекоксиб, инфликсимаб, лефлуномид, этанерцепт, CPH 82,метотрексат, сульфасалазин. Таким образом, настоящее изобретение также относится к комбинации соединения формулы (I) и другого средства, способного предотвращать или лечить воспалительные заболевания. Указанная комбинация может быть использована в качестве лекарственного средства. Настоящее изобретение также относится к продукту, содержащему (а) соединение формулы (I) и (b) другое средство, способное предотвращать или лечить воспалительные заболевания, как комбинированному препарату для одновременного, отдельного или последовательного применения для профилактики или лечения воспалительных заболеваний. Различные лекарственные средства могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями. При использовании в качестве лекарственного средства для профилактики или лечения депрессии соединения формулы (I) могут быть использованы в комбинации с другими традиционными лекарственными средствами, используемыми для борьбы с депрессией, такими как ингибиторы обратного захвата норэлинефрина, селективные ингибиторы обратного захвата серотонина (SSRI), ингибиторы моноаминоксидазы (MAOI), обратимые ингибиторы моноаминоксидазы (RIMA), ингибиторы обратного захвата серотонина и норадреналина (SNRI), норадренергические и специфические серотонергические антидепрессанты (NaSSA), антагонисты кортикотропин высвобождающего фактора (CRF), антагонисты-адренорецептора и атипичные антидепрессанты. Подходящие примеры ингибиторов обратного захвата норэпинефрина включают амитриптилин,кломипрамин, доксепин, имипрамин, тримипрамин, амоксапин, дезипрамин, мапротилин, нортриптилин,протриптилин, ребоксетин и их фармацевтически приемлемые соли. Подходящие примеры селективных ингибиторов обратного захвата серотонина включают флуоксетин, флувоксамин, пароксетин, сертралин и их фармацевтически приемлемые соли. Подходящие примеры ингибиторов моноаминоксидазы включают изокарбоксазид, фенелзин, транилципромин, селегилин и их фармацевтически приемлемые соли. Подходящие примеры обратимых ингибиторов моноаминоксидазы включают моклобемид и его фармацевтически приемлемые соли. Подходящие примеры ингибиторов обратного захвата серотонина и норадреналина включают венлафаксин и его фармацевтически приемлемые соли. Подходящие атипичные антидепрессанты включают бупропион, литий, нефазодон, тразодон, вилоксазин, сибутрамин и их фармацевтически приемлемые соли. Другие подходящие антидепрессанты включают в себя адиназолам, алапроклат, аминптин, комбинацию амитриптилин/хлордиазепоксида, атипамезол, азамиансерин, базинаприн, бефуралин, бифемелан,бинодалин, бипенамол, брофаромин, бупропион, кароксазон, церикламин, цианопрамин, симоксатон,ситалопрам, клемепрол, кловоксамин, дазепинил, деанол, демексиптилин, дибензепин, дотиепин,дроксидопа, энефексин, эстазолам, этоперидон, фемоксетин, фенгабин, фезоламин, флуотрацен,идазоксан, индалпин, инделоксазин, иприндол, левопротилин, литоксетин, лофепрамин, медифоксамин,метапрамин, метралиндол, миансерин, милнаципран, минаприн, миртазапин, монирелин, небрацетам,нефопам, ниаламид, номифензин, норфлуоксетин, оротирелин, оксафлозан, пиназепам, пирлиндон,пизотилин, ритансерин, ролипрам, серклоремин, сетиптилин, сибутрамин, сулбутиамин, сулпирид,тенилоксазин, тозалинон, тимолиберин, тианептин, тифлукарбин, тофенацин, тофизопам, толоксатон,томоксетин, вералиприд, виквалин, цимелидин и зометапин и их фармацевтически приемлемые соли, и- 22011300 Таким образом, настоящее изобретение также относится к комбинации соединения формулы (I) и другого средства, способного предотвратить или лечить депрессию. Указанная комбинация может быть использована в качестве лекарственного средства. Настоящее изобретение также относится к продукту,содержащему (а) соединение формулы (I) и (b) другое средство, способное предотвращать или лечить депрессию, как комбинированному препарату для одновременного, отдельного или последовательного применения для профилактики или лечения депрессии. Различные лекарственные средства могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями. При использовании в качестве лекарственного средства для профилактики или лечения боли соединения формулы (I) могут быть использованы в комбинации с другими обычными лекарственными средствами, используемыми для борьбы с болью, такими как нестероидные противовоспалительные лекарственные средства (NSAIDS), аналгезирующие средства центрального действия. Подходящие нестероидные противовоспалительные лекарственные средства включают салицилаты, такие как, например, ацетилсалициловая кислота, этензамид, салициламид; производные парааминофенола, такие как, например, парацетамол, пропацетамол, фенидин; антранилаты, такие как, например, этофенамат, флуфенамовая кислота, меклофенамовая кислота,мефенамовая кислота, нифлумовая кислота; арилуксусные кислоты, такие как, например, ацеметацин,буфексамак, диклофенак, индометацин, лоназолак, сулиндак, толметин, набуметон; арилпропионовые кислоты, такие как, например, флурбипрофен, ибупрофен, кетопрофен, напроксен, тиапрофеновая кислота; производные пиразолинона, такие как, например, метамизол, пропифеназон; пиразолидин-3,5 дионы, такие как, например, кебузон, мофебутазон, оксифенбутазон, фенилбутазон; арилсульфонамиды, такие как, например, изоксикам, лорноксикам, пироксикам, теноксикам; кеторолак; оксапрозин; ингибиторы Cox-2, такие как, например, целекоксиб, этодолак, мелоксикам, нимесульфид, рофекоксиб. Подходящие аналгезирующие средства центрального действия включают агонисты опиоида, такие как, например, морфин и производные морфинана, например морфин, кодеин, этилморфин, диацетилморфин, дигидрокодеин, эторфин, гидрокодон, гидроморфон, леворфанол, оксикодон, оксиморфон; такие как, например, производные пиперидина, например петидин, кетобемидон, фентанил, альфентанил,ремифентанил, суфентанил; такие как, например, метадон и принадлежащие к такому же классу соединения, например левометадон, ацетат левометадона, декстроморамид, декстропропоксифен, дифеноксилат, лоперамид, пиритрамид; тилидин; трамадол; виминол. Подходящие аналгезирующие средства центрального действия включают смешанные опиоидные агонист-антагонисты и частичные агонисты, такие как, например, бупренорфин, буторфанол, дезоцин,мептазинол, налбуфин, налорфин, пентазоцин; антагонисты опиоида, такие как, например, леваллорфан,налоксон, налтрексон; соединения неопиоидной природы, такие как, например, карбамазепин, клонидин,флупиртин, нефопам. Таким образом, настоящее изобретение также относится к комбинации соединения формулы (I) и другого средства, способного предотвратить или лечить боль. Указанная комбинация может быть использована в качестве лекарственного средства. Настоящее изобретение также относится к продукту,содержащему (а) соединение формулы (I) и (b) другое средство, способное предотвращать или лечить боль, как комбинированному препарату для одновременного, отдельного или последовательного применения для профилактики или лечения боли. Различные лекарственные средства могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями. Нижеследующие примеры иллюстрируют настоящее изобретение. Экспериментальная часть В дальнейшем "DMF" обозначает N,N-диметилформамид, "DIPE" означает диизопропиловый эфир,"DMSO" означает диметилсульфоксид, "THF" означает тетрагидрофуран, "DMA" означаетa. Получение промежуточного соединения 1 Смесь 2,4-дихлор-5-нитропиримидина (0,05 моль) в DMA (400 мл) охлаждают до -20C и добавляют N-этил-N-(1-метилэтил)-2-пропанамин (0,05 моль), затем по каплям при -20C добавляют смесь 3-бромбензоламина (0,05 моль) в DMA (200 мл) и реакционную смесь перемешивают при -20C в течение 2 ч. Реакционную смесь используют, как таковую, на следующей стадии реакции.b. Получение промежуточного соединения 2NaSCH3, 21% в H2O (0,05 моль), добавляют по каплям к промежуточному соединению 1 (0,05 моль) и реакционную смесь перемешивают в течение 1,5 ч при комнатной температуре, затем смесь осторожно выливают в H2O. Полученный осадок перемешивают на протяжении выходных дней, отфильтровывают,промывают и сушат (вакуум), получая 15,73 г (92,5%). Продукт перекристаллизовывают из CH3CN, затем полученный осадок отфильтровывают, промывают и сушат (вакуум). Продукт перекристаллизовывают из CH3CN, затем полученный осадок отфильтровывают, промывают и сушат (вакуум), получая промежуточное соединение 2.c. Получение промежуточного соединения 3 Смесь промежуточного соединения 2 (0,028 моль) в CH3OH (250 мл) гидрируют с Pt/C 5% (2 г) в качестве катализатора в присутствии раствора тиофена в DIPE (4%, 1 мл). После поглощения H2 (3 экв.) катализатор отфильтровывают и фильтрат упаривают. Остаток кристаллизуют из CH3CN, затем полученный осадок отфильтровывают, промывают и сушат (вакуум). Выход: 5,2 г промежуточного соединения 3. Пример A1a. Получение промежуточного соединения 34 Смесь 2,4-дихлор-5-нитропиримидина (0,033 моль) в аналитически чистом DMF (100 мл) перемешивают в атмосфере N2 при -50C, затем по каплям добавляют раствор метилового эфира 3-аминобензойной кислоты (0,033 моль) в аналитически чистом DMF (30 мл) в течение 2 ч при температуре от -40 до -50C. Смеси дают возможность медленно нагреться до 0C и снова охлаждают до -40C. Добавляют по каплям NaSCH3 (21% в H2O) (0,066 моль) и реакционной смеси дают возможность медленно достичь комнатной температуры, затем смесь перемешивают в течение 1 ч при комнатной температуре. Добавляют смесь лед-вода (100 мл) и смесь перемешивают в течение 30 мин, затем полученный осадок отфильтровывают и сушат. Выход: 7,94 г промежуточного соединения 34 (75%). Пример 42.a. Получение промежуточного соединения 4(полученного согласно A1.b) (0,07 моль) и Et3N (10 г) в ТГФ (250 мл) гидрируют с Pd/C, 10% (5 г) в качестве катализатора в присутствии раствора тиофена в DIPE (4%, 5 мл). После поглощения H2 (3 экв.) катализатор отфильтровывают и фильтрат упаривают. Остаток перемешивают вDIPE с небольшим количеством CH3CN. Осадок отфильтровывают и сушат. Выход: 12,3 г промежуточного соединения 4 (70,2%). Фильтрат подкисляют смесью HCl/2-пропанол при перемешивании. Смесь перемешивают в течение 30 мин. Полученный осадок отфильтровывают и сушат. Выход: 5,17 г промежуточного соединения 4 (25,7%).b. Получение промежуточного соединения 5(400 мл) и содержимое охлаждают до 0-5C. По каплям добавляют раствор NaNO2 (0,1 моль) в H2O(40 мл) на протяжении периода времени 30 мин. Затем реакционную смесь перемешивают в течение еще 30 мин при охлаждении на бане со льдом. Затем реакционную смесь перемешивают на протяжении ночи при комнатной температуре. Полученный осадок отфильтровывают, промывают водой, 2-пропаноном,затем DIPE и сушат. Выход: 18,14 г промежуточного соединения 5 (87%). с-1. Получение промежуточного соединения 6 Промежуточное соединение 5 (15 г, 0,058 моль) перемешивают в HOAc (700 мл) и охлаждают на бане со льдом. По каплям добавляют раствор KMnO4, р.а. (24 г, 0,15 моль) в деминерализованной H2O(300 мл) на протяжении периода 60 мин при охлаждении на бане со льдом. Смесь перемешивают в течение 1 ч на бане со льдом, затем в течение 2 ч при комнатной температуре. Добавляют бисульфит натрия до изменения окраски реакционной смеси. Добавляют EtOAc (такое же количество), энергично перемешивая в течение некоторого времени. Смесь оставляют на ночь. Смесь концентрируют до объема 50 мл. Водный концентрат перемешивают некоторое время и полученный осадок отфильтровывают и сушат. Выход: 11,023 г промежуточного соединения 6 (64,8%). с-2. Получение промежуточного соединения 23 Смесь 3-хлорпероксибензойной кислоты (0,0125 моль, безводная) в CH2Cl2 (100 мл) сушат (MgSO4),фильтруют и фильтрат добавляют по каплям к раствору промежуточного соединения 22 (полученного согласно A2.b, структуру см. ниже) (0,0063 моль) в CH2Cl2 (100 мл), затем реакционную смесь перемешивают на протяжении ночи при комнатной температуре и промывают раствором NaHCO3/H2O. Органический слой отделяют, сушат (MgSO4), фильтруют и растворитель выпаривают. Остаток суспендируют в смеси DIPE/CH3CN, затем требуемый продукт отфильтровывают, промывают и сушат (вакуум). Выход: 1,9 г промежуточного соединения 23. с-3. Получение промежуточного соединения 25 Смесь промежуточного соединения 24(полученного согласно A2.b) (0,02 моль) в CH2Cl2, р.а. (250 мл) и метанола, р.а. (50 мл) перемешивают при комнатной температуре до полного растворения и затем порциями добавляют 3-хлорпероксибензойную кислоту (0,04 моль, 70%). Реакционную смесь перемешивают в течение 2 ч при комнатной температуре и добавляют дополнительно 3-хлорпероксибензойную кислоту (22,5 г, каждые 1/2 ч). Полученную смесь перемешивают на протяжении ночи при комнатной температуре и промывают расчетным количеством раствора NaHCO3/H2O. Органический слой отделяют, сушат (MgSO4), фильтруют и растворитель выпаривают. Остаток кристаллизуют из CH3CN, затем полученный осадок отфильтровывают и сушат. Фильтрат упаривают и остаток- 25011300 очищают флэш-колоночной хроматографией (элюент: смесь CH2Cl2/CH3OH 98/2). Фракции продукта собирают и растворитель выпаривают. Остаток перекристаллизовывают из CH3OH с небольшим количеством H2O, затем полученный осадок отфильтровывают и сушат. Выход: 1,984 г промежуточного соединения 25 (29%). с-4 а. Получение промежуточного соединения 27 Смесь промежуточного соединения 24 (полученного согласно A2.b) (0,020 моль) в 12 н. HCl, р.а.(100 мл) и H2O (деминерализованная) (200 мл) перемешивают и кипятят с обратным холодильником в течение 6 ч, затем реакционную смесь перемешивают на протяжении выходных дней при комнатной температуре. Полученный осадок отфильтровывают и сушат. Выход: 3,61 г промежуточного соединения 27 (58,5%, т.пл.:260C). с-4b. Получение промежуточного соединения 28 Смесь промежуточного соединения 27 (полученного согласно A2.c-4 а) (0,001 моль) и Et3N(0,0025 моль) в CH2Cl2, р.а. (15 мл) перемешивают при комнатной температуре и добавляют по каплям смесь метоксиацетилхлорида (0,0012 моль) в CH2Cl2, р.а. (1 мл), затем реакционную смесь перемешивают на протяжении ночи при комнатной температуре и промывают H2O. Органический слой отделяют,сушат, фильтруют и растворитель выпаривают. Остаток растворяют в CH2Cl2 (15 мл) и добавляют 3-хлорпероксибензойную кислоту (0,002 моль, 70%). Полученную смесь перемешивают в течение 2 ч при комнатной температуре и промывают раствором NaHCO3. Органический слой отделяют, сушат,фильтруют и растворитель выпаривают. Остаток перемешивают на протяжении ночи в DIPE и затем полученный осадок отфильтровывают и сушат. Выход: 0,392 г промежуточного соединения 28 (100%). с-5. Получение промежуточного соединения 32 Смесь промежуточного соединения 31CH2Cl2 (80 мл) и метанола (20 мл) перемешивают при комнатной температуре и порциями добавляют 3-хлорпероксибензойную кислоту (0,024 моль). Реакционную смесь перемешивают в течение 3 ч при комнатной температуре, затем добавляют смесь NaHCO3 (0,025 моль) в H2O и полученную смесь решительно перемешивают. После прекращения образования газа слои разделяют. Органический слой сушат(MgSO4), фильтруют и растворитель выпаривают. Остаток перемешивают в DIPE с небольшим количеством CH3CN, затем осадок отфильтровывают и сушат. Выход: 1,218 г промежуточного соединения 32 (39%). с-6. Получение промежуточного соединения 40 Смесь промежуточного соединения 27 (полученного согласно A2.c-4 а) (0,005 моль) в CH2Cl2(50 мл) перемешивают при комнатной температуре и добавляют морфолинометилполистирол HL смолу(загрузка: 4 ммоль/г; 200-400 меш; 0,020 моль Novabiochem), затем по каплям при комнатной температуре добавляют смесь этилового эфира хлоркарбоновой кислоты (0,006 моль) в CH2Cl2 (20 мл) и реакционную смесь перемешивают на протяжении выходных дней при комнатной температуре. Смесь фильтруют через стеклянный фильтр и поглотитель промывают смесью CH2Cl2/CH3OH (30 мл; 80/20). К фильтрату добавляют 3-хлорпероксибензойную кислоту (0,015 моль; 70%) и полученную смесь перемешивают на(0,045 моль; загрузка: 3,7 ммоль/г; 20-50 меш; Novabiochem) и реакционную смесь перемешивают на протяжении ночи при комнатной температуре. Поглотитель отфильтровывают и фильтрат упаривают,получая промежуточное соединение 40.d. Получение промежуточного соединения 6 а Смесь промежуточного соединения 6 (0,001 моль) и 1-(3-аминофенил)этанона (0,002 моль) в 2-метоксиэтаноле (10 мл) перемешивают и кипятят с обратным холодильником в течение 16 ч и раствор охлаждают. Полученный осадок отфильтровывают, промывают смесью EtOH/DIPE и сушат. Выход: 0,250 г промежуточного соединения 6 а (72%, т.пл.: 220-224C). Фильтрат упаривают и остаток перемешивают в смеси CH3CN/CH3OH (2 мл/2 мл). Смесь перемешивают некоторое время, затем осадок отфильтровывают и сушат. Выход: 0,098 г промежуточного соединения 6 а (28%). е-1. Получение промежуточного соединения 6b К суспензии промежуточного соединения 6 а (0,00135 моль, 1 экв.) в DMF (3 мл) добавляют смесьDMF/DMA (0,00675 моль, 5 экв.) и реакционную смесь нагревают при 115C в течение 2 ч, затем перемешивают на протяжении ночи при комнатной температуре. Полученный осадок отфильтровывают и остаток растирают с диэтиловым эфиром на воронке. Выход: 0,38 г промежуточного соединения 6b (70%; т.пл.: 240-244C). е-2. Получение промежуточного соединения 6b и промежуточного соединения 6 с Промежуточное соединение 6 с Смесь промежуточного соединения 6 а (0,0056 моль, 1 экв.) в беспримесной смеси DMF/диэтиламин(6 мл) нагревают на протяжении ночи при 110-120C, затем EtOH дистиллируют и добавляют дополнительно смесь DMF/диэтиламин (2 мл). Полученную суспензию нагревают при 120-130C в течение 5 ч,затем добавляют DMF (2 мл) и дополнительно смесь DMF/диэтиламин (1 мл). Реакционную смесь нагревают при 140C в течение 2 ч, добавляют дополнительно DMF (1 мл) и продолжают нагревание. Полученный раствор перемешивают и кипятят с обратным холодильником в течение 1 ч и затем перемешивают при комнатной температуре на протяжении ночи. Полученный осадок отфильтровывают и растирают на воронке с Et2O и гексаном. Выход 0,38 г промежуточного соединения 6b (17%, т.пл.: 235-236C). Маточный слой концентрируют и остаток собирают. Выход: 1,12 г промежуточного соединения 6 с (50%, т.пл.: 176-179C). Пример A3 а. Получение промежуточного соединения 7NaOEt (0,1 г) и реакционную смесь перемешивают на протяжении ночи. Добавляют одной порцией метиловый эфир гидразинкарбоновой кислоты (0,36 моль) и реакционную смесь перемешивают и кипятят с обратным холодильником на протяжении ночи. Реакционную смесь концентрируют и вновь растворяют в DMF (150 мл) и нагревают при 140C на протяжении выходных дней. Реакционную смесь концентрируют (вакуум) и остаток суспендируют в H2O (500 мл) и фильтруют. Полученный остаток снова суспендируют в смеси H2O/EtOH (2000 мл) и эту суспензию нагревают при температуре кипения с обратным холодильником на протяжении ночи. Горячий раствор фильтруют в охлаждаемую льдом колбу Эрленмейера и раствор перемешивают в течение 2 ч. Осадок фильтруют и сушат в вакуумном сушильном шкафу (60C). Выход: 11,84 г промежуточного соединения 7 (45,9%).b. Получение промежуточного соединения 8 Смесь промежуточного соединения 7 (10 г; 0,048 моль) в MeOH (150 мл) и THF (100 мл) гидрируют при 50C с Pd/C 10% (1 г) в качестве катализатора в присутствии раствора тиофена в DIPE (4%, 1 мл). После поглощения H2 (3 экв.), катализатор отфильтровывают и фильтрат концентрируют. Эту фракцию суспендируют в ацетоне, фильтруют и сушат (вакуум 60C). Выход: 7,06 г промежуточного соединения 8 (83,5%). 4-(3-Аминофенил)пиримидин-2-иламин получают аналогичным способом. Раствор 4-(3-нитрофенил)пиримидин-2-иламина (0,046 моль) в MeOH (250 мл) гидрируют при 50C с Pd/C 10% (2 г) в качестве катализатора в присутствии раствора тиофена в DIPE (4% об./об., 1 мл). После поглощения H2 (3 экв.), катализатор отфильтровывают и фильтрат концентрируют и сушат (вакуум 60C). Выход: 8,64 г 4-(3-аминофенил)пиримидин-2-иламина (87%, т.пл.: 190-194C). Пример A4. а. Получение промежуточного соединения 9 Смесь натриевой соли 2-хлор-5-нитро-4(1H)-пиримидинона (0,051 моль), 3-(1-метил-1 Н-имидазол 2-ил)бензоламина (0,056 моль) и N-этил-N-(1-метилэтил)-2-пропанамина (0,168 моль) в H2O (200 мл) иTHF (100 мл) перемешивают и кипятят с обратным холодильником в течение 1 дня, затем реакционную смесь охлаждают до комнатной температуры и растворитель выпаривают при пониженном давлении. Остаток перемешивают в CH3OH и полученный осадок отфильтровывают, промывают CH3OH и затем сушат (вакуум). Выход: 13,6 г промежуточного соединения 9 (85%).b. Получение промежуточного соединения 10 Суспензию промежуточного соединения 9 (0,0256 моль) в смеси 6 н. HCl/2-пропанол перемешивают при комнатной температуре в течение 1 ч и затем растворитель выпаривают при пониженном давлении. К остатку добавляют POCl3 (100 мл) и реакционную смесь перемешивают и кипятят с обратным холодильником в течение 1 ч, затем перемешивают при комнатной температуре в течение 1 ч. Растворитель выпаривают при пониженном давлении и затем совместно выпаривают с толуолом. Количественный выход промежуточного соединения 10.- 28011300 с. Получение промежуточного соединения 11 Смесь промежуточного соединения 10 (0,000502 моль), 4-метоксибензоламина (0,000624 моль) иN-этил-N-(1-метилэтил)-2-пропанамина (0,000624 моль) в DMA (5 мл) перемешивают при 100C в течение 1 ч и реакционную смесь используют, как таковую, на следующей стадии реакции.d. Получение промежуточного соединения 12 Смесь промежуточного соединения 11 (0,000502 моль) в DMA (достаточное количество) гидрируют на протяжении ночи с Pt/C (каталитическое количество) в качестве катализатора. После поглощения H2(3 экв.) катализатор отфильтровывают и фильтрат упаривают. Выход: промежуточное соединение 12. Пример A5. а. Получение промежуточного соединения 13 Раствор циклогексанамина (0,062 моль) в DMA (20 мл) добавляют по каплям к охлаждаемому(8,1 г) в DMA (80 мл), затем реакционной смеси дают возможность достичь комнатной температуры на протяжении ночи. Выход: промежуточное соединение 13, используемое как таковое на следующей стадии реакции.b. Получение промежуточного соединения 14(0,0257 моль), получая смесь (I). Смесь 4-(4-морфолинил)бензоламина (0,0257 моль) в DMA (25 мл, р.а.) добавляют по каплям при 80C к смеси (I) и реакционную смесь перемешивают на протяжении ночи,затем выливают в смесь лед-вода (500 мл). Полученное твердое вещество отфильтровывают и сушат в вакуумном сушильном шкафу при 75C. Эту фракцию нагревают при температуре образования флегмы в смеси 2-пропанол/2-пропанол (6 н. HCl) и охлаждают, затем продукт отфильтровывают и сушат. Выход: 9,6 г промежуточного соединения 14.- 29011300 Пример A5 а. а. Получение промежуточного соединения 41 Смесь 2,4-дихлор-5-нитропиримидина (5 ммоль) в CH2Cl2 (20 мл) перемешивают при -(30-40)C. Альтернативно перемешивают раствор 3-(5-оксазолил)бензоламина (5 ммоль) в CH2Cl2 (10 мл) и добавляют по каплям раствор N,N-диэтилбензоламина (5 ммоль) в CH2Cl2 (10 мл) на протяжении периода 1 ч с последующим перемешиванием в течение 2 ч при -(20-30)C. Смеси дают возможность достичь комнатной температуры при перемешивании. Смесь разбавляют 50 мл CH2Cl2 и добавляют 50 мл ледяной воды. Осадок отфильтровывают и сушат. Выход: 490 мг промежуточного соединения 41. Слои фильтрата разделяют и органический слой сушат, фильтруют и упаривают. Остаток перемешивают в CH3CN. Осадок отфильтровывают и сушат. Выход: 305 мг промежуточного соединения 41.b. Получение промежуточного соединения 42 Смесь промежуточного соединения 41 (1 ммоль) в THF (50 мл) гидрируют с Pt/C 5% (0,2 г) в качестве катализатора в присутствии раствора тиофена в DIPE (4% об./об., 0,5 мл) и в присутствии триэтиламина (эквимолярное). После поглощения H2 катализатор отфильтровывают и фильтрат упаривают. Выход: 300 мг промежуточного соединения 42. с. Получение промежуточного соединения 43 Смесь промежуточного соединения 42 (полученного согласно A2b.b) (0,001 моль) и 1 н. HCl(0,002 моль) в уксусной кислоте (20 мл) перемешивают при комнатной температуре, затем по каплям добавляют смесь NaNO2 (0,001 моль) в H2O (2 мл) и реакционную смесь перемешивают на протяжении ночи при комнатной температуре. Растворитель выпаривают и остаток перемешивают в CH3CN. Полученный осадок отфильтровывают и сушат. Выход: 0,190 г промежуточного соединения 43. Пример A6. а. Получение промежуточного соединения 15 Смесь промежуточного соединения 13 (полученного согласно A5.а) (0,031 моль), гидрохлорида 4(4-метил-1-пиперазинил)бензоламина (0,031 моль) и N-этил-N-(1-метилэтил)-2-пропанамина (10 г) нагревают при 60C в течение 3 ч, затем реакционную смесь охлаждают и по каплям добавляют к H2O
МПК / Метки
МПК: C07D 487/00
Метки: производные, гликогенсинтазы-3, киназы, ингибиторов, триазолопиримидина, качестве
Код ссылки
<a href="https://eas.patents.su/30-11300-proizvodnye-triazolopirimidina-v-kachestve-ingibitorov-kinazy-glikogensintazy-3.html" rel="bookmark" title="База патентов Евразийского Союза">Производные триазолопиримидина в качестве ингибиторов киназы гликогенсинтазы-3</a>
Предыдущий патент: Способы образования дисульфидных связей и гликозилирования белков и реагенты, применяемые в этих способах
Следующий патент: Применение галоидного производного гидроксимовой кислоты для лечения нейродегенеративных заболеваний
Случайный патент: Передвижное устройство для укладки под водой линии трубопровода или связи в траншею (варианты) и способ укладки под водой линии трубопровода или связи в траншею












