Замещенные амины (варианты), способ их получения и их применение в качестве ингибиторов транспорта глицина (варианты), композиция (варианты), промежуточный иодид и способ его получения, способ леченияпациента (варианты)
Номер патента: 6636
Опубликовано: 24.02.2006
Авторы: Дилейни Уильям, Игл Иэн, Шумахер Ричард, Ван Чжаоцин, Техим Ашок, Мэддейфорд Шон, Хоппер Аллан Т.
Формула / Реферат
1. Замещенные амины общей формулы I
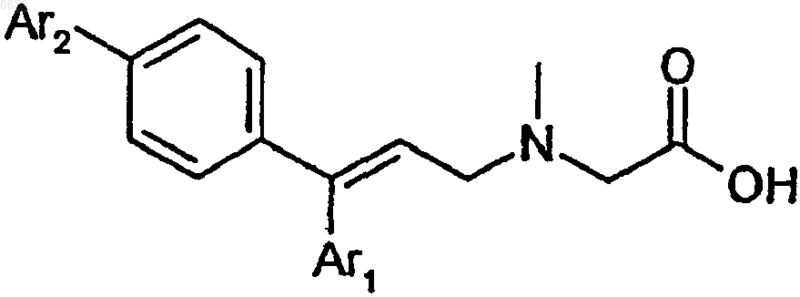
где Ar1 означает тиофеновую группу, выбранную из остатков 2- или 3-тиофена, необязательно содержащую один заместитель, выбранный из метила или этила, и
Ar2 выбран из группы, содержащей тиофен, фуран и замещенный фенил, причем заместитель фенильной группы выбран из ряда C1-6алкил, галоген, C1-6галогеналкил, C1-6алкокси, C1-6галогеналкокси, циано;
и его соли, сольваты и гидраты,
или Ar1 означает 2-метилфенил, а Ar2 означает 3-тиенил.
2. Соединение по п.1, где Ar1 означает 2-тиофен.
3. Соединение по п.1, где Ar1 означает 2-(3-метилтиофен).
4. Соединение по п.1, где Ar1 означает 3-тиофен.
5. Соединение по п.1, где Ar1 означает 3-(4-метилтиофен).
6. Соединение по п.1, где Ar2 означает замещенный фенил, в котором заместитель выбран из ряда CF3, Me, iPr, MeO, CN и CF3O.
7. Соединение по п.1, где Ar2 означает фуран.
8. Соединение по п.1, где Ar2 означает тиофен.
9. Соединение по п.1, выбранное из группы, содержащей
(Z)-N-(1-(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(3-тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(2-тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(2-фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(3-метоксифенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(3-метилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(3-(трифторметокси)фенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(3-цианофенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(3-тиенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(3-трифторметил)фенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин,
(Z)-N-(1-(4-(3-метоксифенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин и
(Z)-N-(1-(4-(3-метилфенил)фенил)-1-(3-метил-2-тиенил)проп-1-ен-3-ил)саркозин.
10. Соединение по п.9, представляющее собой
(Z)-N-(1-(4-(2-фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин.
11. Соединение по п.9, представляющее собой
(Z)-N-(1-(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин.
12. Соединение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозин.
13. Композиция, отличающаяся тем, что она содержит соединение по п.1 и носитель.
14. Композиция, отличающаяся тем, что она содержит соединение по п.10 и носитель.
15. Композиция, отличающаяся тем, что она содержит соединение по п.11 и носитель.
16. Композиция, отличающаяся тем, что она содержит соединение по п.12 и носитель.
17. Фармацевтическая композиция, отличающаяся тем, что она содержит терапевтически эффективное количество соединения по п.1 и фармацевтически приемлемый носитель.
18. Фармацевтическая композиция, отличающаяся тем, что она содержит терапевтически эффективное количество соединения по п.10 и фармацевтически приемлемый носитель.
19. Фармацевтическая композиция, отличающаяся тем, что она содержит терапевтически эффективное количество соединения по п.11 и фармацевтически приемлемый носитель.
20. Фармацевтическая композиция, отличающаяся тем, что она содержит терапевтически эффективное количество соединения по п.12 и фармацевтически приемлемый носитель.
21. Способ лечения пациента в патологическом состоянии, при котором назначают ингибиторы транспорта глицина, отличающийся тем, что пациенту вводят фармацевтическую композицию по п.17.
22. Способ по п.21, отличающийся тем, что патологическим состоянием является шизофрения.
23. Способ по п.21, отличающийся тем, что патологическим состоянием является дисфункция познавательных способностей.
24. Способ по п.21, отличающийся тем, что патологическим состоянием является болезнь Альцгеймера.
25. Способ лечения пациента в патологическом состоянии, при котором назначают ингибиторы транспорта глицина, отличающийся тем, что пациенту вводят фармацевтическую композицию по п.18.
26. Способ по п.25, отличающийся тем, что патологическим состоянием является шизофрения.
27. Способ по п.25, отличающийся тем, что патологическим состоянием является дисфункция познавательных способностей.
28. Способ по п.25, отличающийся тем, что патологическим состоянием является болезнь Альцгеймера.
29. Способ лечения пациента в патологическом состоянии, при котором назначают ингибиторы транспорта глицина, отличающийся тем, что пациенту вводят фармацевтическую композицию по п.19.
30. Способ по п.29, отличающийся тем, что патологическим состоянием является шизофрения.
31. Способ по п.29, отличающийся тем, что патологическим состоянием является дисфункция познавательных способностей.
32. Способ по п.29, отличающийся тем, что патологическим состоянием является болезнь Альцгеймера.
33. Способ лечения пациента в патологическом состоянии, при котором назначают ингибиторы транспорта глицина, отличающийся тем, что пациенту вводят фармацевтическую композицию по п.20.
34. Способ по п.33, отличающийся тем, что патологическим состоянием является шизофрения.
35. Способ по п.33, отличающийся тем, что патологическим состоянием является дисфункция познавательных способностей.
36. Способ по п.33, отличающийся тем, что патологическим состоянием является болезнь Альцгеймера.
37. Применение замещенных аминов общей формулы I
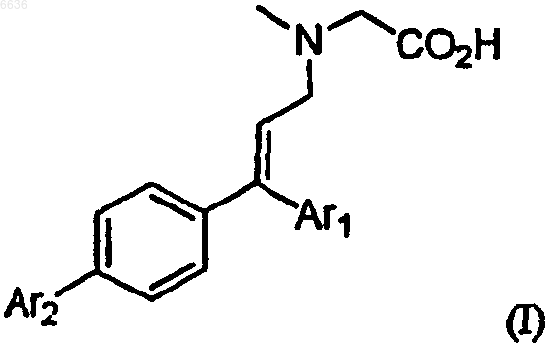
где Ar1 означает группу тиенила, необязательно содержащую один заместитель, выбранный из метила или этила, и
Ar2 выбран из группы, содержащей тиенил, фурил и замещенный фенил, где заместители фенильной группы выбраны из ряда C1-6алкил, галоген, C1-6галогеналкил, C1-6алкокси, C1-6галогеналкокси, циано,
в качестве ингибитора транспорта глицина для лечения пациента в патологическом состоянии, при котором требуется назначение ингибиторов транспорта глицина.
38. Применение по п.37 для лечения пациента в патологическом состоянии при заболеваниях, выбранных из следующей группы: шизофрения, дисфункция познавательных способностей, деменция, в частности болезнь Альцгеймера, нарушение функции внимания, депрессия, аутизм, нарушение Ретта, детская дезинтеграция, нарушение Аспергера и атипичный аутизм.
39. Применение по п.38, в котором патологическим состоянием является шизофрения.
40. Применение по п.38, где замещенный амин представлен (Z)-N-(1-(4-(2-фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозином.
41. Применение по п.39, где замещенный амин представлен (Z)-N-(1-(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозином.
42. Применение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозина в качестве ингибитора транспорта глицина для лечения пациента в патологическом состоянии, при котором требуется назначение ингибиторов транспорта глицина.
43. Применение замещенных аминов общей формулы I

где Ar1 означает группу тиенила, необязательно содержащую один заместитель, выбранный из метила или этила, и
Ar2 выбран из группы, содержащей тиенил, фурил и замещенный фенил, причем заместители фенильной группы выбраны из ряда C1-6алкил, галоген, C1-6галогеналкил, C1-6алкокси, C1-6галогеналкокси и циано,
в качестве лекарственного средства для лечения пациента в патологическом состоянии, которое требует назначения ингибитора транспорта глицина.
44. Применение по п.43 для лечения пациента в патологическом состоянии при заболеваниях, выбранных из следующей группы: шизофрения, дисфункция познавательных способностей, деменция (включая болезнь Альцгеймера), нарушение функции внимания, депрессия, аутизм, нарушение Ретта, детская дезинтеграция, нарушение Аспергера и атипичный аутизм.
45. Применение по п.44, в котором патологическим состоянием является шизофрения.
46. Применение по п.45, где замещенный амин представлен (Z)-N-(1-(4-(2-фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозином.
47. Применение по п.45, где замещенный амин представлен (Z)-N-(1-(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозином.
48. Применение по п.43, где замещенный амин представлен (Z)-N-(1-(4-(2-фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозином.
49. Применение по п.43, где замещенный амин представлен (Z)-N-(1-(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозином.
50. Применение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозина в качестве лекарственного средства для лечения пациента в патологическом состоянии, которое требует назначения ингибитора транспорта глицина.
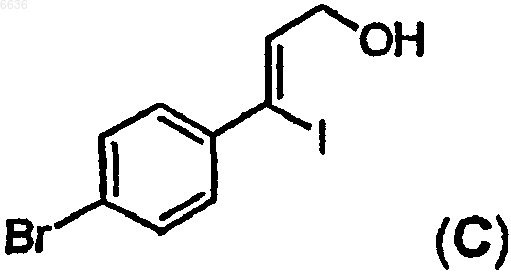
51. Способ получения промежуточного иодида C
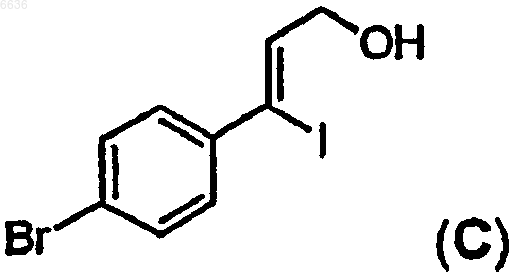
отличающийся тем, что проводят восстановление промежуточного соединения B
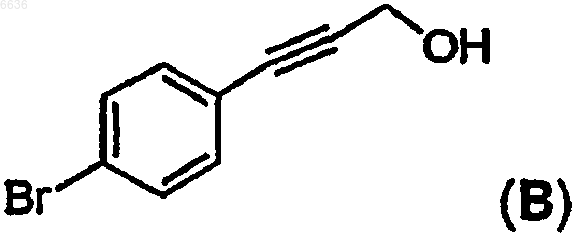
в присутствии натрий бис(2-метоксиэтокси)алюминий гидрида (Red-Al) и полученное производное обрабатывают иодом с образованием иодида C.
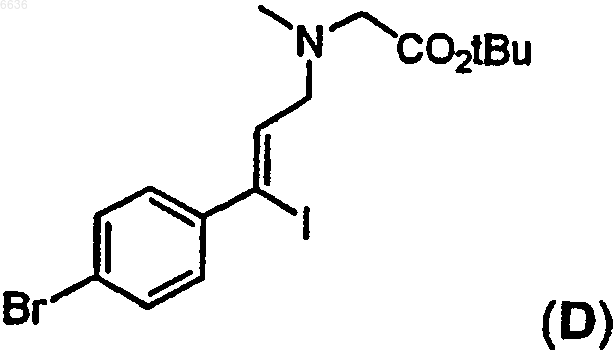
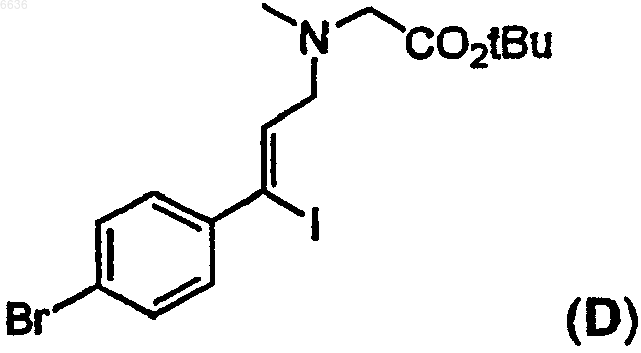
52. Способ получения промежуточного производного D
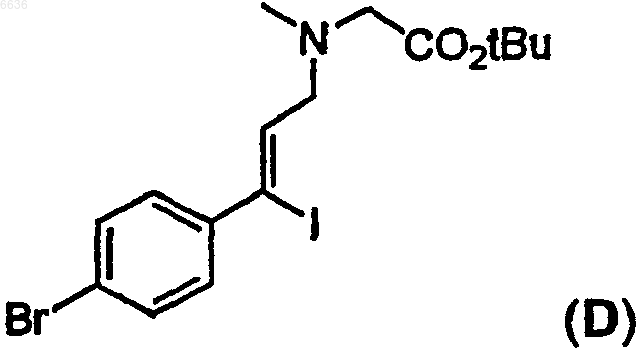
отличающийся тем, что осуществляют восстановление промежуточного соединения B

в присутствии натрий бис(2-метоксиэтокси)алюминий гидрида (Red-Al), затем полученное производное обрабатывают иодом с образованием иодида C

после этого спиртовой остаток иодида C превращают в бромид, а затем осуществляют замещение брома остатком трет-бутилового эфира саркозина с образованием промежуточного производного D.
53. Способ по п.52, отличающийся тем, что бромид иодида C получают посредством обработки иодида C, содержащего спиртовой остаток, N-бромсукцинимидом в присутствии трифенилфосфина.
54. Способ получения промежуточного производного E
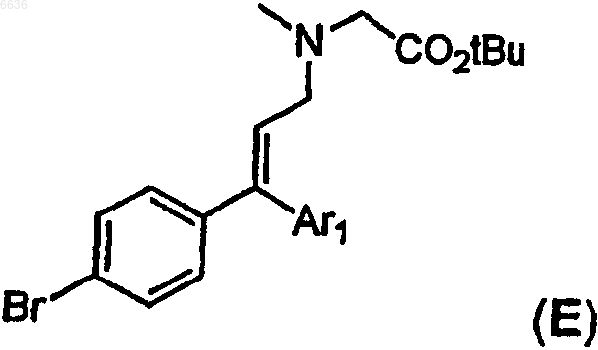
где Ar1 означает тиенил, необязательно замещенный одним заместителем, который выбирают из метила или этила,
отличающийся тем, что осуществляют восстановление промежуточного соединения B
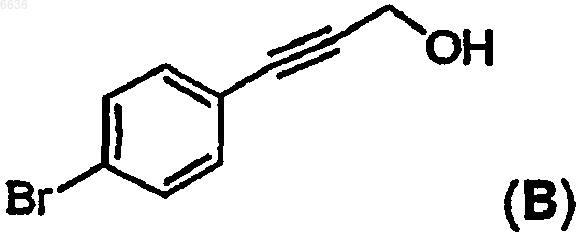
в присутствии натрий бис(2-метоксиэтокси)алюминий гидрида (Red-Al), затем полученное производное обрабатывают иодом с образованием иодида C
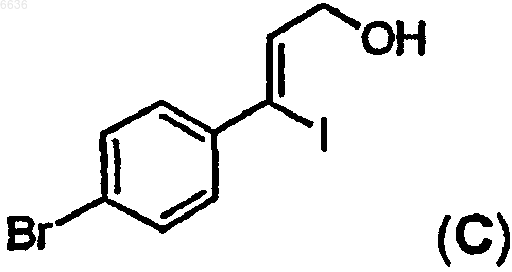
после этого спиртовой остаток иодида C превращают в бромид, а затем осуществляют замещение брома остатком трет-бутилового эфира саркозина с образованием промежуточного производного D
и проводят конденсацию производного D с бороновой кислотой формулы Ar1B(OH)2, где Ar1 определен выше, в присутствии палладиевого (0) катализатора с образованием промежуточного производного формулы E.
55. Способ по п.54, отличающийся тем, что бромид иодида C получают посредством обработки иодида C, содержащего спиртовой остаток, N-бромсукцинимидом в присутствии трифенилфосфина.
56. Способ получения соединения формулы G
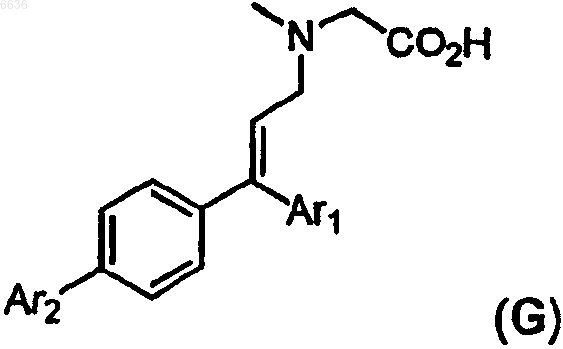
где Ar1 означает тиенил, необязательно замещенный одним заместителем, который выбирают из метила или этила, и
Ar2 выбирают из группы, содержащей тиенил, фурил и замещенный фенил, где заместители фенильной группы выбирают из ряда C1-6алкил, галоген, C1-6галогеналкил, C1-6алкокси, C1-6галогеналкокси и циано,
отличающийся тем, что осуществляют восстановление промежуточного соединения B
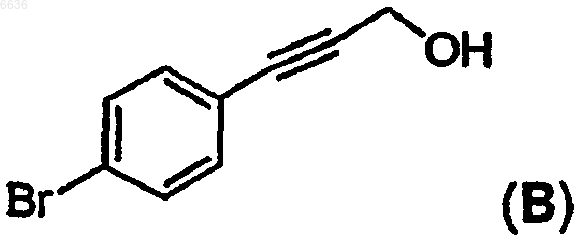
в присутствии натрий бис(2-метоксиэтокси)алюминий гидрида (Red-Al) и полученное производное обрабатывают иодом с образованием иодида C
после этого спиртовой остаток иодида C превращают в бромид, а затем проводят замещение брома остатком трет-бутилового эфира саркозина с образованием промежуточного производного D
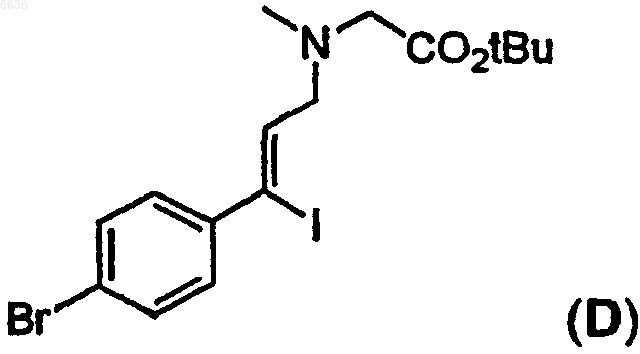
после этого осуществляют конденсацию производного D с бороновой кислотой формулы Ar1B(OH)2, где Ar1 определен выше, в присутствии палладиевого (0) катализатора собразованием промежуточного производного формулы E
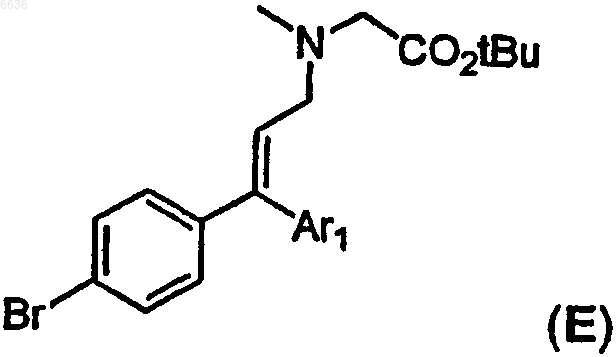
затем проводят конденсацию производного E с арилбороновой кислотой формулы Ar2B(OH)2, где Ar2 определен выше, в присутствии палладиевого (0) катализатора с образованием промежуточного производного формулы F
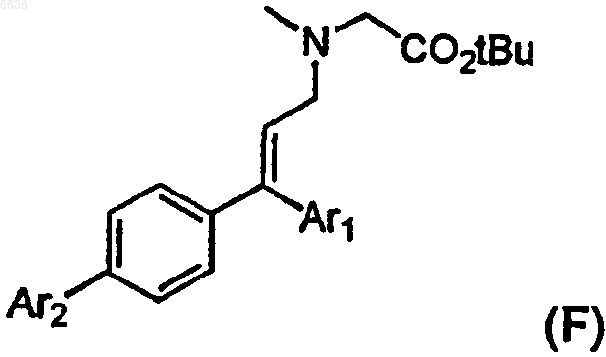
и осуществляют гидролиз сложноэфирной группы промежуточного производного F с образованием соединения формулы G.
57. Способ по п.56, отличающийся тем, что бромид иодида C получают посредством обработки иодида C, содержащего спиртовой остаток, N-бромсукцинимидом в присутствии трифенилфосфина.
58. Способ по п.56, отличающийся тем, что гидролиз проводят обработкой муравьиной кислотой.
59. Замещенные амины общей формулы I

где Ar1 означает тиофеновую группу, выбранную из остатков 2- или 3-тиофена, необязательно содержащую один заместитель, выбранный из метила или этила, и
Ar2 выбран из группы, содержащей тиофен, фуран и замещенный фенил, причем заместитель фенильной группы выбран из ряда C1-6алкил, галоген, C1-6галогеналкил, C1-6алкокси, C1-6галогеналкокси, циано, полученные способом по п.56.
60. Соединение, выбранное из группы, содержащей (Z)-N-(1-(4-(2-фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин и (Z)-N-(1-(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин, полученное способом по п.56.
61. Промежуточный иодид формулы C
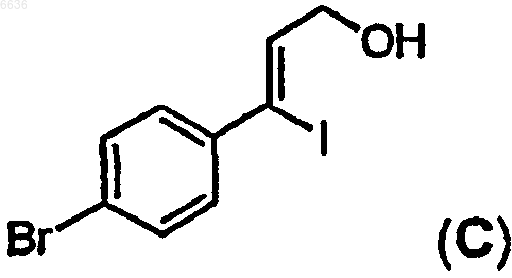
62. Промежуточный замещенный амин формулы D
63. Промежуточные замещенные амины общей формулы E
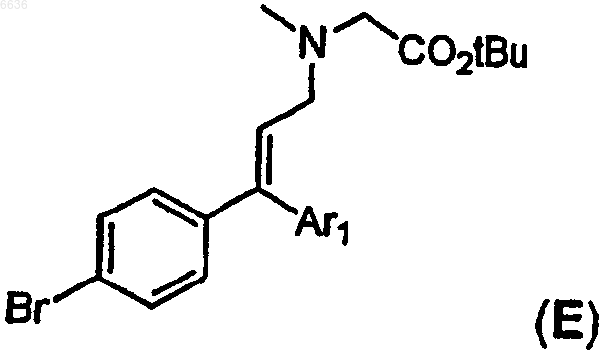
где Ar1 означает тиенил, необязательно замещенный одним заместителем, метилом или этилом.
Текст
006636 Область техники, к которой относится изобретение Настоящее изобретение относится к классу замещенных аминов, к содержащим их фармацевтическим композициям и к способам лечения неврологических и нейропсихических нарушений с использованием таких соединений. Уровень техники Проведение нервного импульса через синапс является сложной формой межклеточной коммуникации,которая включает множество важных специализированных структур, расположенных как в пресинаптических и постсинаптических окончаниях, так и в окружающих глиальных клетках (см. статью Kanner иSchuldiner, CRC Critical Reviews in Biochemistry, 1987, 22:1032). Вещества-переносчики связывают нейромедиаторы в синапсе и таким образом регулируют концентрацию нейромедиаторов, выделяющихся из синапса, а также продолжительность их существования в синапсе, причем оба фактора влияют на эффективность проведения нервного импульса через синапс. Кроме того, предотвращение распространения нейромедиатора в соседние синапсы с помощью переносчиков обеспечивает точность проведения нервного импульса через синапс. И, наконец, за счет связывания высвобожденного нейромедиатора в пресинаптических окончаниях переносчики обеспечивают повторное использование нейромедиатора. Транспорт нейромедиатора зависит от внеклеточного натрия и разности потенциалов по сторонам мембраны. В условиях интенсивного нейронального возбуждения, например во время приступа, переносчики могут проявлять обратную функцию, то есть высвобождать нейромедиатор по кальцийнезависимому внутриклеточному механизму (см. статью Attwell и соавт., Neuron, 1993, 11:401-407). Таким образом, фармакологическое модулирование переносчиков нейромедиаторов является средством модификации синаптической активности, что позволяет использовать такой процесс для лечения неврологических и психических нарушений. Аминокислота глицин является главным нейромедиатором в нервной системе млекопитающих и проявляет функциональную активность как в тормозных, так и в возбужденных синапсах. Термин "нервная система" означает как центральную, так и периферическую нервную систему. Эти особые функции глицина опосредованы двумя различными типами рецепторов, каждый из которых ассоциирован с разным классом переносчиков глицина. Тормозная активность глицина опосредована рецепторами глицина,которые чувствительны к судорожному алкалоиду, стрихнину, и которые в связи с этим названы "стрихнинчувствительными". Такие рецепторы содержат внутренние хлоридные каналы, которые открываются при связывании глицина с рецептором, что приводит к увеличению хлоридной проводимости, причем предел возбуждения действующего потенциала увеличивается. Стрихнинчувствительные рецепторы глицина обнаружены преимущественно в спинном мозге и в стволовой части головного мозга, и, таким образом, фармацевтические агенты, вызывающие активацию таких рецепторов, увеличивают тормозную нейропередачу сигнала в этих участках. Глицин участвует также в возбужденном проведении нервного импульса через синапс путем модулирования действия глютамата, основного возбуждающего нейромедиатора в центральной нервной системе (см. статьи Johnson и Ascher, Nature, 1987, 325:529-531; Fletcher и соавт., Проведение нервного импульса с участием глицина (Glycine Transmission), под ред. Otterson и Storm-Mathisen, 1990, стр. 193-219). Предполагают, что глицин является необходимым коагонистом класса глютаматных рецепторов, названных N-метил-D-аспартатными рецепторами (рецептор NMDA). При активации рецепторов NMDA увеличивается проводимость ионов натрия и кальция, что приводит к деполяризации нейрона и повышает вероятность возбуждения действующего потенциала. Рецепторы NMDA в гиппокампальном участке мозга играют важную роль в модели синаптической пластичности, известной как долгосрочное потенциирование (ДП), которое является важной составляющей в некоторых типах обучения и памяти (см. статьи Hebb D.O. (1949) Организация поведения (TheOrganization of Behavior), Wiley, NY; Bliss и Collingridge, Nature, 1993, 361:31-39; Morris и соавт., Nature,1986, 319:774-776). Повышенная экспрессия отдельных субъединиц рецептора NMDA у трансгенных мышей приводит к увеличению токов, опосредованных рецептором NMDA, увеличению ДП и лучшей воспроизводимости в некоторых видах испытаний на обучаемость и память (Tang и соавт., Nature, 1999, 401:63). И, наоборот, при пониженной экспрессии отдельных субъединиц рецептора NMDA у трансгенных мышей наблюдается поведение, аналогичное поведению моделей животных с шизофренией, индуцированной фармакологическими препаратами, включая повышенную локомоцию, увеличенную стереотипию и недостаточность социальных/сексуальных взаимодействий (см. статьи Mohn и соавт., Cell, 1999,98:427-436). Такое аберрантное поведение можно улучшить с помощью антипсихотических средств на основе галоперидола и клозапина. Рецепторы NMDA широко распространены в ткани мозга, причем наиболее высокая плотность наблюдается в коре головного мозга и гиппокампальном участке. С помощью молекулярного клонирования были обнаружены два класса переносчиков глицина в мозговой ткани млекопитающих, названных GlyT-1 и GlyT-2. Показано, что GlyT-1 содержится в ткани головного и спинного мозга, причем предполагают, что его распределение соответствует распределению глютаматергических путей и рецепторов MNDA (см. статью Smith и соавт., Neuron, 1992, 8:927-935). Затем с помощью молекулярного клонирования были обнаружены четыре варианта GlyT-1, названных GlyT-1a,GlyT-1b, GlyT-1 с и GlyT-1d. Два из этих вариантов (1 а и 1b) были выявлены у грызунов, причем каждый-1 006636 их них характеризуется уникальным распределением в ткани мозга и периферических тканях (см. статьиBorowsky и соавт., Neuron, 1993, 10:851-863; Adams и соавт., J. Neuroscience, 1995, 15:2524-2532). Третий вариант, 1 с, был обнаружен только в тканях человека (см. статью Kim и соавт., Molecular Pharmacology,1994, 45:608-617). Четвертый вариант обнаружен в тканях человека (см. патент США 6008015). Эти варианты образуются путем различного использования сплайсинга и экзона и отличаются по N-концевым фрагментам. GlyT-2 обнаружен предпочтительно в стволовой части мозга и спинном мозге, а его распределение точно соответствует распределению стрихнинчувствительных рецепторов глицина (см. статьиLiu и соавт., J. Biological Chemistry, 1993, 268:22802-22808; Jursky и Nelson, J. Neurochemistry, 1995,64:1026-1033). Другим отличительным признаком транспорта глицина, опосредованного GlyT-2, является отсутствие ингибирования указанного транспорта саркозином, которое происходит в случае транспорта глицина, опосредованного GlyT-1. Эти данные находятся в соответствии с тем фактом, что при регулировании уровня глицина в синапсе переносчиками GlyT-1 и GlyT-2 происходит избирательное влияние на активность рецепторов NMDA и стрихнинчувствительных рецепторов глицина, соответственно. Таким образом, следует ожидать, что соединения, которые ингибируют или активируют вещества-переносчики глицина, будут изменять функцию рецепторов за счет изменения концентрации глицина в синапсе и, следовательно, обеспечивать терапевтическое действие при лечении множества патологических состояний. Например, соединения, которые ингибируют опосредованный GlyT-1 транспорт глицина, могут увеличивать концентрацию глицина, связанного с рецепторами NMDA, которые расположены, в основном, в переднем мозге, а также в других тканях. Можно предположить, что такое увеличение концентрации может повысить активность рецепторов NMDA, и, таким образом, существует возможность смягчить симптомы шизофрении и повысить познавательные функции. В другом варианте, соединения, которые напрямую взаимодействуют с компонентом рецептора глицина в составе рецептора NMDA, могут оказывать аналогичные или сходные действия, такие как увеличение или уменьшение наличия внеклеточного глицина, вызванное ингибированием или увеличением активности GlyT-1, соответственно. См.,например, статьи Pitkanen и соавт., Eur. J. Pharmacol., 1994, 253:125-129; Thiels и соавт., Neuroscience,1992, 46:501-509; Kretschmer и Schmidt, J. Neurosci., 1996, 16:1561-1569. Показано, что многие соединения, эффективные в связывании и ингибировании переносчика GlyT-1,характеризуются токсичностью при применении in vivo. Несмотря на то, что такие соединения используют в качестве фармацевтических средств при исследовании функции переносчиков, токсичность ограничивает использование таких соединений в качестве фармацевтических препаратов. Таким образом, в настоящее время существует необходимость в получении соединений, воздействующих на транспорт глицина. Необходимы также соединения, которые воздействуют на транспорт глицина, но при этом являются в достаточной степени нетоксичными и могут быть использованы в фармацевтических композициях. Сущность изобретения Настоящее изобретение относится к соединениям, которые являются эффективными при ингибировании переносчиков GlyT-1 и являются в достаточной степени нетоксичными для использования их в медицине. Прежде всего, соединения по настоящему изобретению проявляют неожиданно улучшенный профиль токсичности по сравнению с другими известными ингибиторами GlyT-1. Согласно одному объекту изобретения предложены замещенные амины общей формулы I где Аr1 означает тиофеновую группу, выбранную из остатков 2- или 3-тиофена (т.е. присоединенных по положению 2 или 3), необязательно содержащую один заместитель, выбранный из метила или этила, и Аr2 выбран из группы, включающей тиофен, фуран и замещенный фенил, причем заместитель фенильной группы выбирают из ряда С 1-6 алкил, галоген, С 1-6 галогеналкил, С 1-6 алкокси, С 1-6 галогеналкокси, циано; а также их соли, сольваты и гидраты. В соответствии с другим объектом изобретения предложено соединение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозин. Показано, что соединения общей формулы I и соединение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозин ингибируют транспорт глицина, опосредованный GlyT-1, или являются предшественниками (например, пролекарствами) таких соединений. Ингибиторы транспорта GlyT-1 используют для лечения шизофрении, а также других связанных с ЦНС нарушений, таких как дисфункция познавательных способностей, деменция (включая деменцию, связанную с болезнью Альцгеймера), нарушение функции внимания, депрессия и глубокие развивающиеся нарушения, такие как аутизм, нарушение Ретта, детская дезинтеграция, нарушение Аспергера и неспецифические глубокие развивающиеся нарушения (например, атипичный аутизм).-2 006636 Следующий объект изобретения относится к композиции, содержащей соединение общей формулыI или соединение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозин и носитель. Еще один объект изобретения относится к фармацевтической композиции, содержащей соединение общей формулы I и фармацевтически приемлемый носитель. Кроме того, другой объект изобретения относится к фармацевтической композиции, содержащей соединение общей формулы I в количестве,эффективном для ингибирования транспорта глицина, и фармацевтически приемлемый носитель. Другой объект изобретения относится к фармацевтической композиции, содержащей соединение(Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозин и фармацевтически приемлемый носитель. Еще один объект изобретения относится к композиции, содержащей соединение (Z)-N-(1-(4-(3 тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозин в количестве, эффективном для ингибирования транспорта глицина, и фармацевтически приемлемый носитель. Другой объект изобретения относится к композициям, содержащим соединения общей формулы I или соединение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозин в количестве, пригодном для фармацевтического использования при лечении заболеваний, для которых требуется применение ингибитора транспорта глицина. Предпочтительными являются композиции, содержащие соединения,которые используют для лечения заболеваний, при которых требуется ингибирование транспорта глицина, опосредованного GlyT-1, таких как шизофрения или дисфункция познавательных способностей. Соединения общей формулы I или соединение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп 1-ен-3-ил)саркозин могут быть использованы при лечении пациентов с заболеванием, для которого показано назначение ингибитора транспорта глицина, причем показания упомянуты выше. Предпочтительным заболеванием является шизофрения. Соединения могут быть использованы также при изготовлении лекарственного средства для лечения пациентов с заболеванием, для которого показано назначение ингибитора транспорта глицина. Определения Термин "алкил", использованный вданном контексте, означает радикалы с прямой или разветвленной цепью, содержащие атомы углерода и водорода, причем радикалы содержат 1, 2, 3, 4, 5 или 6 атомов углерода и включают метил, этил и т.п. Термин C1-6, использованный в данном контексте, означает алкильный радикал, содержащий 1, 2, 3,4, 5 или 6 атомов углерода. Термин "алкокси", использованный вданном контексте, означает прямые или разветвленные алкильные группы, содержащие в концевом фрагменте оксирадикалы, содержащие 1, 2, 3, 4, 5 или 6 атомов углерода, и включает метокси, этокси, трет-бутокси и т.п. Термин "галоген", использованный в данном контексте, включает фтор, хлор, бром и т.п. Термин "галогеналкил", использованный в данном контексте, означает алкильную группу, содержащую один или более заместителей, независимо выбранных из атомов галогена, такую как -СF3. Аналогичным образом термин "галогеналкокси" означает алкоксигруппу, содержащую один или более заместителей, независимо выбранных из атомов галогена, такую как -ОСF3. Сведения, подтверждающие возможность осуществления изобретения Подходящие варианты воплощения изобретения включают в себя соединения общей формулы I, где Аr1 выбирают из необязательно замещенных остатков 2-тиофена или 3-тиофена (т.е. присоединенных по положению 2 или 3). В подходящем варианте воплощения изобретения Аr1 означает 2-тиофен. В предпочтительном варианте изобретения Аr1 означает 2-(3-алкилтиофен), предпочтительно 2-(3-метилтиофен). В другом предпочтительном варианте воплощения изобретения Аr1 означает 3-тиофен. Еще в одном предпочтительном варианте изобретения Аr1 означает 3-(4-алкилтиофен), предпочтительно 3-(4-метилтиофен). В подходящих вариантах воплощения изобретения Аr2 выбирают из замещенных фенила, тиофена и фурана. В более предпочтительном варианте изобретения Аr2 означает замещенный фенил, причем такие заместители находятся в положении 3 или 4 и заместители выбирают из ряда С 1-6 алкил, галоген, С 1-6 галогеналкил, С 1-6 алкокси, С 1-6 галогеналкокси и циано. В другом предпочтительном варианте заместитель фенильной группы в положении 3 или 4 выбирают из ряда СF3, Me, iPr, MeO, CN и СF3 О. В предпочтительном варианте Аr2 означает 3-метоксифенил. В другом предпочтительном варианте Аr2 означает 3 метилфенил. Еще в одном предпочтительном варианте Аr2 означает 3-трифторметоксифенил. В другом варианте Аr2 означает 3-тритфрометилфенил. Еще в другом предпочтительном варианте Аr2 означает 4 изопропилфенил и в другом предпочтительном варианте Аr2 означает 3-цианофенил. В подходящем варианте воплощения изобретения Аr2 означает тиофен. В другом варианте воплощения изобретения Аr2 означает 2-тиофен. Еще в одном предпочтительном варианте Аr2 означает 2-фуран. Наиболее предпочтительные варианты воплощения изобретения включают в себя(Z)-N-(1-(4-(3-метоксифенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин (соединение G(v,(Z)-N-(1-(4-(3-метилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин (соединение G(vi,(Z)-N-(1-(4-(3-(трифторметокси)фенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин (соединение G(vii,(Z)-N-(1-(4-(3-цианофенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин (соединение G(viii,(Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-тиенил)проп-1-ен-3-ил)саркозин (соединение G(ix,(Z)-N-(1-(4-(3-тиенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин (соединение G(x,(Z)-N-(1-(4-(3-(трифторметил)фенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин (соединение G(xi,(Z)-N-(1-(4-(3-метоксифенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин (соединение G(xii,(Z)-N-(1-(4-(3-метилфенил)фенил)-1-(3-метил-2-тиенил)проп-1-ен-3-ил)саркозин (соединение G(xiii. Наиболее предпочтительным вариантом воплощения изобретения является (Z)-N-(1-(4-(2-фурил) фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин (соединение G(iv. Другом подходящим вариантом воплощения изобретения является (Z)-N-(1-(4-(3-тиенил)фенил)-1(2-метилфенил)проп-1-ен-3-ил)саркозин (соединение G(xiv. В другом варианте воплощения изобретения соединение общей формулы I получают в меченной форме, такой как форма с радиоактивной меткой (например, с помощью введения в структуру 3H или 14 С или с помощью получения конъюгатов с 125I). В предпочтительном варианте изобретения такие соединения, предпочтительно связывающиеся с GlyT-1, могут быть использованы для идентификации лигандоврецепторов GlyT-1 по известным методикам. Анализ проводят при инкубировании рецептора или ткани в присутствии анализируемого лиганда и затем при инкубировании полученной смеси с эквимолярным количеством радиоактивно меченного соединения по изобретению. Таким образом, лигандами-рецепторами GlyT-1 являются такие соединения, которые в значительной степени взаимодействуют с участком связывания GlyT-1 и препятствуют связыванию с радиоактивно меченным соединением по настоящему изобретению. В другом варианте исследуемый лиганд-рецептор GlyT-1 можно идентифицировать следующим методом: сначала инкубируют радиоактивную форму соединения по настоящему изобретению,а затем инкубируют полученную смесь в присутствии исследуемого лиганда. Более активный лигандрецептор GlyT-1, присутствующий в эквимолярной концентрации, будет вытеснять радиоактивно меченное соединение по изобретению. Основно-аддитивные соли соединений общей формулы I предпочтительно получают с использованием фармацевтически приемлемых кислот. В объем изобретения включены также кислотно-аддитивные соли, сольваты и гидраты соединений по настоящему изобретению. Перевод данной соли соединения в желаемую соль соединения проводят с использованием стандаpтных методик, известных в данной области техники. Синтез 1Na2CO3, ДМЭ,(нагревание), 3 ч; (ж) муравьиная кислота, 40 С, в течение ночи. Соединения общей формулы I легко получить способом, показанным выше на схеме Синтез 1. Промежуточное производное В получают при взаимодействии 4-бромиодбензола с пропаргиловым спиртом в присутствии палладиевого катализатора. Соединение В превращают в иодид С при обработке-4 006636 натрий бис(2-метоксиэтокси)алюминий гидридом (Red-AI) с последующим добавлением иода. После двух стадий, включающих перевод спирта в бромид и последующее замещение остатком саркозина, получают промежуточное производное D. Промежуточное производное D является особенно ценным, так как из него можно получить ряд производных, в которых арильная группа может быть ориентирована в зависимости от требуемого стереохимического изомера. Например, общее промежуточное соединение D взаимодействует с различными бороновыми кислотами с образованием продуктов формулы Е. Продукты формулы Е также являются ценными промежуточными производными. Из этих продуктов получают ряд соединений, содержащих 4'-арильные группы (Аr2-группы). Продукты Е взаимодействуют с различными бороновыми кислотами с образованием ряда продуктов формулы F, которые могут быть деблокированы на последней стадии в присутствии муравьиной кислоты, при этом получают конечные соединения типа G. С использованием описанных в данном контексте реакций получают следующие соединения по настоящему изобретению:-5 006636 Соединения по настоящему изобретению могут быть введены пероральным, подъязычным, ректальным, интраназальным, вагинальным, местным (включая использование пластыря или других средств чрескожной доставки) способами, введением в легкие с использованием аэрозоля или парентеральным способом, включая, например, внутримышечный, подкожный, внутрибрюшинный, внутриартериальный,внутривенный или спинальный способы. Введение можно проводить с помощью насоса для периодической или непрерывной доставки. Соединения по настоящему изобретению можно вводить в отдельности или в смеси с фармацевтически приемлемым носителем или наполнителем согласно утановленным в фармацевтической практике стандартам. Для перорального введения соединения по настоящему изобретению могут быть использованы в форме таблеток, капсул, лепешек, жевательной резинки, пилюль, порошков, сиропов, эликсиров, водных растворов, суспензий и т.п. В случае таблеток носители, которые могут быть использованы, включают в себя лактозу, цитрат натрия и соли фосфорной кислоты. Для изготовления таблеток широко используются различные дезинтегрирующие агенты, такие как крахмал, и замасливатели, такие как стеарат магния и тальк. Для перорального введения в форме капсул в качестве разбавителей используют лактозу и высокомолекулярные полиэтиленгликоли. При необходимости добавляют определенные подсластители и/или ароматизаторы. Для парентерального введения обычно получают стерильные растворы соединений по изобретению, затем соответствующим образом доводят рН раствора и добавляют буферные вещества. Для внутривенного введения получают растворы с контролируемой общей концентрацией растворимых веществ, чтобы обеспечить образование изотонического раствора. Для введения в глаз мази и капли могут быть доставлены с помощью офтальмологических систем доставки, известных в данной области техники, таких как аппликаторы или капельницы для глаз. Такие композиции могут включать в себя мукомиметики, такие как гиалуроновая кислота, хондроитин сульфат,гидроксипропилметилцеллюлоза или поливиниловый спирт, консерванты, такие каксорбиновая кислота,ЭДТУ или хлорид бензилхрома, а также известные количества разбавителей и/или носителей. Для введения в легкие разбавители и/или носители выбирают таким образом, чтобы обеспечить образование аэрозоля. Соединения по изобретению в форме суппозитория используют для вагинального, уретрального и ректального введения. Такие суппозитории, в основном, содержат смесь веществ, которые являются твердыми при комнатной температуре, но плавятся при температуре тела. Соединения, используемые для получения таких носителей, в основном, включают в себя масло какао, глицеринсодержащий желатин, гидрогенизированное растительное масло, смеси полиэтиленгликолей различной молекулярной массы и сложные эфиры жирных кислот и полиэтиленгликоля. Подробное обсуждение лекарственных форм в виде суппозиториев см. в справочнике по фармацевтике Ремингтона (Remington's Pharmaceutical Sciences),16-изд., Mack Publishing, Easton, PA, 1980, стр. 1530-1533. Аналогичным образом, для вагинального,уретрального и ректального введения можно использовать гели и кремы. Специалистам в данной области техники известны многочисленные наполнители для введения, и такие наполнители включают в себя, без ограничения перечисленным, составы с замедленным высвобождением лекарственного средства, липосомальные составы и полимерные матрицы. Примеры фармацевтически приемлемых кислотно-аддитивных солей для использования по настоящему изобретению включают в себя соли неорганических кислот, таких как соляная, бромистоводородная, фосфорная, метафосфорная, азотная и серная кислоты, и соли органических кислот, таких как, например, винная, уксусная, лимонная, яблочная, молочная, фумаровая, бензойная, гликолевая, янтарная, п-толуолсульфоновая и арилсульфоновая кислоты. Примеры фармацевтически приемлемых основно-аддитивных солей для использования по настоящему изобретению включают в себя соли нетоксичных металлов, таких как натрий или калий, соли аммония и соли органических аминов, такие как соли триэтиламина. Множество соответствующих солей известны специалистам в данной области техники. Терапевты или медицинские работники другого профиля могут выбрать соответствующую дозу и курс лечения на основе массы тела пациента, его возраста и физического состояния. В основном, дозу выбирают таким образом, чтобы поддерживать уровень соединений по изобретению в сыворотке крови в диапазоне от приблизительно 0,01 до приблизительно 1000 мкг/см 3, предпочтительно от приблизительно 0,1 до приблизительно 100 мкг/см 3. Для парентерального введения другой мерой предпочтительного количества является доза от приблизительно 0,001 до приблизительно 10 мг/кг (в другом варианте от приблизительно 0,01 до приблизительно 10 мг/кг), более предпочтительно от приблизительно 0,01 до приблизительно 1 мг/кг (от приблизительно 0,1 до приблизительно 1 мг/кг). Для перорального введения другой мерой предпочтительного количества для введения является доза от приблизительно 0,001 до приблизительно 10 мг/кг (от приблизительно 0,1 до приблизительно 10 мг/кг), более предпочтительно от приблизительно 0,01 до приблизительно 1 мг/кг (от приблизительно 0,1 до приблизительно 1 мг/кг). Для введения в форме суппозитория другой мерой предпочтительного количества для введения является доза от приблизительно 0,1 до приблизительно 10 мг/кг, более предпочтительно от приблизительно 0,1 до приблизительно 1 мг/кг. Для определения ингибирующей активности в отношении транспорта глицина используют эукариотные клетки, предпочтительно клетки QT-6, полученные из фибробластов перепела. Указанные клетки трансфицируютдля экспрессии одного из четырех вариантов GlyT-1 человека, а именно GlyT-1a, GlyT-1b,GlyT-1 с и GlyT-1d человека или GlyT-2 человека. Последовательности указанных переносчиков GlyT-1GlyT-1a, для которого последовательность определена просто сравнением с соответствующей последовательностью GlyT-1 крысы. В настоящее время показано, что последовательность фрагмента, кодирующего N-концевой участок белка, соответствует определенной Kim и соавт. Последовательность GlyT-1d описана в патенте США 6008015, который полностью включен в данный контекст в качестве ссылки. Последовательность GlyT-2 человека описана в патенте США 5919653, который полностью включен в данный контекст в качестве ссылки. Подходящие векторы экспрессии наряду с прочими включают в себя(Stratagene), pMAM и рМАМ neo (Clontech). Подходящий экспрессионный вектор способен стимулировать экспрессию ДНК, кодирующую GlyT, в подходящих клетках хозяина, предпочтительно клетках немлекопитающего, которые могут включать в себя эукариоты, грибы или прокариоты. Такие предпочтительные клетки хозяина включают клетки земноводных, птиц, грибов, насекомых и пресмыкающихся. Примеры Пример 1. 1-(4-Бромфенил)проп-1-ин-3-ол (промежуточное соединение В). К раствору 4-бромиодбензола (10,0 г, 35,3 ммоль) в триэтиламине (Еt3N, 100 мл) добавляют пропаргиловый спирт (2,7 мл, 2,57 г, 45,9 ммоль), CuI (0,81 г, 4,24 ммоль) и Рd(РРh3)4 (1,63 г, 1,41 ммоль). Полученную смесь перемешивают в течение ночи, а затем концентрируют. После очистки колоночной хроматографией (20-35% ЕtOАс/гексан) получают 1-(4-бромфенил)-1-пропин-3-ол В (6,58 г, 88%) в виде твердого вещества желтого/оранжевого цвета. 1H ЯМР (300 МГц, CDCl3) 1,77 (t, 1H), 4,48 (d, 2H), 7,29 (d, 2H), 7,45 (d, 2H). Пример 2. (Z)-1-(4-Бромфенил)-1-иодпроп-1-ен-3-ол (промежуточное соединение С). Раствор 1-(4-бромфенил)-1-пропин-3-ола В (6,58 г, 31,2 ммоль) в безводном тетрагидрофуране(ТГФ, 66 мл) охлаждают на ледяной бане. Затем в течение 15 мин по каплям добавляют 65 мас./мас.% раствор Red-Al в толуоле (РhМе, 18,7 мл, 19,4 г, 62,4 ммоль). Через 1 ч добавляют этилацетат (ЕtOАс, 3,0 мл,2,75 г, 31,2 ммоль). Полученную реакционную смесь охлаждают на бане сухой лед/ацетон. По каплям добавляют раствор I2 (12,7 г, 49,9 ммоль) в безводном THF (66 мл). Реакционную смесь медленно нагревают до комнатной температуры в течение ночи. Реакцию останавливают насыщенным Nа 2SО 3 и реакционную смесь фильтруют через слой целита. Осадок тщательно промывают ЕtOАс. Фильтрат промывают водой и солевым раствором, сушат (МgSO4), фильтруют и концентрируют. После очистки колоночной хроматографией (20% ЕtOАс/гексан) получают (Z)-1-(4-бромфенил)-1-иодпропен-3-ол С (8,82 г, 83%) в виде твердого вещества желтого цвета. 1H ЯМР (300 МГц, CDCl3) 1,82 (t, 1H), 4,37 (коллапс dd, 2H), 6,25(t, 1H), 7,34 (d, 2H), 7,44 (d, 2H). Пример 3. трет-Бутиловый эфир (Z)-N-(1-(4-бромфенил)-1-иодпроп-1-ен-3-ил)саркозина (промежуточное производное D). Раствор (Z)-1-(4-бромфенил)-1-иодпропен-3-ола С (8,81 г, 26,0 ммоль) в CH2Cl2 (220 мл) охлаждают на бане сухой лед/ацетонитрил в атмосфере аргона. Добавляют РРh3 (10,9 г, 41,6 ммоль) и N-бромсукцинимид (МВS, 7,40 г, 41,6 ммоль). Через 1 ч реакцию останавливают насыщенным NаНСО 3. Смесь промывают насыщенным NаНСО 3 и солевым раствором, сушат (Na2SO4), фильтруют и концентрируют. Остаток немедленно переносят в безводный ацетонитрил (MeCN, 104 мл). Добавляют гидрохлорид третбутилового эфира саркозина (5,20 г, 28,6 ммоль), К 2 СО 3 (35,9 г, 260 ммоль) и KI (21,6 г, 130 ммоль). Смесь перемешивают в течение ночи, затем фильтруют и осадок промывают ЕtOАс. Фильтрат распределяют между ЕtOАс и водой. Органическую фазу промывают солевым раствором, сушат (MgSO4), фильтруют и концентрируют. После очистки колоночной хроматографией (20% ЕtOАс/гексан) получают третбутиловый эфир (Z)-N-(1-(4-бромфенил)-1-иодпроп-1-ен-3-ил)саркозина D (9,63 г, 80% в расчете на две стадии) в виде масла светло-коричневого цвета. 1H ЯМР (300 МГц, CDCl3) 1,48 (s, 9H), 2,46 (s, 3 Н), 3,23(промежуточное производное E(i. К раствору трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-иодпроп-1-ен-3-ил)саркозина D (29,86 г,64,06 ммоль) в диметоксиэтане (300 мл) добавляют 3-тиофенбороновую кислоту (9,02 г, 70,47 ммоль),Pd(PPh3)4 (3,70 г, 3,20 ммоль) и 2 М раствор Nа 2 СО 3 (300 мл). Полученную реакционную смесь нагревают при 90 С и интенсивном механическом перемешивании в течение 4,5 ч. Смесь охлаждают и распределяют между ЕtOАс и водой. Органическую фазу промывают солевым раствором, сушат (МgSО 4), фильтруют и концентрируют. После очистки колоночной хроматографией (2-5% ацетон/гексан) получают трет-бутиловый эфир (Z)-N-(1-(4-бромфенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина E(i) (27,06 г, 78%) в виде масла желтого цвета. 1H ЯМР (300 МГц, CDCl3) 1,43 (s, 9H), 2,36 (s, 3 Н), 3,14 (s, 2H), 3,28 (d, 2H),6,16 (s, 1H), 6,86 (d, 1H), 7,12-7,14 (m, 3 Н), 7,32 (коллапс dd, 1H), 7,41 (d, 2H). Пример 4-2. трет-Бутиловый эфир (Z)-N-(1-(4-бромфенил)-1-(2-тиенил)проп-1-ен-3-ил)саркозина(промежуточное производное E(ii. трет-Бутиловый эфир (Z)-N-(1-(4-бромфенил)-1-(2-тиенил)проп-1-ен-3-ил)саркозина E(ii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-иодпроп-1-ен-3-ил)саркозинаD и 2-тиофенбороновой кислоты, при этом получают 243 мг (52%) масла желтого цвета. 1H ЯМР (300 МГц,-7 006636CDCl3) 1,43 (s, 9 Н), 2,39 (s, 3H), 3,16 (s, 2H), 3,38 (d, 2H), 6,16 (s, 1 Н), 6,90 (d, 1 Н), 7,04 (коллапс dd, 1 Н),7,19 (d, 2H), 7,35 (d, 1H), 7,42 (d, 2H). Пример 4-3. трет-Бутиловый эфир (Z)-N-(1-(4-бромфенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозина (промежуточное производное Е(iii. трет-Бутиловый эфир (Z)-N-(1-(4-бромфенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозина E(iii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-иодпроп-1-ен-3 ил)саркозина D и 3-метил-4-тиофенбороновой кислоты, при этом получают 574 мг (61%) масла желтого цвета. 1H ЯМР (300 МГц, CDCl3) 1,42 (s, 9H), 1,85 (s, 3H), 2,33 (s, 3H), 3,10-3,12 (m, 4H), 6,35 (t, 1H), 6,99(d, 1H), 7,03 (d, 1H), 7,10 (d, 2H), 7,38 (d, 2H). Пример 4-4. трет-Бутиловый эфир (Z)-N-(1-(4-бромфенил)-1-(3-метил-2-тиенил)проп-1-ен-3-ил)саркозина (промежуточное производное Е(iv. трет-Бутиловый эфир (Z)-N-(1-(4-бромфенил)-1-(3-метил-2-тиенил)проп-1-ен-3-ил)саркозина E(iv) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-иодпроп-1-ен-3 ил)саркозина D и 3-метил-2-тиофенбороновой кислоты, при этом получают 436 мг (47%) масла желтого цвета. 1H ЯМР (300 МГц, CDCl3) 1,43 (s, 9H), 1,97 (s, 3H), 2,35 (s, 3H), 3,12 (s, 2H), 3,16 (d, 2H), 6,43 (t,1H), 6,90 (d, 1H), 7,14 (d, 2H), 7,26 (d, 1H), 7,40 (d, 2H). Пример 4-5. трет-Бутиловый эфир (Z)-N-(1-(4-бромфенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозина (промежуточное производное E(v. трет-Бутиловый эфир (Z)-N-(1-(4-бромфенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозина E(v) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-иодпроп-1-ен-3-ил) саркозина D и 2-толуилбороновой кислоты, при этом получают 379 мг (66%) масла желтого цвета. Пример 5-1. трет-Бутиловый эфир (Z)-N-(1-(4-(4-изопропилфенил)фенил-1-(3-тиенил)проп-1-ен-3 ил)саркозина (промежуточное производное F(i. К раствору трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина(16,41 г, 100,1 ммоль), Рd(РРh3)4 (2,89 г, 2,50 ммоль) и 2 М раствор Na2CO3 (210 мл). Смесь кипятят с обратным холодильником в течение 2 ч при интенсивном перемешивании. Затем смесь охлаждают и распределяют между ЕtOАс и водой. Органическую фазу промывают солевым раствором, сушат (МgSО 4),фильтруют и концентрируют. После очистки колоночной хроматографией (2-5% ацетон/гексан) с последующим вторым циклом хроматографии (2-20% EtOAc/гексан) получают трет-бутиловый эфир (Z)-N-(1(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина F(i) (18,65 г, 81%) в виде масла желтого цвета. 1H ЯМР (300 МГц, CDCl3) 1,29 (d, 6H), 1,44 (s, 9H), 2,39 (s, 3 Н), 2,95 (hept, 1H), 3,16 (s,2 Н), 3,30 (d, 2H), 6,26 (t, 1H), 6,93 (d, 1H), 7,18 (d, 1 Н), 7,26-7,35 (m, 5H), 7,50-7,54 (m, 4H). Пример 5-2. трет-Бутиловый эфир (Z)-N-(1-(4-(3-тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина (промежуточное производное F(ii. трет-Бутиловый эфир (Z)-N-(1-(4-(3-тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина F(ii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(3-тиенил)проп-1-ен 3-ил)саркозина E(i) и 3-тиофенбороновой кислоты, при этом получают 1,00 г (50%) масла желтого цвета. Пример 5-3. трет-Бутиловый эфир (Z)-N-(1-(4-(2-тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина (промежуточное производное F(iii. трет-Бутиловый эфир (Z)-N-(1-(4-(2-тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина F(iii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(3-тиенил)проп-1-ен 3-ил)саркозина E(i) и 2-тиофенбороновой кислоты, при этом получают 300 мг (64%) масла желтого цвета. Пример 5-4. трет-Бутиловый эфир (Z)-N-(1-(4-(2-фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина (промежуточное производное F(iv. трет-Бутиловый эфир (Z)-N-(1-(4-(2-фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина F(iv) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(3-тиенил)проп-1-ен 3-ил)саркозина E(i) и 2-фуранбороновой кислоты, при этом получают 216 мг (82%) масла желтого цвета. 1F(v) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(3 тиенил)проп-1-ен-3-ил)саркозина E(i) и 3-метоксифенилбороновой кислоты, при этом получают 241 мг(99%) масла желтого цвета. 1H ЯМР (300 МГц, CDCl3) 1,44 (s, 9H), 2,39 (s, 3 Н), 3,17 (s, 2H), 3,30 (d, 2 Н),3,86 (s, 3 Н), 6,26 (t, 1H), 6,88-6,93 (m, 2H), 7,12 (s, 1H), 7,18-7,19 (m, 2H), 7,33-7,38 (m, 4H), 7,52 (d, 2H). Пример 5-6. трет-Бутиловый эфир (Z)-N-(1-(4-(3-метилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил) саркозина (промежуточное производное F(vi. трет-Бутиловый эфир (Z)-N-(1-(4-(3-метилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина F(vi) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(3-тиенил)проп-1 ен-3-ил)саркозина E(i) и 3-метилфенилбороновой кислоты, при этом получают 150 мг (64%) масла блед-8 006636 но-желтого цвета. 1H ЯМР (300 МГц, CDCl3) 1,45 (s, 9H), 2,40 (s, 3 Н), 2,42 (s, 3 Н), 3,17 (s, 2H), 3,32 (d,2H), 6,26 (t, 1H), 6,94 (d, 1H), 7,15-7,19 (m, 3H), 7,30-7,41 (m, 5H), 7,52 (d, 2H). Пример 5-7. трет-Бутиловый эфир (Z)-N-(1-(4-(3-(трифторметокси)фенил)фенил)-1-(3-тиенил)проп 1-ен-3-ил)саркозина (промежуточное производное F(vii. трет-Бутиловый эфир (Z)-N-(1-(4-(3-(трифторметокси)фенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил) саркозина F(vii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1(3-тиенил)проп-1-ен-3-ил)саркозина E(i) и 3-(трифторметокси)фенилбороновой кислоты, при этом получают 127 мг (51%) масла желтого цвета. Пример 5-8. трет-Бутиловый эфир (Z)-N-(1-(4-(3-цианофенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил) саркозина (промежуточное производное F(viii. трет-Бутиловый эфир (Z)-N-(1-(4-(3-цианофенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина F(viii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(3-тиенил)проп-1-ен-3 ил)саркозина E(i) и 3-цианофенилбороновой кислоты, при этом получают 57 мг (77%) масла желтого цвета. Пример 5-9. трет-Бутиловый эфир (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-тиенил)проп-1-ен-3-ил)саркозина (промежуточное производное F(ix. трет-Бутиловый эфир (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-тиенил)проп-1-ен-3-ил)саркозина F(ix) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(2-тиенил)проп-1-ен 3-ил)саркозина E(ii) и 3-тиофенбороновой кислоты, при этом получают 152 мг (76%) масла желтого цвета. 1H ЯМР (300 МГц, CDCl3) 1,44 (s, 9 Н), 2,40 (s, 3H), 3,18 (s, 2H), 3,41 (d, 2H), 6,24 (t, 1 Н), 6,94 (d, 1 Н),7,06 (dd, 1H), 7,35-7,39 (m, 4 Н), 7,46 (d, 1H), 7,54 (d, 2H). Пример 5-10. трет-Бутиловый эфир (Z)-N-(1-(4-(3-тиенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3 ил)саркозина (промежуточное производное F(x. трет-Бутиловый эфир (Z)-N-(1-(4-(3-тиенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозина F(x) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(4-метил-3-тиенил)проп 1-ен-3-ил)саркозина E(iii) и 3-тиофенбороновой кислоты, при этом получают 222 мг (64%) масла желтого цвета. Пример 5-11. трет-Бутиловый эфир (Z)-N-(1-(4-(3-(трифторметил)фенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозина (промежуточное производное F(xi. трет-Бутиловый эфир (Z)-N-(1-(4-(3-(трифторметил)фенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен 3-ил)саркозина F(xi) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозина E(iii) и 3-(трифторметил)фенилбороновой кислоты,при этом получают 260 мг (54%) масла светло-желтого цвета. Пример 5-12. трет-Бутиловый эфир (Z)-N-(1-(4-(3-метоксифенил)фенил)-1-(4-метил-3-тиенил)проп 1-ен-3-ил)саркозина (промежуточное производное F(xii. трет-Бутиловый эфир (Z)-N-(1-(4-(3-метоксифенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозина F(xii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(4 метил-3-тиенил)проп-1-ен-3-ил)саркозина E(iii) и 3-метоксифенилбороновой кислоты, при этом получают 193 мг (69%) масла желтого цвета. Пример 5-13. трет-Бутиловый эфир (Z)-N-(1-(4-(3-метилфенил)фенил)-1-(3-метил-2-тиенил)проп-1 ен-3-ил)саркозина (промежуточное производное F(xiii. трет-Бутиловый эфир (Z)-N-(1-(4-(3-метилфенил)фенил)-1-(3-метил-2-тиенил)проп-1-ен-3-ил)саркозина F(xiii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(3-метил 2-тиенил)проп-1-ен-3-ил)саркозина E(iv) и 3-метилфенилбороновой кислоты, при этом получают 176 мг(73%) масла желтого цвета. 1H ЯМР (300 МГц, CDCl3) 1,44 (s, 9 Н), 2,02 (s, 3 Н), 2,37 (s, 3 Н), 2,41 (s, 3 Н),3,14 (s, 2H), 3,19 (d, 2H), 6,50 (t, 1 Н), 6,92 (d, 1 Н), 7,16 (d, 1 Н), 7,26-7,39 (m, 6H), 7,50 (d, 2H). Пример 5-14. трет-Бутиловый эфир (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил) саркозина (промежуточное производное F(xiv. трет-Бутиловый эфир (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозина F(xiv) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-бромфенил)-1-(2-метилфенил)проп 1-ен-3-ил)саркозина E(v) и 3-тиофенбороновой кислоты, при этом получают 62 мг (48%) масла желтого цвета. Пример 6-1. (Z)-N-(1-(4-(4-Изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозина (G(i. трет-Бутиловый эфир (Z)-N-(1-(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозинаF(i) (18,62 г, 40,3 ммоль) растворяют в 96%-ном растворе муравьиной кислоты (200 мл). Раствор нагревают при 40 С в течение ночи, а затем концентрируют. Остаток дважды упаривают в смеси с CH2Cl2. При очистке колоночной хроматографией (2-15% MeOH/CH2Cl2) получают твердое вещество бледножелтого цвета. При растирании полученного вещества с метанолом (МеОН) получают чистый (Z)-N-(1(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин G(i) (11,38 г, 70%) в виде твердого вещества белого цвета. 1H ЯМР (300 МГц, метанол-d4) 1,23 (d, 6 Н), 2,47 (s, 3 Н), 2,92 (hept, 1H), 3,26 (s,2 Н), 3,50 (d, 2H), 6,22 (t, 1H), 6,94 (d, 1H), 7,32 (d, 4H), 7,46 (d, 1H), 7,57-7,65 (m, 5H). Пример 6-2. (Z)-N-(1-(4-(3-Тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин (G(ii.(Z)-N-(1-(4-(3-Тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин G(ii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозинаF(ii), при этом получают 486 мг (61%) порошка белого цвета.(Z)-N-(1-(4-(2-Тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин G(iii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(2-тиенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозинаF(iii), при этом получают 145 мг (53%) порошка белого цвета. Пример 6-4. (Z)-N-(1-(4-(2-Фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин (G(iv.(Z)-N-(1-(4-(2-Фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин G(iv) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(2-фурил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозинаF(iv), при этом получают 158 мг (97%) бесцветного масла. 1H ЯМР (300 МГц, метанол-d4) 2,74 (s, 3 Н),3,63 (s, 2 Н), 3,88 (d, 2 Н), 6,31 (t, 1H), 6,42 (s, 1H), 6,58 (d, 1 Н), 6,80 (d, 1H), 7,10 (s, 1H), 7,25 (d, 2H), 7,31(Z)-N-(1-(4-(3-Метоксифенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин G(v) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-метоксифенил)фенил)-1-(3-тиенил)проп-1-ен 3-ил)саркозина F(v), при этом получают 156 мг (74%) пены грязно-белого цвета. 1H ЯМР (300 МГц, метанол-d4) 2,76 (s, 3 Н), 3,56 (s, 2H), 3,82 (s, 3 Н), 3,91 (d, 2H), 6,36 (t, 1H), 6,82-6,88 (m, 2H), 7,06-7,11 (m,3 Н), 7,26-7,32 (m, 4H), 7,46 (d, 2H). Пример 6-6. (Z)-N-(1-(4-(3-Метилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин (G(vi.(Z)-N-(1-(4-(3-Метилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин G(vi) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-метилфенил)фенил)-1-(3-тиенил)проп-1-ен-3 ил)саркозина F(vi), при этом получают 127 мг (100%) бесцветного масла. 1H ЯМР (300 МГц, метанол-d4) 2,38 (s, 3 Н), 2,76 (s, 3 Н), 3,56 (s, 2H), 3,90 (d, 2H), 6,36 (t, 1H), 6,83 (d, 1H), 7,10-7,15 (m, 2H), 7,24-7,33 (m,6H), 7,46 (d, 2H). Пример 6-7. (Z)-N-(1-(4-(3-(Трифторметокси)фенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин (G(vii.(Z)-N-(1-(4-(3-(Трифторметокси)фенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин G(vii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-(трифторметокси)фенил)фенил)-1-(3 тиенил)проп-1-ен-3-ил)саркозина F(vii), при этом получают 80 мг (78%) порошка белого цвета. Пример 6-8. (Z)-N-(1-(4-(3-Цианофенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин (G(viii.(Z)-N-(1-(4-(3-Цианофенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин G(viii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-цианофенил)фенил)-1-(3-тиенил)проп-1-ен-3 ил)саркозина F(viii), при этом получают 48 мг (84%) порошка белого цвета. Пример 6-9. (Z)-N-(1-(4-(3-Тиенил)фенил)-1-(2-тиенил)проп-1-ен-3-ил)саркозин (G(ix.(Z)-N-(1-(4-(3-Тиенил)фенил)-1-(2-тиенил)проп-1-ен-3-ил)саркозин G(iх) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-тиенил)проп-1-ен-3-ил)саркозинаF(ix), при этом получают 108 мг (59%) порошка белого цвета. 1H ЯМР (300 МГц, CDCl3) 2,73 (s, 3 Н), 3,44(Z)-N-(1-(4-(3-Тиенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин G(x) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-тиенил)фенил)-1-(4-метил-3-тиенил)проп-1 ен-3-ил)саркозина F(x), при этом получают 157 мг (82%) порошка белого цвета. Пример 6-11. (Z)-N-(1-(4-(3-(Трифторметил)фенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин (G(xi.(Z)-N-(1-(4-(3-(Трифторметил)фенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин G(xi) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-(трифторметил)фенил)фенил)-1(4-метил-3-тиенил)проп-1-ен-3-ил)саркозина F(xi), при этом получают 99 мг (73%) порошка белого цвета. Пример 6-12. (Z)-N-(1-(4-(3-Метоксифенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин (G(xii.(Z)-N-(1-(4-(3-Метоксифенил)фенил)-1-(4-метил-3-тиенил)проп-1-ен-3-ил)саркозин G(хii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-метоксифенил)фенил)-1-(4-метил-3 тиенил)проп-1-ен-3-ил)саркозина F(xii), при этом получают 152 мг (69%) порошка белого цвета. Пример 6-13. (Z)-N-(1-(4-(3-Метилфенил)фенил)-1-(3-метил-2-тиенил)проп-1-ен-3-ил)саркозин (G(xiii.(Z)-N-(1-(4-(3-Метилфенил)фенил)-1-(3-метил-2-тиенил)проп-1-ен-3-ил)саркозин G(xiii) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-метилфенил)фенил)-1-(3-метил-2 тиенил)проп-1-ен-3-ил)саркозина F(xiii), при этом получают 129 мг (99%) порошка белого цвета. 1H ЯМР(Z)-N-(1-(4-(3-Тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозин G(xiv) получают аналогичным способом из трет-бутилового эфира (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3 ил)саркозина F(xiv), при этом получают 37 мг (61%) порошка белого цвета. Пример 7. Анализ транспорта, опосредованного GlyT-1. В этом примере описан метод определения поглощения глицина трансфицированными культуральными клетками.- 10006636 Клетки, устойчиво трансфицированные GlyT-1c (см. статью Kim и соавт., Molecular Pharmacology,1994, 45:608-617), дважды промывают буферным раствором HEPES, содержащим хлористый натрий(БХН). Затем клетки инкубируют в течение 10 мин при 37 С в следующих условиях: а) в отсутствие потенциального конкурирующего лиганда, б) в присутствии 10 мМ нерадиоактивного глицина или в) при определенной концентрации исследуемого лекарственного средства. Диапазон концентраций исследуемого лекарственного средства используют для получения данных, которые используют для расчета концентрации, при которой наблюдается 50% ингибирование (например, величины IС 50, которая равна концентрации лекарственного средства, ингибирующего поглощение глицина на 50%). Затем добавляют раствор, содержащий [3 Н]глицин в конечной концентрации 50 нМ (17,5 Ки/ммол). Клетки инкубируют при легком встряхивании в течение еще 30 мин при 37 С, после чего реакционную смесь отбирают и клетки промывают 3 раза ледяным БХН. Клетки лизируют сцинтиляционным раствором и уравновешивают. Радиоактивность клеток измеряют на сцинтилляционном счетчике. Данные сравнивают с результатами, полученными при инкубировании тех же клеток в присутствии или в отсутствие исследуемого лекарственного средства в зависимости от типа проводимого анализа. Соединения по настоящему изобретению проявляют активность ингибиторов GlyT-1. Пример 8. Анализ взаимодействия с участком связывания глицина, ассоциированным с рецепторами NMDA. В этом примере описан метод анализа взаимодействия соединений с участком связывания в составе рецептора NMDA. В этом анализе для связывания с гиппокампальной тканью крысы используют известный агент, связывающийся с участком, специфичным к NMDA глицину (меченный тритием MDL 105519 производства фирмы Amersham). Затем добавляют исследуемое соединение, при этом происходит замещение "горячего" лиганда. При связывании исследуемого соединения происходит замещение "горячего лиганда" и в результате наблюдается снижение радиоактивности, которое можно измерить. В основном,соединения исследуют в двух концентрациях, и если наблюдается ингибирование, то соединения исследуют повторно при нескольких концентрациях, получают дозозависимую кривую, которую используют для определения величины IC50. Для анализа исследуемые соединения разбавляют 50 мМ трис-ацетатным буферным раствором. Аликвотные части мембранных фракций из гиппокампальной ткани крысы, используемых для анализа,промывают 2 раза холодным 10 мМ трис-ацетатным буферным раствором и центрифугируют на ультрацентрифуге при 20000 об./мин в течение 15 мин, причем перед каждой промывкой фракцию гомогенизируют. Полученные осадки ресуспендируют в 50 мМ трис-ацетатном буферном растворе и получают мембранные фракции в концентрации, необходимой для анализа. Неспецифическое связывание определяют в присутствии 1 мМ глицина. Суммарное связывание определяют в присутствии только трис-ацетатного буферного раствора. Реакционную смесь готовят смешиванием 75 мкл гомогенизированной гиппокампальной мембранной фракции с [3H]MDL 105519 до конечной концентрации 5 нМ и с глицином или исследуемым соединением в виде раствора в трис-ацетатном буферном растворе. Реакционную смесь встряхивают в процессе инкубирования при комнатной температуре в течение 30 мин. Клетки из планшет собирают на специальных фильтрах GFC с использованием прибора для сбора клеток 48w Brandell Harvester. Фильтры GFC предварительно обрабатывают 0,5% раствором БСА в дистиллированной воде, по крайней мере, в течение 30 мин для снижения неспецифического связывания "горячего" лиганда на фильтре. Лунки планшета промывают 4-5 объемами холодного 50 мМ трис-ацетатного буферного раствора. Затем фильтры помещают в сцинтилляционные флаконы, в которые добавляют по 2 мл сцинцилляционной жидкости. Флаконы выдерживают в течение ночи и радиоактивность измеряют на -счетчике Beckman. Полученные данные анализируют с использованием программного обеспечения Prism. Соединения по настоящему изобретению не взаимодействуют с участками связывания глицина, ассоциированными с NMDA-рецептором. Пример 9. Анализ связывания с рецептором глицина. В этом примере описан метод анализа конкурентной реакции соединений с рецептором глицина. В этом анализе для связывания с тканью спинного мозга крысы используют известный агент, связывающийся с рецептором глицина, [3H]стрихнин. Затем добавляют исследуемое соединение, при этом происходит замещение "горячего" лиганда. При связывании исследуемого соединения происходит замещение"горячего" лиганда, и в результате наблюдается снижение радиоактивности, которое можно измерить. В основном, соединения исследуют в двух концентрациях, и если наблюдается ингибирование, то соединения исследуют повторно при нескольких концентрациях, получают дозозависимую кривую, которую используют для определения величины IC50. Для анализа исследуемые соединения разбавляют калийфосфатным буферным раствором. Аликвотные части мембранных фракций из спинного мозга крысы, используемые для анализа, промывают двумя порциями холодного фосфатного буферного раствора, причем перед каждой промывкой фракции центрифугируют на микроцентрифуге при 4 С при 14000 об./мин. Полученные осадки ресуспендируют в объеме фосфатного буферного раствора и получают соответствующие концентрации, необходимые для- 11006636 анализа. Неспецифическое и суммарное связывание определяют в присутствии только глицина в конечной концентрации 10 мМ и только фосфатного буферного раствора соответственно. Реакционную смесь готовят смешиванием 150 мкл мембранной фракции из спинного мозга крысы с[3H]стрихнином в конечной концентрации 7 нМ и с глицином или исследуемым соединением. Реакционную смесь встряхивают в процессе инкубирования на ледяной бане в течение 2 ч. Клетки из планшет собирают на специальных фильтрах GFC с использованием прибора для сбора клеток 48w Brandell Harvester. Фильтры GFC предварительно обрабатывают 0,5% раствором БСА в дистиллированной воде, по крайней мере, в течение 30 мин для снижения неспецифического связывания. Лунки планшета промывают 4-5 объемами холодного фосфатного буферного раствора. Затем фильтры помещают в сцинтилляционные флаконы, в которые добавляют по 2 мл сцинцилляционной жидкости. Флаконы выдерживают в течение ночи и радиоактивность измеряют на -счетчике Beckman. Полученные данные анализируют с использованием программного обеспечения Prism. Соединения по настоящему изобретению не проявляют значительного связывания с рецептором глицина. Пример 10. Метод исследования токсичности у мышей. В этом примере описан метод исследования хронической токсичности ингибиторов GlyT-1 с использованием перорального введения соединений в течение 5 дней. Соединения вводят перорально (ПО) самцам мышей CD-1 в течение 5 дней в дозе 40 мг/кг/сут. Для всех исследованных соединений каждый день регистрируют поведенческие признаки (клинические симптомы) и массу тела. Самцов мышей CD-1 получают на фирме Charles River Labs (Kingston, NY). Масса тела мышей после доставки составляет 2025 г. За 5 дней до испытаний животных акклиматизируют в виварии с контролируемыми температурой/влажностью (22,22,2 С/50%5%) и полным 12-часовым циклом день-ночь (с включением света в 7.00 ч). В процессе акклиматизации и испытаний все животные получают корм (Purina Labdiet Rodentchow 5001) и воду (фирмы Elizabethtown Water Company) по желанию. За день до испытаний животных произвольно распределяют в группы. Все выбранные для испытаний особи весят по крайней мере 20 г и находятся в хорошем состоянии. Каждое животное получает дозу 1 раз в день в течение 5 суток. После введения дозы в течение 5 суток животные оставались на своих местах для реабилитации в течение 3 суток. Исходный раствор каждого исследуемого соединения готовят свежим непосредственно в день начала испытаний. Аликвотные части указанного раствора разбавляют до необходимой концентрации для ежедневного введения. Исходные растворы хранят в холодильнике до использования. Каждое соединение растворяют в небольшом количестве дистиллированной воды. Для увеличения растворимости каждого исследуемого агента можно добавить эквивалентное количество гидроксида натрия (2 н. раствор). Затем добавляют количество носителя, необходимое до конечного объема. Конечные объемы доводят до соответствующей величины процентного содержания свободного основания, если оно присутствует. В качестве носителя в данном эксперименте используют гидроксипропилциклодекстрин (ГПЦД) фирмы Acros, партия 011849601, который растворяют в дистиллированной воде до концентрации 10 мас./об.%. рН доводят с использованием гидроксида натрия (2 н.) до величины, равной рН исследуемых агентов (обычно между 8 и 10). Все полученные соединения исследуют в виде прозрачного раствора или в виде слегка опалесцирующей суспензии. Суспензии смешивают непосредственно перед использованием. Всем животным вводят либо исследуемое соединение, либо носитель ПО с помощью желудочного зонда с иглами размером 21 в количестве 10,0 мл/кг. Для определения суточных доз используют массу тела животного, которых взвешивают каждый день. Все исследуемые соединения взвешивают на аналитических весах Denver Instruments, модельА 250. Животных взвешивают на портативных весах Тор loading Ohaus, модельLS2000. Поведение животных (клинические симптомы) оценивают непосредственно после введения исследуемых агентов, а затем через 4 и 24 ч. У животных выявляют 27 отдельных клинических сипмтомов. Активность Описывают аномально повышенную или пониженную активность животного Атаксия Неуверенная походка, неспособность координировать произвольные движения мышц Каталепсия Состояние, характеризующееся воскообразным окоченением в конечностях,которым можно придать различные положения, сохраняющиеся в течение времени,отсутствие ответной реакции на стимул, слабый пульс и редкое дыхание, бледная кожа Хроматурия Красноватые выделения в моче Хромодакриорея Красноватые выделения из глаз Состояние стула Мягкий и водянистый, твердый и малого размера Судороги Клонические: генерализованный скачкообразный тонус и расслабление скелетных мышц Тонические: генерализованный устойчивый тонус мышц, часто сопровождается выпрямлением задней и/или передней конечности- 12006636 Цианоз Смертельный исход Энофтальм Носовое кровотечение Экзофтальм Вялость Искаженная поза Повышенная чувствительность к касанию Лакримация (обоих глаз) Боковое лежачее положение Потеря установочного рефлекса (неспособность выпрямиться) Миоз Мидриаз Пальпебральный птоз Пилоэрекция Хрипы Синеватый цвет внешних тканей (уши, пальцы, хвост) Выявляют случаи естественной смерти или эвтаназии Аномальная ретракция глаза в глазнице Красноватые выделения из носа Аномальное выпячивание глаз Отсутствие тонуса в скелетных мышцах Животные пытаются двигаться высоко над полом Животные повизгивают или проявляют чрезвычайно высокую активность при обработке Секреция из глаз и слезотечение Животное находится в самопроизвольном лежачем положении Если животное положить в лежачее положение, оно остается в этом положении Сильное сужение зрачков глаз Сильное расширение зрачков глаз Относится к опущению верхних век обоих глаз Шерсть встает дыбом на затылке и спине Мокрые (слизистые): наблюдается клокочущий звук во время дыхания Сухие: наблюдается резкий или свистящий звук при дыхании Необычное увеличение или уменьшение активности дыхания Воскообразное: конечности остаются в положении, которое им придали Типа "свинцовая труба": мышечная ригидность, неустранимое окоченение конечностей Образование слюны и избыточное выделение слюны Замедленная реакция животного на прикосновение или при обработке Непрерывное повторение определенных бессмысленных движений Мелкоразмашистое: непрерывное быстрое дрожание тела и/или конечностей Крупноразмашистое: быстрое дрожание тела и/или конечностей, которое в течение времени то увеличивается, то уменьшается Любое животное, у которого 1) в течение 2 последовательных дней испытаний наблюдается потеря в массе тела на 75% по сравнению со средней массой тела животных в контрольной группе или 2) наблюдаются начальные признаки агонии, например животное не может есть и пить нормальным образом,забивали до проведения заключительного этапа испытаний. Данные токсичности, определенные указанным выше методом анализа для соединений G(i)-G(xiv) включительно, приведены в табл. 1-14. За животными наблюдают непосредственно после введения и снова через 4 и 24 ч. Полученные результаты регистрируют с использованием следующего цифрового кода: 0 - нормальное состояние,1 - активность (повыш./пониж.),2 - торможение/летаргия,3 - пилоэрекция,4 - стереотипия,5 - мягкий стул,6 - хромодакриорея,7 - носовое кровотечение,8 - цианоз,9 - вялость,10 - дыхание,11 - искаженная поза,12 - энофтальм,13 - экзофтальм,14 - пальпебральный птоз,15 - потеря установочного рефлекса,16 - хроматурия,17 - слюнотечение,18 - лакримация,19 - миоз,20 - мидриаз,- 13006636 21 - окоченение,22 - атаксия,23 - дрожание,24 - судороги,25 - каталепсия,26 - боковое лежачее положение,27 - смертельный исход Таблица 1 Соединение G(iii)+ - вызванные прикосновением Таблица 6 Соединение G(x)- 20006636 Сравнение результатов показало, что соединения общей формулы I являются менее токсичными,чем другие ингибиторы GlyT-1 с аналогичной активностью. Например, как показано в табл. 15, 16, 17 и 18, соединения Н, I, J и К, представленные ниже, характеризуются более высокой токсичностью по сравнению с соединениями по настоящему изобретению.- В данном эксперименте наблюдения проводят только 1 раз в сутки.I - сильный зуд Таблица 17 Соединение J Животных забивают при выявлении признаков агонии. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Замещенные амины общей формулы I где Аr1 означает тиофеновую группу, выбранную из остатков 2- или 3-тиофена, необязательно содержащую один заместитель, выбранный из метила или этила, иAr2 выбран из группы, содержащей тиофен, фуран и замещенный фенил, причем заместитель фенильной группы выбран из ряда С 1-6 алкил, галоген, С 1-6 галогеналкил, С 1-6 алкокси, С 1-6 галогеналкокси,циано; и его соли, сольваты и гидраты,или Аr1 означает 2-метилфенил, а Аr2 означает 3-тиенил. 2. Соединение по п.1, где Аr1 означает 2-тиофен. 3. Соединение по п.1, где Аr1 означает 2-(3-метилтиофен). 4. Соединение по п.1, где Аr1 означает 3-тиофен. 5. Соединение по п.1, где Аr1 означает 3-(4-метилтиофен). 6. Соединение по п.1, где Аr2 означает замещенный фенил, в котором заместитель выбран из ряда СF3, Me, iPr, MeO, CN и CF3O. 7. Соединение по п.1, где Аr2 означает фуран. 8. Соединение по п.1, где Аr2 означает тиофен. 9. Соединение по п.1, выбранное из группы, содержащей(Z)-N-(1-(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин. 12. Соединение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозин. 13. Композиция, отличающаяся тем, что она содержит соединение по п.1 и носитель. 14. Композиция, отличающаяся тем, что она содержит соединение по п.10 и носитель. 15. Композиция, отличающаяся тем, что она содержит соединение по п.11 и носитель. 16. Композиция, отличающаяся тем, что она содержит соединение по п.12 и носитель. 17. Фармацевтическая композиция, отличающаяся тем, что она содержит терапевтически эффективное количество соединения по п.1 и фармацевтически приемлемый носитель. 18. Фармацевтическая композиция, отличающаяся тем, что она содержит терапевтически эффективное количество соединения по п.10 и фармацевтически приемлемый носитель. 19. Фармацевтическая композиция, отличающаяся тем, что она содержит терапевтически эффективное количество соединения по п.11 и фармацевтически приемлемый носитель. 20. Фармацевтическая композиция, отличающаяся тем, что она содержит терапевтически эффективное количество соединения по п.12 и фармацевтически приемлемый носитель. 21. Способ лечения пациента в патологическом состоянии, при котором назначают ингибиторы транспорта глицина, отличающийся тем, что пациенту вводят фармацевтическую композицию по п.17. 22. Способ по п.21, отличающийся тем, что патологическим состоянием является шизофрения. 23. Способ по п.21, отличающийся тем, что патологическим состоянием является дисфункция познавательных способностей. 24. Способ по п.21, отличающийся тем, что патологическим состоянием является болезнь Альцгеймера. 25. Способ лечения пациента в патологическом состоянии, при котором назначают ингибиторы транспорта глицина, отличающийся тем, что пациенту вводят фармацевтическую композицию по п.18. 26. Способ по п.25, отличающийся тем, что патологическим состоянием является шизофрения. 27. Способ по п.25, отличающийся тем, что патологическим состоянием является дисфункция познавательных способностей. 28. Способ по п.25, отличающийся тем, что патологическим состоянием является болезнь Альцгеймера. 29. Способ лечения пациента в патологическом состоянии, при котором назначают ингибиторы транспорта глицина, отличающийся тем, что пациенту вводят фармацевтическую композицию по п.19. 30. Способ по п.29, отличающийся тем, что патологическим состоянием является шизофрения. 31. Способ по п.29, отличающийся тем, что патологическим состоянием является дисфункция познавательных способностей. 32. Способ по п.29, отличающийся тем, что патологическим состоянием является болезнь Альцгеймера. 33. Способ лечения пациента в патологическом состоянии, при котором назначают ингибиторы транспорта глицина, отличающийся тем, что пациенту вводят фармацевтическую композицию по п.20. 34. Способ по п.33, отличающийся тем, что патологическим состоянием является шизофрения. 35. Способ по п.33, отличающийся тем, что патологическим состоянием является дисфункция познавательных способностей. 36. Способ по п.33, отличающийся тем, что патологическим состоянием является болезнь Альцгеймера. 37. Применение замещенных аминов общей формулы I где Аr1 означает группу тиенила, необязательно содержащую один заместитель, выбранный из метила или этила, и Аr2 выбран из группы, содержащей тиенил, фурил и замещенный фенил, где заместители фенильной группы выбраны из ряда С 1-6 алкил, галоген, С 1-6 галогеналкил, С 1-6 алкокси, С 1-6 галогеналкокси, циано,в качестве ингибитора транспорта глицина для лечения пациента в патологическом состоянии, при котором требуется назначение ингибиторов транспорта глицина.- 24006636 38. Применение по п.37 для лечения пациента в патологическом состоянии при заболеваниях, выбранных из следующей группы: шизофрения, дисфункция познавательных способностей, деменция, в частности болезнь Альцгеймера, нарушение функции внимания, депрессия, аутизм, нарушение Ретта,детская дезинтеграция, нарушение Аспергера и атипичный аутизм. 39. Применение по п.38, в котором патологическим состоянием является шизофрения. 40. Применение по п.38, где замещенный амин представлен (Z)-N-(1-(4-(2-фурил)фенил)-1-(3 тиенил)проп-1-ен-3-ил)саркозином. 41. Применение по п.39, где замещенный амин представлен (Z)-N-(1-(4-(4-изопропилфенил)фенил)1-(3-тиенил)проп-1-ен-3-ил)саркозином. 42. Применение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозина в качестве ингибитора транспорта глицина для лечения пациента в патологическом состоянии, при котором требуется назначение ингибиторов транспорта глицина. 43. Применение замещенных аминов общей формулы I где Аr1 означает группу тиенила, необязательно содержащую один заместитель, выбранный из метила или этила, и Аr2 выбран из группы, содержащей тиенил, фурил и замещенный фенил, причем заместители фенильной группы выбраны из ряда С 1-6 алкил, галоген, С 1-6 галогеналкил, С 1-6 алкокси, С 1-6 галогеналкокси и циано,в качестве лекарственного средства для лечения пациента в патологическом состоянии, которое требует назначения ингибитора транспорта глицина. 44. Применение по п.43 для лечения пациента в патологическом состоянии при заболеваниях, выбранных из следующей группы: шизофрения, дисфункция познавательных способностей, деменция(включая болезнь Альцгеймера), нарушение функции внимания, депрессия, аутизм, нарушение Ретта,детская дезинтеграция, нарушение Аспергера и атипичный аутизм. 45. Применение по п.44, в котором патологическим состоянием является шизофрения. 46. Применение по п.45, где замещенный амин представлен (Z)-N-(1-(4-(2-фурил)фенил)-1-(3 тиенил)проп-1-ен-3-ил)саркозином. 47. Применение по п.45, где замещенный амин представлен (Z)-N-(1-(4-(4-изопропилфенил)фенил)1-(3-тиенил)проп-1-ен-3-ил)саркозином. 48. Применение по п.43, где замещенный амин представлен (Z)-N-(1-(4-(2-фурил)фенил)-1-(3 тиенил)проп-1-ен-3-ил)саркозином. 49. Применение по п.43, где замещенный амин представлен (Z)-N-(1-(4-(4-изопропилфенил)фенил)1-(3-тиенил)проп-1-ен-3-ил)саркозином. 50. Применение (Z)-N-(1-(4-(3-тиенил)фенил)-1-(2-метилфенил)проп-1-ен-3-ил)саркозина в качестве лекарственного средства для лечения пациента в патологическом состоянии, которое требует назначения ингибитора транспорта глицина. 51. Способ получения промежуточного иодида С отличающийся тем, что проводят восстановление промежуточного соединения В в присутствии натрий бис(2-метоксиэтокси)алюминий гидрида (Red-Al) и полученное производное обрабатывают иодом с образованием иодида С. 52. Способ получения промежуточного производного D отличающийся тем, что осуществляют восстановление промежуточного соединения В в присутствии натрий бис(2-метоксиэтокси)алюминий гидрида (Red-Al), затем полученное производное обрабатывают иодом с образованием иодида С после этого спиртовой остаток иодида С превращают в бромид, а затем осуществляют замещение брома остатком трет-бутилового эфира саркозина с образованием промежуточного производного D. 53. Способ по п.52, отличающийся тем, что бромид иодида С получают посредством обработки иодида С, содержащего спиртовой остаток, N-бромсукцинимидом в присутствии трифенилфосфина. 54. Способ получения промежуточного производного Е где Аr1 означает тиенил, необязательно замещенный одним заместителем, который выбирают из метила или этила,отличающийся тем, что осуществляют восстановление промежуточного соединения В в присутствии натрий бис(2-метоксиэтокси)алюминий гидрида (Red-Al), затем полученное производное обрабатывают иодом с образованием иодида С после этого спиртовой остаток иодида С превращают в бромид, а затем осуществляют замещение брома остатком трет-бутилового эфира саркозина с образованием промежуточного производного D и проводят конденсацию производного D с бороновой кислотой формулы Аr1 В(ОН)2, где Аr1 определен выше, в присутствии палладиевого (0) катализатора с образованием промежуточного производного формулы Е. 55. Способ по п.54, отличающийся тем, что бромид иодида С получают посредством обработки иодида С, содержащего спиртовой остаток, N-бромсукцинимидом в присутствии трифенилфосфина. 56. Способ получения соединения формулы G где Аr1 означает тиенил, необязательно замещенный одним заместителем, который выбирают из метила или этила, и Аr2 выбирают из группы, содержащей тиенил, фурил и замещенный фенил, где заместители фенильной группы выбирают из ряда С 1-6 алкил, галоген, С 1-6 галогеналкил, С 1-6 алкокси, С 1-6 галогеналкокси и циано,отличающийся тем, что осуществляют восстановление промежуточного соединения В в присутствии натрий бис(2-метоксиэтокси)алюминий гидрида (Red-Al) и полученное производное обрабатывают иодом с образованием иодида С после этого спиртовой остаток иодида С превращают в бромид, а затем проводят замещение брома остатком трет-бутилового эфира саркозина с образованием промежуточного производного D после этого осуществляют конденсацию производного D с бороновой кислотой формулыAr1B(OH)2, где Аr1 определен выше, в присутствии палладиевого (0) катализатора собразованием промежуточного производного формулы Е затем проводят конденсацию производного Е с арилбороновой кислотой формулы Аr2 В(ОН)2, где Аr2 определен выше, в присутствии палладиевого (0) катализатора с образованием промежуточного производного формулы F и осуществляют гидролиз сложноэфирной группы промежуточного производного F с образованием соединения формулы G. 57. Способ по п.56, отличающийся тем, что бромид иодида С получают посредством обработки иодида С, содержащего спиртовой остаток, N-бромсукцинимидом в присутствии трифенилфосфина. 58. Способ по п.56, отличающийся тем, что гидролиз проводят обработкой муравьиной кислотой. 59. Замещенные амины общей формулы I где Ar1 означает тиофеновую группу, выбранную из остатков 2- или 3-тиофена, необязательно содержащую один заместитель, выбранный из метила или этила, и Аr2 выбран из группы, содержащей тиофен, фуран и замещенный фенил, причем заместитель фенильной группы выбран из ряда С 1-6 алкил, галоген, С 1-6 галогеналкил, С 1-6 алкокси, С 1-6 галогеналкокси,циано, полученные способом по п.56. 60. Соединение, выбранное из группы, содержащей (Z)-N-(1-(4-(2-фурил)фенил)-1-(3-тиенил)проп 1-ен-3-ил)саркозин и (Z)-N-(1-(4-(4-изопропилфенил)фенил)-1-(3-тиенил)проп-1-ен-3-ил)саркозин, полученное способом по п.56. 61. Промежуточный иодид формулы С 62. Промежуточный замещенный амин формулы D 63. Промежуточные замещенные амины общей формулы Е где Аr1 означает тиенил, необязательно замещенный одним заместителем, метилом или этилом.
МПК / Метки
МПК: A61P 25/28, C07D 409/10, C07D 333/20, A61K 31/381
Метки: иодид, варианты, замещенные, леченияпациента, промежуточный, применение, ингибиторов, композиция, амины, способ, транспорта, качестве, глицина, получения
Код ссылки
<a href="https://eas.patents.su/29-6636-zameshhennye-aminy-varianty-sposob-ih-polucheniya-i-ih-primenenie-v-kachestve-ingibitorov-transporta-glicina-varianty-kompoziciya-varianty-promezhutochnyjj-iodid-i-sposob-ego-poluc.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные амины (варианты), способ их получения и их применение в качестве ингибиторов транспорта глицина (варианты), композиция (варианты), промежуточный иодид и способ его получения, способ леченияпациента (варианты)</a>
Предыдущий патент: Молекулярные метки для систем органических растворителей
Следующий патент: Способ рафинирования и модифицирования железоуглеродистого расплава
Случайный патент: Производные резорцина












