Замещённые производные оксадиазаспиро [5.5] ундеканона и их применение в качестве антагонистов нейрокинина
Номер патента: 12421
Опубликовано: 30.10.2009
Авторы: Схунтьес Брюно, Понселе Алан Филипп, Янссенс Франс Эдуард, Купа Софи
Формула / Реферат
1. Соединение в соответствии с общей формулой (I)
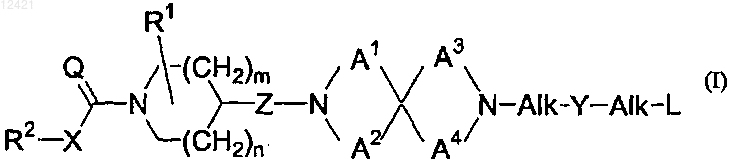
его фармацевтически приемлемые кислотно-аддитивные соли, его стереохимически изомерные формы и его N-оксидная форма, где
R2 представляет собой Ar2;
X представляет собой ковалентную связь;
Q представляет собой О;
R1 выбирают из группы Ar1 и Ar1-алкила;
n представляет собой целое число, равное 1;
m представляет собой целое число, равное 1;
Z представляет собой ковалентную связь;
А2 и А4, каждый независимо друг от друга, представляют собой -СН2СН2-;
А1 представляет собой -СН2СН2- или -С(=O)O-;
А3 представляет собой -СН2СН2- или -OC(=O)- при условии, что один из А1 или А3 представляет собой -С(=O)O- или -OC(=O)-;
каждый Alk представляет независимо один от другого ковалентную связь; двухвалентный прямой или разветвленный, насыщенный или ненасыщенный углеводородный радикал, имеющий от 1 до 6 атомов углерода;
Y представляет собой ковалентную связь или двухвалентный радикал формулы -C(=O)-;
L выбирают из группы водорода, алкила, Ar3 и Het2;
Ar1 представляет собой фенил, необязательно замещенный 1, 2 или 3 заместителями, независимо один от другого выбранными из группы галогена и алкила;
Ar2 представляет собой фенил, необязательно замещенный 1, 2 или 3 заместителями, каждый из которых независимо один от другого выбирают из группы галогена, алкила, гидрокси и алкилокси;
Ar3 представляет собой фенил, необязательно замещенный 1, 2 или 3 заместителями, каждый из которых независимо один от другого выбирают из группы алкила, галогена, гидрокси;
Het2 представляет собой моноциклический гетероциклический радикал, выбранный из группы пирролидинила, дигидро-2Н-пиранила, пиранила, диоксолила, имидазолидинила, тетрагидропиридинила, тетрагидропиримидинила, пиразолидинила, пиперидинила, морфолинила, дитианила, тиоморфолинила, пиперазинила, имидазолидинила, тетрагидрофуранила, 2Н-пирролила, пирролинила, имидазолинила, пиразолинила, пирролила, имидазолила, пиразолила, триазолила, фуранила, тиенила, оксазолила, диоксазолила, оксазолидинила, изоксазолила, тиазолила, тиадиазолила, изотиазолила, пиридинила, 1Н-пиридинила, пиримидинила, пиразинила, пиридазинила, триазинила и тетразолила; где моногетероциклический радикал может быть необязательно замещен по любому атому одним или более алкильными радикалами;
алкил представляет собой прямой или разветвленный насыщенный углеводородный радикал, имеющий от 1 до 6 атомов углерода или циклические насыщенные углеводородные радикалы, имеющие от 3 до 6 атомов углерода; каждый углеводородный радикал необязательно замещен по одному или более атомов углерода одним или более радикалами, выбранными из группы фенила, галогена, тригалогенметила, аминокарбонила, метила, этила, пропила, изопропила, трет-бутила, циано, оксо, гидрокси, формила и амино.
2. Соединение по п.1, характеризующееся тем, что спиро-фрагмент имеет формулу (f1) или (f2), где переменные определены, как в формуле (I), и "а" обозначает пиперидинил-фрагмент формулы (I) и "b" обозначает Alk-Y-Alk-L-фрагмент формулы (I)
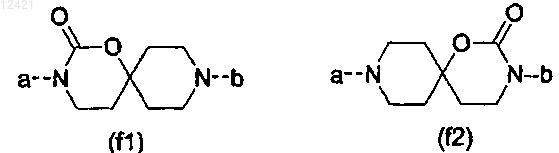
3. Соединение по любому из пп.1, 2, характеризующееся тем, что R1 представляет собой бензил, присоединенный по 2-му положению, или R1 представляет собой фенил, присоединенный по 3-му положению.
4. Соединение по любому из пп.1-3, характеризующееся тем, что фрагмент R2-X-C(=Q)- представляет собой 3,5-ди(трифторметил)фенилкарбонил.
5. Соединение по любому из пп.1-4, характеризующееся тем, что каждый Alk независимо друг от друга представляет собой ковалентную связь или -СН2-.
6. Соединение по любому из пп.1-5, характеризующееся тем, что L выбирают из группы водорода, изопропила, пентила, трет-бутила, циклопропила, циклогексила, тетрагидрофуранила, пирролила, фуранила, тиенила, тиадиазолила, фенила, пиридинила и пиразинила.
7. Соединение по любому из пп.1-6, характеризующееся тем, что
R2 представляет собой фенил, необязательно замещенный 1, 2 или 3 галогеналкильными заместителями;
X представляет собой ковалентную связь;
Q представляет собой О;
R1 представляет собой фенил или бензил;
n является целым числом, равным 1;
m является целым числом, равным 1;
Z представляет собой ковалентную связь;
А2 и А4, каждый независимо друг от друга, представляют собой -CH2CH2-;
А1 представляет собой -СН2СН2- или -С(=O)O-;
А3 представляет собой -СН2СН2- или -OC(=O)- при условии, что один из А1 или А3 представляет собой -С(=O)O- или -OC(=O)-;
каждый Alk представляет собой независимо один от другого ковалентную связь или двухвалентный прямой, насыщенный углеводородный радикал, имеющий от 1 до 2 атомов углерода;
Y представляет собой ковалентную связь или двухвалентный радикал формулы -С(=O)-;
L выбирают из группы водорода, алкила, Ar3 и Het2;
Ar3 представляет собой фенил, необязательно замещенный заместителем, выбранным из группы алкила, галогена и гидрокси;
Het2 представляет собой моноциклический гетероциклический радикал, выбранный из группы тетрагидрофуранила, пирролила, фуранила, тиенила, тиадиазолила, пиридинила и пиразинила; где каждый моноциклический гетероциклический радикал может быть необязательно замещен по любому атому одним или более алкильными радикалами;
и
алкил представляет собой прямой или разветвленный насыщенный углеводородный радикал, имеющий от 1 до 6 атомов углерода, или циклические насыщенные углеводородные радикалы, имеющие от 3 до 6 атомов углерода.
8. Соединение по п.1, представляющее собой соединение формулы
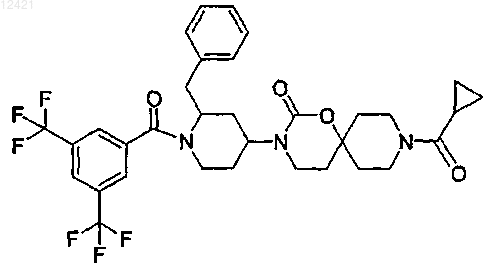
9. Применение соединения по любому из пп.1-8 в качестве лекарственного средства.
10. Применение соединения по любому из пп.1-8 в качестве перорально активного лекарственного средства системного проникновения.
11. Применение соединения по любому из пп.1-10 для производства лекарственного средства для лечения тахикинин-опосредованных состояний.
12. Применение соединения по пп.1-10 для производства лекарственного средства для лечения и/или профилактики шизофрении, рвоты, тревожности и депрессии, синдрома раздраженного кишечника (IBS), нарушений циркадного ритма, преэклампсии, ноцицепции, боли, в частности висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (ХОЗЛ) и расстройств мочеиспускания, таких как недержание мочи.
13. Фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и, в качестве активного ингредиента, терапевтически эффективное количество соединения по любому из пп.1-10.
14. Способ получения фармацевтической композиции по п.13, характеризующийся тем, что фармацевтически приемлемый носитель тщательно смешивают с терапевтически эффективным количеством соединения по любому из пп.1-10.
15. Способ получения соединения формулы (Ia), характеризующийся взаимодействием промежуточного соединения формулы (IIа) с 1,1'-карбонилдиимидазолом, где все переменные являются такими, как определено в п.1, в реакционно-инертном растворителе,
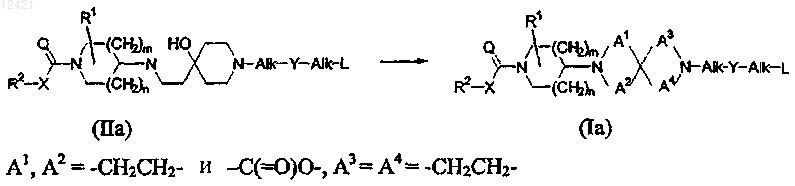
и, если требуется, превращением соединений формулы (Ia) одно в другое, следуя известным в данной области превращениям, и дополнительно, если требуется, превращением соединений формулы (Ia) в терапевтически активную нетоксичную кислотно-аддитивэую соль обработкой кислотой, или в терапевтически активную нетоксичную основно-аддитивную соль обработкой основанием, или наоборот, превращением кислотно-аддитивной соли в свободное основание обработкой щелочью или превращением основно-аддитивной соли в свободную кислоту обработкой кислотой; и, если требуется, получением стереохимически изомерных форм, их N-оксидов и четвертичных аммониевых солей.
16. Способ получения соединения формулы (Ib), характеризующийся восстановительным N-алкилированием промежуточного соединения формулы (IIb) промежуточным соединением формулы (III), где все переменные являются такими, как определено в п.1, в реакционно-инертном растворителе и необязательно в присутствии подходящего восстанавливающего агента,
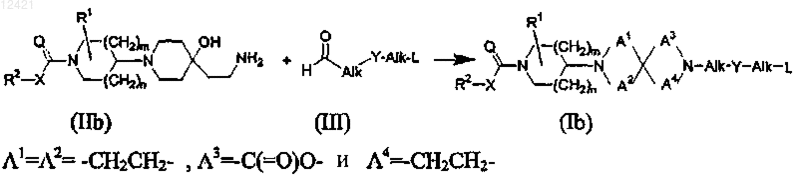
и, если требуется, превращением соединений формулы (Ib) одно в другое, следуя известным в данной области превращениям, и дополнительно, если требуется, превращением соединений формулы (Ib) в терапевтически активную нетоксичную кислотно-аддитивную соль обработкой кислотой, или в терапевтически активную нетоксичную основно-аддитивную соль обработкой основанием, или, наоборот, превращением кислотно-аддитивной соли в свободное основание обработкой щелочью, или превращением основно-аддитивной соли в свободную кислоту обработкой кислотой; и, если требуется, получением стереохимически изомерных форм, их N-оксидов и четвертичных аммониевых солей.
17. Способ по п.15 или 16, характеризующийся тем, что фрагмент Alk-Y-Alk-L- в соединениях формул (IIa), (Ia) и (Ib) и фрагмент Alk-L- в соединении формулы (III) является бензилом.
Текст
012421 Область техники, к которой относится изобретение Это изобретение касается замещенных производных оксадиазаспиро[5.5]ундеканона, имеющих антагонистическую активность в отношении нейрокинина, в частности, NK1-антагонистическую активность, NK3-антагонистическую активность, объединенную NK1/NK2-антагонистическую активность и объединенную NK1/NK2/NK3-антагонистическую активность, их получения, композиций, их содержащих, и их применения в качестве лекарственного средства, в частности, для лечения и/или профилактики шизофрении, рвоты, тревожности и депрессии, синдрома раздраженного кишечника (IBS), нарушений циркадного ритма, преэклампсии, ноцицепции, боли, в частности, висцеральной и невропатической боли,панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких(ХОЗЛ) и расстройств мочеиспускания, таких как недержание мочи. Уровень техники Тахикинины относятся к семейству короткоцепочечных пептидов, широко распространенных в центральной и периферической нервной системе млекопитающих (Bertrand and Geppetti, Trends Pharmacol.Sci. 17: 255-259 (1996); Lundberg, Can. J. Physiol. Pharmacol. 73: 908-914 (1995); Maggi, Gen. Pharmacol. 26: 911-944 (1995); Regoli et al., Pharmacol. Rev. 46 (1994. Они имеют общую С-концевую последовательность аминокислот Phe-Xaa-Gly-Leu-Met-NH2. Тахикинины высвобождаются из периферических сенсорных нервных окончаний, и, как полагают, они участвуют в нейрогенном воспалении. В спинном мозге/центральной нервной системе тахикинины играют роль в передаче/восприятии болевых ощущений и в некоторых вегетативных рефлексах и поведении. Тремя главными тахикининами являются вещество Р (SP), Нейрокинин A (NKA) и Нейрокинин В (NKB) с преимущественной афинностью к трем различным подтипам нейрокининовых рецепторов, называемых NK1, NK2 и NK3, соответственно. Однако функциональные исследования клонированных рецепторов позволяют предположить сильное функциональное перекрестное взаимодействие между 3 тахикининами и их соответствующими нейрокининовыми рецепторами (Maggi and Schwartz, Trends Pharmacol. Sci 18: 351-355 (1997. Видовые отличия в структуре NK1-рецепторов обусловливают видозависимые различия активности(1994. Человеческий NK1-рецептор имеет большое сходство с NK1-рецептором морских свинок и песчанок, но в значительной мере отличается от NK1-рецепторов грызунов. Исследование антагонистов нейрокинина привело, на сегодняшний день, к получению серии пептидных соединений, которые, как может ожидаться, являются метаболически слишком лабильными для применения в качестве фармацевтически активных веществ (Longmore J. et al., DNP 8(1):5-23 (1995. Тахикинины участвуют в патогенезе шизофрении, депрессии, тревожных состояний (стрессобусловленных), рвоты, воспалительных реакций, сокращения гладкой мускулатуры и восприятия боли. Антагонисты нейрокинина находятся в разработке для таких показаний, как рвота, тревожность и депрессия, синдром раздраженного кишечника (IBS), нарушения циркадного ритма, висцеральная боль,нейрогенное воспаление, астма, расстройства мочеиспускания и ноцицепция. Особенно NK1 антагонисты имеют высокий терапевтический потенциал в отношении рвоты и депрессии и NK2 антагонисты имеют высокий терапевтический потенциал в лечении астмы. NK3-антагонисты, вероятно,играют роль в лечении боли/воспаления (Giardina, G. et al. Exp. Opin. Ther. Patents, 10(6): 939-960 (2000 и шизофрении. Шизофрения Недавно было показано, что NK3-антагонист SR142801 (Sanofi), не вызывая отрицательных симптомов, имеет антипсихотическую активность у пациентов с шизофренией (Arvantis, L. ACNP Meeting,December 2001). Активация NK1-рецепторов вызывает тревожность, стрессовые события вызывают повышение уровня вещества Р (SP) в плазме крови и было показано на нескольких животных моделях, чтоNK1-антагонисты являются анксиолитиками. NK1-антагонист, полученный от Merck MK-869, демонстрирует антидепрессивные эффекты в лечении большой депрессии, но данные не позволили сделать какие-либо выводы ввиду высокого уровня реакции на плацебо. Более того, NK1-антагонист, полученный от Glaxo-Welcome (S)-GR205171, как было показано, усиливал выброс допамина во фронтальной коре,но не в стриатуме (Lejeune et al. Soc. Neurosci., November, 2001). Следовательно, было предположено, чтоNK3-антагонизм в комбинации с NK1-антагонизмом будет оказывать положительный эффект против как позитивных, так и отрицательных симптомов шизофрении. Тревожность и депрессия Депрессия является одним из наиболее распространенных аффективных расстройств в современном обществе с высокой и еще повышающейся степенью превалирования, особенно среди молодых членов популяции. Уровень заболеваемости в течение жизни большой депрессией (MDD, DSM-IV) в настоящее время оценивается, как равный 10-25% у женщин и 5-12% для мужчин, в то время как у примерно 25% пациентов пожизненная MDD является рецидивирующей без полного промежуточного восстановления и накладывается на дистимическое расстройство. Существует высокий уровень совместной заболеваемости депрессией с другими психическими расстройствами и, особенно, среди популяции молодых людей,высок уровень связи с зависимостью от наркотиков и алкоголя. Ввиду того, что депрессия в основном поражает популяцию в возрасте между 18-44 годами, то есть наиболее продуктивную популяцию, оче-1 012421 видно, что она наносит значительный ущерб отдельным людям, семьям и всему обществу. Среди всех терапевтических возможностей, терапия антидепрессантами является бесспорно наиболее эффективной. Огромное количество антидепрессантов было создано и выпущено на рынок в течение последних 40 лет. Тем не менее, ни один из существующих антидепрессантов не удовлетворяет всем критериям идеального лекарства (высокая терапевтическая и профилактическая эффективность, быстрое начало действия, абсолютно приемлемая безопасность при коротком и длительном применении, простая и удобная фармакокинетика) или не имеет побочных эффектов, которые тем или иным образом ограничивают применение во всех группах и подгруппах пациентов с депрессией. Вследствие того, что в настоящее время не только не существует лечения причины депрессии, и оно, по-видимому, не будет получено в ближайшее время, и не существует антидепрессанта, эффективного у более чем 60-70% пациентов; оправдана разработка нового антидепрессанта, который может обойти любые недостатки доступных лекарств. Некоторые открытия показали участие SP в состояниях тревожности, вызванных стрессом. Центральное введение вещества Р индуцирует сердечно-сосудистую реакцию, напоминающую классическую реакцию "борьба или полет", физиологически характеризующуюся дилатацией сосудов в скелетных мышцах и снижением брыжеечного и почечного кровотока. Эта сердечно-сосудистая реакция сопровождается поведенческой реакцией, наблюдаемой у грызунов после повреждающих стимулов или стресса(Culman and Unger, Can. J. Physiol. Pharmacol. 73: 885-891 (1995. У мышей системно введенные NK1 агонисты и антагонисты являются анксиогенными и анксиолитическими агентами, соответственно(Teixeira et al., Eur. J. Pharmacol. 311: 7-14 (1996. Способность NK1-антагонистов ингибировать возбуждение, вызванное SP (или электрошоком; Ballard et al., Trends Pharmacol. Sci. 17: 255-259 (2001 может соответствовать этой антидепрессантной/анксиолитической активности, в то время как у песчанок возбуждение играет роль сигнала оповещения или предупреждения для особей этого же вида.NK1-рецептор широко распространен в лимбической системе и в путях развития страха в мозге,включая миндалевидное тело, гиппокамп, перегородку, гипоталамус и periaqueductal grey. Дополнительно вещество Р центрально высвобождается в ответ на травматические или повреждающие стимулы и передача нервного импульса, связанная с веществом Р может давать вклад в или участвовать в тревожности, страхе и эмоциональных расстройствах, которые сопровождают аффективные расстройства, такие как депрессия и тревожность. В подтверждение этой точки зрения могут наблюдаться изменения в содержании вещества Р в отдельных участках мозга в ответ на стрессовые стимулы (Brodin et al., Neuropeptides 26: 253-260 (1994. Центральное введение миметиков (агонистов) вещества Р индуцирует развитие ряда защитных поведенческих и сердечно-сосудистых изменений включая изменяемое отвращение к месту нахождения(Elliott, Exp. Brain. Res. 73: 354-356 (1988, потенцируемую акустическую реакцию испуга (Krase et al,Behav. Brain. Res. 63: 81-88 (1994, стрессовые вокализации, реакция избегания (Kramer et al, Science 281: 1640-1645 (1998 и тревожность на приподнятом крестообразном лабиринте (Aguiar and Brandao,Physiol. Behav. 60: 1183-1186 (1996. Эти соединения не изменяют моторную активность и координацию на аппарате rotarod или способность передвигаться в клетке. Понижающая регуляция биосинтеза вещества Р происходит в ответ на введение известных анксиолитиков и антидепрессантов (Brodin et al, Neuropeptides 26: 253-260 (1994); Shirayama et al, Brain. Res. 739: 70-78 (1996. Сходным образом, индуцируемый системно вводимым NK1-агонистом голосовой ответ у морских свинок может быть антагонизирован антидепрессантами, такими как имипрамин и флуоксетин, также как L-733060, NK1-антагонистом. Эти исследования обеспечивают опыт, который показывает, что блокада центральных NK1-рецепторов может ингибировать психологический стресс по механизму, напоминающему действие антидепрессантов и анксиолитиков (Rupniak and Kramer, Trends Pharmacol. Sci. 20: 1-12 (1999, но без побочных эффектов настоящих лекарственных препаратов. Рвота Тошнота и рвота находятся среди наиболее тяжелых побочных эффектов химиотерапии рака. Они снижают качество жизни и могут вынудить пациентов откладывать или отвергать потенциальные лекарственные средства (Kris et al, J. Clin. Oncol, 3: 1379-1384 (1985. Частота, интенсивность и характер рвоты определяется различными факторами, такими как химиотерапевтический агент, дозировка и способ введения. Обычно, ранняя или острая рвота начинается в пределах первых 4 ч после химиотерапии, достигая пика между 4 ч и 10 ч, и снижаясь к 12-24 ч. Отсроченная рвота (развивающаяся после 24 ч и длящаяся до 3-5 дней после химиотерапии) наблюдается в отношении химиотерапевтических лекарств с высоким тошнотворным эффектом (уровень 4 и 5 в соответствии с Hesketh et al., J. Clin. Oncol. 15: 103(1997. У людей эти противораковые терапии с высоким тошнотворным эффектом, включающие цисплатин, индуцируют острую рвоту в 98% и отсроченную рвоту у 60-90% раковых больных. Животные модели химиотерапии, такие как цисплатин-индуцированная рвота у хорьков (Rudd andNaylor, Neuropharmacology 33: 1607-1608 (1994); Naylor and Rudd, Cancer. Surv. 21: 117-135 (1996, успешно предсказали клиническую эффективность антагонистов 5-НТ 3 рецепторов. Несмотря на то, что это открытие привело к успешной терапии недомогания, вызванного химиотерапией и радиацией у раковых больных, антагонисты 5-НТ 3, такие как ондансетрон и гранисетрон (или ассоциированные или нет с-2 012421 дексаметазоном), эффективны в контролировании острой фазы рвоты (первые 24 ч), но могут только уменьшить развитие отсроченной рвоты (24 ч) со слабой эффективностью (De Mulder et al., Annuals ofInternal Medicine 113:834-840 (1990); Roila, Oncology 50: 163-167 (1993. Несмотря на эти в настоящее время наиболее эффективные средства для предотвращения как острой, так и отсроченной рвоты, еще 50% пациентов страдают от отсроченной рвоты и/или тошноты (Antiemetic Subcommittee, Annals Oncol. 9:811-819 (1998. В противоположность 5-НТ 3 антагонистам, теперь было показано, что NK1 - антагонисты, такие как СР-99994 (Piedimonte et al., L. Pharmacol. Exp. Ther. 266: 270-273 (1993 и апрепитант (также известный как МК-869 или L-754030; Kramer et al., Science 281: 1640-1645 (1998); Rupniak and Kramer, Trends Pharmacol. Sci. 20: 1-12 (1999 ингибируют не только острую, но и отсроченную фазу цисплатининдуцированной рвоты у животных (Rudd et al., Br. J. Pharmacol. 119:931-936 (1996); Tattersall et al., Neuropharmacology 39: 652-663 (2000. Было также показано, что NK1-антагонисты уменьшают отсроченную рвоту у человека в отсутствие сопутствующей терапии (Cocquyt et al., Eur. J. Cancer 37: 835-842(2001); Navari et al., N. Engl. L. Med. 340: 190-195 (1999. При введении совместно с дексаметазоном и 5 НТ 3 антагонистами, более того, было показано, что NK1-антагонисты (такие как MK-869 и CJ-11974,также известный как Эзлопитант) вызывают дополнительные эффекты в отношении предотвращения острой рвоты (Campos et al., J. Clin. Oncol. 19: 1759-1767 (2001); Hesketh et al., Clin. Oncol. 17: 338-343(1999. Центральные рецепторы нейрокинина NK1 могут играть основную роль в регуляции рвоты. Антагонисты NK1 активны против широкого ряда стимулов рвоты (Watson et al., Br. J. Pharmacol. 115 84-94nucleus tractus solitarius. Кроме NK1-антагонизма, проникновение в ЦНС является, таким образом, предпосылкой для противорвотной активности этих соединений. Рвота, индуцируемая у хорьков лоперамидом, может быть использована в качестве быстрой и надежной модели скрининга для противорвотной активности NK1-антагонистов. Дополнительное увеличение их терапевтического значения в лечении как острой, так и отсроченной фаз цисплатин-индуцируемой рвоты было показано в созданной модели на хорьках (Rudd et al., Br. J. Pharmacol. 119: 931-936 (1994. Эта модель позволяет изучить острую и отсроченную рвоту после цисплатина, которая была подтверждена в показателях чувствительности по отношению к антагонистам 5-НТ 3 рецепторов, глюкокортикоидам (Sam et al., Eur. J. Pharmacol. 417: 231237 (2001 и другим фармакологическим агентам. Маловероятно то, что любое будущее вещество от рвоты найдет клиническое применение, если только не успешное лечение как острой, так и отсроченной фаз рвоты. Висцеральная боль и синдром раздраженного кишечника (IBS) Висцеральное ощущение относится ко всей сенсорной информации, возникающей во внутренних органах (сердце, легких, желудочно-кишечном тракте, печеночно-желчном и уро-генитальном тракте),передающейся в центральную нервную систему, приводя к сознательному восприятию. Блуждающий нерв посредством узловатого ганглия и первичные симпатические афферентные нервы посредством заднекорешковых ганглиев (ЗКГ) и нейроны второго порядка в спинном роге служат начальными путями,по которым висцеральная сенсорная информация передается в ствол головного мозга и в соматовисцеральную кору. Висцеральная боль может быть вызвана процессами новообразования (например, рак поджелудочной железы), воспалением (например, холециститом, перитонитом), ишемией и механической обструкцией (например, камень в уретре). Основа медицинского воздействия в отношении висцеральной боли, сопряженной с органическими нарушениями (в данном случае рак внутренних органов), все еще сфокусирована на опиатах. Последние данные позволяют предположить, что неорганические висцеральные нарушения, такие как синдром раздраженного кишечника (IBS), боль в груди, не связанная с сердцем (NCCP), хроническая боль в области таза могут происходить от состояния "висцеральная гипералгезия". Последняя определяется как состояние, при котором физиологические, неболевые висцеральные стимулы (например, растяжение кишки) приводят к сознательному восприятию боли ввиду сниженного порога восприятия боли. Висцеральная гипералгезия может отражать состояние постоянного, поствоспалительного возвращения к исходному состоянию порога деполяризации мембраны в синапсах нейронах в пределах висцеральных сенсорных путей. Первоначальное воспаление может происходить на периферии (например, инфекционный гастроэнтерит) или в месте интеграции висцеральной сенсорной информации (нейрогенное воспаление в задних корешках). Было показано, что SP и пептид, связанный с геном кальцитонина (CGRP), действуют в качестве противовоспалительных нейропептидов в нейрогенном воспалении. Висцеральная гипералгезия в настоящее время рассматривается как одно из первых направлений разработки лекарственных средств, имеющего своей целью лечение функциональных заболеваний кишечника, которые случаются у 15-25% популяции Запада. Они составляют огромную социоэкономическую проблему в аспектах стоимости медицинского обеспечения, стоимости лечения и прогулов. Компоненты лечения в настоящее время, среди прочих, включают противоспазматические агенты (IBS иNCCP), агенты, усиливающие моторику (например, tegasorod при IBS с преобладанием запора), слаби-3 012421 тельные средства (IBS с преобладанием запора), и лоперамид (IBS с преобладанием диареи). Как было показано, ни один из этих подходов не является очень эффективным, особенно в лечении боли. Небольшая доза трициклических антидепрессантов и SSRI применяются для лечения висцеральной гипералгезии при IBS с преобладающей болью, но оба класса соединений могут иметь значительные эффекты в отношении проходимости толстого кишечника. Продолжающиеся исследования в этой области выявили значительное количество молекулярных мишеней, которые могут служить для разработки лекарственных средств против висцеральной гипералгезии. Они включают рецепторы к нейрокинину, рецепторCGRP, рецепторы 5-НТ 3, глутаматные рецепторы, и каппа-опиоид рецептор. Идеально, если "висцеральное обезболивающее соединение" блокирует повышенную передачу ощущения от внутренних органов к ЦНС без воздействия на нормальный физиологический гомеостаз желудочно-кишечного тракта в отношении проталкивающей двигательной активности, абсорбции и секреции и ощущения. Существуют очевидные доказательства того, что тахикинин связан с висцеральной ноцицептивной сигнальной системой. Множество доклинических публикаций о роли NK1-, NK2- и NK3-рецепторов в висцеральной боли и висцеральной гипералгезии показывает различие между участием NK1-, NK2- и NK3-рецепторов в различных моделях гиперчувствительности грызунов при воспалении. Недавно, Kamp et al., J. Pharmacol. Exp. Ther. 299: 105-113 (2001) предположили, что антагонист рецептора нейрокинина общего действия может быть более активным, чем селективный антагонист рецептора нейрокинина. Вещество Р и NK1-, NK2- и NK3 рецепторы увеличены при клинических болевых состояниях, включая состояния висцеральной боли (Leeet al., Gastroenterol. 118: A846 (2000. Учитывая последние неудачи при использовании антагонистов рецептора NK1 в качестве аналгетиков в исследованиях человеческой боли (Goldstein et al., Clin. Pharm.Ther. 67: 419-426 (2000, может быть необходимым наличие значительного клинического эффекта у комбинаций антагонистов. Антагонисты NK3 рецептора являются антигипералгезическими средствами(Julia et al, Gastroenterol. 116: 1124-1131 (1999); J. Pharmacol. Exp. Ther. 299: 105-113 (2001. Недавно было показано участие NK1- и NK3-рецепторов, но не NK2-рецепторов, на уровне спины в висцеральной гиперчувствительности, опосредованной ноцицептивными и не ноцицептивными афферентными стимулами (GaudreauPloudre, Neurosci. Lett. 351: 59-62 (2003. Комбинирование антагонистической активности NK1-2-3 может, следовательно, представлять собой интересную терапевтическую мишень для разработки новых принципов терапии висцеральной гипералгезии. Было опубликовано некоторое количество доклинических публикаций о роли NK1-рецепторов в висцеральной боли. При использовании мышей с выбитым NK1-рецептором и NK1-антагонистов в животных моделях, различные группы показали важную роль, играемую NK1-рецептором в гипералгезии и висцеральной боли. Локализация NK1-рецепторов и вещества Р играет основную роль скорее в висцеральной, чем в соматической боли. Действительно, более 80% висцеральных первичных афферентов содержат вещество Р по сравнению с только 25% афферентов кожи. NK1-рецепторы также участвуют в моторике желудочно-кишечного тракта (Tonini et al., Gastroenterol. 120: 938-945 (2001); Okano et al., J.Pharmacol. Exp. Ther. 298: 559-564 (2001. Ввиду наличия этой двойной роли в моторике желудочнокишечного тракта и в ноцицепции, считается, что NK1-антагонисты способны улучшать симптомы у пациентов с синдромом раздраженного кишечника. Недержание мочи Неотложное недержание мочи обусловлено гиперрефлексией мочевого пузыря или детрузора ("раздражимый пузырь"). Эта гиперрефлексия связана с повышенной возбудимостью С-волокон сенсорных афферентов мочевого пузыря, идущих к спинному мозгу. Происхождение повышенной возбудимости С-волокон имеет множество причин, но обнаруживается, например, после инфицирования мочевого пузыря и хронического растяжения стенки мочевого пузыря (например, при доброкачественной гиперплазии простаты, ВРН). Таким образом, лечение должно быть направлено на снижение повышенной возбудимости нейронов. Впрыскивание в мочевой пузырь ваниллоидов (например, капсаицина) приводит к длительному положительному эффекту на повышенную возбудимость детрузора, не поддающуюся обычному лечению антихолинергическими лекарственными препаратами. Аналогично исследованиям на животных, эффект ваннилоидов обусловлен нейротоксическим эффектом на сенсорные нервные окончания. В мочевом пузыре человека субэндотелиальные сенсорные нервные окончания содержат тахикинины, которые вызывают повышенную возбудимость детрузора. NK-рецепторы, участвующие в этом влиянии, представлены периферическими NK2-рецепторами и,в меньшей степени, также NK1-рецепторами. Было заявлено, что последние играют роль в повышенной возбудимости мочевого пузыря на уровне спинного мозга. Как следствие, центрально действующийNK1/действующий на периферии антагонист NK2 предпочтителен для лечения повышенной возбудимости детрузора. Интересно, что активация NK2 рецепторов повышает ароматазную активность в клетках Сертоли. Антагонисты NK2 рецепторов снижают уровни тестостерона в сыворотке крови мышей, и это может иметь терапевтическую значимость в лечении ВРН. Известный уровень техники Соединения, содержащие пиперидинил-фрагмент, замещенный пиперидинилом или пирролидинилом, были опубликованы в WO 97/24324 (июль 10, 1997), WO 97/24350 (июль 10, 1997) и WO 97/24356(июль 10, 1997), все - Janssen Pharmaceutica N. V. для применения в качестве антагонистов вещества Р(нейрокинина). Соединения, содержащие замещенный диазаспиро[4.5]деканил-фрагмент были опубликованы в WO 01/94346 (декабрь 13, 2001) F. Hoffmann-La Roche AG для применения в качестве антагонистов рецептора нейрокинина. Соединения настоящего изобретения структурно отличаются от соединений предыдущего уровня техники как тем, что все соединения настоящего изобретения содержат пиперидинил-фрагмент, замещенный фрагментом оксадиазаспиро[5.5]ундеканона, так и их улучшенной способностью служить мощными, перорально и центрально активными антагонистами нейрокинина с терапевтической значимостью, особенно для лечения и/или профилактики шизофрении, рвоты, тревожности и депрессии, синдрома раздраженного кишечника (IBS), нарушений циркадного ритма, преэклампсии, ноцицепции, боли,особенно висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (ХОЗЛ) и расстройств мочеиспускания, такого как недержание мочи. Описание изобретения Настоящее изобретение касается новых замещенных производных оксадиазаспиро[5.5]ундеканона формулы (I) их фармацевтически приемлемых кислотно-аддитивных или основно-аддитивных солей, их стереохимически изомерных форм, их N-оксидной формы и их пролекарств, гдеX представляет собой ковалентную связь или двухвалентный радикал формулы -O-, -S- или -NR3-;Q представляет собой О или NR3; каждый R3 независимо один от другого представляет собой водород или алкил;R1 выбирают из группы Аr1, Ar1-алкила и ди(Ar1)-алкила;n представляет собой целое число, равное 0, 1 или 2;m представляет собой целое число, равное 1 или 2, при условии, что если m представляет собой 2,тогда n представляет собой 1;Z представляет собой ковалентную связь или двухвалентный радикал формулы -СН 2- или С(=O); А 1, А 2, А 3 и А 4, каждый независимо друг от друга, выбирают из группы -СН 2 СН 2-, -С(=O)O- и-OC(=O)-, при условии, что, по меньшей мере, выбирают один из -С(=O)O- и -OC(=O)-, и что =O располагается в альфа-положении по отношению к N-атому; каждый Alk представляет независимо один от другого ковалентную связь; двухвалентный прямой или разветвленный, насыщенный или ненасыщенный углеводородный радикал, имеющий от 1 до 6 атомов углерода; или циклический насыщенный или ненасыщенный углеводородный радикал, имеющий от 3 до 6 атомов углерода; каждый радикал необязательно замещен по одному или более атомам углерода одним или более радикалами, выбираемыми из фенила, галогена, циано, гидрокси, формила и амино;Y представляет собой ковалентную связь или двухвалентный радикал формулы -C(=O)-, -SO2-,C=CH-R или C=N-R, где R представляет собой Н, CN или нитро;L выбирают из группы водорода, алкила, алкенила, алкилокси, алкилоксиалкилокси, алкилкарбонилокси, алкилоксикарбонила, моно- и ди(алкил)амино, моно- и ди(алкилоксикарбонил)амино, моно- и ди(алкилкарбонил)амино, моно- и ди(Ar3)амино, моно- и ди(Ar3 алкил)амино, моно- и ди(Het2)амино, моно- и ди(Het2 алкил)амино, алкилсульфонила, норборнила, адамантила, трициклоундецила, Ar3, Ar3-окси,Ar3 карбонила, Het2, Het-окси, Het2 карбонила и моно- и ди(Het2 карбонил)амино;Ar1 представляет собой фенил, необязательно замещенный 1, 2 или 3 заместителями, независимо один от другого выбранными из группы галогена, алкила, циано, аминокарбонила и алкилокси;Ar2 представляет собой нафталенил или фенил, каждый из которых необязательно замещен 1, 2 или 3 заместителями, каждый из которых независимо один от другого выбирают из группы галогена, нитро,амино, моно- и ди(алкил)амино, циано, алкила, гидрокси, алкилокси, карбоксила, алкилоксикарбонила,аминокарбонила и моно- и ди(алкил)аминокарбонила;Ar3 представляет собой нафталенил или фенил, необязательно замещенный 1, 2 или 3 заместителями, каждый из которых независимо один от другого выбирают из группы алкилокси, алкилкарбониламино, метансульфонила, Ar1 карбонилоксиалкила, Ar1 алкилоксикарбонила, Ar1 алкилоксиалкила, алкила,галогена, гидрокси, пиридинила, морфолинила, пирролила, пирролидинила, имидазо[1,2-а]пиридинила,морфолинилкарбонила, пирролидинилкарбонила, амино и циано;Het1 представляет собой моноциклический гетероциклический радикал, выбранный из группы пирролила, пиразолила, имидазолила, фуранила, тиенила, оксазолила, изоксазолила, тиазолила, изотиазолила, пиридинила, пиримидинила, пиразинила и пиридазинила; или бициклический гетероциклический радикал, выбранный из группы хинолинила, хиноксалинила, индолила, бензимидазолила, бензоксазолила, бензизоксазолила, бензотиазолила, бензизотиазолила, бензофуранила, бензотиенила, инданила и хро-5 012421 менила; где каждый моно- и бициклический гетероциклический радикал может быть необязательно замещен по любому из атомов одним или более радикалами, каждый из которых независимо один от другого выбирают из группы галогена, оксо и алкила;Het2 представляет собой моноциклический гетероциклический радикал, выбранный из группы пирролидинила, дигидро-2 Н-пиранила, пиранила, диоксолила, имидазолидинила, тетрагидропиридинила,тетрагидропиримидинила, пиразолидинила, пиперидинила, морфолинила, дитианила, тиоморфолинила,пиперазинила, имидазолидинила, тетрагидрофуранила, 2 Н-пирролила, пирролинила, имидазолинила,пиразолинила, пирролила, имидазолила, пиразолила, триазолила, фуранила, тиенила, оксазолила, диоксазолила, оксазолидинила, изоксазолила, тиазолила, тиадиазолила, изотиазолила, пиридинила, 1 Нпиридинила, пиримидинила, пиразинила, пиридазинила, триазинила и тетразолила; или бициклический гетероциклический радикал, выбранный из группы 2,3-дигидробензо[1,4]диоксина, октагидробензо[1,4]диоксина, октабициклогептила, бензопиперидинила, хинолинила, хиноксалинила, индолила, изоиндолила, хроманила, бензимидазолила, имидазо[1,2-а]пиридинила, бензоксазолила,бензодиоксолила, бензизоксазолила, бензоксадиазолила, бензотиазолила, бензизотиазолила, бензофуранила, дигидроизобензофуранила или бензотиенила; где каждый моно- и бициклический гетероциклический радикал может быть необязательно замещен по любому атому одним или более радикалами, выбранными из группы Ar1, Ar1 алкила, Ar1 алкилоксиалкила, галогена, гидрокси, алкила, пиперидинила,пирролила, тиенила, оксо, алкилокси, алкилкарбонила, Ar1 карбонила, моно- и ди(алкил)аминоалкила,алкилоксиалкила и алкилоксикарбонила; алкил представляет собой прямой или разветвленный насыщенный углеводородный радикал,имеющий от 1 до 6 атомов углерода, или циклические насыщенные углеводородные радикалы, имеющие от 3 до 6 атомов углерода; каждый углеводородный радикал необязательно замещен по одному или более атомам углерода одним или более радикалами, выбранными из группы фенила, галогена, тригалогенметила, аминокарбонила, метила, этила, пропила, изопропила, трет-бутила, циано, оксо, гидрокси,формила и амино; и алкенил представляет собой прямой или разветвленный ненасыщенный углеводородный радикал,имеющий от 1 до 6 атомов углерода и имеющий 1 или более ненасыщенных связей; или циклический ненасыщенный углеводородный радикал, имеющий от 3 до 6 атомов углерода и имеющий 1 или более ненасыщенных связей; каждый углеводородный радикал необязательно замещен по одному или более атомам углерода одним или более радикалами, выбранными из группы фенила, галогена, циано, оксо,гидрокси, формила и амино. Данное изобретение дополнительно касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм,формы N-оксида и его пролекарства в качестве лекарственного средства. Данное изобретение дополнительно касается композиций, содержащих соединение общей формулы(I), его фармацевтически приемлемую кислотно-аддитивную или основно-аддитивную соль, его стереохимически изомерные формы, форму N-оксида и его пролекарство, так же как и способов получения указанных соединений и указанных композиций в соответствии с данным изобретением. Данное изобретение дополнительно касается применения соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерной формы, для производства лекарственного средства для лечения состояний, опосредованных тахикинином, в частности, для лечения и/или профилактики шизофрении, рвоты, тревожности и депрессии, синдрома раздраженного кишечника (IBS), нарушений циркадного ритма, преэклампсии, ноцицепции, боли, в частности, висцеральной и невропатической боли, панкреатита, нейрогенного воспаления,астмы, хронического обструктивного заболевания легких (ХОЗЛ) и расстройств мочеиспускания, такого как недержание мочи. Подробное описание изобретения В частности, данное изобретение касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм,формы N-оксида и его пролекарства, где спиро-фрагмент имеет одну из следующих химических структур в соответствии с любой из формул (f1)-(f5), где все переменные определены как в формуле (I) и "а" обозначает пиперидинил-фрагмент формулы (I) и "b" обозначает Alk-Y-Alk-L-фрагмент формулы (I). Более конкретно, данное изобретение касается соединения общей формулы (I), его фармацевтиче-6 012421 ски приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства, где спиро-фрагмент имеет формулу (f1) или (f2), где переменные определены как в формуле (I) и "а" обозначает пиперидинил-фрагмент формулы (I) и "b" обозначает Alk-Y-Alk-L-фрагмент формулы (I). Более конкретно, данное изобретение касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства, где R1 представляет собой бензил и присоединен по 2-му положению, или R1 представляет собой фенил и присоединен по 3-му положению, как приведено в качестве примера в любой из следующих формул для соединений формулы (I), где m и n равны 1. Более конкретно, данное изобретение касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства, где фрагмент R2-X-C(=Q)- представляет собой 3,5-ди(трифторметил)фенилкарбонил. Более конкретно, данное изобретение касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства, где m и n оба равны 1. Более конкретно, данное изобретение касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства, где Z представляет собой ковалентную связь. Более конкретно, данное изобретение касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства, где Y представляет собой ковалентную связь или -C(=O)-. Более конкретно, данное изобретение касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства, где каждый Alk независимо от других представляет собой ковалентную связь или -СН 2-. Более конкретно, данное изобретение касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства, где L выбирают из группы водорода, изопропила, пентила,циклопропила, циклогексила, тетрагидрофуранила, пирролила, фуранила, тиенила, тиадиазолила, фенила, пиридинила и пиразинила. Предпочтительно, L представляет собой циклопропил. Более конкретно, данное изобретение касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства, гдеX представляет собой ковалентную связь;R1 представляет собой фенил или бензил;Z представляет собой ковалентную связь; А 1, А 2, А 3 и А 4, каждый независимо один от другого, выбирают из группы -СН 2 СН 2-, -С(=O)O- и-OC(=O)-, при условии, что выбран по меньшей мере один из -C(=O)O- и -OC(=O)- и что =O располагается в альфа-положении по отношению к N-атому;t является целым числом, равным 0; каждый Alk представляет собой независимо один от другого ковалентную связь или двухвалентный прямой, насыщенный углеводородный радикал, имеющий от 1 до 2 атомов углерода;Y представляет собой ковалентную связь или двухвалентный радикал формулы -С(=O)-;L выбирают из группы водорода, алкила, Ar3 и Het2;Ar3 представляет собой фенил, необязательно замещенный заместителем, выбранным из группы алкила, галогена и гидрокси;Het2 представляет собой моноциклический гетероциклический радикал, выбранный из группы тетрагидрофуранила, пирролила, фуранила, тиенила, тиадиазолила, пиридинила и пиразинила; где каждый моноциклический гетероциклический радикал может быть необязательно замещен по любому атому одним или более алкильными радикалами; и алкил представляет собой прямой или разветвленный насыщенный углеводородный радикал,имеющий от 1 до 6 атомов углерода или циклические насыщенные углеводородные радикалы, имеющие от 3 до 6 атомов углерода. Более конкретно, данное изобретение касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства, где соединение представляет собой соединение 1.4, как описано в данной заявке, в частности, в любой из таблиц, в частности в любой из табл. 1-2. В рамках данной заявки алкил определен как одновалентный прямой или разветвленный насыщенный углеводородный радикал, имеющий от 1 до 6 атомов углерода, например, метил, этил, пропил, бутил, 1-метилпропил, 1,1-диметилэтил, пентил, гексил; алкил дополнительно определяет одновалентный циклический насыщенный углеводородный радикал, имеющий от 3 до 6 атомов углерода, например,циклопропил, метилциклопропил, циклобутил, циклопентил и циклогексил. Определение алкила также включает алкильный радикал, который необязательно замещен по одному или более атомам углерода одним или более радикалами фенила, галогена, циано, оксо, гидрокси, формила и амино, например, гидроксиалкил, в частности, гидроксиметил и гидроксиэтил и полигалогеналкил, в частности, дифторметил и трифторметил. В рамках этой заявки галоген является общим названием радикала фтора, хлора, брома и иода. В рамках этой заявки под "соединениями в соответствии с данным изобретением" подразумевается соединение общей формулы (I), его фармацевтически приемлемая кислотно-аддитивная или основноаддитивная соль, его стереохимически изомерные формы, форма N-оксида и его пролекарство. В рамках этой заявки, особенно во фрагменте Alka-Y-Alkb в формуле (I), где два или более последовательных элемента указанного фрагмента обозначают ковалентную связь, тогда подразумевается одинарная ковалентная связь. Например, когда Alka и Y оба обозначают ковалентную связь и Alkb представляет собой -СН 2-, тогда фрагмент Alka-Y-Alkb обозначает -СН 2-. Сходным образом, если Alka, Y и Alkb каждый обозначают ковалентную связь и L обозначает Н, тогда фрагмент Alka-Y-Alkb-L обозначает -Н. Фармацевтически приемлемые соли определены как включающие терапевтически активные нетоксичные кислотно-аддитивные соли, которые соединения формулы (I) способны образовывать. Указанные соли могут быть получены воздействием на основные формы соединений формулы (I) подходящими кислотами, например, неорганическими кислотами, например, галогенводородной кислотой, в частности,хлористо-водородной, бромисто-водородной, серной, азотной и фосфорной кислотами; органическими кислотами, например, уксусной кислотой, гидроксиуксусной кислотой, пропановой, молочной, пировиноградной, щавелевой, малоновой, янтарной, малеиновой, фумаровой, яблочной, винной, лимонной, метансульфоновой, этансульфоновой, бензолсульфоновой, п-толуолсульфоновой, цикламовой, салициловой, п-аминосалициловой и памовой кислотой. Соединения формулы (I), содержащие кислые протоны, могут быть также переведены в их терапевтически активные нетоксичные соли присоединения металла или амина обработкой подходящими органическими и неорганическими основаниями. Подходящие формы основных солей содержат, например,аммонийные соли, соли щелочных и щелочноземельных металлов, в частности, соли лития, натрия, калия, магния и кальция, соли органических оснований, например, бензатина, N-метил-D-глюкамина, гидрамина и соли аминокислот, например, аргинина и лизина. Наоборот, указанные солевые формы могут быть переведены в свободные формы обработкой подходящим основанием или кислотой. Термин аддитивная соль, используемый в рамках этой заявки, также включает сольваты, которые соединения формулы (I), также как и их соли, способны образовать. Такие сольваты являются, например,гидратами и алкоголятами. Формы N-оксидов соединений формулы (I), как подразумевается, включают те соединения формулы (I), где один или несколько атомов азота окислены до так называемого N-оксида, особенно те Nоксиды, где имеется один или более третичных азотов (например, пиперазинил или пирролидинил) являются N-окисленными. Такие N-оксиды могут быть легко получены квалифицированным специалистом, не обладающим какими-либо изобретательскими навыками, и они являются очевидными альтернативами соединениям формулы (I), так как эти соединения являются метаболитами, которые образуются в результате окисления в организме человека после приема. Как в общем известно, окисление является обычно первым шагом метаболизма лекарства (Textbook of Organic Medicinal and Pharmaceutical Chenistry, 1977, pages 70-75). Как также в общем известно, форма метаболита соединения может быть также введена человеку вместо как такового соединения, возможно, с получением тех же эффектов. Соединения в соответствии с данным изобретением имеют по меньшей мере 2 окисляемых азота(фрагменты третичного амина). Следовательно, очень вероятно, что при метаболизме в организме человека образуются N-оксиды.-8 012421 Соединения формулы (I) могут быть превращены в соответствующие N-оксидные формы следуя методикам, известным в данной области для превращения трехвалентного азота в его N-оксидную форму. Указанная реакция N-окисления может быть, в общем, проведена взаимодействием исходного вещества формулы (I) с подходящим органическим или неорганическим перекисным соединением. Подходящие неорганические перекиси включают, например, пероксид водорода, пероксиды щелочных и щелочно-земельных металлов, например, пероксид натрия, пероксид калия; подходящие органические перекиси могут включать пероксикислоты, такие как, например, бензолпероксикарбоновая кислота, или галогензамещенную бензолпероксикарбоновую кислоту, например, 3-хлорбензолпероксикарбоновую кислоту, пероксиалкановые кислоты, например, пероксиуксусную кислоту, алкилгидроперекиси, например,трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие спирты, например, этанол и подобные, углеводороды, например, толуол, кетоны, например, 2-бутанон, галогенированные углеводороды, например, дихлорметан, и смеси таких растворителей. Термин "стереохимически изомерные формы", используемый здесь и ранее, определяет все возможные изомерные формы, которые соединения формулы (I) могут принимать. Если иначе не указано или не определено, химическое обозначение соединений обозначает смесь всех возможных стереохимически изомерных форм, имеющих такое обозначение, указанные смеси, содержащие все диастереомеры и энантиомеры основной молекулярной структуры. Более конкретно, стереогенные центры могут иметьR- или S-конфигурацию; заместители двухвалентных циклических (частично) замещенных радикалов могут иметь либо цис- или транс-конфигурацию. Соединения, имеющие двойные связи, могут иметь Еили Z-стереохимию двойной связи. Стереохимически изомерные формы соединений формулы (I) очевидно находятся в пределах объема данного изобретения. Следуя номенклатуре CAS, когда два стереогенных центра известной абсолютной конфигурации присутствуют в молекуле, обозначение R или S присваивается (основываясь на правиле Канна-ИнгольдаПрелога) хиральному центру с наименьшим номером, от которого ведется отсчет. R и S каждый обозначают оптически чистые стереогенные центры с неопределенной абсолютной конфигурацией. Если используются обозначения и : положение наиболее приоритетного заместителя на ассиметрическом атоме углерода в кольцевой системе, имеющего низший номер в кольце, всегда произвольно находится в положении средней плоскости, определяемой кольцевой системой. Положение заместителя наивысшего приоритета на другом ассиметрическом атоме углерода в кольцевой системе (атом водорода в соединениях формулы (I относительно положения заместителя наивысшего приоритета по отношению к атому отсчета обозначают , если он находится на той же стороне средней плоскости, определяемой кольцевой системой, или , если он находится на другой стороне средней плоскости, определяемой кольцевой системой. Соединения формулы (I) и некоторые из промежуточных соединений имеют по меньшей мере два стереогенных центра в их структуре. Данное изобретение также включает производные (обычно называемые "пролекарства") фармакологически активных соединений данного изобретения, которые разрушаются in vivo с образованием соединений данного изобретения. Пролекарства обычно (но не всегда) имеют меньшую активность в отношении мишени-рецептора, чем соединения, до которых они разрушаются. Пролекарства особенно применимы, когда интересующее соединение имеет химические или физические свойства, которые затрудняют введение или делают его неэффективным. Например, интересующее соединение может быть плохо растворимым, плохо транспортируемым через слизистую оболочку, или оно может иметь нежелательно короткий период полужизни в плазме. Дополнительное обсуждение пролекарств может быть найдено в Stella, V. J. et al., "Prodrugs", Drug Delivery Systems, 1985, pp. 112-176, и Drugs, 1985, 29, pp. 455473. Формы пролекарств фармакологически активных соединений в соответствии с данным изобретением являются, в основном, соединениями формулы (I), их фармацевтически приемлемыми кислотноаддитивными или основно-аддитивными солями, их стереохимически изомерными формами и его Nоксидной формой, имеющими кислотную группу, которая этерифицирована или амидирована. Включенными в такие этерифицированные кислотные группы являются группы формулы -COORx, где Rx представляет собой C1-6 алкил, фенил, бензил или одну из следующих групп: Амидированные группы включают группы формулы -CONRYRZ, где RY представляет собой Н, C1-6 алкил, фенил или бензил и RZ представляет собой -ОН, Н, C1-6 алкил, фенил или бензил. Соединения в соответствии с данным изобретением, имеющие амино группу, могут быть превращены в производные под действием кетона или альдегида, такого как формальдегид для образования основания Манниха. Это основание будет гидролизоваться первым в водном растворе.-9 012421 Соединения формулы (I), полученные в способах, описанных ниже, могут быть синтезированы в форме рацемических смесей энантиомеров, которые могут быть отделены один от другого, следуя известным в данной области методикам разделения. Рацемические соединения формулы (I) могут быть переведены в формы соответствующих диастереомерных солей реакцией с подходящей хиральной кислотой. Указанные формы диастереомерных солей последовательно разделяют, например, с помощью селективной или фракционированной кристаллизации и энантиомеры высвобождаются с помощью щелочи. Альтернативный способ разделения энантиомерных форм соединений формулы (I) включает жидкостную хроматографию с использованием хиральной неподвижной фазы. Указанные чистые стереохимически изомерные формы могут быть также получены из соответствующих чистых стереохимически изомерных форм подходящих исходных материалов, с обеспечением стереоспецифичности реакции. Предпочтительно, если интересует конкретный стереоизомер, указанное соединение будет синтезировано с помощью стереоспецифических способов получения. В этих способах преимущественно используются энантиомерно чистые исходные материалы. Фармакология Вещество Р и другие тахикинины участвуют во множестве биологических процессов, таких как передача болевых ощущений (ноцицепция), нейрогенное воспаление, сокращение гладких мышц, экстравазация белков плазмы крови, расслабление сосудов, секреция, дегрануляция тучных клеток и также в активации иммунной системы. Ряд заболеваний, как полагают, возникает за счет активации нейрокининовых рецепторов, в частности, рецептора NK1, за счет повышенного высвобождения вещества Р и других нейрокининов в отдельных клетках, таких как клетки в нейрональных сплетениях желудочно-кишечного тракта, немиелинизированных первичных сенсорных афферентных нейронах, симпатических и парасимпатических нейронах и ненейрональных клеточных типах (DNP 8(1):5-23 (1995) и Longmore J. et al.,"Neurokinin Receptors" Pharmacological Reviews 46(4): 551-599 (1994. Соединения настоящего изобретения являются потенциальными ингибиторами эффектов, опосредованных нейрокинином, в частности тех, что обусловлены рецепторами NK1, NK2 и NK3 и, следовательно, могут быть описаны как антагонисты нейрокинина, особенно, как антагонисты вещества Р, как это может быть определено in vitro релаксацией, вызванной антагонизмом вещества Р коронарных артерий свиньи. Аффинность связывания настоящих соединений в отношении нейрокининовых рецепторов человека, морской свинки и песчанки может быть также определена in vivo в тесте связывания с рецептором с использованием 3 Н-вещества-Р в качестве радиолиганда. Изучаемые соединения также демонстрируют антагонистическую активность в отношении вещества Р in vivo, что может быть доказано с помощью, к примеру, антагонизма индуцируемой веществом Р экстравазации белков плазмы у морских свинок, или антагонизма вызванной лекарствами рвоты у хорьков (Watson et al., Br. J. Pharmacol. 115:8494 (1995. Ввиду их способности антагонизировать действие тахикининов блокированием рецепторов нейрокинина, и в частности, блокированием рецепторов NK1, NK2 и NK3, соединения в соответствии с данным изобретением применимы в качестве лекарственных средств, в частности, в профилактическом и терапевтическом лечении тахикинин-опосредованных состояний. В частности они являются соединениями в соответствии с данным изобретением, которые применимы в качестве перорально активных, системно проникающих лекарственных средств в профилактическом и терапевтическом лечении тахикининопосредованных состояний. Более конкретно было обнаружено, что некоторые соединения проявляют объединенную NK1/NK2 антагонистическую активность и объединенную NK1/NK2/NK3 антагонистическую активность, как это можно видеть из таблицы в экспериментальной части. Данное изобретение, следовательно, касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм,формы N-оксида и его пролекарства, для применения в качестве лекарственного средства. Данное изобретение также касается соединения общей формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формыN-оксида и его пролекарств, для производства лекарственного средства для лечения, или профилактического или терапевтического или обоих, состояний опосредованных тахикинином. Соединения в соответствии с данным изобретением применимы в лечении расстройств ЦНС, в частности, шизоаффективных расстройств; депрессии; тревожных расстройств; расстройств, вызванных стрессом; расстройств сна; когнитивных расстройств; расстройств личности; расстройств, связанных с приемом пищи; нейродегенеративных заболеваний; расстройств, связанных с болезненным пристрастием; расстройств настроения; сексуальной дисфункции; висцеральной боли и других ЦНС-связанных состояний; воспаления; аллергических нарушений; рвоты; желудочно-кишечных расстройств, в частности,синдрома раздраженного кишечника (IBS); кожных заболеваний; вазоспастических заболеваний; фиброзных и коллагеновых заболеваний; расстройств, связанных с усилением или подавлением иммунитета; ревматоидных заболеваний; и для контроля массы тела. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике шизоаффективных расстройств, являющихся результатом различных причин, включая шизоаф- 10012421 фективные расстройства типа мании, депрессивного типа и смешанного типа; параноидальную, дезорганизованную, кататоническую, недифференцированную и остаточную шизофрению; шизофреноформное расстройство; бредовые расстройства; краткое психотическое расстройство; разделенное психотическое расстройство; психотическое расстройство, вызванное веществом; и психотическое расстройство иначе не определенное. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике депрессии, включая, но не ограничиваясь основными депрессивными расстройствами, включая биполярную депрессию; униполярную депрессию; единственные или повторяющиеся основные депрессивные эпизоды с или без психотических черт, кататонических черт, меланхолических черт, атипических черт или послеродового начала, и в случае повторяющихся эпизодов с или без сезонного характера. Другие расстройства настроения, охваченные термином "основное депрессивное расстройство", включают дистимическое расстройство с ранним или поздним началом и с или без атипических черт; биполярное расстройство I; биполярное расстройство II; циклотимическое расстройство; повторяющееся краткое депрессивное расстройство; смешанное аффективное расстройство; невротическую депрессию; посттравматическое стрессовое расстройство и социальную фобию; деменцию по типу Альцгеймера с ранним или поздним началом или с депрессивным настроением; васкулярную деменцию с депрессивным настроением; расстройства настроения, вызванные веществом, такие как расстройства настроения, вызванные алкоголем, амфетаминами, кокаином, галлюциногенами, ингалянтами, опиоидами, фенциклидином, седативными средствами, гипнотическими средствами, анксиолитиками и другими веществами; шизоаффективное расстройство депрессивного типа; и расстройство приспособляемости с депрессивным настроением. Основные депрессивные расстройства могут быть также результатом общего медицинского состояния, включающего, но не ограничиваясь ими, инфаркт миокарда, диабет, невынашивание или выкидыш и др. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике тревожных расстройств, включая, но не ограничиваясь ими, приступ панического беспокойства,боязнь открытых пространств, паническое расстройство с боязнью открытых пространств; боязнь открытых пространств без панического расстройства, специфическую фобию; социальную фобию; обсессивнокомпульсивное расстройство; расстройство, связанное с посттравматическим стрессом; расстройство,связанное с острым стрессом; генерализованное тревожное расстройство; тревожное расстройство, возникшее благодаря общему медицинскому состоянию; вызванное наркотиками тревожное расстройство и иначе не определенное тревожное расстройство. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике расстройств, вызванных стрессом, связанных с депрессией и/или тревожностью, включая, но не ограничиваясь, острой стрессовой реакцией; расстройствами приспособляемости, такими как краткая депрессивная реакция и пролонгированная депрессивная реакция; реакция тревожности и депрессии; расстройство приспособляемости с доминирующим расстройством других эмоций; расстройство приспособляемости с доминирующим расстройством поведения; расстройство приспособляемости со смешанным расстройством эмоций и поведения; расстройство приспособляемости с другими специфическими доминирующими симптомами; и другими реакциями на жесткий стресс. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике расстройств сна, включая, но не органичиваясь ими, дисомнии и/или парасомнии как первичные расстройства сна; апноэ во сне; нарколепсия; расстройства циркадного ритма; расстройства сна, связанные с другим психическим расстройством; расстройство сна, связанное с общим медицинским состоянием; и расстройство сна, связанное с приемом наркотиков. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике расстройств познавательной функции, включая, но не ограничиваясь ими, слабоумие; расстройства памяти и познавательной функции иначе не определенные, особенно слабоумие, обусловленное дегенеративными расстройствами, повреждениями, травмами, инфекциями, сосудистыми нарушениями,токсинами, гипоксией, недостатком витаминов или эндокринными нарушениями; слабоумие по типу Альцгеймера с ранним или поздним началом или с депрессивным настроением; слабоумие, связанное со СПИДом, или расстройства памяти, вызванные алкоголем или другими причинами недостатка тиамина,билатеральное повреждение височной доли, возникшее благодаря энцефалиту, вызванному простым герпесом, и другому лимбическому энцефалиту, потеря нейронов, вторичная по отношению к гипоксии/гипогликемии/выраженным судорогам и хирургическому вмешательству, дегенеративные расстройства, сосудистые расстройства или патология в районе желудочка III. Более того, соединения в соответствии с данным изобретением также применимы в качестве усилителей памяти и/или познавательной способности у здоровых людей с отсутствием недостатка в познавательной функции и/или памяти. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике расстройств личности, включая, но не ограничиваясь ими, параноидальное расстройство личности; шизоидное расстройство личности; шизотипическое расстройство личности; антисоциальное расстройство личности; пограничное расстройство личности; сценическое расстройство личности; нарциссическое расстройство личности; замкнутое расстройство личности; зависимое расстройство личности;- 11012421 обсессивно-компульсивное расстройство личности и иначе неопределенное расстройство личности. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике расстройств, связанных с приемом пищи, включая нервную анорексию, атипическую нервную анорексию; нервную булимию; атипическую нервную булимию; переедание, связанное с другими физиологическими расстройствами; рвоту, связанную с другими физиологическими нарушениями; и неопределенные расстройства пищеварения. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике нейродегенеративных заболеваний, включая, но не ограничиваясь ими, болезнь Альцгеймера; хорея Гентингтона; болезнь Крейфельда-Якоба; болезнь Пика; расстройства демиелинизации, такие как множественный склероз и боковой амиотрофический склероз (БАС); другие нейропатии и невралгия; множественный склероз; амиотрофический латеральный склероз; удар и травма головы. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике расстройств, связанных с аддикцией (болезненным пристрастием), включая но не ограничиваясь ими, зависимость от веществ или отмену с или без физиологической зависимости, особенно, когда веществом является алкоголь, амфетамины, амфетаминоподобные вещества, кофеин, кокаин, галлюциногены,ингалянты, никотин, опиоиды (такие как каннабис, героин и морфин) фенциклидин, фенциклидиноподобные вещества, седативно-гипнотические средства, бензодиазепины и/или другие вещества, особенно применимые для лечения синдрома отмены указанных выше веществ и алкогольного абстинентного делирия. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике расстройств настроения, вызванных, особенно, алкоголем, амфетаминами, кофеином, каннабисом, кокаином, галлюциногенами, ингалянтами, никотином, опиоидами, фенциклидином, седативными средствами, гипнотическими средствами, анксиолитиками и другими веществами. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике сексуальной дисфункции, включая, но не ограничиваясь, расстройства, связанные со снижением полового влечения; расстройства, связанные с половым возбуждением; расстройства оргазма; сексуальные расстройства, связанные с болью; сексуальное расстройство, возникшее в результате общего медицинского состояния; сексуальное расстройство, индуцированное веществами, и иначе не определенное сексуальное расстройство. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике боли, включая, но не ограничиваясь, травматическую боль, такую как боль после оперативного вмешательства; травматическую авульсивную боль, такую как плечевое сплетение; хроническую боль,такую как артритная боль, имеющая место при остеоревматоидном или псориатическом артрите; невропатическую боль, такую как постгерпетическая невралгия, невралгия тройничного нерва, сегментарная или межреберная невралгия, фибромиалгия, каузалгия, периферическая невропатия, диабетическая невропатия, невропатия, вызванная химиотерапией, невропатия, связанная со СПИДом, затылочная невралгия, невралгия при синдроме коленчатого ганглия, глоссофарингеальная невралгия, симпатическая рефлекторная дистрофия и фантомная боль в ампутированных конечностях; различные формы головной боли, такую как мигрень, острую или хроническую головную боль напряжения, височно-челюстную боль,боль в гайморовой пазухе и кластерная головная боль; зубную боль; раковую боль; висцеральную боль; боль в желудочно-кишечном тракте; боль при защемлении нерва; боль при спортивных повреждениях; дисменорею; менструальную боль; менингит; арахноидит; мышечно-скелетную боль; боль в поясничнокрестцовом отделе, такую как стеноз позвоночника, выпадение диска, воспаление седалищного нерва,ангину, анкилозирующий спондилоартрит; подагру; ожоги; боль рубца; зуд; и таламическую боль, например, таламическую боль после удара. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике следующих других ЦНС-связанных состояний: акинезия, синдром акинезии-ригидности, дискинезия и паркинсонизм, вызванный лекарственным средством, синдром Жилль де ла Туретта и его симптомы, тремор, хорея, миоклония, тики и дистония, расстройство дефицита внимания/гиперактивности(ADHD), болезнь Паркинсона, паркинсонизм, вызванная лекарствами, постэнцефалический паркинсонизм, прогрессивный надъядерный паралич, множественная системная атрофия, кортикобазальная дегенерация, комплекс паркинсонизма и слабоумия при БАС и кальцификации базальных ганглиев, расстройства поведения у слабоумных и людей с задержкой умственного развития, включая беспокойство и возбуждение, экстрапирамидальные двигательные расстройства, синдром Дауна и акатизию. В частности, соединения в соответствии с данным изобретением применимы в лечении или профилактике воспаления, включая, но не ограничиваясь ими, воспалительные состояния при астме, гриппе,хроническом бронхите и ревматоидном артрите; воспалительные состояния в желудочно-кишечном тракте, например, но не ограничиваясь ими, болезнь Крона, язвенный колит, воспалительное заболевание кишечника и повреждение, вызванное нестероидными противовоспалительными лекарствами; воспалительные состояния кожи, такие как герпес и экзема; воспалительные состояния мочевого пузыря, например, цистит и неотложное недержание мочи; воспаление глаз и зубов и панкреатит, в частности, хронический и острый панкреатит.- 12012421 В частности, соединения в соответствии с данным изобретением также применимы в лечении или профилактике аллергических нарушений, включая, но не ограничиваясь ими, аллергические поражения кожи, такие как, но не ограничиваясь ими, крапивница; и аллергические поражения дыхательных путей,такие как, но не ограничиваясь ими, ринит. В частности, соединения в соответствии с данным изобретением также применимы в лечении или профилактике рвоты, а именно морской болезни, отрыжки и рвоты, включая, но не ограничиваясь ими,острую рвоту, отсроченную рвоту и досрочную рвоту; рвоту, индуцированную лекарствами, такими как химиотерапевтические агенты, например, алкилирующие агенты, например, циклофосфамид, кармустин,ломустин и хлорамбуцил; цитотоксические антибиотики, например, дактиномицин, доксорубицин, митомицин-С и блеомицин; антиметаболиты, например, цитарабин, метотрексат и 5-фторурацил; алкалоиды барвинка, например, этопозид, винбластин и винкристин; и другие лекарства, такие как цисплатин,дакарбазин, прокарбазин и гидроксимочевина; и их комбинации; лучевая болезнь; радиационная терапия,например, в лечении рака; яды; токсины, например, токсины появление которых вызвано метаболическими нарушениями или инфекцией, такой как, гастрит, или высвобождаемые во время бактериальной или вирусной желудочно-кишечной инфекции; беременность; вестибулярные нарушения, такие как, укачивание в транспорте, истинное головокружение, головокружение и болезнь Меньяра; головокружение после оперативного вмешательства; желудочно-кишечная обструкция; сниженная желудочно-кишечная подвижность; висцеральная боль, такая как инфаркт миокарда или перитонит; мигрень; повышенное внутричерепное давление; сниженное внутричерепное давление (например, горная болезнь); опиоидные аналгетики, такие как морфин; болезнь желудочно-пищеводного рефлюкса; изжога; излишнее потребление еды или питья; повышенная кислотность желудочного сока; кислая отрыжка; изжога/регургитация; изжога, например, эпизодическая изжога, ночная изжога и изжога, вызванная едой; и диспепсия. В частности, соединения в соответствии с данным изобретением также применимы в лечении или профилактике желудочно-кишечных расстройств, включая, но не ограничиваясь ими, синдром раздраженного кишечника (IBS), кожные нарушения, такие как, псориаз, зуд и солнечный ожог; ангиоспастические заболевания, такие как ангина, сосудистая головная боль и болезнь Рейно, церебральная ишемия,например, церебральный сосудистый спазм с последующим субарахноидальным кровоизлиянием; фиброзные и коллагеновые болезни, такие как, склеродермия и эозинофильный фасциолез; нарушения, связанные с усилением или подавлением иммунитета, например, системная красная волчанка и ревматоидные заболевания, такие как, фиброзит; кашель; и контроль массы тела, включая ожирение. Более конкретно, соединение в соответствии с данным изобретением применимо для производства лекарственного средства для лечения и/или профилактики шизофрении, рвоты, тревожности и депрессии, синдрома раздраженного кишечника (IBS), нарушений циркадного ритма, преэклампсии, ноцицепции, боли, в частности, висцеральной и невропатической боли, панкреатита, нейрогенного воспаления,астмы, хронического обструктивного заболевания легких (ХОЗЛ) и расстройств мочеиспускания, таких как недержание мочи. Настоящее изобретение также касается способа лечения и/или профилактики шизофрении, рвоты,тревожности и депрессии, синдрома раздраженного кишечника (IBS), нарушений циркадного ритма, преэклампсии, ноцицепции, боли, в частности, висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (ХОЗЛ) и расстройств мочеиспускания, таких как недержание мочи, включающего введение пациенту эффективного количества соединения данного изобретения, в частности, в соответствии с формулой (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм,формы N-оксида и его пролекарств. Данное изобретение также касается фармацевтической композиции, содержащей фармацевтически приемлемый носитель и, в качестве активного ингредиента, терапевтически эффективное количество соединения данного изобретения, в частности, соединения в соответствии с формулой (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, формы N-оксида и его пролекарства. Соединения в соответствии с данным изобретением, в частности, соединения в соответствии с формулой (I), их фармацевтически приемлемые кислотно-аддитивные или основно-аддитивные соли, их стереохимически изомерные формы, форма N-оксида и их пролекарств, или любая подгруппа или их комбинация может быть сформулирована в различные фармацевтические формы для целей введения. В качестве подходящих композиций могут быть приведены все композиции, обычно применяемые для системно вводимых лекарств. Для получения фармацевтических композиций этого изобретения эффективное количество конкретного соединения, необязательно в форме аддитивной соли, в качестве активного ингредиента объединяют в однородной смеси с фармацевтически приемлемым носителем, где носитель может иметь широкий ряд форм в зависимости от желаемой формы препарата, требуемой для введения. Желательно, чтобы эти фармацевтические композиции находились в единично дозированной форме,подходящей, в частности, для введения перорально, ректально, подкожно, парентерально или ингаляционно. Например, в получении композиций в оральной дозированной форме, могут быть применены любые из обычных фармацевтических сред, таких как вода, гликоли, масла, спирты и тому подобные в слу- 13012421 чае пероральных жидких препаратов, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, разбавители, лубриканты, связующие агенты,дезинтегранты и тому подобные в случае порошков, пилюль, капсул и таблеток. Ввиду простоты введения, таблетки и капсулы представляют собой наиболее предпочтительные формы пероральных единиц дозирования, в которых очевидно используются твердые фармацевтические носители. Для парентеральных композиций носитель обычно содержит стерильную воду, по меньшей мере, в большом количестве,таким образом, что могут быть включены другие ингредиенты, например, для достижения растворимости. Могут быть получены, например, инъекционные растворы, в которых носитель включает солевой раствор, раствор глюкозы или смесь растворов соли и глюкозы. Могут быть также получены инъекционные суспензии, для чего могут быть использованы подходящие жидкие носители, суспендирующие агенты и тому подобные. Также используются препараты твердых форм, которые создаются для превращения незадолго до использования в препараты жидких форм. В композициях, подходящих для подкожного введения, носитель необязательно содержит агент, усиливающий проникновение и/или подходящий увлажняющий агент, необязательно объединенный с подходящими добавками любой природы в меньших пропорциях, причем добавки не наносят коже значительный повреждающий эффект. Указанные добавки могут облегчить введение в кожу и/или могут быть полезными в получении желаемых композиций. Эти композиции могут быть введены различными путями, например, в виде трансдермального пластыря, в виде наклейки, в виде мази. Особенно предпочтительно создавать указанные выше фармацевтические композиции в единичных дозированных формах для простоты введения и универсальности дозировки. Термин единичная дозированная форма, используемый в данном документе, относится к физически разделенным единицам дозирования, применимым в качестве единичных доз, где каждая единица содержит установленное количество активного ингредиента, которое, по подсчетам, должно оказать желаемый терапевтический эффект совместно с необходимым фармацевтическим носителем. Примерами таких единичных дозированных форм являются таблетки (включая таблетки с меткой или с покрытием), капсулы, пилюли, пакетики с порошком, облатки, суппозитории, инъекционные растворы или суспензии и подобные. Ввиду того, что соединения данного изобретения представляют собой активные пероральные, в основном центрально действующие антагонисты NK, особенно предпочтительны фармацевтические композиции, содержащие указанные соединения для перорального введения. Синтез Соединения в соответствии с данным изобретением могут быть, в основном, получены с помощью последовательных стадий, каждая из которых известна квалифицированному специалисту. Целевые соединения формулы (Ia) приемлемо получать взаимодействием промежуточного соединения формулы (IIa) с 1,1'-карбонилдиимидазолом. Взаимодействие может быть осуществлено в инертном растворителе, таком как, например, дихлорметан. Реакция может быть вполне проведена при комнатной температуре. Целевые соединения формулы (Ib) могут быть получены восстановительным N-алкилированием промежуточного соединения формулы (IIb) с промежуточным соединением формулы (III). Указанное восстановительное N-алкилирование может быть осуществлено в реакционно-инертном растворителе,таком как, например, дихлорметан, этанол или толуол или их смеси, и в присутствии подходящего восстанавливающего агента, такого как, например, боргидрид, например, боргидрид натрия, цианоборгидрид натрия или триацетоксиборгидрид. В случае, когда в качестве восстанавливающего агента используют боргидрид, может быть удобно использовать комплексообразующий агент, такой как, например,изопропилат титана (IV) как описано в J. Org. Chem, 1990, 55, 2552-2554. Может быть также удобно использовать водород в качестве восстанавливающего агента в комбинации с подходящим катализатором,таким как, например, палладий-на-угле. В случае, когда в качестве восстанавливающего агента используется водород, может быть предпочтительно добавлять в реакционную смесь дегидратирующий агент,такой как, например, трет-бутоксид алюминия. Для того, чтобы предотвратить нежелательную дальнейшую гидрогенизацию определенных функциональных групп в реактивы и продукты реакции может быть также предпочтительно добавлен соответствующий яд катализатора, например, тиофен или хинолинсера. Перемешивание и необязательно повышенные температуры и/или давление могут увеличить скорость реакции. Особенно предпочтительным является получение целевого соединения, в котором фрагмент Alk-YAlk-L- является бензилом. Указанное целевое соединение является фармакологически активным и может быть переведено в целевое соединение формулы (I'), в котором фрагмент Alk-Y-Alk-L- является водородом восстановительной гидрогенизацией с использованием, например, водорода в качестве восстанавливающего агента в комбинации с подходящим катализатором, таким как, например, палладий-на-угле или платина-на-угле. Полученное целевое соединение в соответствии с изобретением может быть переведено в другие соединения формулы (I) с помощью известных в данной области реакций, например, ацилирования и алкилирования. В частности, целевые соединения формулы (Ic) могут быть получены взаимодействием целевого соединения формулы (I') с промежуточным соединением формулы (IV), где W1 является соответствующей уходящей группой, такой как, например, галоген, например, хлор или бром или сульфонилокси уходящей группой, например, метансульфонилокси или бензолсульфонилокси. Реакция может быть проведена в реакционно-инертном растворителе, таком как, например, хлорированный углеводород, например,дихлорметан, или кетон, например, метилизобутилкетон, и в присутствии подходящего основания, такого, как, например, карбонат натрия, гидрокарбонат натрия или триэтиламин. Перемешивание может увеличить скорость реакции. Реакцию удобно проводить при температуре, варьирующей между комнатной и температурой образования флегмы. Альтернативно, целевые соединения формулы (Id) могут быть также получены взаимодействием целевого соединения формулы (I') с карбоновой кислотой формулы (V). Реакция может быть проведена в реакционно-инертном растворителе, таком как, например, хлорированный углеводород, например, дихлорметан, и в присутствии подходящего основания, такого, как, например, карбонат натрия, гидрокарбонат натрия или триэтиламин, и в присутствии активатора, такого как, например, DCC (дициклогексилкарбодиимид), CDI (карбонилдиимидазол) и EDCI. Реакцию удобно проводить при температуре, варьирующей между комнатной и температурой образования флегмы. Целевые соединения формулы (Ie) могут быть получены алкилированием целевого соединения формулы (I') с соединением формулы (VI), где W2 в формуле (VI) является соответствующей уходящей группой, такой как, например, галоген, например, хлор или бром, или сульфонилокси уходящей группой,например, метансульфонилокси или бензолсульфонилокси. Реакция может быть проведена в реакционно-инертном растворителе, таком как, например, хлорированный углеводород, например, дихлорметан,спирт, например, этанол, или кетон, например, метилизобутилкетон, и в присутствии подходящего основания такого, как, например, карбонат натрия, гидрокарбонат натрия или триэтиламин. Перемешивание может увеличить скорость реакции. Реакцию удобно проводить при температуре, варьирующей между комнатной и температурой образования флегмы. Целевые соединения формулы (If) могут быть получены восстановительным N-алкилированием промежуточного соединения формулы (I') с промежуточным соединением формулы (VII). Указанное восстановительное N-алкилирование может быть осуществлено в реакционно-инертном растворителе,таком как, например, дихлорметан, этанол или толуол или их смеси, и в присутствии подходящего восстанавливающего агента, такого как, например, боргидрид, например, боргидрид натрия, цианоборгидрид натрия или триацетоксиборгидрид. В случае, когда в качестве восстанавливающего агента используют боргидрид, может быть удобно использовать комплексообразующий агент, такой как, например,изопропилат титана (IV), как описано в J. Org. Chem, 1990, 55, 2552-2554. Может быть также удобно использовать водород в качестве восстанавливающего агента в комбинации с подходящим катализатором,таким как, например, палладий-на-угле или платина-на-угле. В случае, когда в качестве восстанавливающего агента используется водород, может быть предпочтительно добавлять в реакционную смесь дегидратирующий агент, такой как, например, трет-бутоксид алюминия. Для того, чтобы предотвратить нежелательную дальнейшую гидрогенизацию определенных функциональных групп в реактивы и продукты реакции может быть также предпочтительно добавлен соответствующий яд катализатора, например, тиофен или хинолин-сера. Перемешивание и необязательно повышенные температуры и/или давление могут повысить скорость реакции. Целевые соединения формулы (Ig) удобно получать с помощью реакции Манниха с бороновой кислотой, как описано в Tetrahedron, 1997, 53, 16463-16470; J. Am. Chem. Soc. 1998, 120, 11798-11799 илиTetrahedron Letters, 2002, 43, 5965-5968, с промежуточным соединением формулы (I') и промежуточными соединениями формул (VIII) и (IX), где Y в формуле (VIII) является двухвалентным радикалом формулы-СН 2- или С(=О), и W3 в формуле (IX) является водородом или алкильной цепью. Указанная реакция Манниха с бороновой кислотой может быть проведена в одном сосуде с углеводом или его димером формулы (VIII) и арилбороновой кислотой или арилбороновым эфиром формулы (IX) в реакционноинертном растворителе, таком как, например, дихлорметан, этанол или 2,2,2-трифторэтанол или их смеси. Перемешивание может увеличить скорость реакции. Реакцию удобно проводить при температуре,варьирующей между комнатной и температурой образования флегмы. Следующие примеры предназначены для иллюстрации, а не ограничения объема настоящего изобретения. Экспериментальная часть Здесь и далее "RT" подразумевает комнатную температуру, "CDI" подразумевает 1,1'карбонилдиимидазол, "DIPE" подразумевает простой диизопропиловый эфир, "MIK" подразумевает метилизобутилкетон, "BINAP" подразумевает [1,1'-динафталин]-2,2'-диилбис[дифенилфосфин], "NMP" подразумевает 1-метил-2-пирролидинон, "Pd2(dba)3" подразумевает трис(дибензилиденацетон)дипалладий, "DMF" подразумевает N,N-диметилформамид, "EDCI" подразумевает гидрохлорид 1-этил-3-(3 диметиламинопропил)карбодиимида и "НОВТ" подразумевает гидроксибензотриазол. Получение промежуточных соединений Пример А 1. а. Получение промежуточного соединения 1Et3N (0,55 моль) добавляли к перемешиваемой смеси 7-(фенилметил)-1,4-диокса-8-азаспиро[4.5]декана (0,5 моль) в толуоле (1500 мл). Добавляли 3,5-бис(трифторметил)бензоилхлорид (0,5 моль) в течение 1 ч (экзотермическая реакция). Смесь перемешивали при комнатной температуре в течение 2 ч, затем оставляли для отстаивания на выходные и промывали три раза водой (500 мл, 2250 мл). Органический слой отделяли, высушивали, фильтровали и растворитель выпаривали. Выход: 245 г (100%). Кристаллизация 2 г этой фракции из петролейного эфира давала 1 г промежуточного соединения 1. (50%).b. Получение промежуточного соединения 2HCl хч (300 мл) добавляли к смеси промежуточного соединения 1 (0,5 моль) в этаноле (300 мл) и Н 2 О (300 мл). Реакционную смесь перемешивали при 60 С в течение 20 ч. Осадок отфильтровывали, растирали, перемешивали в Н 2 О, отфильтровывали, промывали петролейным эфиром и высушивали. Выход: 192 г промежуточного соединения 2 +-)-1-[3,5-бис(трифторметил)бензоил]-2-(фенилметил)-4 пиперидинон) (89,4%) (смесь R и S энантиомеров). с. Получение промежуточного соединения 3 и промежуточного соединения 4 Промежуточное соединение 2 разделяли на оптические изомеры с помощью хиральной колоночной хроматографии на Chiralpak (CHIRALPAK AS 1000 А 20 mm (DAICEL); элюент: гексан/2-пропанол 7 0/30). Две фракции продукта собирали и каждый растворитель выпаривали. Выход фракции 1: 32,6 г промежуточного соединения 3 (R), и фракции 2: 30,4 г промежуточного соединения 4 (S). Пример А 2. а. Получение промежуточного соединения 5 и промежуточного соединения 11European Journal of Medicinail Chemistry (1974), 9(4), 416-23 содержание которого включено в данный документ посредством ссылки) (0,0723 моль), промежуточного соединения 2 (полученного в соответствии с A1.b) (0,082 моль) и Pd/C (3,57 г) в Ti(iPrO)4 (39 мл), СН 3 ОН (370 мл) и тиофена (2,5 мл) гидрогенизировали при 50 С в течение 30 ч под давлением в 3 бар, затем фильтровали через целит. Целит промывали CH3OH/CH2Cl2. Фильтрат упаривали. Остаток растворяли в CH2Cl2, вливали в Н 2 О, подщелачивали с помощью K2CO3 10% и Н 2 О, перемешивали в течение 10 мин и фильтровали через целит. Целит промывали несколько раз CH2Cl2. Фильтрат экстрагировали CH2Cl2. Органический слой промывали CH2Cl2,высушивали (MgSO4), фильтровали и растворитель выпаривали досуха. Остаток очищали колоночной хроматографией на Kromasil (элюент: CH2Cl2/CH3OH/NH4OH 90/10/0,1 до 90/10/0,4; 20-45 мкм). Чистые фракции собирали и растворитель выпаривали. Выход фракции 1: 3,8 г промежуточного соединения 5b. Получение промежуточного соединения 12N-этил-N-(1-метилэтил)-2-пропанамин (0,0059 моль) и затем трифосген (0,0014 моль) добавляли при 0 С к раствору промежуточного соединения 11 (полученного в соответствии с А 2.а) (0,0029 моль) вCH2Cl2 (100 мл). Смесь перемешивали в течение 2 ч. Добавляли Н 2 О и лед. Органический слой промывали NaCl, высушивали (MgSO4), фильтровали и растворитель выпаривали досуха. Остаток (1,2 г) очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2/CH3OH/NH4OH 97/3/0,1; 15-40 мкм). Чистые фракции собирали и растворитель выпаривали. Выход: 0,62 г промежуточного соединения 12 (2R-цис)c. Получение промежуточного соединения 13 Смесь промежуточного соединения 12 (полученного в соответствии с A2.b) (0,0009 моль) и Pd/C 10% (0,1 г) в СН 3 ОН (15 мл) гидрогенизировали при комнатной температуре в течение 18 ч под давлением в 3 бара, затем фильтровали через целит. Целит промывали CH2Cl2/CH3OH. Фильтрат упаривали. Выход: 0,46 г промежуточного соединения 13 (86%). Пример A3. а. Получение промежуточных соединений 6 и 7 Смесь промежуточного соединения 2 (полученного в соответствии с A1.b) (0,1 моль), 1,4-диокса-8 азаспиро[4.5]декана (0,1 моль) и Ti(iPrO)4 (0,1 моль) в СН 3 ОН (500 мл) гидрогенизировали при 50 С в атмосфере H2 с Pd/C 10% (5 г) в качестве катализатора в присутствии раствора тиофена (3 мл). После поглощения H2 (1 экв.), катализатор отфильтровывали и фильтрат упаривали. Остаток поглощали смесьюCH2Cl2/H2O и перемешивали в течение 15 мин. Органический слой отделяли, промывали Н 2 О, высушивали и растворитель выпаривали. Остаток очищали колоночной хроматографией на силикагеле (градиент элюента: CH2Cl2/СН 3 ОН 98/2, 97/3). Две фракции продукта собирали и их растворитель выпаривали. Выход фракции 1: 17 г (нечистый). Выход фракции 2: 12,7 г промежуточного соединения 6. Выход фракции 3: 13,7 г промежуточного соединения 7.b. Получение промежуточного соединения 8 Смесь промежуточного соединения 7 (полученного в соответствии с A3.а) (0,025 моль) в HCl (концентрированной) (200 мл) перемешивали в течение 4 ч при комнатной температуре. Реакционную смесь вливали в смесь льда/(50% раствора NaOH) и добавляли CH2Cl2. Органический слой отделяли, промывали 2 раза Н 2 О, высушивали и растворитель выпаривали. Добавляли толуол к остатку и растворитель выпаривали. Затем остаток кристаллизовали из DIPE. Выход: 10,85 г промежуточного соединения 8. с. Получение промежуточного соединения 9nBuLi 1,6 M (0,012 моль) добавляли медленно при -20 С к раствору изопропиламина (0,012 моль) вTHF (20 мл). Смесь охлаждали до -70 С. Медленно добавляли раствор ацетонитрила (0,012 моль) в THF(10 мл). Смесь перемешивали при -70 С в течение 1 ч. Медленно добавляли промежуточное соединение 8 (полученное в соответствии с А 3.b) (0,006 моль) в THF (40 мл). Смесь перемешивали при -78 С в течение 30 мин, вливали в насыщенный раствор NH4Cl и экстрагировали EtOAc. Органический слой отделяли, высушивали (MgSO4), фильтровали и растворитель выпаривали. Остаток (2,2 г) очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2/CH3OH/NH4OH 95/5/0,1; 15-40 мкм). Чистые фракции собирали и растворитель выпаривали. Выход: 1,2 г промежуточного соединения 9d. Получение промежуточного соединения 10 Смесь промежуточного соединения 9 (полученного в соответствии с A3.с) (0,002 моль) и NiRa (1,2 г) в MeOH/NH3 (20 мл) гидрогенизировали при комнатной температуре в течение 2 ч под давлением в 3 бара, затем фильтровали через целит. Целит промывали CH2Cl2/CH3OH. Фильтрат упаривали. Органический слой отделяли, высушивали (MgSO4), фильтровали и растворитель выпаривали. Выход: 1 г промежуточного соединения 10 (82%). Получение целевых соединений Пример В 1. а. Получение целевого соединения 1.2 Частями добавляли CDI (0,004 моль) при комнатной температуре к раствору промежуточного соединения 5 (полученного в соответствии с А 2) (0,003 моль) в CH2Cl2 (20 мл). Смесь перемешивали при комнатной температуре в течение 18 ч. Органический слой промывали K2CO3 10%, высушивали(MgSO4), фильтровали и растворитель выпаривали. Остаток (1,9 г) очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2/CH3OH/NH4OH 97/3/0,1; 15-40 мкм). Чистые фракции собирали и растворитель упаривали. Выход: 0,58 г целевого соединения 1,2 (32%).b. Получение целевого соединения 1.1 Смесь целевого соединения 1.2 (0,001 моль) и Pd/C (0,5 г) в СН 3 ОН (6 мл) гидрогенизировали при 50 С в течение 18 ч под давлением в 3 бара, затем фильтровали через целит. Целит промывалиCH2Cl2/CH3OH. Фильтрат упаривали. Выход: 0,57 г целевого соединения 1.1 (100%). Пример В 2. Получение целевого соединения 1.4 Частями добавляли EDCI (0,001 моль) при комнатной температуре к раствору целевого соединения 1.1 (0,001 моль), циклопропанкарбоновой кислоты (0,001 моль), HOBt (0,001 моль) и Et3N (0,001 моль) вCH2Cl2 (6 мл). Смесь перемешивали при комнатной температуре в течение 18 ч. Органический слой промывали K2CO3 10%, высушивали (MgSO4), фильтровали и растворитель выпаривали. Остаток (0,6 г) очищали колоночной хроматографией на силикагеле (градиент элюента: CH2Cl2/CH3OH 98/2 95/5; 45-60- 19012421 мкм). Чистые фракции собирали и растворитель выпаривали. Выход: 0,55 г целевого соединения 1.4. Когда требуется, чтобы L-фрагмент содержал хиральный центр, смесь может быть или далее разделена с использованием подходящей колоночной хроматографии, либо также могут быть использованы в получении хиральные вещества (например, целевое соединение 1.6 с использованием (3R)-тетрагидро-3 фуранкарбоновой кислоты, которая является коммерчески доступной). Пример В 3. Получение целевого соединения 2.24. При комнатной температуре добавляли о-хлорбензальдегид (1,2 эквивалента) к раствору промежуточного соединения 10 (полученного в соответствии с A3.d) в МеОН. Смесь перемешивали при комнатной температуре в течение 1 ч. Добавляли NaBH3CN (1,2 экв.). Смесь перемешивали при комнатной температуре в течение 18 ч, фильтровали и промывали CH2Cl2. Добавляли PS-TS-NHNH2 (0,6 экв.). Смесь перемешивали при комнатной температуре в течение 3 ч. Выход: 11 мг (4,3%) целевого соединения 2.24. Следующие соединения были получены в соответствии с одним из приведенных выше примеров. Таблица 1- 21012421 С. Аналитические данные. Для всех соединений были записаны данные по ЖХМС. Условия ЖХМС. Общая методика Градиентную ВЭЖХ осуществляли с помощью системы Alliance НТ 2795 (Waters), состоящей из насоса для четырехкомпонентных смесей с дегазатором, автодозатора и детектора DAD. Элюат с колонки разделяли на МС-детекторе. МС-детекторы оснащены источником электрораспылительной ионизации. Напряжение капиллярной иглы составляло 3 кВ и температура источника поддерживалась при значении 100 С. В качестве газа-распылителя использовали азот. Получение данных осуществляли с помощью системы данных Waters-Micromass MassLynx-Openlynx. Способ 1. В дополнение к общей методике: обращено-фазовую ВЭЖХ проводили на колонке Kromasil C18 (5 мкм, 4,6150 мм) со скоростью потока, равной 1 мл/мин. Две подвижных фазы (подвижная фаза А: 100% 6,5 мМ ацетата аммония + 0,2% муравьиной кислоты; подвижная фаза В: 100% ацетонитрил), где для пробега использовалось условие градиента от 60% А и 40% В в течение 1 мин до 100% В в течение 4 мин, 100% В в течение 5 мин до 60% А и 40% В в течение 3 мин, и повторное уравновешивание 60% А и 40% В в течение 3 мин. Использовался объем для введения, равный 5 мкл. Напряжение конуса составляло 20 В для режима положительной ионизации. Масс-спектры получали сканированием от 100 до 900 в 1 с с использованием времени выдержки, равного 0,1 с. Способ 2. В дополнение к общей методике: обращено-фазовую ВЭЖХ проводили на колонке Kromasil C18(3,5 мкм, 4,6100 мм) со скоростью потока, равной 0,8 мл/мин. Три подвижных фазы (подвижная фаза А: 100% 7 мМ ацетата аммония; подвижная фаза В: 100% ацетонитрил; подвижная фаза С: 0,2% муравьиной кислоты + 99,8% сверхчистой воды), где для пробега использовалось условие градиента от 35% А,30% В и 35% С (в течение 1 мин) до 100% В в течение 4 мин, 100% В в течение 4 мин и повторное уравновешивание с первоначальными условиями в течение 2 мин. Использовался объем для введения, равный 10 мкл. Напряжение конуса составляло 20 В для режима положительной и отрицательной ионизации. Масс-спектры получали сканированием от 100 до 1000 в 0,4 с с использованием отсрочки между сканированиями, равной 0,3 с. Таблица 3. ЖХМС главных пиков и времена удерживания для всех соединенийD. Фармакологический пример. Пример D.1. Эксперимент по связыванию с h-NK1, h-NK2 и h-NK3 рецепторами. Соединения в соответствии с данным изобретением были исследованы на предмет взаимодействия с различными рецепторами нейротрансмиттеров, ионными каналами и сайтами связывания с переносчиками с применением методики связывания с радиолигандом. Мембраны, полученные из гомогенатов ткани или из клеток, экспрессирующих рецептор или интересующий переносчик, инкубировали с радиоактивно-меченым веществом ([3 Н] - или [125I] лигандом) для мечения определенного рецептора. Специфическое связывание рецептора с радиолигандом отличали от неспецифического мечения мембраны с помощью селективного ингибирования мечения рецептора немеченым лекарством (контроль), известного, как конкурирующего с радиолигандом за связывание с сайтами рецептора. После инкубации меченые мембраны собирали и промывали избытком холодного буфера для удаления не связавшейся радиоактивности с помощью быстрой фильтрации под вакуумом. Мембранно-связанная радиоактивность была оценена с помощью сцинтилляционного счетчика, и результаты были выражены в виде числа импульсов в минуту (cpm). Соединения растворяли в ДМСО и тестировали при 10 концентрациях, варьирующих от 10-10 до 10-5 М. Оценивалась способность соединений данного изобретения вытеснять [3 Н]-вещество Р из клонированных человеческих h-NK1 рецепторов, экспрессируемых СНО клетками, вытеснять [3 Н]-SR-48968 из клонированных человеческих h-NK2 рецепторов, экспрессируемых Sf9 клетками, и вытеснять [3 Н]-SR142801 из клонированных человеческих h-NK3 рецепторов, экспрессируемых СНО клетками. Значения связывания с рецептором (pIC50) для h-NK1 рецепторов варьирует для всех соединений данного изобретения между 10 и 6. Пример D.2. Сигнальная трансдукция (СТ). Этот тест позволяет оценить функциональную антагонистическую активность NK1 in vitro. Для из- 23012421 мерений концентраций внутриклеточного Са 2+ клетки выращивали в 96-луночных (черная стенка/прозрачное дно) планшетах Costar в течение 2 дней до достижения слияния. Клетки осаждали 2 мкМCaCl2; рН 7,4) содержащим 2,5 мМ пробенецида и 0,1% БСА (Са 2+-буфер). Клетки предварительно инкубировали с различными концентрациями антагонистов в течение 20 мин при комнатной температуре, и Са 2+-сигналы после добавления агонистов оценивали в флуоресцентном приборе с сигнальной пластиной(FLIPR произведенного Molecular Devices, Crawley, England). Пик Ca2+-перехода рассматривался как ожидаемый сигнал и средние значения соответствующих лунок анализировали как описано ниже. Сигмовидные кривые доза-эффект анализировали с помощью компьютеризированной обработки данных, с использованием программы GraphPad. Значение EC50 соединения является эффективной дозой,демонстрирующей 50% максимального эффекта. Для средних кривых наиболее выраженная реакция на агонист была приравнена к 100%. Для реакций антагониста значение IC50 подсчитывали, используя нелинейную регрессию. Данные pIC50 для сигнальной трансдукции, оцениваемой для представленной выборки соединений,представлены в табл. 4. Последние колонки показывают - не будучи ими ограниченными - для какого действия данные соединения могут быть подходящими. Конечно ввиду того, что для некоторых рецепторов к нейрокинину не были получены данные, очевидно, что эти соединения могут быть отнесены к другому подходящему применению. Таблица 4. Фармакологические данные сигнальной трансдукции для выбранных соединений- 24012421 Е. Примеры композиций. Термин "Активный ингредиент" (А.И.), используемый на протяжении этих примеров, касается соединения формулы (I), его фармацевтически приемлемой кислотно-аддитивной или основно-аддитивной соли, его стереохимически изомерных форм, его N-оксидной формы и его пролекарств. Пример Е.1. Пероральные капли. 500 г А.И. растворяли в 0,5 л 2-гидроксипропановой кислоты и 1,5 л полиэтиленгликоля при 6080 С. После охлаждения до 30-40 С добавляли 35 л полиэтиленгликоля и смесь тщательно перемешивали. Затем добавляли раствор 1750 г сахарина натрия в 2,5 л очищенной воды и во время перемешивания добавляли 2,5 л ароматизатора какао и полиэтиленгликоля q.s. до объема 50 л, получая пероральный раствор капель, содержащий 10 мг/мл А.И. Полученный раствор помещали в подходящие контейнеры. Пример Е.2. Раствор для перорального применения. 9 г метил-4-гидроксибензоата и 1 г пропил-4-гидроксибензоата растворяли в 4 л кипящей очищенной воды. В 3 л этого раствора растворяли первые 10 г 2,3-дигидроксибутандиовой кислоты и после этого 20 г А.И. Последний раствор объединяли с оставшейся частью начального раствора и было добавлено 12 л 1,2,3-пропантриола и 3 л 70% раствора сорбита. 40 г сахарина натрия растворяли в 0,5 л воды и добавляли 2 мл малиновой эссенции и 2 мл эссенции крыжовника. Последний раствор объединяли с первым, добавляли воду q.s. до объема, равного 20 л, с получением раствора для перорального применения,содержащего 5 мг активного ингредиента на чайную ложку (5 мл). Полученным раствором заполняли подходящие контейнеры. Пример Е.3. Таблетки, покрытые пленкой. Получение ядра таблетки. Смесь 100 г А.И., 570 г лактозы и 200 г крахмала тщательно перемешивали и после этого увлажняли раствором 5 г додецилсульфата натрия и 10 г поливинилпирролидона примерно в 200 мл воды. Влажную порошковую смесь просеивали, высушивали и просеивали опять. Затем добавляли 100 г микрокристаллической целлюлозы и 15 г гидрогенизированного растительного масла. Общую смесь тщательно перемешивали и прессовали в таблетки, с получением 10000 таблеток, каждая содержит 10 мг активного ингредиента. Покрытие. К раствору 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляли раствор 5 г этилцеллюлозы в 150 мл дихлорметана. Затем добавляли 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. 10 г полиэтиленгликоля расплавляли и растворяли в 75 мл дихлорметана. Последий раствор добавляли к первому и затем туда добавляли 2,5 г октадеканоата магния, 5 г поливинилпирролидона и 30 мл концентрированной окрашенной суспензии и всю смесь гомогенизировали. Ядра таблеток покрывали полученной таким образом смесью в аппарате для нанесения покрытия. Пример Е.4. Инъекционный раствор. 1,8 г метил-4-гидроксибензоата и 0,2 г пропил-4-гидроксибензоата растворяли примерно в 0,5 л кипящей воды для инъекций. После охлаждения примерно до 50 С добавляли при перемешивании 4 г молочной кислоты, 0,05 г пропиленгликоля и 4 г А.И. Данный раствор охлаждали до комнатной температуры и дополняли водой для инъекций q.s. до 1 л, с получением раствора, содержащего 4 мг/мл А.И. Раствор стерилизовали фильтрованием и помещали в стерильные контейнеры. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение в соответствии с общей формулой (I) его фармацевтически приемлемые кислотно-аддитивные соли, его стереохимически изомерные формы и его N-оксидная форма, гдеX представляет собой ковалентную связь;R1 выбирают из группы Ar1 и Ar1-алкила;n представляет собой целое число, равное 1;m представляет собой целое число, равное 1;Z представляет собой ковалентную связь; А 2 и А 4, каждый независимо друг от друга, представляют собой -СН 2 СН 2-; А 1 представляет собой -СН 2 СН 2- или -С(=O)O-; А 3 представляет собой -СН 2 СН 2- или -OC(=O)- при условии, что один из А 1 или А 3 представляет собой -С(=O)O- или -OC(=O)-; каждый Alk представляет независимо один от другого ковалентную связь; двухвалентный прямой- 25012421 или разветвленный, насыщенный или ненасыщенный углеводородный радикал, имеющий от 1 до 6 атомов углерода;Y представляет собой ковалентную связь или двухвалентный радикал формулы -C(=O)-;L выбирают из группы водорода, алкила, Ar3 и Het2;Ar1 представляет собой фенил, необязательно замещенный 1, 2 или 3 заместителями, независимо один от другого выбранными из группы галогена и алкила;Ar2 представляет собой фенил, необязательно замещенный 1, 2 или 3 заместителями, каждый из которых независимо один от другого выбирают из группы галогена, алкила, гидрокси и алкилокси;Ar3 представляет собой фенил, необязательно замещенный 1, 2 или 3 заместителями, каждый из которых независимо один от другого выбирают из группы алкила, галогена, гидрокси;Het2 представляет собой моноциклический гетероциклический радикал, выбранный из группы пирролидинила, дигидро-2 Н-пиранила, пиранила, диоксолила, имидазолидинила, тетрагидропиридинила,тетрагидропиримидинила, пиразолидинила, пиперидинила, морфолинила, дитианила, тиоморфолинила,пиперазинила, имидазолидинила, тетрагидрофуранила, 2 Н-пирролила, пирролинила, имидазолинила,пиразолинила, пирролила, имидазолила, пиразолила, триазолила, фуранила, тиенила, оксазолила, диоксазолила, оксазолидинила, изоксазолила, тиазолила, тиадиазолила, изотиазолила, пиридинила, 1 Нпиридинила, пиримидинила, пиразинила, пиридазинила, триазинила и тетразолила; где моногетероциклический радикал может быть необязательно замещен по любому атому одним или более алкильными радикалами; алкил представляет собой прямой или разветвленный насыщенный углеводородный радикал,имеющий от 1 до 6 атомов углерода или циклические насыщенные углеводородные радикалы, имеющие от 3 до 6 атомов углерода; каждый углеводородный радикал необязательно замещен по одному или более атомов углерода одним или более радикалами, выбранными из группы фенила, галогена, тригалогенметила, аминокарбонила, метила, этила, пропила, изопропила, трет-бутила, циано, оксо, гидрокси,формила и амино. 2. Соединение по п.1, характеризующееся тем, что спиро-фрагмент имеет формулу (f1) или (f2), где переменные определены, как в формуле (I), и "а" обозначает пиперидинил-фрагмент формулы (I) и "b" обозначает Alk-Y-Alk-L-фрагмент формулы (I) 3. Соединение по любому из пп.1, 2, характеризующееся тем, что R1 представляет собой бензил,присоединенный по 2-му положению, или R1 представляет собой фенил, присоединенный по 3-му положению. 4. Соединение по любому из пп.1-3, характеризующееся тем, что фрагмент R2-X-C(=Q)- представляет собой 3,5-ди(трифторметил)фенилкарбонил. 5. Соединение по любому из пп.1-4, характеризующееся тем, что каждый Alk независимо друг от друга представляет собой ковалентную связь или -СН 2-. 6. Соединение по любому из пп.1-5, характеризующееся тем, что L выбирают из группы водорода,изопропила, пентила, трет-бутила, циклопропила, циклогексила, тетрагидрофуранила, пирролила, фуранила, тиенила, тиадиазолила, фенила, пиридинила и пиразинила. 7. Соединение по любому из пп.1-6, характеризующееся тем, чтоX представляет собой ковалентную связь;R1 представляет собой фенил или бензил;Z представляет собой ковалентную связь; А 2 и А 4, каждый независимо друг от друга, представляют собой -CH2CH2-; А 1 представляет собой -СН 2 СН 2- или -С(=O)O-; А 3 представляет собой -СН 2 СН 2- или -OC(=O)- при условии, что один из А 1 или А 3 представляет собой -С(=O)O- или -OC(=O)-; каждый Alk представляет собой независимо один от другого ковалентную связь или двухвалентный прямой, насыщенный углеводородный радикал, имеющий от 1 до 2 атомов углерода;Y представляет собой ковалентную связь или двухвалентный радикал формулы -С(=O)-;L выбирают из группы водорода, алкила, Ar3 и Het2;Ar3 представляет собой фенил, необязательно замещенный заместителем, выбранным из группы алкила, галогена и гидрокси;Het2 представляет собой моноциклический гетероциклический радикал, выбранный из группы тетрагидрофуранила, пирролила, фуранила, тиенила, тиадиазолила, пиридинила и пиразинила; где каждый моноциклический гетероциклический радикал может быть необязательно замещен по любому атому одним или более алкильными радикалами; и алкил представляет собой прямой или разветвленный насыщенный углеводородный радикал,имеющий от 1 до 6 атомов углерода, или циклические насыщенные углеводородные радикалы, имеющие от 3 до 6 атомов углерода. 8. Соединение по п.1, представляющее собой соединение формулы 9. Применение соединения по любому из пп.1-8 в качестве лекарственного средства. 10. Применение соединения по любому из пп.1-8 в качестве перорально активного лекарственного средства системного проникновения. 11. Применение соединения по любому из пп.1-10 для производства лекарственного средства для лечения тахикинин-опосредованных состояний. 12. Применение соединения по пп.1-10 для производства лекарственного средства для лечения и/или профилактики шизофрении, рвоты, тревожности и депрессии, синдрома раздраженного кишечника(IBS), нарушений циркадного ритма, преэклампсии, ноцицепции, боли, в частности висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (ХОЗЛ) и расстройств мочеиспускания, таких как недержание мочи. 13. Фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и, в качестве активного ингредиента, терапевтически эффективное количество соединения по любому из пп.1-10. 14. Способ получения фармацевтической композиции по п.13, характеризующийся тем, что фармацевтически приемлемый носитель тщательно смешивают с терапевтически эффективным количеством соединения по любому из пп.1-10. 15. Способ получения соединения формулы (Ia), характеризующийся взаимодействием промежуточного соединения формулы (IIа) с 1,1'-карбонилдиимидазолом, где все переменные являются такими,как определено в п.1, в реакционно-инертном растворителе, и, если требуется, превращением соединений формулы (Ia) одно в другое, следуя известным в данной области превращениям, и дополнительно, если требуется, превращением соединений формулы (Ia) в терапевтически активную нетоксичную кислотно-аддитивную соль обработкой кислотой, или в терапевтически активную нетоксичную основно-аддитивную соль обработкой основанием, или наоборот, превращением кислотно-аддитивной соли в свободное основание обработкой щелочью или превращением основно-аддитивной соли в свободную кислоту обработкой кислотой; и, если требуется, получением стереохимически изомерных форм, их N-оксидов и четвертичных аммониевых солей. 16. Способ получения соединения формулы (Ib), характеризующийся восстановительным Nалкилированием промежуточного соединения формулы (IIb) промежуточным соединением формулы(III), где все переменные являются такими, как определено в п.1, в реакционно-инертном растворителе и необязательно в присутствии подходящего восстанавливающего агента, и, если требуется, превращением соединений формулы (Ib) одно в другое, следуя известным в данной области превращениям, и дополнительно, если требуется, превращением соединений формулы (Ib) в- 27012421 терапевтически активную нетоксичную кислотно-аддитивную соль обработкой кислотой, или в терапевтически активную нетоксичную основно-аддитивную соль обработкой основанием, или, наоборот, превращением кислотно-аддитивной соли в свободное основание обработкой щелочью, или превращением основно-аддитивной соли в свободную кислоту обработкой кислотой; и, если требуется, получением стереохимически изомерных форм, их N-оксидов и четвертичных аммониевых солей. 17. Способ по п.15 или 16, характеризующийся тем, что фрагмент Alk-Y-Alk-L- в соединениях формул (IIa), (Ia) и (Ib) и фрагмент Alk-L- в соединении формулы (III) является бензилом.
МПК / Метки
МПК: A61K 31/537, C07D 498/10, A61P 25/18, A61P 25/24
Метки: применение, оксадиазаспиро, нейрокинина-2, 5.5, замещённые, качестве, антагонистов, ундеканона, производные
Код ссылки
<a href="https://eas.patents.su/29-12421-zameshhyonnye-proizvodnye-oksadiazaspiro-55-undekanona-i-ih-primenenie-v-kachestve-antagonistov-nejjrokinina.html" rel="bookmark" title="База патентов Евразийского Союза">Замещённые производные оксадиазаспиро [5.5] ундеканона и их применение в качестве антагонистов нейрокинина</a>
Предыдущий патент: Улучшенный способ очистки периндоприла
Следующий патент: Фармацевтическая липидная композиция в виде частиц
Случайный патент: Моющие средства для стирки на основе композиций, полученных в результате метатезиса натурального масла












