Производные индол-2-карбоксамидина как антагонисты nmda рецептора
Номер патента: 9981
Опубликовано: 28.04.2008
Авторы: Фаркаш Шандор, Колок Шандор, Борза Иштван, Надь Йожеф, Хорват Чилла
Формула / Реферат
1. Производные индол-2-карбоксамидина, имеющие формулу (I)
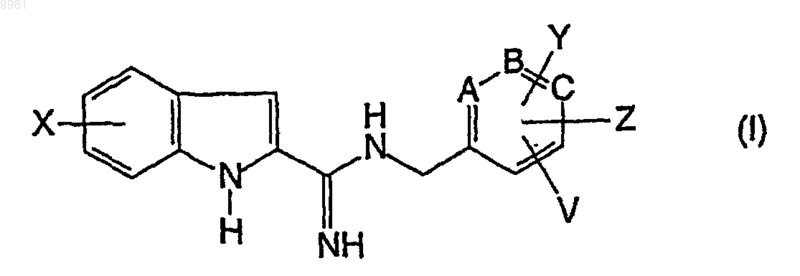
где заместители имеют следующее значение:
X представляет собой водород или атом галогена, С1-С4 алкил, С1-С4 алкокси, трифторметильную группу,
Y, V и Z независимо представляют собой атом водорода или галогена, гидрокси, циано, С1-С4 алкилсульфонамидо, необязательно замещенный атомом галогена или атомами галогена, С1-С4 алканоиламидо, необязательно замещенный атомом галогена или атомами галогена, трифторметил, трифторметокси, С1-С4 алкил, С1-С4 алкокси группу или соседние V и Z группы вместе с одним или более идентичным или отличающимся дополнительным гетероатомом и -CH= и/или -СН2- группами могут формировать необязательно замещенное 4-7-членное гомо- или гетероциклическое кольцо, предпочтительно бензольное, диоксолановое кольцо,
А, В и С независимо друг от друга представляют собой -CH=группу или один из них является атомом азота,
и их соли.
2. Соединение по п.1, выбранное из следующей группы производных индол-2-карбоксамидина: N-(2,6-диметоксибензил)-1Н-индол-2-карбоксамидин, N-(2-этоксибензил)-1H-индол-2-карбоксамидин, N-(3-метоксибензил)-5-метокси-1H-индол-2-карбоксамидин, N-(2,6-диметоксибензил)-5-хлор-1Н-индол-2-карбоксамидин, N-(2,6-диметоксибензил)-5-метокси-1H-индол-2-карбоксамидин, N-(2-этоксибензил)-5-фтор-1H-индол-2-карбоксамидин, N-(2,6-диметоксибензил)-5-фтор-1Н-индол-2-карбоксамидин, и его соли.
3. Фармацевтические композиции, содержащие эффективное количество производных индол-2-карбоксамидина, имеющих формулу (I), где значения А, В, С, X, Y, V, Z являются теми же, которые приведены в п.1, или их солей в качестве активного компонента, и вспомогательные материалы, которые широко используются на практике, такие как носители, наполнители, разжижители, стабилизаторы, увлажняющие или эмульгирующие агенты, вещества, влияющие на рН и осмотическое давление, отдушки или ароматизирующие вещества, а также активирующие композицию и доставляющие композицию добавки.
4. Способ получения производных индол-2-карбоксамидина, имеющих формулу (I), где значения А, В, С, X, Y, V, Z являются теми же, которые приведены в п.1, характеризующийся реакцией соли алкильного сложного эфира карбоксимидной кислоты с формулой (II)
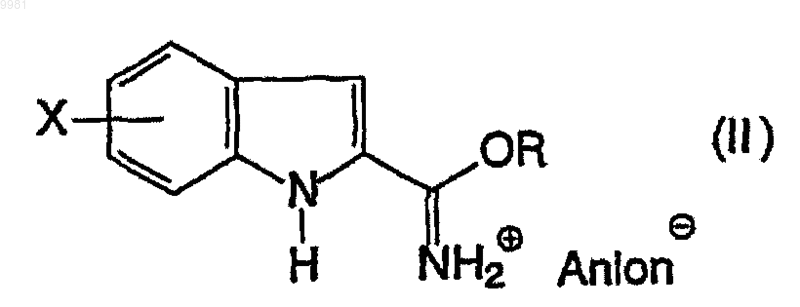
где значение X дано в п.1, Анион обозначает один эквивалент аниона, R представляет собой С1-С4 алкил, с аралкиламином формулы (III)
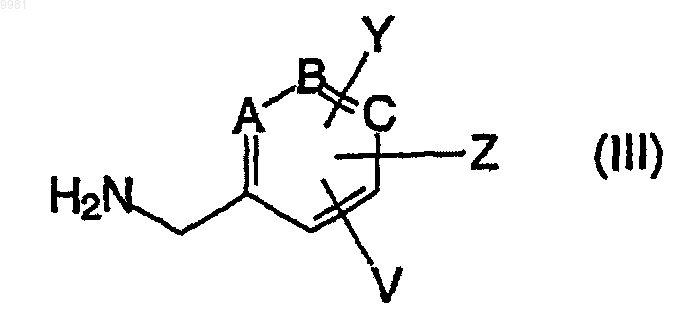
где значения А, В, С, Y, V, Z являются теми же, которые определены в п.1,
затем необязательно трансформацией полученных таким образом производных индол-2-карбоксамидина формулы (I), где значения А, В, С, X, Y, V, Z определены в п.1, в другие соединения формулы (I) путем введения новых заместителей и/или модификации, или удаления имеющихся заместителей, и/или путем формирования соли, и/или освобождения соединения формулы (I) из состава солей посредством известных методов.
5. Способ по п.4, характеризующийся реакцией гидрохлорида алкильного эфира карбоксимидной кислоты формулы (II), где значения X и R определены в п.1, Анион обозначает ион Cl-, с аралкиламином формулы (III), где значения А, В, С, Y, V, Z определены в п.1, в присутствии основания.
6. Способ по п.4, характеризующийся реакцией гидрохлорида алкильного эфира карбоксимидной кислоты формулы (II), где значения X и R определены в п.1 и Анион обозначает ион Сl-, с аралкиламином формулы (III), где значения А, В, С, Y, V, Z определены в п.1, в присутствии избытка аралкиламина формулы (III), где значения А, В, С, Y, V, Z определены в п.1, в алифатическом спирте.
7. Способ производства фармацевтических композиций, обладающих эффектом селективного антагониста NR2B рецептора NMDA, характеризующийся смешиванием производного индол-2-карбоксамидина формулы (I), где значения А, В, С, X, Y, V, Z определены в п.1, или его фармацевтически приемлемых солей в качестве активного компонента, и вспомогательных материалов, которые широко используются на практике, таких как носители, наполнители, разжижители, стабилизаторы, увлажняющие или эмульгирующие агенты, вещества, влияющие на рН и осмотическое давление, отдушки или ароматизирующие вещества, а также добавки, активирующие композицию и доставляющие композицию.
8. Способ лечения и облегчения симптомов следующих заболеваний млекопитающих, включая человека: травматического повреждения головного или спинного мозга, повреждения нервных клеток, связанных с наличием вируса иммунодефицита человека (HIV), бокового амиотрофического склероза (болезнь Шарко), толерантности и/или зависимости при лечении боли с применением синтетических наркотических препаратов (опиоидов), синдромов отмены, например, алкоголя, опиоидов или кокаина, ишемических расстройствах ЦНС, хронических нейродегенеративных заболеваний, таких как болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, боли и хронических болевых состояний, таких как невропатическая боль или боль, связанная с раковым заболеванием, эпилепсии, тревожности, депрессии, мигрени, психоза, мышечного спазма, слабоумия различного происхождения, гипогликемии, дегенеративных расстройств сетчатки, глаукомы, астмы, звона в ушах, потери слуха, индуцируемой антибиотиком-аминогликозидом, характеризующийся введением эффективного количества/количеств производного индол-2-карбоксамидина формулы (I), где значение А, В, С, X, Y, V, Z определено в п.1, или оптических изомеров, или рацематов, или их фармацевтически приемлемых солей как самих по себе, так и в комбинации с носителями, наполнителями и тому подобное, обыкновенно использующимся в фармацевтике млекопитающему, нуждающемуся в лечении.
9. Применение производного индол-2-карбоксамидина формулы (I), где значение А, В, С, X, Y, V, Z определено в п.1, или оптических изомеров, или рацематов, или их фармацевтически приемлемых солей для приготовления фармацевтических препаратов для лечения и облегчения симптомов следующих заболеваний млекопитающих, включая человека: травматического повреждения головного или спинного мозга, повреждения нервных клеток, связанных с наличием вируса иммунодефицита человека (HIV), бокового амиотрофического склероза (болезнь Шарко), толерантности и/или зависимости при лечении боли с применением синтетических наркотических препаратов (опиоидов), синдромов отмены, например, алкоголя, опиоидов или кокаина, ишемических расстройств ЦНС, хронических нейродегенеративных расстройств, таких как, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, боли и хронических болевых состояний, таких как невропатическая боль или боль, связанная с раковым заболеванием, эпилепсии, тревожности, депрессии, мигрени, психоза, мышечного спазма, слабоумия различного происхождения, гипогликемии, дегенеративных расстройств сетчатки, глаукомы, астмы, звона в ушах, потери слуха, индуцируемой антибиотиком-аминогликозидом.
Текст
009981 Область техники, к которой относится изобретение Настоящее изобретение касается новых производных индол-2-карбоксамидина, которые являются антагонистами NMDA рецептора, или являются промежуточными продуктами для их получения. Уровень техники Рецепторы N-метил-D-аспартата (NMDA) представляют собой лиганд-управляемые катионные каналы, широко экспрессируемые в центральной нервной системе. Рецепторы NMDA участвуют в связанных с развитием и адаптационных изменениях центральной нервной системы. Сверхактивация рецепторов NMDA их натуральным лигандом глутаматом может приводить к перегрузке клеток кальцием. Это запускает каскад внутриклеточных событий, которые изменяют функционирование клетки, и, в конечном счете, могут привести к гибели нейронов [TINS, 10, 299-302 (1987)]. Антагонисты рецепторовNMDA могут применяться для лечения многих заболеваний, которые сопровождаются избыточным выделением глутамата. Рецепторы NMDA представляют собой гетеромерные комплексы, состоящие из, по меньшей мере,одной субъединицы NR1 и одной или более из четырех субъединиц NR2 (NR2A-D). Недавно были обнаружены субъединицы NR3A и NR3B. Как пространственное распределение в центральной нервной системе (ЦНС), так и фармакологическая чувствительность рецепторов NMDA, имеющих в своем составе различные NR2 субъединицы, являются различными. Особенно интересной является NR2B субъединица в связи с ее ограниченным распределением (наивысшие плотности в переднем мозге и в студенистом веществе спинного мозга). Соединения, селективные для данного подтипа, являются доступными, и их эффективность была показана на животных моделях инсульта [Stroke, 28, 2244-2251 (1997)], при травматических повреждениях мозга [Brain Res., 792, 291-298 (1998)], болезни Паркинсона [Exp. Neurol., 163,239-243 (2000)], невропатической и воспалительной боли [Neuropharmacology, 38, 611-623 (1999)]. Более того, ожидается, что селективные антагонисты NR2B подтипа рецепторов NMDA являются более предпочтительными в плане побочного действия по сравнению с неселективными антагонистами рецепторовNMDA. Селективное в отношении NR2B соединение CP-101,606 при проведении клинических испытаний хорошо переносилось и не проявляло нежелательных эффектов, характерных для неселективных антагонистов, а именно психотомиметических эффектов, галлюцинаций и дисфории в дозах, которые снижают невропатическую боль (C.N. Sang, et al. Program No. 814.9. 2003 Abstract Viewer/Itinerary Planner. Washington, DC: Society for Neuroscience, 2003. Online). Антагонизм, селективный в отношении NR2B подтипа рецепторов NMDA, может быть достигнут с использованием соединений, которые специфически связываются и действуют на аллостерический регуляторный центр рецепторов, содержащих NR2B субъединицу. Этот связывающий центр может быть охарактеризован путем исследования замещения (связывания) с использованием специфических радиактивномеченых лигандов, таких как [3H]-Ro 25,6981 [J. Neurochem., 70,2147-2155 (1998)]. Близкие структурные аналоги амидиновых производных карбоновой кислоты, имеющих формулу(I), из литературы не известны. Однако некоторые другие производные карбоксамидина описаны как селективные антагонисты NR2B подтипа NMDA в следующих публикациях: Циннамамидины описаны в WO 200198262 и Bioorg. Med. Chem. Letters, 13, 693-696. (2003). Бензамидины описаны в WO 200067751 и Bioorg. Med. Chem. Letters, 13, 693-696. (2003), а также вBioorg. Med. Chem. Letters, 13, 697-700. (2003). Сущность изобретения Неожиданно было обнаружено, что новые производные индол-2-карбоксамидина настоящего изобретения, имеющие формулу (I), являются функциональными антагонистами рецепторов NMDA кортикальных нейронов крысы с IC50 меньше 1 мкмол. Этот эффект связан с ингибированием этими соединениями рецепторов, содержащих субъединицу NR2B, поскольку они не эффективны в отношении рецепторов NMDA, содержащих субъединицу NR2A, при 10 мкмол. Таким образом, можно полагать, что они являются антагонистами, специфическими в отношении NR2B подтипа NMDA, и могут быть полезны в терапевтических целях. Подробное описание изобретения Настоящее изобретение, таким образом, касается, в первую очередь, новых производных индол-2 карбоксамидина, имеющих формулу (I) где заместители имеют следующие значения:X представляет собой атом водорода или галогена, С 1-С 4 алкил, С 1-С 4 алкокси, трифторметильную группу, Y, V и Z независимо друг от друга представляют собой атом водорода или галогена, гидрокси,циано, С 1-С 4 алкилсульфонамидо, не обязательно замещенный атомом или атомами галогена, С 1-С 4 алка-1 009981 ноиламидо, не обязательно замещенный атомом или атомами галогена, трифторметил, трифторметокси,С 1-С 4 алкил, С 1-С 4 алкоксигруппу, или соседние V И Z группы вместе с одним или более идентичным или отличающимся дополнительным гетероатомом и -CH= и/или -СН 2- группами могут формировать не обязательно замещенное 4-7-членное гомо- или гетероциклическое кольцо, предпочтительно бензольное,диоксолановое кольцо, А, В и С, независимо друг от друга, представляют собой замещенный атом углерода или один из них является атомом азота, и их солей. Следующими объектами настоящего изобретения являются способы производства производных индол-2-карбоксамидина, соответствующих формуле (I), и фармацевтического производства медикаментов, содержащих в своем составе данные соединения, равно как и способы лечения с применением данных соединений, что означает введение препаратов в организм нуждающегося в лечении млекопитающего, включая человека, эффективного количества/количеств производных индол-2-карбоксамидина настоящего изобретения, соответствующих формуле (I), как самих по себе, так и в составе медикамента. Новые производные индол-2-карбоксамидина настоящего изобретения, соответствующие формуле(I), являются высоко эффективными и селективными антагонистами рецепторов NMDA, и более того,большая часть этих соединений являются селективными антагонистами NR2B подтипа рецепторовNMDA. Согласно настоящему изобретению, производные индол-2-карбоксамидина, соответствующие формуле (I), синтезируются путем реакции соли алкильного сложного эфира карбоксимидной кислоты формулы (II) где значение X указано в п.1 Формулы изобретения, Анион обозначает один эквивалент аниона, R представляет собой С 1-С 4 алкил - с аралкиламином формулы (III) где значения А, В, С, Y, V, Z являются теми же, которые определены ранее для формулы (I),после чего полученные производные индол-2-карбоксамидина формулы (I) - где значения А, В, С,Y, V, Z имеют те же значения, которые определены для формулы (I), превращаются в другие соединения формулы (I) путем введения новых заместителей, и/или модификации, или удаления имеющихся заместителей, и/или путем формирования соли, и/или освобождения соединения из состава солей известными методами. Соединения настоящего изобретения легко получаются путем реакции подходящих гидрохлоридов алкильных сложных эфиров карбоксимидной кислоты с подходящим аралкиламином в реакционноинертном растворителе при подходящей температуре в присутствии основания. Типичными растворителями для таких реакций являются этанол, метанол, метиленхлорид, этилендихлорид, тетрагидрофуран. Желаемые гидрохлориды алкильных сложных эфиров карбоксимидной кислоты (например, этиловый эфир) легко получаются в реакции Пиннера (Pinner reaction), a именно путем реагирования соответствующего нитрила с насыщенным раствором соляной кислоты в спирте. Нитрильные реагенты, необходимые для получения реагентов гидрохлорида алкильного эфира карбоксимидной кислоты получаются путем реакции соответствующих амидов с оксихлоридом фосфора. Амиды кислот получаются путем амидирования соответствующих хлоридов кислот согласно хорошо известным методам. Хлориды кислот получаются в реакции подходящей карбоновой кислоты с тионилхлоридом, последний обычно выполняет роль как реагента, так и растворителя. В реакции соединения формулы (II) с соединением формулы(III) применяемым основанием является молярный избыток реагента аралкиламина формулы (III). Необходимое время реакции составляет 1-24 ч, предпочтительно 6 ч. Предпочтительная температура реакции составляет от примерно 20C до примерно 30C. Реакционная смесь очищается колоночной хроматографией с использованием Kieselgel 60 (Merck) в качестве адсорбента и подходящего элюента. Нужные фракции подкисляются соляной кислотой и концентрируются для получения солянокислой соли готового продукта. Качество и количество продукта определялось методом HPLC-MS. 1 Н-индол-2-карбоновые кислоты, необходимые для получения реагентов: гидрохлоридов алкильных эфиров карбоксимидной кислоты формулы (II) и бензиламинов формулы (III), являются коммерчески доступными. Протоколы экспериментов Экспрессия рекомбинантных рецепторов NMDA Чтобы доказать селективность соединений по изобретению в отношении NR2B тестировали их на клеточных линиях, устойчиво экспрессирующих рекомбинантные рецепторы NMDA с субъединичным составом NR1(-3)/NR2A. кДНК субъединиц NR1 (-3) и NR2A человека, субклонированные в индуцибельные экспрессионные векторы млекопитающих, были интродуцированы в HEK 293 клетки, не содер-2 009981 жащие рецепторов NMDA, с использованием опосредованного положительно заряженными липидами метода трансфекции [Biotechniques, 1997 May; 22, 982-7. (1997); Neurochemistry International, 43, 19-29.(2003)]. Устойчивость к неомицину и гигромицину использовалась для отбора клонов, содержащих оба вектора, и на основе этих клонов были получены моноклональные клеточные линии, обеспечивающие наибольший ответ на взаимодействие с NMDA. Соединения тестировались на их ингибирующую активность в отношении вызванного NMDA увеличения уровня внутриклеточного кальция, который регистрировался при флуоресцентных измерениях содержания кальция. Исследования проводились через 48-72 часов после добавления индуцирующего агента. Кетамин (500 мкМ) также присутствовал в ходе индукции с целью предотвращения цитотоксичности. Определение активности антагониста NMDA in vitro посредством измерения внутриклеточной концентрации кальция с использованием сканирующего флуориметра для прочтения планшетов в культуре корковых клеток крысы Измерения внутриклеточной концентрации кальция были произведены с использованием культур первичных клеток новой коры головного мозга, полученных из 17-дневных эмбрионов крыс линииCharles River (подробное описание получения культуры клеток коры головного мозга смотри в Johnson,M.I.; Bunge, R.P. (.1992): Primary cell cultures of peripheral and central neurons and glia. In: Protocols for Neural Cell Culture, eds: Fedoroff, S.; Richardson A., The Humana Press Inc., 51-75.) После выделения клетки были рассеяны на стандартные 96-луночные микропланшеты, после чего культуры инкубировались в атмосфере 95% воздуха, 5% CO2 при 37C до проведения измерений концентрации кальция. Культуры клеток использовались для измерения внутриклеточной концентрации кальция in vitro по истечении 3-7 дней. Перед измерениями в клетки вводили флуоресцентный Са 2+-чувствительный краситель Fluo-4/AM (2 мкМ). Для остановки введения красителя в клетки, клетки дважды промывали раствором, использовавшимся в ходе измерений (140 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2, 5 мМ HEPES, 5 мМHEPES-Na, 20 мМ глюкозы, 10 мкМ глицина, pH=7,4). После промывки к клеткам добавляли тестируемые соединения, растворенные в указанном выше растворе (90 мкл/лунку). Измерения внутриклеточной концентрации кальция производили с использованием сканирующего флуориметра для прочтения планшетов: увеличение флуресценции Fluo-4, которое соответствовало увеличению внутриклеточной концентрации кальция, индуцировали посредством введения 40 мкМ NMDA. Ингибирующую активность тестируемых соединений определяли посредством измерения снижения роста концентрации кальция в присутствии различных концентраций тестируемых соединений. Кривые зависимости доза-эффект и значения IC50 определяли, используя данные, полученные, по меньшей мере, в трех независимых экспериментах. Ингибирующая активность соединения в одной концентрационной точке выражалась как процент ингибирования (ослабления) ответа на NMDA. По экспериментальным точкам были построены сигмоидальные кривые концентрация-ингибирование, и значенияIC50 были определены как концентрация, которая обеспечивает полумаксимальное ингибирование, вызываемое данным соединением. В табл. 1 приведены данные об активности наиболее эффективных соединений настоящего изобретения как антагонистов NR2B, полученные в данном тесте. В табл. 2 приведены результаты, полученные с селективным по отношению к NR2B антагонистом CI-1041 и неселективным антагонистом NMDA рецепторов MK-801, которые использовались как соединения для сравнения.-3 009981 Таблица 1. Активность соединений как антагонистов NMDA, измеренная флуориметрическим методом на клетках коры или клетках, экспрессирующих субъединицы NR1-3/NR2A-4 009981 Таблица 2. NMDA антагонистическая активность соединений, используемых для сравнения, измеренная флуориметрическим методом на клетках коры или клетках, экспрессирующих субъединицы NR13/NR2A Соединениями для сравнения являются следующие:MK-801: (+)-5-метил-10,11-дигидро-5 Н-дибензо[а,d]циклогептен-5,10-имин. Расстройства, которые могут быть успешно вылечены антагонистами рецепторов NMDA, действующими по центрам NR2B, как было недавно описано в обзоре Loftis [PharmacologyTherapeutics, 97,55-85 (2003)], включают в себя шизофрению, болезнь Паркинсона, болезнь Хантингтона, эксцитотоксичность (цитотоксичность), вызываемую гипоксией и ишемией, припадки, лекарственную зависимость и боль, в особенности невропатическую, воспалительную и внутреннюю боль любой природы [Eur. J.Pharmacol., 429, 71-78 (2001)]. Благодаря незначительной тяжести их побочных эффектов, по сравнению с неселективными антагонистами NMDA, селективные антагонисты NR2B могут быть полезны при тех заболеваниях, при которых может быть эффективным антагонист NMDA, таких как боковой амиотрофический склероз (болезнь Шарко) [Neurol. Res., 21, 309-12 (1999)], синдромы отмены, например, алкоголя, опиоидов или кокаина[Drug and Alcohol Depend., 59, 1-15 (2000)], мышечный спазм [Neurosci. Lett., 73, 143-148 (1987)], слабоумие различного происхождения [Expert Opin. Investig. Drugs, 9, 1397-406 (2000)], тревожность, депрессия, мигрень, гипогликемия, дегенеративные расстройства сетчатки (например, цитомегаловирусные(CMV) ретиниты), глаукома, астма, звон в ушах, потеря слуха [Drug News Perspect. 11, 523-569 (1998) и международная заявка WO 00/00197]. Таким образом, эффективные количества соединений настоящего изобретения могут с успехом применяться для лечения травматических повреждений головного или спинного мозга, толерантности и/или зависимости при лечении болей с применением синтетических наркотических препаратов (опиоидов), развития устойчивости, снижения злоупотребления и синдромов отмены при лекарственной зависимости и зависимости от, например, алкоголя, опиоидов или кокаина, ишемических расстройств ЦНС,хронических нейродегенеративных расстройств, таких как, например, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, болей и хронических болевых состояний, таких как, например, невропатическая боль. Соединения, являющиеся объектом настоящего изобретения, а также их фармацевтически приемлемые соли, могут использоваться как сами по себе, так и, соответственно, в составе фармацевтических композиций. Данные композиции (лекарства) могут быть в твердой, жидкой, либо полужидкой формах,кроме того, в них могут входить фармацевтические вспомогательные лекарственные вещества и вспомогательные материалы, которые широко применяются на практике, такие как носители, наполнители, разжижители, стабилизаторы, увлажняющие или эмульгирующие агенты, вещества, влияющие на рН и осмотическое давление, отдушки или ароматизирующие вещества, а также добавки, активирующие и доставляющие композицию. Дозировка, необходимая для обеспечения терапевтического эффекта, может варьировать в широких пределах, и будет оптимизироваться под индивидуальные требования в каждом конкретном случае в зависимости от стадии заболевания, состояния и массы тела нуждающегося в лечении пациента, так же,как и от чувствительности пациента к активному веществу, способа введения и частоты приема препарата в течение дня. Точная доза используемого активного вещества может быть безошибочно определена-5 009981 лечащим врачом, опытным в данной области, и имеющим полную информацию о нуждающемся в лечении пациенте. Фармацевтические композиции, содержащие активное вещество в соответствии с настоящим изобретением, содержат, как правило, от 0,01 до 100 мг активного вещества в единичной дозированной форме. Само собой, возможно, что количество активного вещества в некоторых композициях выходит за верхние либо нижние пределы указанного выше диапазона. Твердые формы фармацевтических композиций могут представлять собой, например, таблетки,драже, капсулы, пилюли или ампулы, содержащие лиофилизированные порошки, пригодные для приготовления инъекций. Жидкие композиции представляют собой пригодные для инъекций и вливаний композиции, жидкие медикаменты, капсулы с жидким содержимым (packing fluids) и капли. Полужидкие композиции могут представлять собой мази, бальзамы, крема, взбалтываемые микстуры и суппозитории. Для того чтобы их удобно было применять, является пригодным, если фармацевтические композиции включают в себя дозированные формы, содержащие в своем составе такое количество активного вещества, которое пригодно для однократного приема, либо нескольких повторных приемов, или приема их половины, трети, либо четвертой части. Такими дозированными формами являются, например, таблетки, которые могут быть покрыты бороздками, позволяющими разламывать их пополам или на четыре части с целью приема строго необходимого количества активного вещества. Таблетки могут быть покрыты кислоторастворимым слоем для того, чтобы гарантировать высвобождение содержащегося в таблетке активного вещества после прохождения таблетки через желудок. Такие таблетки являются покрытыми энтеросолюбильной оболочкой. Подобный эффект может быть также достигнут при инкапсулировании активного вещества. Фармацевтические композиции, пригодные для перорального применения, могут содержать, например, лактозу или крахмал в качестве наполнителей, натриевую соль карбоксиметилцеллюлозы, метилцеллюлозу, поливинилпирролидон либо крахмальную пасту в качестве связующих веществ или гранулирующих агентов. Картофельный крахмал или микрокристаллическая целлюлоза добавляются как дезинтегрирующие агенты, но также могут использоваться ультраамилопектин либо формальдегид казеин. Тальк, коллоидная кремниевая кислота, стеарин, стеараты кальция или магния могут применяться в качестве антиадгезивных и смазывающих веществ. Таблетки могут быть изготовлены, например, посредством влажного гранулирования с последующим спрессовыванием. Смешанные активные вещества и наполнители, также как и, в данном случае,часть дезинтегрирующих веществ, подвергаются гранулированию с применением водного, спиртового,либо водно-спиртового раствора связующих веществ с использованием соответствующего оборудования,после чего гранулят подвергается высушиванию. К высушенному грануляту добавляются другие дезинтегрирующие вещества, смазывающие вещества и антиадгезивные агенты, после чего смесь спрессовывается в таблетку. В данном случае таблетки изготавливаются с бороздкой посередине, что облегчает прием препарата. Таблетки могут быть изготовлены непосредственно из смеси активного вещества и подходящих вспомогательных веществ путем спрессовывания. В данном случае таблетки могут покрываться дополнительными веществами, широко применяющимися в фармакологической практике, такими как, например, стабилизаторы, ароматизаторы, красители, такие как сахар, производные целлюлозы (метил- или этилцеллюлоза, натриевая соль карбоксиметилцеллюлозы, и т.д.), поливинилпирролидон, фосфат кальция, карбонат кальция, пищевые красители, пищевые добавки, ароматизирующие вещества, пигменты на основе окиси железа, и т.д. В случае капсул смесь активного вещества и вспомогательных веществ заключается внутрь капсул. Жидкие композиции, предназначенные для перорального применения, такие как, например, суспензии, сиропы, эликсиры могут приготавливаться с применением воды, гликолей, масел, спиртов, красителей и ароматизирующих веществ. Композиции, предназначенные для ректального применения, изготавливаются в виде суппозиториев или растворов для клизм. Суппозитории, помимо активного вещества, могут содержать в своем составе носитель, так называемые основы для суппозиториев (adeps pro suppository). Носителями могут являться растительные масла, такие как гидрированные растительные масла, триглицериды C12-C18 жирных кислот (предпочтительно, носители, имеющие торговое название Witepsol). Активное вещество гомогенно смешивается с измельченной основой для суппозиториев, после чего формуются суппозитории. Композиция, предназначенная для парентерального применения, изготавливается в виде раствора для инъекций. Для приготовления раствора для инъекций активные вещества растворяются в дистиллированной воде и/или в различных органических растворителях, таких как гликолиевые эфиры, в данном случае, в присутствии солюбилизаторов, например, полиоксиэтиленсорбитан-монолаурата, -моноолеата,либо моностеарата (Tween 20, Tween 60, Tween 80). Раствор для инъекций может также содержать различные вспомогательные вещества, такие как консервирующие агенты, например этилендиаминтетраацетат, также как и регулирующие рН агенты и буфера и, в данном случае, местное анестезирующее вещество, например, лидокаин. Раствор для инъекций, содержащий активное вещество, являющееся предметом настоящего изобретения, перед внесением в ампулы подвергается фильтрованию и стерилизуется-6 009981 после наполнения ампулы. Если активное вещество является гигроскопическим, в таком случае оно может быть стабилизировано посредством лиофилизации. Следующие далее примеры иллюстрируют настоящее изобретение, никоим образом его не ограничивая. Характеристический метод Соединения, являющиеся объектом настоящего изобретения, были охарактеризованы с применением высокоэффективной жидкостной хроматографии, совмещенной с масс-селективным детектором (massselective detector) (LC/MS), с использованием HP 1100 бинарно-градиентной хроматографической системы с устройством отбора проб из микропланшета (Agilent, Waldbronn), управляемой компьютерной программой ChemStation software. HP диодный лучевой детектор (diode array detector) использовался для регистрации ультрафиолетовых (UV) спектров при 225 и 240 нм. Все эксперименты были проведены с использованием HP MSD (Agilent, Waldbronn) однолучевого четырехканального спектрометра (singlequadruple spectrometer), оборудованного источником для электрорассеивающей ионизации (electrosprayionization source) для установления структуры. Синтезированные продукты были растворены в 1 мл DMSO (Aldrich, Germany). 100 мкл каждого раствора было разбавлено DMSO до объема 1000 мкл. Эксперименты по аналитической хроматографии были произведены на колонке Discovery RP С-16 Amide, 5 см х 4,6 мм х 5 мкм фирмы Supelco (Bellefonte,Pennsylvania) при скорости потока равной 1 мл/минуту для хорошего разрешения. Полученные соединения были охарактеризованы по величине их k' фактора (чистота, коэффициент емкости). Факторы k' вычисляли в соответствии со следующей формулой: где k'= коэффициент емкости, tR= время удержания и t0 = время удержания элюента. В качестве элюента А использовали трифторацетиловую кислоту (TFA) (Sigma, Germany), содержащую 0,1% воды, в качестве элюента В использовали 95% ацетонитрил (Merck, Germany), содержащий 0,1% TFA и 5% элюента А. Использовали градиентную элюцию, длившуюся в течение 5 минут, которую начинали со 100% элюента А и продолжали до 100% элюента В. Нижеследующие примеры иллюстрируют в деталях способ по настоящему изобретению, никоим образом его не ограничивая. Пример 1. Гидрохлорид N-бензил-1H-индол-2-карбоксамидина. 1a) Амид 1 Н-индол-2-карбоновой кислоты. Смесь 10,0 г (62 ммоль) 1 Н-ндол-2-карбоновой кислоты (Aldrich), 10,0 мл (76 ммоль) тионилхлорида, 100 мл хлороформа и 1 капли диметилформамида нагревали с обратным холодильником в течение 2 ч. Реакционную смесь охлаждали до 20C, вливали в смесь 100 мл 25% нашатырного спирта и 100 г льда,затем перемешивали в течение 2 ч. Осевший продукт отфильтровывали и промывали водой для получения 8,96 г (90%) титульного соединения. Точка плавления: 231-232 С. 1b) 1 Н-индол-2-карбонитрил. Смесь 8,96 г (56 ммоль) амида 1H-индол-2-карбоновой кислоты, 26,0 мл (279 ммоль) оксихлорида фосфора и 230 мл хлороформа нагревали с обратным холодильником в течение 2 ч. Реакционную смесь охлаждали до 20C, вливали в 100 мл воды и перемешивали в течение 1 ч. После отделения органический слой высушивали над сульфатом натрия и концентрировали. Осадок очищали методом колоночной хроматографии, используя Kieselgel 60 (Merck) в качестве адсорбента и смесь гексана с этилацетатом в отношении 4:1 в качестве элюента, для получения 5,28 г (66,4%) титульного соединения. Точка плавления : 94-95 С. 1c) Гидрохлорид этилового эфира 1 Н-индол-2-карбоксимидной кислоты. К раствору 20 мл концентрированной насыщенной соляной кислоты в этаноле добавляли 2,23 г(15,7 ммоль) 1H-индол-2-карбонитрила. Реакционную смесь перемешивали при 20C в течение 2 ч, затем концентрировали и остаток кристаллизовали с эфиром для получения 3,1 г (82%) титульного соединения. Точка плавления: 170C. 1d) Гидрохлорид N-бензил-1 Н-индол-2-карбоксамидина. К раствору 32,1 мг (0,3 ммоль) бензиламина в 1 мл этанола добавляли 28,2 мг (0,15 ммоль) гидрохлорида этилового эфира 1H-индол-2-карбоксимидной кислоты в 1 мл этанола. Реакционную смесь перемешивали при комнатной температуре в течение 6 часов и затем концентрировали. Остаток очищали посредством колоночной хроматографии, используя Kieselgel 60 (Merck) в качестве адсорбента и смесь толуола с метанолом в отношении 4 : 1 в качестве элюента. Фракции, содержащие продукт, подкисляли соляной кислотой и концентрировали. Качество и количество продукта определяли, используя методHPLC-MS, как описано выше, k' = 2,46. В табл. 3 внесены замещенные производные гидрохлорида этилового эфира 1H-индол-2-карбоксимидной кислоты, которые являются представителями соединений с формулой (I), которые получены из соответствующей 1 Н-индол-2-карбоновой кислоты, согласно способу, описанному в примере 1, и охарактеризованы при использовании выше описанного характеристического метода. Использованные производные аралкиламина являются коммерческими продуктами. Пример 2. Приготовление фармацевтических композиций. а) Таблетки. 0,01-50% активного компонента формулы 1,15-50% лактозы, 15-50% картофельного крахмала, 515% поливинилпирролидона, 1-5% талька, 0,01-3% стеарата магния, 1-3% коллоидной двуокиси кремния и 2-7% ультраамилопектина смешивают, затем гранулируют посредством сырой грануляции и спрессовывают в таблетки.b) Драже, таблетки, покрытые тонкой оболочкой. Таблетки, изготовленные согласно способу, описанному выше, покрывают слоем, состоящим из энтеро- или гастрорастворимой оболочки, или из сахара и талька. Драже покрывают смесью пчелиного воска и карнаубского воска. с) Капсулы. 0,01-50% активного компонента, имеющего формулу I, 1-5% лаурилсульфата натрия, 15-50% крахмала, 15-50% лактозы, 1-3% коллоидной двуокиси кремния и 0,01-3% стеарата магния тщательно смешивают, смесь пропускают через сетчатый фильтр и вносят в твердые желатиновые капсулы.d) Суспензии. Компоненты: 0,01-15% активного компонента, имеющего формулу I, 0,1-2% гидроксида натрия,0,1-3% лимонной кислоты, 0,05-0,2% нипагина (метил 4-гидроксибензоат натрия), 0,005-0,02% нипазола,0,01-0,5% карбопола (полиакриловая кислота), 0,1-5% 96% этанола, 0,1-1% ароматизирующего агента,20-70% сорбитола (70% водный раствор) и 30-50% дистиллированной воды. К раствору нипагина и лимонной кислоты в 20 мл дистиллированной воды добавляют карбопол маленькими порциями при энергичном перемешивании, и раствор оставляют стоять в течение 10-12 ч. Затем при перемешивании добавляют гидроксид натрия в 1 мл дистиллированной воды, водный раствор сорбитола и в завершение - раствор в этаноле отдушивающего вещества с ароматом малины. К этому носителю маленькими порциями добавляют активный компонент и суспендируют смесь при помощи погружаемого в смесь гомогенизатора. В завершение суспензию доводят до желаемого конечного объема дистиллированной водой и суспензию-сироп пропускают через оборудование для помола коллоидов. е) Суппозитории. Для приготовления каждого суппозитория 0,01-15% активного компонента, имеющего формулу I, и 1-20% лактозы тщательно смешивают, затем 50-95% основы для суппозиториев (например, Witepsol 4) расплавляют, охлаждают до 35 С, и смесь активного компонента и лактозы вмешивают в нее, используя гомогенизатор. Полученную смесь формуют в охлаждаемых формах.f) Композиции для ампул в виде лиофилизированного порошка. 5% раствор маннита или лактозы готовят на бидистиллированной воде, применяемой для инъекций,- 20009981 и раствор фильтруют так, как это делается для получения стерильного раствора. 0,01-5% раствор активного компонента, имеющего формулу I, также готовят на бидистиллированной воде, применяемой для инъекций, и этот раствор фильтруют так, как это должно делаться для получения стерильного раствора. Эти два раствора смешивают в стерильных условиях, вносят порциями по 1 мл в ампулы, содержание ампул лиофилизируют и ампулы запаивают под азотом. Содержимое ампул растворяют в стерильной воде или 0,9% (физиологическом) стерильном водном растворе хлористого натрия перед введением. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производные индол-2-карбоксамидина, имеющие формулу (I) где заместители имеют следующее значение:X представляет собой водород или атом галогена, С 1-С 4 алкил, С 1-С 4 алкокси, трифторметильную группу,Y, V и Z независимо представляют собой атом водорода или галогена, гидрокси, циано, С 1-С 4 алкилсульфонамидо, необязательно замещенный атомом галогена или атомами галогена, С 1-С 4 алканоиламидо, необязательно замещенный атомом галогена или атомами галогена, трифторметил, трифторметокси, С 1-С 4 алкил, С 1-С 4 алкоксигруппу или соседние V и Z группы вместе с одним или более идентичным или отличающимся дополнительным гетероатомом и -CH= и/или -СН 2- группами могут формировать необязательно замещенное 4-7-членное гомо- или гетероциклическое кольцо, предпочтительно бензольное, диоксолановое кольцо,А, В и С независимо друг от друга представляют собой -CH=группу или один из них является атомом азота,и их соли. 2. Соединение по п.1, выбранное из следующей группы производных индол-2-карбоксамидина: N(2,6-диметоксибензил)-1 Н-индол-2-карбоксамидин, N-(2-этоксибензил)-1H-индол-2-карбоксамидин, N(3-метоксибензил)-5-метокси-1H-индол-2-карбоксамидин, N-(2,6-диметоксибензил)-5-хлор-1 Н-индол-2 карбоксамидин, N-(2,6-диметоксибензил)-5-метокси-1H-индол-2-карбоксамидин, N-(2-этоксибензил)-5 фтор-1H-индол-2-карбоксамидин, N-(2,6-диметоксибензил)-5-фтор-1 Н-индол-2-карбоксамидин, и его соли. 3. Фармацевтические композиции, содержащие эффективное количество производных индол-2 карбоксамидина, имеющих формулу (I), где значения А, В, С, X, Y, V, Z являются теми же, которые приведены в п.1, или их солей в качестве активного компонента, и вспомогательные материалы, которые широко используются на практике, такие как носители, наполнители, разжижители, стабилизаторы, увлажняющие или эмульгирующие агенты, вещества, влияющие на рН и осмотическое давление, отдушки или ароматизирующие вещества, а также активирующие композицию и доставляющие композицию добавки. 4. Способ получения производных индол-2-карбоксамидина, имеющих формулу (I), где значения А,В, С, X, Y, V, Z являются теми же, которые приведены в п.1, характеризующийся реакцией соли алкильного сложного эфира карбоксимидной кислоты с формулой (II) где значение X дано в п.1, Анион обозначает один эквивалент аниона, R представляет собой С 1-С 4 алкил, с аралкиламином формулы (III) где значения А, В, С, Y, V, Z являются теми же, которые определены в п.1,затем необязательно трансформацией полученных таким образом производных индол-2 карбоксамидина формулы (I), где значения А, В, С, X, Y, V, Z определены в п.1, в другие соединения формулы (I) путем введения новых заместителей и/или модификации, или удаления имеющихся заместителей, и/или путем формирования соли, и/или освобождения соединения формулы (I) из состава солей посредством известных методов.- 21009981 5. Способ по п.4, характеризующийся реакцией гидрохлорида алкильного эфира карбоксимидной кислоты формулы (II), где значения X и R определены в п.1, Анион обозначает ион Cl-, с аралкиламином формулы (III), где значения А, В, С, Y, V, Z определены в п.1, в присутствии основания. 6. Способ по п.4, характеризующийся реакцией гидрохлорида алкильного эфира карбоксимидной кислоты формулы (II), где значения X и R определены в п.1 и Анион обозначает ион Сl-, с аралкиламином формулы (III), где значения А, В, С, Y, V, Z определены в п.1, в присутствии избытка аралкиламина формулы (III), где значения А, В, С, Y, V, Z определены в п.1, в алифатическом спирте. 7. Способ производства фармацевтических композиций, обладающих эффектом селективного антагониста NR2B рецептора NMDA, характеризующийся смешиванием производного индол-2 карбоксамидина формулы (I), где значения А, В, С, X, Y, V, Z определены в п.1, или его фармацевтически приемлемых солей в качестве активного компонента, и вспомогательных материалов, которые широко используются на практике, таких как носители, наполнители, разжижители, стабилизаторы, увлажняющие или эмульгирующие агенты, вещества, влияющие на рН и осмотическое давление, отдушки или ароматизирующие вещества, а также добавки, активирующие композицию и доставляющие композицию. 8. Способ лечения и облегчения симптомов следующих заболеваний млекопитающих, включая человека: травматического повреждения головного или спинного мозга, повреждения нервных клеток, связанных с наличием вируса иммунодефицита человека (HIV), бокового амиотрофического склероза (болезнь Шарко), толерантности и/или зависимости при лечении боли с применением синтетических наркотических препаратов (опиоидов), синдромов отмены, например, алкоголя, опиоидов или кокаина, ишемических расстройствах ЦНС, хронических нейродегенеративных заболеваний, таких как болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, боли и хронических болевых состояний, таких как невропатическая боль или боль, связанная с раковым заболеванием, эпилепсии, тревожности, депрессии,мигрени, психоза, мышечного спазма, слабоумия различного происхождения, гипогликемии, дегенеративных расстройств сетчатки, глаукомы, астмы, звона в ушах, потери слуха, индуцируемой антибиотиком-аминогликозидом, характеризующийся введением эффективного количества/количеств производного индол-2-карбоксамидина формулы (I), где значение А, В, С, X, Y, V, Z определено в п.1, или оптических изомеров, или рацематов, или их фармацевтически приемлемых солей как самих по себе, так и в комбинации с носителями, наполнителями и тому подобное, обыкновенно использующимся в фармацевтике млекопитающему, нуждающемуся в лечении. 9. Применение производного индол-2-карбоксамидина формулы (I), где значение А, В, С, X, Y, V, Z определено в п.1, или оптических изомеров, или рацематов, или их фармацевтически приемлемых солей для приготовления фармацевтических препаратов для лечения и облегчения симптомов следующих заболеваний млекопитающих, включая человека: травматического повреждения головного или спинного мозга, повреждения нервных клеток, связанных с наличием вируса иммунодефицита человека (HIV),бокового амиотрофического склероза (болезнь Шарко), толерантности и/или зависимости при лечении боли с применением синтетических наркотических препаратов (опиоидов), синдромов отмены, например, алкоголя, опиоидов или кокаина, ишемических расстройств ЦНС, хронических нейродегенеративных расстройств, таких как болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, боли и хронических болевых состояний, таких как невропатическая боль или боль, связанная с раковым заболеванием, эпилепсии, тревожности, депрессии, мигрени, психоза, мышечного спазма, слабоумия различного происхождения, гипогликемии, дегенеративных расстройств сетчатки, глаукомы, астмы, звона в ушах,потери слуха, индуцируемой антибиотиком-аминогликозидом.
МПК / Метки
МПК: C07D 401/12, A61P 25/00, A61K 31/405, C07D 209/42, C07D 405/12
Метки: рецептора, производные, индол-2-карбоксамидина, антагонисты
Код ссылки
<a href="https://eas.patents.su/23-9981-proizvodnye-indol-2-karboksamidina-kak-antagonisty-nmda-receptora.html" rel="bookmark" title="База патентов Евразийского Союза">Производные индол-2-карбоксамидина как антагонисты nmda рецептора</a>
Предыдущий патент: Новый способ синтеза сложных эфиров n-[(s)-1-карбоксибутил]-(s)-аланина и их применение для синтеза периндоприла
Следующий патент: Производные бензоксазина в качестве модуляторов 5-нт-6, способ их получения, фармацевтические композиции, содержащие эти производные, и их применение
Случайный патент: Циклические пептидные антигрибковые агенты












