Гетероциклические соединения, содержащие их композиции и способы их применения
Номер патента: 16495
Опубликовано: 30.05.2012
Авторы: Оджери Дэвид Дж., Карсон Кеннет Г., Джессоп Теодор К., Бо Саймон Д.П., Багданофф Джеффри, Тарвер Джеймс Э.
Формула / Реферат
1. Соединение формулы I(a)
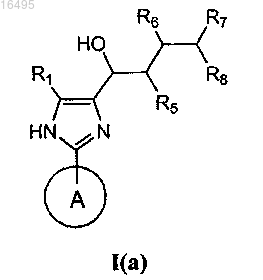
или формулы I(b)

или его фармацевтически приемлемая соль или сольват, где
A представляет 5- или 6-членный гетероцикл, содержащий по меньшей мере один атом азота и необязательно замещенный C1-10-алкокси, C1-10-алкилфенилом, C1-10-алкилом, фенилом или гидроксилом;
R1 представляет водород или C1-4-алкил;
R5 представляет OR5a, OC(O)R5a или водород;
R6 представляет OR6A, OC(O)R6A или водород;
R7 представляет OR7A, OC(O)R7A или водород;
R8 представляет CH2OR8A, CH2OC(O)R8A, водород и
каждый из R5A, R6A, R7A и R8A независимо представляет водород или C1-4-алкил.
2. Соединение по п.1, в котором A представляет дигидроимидазол, дигидроизоксазол, дигидропиразол, дигидротиазол, имидазол, изоксазол, изоксазолидин или пиразол.
3. Соединение по п.1, которое имеет формулу II(a)

или формулу II(b)
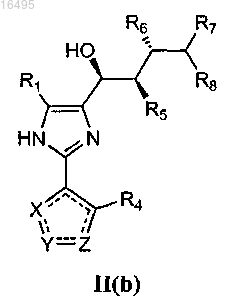
или формулу III(a)
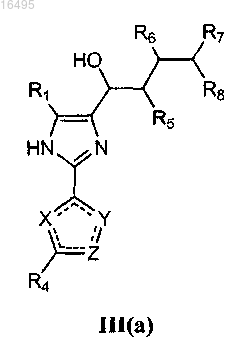
или формулу III(b)
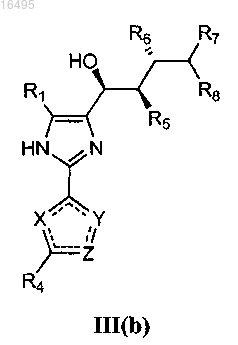
где X представляет CR4, CHR4, N, NR9, O или S;
Y представляет CR4, CHR4, N, NR9, O или S;
Z представляет CR4, CHR4, N, NR9, O или S;
R1 представляет водород или C1-4алкил;
каждый R4 независимо представляет водород, OR4A, OC(O)R4A, C1-10-алкил, фенил, C1-10-алкилфенил, фенил-C1-10-алкил или галоген;
R4a представляет водород или C1-4-алкил и
каждый R9 независимо представляет водород, C1-10-алкил, фенил, C1-10-алкилфенил или фенил-C1-10-алкил.
4. Соединение по п.3, в котором R4 представляет водород, C1-10-алкил, фенил или C1-10-алкилфенил.
5. Соединение по п.3 или 4, в котором X представляет N и Y представляет O, или X представляет N и Y представляет NR9, или X представляет N и Y представляет S, или X представляет N и Z представляет O, или X представляет N и Z представляет NR9, или X представляет N и Z представляет S, или X представляет N, Y представляет N и Z представляет NR9.
6. Соединение по п.3 или 5, в котором R9 представляет водород, C1-10-алкил, фенил или C1-10-алкилфенил.
7. Соединение по любому из пп.1-6, в котором R1 представляет водород.
8. Соединение по любому из пп.1-7, где один или более из R5, R6, R7 и R8 представляют ацетат или гидроксил.
9. Соединение по п.8, в котором все R5, R6, R7 и R8 представляют ацетат или все R5, R6, R7 и R8 представляют гидроксил.
10. Соединение по п.1, которое представляет
(1R,2S,3R)-1-(2-(5-метилизоксазол-3-ил)-1H-имидазол-5-ил)бутан-1,2,3,4-тетраол;
(1R,2S,3R)-1-(2-(5-этилизоксазол-3-ил)-1H-имидазол-5-ил)бутан-1,2,3,4-тетраол;
(1R,2S,3R)-1-(2-(изоксазол-3-ил)-1H-имидазол-5-ил)бутан-1,2,3,4-тетраол;
(1R,2S,3R)-1-(2-(2-метилтиазол-4-ил)-1H-имидазол-4-ил)бутан-1,2,3,4-тетраол;
(1R,2S,3R)-1-(2-(1-бензил-1H-1,2,4-триазол-3-ил)-1H-имидазол-4-ил)бутан-1,2,3,4-тетраол гидрохлорид;
(1R,2S,3R)-1-(1Н,1'Н-2,2'-биимидазол-5-ил)бутан-1,2,3,4-тетраол;
(1R,2S,3R)-1-(2-(5-метокси-4,5-дигидроизоксазол-3-ил)-1H-имидазол-5-ил)бутан-1,2,3,4-тетраол или
(1R,2S,3R)-1-(2-(5-метил-1Н-пиразол-3-ил)-1H-имидазол-5-ил)бутан-1,2,3,4-тетраол.
11. Соединение по п.10, которое представляет (1R,2S,3R)-1-(2-(изоксазол-3-ил)-1H-имидазол-5-ил)бутан-1,2,3,4-тетраол.
12. Применение соединения по любому из пп.1-11 в качестве лекарственного средства.
13. Применение соединения по любому из пп.1-11 в качестве лекарственного средства для подавления иммунного ответа у пациента.
14. Применение соединения по любому из пп.1-11 в качестве лекарственного средства для лечения, регулирования или предотвращения заболевания или расстройства, где заболевание или расстройство представляет рассеянный склероз, псориаз, псориатический артрит, ревматоидный артрит, отторжение трансплантата или диабет I типа.
Текст
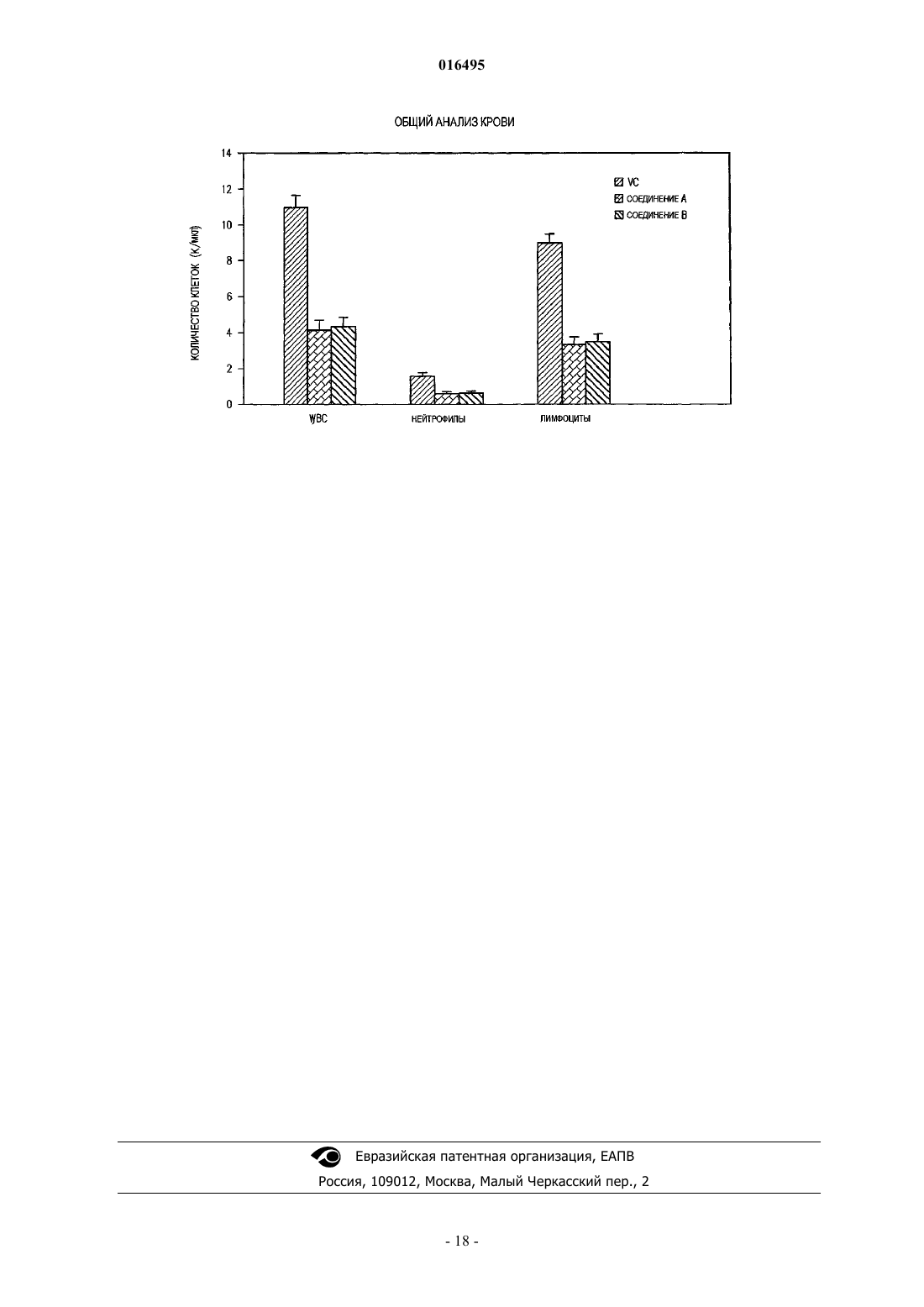
ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ИХ КОМПОЗИЦИИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ Описаны гетероциклические соединения, композиции, содержащие их, и способы их применения для лечения, предотвращения и регулирования воспалительных и аутоиммунных заболеваний и расстройств. 016495 Настоящая заявка претендует на приоритет предварительной заявки США 60/904357, поданной 1 марта 2007, содержание которой вводится в данное изобретение посредством ссылки. 1. Область техники, к которой относится изобретение Изобретение относится к соединениям на основе имидазола и способам их применения для лечения,предотвращения и регулирования различных заболеваний и расстройств. 2. Уровень техники Сфингозин-1-фосфат (S1P) является биоактивной молекулой, оказывающей значительное воздействие на многие системы органов. Saba, J.D. and Hla, T. Circ. Res. 94:724-734 (2004). Хотя некоторые считают, что данное соединение является внутриклеточным вторичным мессенджером, механизм его действия еще является предметом обсуждений. Id. Действительно, даже его метаболизм слабо изучен. Hla, Т.,Science 309:1682-3 (2005). В настоящее время исследователи считают, что S1P образуется путем фосфорилирования сфингозина и разрушается путем дефосфорилирования или расщепления. Его расщепление до этаноламинфосфата и длинноцепочечного альдегида, как сообщается, катализируется S1P лиазой. Id.;PyneРуnе, Biochem J. 349:385-402 (2000). Сфингозин-1-фосфат лиаза является витамин B6-зависимым ферментом, находящимся в мембране эндоплазматического ретикулума. Van Veldhoven and Mannaerts, J. Biol. Chem. 266:12502-12507 (1991);Van Veldhoven and Mannaerts. Adv. Lipid. Res. 26:69 (1993). Полинуклеотидная и аминокислотная последовательности человеческой SP1 лиазы и ее генных продуктов описаны в патентной заявке PCT WO 99/16888. Недавно Schwab и сотрудники сделали вывод, что компонент карамельного красителя III, 2-ацетил 4-тетрагидроксибутилимидазол (THI), ингибирует активность S1P лиазы при введении мышам. Schwab,S. et al, Science 309:1735-1739 (2005). Хотя существует предположение о том, что THI проявляет свое действие по иному механизму (см., например, Pyne, S. G., ACGC Chem. Res. Comm. 11: 108-112 (2000,ясно, что введение соединения мышам и крысам вызывает лимфопению и является причиной накопления зрелых T-клеток в тимусе. См., например, Schwab, supra; Pyne, S.G., ACGC Chem. Res. Comm. 11: 108-112(2000); Gugsyan, R., et al, Immunology 93(3):398-404 (1998); Halweg, K.M. and Bchi, G., J.Org.Chem. 50:1134-1136 (1985); патент США 4567194 Kroeplien and Rosdorfer. Кроме того, отсутствуют сообщения,что THI обладает иммунологическим действием у животных, отличных от мышей и крыс. Хотя в патенте США 4567194 утверждается, что THI и некоторые родственные соединения могут быть пригодны в качестве иммуносупрессорных медицинских агентов, исследования соединения на людях не обнаружили иммунологического действия. См. Thuvander, A. and Oskarsson, A., Fd. Chem. Toxic. 32(1): 7-13 (1994);Houben, G.F., et al, Fd. Chem. Toxic. 30 (9) :749-757 (1992). 3. Сущность изобретения Настоящее изобретение относится, в частности, к соединениям формулы I и их фармацевтически приемлемым солям и сольватам (например, гидратам), в которых A представляет необязательно замещенный гетероцикл; R1 представляет OR1A, OC(O)R1A, C(O)OR1A, водород,галоген, нитрил или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; R2 представляет OR2A, OC(O)R2A, водород, галоген или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; R3 представляет N(R3A)2, водород, гидрокси или необязательно замещенный алкил,арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; и каждыйR1A, R2A и R3A независимо представляет водород или необязательно замещенный алкил, арил, алкиларил,арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил. Настоящее изобретение также включает фармацевтические композиции, содержащие соединения формулы I, и способы лечения воспалительных заболеваний и расстройств с применением соединения формулы I. 4. Подробное описание фигуры Определенные аспекты настоящего изобретения можно понять на основании фигуры, которая показывает действие двух соединений настоящего изобретения на количество лейкоцитов (WBC), нейтрофилов и лимфоцитов при измерении через 18 ч после перорального введения 100 мг на килограмм в сравнении с контролем (VC). 5. Подробное описание Настоящее изобретение относится, в частности, к соединениям, которые, как считают, являются пригодными для лечения, предотвращения и/или регулирования аутоиммунных и воспалительных заболеваний и расстройств. Настоящее изобретение является результатом исследования, в частности, мышей,-1 016495 нокаутных по S1P лиазе. См. патентную заявку США 11/698253, поданную 25 января 2007. 5.1. Определения Если не указано особо, термин "алкенил" относится к неразветвленному, разветвленному и/или циклическому углеводороду, имеющему от 2 до 20 (например, 2-10 или 2-6) атомов углерода, и содержащему по меньшей мере одну углерод-углерод двойную связь. Представители алкенильных остатков включают винил, аллил, 1-бутенил, 2-бутенил, изобутиленил, 1-пентенил, 2-пентенил, 3-метил-1 бутенил, 2-метил-2-бутенил, 2,3-диметил-2-бутенил, 1-гексенил, 2-гексенил, 3-гексенил, 1-гептенил, 2 гептенил, 3-гептенил, 1-октенил, 2-октенил, 3-октенил, 1-ноненил, 2-ноненил, 3-ноненил, 1-деценил, 2 деценил и 3-деценил. Если не указано особо, термин "алкил" относится к неразветвленному, разветвленному и/или циклическому ("циклоалкил") углеводороду, имеющему 1-20 (например, 1-10 или 1-4) атомов углерода. Алкильные остатки, имеющие от 1 до 4 углеродов, называют "низшими алкилами". Примеры алкильных групп включают, но не ограничиваются ими, метил, этил, пропил, изопропил, н-бутил, грет-бутил, изобутил, пентил, гексил, изогексил, гептил, 4,4-диметилпентил, октил, 2,2,4-триметилпентил, нонил, децил,ундецил и додецил. Циклоалкильные остатки могут быть моноциклическими или многоциклическими, и примеры включают циклопропил, циклобутил, циклопентил, циклогексил и адамантил. Дополнительные примеры алкильных остатков имеют линейную, разветвленную и/или циклическую части (например, 1-этил-4-метилциклогексил). Термин "алкил" включают насыщенные углеводороды, так же как алкенильные и алкинильные остатки. Если не указано особо, термин "алкиларил" или "алкил-арил" относится к алкильному остатку, связанному с арильным остатком. Если не указано особо, термин "алкилгетероарил" или "алкил-гетероарил" относится к алкильному остатку, связанному с гетероарильным остатком. Если не указано особо, термин "алкилгетероцикл" или "алкил-гетероцикл" относится к алкильному остатку, связанному с гетероциклильным остатком. Если не указано особо, термин "алкинил" относится к неразветвленному, разветвленному или циклическому углеводороду, имеющему от 2 до 20 (например, 2-20 или 2-6) атомов углерода и содержащему, по меньшей мере, одну углерод-углерод тройную связь. Примеры алкинильных остатков включают ацетиленил, пропинил, 1-бутинил, 2-бутинил, 1-пентинил, 2-пентинил, 3-метил-1-бутинил, 4-пентинил,1-гексинил, 2-гексинил, 5-гексинил, 1-гептинил, 2-гептинил, 6-гептинил, 1-октинил, 2-октинил, 7 октинил, 1-нонинил, 2-нонинил, 8-нонинил, 1-децинил, 2-децинил и 9-децинил. Если не указано особо, термин "алкокси" относится к -O-алкильной группе. Примеры алкоксигрупп включают, но не ограничиваются ими, -OCH3, -OCH2CH3, -O(CH2)2CH3, -O(CH2)3CH3, -O(CH2)4CH3, и-O(CH2)5CH3. Если не указано особо, термин "арил" относится к ароматическому кольцу или ароматической или частично ароматической кольцевой системе, состоящей из атомов углерода и водорода. Арильные остатки могут содержать несколько колец, связанных или сконденсированных вместе. Примеры арильных остатков включают, но не ограничиваются ими, антраценил, азуленил, бифенил, флуоренил, индан, инденил, нафтил, фенантренил, фенил, 1,2,3,4-тетрагидронафталин и толил. Если не указано особо, термин "арилалкил" или"арил-алкил" относится к арильному остатку, связанному с алкильным остатком. Если не указано особо, термин "агент, снижающий количество циркулирующих лимфоцитов" относится к соединению, которое имеет CLRF больший, чем приблизительно 20%. Если не указано особо, термин "фактор снижения циркулирующих лимфоцитов" или "CLRF" относится к уменьшению числа циркулирующих лимфоцитов у мышей, вызванному пероральным введением однократной дозы соединения при концентрации 100 мг/кг, как определено способом, описанным в примерах ниже. Если не указано особо, термины "галоген" и "гало" относятся к фтору, хлору, брому и йоду. Если не указано особо, термин "гетероалкил" относится к алкильному остатку (например, линейному, разветвленному или циклическому), в котором по меньшей мере один из его атомов углерода заменен гетероатомом (например, N, O или S). Если не указано особо, термин "гетероарил" относится к арильному остатку, в котором по меньшей мере один из его атомов углерода заменен гетероатомом (например, N, O или S). Примеры включают, но не ограничиваются ими, акридинил, бензимидазолил, бензофуранил, бензоизотиазолил, бензоизоксазолил, бензохиназолинил, бензотиазолил, бензоксазолил, фурил, имидазолил, индолил, изотиазолил, изоксазолил, оксадиазолил, оксазолил, фталазинил, пиразинил, пиразолил, пиридазинил, пиридил, пиримидинил, пиримидил, пирролил, хиназолинил, хинолинил, тетразолил, тиазолил и триазинил. Если не указано особо, термин "гетероарилалкил" или "гетероарил-алкил" относится к гетероарильному остатку, связанному с алкильным остатком. Если не указано особо, термин "гетероцикл" относится к ароматическому, частично ароматическому или неароматическому моноциклическому или полициклическому кольцу или кольцевой системе,состоящей из углерода, водорода и по меньшей мере одного гетероатома (например, N, O или S). Гетеро-2 016495 цикл может содержать множество (т.е., два или более) колец, сконденсированных или связанных вместе. Гетероциклы включают гетероарилы. Примеры включают, но не ограничиваются ими, бензо[1,3]диоксолил, 2,3-дигидробензо[1,4]диоксинил, циннолинил, фуранил, гидантоинил, морфолинил,оксетанил, оксиранил, пиперазинил, пиперидинил, пирролидинонил, пирролидинил, тетрагидрофуранил,тетрагидропиранил, тетрагидропиридинил, тетрагидропиримидинил, тетрагидротиофенил, тетрагидротиопиранил и валеролактамил. Если не указано особо, термин "гетероциклоалкил" или "гетероцикл-алкил" относится к гетероциклильному остатку, связанному с алкильным остатком. Если не указано особо, термин "гетероциклоалкил" относится к неароматическому гетероциклу. Если не указано особо, термин "гетероциклоалкилалкил" или "гетероциклоалкил-алкил" относится к гетероциклоалкильному остатку, связанному с алкильным остатком. Если не указано особо, термины "регулировать", "регулирующий" и "регулирование" включают предотвращение рецидива конкретного заболевания или расстройства у пациента, который уже страдал от заболевания или расстройства, и/или продление времени, в течение которого пациент, страдающий от заболевания или расстройства, остается в фазе ремиссии. Термины включают регулирование границы,развития и/или продолжительности заболевания или расстройства, или изменение способа, которым пациент отвечает на заболевание или расстройство. Если не указано особо, термин "фармацевтически приемлемые соли" относится к солям, приготовленным из фармацевтически приемлемых нетоксичных кислот или оснований, включая неорганические кислоты и основания и органические кислоты и основания. Подходящие фармацевтически приемлемые соли присоединения основания включают, но не ограничиваются ими, соли металлов, полученные из алюминия, кальция, лития, магния, калия, натрия и цинка, или органические соли, полученные из лизина,N,N'-дибензилэтилендиамина, хлорпрокаина, холина, диэтаноламина, этилендиамина, меглумина (Nметилглюкамина) и прокаина. Подходящие нетоксические кислоты включают, но не ограничиваются ими, неорганические и органические кислоты, такие как уксусная, альгиновая, антраниловая, бензолсульфоновая, бензойная, камфорсульфоновая, лимонная, этенсульфоновая, муравьиная, фумаровая, фуранкарбоновая, галактуроновая, глюконовая, глюкуроновая, глутаминовая, гликолевая, бромоводородная, хлороводородная, изетиновая, молочная, малеиновая, яблочная, миндальная, метансульфоновая,муциновая, азотная, памовая, пантотеновая, фенилуксусная, фосфорная, пропионовая, салициловая,стеариновая, янтарная, сульфаниловая, серная, винная кислота и п-толуолсульфокислота. Избранные нетоксичные кислоты включают хлороводородную, бромоводородную, фосфорную, серную и метансульфокислоту. Таким образом, примеры избранных солей включают гидрохлориды и мезилаты. Другие являются хорошо известными в данной области техники. См., например, Remington's Pharmaceutical Sciences (18th ed., Mack Publishing, Easton PA: 1990) and Remington: The Science and Practice of Pharmacy(19th ed., Mack Publishing, Easton PA: 1995). Если не указано особо, под терминами "предотвратить", "предотвращающий" и "предотвращение" имеется в виду действие, которое происходит перед тем, как пациент начинает страдать от конкретного заболевания или расстройства, которое ингибирует или снижает тяжесть заболевания или расстройства. Другими словами, термины включают профилактику. Если не указано особо, "профилактически эффективное количество" соединения является количеством, достаточным для того, чтобы предотвратить заболевание или состояние, или один или более симптомов, связанных с заболеванием или состоянием, или предотвратить его рецидив. Профилактически эффективное количество соединения относится к количеству терапевтического средства, одного или в комбинации с другими агентами, которое обеспечивает профилактическую пользу при предотвращении заболевания. Термин "профилактически эффективное количество" может включать количество, которое улучшает общую профилактику или усиливает профилактическую эффективность другого профилактического средства. Если не указано особо, термин "агент, повышающий концентрацию S1P" относится к соединению,которое обладает SLEF, по меньшей мере, приблизительно 10-кратным. Если не указано особо, термин "фактор повышения концентрации S1P" или "SLEF" относится к увеличению S1P в селезенке мышей, вызванному пероральным введением однократной дозы соединения при концентрации 100 мг/кг, как определено способом, описанным в примерах ниже. Если не указано особо, термин "смесь стереоизомеров" включает рацемические смеси, так же, как смеси, обогащенные одним из стереоизомеров (например, R/S = 30/70, 35/65, 40/60, 45/55, 55/45, 60/40,65/35 и 70/30). Если не указано особо, термин "стереомерически чистая" относится к композиции, которая содержит один стереоизомер соединения и является главным образом свободным от других стереоизомеров данного соединения. Например, стереомерически чистая композиция соединения, имеющего один стереоцентр, будет, главным образом, свободной от второго стереоизомера соединения. Стереомерически чистая композиция соединения, имеющего два стереоцентра, будет, главным образом, свободна от других диастереомеров соединения. Типичное стереомерически чистое соединение содержит больше чем приблизительно 80% по массе одного стереомера соединения и меньше чем приблизительно 20 мас.%-3 016495 других стереоизомеров соединения, больше чем приблизительно 90 мас.% одного стереоизомера соединения и меньше чем приблизительно 10 мас.% других стереоизомеров соединения, больше чем приблизительно 95 мас.% одного стереоизомера соединения и меньше чем приблизительно 5 мас.% других стереоизомеров соединения, больше чем приблизительно 97 мас.% одного стереоизомера соединения и меньше чем приблизительно 3 мас.% других стереоизомеров соединения или больше чем приблизительно 99 мас.% одного стереоизомера соединения и меньше чем приблизительно 1 мас.% других стереоизомеров соединения. Если не указано особо, термин "замещенный" при использовании для того, чтобы описать химическую структуру или остаток, относится к производному данной структуры или остатка, в котором один или более его атомов водорода заменены атомом, химическим остатком или функциональной группой,такой как, но не ограничиваясь этим, спирт, альдегид, алкокси, алканоилокси, алкоксикарбонил, алкенил,алкил (например, метил, этил, пропил, грет-бутил), алкинил, алкилкарбонилокси (-OC(O)алкил), амидCONH-алкил, CONH-арил и CONH-арилалкил), карбонил, карбоксил, карбоновая кислота, ангидрид карбоновой кислоты, хлорангидрид карбоновой кислоты, циано, эфир, эпоксид, эфир (например, метокси,этокси), гуанидин, галоген, галогеналкил (например, -CCl3, -CF3, -C(CF3)3), гетероалкил, гемиацеталь,имин (первичный и вторичный), изоцианат, изотиоцианат, кетон, нитрил, нитро, кислород (т.е., чтобы обеспечить оксогруппой), фосфодиэфир, сульфид, сульфонамид (например, SO2NH2), сульфон, сульфонил (включая алкилсульфонил, арилсульфонил и арилалкилсульфонил), сульфоксид, тиол (например,сульфгидрил, тиоэфир) и мочевина (-NHCONH-алкил-). Если не указано особо, "терапевтически эффективное количество" соединения является количеством, достаточным для того, чтобы обеспечить терапевтическое действие при лечении или регулировании заболевания или состояния, или задерживать или минимизировать один и/или более симптомов, связанных с заболеванием или состоянием. Терапевтически эффективное количество соединения относится к количеству терапевтического средства, одного или в комбинации с другими терапевтическими средствами, которое обеспечивает терапевтическое действие при лечении или регулировании заболевания или состояния. Термин "терапевтически эффективное количество" может включать количество, которое улучшает общий терапевтический эффект, ослабляет или позволяет устранить симптомы или причины заболевания или состояния, или усиливает терапевтическую эффективность другого терапевтического средства. Если не указано особо, термины "лечить", "подвергать лечению" и "лечение" подразумевают действие, которое наблюдается, когда пациент страдает от конкретного заболевания или расстройства, которое снижает тяжесть заболевания или расстройства, или задерживает или замедляет развитие заболевания или расстройства. Если не указано особо, термин "включают" имеет то же значение, что и "включают, но не ограничиваются", и термин "включает" имеет то же значение, что и "включает, но не ограничивается". Аналогично, термин "такой как" имеет то же значение, что и термин "такой как, но не ограничивается". Если не указано особо, одно или более прилагательных, употребленных непосредственно перед серией существительных истолковываются как относящиеся к каждому из существительных. Например,фраза "необязательно замещенный алкилом, арилом или гетероарилом" имеет то же значение, что и "необязательно, замещенный алкилом необязательно замещенный арилом или необязательно замещенный гетероарилом". Следует отметить, что химический остаток, который образует часть более длинного соединения,может быть описан в данном документе с использованием названия, обычно соответствующего ему, когда оно существует в виде отдельной молекулы, или названия, обычно соответствующего его радикалу. Например, термины "пиридин" и "пиридил" имеют одинаковые значения при использовании для того,чтобы описать остаток, присоединенный к другим химическим остаткам. Таким образом, две фразы"XOH, где X представляет пиридил" и "XOH, где X представляет пиридин" имеют одинаковое значение и включают соединения пиридин-2-ол, пиридин-3-ол и пиридин-4-ол. Следует отметить, что если стереохимия структуры или части структуры не показана, например,жирными или штрихованными линиями, структуру или часть структуры следует понимать как включающую все ее стереоизомеры. Более того, предполагается, что любой атом, показанный на рисунке с неудовлетворительной валентностью, является присоединенным к достаточному количеству атомов водорода, чтобы соответствовать валентности. Кроме того, химические связи, изображенные с одной сплошной линией, параллельной одной пунктирной линии, включают как единичные связи, так и двойные (например, ароматические) связи, если позволяет валентность. 5.2. Соединения Настоящее изобретение включает соединения формулы I и их фармацевтически приемлемые соли и сольваты (например, гидраты), в которых A представляет необязательно замещенный гетероцикл; R1 представляет OR1A, OC(O)R1A, C(O)OR1A, водород, галоген,нитрил или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; R2 представляет OR2A, OC(O)R2A, водород, галоген или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; R3 представляет N(R3A)2, водород, гидрокси или необязательно замещенный алкил,арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; и каждыйR1A, R2A и R3A независимо представляет водород или необязательно замещенный алкил, арил, алкиларил,арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил. Конкретными соединениями являются соединения формулы I(a) или I(b) в которых R5 представляет OR5A, OC(O)R5A, N(R5B)2, NHC(O)R5B, водород или галоген; R6 представляет OR6A, OC(O)R6A, N(R6B)2, NHC(O)R6B, водород или галоген; R7 представляет OR7A, OC(O)R7A,N(R7B)2, NHC(O)R7B, водород или галоген; R8 представляет CH2OR8A, CH2OC(O)R8A, N(R8B)2, NHC(O)R8B,водород или галоген; каждый из R1A, R5A, R6A, R7A и R8A представляет независимо водород или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; и каждый из R5B, R6B, R7B И R8B независимо представляет водород или алкил, необязательно замещенный одной или более гидрокси- или галогеновыми группами. Один вариант осуществления настоящего изобретения включает соединения формулы II и их фармацевтически приемлемые соли и сольваты, в которых X представляет CR4, CHR4, N, NR9,O или S; Y представляет CR4, CHR4, N, NR9, O или S; Z представляет CR4, CHR4, N, NR9, O или S; R1 представляет OR1A, C(O)OR1A, водород, галоген, нитрил или необязательно замещенный алкил, арил,алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; R2 представляетOR2A, OC(O)R2A, водород, галоген или необязательно замещенный алкил, арил, алкиларил, арилалкил,гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; R3 представляет N(R3A)2, водород, гидрокси или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; каждый из R1A, R2A, и R3A независимо представляет водород или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; каждый R4 независимо представляет OR4A, OC(O)R4A, водород, галоген или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; каждый R9 независимо представляет водород или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; и каждый R1A, R2A, R3A и R4A независимо представляет водород или необязательно замещенный алкил,арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил. Конкретные соединения являются соединениями формулы II (а) или II(b) в которых R5 представляет OR5A, OC(O)R5A, N(R5B)2, NHC(O)R5B, водород или галоген; R6 представляет OR6A, OC(O)R6A, N(R6B)2, NHC(O)R6B, водород или галоген; R7 представляет OR7A, OC(O)R7A,N(R7B)2, NHC(O)R7B, водород или галоген; R8 представляет CH2OR8A, CH2OC(O)R8A, N(R8B)2, NHC(O)R8B,водород или галоген; каждый из R1A, R5A, R6A, R7A и R8A независимо представляет водород или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; и каждый из R5B, R6B, R7B и R8B независимо представляет водород или алкил, необязательно замещенный одной или более гидрокси- или галогеновыми группами. Другой вариант осуществления включает соединения формулы III и их фармацевтически приемлемые соли и сольваты, в которых X представляет CR4, CHR4, N, NR9,O или S; Y представляет CR4, CHR4, N, NR9, O или S; Z представляет CR4, CHR4, N, NR9, O или S; R1 представляет OR1A, C(O)OR1A, водород, галоген, нитрил или необязательно замещенный алкил, арил,алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; R2 представляетOR2A, OC(O)R2A, водород, галоген или необязательно замещенный алкил, арил, алкиларил, арилалкил,гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; R3 представляет N(R3A)2, водород, гидрокси или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; каждый из R1A, R2A и R3A независимо представляет водород или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; каждый R4 независимо представляет OR4A, OC(O)R4A, водород, галоген или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; каждый R9 независимо представляет водород или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; и каждый из R1A, R2A, R3A и R4A независимо представляет водород или необязательно замещенный алкил,арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил. Конкретные соединения являются соединениями формулы III (a) или III(b) в которых R5 представляет OR5A, OC(O)R5A, N(R5B)2, NHC(O)R5B, водород или галоген; R6 представляет OR6A, OC(O)R6A, N(R6B)2, NHC(O)R6B, водород или галоген; R7 представляет OR7A, OC(O)R7A,N(R7B)2, NHC(O)R7B, водород или галоген; R8 представляет CH2OR8A, CH2OC(O)R8A, N(R8B)2, NHC(O)R8B,водород или галоген; каждый из R1A, R5A, R6A, R7A и R8A независимо представляет водород или необязательно замещенный алкил, арил, алкиларил, арилалкил, гетероалкил, гетероцикл, алкилгетероцикл или гетероциклалкил; и каждый из R5B, R6B, R7B и R8B независимо представляет водород или алкил, необязательно замещенный одной или более гидрокси- или галогеновыми группами. Что касается различных формул, описанных в данном изобретении (например, формулы I, II и III), в соответствующих случаях в некоторых соединениях настоящего изобретения A представляет 5-членный необязательно замещенный гетероцикл. Примеры включают необязательно замещенный дигидроимида-6 016495 зол, дигидроизоксазол, дигидропиразол, дигидротиазол, диоксолан, дитиолан, дитиол, имидазол, изоксазол, изоксазолидин, оксатиолан и пиразол. В одном варианте осуществления A не является необязательно замещенным фураном, тиофеном или пирролом. В некоторых соединениях A представляет 6-членный необязательно замещенный гетероцикл (например, пиримидин). В некоторых соединениях X представляет CR4 или CHR4. В некоторых соединениях X представляетN или NR9. В некоторых соединениях Z представляет O или S. В некоторых соединениях X представляет N и Y представляет O. В некоторых соединениях X представляет N и Y представляет NR9. В некоторых соединениях X представляет N и Y представляет S. В некоторых соединениях X представляет N и Z представляет O. В некоторых соединениях X представляет N и Z представляет NR9. В некоторых соединениях X представляет N и Z представляет S. В некоторых соединениях X представляет N, Y представляет N, и Z представляет NR9. В некоторых соединениях R1 представляет водород. В некоторых соединениях R1 представляет нитрил. В некоторых соединениях R1 представляет необязательно замещенный низший алкил. В некоторых соединениях R1 представляет OR1A или C(O)OR1A, и R1A представляет, например, водород или необязательно замещенный низший алкил. В некоторых соединениях R2 представляет OR2A. В некоторых соединениях R2 представляетOC(O)R2A и R2A представляет, например, водород. В некоторых соединениях R2 представляет галоген. В некоторых соединениях R3 представляет необязательно замещенный алкил (например, алкил, замещенный одним или более галогенами или OR3A остатками, в которых R3A представляет, например, водород или ацетат). В некоторых соединениях R3 представляет водород. В некоторых соединениях R3 представляет гидроксил. В некоторых соединениях R3 представляет необязательно замещенный гетероалкил (например, алкокси). В некоторых соединениях R3 представляет гетероалкил, замещенный одним или более галогенами, гидроксилами или ацетатами. В некоторых соединениях R4 представляет водород или необязательно замещенный алкил, арил или алкиларил. В некоторых соединениях каждый из R5, R6, R7 и R8 представляет водород или галоген. В некоторых соединениях один или более из R5, R6, R7 и R8 представляют гидроксил или ацетат. В некоторых соединениях все R5, R6, R7 и R8 представляют гидроксил. В некоторых соединениях R9 представляет водород или необязательно замещенный алкил, арил или алкиларил. Соединения настоящего изобретения могут содержать один или более стереоцентров и могут существовать в виде рацемических смесей энантиомеров или смесей диастереомеров. Настоящее изобретение включает стереомерически чистые формы данных соединений, а также смеси данных форм. Стереоизомеры можно синтезировать асимметрически или разделять, применяя стандартные методики, такие как хиральные колонки или хиральные разделяющие агенты. См., например, Jacques, J., et al, Enantiomers,Racemates and Resolution (Wiley Interscience, New York, 1981); Wilen, S. H., et al., Tetrahedron 33:2125Resolving Agents and Optical Resolution, p. 268 (E.L. Eliel, Ed., Univ. of Notre Dame Press, Notre Dame, IN,1972). Кроме того, настоящее изобретение включает смесь стереоизомеров соединений, описанных в данном изобретении. Оно также включает конфигурационные изомеры соединений, описанных в данном изобретении, как в смеси, так и в чистой или, главным образом, чистой форме, такие как цис (Z) и транс(E) алкеновые изомеры и син- и анти-оксимные изомеры. Предпочтительные соединения настоящего изобретения являются агентами, снижающими количество циркулирующих лимфоцитов. Определенные соединения ингибируют количество циркулирующих лимфоцитов, как определено при применении способа, описанного в примерах, более чем приблизительно на 20, 50, 75, 100, 150 или 200%. При этом найдено, что, когда THI способно снизить количество циркулирующих лимфоцитов у мышей, многие аналоги и производные THI, такие как 1-(4-метил-51S,2R,3R)-1,2,3,4-тетрагидроксибутил)тиазол-2-ил)этанон, обладают слабым влиянием или не оказывают влияния на циркулирующие лимфоциты, несмотря на сообщения, утверждающие обратное. См.WO 97/46543. Не ограничиваясь теорией, считают, что соединения настоящего изобретения воздействуют на метаболический путь S1P и могут ингибировать S1P лиазу прямо или косвенно in vivo. Конкретные соединения являются агентами, увеличивающими концентрацию S1P. Определенные соединения увеличивают количество S1P, как определено при применении способа, описанного ниже в примерах, больше чем приблизительно в 10, 15, 20, 25 или 30 раз. Соединения настоящего изобретения можно получить способами, известными в данной области-7 016495 техники (например, изменяя и добавляя подходы, описанные в Pyne, S. G., ACGC Chem. Res. Comm. 11 : 108-112 (2000); Halweg, K.M. and Bchi, G., J.Org.Chem. 50:1134-1136 (1985. Соединения можно также получить способами, описанными ниже, и их вариантами, которые являются очевидными специалистам в данной области техники. Например, соединения формулы I можно получить из имеющихся в продаже и/или легко синтезируемых нитрилов, как показано ниже. где, например, реагирующие вещества смешивают с одним эквивалентом NaOMe в MeOH при комнатной температуре, с последующим добавлением кислоты (например, водной HCl). 5.3. Способы применения Настоящее изобретение включает способ регулирования (например, увеличения) количества S1P у нуждающегося в этом пациента (например, мыши, крысы, собаки, кошки или человека), который включает введение пациенту эффективного количества соединения настоящего изобретения (например, соединения, описанного в данном изобретении). Другой вариант осуществления включает способ снижения числа T-клеток в крови пациента, который включает введение пациенту эффективного количества соединения настоящего изобретения. Другой вариант осуществления включает способ лечения, регулирования или предотвращения заболевания, на которое влияет (или имеющего симптомы, на которые влияет) концентрация S1P, который включает введение нуждающемуся в этом пациенту терапевтически или профилактически эффективного количества соединения настоящего изобретения. Другой вариант осуществления включает способ подавления иммунного ответа у пациента, который включает введение пациенту эффективного количества соединения настоящего изобретения. Другой вариант осуществления включает способ лечения, регулирования или предотвращения аутоиммунного или воспалительного заболевания или расстройства, который включает введение нуждающемуся в этом пациенту терапевтически или профилактически эффективного количества соединения настоящего изобретения. Примеры заболеваний и расстройств включают анкилозирующий спондилит,астму (например, бронхиальную астму), атопический дерматит, болезнь Бехчета, реакции трансплантата против хозяина, синдром Кавасаки, красную волчанку, рассеянный склероз, миастению гравис, поллиноз, псориаз, псориатический артрит, ревматоидный артрит, склеродерму, отторжение трансплантанта(например, органа, клетки или костного мозга), диабет 1 типа и увеит. Дополнительные заболевания и расстройства включают болезнь Аддисона, антифосфолипидный синдром, аутоиммунный атрофический гастрит, аутоиммунную ахлоргидрию, глютеновую болезнь, болезнь Крона, синдром Кушинга, дерматомиозит, синдром Гудпастчера, болезнь Грейвса, тиреоидит Хашимото, идиопатическую адренальную атрофию, идиопатическую тромбопению, синдром ЛамбертаИтона, пемфигоид, вульгарную пузырчатку, пернициозную анемию, полиартериит нодозный, билиарный первичный цирроз печени, первичный склерозирующий холангит, болезнь Рейно, синдром Рейтера, рецидивирующий полихондрит, синдром Шмитта, синдром Шегрена, метастатическую офтальмию, артрит Такаясу, височный артериит, тиротоксикоз, язвенный колит и гранулематоз Вегенера. Количество, способ введения и режим дозирования соединения будет зависеть от факторов, таких как конкретное состояние, которое нужно лечить, предотвращать или регулировать, и возраста, пола и состояния пациента. Функции данных факторов являются хорошо известными в данной области техники и могут быть определены стандартным экспериментом. В конкретном варианте осуществления соединение настоящего изобретения вводят человеку в количестве приблизительно 0,5, 1, 2,5 или 5 миллиграммов на килограмм. 5.4. Фармацевтические составы Настоящее изобретение включает фармацевтические композиции, содержащие одно или более соединений настоящего изобретения. Определенные фармацевтические композиции находятся в стандартной лекарственной форме, подходящей для перорального, мукозального (например, назального, сублингвального, вагинального, буккального или ректального), парентерального (например, подкожного, внутривенного, болюсного, внутримышечного или внутриартериального) или трансдермального введения пациенту. Примеры лекарственных форм включают, но не ограничиваются ими: таблетки; каплеты; капсулы, такие как мягкие эластичные желатиновые капсулы; крахмальные капсулы; пастилки; таблетки для рассасывания; дисперсии; суппозитории; мази; припарки (примочки); пасты; порошки; перевязки; кремы; пластыри; растворы; пэтчи (пластыри); аэрозоли (например, назальные спреи или ингаляторы); гели; жидкие лекарственные формы, подходящие для перорального или мукозального введения пациенту,-8 016495 включая суспензии (например, водные или неводные жидкие суспензии, эмульсии масла в воде или жидкие эмульсии воды в масле), растворы и эликсиры; жидкие лекарственные формы, подходящие для парентерального введения пациенту; и стерильные твердые вещества (например, кристаллические или аморфные твердые вещества), которые можно разбавлять, чтобы получить жидкие лекарственные формы, подходящие для парентерального введения пациенту. Составы должны удовлетворять условиям способа введения. Например, пероральный способ введения требует энтеросолюбильного покрытия для того, чтобы защитить соединения настоящего изобретения от разрушения в желудочно-кишечном тракте. Аналогично, состав может содержать ингредиенты,которые облегчают доставку активного ингредиента (ингредиентов) к месту действия. Например, соединения можно вводить в липосомальных рецептурах для того, чтобы защитить их от деструктивных ферментов, облегчить транспорт в системе кровообращения и осуществлять доставку через клеточные мембраны к внутриклеточным мишеням. Аналогично, плохо растворимые соединения можно вводить в жидкие лекарственные формы (и лекарственные формы, подходящие для разбавления) с добавкой агентов, увеличивающих растворимость,эмульгаторами и поверхностно-активными веществами, такими как, но не ограничиваясь ими, циклодекстрины (например, -циклодекстрин, -циклодекстрин, Captisol и Encapsin (см., например, Davis andBrewster, 2004, Nat. Rev. Drug Disc. 3:1023-1034), Labrasol, Labrafil, Labrafac, cremafor, и неводными растворителями, такими как, но не ограничиваясь ими, этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, диметилсульфоксид (DMSO), биосовместимые масла (например, хлопковое, арахисовое, кукурузное, зародышевое, оливковое, касторовое и кунжутное масло), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли, сложные эфиры жирных кислот и сорбитана и их смеси (например,DMSO:корноил). Плохо растворимые соединения можно также вводить в суспензии, применяя другие методики, известные в данной области техники. Например, наночастицы соединения можно суспендировать в жидкости для того, чтобы получить наносуспензию (см., например, Rabinow, 2004, Nature Rev. Drug Disc. 3:785-796). Формы в виде наночастиц соединений, описанных в данном изобретении, можно получить способами, описанными в публикациях патентов США 2004-0164194, 2004-0195413, 2004-0251332,2005-0042177 А 1, 2005-0031691 А 1, и патентах США 5145684, 5510118, 5518187, 5534270, 5543133,5662883, 5665331, 5718388, 5718919, 5834025, 5862999, 6431478, 6742734, 6745962, содержание каждого из которых вводится в данное изобретение путем ссылки. В одном варианте осуществления форма наночастиц содержит частицы, имеющие средний размер частиц меньше чем приблизительно 2000 нм, меньше чем приблизительно 1000 нм или меньше чем приблизительно 500 нм. Композиция, форма и тип лекарственной формы будут значительно изменяться в зависимости от применения. Например, лекарственная форма, применяемая при неотложном лечении заболевания, может содержать большие количества одного или более активных ингредиентов, чем содержит лекарственная форма, применяемая при длительном лечении того же заболевания. Аналогично, парентеральная лекарственная форма может содержать меньшие количества одного или более активных ингредиентов, чем содержит пероральная лекарственная форма, применяемая при лечении того же заболевания. Эти и другие случаи, в которых конкретные лекарственные формы, включенные в настоящее изобретение, отличаются друг от друга, будут очевидны специалистам в данной области техники. См., например, Remington's Pharmaceutical Sciences, 18th ed., Mack Publishing, Easton PA (1990). 5.4.1. Пероральные лекарственные формы Фармацевтические композиции настоящего изобретения, подходящие для перорального введения,могут существовать в виде дискретных лекарственных форм, таких как, но не ограничиваясь ими, таблетки (например, жевательные таблетки), каплеты, капсулы и жидкости (например, ароматизированные сиропы). Такие лекарственные формы содержат предварительно определенные количества активных ингредиентов и могут быть получены способами, принятыми в фармацевтике, хорошо известными специалистам в данной области. См., например, Remington's Pharmaceutical Sciences, 18th ed., Mack Publishing,Easton PA (1990). Стандартные пероральные лекарственные формы готовят смешиванием активного ингредиента (ингредиентов) в однородной смеси по меньшей мере с одним вспомогательным веществом согласно общепринятым методикам приготовления лекарственных средств. Вспомогательные вещества могут иметь большое разнообразие форм в зависимости от формы заготовки, необходимой для введения. Из-за простоты их введения таблетки и капсулы представляют самые удобные пероральные стандартные лекарственные формы. При желании таблетки можно покрывать стандартными водными или неводными способами. Такие лекарственные формы можно получить общепринятыми в фармацевтике способами. В общем, фармацевтические композиции и лекарственные формы получают однородным и равномерным смешиванием активных ингредиентов с жидкой основой, тонкоизмельченной твердой основой или обоими и затем, при необходимости, формованием продукта в требуемые формы. Разрыхлители можно вводить в твердые лекарственные формы для того, чтобы обеспечить быстрое растворение.-9 016495 Смазывающие вещества можно также вводить для того, чтобы облегчить получение лекарственных форм(например, таблеток). 5.4.2.Парентеральные лекарственные формы Парентеральные лекарственные формы можно вводить пациентам различными способами, включая,но не ограничиваясь, подкожно, внутривенно (включая болюсную инъекцию), внутримышечно и внутриартериально. Поскольку данный способ введения обычно минует естественную защиту пациентов от заражения, парентеральные лекарственные формы являются особым образом стерилизованными, или их можно стерилизовать перед введением пациенту. Примеры парентеральных лекарственных форм включают, но не ограничиваются ими, растворы, готовые для введения, сухие продукты, готовые для растворения или суспендирования в фармацевтически приемлемой среде для введения, суспензии, готовые для введения, и эмульсии. Подходящие среды, которые можно применять, чтобы получить парентеральные лекарственные формы настоящего изобретения, являются хорошо известными в данной области техники. Примеры включают, но не ограничиваются ими, воду для инъекций USP; водные среды, такие как, но не ограничиваясь, раствор хлорида натрия, раствор Рингера, раствор декстрозы, раствор декстрозы и хлорида натрия и лактатный раствор Рингера; смешиваемые с водой среды, такие как, но не ограничиваясь, этиловый спирт, полиэтиленгликоль и полипропиленгликоль; и неводные среды, такие как, но не ограничиваясь, кукурузное масло, хлопковое масло, арахисовое масло, кунжутное масло, этилолеат, изопропилмиристат и бензилбензоат. 5.4.3. Трансдермальные, местные и мукозальные лекарственные формы Трансдермальные, местные и мукозальные лекарственные формы включают, но не ограничиваются ими, офтальмологические растворы, спреи, аэрозоли, кремы, лосьоны, мази, гели, растворы, эмульсии,суспензии или другие формы, известные специалистам в данной области техники. См., например, Remington's Pharmaceutical Sciences, 16th and 18th eds., Mack Publishing, Easton PA (19801990); и Introduction to Pharmaceutical Dosage Forms, 4th ed., LeaFebiger, Philadelphia (1985). Трансдермальные лекарственные формы включают пластыри "резервуарного типа" или "матриксного типа", которые можно применять на коже и носить в течение конкретного периода времени, чтобы обеспечить проникновение требуемого количества активных ингредиентов. Подходящие вспомогательные вещества (например, основы и разбавители) и другие материалы, которые можно применять, чтобы получить трансдермальные, местные и мукозальные лекарственные формы, являются хорошо известными специалистам в фармацевтической области и зависят от конкретной ткани, на которой данная фармацевтическая композиция или лекарственная форма будет применяться. В зависимости от конкретной ткани, которую нужно лечить, можно применять дополнительные компоненты перед, вместе с, или после лечения активными ингредиентами настоящего изобретения. Например, усилители проникновения можно применять, чтобы способствовать доставке активных ингредиентов в ткань.pH фармацевтической композиции или лекарственной формы или ткани, на которой применяют фармацевтическую композицию или лекарственную форму, можно также регулировать для того, чтобы облегчить доставку одного или более активных ингредиентов. Аналогично, полярность основырастворителя, его ионную силу, или тоничность можно регулировать для того, чтобы облегчить доставку. Соединения, такие как стеараты, можно также добавлять к фармацевтическим композициям или лекарственным формам, чтобы выгодно изменять гидрофильность или липофильность одного или более активных ингредиентов так, чтобы облегчить доставку. При этом стеараты могут служить в качестве жидкой среды для создания рецептуры, в качестве эмульгатора или поверхностно-активного вещества, и в качестве агента, улучшающего доставку или проникновение. Различные соли, гидраты или сольваты активных ингредиентов можно применять для того, чтобы дополнительно регулировать свойства полученной в результате композиции. 6. Примеры Аспекты настоящего изобретения можно понять из следующих примеров, которые не ограничивают его объем. 6.1. Синтез (1R,2S,3R)-1-(2-(5-метилизоксазол-3-ил)-1 Н-имидазол-5-ил)бутан-1,2,3,4-тетраола- 10016495 Указанное соединение получали общим способом A, который показан ниже на схеме 2. Схема 2 На которой а представляет DCE: (MeO)2CMe2 (1:1), п-TsOH, 70C; b представляет Ph3CONH2,MeOH, 1N HCl (1,0 экв.); с представляет 2N HCl/диоксан; d представляет н-BuLi 4,0 экв, THF, 0C, затем,N-метил-N-метоксиацетамид 5,0 экв.; и e представляет 1N HCl/диоксан (1:1). В частности, к суспензии 1 (4,34 г, 18,87 ммоль) в дихлорметане (30 мл) добавляли 2,2 диметоксипропан (30 мл) с последующим добавлением моногидрата п-толуолсульфокислоты (900 мг,4,72 ммоль). Суспензию нагревали при 70C в течение 16 ч, затем охлаждали до комнатной температуры и обрабатывали избытком триэтиламина (1 мл). Реакционную смесь концентрировали и остатки летучих веществ удаляли упариванием с толуолом для того, чтобы получить желтый остаток, который использовали немедленно без очистки. Желтый остаток растворяли в MeOH (100 мл) и затем обрабатывали N-тритилгидроксиламином(6,75 г, 24,53 ммоль) и 1N HCl (18,5 мл, 18,5 ммоль). Реакционная смесь становилась прозрачной через 1 ч, и ее выдерживали при комнатной температуре в течение 18 ч. После завершения реакционную смесь нейтрализовали до pH 7 10N раствором NaOH, затем концентрировали при пониженном давлении. Неочищенное вещество очищали хроматографией на силикагеле (32-63 мкм, 10% MeOH/CH2Cl2w/1%NH4OH) для того, чтобы получить защищенный продукт 2 (9,8 г, 91% выход, 2 стадии) в виде белой пены. Безводный 4 М диоксан (20 мл) добавляли к раствору 2 (3,11 г, 5,48 ммоль) в безводном диоксане(40 мл). Через 1 ч реакционную смесь концентрировали в вакууме, затем перерастворяли в безводномDCM (60 мл), обрабатывали избытком триэтиламина (5 мл), затем снова концентрировали. Неочищенный продукт пропускали через силикагель (3-8% MeOH/CH2Cl2 w/0,5-1,0% NH4OH) для того, чтобы получить оксим 3 (1,05 г, 59% выход) в виде белой пены. К раствору 3 (500 мг, 1,54 ммоль) в THF (15 мл) при -45C добавляли по каплям 1,6 М гексановый раствор н-BuLi (3,85 мл, 6,16 ммоль). Через 10 мин добавляли по каплям N-метил-N-метоксиацетамид(0,79 мл, 7,69 ммоль) и реакционную смесь нагревали до комнатной температуры. Через 2 ч реакцию прекращали добавлением NH4Cl (10 мл) и разбавляли водой (5 мл), чтобы растворить твердые вещества. Слои разделяли и водный слой экстрагировали Et2O (220 мл). Объединенные органические фракции промывали соляным раствором (25 мл), затем сушили над MgSO4 и концентрировали в вакууме. Полученную в результате пену очищали флэш-хроматографией на силикагеле (60-90% EtOAc:гексан) для того, чтобы получить белое пенообразное твердое вещество. К раствору промежуточного соединения - белого твердого вещества в диоксане (5 мл) добавляли 1NHCl (5 мл). Реакционную смесь нагревали при 80C в течение 2 ч и затем концентрировали при пониженном давлении досуха. Полученный в результате стекловидный твердый остаток лиофилизовали из воды (8 мл) для того, чтобы получить 4 (224 мг, 48% выход, 2 стадии) в виде рыхлого белого порошка. Данное соединение синтезировали общим способом A, алкилированием промежуточного соединения 3 N-метил-N-метоксиэтиламидом. MS m/z C12H17N3O5 [M+H]+ = 284; 1H ЯМР (400 МГц, D2O):7,24 Данное соединение получали модифицированным общим способом A, как показано ниже на схеме 3. Схема 3 На которой а представляет н-BuLi (4,0 экв), THF, 0C, затем DMF (5,0 экв.); b представляет TFAA,пиридин, DCM; и с представляет 1N HCl/диоксан (1:1), 50C. В частности, к раствору 3 (424 мг, 1,30 ммоль) в THF (15 мл) при -45C добавляли по каплям 2,5 М гексановый раствор н-BuLi (2,1 мл, 5,25 ммоль). Через 10 мин добавляли по каплям безводный DMF(0,505 мл, 6,52 ммоль) и реакционную смесь нагревали до комнатной температуры. Через 2 ч реакцию прекращали добавлением NH4Cl (10 мл) и разбавляли водой (5 мл) для того, чтобы растворить твердые вещества. Слои разделяли и водный слой промывали Et2O (220 мл). Объединенные органические фракции промывали соляным раствором (25 мл), затем сушили над MgSO4 и концентрировали в вакууме. Полученную в результате пену пропускали через слой силикагеля (3-6% MeOH: CH2Cl2 с 0,5% NH4OH) для того, чтобы получить гемиацеталь 5 (220 мг, 47% выход) в виде белой пены. К раствору 5 (130 мг, 0,37 ммоль) в THF последовательно при 0C добавляли пиридин (120 мкл,1,48 ммоль) и ангидрид трифторуксусной кислоты. Реакционную смесь нагревали до комнатной температуры в течение 10 мин и затем нагревали при 55C в течение 16 ч. После завершения реакционную смесь концентрировали в вакууме, затем очищали флэш-хроматографией на силикагеле (60-90%EtOAc:гексан) для того, чтобы получить гетеробициклический бискеталь (60 мг, 47% выход) в виде белой пены, с которого в конце удаляли защитную группу, применяя стандартные кислые условия для того,чтобы получить соединение примера 3 в виде белого кристаллического твердого остатка. MS m/zC10H13N3O5 [M+H]+ = 256; 1H ЯМР (400 МГц, D2O)8,87 (с, 1H), 7,55 (с, 1H), 7,05 (с, 1H), 5,21 (с, 1H),3,75 (м, 3H), 3,63 (м, 2H). 6.4. Альтернативный синтез (1R,2S,3R)-1-(2-(изоксазол-3-ил)-1 Н-имидазол-5-ил)бутан-1,2,3,4 тетраола. Указанное соединение также получали подходом, названным в данном изобретении общим способом В, который показан ниже на схеме 4 Схема 4 На которой: а представляет 1,0 экв. NaOMe в MeOH, при комнатной температуре, затем водная HCl. В частности, к раствору нитрила 7 (600 мг, 6,38 ммоль) в MeOH (10 мл) при комнатной температуре добавляли 25% мас./об. MeONa (0,83 мл, 3,83 ммоль). Через 3 ч добавляли фруктозаминацетат (1,53 г,6,38 ммоль) и раствор выдерживали при комнатной температуре с интенсивным перемешиванием в течение 5 ч. Затем добавляли другую порцию 25% мас./об. MeONa (0,66 мл, 3,19 ммоль) к густой суспензии. Через 16 ч реакционную смесь фильтровали и остаток на фильтре промывали ледяным MeOH. Затем остаток на фильтре обрабатывали 1N HCl (20 мл) и фильтровали. Водный раствор концентрировали в вакууме до постоянного веса для того, чтобы получить указанное в заголовке соединение (1,30 г, 66% выход) в виде белого порошка. Указанное в заголовке соединение получали общим способом В, применяя 2-метилтиазол-4 карбонитрил (1,023 г, 8,25 ммоль), метоксид натрия в метаноле (25 мас.%, 1,07 мл, 4,95 ммоль), метанол(8,25 мл) и соединение 8 (2,00 г, 8,26 ммоль). Через 2,5 дня добавляли дополнительную порцию метоксида натрия в метаноле (25 мас.%, 0,891 мл, 4,125 ммоль). Через 24 ч образовавшийся твердый остаток собирали фильтрацией и промывали холодным метанолом для того, чтобы получить указанное в заголовке соединение (1,70 г, 5,96 ммоль, 72% выход). MS m/z C11H15N3O4S [M+H]+ = 286; 1H ЯМР (400 МГц,CD3OD)2,81 (с, 3H), 3,67-3,75 (м, 2H), 3,77-3,88 (м, 2H), 5,21 (с, 1H), 7,47 (с, 1H), 8,35 (с, 1H). 6.6. Синтез гидрохлорида (1R,2S,3R)-1-(2-(1-бензил-1 Н-1,2,4-триазол-3-ил)-1 Н-имидазол-4 ил)бутан-1,2,3,4-тетраола Указанное соединение получали общим способом В со следующими изменениями: 1-бензил-1H1,2,4-триазоле-3-карбонитрил (2,10 г, 11,4 ммоль) растворяли в метаноле (12 мл) и обрабатывали метоксидом натрия в метаноле (25 мас.%, 1,48 мл, 6,8 ммоль) и перемешивали в течение 18 ч, и добавляли 8, и реакционную смесь перемешивали в течение 18 ч. Полученный в результате твердый остаток отделяли фильтрацией, промывали метанолом и сушили в вакууме для того, чтобы получить белый твердый остаток (3,20 г, 9,28 ммоль, 81% выход). Данный твердый остаток суспендировали в THF (50 мл), охлаждали в ледяной бане и добавляли HCl (4 М в диоксане, 7,5 мл, 30 ммоль). Ледяную баню удаляли и суспензию перемешивали в течение 4 ч. Твердый остаток отделяли фильтрацией, промывали THF и сушили в вакууме для того, чтобы получить указанное в заголовке соединение (3,50 г, 9,19 ммоль, 99% выход) в виде белого твердого вещества. MS m/z C16H19N5O4 [M+H]+ = 346; 1H ЯМР (400 МГц, CD3OD)2,81 (с, 3H),3,67-3,75 (м, 2H), 3,77-3,88 (м, 2H), 5,21 (с, 1H), 7,47 (с, 1H), 8,35 (с, 1H). 6.7. Синтез (1R,2S,3R)-1-(1H,1'H-2,2'-биимидазол-5-ил)бутан-1,2,3,4-тетраола Указанное соединение получали общим способом В со следующими изменениями. К раствору 1Hимидазол-2-карбонитрила (0,39 г, 4,17 ммоль) в метаноле (4,8 мл) добавляли раствор метоксида натрия в метаноле (25 мас.%, 0,54 г, 0,57 мл, 2,50 ммоль), перемешивали в течение 16 ч и добавляли в 10 млMeOH соединение 8 (0,964 г, 4,17 ммоль). Образовывался осадок, который фильтровали и промывали ацетоном (15 мл). Фильтрат концентрировали досуха и очищали препаративной ВЭЖХ (10 мМ водный ацетат аммония/ацетонитрил) для того, чтобы получить указанное в заголовке соединение (0,0141 г,0,0554 ммоль) в виде серовато-белого твердого вещества. MS m/z C10H14N4O4 [M+H]+ = 255; 1H ЯМР (400 МГц, CD3OD)3,56-3,57 (м, 2H), 3,67-3,74 (м, 2H), 4,90 (с, 1H), 7,04 (с, 1H). 6.8. Синтез (1R,2S,3R)-1-(2-(5-метокси-4,5-дигидроизоксазол-3-ил)-1H-имидазол-5-ил)бутан-1,2,3,4 тетраола 1 М раствор HCl (10 мл) добавляли при комнатной температуре к раствору имидазола 5 (схема 3,- 13016495 500 мг, 1,41 ммоль) в MeOH (10 мл). Реакционную смесь нагревали при 50C в течение 8 ч, охлаждали до комнатной температуры и концентрировали досуха для того, чтобы получить указанное в заголовке соединение (430 мг, 100% выход) в виде слегка желтого порошка в виде смеси 1:1 диастереомеров. MS m/z Указанное в заголовке соединение получали из 1-(5-4S,4'R,5R)-2,2,2',2'-тетраметил-4,4'-би(1,3 диоксолан)-5-ил)-1H-имидазол-2-ил)этанона (соединение 9) следующим способом. Раствор 9 (975 мг,3,15 ммоль) в THF (15 мл) медленно добавляли при -10C к раствору гексаметилдисилазана калия (15,72 мл 0,5 М толуольного раствора, 7,86 ммоль) в THF (15 мл). Реакционную смесь выдерживали при -10C в течение 10 мин перед добавлением этилацетата (1,55 мл, 15,75 ммоль). Реакционную смесь нагревали до комнатной температуры в течение 1 ч, затем реакцию прекращали добавлением 30 мл NH4Cl (насыщенный водный). Слои разделяли и водный слой промывали EtOAc (230 мл). Объединенные органические фракции промывали водой (30 мл) и соляным раствором (30 мл), затем сушили над MgSO4 и концентрировали. Полученное в результате рыжеватое вещество применяли без дополнительной очистки. Неочищенное вещество растворяли в EtOH (20 мл) и подкисляли 1N HCl (5 мл). Затем перемешиваемый раствор обрабатывали при комнатной температуре избытком моногидрата гидразина (200 мкл). После завершения реакционную смесь доводили до pH 7 1N NaOH, затем концентрировали до -10 мл объема. Добавляли DCM (30 мл) для того, чтобы растворить твердые вещества, которые выпали из водного раствора, и слои разделяли. Органический слой сушили над MgSO4 и концентрировали. Неочищенный остаток пропускали через силикагель (5-10% MeOH:DCM элюент) для того, чтобы получить защищенный пиразол (204 мг, 19% выход) в виде прозрачной пены. Раствор 1N HCl (5 мл) добавляли при комнатной температуре к раствору защищенного гетеробицикла (180 мг, 0,52 ммоль) и реакционную смесь нагревали при 50C. Через 1,5 ч реакционную смесь охлаждали до комнатной температуры, затем концентрировали досуха. Пену перерастворяли в 2 млMeOH, затем растирали с 3 мл Et2O и охлаждали до 0C перед декантированием жидкости. Твердый остаток промывали Et2O (22 мл), затем сушили при высоком вакууме для того, чтобы получить указанное в заголовке соединение (130 мг, 70% выход) в виде белого порошка. MS m/z C16H16N4O4 [M+H]+ = 269; 1H ЯМР (400 МГц, D2O)7,28 (с, 1H), 6,52 (с, 1H), 5,07 (д, J=0,9 Гц, 1H), 3,74-3,54 (м, 4H), 2,22 (с, 1H); 13C ЯМР (D2O):142,8, 139,1, 136,3, 134,1, 116,0, 104,0, 72,6, 70,6, 64,4, 62,7, 9,6. 6.10. Количественное определение действия на лимфоциты у мышей. Соединения вводили перорально при принудительном питании или в питьевой воде. Для экспериментов с пероральным дозированием кристаллические соединения суспендировали с концентрацией 10 мг/мл в среде (например, воде). Мышам (Fl гибриды 129/В 6 штамма) принудительно вводили однократную 100 мг/кг дозу соединения (эквивалент 100 миллиграммам на килограмм свободного основания для каждого соединения) или только среду в контрольной группе, и возвращали в их клетки. Мышам вводили наркоз, применяя изофлуоран через 18 ч после введения дозы, и ткани собирали для анализа, как описано ниже. Что касается исследований с применением питьевой воды, соединения растворяли до концентрации 50 мг/л в подкисленной воде (pH 2,8), содержащей 10 г/л глюкозы. Мышам обеспечивали свободный доступ к воде, содержащей соединение (или раствор глюкозы в качестве контроля), в течение 72 ч. После завершения 72-часового периода ткани собирали для анализа. СВС измерения проводили следующим образом. Мышам вводили наркоз, применяя изофлуоран, и кровь собирали позади глазничного сплетения в пробирку для взятия крови с EDTA (Capiject-MQK, Terumo Medical Corp., Elkton, MD). Автоматизированные СВС анализы проводили, применяя Cell-Dyn 3500(Abbott Diagnostics, Abbott Park, IL) или HemaVet 850 (Drew Scientific, Inc., Oxford, CT) прибор. Измерения проточной цитометрии (FACS) проводили следующим образом. Двадцать пять мкл цельной крови лизировали гипотоническим шоком, промывали один раз 2 мл промывочного буфераFACS (FWB: PBS/0,1% BSA/0,1% NaN3/2 мМ EDTA) и окрашивали в течение 30 мин при 4C до черноты смесью антител, связанных с хромофором, разбавленных в 50 мкл FWB. После окрашивания клетки промывали один раз 2 мл FWB и повторно суспендировали в 300 мкл FWB для получения информации. Стандартные методики для нестерильного удаления селезенки и тимуса были следующими. Органы диспергировали до одноклеточной суспензии пропусканием ткани через 70 мкм клеточное сито (Falcon,- 14016495Diego, CA) (1/10 разбавление в FWB) в течение 15 мин при 4C. Клетки окрашивали смесью антител,связанных с хромофором, разбавленных в 50-100 мкл FWB, добавленных непосредственно к клеткам вFc Block, в течение 30 мин при 4C до черноты. После окрашивания клетки промывали один раз 1 млFWB, повторно суспендировали в 300 мкл FWB для получения информации. Все антитела были получены у BD-PharMingen, San Diego CA, если не указано особо. Образцы анализировали, применяя FACSCalibur проточный цитометр и CellQuest Pro software (Becton Dickinson Immunocytometry Systems, SanJose, CA). Смеси антител, применяемые для тимуса, были: TCRb APC Cy7; CD4 APC; CD8 PerCP; CD69 FITC; и CD62L PEI. Смеси антител, применяемые для селезенки и крови, были: В 220 PerCP; TCRb APC; CD4APC Cy7; CD8 РЕ Cy7; CD69 FITC и CD62L РЕ. 6.11. Количественное определение действия на концентрации S1P у мышей. Концентрации S1P в мышиной (F1 гибриды 129/B6 штамма) селезенке определяли, применяя вариант радиоанализа на связывание с рецептором, описанный в Murata, N., et al, Anal. Biochem. 282:115-120(2000). В данном способе применяют HEK293F клетки, сверхэкспрессирующие Edg-1, один из подтипов рецептора S1P, и он основан на конкуренции меченого S1P с немеченым S1P в данном образце.HEK2 93F клетки трансфицируют вектором, экспрессирующим pEFneo S1P рецептор (Edg-1), и отбирают G418-устойчивый клеточный клон. HEK293F клетки, экспрессирующие Edg-1, выращивают в 12 мультипланшетах в DMEM, содержащей 5% (об./об.) FBS во влажной атмосфере воздух:CO2 (19:1). За двадцать четыре часа до эксперимента среду заменяют на свежую DMEM (без сыворотки), содержащую 0,1% (мас./об.) BSA. Через восемнадцать часов после введения испытуемого соединения мышей умерщвляли, и их селезенки удаляли и замораживали. S1P получали из замороженных тканей, применяя известные способы. См., например, Yatomi, Y., et al, FEBS Lett. 404:173-174 (1997). В частности, 10 мыщиных селезенок в 1 мл ледяного 50 мМ фосфатного буфера (рН 7,5), содержащего 1 мМ EGTA, 1 мМ DTT и полные ингибиторы протеаз фирмы Roche, гомогенизировали три раза с одноминутным интервалом на льду. Полученную смесь центрифугировали при 2500 об./мин и 4C в течение 10 мин для того, чтобы удалить клеточный детрит. Затем надосадочную жидкость ультрацентрифугировали при 45000 об./мин и 4C в 70Ti роторе в течение 1 ч для того, чтобы отделить мембранно-связанные белки. Надосадочную жидкость выбрасывали и осадок повторно суспендировали в минимальном объеме (1 мл) ледяного 50 мМ фосфатного буфера (pH 7,5), содержащего 1 мМ EGTA, 1 мМ DTT и 33% глицерина, в присутствии полных ингибиторов протеаз фирмы Roche. Суммарную концентрацию белка измеряли, применяя анализ по Брэдфорду.S1P экстрагировали в хлороформ/KCl/NH4OH (рН 12), и верхнюю водную фазу сохраняли. Затем ее экстрагировали в хлороформ/метанол/HCl (pH1), и нижний органический слой сохраняли и упаривали для того, чтобы получить S1P, который хранили замороженным до применения. Непосредственно перед анализом высушенный образец растворяли обработкой ультразвуком в буфере для связывания,состоящем из 20 мМ Tris-HCl (pH 7,5), 100 мМ NaCl, 15 мМ NaF и 0,4% (мас./об.) BSA. Содержание S1P образца определяли радиоанализом на связывание с рецептором на основе конкурентного связывания [33P]S1P с S1P в образце на клетках, экспрессирующих Edg-1. Клетки HEK293F,экспрессирующие Edg-1, в соединенных 12 мультипланшетах промывали дважды ледяным буфером для связывания и затем выдерживали с тем же самым буфером, содержащим 1 нМ [33P]S1P (приблизительно 1800 распадов в минуту на лунку) и увеличенные дозы аутентичного S1P или испытуемого образца с конечным объемом 0,4 мл. Планшеты выдерживали на льду в течение 30 мин, и клетки промывали дважды тем же самым ледяным буфером для связывания для того, чтобы удалить несвязанные лиганды. Клеткам придавали растворимость, применяя раствор, состоящий из 0,1% SDS, 0,4% NaOH и 2% Na2CO3, и радиоактивность измеряли жидкостным сцинтилляционным счетчиком. Содержание S1P в лунках для анализа оценивали экстраполяцией из стандартной кривой замещения. Содержание S1P в первоначальном испытуемом образце (образцах) вычисляли умножением величины, полученной из стандартной кривой, применяя коэффициент извлечения S1P экстракцией и фактор разбавления. 6.12. Действия соединений на лимфоциты у мышей. Применяя способы, описанные выше, определяли действия in vivo различных соединений. Действия двух из соединений по сравнению с контрольными группами показаны на фигуре 1. Соединения вводили мышам (F1 гибриды 129/B6 штамма) в питьевой воде. Результаты получены через 18 ч после перорального введения соединений при концентрации 100 мг/кг. Все цитируемые публикации, патенты и патентные заявки вводятся в данное изобретение полностью с помощью ссылки. или его фармацевтически приемлемая соль или сольват, гдеA представляет 5- или 6-членный гетероцикл, содержащий по меньшей мере один атом азота и необязательно замещенный C1-10-алкокси, C1-10-алкилфенилом, C1-10-алкилом, фенилом или гидроксилом;R1 представляет водород или C1-4-алкил;R8 представляет CH2OR8A, CH2OC(O)R8A, водород и каждый из R5A, R6A, R7A и R8A независимо представляет водород или C1-4-алкил. 2. Соединение по п.1, в котором A представляет дигидроимидазол, дигидроизоксазол, дигидропиразол, дигидротиазол, имидазол, изоксазол, изоксазолидин или пиразол. 3. Соединение по п.1, которое имеет формулу II(a)R1 представляет водород или C1-4 алкил; каждый R4 независимо представляет водород, OR4A, OC(O)R4A, C1-10-алкил, фенил, C1-10-алкилфенил, фенил-C1-10-алкил или галоген;R4A представляет водород или C1-4-алкил и каждый R9 независимо представляет водород, C1-10-алкил, фенил, C1-10-алкилфенил или фенил-C1-10 алкил. 4. Соединение по п.3, в котором R4 представляет водород, C1-10-алкил, фенил или C1-10-алкилфенил. 5. Соединение по п.3 или 4, в котором X представляет N и Y представляет O, или X представляет N и Y представляет NR9, или X представляет N и Y представляет S, или X представляет N и Z представляетO, или X представляет N и Z представляет NR9, или X представляет N и Z представляет S, или X представляет N, Y представляет N и Z представляет NR9. 6. Соединение по п.3 или 5, в котором R9 представляет водород, C1-10-алкил, фенил или C1-10 алкилфенил. 7. Соединение по любому из пп.1-6, в котором R1 представляет водород. 8. Соединение по любому из пп.1-7, где один или более из R5, R6, R7 и R8 представляют ацетат или гидроксил. 9. Соединение по п.8, в котором все R5, R6, R7 и R8 представляют ацетат или все R5, R6, R7 и R8 представляют гидроксил. 10. Соединение по п.1, которое представляет(1R,2S,3R)-1-(2-(5-метил-1 Н-пиразол-3-ил)-1H-имидазол-5-ил)бутан-1,2,3,4-тетраол. 11. Соединение по п.10, которое представляет (1R,2S,3R)-1-(2-(изоксазол-3-ил)-1H-имидазол-5 ил)бутан-1,2,3,4-тетраол. 12. Применение соединения по любому из пп.1-11 в качестве лекарственного средства. 13. Применение соединения по любому из пп.1-11 в качестве лекарственного средства для подавления иммунного ответа у пациента. 14. Применение соединения по любому из пп.1-11 в качестве лекарственного средства для лечения,регулирования или предотвращения заболевания или расстройства, где заболевание или расстройство представляет рассеянный склероз, псориаз, псориатический артрит, ревматоидный артрит, отторжение трансплантата или диабет I типа.
МПК / Метки
МПК: A61K 31/4196, C07D 413/04, A61K 31/422, C07D 417/04, C07D 403/04, A61K 31/427, A61P 37/00, A61P 29/00
Метки: применения, содержащие, способы, гетероциклические, композиции, соединения
Код ссылки
<a href="https://eas.patents.su/19-16495-geterociklicheskie-soedineniya-soderzhashhie-ih-kompozicii-i-sposoby-ih-primeneniya.html" rel="bookmark" title="База патентов Евразийского Союза">Гетероциклические соединения, содержащие их композиции и способы их применения</a>
Предыдущий патент: (2r,4αs,10αr)-4α-бензил-7-((2-метилпиридин-3-ил)карбамоил)-2-(трифторметил)-1,2,3,4,4α,9,10,10α-октагидрофенантрен-2-илдигидрофосфат или его соль
Следующий патент: Способ получения смеси синтез-газа
Случайный патент: N-ацилированные октасахариды, активирующие рецепторы fgf, их получение и применение в терапии