Соединения (тиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ила, обладающие двойной активностью обратных агонистов рецепторов h1/антагонистов рецепторов 5-ht2a
Формула / Реферат
1. Соединение согласно формуле
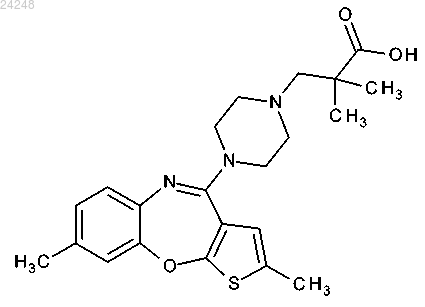
или его фармацевтически приемлемая соль.
2. Соединение по п.1, которое представляет собой соль хлороводородной кислоты.
3. Соединение по п.1, которое представляет собой тозилатную соль.
4. Фармацевтическая композиция для лечения бессонницы, содержащая соединение по п.1 или его фармацевтически приемлемую соль в комбинации по меньшей мере с одним фармацевтически приемлемым носителем, разбавителем или наполнителем.
5. Применение соединения по п.1 или его фармацевтически приемлемой соли для лечения бессонницы.
6. Применение по п.5, где бессонница характеризуется трудностями в засыпании или поддержании сна, или обоими, тем и другим.
7. Применение по п.5 или 6 у человека.
8. Применение соединения по п.1 или его фармацевтически приемлемой соли при приготовлении лекарственного средства для лечения бессонницы.
9. Применение по п.8, отличающееся тем, что бессонница характеризуется трудностями в засыпании или поддержании сна, или и тем, и другим у млекопитающего.
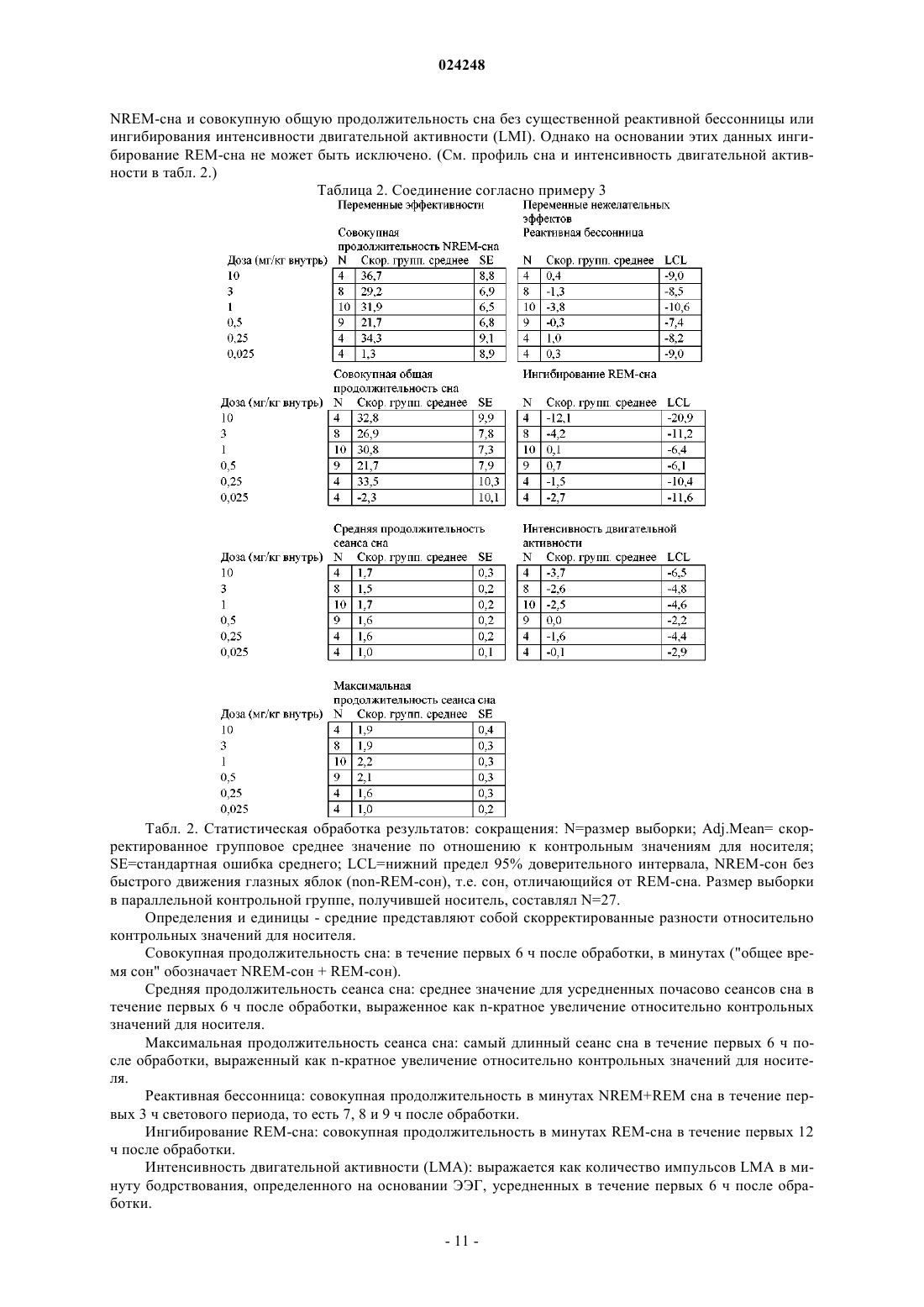
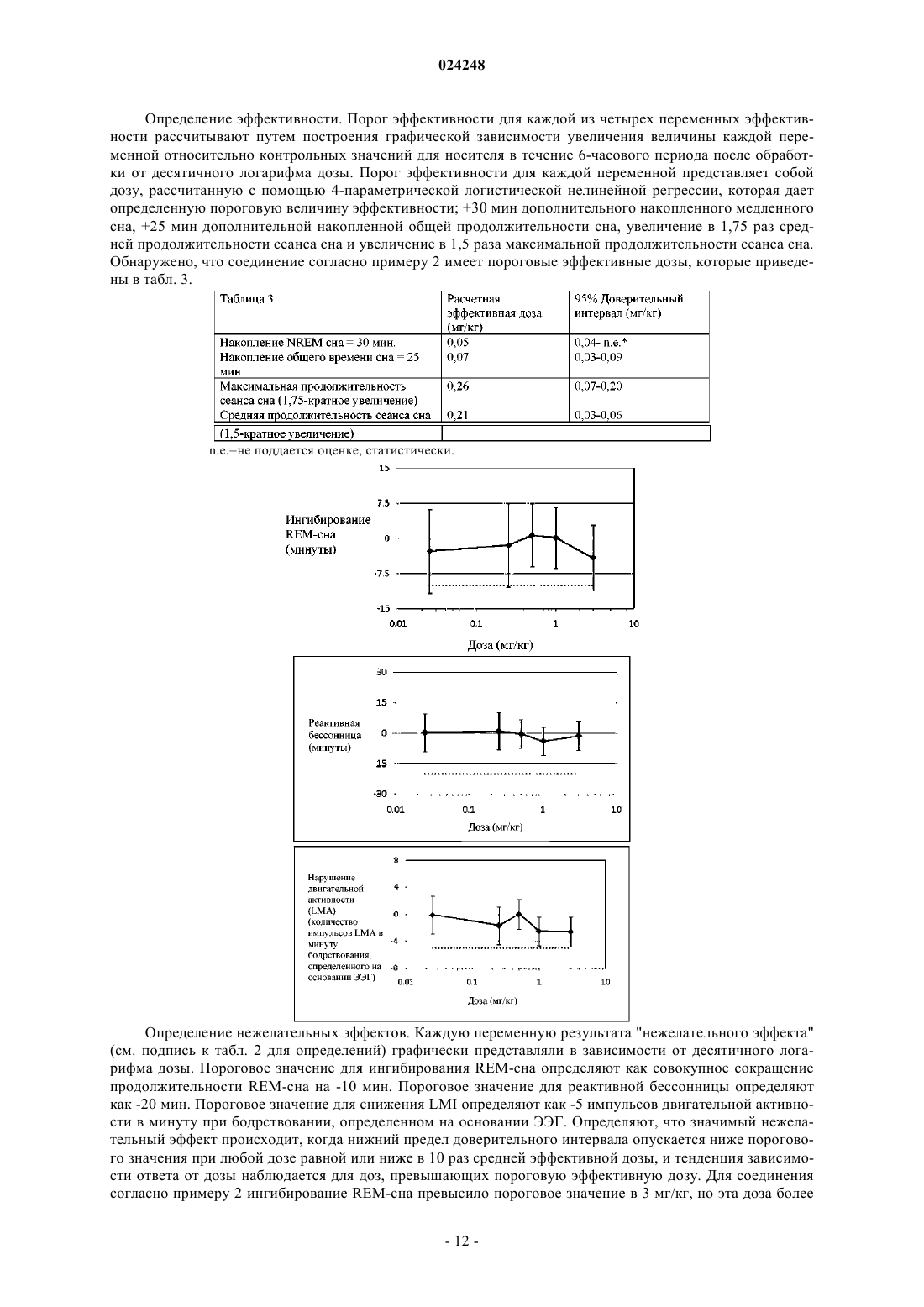
Текст
СОЕДИНЕНИЯ (ТИЕНО[2,3-B][1,5]БЕНЗОКСАЗЕПИН-4-ИЛ)ПИПЕРАЗИН-1 ИЛА, ОБЛАДАЮЩИЕ ДВОЙНОЙ АКТИВНОСТЬЮ ОБРАТНЫХ АГОНИСТОВ РЕЦЕПТОРОВ H1/АНТАГОНИСТОВ РЕЦЕПТОРОВ 5-HT2A В настоящей заявке описан обратный агонист рецепторов H1/антагонист рецепторов 5-HT2A,обладающий двойной активностью, согласно формуле Ледгард Эндрю Джеймс (US) его применение, а также способы его получения.(71)(73) Заявитель и патентовладелец: ЭЛИ ЛИЛЛИ ЭНД КОМПАНИ (US) Гистамин играет важную роль в различных физиологических процессах посредством взаимодействия по меньшей мере с четырьмя различными рецепторами, связанными с G-белками, в частности с рецепторами H1-H4. В центральной нервной системе (ЦНС) рецепторы H1 играют ключевую роль в цикле регулирования сна, и известно, что антагонисты/обратные агонисты H1 вызывают сонливость. Серотонин также играет важную роль в различных физиологических процессах посредством взаимодействия по меньшей мере с четырнадцатью различными рецепторами, связанными с G-белками. Модуляция рецепторов 5-HT2A в ЦНС играет ключевую роль в цикле регулирования сна, причем было показано, что антагонисты 5-HT2A улучшают медленный сон и поддержание сна у пациентов с бессонницей. Соединения, обладающие активностью обратных агонистов или антагонистов рецепторов H1 или 5HT2A (например, доксепин и тразодон соответственно), использовали при лечении бессонницы, и они продемонстрировали значимое фармакологическое действие в исследованиях сна на животных. Однако на данный момент на рынке отсутствуют обладающие двойной активностью селективные обратные агонисты/антагонисты рецепторов H1/5-HT2A. В патенте WO 2007/022068 описаны некоторые замещенные соединения (тиено[2,3-b][1,5]бензодиазепин-4-ил)пиперазин-1-ила и (тиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ила для применения в лечении нарушений сна. В настоящем изобретении предложена 3-[4-(2,8-диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропановая кислота и е фармацевтически приемлемые соли, которые являются сильными обратными агонистами рецептора H1, сильными антагонистами рецептора 5-HT2A и обладают хорошей селективностью в отношении этих рецепторов, особенно по сравнению с другими рецепторами гистамина, рецепторами серотонина и другими физиологически значимыми рецепторами, в частности по сравнению с рецепторами 5-HT2C, рецепторами ГАМК типа A (ГАМКА), мускариновыми рецепторами,дофаминергическими рецепторами, адренергическими рецепторами и каналом hERG. В экспериментах на животных моделях было показано, что указанные соединения также можно применять в лечении нарушений сна, характеризующихся плохим поддержанием сна. Таким образом, полагают, что указанные соединения можно применять в лечении нарушений сна, которые характеризуются недостаточной продолжительностью латентного периода сна или недостаточным поддержанием сна, или и тем, и другим,например, в лечении бессонницы, как, например, хронической или преходящей первичной бессонницы,или хронической или преходящей вторичной бессонницы, или обеих. Примеры вторичной бессонницы включают, но не ограничиваются ими, бессонницу, связанную с депрессивными расстройствами (например, большим депрессивным расстройством, дистимией и/или циклотимией), бессонницу, связанную с тревожными расстройствами (например, генерализованным тревожным расстройством и/или социальной фобией), бессонницу, связанную с болью (например, фибромиалгией, хроническими болями костей или суставов, такими как связанные с воспалительным артритом или остеоартритом, или диабетической невропатической болью), бессонницу, связанную с аллергической реакцией (например, аллергической астмой, зудом, ринитом, заложенностью и т.д.), бессонницу, связанную с нарушениями со стороны легких или дыхательных путей (например, с обструктивным апноэ сна, реактивной болезнью дыхательных путей и т.д.), бессонницу, связанную с психическими нарушениями, слабоумием и/или нейродегенеративными заболеваниями, и/или бессонницу, связанную с нарушениями сна, которые вызваны циркадными ритмами (например, нарушение сна при посменной работе, нарушение сна из-за смены часовых поясов,синдром отсроченного наступления фазы сна, синдром раннего наступления фазы сна, синдром не-24 часового цикла сна и бодрствования и т.д.). Кроме того, соединения согласно настоящему изобретению при одновременном введении с селективными ингибиторами обратного захвата серотонина демонстрируют усиление их действия в отношении стадии сна без быстрых движений глазных яблок (NREM-сон). В настоящем изобретении предложено соединение согласно формуле I или его фармацевтически приемлемая соль. То есть 3-[4-(2,8-диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропановая кислота или ее фармацевтически приемлемая соль. Согласно другому аспекту настоящего изобретения предложена фармацевтическая композиция, содержащая соединение согласно формуле I или его фармацевтически приемлемую соль в комбинации по меньшей мере с одним фармацевтически приемлемым носителем, разбавителем или наполнителем. Также согласно данному аспекту настоящего изобретения предложена фармацевтическая композиция для лечения бессонницы, как например, бессонницы, которая характеризуется длительным латентным периодом сна или недостаточным поддержанием сна, или и тем, и другим, такой, как например, первичная бессонница, нарушение сна из-за смены часовых поясов, нарушение сна при посменной работе, синдром отстроченного наступления фазы сна, синдром раннего наступления фазы сна и/или синдром не-24 часового цикла сна и бодрствования, содержащая соединение согласно формуле I или его фармацевтически приемлемую соль в комбинации с одним или более фармацевтически приемлемыми наполнителями,носителями или разбавителями. Согласно другому варианту реализации данного аспекта настоящего изобретения предложена фармацевтическая композиция, содержащая соединение согласно формуле I или его фармацевтически приемлемую соль в комбинации по меньшей мере с одним фармацевтически приемлемым носителем, наполнителем или разбавителем и возможно другими терапевтическими ингредиентами. Согласно другому варианту реализации данного аспекта настоящего изобретения фармацевтическая композиция дополнительно содержит второй терапевтический агент, который является ингибитором обратного захвата серотонина, такой как, например, циталопрам, флуоксетин, пароксетин и/или флувоксетин. В настоящем изобретении также предложен способ лечения бессонницы, например, бессонницы,которая характеризуется длительным латентным периодом сна или недостаточным поддержанием сна,или и тем, и другим, такой, как например, первичная бессонница, нарушение сна из-за смены часовых поясов, нарушение сна при посменной работе, синдром отстроченного наступления фазы сна, синдром раннего наступления фазы сна и/или синдром не-24-часового цикла сна и бодрствования, у млекопитающего, включающий введение млекопитающему, нуждающемуся в таком лечении, эффективного количества соединения согласно формуле I или его фармацевтически приемлемой соли. Согласно другому варианту реализации данного аспекта изобретения указанный способ дополнительно включает одновременное, раздельное или последовательное введение второго терапевтического агента, который является ингибитором обратного захвата серотонина, такого как, например, циталопрам, флуоксетин, пароксетин и/или флувоксетин. Согласно одному конкретному варианту реализации указанных способов лечения млекопитающее представляет собой человека. В настоящем изобретении также предложено соединение согласно формуле I или его фармацевтически приемлемая соль для применения в терапии. Согласно данному аспекту изобретения предложено соединение согласно формуле I или его фармацевтически приемлемая соль для применения при лечении бессонницы. Согласно другим вариантам реализации настоящего изобретения бессонница характеризуется длительным латентным периодом сна или недостаточным поддержанием сна, или и тем, и другим,как например, первичная бессонница, нарушение сна из-за смены часовых поясов, нарушение сна при посменной работе, синдром отстроченного наступления фазы сна, синдром раннего наступления фазы сна и/или синдром не-24-часового цикла сна и бодрствования. Согласно другому варианту реализации данного аспекта изобретения предложено соединение согласно формуле I или его фармацевтически приемлемая соль для одновременного, раздельного или последовательного применения с ингибитором обратного захвата серотонина, таким как, например, циталопрам, флуоксетин, пароксетин и/или флувоксетин, в лечении бессонницы. Согласно одному конкретному варианту реализации данного аспекта настоящего изобретения указанное применение предложено в отношении млекопитающего, в частности человека. В другом аспекте настоящего изобретения предложено применение соединения согласно формуле I или его фармацевтически приемлемой соли при приготовлении лекарственного препарата для лечения бессонницы, такой как, например, первичной бессонницы, которая характеризуется длительным латентным периодом сна или недостаточным поддержанием сна, или и тем, и другим, такой как, например,первичная бессонница, нарушение сна из-за смены часовых поясов, нарушение сна при посменной работе, синдром отстроченного наступления фазы сна, синдром раннего наступления фазы сна и/или синдром не-24-часового цикла сна и бодрствования. В другом варианте реализации данного аспекта изобретения предложено применение соединения согласно формуле I или его фармацевтически приемлемой соли и второго терапевтического агента, который представляет собой ингибитор обратного захвата серотонина,такой как, например, циталопрам, пароксетин, флуоксетин и/или флувоксетин, при приготовлении лекарственного препарата для лечения бессонницы, такой, как например, бессонница, которая характеризуется длительным латентным периодом сна и/или недостаточным поддержанием сна, такой, как например, первичная бессонница, нарушение сна из-за смены часовых поясов, нарушение сна при посменной работе, синдром отстроченного наступления фазы сна, синдром раннего наступления фазы сна и/или синдром не-24-часового цикла сна и бодрствования. Приведенная ниже нумерация трициклической кольцевой структуры будет использована для ясности по всему тексту настоящей заявки Соединение согласно настоящему изобретению имеет основные и кислотные остатки, и, соответственно, реагирует с рядом органических и неорганических кислот и оснований с образованием фармацевтически приемлемых солей. Фармацевтически приемлемые соли соединения согласно настоящему изобретению включены в область настоящей заявки. В настоящей заявке термин "фармацевтически приемлемая соль" относится к любой соли соединения согласно настоящему изобретению, которая, по существу, нетоксична для живых организмов. Такие соли включают соли, перечисленные в Journal of Pharmaceutical Science. 66, 2-19 (1977), которые известны специалистам в данной области. В настоящей заявке сокращения определяют следующим образом:"Соляной раствор" обозначает насыщенный водный раствор NaCl."DMEM" обозначает минимальную эссенциальную среду Игла, модифицированную по способу Дульбекко."ФБС" обозначает фетальную бычью сыворотку."ВЭЖХ" обозначает высокоэффективную жидкостную хроматографию."Час" обозначает час или часы."ИК 50" обозначает концентрацию, при которой достигается 50% от максимального ингибирования."Мин" обозначает минуту или минуты."ЯМР" обозначает ядерный магнитный резонанс."ТГФ" обозначает тетрагидрофуран. Общая химия Соединение согласно настоящему изобретению может быть приготовлено в соответствии со следующими примерами синтеза. Препарат 1. Метил-5-метилтиофен-3-карбоксилат Смешивают 4-бром-2-метилтиофен (24,5 г, 138,37 ммоль), бис-(1,3-дифенилфосфино)пропан (2,35 г, 5,53 ммоль), ацетат палладия (1,24 г, 5,53 ммоль), триэтиламин (38,57 мл, 276,73 ммоль), метанол (40 мл) и диметилсульфоксид (80 мл) и продувают реакционный сосуд монооксидом углерода. Повышают давление монооксида углерода до 30 фунт/кв. дюйм и нагревают смесь до 70C при постоянном перемешивании в течение 24 ч в атмосфере монооксида углерода. Выпаривают летучие вещества при пониженном давлении с получением темно-оранжевого раствора. Добавляют воду (300 мл) и проводят экстракцию этилацетатом (3150 мл), затем промывают объединенные органические экстракты водой (2100 мл). Высушивают над сульфатом натрия, фильтруют и выпаривают при пониженном давлении. Добавляют 10% диэтиловый эфир в изогексане (500 мл) и удаляют полученный темно-желтый осадок с помощью фильтрования. Выпаривают фильтрат при пониженном давлении с получением метил 5 метилтиофен-3-карбоксилата (18,894 г, выход 87,42%) в виде жидкости. 1H-ЯМР (400,13 МГц, CDCl3):7,84 (d, J=1,5, 1H), 7,16 (t, J=1,5, 1H), 3,83 (с, 3H) и 2,46 (d, J=1,5, 3H). Препарат 2. 5-Метилтиофен-3-карбоновая кислота В 250-мл колбу вносят метил-5-метилтиофен-3-карбоксилат (16,4 г, 104,99 ммоль, 1,00 экв.) и растворяют в метаноле (57,40 мл). Добавляют NaOH (12,60 г, 314,97 ммоль, 3 экв.) и воду (19,68 мл). Нагревают суспензию с использованием обратного холодильника (65C) в течение 45 мин до завершения реакции путем проведения ЖХ-МС. Реакционную смесь охлаждают до комнатной температуры, затем добавляют 5 М водный раствор HCl (85 мл, 5 объемов) с последующим добавлением этилацетата (130 мл, 7,5 объема). Перемешивают в течение 15 мин до растворения твердых веществ. Разделяют слои и экстрагируют водный слой этилацетатом (2130 мл). Промывают объединенные органические экстракты водой(3130 мл), а затем насыщенным солевым раствором (85 мл). Высушивают над сульфатом натрия, фильтруют и концентрируют с получением твердого вещества 5-метилтиофен-3-карбоновой кислоты (13,93 г,выход 93,32%). МС (м/з): 141,0 (M-H). 1H-ЯМР (400,13 МГц, CDCl3): 7,99 (d, J=1,5 Гц, 1H), 7,20 (d, t =1,5 Гц, 1H), 2,50 (d, J=1,5, 3H). Препарат 3. 2-Бром-5-метилтиофен-3-карбоновая кислота К раствору 5-метилтиофен-3-карбоновой кислоты (13,93 г, 97,98 ммоль, 1,00 экв.) в уксусной кислоте (119,80 мл) по каплям в течение 20 мин добавляют бром (5,03 мл, 97,98 ммоль, 1,00 экв.) в виде раствора в уксусной кислоте (59,90 мл). Реакционную смесь перемешивают при комнатной температуре в течение 1 ч до завершения реакции путем проведения ЖХ-МС. Медленно выливают реакционную смесь в воду (696,50 мл) при комнатной температуре и собирают полученный осадок с помощью фильтрования. Промывают водой (100 мл) и высушивают в вакууме в атмосфере азота на подложке в течение 16 ч с получением белого твердого вещества 2-бром-5-метилтиофен-3-карбоновой кислоты (20,55 г, выход 94,88%). МС (м/з): 218,89, 220,79 (M-H). 1H-ЯМР (400,13 МГц, CDCl3): 7,08 (d, J=1,5 Гц, 1H), 2,42 (s,3H). Препарат 4. 2-Бром-N-(2-гидрокси-4-метилфенил)-5-метилтиофен-3-карбоксамид В колбе объемом 1 л к суспензии 2-бром-5-метилтиофен-3-карбоновой кислоты (45,2 г, 204,46 ммоль, 1,00 экв.) в дихлорметане (316,40 мл) добавляют диметилформамид (500 мкл) и затем по каплям 2 М оксалилхлорид в дихлорметане (112,45 мл, 224,90 ммоль, 1,1 экв.) (Осторожно Происходит образование газа). Реакционную смесь перемешивают при комнатной температуре в течение 2 ч до превращения реакционной смеси в прозрачный, темный раствор и завершения реакции путем проведения ТСХ(элюент 30% EtOAc в изогексане). Выпаривают раствора досуха, а затем повторно растворяют полученное в результате твердое вещество в безводном тетрагидрофуране (678 мл). Вносят этот раствор в колбу,содержащую 6-амино-м-крезол (33,40 г, 265,79 ммоль 1,3 экв.), пиридин (82,67 мл, 1,02 моль, 5 экв.) и безводный тетрагидрофуран (678 мл). Перемешивают при комнатной температуре в течение 2 ч до завершения реакции путем проведения ЖХ-МС. Выливают реакционную смесь в 1 М водный раствор HCl(2,71 л, 60 объемов) при постоянном перемешивании и собирают полученный осадок с помощью фильтрования. Промывают 1 М водным раствором HCl (250 мл), а затем водой (250 мл) и сушат под вакуумом на фильтровальной подложке в течение ночи с получением красного твердого вещества 2-бром-N-(2 гидрокси-4-метилфенил)-5-метилтиофен-3-карбоксамида (62,34 г, выход 93,47%). Если необходимо,твердое вещество может быть дополнительно очищено путем промывания метанолом. МС (м/з): 325,98,327,93 (M+H). Препарат 5. 2,8-Диметил-5H-тиено [2,3-b][1,5]бензоксазепин-4-он лия (79,23 г, 573,30 ммоль, 3 экв.) Реакционную смесь нагревают до 140C при перемешивании в течение 4 ч до завершения реакции путем проведения ЖХ-МС. Реакционную смесь охлаждают до комнатной температуры и затем выливают в воду (2,5 л), контролируя количество выделившегося тепла с помощью бани со льдом. Смесь подкисляют 2 М водным раствором HCl (450 мл), экстрагируют дихлорметаном(4800 мл) и промывают органическую фазу насыщенным водным раствором бикарбоната натрия (1,2 л),а затем водой (22 л). Органическую фазу высушивают, фильтруют и концентрируют. Очищают методом флэш-хроматографии на силикагеле (750 г) и элюируют в градиенте от 0 до 20% этилацетата в дихлорметане с получением твердого вещества 2,8-диметил-5H-тиено[2,3-b][1,5]бензоксазепин-4-она (28,1 г; 59,94%). МС (м/з): 246,09 (M+H). Препарат 6. 4-Хлор-2,8-диметилтиено[2,3-b][1,5]бензоксазепин Нагревают суспензиию 2,8-диметил-5H-тиено[2,3-b][1,5]бензоксазепин-4-она (26,84 г, 109,42 ммоль, 1,00 экв.) в метоксибензоле (107,36 мл) в 500-мл колбе до приблизительно 60C. Добавляют N,Nдиметиланилин (38,89 мл, 306,37 ммоль, 2,8 экв.) в виде одной части, а затем фосфорилхлорид (23,39 мл,251,66 ммоль, 2,3 экв.) в течение 15 мин. Прогревают полученный раствор при 100C в течение 2 ч до завершения реакции путем проведения ЖХ-МС. Незначительно охлаждают реакционную смесь и выпаривают с получением темного масла 4-хлор-2,8-диметилтиено[2,3-b][1,5]бензоксазепина (28,85 г, предполагаемый количественный выход). МС (м/з): 264,0 (M+H). Препарат 7. Метил 3-[4-(2,8-диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропаноат К раствору 4-хлор-2,8-диметилтиено[2,3-b][1,5]бензоксазепина (28,85 г, 109,39 ммоль, 1,00 экв.) в ацетонитриле (288,50 мл) добавляют метил-2,2-диметил-3-пиперазин-1-ил-пропаноат (59,77 г, 218,77 ммоль, 2 экв.) и карбонат калия (136,06 г, 984,47 ммоль, 9 экв.) Смесь нагревают при слабой рециркуляции в обратном холодильнике (82C) в течение 3 ч до завершения реакции путем проведения ЖХ-МС. Реакционную смесь охлаждают и выпаривают. Затем разделяют между водой (300 мл) и этилацетатом(3300 мл). Промывают объединенные органические экстракты водой (2300 мл), а затем насыщенным солевым раствором. Высушивают над сульфатом натрия, фильтруют и выпаривают. Очищают методом флэш-хроматографии на силикагеле (800 г) и элюируют в градиенте от 0 до 30% этилацетата в изогексане с получением густого масла метил-3-[4-(2,8-диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропаноата (37,95 г, выход 81,14%). МС (м/з): 428,1 (M+H). Пример 1. 3-[4-(2,8-Диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропановая кислота К взвеси метил-3-[4-(2,8-диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропаноата (37,95 г, 88,76 ммоль, 1,00 экв.) в изопропиловом спирте (227,70 мл) и воде (227,70 мл) добавляют гидроксид натрия (10,65 г, 266,27 ммоль, 3 экв.) и нагревают смесь при слабой рециркуляции в обратном холодильнике (85C) в течение 1,5 ч до полного растворения и завершения реакции путем проведения ЖХ-МС. Реакционную смесь охлаждают до комнатной температуры и нейтрализуют до значения pH, составляющего приблизительно 6,0-6,5, 2 М водным раствором HCl (приблизительно 120 мл) с получением твердого осадка. Удаляют органический растворитель в вакууме с получением суспензии. Проверяют pH суспензии и, если необходимо, дополнительно доводят до значения pH, равного 6,0-6,5, с помощью 2 М водного раствора HCl (приблизительно 15 мл). Суспензию фильтруют и промывают водой,затем высушивают в течение 24 ч под вакуумом. Ресуспендируют неочищенный твердый материал в аце-5 024248 тонитриле (100 мл, 2,5 объема), обрабатывают ультразвуком и затем осторожно нагревают (40C) при перемешивании в течение 15 мин. Продукт фильтруют, промывают ацетонитрилом (320 мл), а затем высушивают в вакууме с получением твердого вещества 3-[4-(2,8-диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропановой кислоты (29,5 г, выход 80,37%). МС (м/з): 414,1 К суспензии 3-[4-(2,8-диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропановой кислоты (300 мг, 725,44 мкмоль, 1,00 экв.) в изопропиловом спирте (4,50 мл) при 50C добавляют 4 М HCl в 1,4-диоксане (453,40 мкл, 1,81 ммоль, 2,5 экв.) Нагревают полученный раствор до 60C в течение 30 мин, а затем охлаждают до комнатной температуры. Выпаривают в вакууме, ресуспендируют полученное твердое вещество в диэтиловом эфире (4,50 мл) в течение 15 мин, затем собирают фильтрованием и высушивают на подложке. Далее высушивают в вакуумной печи в течение 1 ч с получением кристаллического твердого вещества 3-[4-(2,8-диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропановой кислоты дигидрохлорида (346 мг, 98,0%). МС (м/з): 414,0 (M+H). Пример 3. 3-[4-(2,8-Диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропановая кислота; 4-метилбензолсульфоновая кислота К суспензии 3-[4-(2,8-диметилтиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ил]-2,2-диметилпропановой кислоты (300 мг, 725,44 мкмоль, 1,00 экв.) в этаноле (6 мл) при 50C добавляют п-толуолсульфоновую кислоту (124,92 мг, 725,44 мкмоль, 1 экв.) и перемешивают полученный раствор в течение 30 мин при 50C. Раствор охлаждают до комнатной температуры и выпаривают под вакуумом с получением твердого вещества. Ресуспендируют твердое вещество в диэтиловом эфире (4,50 мл) в течение 15 мин, затем собирают фильтрованием и сушат на подложке. Далее сушат в вакуумной печи в течение 1 ч с получением кристаллического твердого вещества 3-[4-(2,8-диметилтиено[2,3-b][1,5]бензоксазепин-4 ил)пиперазин-1-ил]-2,2-диметилпропановой кислоты; 4-метилбензолсульфоновой кислоты (413 мг, 97%). МС (м/з): 414,0 (M+H). Данные из литературных источников (Morairty S.R., Hedley L., Flores J., Martin R., Kilduff T.S.and Wake Disorders, CNSNeurological Disorders-Drug Targets, vol. 6, pg. 31-43 (2007 и данные, полученные в ходе доклинических исследований на животных, подтверждают роль обратных агонистов рецепторов H1/антагонистов рецепторов 5-HT2A, обладающих двойной активностью, в лечении бессонницы и в симптоматическом лечении бессонницы, связанной с другими заболеваниями, такими как депрессивные расстройства, тревожные расстройства, боли, аллергии, нарушения со стороны легких или дыхательных путей, психические нарушения, слабоумие и/или нейродегенеративные заболевания, и/или с нарушениями циркадного ритма сна. В частности, в ходе экспериментов на грызунах без непропорциональной или клинически значимой пониженной активности, уменьшения продолжительности сна с быстрыми движениями глазных яблок (REM-сна) или повышенной сонливости, активность мозга которых контролировали с помощью ЭЭГ, было обнаружено, что некоторые обратные агонисты рецепторовH1/антагонисты рецепторов 5-HT2A с двойной активностью эффективно увеличивают общую продолжительность сна. Чтобы дополнительно продемонстрировать свойства соединений согласно настоящему изобретению они могут быть исследованы с помощью количественных анализов in vitro и in vivo, представленных ниже: Количественные исследования связывания и активности in vitro Исследование конкурентного связывания с рецептором H1 Эксперименты по исследованию связывания [H3]-пириламина осуществляют с помощью сцинтил-6 024248 ляционного анализа сближения (SPA) в 96-луночных планшетах. Мембраны, используемые в этом исследовании, готовят из клеток линии HEK-293, стабильно экспрессирующих рекомбинантный рецепторH1 (человеческий). Инкубацию инициируют добавлением смеси гранул SPA PVT WGA (1 мг/лунку, Perkin Elmer (Массачусетс, США) RPNQ0001) и 3 мкг мембран к буферу для исследования (67 мМ Трис, pH 7,6), содержащему 3,5 нМ [H3]-пириламина и различные концентрации исследуемого соединения (10 точечные кривые зависимости ответа от концентрации). Неспецифическое связывание определяют в присутствии 10 мкМ трипролидина. Образцы инкубируют в течение 4 ч при комнатной температуре(22C) и затем считывают данные с помощью устройства Microbeta Trilux. Исследование конкурентного связывания с рецептором 5-HT2A Эксперименты по исследованию связывания [H3]-кетансерина осуществляют с помощью SPA в 96 луночных планшетах. Мембраны, используемые в этом исследовании, готовят из клеток линии AV-12,стабильно экспрессирующих рекомбинантный рецептор 5-HT2A (человека). Инкубацию инициируют добавлением смеси гранул WGA YSi SPA (1 мг/лунку, Perkin Elmer (Массачусетс, США), RPNQ0011) и 2 мкг мембран к буферу для исследования (67 мМ Трис, 0,5 мМ ЭДТА, pH 7,6), содержащему 3,1 нМ [H3]кетансерина и различные концентрации исследуемого соединения (10-точечные кривые зависимости ответа от концентрации). Неспецифическое связывание определяют в присутствии 20 мкМ 1-(1-нафтил)пиперазина. Образцы инкубируют в течение 4 ч при комнатной температуре (22C) и затем считывают данные с помощью устройства Microbeta Trilux. Исследование конкурентного связывания с рецептором 5-HT2C Эксперименты по исследованию связывания [I125]-DOI осуществляют с помощью SPA в 96 луночных планшетах. Мембраны, используемые в этом исследовании, готовят из клеток линии AV-12,стабильно экспрессирующих рекомбинантный рецептор 5-HT2C (человеческий). Инкубацию инициируют добавлением смеси гранул SPA PVT WGA (0,5 мг/лунку, Perkin Elmer (Массачусетс, США), RPNQ0001) и 2,5 мкг мембран к буферу для исследования (50 мМ Трис-HCl, 10 мМ MgCl2, 0,5 мМ ЭДТА, 10 мкМ паргилина, 0,1% аскорбиновой кислоты, pH 7,4), содержащему 0,2 нМ [I125]-DOI и различные концентрации исследуемого соединения (10-точечные кривые зависимости ответа от концентрации). Неспецифическое связывание определяют в присутствии 20 мкМ 1-(1-нафтил)пиперазина. Образцы инкубируют в течение 4 ч при комнатной температуре (22C) и затем считывают данные с помощью устройства Microbeta Trilux. Анализ данных из исследований связывания Кривые оценивают, используя уравнение нелинейной 4-параметрической логистической регрессии,чтобы получить концентрацию конкурента, которая вызывает 50% ингибирование связывания радиолиганда (ИК 50). Равновесные константы диссоциации (Ki) рассчитывают в соответствии с уравнениемKi=IC50/(1+L/Kd), где L - это концентрация радиоактивного лиганда, используемого в эксперименте, и Kd- это равновесная константа диссоциации радиолиганда в отношении рецептора, которая определяется на основании стандартного анализа насыщения или экспериментов по исследованию конкурентного связывания гомологичных соединений. Приведенные в настоящей заявке значения Ki, где указаны значения n,представлены как среднее геометрическоестандартная ошибка среднего (SEM) с числом повторных определений, указанных как n. Геометрические средние рассчитывают с помощью уравнения GeoMean = 10(Average (log Ki 1+ log Ki 2 + log Ki n)/sqrt n). Исследование антагонистического действия в отношении ГАМКА рецепторов с использованием нативных рецепторов в первичной культуре нейронов Активность соединений в отношении нативных рецепторов ГАМКА оценивают путем мониторинга потоков кальция с помощью системы FLIPR, адаптированной для 96-луночных планшетов (планшетридер для регистрации флуориметрических изображений (FLIPR, Molecular Devices. Вкратце, эмбриональные кортикальные нейроны выделяют из крысиных эмбрионов на 18 дне гестации (E18) и высевают в оптимальной плотности на покрытые поли-D-лизином 96-луночные планшеты с черными стенками и прозрачным дном для использования в системе FLIPR. После загрузки клеток чувствительным к кальцию красителем (Fluo4-AM, Molecular Devices) клетки промывают в растворе с низкой концентрацией анионов хлора (хлорид заменен на глюконат). В этих условиях активация рецепторов ГАМКА вызывает отток ионов хлора (по направлению химического градиента), что приводит к деполяризации мембраны и, следовательно, активации потенциал-зависимых кальциевых каналов (ПЗКК). Вход ионов кальция через ПЗКК регистрируют и исследуют в автономном режиме с использованием системы FLIPR. Для фармакологической апробации исследования концентрационные кривые регистрируют для стандартного агониста (ГАМК) и стандартного антагониста (габазин). Любые эффекты определяют в режиме концентрационных кривых в сравнении с фиксированной 10 мкМ концентрацией агониста ГАМК (которая эквивалентна ЭК 90 в отношении ГАМК). Методы Антагонистическое действие соединений количественно оценивают с помощью 10-точечных кривых зависимости ответа от дозы путем сравнения пикового флуоресцентного ответа на агонист ГАМК в присутствии и в отсутствие исследуемого соединения. Окно анализа определяют как максимальный от-7 024248 вет, полученный при действии ГАМК в заданной ЭК 90, минус ответ, полученный при полностью ингибирующей концентрации габазина (50 мкМ). Антагонистическое действие рассчитывают как процент от окна анализа. Все данные рассчитывают как относительные величины ИК 50 с использованием программы для построения 4-параметрической логистической модели (Prism Graphpad 3.01). Антагонистическую активность всех соединений сравнивают с активностью габазина с тремя повторами определений для каждого испытания. Далее соединения согласно настоящему изобретению могут быть испытаны в исследованиях связывания и исследованиях функциональной активности с помощью способов, хорошо известных для других физиологически важных рецепторов, включая, но не ограничиваясь перечисленными: канал hERG, другие рецепторы серотонина (в частности, рецепторы 5-HT1B, 5-HT1D, отсутствие агонистической активности в отношении рецепторов 5-HT2B, рецепторы 5-HT2C, 5-HT5, 5-HT6 и 5-HT7), рецепторы дофамина (в частности, D1, D2 и D3), рецепторы ГАМКА, адренергические рецепторы и транспортеры моноаминов. Соединение согласно примеру 2 исследовали, по существу, как описано выше, причем обнаружено,что указанное соединение имеет профили активности, которые приведены в табл. 1. Таблица 1. Данные по исследованию селективности Таким образом, физиологически значимые дозы соединений согласно настоящему изобретению,как ожидается, обеспечат существенное ингибирование рецепторов H1 и 5-HT2A in vivo, при этом, по существу, не взаимодействуя с другими физиологически значимыми рецепторами, и таким образом, как ожидается, обеспечат желаемое фармакологическое действие, избегая при этом нежелательных эффектов, связанных с нецелевой активностью. Нежелательные эффекты включают, но не ограничиваются ими, антагонистическую активность в отношении рецепторов 5-HT2C, связанную с увеличением веса после начала лечения, агонистическую активность в отношении рецепторов 5-HT2B, связанную с вальвулопатией, модуляцию канала hERG, связанную с пролонгацией интервала QT, и антагонистическую активность в отношении ГАМКА, связанную с судорожной активностью. Кроме того, селективность в отношении рецепторов дофамина, других рецепторов серотонина, адренорецепторов и транспортеров моноаминов позволяет избежать нежелательного воздействия на нормальную физиологию цикла сна/бодрствования. Исследование занятости рецепторов 5-HT2A: занятость рецепторов (ЗР) исследуют, чтобы продемонстрировать активность соединений в качестве антагонистов/обратных агонистов рецепторов 5-HT2Ain vivo. Вкратце, самцы крыс линии Sprague-Dawley (Harlan Sprague-Dawley, Индианаполис, Индиана,США) весом приблизительно 230-280 г получают неограниченный доступ к пище и воде до начала 3 часового экспериментального протокола. В качестве положительного контроля используют 1 мг/кг кетансерина (неселективный антагонист 5-HT2A), чтобы установить пригодность исследования. Исследуемые соединения или контроль вводят через желудочный зонд в носителе, состоящем из 20% гидроксипропил бета-циклодекстрина. В качестве индикатора используют MDL 100907 R)-(+)(2,3-диметоксифенил)-1-[2-(4-фторфенил)этил]-4-пиперидинметанола), селективный антагонист 5-HT2A. MDL 100907 суспендируют в воде с 5 мкл разбавленной молочной кислоты (1 мг/мл), разведенной до 6 мкг/мл нормальным физиологическим раствором, и вводят в объеме 1 мл/кг внутривенно через латеральную хвостовую вену с получением дозы индикатора в 3 мкг/кг. Крысам вводят исследуемое соединение, кетансерин или носитель (N=4), затем через 1 ч внутривенно вводят 3 мкг/кг дозу индикатора MDL 100907. Полагают, что занятость рецептора измеряется именно в момент введения индикатора. Через пятнадцать минут после введения индикатора крыс умерщвляют путем цервикальной дислокации. Собирают образцы плазмы и берут образцы лобной коры и мозжечка. Уровень индикатора MDL 100907 измеряют в каж-8 024248 дом образце коры и мозжечка. ЗР рассчитывают с использованием хорошо известного метода определения соотношений, в котором используется участок с высокой плотностью рецепторов, представляющий общее связывание (лобная кора), нормализованный к области с отсутствующим или очень низким уровнем рецепторов (мозжечок). Этот участок, обозначенный как нулевой участок, используют для контроля неспецифического связывания индикаторного лиганда. Соотношение уровней индикатора в коре по сравнению с мозжечком у животных, получивших только носитель, представляет собой 0% занятости. Соотношение равное 1 представляет собой 100% занятость и достигается, когда специфическое связывание индикатора MDL 100907 с рецептором 5-HT2A полностью блокируется. Промежуточные соотношения уровней индикатора в коре по сравнению с мозжечком, полученные в группе животных, предварительно обработанных исследуемым соединением, интерполируют с помощью линейной аппроксимации между соотношением уровней индикатора у получивших носитель животных (0% занятость) и соотношением 1 (100% занятость) для того, чтобы определить процент ЗР 5-HT2A. Исследование с использованием MDL 100907: образцы коры и мозжечка взвешивают и помещают в конические центрифужные пробирки на льду. В каждую пробирку добавляют по четыре объема(масс/об.) ацетонитрила, содержащего 0,1% муравьиную кислоту. Затем образцы гомогенизируют и центрифугируют при 14000 оборотов в минуту (21920 g) в течение 16 мин. Супернатант разбавляют путем добавления 100-900 мкл стерильной воды в ВЭЖХ флаконах для инъекций для исследования методом ЖХ/МС/МС. Исследование с использованием MDL 100907 проводят на детекторе для ВЭЖХ системыAgilent 1200 (Agilent Technologies, Пало Альто, Калифорния, США) и масс-спектрометра API 4000. Хроматографическое разделение проводят на колонке C18 2,150 мм (Agilent971700-907) с подвижной фазой, состоящей из 60% ацетонитрила в воде с общим содержанием муравьиной кислоты 0,1%. Детектирование MDL 100907 осуществляют путем мониторинга ионного перехода от предшественника к продукту с отношением массы к заряду (m/z) от 374,2 до 123,0. Стандарты готовят добавлением известных количеств аналита к образцам ткани мозга из необработанных крыс и обрабатывают как описано выше. Статистические методы: кривые для каждого исследования аппроксимировали с помощью 4 параметрической логистической функции с нижним фиксированным пределом 0%, используя программное обеспечение JMP, версия 8.0 (SAS Institute Inc., Кэри Северная Каролина, США), абсолютное значение эффективной дозы (ЭД 50) рассчитывали с помощью программного обеспечения. Значения приведены в виде средних величин, стандартных ошибок и 95% доверительных интервалов. Соединение согласно примеру 2 исследовали, по существу, как описано выше, причем было обнаружено, что указанное соединение обеспечивает высокую занятость рецепторов 5-HT2A с ЭД 50, равной 0,09 мг/кг. Ингибирование активности DOI-индуцированного качания головой: способность соединения согласно настоящему изобретению блокировать активность качания головой, индуцированного агонистом рецептора 5-HT2A 2,5-диметокси-4-йодамфетамином (DOI), дополнительно демонстрирует его антагонистическую активность в отношении рецептора 5-HT2A (см., например, Bartoszyk G.D., van Amsterdam C.,Bttcher H., Seyfried C.A. EMD 281014, a new selective serotonin 5-HT2A receptor antagonist. Eur J Pharmacol. 2003, 473: 229-230). Вкратце, самцов мышей линии C57BL/6J (20-25 г, Charles River) размещают в стандартных условиях содержания (по 32 мыши в большой клетке с индивидуальной вентиляцией, световая фаза с 07.00 до 19.00, постоянная температура (19-23C) и влажность (50% 10%), неограниченный доступ к пище и воде). Мыши получали носитель (0,25% метилцеллюлоза), DOI (3 мг/кг в физиологическом растворе) или исследуемое соединение в дозе 10 мг/кг внутрь плюс DOI (3 мг/кг в физиологическом растворе). Исследуемые соединения оценивают индивидуально в группах по четыре животных в одном эксперименте с n=4 для каждого соединения, вместе с носителем и DOI+носитель (n=8). После предварительной обработки исследуемым соединением в течение 60 мин мыши получают носитель (физиологический раствор) или 3 мг/кг DOI подкожно, затем животных помещают в прозрачные плексигласовые камеры для наблюдения. Через пять минут после введения DOI или носителя количество визуально подсчитанных качаний головой, которое продемонстрировала каждая отдельная мышь, подсчитывают в течение 15 мин. Данные анализируют с использованием дисперсионного анализа и post-hoc теста Даннета. Соединение согласно примеру 2 исследовали, по существу, как описано выше, причем было обнаружено,что указанное соединение в дозе 10 мг/кг ингибирует DOI-индуцированную реакцию качания головой на 100%. Мониторинг сна и поведения у крыс: соединение согласно настоящему изобретению исследуют на крысах для установления его способности увеличивать продолжительность сна или уменьшать прерывание сна, или оказывать оба вида активности без нежелательных эффектов, таких как ингибированиеREM-сна, двигательная недостаточность при пробуждении и/или реактивная бессонница. Экспериментальных животных постоянно контролировали с помощью регистрации электроэнцефалограмм (ЭЭГ),электромиограмм (ЭМГ) и движения для измерения совокупной продолжительности NREM-сна, совокупной общей продолжительности сна, средней продолжительности сеанса сна, максимальной продолжительности сеанса сна, реактивной бессонницы, ингибирования REM-сна и интенсивности двигательной активности во время бодрствования. Методы таких исследований известны в данной области (см.,например, методы, описанные в Edgar D.M., Seidel W.F. Modafinil induces wakefulness without intensifyingof a microcomputer-based system for mice. Sleep 1991, 14: 48-55; and Gross B.A., Walsh C.M., Turakhia A.A.,Booth V., Mashour G.A., Poe G.R. Open-source logic-based automated sleep scoring software using electrophysiological recordings in rats. J Neurosci Methods. 2009; 184(1): 10-8). Исследования проводят следующим образом. Подготовка животных. Взрослых самцов крыс линии Wistar (приблизительно 270-300 г на время операции) хирургически готовят для хронической регистрации ЭЭГ, ЭМГ и движения следующим образом: крыс готовили хирургическим путем, вживляя черепно-мозговой имплантат, который состоит из четырех винтов из нержавеющей стали для записи ЭЭГ (два фронтальных [3,9 мм антерально относительно брегмы и 2,0 мм медиолатерально] и два затылочных [6,4 мм постерально относительно брегмы 5,5 мм медиолатерально]) и двух проводов из нержавеющей стали с тефлоновым покрытием для записи ЭМГ (расположенных под затылочными трапециевидными мышцами). Все провода припаивают к миниатюрному разъему (Microtech, Бутвин, Пенсильвания, США) до начала операции. Комплекс имплантата прикрепляют к черепу с помощью комбинации винтов из нержавеющей стали для регистрации ЭЭГ,цианоакрилата, применяемого между разъемом имплантата и черепом, а также зубного акрила. Двигательную активность контролируют с помощью миниатюрного передатчика (Minimitter PDT4000G, PhilipsRespironics, Бенд, Орегон, США), который хирургическим путем помещают в брюшную полость. Не меньше 3 недель предусматривается для восстановления животного. Окружающая среда при регистрации. Каждая крыса содержится индивидуально в микроизолирующей клетке, модифицированной путем вставки поликарбонатной стойки с фильтром на конце, чтобы обеспечить большую вертикальную внутреннюю высоту. Гибкий кабель, который минимально ограничивает движение животного, соединяют одним концом с переключателем, прикрепленным к клетке сверху, а другим концом к черепному имплантату животного. Каждую клетку располагают в отдельных, вентилируемых отсеках камеры регистрации цикла сон-бодрствование, изготовленной из нержавеющей стали. Пища и вода доступны без ограничений, температуру окружающей среды поддерживают на уровне приблизительно 231C. На протяжении всего исследования поддерживают 24-часовой цикл светтемнота (LD 12:12), используя флуоресцентный свет. Средняя относительная влажность составляет приблизительно 50%. Животных не беспокоят по меньшей мере в течение 30 ч до и после завершения каждой обработки. Дизайн исследования и дозирование. Носитель (плацебо, метилцеллюлоза 15 сП 0,25% в воде) или один из уровней дозы исследуемого соединения вводят внутрь в количестве 1 мл/кг псевдорандомизированным образом так, чтобы ни одна крыса не получила одну и ту же обработку два раза, причем ни одна из крыс не получает более двух из 8 обработок в любом одном исследовании. Каждую крысу вынимают из клетки приблизительно на одну минуту для взвешивания и обработки. До начала и после завершения каждой обработки проводят по меньшей мере 6-дневный период "вымывания". Сбор данных. Разграничение сна и бодрствования может быть автоматизировано (например, VanGelder et al., 1991 (см. выше); Edgar et al., 1997 (см. выше); Winrow C.J., et al., Neuropharmacology 2010; 58(l):185-94.; and Gross et al., 2009 (см. выше. Сигнал ЭЭГ усиливают и фильтруют ( 10000, полоса пропускания 1-30 Гц), сигнал ЭМГ усиливают и интегрируют (полоса пропускания 10-100 Гц, RMS интеграция) и одновременно контролируют неспецифическую двигательную активность (LMA). Состояние повышенной активности ЦНС классифицируют по 10-секундным эпохам как NREM-сон, REM-сон,бодрствование или бодрствование с доминирующим тета-ритмом. Двигательную активность (LMA) записывают как количество импульсов в минуту и детектируют с помощью коммерчески доступных приемников телеметрии (ER4000, Minimitter, Бенд, Орегон, США). Статистический анализ. Всех животных, имеющих по меньшей мере один результат, включают в обобщенные результаты (например, включают соответствующие данные, полученные при обработке животных, для которых доступны данные телеметрии, но нет данных ЭЭГ). Период наблюдения после завершения обработки разделен на интервалы после завершения дозирования, соответствующие каждому результату, где время дозирования определяется как начало в час=0, а результаты обобщены за период наблюдения путем вычисления среднего почасового или совокупного значения по каждому периоду (см. подпись к табл. 2 для точного определения каждого результата). Сеансы сна анализируют по логарифмической шкале, чтобы стабилизировать вариабельность, все другие переменные анализируют по линейной шкале. Каждый результат в каждом периоде анализируют с помощью ковариационного анализа с использованием в качестве факторов группы обработки и даты обработки и в качестве ковариаты соответствующего интервала до начала обработки, на 24 ч ранее. Скорректированные средние и изменение относительно средних величин для носителя и соответствующих стандартных ошибок приведены для каждой группы обработки. Результаты, которые анализировали по логарифмической шкале, обратно преобразованы для получения геометрических средних и средних результатов соотношения для носителя. Соединение согласно примеру 2 исследовали, по существу, как описано выше. Обнаружено, что соединение согласно примеру 2 в дозе 3 мг/кг значительно увеличивает совокупную продолжительностьNREM-сна и совокупную общую продолжительность сна без существенной реактивной бессонницы или ингибирования интенсивности двигательной активности (LMI). Однако на основании этих данных ингибирование REM-сна не может быть исключено. (См. профиль сна и интенсивность двигательной активности в табл. 2.) Таблица 2. Соединение согласно примеру 3 Табл. 2. Статистическая обработка результатов: сокращения: N=размер выборки; Adj.Mean= скорректированное групповое среднее значение по отношению к контрольным значениям для носителя;SE=стандартная ошибка среднего; LCL=нижний предел 95% доверительного интервала, NREM-сон без быстрого движения глазных яблок (non-REM-сон), т.е. сон, отличающийся от REM-сна. Размер выборки в параллельной контрольной группе, получившей носитель, составлял N=27. Определения и единицы - средние представляют собой скорректированные разности относительно контрольных значений для носителя. Совокупная продолжительность сна: в течение первых 6 ч после обработки, в минутах ("общее время сон" обозначает NREM-сон + REM-сон). Средняя продолжительность сеанса сна: среднее значение для усредненных почасово сеансов сна в течение первых 6 ч после обработки, выраженное как n-кратное увеличение относительно контрольных значений для носителя. Максимальная продолжительность сеанса сна: самый длинный сеанс сна в течение первых 6 ч после обработки, выраженный как n-кратное увеличение относительно контрольных значений для носителя. Реактивная бессонница: совокупная продолжительность в минутах NREM+REM сна в течение первых 3 ч светового периода, то есть 7, 8 и 9 ч после обработки. Ингибирование REM-сна: совокупная продолжительность в минутах REM-сна в течение первых 12 ч после обработки. Интенсивность двигательной активности (LMA): выражается как количество импульсов LMA в минуту бодрствования, определенного на основании ЭЭГ, усредненных в течение первых 6 ч после обработки. Определение эффективности. Порог эффективности для каждой из четырех переменных эффективности рассчитывают путем построения графической зависимости увеличения величины каждой переменной относительно контрольных значений для носителя в течение 6-часового периода после обработки от десятичного логарифма дозы. Порог эффективности для каждой переменной представляет собой дозу, рассчитанную с помощью 4-параметрической логистической нелинейной регрессии, которая дает определенную пороговую величину эффективности; +30 мин дополнительного накопленного медленного сна, +25 мин дополнительной накопленной общей продолжительности сна, увеличение в 1,75 раз средней продолжительности сеанса сна и увеличение в 1,5 раза максимальной продолжительности сеанса сна. Обнаружено, что соединение согласно примеру 2 имеет пороговые эффективные дозы, которые приведены в табл. 3. Определение нежелательных эффектов. Каждую переменную результата "нежелательного эффекта"(см. подпись к табл. 2 для определений) графически представляли в зависимости от десятичного логарифма дозы. Пороговое значение для ингибирования REM-сна определяют как совокупное сокращение продолжительности REM-сна на -10 мин. Пороговое значение для реактивной бессонницы определяют как -20 мин. Пороговое значение для снижения LMI определяют как -5 импульсов двигательной активности в минуту при бодрствовании, определенном на основании ЭЭГ. Определяют, что значимый нежелательный эффект происходит, когда нижний предел доверительного интервала опускается ниже порогового значения при любой дозе равной или ниже в 10 раз средней эффективной дозы, и тенденция зависимости ответа от дозы наблюдается для доз, превышающих пороговую эффективную дозу. Для соединения согласно примеру 2 ингибирование REM-сна превысило пороговое значение в 3 мг/кг, но эта доза более чем в 10 раз превышает самую консервативную эффективную дозу в 0,26 мг/кг (табл. 3); кажущееся ингибирование REM-сна при дозах в 0,25 и 0,025 мг/кг не является частью дозозависимой тенденции и не является статистически значимым и, следовательно, может считаться артефактом небольшого размера выборки при этих дозах. Тем не менее, на основании этих данных ингибирование REM-сна не может быть исключено. Можно сделать вывод, что при дозах более чем в 10 раз превышающих самую высокую консервативную эффективную дозу не наблюдают нежелательных явлений, таких как ингибированиеREM-сна, реактивная бессонница или снижение количества импульсов LMI, однако ингибированиеREM-сна не может быть исключено. Отрицательные значения указывают на ингибирование REM-сна,реактивную бессонницу и снижение импульсов LMI соответственно. В дальнейших исследованиях соединения согласно настоящему изобретению могут быть совместно введены с селективными ингибиторами обратного захвата серотонина, чтобы продемонстрировать усиление их действия на сон без быстрых движений глазных яблок (NREM-сон) и поддержание сна. Соединение согласно примеру 2 вводят совместно с циталопрамом в исследованиях сна на крысах, по существу, как описано выше для ведения соединения по отдельности, причем обнаружено, что указанное соединение существенно увеличивает время NREM-сна в значительно более низких дозах. Плазматический клиренс. Важным фактором для соединений, которые можно применять в лечении нарушений сна, таких как бессонница, является надлежащее выведение из организма с благоприятной скоростью клиренса, чтобы избежать нежелательных эффектов, таких как длительная сонливость, превышающая требуемый период сна, сонливость в дневное время, нарушение когнитивных способностей после пробуждения и т.д. В настоящем изобретении предложены соединения с улучшенными скоростями клиренса. Скорость клиренса исследуют, по существу, как описано ниже. Самцов крыс линии Sprague Dawley (масса тела в диапазоне 250-320 г) с постоянной канюлей в бедренной артерии получают из Charles River, Уилмингтон, Массачусетс 01887, США. Исследуемое соединение вводят внутривенно в виде раствора (1 мл/кг) в 20% каптизоле в 22,5 мМ фосфатном буфере,pH 2, с конечной концентрацией лекарственного средства 1,0 мг/мл (эквивалент свободного основания). Образцы крови собирают в течение 24 ч, используя постоянную канюлю. Образцы плазмы получают центрифугированием и хранят в замороженном виде (-20C) или на сухом льду до проведения исследования. Самцов собак породы английский бигль (масса тела в диапазоне 10-12 кг) получают из Marshall Bioresources, США. Исследуемое соединение вводят внутривенно в виде раствора (1 мл/кг) в 20% каптизоле в 22,5 мМ фосфатного буфера, pH 2, с конечной концентрацией лекарственного средства 1,0 мг/мл(эквивалент свободного основания). Образцы крови получают из шейной вены в течение 24 ч. Образцы плазмы получают центрифугированием и хранят в замороженном виде (-20C) до проведения исследования. Замороженные образцы плазмы оттаивают при комнатной температуре для биоанализа концентраций исследуемого соединения. Соответствующее соединение для внутреннего стандарта в смеси ацетонитрил/метанол (1:1, об./об.) добавляют ко всем образцам плазмы (1:1, об./об.). Образцы центрифугируют для удаления осажденного белка до проведения исследования. Супернатанты исследуют с помощью впрыскивания и быстрого градиентного элюирования на колонке Javelin Betasil C18 (202,1 мм картридж, подвижная фаза A:вода/1 М NH4HCO3, 2000:10 об./об., подвижная фаза В: MeOH/1 М NH4HCO3,2000:10 об./об.). Элюированные аналиты детектируют методом ЖХ-МС-МС, используя тройной квадрупольный масс-спектрометр Sciex API 4000c. Концентрации соединения определяют на основании концентраций стандартов, приготовленных и исследованных в одинаковых условиях. Клиренс рассчитывают с использованием некомпартментной модели с помощью программного обеспечения Watson 7.4,Thermo Fisher Scientific, Inc. Клиренс=Доза/Площадь под кривой концентрации в плазме-время. Соединение согласно примеру 2 исследовали, по существу, как описано выше, причем было обнаружено, что указанное соединение имеет благоприятный профиль клиренса. Хотя существует возможность вводить соединения непосредственно без использования какого-либо состава, в соответствии с применением в способах согласно данному изобретению, соединения обычно вводят в виде фармацевтических композиций, содержащих соединение или его фармацевтически приемлемую соль в качестве активного ингредиента, и по меньшей мере один фармацевтически приемлемый носитель, разбавитель и/или наполнитель. Такие композиции можно вводить различными способами, в том числе внутрь, подъязычно, назально, подкожно, внутривенно и внутримышечно. Указанные фармацевтические композиции и способы их получения хорошо известны в данной области (см., например,Remington: The Science and Practice of Pharmacy (University of the Sciences in Philadelphia, ed., 21st ed., Lippincott WilliamsWilkins Co., 2005. Композиции предпочтительно готовят в виде лекарственной формы с однократной дозировкой,причем каждая дозировка содержит от приблизительно 0,1 до приблизительно 60 мг, чаще от приблизительно 0,5 до приблизительно 30 мг, как, например, от приблизительно 1 до приблизительно 10 мг активного ингредиента. Термин "лекарственная форма с однократной дозировкой" относится к физически дискретным единицам, пригодным в качестве единичных доз для человеческих субъектов и других млекопитающих, причем каждая единица дозы содержит предварительно определенное количество активного материала, рассчитанное для получения желаемого терапевтического эффекта, в комбинации по меньшей мере с одним фармацевтически приемлемым носителем, разбавителем и/или наполнителем. Соединения согласно формуле I в целом эффективны в широком диапазоне доз. Например, дозы для введения раз в сутки обычно находятся в диапазоне от приблизительно 0,002 до приблизительно 1,0 мг/кг, чаще от приблизительно 0,008 до 0,5 мг/кг и, например, между 0,015 и 0,15 мг/кг массы тела. В некоторых случаях уровни доз, которые меньше нижнего предела вышеуказанного диапазона, могут быть более чем достаточными, тогда как в других случаях еще более высокие дозы могут быть использованы без какого-либо вредного нежелательного эффекта, и, следовательно, вышеуказанные диапазоны доз не предназначены для ограничения объема настоящего изобретение каким бы то ни было образом. Следует понимать, что количество фактически вводимого соединения будет определяться врачом, исходя из соответствующих обстоятельств, включая заболевание, которое лечат, выбранного способа введения, фактического соединения или введенных соединений, возраста, веса и реакции конкретного пациента, а также тяжести симптомов у пациента. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение согласно формуле или его фармацевтически приемлемая соль. 2. Соединение по п.1, которое представляет собой соль хлороводородной кислоты. 3. Соединение по п.1, которое представляет собой тозилатную соль. 4. Фармацевтическая композиция для лечения бессонницы, содержащая соединение по п.1 или его фармацевтически приемлемую соль в комбинации по меньшей мере с одним фармацевтически приемлемым носителем, разбавителем или наполнителем. 5. Применение соединения по п.1 или его фармацевтически приемлемой соли для лечения бессонницы. 6. Применение по п.5, где бессонница характеризуется трудностями в засыпании илиподдержании сна, или обоими, тем и другим. 7. Применение по п.5 или 6 у человека. 8. Применение соединения по п.1 или его фармацевтически приемлемой соли при приготовлении лекарственного средства для лечения бессонницы. 9. Применение по п.8, отличающееся тем, что бессонница характеризуется трудностями в засыпании или поддержании сна, или и тем, и другим у млекопитающего.
МПК / Метки
МПК: A61P 25/04, A61K 31/5513, C07D 498/04
Метки: 5-ht2а, активностью, рецепторов, тиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ила, двойной, обладающие, обратных, агонистов, соединения
Код ссылки
<a href="https://eas.patents.su/15-24248-soedineniya-tieno23-b15benzoksazepin-4-ilpiperazin-1-ila-obladayushhie-dvojjnojj-aktivnostyu-obratnyh-agonistov-receptorov-h1-antagonistov-receptorov-5-ht2a.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения (тиено[2,3-b][1,5]бензоксазепин-4-ил)пиперазин-1-ила, обладающие двойной активностью обратных агонистов рецепторов h1/антагонистов рецепторов 5-ht2a</a>
Предыдущий патент: Способ получения минеральных удобрений пролонгированного антиоксидантно-восстанавливающего действия
Следующий патент: Способ получения бутадиена и/или бутенов из н-бутана
Случайный патент: Трансфер-пирамида для получения лечебно-профилактических препаратов