Производные 2-оксоалкил-1-пиперазин-2-она, их получение и их применение в терапии
Номер патента: 19924
Опубликовано: 30.07.2014
Авторы: Боно Франсуаз, Барони Марко, Дельбари-Госсар Сандрин
Формула / Реферат
1. Соединение формулы (I)
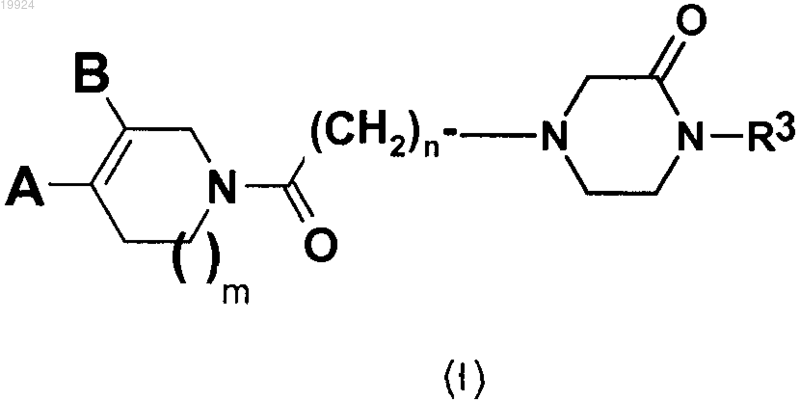
где m равно 0 или 1;
А означает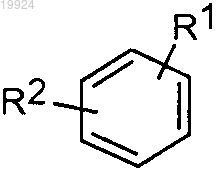 и В означает атом водорода илиА означает атом водорода и В означает
и В означает атом водорода илиА означает атом водорода и В означает ;
;R1 и R2, одинаковые или разные, независимо означают атом водорода или галогена, С1-4алкил, С1-4фторалкил, С1-2перфторалкил, С1-4алкокси или трифторметокси;
n равно 1 или 2;
R3 означает группу формулы
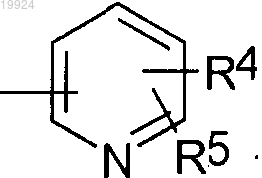
где R4 и R5, одинаковые или разные, находятся в любых свободных положениях и независимо означают атом водорода или галогена, С1-4алкил, С1-4фторалкил, С1-2перфторалкил,
в виде оснований или солей присоединения с кислотами.
2. Соединение по п.1, где
m означает 1;
А означает
и В означает атом водорода;
R1 и R2, одинаковые или разные, независимо означают атом водорода, галогена, С1-4алкил, С1-4фторалкил, С1-2перфторалкил, С1-4алкокси или трифторметокси;
n равно 1 или 2;
R3 означает группу формулы
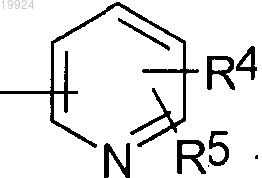
где R4 и R5, одинаковые или разные, находятся в любых свободных положениях и независимо означают атом водорода или галогена, С1-4алкил, С1-4фторалкил, С1-2перфторалкил,
в виде оснований или солей присоединения с кислотами.
3. Соединение по любому из пп.1, 2, где R1 отличен от Н, в виде оснований или солей присоединения с кислотами.
4. Соединение по любому из пп.1-3, где R1 находится в положении -2-, -3- или -4- и означает атом хлора, радикал CF3 и R2 означает водород или 3- или 4-Cl, в виде оснований или солей присоединения с кислотой.
5. Соединение по любому из пп.1-4, где R3 означает 2-пиридинил, замещенный R4 и R5, значения которых определены в п.1, в виде оснований или солей присоединения с кислотами.
6. Соединение по любому из пп.1-5, где n=1, в виде оснований или солей присоединения с кислотой.
7. Соединение по любому из пп.1-6, где R1 означает CF3; R2 означает 4-хлор; R3 означает остаток 2-пиридила, замещенного в положении 5 группой CF3, и n=1, в виде основания или солей присоединения с кислотами.
8. Соединение по любому из пп.1-7, выбранное из следующих соединений:
соединение № 1: 4-{2-[4-(4-хлор-3-трифторметилфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 2: 4-{2-[4-(4-хлор-3-трифторметилфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(5-метилпиридин-2-ил)пиперазин-2-он;
соединение № 3: 4-{2-[4-(4-хлорфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 4: 4-{2-оксо-2-[4-(3-трифторметилфенил)-3,6-дигидро-2Н-пиридин-1-ил]этил}-1-пиридин-2-илпиперазин-2-он;
соединение № 5: 4-{2-[4-(4-хлор-3-фторметилфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-пиридин-2-илпиперазин-2-он;
соединение № 6: 4-{2-[4-(4-хлорфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-пиридин-2-илпиперазин-2-он;
соединение № 7: 4-{2-[4-(2,3-дихлорфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 8: 4-{2-[4-(4-хлорфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(6-хлорпиридин-2-ил)пиперазин-2-он;
соединение № 9: 4-{2-[4-(3-хлорфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 10: 4-{2-[4-(4-трифторметилфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 11: 4-{2-[4-(3-трифторметилфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 12: 4-{2-[4-(4-хлор-3-трифторметилфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-пиридин-3-илпиперазин-2-он;
соединение № 13: 1-(6-хлорпиридин-3-ил)-4-{2-[4-(4-хлор-3-трифторметилфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}пиперазин-2-он;
соединение № 14: 4-{2-оксо-2-[5-(3-трифторметилфенил)-3,6-дигидро-2Н-пиридин-1-ил]этил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 15: 4-{2-оксо-2-[4-(3-трифторметилфенил)-3,6-дигидро-2Н-пиридин-1-ил]этил}-1-пиридин-2-илпиперазин-2-он;
соединение № 16: 4-{2-[4-(4-хлор-3-трифторметилфенил)-2,5-дигидропиррол-1-ил]-2-оксоэтил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 17: 4-{2-[4-(3,5-бис-трифторметилфенил-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 18: 4-{2-[4-(3-метилфенил)-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 19: 4-{2-[4-фенил-3,6-дигидро-2Н-пиридин-1-ил]-2-оксоэтил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 20: 4-{2-оксо-2-[5-(2,3-дихлорфенил)-3,6-дигидро-2Н-пиридин-1-ил]этил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он;
соединение № 21: 4-{2-оксо-2-[5-(3-метоксифенил)-3,6-дигидро-2Н-пиридин-1-ил]этил}-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он,
в виде оснований или солей присоединения с кислотами.
9. Способ получения соединения формулы (I) по любому из пп.1-8, где А, В, m, n, R3 имеют значения, определенные выше, включающий стадию реакции соединения формулы (IV)
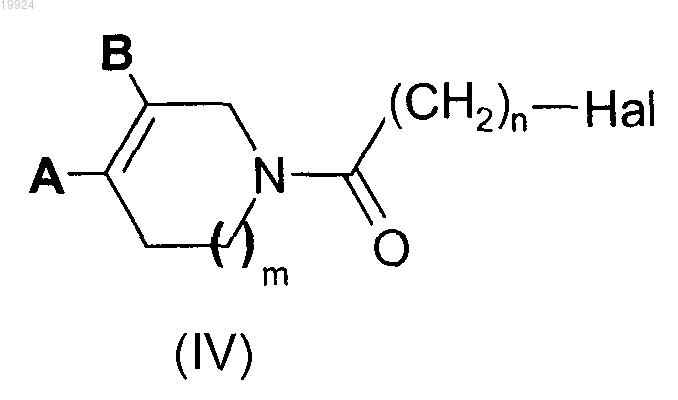
где А, В, m и n имеют значения, которые определены в общей формуле (I); и
Hal означает атом галогена,
с соединением общей формулы (V)
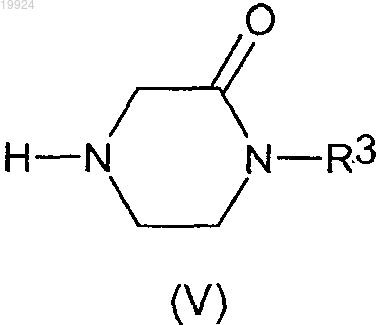
где R3 имеет значение, которое определено в общей формуле (I),
в присутствии основания.
10. Соединение формулы (IV)

где А, В, m и n имеют значения, которые определены в любом из пп.1-8; и
Hal означает атом галогена,
за исключением 2-хлор-1-[4-(2-метоксифенил)-3,6-дигидро-2Н-пиридин-1-ил]этанона и 2-хлор-1-[4-(4-бромфенил)-3,6-дигидро-2Н-пиридин-1-ил]этанона, в виде основания или солей присоединения с кислотой.
11. Лекарственное средство, отличающееся тем, что оно включает соединение формулы (I) по любому из пп.1-8 или соль присоединения этого соединения с фармацевтически приемлемой кислотой, предназначенное для профилактики или лечения p75NTR-зависимых заболеваний.
12. Фармацевтическая композиция, отличающаяся тем, что она содержит соединение формулы (I) по любому из пп.1-8 или фармацевтически приемлемую соль, а также по меньшей мере один фармацевтически приемлемый эксципиент для получения лекарственного средства, предназначенного для профилактики или лечения p75NTR-зависимых заболеваний.
13. Соединение общей формулы (I)

по любому из пп.1-8 для получения лекарственного средства, предназначенного для профилактики или лечения p75NTR-зависимых заболеваний.
14. Соединение общей формулы (I)

в которой А, В, R3, m и n имеют значения, определенные в пп.1-8,
обладающее способностью ингибировать димеризацию рецептора р75NTR независимо от его лиганда.
Текст
Объектом изобретения являются производные 4-2-[фенил-3,6-дигидропиридин-1 ил]-2-оксоалкил-1-пиперазин-2-она и 4-2-[фенил-2,5-дигидропиррол-1-ил]-2-оксоалкил-1 пиперазин-2-она общей формулы (I), где А, В, m, R3 и n имеют те же значения, что в п.1, их получение и их применение в терапии. Объектом настоящего изобретения являются производные 4-2-[фенил-3,6-дигидропиридин-1-ил]2-оксоалкил-1-пиперазин-2-она и 4-2-[фенил-2,5-дигидропиррол-1-ил]-2-оксоалкил-1-пиперазин-2 она, их получение и их применение в терапии. Соединения согласно настоящему изобретению обладают аффинностью к рецептору p75NTR нейротрофинов. Нейротрофины принадлежат к семейству белков, биологическим эффектом которых является, в частности, выживание и дифференцировка клеток. Рецептор p75NTR, рецептор всех нейротрофинов, является трансмембранным гликопротеином из рецепторного семейства фактора некроза опухолей (TNF, англ. Tulmor Necrosis Factor) (W.J. Friedman, L.A.Greene, Exp. Cell. Res., 1999, 253, 131-142). Рецептор p75NTR экспрессируется в различных типах клеток, и ему приписывают ряд биологических функций: с одной стороны, модуляция аффинности нейротрофинов к рецепторам тирозинкиназы (trk); с другой стороны, в отсутствие trk индукция сигнала гибели клеток апоптозом. Вместе с тем предшественники нейротрофинов, пронейротрофины, способны фиксироваться на p75NTR с высокой аффинностью и рассматриваются как мощные индукторы апоптоза, зависящие отp75NTR в нейронах и некоторых клеточных линиях. В многочисленных работах показано, что на уровне центральной нервной системы апоптоз проявляется в различных патологиях, таких как боковой амиотрофический склероз, рассеянный склероз, болезни Альцгеймера, Паркинсона и Гентингтона и прионные заболевания. Известно также, что p75NTR суперэкспрессируется при различных типах нейродегенеративных заболеваний, таких как болезнь Альцгеймера и боковой амиотрофический склероз (ALS) (Longo F.M. et al., Curr. Alzheimer Res. 2007; 4: 503506; Lowry K.S. et al., Amyotroph. Lateral. Scler. Other. Motor. Neuron. Disord. 2001; 2: 127-34). Результаты указывают на то, что p75NTR могут играть преобладающую роль в механизмах, приводящих к гибели нейронов в результате постишемического апоптоза (P.P. Roux et al., J. Neurosci., 1999, 19,6887-6896). Результаты (V. Della-Bianca et al., J. Biol. Chem., 2001, 276: 38929-33, S. Rabizadeh et al., Proc. Nat.Acad. Sci. USA, 1994, 91, 10703-10706) подтверждают гипотезу, согласно которой p75NTR может играть важную роль в гибели нейронов, вызванной инфекционным прионным белком (трансмиссивная губчатая энцефалопатия) или бета-амилоидным белком (болезнь Альцгеймера). Рецептор p75NTR связан также с рецептором Nogo и участвует в трансферации сигналов ингибиторных эффектов этих белков миелина при осевом росте. Поэтому рецептор p75NTR играет главную роль в регуляции пластичности нейронов и во взаимодействиях нейроны-глия и, таким образом, является лучшей терапевтической мишенью для содействия восстановлению нервных клеток. Было сделано предположение, что, помимо нервной системы и нейродегенеративных заболеваний,p75NTR может играть роль в сердечно-сосудистых заболеваниях, таких как атеросклероз и ишемия миокарда (M.L. Bochaton-Pialat et al., Am. J. Pathol., 1995, 146, 1-6; H. Perlman, Circulation, 1997, 95, 981-987). В недавних работах отмечалось увеличение экспрессии p75NTR и нейротрофинов и массивный апоптоз в заболеваниях атеросклерозом. В ряде работ указано, что p75NTR является медиатором воспаления (Rihl M. et al., Ann. Rheum Dis. 2005; 64(11): 1542-9; Raychaudhuri S.P. et al., Prog. Brain. Res. 2004; 146: 433-7, Tokuoka S. et al., Br. J.p75NTR играет также решающую роль в биологии опухоли. Известно, что многочисленные соединения взаимодействуют с системой trkA/NGF/p75NTR или имеют активность типа NGF (фактор роста нервов, англ. nerve growth factor). Так, в заявке на патентWO 00/59893 описаны производные замещенных пиримидинов, обладающих активностью типа NGF и/или увеличивающих активность NGF на клетках РС 12. В заявке на патент WO 03/104225 описаны соединения, обладающие аффинностью к рецепторамp75NTR. Эти соединения сильно метаболизируются и обладают высокой степенью ингибирования генаhERG (the human Ethergo-go Related Gene). Ген hERG кодирует белок Kv11.1. ионного K+-канала. Этот белок известен своим вкладом в электрическую активность сердца. Когда мощность канала, проводящего электрический ток через клеточную мембрану, ингибируется действием лекарственных средств, это может привести к потенциально смертельному заболеванию, именуемому QT синдромом. Некоторые лекарственные средства ингибируют этот белок, создавая риск внезапной смерти как нежелательный побочный эффект. Это привело к тому,что ингибирование hERG стало центральной проблемой как в регулировании лекарственных средств, так и в их разработке (Sanguinetti M.C., Tristani-Firouzi M. (March 2006). "hERG potassium channels and cardiacarrhythmia". Nature. 440, 7083: 463-9). Объектом настоящего изобретения являются новые соединения, обладающие аффинностью к рецепторам p75NTR и не приводящие к нежелательным последствиям из-за сильного метаболизма и сильного ингибирования hERG, как соединения предшествующего уровня техники. Таким образом, изобретение имеет преимущество при разработке новых лекарственных средств. Объектом настоящего изобретения являются соединения, отвечающие формуле (I) и B означает атом водорода илиA означает атом водорода и B означаетR1 и R2, одинаковые или разные, независимо означают атом водорода или галогена, С 1-4 алкил,С 1-4 фторалкил, С 1-2 перфторалкил, С 1-4 алкокси или трифторметокси; где R4 и R5, одинаковые или разные, находятся в любых свободных положениях и независимо означают атом водорода или галогена, С 1-4 алкил, С 1-4 фторалкил, С 1-2 перфторалкил. Соединения формулы (I) могут содержать один или несколько асимметрических атомов углерода. Так, они могут существовать в форме энантиомеров или диастереоизомеров. Эти энантиомеры, диастереоизомеры, а также их смеси, в том числе рацемические смеси, составляют часть настоящего изобретения. Соединения формулы (I) могут существовать в виде оснований или солей присоединения с кислотами. Такие соли присоединения составляют часть настоящего изобретения. Эти соли могут быть получены из фармацевтически приемлемых кислот, но соли других кислот,используемых, например, для очистки или выделения соединений формулы (I), также составляют часть настоящего изобретения. В рамках настоящего изобретения подразумевают под атомом галогена: фтор, хлор, бром или йод; под алкилом: насыщенную алифатическую группу, линейную или разветвленную. В качестве примеров можно назвать С 1-4 алкил, который может представлять собой метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил; под фторалкилом: алкил, в котором один или несколько атомов водорода замещены атомом фтора; под перфторалкилом: алкил, в котором все атомы водорода замещены атомом фтора; под алкокси: радикал -О-алкил, где алкил имеет значение, определенное выше. Среди соединений формулы (I), являющихся объектами настоящего изобретения, другая группа состоит из соединений формулы (I), гдеR1 и R2, одинаковые или разные, независимо означают атом водорода, галогена, С 1-4 алкил,С 1-4 фторалкил, С 1-2 перфторалкил, С 1-4 алкокси или трифторметокси; где R4 и R5, одинаковые или разные, находятся в любых свободных положениях и независимо означают атом водорода или галогена, С 1-4 алкил, С 1-4 фторалкил, С 1-2 перфторалкил,в виде основания или солей присоединения с кислотами. Среди соединений формулы (I), являющихся объектами настоящего изобретения, другая группа состоит из соединений, где R1 отличен от Н, в виде оснований или солей присоединения с кислотами. Среди соединений формулы (I), являющихся объектами настоящего изобретения, другая группа состоит из соединений, где R1 находится в положении -2-, -3- или -4- и означает атом хлора, радикал CF3, иR2 означает водород или 3- или 4-Cl, в виде оснований или солей присоединения с кислотами. Среди соединений формулы (I), являющихся объектами настоящего изобретения, другая группа состоит из соединений, где R3 означает 2-пиридинил, замещенный R4 и R5, в виде оснований или солей присоединения с кислотами. Среди соединений формулы (I), являющихся объектами настоящего изобретения, другая группа состоит из соединений, где n=1, в виде оснований или солей присоединения с кислотами. Среди соединений формулы (I), являющихся объектами настоящего изобретения, другая группа состоит из соединений, где R1 означает CF3; R2 означает 4-хлор; R3 означает остаток 2-пиридила, замещенного в положении 5 группой CF3; и n=1, в виде основания или солей присоединения с кислотами. Среди соединений формулы (I), являющихся объектами настоящего изобретения, можно назвать следующие соединения: соединение 19: 4-2-[4-фенил-3,6-дигидро-2 Н-пиридин-1-ил]-2-оксоэтил-1-(5 трифторметилпиридин-2-ил)пиперазин-2-он; соединение 20: 4-2-оксо-2-[5-(2,3-дихлорфенил)-3,6-дигидро-2 Н-пиридин-1-ил]этил-1-(5 трифторметилпиридин-2-ил)пиперазин-2-он; соединение 21: 4-2-оксо-2-[5-(3-метоксифенил)-3,6-дигидро-2 Н-пиридин-1-ил]этил-1-(5 трифторметилпиридин-2-ил)пиперазин-2-он,в виде основания или соли присоединения с кислотой. Далее под "защитной группой Pg" подразумевают группу, которая позволяет, с одной стороны, во время синтеза защитить такую реакционноспособную группу, как гидрокси или амин, и, с другой стороны, восстановить полностью реакционноспособную группу в конце синтеза. Примеры защитных групп,так же как способы защиты и удаления защиты, приведены в "Protective Groups in Organic Synthesis",Green et al., 2nd Edition (John WileySons., Inc., New York). В соответствии с настоящим изобретением можно получить соединения общей формулы (I) согласно следующему способу. Соединения формулы (I), где А, В, m, n, R3 имеют значения, определенные выше, могут быть получены реакцией соединения формулы (IV), определенной выше, с соединением формулы (V), определенной выше, согласно способам, известным специалисту в данной области, описанным в WO 03/104225. Более конкретно, способ получения соединений общей формулы (I) включает реакцию соединения формулы (IV) где А, В, m и n имеют те же значения, что и в общей формуле (I); иHal означает атом галогена, например хлор,с соединением общей формулы (V): где R3 имеет значение, как в общей формуле (I),в присутствии основания, в растворителе, описанном в WO 03/104225. Так, в качестве примера основания можно назвать такие органические основания, как триэтиламин,N,N-диизопропиламин, диизопропилэтиламин (DPEA) или N-метилморфолин, или карбонаты или бикарбонаты щелочного металла, такие как карбонат калия, карбонат натрия или бикарбонат натрия, в отсутствие или в присутствии йодида щелочного металла, такого как йодид калия или йодид натрия. Реакцию проводят предпочтительно в таком растворителе, как ацетонирил, N,N-диметилформамид (DMF),N-метилпирродинон (NMP), толуол или пропан-2-ол, при температуре в пределах от комнатной до температуры кипения растворителя. Под комнатной температурой подразумевают температуру в пределах от 5 до 25 С. К примеру, реакцию можно проводить в присутствии бикарбоната натрия, йодида натрия в таком растворителе, как DMF. Реакцию проводят предпочтительно в микроволновом реакторе. В соединениях общей формулы (I), полученных таким образом, R, R1, R2, R4, R5, R6 и R7 могут меняться в результате реакций, обычно используемых специалистом, как, например, гидролиз сложноэфирной группы для получения карбоксильной группы. Соли присоединения с кислотой соединений общей формулы (I) могут быть получены путем добавления кислоты, подходящей для соединения формулы (I), в виде свободного основания. Соединения формулы (IV), где R1 и R2 имеют значения, определенные для соединений формулы (I),могут быть получены реакцией соединения формулы (II) с соединением формулы (III) согласно способам, известным специалисту в данной области, например, в присутствии основания, в растворителе, описанном в WO 03/104225. Более конкретно, соединения формулы (IV) могут быть получены реакцией соответствующего соединения формулы (II) где А, В, m имеют такие же значения, что в общей формуле (I),в случае необходимости, в виде соли присоединения с кислотой, и соединения формулы (III) где n и Hal имеют такие же значения, что в формуле (IV); иHal' означает атом галогена, идентичный или отличный, предпочтительно Hal' означает атом хлора. Эту реакцию проводят, как правило, в присутствии основания, такого как триэтиламин,N,N-диизопропилэтиламин или N-метилморфолин, в таком растворителе, как дихлорметан, хлороформ,тетрагидрофуран, диоксан или смесь этих растворителей, при температуре в интервале от 0C до комнатной температуры. Соединения формулы (II) и (III), как правило, коммерчески доступны или могут быть получены согласно способам, известным специалисту в данной области. Соединения формулы (V), где R3 имеет такое же значение, что в формуле (I), могут быть получены согласно способам, известным специалисту в данной области. Они могут быть получены, например, согласно следующему способу. Схема 2 Более конкретно, соединение формулы (V) может быть получено из соответствующего соединения формулы (XI), где R3 имеет такое же значение, что в формуле (I), и Pg означает защитную группу атома азота, такую как бензил. Эту реакцию можно проводить путем применения или адаптации любого способа, известного специалисту в данной области; как правило, эту реакцию проводят в кислой среде в присутствии катализатора, такого как Pd/C. Соединение формулы (XI) может быть получено из соединения формулы (VIII), где R3 имеет такое же значение, что и в формуле (I), и Pg означает защитную группу, в присутствии соединения формулы(VI). Как правило, эту реакцию проводят при температуре в пределах от комнатной до температуры кипения реакционной смеси, которая может содержать воду. По альтернативному варианту соединения формулы (XI) могут быть получены из соединения формулы (IX) взаимодействием с гидридами щелочных металлов в инертных растворителях, таких как толуол, диметилформамид или диметилсульфоксид при температуре в пределах между комнатной температурой и температурой кипения реакционной смеси. Соединение формулы (IX) может быть получено из соединения формулы (VIII) взаимодействием с бром- или хлорэтилацетатом в таких растворителях, как бутанол или ацетон, в присутствии такого основания, как карбонат калия, при температуре в пределах от комнатной температуры до температуры кипения реакционной смеси. Соединение формулы (VIII) может быть получено из соединения формулы (VII), где R3 имеет такое же значение, что и в формуле (I), и X означает атом галогена, такого как хлор, в присутствии соединения(X), где Pg означает защитную группу, значение которой определено в формуле (VIII). Как правило, эту реакцию проводят при температуре в пределах от комнатной до температуры кипения реакционной смеси. В некоторых случаях способ по изобретению включает последующую стадию, которая состоит в выделении полученного желаемого продукта. Согласно другому из аспектов изобретения объектом его являются соединения формулы (IV)Hal означает атом галогена, например хлора,в виде оснований или солей присоединения с кислотами. Эти соединения подходят в качестве промежуточных соединений синтеза соединений формулы (I). Исходные соединения и реактивы из табл. 1 и 2, в случае когда способ их получения не описан, являются коммерчески доступными или описаны в литературе или могут быть получены согласно описанным способам или способам, известным специалисту в данной области. Следующие примеры описывают получение некоторых соединений по изобретению. Эти примеры не носят ограничительный характер и приведены лишь для иллюстрации настоящего изобретения. Номера соединений в примерах соответствуют номерам, приведенным в нижеследующей таблице, которая иллюстрирует химические структуры и физические свойства некоторых соединений по изобретению. Анализ HPLC провели с помощью системы ThermoElectron LCQ Deca XP Мах, снабженной детектором для масс-спектрометрии на ионных ловушках, а также детектором с диодным стержнем. Условия анализа путем жидкостной хроматографии, связанной с масс-спектрометрией (LC/UV/MS),следующие: хроматографическая система A: элюант A = H2O + 0,01% TFA,элюант B = CH3CN,градиент от 98% A до 95% B за 10 мин, затем элюирование 95% B в течение 5 мин,расход 0,5 мл/мин; температура 40C,впрыскивание 2 мкл раствора 0,1 мг/мл в смеси с CH3CN:H2O=9:1; хроматографическая система B: элюант A = H2O + 0,05% TFA,элюант B = CH3CN + 0,035% TFA,градиент от 98% A до 95% B за 12 мин, затем элюирование 95% B в течение 3 мин,расход 0,7 мл/мин, температура 40C,впрыскивание 2 мкл раствора 0,1 мг/мл в смеси с CH3CN:H2O=9:1; хроматографическая система C: элюант A = буфер ацетат аммония 5 мМ рН 6,5,элюант B = CH3CN,градиент от 98% A до 95% B за 10 мин, затем элюирование 95% B в течение 5 мин,расход 0,7 мл/мин, температура 40C,впрыскивание 2 мкл раствора 0,1 мг/мл в смеси с CH3CN:H2O=9:1. Продукты обнаружены в УФ при 220 нм. Используемые колонки С 18 с гранулометрией от 2 до 4 мкм, предпочтительно 3,5 мкм. Масс-спектрометрическая часть: тип ионизации: положительное электрораспыление (API-ES полярность+); сканирование от 120 до 1500 а.е.м. Спектры ядерного магнитного резонанса протона (ЯМР 1 Н) были зарегистрированы в следующих условиях:a) 500 МГц на аппарате Bruker, снабженном консолью Avance III;b) 400 МГц на аппарате Bruker, снабженном консолью Avance I. Химические сдвиги даны в ppm относительно частоты TMS. Все спектры зарегистрированы при температуре 40 С. Сокращения, используемые для характеристики сигналов, следующие:RMN,2Xm = 2 частично наложенных друг на друга мультиплета. Получение продукта 1. Хлоргидрат 1-(5-трифторметилпиридин-2-ил)пиперазин-2-он. В колбе нагревают при 135 С в течение 6 ч 10 г 2-хлор-5-(трифторметил)пиридина (соединение формулы (VII и 40,5 мл N-бензилэтилендиамина (соединение формулы (X. Выливают в воду и экстрагируют этилацетатом. Сушат и упаривают в вакууме; полученный таким образом сырой продукт очищают быстрой хроматографией. Выделенный продукт (соединение формулы (VIII, 14 г, солюбилизируют в 200 мл раствора 2 н. HCl. Добавляют 30 г трехмерного глиоксальдигидрата (соединение VI) и оставляют перемешиваться при комнатной температуре в течение 72 ч. Экстрагируют этилацетатом. Сушат и упаривают в вакууме; полученный таким образом сырой продукт очищают быстрой хроматографией. Выделенный продукт (соединение формулы (XI, 10 г, солюбилизируют в 450 мл этанола, затем добавляют 15 мл раствора изопропанола, насыщенного HCl, и 3 г Pd/C до 10%. Оставляют реагировать в потоке водорода на 4 ч при температуре 40 С. Фильтруют и упаривают в вакууме и получают 3 г основного соединения (соединение формулы (V. Т.пл. 205-207C. Получение продукта 2. Хлоргидрат 1-(5-метилпиридин-2-ил)пиперазин-2-он. В колбе нагревают при 135C в течение 5 ч 4,7 г 2-хлор-5-метилпиридина (соединение формулы(VII и 27,5 мл N-бензилэтилендиамина (соединение формулы (X. Выливают в воду и экстрагируют этилацетатом. Сушат и упаривают в вакууме; полученный таким образом сырой продукт очищают быстрой хроматографией. Выделяют 3,6 г продукта (соединение формулы (VIII). 1,5 г этого продукта солюбилизируют в 3 мл этанола. Добавляют 0,85 г карбоната натрия и 1,05 г этилбромацетата и нагревают с обратным холодильником в течение 3 ч. Выливают в воду и экстрагируют этилацетатом. Сушат и упаривают в вакууме; полученный таким образом сырой продукт (2 г) очищают быстрой хроматографией. Выделенный продукт (соединение формулы (IX, 1 г, затем солюбилизируют в толуоле, затем этот раствор медленно добавляют в токе азота к суспензии 0,25 г гидрида натрия 60% (NaH) в 25 мл толуола. Нагревают с обратным холодильником в течение 2 ч. Выливают в воду и экстрагируют этилацетатом. Сушат и упаривают в вакууме. Получают 0,6 г сырого соединения в виде масла (соединение формулы (IX которое солюбилизируют в 25 мл этанола, затем добавляют 1,5 мл раствора изопропанола, насыщенного HCl и 0,3 г Pd/C 10%. Оставляют в токе водорода на 4 ч при температуре 40C. Фильтруют и упаривают в вакууме и получают 0,3 г основного соединения (соединение формулы (V. Получение продукта 3. 2-Хлор-1-[4-[3-трифторметил-4-хлорфенил]-1-[3,6-дигидро-1(2 Н)пиридинил-1-этанон. Охлаждают до 0 С хлоргидрат 4-[3-(трифторметил)-4-хлорфенил]-3,6-дигидро-1(2 Н)пиридина (соединение формулы (II (3,94 г) и 3,8 мл триэтиламина в 33,5 мл дихлорметана. Медленно добавляют 2 хлорацетилхлорид (соединение формулы (III и оставляют на 1 ч 30 мин при перемешивании. Добавляют воду и экстрагируют дихлорметаном. Органическую фазу сушат над Na2SO4, фильтруют и упаривают в вакууме. Получают 4,2 г соединения в виде аморфного твердого вещества (соединение формулы (IV. Пример 1. Соединение 1: 4-2-[4-(4-хлор-3-трифторметилфенил)-3,6-дигидро-2 Н-пиридин-1-ил]-2 оксоэтил-1-(5-трифторметилпиридин-2-ил)пиперазин-2-он и его хлоргидрат. В микроволновом реакторе нагревают при 180C в течение 30 мин смесь продукта 3 (0,49 мг), продукта 1 (0,4 мг), карбоната калия (0, 41 г), йодида натрия (0,45 г) в 7 мл диметилформамида. Реакционную смесь выливают в воду и экстрагируют этилацетатом. Органическую фазу сушат над Na2SO4, фильтруют и упаривают, получая 700 мг сырого продукта в виде масла. Очищают хроматографией на колонке с силикагелью, элюируя смесью циклогексан/этилацетат = 1/1. Хлоргидрат получают добавлением раствора соляной кислоты в изопропаноле. Получают 200 мг основного продукта. 2: 4-2-[4-(4-хлор-3-трифторметилфенил)-3,6-дигидро-2 Н-пиридин-1-ил]-2 оксоэтил-1-(5-метилпиридин-2-ил)пиперазин-2-он и его хлоргидрат. Поступая так же, как в примере 1, но используя продукт 2 вместо продукта 1, получают основное соединение.(Аппарат а).(м.д., ДМСО-d6): 2,32 (с, 3 Н), 2,56 (м, 1 Н), 2,65 (м, 1 Н), 3,10-3,60 (м), 3,64 (м, 1 Н),3,77 (м, 1 Н), 3,98 (м, 2 Н), 4,05-4,51 (м, 6 Н), 6,41 (м, 1 Н), 7,69 (дд, J=8,4 Гц и 2,0 Гц, 1 Н), 7,73 (д, J=8,5 Гц,1 Н), 7,75-7,81 (м, 2 Н), 7,83 (ушир.д, J=9,3 Гц, 1 Н), 8,31 (ушир.д, J=2 Гц, 1 Н). Следующая таблица иллюстрирует химические структуры и физические свойства некоторых примеров соединений по изобретению. В этой таблице в колонке "Соль": "-" означает соединение в виде свободного основания, а "HCl" означает соединение в форме хлоргидрата. Соединения по изобретению явились объектом биохимических исследований. Клеточная культура. Штамм SH-SY-5Y (человеческая нейробластома) обычным образом культивировали в культуральной среде DMEM (англ. Dulbecco's Modified Eagle's Medium) (Gibco BRL, France), содержащей SVF (5%)(4 мМ) в культуральных сосудах, покрытых коллагеном (Becton Dickinson, France). Материнский штамм SK-N-BE (человеческая нейробластома) и клон Вер 75, стабильно экспрессирующий полную форму рецептора p75NTR человека (SK-N-BE Вер 75), культивировали обычным образом в культуральной среде RPMI, содержащей SVF (5%), пируват натрия (1 мМ) и глутамин (4 мМ). В клеткиSK-N-BE Вер 75 добавили гигромицин (200 мкл/20 мл среды) в качестве агента селекции. Изучение связывания 125I NGF с рецептором p75NTR. Изучение связывания NGF (фактор роста нервов, меченный радиоактивным изотопом йод-125, Amersham-2000 Ci/ммоль) проводили на клеточной суспензии штамма SK-N-BE Вер 75 в соответствии со способом, описанным Weskamp (Neuron, 1991, 6, 649-663). Было определено неспецифическое связывание путем определения общего связывания через 1 ч предварительного инкубирования клеток при 37 С в присутствии NGF, не меченного радиоактивным изотопом (1 мкМ). Специфическое связывание определяли по разнице между измерением общего связывания и неспецифического связывания. Сравнительные эксперименты проводили, используя концентрацию NGF-йодированного (125I NGF), равную 0,3 нМ. Ингибирующие концентрации в 50% (CI50) фиксации 125I NGF на рецепторе p75NTR соединений по изобретению являются низкими и варьируют в пределах от 10-6 до 10-11 М. В этом исследовании соединения формулы (I) проявили активность, выраженную в концентрацияхCI50, которые варьируют от 10-6 до 10-11 М. Например, соединения 3 и 1 показали концентрацию CI50, равную соответственно 0,1 и 5,2 нМ. Изучение димеризации рецептора p75NTR независимо от его лиганда. Изучение димеризации рецептора p75NTR провели на клеточной суспензии штамма SK-N-BE Bet 75. Клетки (2,5104 клеток/лунки) поместили в лунки (96-луночные планшеты) на 24 ч, затем предварительно инкубировали в течение 1 ч при 37 С в присутствии или в отсутствие соединений по изобретению. Затем добавили супернатант, полученный из культуры человеческих клеток почечного происхождения HEK 293, выделив через 48 ч трансфекции и отделив растворимую форму рецептора p75NTR (внеклеточная часть рецептора), связанную с щелочной фосфатазой, при конечной концентрации 10 нМ. Количественное определение специфического связывания растворимого рецептора p75NTR с рецептором, находящимся на клетках SK-N-BE Вер 75, установили путем измерения энзиматической активности щелочной фосфатазы после инкубирования клеток в течение 1 ч при 37 С в присутствии супернатанта. После фильтрации и переноса фильтров в 24-луночные планшеты определили активность щелочной фосфатазы путем добавления хемолюминесцента CDP-Star (ready-to-use, Roche). Ингибирующие концентрации в 50%(CI50) димеризации рецептора p75NTR соединений по изобретению являются низкими и варьируют в пределах от 10-6 до 10-11 М. Например, соединения примеров 1, 2 и 3 показали концентрации CI50, равные соответственно 1,34, 3,88, 0,11 нМ. Измерение апоптоза. Клетки (штаммы человеческих нейробластом SH-SY-5Y и SK-N-BE Вер 75) поместили в чашки Петри диаметром 35 мм (Biocoat collagen (105 клеток/лунки в подходящую культуральную среду, содержащую 5% SVF, на 24 ч. Культуральную среду далее удалили, клетки промыли PBS (англ. Dulbecco'sPhosphate buffered saline), затем добавили либо свежую среду, содержащую 5% SVF, либо среду, содержащую NGF (в концентрации 10 нг/мл), либо бета-амилоид пептид (А 1-40) (в концентрации 10 мкМ), в присутствии или в отсутствие соединений по изобретению. Степень апоптоза определили через 48 ч после обработок в случае штамма SH-SY-5Y и через 24 ч в случае штамма SK-N-BE Вер 75 путем количественного определения цитоплазматических гистонов, связанных с фрагментами ADN (cell death detection ELISA, Boehringer Mannheim, Allemagne). Степени апоптоза выражены в количестве олигонуклеосомы/105 клеток. Каждое значение соответствует среднему значению из 9 экспериментальных точек, распределенных по 3 независимым экспериментам. Соединения формулы (I) проявляют ингибирующую активность апоптоза, индуцированного NGF,выраженную в концентрации CI50, которая варьирует от 10-6 до 10-11 М. Например, соединение примера 1 показало концентрацию CI50, равную 1,61 нМ, а соединение примера 5 показало концентрацию CI50,равную 5,2 нМ. Таким образом, фиксация соединений по изобретению на рецепторе p75NTR выражается, с одной стороны, на биохимическом уровне в ингибировании димеризации рецептора, вызванной нейротрофинами, или независимо от лиганда, и, с другой стороны, на клеточном уровне в ингибировании проапоптотического эффекта, вызванного рецептором p75NTR. Так, согласно одному из объектов настоящего изобретения соединения формулы (I) проявляют очень интересную активность ингибирования димеризации рецептора p75NTR независимо от его лиганда. Таким образом, соединения по настоящему изобретению можно использовать для получения лекарственных средств, в особенности лекарств, предназначенных для профилактики или лечения любой патологии, где участвует рецептор р 75 Так, согласно одному из своих аспектов изобретения объектом его являются лекарственные средства, которые содержат соединение формулы (I) или соль присоединения последнего с фармацевтически приемлемой кислотой. Согласно другому аспекту объектом изобретения является соединение формулы (I) или соль присоединения последнего с фармацевтически приемлемой кислотой для профилактики или лечения нижеуказанных патологий. Таким образом, соединения по изобретению можно использовать в случае человека или животного для лечения или профилактики различных р 75NTR-зависимых заболеваний, таких как центральные и периферические нейродегенеративные заболевания, такие как старческое слабоумие, эпилепсия, болезнь Альцгеймера, болезнь Паркинсона, хорея Гентингтона, синдром Дауна, прионные заболевания, амнезия,шизофрения, депрессия, биполярное расстройство; боковой амиотрофический склероз, рассеянный склероз; сердечно-сосудистые заболевания, такие как постишемические повреждения сердца, кардиомиопатии, инфаркт миокарда, сердечная недостаточность, сердечная ишемия, церебральный инфаркт; периферические невропатии (диабетического происхождения, травматизм или ятрогенное заболевание); повреждения оптического нерва и сетчатки (пигментная дегенерация сетчатки, глаукома); ишемия сетчатки; макулярная дегенерация; травма спинного мозга и черепно-мозговые травмы; атеросклероз; стенозы; повреждения в результате рубцевания; алопеция. Соединения по изобретению можно также использовать в лечении рака, такого как рак легких, щитовидной железы, поджелудочной железы, предстательной железы, тонкой и толстой кишки, молочной железы, в лечении опухолей, метастазов и лейкемий. Соединения по изобретению можно также использовать в лечении респираторных нарушений, таких как воспаление легких, аллергия и астма, хроническая закупоривающая бронхопневмопатия. Соединения по изобретению можно также использовать в лечении заболеваний кожи (кожи, подкожных тканей и прилежащих органов), соматических, висцеральных заболеваний (на уровне сердечнососудистой, респираторной, желудочно-кишечной или мочеполовой системы) и неврологических заболеваний. Соединения по изобретению можно использовать в лечении хронических невропатических заболеваний и заболеваний воспалительного характера и для лечения аутоиммунных заболеваний, таких как ревматоидный полиартрит. Соединения по изобретению также можно использовать для лечения таких заболеваний, как анкилозный спондилоартрит, псориатический ревматизм, бляшковидный псориаз. Соединения по изобретению также можно использовать в лечении переломов костей, для лечения или профилактики таких заболеваний костей, как остеопороз. Таким образом, объектом настоящего изобретения является соединение формулы (I) по изобретению для профилактики или лечения любой патологии, где участвует рецептор p75NTR, или, более конкретно, вышеуказанных патологий. Согласно другому из своих аспектов настоящее изобретение включает фармацевтические композиции, включающие в качестве действующего начала соединение по изобретению. Эти фармацевтические композиции содержат одну эффективную дозу по меньшей мере одного соединения по изобретению или одну фармацевтически приемлемую соль указанного соединения, а также по меньшей мере один фармацевтически приемлемый эксципиент. Указанные эксципиенты выбирают согласно фармацевтической форме и желаемому способу введения из обычных эксципиентов, известных специалисту в данной области. В фармацевтических композициях согласно настоящему изобретению для перорального, подъязычного, внутрикожного, внутримышечного, внутривенного, топического, местного, внутритрахеального,внутриносового, чрескожного или ректального введения действующее начало вышеприведенной формулы (I) или его соль может быть введено в стандартной лекарственной форме в смеси с обычными фармацевтическими эксципиентами животным или человеку для профилактики или лечения вышеуказанных расстройств или заболеваний. Подходящие стандартные лекарственные формы включают формы для перорального введения, такие как таблетки, мягкие или твердые желатиновые капсулы, порошки, гранулы и растворы или суспензии для перорального введения, формы для подъязычного, щечного введения, внутритрахеального, внутриглазного, внутриносового введения, введения путем ингаляции, формы для топического, парентерального, такого как чрескожного, подкожного, внутримышечного или внутривенного, формы для ректального введения и имплантаты. Для топического нанесения соединения по изобретению можно использовать в кремах, гелях, мазях или лосьонах. Для примера стандартная лекарственная форма соединения по изобретению в форме таблетки может содержать следующие компоненты: Суточная доза активного начала может доходить от 0,01 до 100 мг/кг, в один или несколько приемов, предпочтительно от 0,02 до 50 мг/кг. Как правило, суточная доза соединения по изобретению будет самой низкой эффективной дозой соединения, способного вызвать терапевтический эффект. Могут иметь место особые случаи, когда подходят более высокие или более низкие дозы; такие дозы не выходят за рамки настоящего изобретения. В обычной практике доза, подбираемая для каждого пациента, определяется врачом в зависимости от способа введения, массы тела и индивидуальной реакции указанного пациента. Настоящее изобретение согласно другому из своих аспектов включает также способ лечения указанных выше патологий, который включает введение пациенту эффективной дозы соединения по изобретению или одной из его фармацевтически приемлемых солей. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I) и В означает атом водорода или; А означает атом водорода и В означаетR1 и R2, одинаковые или разные, независимо означают атом водорода или галогена, С 1-4 алкил,С 1-4 фторалкил, С 1-2 перфторалкил, С 1-4 алкокси или трифторметокси; где R4 и R5, одинаковые или разные, находятся в любых свободных положениях и независимо означают атом водорода или галогена, С 1-4 алкил, С 1-4 фторалкил, С 1-2 перфторалкил,в виде оснований или солей присоединения с кислотами. 2. Соединение по п.1, гдеR1 и R2, одинаковые или разные, независимо означают атом водорода, галогена, С 1-4 алкил,С 1-4 фторалкил, С 1-2 перфторалкил, С 1-4 алкокси или трифторметокси;R3 означает группу формулы где R4 и R5, одинаковые или разные, находятся в любых свободных положениях и независимо означают атом водорода или галогена, С 1-4 алкил, С 1-4 фторалкил, С 1-2 перфторалкил,в виде оснований или солей присоединения с кислотами. 3. Соединение по любому из пп.1, 2, где R1 отличен от Н, в виде оснований или солей присоединения с кислотами. 4. Соединение по любому из пп.1-3, где R1 находится в положении -2-, -3- или -4- и означает атом хлора, радикал CF3 и R2 означает водород или 3- или 4-Cl, в виде оснований или солей присоединения с кислотой. 5. Соединение по любому из пп.1-4, где R3 означает 2-пиридинил, замещенный R4 и R5, значения которых определены в п.1, в виде оснований или солей присоединения с кислотами. 6. Соединение по любому из пп.1-5, где n=1, в виде оснований или солей присоединения с кислотой. 7. Соединение по любому из пп.1-6, где R1 означает CF3; R2 означает 4-хлор; R3 означает остаток 2-пиридила, замещенного в положении 5 группой CF3, и n=1, в виде основания или солей присоединения с кислотами. 8. Соединение по любому из пп.1-7, выбранное из следующих соединений: соединение 19: 4-2-[4-фенил-3,6-дигидро-2 Н-пиридин-1-ил]-2-оксоэтил-1-(5 трифторметилпиридин-2-ил)пиперазин-2-он; соединение 20: 4-2-оксо-2-[5-(2,3-дихлорфенил)-3,6-дигидро-2 Н-пиридин-1-ил]этил-1-(5 трифторметилпиридин-2-ил)пиперазин-2-он; соединение 21: 4-2-оксо-2-[5-(3-метоксифенил)-3,6-дигидро-2 Н-пиридин-1-ил]этил-1-(5 трифторметилпиридин-2-ил)пиперазин-2-он,в виде оснований или солей присоединения с кислотами. 9. Способ получения соединения формулы (I) по любому из пп.1-8, где А, В, m, n, R3 имеют значения, определенные выше, включающий стадию реакции соединения формулы (IV)Hal означает атом галогена,с соединением общей формулы (V)Hal означает атом галогена,за исключением 2-хлор-1-[4-(2-метоксифенил)-3,6-дигидро-2 Н-пиридин-1-ил]этанона и 2-хлор-1-[4-(4 бромфенил)-3,6-дигидро-2 Н-пиридин-1-ил]этанона, в виде основания или солей присоединения с кислотой. 11. Лекарственное средство, отличающееся тем, что оно включает соединение формулы (I) по любому из пп.1-8 или соль присоединения этого соединения с фармацевтически приемлемой кислотой,предназначенное для профилактики или лечения p75NTR-зависимых заболеваний. 12. Фармацевтическая композиция, отличающаяся тем, что она содержит соединение формулы (I) по любому из пп.1-8 или фармацевтически приемлемую соль, а также по меньшей мере один фармацевтически приемлемый эксципиент для получения лекарственного средства, предназначенного для профилактики или лечения p75NTR-зависимых заболеваний. 13. Соединение общей формулы (I) по любому из пп.1-8 для получения лекарственного средства, предназначенного для профилактики или лечения p75NTR-зависимых заболеваний. 14. Соединение общей формулы (I) в которой А, В, R3, m и n имеют значения, определенные в пп.1-8,обладающее способностью ингибировать димеризацию рецептора р 75NTR независимо от его лиганда.
МПК / Метки
МПК: A61P 29/00, A61K 31/496, C07D 401/14, A61P 25/00, A61P 35/00
Метки: применение, производные, получение, терапии, 2-оксоалкил-1-пиперазин-2-она
Код ссылки
<a href="https://eas.patents.su/14-19924-proizvodnye-2-oksoalkil-1-piperazin-2-ona-ih-poluchenie-i-ih-primenenie-v-terapii.html" rel="bookmark" title="База патентов Евразийского Союза">Производные 2-оксоалкил-1-пиперазин-2-она, их получение и их применение в терапии</a>
Предыдущий патент: Композиции со сниженным образованием димеров
Следующий патент: Стерилизатор с трубчатым распылителем
Случайный патент: Клей для огнеупорных материалов и керамики












