Производные бензофуранила как ингибиторы 5-нт6-рецептора
Номер патента: 15671
Опубликовано: 31.10.2011
Авторы: Сутин Лори, Йоханссон Гари, Кальдирола Патриция
Формула / Реферат
1. Соединение формулы (I)
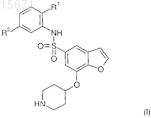
или его фармацевтически приемлемая соль, где R1представляет метокси и R2представляет метил; либо R1представляет метокси и R2представляет гидроксиметил; либо R1представляет гидроксил и R2представляет метил.
2. Применение соединения по п.1 для лечения или профилактики расстройства, связанного с 5-НТ6-рецептором, такого как ожирение, диабет II типа, для уменьшения массы тела и снижения увеличения массы тела.
3. Фармацевтический препарат для лечения или профилактики расстройства, связанного с 5-НТ6-рецептором, включающий соединение по п.1 в качестве активного ингредиента в сочетании с фармацевтически приемлемым разбавителем или носителем.
4. Фармацевтический препарат по п.3 для лечения или профилактики расстройства, такого как ожирение, диабет II типа, для уменьшения массы тела и снижения увеличения массы тела.
5. Способ лечения или профилактики расстройства, связанного с 5-НТ6-рецептором, такого как ожирение, диабет II типа, для уменьшения массы тела и снижения увеличения массы тела, который включает введение субъекту, нуждающемуся в таком лечении, эффективного количества соединения по п.1.
6. Способ модулирования активности 5-НТ6-рецептора, включающий введение субъекту, нуждающемуся в нем, эффективного количества соединения по п.1.
7. Применение соединения по п.1 для изготовления медикамента для использования в лечении или профилактике расстройства, связанного с 5-НТ6-рецептором, такого как ожирение, диабет II типа, для уменьшения массы тела и снижения увеличения массы тела.
Текст
ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ЕВРАЗИЙСКОМУ ПАТЕНТУ Дата публикации и выдачи патента ПРОИЗВОДНЫЕ БЕНЗОФУРАНИЛА КАК ИНГИБИТОРЫ 5-НТ 6-РЕЦЕПТОРА Настоящее изобретение относится к соединениям формулы (I), где R1 и R2 определены в описании; к фармацевтическим препаратам, включающим данные соединения, и к применению соединений для профилактики и лечения болезненных состояний, относящихся к ожирению, диабету II типа и/или для уменьшения массы тела и снижения увеличения массы тела. 015671 Область техники Настоящее изобретение относится к замещенным сульфонамидным соединениям, к фармацевтическим препаратам, включающим данные соединения и к применению данных соединений для профилактики и лечения болезненных состояний, относящихся к ожирению, диабету II типа и/или для уменьшения массы тела и снижения увеличения массы тела, а также в косметических целях. Уровень техники Ожирение представляет собой состояние, характеризующееся увеличением содержания жира в организме, приводящим к избыточной по сравнению с общепринятыми нормами массе тела. Ожирение является наиболее важным расстройством питания в западном мире и представляет собой наиболее важную проблему со здоровьем во всех индустриальных странах. Данное расстройство приводит к росту смертности вследствие увеличения частоты заболеваний, таких как сердечно-сосудистое заболевание,заболевание пищеварительного тракта, заболевание легких, рак и диабет II типа. Поиск соединений, которые снижают массу тела, продолжается в течение многих десятилетий. Одно направление исследований заключалось в активации серотонинергических систем либо путем прямой активации подтипов рецептора серотонина, либо путем ингибирования обратного захвата серотонина. Однако точный профиль требуемого подтипа рецептора неизвестен. Серотонин (5-гидрокситриптамин или 5-НТ), ключевой медиатор периферической и центральной нервной системы, модулирует широкий спектр физиологических и патологических функций, включая тревогу, регуляцию сна, агрессию, питание и депрессию. Идентифицированы и клонированы многочисленные подтипы рецепторов серотонина. Один из них, 5-НТ 6-рецептор, был клонирован несколькими группами в 1993 (Ruat, M. et al. (1993) Biochem. Biophys. Res. Commun. 193: 268-276; Sebben, M. et al.(1994) NeuroReport 5: 2553-2557). Данный рецептор позитивно связан с аденилилциклазой и проявляет сродство к антидепрессантам, таким как клозапин. Недавно был описан эффект агониста 5-НТ 6 и антисмысловых олигонуклеотидов 5-НТ 6 по снижению потребления пищи крысами (Bentley, J.C. et al. (1999)WO 2004/000828 и WO 02/100822, оба на имя Biovitrum AB, раскрывают сульфонамидные производные, которые связываются с 5-НТ 6-рецептором и которые могут быть использованы для лечения болезненных состояний, относящихся к ожирению, диабету II типа. Однако сульфонамидные производные по настоящему изобретению ранее описаны не были. Краткое описание чертежей На фиг. 1 представлены данные по влиянию на массу тела терапии соединением примера 1. На фиг. 2 - данные по влиянию на потребление пищи терапии соединением примера 1. Описание изобретения Неожиданно было найдено, что соединения формулы (I) проявляют сродство и селективность к 5 НТ 6-рецептору в качестве антагонистов в низком наномолярном диапазоне, причем данные сродство и селективность являются неожиданно высокими по сравнению с соединениями, известными из уровня техники. Соединения по изобретению и их фармацевтически приемлемые соли обладают активностью антагонистов, агонистов и частичных агонистов 5-НТ 6-рецептора и, как полагают, потенциально могут найти применение для лечения или профилактики ожирения, диабета II типа, для уменьшения массы тела и снижения увеличения массы тела, а также для лечения или профилактики расстройств центральной нервной системы. Уменьшение массы тела и снижение увеличения массы тела (например, лечение расстройств, связанных с массой тела) достигается помимо прочего путем уменьшения потребления пищи. Использованный здесь термин "расстройства, связанные с массой тела" относится к расстройствам, вызванным дисбалансом между потреблением энергии и расходом энергии, приводящим к отклоняющейся от нормы (например, избыточной) массе тела. Такие расстройства, связанные с массой тела, включают ожирение. Соединения формулы (I) Целью настоящего изобретения является соединение формулы (I)-1 015671 или его фармацевтически приемлемая соль, где R1 представляет метокси и R2 представляет метил; либо R1 представляет метокси и R2 представляет гидроксиметил; либо R1 представляет гидроксил и R2 представляет метил. Соединения формулы (I) могут быть использованы сами по себе или, где когда удобно, как их фармацевтические приемлемые соли (кислые или основные аддитивные соли). Подразумевается, что фармацевтически приемлемые аддитивные соли, упомянутые выше, включают терапевтически активные нетоксичные соли присоединения кислоты и основания (аддитивные формы солей), которые способны образовывать данные соединения. Соединения, которые обладают основными свойствами, могут быть переведены в их фармацевтически приемлемые кислотно-аддитивные соли обработкой основной формы подходящей кислотой. Типовые кислоты включают неорганические кислоты, такие как хлористый водород, бромистый водород, йодистый водород, серная кислота, фосфорная кислота; и органические кислоты, такие как уксусная кислота, пропановая кислота, гидроксиуксусная кислота, молочная кислота, пировиноградная кислота, гликолевая кислота, малеиновая кислота, малоновая кислота, щавелевая кислота, бензолсульфоновая кислота, толуолсульфоновая кислота, метансульфоновая кислота,трифторуксусная кислота, фумаровая кислота, янтарная кислота, яблочная кислота, винная кислота, лимонная кислота, салициловая кислота, п-аминосалициловая кислота, памовая кислота, бензойная кислота, аскорбиновая кислота и тому подобное. Типичными основно-аддитивными формами солей являются натриевые, калиевые, кальциевые соли и соли с фармацевтически приемлемыми аминами, такими как,например, аммиак, алкиламины, бензатин, и аминокислотами, такими как, например, аргинин и лизин. Использованный здесь термин "аддитивная соль" также включает сольваты, которые способны образовывать данные соединения и их соли, такие как, например, гидраты, алкоголяты и тому подобное. Для клинического применения соединения изобретения составляют в фармацевтические препараты для перорального, ректального, парентерального или другого способа введения. Фармацевтические препараты обычно получают смешением активного вещества или его фармацевтически приемлемой соли с обычными фармацевтическими эксципиентами. Препараты могут быть получены далее известными способами, такими как гранулирование, сжатие, микроинкапсулирование, нанесение распылением и так далее. Препараты могут быть получены обычными способами в виде лекарственных форм - таблеток, капсул, гранул, порошков, сиропов, суспензий, суппозиториев или инъекций. Жидкие препараты могут быть получены растворением или суспендированием активного вещества в воде или других подходящих наполнителях. Таблетки и гранулы могут быть покрыты слоем покрытия обычным способом. Другой целью настоящего изобретения является вышеуказанное соединение для применения в терапии. Другой целью настоящего изобретения является вышеуказанное соединение для применения в лечении или профилактике расстройства, связанного с 5-НТ 6-рецептором, такого как ожирение, диабет II типа и/или для уменьшения массы тела и снижения увеличения массы тела. Другой целью настоящего изобретения является фармацевтический препарат, включающий вышеуказанное соединение в качестве активного ингредиента в комбинации с фармацевтически приемлемым разбавителем или носителем. Другой целью настоящего изобретения является фармацевтический препарат, включающий вышеуказанное соединение для применения в лечении или профилактике расстройства, связанного с 5-НТ 6 рецептором, такого как ожирение, диабет II типа и/или для уменьшения массы тела и снижения увеличения массы тела. Другой целью настоящего изобретения является способ лечения или профилактики расстройства,связанного с 5-НТ 6-рецептором, такого как ожирение, диабет II типа и/или для уменьшения массы тела и снижения увеличения массы тела, который включает введение субъекту, нуждающемуся в таком лечении, эффективного количества вышеуказанного соединения. Другой целью настоящего изобретения является способ модулирования активности 5-НТ 6 рецептора, включающий введение нуждающемуся в нем субъекту эффективного количества вышеуказанного соединения. Другой целью настоящего изобретения является применение вышеуказанного соединения для изготовления медикамента для использования в лечении или профилактике расстройства, связанного с 5 НТ 6-рецептором, такого как ожирение, диабет II типа и/или для уменьшения массы тела и снижения увеличения массы тела. Описанные здесь способы могут также включать стадии идентификации того, что субъект нуждается в лечении ожирения, диабета II типа или же нуждается в уменьшении массы тела и снижении увеличения массы тела. Изобретение далее относится к применению в косметических целях одного или нескольких соединений любой из описанных здесь формул для того, чтобы вызвать снижение массы, а также фармацевтических препаратов, содержащих указанные соединения. Кроме того, изобретение относится к нетерапевтическому способу улучшения внешнего вида тела млекопитающего, включающего человека, где способ включает пероральное введение указанному млекопитающему одного или нескольких соединений любой из описанных здесь формул."Эффективное количество" относится к количеству соединения, которое оказывает терапевтиче-2 015671 ский эффект у подвергнутого лечению субъекта. Терапевтический эффект может быть объективным (то есть измеримым в определенном испытании или по определенному маркеру) или субъективным (то есть субъект указывает на или чувствует эффект). Для клинического применения соединения изобретения составляют в фармацевтические препараты для перорального, ректального, парентерального или другого способа введения. Обычно количество активных веществ находится в диапазоне 0,1-95 мас.% препарата, предпочтительно в диапазоне 0,2-20 мас.% в препаратах для парентерального применения и предпочтительно в диапазоне от 1 до 50 мас.% в препаратах для перорального введения. Типичная дневная доза активного вещества изменяется в широком диапазоне и будет зависеть от различных факторов, таких как, например, индивидуальные требования каждого пациента и путь введения. В целом пероральные и парентеральные дозировки будут находиться в диапазоне от 50 до 300 мг активного вещества в день, предпочтительно от 50 до 150 мг в день. Способы получения В другом аспекте изобретение относится к способам получения соединений любой из указанных здесь формул, включающим взаимодействие любого одного или нескольких соединений описанных здесь формул, включающим любые описанные здесь приемы. Соединения вышеуказанных формул могут быть получены обычными способами или по аналогии с ними и особенно согласно нижеприведенным способам или по аналогии с ними. Соединения, используемые в вышеописанном синтетическом пути, могут включать, например, растворители, реагенты, катализаторы, защитные группы и реагенты удаления защитных групп. Вышеописанные способы могут также дополнительно включать стадии (либо до, либо после конкретно описанных здесь стадий) введения или удаления подходящих защитных групп, чтобы, в конечном счете, провести синтез соединений любой из вышеописанных формул, их солевых форм или препаратов, которые включают данные соединения или их солевые формы. Кроме того, для получения желаемых соединений могут быть реализованы различные синтетические пути в альтернативной последовательности или альтернативном порядке. Трансформации синтетической химии и методики работы с защитными группами(введение и удаление защиты), пригодные для использования в синтезе подходящих соединений, известны из уровня техники и включают, например, такие, которые описаны в работах R. Larock, Comprehensive Organic Transformations, VCH Publishers (1989); T.W. Greene and P.G.M. Wuts, Protective Groups inSynthesis, John Wiley and Sons (1995), и более поздние их издания. Приведенные ниже конкретные примеры следует интерпретировать как иллюстративные и никоим образом не ограничивающие раскрытие. Не вдаваясь в дополнительные уточнения, предполагается, что специалист в данной области техники сможет, основываясь на приведенном здесь описании, использовать настоящее изобретение во всей его полноте. Все публикации, процитированные здесь, включены в виде ссылки во всей их полноте. Пример 1.N-[7-(4-пиперидинил)окси-1-бензофуран-5-ил]-2-метокси-5-метилбензолсульфонамид Соединение примера 1 было получено следующим образом: 7-иод-N-(2-метокси-5-метилфенил)-1-бензофуран-5-сульфонамид получали, исходя из 2,3 дигидробензофурана. Обработка хлорсульфоновой кислотой дает соответствующий сульфонилхлорид,который иодировали, используя монохлорид иода. Ароматизацию проводили, используя NBS, с получением 7-иод-N-(2-метокси-5-метилфенил)-1-бензофуран-5-сульфонамида после обработки крезидином. Гидролиз 7-иод-N-(2-метокси-5-метилфенил)-1-бензофуран-5-сульфонамида в щелочном растворе,используя медь в качестве катализатора, приводит к 7-гидрокси-N-(2-метокси-5-метилфенил)-1 бензофуран-5-сульфонамиду. Реакция с содержащим метилкарбаматную защиту мезилатом 4 гидроксипиридина,приводит к метил 4-[(5-[(2-метокси-5-метилфенил)амино]сульфонил-1 бензофуран-7-ил)окси]пиперидин-1-карбоксилату, который гидролизуется в щелочном растворе, давая названное в заглавие соединение.N-[7-(4-пиперидинил)окси-1-бензофуран-5-ил]-2-гидрокси-5-метилбензолсульфонамид. Биологические испытания Способность соединений по изобретению связываться с 5-НТ 6-рецептором и обладать фармацевтической применимостью может быть определена с использованием анализов in vivo и in vitro, известных в данной области техники.(а) Анализ на связывание 5-НТ 6 Для 5-НТ 6-рецептора эксперимент по определению сродства к связыванию проводили в клетках НЕК 293, трансфецированных 5-НТ 6-рецептором, используя (3H)-LSD в качестве меченого лиганда согласно общему способу, как описано Boess F.G. at al. Neuropharmacology vol. 36(4/5) 713-720, 1997. Материалы Культура клеток Клеточную линию НЕК-293, трансфецированную 5-НТ 6-рецептором, культивировали в модифицированной по Дульбекко среде Игла, содержащей 5% диализированной эмбриональной телячьей сыворотки (Gibco BRL 10106-169), 0,5 мМ пирувата натрия и 400 мкг/мл генетицина (G-418) (Gibco BRL 10131019). Клетки пассировали 1:10 дважды в неделю. Химикаты Радиолиганд [3 Н] LSD 60-240 Ки/ммоль, полученный от Amersham Pharmacia Biotech (Бакингемшир, Англия), находился в этаноле и хранился при -20 С. Соединения растворяли в 100% ДМСО и разводили связывающим буфером. Использованные процессы и оборудование одноразового пользования Соединения разводили в 96-луночных полипропиленовых планшетах Costar с V-образным дном лунок (Corning Inc. Costar, Нью-Йорк, США). Образцы инкубировали в Packard Optiplate (Packard Instruments B.V., Гронинген, Нидерланды). Общее количество добавленного радиолиганда измеряли в 24 луночных планшетах Barex от Packard (Packard Instruments B.V., Гронинген, Нидерлады) в присутствии сцинтилляционной жидкости Microscint 20 (Packard Bioscience, Мериден, Коннектикут, США). Буфер Связывающий буфер состоял из 20 мМ HEPES, 150 мМ NaCl, 10 мМ MgCl2 и 1 мМ EDTA, рН 7,4. Способы Получение мембран Клетки выращивали до приблизительно 90% конфлюэнтности в чашках для культивированияNUNC 24,524,5. Среду отсасывали и после промывания охлажденным льдом PBS клетки соскабливали,используя 25 мл трис-буфера (50 мМ Tris-HCl, 1 мМ EDTA, 1 мМ EGTA, рН 7,4) и оконный скребок. Затем клетки разрушали гомогенизатором Polytron, и оставшиеся твердые частицы удаляли низкоскоростным центрифугированием, 1000 g в течение 5 мин. В заключение мембраны отделяли высокоскоростным центрифугированием (20000 g), суспендировали в связывающем буфере и замораживали в аликвотах при -70 С. Связывание радиолиганда Замороженные клеточные мембраны размораживали, немедленно регомогенизировали, используя гомогенизатор Polytron, и связывали со SPA-гранулами агглютинина пшеничных зародышей (AmershamLife Sciences, Кардифф, Англия) в течение 30 мин при непрерывном встряхивании пробирок. По окончании связывания гранулы центрифугировали в течение 10 мин при 1000 g и впоследствии суспендировали в 20 мл связывающего буфера на каждый 96-луночный планшет. Затем инициировали реакцию связыва-4 015671 ния добавлением радиолиганда и тестируемых соединений к суспензии гранул-мембран. После инкубации при комнатной температуре аналитические планшеты подвергали сцинтилляционным измерениям. Следовали оригинальному SPA-способу за исключением того, что мембраны получали из клеток НЕК 239, экспрессирующих человеческий 5-НТ 6-рецептор, а не из клеток HeLa (Dinh DM, Zaworski PG,Gill GS, Schlachter SK, Lawson CF, Smith MW. Validation of human 5-HT6 receptors expressed in HeLa cellLSD являлось насыщаемым, тогда как неспецифическое связывание возрастало линейно с концентрацией добавленного радиолиганда. [3 Н] LSD связывался с высоким сродством с 5-НТ 6-рецепторами. ВеличинаKd была оценена равной 2,60,2 нМ на основе четырех отдельных экспериментов. Общее связывание при 3 нМ [3 Н] LSD, концентрации радиолиганда, использованной в конкурентных экспериментах, типично составляло 6000 распадов в минуту, и специфическое связывание составляло более чем 70%. 5-НТ вызывал зависящее от концентрации ингибирование [3 Н] LSD-связывания с общим средним значением Ki, равным 236 нМ, при тестировании по двум различным препаратам мембран. Вариабельность между анализами по трем экспериментам показала CV в 10% со средним значением Ki,равным 173 нМ (SD 30) и коэффициентом Хилла, равным 0,94 (SD 0,09). Разброс между анализами составлял 3% (n=4). Значения Ki для соединения примера 1 представлены в табл. 3. Все немеченые лиганды смещали специфическое связывание [3 Н] LSD зависящим от концентрации образом, хотя и с разными эффективностями. Порядок изменения эффективности для соединений был следующим: метиотепин (2 нМмиансерин (190 нМ)5-НТ (236 нМ)метисергид (482 нМ)месулергид (1970 нМ). Определение белка Концентрации белка определяли с помощью BioRad Protein Assay (Bradford MM. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding.Anal Biochem 1976;72:248-54. Бычий сывороточный альбумин использовали как стандарт. Счет сцинтилляции Радиоактивность измеряли в сцинтилляционном счетчике Packard TopCount (Packard Instruments,Мериден, Коннектикут, США) при эффективности счета, равной приблизительно 20%. Эффективность счета определяли в отдельных экспериментальных сериях. Эксперименты с насыщением В экспериментах с насыщением использовали по крайней мере 6 концентраций радиолиганда в двух экземплярах (0,1-20 нМ [3 Н] LSD). Специфическое связывание рассчитывали как разницу между общим связыванием и неспецифическим связыванием, которое определяли как связывание радиолиганда в присутствии 5 мкМ лизурида. Bmax и константу диссоциации Kd определяли из нелинейнорегрессионного анализа, используя уравнение 1. Lu представляет собой несвязанную концентрацию радиолиганда, а у представляет собой связанное количество. Конкурентные эксперименты Общее и неспецифическое связывание радиолиганда определяли в восьми повторах каждого. Образцы, содержащие тестируемое соединение, анализировали дважды при 11 концентрациях. Инкубации проводили при комнатной температуре в течение 3 ч. Значение IC50, то есть концентрацию тестируемого соединения, которая ингибирует 50% специфического связывания радиолиганда, определяли нелинейнорегрессионным анализом, и значение Ki рассчитывали, используя способ [Cheng Y.C. Biochem. Pharmacol. 22, 3099-3108, 1973S] уравнения 2.(а) Анализ на внутреннюю активность 5-НТ 6 Антагонисты 5-НТ 6-рецептора характеризовали измерением ингибирования 5-НТ-индуцированного увеличения сАМР в клетках НЕК 293, экспрессирующих человеческий 5-НТ 6-рецептор (см. Boess et al.(1997) Neuropharmacology 36: 713-720). Вкратце, клетки НЕК 293/5-НТ 6 высевали в покрытых полилизином 96-луночных планшетах с плотностью 25000/ячейку и выращивали в DMEM (модифицированной по Дульбекко среде Игла) (без фенолового красного), содержащей 5% диализированной эмбриональной телячьей сыворотки, в течение 48 ч при 37 С в инкубаторе с 5% СО 2. Затем среду отсасывали и заменяли на 0,1 мл среды для анализа (Hanks Balance Salt Solution, содержащий 20 мМ HEPES, 1,5 мМ изобутилметилксантина и 1 мг/мл альбумина бычьей сыворотки). После добавления тестируемых веществ, растворенных в 50 мкл среды для анализа, клетки инкубировали в течение 10 мин при 37 С в инкубаторе с 5% СО 2. Затем среду вновь отсасывали и определяли содержание сАМР, используя набор радиоактивного сАМР (Amersham Pharmacia Biotech, BIOTRAK PPA559). Эффективность антагонистов устанавливали-5 015671 количественно путем определения концентрации, которая вызывала 50% ингибирование 5-НТиндуцированного увеличения сАМР (при [5-НТ]=8-кратному ЕС 50), используя формулуIC50,корр=IC50/(1+[5 НТ]/ЕС 50). Соединение примера 1 имеет селективное сродство к 5-НТ 6-рецепторам со значениями Ki и IC50,корр от 0,5 нМ до 5 мкМ или показывает % ингибирования [3 Н] LSD20% при 50 нМ и является антагонистом, агонистом или частичным агонистом 5-НТ 6. Соединение примера 1 показывает хорошую селективность относительно 5-HT1a, 5-НТ 2 а, 5-HT2b и 5-НТ 2 с (значения см. в табл. 3). Были использованы дополнительные анализы для соединения примера 1, см. табл. 1. Таблица 1. Дополнительные анализы, использованные для соединения примера 1 Способы и материалы Тестируемые соединения Соединение примера 1 растворяли в 5% (мас./об.) PEG 400, 0,2% Tween 80 + 10 мМ ацетатного натриевого буфера, рН 6. Соответствующий раствор использовали в качестве наполнителя. Стабильность растворов контролировали после хранения в течение 14 дней. Растворы готовили дважды в неделю и хранили в морозильной камере. Растворы анализировали на фактические концентрации и устанавливали,что они оставались сходными между двумя анализами. Животные Сто (100) самцов крыс Sprague-Dawley были выращены, используя диету с высоким содержанием жира, в Scanbur ВК АВ (Соллентуна, Швеция), которые по прибытию на станцию по уходу за животными фирмы Biovitrum весили приблизительно 700 г (возраст 17 недель). После прибытия крыс откармливали и взвешивали в течение приблизительно трех недель. Крыс содержали по одной в стандартных клетках при постоянных комнатных условиях (темп. 22+/-1 С, влажность 40-60%, цикл 12 ч свет/темнота, выключение света в 10 ч утра). Крысы получали тот же корм с высоким содержанием жира(45 ккал% жира, 4,7 ккал/г; D12451), который они получали в Scanbur. Корма приобретались у ResearchDiets, Inc., Нью-Джерси, США, состояли из шариков и хранились в сухих и прохладных условиях. Проведение эксперимента Отбирали откормленных пищей с высоким содержанием жира животных, которые приобрели наибольшую массу. Данная популяция весила 79960 г. Отобранные сорок восемь (48) крыс были рандомизированы и поделены на пять терапевтических групп, чтобы получить насколько это возможно гомогенные группы по массе тела. Каждая терапевтическая группа состояла из 12 крыс: Группа 1 - наполнитель,Группа 2 - соединение примера 1-5 мг/кг (11 мкмоль/кг), Группа 3 - соединение примера 1-15 мг/кг (33 мкмоль/кг), Группа 4 - соединение примера 1-30 мг/кг (66 мкмоль/кг). Дополнительные девять (9) крыс-6 015671 выделили для измерения действия соединения и фармакокинетики в каждой дозировочной группе параллельно для седьмого и двадцать девятого дней. Исследование начинали измерением базисной линии в течение пяти дней, чтобы адаптировать крыс к методике проведения исследования и к экспериментаторам. Тестируемое соединение вводили перорально один раз в день в 9-10 ч утра в объеме 2,5 мл/кг, то есть в среднем 2 мл на (800 г) крысу. Шарики корма и вес тела взвешивали каждый день в связи с инъекциями (введениями). Бутылки с водой взвешивали раз в неделю. Взвешивания проводили на связанных с компьютером весах Mettler Toledo PR 5002. Все данные переводились в шаблон Excel. На двадцать восьмой день отбирали образцы крови для определения сывороточной глюкозы, инсулина, лептина, свободных жирных кислот, триглицеридов, холестерина, HDL, LDL, ALAT, ASAT и мочевины. Также определяли гематокрит. Диссектировали и взвешивали эпидидимальную белую жировую ткань, печень и икроножную мышцу. Фармакокинетика Описанные выше животные-спутники для воздействия на плазму (3 животных/доза) получали пероральную терапию 5, 15 и 30 мг/кг/dag - Пример 1. На 7 день образцы крови отбирали из хвостовой вены во временных точках: до введения дозы, через 10, 30 мин, 1, 2, 3, 4, 6, 8 или 24 ч после введения дозы. У животных в терапевтической группе 15 мг/кг/dag новые образцы крови отбирали на 28 день в соответствующих временных точках, как в 7 день. Образцы крови (примерно 150 мкл) собирали в гепаринизированные пробирки и помещали на лед до проведения центрифугирования (4000 об/мин, 5 мин, +4 С). До проведения анализа плазму хранили при -20 С. Образцы крови анализировали HPLC и тандемной масс-спектрометрией с ионизацией электроспреем. Статистика Потребление пищи и воды и данные по массе тела рассчитывали в граммах и % значений, отвечающих основному обмену, и выражали как среднее +/- SD и/или +/- SEM. Значение, отвечающее основному обмену, в день до начала терапии (день 0) считали репрезентативным, поскольку усреднение значений по всем дням, предшествующим терапии, не меняло результатов. Данные по массе тела и потреблению пищи статистически анализировали двойным одномерным анализом ANOVA с повторяющимися измерениями (терапия х время) с последующим одинарным анализом ANOVA для сравнения между терапевтическими группами в выбранных временных точках. Измерения клинической биохимии анализировали одинарным анализом ANOVA с последующим t-тестом Даннета для проверки значимости терапевтических групп против контроля с наполнителем. Различие между двумя группами рассматривалось как значимое, если Р 0,05. Статистические оценки проводили, используя SPSS для Windows. Результаты Влияние на массу тела Цель долгосрочного исследования заключалась в том, чтобы установить, приведет ли пролонгированный период терапии, равный четырем неделям, к сохраняющемуся снижению массы тела и, кроме того, в определении минимально эффективной дозы. Дозы выбирали, основываясь на предыдущих срочных и долгосрочных исследованиях с соединением примера 1. Масса тела уменьшалась значительно за счет введения соединения примера 1 на протяжении всего периода терапии (группы с повтореннымANOVA F(3,42) = 12,6; Р 0,001) (фиг. 1). Снижение массы тела составляло 3,9, 3,7 и 6,9% для доз 5, 15 и 30 мг/кг, соответственно (t-тест Даннета Р 0,001 для всех групп против наполнителя) (см. табл. 2). Таблица 2. Сводка о влиянии 28-дневной терапии соединением примера 1 на массу тела DIO-крыс Приобретенная масса тела рассчитана как масса в 28 день - начало; Уменьшение означает граммы или % против наполнителя в день 28. Значения Р основаны на значениях, отвечающих основному обмену, (%), используя t-тест Даннета. Влияние на потребление пищи Соединение примера 1 значительно уменьшало потребление пищи на протяжении первых семи дней,как показано на фиг. 2 (группы с повторенным ANOVA F(3, 42) = 9,887; Р 0,001). t-Тест Даннета показал, что дозы 15 и 30 мг/кг значительно отличались от наполнителя (Р 0,001), тогда как доза 5 мг/кг - нет. Таким образом, минимально эффективной дозой является 15 мг/кг. Влияние на прием пищи ослаблялось в период с 8 по 14 дни, но оставалось пониженным в течение остальной части периода терапии, хотя не было статистически значимым (группы F(3, 42) = 2,459; Р 0,076). Среднее снижение по дням с 15 по 28 составляло 7-12%, но только наибольшая доза действительно достигала статистической значимости (Р 0,035).-7 015671 Таблица 3. Биологические данные для соединения примера 1. In vitro связывание с человеческим 5-НТ 6-рецептором В табл. 4-6 приведены некоторые значения для соединения известного уровня техники по аналогии со значениями, приведенными в табл. 3 для соединения примера 1. Таблица 4. Значения, приведенные для примера 148 (гидрохлорид N-(7-пиперазин-1-илбензофуран-5-ил)-1-нафтилсульфонамида) из WO 02/100822. В примере 148 NH-часть сульфонамидной группы связана с бензофурановым кольцом. Данные табл. 4 свидетельствуют, что соединение примера 1 обладает большей селективностью к 5 НТ 6 относительно 5-НТ 2 а, 5-НТ 2b и 5-НТ 2 с по сравнению с соединением примера 148, раскрытым в WO 02/100822. Чтобы достичь хорошей селективности к 5-НТ 6 относительно 5-НТ 2 а, 5-НТ 2b и 5-НТ 2 с, Kiсвязывание для последних рецепторов должно быть по крайней мере в 100 раз больше по сравнению с 5 НТ 6-связыванием. Таблица 5. Значения, приведенные для соединения А (гидрохлорида [7-(пиперидин-4-илокси)бензофуран-5-ил]амида 5-хлортиофен-2-сульфоновой кислоты) и соединения В (N-[7-(4 пиперидинилокси)-1-бензофуран-5-ил]-2-трифторметилбензолсульфонамида), охватываемых (защищенных), но не раскрытых конкретно в WO 2004/000828. В обоих соединениях А и В NH-часть сульфонамидной группы связана с бензофурановым кольцом. Данные табл. 5 свидетельствуют, что соединение примера 1 обладает как большей селективностью к 5-НТ 6 относительно 5-НТ 2 а, 5-НТ 2b и 5-НТ 2 с, так и лучшими значениями 1, 2, к (КОР) и 5-НТ 3-8 015671 ингибирования по сравнению с Соединениями А и В, защищенными WO 2004/000828. Чтобы достичь хорошей селективности к 5-НТ 6 относительно 1, 2, к (КОР) и 5-НТ 3, % ингибирования для последних должен быть 70% при 1 мкМ. Таблица 6. Значения, приведенные для соединения С (N-[7-(4-пиперидинил)окси-1-бензофуран-5 ил]-2-метокси-6-метилбензолсульфонамида) и соединения D (N-[7-(3-пиперидинил)окси-1-бензофуран-5 ил]-2-метокси-5-метилбензолсульфонамида), охватываемых (защищенных), но не раскрытых конкретно в WO 2004/000828. В обоих соединениях С и D SO2-часть сульфонамидной группы связана с бензофурановым кольцом. Данные табл. 6 свидетельствуют, что соединение примера 1 обладает большей селективностью к 5 НТ 6 относительно 5-НТ 2 а, 5-НТ 2b и 5-НТ 2 с по сравнению с соединениями С и , защищенными в WO 2004/000828. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I) или его фармацевтически приемлемая соль, где R1 представляет метокси и R2 представляет метил; либо R1 представляет метокси и R2 представляет гидроксиметил; либо R1 представляет гидроксил и R2 представляет метил. 2. Применение соединения по п.1 для лечения или профилактики расстройства, связанного с 5-НТ 6 рецептором, такого как ожирение, диабет II типа, для уменьшения массы тела и снижения увеличения массы тела. 3. Фармацевтический препарат для лечения или профилактики расстройства, связанного с 5-НТ 6 рецептором, включающий соединение по п.1 в качестве активного ингредиента в сочетании с фармацевтически приемлемым разбавителем или носителем. 4. Фармацевтический препарат по п.3 для лечения или профилактики расстройства, такого как ожирение, диабет II типа, для уменьшения массы тела и снижения увеличения массы тела. 5. Способ лечения или профилактики расстройства, связанного с 5-НТ 6-рецептором, такого как ожирение, диабет II типа, для уменьшения массы тела и снижения увеличения массы тела, который включает введение субъекту, нуждающемуся в таком лечении, эффективного количества соединения по п.1. 6. Способ модулирования активности 5-НТ 6-рецептора, включающий введение субъекту, нуждающемуся в нем, эффективного количества соединения по п.1. 7. Применение соединения по п.1 для изготовления медикамента для использования в лечении или профилактике расстройства, связанного с 5-НТ 6-рецептором, такого как ожирение, диабет II типа, для уменьшения массы тела и снижения увеличения массы тела.
МПК / Метки
МПК: A61K 31/443, A61P 3/04, C07D 405/12
Метки: производные, ингибиторы, бензофуранила, 5-нт6-рецептора
Код ссылки
<a href="https://eas.patents.su/10-15671-proizvodnye-benzofuranila-kak-ingibitory-5-nt6-receptora.html" rel="bookmark" title="База патентов Евразийского Союза">Производные бензофуранила как ингибиторы 5-нт6-рецептора</a>
Предыдущий патент: Антисмысловые соединения, нацеленные на коннексины, и способы их применения
Следующий патент: Тканезащитные пептиды и их применения
Случайный патент: Привод дозирующего ингалятора