2-(3,5 -бис-трифторметилфенил)-n-[6-(1,1-диоксо-1лямда6-тиоморфолин-4-ил)-4-(2- метил- или 4-фтор-2-метил) фенилпиридин-3-ил]-n-метилизобутирамид
Номер патента: 6238
Опубликовано: 27.10.2005
Авторы: Хоффманн Торстен, Слейт Эндрю, Поли Соня Мария, Шнидер Патрик, Баллар Мария Тереса
Формула / Реферат
1. Соединение формулы
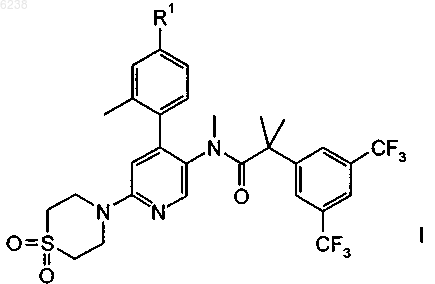
где R1 означает водород или фтор;
и его фармацевтически приемлемые кислотно-аддитивные соли.
2. Соединение формулы I по п.1, где соединение означает 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-1l6-тиоморфолин-4-ил)-4-ортотолилпиридин-3-ил]-N-метилизобутирамид.
3. Соединение формулы I по п.1, где соединение означает 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-1l6-тиоморфолин-4-ил)-4-(4-фтор-2-метилфенил)пиридин-3-ил]-N-метилизобутирамид.
4. Лекарственное средство, содержащее соединение формулы I по пп.2 и 3 и фармацевтически приемлемые эксципиенты.
5. Лекарственное средство по п.4 для лечения заболеваний, опосредованных рецептором NK-1.
6. Способ получения соединения формулы I по п.1, включающий взаимодействие соединения формулы

с пероксимоносульфатом калия с образованием соединения формулы
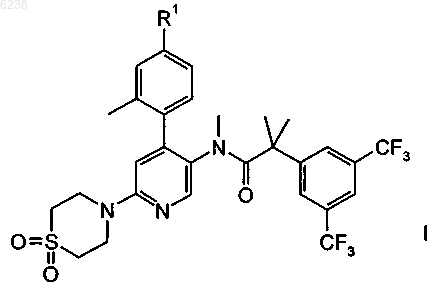
где R1 означает водород или фтор,
и при необходимости превращение полученного соединения в фармацевтически приемлемую кислотно-аддитивную соль.
7. Соединение формулы I по любому из пп.1, 2 или 3, полученное способом по п.6.
8. Применение соединения формулы I по любому из пп.1-3 для лечения заболеваний.
9. Применение соединения формулы I по п.8 для лечения заболеваний, опосредованных рецептором NK-1.
10. Применение соединения формулы I по любому из пп.1-3 для получения лекарственных средств для лечения заболеваний, опосредованных рецептором NK-1.
11. Применение по п.10 для получения лекарственных средств для лечения мигрени, ревматоидного артрита, астмы, повышенной реактивности бронхов, воспалительного заболевания кишечника или для лечения состояний, включающих болезнь Паркинсона, тревогу, депрессию, боль, головную боль, болезнь Альцгеймера, рассеянный склероз, отек, аллергический ринит, болезнь Крона, глазную травму, воспаления глаз, психоз, укачивание, индуцированную рвоту, рвоту, недержание мочи, психоиммунологические или психосоматические состояния, онкологические заболевания, синдром отмены лекарственных средств от опиоидов до никотина, травму мозга или доброкачественную гиперплазию предстательной железы.
12. Применение по пп.10 и 11 для получения лекарственных средств для лечения депрессии, тревоги или рвоты.
Текст
где R1 означает водород или фтор, и к его фармацевтически приемлемым кислотно-аддитивным солям. Изобретение прежде всего относится к следующим соединениям: 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)-4-ортотолилпиридин-3 ил]-N-метилизобутирамид и 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)-4-(4-фтор-2-метилфенил) пиридин-3-ил]-N-метилизобутирамид. Указанные два соединения являются новыми соединениями. В общем виде эти соединения описаны в ЕР 1035115. Соединения формулы I и их соли обладают ценными терапевтическими свойствами. Установлено,что соединения по настоящему изобретению являются высоко селективными антагонистами рецептора нейрокинина (NK-1, вещества Р). Вещество Р представляет собой природный ундекапептид, относящийся к семейству пептидов тахикинина, названных так благодаря их способности стимулировать сокращение гладких мышц внесосудистой ткани. Рецептор вещества Р является членом суперсемейства рецепторов, ассоциированных с G-белком. Нейропептидный рецептор вещества Р (NK-1) широко распространен в нервной системе млекопитающих (прежде всего в головном мозге и спинальных ганглиях), в кровеносной системе и в периферических тканях (прежде всего в двенадцатиперстной кишке и тощей кишке) и принимает участие в регуляции ряда различных биологических процессов. Центральное и периферическое действие тахикининового вещества Р млекопитающих связано с многими воспалительными процессами, которые включают мигрень, ревматоидный артрит, астму и воспалительное заболевание кишечника, а также с опосредованием рвотного рефлекса и модуляцией нарушений центральной нервной системы (ЦНС), таких как болезнь Паркинсона (Neurosci. Res., 7, 187-214(1996, тревога (Can. J. Phys., 75, 612-621 (1997 и депрессия (Science, 281, 1640-1645 (1998. Обоснование возможности применения антагонистов рецептора тахикинина в случае боли, головной боли, прежде всего мигрени, болезни Альцгеймера, рассеянного склероза, ослабления синдрома отмены морфина, сердечно-сосудистых изменений, отека, такого как отек, вызванный термическим ожогом, хронических воспалительных заболеваний, таких как ревматоидный артрит, астма/повышенная реактивность бронхов и другие респираторные заболевания, включая аллергический ринит, воспалительные заболевания кишечника, включая язвенный колит и болезнь Крона, травмы глаз и воспалительное заболевание глаз, рассматривается в статье "Tachykinin Receptor and Tachykinin Receptor Antagonists", J.Auton. Pharmacol., 13, 23-93 (1993). Кроме того, исследуется возможность применения антагонистов рецептора нейрокинина-1 при лечении ряда физиологических состояний, ассоциированных с избытком или дисбалансом тахикинина,прежде всего вещества Р. Примеры состояний, при которых показано применение вещества Р, включают такие состояния центральной нервной системы, как тревога, депрессия и психоз (WO 95/16679, WO 95/18124 и WO 95/23798). Кроме того, антагонисты рецептора нейрокинина-1 используются при лечении укачивания и приступов рвоты. Кроме того, в The New England Journal of Medicine, 340, 3, 190-195 (1999) описано ослабление приступов рвоты, индуцированной цисплатином, при введении селективного антагониста рецептора нейрокинина-1. Возможность применения антагонистов рецептора нейрокинина-1 при лечении некоторых форм недержания мочи описана также в Neuropeptides, 32(1), 1-49 (1998) и в Eur. J. Pharmacol., 383(3), 297-303(1999). Кроме того, в US 5972938 описан способ лечения психоиммунологического или психосоматического нарушения введением антагониста рецептора тахикинина, такого как антагонист рецептора NK-1. В Life Sci., 67(9), 985-1001 (2000) описано, что астроциты экспрессируют функциональные рецепторы ко многим нейромедиаторам, включая вещество Р, что является важным стимулом реактивных астроцитов при развитии ЦНС, инфекции или травме. При опухолях мозга злокачественные глиальные клетки, происходящие из астроцитов, стимулируются тахикининами через рецепторы NK-1 в результате чего выделяют растворимые медиаторы и увеличивают скорость пролиферации. Следовательно, селективные антагонисты рецептора NK-1 могут найти применение при разработке способов лечения злокачественных глиом в онкологии.-1 006238 В Nature (London), 405(6783), 180-183 (2000) описано, что у мышей с генетическим нарушением рецептора NK-1 наблюдается потеря чувствительности к действию морфина. Следовательно, антагонисты рецептора NK-1 могут применяться для лечения симптомов привыкания к наркотическим лекарственным средствам, таким как опиоиды и никотин, а также для снижения злоупотребления/влечения к таким средствам. Сообщается также, что антагонисты рецептора NK-1 обладают лечебным действием при терапии черепно-мозговых травм (устное сообщение проф. Ниммо "Neurokinin-1 (NK-1) Receptor Antagonists Improve the Neurological Outcome Following Traumatic Brain Injury" Ha Международной конференции по тахикинину в La Grande Motte, France, 17-20 октября 2000 г.; авторы: A.J. Nimmo, C.J. Bennett, X. Hu, I.Cernak, R. Vink). Кроме того, соединения по настоящему изобретению используются при лечении доброкачественной гиперплазии предстательной железы (ВРН), распространенного заболевания у пожилых мужчин. ВРН может прогрессировать и привести к удерживанию мочи, инфекциям, камням в мочевом пузыре и почечной недостаточности. Такие показания описаны в ЕР 01109853.0. Соединения формулы (I) можно также использовать в форме их пролекарств, например, в форме Nоксидов. Дополнительно к полезным свойствам соединений по изобретению пролекарства характеризуются дополнительными преимуществами в отношении абсорбции, фармакокинетического распределения и транспорта в мозг. Объектом настоящего изобретения являются соединения формулы (I) и их фармацевтически приемлемые соли, способ получения вышеуказанных соединений, лекарственные средства, содержащие указанные соединения, и их получение, а также применение вышеуказанных соединений при лечении или профилактике заболеваний, прежде всего заболеваний и нарушений, указанных выше, или применение при получении соответствующих лекарственных средств. Наиболее предпочтительными показаниями по настоящему изобретению являются показания к применению, которые включают нарушения центральной нервной системы, например, к лечению или профилактике введением антагониста рецептора NK-1 некоторых депрессивных состояний, тревоги или приступов рвоты. Основной депрессивный период определяют как период по меньшей мере две недели,во время которого в течение большинства дней или почти каждый день наблюдается подавленное настроение или потеря интереса к чему-либо или удовольствия от чего-либо, или почти полная потеря активности. Термин "фармацевтически приемлемая кислотно-аддитивная соль", используемый в тексте заявки,означает соли неорганических и органических кислот, таких как хлористо-водородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота,малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфокислота, паратолуолсульфокислота и т.п. Соединения формулы (I) и их фармацевтически приемлемые соли получают известными в данной области техники методами, например, способом, описанным ниже, который включает взаимодействие соединения формулы где R1 означает водород или фтор и, при необходимости, превращение полученного соединения в фармацевтически приемлемую кислотно-аддитивную соль. В соответствии с вариантом вышеописанного способа к раствору 2-(3,5-бис-трифторметилфенил)N-метил-N-(6-тиоморфолин-4-ил-4-ортотолилпиридин-3-ил)изобутирамида или 2-(3,5-бис-трифторме-2 006238 тилфенил)-N-метил-N-(6-тиоморфолин-4-ил-4-(4-фтор-2-метилфенил)пиридин-3-ил)изобутирамида в спирте, таком как метанол, добавляют OXONE или любые другие пригодные окислители, известные специалисту в данной области, и смесь перемешивают при комнатной температуре в течение приблизительно двух суток. После очистки получают необходимое соединение формулы I с высоким выходом. Соли получают при комнатной температуре известными способами, в том числе известными специалисту в данной области. Для этих целей получают соли как неорганических, так и органических кислот. Примерами таких солей являются гидрохлориды, гидробромиды, сульфаты, нитраты, цитраты, ацетаты, малеаты, сукцинаты, метансульфонаты, паратолуолсульфонаты и т.п. Способы получения соединений формулы I более подробно показаны на схеме и описаны в примерах 1 и 2. Исходные соединения формул III, IV, VIII и XII являются известными соединениями или их можно получить известными в данной области техники методами. На схеме используются следующие сокращения: На схеме R1 означает водород или фтор. Как указано выше, соединения формулы I и их фармацевтически приемлемые кислотно-аддитивные соли обладают ценными фармакологическими свойствами. Установлено, что соединения по настоящему изобретению являются антагонистами рецептора нейрокинина-1 (NK-1, вещество Р). Соединения формулы I испытывают на биологическую активность, как описано ниже. Сродство соединений, 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)-4 ортотолилпиридин-3-ил]-N-метилизобутирамида и 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16 тиоморфолин-4-ил)-4-(4-фтор-2-метилфенил)пиридин-3-ил]-N-метилизобутирамида к рецептору NK-1 человека определяли на клетках СНО, инфицированных рецептором NK-1 человека (при использовании системы экспрессии вируса леса Семлики) и веществом Р, содержащим радиоактивную метку [3 Н] (ко-3 006238 нечная концентрация 0,6 нМ). Анализ связывания проводили в буферном растворе (HEPES, 50 мМ, рН 7,4), содержащим БСА (0,04%), лейпептин (8 мкг/мл), МnСl2 (3 мМ) и фосфорамидон (2 мкМ). Реакционная смесь для анализа содержала 250 мкл суспензии мембранной фракции (1,25105 клеток/пробирка),0,125 мкл раствора конкурирующего агента в буферном растворе и 125 мкл раствора [3 Н] вещества Р. Кривые конкурентного связывания определяли по меньшей мере при семи концентрациях анализируемого соединения. Пробирки с образцами инкубировали при комнатной температуре в течение 60 мин, а затем реакционную смесь быстро фильтровали в вакууме через фильтры GF/C, предварительно пропитанные PEI (0,3%) в течение 60 мин и промытых (22 мл) буферным раствором HEPES (50 мМ, рН 7,4). Радиоактивную метку на фильтрах измеряли на сцинтилляционном счетчике. Все анализы проводили при трехкратном повторе по меньшей мере в двух паралелльных опытах. Соединения 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)-4-ортотолилпиридин-3-ил]-N-метилизобутирамида и 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16 тиоморфолин-4-ил)-4-(4-фтор-2-метилфенил)пиридин-3-ил]-N-метилизобутирамида являются эффективными и селективными лигандами рекомбинантных рецепторов NK-1 человека, экспрессированных в СНО клетках. Указанные соединения характеризуются сродством с рецептором NK-1 человека, причем их pKi составляют 8,9 и 9,5 соответственно, а их селективность к рецептору NK-1 на три порядка выше,чем к другим нейрокининовым рецепторам. Активность in vitro определяли, изучая воздействие указанных соединений на индуцированный веществом Р приток Са 2+ в клетки СНО, экспрессирующие рекомбинантный рецептор NK-1 человека. В этих клетках вещество Р вызывает концентрационнозависимый приток Са 2+, который измеряют методомFLIPR. При повышенных концентрациях 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)-4-ортотолилпиридин-3-ил]-N-метилизобутирамид и 2-(3,5-бис-трифторметилфенил)-N-[6(1,1-диоксо-16-тиоморфолин-4-ил)-4-(4-фтор-2-метилфенил)пиридин-3-ил]-N-метилизобутирамид ингибировали приток Са 2+, индуцированный веществом Р. Эти данные свидетельствуют, что оба соединения являются антагонистами рецептора NK-1 человека. При исследовании in vivo 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)4-ортотолилпиридин-3-ил]-N-метилизобутирамид подавляет рефлекс постукивания лапами, индуцированный у карликовой песчанки интрацеребровентрикулярной инъекцией агониста рецептора NK-1. Доза указанного соединения, рассчитанная на 50% ингибирования рефлекса постукивания лапами при пероральном введении, составляет 0,8 мг/кг. Кроме того, измеряли уровень в плазме, необходимый для полного подавления этого рефлекса и было установлено, что для полного блокирования рефлекса постукивания лапами необходимая общая концентрация в плазме составляет 10 нг/мл. Аналогичным образом, 2(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)-4-(4-фтор-2-метилфенил)пиридин-3-ил]-N-метилизобутирамид также подавлял рефлекс постукивания лапами у песчанки, индуцированный агонистом рецептора NK-1. Доза указанного соединения, рассчитанная на 50% ингибирования рефлекса постукивания лапами при пероральном введении, составляет 0,1 мг/кг. Уровень в плазме, необходимый для полного подавления этого рефлекса составляет менее 10 нг/мл. Следовательно, оба соединения, 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)-4-ортотолилпиридин-3-ил]-N-метилизобутирамид и 2-(3,5-бис-трифторметилфенил)-N-[6(1,1-диоксо-16-тиоморфолин-4-ил)-4-(4-фтор-2-метилфенил)пиридин-3-ил]-N-метилизобутирамид, являются эффективными антагонистами NK-1-индуцированного рефлекса у карликовых песчанок. Фармакокинетические параметры указанных соединений определяли в экспериментах на крысах и собаках. При испытании на крысах 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин 4-ил)-4-ортотолилпиридин-3-ил]-N-метилизобутирамид характеризовался полупериодом выведения 9 ч,клиренсом 4,7 мл/мин/кг, объемом распределения (ред) 4 л/кг и пероральной биодоступностью 10%. При испытании на собаках соединение характеризовалось полупериодом выведения 8 ч, клиренсом 5 мл/мин/кг и объемом распределения 4 л/кг. Аналогичным образом, при испытании на крысах 2-(3,5-бистрифторметилфенил)-N-[6-( 1,1-диоксо-16-тиоморфолин-4-ил)-4-(4-фтор-2-метилфенил)пиридин-3-ил]N-метилизобутирамид характеризовался полупериодом выведения 21 ч, клиренсом 0,3-1,2 мл/мин/кг,объемом распределения 0,7 л/кг и пероральной биодоступностью 61%. При испытании на собаках соединение характеризовалось полупериодом выведения 56 ч, клиренсом 1,4 мл/мин/кг и объемом распределения 1,5 л/кг. Соединения формулы (I), а также их фармацевтически приемлемые кислотно-аддитивные соли можно использовать в качестве лекарственных средств, например, в форме фармацевтических препаратов. Фармацевтичсекие препараты можно вводить пероральным способом, например, в форме таблеток,таблеток в оболочке, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Однако эффективным является также введение ректальным способом, например в форме суппозиториев,или парентеральным способом, например в форме инъекционных растворов. Соединения формулы (I) и их фармацевтически приемлемые кислотно-аддитивные соли можно перерабатывать в смеси с фармацевтически инертными неорганическими или органическими эксципиентами в таблетки, таблетки в оболочке, драже и твердые желатиновые капсулы. В качестве таких эксципи-4 006238 ентов при получении таблеток, драже и твердых желатиновых капсул используются лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.п. Пригодными эксципиентами для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п. Пригодными эксципиентами при получении растворов и сиропов являются вода, полиолы, сахароза, инвертный сахар, глюкоза и т.п. Пригодными эксципиентами для инъекционных растворов являются, например, вода, спирты, полиолы, глицерин, растительные масла и т.п. Пригодными эксципиентами для суппозиториев являются, например, природные или отвержденные масла, воски, жиры, полутвердые или жидкие полиолы и т.п. Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие агенты, эмульгаторы, подсластители, красители, ароматизаторы, соли для изменения осмотического давления, буферные вещества, маскирующие агенты или антиоксиданты. Кроме того, они могут содержать другие фармацевтически ценные вещества. Дозы могут изменяться в широких пределах и должны соответствовать индивидуальным требованиям в каждом конкретном случае. В общем случае при пероральном введении достаточной является суточная доза от приблизительно 10 до 1000 мг соединения формулы (I) на одного пациента, хотя в случае необходимости верхний предел можно превысить. Изобретение иллюстрируется примерами 1 и 2, не ограничивающими его объем. Пример 1. 2-(3,5-Бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)-4-ортотолилпиридин-3-ил]-N-метилизобутирамид. а). 4-(5-Нитропиридин-2-ил)тиоморфолин. К раствору 20 г (126 ммоль) 2-хлор-5-нитропиридина в 200 мл тетрагидрофурана в течение 10 мин по каплям добавляли 32,5 мл (315 ммоль) тиоморфолина и реакционную смесь кипятили с обратным холодильником в течение 2 ч. Затем смесь охлаждали до комнатной температуры, растворитель удаляли в вакууме, остаток растворяли в 200 мл этилацетата. Органическую фазу промывали 200 мл 1 н. раствора бикарбоната натрия, сушили (над сульфатом магния) и упаривали, при этом получали 29,3 г (выход количественный) указанного в заголовке соединения в виде твердого вещества желтого цвета. МС: т/е (%) 225 (М+, 78), 152 (100), 124 (62). б). 2,2-Диметил-N-(6-тиоморфолин-4-илпиридин-3-ил)пропионамид. К суспензии 1,0 г (4,4 ммоль) 4-(5-нитро-2-пиридил)тиоморфолина в 8 мл этанола и 2 мл воды добавляли 1,5 г (27 ммоль) порошка железа, добавляли несколько капель 3 н. раствора НСl в диэтиловом эфире и реакционную смесь нагревали при 85 С в течение 18 ч. Затем суспезию фильтровали, остаток пятикратно порциями по 10 мл промывали этанолом. Фильтрат упаривали в вакууме, при этом получали 870 мг масла пурпурного цвета. Неочищенный продукт растворяли в 10 мл дихлорметана, добавляли при перемешивании 700 мг (6 ммоль) пивалоилхлорида и 860 мг (7 ммоль) N-этилдиизопропиламина и реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем добавляли 30 мл воды и 3 мл 1 н. НСl до рН 1. Органический слой отделяли, водный слой промывали 1 н. НСl, добавляли карбонат натрия до рН 10 и экстрагировали дихлорметаном. Органический слой сушили (над сульфатом натрия) и упаривали, при этом получали 630 мг (51%) указанного в заголовке соединения в виде кристаллов пурпурного цвета. МС: m/е (%) 280 (М+Н+, 100). в). N-(4-Иод-6-тиоморфолин-4-илпиридин-3-ил)-2,2-диметилпропионамид. Раствор 75 г (268 ммоль) 2,2-диметил-N-(6-тиоморфолин-4-илпиридин-3-ил)пропионамида, 187 г(1,61 моль) N,N,N',N'-тетраметилэтилендиамина и 85 г (604 ммоль) 2,2,6,6-тетраметилпиперидина в 750 мл тетрагидрофурана в атмосфере аргона охлаждали в бане с сухим льдом до -65 С и в течение 30 мин по каплям добавляли 805 мл (1,29 моль) 1,6 н. раствора н-бутиллития в гексане. Реакционную смесь нагревали до -15 С и перемешивали при указанной температуре в течение 3 ч. Затем охлаждали до -70 С, в течение 2 ч по каплям добавляли 354 г (1,40 моль) иода (растворенного в 1000 мл тетрагидрофурана) и продолжали перемешивать в течение 1 ч. Суспензию нагревали до -60 С и выливали в 1000 мл 30% раствора пентагидрата тиосульфата натрия. Затем добавляли 750 мл трет-бутилметилового эфира и отделяли органическую фазу. Водный слой трижды порциями по 750 мл экстрагировали трет-бутилметиловым эфиром, объединенные органические слои сушили (над сульфатом натрия) и упаривали. После очистки продукта экспресс-хроматографией получали 68,9 г (63%) указанного в заголовке соединения в виде кристаллов светло-коричневого цвета. МС: m/е (%) 406 (М+Н+, 100). г). 2,2-Диметил-N-(6-тиоморфолин-4-ил-4-ортотолилпиридин-3-ил)пропионамид. Смесь 4,05 г (10,0 ммоль) N-(4-иод-6-тиоморфолин-4-илпиридин-3-ил)-2,2-диметилпропионамида,54 мл толуола, 16 мл 2 н. раствора карбоната натрия, 347 мг (0,3 ммоль) тетракис(трифенилфосфин)палладия(0), 67 мг (0,3 ммоль) ацетата палладия(II) и 1,50 г (11,0 ммоль) ортотолилбороновой кислоты в атмосфере аргона нагревали при 80 С в течение 18 ч. Затем охлаждали до комнатной температуры, водную фазу отделяли и дважды промывали этилацетатом. Объединенные органические слои промывали 50 мл солевого раствора, сушили (над сульфатом натрия) и упаривали. По-5 006238 сле очистки продукта экспресс-хроматографией получали 3,57 г (выход количественный) указанного в заголовке соединения в виде твердого вещества светло-коричневого цвета. МС: m/е (%) 392 (M+Na+, 4),370 (М+Н+, 100). д). 6-Тиоморфолин-4-ил-4-ортотолилпиридин-3-иламин. Суспензию 3,45 г (9,3 ммоль) 2,2-диметил-N-(6-тиоморфолин-4-ил-4-ортотолилпиридин-3-ил) пропионамида в 95 мл 3 н. соляной кислоты в атмосфере аргона нагревали при 110 С в течение ночи. Затем реакционную смесь охлаждали до комнатной температуры, дважды порциями по 100 мл промывали диэтиловым эфиром и фильтровали через целит. Фильтрат разбавляли 20 мл воды и при охлаждении льдом добавляли 28% раствор гидроксида натрия до рН 11. Продукт экстрагировали дихлорметаном(тремя порциями по 100 мл), объединенные органические слои промывали 50 мл солевого раствора, сушили (над сульфатом натрия) и упаривали, при этом получали 2,53 г (95%) указанного в заголовке соединения в виде твердого вещества коричневого цвета. МС: m/е (%) 286 (М+Н+, 100). е). Метил(6-тиоморфолин-4-ил-4-ортотолилпиридин-3-ил)амин. К раствору 2,46 г (8,6 ммоль) 6-тиоморфолин-4-ил-4-ортотолилпиридин-3-иламина в 38 мл тетрагидрофурана добавляли 2,38 г (17 ммоль) карбоната калия (растворенного в 25 мл воды) и 1,03 г (9,5 ммоль) этилхлорформиата, реакционную смесь перемешивали при комнатной температуре в течение 1 ч,а затем выпаривали тетрагидрофуран. Водный слой дважды порциями по 50 мл экстрагировали дихлорметаном, органический слой сушили (над сульфатом натрия) и упаривали в вакууме. Полученное масло растворяли в 30 мл тетрагидрофурана, в течение 30 мин добавляли 7,4 мл (2,6 ммоль) 3,5 М раствора бис(2-метоксиэтокси)алюминийгидрида натрия в толуоле и реакционную смесь перемешивали при 50 С в течение ночи. Затем смесь охлаждали до 0 С и по каплям добавляли 7,5 мл 1 н. раствора гидроксида натрия. Тетрагидрофуран удаляли в вакууме и добавляли 10 мл воды. Водный слой дважды порциями по 20 мл экстрагировали дихлорметаном, объединенные органические слои сушили (над сульфатом натрия) и упаривали. После очистки остатка экспресс-хроматографией получал 2,37 г (92%) указанного в заголовке соединения в виде твердого вещества желтого цвета. МС: m/е (%) 300 (М+Н+, 100). ж). 2-(3,5-Бис-трифторметилфенил)-N-метил-N-(6-тиоморфолин-4-ил-4-ортотолилпиридин-3-ил) изобутирамид. Раствор 2,32 г (7,7 ммоль) метил(6-тиоморфолин-4-ил-4-ортотолилпиридин-3-ил)амина и 1,50 г(11,6 ммоль) N-этилдиизопропиламина в 20 мл тетрагидрофурана охлаждали на ледяной бане и по каплям добавляли 2,72 г (8,5 ммоль) 2-(3,5-бис-трифторметилфенил)-2-метилпропионилхлорида. Реакционную смесь перемешивали при комнатной температуре в течение ночи и упаривали в вакууме. Остаток суспендировали в 200 мл 1 н. раствора карбоната натрия, экстрагировали этилацетатом (тремя порциями по 200 мл), объединенные органические слои сушили (над сульфатом натрия) и упаривали. Остаток кристаллизовали из этанола, при этом получали 3,60 г (80%) указанного в заголовке соединения в виде кристаллов белого цвета. МС: m/е (%) 582 (М+Н+, 100). з). 2-(3,5-Бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)-4-ортотолилпиридин 3-ил]-N-метилизобутирамид. К раствору 1,00 г (1,72 ммоль) 2-(3,5-бис-трифторметилфенил)-N-метил-N-(6-тиоморфолин-4-ил-4 ортотолилпиридин-3-ил)изобутирамида в 10 мл метанола добавляли 1,59 г (2,58 ммоль) OXONE и перемешивали при комнатной температуре в течение 2 сут. Затем к смеси последовательно добавляли 5 мл 38% раствора гидросульфита натрия и 20 мл насыщенного раствора карбоната натрия и метанол удаляли в вакууме. Остаток разбавляли 25 мл воды и экстрагировали дихлорметаном (тремя порциями по 25 мл). Объединенные органические слои сушили (над сульфатом натрия) и упаривали, остаток очищали экспресс-хроматографией и продукт кристаллизовали из этанола, при этом получали 980 мг (93%) указанного в заголовке соединения в виде кристаллов белого цвета. tпл.200-201 С. MC: m/e (%) 636 (M+Na+, 20),614 (М+Н+, 100). Пример 2. 2-(3,5-Бис-трифторметилфенил)-N-[6-(1,1-диоксо-16-тиоморфолин-4-ил)-4-(4-фтор-2 метилфенил)пиридин-3-ил]-N-метилизобутирамид. Указанное в заголовке соединение получали в виде кристаллов белого цвета по методикам и с выходами, описанными выше при получении 2-(3,5-бис-трифторметилфенил)-N-[6-(1,1-диоксо-16 тиоморфолин-4-ил)-4-ортотолилпиридин-3-ил]-N-метилизобутирамида при использовании на стадии г) 4-фтор-2-метилфенилбороновой кислоты вместо ортотолилбороновой кислоты. tпл.162,1-163,6C. Пример А. Таблетки указанного состава получали обычным способом. Ингредиент мг/таблетка Активное соединение 5 Лактоза 45 Кукурузный крахмал 15 Микрокристаллическая целлюлоза 34 Стеарат магния 1 Масса таблетки 100-6 006238 Пример Б. Капсулы указанного состава получали по следующей методике. Ингредиент мг/капсула Активное соединение 10 Лактоза 155 Кукурузный крахмал 30 Тальк 5 Масса наполнителя капсулы 200 Активное соединение, лактозу и кукурузный крахмал сначала смешивали в смесителе, а затем в измельчителе. Затем смесь помещали в смеситель, добавляли тальк и тщательно перемешивали. Полученной смесью заполняли желатиновые капсулы. Пример В. Суппозитории указанного состава получали по следующей методике. Ингредиент мг/суппозиторий Активное соединение 15 Масса суппозитория 1285 Общая масса 1300 Массу суппозитория расплавляли в стеклянном или стальном сосуде, тщательно смешивали и охлаждали до 45 С. К полученной смеси добавляли тонко измельченное активное соединение и перемешивали до полного диспергирования. Затем смесь помещали в формы соответствующего размера, охлаждали, суппозитории извлекали из форм и по отдельности заворачивали в вощеную бумагу или металлическую фольгу. Пример Г. Раствор для инъекции указанного состава получают по обычной методике. Ингредиент Количество Активное соединение 1,0 мг 1 н. НСl 20,0 мкл Уксусная кислота 0,5 мгq.s. до 1 мл ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы где R1 означает водород или фтор; и его фармацевтически приемлемые кислотно-аддитивные соли. 2. Соединение формулы I по п.1, где соединение означает 2-(3,5-бис-трифторметилфенил)-N-[6(1,1-диоксо-16-тиоморфолин-4-ил)-4-ортотолилпиридин-3-ил]-N-метилизобутирамид. 3. Соединение формулы I по п.1, где соединение означает 2-(3,5-бис-трифторметилфенил)-N-[6(1,1-диоксо-16-тиоморфолин-4-ил)-4-(4-фтор-2-метилфенил)пиридин-3-ил]-N-метилизобутирамид. 4. Лекарственное средство, содержащее соединение формулы I по пп.2 и 3 и фармацевтически приемлемые эксципиенты. 5. Лекарственное средство по п.4 для лечения заболеваний, опосредованных рецептором NK-1. 6. Способ получения соединения формулы I по п.1, включающий взаимодействие соединения формулы где R1 означает водород или фтор,и при необходимости превращение полученного соединения в фармацевтически приемлемую кислотно-аддитивную соль. 7. Соединение формулы I по любому из пп.1, 2 или 3, полученное способом по п.6. 8. Применение соединения формулы I по любому из пп.1-3 для лечения заболеваний. 9. Применение соединения формулы I по п.8 для лечения заболеваний, опосредованных рецепторомNK-1. 10. Применение соединения формулы I по любому из пп.1-3 для получения лекарственных средств для лечения заболеваний, опосредованных рецептором NK-1. 11. Применение по п.10 для получения лекарственных средств для лечения мигрени, ревматоидного артрита, астмы, повышенной реактивности бронхов, воспалительного заболевания кишечника или для лечения состояний, включающих болезнь Паркинсона, тревогу, депрессию, боль, головную боль, болезнь Альцгеймера, рассеянный склероз, отек, аллергический ринит, болезнь Крона, глазную травму, воспаления глаз, психоз, укачивание, индуцированную рвоту, рвоту, недержание мочи, психоиммунологические или психосоматические состояния, онкологические заболевания, синдром отмены лекарственных средств от опиоидов до никотина, травму мозга или доброкачественную гиперплазию предстательной железы. 12. Применение по пп.10 и 11 для получения лекарственных средств для лечения депрессии, тревоги или рвоты.
МПК / Метки
МПК: C07D 417/00, A61P 29/00
Метки: фенилпиридин-3-ил]-n-метилизобутирамид, 4-фтор-2-метил, 2-(3,5, бис-трифторметилфенил)-n-[6-(1,1-диоксо-1лямда6-тиоморфолин-4-ил)-4-(2, метил
Код ссылки
<a href="https://eas.patents.su/9-6238-2-35-bis-triftormetilfenil-n-6-11-diokso-1lyamda6-tiomorfolin-4-il-4-2-metil-ili-4-ftor-2-metil-fenilpiridin-3-il-n-metilizobutiramid.html" rel="bookmark" title="База патентов Евразийского Союза">2-(3,5 -бис-трифторметилфенил)-n-[6-(1,1-диоксо-1лямда6-тиоморфолин-4-ил)-4-(2- метил- или 4-фтор-2-метил) фенилпиридин-3-ил]-n-метилизобутирамид</a>
Предыдущий патент: Производные аминоалкилбензоилбензофурана, способ их получения и содержащие их композиции
Следующий патент: Направленные к мишени мультимерные контрастные вещества, основанные на пептидах
Случайный патент: Игровой автомат












