Способ получения замещенного бензолсульфоната 8-арилхинолиния
Номер патента: 5864
Опубликовано: 30.06.2005
Авторы: Леблонд Карл, Десмонд Ричард, Хо Гуо-Дзие, Конлон Дэвид А., Вайлая Анант, Драю Антуанетт, Пайпик Бренда
Формула / Реферат
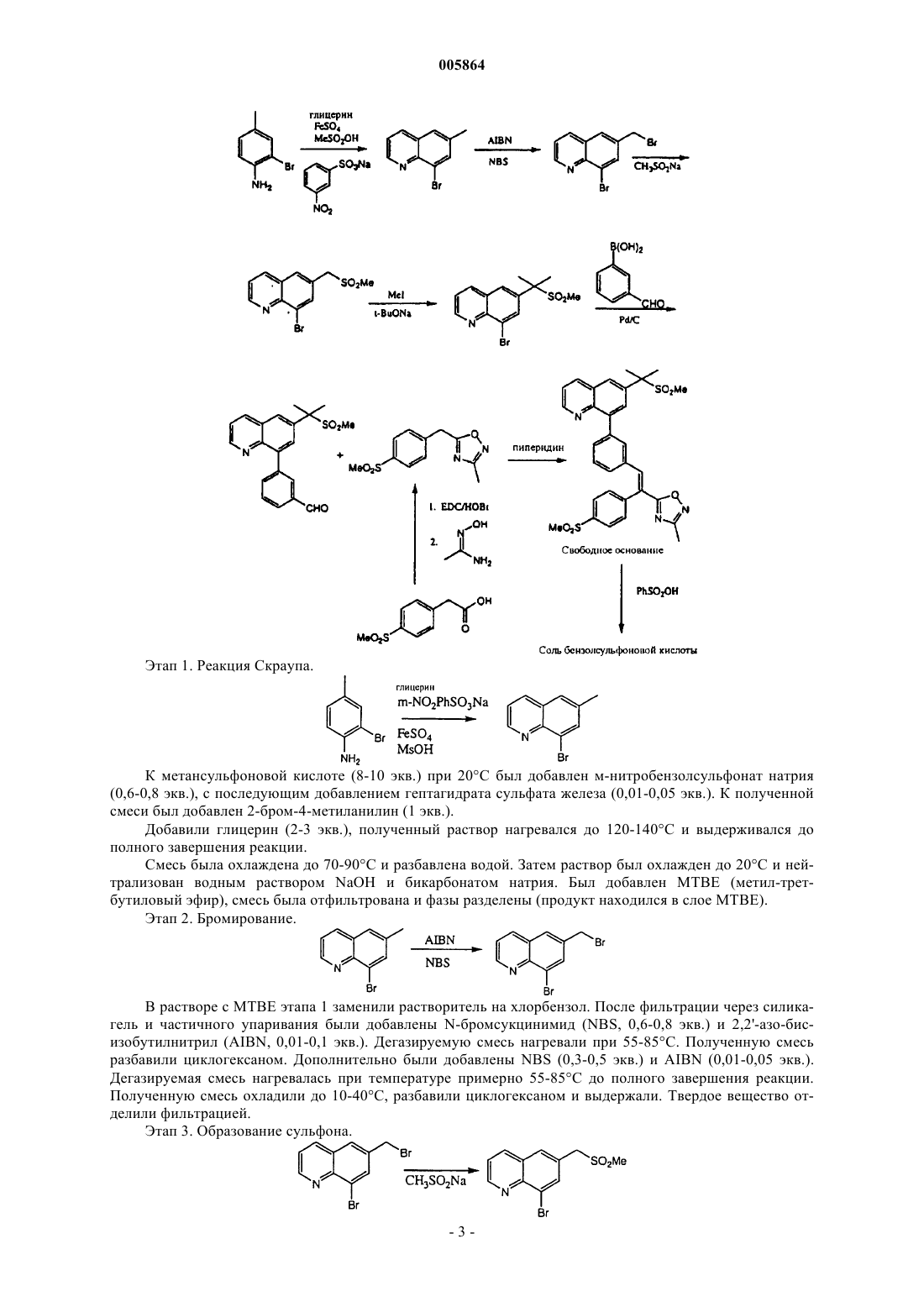
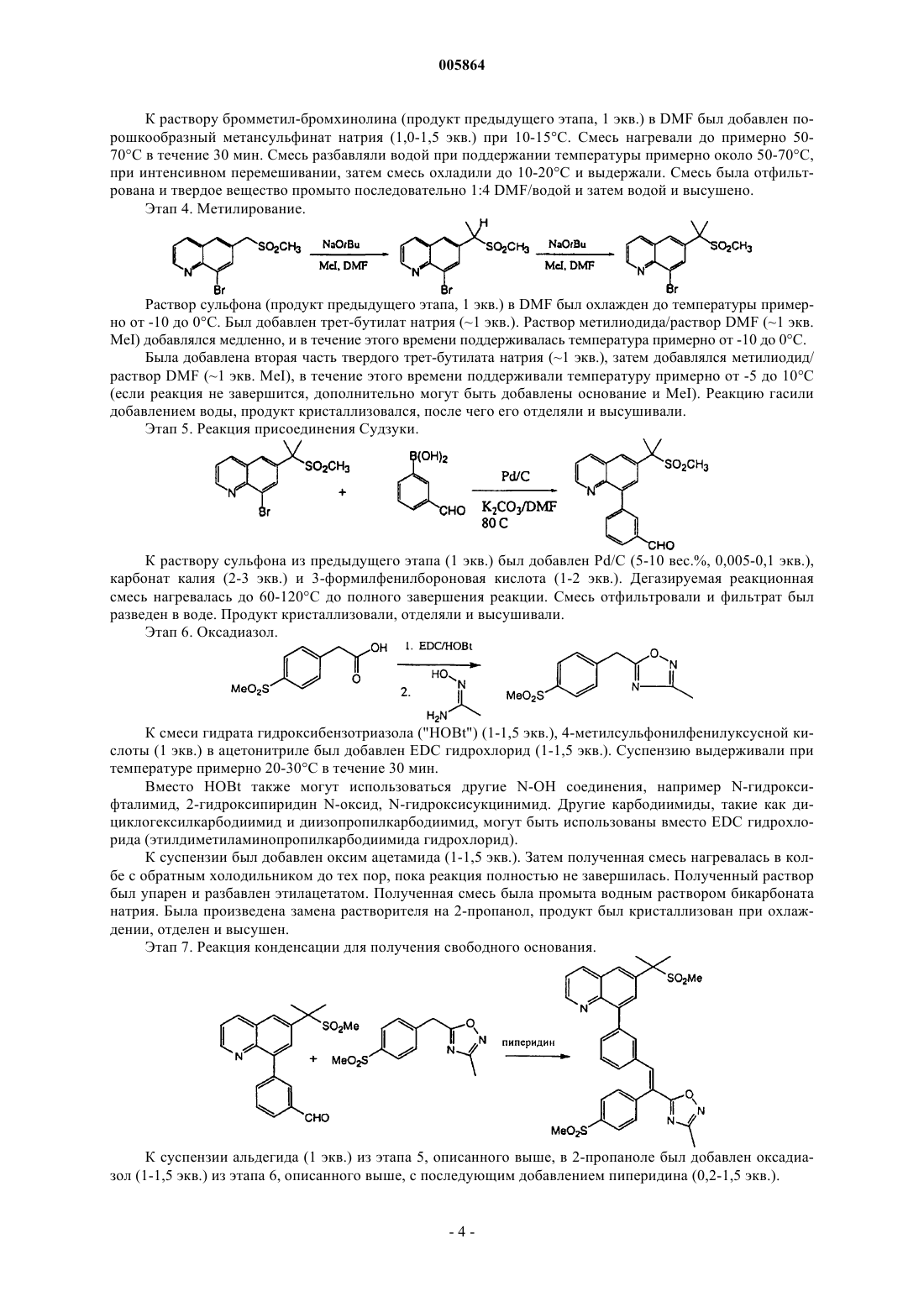
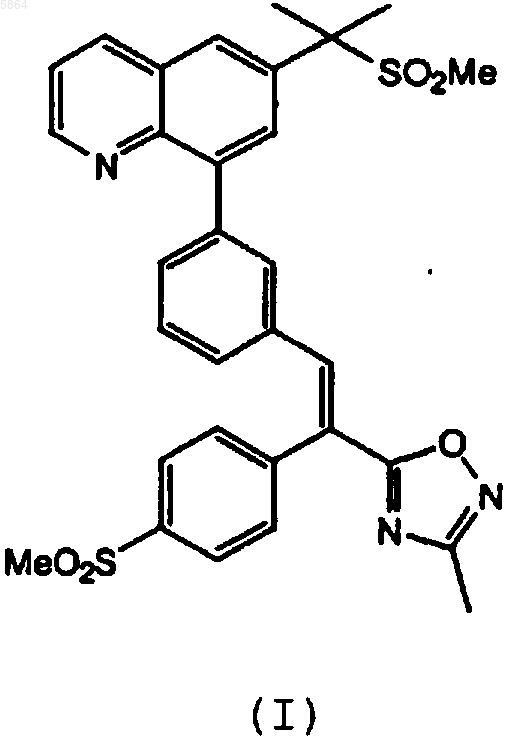
1. Способ получения замещенного 8-арилхинолина формулы I
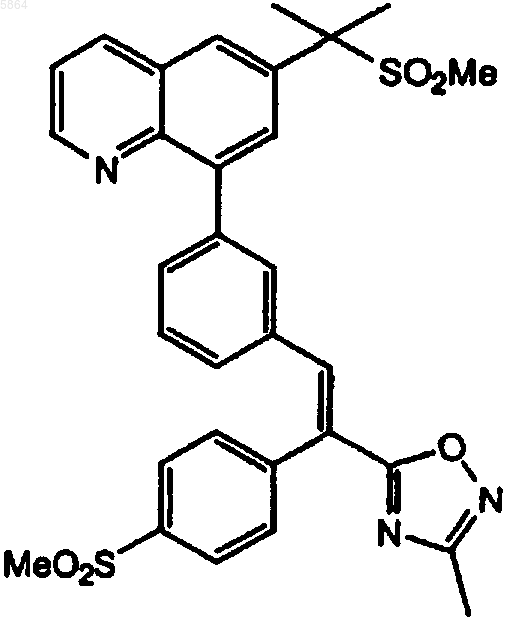
включающий взаимодействие соединения
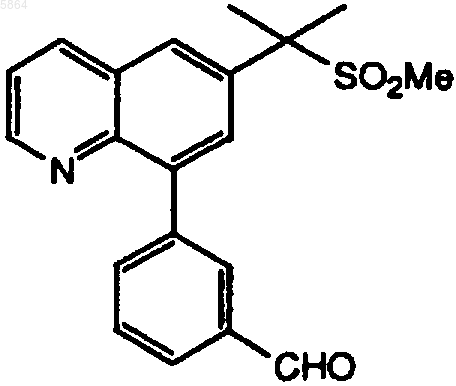
с соединением
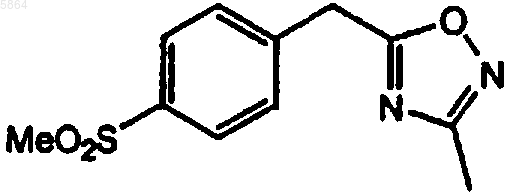
в присутствии основного инициатора.
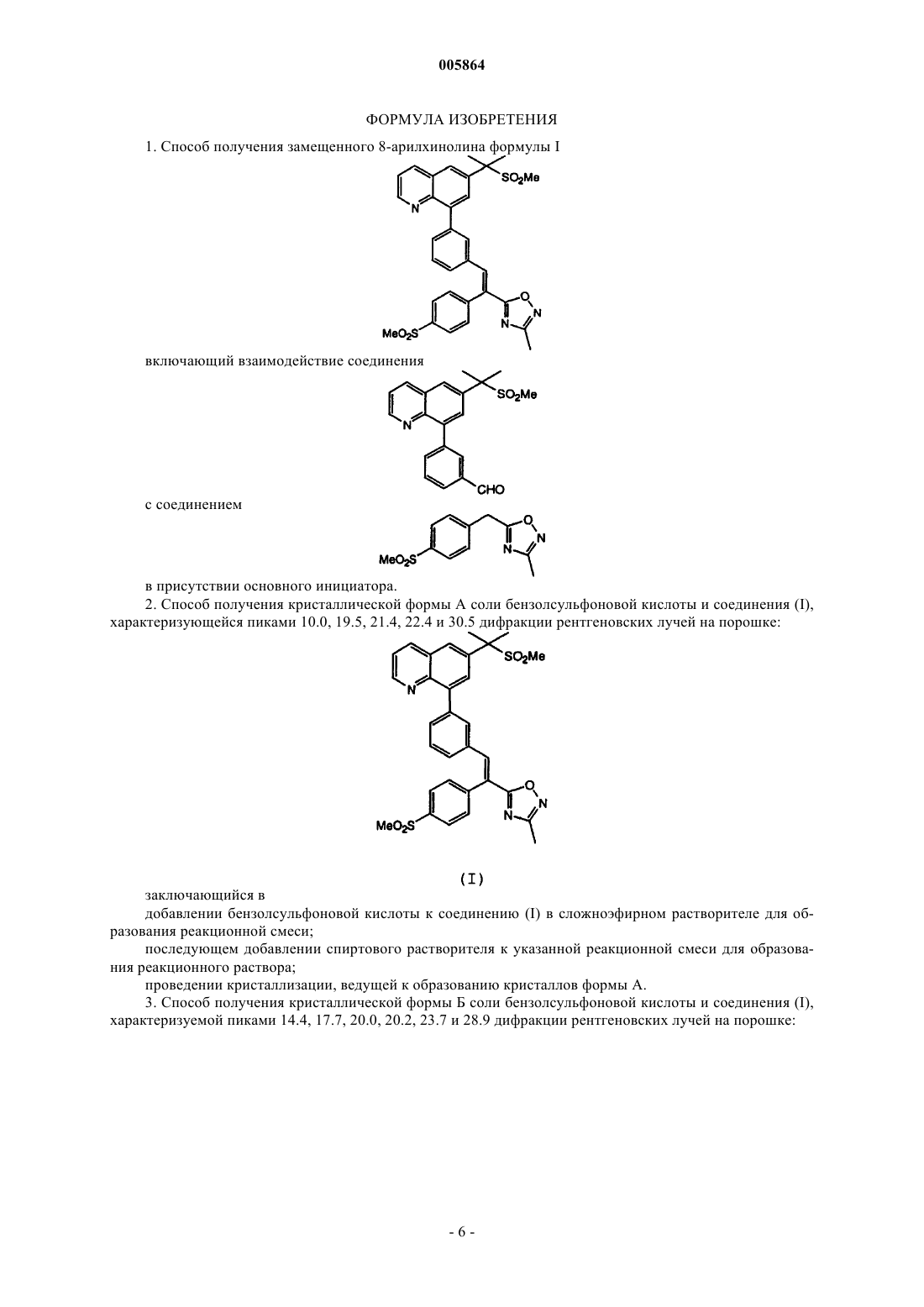
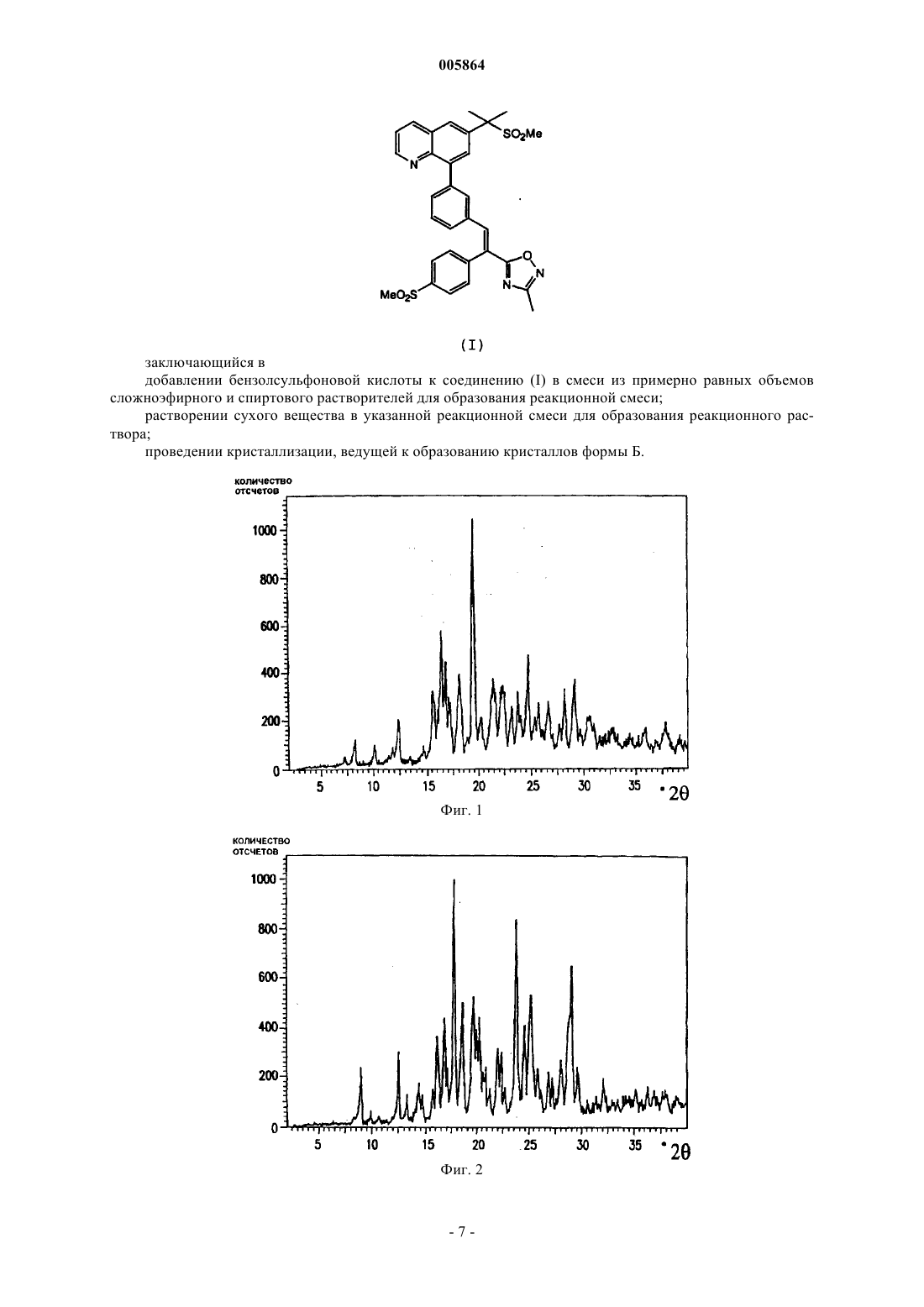
2. Способ получения кристаллической формы А соли бензолсульфоновой кислоты и соединения (I), характеризующейся пиками 10.0, 19.5, 21.4, 22.4 и 30.5 дифракции рентгеновских лучей на порошке

заключающийся в добавлении бензолсульфоновой кислоты к соединению (I) в сложноэфирном растворителе для образования реакционной смеси; последующем добавлении спиртового растворителя к указанной реакционной смеси для образования реакционного раствора; проведении кристаллизации, ведущей к образованию кристаллов формы А.
3. Способ получения кристаллической формы Б соли бензолсульфоновой кислоты и соединения (I), характеризуемой пиками 14.4, 17.7, 20.0, 20.2, 23.7 и 28.9 дифракции рентгеновских лучей на порошке
заключающийся в добавлении бензолсульфоновой кислоты к соединению (I) в смеси из примерно равных объемов сложноэфирного и спиртового растворителей для образования реакционной смеси; растворении сухого вещества в указанной реакционной смеси для образования реакционного раствора; проведении кристаллизации, ведущей к образованию кристаллов формы Б.
Текст
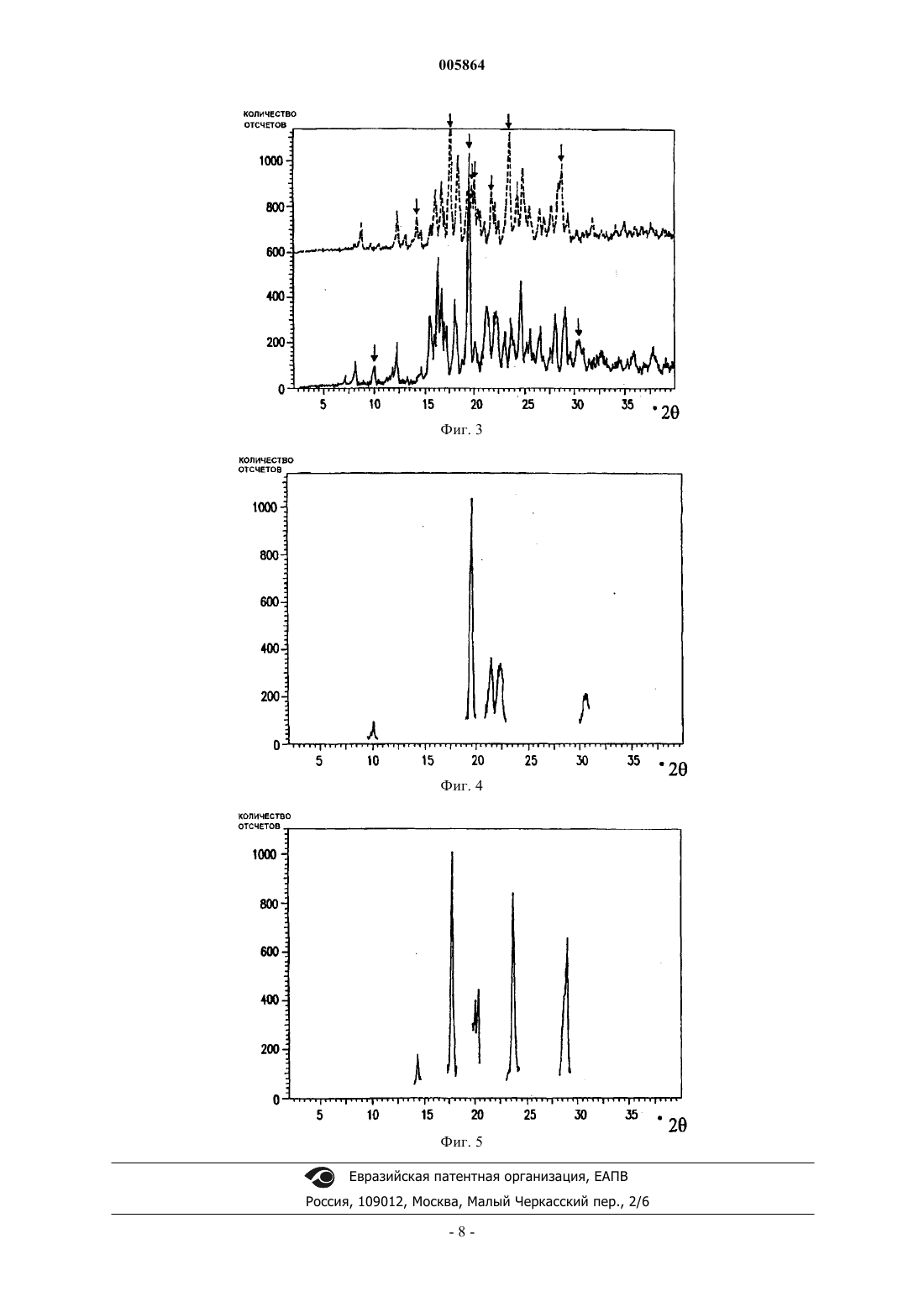
005864 Предпосылки создания изобретения Область, к которой относится изобретение Настоящее изобретение относится к способу получения бензолсульфоновой соли замещенных 8 арилхинолинов. Более точно, данное изобретение относится к способу получения 6-[1-метил-1-(метилсульфонил)этил]-8-[3-[(Е)-2-[3-метил-1,2,4-оксадиазол-5-ил]-2-[4-(метилсульфонил)фенил]этенил]фенил] хинолиния бензолсульфоната, являющегося ингибитором фосфодиэстеразы-4. Основные предпосылки Гормоны представляют собой соединения, различными путями влияющие на клеточную активность. Во многих отношениях, гормоны действуют как мессенджеры, инициирующие определенные клеточные реакции и типы активности. Однако многие действия, производимые гормонами, не являются следствием действия исключительно только гормона. Напротив, первоначально гормоны связываются с рецептором, таким образом, инициируя освобождение вторичного соединения, которое затем воздействует на клеточную активность. В такой схеме гормон известен как первичный мессенджер, в то время как вторичное вещество называется вторичным мессенджером. Циклический аденозинмонофосфат (аденозин 3',5'-цикломонофосфат, "цАМФ" или "циклический АМФ") известен в качестве вторичного мессенджера гормонов, включающих адреналин, глюкагон, кальцитонин, кортикотропин, липотропин, лютеинизирующий гормон, норэпинефрин (норадреналин), паратиреоидный гормон, тиреотропный гормон и вазопрессин. Таким образом, цАМФ является посредником клеточного ответа на действие гормонов. Циклический АМФ также медиирует клеточный ответ на различные нейромедиаторы. Фосфодиэстеразы ("ФДЭ") являются семейством ферментов, которые в ходе обмена преобразуют 3',5'-циклические нуклеотиды в 5'-нуклеозидмонофосфаты, таким образом, подавляя активность цАМФ как вторичного мессенджера. Вызывают существенный интерес такие ФДЭ, как фосфодиэстераза-4("ФДЭ 4", также известная как "ФДЭIV"), обладающая высоким сродством, цАМФ специфическая, ФДЭ типа IV, в качестве потенциальной мишени для разработки новых антиастматических и противовоспалительных соединений. Известно, по меньшей мере, существование четырех изоэнзимов ФДЭ 4, каждый из которых кодируется отдельным геном. Предполагается, что каждый из этих четырех известных продуктов гена ФДЭ 4 играет разные роли в аллергических и/или воспалительных реакциях. Таким образом,считается, что ингибирование ФДЭ 4, и в особенности специфических изоформ ФДЭ 4, вызывающих нежелательные реакции, может благотворно воздействовать на аллергию и воспалительные симптомы. Было бы желательно обеспечить новые вещества и соединения, подавляющие активность ФДЭ 4. Вещества, подавляющие активность ФДЭ 4, являются пригодными для лечения млекопитающих,например, в случаях астмы, хронических бронхитов, хронической обструктивной болезни легких(ХОБЛ), эозинофильной гранулемы, псориаза и других доброкачественных или злокачественных пролиферативных кожных заболеваний, эндотоксического токсического шока (и связанных состояний, таких как ламиниты и колики у лошадей), септического шока, неспецифических язвенных колитов, болезни Крона, реперфузионных повреждений миокарда и головного мозга, воспалительных артритов, остеопороза, хронических гломерулонефритов, атопических дерматитов, крапивницы, респираторного дистресссиндрома взрослых, респираторного дистресс-синдрома младенцев, хронической обструктивной болезни легких (ХОБЛ) у животных, несахарного диабета, аллергического ринита, аллергического конъюнктивита, весеннего конъюнктивита, артериального рестиноза, атеросклероза, нейрогенного воспаления, боли,кашля, ревматического артрита, анкилозирующего спондилоартрита, отторжения трансплантата и реакции "трансплантат против хозяина", повышенной секреции желудочного сока, сепсиса или септического шока, индуцированного бактериями, грибком или вирусом, воспаления и цитокин-опосредованной хронической дегенерации ткани, остеоартритов, карциномы, кахексии, гипотрофии мышц, депрессии, нарушения памяти, монополярной депрессии, острого и хронического нейродегенеративного расстройства с воспалительным компонентом, болезни Паркинсона, болезни Альцгеймера, спинно-мозговой травмы,повреждения головы, рассеянного склероза, роста новообразований и злокачественной инвазии нормальных тканей. Основную озабоченность при использовании ингибиторов ФДЭ 4 вызывает побочный эффект в виде рвоты, который наблюдается в случае некоторых веществ-кандидатов, как это описано в С.Med. Chem., 41:821-835 (1998), Burnouf также описал широкий разброс по тяжести нежелательных побочных действий, проявляемых различными соединениями. Как показано в M.D. Houslay et al., Adv. InPharmacol., 44:33-89 (1998), and D. Spina et al., Adv. In Pharmacol., 44:33-89 (1998), существует большой интерес и проводятся интенсивные исследования в отношении терапии с помощью ингибиторов ФДЭ 4. Международная патентная заявка WO9422852 описывает хинолины как ингибиторы ФДЭ 4. А.Н. Cook, et al., J. Chem. Soc., 413-417 (1943) описывает -пиридилхинолины. Другие соединения хинолинов описаны у Kei Manabe et al., J. Org. Chem., 58 (24):6692-6700 (1993); Kei Manabe et al., J. Am.Chem. Soc., 115(12):5324-5325 (1993); и Kei Manabe et al., J. Am. Chem. Soc., 114 (17):6940-6941 (1992). Различными исследователями описаны соединения, включающие кольцевые системы, как эффективные в ряде случаев терапии. Например, международная патентная заявка WO98/25883 описывает кетобензамиды в качестве ингибиторов калпаина, европейская патентная заявка ЕР 811610 и патентные-1 005864 заявки США 5,679,712, 5,693,672 и 5,747,541 описывают замещенный бензоилгуанидин как блокатор натриевых каналов, патентная заявка США 5,736,297 описывает кольцевые системы, используемые в качестве фоточувствительных составов. Патентные заявки США 5,491,147, 5,608,070, 5,622,977, 5,739,144, 5,776,958, 5,780,477, 5,786,354,5,798,373, 5,849,770, 5,859,034, 5,866,593, 5,891,896 и международная патентная заявка WО 95/35283 описывают ингибиторы ФДЭ 4, являющиеся тризамещенными арил- или гетероарилфенилпроизводными. Патентная заявка США 5,580,888 описывает ингибиторы ФДЭ 4, которые являются стирилпроизводными. Патентная заявка США 5,550,137 описывает ингибиторы ФДЭ 4, являющиеся фениламинокарбонилпроизводными. Патентная заявка США 5,340,827 описывает ингибиторы ФДЭ 4, представляющие собой соединения фенилкарбоксамидов. Патентная заявка США 5,780,478 описывает ингибиторы ФДЭ 4, являющиеся тетразамещенными фенилпроизводными. Международная патентная заявка WO96/00215 описывает производные замещенных оксимов, которые используются в качестве ингибиторов ФДЭ 4. Патентная заявка США 5,633,257 описывает ингибиторы ФДЭ 4, которые являются цикло(алкил и алкенил)фенилалкенил(арил и гетероарил)-соединениями. Однако сохраняется потребность в новых веществах и соединениях, которые с минимальным побочным действием терапевтически ингибируют ФДЭ 4. Кроме того, остается необходимость в эффективных способах производства соединений, терапевтически ингибирующих ФДЭ 4. Краткое изложение сущности изобретения Настоящее изобретение относится к способу синтеза 6-[1-метил-1-(метилсульфонил)этил]-8-[3-[(Е)2-[3-метил-1,2,4-оксадиазол-5-ил]-2-[4-(метилсульфонил)фенил]этенил]фенил]хинолина и его бензолсульфонатной соли. Краткое описание чертежей Фиг. 1 - диаграмма зависимости количества отсчетов отпри дифракции Х-лучей на порошке полиморфа формы А соли бензолсульфоновой кислоты (БСК) и 6-[1-метил-1-(метилсульфонил)этил]-8-[3[(Е)-2-[3-метил-1,2,4-оксадиазол-5-ил]-2-[4-(метилсульфонил)фенил]этенил]фенил]хинолина. Фиг. 2 - диаграмма зависимости количества отсчетов отпри дифракции Х-лучей на порошке полиморфа формы Б соли БСК и 6-[1-метил-1-(метилсульфонил)этил]-8-[3-[(Е)-2-[3-метил-1,2,4 оксадиазол-5-ил]-2-[4-(метилсульфонил)фенил]этенил]фенил]хинолина. Фиг. 3 - сравнение дифракции Х-лучей на порошке полиморфа формы А (нижняя линия) и формы Б(верхняя линия) соли БСК и 6-[1-метил-1-(метилсульфонил)этил]-8-[3-[(Е)-2-[3-метил-1,2,4-оксадиазол 5-ил]-2-[4-(метилсульфонил)фенил]этенил]фенил]хинолина. Фиг. 4 - диаграмма характерных пиков дифракции Х-лучей на порошке полиморфа формы А соли БСК и 6-[1-метил-1-(метилсульфонил)этил]-8-[3-[(Е)-2-[3-метил-1,2,4-оксадиазол-5-ил]-2-[4-(метилсульфонил)фенил]этенил]фенил]хинолина. Фиг. 5 - диаграмма характерных пиков дифракции Х-лучей на порошке полиморфа формы Б соли БСК и 6-[1-метил-1-(метилсульфонил)этил]-8-[3-[(Е)-2-[3-метил-1,2,4-оксадиазол-5-ил]-2-[4-(метилсульфонил)фенил]этенил]фенил]хинолина. Подробное описание изобретения В соответствии с настоящим изобретением получают соединение ("свободное основание")(0,6-0,8 экв.), с последующим добавлением гептагидрата сульфата железа (0,01-0,05 экв.). К полученной смеси был добавлен 2-бром-4-метиланилин (1 экв.). Добавили глицерин (2-3 экв.), полученный раствор нагревался до 120-140 С и выдерживался до полного завершения реакции. Смесь была охлаждена до 70-90 С и разбавлена водой. Затем раствор был охлажден до 20 С и нейтрализован водным раствором NaOH и бикарбонатом натрия. Был добавлен МТВЕ (метил-третбутиловый эфир), смесь была отфильтрована и фазы разделены (продукт находился в слое МТВЕ). Этап 2. Бромирование. В растворе с МТВЕ этапа 1 заменили растворитель на хлорбензол. После фильтрации через силикагель и частичного упаривания были добавлены N-бромсукцинимид (NBS, 0,6-0,8 экв.) и 2,2'-азо-бисизобутилнитрил (AIBN, 0,01-0,1 экв.). Дегазируемую смесь нагревали при 55-85 С. Полученную смесь разбавили циклогексаном. Дополнительно были добавлены NBS (0,3-0,5 экв.) и AIBN (0,01-0,05 экв.). Дегазируемая смесь нагревалась при температуре примерно 55-85 С до полного завершения реакции. Полученную смесь охладили до 10-40 С, разбавили циклогексаном и выдержали. Твердое вещество отделили фильтрацией. Этап 3. Образование сульфона.-3 005864 К раствору бромметил-бромхинолина (продукт предыдущего этапа, 1 экв.) в DMF был добавлен порошкообразный метансульфинат натрия (1,0-1,5 экв.) при 10-15 С. Смесь нагревали до примерно 5070 С в течение 30 мин. Смесь разбавляли водой при поддержании температуры примерно около 50-70 С,при интенсивном перемешивании, затем смесь охладили до 10-20 С и выдержали. Смесь была отфильтрована и твердое вещество промыто последовательно 1:4 DMF/водой и затем водой и высушено. Этап 4. Метилирование. Раствор сульфона (продукт предыдущего этапа, 1 экв.) в DMF был охлажден до температуры примерно от -10 до 0 С. Был добавлен трет-бутилат натрия (1 экв.). Раствор метилиодида/раствор DMF (1 экв. МеI) добавлялся медленно, и в течение этого времени поддерживалась температура примерно от -10 до 0 С. Была добавлена вторая часть твердого трет-бутилата натрия (1 экв.), затем добавлялся метилиодид/ раствор DMF (1 экв. МеI), в течение этого времени поддерживали температуру примерно от -5 до 10 С(если реакция не завершится, дополнительно могут быть добавлены основание и МеI). Реакцию гасили добавлением воды, продукт кристаллизовался, после чего его отделяли и высушивали. Этап 5. Реакция присоединения Судзуки. К раствору сульфона из предыдущего этапа (1 экв.) был добавлен Pd/C (5-10 вес.%, 0,005-0,1 экв.),карбонат калия (2-3 экв.) и 3-формилфенилбороновая кислота (1-2 экв.). Дегазируемая реакционная смесь нагревалась до 60-120 С до полного завершения реакции. Смесь отфильтровали и фильтрат был разведен в воде. Продукт кристаллизовали, отделяли и высушивали. Этап 6. Оксадиазол. К смеси гидрата гидроксибензотриазола ("HOBt") (1-1,5 экв.), 4-метилсульфонилфенилуксусной кислоты (1 экв.) в ацетонитриле был добавлен EDC гидрохлорид (1-1,5 экв.). Суспензию выдерживали при температуре примерно 20-30 С в течение 30 мин. Вместо HOBt также могут использоваться другие N-OH соединения, например N-гидроксифталимид, 2-гидроксипиридин N-оксид, N-гидроксисукцинимид. Другие карбодиимиды, такие как дициклогексилкарбодиимид и диизопропилкарбодиимид, могут быть использованы вместо EDC гидрохлорида (этилдиметиламинопропилкарбодиимида гидрохлорид). К суспензии был добавлен оксим ацетамида (1-1,5 экв.). Затем полученная смесь нагревалась в колбе с обратным холодильником до тех пор, пока реакция полностью не завершилась. Полученный раствор был упарен и разбавлен этилацетатом. Полученная смесь была промыта водным раствором бикарбоната натрия. Была произведена замена растворителя на 2-пропанол, продукт был кристаллизован при охлаждении, отделен и высушен. Этап 7. Реакция конденсации для получения свободного основания. К суспензии альдегида (1 экв.) из этапа 5, описанного выше, в 2-пропаноле был добавлен оксадиазол (1-1,5 экв.) из этапа 6, описанного выше, с последующим добавлением пиперидина (0,2-1,5 экв.).-4 005864 Вместо 2-пропанола, могут быть использованы другие растворители, например DMF, ацетонитрил,1-пропанол, толуол, сложные эфиры и другие спирты. Пиперидин служит в качестве основного инициатора. Вместо пиперидина могут быть использованы другие основные амины, особенно вторичные амины. Полученная смесь нагревалась в колбе с обратным холодильником над молекулярными ситами до полного завершения реакции. Затем охлажденный продукт был отделен фильтрацией и высушен. Соль свободного основания и бензолсульфоновой кислоты (БСК) существует в двух кристаллических формах ("форма А" и "форма Б"). Формы были синтезированы следующими способами. Этап 8. Образование соли. Форма А К суспензии свободного основания (1 экв.) из этапа 7, описанного выше, в этилацетате была добавлена бензолсульфокислота (1-1,2 экв.). Вместо этилацетата, могут быть использованы другие сложные эфиры. Был добавлен метанол и полученную смесь нагревали до полного растворения твердого вещества. Вместо метанола могут быть использованы другие спирты, такие как этанол или пропанол. Полученный раствор отфильтровали и упарили. Во время упаривания продукт кристаллизовался. Полученная смесь была разбавлена этилацетатом и выдержана. Желтое твердое вещество было собрано путем фильтрации. ВЭЖХ (высокоэффективная жидкостная хроматография) показала молярное соотношение 1:1 6-[1-метил-1-(метилсульфонил)этил]-8-[3-[(Е)-2-[3-метил-1,2,4-оксадиазол-5-ил]-2-[4-(метилсульфонил)фенил]этенил]фенил]хинолина и бензолсульфоновой кислоты. Точка плавления по ДСК (дифференциальной сканирующей калориметрии): 193 С. Спектрограмма дифракции рентгеновских лучей на порошке ("ДРЛП") для формы А приведена на фиг. 1. Идентифицирующие пики сведены в таблицу ниже и показаны на фиг. 4. Пики, идентифицирующие полиморф формы А (2) 10,0 19,5 21,4 22,4 30,5 Форма Б К суспензии свободного основания (1 экв.) из этапа 7, описанного выше, в смеси изопропилацетата(i-PrOAc) и метанола (1:1) была добавлена БСК (1-1,2 экв.). Вместо i-PrOAc, могут быть использованы другие сложные эфиры, и вместо метанола могут быть использованы другие спирты, такие как этанол или пропанол. Смесь выдерживали при 20-50 С до полного растворения твердого вещества. Полученную смесь фильтровали и перегоняли, в течение этого времени поддерживался объем путем добавления 9:1(об./об.) смеси i-PrOAc /метанол. Продукт кристаллизовался во время перегонки. Полученную смесь выдерживали при 20-70 С в течение 2-10 ч до обеспечения завершения образования формы Б. Полученное беловатое твердое вещество было выделено путем фильтрации и высушено. ВЭЖХ показала 1:1 молярное соотношение 6-[1-метил-1-(метилсульфонил)этил]-8-[3-[(Е)-2-[3 метил-1,2,4-оксадиазол-5-ил]-2-[4-(метилсульфонил)фенил]этенил]фенил]хинолина и БСК. Точка плавления по ДСК: 210 С. Спектрограмма дифракции рентгеновских лучей на порошке ("ДРЛП") для формы Б показана на фиг. 2. Идентифицирующие пики сведены в таблицу ниже и показаны на фиг. 5. На фиг. 3 спектры сравниваются с идентифицирующими пиками, указанными стрелками. Пики, идентифицирующие полиморф формы Б (2) 14,4 17,7 20,0 20,2 23,7 28,9-5 005864 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения замещенного 8-арилхинолина формулы I в присутствии основного инициатора. 2. Способ получения кристаллической формы А соли бензолсульфоновой кислоты и соединения (I),характеризующейся пиками 10.0, 19.5, 21.4, 22.4 и 30.5 дифракции рентгеновских лучей на порошке: заключающийся в добавлении бензолсульфоновой кислоты к соединению (I) в сложноэфирном растворителе для образования реакционной смеси; последующем добавлении спиртового растворителя к указанной реакционной смеси для образования реакционного раствора; проведении кристаллизации, ведущей к образованию кристаллов формы А. 3. Способ получения кристаллической формы Б соли бензолсульфоновой кислоты и соединения (I),характеризуемой пиками 14.4, 17.7, 20.0, 20.2, 23.7 и 28.9 дифракции рентгеновских лучей на порошке: заключающийся в добавлении бензолсульфоновой кислоты к соединению (I) в смеси из примерно равных объемов сложноэфирного и спиртового растворителей для образования реакционной смеси; растворении сухого вещества в указанной реакционной смеси для образования реакционного раствора; проведении кристаллизации, ведущей к образованию кристаллов формы Б.
МПК / Метки
МПК: C07D 413/10
Метки: замещенного, способ, 8-арилхинолиния, бензолсульфоната, получения
Код ссылки
<a href="https://eas.patents.su/9-5864-sposob-polucheniya-zameshhennogo-benzolsulfonata-8-arilhinoliniya.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения замещенного бензолсульфоната 8-арилхинолиния</a>
Предыдущий патент: Композиции мезотриона
Следующий патент: Аналог фрагмента эпидермального фактора роста, его конъюгат с доксорубицином и фармацевтическая композиция на основе конъюгата
Случайный патент: Сбалансированный инфузионный раствор