Способ получения 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1н-индола
Формула / Реферат
1. Способ получения 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1H-индола формулы (1)

отличающийся тем, что он включает:
а) проведение реакции 2-бром-4'-бензилоксипропиофенона формулы (8) с пара-бензилоксианилина гидрохлоридом формулы (9)
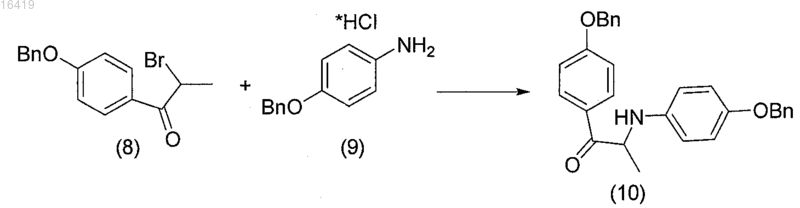
в среде органического растворителя и в присутствии неорганического или органического основания;
б) выделение промежуточного соединения N-(4-бензилоксифенил)-α-амино-4-бензилоксипропиофенона формулы (10) в твердом состоянии;
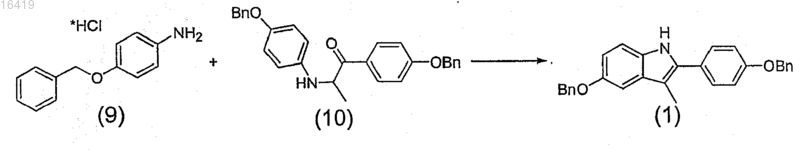
в) получение 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1Н-индол формулы (1) циклизацией N-(4-бензилооксифенил)-α-амино-4-бензилоксипропиофенона формулы (10) действием пара-бензилоксианилина гидрохлорида формулы (9) в среде органического растворителя из группы спиртов С1-С4, толуола, ацетона и метилтетрагидрофурана
2. Способ по п.1, отличающийся тем, что реакцию проводят в среде органического растворителя из группы С1-С4 спиртов, толуола, ацетона, метилтетрагидрофурана и в присутствии неорганического или органического основания из группы, включающей карбонат натрия, карбонат калия, триэтиламин, диизопропилэтиламин.
3. Способ по п.2, отличающийся тем, что в качестве растворителя применяют этанол, а в качестве основания применяют триэтиламин.
4. Способ по любому из пп.1, 2, отличающийся тем, что реакцию проводят при кипячении с обратным холодильником.
5. Способ по любому из пп.1-4, отличающийся тем, что промежуточное соединение N-(4-бензилоксифенил)-α-амино-4-бензилоксипропиофенон дополнительно очищают кристаллизацией из органического растворителя, который выбран из группы жидких C1-C15 алифатических, алициклических или ароматических углеводородов или их окисленных или азотсодержащих производных или их смесей.
6. Способ по п.5, отличающийся тем, что для кристаллизации промежуточного соединения применяют смесь полярного и неполярного растворителя, такую как смеси этил ацетат-этанол, толуол-метанол, ТГФ (тетрагидрофуран)-метанол.
7. Способ по п.1, отличающийся тем, что пара-бензилоксианилина гидрохлорид формулы (9) применяют в молярном соотношении от 1:20 до 1:1, предпочтительно 1:5 по отношению к соединению формулы (10).
8. Способ по п.1 или 7, отличающийся тем, что реакцию проводят в автоклаве в инертной атмосфере при повышенной температуре 100-120°С.
9. Способ по пп.1, 7 или 8, отличающийся тем, что применяют органический растворитель из группы C1-C4 спиртов, предпочтительно этанол.
10. Кристаллический N-(4-бензилоксифенил)-α-амино-4-бензилоксипропиофенон формулы (10).
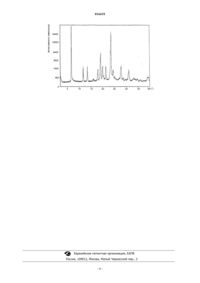
11. Вещество по п.10, отличающееся тем, что имеет следующие значения характеристических углов дифракции 2θ на профиле порошковой рентгеновской дифрактометрии: 6,71; 19,00; 19,13; 23,49; 23,63.
12. Применение N-(4-бензилоксифенил)-α-амино-4-бензилоксипропиофенона формулы (10) для получения 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1H-индола формулы (1).
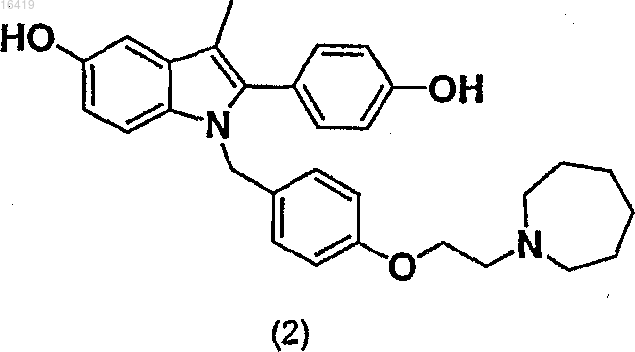
13. Применение N-(4-бензилоксифенил)-α-амино-4-бензилоксипропиофенона формулы (10) для получения 2-(4-гидроксифенил)-1-[4-(2-азепан-1-илэтокси)бензил]-3-метил-1Н-индол-5-ола (базедоксифена) формулы (2).
Текст
Способ получения 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1 Н-индола формулы (1) путем реакции 2-бром-4'-бензилоксипропиофенона и 4-бензилоксианилина гидрохлорида, при котором высокой чистоты продукта достигают путем выделения промежуточного соединения N(4-бензилоксифенил)амино-4-бензилоксипропиофенона формулы (10) в твердом состоянии. Способ применим для получения базедоксифена формулы (2). 016419 Область техники Изобретение относится к новому способу получения 5-бензилокси-2-(4-бензилоксифенил)-3-метил 1 Н-индола формулы (1) применяемого для получения 2-(4-гидроксифенил)-1-[4-(2-азепан-1-илэтокси)бензил]-3-метил-1 Н-индол 5-ола (базедоксифена) формулы (2) Базедоксифен является агонистом эстрогена; он применяется в гормональной заместительной терапии для предупреждения потери костной ткани, замещения эстрогена и профилактики заболеваний сердца и вен у женщин в постменопаузной фазе. Предшествующий уровень техники Из литературы известны два аналогичных способа получения базидоксифена - см. схему 1. Эти способы различаются защитными группами (PG - метил, бензил), способом получения и связывания цепи с азотом в индольном гетероцикле и способом удаления защитной группы. Схема 1 5-Метокси-2-(4-метоксифенил)-3-метил-1 Н-индол формулы (3 а) получали способом Бишера (J. Общий выход двухстадийного синтеза составляет 22%. 5-Бензилокси-2-(4-бензилоксифенил)-3-метил-1 Н-индол формулы (1) также получали способом Бишера из 2-бром-4'-бензилоксипропиофенона формулы (8) и 4-бензилоксианилина гидрохлорида формулы (9) в N,N-диметилформамиде (ЕР 0802183). 2-Бром-4'-бензилоксипропиофенон формулы (8) получают бромированием 4-бензилоксипропиофенона формулы (7) бромом в уксусной кислоте. Общий выход двухстадийного синтеза (см. схему 3) составляет 47%. Схема 3 В WO 99/19293 упоминается выполнение второй стадии в толуоле при кипячении с обратным холо-1 016419 дильником с N,N-диизопропилэтиламином, однако без каких-либо дополнительных подробностей в примерах или литературных ссылках. Проверочные синтезы показали, что применение вышеописанных способов не позволяет получать соединения формулы (1) с достаточно высоким выходом и особенно с достаточной чистотой. При воспроизведении способа согласно патенту ЕР 802183 (схема 4) было обнаружено, что в течение этого синтеза образуются значительные количества нежелательных веществ. Схема 4 Выделение соединения формулы (1), полученного этим способом, значительно затруднено, а при его очистке значительно уменьшается выход. При проведении реакции в соответствии с заявкой на патент WO 99/19293, в которой описывается получение соединения формулы (1) в среде толуола и N,N-диизопропилэтиламина с одновременным удалением воды азеотропной отгонкой, было обнаружено, что проведение реакции занимает несколько десятков часов. В течение этого времени уже образуется значительное количество вторичных веществ, что уменьшает выход и ухудшает качество продукта. По этой причине была предпринята попытка найти более эффективный путь синтеза, результатом чего явился новый способ получения 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1H-индола формулы 1, что и составляет предмет настоящего изобретения. Описание изобретения Изобретение относится к новому способу получения 5-бензилокси-2-(4-бензилоксифенил)-3-метил 1 Н-индола формулы 1, который основан на выделении промежуточного соединения N-(4 бензилоксифенил)амино-4-бензилоксипропиофенона формулы (10). Это промежуточное соединение предпочтительно получают реакцией 4-бензилоксианилина или его соли с соединением формулы (11) где LG представляет собой уходящую группу, например, Cl, Br, I, алкилсульфонил или арилсульфонил. Способ получения включает: а) реакцию 2-бром-4'-бензилоксипропиофенона формулы (8) с пара-бензилоксианилина гидрохлоридом формулы (9), причем реакцию проводят в среде органического растворителя из группы C1-C4 спиртов, толуола, ацетона, метилтетрагидрофурана и в присутствии неорганического или органического основания из группы, включающей карбонат натрия, карбонат калия, диизопропилэтиламин (ДИПЭА) и триэтиламин; Схема 5c) циклизацию N-(4-бензилоксифенил)амино-4-бензилоксипропиофенона формулы (10) реакцией с пара-бензилоксианилина гидрохлоридом формулы (9) в среде пригодного органического растворителя из группы С 1-С 4 спиртов, толуола, ацетона, метилтетрагидрофурана с получением 5-бензилокси-2(4-бензилоксифенил)-3-метил-1H-индола формулы (1) в твердой фазе. Схема 6 Было обнаружено, что выгодно проводить синтез 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1Hиндола формулы (1) в две стадии с выделением промежуточного соединения формулы (10) в соответст-2 016419 вии со схемой 7. Схема 7 На первой стадии исходные соединения (8) и (9) реагируют в среде органического растворителя из группы С 1-С 4 спиртов, толуола, кетонов, метилтетрагидрофурана, предпочтительно этанола, и неорганического или органического основания из группы, включающей карбонат натрия, триэтиламин и ДИПЭА,предпочтительно триэтиламин, при температуре кипения в течение 4-6 ч. В этих условиях через несколько часов образуется суспензия промежуточного соединения 10 и возможно неорганических солей (соответствующих использованному основанию). Промежуточное соединение выделяют фильтрованием. Выход продукта составляет от 81 до 100%. Продукт можно перекристаллизовать растворением в смеси полярного и неполярного растворителя(этилацетат-этанол, толуол-метанол, ТГФ (тетрагидрофуран)метанол). На второй стадии N-(4-бензилоксифенил)амино-4-бензилоксипропиофенон формулы (10) суспендируют вместе с пара-бензилоксианилина гидрохлоридом формулы (9) (молярное соотношение 1:201:1, предпочтительно 1:5 по отношению к соединению формулы (10 в органическом растворителе из группы С 1-С 4 спиртов, толуола и метилтетрагидрофурана, предпочтительно этанола, и смесь нагревают в автоклаве в инертной атмосфере при 100-120 С. Через несколько часов (4-5) реакционную смесь охлаждают до температуры помещения. Кристаллизующийся продукт, 5-бензилокси-2-(4-бензилоксифенил)-3 метил-1 Н-индол формулы (1), отфильтровывают, промывают этанолом и возможно перекристаллизовывают из смеси полярного и неполярного растворителя (этилацетат-этанол, толуол-метанол, ТГФметанол). Выход реакции составляет от 75 до 80%. Выгодно, что исходный анилин формулы (9) можно получать из маточного раствора, после концентрирования и перемешивания концентрированной смеси в этилацетате, снова с почти 100% выходом. Этот оригинальный способ основан на получении и выделении нового вещества, промежуточного соединения N-(4-бензилоксифенил)амино-4-бензилоксипропиофенона формулы (10). Основные преимущества этого способа заключаются в более высоким выходе (60-75%) по сравнению с известными способами (35-53%), простом выделении промежуточного соединения N-(4-бензилоксифенил)амино 4-бензилоксипропиофенона формулы (10), а также конечного продукта 5-бензилокси-2-(4 бензилоксифенил)-3-метил-1 Н-индола формулы (1) путем фильтрования прямо из реакционной смеси без применения каких-либо дополнительных химикатов и, более того, достижении высокого качества уже у сырого продукта (98-100% согласно ВЭЖХ). Другим преимуществом является то, что исходный бензилоксианилина гидрохлорид формулы (9), применяемый в реакции циклизации, не расходуется и может быть получен из маточных растворов после выделения 5-бензилокси-2-(4-бензилоксифенил)-3 метил-1H-индола формулы (1) с количественным выходом. Краткое описание графических материалов Чертеж представляет картину рентгеновской дифрактометрии N-(4-бензилоксифенил)амино-4 бензилоксипропиофенона формулы (10) (условия рентгеновского анализа: аналитический дифрактометрX'Pert PRO P, излучение CuKa (1=1,542 ) в диапазоне 4-40 2 с увеличением 0,008. Примеры Более подробно изобретение описывается нижеследующими примерами. Получение N-(4-бензилоксифенил)амино-4-бензилоксипропиофенона (10). 1) -Бром-4-бензилоксипропиофенон (20 г; 62,7 ммоль), 4-бензилоксианилин (16 г; 67,9 ммоль) и триэтиламин (19 мл; 136,4 ммоль) суспендировали в 250 мл толуола и смесь кипятили с обратным холодильником в течение 5 ч. Затем реакционную смесь фильтровали и концентрировали до приблизительно 1/3 объема. Этанол (80 мл) добавляли к концентрированной смеси и смесь охлаждали до 5 С. После фильтрования получали 19,2 г (71%) продукта серого цвета, N-(4-бензилоксифенил)амино-4-3 016419 бензилоксипропиофенона (10), с температурой плавления 124,5-126 С. 2) -Бром-4-бензилоксипропиофенон (26 г; 81,5 ммоль), 4-бензилоксианилин (23 г; 97,8 ммоль) и карбонат натрия (20,7 г; 196 ммоль) суспендировали в 300 мл этанола и смесь кипятили с обратным холодильником в течение 5 ч. В течение указанного времени осаждается продукт. После охлаждения реакционной смеси фильтрованием выделяли смесь солей (NaBr, NaCl, карбонат натрия) и кристаллизованный продукт. Выделенную смесь веществ растворяли в смеси толуол-вода. После отделения водной фазы органическую фазу концентрировали. К концентрированному остатку добавляли этанол. Осевший слегка желтоватый кристаллический продукт отделяли фильтрованием и промывали этанолом. Получили 30,2 г(85%) N-(4-бензилоксифенил)амино-4-бензилоксипропиофенона (10). Температура плавления 126,0127,1 С. 3) -Бром-4-бензилоксипропиофенон (16,1 г; 50,5 ммоль), 4-бензилоксианилин (14,2 г; 60,1 ммоль) и триэтиламин (16,1 мл; 115,6 ммоль) суспендировали в 130 мл этанола и смесь кипятили с обратным холодильником в течение 5 ч. Затем при перемешивании смесь в течение 1 ч охлаждали до температуры помещения. Фильтрованный продукт промывали этанолом и сушили. Получали 21,9 г (99,5%) N-(4 бензилоксифенил)амино-4-бензилоксипропиофенона (10). Температура плавления 122,6-125,4 С. Сырой продукт, N-(4-бензилоксифенил)амино-4-бензилоксипропиофенон (10) (15,4 г) растворяли в толуоле (40 мл) нагреванием до 60 С. Раствор отфильтровали и к фильтрату добавляли этанол(40 мл). После охлаждения до 10-15 С получали 13,8 г (89,6%) продукта белого цвета с температурой плавления 126,1-127,1 С. 1 Н-ЯМР (ДМСО)8,10 (d, 2H); 7,3-7,5 (m, 12H); 7,19 (d, 2H); 7,06 (d, 2H); 5,5 (q, 1H); 5,24 (s, 2H); 5,08 (s, 2H); 1,48 (d, 3 Н). Рентгеновская дифрактограмма полученного продукта показана на чертеже; значения характеристических углов дифракции 2: 6,71; 19,00, 19,13; 23,49; 23,63. Получение 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1 Н-индола (1). 1) Исходный N-(4-бензилоксифенил)амино-4-бензилоксипропиофенон (22) (30,4 г; 69,7 ммоль) и 4-бензилоксианилина гидрохлорид (3,3 г; 13,9 ммоль) суспендировали в этаноле (380 мл) и смесь нагревали до 110-115 С в инертной атмосфере в автоклаве. Через 5 ч нагрев прекращали и реакционную массу перемешивали в течение ночи. Кристаллический продукт белого цвета отфильтровывали и промывали этанолом. Получали 23,3 г (79%) 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1 Н-индола (3b) с температурой плавления 152,4-153,4 С. 1 Н-ЯМР (ДМСО)10,65 (s, 1H); 7,55 (d, 2H); 7,50 (d, 4H); 7,30-7,45 (m, 6H); 7,21(d, 1H); 7,10 (d,2H); 7,10 (d, 1H); 6,91 (dd, 1H); 5,16 (s, 2H); 5,11 (s, 2H); 2,33 (s, 3 Н). МС эу (масс-спектрометрия, электронный удар) m/z 419. 2) Исходный N-(4-бензилоксифенил)амино-4-бензилоксипропиофенон (22) (30,4 г; 69,7 ммоль) и 4-бензилоксианилина гидрохлорид (3,3 г; 13,9 ммоль) суспендировали в пропан-2-оле (380 мл) и смесь нагревали до 110-115 С в инертной атмосфере в автоклаве. Через 5 ч нагрев прекратили и реакционную массу перемешивали в течение ночи. Кристаллизованный продукт бежевого цвета отфильтровали и промывали малым количеством пропан-2-ола. Получали 24,2 г (82%) 5-бензилокси-2-(4-бензилоксифенил)3-метил-1 Н-индола (3b) с температурой плавления 152,0-153,2 С. Маточные растворы после фильтрования концентрировали и концентрат перемешивали в этилацетате (30 мл). Осадок кристаллического вещества фильтровали. Получали 3,3 г 4-бензилоксианилина гидрохлорида бежевого цвета. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1H-индола формулы (1) в среде органического растворителя и в присутствии неорганического или органического основания; б) выделение промежуточного соединения(10) действием парабензилоксианилина гидрохлорида формулы (9) в среде органического растворителя из группы спиртов С 1-С 4, толуола, ацетона и метилтетрагидрофурана 2. Способ по п.1, отличающийся тем, что реакцию проводят в среде органического растворителя из группы С 1-С 4 спиртов, толуола, ацетона, метилтетрагидрофурана и в присутствии неорганического или органического основания из группы, включающей карбонат натрия, карбонат калия, триэтиламин, диизопропилэтиламин. 3. Способ по п.2, отличающийся тем, что в качестве растворителя применяют этанол, а в качестве основания применяют триэтиламин. 4. Способ по любому из пп.1, 2, отличающийся тем, что реакцию проводят при кипячении с обратным холодильником. 5. Способ по любому из пп.1-4, отличающийся тем, что промежуточное соединение N-(4 бензилоксифенил)амино-4-бензилоксипропиофенон дополнительно очищают кристаллизацией из органического растворителя, который выбран из группы жидких C1-C15 алифатических, алициклических или ароматических углеводородов или их окисленных или азотсодержащих производных или их смесей. 6. Способ по п.5, отличающийся тем, что для кристаллизации промежуточного соединения применяют смесь полярного и неполярного растворителя, такую как смеси этил ацетат-этанол, толуол-метанол,ТГФ (тетрагидрофуран)-метанол. 7. Способ по п.1, отличающийся тем, что пара-бензилоксианилина гидрохлорид формулы (9) применяют в молярном соотношении от 1:20 до 1:1, предпочтительно 1:5 по отношению к соединению формулы (10). 8. Способ по п.1 или 7, отличающийся тем, что реакцию проводят в автоклаве в инертной атмосфере при повышенной температуре 100-120 С. 9. Способ по пп.1, 7 или 8, отличающийся тем, что применяют органический растворитель из группы C1-C4 спиртов, предпочтительно этанол. 10. Кристаллический N-(4-бензилоксифенил)амино-4-бензилоксипропиофенон формулы (10). 11. Вещество по п.10, отличающееся тем, что имеет следующие значения характеристических углов дифракции 2 на профиле порошковой рентгеновской дифрактометрии: 6,71; 19,00; 19,13; 23,49; 23,63. 12. Применение N-(4-бензилоксифенил)амино-4-бензилоксипропиофенона формулы (10) для получения 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1H-индола формулы (1). 13. Применение N-(4-бензилоксифенил)амино-4-бензилоксипропиофенона формулы (10) для получения 2-(4-гидроксифенил)-1-[4-(2-азепан-1-илэтокси)бензил]-3-метил-1 Н-индол-5-ола (базедоксифена) формулы (2).
МПК / Метки
МПК: C07C 217/80, C07D 209/12
Метки: способ, получения, 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1н-индола
Код ссылки
<a href="https://eas.patents.su/7-16419-sposob-polucheniya-5-benziloksi-2-4-benziloksifenil-3-metil-1n-indola.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1н-индола</a>