Производные бензотиофена и индола, способ их получения и содержащие их фармацевтические композиции
Номер патента: 4147
Опубликовано: 26.02.2004
Авторы: Верберен Тони, Де Нантей Гийом, Рюпэн Алан, Лиля Кристин
Формула / Реферат
1. Производные бензотиофена и индола формулы (I)

где X представляет атом серы или группу NH;
Y представляет атом кислорода, атом серы или группу NH;
T представляет атом азота, когда связь, соединяющая его со смежным углеродным атомом, является одинарной (-), или атом углерода или группу CH, в зависимости от того, является ли связь, соединяющая его со смежным углеродным атомом, одинарной (-) или двойной (=);
A представляет одинарную связь или группу, выбранную из (C1-C6)алкилена (необязательно замещенного одной или несколькими неразветвленными или разветвленными (C1-C6)алкильными группами, арильными группами, арил-(C1-C6)алкильными группами, в которых алкильная часть является неразветвленной или разветвленной, циклоалкильными группами, гетероциклоалкильными группами или гетероарильными группами), арилена и группы -SO2-R4- (причем с T связан фрагмент SO2), где R4 представляет собой арилен;
W представляет группу, выбранную из гидрокси, неразветвленного или разветвленного (C1-C6)алкокси;
U1 представляет атом кислорода, атом серы или неразветвленную или разветвленную (C1-C6)алкиленовую цепь, в которой один или несколько углеродных атомов могут необязательно быть заменены одним или несколькими гетероатомами, выбранными из кислорода, азота и серы, причем указанная алкиленовая цепь является необязательно замещенной одной или несколькими одинаковыми или разными группами, выбранными из галогена, гидрокси, неразветвленного или разветвленного (C1-C6)алкила и неразветвленного или разветвленного (C1-C6)алкокси;
V1 представляет ариленовую группу;
U2 представляет одинарную связь, атом кислорода, азота или серы или неразветвленную или разветвленную (C1-C6)алкиленовую цепь, в которой один или несколько углеродных атомов могут необязательно быть заменены одной или несколькими одинаковыми или разными группами, выбранными из атомов кислорода, серы и азота (причем атом азота является замещенной группой, выбранной из водорода и неразветвленного или разветвленного (C1-C6)алкила) и группы SO2;
V2 представляет арил или пиридил;
Ra, Rb и Rc, которые могут быть одинаковыми или разными, каждый независимо от других представляет группу, выбранную из
водорода,
неразветвленного или разветвленного (C1-C6)алкокси,
феноксифенокси, пиридилметилфенокси, бензилбензилокси, феноксибензилокси, фенилтиобензилокси, фенилсульфонилбензилокси, феноксифенилсульфонилбензилокси и
арил(C1-C6)алкокси, в котором алкоксильная часть является неразветвленной или разветвленной;
R1 представляет фенил, пиридил, хинолил, пиридилоксифенил, имидазолилфенил, необязательно замещенные одним-пятью одинаковыми или разными заместителями, каждый из которых независимо от других выбран из галогена, гидрокси, циано, нитро, карбокси, неразветвленного или разветвленного (C1-C6)алкила, неразветвленного или разветвленного (C1-C6)алкокси;
R2 представляет группу, выбранную из атома водорода, арильной или пиридильной группы; причем подразумевается, что
арильная группа представляет собой фенильную, бифенильную, нафтильную, тетрагидронафтильную или дигидронафтильную группу, каждая из которых является необязательно замещенной одной или несколькими одинаковыми или разными группами, выбранными из галогена, гидрокси, циано, нитро, неразветвленного или разветвленного (C1-C6)алкила (необязательно замещенного одной или несколькими группами, выбранными из гидрокси, амино и моно- или ди-(C1-C6)алкиламино, в которых каждая из алкильных частей является неразветвленной или разветвленной), неразветвленного или разветвленного (C1-C6)тригалогеналкила, неразветвленного или разветвленного (C1-C6)алкокси, арилокси, неразветвленного или разветвленного (C1-C6)ацила, карбокси, неразветвленного или разветвленного (C1-C6)алкоксикарбонила и амино (причем амино необязательно замещен одной или двумя одинаковыми или разными неразветвленными или разветвленными (C1-C6)алкильными группами),
их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
2. Соединения формулы (I) по п.1, где Y представляет атом кислорода, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
3. Соединения формулы (I) по п.1, где R1 представляет группу, выбранную из фенила, необязательно замещенного группой, такой как определен для формулы (I), необязательно замещенного хинолила и необязательно замещенного пиридила, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
4. Соединения формулы (I) по п.1, где R2 представляет группу, выбранную из арила и пиридила, причем каждая из этих групп является необязательно замещенной, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
5. Соединения формулы (I) по п.1 или 4, где R2 представляет пиридильную группу, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
6. Соединения формулы (I) по п.1, где U1 представляет неразветвленную (C1-C4)алкиленовую цепь, в которой один углеродный атом заменен атомом кислорода, V1 представляет ариленовую группу, U2 представляет одинарную связь и V2 представляет арильную группу, необязательно замещенную одной из групп, определенных для формулы (I), их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
7. Соединения формулы (I) по п.1 или 6, где -U1-V1-U2-V2 представляет группировку [1,1'-бифенил]-4-илметокси, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
8. Соединения формулы (I) по п.1, где по крайней мере одна из групп Ra, Rb или Rc представляет группировку формулы -U1-V1-U2-V2, такую, как определена для формулы (I), их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
9. Соединения формулы (I) по любому из пп.1 или 2, где X представляет атом серы и Y представляет атом кислорода, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
10. Соединения формулы (I) по п.1, где X представляет атом серы, Y представляет атом кислорода, R1 представляет необязательно замещенную фенильную группу или необязательно замещенную пиридильную группу и A представляет одинарную связь, когда Т представляет атом углерода или группу CH, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
11. Соединения формулы (I) по п.1, где X представляет атом серы, Y представляет атом кислорода, R1 представляет фенильную группу, необязательно замещенную группой, определенной для формулы (I), и A представляет алкиленовую группу (необязательно замещенную неразветвленной или разветвленной (C1-C6)алкильной группой, арильной группой или арил-(C1-C6)алкильной группой, в которых алкильная часть является неразветвленной или разветвленной) или ариленовую группу, когда T представляет атом азота, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основаншхь.
12. Соединения формулы (I) по п.1, где они представляют собой соединения формулы (I bis)
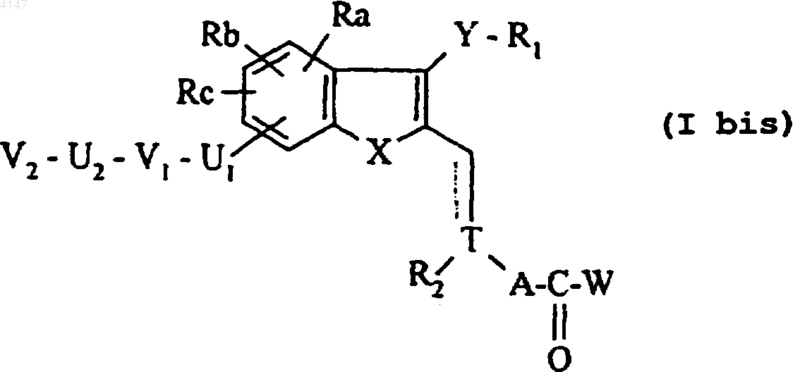
где X представляет атом серы,
Y представляет атом кислорода,
R1 представляет необязательно замещенную фенильную группу или гетероарильную группу, выбранную из необязательно замещенного пиридила и необязательно замещенного хинолила,
A представляет одинарную связь,
T представляет атом углерода,
Ra и Rc представляют каждый атом водорода,
U1 представляет неразветвленную (C1-C4)алкиленоксильную цепь,
V1 представляет ариленовую группу,
U2 представляет одинарную связь,
V2 представляет арильную группу,
Rb представляет группировку -U1-V1-U2-V2, такую как определена выше,
R2 представляет гетероарильную группу,
W представляет группу, такую как определена для формулы (I), их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
13. Соединения формулы (I) по п.12, где они представляют собой соединения формулы (I bis), где Rb и -U1-V1-U2-V2 каждый представляют группировку [1,1'-бифенил]-4-илметокси, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
14. Соединения формулы (I) по п.12, где они представляют собой соединения формулы (I bis), где R2 представляет пиридильную группу, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
15. Соединения формулы (I) по п.12, где они представляют собой соединения формулы (I bis), где R1 представляет
фенильную группу, необязательно замещенную одной-тремя группами, выбранными из галогена, неразветвленого или разветвленного (C1-C6)алкила, гетероарила, гетероарил-(C1-C6)алкокси, в котором алкоксильная часть является неразветвленной или разветвленной, неразветвленного или разветвленного (C1-C6)алкокси, амино и неразветвленного или разветвленного амино-(C1-C6)алкокси, причем аминофрагмент может быть замещенным одной или двумя одинаковыми или разными неразветвленными или разветвленными (C1-C6)алкильными группами,
или гетероарильную группу, выбранную из пиридила и хинолила, необязательно замещенных атомом галогена или неразветвленной или разветвленной (C1-C6)алкильной группой,
их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
16. Соединение формулы (I) по п.1, которое представляет собой (E)-3-[5,6-бис([1,1'-бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновую кислоту, ее изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
17. Соединения формулы (I) по п.1, которыми являются:
этил (E)-3-[5,6-бис([1,1'-бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеноат,
(E)-3-[5,6-бис([1,1'-бифенил]-4-илметокси)-3-(3-пиридилокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота,
3-(E)-{5,6-бис([1,1'-бифенил]-4-илметокси)-3-(6-метил)пиридил-3-окси]бензо[b]тиофен-2-ил}-2-(4-пиридил)-2-пропеновая кислота,
3-(E)-[5,6-бис([1,1'-бифенил]-4-илметокси)-3-(6-хинолилокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота,
(E)-3-[5,6-бис([1,1'-бифенил]-2-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота,
их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием.
18. Фармацевтические композиции, содержащие в качестве активного компонента по крайней мере одно соединение формулы (I) по любому из пп.1-17 как таковое или в сочетании с одним или несколькими инертными нетоксичными фармацевтически приемлемыми наполнителями или носителями.
19. Применение фармацевтических композиций по п.18 в качестве ингибитора PAI-1.
20. Применение фармацевтических композиций по п.18 в лечении тромбоза, патологий, причиной которых является тромбоз, и патологий, вызывающих повышение тромботического риска.
Текст
1 Настоящее изобретение относится к новым соединениям бензотиофена, бензофурана и индола, к способу их получения и к содержащим их фармацевтическим композициям. Эти новые соединения полезны из-за их терапевтической активности в области фибринолиза и тромбоза,благодаря их свойству ингибировать активностьPAI-1 является мощным ингибитором активаторов плазминогена (тканевого активатора плазминогена и урокиназы). In vitro и in vivo он ингибирует разрушение фибринозных сгустков,образованных в результате действия тромбина на фибриноген. Ряд эпидемиологических исследований показал, что у человека высокие уровни PAI-1 ассоциируются с более частыми тромбоэмболическими нарушениями. Кроме того, в экспериментальных моделях тромбоза и моноклинальных антител снижает частоту возникновения тромбозов или реокклюзий. Терапевтическая ценность молекул, обладающих свойством ингибировать активность PAI-1 в фибринозном сгустке, который уже образован или находится в процессе образования, заключается, таким образом, в обеспечении возможности разрушения сгустка на более ранней стадии, до того как он сочетается с фактором ХIIIа, и снижении тем самым возможности развития тромбоэмболии у пациентов, имеющих высокие уровни PAI-1. Такие соединения полезны для лечения всех патологий, причиной которых является тромбоз(таких как инфаркт миокарда, стенокардия, перемежающаяся хромота, инсульты, тромбоз глубоких вен или легочная эмболия), и патологий с повышенным риском тромбоза (таких как гипертензия, гиперхолестеринемия, диабет,ожирение, генетические аномалии свертывания крови (фактор V Лейден, дефицит белков С и S) или приобретенные аномалии свертывания). Кроме того, что соединения по настоящему изобретению новые, они, как доказано, являются более мощными ингибиторами PAI-1,чем описанные в литературе, что делает их потенциально полезным для лечения тромбоза,патологий, причиной которых является тромбоз,и патологий, вызывающих повышение тромботического риска. Ряд антитромботических средств уже описан в литературе. Это касается, в частности, соединений, раскрытых в описаниях к патентамWO 97/45424, WO 94/08962, ЕР 540051 и GB 2225012. В частности, настоящее изобретение относится к соединениям формулы (I)X представляет атом серы или группу NH;Y представляет атом кислорода, атом серы или группу NH; Т представляет атом азота, когда связь, соединяющая его со смежным углеродным атомом,является одинарной (-), или атом углерода или группу СН, в зависимости от того, является ли связь, соединяющая его со смежным углеродным атомом, одинарной (-) или двойной ( = ); А представляет одинарную связь или группу,выбранную из (С 1-С 6)алкилена (необязательно замещенного одной или несколькими неразветвленными или разветвленными (С 1-С 6)алкильными группами, арильными группами, арил-(С 1-С 6)алкильными группами, в которых алкильная часть является неразветвленной или разветвленной, циклоалкильными группами, гетероциклоалкильными группами или гетероарильными группами), арилена и группы -SO2-R4- (причем с Т связан фрагментU1 представляет атом кислорода, атом серы или неразветвленную или разветвленную(С 1-С 6)алкиленовую цепь, в которой один или несколько углеродных атомов могут необязательно быть заменены одним или несколькими гетероатомами, выбранными из кислорода, азота и серы, причем указанная алкиленовая цепь является необязательно замещенной одной или несколькими одинаковыми или разными группами,выбранными из галогена, гидрокси, неразветвленного или разветвленного (С 1-С 6)алкила и неразветвленного или разветвленного (С 1-С 6)алкокси;U2 представляет одинарную связь, атом кислорода, азота или серы или неразветвленную или разветвленную (С 1-С 6)алкиленовую цепь, в которой один или несколько углеродных атомов могут, необязательно, быть заменены одной или несколькими одинаковыми или разными группами, выбранными из атомов кислорода, серы и азота (причем атом азота является замещенной группой, выбранной из водорода и неразветвленного или разветвленного (С 1-С 6)алкила) и группы SO2;V2 представляет арил или пиридил;Ra, Rb и Rc, которые могут быть одинаковыми или разными, каждый независимо от других представляет группу, выбранную из водорода,неразветвленного или разветвленного (С 1-С 6) алкокси,феноксифенокси, пиридилметилфенокси, бензилбензилокси, феноксибензилокси, фенилтиобензилокси, фенилсульфонилбензилокси, феноксифенилсульфонилбензилокси, иapил(С 1-С 6)алкокси, в котором алкоксильная часть является неразветвленной или разветвленной; 3 замещенные одним-пятью одинаковыми или разными заместителями, каждый из которых независимо от других выбран из галогена, гидрокси, циано, нитро, карбокси, неразветвленного или разветвленногоR2 представляет группу, выбраную из атома водорода, арильной или пиридильной группы, причем подразумевается, что арильная группа представляет собой фенильную, бифенильную, нафтильную, тетрагидронафтильную или дигидронафтильную группу,каждая из которых является необязательно замещенной одной или несколькими одинаковыми или разными группами, выбранными из галогена, гидрокси, циано, нитро, неразветвленного или разветвленного (С 1-С 6)алкила (необязательно замещенного одной или несколькими группами, выбранными из гидрокси, амино и моно- или ди-(С 1-С 6)алкиламино, в которых каждая из алкильных частей является неразветвленной или разветвленной), неразветвленного или разветвленного(С 1-С 6)тригалогеналкила, неразветвленного или разветвленного (С 1-С 6)алкокси, арилокси, неразветвленного или разветвленного (С 1-С 6)ацила, карбокси, неразветвленного или разветвленного (С 1-С 6)алкоксикарбонила и амино (причем амино необязательно замещен одной или двумя одинаковыми или разными неразветвленными или разветвленными (С 1-С 6)алкильными группами),их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. Из фармацевтически приемлемых кислот можно упомянуть, не налагая никакого ограничения, хлористо-водородную кислоту, бромисто-водородную кислоту, серную кислоту, фосфоновую кислоту, уксусную кислоту, трифторуксусную кислоту, молочную кислоту, пиовиноградную кислоту, малоновую кислоту, янтарную кислоту, глутаровую кислоту, фумаровую кислоту, винную кислоту, малеиновую кислоту,лимонную кислоту, аскорбиновую кислоту, щавелевую кислоту, метансульфоновую кислоту,камфорную кислоту и так далее. Из фармацевтически приемлемых оснований можно упомянуть, не налагая никакого ограничения, гидроксид натрия, гидроксид калия,триэтиламин, трет-бутиламин и так далее. Из гетероциклоалкилов можно упомянуть,не налагая никакого ограничения, такие гетероциклоалкилы, как пиперидин, пиперазин и морфолин. Из гетероарилов можно упомянуть, не налагая никакого ограничения, такие гетероарилы, как пиридин, пиримидин, хинолин, изохинолин, 1,3-дигидро 2 Н-пирролопиридин-2-он, 3 Н-имидазопиридин, 1 Нпирролопиридин, 1,2,3,4-тетрагидронафтопиридин и 2,3-дигидро-1 Н-пирролопиридин. Предпочтительными соединениями по настоящему изобретению являются те, в которыхX представляет атом серы или группу NR3, в которой R3 такой, как определен в формуле (I). Предпочтительными соединениями по настоящему изобретению являются те, в которыхY представляет атом кислорода. Заместителями R1, предпочтительными в соответствии с настоящим изобретением, являются группы, выбранные из фенила, необязательно замещенного группой, определенной для формулы (I), необязательно замещенного хинолила и необязательно замещенного пиридила. Заместителями R2, предпочтительными в соответствии с настоящим изобретением, являются группы, выбранные из арила и гетероарила, причем каждая из этих групп является необязательно замещенной. В соответствии с предпочтительным вариантом предпочтительным заместителем R2 является пиридильная группа. Заместителями -U1-V1-U2-V2, предпочтительными в соответствии с настоящим изобретением, являются заместители в которых U1 представляет неразветвленную (С 1-С 4)алкиленовую цепь, в которой один из углеродных атомов заменен атомом кислорода, V1 представляет ариленовую группу, U2 представляет одинарную связь и V2 представляет арильную группу, необязательно замещенную одной из групп,определенных для формулы (I). Особенно выгодно, когда предпочтительный заместитель -U1-V1-U2-V2 представляет собой группировку [1,1'-бифенил]-4-илметокси. В соответствии с предпочтительным вариантом осуществления настоящего изобретения предпочтительными соединениями являются те,в которых одна из групп Ra, Rb или Rc представляет группировку формулы -U1-V1-U2-V2,такую, как определена для формулы (I). В соответствии с выгодным вариантом осуществления настоящего изобретения предпочтительными соединениями являются те, в которых X представляет атом серы и Y представляет атом кислорода. В соответствии с особо выгодным вариантом осуществления настоящего изобретения предпочтительными соединениями являются те,в которыхR1 представляет необязательно замещенную фенильную группу или необязательно замещенную пиридильную группу,А представляет одинарную связь, когда Т представляет атом углерода или группу СН. В соответствии с третьим выгодным вариантом предпочтительными соединениями по настоящему изобретению являются те, в которыхR1 представляет фенильную группу, необязательно замещенную группой, определенной для формулы (I),А представляет алкиленовую группу (необязательно замещенную неразветвленной или разветвленной (С 1-С 6)алкильной группой, арильной группой или арил-(С 1-С 6)алкильной группой, в которых алкильная часть является неразветвленной или разветвленной) или ариленовую группу, когда Т представляет атом азота. В соответствии с четвертым выгодным вариантом предпочтительными соединениями по настоящему изобретению являются соединения формулы (I bis)R1 представляет необязательно замещенную фенильную группу или гетероарильную группу, выбранную из необязательно замещенного пиридила и необязательно замещенного хинолила,А представляет одинарную связь,Т представляет атом углерода,Ra и Rc представляют каждый атом водорода,U1 представляет неразветвленную (С 1-С 4)алкиленоксильную цепь,V1 представляет ариленовую группу,U2 представляет одинарную связь,V2 представляет арильную группу,Rb представляет группировку -U1-V1-U2V2, такую, как определена выше,R2 представляет гетероарильную группу,W представляет группу, такую, как определена для формулы (I). В очень выгодном варианте предпочтительными соединениями по настоящему изобретению являются соединения формулы (I bis), гдеRb и -U1-V1-U2-V2 представляют каждый группировку [1,1'-бифенил]-4-илметокси. В другом очень выгодном варианте предпочтительными соединениями по настоящему изобретению являются соединения формулы (Ibis), где R2 представляет пиридильную группу. В третьем очень выгодном варианте предпочтительными соединениями по настоящему изобретению являются соединения формулы (I(С 1-С 6)алкила, гетероарила, гетероарил-(С 1-С 6) алкокси, в котором алкоксильная часть является неразветвленной или разветвленной, неразветвленного или разветвленного (С 1-С 6)алкокси, 004147 6 амино и неразветвленного или разветвленного амино-(С 1-С 6)алкокси, причем аминофрагмент может быть замещенным (в каждой из двух указанных групп) одной или двумя одинаковыми или разными неразветвленными или разветвленными (С 1-С 6)алкильными группами,или гетероарильную группу, выбранную из пиридила и хинолила необязательно замещенных атомом галогена или неразветвленной или разветвленной (С 1-С 6)алкильной группой. Предпочтительными соединениями по настоящему изобретению являются 7 Изомеры, а также аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием, предпочтительных соединений составляют неотъемлемую часть настоящего изобретения. Соединения формулы (I) получают следующим способом. В качестве исходного материала используют соединение формулы (II) где Ra, Rb и Rc такие, как определены для формулы (I), G представляет гидроксигруппу, защищенную защитной группой, обычно используемой в органическом синтезе, и Q представляет атом галогена или гидроксигруппу, причем предпочтительно Q представляет атом галогена,когда X представляет атом серы или группуNR3, где R3 такой, как определен для формулы(I), и Q представляет гидроксигруппу, когда X представляет атом кислорода, которое (соединение формулы (II подвергают взаимодействию при основных условиях, когда Q представляет атом галогена, с соединением формулы н - Y1 -R1 (III) где R1 такой, как определен для формулы(I), и Y1 представляет атом кислорода, атом серы или группу NR3, где R3 такой, как определен для формулы (I), с получением соединений формулы (IV/а)(НО)2 В - R1 (V) где R1 такой, как определен для формулы(I), с получением соединений формулы (IV/b) где Ra, Rb, Rc, G и R1 такие, как определены выше, и X1 представляет группу NR3, где R3 представляет гетероарил-(C1-C6)-алкильную группу, в которой алкильная часть является неразветвленной или разветвленной,или, когда Q представляет гидроксигруппу, с соединением формулы (VI)Hal - R1 (VI) где Hal представляет атом галогена и R1 такой,как определен выше, с получением соединений формулы (IV/c) где Ra, Rb, Rc, G, X и R1 такие, как определенны выше, причем совокупность соединений формул(IV/a), (IV/b) и (IV/c) составляет соединения формулы (IV) где Ra, Rb, Rc, G, R1, X и Y такие, как определены для формулы (I), которые (соединения формулы (IV конденсируют в присутствии уксусного ангидрида с соединением формулы (VII) где R'2 имеет такое же определение, как R2 для формулы (I), за исключением того, что R'2 не может представлять атом водорода, и W1 представляет группу, выбранную из неразветвленного или разветвленного (C1-C6)алкокси, арилокси,арил-(С 1-С 6)алкокси, в котором алкоксильная часть является неразветвленной или разветвленной, циклоалкилокси, гетероциклоалкокси, гетероарилокси и аминогруппы (которая сама является необязательно замещенной одной или двумя одинаковыми или разными группами,каждая из которых независимо от других выбрана из неразветвленного или разветвленного(С 1-С 6)алкила, арила, арил-(С 1-С 6)алкила, в котором алкильная часть является неразветвленной или разветвленной, и циклоалкила), с получением соединений формулы (VIII) где Ra, Rb, Rc, G, R1, R'2, X, Y и W1 такие, как определены выше, с гидроксильной функциональной группы которых (соединений формулыVIII) удаляют защитную группу при обычных условиях органического синтеза и которые затем подвергают в основной среде взаимодействию с соединением формулы (IX)V2 - U2 - V1 - U2 - Hal (IX) где U1, V1, U2 и V2 такие, как определены для формулы (I), и Hal представляет атом галогена,с получением соединений формулы (I/a), частный случай соединений формулы (I) где Ra, Rb, Rc, U1, V1, U2, V2, R1, R'2, X, Y и W1 такие, как определены выше, которые (соединения формулы (I/a, если требуется, подвергают воздействию либо условий каталитического гидрирования (в присутствии палладия) с получением соединений формулы (I/b), частный случай соединений формулы (I) либо условий гидролиза в основной среде с получением соединений формулы (1/с), частный случай соединений формулы (I) либо условий гидролиза в основной среде с получением соединений формулы (I/f), частный случай соединений формулы (I где Ra, Rb, Rc, U1, V1, U2, V2, R1, R'2, X и Y такие, как определены выше, двойную связь которых (соединений формулы (I/с, если требуется,восстанавливают путем каталитического гидрирования с получением соединений формулы(I/d), частный случай соединений формулы (I) где Ra, Rb, Rc, U1, V1, U2, V2, R1, R2, X, Y и A1 такие, как определены выше,либо условий каталитического гидрирования с получением соединений формулы (I/g),частный случай соединений формулы (I) где Ra, Rb, Rc, U1, V1, U2, V2, R1, R'2, X и Y такие, как определены выше, или подвергают (соединения формулы (IV воздействию илида фосфора формулы (X)W1 такие, как определены выше,которые (соединения (Ig могут быть обработаны в условиях основного гидролиза с получением соединений формулы (I/h), частный случай соединений формулы (I) где R' представляет неразветвленную или разветвленную (C1-C6)алкильную группу или фенильную группу, R2 такой, как определен для формулы (I), W1 такой, как определен выше, и А представляет одинарную связь, алкиленовую группу (необязательно замещенную одной или несколькими группами, выбранными из неразветвленного или разветвленного (C1-C6)алкила,арила, арил-(C1-C6)алкила, в котором алкильная часть является неразветвленной или разветвленной, циклоалкила, гетероциклоалкила и гетероарила), ариленовую группу, циклоалкиленовую группу, гетероциклоалкиленовую группу или гетероариленовую группу, с получением соединений формулы (XI) где Ra, Rb, Rc, G, R1, R2, X, Y, A1 и W1 такие, как определены выше, с гидроксильной функциональной группы которых (соединений формулы(XI удаляют защитную группу при обычных условиях органического синтеза и которые затем подвергают в основной среде взаимодействию с соединением формулы (IX):V2 - U2 - V1 - U2 - Hal (IX) где U1, V1, U2 и V2 такие, как определены для формулы (I), и Hal представляет атом галогена, с получением соединений формулы (I/е),частный случай соединений формулы (I) где Ra, Rb, Rc, U1, V1, U2, V2, R1, R2, X, Y и A1 такие, как определены выше,или с гидроксильной функциональной группы которых (соединений формулы (IV удаляют защитную группу при обычных условиях органического синтеза и которые затем подвергают в основной среде взаимодействию с соединением формулы (IX)V2 - U2 - V1 - U1 - Hal (IX) где U1, V1, U2 и V2 такие, как определены для формулы (I), и Hal представляет атом галогена,с получением соединений формулы (XII) где Ra, Rb, Rc, U1, V1, U2, V2, R1, X и Y такие,как определены выше,альдегидную функциональную группу которых (соединений формулы (XII восстанавливают до первичного спирта с получением соединений формулы (XIII) где Ra, Rb, Rc, U1, V1, U2, V2, R1, X и Y такие,как определены для формулы (I),концевую гидроксильную группу которых(соединений формулы (XIII заменяют при традиционных условиях атомом галогена с получением соединений формулы (XIV) где Ra, Rb, Rc, U1, V1, U2, V2, R1, X и Y такие,как определены выше, и Hal представляет атом хлора или брома, в которых (соединениях формулы (XIV атом галогена замещают в основных условиях аминированным соединением формулыR2 - NH - A1 - СО - W1 (XV) где R2 такой, как определен для формулы (I), иA1 и W1 такие, как определены выше,с получением соединений формулы (I/i),частный случай соединений формулы (I)(соединений формулы (I/i гидролизуют в основных условиях с получением соединений формулы (I/j), частный случай соединений формулы (I) где Ra, Rb, Rc, U1, V1, U2, V2, R1, R2, X, Y и A1 такие, как определены выше,или которые (соединения (XIV сначала обрабатывают азидом натрия и полученный азид восстанавливают до первичного амина в условиях каталитического гидрирования с получением соединений формулы (XVI) где Ra, Rb, Rc, U1, V1, U2, V2, R1, X и Y такие,как определены для формулы (I),которые (соединения формулы (XVI конденсируют в основных условиях с хлорсульфонильным соединением формулы (XVII) Сl - SO2 - R4 - СО - W1 (XVII) где R4 такой, как определен для формулы (I), иW такой, как определен выше,с получением соединений формулы (I/k),частный случай соединений формулы (I) где Ra, Rb, Rc, U1, V1, U2, V2, R1, R2, X, Y и W1 такие, как определены выше, которые (соединения формулы (I/k подвергают, если требуется, воздействию условий гидролиза в основных условиях с получением соединений формулы (I/l), частный случай соединений формулы (I)Hal - R'2 (XVIII) где Hal представляет атом галогена, такой как иод, и R'2 такой, как определен выше,с получением соединений формулы (I/m),частный случай соединений формулы (I)W1 такие, как определены выше,которые (соединения (Im обрабатывают в условиях гидролиза в основной среде с получением соединений формулы (1/n), частный случай соединений формулы (I)(I/c), (I/d), (I/f), (I/h), (I/j), (I/l) и (I/n) составляет соединения формулы (I') где Ra, Rb, Rc, U1, V1, U2, V2, R1, R2, X, Y, Z и А такие, как определены для формулы (I),которые (соединения формулы (I' подвергают взаимодействию с O-замещенным гидроксиламином с получением, после снятия защиты у функциональной гидроксиламиногруппы, соединений формулы (I/o), частный случай соединений формулы (I) где Ra, Rb, Rc, U1, V1, U2, V2, R1, R2, X, Y, Z и А такие, как определены выше,причем соединения (I/a)-(I/о) составляют совокупность соединений по настоящему изобретению, которые, при необходимости, очищают традиционными методами очистки, разделяют, если требуется, на различные их изомеры в соответствии с традиционными методами разделения и преобразуют, когда нужно, в их аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 13 Соединения формулы (II) получают традиционными методами органического синтеза. В частности, соединения формулы (II), где X представляет атом кислорода и Q представляет гидроксигруппу, получают из соединения формулы (II/A) схема синтеза которых описана в J.Med.Chem.,1992, 35, 958-965 и в которых Ra, Rb, Rc и G такие, как определены выше, и R' представляет неразветвленную или разветвленную (C1-C6)алкильную группу,функциональную гидроксигруппу которых защищают в основных условиях триалкилсилильной группой, и сложноэфирную функциональную группу которых затем восстанавливают, например воздействием LiAlH4, до первичного спирта, окисляемого далее до альдегида,после чего снимают защиту у его спиртовой функциональной части с помощью н-Вu4 НF,обеспечивая возможность получения конкретных соединений формулы (II), где X представляет атом кислорода и Q представляет гидроксигруппу. Конкретные соединения формулы (II), гдеX представляет группу NR3, получают из соединений формулы (II/В) схема синтеза которых описана в Heterocycles, 1992,34 (12), 2349-62 и в Synthesis, 1984, 862-865 и в которых Ra, Rb, Rc, G и R3 такие, как определены выше, и R' представляет неразветвленную или разветвленную (C1-C6)алкильную группу, сложноэфирную функциональную группу которых восстанавливают до первичного спирта, окисляемого далее до альдегида воздействием диоксида марганца с получением соединений формулы (II), где X представляет группу NR3 и Q представляет атом галогена. Конкретные соединения формулы (II), гдеX представляет атом серы, получают из соединений формулы (II/C) схема синтеза которых описана вRa, Rb, Rc и G такие, как определены выше, функциональную группу карбоновой кислоты которых сначала восстанавливают до первичного спирта и затем окисляют до альдегида с получением соединений формулы (II), где X представляет атом серы и Q представляет атом галогена. Соединения формул (III), (V), (VI), (VII),(IX), (X), (XV), (XVII) и (XVIII) либо являются коммерческими продуктами, либо могут быть 14 получены традиционными методами органического синтеза. Настоящее изобретение относится также к фармацевтическим композициям, содержащим в качестве активного компонента по крайней мере одно соединение формулы (I), его оптические изомеры или его аддитивную соль с фармацевтически приемлемым основанием или фармацевтически приемлемой солью, как таковое или в сочетании с одним или несколькими инертными нетоксичными фармацевтически приемлемыми наполнителями или носителями. Из фармацевтических композиций по настоящему изобретению можно упомянуть, в частности, те, которые пригодны для перорального, парентерального (внутривенного, внутримышечного или подкожного), чрескожного, назального, ректального, перлингвального, глазного или респираторного введения, и особенно таблетки или драже, подъязычные таблетки,пилюли, желатиновые капсулы, лепешки, суппозитории, кремы, мази, кожные гели, препараты для инъекций или питья, аэрозоли, глазные капли или капли в нос и т.д. Полезная доза зависит от возраста и массы пациента, способа введения, характера и тяжести расстройства и всякого проводимого сопутствующего лечения и находится в пределах от 0,1 мг до 1 г в один или несколько приемов в сутки. Следующие ниже примеры иллюстрируют настоящее изобретение, но ни в коей мере не ограничивают его. Использованные исходные материалы являются известными продуктами или получены известными методами. Различные стадии синтеза дают промежуточные продукты синтеза, пригодные для получения соединений по настоящему изобретению. Структуры соединений, описанных в примерах и на стадиях синтеза, определяли обычными методами спектрофотометрии (инфракрасный, ЯМР, масс-спектрометрия и т.д.). Пример-1. Этил (Е)-3-[5,6-бис([1,1'-бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеноат Стадия А. 3-Хлор-5,6-(метилендиокси)бензо[b]тиофен-2-карбонилхлорид К суспензии 0,26 мл 3,4-(метилендиокси)коричной кислоты в 365 мл хлорбензола добавляют последовательно при температуре окружающей среды 0,026 моль пиридина и по каплям 1,33 моль SOCl2. Затем реакционную смесь нагревают при температуре кипения с обратным холодильником в течение 2 дней. После возврата к температуре окружающей среды образуется осадок. После фильтрования, промывки гексаном и высушивания получают 51,2 г целевого продукта. Стадия В. 3-Хлор-5,6-(метилендиокси)бензо[b]тиофен-2-карбоновая кислота 15 К раствору 70 ммоль соединения стадии А в 250 мл диоксана добавляют 40 мл воды. После 20-часового нагревания при температуре кипения с обратным холодильником и затем возврата к температуре окружающей среды образуется осадок. После фильтрования и промывки водой до получения нейтральной среды осадок сушат над Р 2 О 5 при пониженном давлении, обеспечивая возможность выделения целевого продукта. Стадия С. (3-Хлор-5,6-(метилендиокси)бензо[b]тиофен-2-ил)-метанол К раствору 0,15 моль LiAlH4 в 450 мл тетрагидрофурана добавляют 0,14 моль соединения, полученного на стадии В, при 5 С под инертной средой. После 2-часовой реакции при температуре окружающей среды реакционную смесь гидролизуют путем добавления 85 мл изопропанола и 31 мл насыщенного раствора хлорида натрия. После перемешивания в течение 12 ч при температуре окружающей среды реакционную смесь фильтруют через целит. Затем органическую фазу концентрируют при пониженном давлении, растворяют в дихлорметане и промывают водой и затем насыщенным раствором NaCl. После высушивания органической фазы над сульфатом кальция раствор концентрируют при пониженном давлении, что позволяет получить целевой продукт. Стадия D. 3-Хлор-5,6-(метилендиокси)бензо[b]тиофен-2-карбальдегид К суспензии 0,12 моль соединения, полученного на стадии С, в 925 мл безводного диоксана добавляют при температуре окружающей среды в инертной атмосфере 3,5 эквивалента МnО 2. После 3,5-часовой реакции при нагревании при температуре кипения с обратным холодильником реакционную смесь фильтруют, пока она горячая, через целит и промывают диоксаном, а затем фильтрат концентрируют при пониженном давлении. Полученный остаток растворяют в 100 мл этилацетата и полученный раствор нагревают при температуре кипения с обратным холодильником и затем возвращают к температуре окружающей среды. Образуется осадок, который отфильтровывают, промывают этилацетатом и затем водой и пентаном и наконец высушивают в вакууме с получением целевого продукта. Стадия Е. 3-(4-Хлорфенокси)-5,6-(метилендиокси)бензо-[b]тиофен-2-карбальдегид К раствору 0,10 моль 4-хлорфенола в 250 мл диметилформамида добавляют при температуре окружающей среды в инертной атмосфере 1 эквивалент гидрида натрия и затем 0,094 моль продукта, полученного на стадии D. После 12 часовой реакции при 80 С реакционную смесь концентрируют при пониженном давлении. Остаток разбавляют этилацетатом, промывают водой и затем водным раствором NaOH и потом водным раствором NaCl, сушат над сульфатом кальция, фильтруют и концентрируют при пониженном давлении. Хроматография на силика 004147 16 геле (дихлорметан/этилацетат: 98/2) позволяет выделить целевой продукт. Стадия F. Этил (Е)-3-[3-(4-хлорфенокси)5,6-(метилендиокси)-бензо[b]тиофен-2-ил]-2-(4 пиридил)-2-пропеноат Раствор, содержащий 85 ммоль продукта,полученного на стадии Е, 127 ммоль этил 4 пиридилацетата и 75 мл уксусного ангидрида,нагревают при 100 С в течение 18 ч. После возврата к температуре окружающей среды реакционную смесь гидролизуют насыщенным раствором NaHCO3 и экстрагируют этилацетатом. Органические фазы промывают водой и затем раствором NaCl, сушат над сульфатом кальция,фильтруют и концентрируют при пониженном давлении. Хромагография на силикагеле (дихлорметан/этанол: 98/2) позволяет выделить целевой продукт. Стадия G: Этил (Е)-3-[3-(4-хлорфенокси)5,6-(дигидрокси)-бензо[b]тиофен-2-ил]-2-(4 пиридил)-2-пропеноат К раствору 0,025 моль продукта, полученного на стадии F, в 170 мл безводного дихлорметана добавляют по каплям при 5 С под аргоном 0,1 моль ВВr3 в виде 1 М раствора в дихлорметане. После перемешивания в течение 2 ч к реакционной смеси добавляют по каплям 125 мл спирта и затем смесь концентрируют при пониженном давлении. Остаток растворяют в этилацетате и перемешивают в течение 30 мин. Образовавшийся осадок отфильтровывают,промывают этилацетатом и затем высушивают в вакууме с получением целевого продукта. Стадия Н. Этил (Е)-3-[5,6-бис[1,1'-бифенил]3-(4-ил-метокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеноат К раствору 2,1 ммоль продукта, полученного на стадии G, и 4,6 ммоль 4-(хлорметил)1,1'-дифенила в 30 мл безводного диметилформамида добавляют 7,5 ммоль К 2 СО 3. После 12 часовой редакции при 80 С реакционную смесь возвращают к температуре окружающей среды и добавляют 30 мл воды, вызывая образование осадка. Осадок отфильтровывают, промывают водой и затем высушивают в вакууме. Хроматография на силикагеле (дихлорметан/этил-ацетат: 95/5) позволяет выделить целевой продукт. Температура плавления: 212 С Элементный микроанализ: Вычислено Найдено Пример 2. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-(4-хлорфенокси)бензо[b]тиофен 2-ил]-2-(4-пиридил)-2-пропеновая кислота. Раствор, содержащий 1,5 ммоль продукта примера 1, 3 мл водного 1 н раствора гидроксида натрия и 30 мл этанола, нагревают при температуре кипения с обратным холодильником в течение 12 ч. После возврата к температуре окружающей среды реакционную смесь концентри 17 руют при пониженном давлении и остаток разбавляют водой и затем растворяют в этилацетате. Органическую фазу подкисляют путем добавления 6 мл 1 н раствора HCl. Образуется осадок, который отфильтровывают, промывают водой и затем высушивают при пониженном давлении с получением целевого соединения. Элементный микроанализ: Вычислено Найдено Пример 3. Натрий (Е)-3-[5,6-бис([1,1'бифенил]-4-ил-метокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеноат. К суспензии 1 г продукта примера 2 в 2,5 мл 1 н раствора гидроксида натрия добавляют воду до полного разведения. Лиофилизация дает целевой продукт. Пример 4. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-(4-хлорфенокси)бензо[b]тиофен 2-ил]-2-фенил-2-пропеновая кислота. Методика такая, как в примере 1, стадии А-Н, с использованием фенилэтановой кислоты в качестве реагента на стадии F. Пример 5. Этил (Е)-3-[5,6-бис([1,1'бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]пропеноат. К суспензии 0,02 моль (этоксикарбонилметил)трифенилфосфонийбромида в 90 мл тетрагидрофурана добавляют по каплям при 0 С в инертной атмосфере 20 мл 1 М раствора третбутилата калия в тетрагидрофуране. По окончании добавления и возвращении смеси к температуре окружающей среды добавляют 0,01 моль полученного на стадии Е примера 1 соединения,разведенного 30 мл тетрагидрофурана. Через 12 ч реакционную смесь гидролизуют добавлением 100 мл 1 н раствора HCl и затем экстрагируют этилацетатом. Объединенные органические фазы промывают водой и затем насыщенным раствором NaCl, сушат над сульфатом натрия,фильтруют и концентрируют при пониженном давлении. Хроматография на силикагеле (пентан/этилацетат: 90/10) позволяет выделить целевой продукт. Пример 6. Этил 2-([5,6-бис([1,1'-бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b] тиофен-2-ил]метиланилино)-ацетат. Стадия 1. [5,6-(Метилендиокси)-3-(4-хлорфенокси)бензо[b]-тиофен-2-ил]метанол. К раствору 24 ммоль соединения, полученного на стадии Е примера 1, в 100 мл метанола добавляют при температуре окружающей среды 26 ммоль NaBH4. После реакции в течение 2 ч добавляют к реакционной смеси один эквивалент NaBH4. После 12-часовой реакции раствор концентрируют и затем разбавляют этилацетатом, промывают 1 н раствором HCl,затем водой и далее насыщенным растворомNaCl, после чего сушат над сульфатом кальция,фильтруют и концентрируют при пониженном 18 давлении. Хроматография на силикагеле (дихлорметан/этилацетат: 95/5) позволяет выделить целевой продукт. Стадия 2. [2-Хлорметил-3-(4-хлорфенокси)-5,6-(метилендиокси)]бензо[b]тиофен. К 4 ммоль соединения стадии 1, разведенного 10 мл дихлорметана, добавляют по каплям при 0 С 0,63 мл SOCl2. После возврата к температуре окружающей среды с последующим нагреванием обратным холодильником в течение 6 ч при температуре кипения дихлорметана, реакционную смесь концентрирует при пониженном давлении с получением целевого продукта. Стадия 3. Этил 2-([3-(4-хлорфенокси)-5,6(метилендиокси)-бензо[b]тиофен-2-ил]метил анилино)ацетат. Раствор, содержащий 6,5 ммоль соединения, полученного на стадии 2, в 16 мл диметилформамида, 1,5 эквивалента сложного этилового эфира N-фенилглицина и 1,5 эквивалента К 2 СО 3 нагревают при 80 С в течение 18 ч. После выпаривания растворителя остаток разводят этилацетатом и органическую фазу промывают водой и затем насыщенным раствором NaCl,сушат над сульфатом кальция, фильтруют и выпаривают при пониженном давлении. Хроматография на силикагеле (толуол/этилацетат: 98/2) позволяет выделить 2,56 г целевого продукта в виде масла. Стадия 4. Этил 2-([5,6-бис([1,1'-бифенил]4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]метиланилино)-ацетат. Методика такая же, как в примере 1, стадии G-H, с использованием продукта, полученного на описанной выше стадии 3, в качестве субстрата. Пример 7. Этил 2-([5,6-бис([1,1'-бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]метиламино)-бензоат. Методика такая же, как в примере 6, с использованием этилантранилата в качестве реагента на стадии 3. Пример 8. Метил 2-[([5,6-бис([1,1'-бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]метиламино)-сульфонил]бензоат Стадия 1. [2-Азидометил-3-(4-хлорфенокси)-5,6-(метилендиокси)]бензо[b]тиофен. Раствор, содержащий 41 ммоль соединения, полученного на стадии 2 примера 6, и 78 ммоль азида натрия, в 80 мл диметилформамида перемешивают при температуре окружающей среды в течение 48 ч. Затем реакционную среду концентрируют при пониженном давлении. Остаток разбавляют этилацетатом и промывают водой и затем насыщенным раствором NaCl. Органическую фазу сушат над сульфатом кальция, фильтруют и выпаривают с получением целевого продукта. Стадия 2. [2-Аминометил-3-(4-хлорфенокси)-5,6-(метилендиокси)]бензо[b]тиофен. Раствор, содержащий 41 ммоль соединения, полученного на описанной выше стадии 1, 19 и 1 г Pd/C в 6,5 мл хлороформа и 300 мл безводного метанола, помещают в среду водорода при температуре окружающей среды. Через 12 ч реакционную смесь фильтруют и концентрируют при пониженном давлении с получением целевого продукта. Стадия 3: Метил 2-[([3-(4-хлорфенокси)5,6-(метилендиокси)бензо[b]тиофен-2-ил]метиламино)сульфонил]бензоат Раствор, содержащий 6,5 ммоль соединения, полученного на описанной выше стадии 2,6,5 ммоль метил 2-(хлорсульфонил)бензоата и 15,7 ммоль N-метилморфолина в 50 мл дихлорметана, перемешивают при температуре окружающей среды. Через 12 ч реакционную смесь промывают водой и затем насыщенным раствором NaCl,сушат над сульфатом натрия и концентрируют при пониженном давлении. Хроматография на силикагеле (дихлорметан/этилацетат: 98/2) позволяет выделить целевой продукт. Стадия 4. Метил 2-[([5,6-бис([1,1'-бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]метил-амино)сульфонил]бензоат. Методика такая же, как в примере 1, стадии G-H, с использованием продукта, полученного на описанной выше стадии 3, в качестве субстрата. Пример 9. 2-[([5,6-Бис([1,1'-бифенил]-4 илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2 ил]метиламино)сульфонил]бензойная кислота Методика такая же, как в примере 2, с использованием соединения, полученного на стадии 4 примера 8, в качестве субстрата. Пример 10. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-(3-пиридилокси)бензо[b]тиофен-2-ил]-2-(4-пиридил) -2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 3-гидроксипиридина в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Температура плавления: 237 С Элементный микроанализ Вычислено Найдено Пример 11. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-(4-хлорфенокси)-1 Н-2-индолил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, стадии Е-Н, с использованием 3-бром-5,6 диметокси-1 Н-2-индолкарбальдегида в качестве субстрата на стадии Е, после чего следуют процедуре, описанной в примере 2. Пример 12. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-[(4-метоксифенилсульфонил]бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 4-метоксибензолтиола в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. 20 Пример 13. 3-(Е)-3-[4-(2-(Диметиламино)этокси)фенокси]-5,6-бис([1,1'-бифенил]-4-илметокси)бензо[b]-тиофен-2-ил 2-фенил-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 2-(диметиламино)этоксифенола в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Пример 14. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-(3,4-дихлорфенокси)бензо[b]тиофен 2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 3,4-дихлорфенола в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Пример 15. 3-(Е)-5,6-Бис([1,1'-бифенил]4-илметокси)-3-[6-(метил)пиридил-3-окси]бензо[b]тиофен-2-ил-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 2-метил-5-гидроксипиридина в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ: Вычислено Найдено Пример 16. 3-(Е)-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-[6-хинолилокси]бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 6-гидроксихинолина в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ: Вычислено Найдено Пример 17. (Е)-3-[5,6-Бис([1,1'-бифенил]-2 илметокси)-3-(4-хлорфенокси)бензо[b]тио-фен 2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 2-(бромметил)-1,l'-бифенила в качестве реагента на стадии Н, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ: Вычислено Найдено Пример 18. (Е)-3-[5,6-Бис(4-феноксифенокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 1-бром-4-феноксибензола в качестве реагента на стадии Н, после чего следуют процедуре, описанной в примере 2. Пример 19. (Е)-3-3-(4-Хлорфенокси)-5,6 бис[4-(4-пиридилметил)фенокси]бензо[b]тиофен-2-ил-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 4-(4-хлорбензил)пиридина в качестве реагента на стадии Н, после чего следуют процедуре, списанной в примере 2. Пример 20. (Е)-3-[5,6-Бис([1,1'-бифенил]-3 илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 3-(бромметил)-1,1'-бифенила в качестве реагента на стадии Н, после чего следуют процедуре, описанной в примере 2. Температура плавления: 205-210 С Пример 21. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-(4-хлор-3-фторфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 4-хлор-3-фторфенола в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ: Вычислено Найдено Пример 22. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-(4-хлор-3,5-диметилфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 4-хлор-3,5-диметилфенола в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ Вычислено Найдено Пример 23. (Е)-3-[5,6-Бис(1,1'-бифенил]-4 илметокси)-3-(4-хлор-3-метилфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 4-хлор-3-метилфенола в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ Вычислено Найдено Пример 24. (Е)-3-5,6-Бис([1,1'-бифенил]4-илметокси)-3-[4-(4-пиридилокси)фенокси]бензо[b]тиофен-2-ил-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 4-пиридилоксифенола в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Температура плавления 265 С Элементный микроанализ: Вычислено Пример 25. (Е)-3-5,6-Бис([1,1'-бифенил]4-илметокси)-3-[4-(1 Н-имидазол-1-илфенокси]бензо[b]тиофен-2-ил-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 4-(1 Н-имидазол-1-ил)фенола в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ Вычислено Найдено Пример 26. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-феноксибензо[b]тиофен-2-ил]-2(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием фенола в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ: Вычислено Найдено Пример 27. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-(3-фторфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 3-фторфенола в качестве реагента на стадии Е, после чего следуют процедуре,описанной в примере 2. Элементный микроанализ: Вычислено Найдено Пример 28. (Е)-3-[5,6-Бис([1,1'-бифенил]-4 илметокси)-3-(3,4-дифторфенокси)бензо[b]тиофен 2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 3,4-дифторфенола в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ: Вычислено Найдено Пример 29. (Е)-3-5,6-Бис([1,1'-бифенил]4-илметокси)-3-[(6-хлор-3-пиридил)окси]бензо[b]тиофен-2-ил-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 2-хлор-5-гидроксипиридина в качестве реагента на стадии Е, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ: Вычислено Найдено Пример 30. (Е)-3-3-(4-Хлорфенокси)-5,6 бис[(4-метокси-[1,1'-бифенил]-4-ил)метокси]бензо[b]тиофен-2-ил-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 4-(бромметил)-4'-метокси-1,1'-бифенила в качестве реагента на стадии Н, после чего следуют процедуре, описанной в примере 2. Температура плавления 235 С Элементный микроанализ: Вычислено Найдено Пример 31. (Е)-3-[5,6-Бис(2-[1,1'-бифенил]-4 илэтокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 4-(2-бромэтил)-1,1'-бифенила в качестве реагента на стадии Н, после чего следуют процедуре, описанной в примере 2. Пример 32. (Е)-3-[5,6-Бис[(4-бензилбензил)окси]-3-(4-хлорфенокси)бензо[b]тиофен-2 ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 1-бензил-4-(бромметил)бензола в качестве реагента на стадии Н, после чего следуют процедуре, описанной в примере 2. Пример 33. (Е)-3-3-(4-Хлорфенокси)-5,6 бис[(4-феноксибензил)окси]бензо[b]тиофен-2 ил-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 1-(бромметил)-4-феноксибензола в качестве реагента на стадии Н, после чего следуют процедуре, описанной в примере 2. Пример 34. (Е)-3-(3-(4-Хлорфенокси)-5,6 бис([4-(фенилсульфанил)бензил]окси)бензо[b]тиофен-2-ил)-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 1-(бромметил)-4-(фенилсульфанил)бензола в качестве реагента на стадии Н, после чего следуют процедуре, описанной в примере 2. Пример 35. (Е)-3-(3-(4-Хлорфенокси)-5,6 бис[4-(фенилсульфонил)бензил]оксибензо[b]тиофен-2-ил)-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 1-(бромметил)-4-(фенилсульфонил)бензола в качестве реагента на стадии Н, после чего следуют процедуре, описанной в примере 2. Пример 36. (Е)-3-[3-(4-Хлорфенокси)-5,6 бис(4-[4-(феноксифенил)сульфонил]бензилокси)бензо[b]тиофен-2-ил)-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 1-(бромметил)-4-[(4-феноксифенил)сульфонил]бензола в качестве реагента на стадии Н, после чего следуют процедуре, описанной в примере 2. 24 Пример 37. (Е)-3-[6-(Бензилокси)-5-([1,1'бифенил]-4-ил-метокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота. Стадия 1. (Е)-3-[6-(Бензилокси)-3-(4-хлорфенокси)-5-гидроксибензо[b]тиофен-2-ил]-2-(4 пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, стадии А-Н, с использованием хлорметилфенила. Стадия 2. (Е)-3-[6-(Бензилокси)-5-([1,1'бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как на стадии Н примера 1, после чего следуют процедуре, описанной в примере 2. Элементный микроанализ: Вычислено Найдено Пример 38. (Е)-3-[6-([1,1'-бифенил]-4 илметокси)-3-(4-хлорфенокси)-5-феноксибензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновая кислота. Методика такая же, как в примере 1, с использованием 4-хлорметил-(1,1'-бифенила) и затем хлорметилфенила в качестве реагентов на стадии Н. Пример 39. 3-[6-([1,1-Бифенил]-4-илметокси-5-([1,1'-бифенил]-4-илокси)-3-(4-хлорфенокси)бензо[b]-тиофен-2-ил]-2-фенилпропановая кислота. Методика такая же, как в примере 1, стадии A-F, с использованием фенилэтановой кислоты вместо этил 4-пиридилацетата в качестве реагента на стадии F, после чего выполняют стадии G-H, описанные в примере 1. Полученный описанным образом продукт обрабатывают потоком водорода в присутствии 10%-ного Pd/C в метаноле в течение 24 ч. По окончании реакции фильтрование через целит и затем хроматография на силикагеле позволяют выделить целевой продукт. Пример 40. 2-([6-([1,1'-Бифенил]-4-илметокси-5-([1,1'-бифенил]-4-илокси)-3-(4-хлорфенокси)бензо[b]-тиофен-2-ил]метиламино)бензойная кислота. Методика такая же, как в примере 2, стадии A-F, с использованием соединения, полученного в примере 7, в качестве исходного материала. Фармакологическое исследование соединений по настоящему изобретению Пример 41. Ингибирование активностиPAI-1. Ингибирование активности PAI-1 осуществляют in vitro в ячейках микропластинки, в которых образование и затем разрушение фибринового сгустка непрерывно контролируют путем измерения его мутности с использованием спектрофотометра. Для этого, пользуясь в 25 качестве разбавителя 50 мМ фосфатным буфером с рН 7,4, содержащим 0,05% бычьего сывороточного альбумина, вносят 50 мкл ингибитора в присутствии 50 мкл 2 нМ раствора рекомбинантного активного человеческого PAI-1 в течение 5 мин при температуре окружающей среды. Затем добавляют 50 мкл 0,42 нМ раствора тканевого активатора плазминогена, 50 мкл 800 нМ раствора человеческого плазминогена и 50 мкл раствора фибриногена (2 г/л) и инициируют образование фибрина путем добавления 50 мкл 14 нМ очищенного человеческого тромбина. В отсутствие продукта измеряют ингибирование разрушения через два часа после начала образования фибрина по спектральной поглощательной способности сгустка, что дает 100% активности PAI-1. В отсутствие продукта и PAI-1 измеряют разрушение по спектральной поглощательной способности разрушенного сгустка, что дает 0% активности PAI-1. Концентрацию продукта, которая ингибирует активность PAI-1 на 50%, определяют путем измерения спектральной поглощательной способности сгустка через два часа после фибринообразования в присутствии PAI-1 при увеличении концентрации продукта. Например, соединения примеров 2, 10 и 26 имеют IC50, равную 0,13 мкМ, 0,53 мкМ и 0,06 мкМ, соответственно. Этот результат демонстрирует очень высокую фибринолитическую активность соединений по настоящему изобретению. Эталонным продуктом являетсяXR 5082, имеющий IC50, равный 190 мкМ. Пример 42. Фармацевтическая композиция Состав для получения 1000 таблеток, содержащих каждая 10 мг активного компонента: Соединение примера 2 10 г Гидроксипропилцеллюлоза 2 г Поливинилпирролидон 2 г Пшеничный крахмал 10 г Лактоза 10 г Стеарат магния 3 г ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производные бензотиофена и индола формулы (I)X представляет атом серы или группу NH;Y представляет атом кислорода, атом серы или группу NH; Т представляет атом азота, когда связь, соединяющая его со смежным углеродным атомом, является одинарной (-), или атом углерода или группу СН, в зависимости от того, является ли связь, соединяющая его со смежным углеродным атомом, одинарной (-) или двойной (=); А представляет одинарную связь или группу, выбранную из (С 1-С 6)алкилена (необязательно 26 замещенного одной или несколькими неразветвленными или разветвленными (С 1-С 6)алкильными группами, арильными группами, арил-(С 1-С 6)алкильными группами, в которых алкильная часть является неразветвленной или разветвленной, циклоалкильными группами, гетероциклоалкильными группами или гетероарильными группами), арилена и группы -SO2-R4- (причем с Т связан фрагментU1 представляет атом кислорода, атом серы или неразветвленную или разветвленную(С 1-С 6)алкиленовую цепь, в которой один или несколько углеродных атомов могут необязательно быть заменены одним или несколькими гетероатомами, выбранными из кислорода, азота и серы, причем указанная алкиленовая цепь является необязательно замещенной одной или несколькими одинаковыми или разными группами, выбранными из галогена, гидрокси, неразветвленного или разветвленного (С 1-С 6)алкила и неразветвленного или разветвленногоU2 представляет одинарную связь, атом кислорода, азота или серы или неразветвленную или разветвленную (С 1-С 6)алкиленовую цепь, в которой один или несколько углеродных атомов могут необязательно быть заменены одной или несколькими одинаковыми или разными группами, выбранными из атомов кислорода, серы и азота (причем атом азота является замещенной группой, выбранной из водорода и неразветвленного или разветвленного (С 1-С 6)алкила) и группы SO2;V2 представляет арил или пиридил;Ra, Rb и Rc, которые могут быть одинаковыми или разными, каждый независимо от других представляет группу, выбранную из водорода,неразветвленного или разветвленного (С 1-С 6) алкокси,феноксифенокси, пиридилметилфенокси, бензилбензилокси, феноксибензилокси, фенилтиобензилокси, фенилсульфонилбензилокси, феноксифенилсульфонилбензилокси, и арил(С 1-С 6)алкокси, в котором алкоксильная часть является неразветвленной или разветвленной;R1 представляет фенил, пиридил, хинолил,пиридилоксифенил, имидазолилфенил, необязательно замещенные одним-пятью одинаковыми или разными заместителями, каждый из которых независимо от других выбран из галогена,гидрокси, циано, нитро, карбокси, неразветвленного или разветвленного (С 1-С 6)алкила, неразветвленного или разветвленного (C1-С 6)алкокси;R2 представляет группу, выбранную из атома водорода, арильной или пиридильной группы; причем подразумевается, что арильная группа представляет собой фенильную, бифенильную, нафтильную, тетрагидронафтильную или дигидронафтильную группу,каждая из которых является необязательно замещенной одной или несколькими одинаковыми или разными группами, выбранными из галогена, гидрокси, циано, нитро, неразветвленного или разветвленного (С 1-С 6)алкила (необязательно замещенного одной или несколькими группами, выбранными из гидрокси, амино и моно- или ди-(С 1-С 6)алкиламино, в которых каждая из алкильных частей является неразветвленной или разветвленной), неразветвленного или разветвленного (С 1-С 6)тригалоген-алкила,неразветвленного или разветвленного (С 1 С 6)алкокси, арилокси, неразветвленного или разветвленного (С 1-С 6)ацила, карбокси, неразветвленного или разветвленного (С 1-С 6)алкоксикарбонила и амино (причем амино необязательно замещен одной или двумя одинаковыми или разными неразветвленными или разветвленными (С 1-С 6)алкильными группами),их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 2. Соединения формулы (I) по п.1, где Y представляет атом кислорода, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 3. Соединения формулы (I) по п.1, где R1 представляет группу, выбранную из фенила,необязательно замещенного группой, такой как определен для формулы (I), необязательно замещенного хинолила и необязательно замещенного пиридила, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 4. Соединения формулы (I) по п.1, где R2 представляет группу, выбранную из арила и пиридила, причем каждая из этих групп является необязательно замещенной, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 5. Соединения формулы (I) по п.1 или 4,где R2 представляет пиридильную группу, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 6. Соединения формулы (I) по п.1, где U1 представляет неразветвленную (С 1-С 4)алкиленовую цепь, в которой один углеродный атом заменен атомом кислорода, V1 представляет ариленовую группу, U2 представляет одинарную связь и V2 представляет арильную группу, необязательно замещенную одной из групп, определенных для формулы (I), их изомеры и адди 004147 28 тивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 7. Соединения формулы (I) по п.1 или 6,где -U1-V1-U2-V2 представляет группировку[1,1'-бифенил]-4-илметокси, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 8. Соединения формулы (I) по п.1, где по крайней мере одна из групп Ra, Rb или Rc представляет группировку формулы -U1-V1-U2-V2,такую, как определена для формулы (I), их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 9. Соединения формулы (I) по любому из пп.1 или 2, где X представляет атом серы и Y представляет атом кислорода, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 10. Соединения формулы (I) по п.1, где X представляет атом серы, Y представляет атом кислорода, R1 представляет необязательно замещенную фенильную группу или необязательно замещенную пиридильную группу и А представляет одинарную связь, когда Т представляет атом углерода или группу СН, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 11. Соединения формулы (I) по п.1, где X представляет атом серы, Y представляет атом кислорода, R1 представляет фенильную группу,необязательно замещенную группой, определенной для формулы (I), и А представляет алкиленовую группу (необязательно замещенную неразветвленной или разветвленной (С 1-С 6)алкильной группой, арильной группой или арил(С 1-С 6)алкильной группой, в которых алкильная часть является неразветвленной или разветвленной) или ариленовую группу, когда Т представляет атом азота, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 12. Соединения формулы (I) по п.1, где они представляют собой соединения формулы (I bis)X представляет атом серы,Y представляет атом кислорода,R1 представляет необязательно замещенную фенильную группу или гетероарильную группу, выбранную из необязательно замещенного пиридила и необязательно замещенного хинолила, 29 А представляет одинарную связь,Т представляет атом углерода,Ra и Rс представляют каждый атом водорода,U1 представляет неразветвленную (С 1-С 4)алкиленоксильную цепь,V1 представляет ариленовую группу,U2 представляет одинарную связь,V2 представляет арильную группу,Rb представляет группировку -U1-V1-U2V2, такую, как определена выше,R2 представляет гетероарильную группу,W представляет группу, такую как определена для формулы (I), их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 13. Соединения формулы (I) по п.12, где они представляют собой соединения формулы (Ibis), где Rb и -U1-V1-U2-V2 каждый представляют группировку [1,1'-бифенил] -4-илметокси, их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 14. Соединения формулы (I) по п.12, где они представляют собой соединения формулы (Ibis), где R2 представляет пиридильную группу,их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 15. Соединения формулы (I) по п.12, где они представляют собой соединения формулы (Ibis), где R1 представляет фенильную группу, необязательно замещенную одной-тремя группами, выбранными из галогена, неразветвленого или разветвленного (С 1 С 6)алкила, гетероарила, гетероарил-(С 1-С 6)алкокси,в котором алкоксильная часть является неразветвленной или разветвленной, неразветвленного или разветвленного (С 1-С 6)алкокси, амино и неразветвленного или разветвленного амино-(С 1-С 6)алкокси, причем аминофрагмент может быть замещенным одной или двумя одинаковыми или разными неразветвленными или разветвленными (C1-С 6)алкильными группами,или гетероарильную группу, выбранную из пиридила и хинолила, необязательно замещен 30 ных атомом галогена или неразветвленной или разветвленной (С 1-С 6)алкильной группой,их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 16. Соединение формулы (I) по п.1, которое представляет собой (Е)-3-[5,6-бис([1,1'бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]-2-(4-пиридил)-2-пропеновую кислоту, ее изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 17. Соединения формулы (I) по п.1, которыми являются: этил (Е)-3-[5,6-бис([1,1'-бифенил]-4-илметокси)-3-(4-хлорфенокси)бензо[b]тиофен-2-ил]2-(4-пиридил)-2-пропеноат,(Е)-3-[5,6-бис([1,1'-бифенил]-4-илметокси)-3-(3-пиридилокси)бензо[b]тиофен-2-ил]-2(4-пиридил)-2-пропеновая кислота,3-(Е)-5,6-бис([1,1'-бифенил]-4-илметокси)-3-(6-метил)-пиридил-3-окси]бензо[b]тиофен-2-ил-2-(4-пиридил)-2-пропеновая кислота,3-(Е)-[5,6-бис([1,1'-бифенил]-4-илметокси)-3-(6-хинолилокси)бензо[b]тиофен-2-ил]-2(4-пиридил)-2-пропеновая кислота,(Е)-3-[5,6-бис([1,1'-бифенил]-2 илметокси)-3-(4-хлорфенокси)бензо[b]тиофен 2-ил]-2-(4-пиридил)-2-пропеновая кислота,их изомеры и аддитивные соли с фармацевтически приемлемой кислотой или фармацевтически приемлемым основанием. 18. Фармацевтические композиции, содержащие в качестве активного компонента по крайней мере одно соединение формулы (I) по любому из пп.1-17 как таковое или в сочетании с одним или несколькими инертными нетоксичными фармацевтически приемлемыми наполнителями или носителями. 19. Применение фармацевтических композиций по п.18 в качестве ингибитора PAI-1. 20. Применение фармацевтических композиций по п.18 в лечении тромбоза, патологий,причиной которых является тромбоз, и патологий, вызывающих повышение тромботического риска.
МПК / Метки
МПК: A61P 7/02, A61K 31/381, C07D 333/64
Метки: производные, содержащие, получения, бензотиофена, способ, индола, фармацевтические, композиции
Код ссылки
<a href="https://eas.patents.su/16-4147-proizvodnye-benzotiofena-i-indola-sposob-ih-polucheniya-i-soderzhashhie-ih-farmacevticheskie-kompozicii.html" rel="bookmark" title="База патентов Евразийского Союза">Производные бензотиофена и индола, способ их получения и содержащие их фармацевтические композиции</a>
Предыдущий патент: Сульфонамиды и их производные, модулирующие активность эндотелина
Случайный патент: Ступень испарителя мгновенного вскипания












