Способ разделения энантиомеров (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила и применение при синтезе ивабрадина
Номер патента: 15777
Опубликовано: 30.12.2011
Авторы: Гожон Эрик, Лерестиф Жан-Мишель, Дрон Даньель, Фан Маризе, Лекув Жан-Пьерр
Формула / Реферат
1. Способ разделения оптических изомеров (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила формулы (I), где рацемически или энантиомерно обогащенную смесь (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила разделяют на два его энантиомера (S)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрил формулы (Ia) и (R)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрил формулы (Ib) путем хиральной хроматографии.
2. Способ по п.1, который характеризуется тем, что используют непрерывный многоколонный способ разделения.
3. Способ по одному из пп.1 или 2, который характеризуется тем, что используют способ хроматографии с псевдодвижущимся слоем.
4. Способ по одному из пп.1-3, который характеризуется тем, что неподвижная фаза, используемая для хиральной хроматографии, содержит силикагель, пропитанный функционализированным полисахаридом.
5. Способ по одному из пп.1-4, который характеризуется тем, что неподвижная фаза, используемая для хиральной хроматографии, содержит целлюлозное или амилозное производное трис(4-метилбензоата) или трис(3,5-диметилфенилкарбамата).
6. Способ по одному из пп.1-5, который характеризуется тем, что подвижная фаза, используемая для хиральной хроматографии, содержит спирт, другой органический растворитель или смесь спирта и другого органического растворителя.
7. Способ по п.6, который характеризуется тем, что используемый спирт представляет собой изопропанол.
8. Способ по любому из пп.6 или 7, который характеризуется тем, что используемый органический растворитель представляет собой гептан или гексан.
9. Способ по любому из пп.6-8, который характеризуется тем, что подвижная фаза содержит смесь спирта и другого органического растворителя.
10. Способ по п.9, который характеризуется тем, что подвижная фаза содержит смесь изопропанола и гептана или смесь изопропанола и гексана.
11. Способ по п.10, который характеризуется тем, что подвижная фаза содержит смесь изопропанола и гептана или смесь изопропанола и гексана в соотношении, изменяющемся от 50:50 до 2:98.
12. Способ по одному из пп.1-11, который характеризуется тем, что подвижную фазу, используемую для хиральной хроматографии, используют повторно.
13. Способ по одному из пп.1-12, который характеризуется тем, что хиральную хроматографию осуществляют при температуре от 15 до 40°С включительно.
14. Способ по одному из пп.1-13, который характеризуется тем, что разделение оптических изомеров осуществляют на рацемической смеси (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила формулы (I).
15. Способ по одному из пп.1-14, который характеризуется тем, что целевым энантиомером (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила является (S)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрил формулы (Ia).
16. Способ по одному из пп.1-15, который характеризуется тем, что (R) энантиомер (3,4-диметокси-бицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила формулы (Ib) рацемизируют и используют в качестве исходного вещества в способе разделения оптических изомеров.
17. Соединение формулы (Ia)
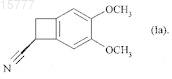
18. Соединение формулы (Ib)
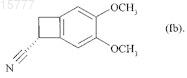
19. Способ синтеза соединения формулы (V)
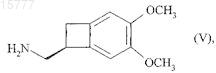
который характеризуется тем, что соединение формулы (Ia)
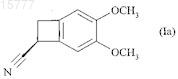
подвергают восстановительной реакции.
20. Способ синтеза по п.19, который характеризуется тем, что восстановление соединения формулы (Ia) осуществляют в присутствии палладия на угле и HCl в атмосфере водорода или в присутствии тетраборогидрида натрия и трифторуксусной кислоты.
21. Способ синтеза ивабрадина, его фармацевтически приемлемых солей и их гидратов, который характеризуется тем, что соединение формулы (I)
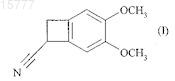
подвергают способу разделения оптических изомеров по п.1, получая соединение формулы (Ia)

которое превращают в соединение формулы (V)
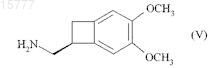
в соответствии со способом по п.19, которое превращают в карбамат формулы (VI)
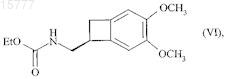
который восстанавливают, получая соединение формулы (III)
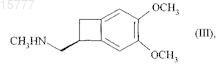
которое превращают в ивабрадин формулы (II)
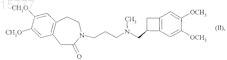
или 3-{3-[{[(7S)-3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил]метил}(метил)амино]пропил}-7,8-диметокси-1,3,4,5-тетрагидро-2H-3-бензазепин-2-он, который может быть необязательно превращен в его соль присоединения с фармацевтически приемлемой кислотой, выбранной из хлористо-водородной кислоты, бромисто-водородной кислоты, серной кислоты, фосфорной кислоты, уксусной кислоты, трифторуксусной кислоты, молочной кислоты, пировиноградной кислоты, малоновой кислоты, янтарной кислоты, глутаровой кислоты, фумаровой кислоты, винной кислоты, малеиновой кислоты, лимонной кислоты, аскорбиновой кислоты, щавелевой кислоты, метансульфоновой кислоты, бензолсульфоновой кислоты и камфорной кислоты, или в его гидрат.
Текст
ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ЕВРАЗИЙСКОМУ ПАТЕНТУ Дата публикации и выдачи патента СПОСОБ РАЗДЕЛЕНИЯ ЭНАНТИОМЕРОВ (3,4-ДИМЕТОКСИБИЦИКЛО[4.2.0] ОКТА-1,3,5-ТРИЕН-7-ИЛ)НИТРИЛА И ПРИМЕНЕНИЕ ПРИ СИНТЕЗЕ ИВАБРАДИНА Способ разделения оптических изомеров соединения формулы (I) с помощью хиральной хроматографии. Применение при синтезе ивабрадина, его солей присоединения с фармацевтически приемлемой кислотой и его гидратов.(71)(73) Заявитель и патентовладелец: ЛЕ ЛАБОРАТУАР СЕРВЬЕ (FR) 015777 Настоящее изобретение относится к способу разделения оптических изомеров (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила формулы (I) и к его применению при синтезе ивабрадина,его солей присоединения с фармацевтически приемлемой кислотой и их гидратов. или 3-3-(7S)-3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил]метил(метил)амино]пропил 7,8-диметокси-1,3,4,5-тетрагидро-2H-3-бензазепин-2-он,и его соли присоединения с фармацевтически приемлемой кислотой, и, в особенности, его гидрохлорид, имеют чрезвычайно ценные фармакологические и терапевтические свойства, в особенности,брадикардические свойства, что делает эти соединения полезными для лечения или предотвращения различных клинических случаев миокардиальной ишемии, таких как стенокардия, инфаркт миокарда и ассоциированные нарушения ритма сердечного ритма, а также при различных патологиях, в которых задействованы нарушения сердечного ритма, в частности, при наджелудочковых расстройствах ритма, и при сердечной недостаточности. Приготовление и терапевтическое применение ивабрадина и его солей присоединения с фармацевтически приемлемой кислотой, и, в особенности, его гидрохлорида, было описано в европейской патентной заявке ЕР 0534859. В этом описании к патенту описан синтез ивабрадина, используя в качестве исходного вещества соединение формулы (III) Соединение формулы (III) получают, используя в качестве исходного вещества соединение формулы (IV) путем разделения с помощью камфорсульфоновой кислоты. Соединение формулы (III) является важным промежуточным соединением при синтезе ивабрадина. Разделение вторичного амина формулы (IV) приводит к получению соединения формулы (III) только в очень небольшом выходе (4-5%). Тем не менее, учитывая фармацевтическую важность ивабрадина и его солей, очень актуальной является возможность получения соединения формулы (III) с помощью эффективного промышленного способа и, в особенности, с хорошим выходом и с очень хорошей химической и энантиомерной чистотой. Заявителем был разработан способ разделения оптических изомеров соединения формулы (I), который предоставляет возможность получения соединения формулы (III) с очень хорошими характеристиками выхода и химической и энантиомерной чистотой. Способ по изобретению предоставляет возможность получать целевой энантиомер соединения формулы (I) в очень хорошем энантиомерном избытке, с высокой продуктивностью и с очень хорошим выходом, при этом экономя на используемых растворителях. В частности, настоящее изобретение относится к способу разделения оптических изомеров (3,4 диметокси-бицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила формулы (I) с получением его энантиомеров абсолютной конфигурации (S) и (R), соответственно формулы (Ia) и (Ib) где рацемически или энантиомерно обогащенную смесь (3,4-диметоксибицикло[4.2.0]окта-1,3,5 триен-7-ил)нитрила разделяют на два его энантиомера, (S)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5 триен-7-ил)нитрил формулы (Ia) и (R)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрил формулы (Ib), путем хиральной хроматографии. Под разделением оптических изомеров понимают разделение двух энантиомеров рацемической смеси или любой смеси этих двух энантиомеров. Под рацемической смесью понимают смесь двух энантиомеров в соотношении от 55:45 до 45:55,предпочтительно в соотношении 50:50. Под энантиомерно обогащенной смесью понимают смесь двух энантиомеров, содержащую существенно большее количество одного из энантиомеров в соотношении, изменяющемся в интервале от 55:45 до 90:10. Под хиральной хроматографией понимают распределение, которое предоставляет возможность разделить энантиомеры смеси с помощью хиральной неподвижной фазы и подвижной фазы, состоящей из растворителя или смеси растворителей. В соответствии с предпочтительным вариантом осуществления изобретения, используют непрерывный многоколонный способ разделения. В соответствии с еще более предпочтительным вариантом осуществления изобретения, используют способ хроматографии с псевдодвижущимся слоем. Под хроматографией с псевдодвижущимся слоем понимают непрерывный процесс хроматографии,который предоставляет возможность стимулировать движение неподвижной фазы в противоположном направлении к движению подвижной фазы. Такой процесс предоставляет возможность разделить соединения, которые тяжело или невозможно разделить с помощью общепринятых хроматографических методик. Если используется хиральная неподвижная фаза, то такой процесс является особенно пригодным для разделения энантиомеров. Использование хроматографии с псевдодвижущимся слоем предоставляет возможность осуществить непрерывное разделение смеси энантиомеров с высокой продуктивностью,при этом уменьшается используемое количество неподвижной и подвижных фаз по сравнению с дискретными хроматографическими процессами. В соответствии с одним из предпочтительных вариантов осуществления изобретения, неподвижная фаза, используемая для хиральной хроматографии, содержит силикагель, пропитанный функционализированным полисахаридом. В соответствии с предпочтительным вариантом осуществления изобретения, неподвижная фаза, используемая для хиральной хроматографии, содержит целлюлозное или амилозное производное трис(4 метилбензоата) или трис(3,5-диметилфенилкарбамата). Подвижная фаза, предпочтительно используемая для хиральной хроматографии, содержит спирт,другой органический растворитель или смесь спирта и другого органического растворителя. Из спиртов, которые можно использовать для хиральной хроматографии, можно отметить, но не ограничиваясь только ими, изопропанол, этанол и метанол. Спирт, предпочтительно используемый для хиральной хроматографии, представляет собой изопропанол. Из органических растворителей, которые можно использовать для хиральной хроматографии, можно отметить, но не ограничиваясь только ими, гептан, гексан, циклогексан, ацетонитрил и метил третбутиловый эфир. Предпочтительно используемый органический растворитель представляет собой гептан или гексан. Подвижная фаза, используемая для хиральной хроматографии, предпочтительно содержит смесь спирта и другого органического растворителя. Еще более предпочтительно подвижная фаза, используемая для хиральной хроматографии, содержит смесь изопропанола и гептана или смесь изопропанола и гексана. В предпочтительном варианте осуществления изобретения, подвижная фаза, используемая для хиральной хроматографии, содержит смесь изопропанола и гептана или смесь изопропанола и гексана в соотношении, изменяющемся от 50:50 до 2:98. В соответствии с предпочтительным вариантом осуществления изобретения, подвижную фазу, используемую для хиральной хроматографии, используют повторно. Хиральную хроматографию предпочтительно осуществляют при температуре от 15 до 40 С включительно. В соответствии с предпочтительным вариантом осуществления изобретения разделение оптических изомеров осуществляют на рацемической смеси (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-2 015777 ил)нитрила формулы (I). В соответствии с одним из предпочтительных вариантов осуществления изобретения, целевым энантиомером (3,4-диметоксибицикло [4.2.0]окта-1,3,5-триен-7-ил)нитрила является (S)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрил формулы (Ia). В соответствии с одним из предпочтительных вариантов осуществления изобретения (R) энантиомер (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила, формулы (Ib), рацемизируют и используют в качестве исходного вещества в способе разделения оптических изомеров. Из соединения формулы (Ia) можно получать соединение формулы (V) путем восстановительной реакции. Восстановление соединения формулы (Ia) предпочтительно осуществляют в присутствии палладия на угле и HCl в атмосфере водорода или в присутствии тетраборогидрида натрия и трифторуксусной кислоты. Соединение формулы (V), получаемое путем восстановления соединения формулы (Ia), пригодно для синтеза ивабрадина формулы (II). В качестве примера, соединение формулы (V) превращают в карбамат формулы (VI) который восстанавливают, получая соединение формулы (III) или 3-3-(7S)-3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил]метил(метил)амино]пропил 7,8-диметокси-1,3,4,5-тетрагидро-2H-3-бензазепин-2-он,который может быть необязательно превращен в его соль присоединения с фармацевтически приемлемой кислотой, выбранной из хлористо-водородной кислоты, бромисто-водородной кислоты, серной кислоты, фосфорной кислоты, уксусной кислоты, трифторуксусной кислоты, молочной кислоты, пировиноградной кислоты, малоновой кислоты, янтарной кислоты, глутаровой кислоты, фумаровой кислоты,винной кислоты, малеиновой кислоты, лимонной кислоты, аскорбиновой кислоты, щавелевой кислоты,метансульфоновой кислоты, бензолсульфоновой кислоты и камфорной кислоты, или в его гидрат. Среди способов, известных для осуществления превращения соединения формулы (III) в ивабрадин, могут быть упомянуты те, которые описаны в европейских патентных заявках ЕР 0534859 и ЕР 1589005. Соединения формул (Ia) и (Ib) являются новыми продуктами, которые полезны в качестве промежуточных соединений синтеза в химической или фармацевтической промышленности, в особенности для синтеза ивабрадина, его солей присоединения с фармацевтически приемлемой кислотой и его гидратов,и, таких образом, они составляют необъемлемую часть настоящего изобретения. Перечень используемых сокращений-3 015777 Пример 1. Разделение энантиомеров (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила путем препаративной хиральной хроматографии Растворяли 480 мг соединения формулы (I) в 5 мл метанола, инъецировали на колонку Prochrom 50 см 50 мм, упаковывали до 25 см с 300 г Chiracel OJ фазы, при скорости потока 80 мл/мин, и элюировали при этой скорости потока в смеси гептан/изопропанол (70/30). Энантиомер формулы (Ia) (конфигурация (S получали с выходом 45,6% и с энантиомерной чистотой 97,6%. Энантиомер формулы (Ib) (конфигурация (R получали с выходом 42,2% и с энантиомерной чистотой 99,3%. Пример 2. [(7S)-3,4-Диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил]метанамин путем восстановления (S)-(3,4-диметокси-бицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила в присутствии NaBH4 Вносили NaBH4 (3 экв.) и ТГФ (10 мл/г) в трехгорлую колбу объемом 125 мл, которую продували потоком азота и оборудовали конденсором, магнитной мешалкой, CaCl2 блокировкой на впускном отверстии для азота и датчиком температуры. По каплям вливали в ТФК (2,97 экв.) при 20-25 С. По каплям добавляли раствор (S)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила (1 экв.) в ТГФ (4 мл/г). Перемешивали при 20-25 С в течение ночи, затем реакционную смесь вливали в водный 0,3 М раствор HCl (0,5 экв.) и перемешивали при 20-25 С в течение 1 ч. Фильтровали через фритту в вакууме,промывали ТГФ и растворитель упаривали при пониженном давлении. Неочищенный реакционный продукт ресуспендировали в дихлорметане (20 мл/г), добавляли 10 мл/г воды и раствор гидроксида натрия (2 мл/г). Перемешивали в течение 15 мин и затем позволяли разделиться; органическую фазу промывали водой, высушивали над MgSO4 и растворитель упаривали при пониженном давлении, получая указанный в заглавии продукт с выходом 78,8% и с энантиомерной чистотой 94,4%. Пример 3. [(7S)-3,4-Диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил]метанамин путем восстановления (S)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила в присутствии палладия на угле Вносили 1 экв. (S)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила, 1 экв. метанольнойHCl 1,12N и 0,1 вес.% 5% палладия на угле в автоклав объемом 125 мл. Промывали метанолом (10 мл/г). Продували азотом и затем водородом, перемешивали при 20 С и гидрировали под давлением 30 бар при этой температуре в течение 5 ч. В автоклаве снижали давление, реакционную смесь фильтровали и растворители отгоняли при пониженном давлении. Полученный гидрохлорид ресуспендировали в дихлорметане (20 мл/г), добавляли 10 мл/г воды и раствор гидроксида натрия (2 мл/г). Перемешивали в течение 15 мин и затем позволяли разделиться, органическую фазу промывали водой, высушивали над MgSO4 и растворитель упаривали при пониженном давлении, получая указанный в заглавии продукт с выходом 90% и с энантиомерной чистотой 95,5%. Пример 4. Рацемические (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрил путем рацемизации (R)-(3,4-диметокси-бицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрил Вносили 100 мг (R)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила (0,53 ммоль), 5 мл изопропанола и 121 мг DBU (1,5 экв.) в колбу, оборудованную конденсором и магнитной мешалкой. Нагревали при 65 С в течение 2 ч и затем позволяли возвратиться до температуры окружающей среды. Фильтровали для получения указанного в заглавии соединения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ разделения оптических изомеров (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7 ил)нитрила формулы (I), где рацемически или энантиомерно обогащенную смесь (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила разделяют на два его энантиомера (S)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрил формулы (Ia) и (R)-(3,4-диметоксибицикло[4.2.0]окта-1,3,5 триен-7-ил)нитрил формулы (Ib) путем хиральной хроматографии. 2. Способ по п.1, который характеризуется тем, что используют непрерывный многоколонный способ разделения. 3. Способ по одному из пп.1 или 2, который характеризуется тем, что используют способ хроматографии с псевдодвижущимся слоем. 4. Способ по одному из пп.1-3, который характеризуется тем, что неподвижная фаза, используемая для хиральной хроматографии, содержит силикагель, пропитанный функционализированным полисахаридом. 5. Способ по одному из пп.1-4, который характеризуется тем, что неподвижная фаза, используемая для хиральной хроматографии, содержит целлюлозное или амилозное производное трис(4 метилбензоата) или трис(3,5-диметилфенилкарбамата). 6. Способ по одному из пп.1-5, который характеризуется тем, что подвижная фаза, используемая для хиральной хроматографии, содержит спирт, другой органический растворитель или смесь спирта и другого органического растворителя. 7. Способ по п.6, который характеризуется тем, что используемый спирт представляет собой изопропанол.-4 015777 8. Способ по любому из пп.6 или 7, который характеризуется тем, что используемый органический растворитель представляет собой гептан или гексан. 9. Способ по любому из пп.6-8, который характеризуется тем, что подвижная фаза содержит смесь спирта и другого органического растворителя. 10. Способ по п.9, который характеризуется тем, что подвижная фаза содержит смесь изопропанола и гептана или смесь изопропанола и гексана. 11. Способ по п.10, который характеризуется тем, что подвижная фаза содержит смесь изопропанола и гептана или смесь изопропанола и гексана в соотношении, изменяющемся от 50:50 до 2:98. 12. Способ по одному из пп.1-11, который характеризуется тем, что подвижную фазу, используемую для хиральной хроматографии, используют повторно. 13. Способ по одному из пп.1-12, который характеризуется тем, что хиральную хроматографию осуществляют при температуре от 15 до 40 С включительно. 14. Способ по одному из пп.1-13, который характеризуется тем, что разделение оптических изомеров осуществляют на рацемической смеси (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила формулы (I). 15. Способ по одному из пп.1-14, который характеризуется тем, что целевым энантиомером (3,4 диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила является (S)-(3,4-диметоксибицикло[4.2.0]окта 1,3,5-триен-7-ил)нитрил формулы (Ia). 16. Способ по одному из пп.1-15, который характеризуется тем, что (R) энантиомер (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила формулы (Ib) рацемизируют и используют в качестве исходного вещества в способе разделения оптических изомеров. 17. Соединение формулы (Ia) 19. Способ синтеза соединения формулы (V) который характеризуется тем, что соединение формулы (Ia) подвергают восстановительной реакции. 20. Способ синтеза по п.19, который характеризуется тем, что восстановление соединения формулы(Ia) осуществляют в присутствии палладия на угле и HCl в атмосфере водорода или в присутствии тетраборогидрида натрия и трифторуксусной кислоты. 21. Способ синтеза ивабрадина, его фармацевтически приемлемых солей и их гидратов, который характеризуется тем, что соединение формулы (I) подвергают способу разделения оптических изомеров по п.1, получая соединение формулы (Ia) в соответствии со способом по п.19, которое превращают в карбамат формулы (VI) который восстанавливают, получая соединение формулы (III) или 3-3-(7S)-3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил]метил(метил)амино]пропил 7,8-диметокси-1,3,4,5-тетрагидро-2H-3-бензазепин-2-он, который может быть необязательно превращен в его соль присоединения с фармацевтически приемлемой кислотой, выбранной из хлористо-водородной кислоты, бромисто-водородной кислоты, серной кислоты, фосфорной кислоты, уксусной кислоты, трифторуксусной кислоты, молочной кислоты, пировиноградной кислоты, малоновой кислоты, янтарной кислоты, глутаровой кислоты, фумаровой кислоты, винной кислоты, малеиновой кислоты, лимонной кислоты, аскорбиновой кислоты, щавелевой кислоты, метансульфоновой кислоты, бензолсульфоновой кислоты и камфорной кислоты, или в его гидрат.
МПК / Метки
МПК: C07C 255/47, C07D 223/16, C07B 57/00
Метки: разделения, синтезе, применение, способ, 3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила, энантиомеров, ивабрадина
Код ссылки
<a href="https://eas.patents.su/7-15777-sposob-razdeleniya-enantiomerov-34-dimetoksibiciklo420okta-135-trien-7-ilnitrila-i-primenenie-pri-sinteze-ivabradina.html" rel="bookmark" title="База патентов Евразийского Союза">Способ разделения энантиомеров (3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)нитрила и применение при синтезе ивабрадина</a>
Предыдущий патент: Способ получения экстракционной фосфорной кислоты
Следующий патент: Фосфорсодержащая формовочная смесь для получения литейной формы для металлообработки
Случайный патент: Мутантные белки (мутеины) фактора роста фибробластов 21











