Способ получения ингибиторов фосфодиэстеразы iv
Формула / Реферат
1. Способ получения соединения структурной формулы 1

который включает стадии:
1) обработки соединения структурной формулы 2

катализатором, Ni(acac)2, в простом эфирном растворителе при -35 - -15шС с последующей обработкой цинкатом формулы R13M и выдерживанием в течение 20-30 ч, с получением аддукта 4
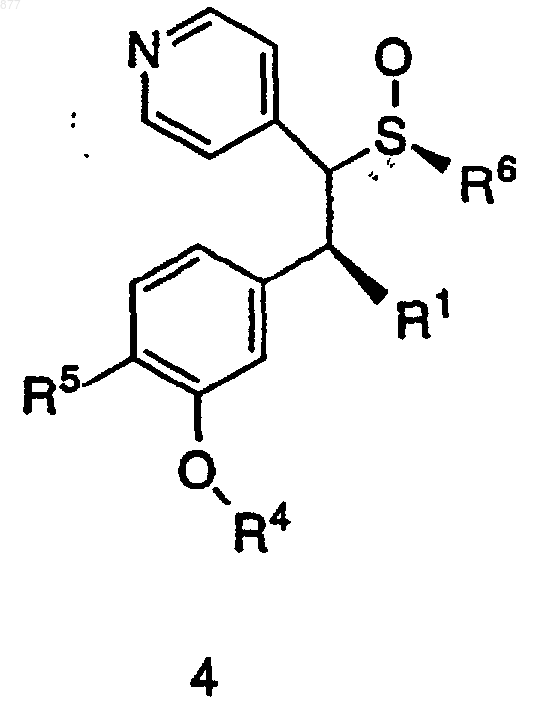
2) обработки аддукта 4 в простом эфирном растворителе и органической кислоте металлическим Zn, с получением продукта 1, где
R1 обозначает C1-6алкил, С2-6алкенил, фенил, незамещенный или замещенный одним или двумя заместителями, которые могут быть одинаковыми или разными, выбранными из группы, состоящей из R2 и Alk(R2)m,
где R2 обозначает
1) галоген,
2) -N(R3)2,
3) -NO2,
4) -CN,
5) -OR3,
6) -С3-6циклоалкокси,
7) -CO(R3),
8) -COOR3,
9) -SR3,
10) -SО3Н,
11) -SO2(R3),
12) -SO2N(RЗ)2,
13) -CON(R3)2,
14) -NHSO2R3,
15) -N(SO2R3)2,
16) -NHSO2N(RЗ)2,
17) -NHCOR3 или
18) -NHCOOR3;
где Alk обозначает прямой или разветвленный C1-6алкилен, С2-6алкенилен или
С2-6алкинилен, необязательно прерванный одной, двумя или тремя группами, -О-, -S-, -S(O)p или -N-(R3)-;
R3 обозначает водород или C1-6алкил или С2-6алкенил;
R4 обозначает
1) С3-6циклоалкил,
2) C1-6алкил или
3) C1-6алкенил;
R5 обозначает
1) галоген,
2) СF3,
3) C1-3алкил или
4) C1-3алкокси;
R6 обозначает
1) толил,
2) фенил,
3) трет-бутил или
4) мезитил;
М обозначает ZnLi или ZnMgBr;
m обозначает ноль или целое число, выбранное из 1, 2 и 3; и
р обозначает целое число, выбранное из 1 и 2.
2. Способ по п.1, где М обозначает ZnMdBr.
3. Способ по п.2, где R1 обозначает фенил.
Текст
1 Предпосылки изобретения Данная заявка направлена на усовершенствованный способ получения ингибиторов фосфодиэстеразы IV, таких как ингибиторы, описанные в WO 94/14742, опубликованной 7 июля 1994. Многие гормоны и нейротрансмиттеры модулируют функцию ткани путем повышения уровней внутриклеточного содержания аденозин-3',5'-циклического монофосфата (сАМР). Роль циклического АМР (сАМР) как вторичного мессенджера хорошо известна. Он ответственен за трансдукцию эффектов разнообразных внеклеточных сигналов, включая гормоны и нейротрансмиттеры. Содержание внутриклеточного сАМР регулируется как путем его синтеза аденилциклазами, так и путем разложения циклическими нуклеотидфосфодиэстеразами (PDE).PDE образуют семейство, по меньшей мере,семи изотипов ферментов (I-VII), которые отличаются по своему сродству к сАМР и/илиEndocrine Rev. 12 218-234). Клинические эффекты ряда лекарств могут быть рационализированы на основе их селективности по отношению к конкретному изотипу PDE. Например, кардиотонические лекарства милринон и запринаст являются ингибиторами PDE III и PDE V, соответственно. (Harrison S.A. et al., (1986) Mol.J. (1989) Mol. Pharmacol. 36 773-781). Антидепрессивное средство ролипрам действует как селективный ингибитор PDE IV. (Schneider Н.Н.et al., (1986) Eur. J. Pharmacol. 127 105-115) . Доступность селективных ингибиторов изотипа PDE дала возможность исследовать роль PDE в разных типах клеток. В частности,установлено, что PDE IV регулирует разложение сАМР во многих воспалительных клетках,например, базофилах (Peachell Р.Т. et al., (1992)G. et al., (1991) Br. J. Pharmacol. 103 1339-1346),и что ингибирование этого изотипа ассоциируется с ингибированием клеточной активации. Поэтому в настоящее время разрабатываются ингибиторы PDE IV в качестве потенциальных противовоспалительных лекарств, в частности,для профилактики и лечения астмы. Известный ранее способ получения соединения I показан на следующей схеме реакции: Этот способ, включающий разделение на энантиомеры в качестве последней стадии, непременно означает промышленно неприемлемый выход продукта. В другом ранее известном способе используется стратегия синтеза с применением 2Sборнан-010,2-сультама в качестве хирального вспомогательного вещества, как показано ниже 4 путем обработки соединения 2 соединением(R1)3 М с последующим восстановительным удалением сульфинильной группы. Подробное описание изобретения Новый способ данного изобретения описывается следующим образом: где Этот способ неприемлем для увеличения масштабов производства продукта из-за а) высокой цены сультама; в) легкой изомеризации хлорангидрида кислоты во время его получения и/или реакции сочетания с сультамом и с) проблемы крайне сильного запаха во время отщепления сультама с использованием энантиола. В настоящее время благодаря данному изобретению предоставляется хиральный синтез, который дает cоединение 1 с высоким выходом и высоким энантиомерным избытком. Краткое описание изобретения Данное изобретение касается нового способа получения соединения структурной формулы 1 где R1 обозначает фенил, замещенный фенил,C1-6 алкил или С 2-6 алкенил, являющегося важным антиастматическим средством, который включает ключевую стадию присоединения R1 к промежуточному соединению 2:R1 обозначает C1-6 алкил, С 2-6 алкенил, фенил, незамещенный или замещенный одним или двумя заместителями, которые могут быть одинаковыми или разными, выбранными из группы,состоящей из R2 и Alk(R2)m, гдеAlk обозначает прямой или разветвленныйC1-6 алкилен, С 2-6 алкенилен или С 2-6 алкинилен, необязательно прерванный одной, двумя или тремя группами -О-,-S-, -S(O)p или -N(R3)-;R3 обозначает водород или C1-6 алкил или С 2-6 алкенил;m обозначает ноль или целое число, выбранное из 1, 2 и 3; и р обозначает целое число, выбранное из 1 и 2. Способ включает обработку олефина 2 и катализатора,ацетилацетоната никеля,Ni(acac)2, в простом эфирном растворителе,таком как THF (тетрагидрофуран), диэтиловый эфир, глиль или диглим, предпочтительно THF,охлаждение до около -35 до -15 С и добавление суспензии цинката, (R1)3 М в том же простом эфирном растворителе также при -35 до -15 С при поддержании температуры ниже примерно-15 С. После выдерживания в течение 20-30 ч смесь гасят раствором хлорида аммония и этилацетатом и доводят рН до около 10 основанием,таким как гидроксид аммония, гидроксид натрия или калия, карбонат натрия или калия. Продукт 4 выделяют из органического слоя,растворяют в простом эфирном растворителе,предпочтительно THF, и органической кислоте,такой как уксусная кислота, пивалиновая кислота, трифторуксусная, хлоруксусная кислота или пропионовая кислота и обрабатывают металлическим цинком. После гашения реакции водой добавляют несмешиваемый органический растворитель, такой как метиленхлорид, хлороформ, толуол или этилацетат и доводят рН до около 6. Продукт 1 выделяют из органического слоя. Исходный материал 2 получают согласно следующей схеме реакции: 6 Все подробности получения соединения 2 представлены в следующем ниже примере. В данной заявке "алкил" обозначает линейный или разветвленный алкил с указанным числом атомов углерода. "Галоген" обозначает хлор, бром, фтор или иод. Пример. Синтез толилсульфинил-пиколина 2b Материалы 4-Пиколин н-BuLi Ментилтолуолсульфинат 2 а Раствор пиколина в THF (351 мл) охлаждался до -50 С и обрабатывался н-BuLi при поддержании внутренней температуры -45 С. Темно-оранжевая реакционная смесь подогревалась до температуры окружающей среды и выдерживалась в течение 1 ч. Полученный темный раствор обрабатывался при 22 С раствором сульфината в THF (120 мл) при поддержании температуры 27 С. Реакционная смесь выдерживалась в течение 30 мин, после чего анализ ЖХВР показал исчезновение сульфината 2 а. Реакционная смесь гасилась 1 М водным раствором NH4Cl (700 мл), добавлялся СН 2 Сl2 (1000 мл), и слои разделялись. Органический слой сушился над Na2SO4 и концентрировался в вакууме. Остаток промывался дважды гексаном(2 х 200 мл) и затем разделялся гексанами (220 мл, 9 мл/г на основе теоретического выхода),давая густую белую суспензию, которая оставлялась на ночь. Смесь фильтровалась, осадок на фильтре промывался гексанами (50 мл) и сушился в вакууме при 38 С, давая 21,46 г продукта (91%). Синтез альдольного аддукта 2d Материалы Циклопентилизованилин 2 с Толилсульфинил-пиколин 2b Трет-амил ONa Гетерогенную смесь альдегида и сульфоксида в THF (235 мл) охлаждали до -15 С и обрабатывали твердым трет-амил-ONa, в результате чего температура повышалась до -8 С. Анализ ЖХВР [образец должен был быть погашен в смеси СН 3 СN/1 н.-NH4Cl (водн.), чтобы избежать ретроальдольной реакции, которая происходит в водном основании] показывает, что реакция завершилась за 15 мин. Смесь гасили(800 мл), слои разделили и органический слой сушили над Na2SO4, фильтровали и концентрировали в вакууме. Остаток промывался гептаном (150 мл), и затем добавлялось 340 мл смеси 2:1 гептан-изопропилацетат (8 мл/г на основе теоретического выхода), и смесь оставлялась на 3 ч. Смесь фильтровалась, и осадок на фильтре промывался гептаном (100 мл) и сушился в вакууме при 36 С, давая 38,8 г продукта (93%) в виде единственного диастереомера.(3:2, 430 мл) охлаждался до 0 С и затем обрабатывался последовательно тозилимидазолом,NaH и имидазолом. Осуществлялся эффективный отвод газа из реакционного сосуда, чтобы обеспечить выделение водорода. Смесь выдерживалась в течение 2 ч, за это время анализ ЖХВР показал, что остается 2% исходного материала. Реакционная смесь гасилась Н 2 О (60 мл), распределялась между этилацетатом (500 мл) и Н 2 О (400 мл), и органический слой сушился над Na2SO4, фильтровался и концентрировался в вакууме. Остаток суспендировался в 365 мл смеси 2:1 гептан-изопропилацетат, и суспензию оставляли на ночь. Фильтрование, промывка смесью 2:1 гептан-изопропилацетат (100 мл) и сушка давали 24,75 г соединения 2 (66%). Синтез аддукта 4 Материалы 2 Раствор ZnCl2 в THF (0,5 М раствор) при 0 С обрабатывался PhMgBr так, чтобы температура оставалась ниже 10 С. Полученную суспензию выдерживали при 0 С в течение 15 мин и при температуре окружающей среды в течение 10 мин. Затем смесь охлаждалась до -25 С. Присоединение. Раствор олефина-2 и Ni(acac)2 в THF (3,5 мл) охлаждался до -25 С и обрабатывался полученной выше суспензией Рh3ZnMgBr так, чтобы внутренняя температура оставалась -22 С. Смесь выдерживалась при -27 С в течение 25 ч, после чего анализ ЖХВР показал, что осталось 4 А% соединения 2. Смесь гасилась NH4Cl(30 мл) , добавлялся этилацетат (50 мл), и величина рН доводилась до около 10 с помощьюNH4OH. Органический слой отделялся и сушился над Na2SO4, фильтровался и концентрировался в вакууме. Остаток растворялся в 2,8 мл THF и 0,4 мл уксусной кислоты и обрабатывался металлическим Zn (160 мг) при температуре окружающей cреды. Реакционная смесь выдерживалась в течение 1 ч при 25 С, анализ ЖХВР показал полный расход исходного материала. Реакционная смесь гасилась Н 2 О, добавлялсяCH2Cl2, и рН доводилась до около 6, давая два четких слоя. [Анализ ЖХВР показал минимальные потери продукта в водном слое]. Органический слой сушился над Na2SO4, фильтровался и концентрировался в вакууме. Хроматография(62%). Анализ хиральной ЖХВР показал энантиомерный избыток 92% (ее). ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения соединения структурной формулы 1 который включает стадии: 1) обработки соединения формулы 2 катализатором, Ni(acac)2, в простом эфирном растворителе при -35 - -15 С с последующей обработкой цинкатом формулы R13M и выдерживанием в течение 20-30 ч, с получением аддукта 4 2) обработки аддукта 4 в простом эфирном растворителе и органической кислоте металлическим Zn, с получением продукта 1, гдеR1 обозначает C1-6 алкил, С 2-6 алкенил, фенил, незамещенный или замещенный одним или двумя заместителями, которые могут быть одинаковыми или разными, выбранными из группы,состоящей из R2 и Alk(R2)m,где R2 обозначает 1) галоген,2) -N(R3)2,3) -NO2,4) -CN,5) -OR3,6) -С 3-6 циклоалкокси,7) -CO(R3),8) -COOR3,9) -SR3,10) -SО 3 Н, 9 11) -SO2(R3),12) -SO2N(RЗ)2,13) -CON(R3)2,14) -NHSO2R3,15) -N(SO2R3)2,16) -NHSO2N(RЗ)2,17) -NHCOR3 или 18) -NHCOOR3; где Alk обозначает прямой или разветвленныйC1-6 алкилен, С 2-6 алкенилен или С 2-6 алкинилен, необязательно прерванный одной, двумя или тремя группами, -О-, -S-,-S(O)p или -N-(R3)-;R3 обозначает водород или C1-6 алкил или С 2-6 алкенил;m обозначает ноль или целое число, выбранное из 1, 2 и 3; и р обозначает целое число, выбранное из 1 и 2. 2. Способ по п.1, где М обозначает ZnMgBr. 3. Способ по п.2, где R1 обозначает фенил.
МПК / Метки
МПК: A61K 31/4409, C07D 213/30, A61P 11/06
Метки: ингибиторов, фосфодиэстеразы, способ, получения
Код ссылки
<a href="https://eas.patents.su/6-877-sposob-polucheniya-ingibitorov-fosfodiesterazy-iv.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения ингибиторов фосфодиэстеразы iv</a>
Предыдущий патент: Способ получения этанола
Следующий патент: Производные циклоалкиламинометилпирролидина
Случайный патент: Продукты с сахарным покрытием и способ их приготовления










