Соль базедоксифена и фумаровой кислоты
Формула / Реферат
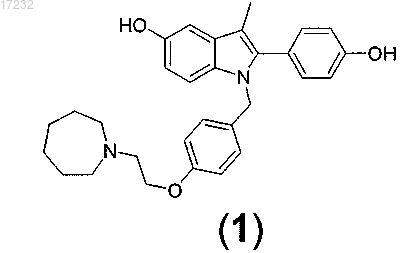
1. Соль 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 (базедоксифена) и двухосновной карбоновой кислоты, причем кислота представляет собой фумаровую кислоту
2. Соль по п.1, где соотношение базедоксифена и кислоты составляет 2:1.
3. Соль по п.2, которая представляет собой фумарат базедоксифена в кристаллической форме.
4. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы А, отличающаяся следующими отражениями на дифракционной рентгенограмме: 8,31; 10,38; 12,78; 13,69; 14,72; 21,53; 22,27; 23,24.
5. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы А, отличающаяся температурой плавления, находящейся в интервале температур от 221 до 224°C.
6. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы А, отличающаяся максимумом при 216°C по данным дифференциальной сканирующей калориметрии.
7. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы В, отличающаяся следующими отражениями на дифракционной рентгенограмме: 5,32; 11,93; 12,85; 14,58; 15,87; 18,40; 19,34; 19,73; 20,47; 21,18; 23,63; 24,50.
8. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы В, отличающаяся температурой плавления, находящейся в интервале температур от 216 до 218°C.
9. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы В, отличающаяся максимумом при 211,4°C по данным дифференциальной сканирующей калориметрии (полиморфная форма В).
10. Соль по любому из пп.4-6 в смеси с солью по любому из пп.7-9 в любых соотношениях.
11. Способ очистки 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола, отличающийся тем, что он включает получение соли свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 и фумаровой кислоты.
12. Способ по п.11, отличающийся тем, что он включает получение соли свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 и фумаровой кислоты с соотношением компонентов 2:1.
13. Применение соли по любому из пп.1-10 для получения фармацевтически пригодных композиций.
Текст
Изобретение относится к новой кристаллической соли базедоксифена, представляющей собой фумарат базедоксифена, посредством которой можно получать активный фармацевтический ингредиент (АФИ) высокого качества с большим выходом. 017232 Область техники Изобретение относится к новой кристаллической соли селективного модулятора эстрогеновых рецепторов 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола и двухосновной карбоновой кислоты, причем кислота представляет собой фумаровую кислоту, и в частности к соли с соотношением компонентов 2:1. Предшествующий уровень техники Базедоксифен принадлежит к селективным модуляторам эстрогеновых рецепторов (СМЭР). Более подробное описание их биологической активности можно найти в источнике Drugs of the Future (Лекарственные средства будущего), 2002, 27(2), 117-121. Получение базедоксифена и его ацетата было опубликовано в патентах США 5998402 и 6479535. Получение базедоксифена также было опубликовано в J. Med. Chem. 2001, 44, 1654-1657. В US 2005/0227965 А 1 сравниваются два кристаллических полиморфа ацетата базедоксифена. В US 2005/0227964 описан аскорбат базедоксифена и его применение. При использовании вещества в фармацевтических целях предъявляются серьезные требования к его качеству. Наиболее эффективным способом очистки является кристаллизация. В случае веществ, не способных к кристаллизации, очень трудно соответствовать всемирно одобренным критериям качества, установленным Международной конференцией по гармонизации (ICH). Кроме того, аморфные формы веществ в большей степени подвержены разложению, в частности гидролизу или окислению, вследствие большой поверхности вещества. Согласно хорошо известной и подтвержденной информации базедоксифен и его производные, известные к настоящему времени, можно классифицировать как вещества, сложно поддающиеся очистке и склонные к разложению. Базедоксифен, так же как и аскорбат базедоксифена, представляют собой некристаллические формы, получаемые концентрированием раствора до сухого остатка. Вследствие этого, в полученном остатке присутствуют все нежелательные нелетучие вещества, образующиеся либо в ходе синтеза, либо в результате разложения активного фармацевтического ингредиента (АФИ). Главным образом это 2-(4 гидроксифенил)-3-метил-1H-индол-5-ол формулы 2 и 1-[4-(2-азепан-1-ил-этокси)бензил]-5-бензилокси 2-(4-гидроксифенил)-3-метил-1H-индол формулы 3, образующиеся в ходе синтеза, и 1-(4 гидроксибензил)-2-(4-гидроксифенил)-3-метил-1H-индол-5-ол формулы 4 и 1-[4-(2-азепан-1-илэтокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ол N-оксид формулы 5, образующиеся вследствие разложения базедоксифена. Предположительно получение базедоксифена в виде кристаллического ацетата также не решает проблемы с качеством. Присутствие даже малых количеств указанных выше или иных примесей препятствует кристаллизации ацетата базедоксифена, получаемого согласно патентным документам US 5998402; US 6479535 или US 2005/0227965. Ацетат можно с успехом получать в аморфной форме с помощью модифицированного способа с выходом около 40%. Ацетат подвергают разложению с образова-1 017232 нием нежелательных примесей, главным образом окислению, в результате которого образуется нежелательное вещество формулы 5. Для подавления данного процесса разложения обычно добавляют в качестве антиоксиданта аскорбиновую кислоту. По этой причине ведутся поиски более подходящей формы базедоксифена, получаемой простым способом с высоким выходом и качество которой соответствует АФИ, и, в то же время, не подвергающейся нежелательному разложению. Описание изобретения Изобретение относится к новой стабильной кристаллической соли 1-[4-(2-азепан-1-илэтокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола (базедоксифена) и кислоты, содержащей две карбоксильные группы, причем кислота представляет собой фумаровую кислоту, а также к способу получения такой соли, отличающемуся взаимодействием 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4 гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 с двухосновной карбоновой кислотой в подходящем растворителе. Указанный способ, в котором легко достигается химическая чистота продукта 99,9% и выше, а содержание отдельных примесей составляет ниже 0,1%, описывается равенством на схеме 1. Кроме того, обнаружили экономически выгодный способ производства данных солей, который можно также применять в промышленном масштабе. Схема 1 С химической точки зрения наш продукт представляет собой соль, содержащую компонент, характеризуемый формулой 1, и двухосновную карбоновую кислоту (R(COOH)2, состоящую из 2 карбоксильных функциональных групп, причем кислота представляет собой фумаровую кислоту. Способ получения вещества формулы 6 отличается использованием подходящего растворителя. Выбор растворителя зависит от растворимостей исходных веществ и продукта, и особенно от способности продукта формировать прочную кристаллическую решетку в данном растворителе. В качестве растворителей можно использовать C1-C5 спирты (например, метанол, этанол, 1-пропанол, 2-пропанол, бутанолы), сложные эфиры карбоновых кислот (например, этилацетат), простые эфиры (например, диоксан, тетрагидрофуран или диэтиловый эфир), кетоны (например, ацетон или циклобутанон), ацетонитрил, их любые смеси и смеси с водой в любых пропорциях. Предпочтительное воплощение изобретения включает использование этанола или его смесей с водой, с этилацетатом или с толуолом в качестве растворителя в соотношениях от 97,5:2,5 до 90:10. Доказано, что выбранный способ приводит к получению кристаллической соли соединения формулы 6, содержащей соединение формулы 1 и фумаровую кислоту. Наиболее предпочтительная форма соли представляет собой соотношение 2:1. Предпочтительная форма соли соединения формулы 6 представляет собой кристаллическую форму,являющуюся химически стабильной, с высокой степенью химической чистоты (выше 99,5% согласно результатам ВЭЖХ), которую можно получить с высокими выходами в определенной кристаллической модификации и которая характеризуется размером частиц, подходящим для дальнейшей обработки. Этим условиям удовлетворяют кристаллические формы соли базедоксифена формулы 1 и фумаровой кислоты. Кристаллическая структура упомянутой соли формулы 6 была однозначно охарактеризована следующими аналитическими методами: порошковой рентгеновской дифракцией (здесь и далее ПРД), определением температуры плавления и дифференциальной сканирующей калориметрией (здесь и далее ДСК). Результаты исследования представлены в примерах и приложенных фигурах. Особенно выгодно получать кристаллическую форму соли соединения формулы 6 по настоящему изобретению, используя в качестве растворителя спирты (C1-C5) или их смеси с толуолом, диметилформамидом (ДМФ) или этилацетатом в соотношениях от 90:10 до 95:5. Способ приводит к образованию исключительно определенной кристаллической модификации (установленной с помощью ДСК и ПРД) с определенным размером частиц, и, дополнительно, данный способ характеризуется высоким качеством продукта и большими выходами, которые воспроизводятся. Указанные выше характеристики кристаллической соли соединения формулы 6 являются очень выгодными с точки зрения их производства и фармацевтического использования. Применяемый способ многократно приводил к получению с выходами от 90 до 95% кристаллической соли фумаровой кислоты и 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1Hиндол-5-ола, характеризующейся высоким качеством (содержание по данным ВЭЖХ более 99,95%). Полученную соль фумаровой кислоты и 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3 метил-1H-индол-5-ола формулы 10 можно использовать для получения фармацевтически пригодных-2 017232 композиций. Объект изобретения далее иллюстрируется более подробно с помощью нижеприведенных примеров, не ограничивающих объем изобретения, защищаемый формулой. Краткое описание фигур На фиг. 1 показана порошковая дифракционная рентгенограмма кристаллической соли фумаровой кислоты и базедоксифена, полученной по примеру 2 (фумарат базедоксифена - полиморфная форма А). На фиг. 2 показана кривая ДСК для кристаллической соли фумаровой кислоты и базедоксифена,полученной по примеру 2 (фумарат базедоксифена - полиморфная форма А). На фиг. 3 показана порошковая дифракционная рентгенограмма кристаллической соли фумаровой кислоты и базедоксифена, полученной по примеру 3 (фумарат базедоксифена - полиморфная форма В). Примеры Пример 1. Получение 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-бензилоксифенил)-5-бензилокси-3 метил-1H-индола (бензилированный базедоксифен). В инертной атмосфере в ДМФ (80 мл) суспендировали NaH (2,7 г, 112 ммоль). При температуре 05C добавляли 5-бензилокси-2-(4-бензилоксифенил)-3-метил-1H-индол (11 г, 26 ммоль), далее суспензию перемешивали в течение 30 мин. Затем в течение 1 ч добавляли по каплям раствор 4-(2-азепан-1-илэтокси)бензилхлорида (8 г, 26 ммоль) в ДМФ (30 мл). Охлаждение отключили и реакционную смесь перемешивали в течение дополнительных 2,5 ч. Далее осторожно по каплям добавляли к реакционной смеси воду (1,2 мл) и реакционную смесь фильтровали через тонкий слой целлита. Дополнительные 35 мл воды добавляли по каплям к ярко-желтому фильтрату при интенсивном перемешивании. Выделившийся белый продукт фильтровали и промывали метанолом. Выход неочищенного продукта составлял 13,7 г (81%). Неочищенный продукт растворяли в 70 мл этилацетата с небольшим количеством активированного угля и фильтровали горячим. К фильтрату добавляли 100 мл метанола. Выход кристаллизации составлял 80,5%. Температура плавления = 109-112C. Содержание по ВЭЖХ 99,8%. Пример 2. Получение соли 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1Hиндол-5-ола и фумаровой кислоты в соотношении 2/1 (фумарат базедоксифена), полиморфная форма А. Исходное соединение, бензилированный базедоксифен формулы 7 (4 г, 6 15 ммоль), растворяли в этаноле (40 мл), затем в инертной атмосфере добавляли катализатор, 2,34%-Pd/C (0,4 г). Реакционную смесь перемешивали в атмосфере водорода в течение 5 ч. Катализатор отфильтровывали в инертной атмосфере через слой целлита. В полученный чистый бесцветный фильтрат вводили затравку фумарата базетоксифена формулы 6 (0,1 г). Затем к раствору по каплям в течение 30 мин добавляли раствор фумаровой кислоты (0,36 г, 3,075 ммоль) в этаноле (10 мл). Выделившийся белый кристаллический продукт отфильтровывали и сушили в потоке азота при температуре 50C. Получали 3 г (93%) кристаллического фумарата (полиморфная форма А) со степенью чистоты по данным ВЭЖХ 99.95%. Температура плавления = 221-224C. Пример 3. Получение соли 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1Hиндол-5-ола и фумаровой кислоты в соотношении 2/1 (фумарат базедоксифена), полиморфная форма В. Исходное соединение, бензилированный базедоксифен формулы 7 (4 г, (3,15 ммоль), растворяли в смеси этанол/этилацетат (95:5) (40 мл), затем в инертной атмосфере добавляли катализатор, 2,34%-Pd/C(0,4 г). Реакционную смесь перемешивали в атмосфере водорода в течение 5 ч. Катализатор отфильтровывали в инертной атмосфере через слой целлита. В полученный чистый бесцветный фильтрат вводили затравку фумарата базедоксифена формулы 6 (0,1 г). Затем к раствору по каплям в течение 30 мин добавляли раствор фумаровой кислоты (0,36 г, 3,075 ммоль) в этаноле (10 мл). Выделившийся белый кристаллический продукт отфильтровывали и предварительно сушили сначала в потоке азота, а затем окончательно сушили в вакуумной сушилке при давлении 15 мбар и температуре 100C. Получали 3,1 г (95%) кристаллического фумарата (полиморфная форма В). Температура плавления = 216-218C. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соль 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 (базедоксифена) и двухосновной карбоновой кислоты, причем кислота представляет собой фумаровую кислоту 2. Соль по п.1, где соотношение базедоксифена и кислоты составляет 2:1. 3. Соль по п.2, которая представляет собой фумарат базедоксифена в кристаллической форме. 4. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1Hиндол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы А, отличающаяся следующими отражениями на дифракционной рентгенограмме: 8,31; 10,38; 12,78; 13,69; 14,72; 21,53; 22,27; 23,24. 5. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1Hиндол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы А, отличающаяся температурой плавления, находящейся в интервале температур от 221 до 224C. 6. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1Hиндол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы А, отличающаяся максимумом при 216C по данным дифференциальной сканирующей калориметрии. 7. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1Hиндол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы В, отличающаяся следующими отражениями на дифракционной рентгенограмме: 5,32; 11,93; 12,85; 14,58; 15,87; 18,40; 19,34; 19,73; 20,47; 21,18; 23,63; 24,50. 8. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1Hиндол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы В, отличающаяся температурой плавления, находящейся в интервале температур от 216 до 218C. 9. Соль свободного основания 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1Hиндол-5-ола формулы 1 и фумаровой кислоты по п.3 в виде полиморфной формы В, отличающаяся максимумом при 211,4C по данным дифференциальной сканирующей калориметрии (полиморфная форма В). 10. Соль по любому из пп.4-6 в смеси с солью по любому из пп.7-9 в любых соотношениях. 11. Способ очистки 1-[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5 ола, отличающийся тем, что он включает получение соли свободного основания 1-[4-(2-азепан-1-илэтокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 и фумаровой кислоты. 12. Способ по п.11, отличающийся тем, что он включает получение соли свободного основания 1[4-(2-азепан-1-ил-этокси)бензил]-2-(4-гидроксифенил)-3-метил-1H-индол-5-ола формулы 1 и фумаровой кислоты с соотношением компонентов 2:1. 13. Применение соли по любому из пп.1-10 для получения фармацевтически пригодных композиций.
МПК / Метки
МПК: A61P 5/30, C07D 209/12, A61K 31/404
Метки: фумаровой, кислоты, соль, базедоксифена
Код ссылки
<a href="https://eas.patents.su/6-17232-sol-bazedoksifena-i-fumarovojj-kisloty.html" rel="bookmark" title="База патентов Евразийского Союза">Соль базедоксифена и фумаровой кислоты</a>
Предыдущий патент: Центробежный сепаратор (варианты) и способ его эксплуатации
Следующий патент: Машина штанговая для внесения минеральных удобрений
Случайный патент: Поверхностно-активные вещества и покрытия для применения в буровых растворах










