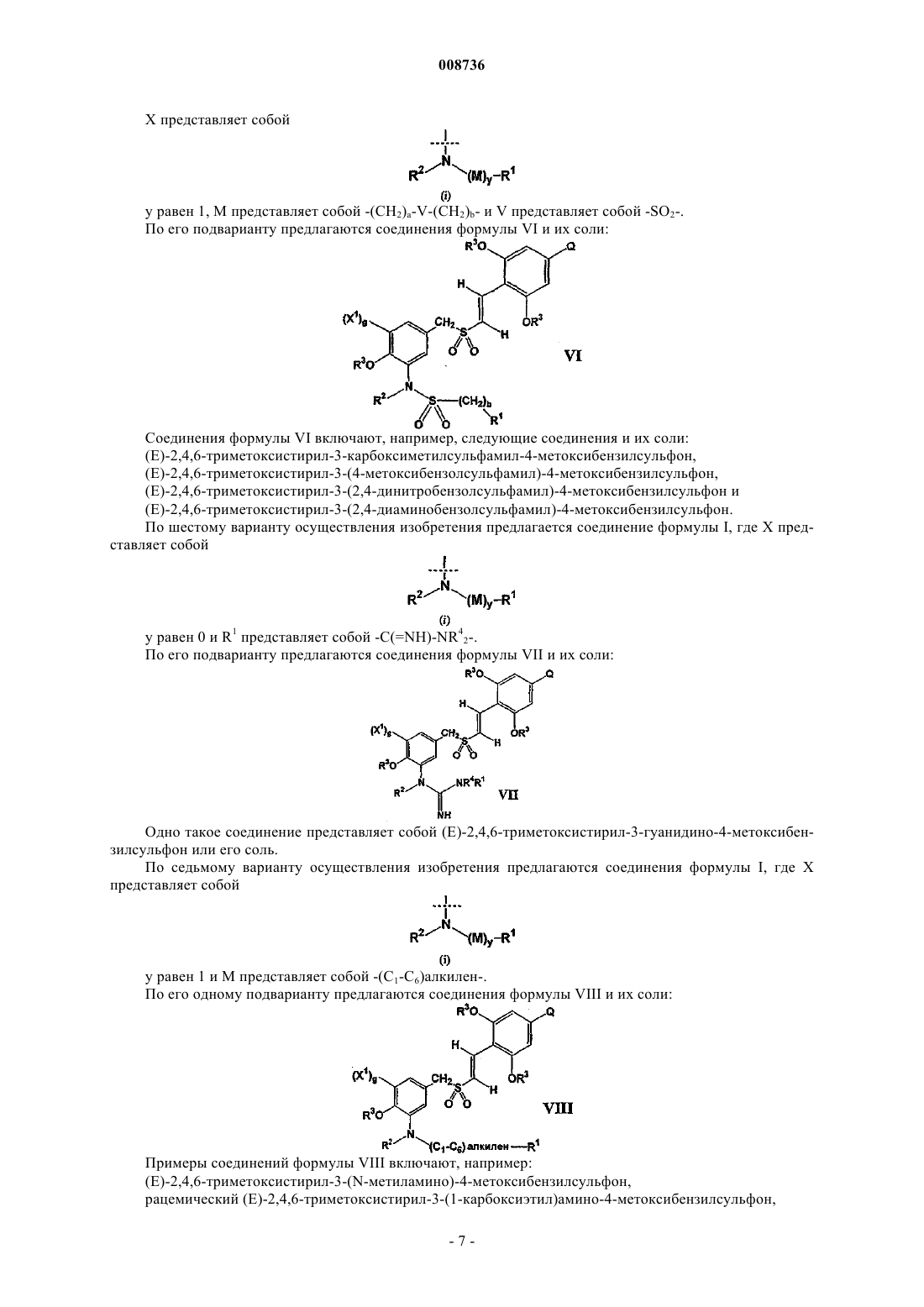
Аминозамещённые (е)-2,6-диалкоксистирил-4-замещённые-бензилсульфоны для лечения пролиферативных расстройств
Номер патента: 8736
Опубликовано: 31.08.2007
Авторы: Редди Рамана М.В., Белл Стэнли К., Редди Премкумар Э.
Формула / Реферат
1. Соединение формулы I
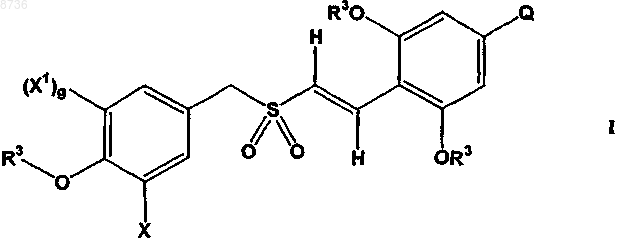
где X выбран из группы, состоящей из приведенных ниже (i) и (ii)

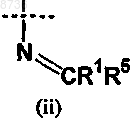
X1 выбран из группы, состоящей из приведенных ниже (i), (ii) и (iii)
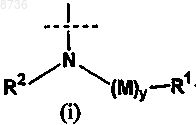
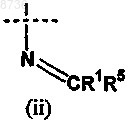
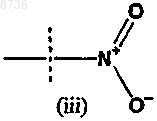
где X1 необязательно защищен одной или несколькими химическими защитными группами;
g равен 0 или 1;
каждый М представляет собой двухвалентную связывающую группу, независимо выбранную из группы, состоящей из -(С1-С6)алкилена-, -(СН2)a-V-(СН2)b-, -(СН2)d-W-(СН2)е- и -Z-;
каждый у независимо выбран из группы, состоящей из 0 и 1;
каждый V независимо выбран из группы, состоящей из арилена, гетероарилена, -С(=O)-, -C(=S)-,
-S(=O)-, -SO2-, -С(=O)O-, -С(=O)(С1-С6)перфторалкилена-, -C(=O)NR4-, -C(=S)NR4- и -SO2NR4-;
каждый W независимо выбран из группы, состоящей из -NR4-, -О- и -S-;
каждый а независимо выбран из группы, состоящей из 0, 1, 2 и 3;
каждый b независимо выбран из группы, состоящей из 0, 1, 2 и 3;
каждый d независимо выбран из группы, состоящей из 1, 2 и 3;
каждый е независимо выбран из группы, состоящей из 0, 1, 2 и 3;
-Z- представляет собой
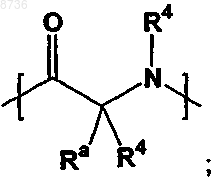
где абсолютная стереохимия -Z- представляет собой D или L или смесь D и L;
каждый Ra независимо выбран из группы, состоящей из -Н, -(С1-С6)алкила, -(СН2)3-NH-C(NH2)(=NH), -СН2С(=O)NH2, -CH2COOH, -CH2SH, -(CH2)2C(=O)-NH2, -(CH2)2COOH, -СН2-(2-имидазолила), -СН(СН3)-СН2-СН3, -СН2-СН(СН3)2, -(CH2)4-NH2, - (СН2)2-S-CH3, фенила, СН2-фенила,
-СН2-ОН, -СН(ОН)-СН3, -СН2-(3-индолила), -СН2-(4-гидроксифенила), -СН(СН3)2 и -СН2-СН3; и включает соединения, где Ra и R1 объединены с образованием 5-, 6- или 7-членного гетероциклического кольца;
каждый R1 независимо выбран из группы, состоящей из -Н, незамещенного арила, замещенного арила, замещенного гетероцикла, незамещенного гетероцикла, -CO2R5, -C(=O)NR42, -CR4R6R7, -C(=NH)-NR42, -(C1-C6)перфторалкила, -CF2Cl, -P(=O)(OR4)2, -OP(=O)(OR4)2 и одновалентной пептидильной части молекулы с молекулярной массой менее 1000; при условии, что когда у равен 0 и R1 представляет собой
-CO2R5, то R5 не является -Н;
каждый R2 независимо выбран из группы, состоящей из -Н, -(C1-С6)алкила и арил(С1-С3)алкила, где -R2 и - (М)y-R1 необязательно могут быть ковалентно связаны с образованием 5-, 6- или 7-членного замещенного или незамещенного гетероцикла;
каждый R3 независимо выбран из -(C1-С6)алкила;
каждый R4 независимо выбран из группы, состоящей из -Н и -(C1-С6)алкила;
каждый R5 независимо выбран из группы, состоящей из -Н, -(C1-С6)алкила и -(C1-С6)ацила;
каждый R6 независимо выбран из группы, состоящей из -Н, -(C1-C6)алкила, -CO2R5, -C(=O)R7, -OR5, -ОС(=O)(СН2)2CO2R5, -SR4, гуанидино, -NR42, -NR43+, -N+(CH2CH2OR5)3, фенила, замещенного фенила, гетероцикла, замещенного гетероцикла и галогена;
каждый R7 независимо выбран из группы, состоящей из Ra, галогена, -NR42 и гетероциклов, содержащих два атома азота; и
Q выбран из группы, состоящей из -Н, -(C1-С6)алкокси, галогена, -(C1-С6)алкила и -NR42;
где заместители замещенного арила и замещенных гетероциклических групп, содержащиеся или включенные в R1, R2, Ra, R6 и R7, независимо выбраны из группы, состоящей из галогена, -(C1-С6)алкила, -NO2, -CуN, -CO2R5, -С(=O)O(С1-С3)алкила, -OR5, -(С2-С6)алкилен-ОН, фосфонато, -NR42, -NHC(=O)(C1-С6)алкила, сульфамила, -ОС(=O)(C1-С3)алкила, -О(С2-С6)алкилен-N((C1-С6)алкила)2 и -CF3; при условии, что
(1) когда R1 представляет собой одновалентную пептидильную часть молекулы с молекулярной массой менее 1000 и V представляет собой -С(=O)-, -C(=S)-, -S(=O)- или -SO2-, и b равен 0,
тогда указанная пептидильная часть молекулы соединена с М через амино-конец пептидильной части молекулы или через аминогруппу боковой цепи с образованием амида, тиоамида, сульфинамида или сульфонамида, соответственно;
(2) когда R1 представляет собой одновалентную пептидильную часть молекулы с молекулярной массой менее 1000 и V представляет собой -C(=O)NR3-, -SO2NR3- или -NR4-, и b равен 0,
тогда указанная пептидильная часть молекулы соединена с М через карбоксиконец пептидильной части молекулы или через карбоксильную группу боковой цепи с образованием имида, сульфонимида или карбоксамида, соответственно; и
(3) когда R1 представляет собой одновалентную пептидильную часть молекулы с молекулярной массой менее 1000 и W представляет собой -S- или -O-, a d равен 0,
тогда указанная пептидильная часть молекулы соединена с М через карбоксиконец пептидильной части молекулы или через карбоксильную группу боковой цепи с образованием сложного эфира тиокарбоновой кислоты или сложного эфира карбоновой кислоты, соответственно;
или соль такого соединения; и где
термин "арил", используемый отдельно или в комбинации с другими терминами, означает карбоциклическую ароматическую систему, содержащую одно или несколько колец (типично одно, два или три кольца), где такие кольца могут быть присоединены в виде боковой группы или могут быть конденсированными;
термин "арилен", сам по себе или в качестве части другого заместителя, означает двухвалентный арильный радикал;
термин "гетероцикл", сам по себе или в качестве части другого заместителя, означает незамещенную или замещенную, стабильную моно- или полициклическую гетероциклическую кольцевую систему, которая состоит из атомов углерода и по меньшей мере одного гетероатома, выбранного из группы, состоящей из N, О и S, и где гетероатомы азота и серы могут быть необязательно окислены, а атом азота необязательно может быть кватернизирован;
термин "гетероарил" относится к гетероциклу, имеющему ароматический характер;
термин "гетероарилен", сам по себе или в качестве части другого заместителя, означает двухвалентный гетероарильный радикал;
термин "одновалентная пептидильная группа" относится к пептиднюьу радикалу в качестве заместителя в молекуле формулы I.
2. Соединение по п.1, выбранное из группы, состоящей из
(Е)-2,4,6-триметоксистирил-3-[4-(4-метилпиперазин-1-ил)бензамидо]-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(ацетоксиацетамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(триэтиламмонийацетамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-[три-(2-гидроксиэтиламмоний)ацетамидо]-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(2-метил-2-гидроксипропионамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(2-метил-2-ацетоксипропионамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(2-ацетоксипропионамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(трифторацетамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(трифторметансульфонамидо)-4-метоксибензилсульфона,
(E)-2,4,6-триметоксистирил-3-[3-(3-карбоксипропаноилокси)ацетамидо]-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(диэтилфосфонатоацетамидо)-4-метоксибензилсульфона,
динатриевой соли (Е)-2,4,6-триметоксистирил-3-(фосфонатоацетамидо)-4-метоксибензилсульфона,
(E)-2,4,6-триметоксистирил-3-(метилкарбамоил)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(пентафторпропионамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-[метил-(2,2-дифтор)малонамидо]-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(2,2-дифтормалонамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(диметиламино-a,a-дифторацетамидо)-4-метоксибензилсульфона и
(Е)-2,4,6-триметоксистирил-3-(2,2,3,3-тетрафторсукцинамидо)-4-метоксибензилсульфона,
или его фармацевтически приемлемая соль.
3. Соединение по п.1, где
каждый V независимо выбран из группы, состоящей из -С(=O)-, -C(=S)-, -S(=O)-, -SO2-, -C(=O)NR4-, -C(=S)NR4- и -SO2NR4-;
-Z- представляет собой
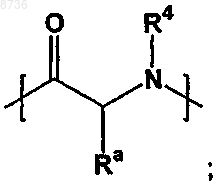
где абсолютная стереохимия -Z- представляет собой D или L;
каждый Ra независимо выбран из группы, состоящей из -Н, -СН3, -(CH2)3-NH-C(NH2)(=NH),
-СН2С(=O)NH2, -CH2COOH, -CH2SH, -(CH2)2C(=O)-NH2, -(СН2)2СООН, -СН2-(2-имидазолила), -СН(СН3)-СН2-СН3, -СН2-СН(СН3)2, -(CH2)4-NH2, -(СН2)2-S-CH3, фенила, СН2-фенила, -СН2-ОН, -СН(ОН)-СН3,
-СН2-(3-индолила), -СН2-(4-гидроксифенила), -СН(СН3)2 и -СН2-СН3; и включает соединения, где Ra и R1 объединены с образованием 5-, 6- или 7-членного гетероциклического кольца;
каждый R1 независимо выбран из группы, состоящей из -Н, незамещенного арила, замещенного арила, замещенного гетероцикла, незамещенного гетероцикла, -CO2R5, -C(=O)NR42, -CHR6R7, -C(=NH)-NR42 и одновалентной пептидильной части молекулы с молекулярной массой менее 1000; при условии, что когда у равен 0 и R1 представляет собой -CO2R5, то R5 не является -Н;
каждый R6 независимо выбран из группы, состоящей из -Н, -(С1-С6)алкила, -CO2R5, -C(=O)R7, -ОН, -SR4, -(C1-C3)алкокси, -(C1-С3)алкилтио, гуанидино, -NR42, фенила, замещенного фенила, гетероцикла, замещенного гетероцикла и галогена; и
каждый R7 независимо выбран из группы, состоящей из -Н, галогена, -(C1-С6)алкила, -NR42 и гетероциклов, содержащих два атома азота;
где заместители замещенного арила и замещенных гетероциклических групп, содержащиеся или включенные в R1, Ra, R6 и R7, независимо выбраны из группы, состоящей из галогена, -(C1-С6)алкила,
-(C1-C6)алкокси, -NO2, -СуN, -CO2R5, -С(=O)О(C1-C3)алкила, -ОН, -(С2-С6)алкилен-ОН, фосфонато, -NR42, -NHC(=O)(C1-С6)алкила, сульфамила, -ОС(=O)(C1-C3)алкила, -О(С2-С6)алкилен-N((C1-С6) алкила)2 и -CF3;
или соль такого соединения.
4. Соединение по п.3, выбранное из группы, состоящей из
(E)-2,4,6-триметоксистирил-4-метокси-3-аминобензилсульфона,
(Е)-2,4,6-триметоксистирил-4-метокси-3-нитробензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(карбоксиацетамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(3,5-динитробензамидо)-4-метоксибензилсульфона,
(E)-2,4,6-триметоксистирил-3-(3,5-диаминобензамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(хлорацетамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-[(4-метилпиперазинил)ацетамидо]-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(бензамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(4-нитробензамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(4-аминобензамидо)-4-метоксибензилсульфона,
(E)-2,4,6-триметоксистирил-3-(ацетамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(диметиламиноацетамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(гидроксиацетамидо)-4-метоксибензилсульфона,
(E)-2,4,6-триметоксистирил-3-(2-гидроксипропионамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(пиридиний-1-ил)ацетамидо-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(этилмалонамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(глутарамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(метилсукцинамидо)-4-метоксибензилсульфона,
(E)-2,4,6-триметоксистирил-3-(сукцинамидо)-4-метоксибензилсульфона,
(E)-2,4,6-триметоксистирил-3-(3-хлорсукцинамидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(аминоацетамидо)-4-метоксибензилсульфона,
(E)-2,4,6-триметоксистирил-3-амино-4-метоксибензилсульфон-L-лизинамида,
(Е)-2,4,6-триметоксистирил-3-амино-4-метоксибензилсульфон-L-серинамида,
(Е)-2,4,6-триметоксистирил-3-амино-4-метоксибензилсульфон-D-серинамида,
(Е)-2,4,6-триметоксистирил-3-(карбоксиметилсульфамил)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(4-метоксибензолсульфамил)-4-метоксибензилсульфона,
(E)-2,4,6-триметоксистирил-3-(2,4-динитробензолсульфамил)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(2,4-диаминобензолсульфамил)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-гуанидино-4-метоксибензилсульфона,
рацемического (Е)-2,4,6-триметоксистирил-3-(1-карбоксиэтил)амино-4-метоксибензилсульфона,
D-(Е)-2,4,6-триметоксистирил-3-(1-карбоксиэтил)амино-4-метоксибензилсульфона,
L-(Е)-2,4,6-триметоксистирил-3-(1-карбоксиэтил)амино-4-метоксибензилсульфона,
(E)-2,4,6-триметоксистирил-3-(карбоксиметиламино)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(N-метиламино)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(4-нитрофенилимино)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(уреидо)-4-метоксибензилсульфона,
(Е)-2,4,6-триметоксистирил-3-(3-карбоксипропиламино)-4-метоксибензилсульфона и
(Е)-2,4,6-триметоксистирил-3-(2-карбоксиэтиламино)-4-метоксибензилсульфона,
или соль такого соединения.
5. Соединение по п.4, уфх указанное соединение представляет собой (E)-2,4,6-триметоксистирил-3-(карбоксиметиламино)-4-метоксибензилсульфон, или соль такого соединения.
6. Соединение по п.5, где указанное соединение представляет собой натриевую или калиевую соль (Е)-2,4,6-триметоксистирил-3-(карбоксиметиламино)-4-метоксибензилсульфона.
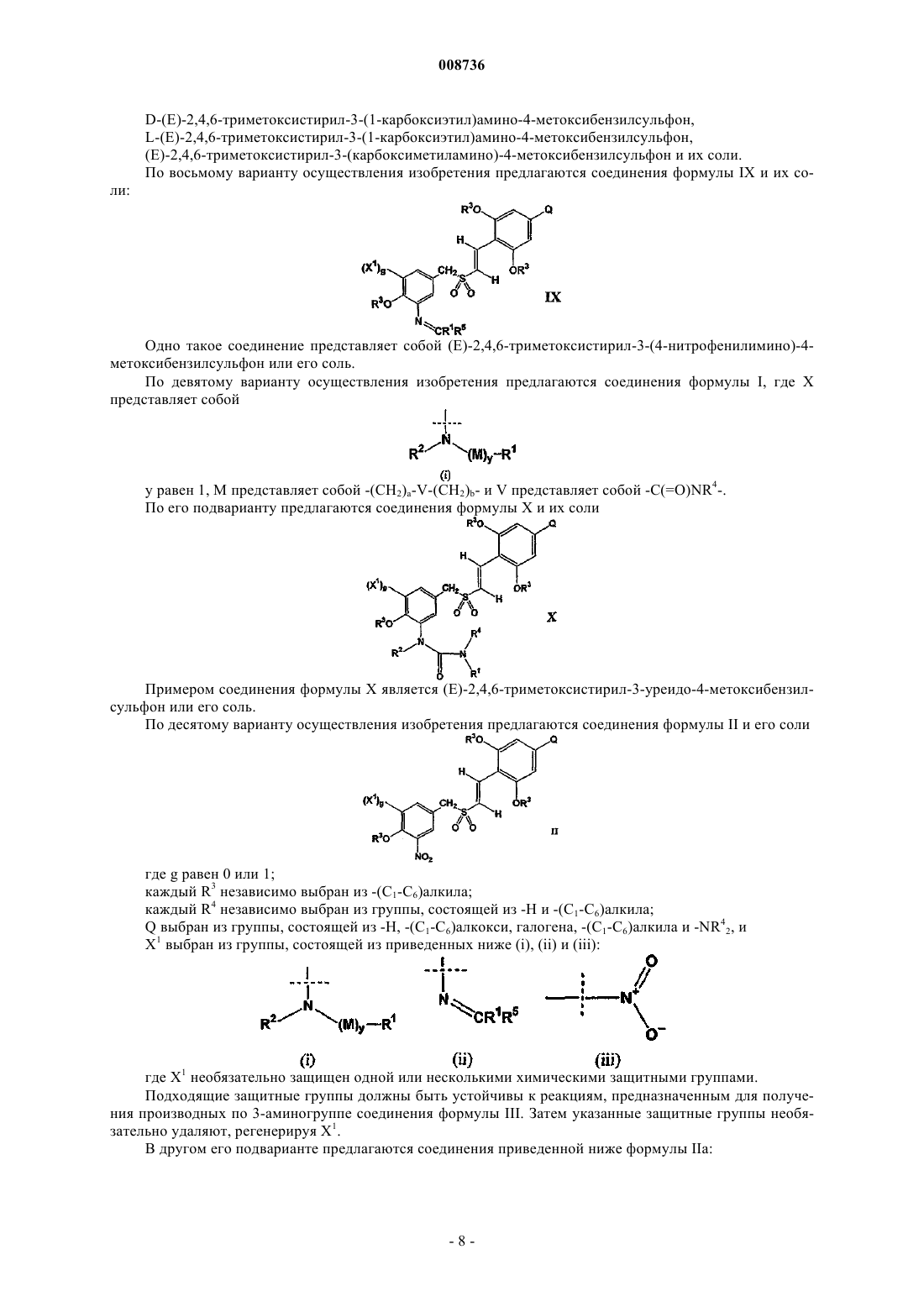
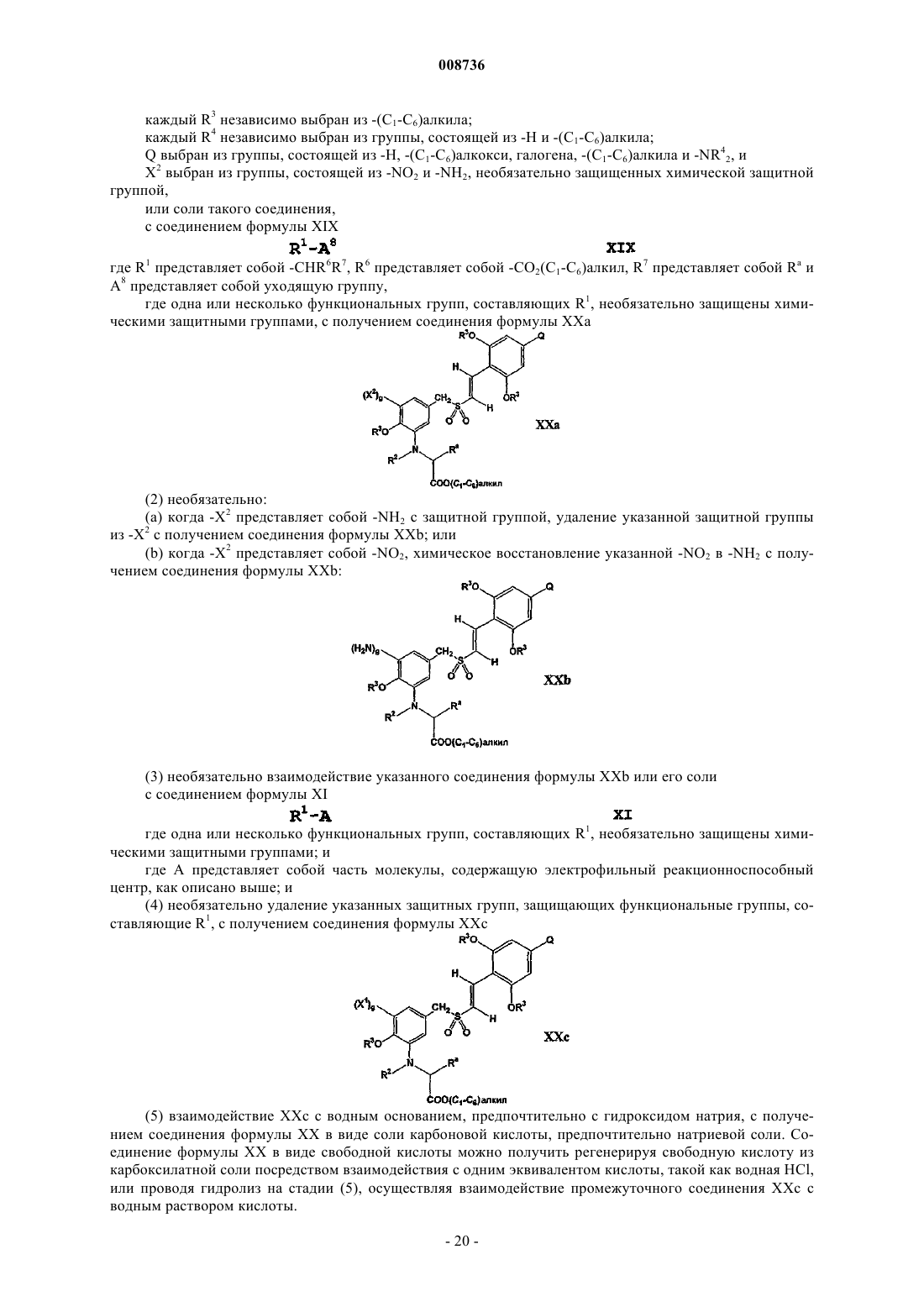
7. Соединение формулы IIа
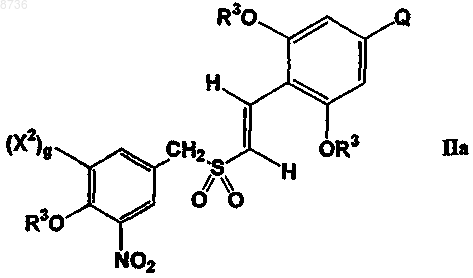
где g равен 0 или 1;
каждый R3 независимо выбран из -(C1-С6)алкила;
каждый R4 независимо выбран из группы, состоящей из -Н и -(C1-С6)алкила;
Q выбран из группы, состоящей из -Н, -(C1-С6)алкокси, галогена, -(C1-C6)алкила и -NR42 и
X2 выбран из группы, состоящей из NO2 и -NH2, необязательно защищенных химической защитной группой;
или его соль.
8. Соединение формулы D
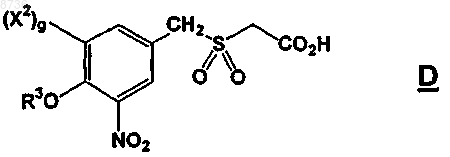
где каждый R3 независимо выбран из -(C1-С6)алкила;
g равен 0 или 1 и
X2 выбран из группы, состоящей из -NО2 и -NH2, необязательно защищенной химической защитной группой;
или соль такого соединения.
9. Коньюгат формулы I-L-Ab, где
I представляет собой соединение по любому из пп.1-6,
Аb представляет собой антитело и
-L- представляет собой простую ковалентную связь или линкер, соединяющий ковалентной связью указанное соединение с указанным антителом.
10. Применение соединения по любому из пп.1-6 или его фармацевтически приемлемой соли, или коньюгата по п.9 в медицине.
11. Фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и по меньшей мере одно соединение по любому из пп.1-6, или его фармацевтически приемлемую соль, или по меньшей мере один коньюгат по п.9.
12. Способ лечения пролиферативных расстройств у индивида, включающий введение указанному индивиду эффективного количества по меньшей мере одного соединения по любому из пп.1-6, или его фармацевтически приемлемой соли, или по меньшей мере одного коньюгата по п.9.
13. Способ по п.12, где пролиферативное расстройство выбрано из группы, состоящей из гемангиоматоза новорожденных, вторичного прогрессирующего рассеянного склероза, хронического прогрессирующего миелодегенеративного заболевания, нейрофиброматоза, ганглионейроматоза, образования келоидов, деформирующего остоза, кистозно-фиброзного заболевания, саркоидоза, болезни Перони и болезни Дюпюитрена, цирроза, атеросклероза и сосудистого рестеноза.
14. Способ по п.12, где пролиферативное расстройство представляет собой рак.
15. Способ по п.14, где рак выбран из группы рака яичника, яичка, шейки матки, матки, влагалища, молочной железы, простаты, легких, почки, прямой кишки, ободочной кишки, желудка, надпочечной железы, устья пищевода, головного мозга, печени, желчного пузыря, кожи, кости, лимфатической системы и глаз, или рак представляет собой гематологическую неоплазию.
16. Способ индуцирования апоптоза опухолевых клеток у индивида, страдающего от рака, включающий введение указанному индивиду эффективного количества по меньшей мере одного соединения по любому из пп.1-6 или по меньшей мере одного коньюгата по п.9.
17. Способ по п.16, где опухолевые клетки выбраны из группы опухолей, состоящей из опухолей яичника, яичка, шейки матки, матки, влагалища, молочной железы, простаты, легких, почки, прямой кишки, ободочной кишки, желудка, надпочечной железы, устья пищевода, головного мозга, печени, желчного пузыря, кожи, кости, лимфатической системы и глаз.
18. Способ получения соединения формулы I
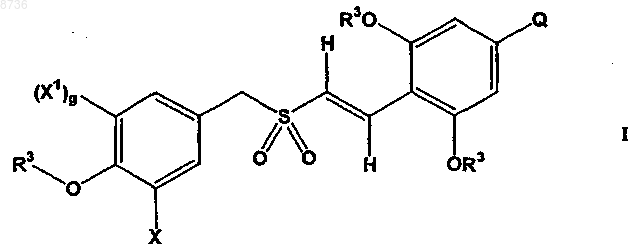
где X выбран из группы, состоящей из приведенных ниже (i) и (ii)
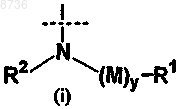
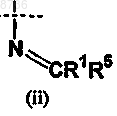
где X1 выбран из группы, состоящей из приведенных ниже (i), (ii) и (iii)
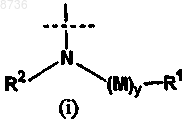
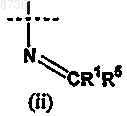
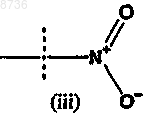
где X1 необязательно защищен одной или несколькими химическими защитными группами;
g равен 0 или 1;
каждый М представляет собой двухвалентную связывающую группу, независимо выбранную из группы, состоящей из -(С1-С6)алкилена-, -(CH2)a-V-(СН2)b-, -(СН2)d-W-(СН2)е- и -Z-;
каждый у независимо выбран из группы, состоящей из 0 и 1;
каждый V независимо выбран из группы, состоящей из арилена, гетероарилена, -С(=O)-, -C(=S)-,
-S(=O)-, -SO2-, -С(=O)O-, -С(=O)(С1-С6)перфторалкилена-, -C(=O)NR4-, -C(=S)NR4- и -SO2NR4-;
каждый W независимо выбран из группы, состоящей из -NR4-, -О- и -S-;
каждый а независимо выбран из группы, состоящей из 0, 1, 2 и 3;
каждый b независимо выбран из группы, состоящей из 0, 1, 2 и 3;
каждый d независимо выбран из группы, состоящей из 1, 2 и 3;
каждый е независимо выбран из группы, состоящей из 0, 1, 2 и 3;
-Z- представляет собой
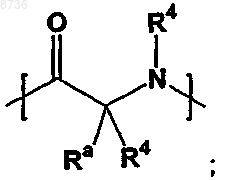
где абсолютная стереохимия -Z- представляет собой D или L или смесь D и L;
каждый Ra независимо выбран из группы, состоящей из -Н, -(С1-С6)алкила, -(СН2)3-NH-C(NH2)(=NH), -СН2С(=O)NH2, -CH2COOH, -CH2SH, -(CH2)2C(=O)-NH2, -(CH2)2COOH, -СН2-(2-имидазолила), -СН(СН3)-СН2-СН3, -СН2-СН(СН3)2, -(CH2)4-NH2, -(СН2)2-S-CH3, фенила, СН2-фенила,
-СН2-ОН, -СН(ОН)-СН3, -СН2-(3-индолила), -СН2-(4-гидроксифенила), -СН(СН3)2 и -СН2-СН3; и включает соединения, где Ra и R1 объединены с образованием 5-, 6- или 7-членного гетероциклического кольца;
каждый R1 независимо выбран из группы, состоящей из -Н, незамещенного арила, замещенного арила, замещенного гетероцикла, незамещенного гетероцикла, -CO2R5, -C(=O)NR42, -CR4R6R7, -C(=NH)-NR42, - (C1-C6)перфторалкила, -CF2Cl, -P(=O)(OR4)2, -OP(=O)(OR4)2 и одновалентной пептидильной части молекулы с молекулярной массой менее 1000; при условии, что когда у равен 0 и R1 представляет собой
-CO2R5, то R5 не является -Н;
каждый R2 независимо выбран из группы, состоящей из -Н, -(C1-С6)алкила и арил(C1-С3)алкила, где -R2 и - (М)y-R1 необязательно могут быть ковалентно связаны с образованием 5-, 6- или 7-членного замещенного или незамещенного гетероцикла;
каждый R3 независимо выбран из -(C1-С6)алкила;
каждый R4 независимо выбран из группы, состоящей из -Н и -(C1-С6)алкила;
каждый R5 независимо выбран из группы, состоящей из -Н, -(C1-С6)алкила и -(C1-С6)ацила;
каждый R6 независимо выбран из группы, состоящей из -Н, -(C1-C6)алкила, -CO2R5, -C(=O)R7, -OR5, -ОС(=O)(СН2)2CO2R5, -SR4, гуанидино, -NR42, -NR43+, -N+(CH2CH2OR5)3, фенила, замещенного фенила, гетероцикла, замещенного гетероцикла и галогена;
каждый R7 независимо выбран из группы, состоящей из Ra, галогена, -NR42 и гетероциклов, содержащих два атома азота; и
Q выбран из группы, состоящей из -Н, -(C1-C6)алкокси, галогена, -(C1-C6)алкила и -NR42;
где заместители замещенного арила и замещенных гетероциклических групп, содержащиеся или включенные в R1, R2, Ra, R6 и R7, независимо выбраны из группы, состоящей из галогена, -(C1-С6)алкила, -NO2, -CуN, -CO2R5, -С(=О)О(С1-С3)алкила, -OR5, -(С2-С6)алкилен-ОН, фосфонато, -NR42, -NHC(=O)(C1-С6)алкила, сульфамила, -ОС(=O)(C1-C3)алкила, -О(С2-С6)алкилен-N((C1-C6)алкила)2 и -CF3;
при условии, что
(1) когда R1 представляет собой одновалентную пептидильную часть молекулы с молекулярной массой менее 1000 и V представляет собой -С(=O)-, -C(=S)-, -S(=O)- или -SO2-, и b равен 0,
тогда указанная пептидильная часть молекулы соединена с М через аминоконец пептидильной части молекулы или через аминогруппу боковой цепи с образованием амида, тиоамида, сульфинамида или сульфонамида, соответственно;
(2) когда R1 представляет собой одновалентную пептидильную часть молекулы с молекулярной массой менее 1000 и V представляет собой -C(=O)NR3-, -SO2NR3- или -NR4-, и b равен 0,
тогда указанная пептидильная часть молекулы соединена с М через карбоксиконец пептидильной части молекулы или через карбоксильную группу боковой цепи с образованием имида, сульфонимида или карбоксамида, соответственно; и
(3) когда R1 представляет собой одновалентную пептидильную часть молекулы с молекулярной массой менее 1000 и W представляет собой -S- или -O-, a d равен 0,
тогда указанная пептидильная часть молекулы соединена с М через карбоксиконец пептидильной части молекулы или через карбоксильную группу боковой цепи с образованием сложного эфира тиокарбоновой кислоты или сложного эфира карбоновой кислоты, соответственно;
или соли такого соединения,
включающий следующие стадии:
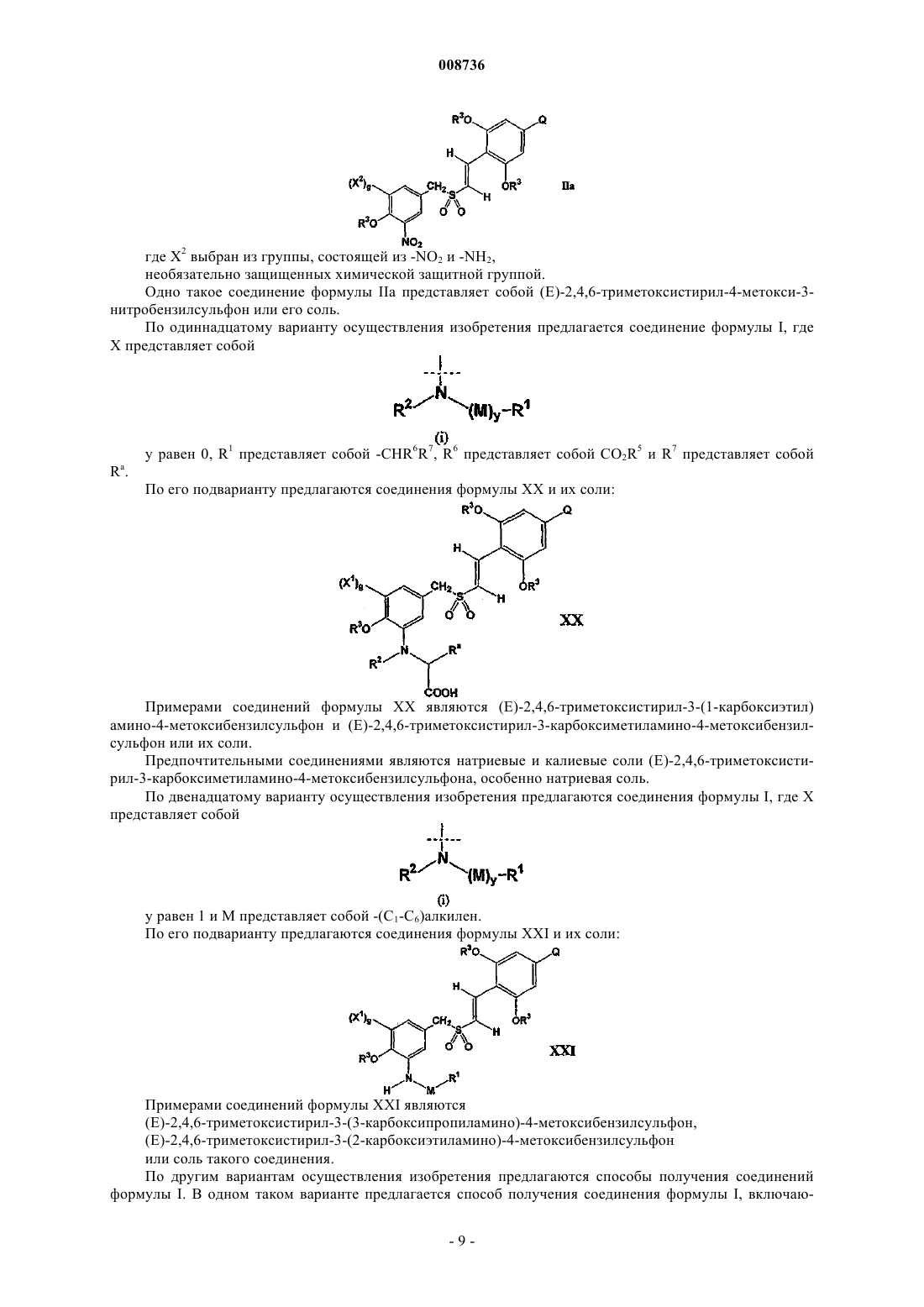
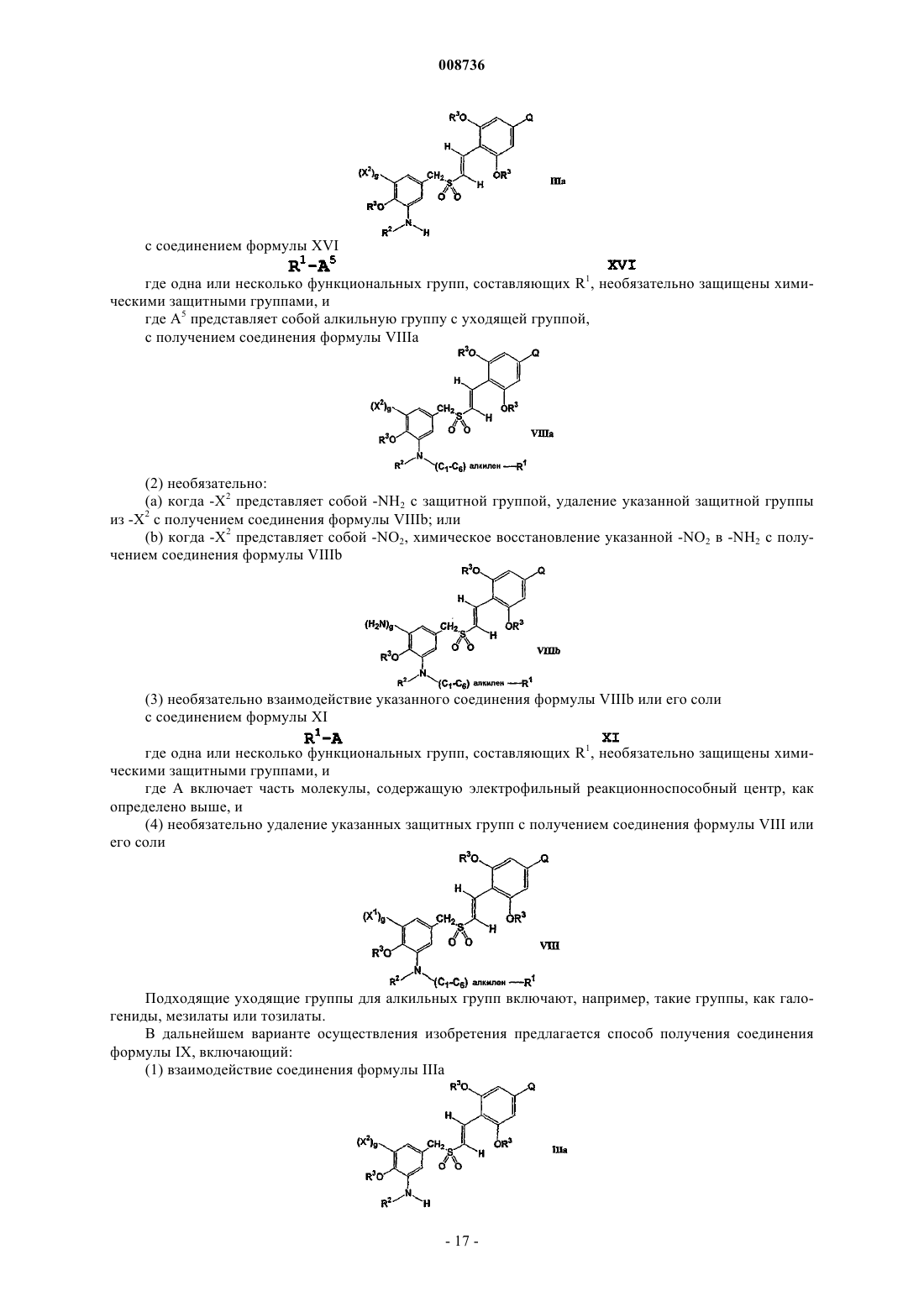
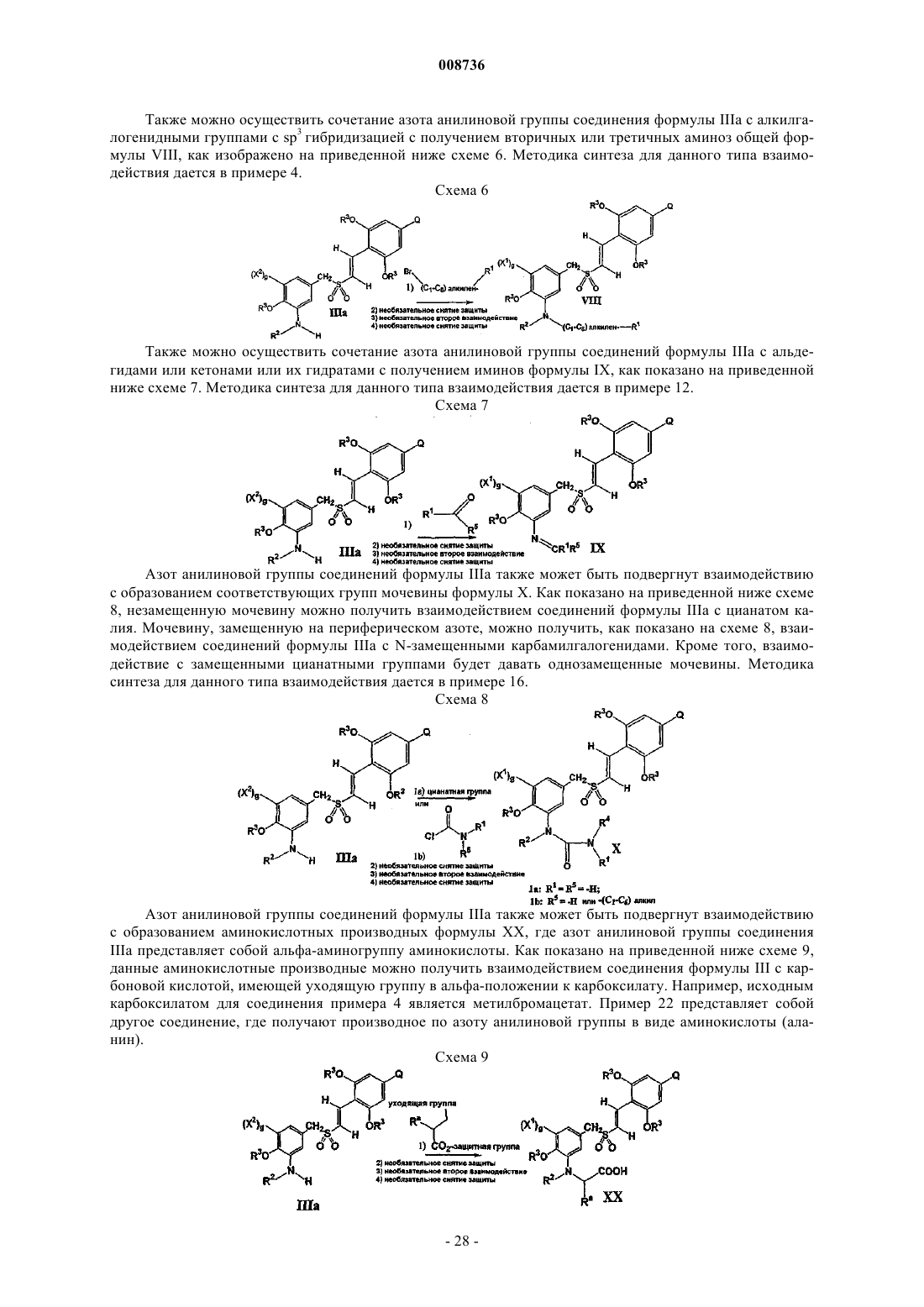
(1) взаимодействие соединения формулы IIIа

где X2 выбран из группы, состоящей из -NO2 и -NH2, необязательно защищенных химической защитной группой, и g, R3, R4 и Q имеют указанные выше значения,
или соли такого соединения, с соединением формулы XI
![]()
где R1, R4, R5, R6 и R7 имеют указанные выше значения,
где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и
А представляет собой часть молекулы, содержащую электрофильный реакционноспособный центр, причем указанная часть молекулы выбрана из группы, состоящей из
(a) алкильной группы, имеющей уходящую группу,
(b) арилгалогенида или арилпсевдогалогенида,
(c) карбоновой кислоты, активированной уходящей группой,
(d) сульфоновой кислоты, активированной уходящей группой,
(e) группы карбаминовой кислоты, активированной уходящей группой,
(f) цианатной группы,
(g) альдегидной или кетонной группы или ее гидрата, или ее кеталя или ацеталя,
(h) группы карбоновой кислоты и амид-связывающего реагента или
(i) промежуточного продукта тиомочевинной группы и йодида 2-хлор-1-метилпиридиния,
с получением соединения формулы Iа
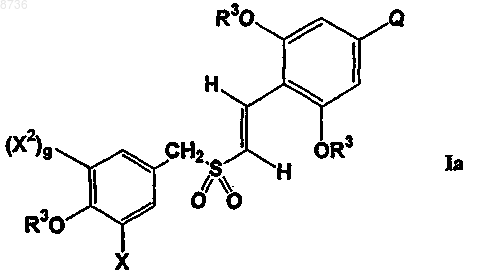
(2) необязательно
(а) когда -X2 представляет собой -NH2 с защитной группой, удаление указанной защитной группы из -X2 с получением соединения формулы Ib; или
(b) когда -Х2 представляет собой -NO2, химическое восстановление указанной -NO2 в -NH2 с получением соединения формулы Ib
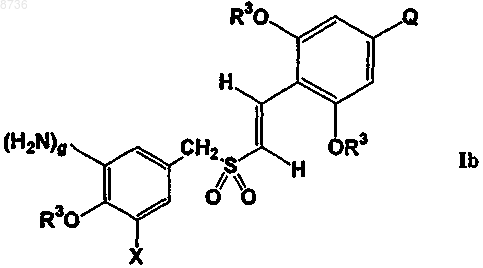
(3) необязательно взаимодействие указанного соединения формулы Ib или его соли с соединением формулы XI
![]()
где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и
где А представляет собой часть молекулы, содержащую электрофильный реакционноспособный центр, как определено выше; и
(4) необязательно удаление указанных защитных групп, защищающих функциональные группы, составляющие R1, с получением соединения формулы I
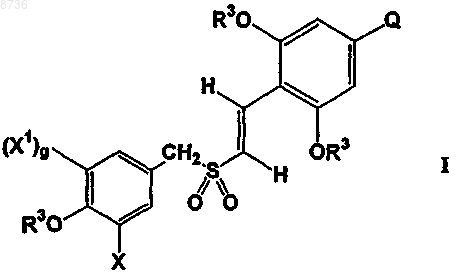
или его соли.
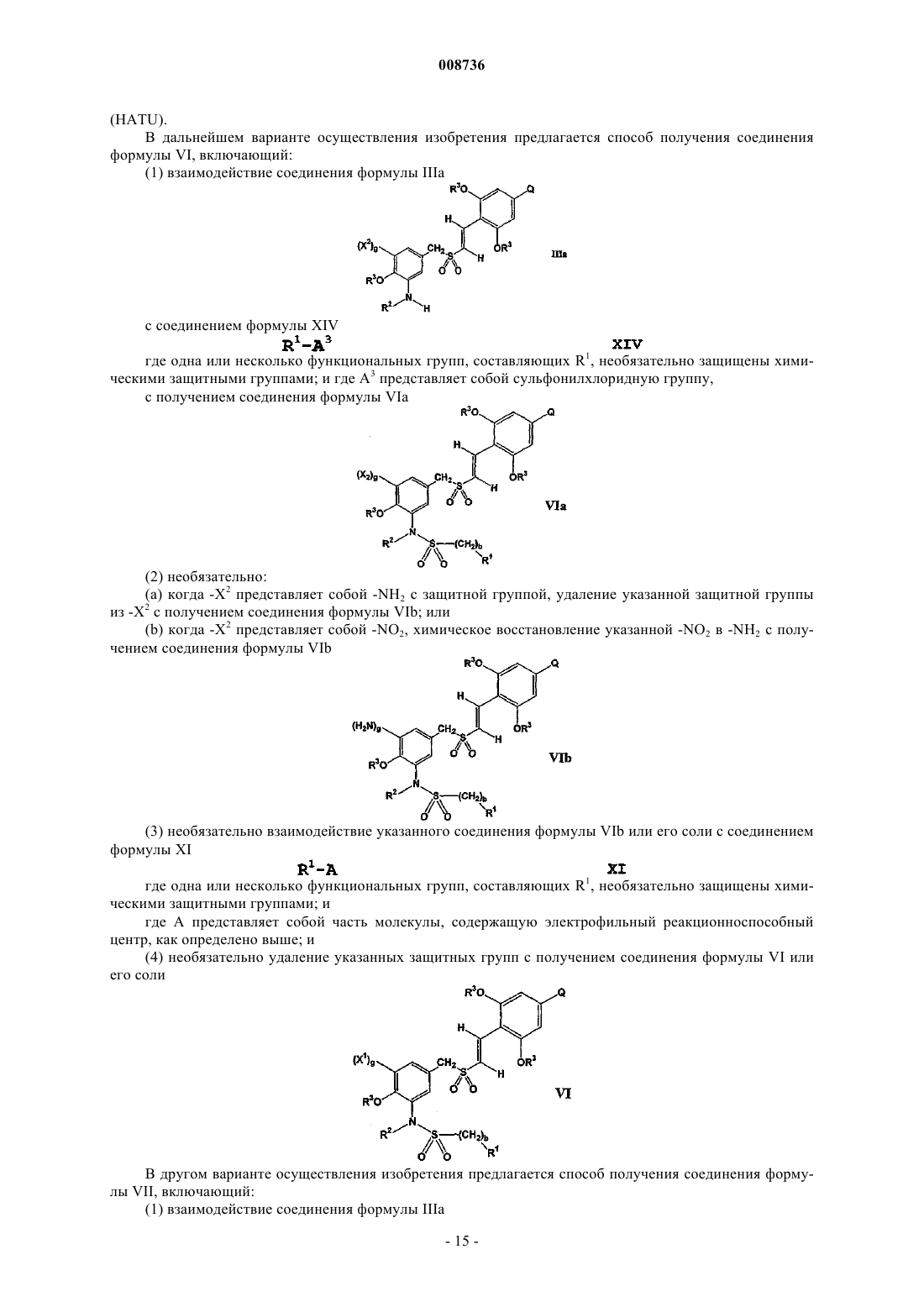
19. Способ по п.18, где соединение формулы IIIа
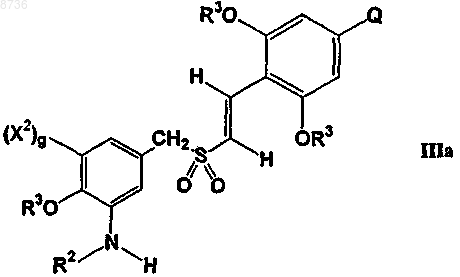
где g, R2, R3, Q и X2 имеют значения, указанные в п.18, или соль такого соединения,
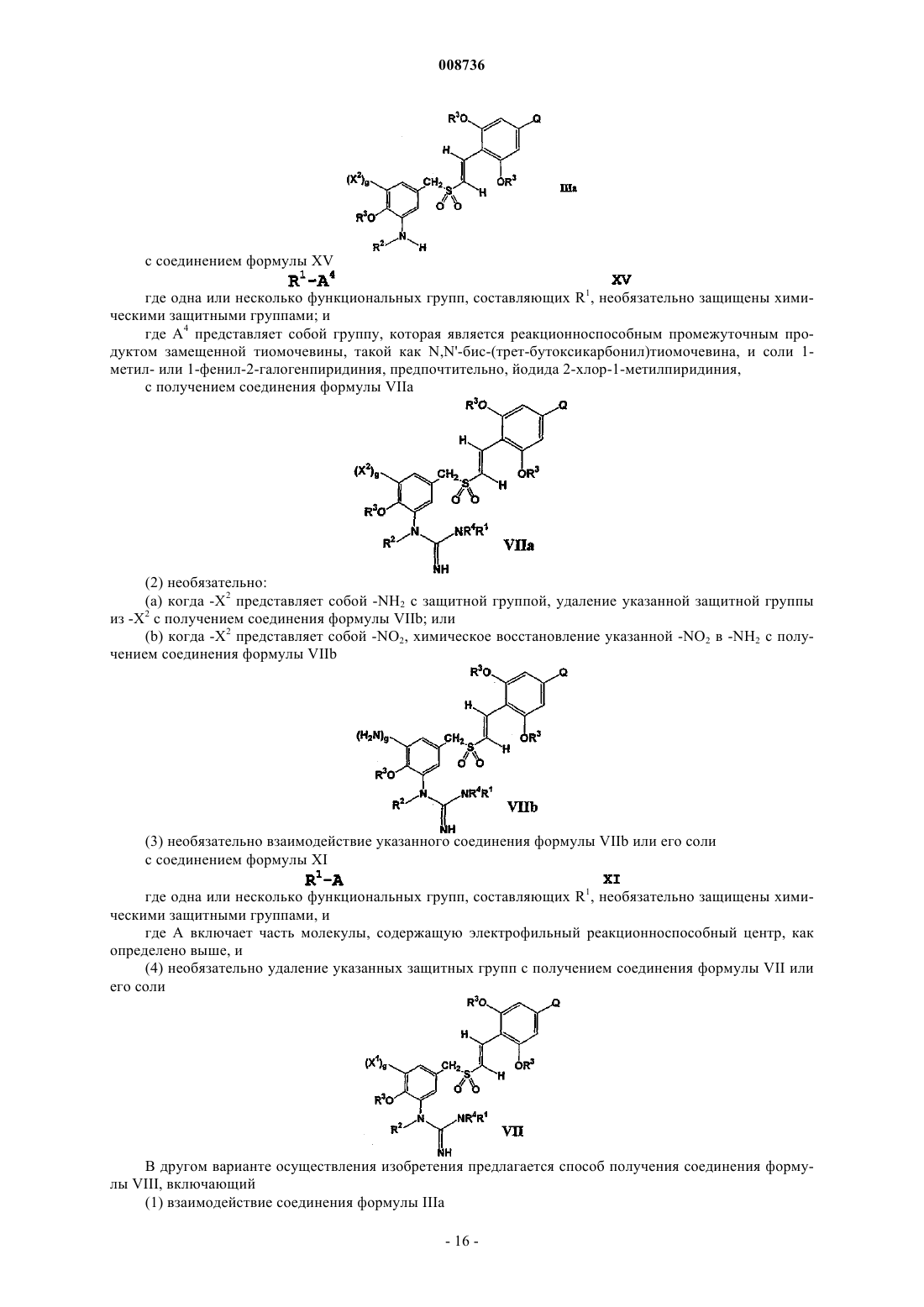
получают способом, включающим химическое восстановление соединения формулы IIа

где g, R2, R3, Q и X2 имеют значения, указанные в п.18,
или соли такого соединения,
с получением указанного соединения формулы IIIа или его соли.
20. Способ по п.19, где соединение формулы IIа получают конденсацией соединения формулы D
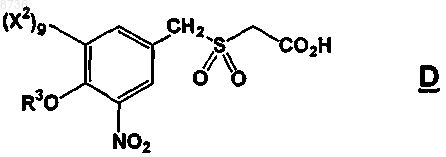
где R3, g и X2 имеют значения, указанные в п.18,
с соединением формулы Е
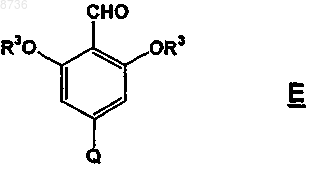
где R3 и Q имеют значения, указанные в п.18,
или его солью;
получая указанное соединение формулы IIа или соль такого соединения.
Текст
008736 Область изобретения Изобретение относится к композициям и способам лечения рака и других пролиферативных расстройств. Предпосылки изобретения Внеклеточные сигналы, получаемые трансмембранными рецепторами, посылаются в клетки путями сигнальной трансдукции (Pelech et al., Science 257:1335 (1992, которые вовлечены в большую совокупность физиологических процессов, таких как индукция клеточной пролиферации, дифференцировка или апоптоз (Davis et al., J. Biol. Chem. 268:14553 (1993. Митоген-активируемый протеинкиназный (МАРК) каскад представляет собой основную сигнальную систему, посредством которой клетки осуществляют трансдукцию внеклеточных сигналов во внутриклеточную реакцию (Nishida et al., Trends Biochem. Sci. 18:128 (1993); Blumer et al., Trends Biochem. Sci. 19:236 (1994. Многие стадии данного каскада сохраняются, и пептиды со значительной степенью гомологии с MAP киназами были открыты в различных видах. В клетках млекопитающих внеклеточные регулируемые сигналом киназы (ERK), ERK-1 и ERK-2,являются исходными и наиболее хорошо изученными членами семейства МАРК, причем каждая из них обладает уникальной особенностью активироваться фосфорилированием на треониновом и тирозиновом остатках посредством расположенной "выше" киназной двойной специфичности (Posada et al., Science 255:212 (1992), Biggs III et al., Proc. Natl. Acad. Sci. USA 89:6295 (1992), Garner et al., Genes Dev. 6:1280(1992. В недавних исследованиях идентифицировали дополнительную подгруппу МАРК, известных как cJun NH2-терминальные киназы 1 и 2 (JNK-1 и JNK-2), которые имеют различные субстратные специфичности и регулируются различными стимулами (Hibi et al., Genes Dev. 7:2135 (1993. JNK являются членами класса стресс-активируемых протеинкиназ (SPK). Было показано, что JNK активируются обработкой клеток УФ-излучением, провоспалительными цитокинами и стрессами от воздействия окружающей среды (Derijard et al., Cell 1025 (1994. Активированная JNK связывается с концевой аминогруппой сJun белка и увеличивает транскрипционную активность белка, фосфорилируя его по ser63 и ser73 (Adleret al., Proc. Natl. Acad. Sci. USA 89:5341 (1992), Kwok et al., Nature 370:223 (1994. Анализ установленной первичной последовательности JNK показывает, что они отдаленно связаны с ERK (Davis et al., Trends Biochem. Sci. 19:470 (1994. Как ERK, так и JNK фосфорилируются по Туr иThr в ответ на внешний раздражитель, что приводит к их активации (Davis, Trends Biochem. Sci. 19:470(1994. Участки фосфорилирования (Thr и Туr), которые играют решающую роль в их активации, сохраняются у ERK и JNK (Davis, Trends Biochem. Sci. 19:470 (1994. Однако данные участки фосфорилирования размещены внутри различных двойственных мотивов фосфорилирования: Thr-Pro-Tyr (JNK) и ThrGlu-Tyr (ERK). Фосфорилирование MARK и JNK внешним сигналом часто включает активацию протеинтирозинкиназ (РТК) (Gille et al., Nature 358:414 (1992, которые составляют огромное семейство белков, охватывающее несколько рецепторов факторов роста и другие трансдуцирующие сигнал молекулы. Протеинтирозинкиназы представляют собой ферменты, которые катализируют хорошо характеризованную химическую реакцию: фосфорилирования тирозинового остатка (Hunter et al., Annu Rev Biochem 54:897 (1985. Рецепторы тирозинкиназы, в частности, являются привлекательными мишенями для разработки лекарственных препаратов, поскольку блокаторы субстратного домена данных киназ, вероятно, дают эффективное и селективное антипролиферативное вещество. Потенциальное использование блокаторов протеинтиразинкиназы в качестве антипролиферативного вещества было установлено еще в 1981, когда кверцетин был предложен в качестве РТК блокатора (Graziani et al., Eur. J. Biochem. 135:583589 (1983. Наиболее вероятный путь МАРК включает внеклеточные регулируемые сигналом киназы, которые составляют Ras/Raf/MEK/ERK киназный каскад (Boudewijn et al., Trends Biochem. Sci. 20, 18 (1995. Как только данный путь активируется различными стимулами, МАРК фосфорилирует разнообразные белки,включая отдельные факторы транскрипции, которые перемещаются в ядро и активируют транскрипцию генов. Отрицательная регуляция данного пути могла бы остановить каскад данных событий. Таким образом, необходимы противораковые химиотерапевтические препараты, которые нацелены на рецепторные тирозинкиназы и которые останавливают Ras/Raf/MEK/ERK киназный каскад. Онкогенные белки в целом и трансдуцирующие сигнал белки, в частности, вероятно, являются более селективными мишенями для химиотерапии, поскольку они представляют подкласс белков, чья активность является существенной для клеточной пролиферации, и поскольку их активность существенно усиливается при пролиферативных заболеваниях. Также необходимы новые клеточные антипролиферативные вещества и противораковая терапия, в частности, которые являются весьма селективными в обеспечении гибели пролиферирующих клеток,таких как клетки опухоли, но, не затрагивая нормальные клетки. Краткое изложение изобретения Цель изобретения состоит в предложении соединений, композиций и способов лечения рака и других пролиферативных расстройств. Биологически активные соединения находятся в форме замещенных стирилбензилсульфонов.-1 008736 Цель изобретения состоит в предложении соединений, которые являются селективными в обеспечении гибели клеток опухоли, не затрагивая нормальные клетки. По одному варианту осуществления изобретения соединения по изобретению имеют формулу I где X выбран из группы, состоящей из приведенных ниже (i) и (ii):X1 выбран из группы, состоящей из приведенных ниже (i), (ii) и (iii): где X1 необязательно защищен одной или несколькими химическими защитными группами;g равен 0 или 1; каждый М представляет собой двухвалентную связывающую группу, независимо выбранную из группы, состоящей из -(С 1-С 6)алкилена-, -(СН 2)a-V-(СН 2)b-, -(СН 2)d-W-(СН 2)е- и -Z-; каждый у независимо выбран из группы, состоящей из 0 и 1; каждый V независимо выбран из группы, состоящей из арилена, гетероарилена, -С(=O)-, -C(=S)-,-S(=O)-, -SO2-, -С(=O)O-, -С(=O)(С 1-С 6)перфторалкилена-, -C(=O)NR4-, -C(=S)NR4 -и -SO2NR4-; каждый W независимо выбран из группы, состоящей из -NR4-, -O- и -S-; каждый а независимо выбран из группы, состоящей из 0, 1, 2 и 3; каждый b независимо выбран из группы, состоящей из 0, 1, 2 и 3; каждый d независимо выбран из группы, состоящей из 1, 2 и 3; каждый е независимо выбран из группы, состоящей из 0, 1, 2 и 3; где абсолютная стереохимия -Z- представляет собой D или L или смесь D и L; каждый Ra независимо выбран из группы, состоящей из -Н, -(C1-C6)алкила, -(СН 2)3-NH-C(NH2)(=NH), -СН 2 С(=O)NH2, -CH2COOH, -CH2SH, -(CH2)2C(=O)-NH2, -(CH2)2COOH, -СН 2-(2-имидазолила),-СН(СН 3)-СН 2-СН 3, -СН 2-СН(СН 3)2, -(CH2)4-NH2, -(CH2)2-S-CH3, фенила, СН 2-фенила, -СН 2-ОН,-СН(ОН)-СН 3, -СН 2-(3-индолила), -СН 2-(4-гидроксифенила), -СН(СН 3)2 и -СН 2-СН 3; и включает соединения, где Ra и R1 объединены с образованием 5-, 6- или 7-членного гетероциклического кольца; каждый R1 независимо выбран из группы, состоящей из -Н, незамещенного арила, замещенного арила, замещенного гетероцикла, незамещенного гетероцикла, -CO2R5, -C(=O)NR42, -CR4R6R7, -C(=NH)NR42, -(C1-C6)перфторалкила, -CF2Cl, -P(=O)(OR4)2, -OP(=O)(OR4)2 и одновалентной пептидильной части молекулы с молекулярной массой менее 1000; при условии, что когда у равен 0 и R1 представляет собой-CO2R5, то R5 не является -Н; каждый R2 независимо выбран из группы, состоящей из -Н, -(C1-С 6)алкила и арил(С 1-С 3)алкила, где 2-R и -(M)y-R1 необязательно могут быть ковалентно связаны с образованием 5-, 6- или 7-членного замещенного или незамещенного гетероцикла; каждый R3 независимо выбран из -(C1-С 6)алкила; каждый R4 независимо выбран из группы, состоящей из -Н и -(C1-С 6)алкила; где когда R4 и R1 присоединены к одному и тому же атому азота, R1 и R4 могут объединяться с образованием гетероцикла; и когда две R4 группы связаны с одним и тем же атомом азота геминально, две R4 группы могут объединяться с образованием гетероцикла; каждый R5 независимо выбран из группы, состоящей из -Н, -(C1-С 6)алкила и -(C1-С 6)ацила; каждый R6 независимо выбран из группы, состоящей из -Н, -(C1-C6)алкила, -CO2R5, -C(=O)R7, -OR5,-ОС(=O)(СН 2)2CO2R5, -SR4, гуанидино, -NR42, -N+R43, -N+(СН 2 СН 2OН)3, фенила, замещенного фенила,-2 008736 гетероцикла, замещенного гетероцикла и галогена; каждый R7 независимо выбран из группы, состоящей из -Н, Ra, галогена, -(C1-С 6)алкила, -NR42 и гетероциклов, содержащих два атома азота; иQ выбран из группы, состоящей из -Н, -(C1-С 6)алкокси, галогена, -(C1-С 6)алкила и -NR42; где заместители замещенного арила и замещенных гетероциклических групп, содержащиеся или включенные в R1, Ra, R2, R6 и R7, независимо выбраны из группы, состоящей из галогена, -(C1-С 6)алкила,-(C1-С 6)алкокси, -NO2, -CN, -CO2R5, -C(=O)O(C1-C3)алкила, -OR5, -(C2-C6)алкилен-ОН, фосфонато,-NR42, -NHC(=O)(C1-С 6)алкила, сульфамила, -ОС(=O)(C1-C3)алкила, -О(С 2-С 6)алкилен-NC1-С 6)алкила)2 и -CF3; при условии, что(1) когда R1 представляет собой одновалентную пептидильную часть молекулы с молекулярной массой менее 1000 и V представляет собой -С(=O)-, -C(=S)-, -S(=O)- или -SO2-, и b равен 0, тогда указанная пептидильная часть молекулы соединена с М через аминоконец пептидильной части молекулы или через аминогруппу боковой цепи с образованием амида, тиоамида, сульфинамида или сульфонамида,соответственно;(2) когда R1 представляет собой одновалентную пептидильную часть молекулы с молекулярной массой менее 1000 и V представляет собой -C(=O)NR3-, -SO2NR3- или -NR4-, и b равен 0, тогда указанная пептидильная часть молекулы соединена с М через карбоксиконец пептидильной части молекулы или через карбоксильную группу боковой цепи с образованием имида, сульфонимида или карбоксамида, соответственно; и(3) когда R1 представляет собой одновалентную пептидильную часть молекулы с молекулярной массой менее 1000 и W представляет собой -S- или -O-, a d равен 0, тогда указанная пептидильная часть молекулы соединена с М через карбоксиконец пептидильной части молекулы или через карбоксильную группу боковой цепи с образованием сложного эфира тиокарбоновой кислоты или сложного эфира карбоновой кислоты, соответственно; или соль такого соединения. По одному его подварианту, предлагаются соединения формулы I, где каждый V независимо выбран из группы, состоящей из -С(=O)-, -C(=S)-, -S(=O)-, -SO2-, -C(=O)NR4-,-C(=S)NR4- и -SO2NR4-; где абсолютная стереохимия -Z- представляет собой D или L; каждый Ra независимо выбран из группы, состоящей из -Н, -СН 3, -(CH2)3-NH-C(NH2)(=NH), -СН 2 С-СН 2-СН 3, -СН 2-СН(СН 3)2, -(CH2)4-NH2, -(CH2)2-S-CH3, фенила, СН 2-фенила, -СН 2-ОН, -СН(ОН)-СН 3,-СН 2-(3-индолила), -СН 2-(4-гидроксифенила), -СН(СН 3)2 и -СН 2-СН 3; и включает соединения, где Ra и R1 объединены с образованием 5-, 6- или 7-членного гетероциклического кольца; каждый R1 независимо выбран из группы, состоящей из -Н, незамещенного арила, замещенного арила, замещенного гетероцикла, незамещенного гетероцикла, -CO2R5, -C(=O)NR42, -CHR6R7, -C(=NH)NR42 и одновалентной пептидильной части молекулы с молекулярной массой менее 1000; при условии,что когда у равен 0 и R1 представляет собой -CO2R5, то R5 не является -Н; каждый R6 независимо выбран из группы, состоящей из -Н, -(C1-С 6)алкила, -CO2R5, -C(=O)R7, -ОН,4-SR , -(C1-C3)алкокси, -(C1-С 3)алкилтио, гуанидино, -NR42, фенила, замещенного фенила, гетероцикла,замещенного гетероцикла и галогена; и каждый R7 независимо выбран из группы, состоящей из -Н, галогена, -(C1-С 6)алкила, -NR42 и гетероциклов, содержащих два атома азота; где заместители замещенного арила и замещенных гетероциклических групп, содержащиеся или включенные в R1, Ra, R2, R6 и R7, независимо выбраны из группы, состоящей из галогена, -(C1-С 6)алкила,-(C1-С 6)алкокси, -NO2, -CN, -CO2R5, -С(=O)О(C1-С 3)алкила, -ОН, -(С 2-С 6)алкилен-ОН, фосфонато,-NR42, -NHC(=O)(C1-C6)алкила, сульфамила, -ОС(=O)(C1-C3)алкила, -O(С 2-С 6)алкилен-NC1-С 6)алкила)2 и -CF3. По предпочтительному подварианту осуществления изобретения предлагаются соединения форму-С(=O)-, -C(=S)-, -S(=O)-, -SO2-,лы I, где каждый V независимо выбран из группы, состоящей из-С(=O)O-, -C(=O)NR4-, -C(=S)NR4- и -SO2NR4-. По более предпочтительному подварианту осуществления изобретения предлагаются соединения формулы I, где каждый V независимо выбран из группы, состоящей из-С(=O)-, -C(=S)-,-S(=O)-, -SO2-, -С(=O)O-, -C(=O)NR4-, -C(=S)NR4- и -SO2NR4-. По его другому подварианту предлагаются соединения формулы I, где Z имеет абсолютную L конфигурацию. Предпочтительные соединения формулы I включают, например, следующие соединения и их соли:(Е)-2,4,6-триметоксистирил-3-(2,2,3,3-тетрафторсукцинамидо)-4-метоксибензилсульфон. По первому варианту осуществления изобретения предлагается соединение формулы I, где у равен 0 и R2 представляет собой Н. По подварианту предлагаются соединения приведенной ниже формулы III: где g равен 0 или 1; каждый R2 независимо выбран из группы, состоящей из -Н, -(C1-С 6)алкила и арил(C1-С 3)алкила, где 2-R и -(M)y-R1 необязательно могут быть ковалентно связаны с образованием 5-, 6- или 7-членного замещенного или незамещенного гетероцикла; каждый R3 независимо выбран из -(C1-С 6)алкила; каждый R4 независимо выбран из группы, состоящей из -Н и -(C1-С 6)алкила;X1 выбран из группы, состоящей из приведенных ниже (i), (ii) и (iii): где X1 необязательно защищен одной или несколькими химическими защитными группами. Подходящие защитные группы должны быть устойчивы к реакциям, предназначенным для получения производного по 3-аминогруппе соединения формулы III. Затем указанные защитные группы необязательно удаляют, регенерируя X1. В другом подварианте предлагаются соединения приведенной ниже формулы IIIа: где X2 выбран из группы, состоящей из -NO2 и -NH2, где указанная -NH2 группа необязательно защищена химической защитной группой. Стратегия синтеза соединений формулы I включает получение производных первичной или вторичной аминогрупп в положении 3 соединения формулы IIIа. Такие способы получения производных 3 аминогруппы включают, например, реакции с образованием карбоксамидов, сульфонамидов, алкиламинов, азотсодержащих гетероциклов, иминов, гуанидинов, мочевин, амидинов и аминокетонов. Промежуточное соединение формулы IIIа также включает нитрогруппу или защищенную аминогруппу в положении 5. В стратегии синтеза данный 5-заместитель служит в качестве второй, латентной аминогруппы. Использование данной стратегии защитной группы позволяет раздельное получение производных двух данных аминогрупп, т.е. 3-аминогруппы соединения формулы IIIа и группы в положении 5, которая инертна к условиям получения производного 3-аминогруппы. Поэтому, путь синтеза включает сначала получение производного 3-аминогруппы, с последующим превращением 5-заместителя в аминогруппу путем (а) снятия защиты, если X2 представляет собой защищенный амин, или (b) химического восстановления, если X2 представляет собой нитрогруппу. Поэтому, с ретросинтетической точки зрения,путь синтеза дает возможность раздельного получения производных двух аминогрупп, одна из которых,в положении 5, является защищенной (химической защитной группой или находясь в окисленном состоянии - в виде нитрогруппы) и, таким образом, инертной к условиям получения производного 3 аминогруппы. Подходящие химические защитные группы для защищенного амина в положении 5 включают, например, бензил, 2,4-диметоксибензил и бензилоксикарбонил (CBZ). Аналогичным образом, когда X2 представляет собой -NO2, может быть получено производное 3-аминогруппы вышеуказанным образом. Затем -NO2 группу можно необязательно восстановить химически в соответствующую 5 аминогруппу посредством разнообразных методик, известных специалисту в данной области. Затем необязательно получают производное 5-аминогруппы, образованной восстановлением 5 нитрогруппы или удалением защитной группы из защищенного 5-аминосодержащего соединения. Получение производного 5-аминогруппы может быть таким же или отличаться от получения производного 3 аминогруппы. По подварианту вышеуказанных соединений формулы IIIа предлагаются соединения, где Q представляет собой -(C1-С 6)алкокси. По другому подварианту соединений формулы IIIa, Q представляет собой -ОСН 3. По дальнейшему подварианту соединений формулы IIIa, R3 представляет собой -СН 3. Одним таким соединением является (E)-2,4,6-триметоксистирил-4-метокси-3-аминобензилсульфон. По второму варианту осуществления изобретения на практике предлагается соединение формулы I,где:R1 выбран из группы, состоящей из незамещенного арила, замещенного арила, замещенного гетероцикла, незамещенного гетероцикла, -CO2R3, -C(=O)NR42, -CHR6R7, -C(=NH)-NR42 и одновалентной пептидильной части молекулы с молекулярной массой менее 1000. По третьему варианту осуществления изобретения на практике предлагается соединение формулы у равен 1, М представляет собой -(СН 2)a-V-(CH2)b- и V представляет собой -С(=О)-. По его подварианту предлагаются приведенные ниже соединения формулы IV и их соли: Предпочтительные соединения формулы IV включают, например, следующие соединения и их соли:(Е)-2,4,6-триметоксистирил-3-(аминоацетамидо)-4-метоксибензилсульфон,или соль такого соединения. По четвертому варианту осуществления изобретения предлагаются соединения формулы I, где X представляет собой у равен 1 и М представляет собой -Z-. По его подварианту предлагаются соединения формулы V и их соли: где каждый Ra независимо выбран из группы, состоящей из -Н, -СН 3, -(CH2)3-NH-C(NH2)(=NH),-СН 2 С(=O)NH2, -CH2COOH, -CH2SH, -(СН 2)2 С(=О)-NH2, -(СН 2)2 СООН, -СН 2-(2-имидазолила), -СН(СН 3)-СН 2-СН 3, -СН 2 СН(СН 3)2, -(CH2)4-NH2, -(CH2)2-S-CH3, фенила, СН 2-фенила, -СН 2-ОН, -СН(ОН)СН 3, -СН 2-(3-индолила), -СН 2-(4-гидроксифенила), -СН(СН 3)2 и -СН 2-СН 3; и включает соединения, где Ra и R1 объединены с образованием 5-, 6- или 7-членного гетероциклического кольца. Гетероциклические кольца, образованные комбинацией Ra и R1 включают, например, пирролидин,гидроксипирролидин, пиперидин, гомопиперидин и тиазолидин. Предпочтительные соединения формулы V включают, например, следующие соединения и их соли:(Е)-2,4,6-триметоксистирил-3-амино-4-метоксибензилсульфон-D-серинамид. По пятому варианту осуществления изобретения предлагаются соединения формулы I, где у равен 1, М представляет собой -(СН 2)a-V-(СН 2)b- и V представляет собой -SO2-. По его подварианту предлагаются соединения формулы VI и их соли:(Е)-2,4,6-триметоксистирил-3-(2,4-диаминобензолсульфамил)-4-метоксибензилсульфон. По шестому варианту осуществления изобретения предлагается соединение формулы I, где X представляет собой у равен 0 и R1 представляет собой -С(=NH)-NR42-. По его подварианту предлагаются соединения формулы VII и их соли: Одно такое соединение представляет собой (Е)-2,4,6-триметоксистирил-3-гуанидино-4-метоксибензилсульфон или его соль. По седьмому варианту осуществления изобретения предлагаются соединения формулы I, где X представляет собой у равен 1 и М представляет собой -(C1-С 6)алкилен-. По его одному подварианту предлагаются соединения формулы VIII и их соли: Примеры соединений формулы VIII включают, например:D-(E)-2,4,6-триметоксистирил-3-(1-карбоксиэтил)амино-4-метоксибензилсульфон,L-(E)-2,4,6-триметоксистирил-3-(1-карбоксиэтил)амино-4-метоксибензилсульфон,(E)-2,4,6-триметоксистирил-3-(карбоксиметиламино)-4-метоксибензилсульфон и их соли. По восьмому варианту осуществления изобретения предлагаются соединения формулы IX и их соли: Одно такое соединение представляет собой (E)-2,4,6-триметоксистирил-3-(4-нитрофенилимино)-4 метоксибензилсульфон или его соль. По девятому варианту осуществления изобретения предлагаются соединения формулы I, где X представляет собой у равен 1, М представляет собой -(СН 2)a-V-(СН 2)b- и V представляет собой -C(=O)NR4-. По его подварианту предлагаются соединения формулы X и их соли Примером соединения формулы X является (Е)-2,4,6-триметоксистирил-3-уреидо-4-метоксибензилсульфон или его соль. По десятому варианту осуществления изобретения предлагаются соединения формулы II и его соли где g равен 0 или 1; каждый R3 независимо выбран из -(C1-С 6)алкила; каждый R4 независимо выбран из группы, состоящей из -Н и -(C1-С 6)алкила;X1 выбран из группы, состоящей из приведенных ниже (i), (ii) и (iii): где X1 необязательно защищен одной или несколькими химическими защитными группами. Подходящие защитные группы должны быть устойчивы к реакциям, предназначенным для получения производных по 3-аминогруппе соединения формулы III. Затем указанные защитные группы необязательно удаляют, регенерируя X1. В другом его подварианте предлагаются соединения приведенной ниже формулы IIа: где X2 выбран из группы, состоящей из -NO2 и -NH2,необязательно защищенных химической защитной группой. Одно такое соединение формулы IIа представляет собой (Е)-2,4,6-триметоксистирил-4-метокси-3 нитробензилсульфон или его соль. По одиннадцатому варианту осуществления изобретения предлагается соединение формулы I, где у равен 0, R1 представляет собой -CHR6R7, R6 представляет собой CO2R5 и R7 представляет собой По его подварианту предлагаются соединения формулы XX и их соли: Примерами соединений формулы XX являются (Е)-2,4,6-триметоксистирил-3-(1-карбоксиэтил) амино-4-метоксибензилсульфон и (Е)-2,4,6-триметоксистирил-3-карбоксиметиламино-4-метоксибензилсульфон или их соли. Предпочтительными соединениями являются натриевые и калиевые соли (Е)-2,4,6-триметоксистирил-3-карбоксиметиламино-4-метоксибензилсульфона, особенно натриевая соль. По двенадцатому варианту осуществления изобретения предлагаются соединения формулы I, где X представляет собой у равен 1 и M представляет собой -(C1-C6)алкилен. По его подварианту предлагаются соединения формулы XXI и их соли: Примерами соединений формулы XXI являются(E)-2,4,6-триметоксистирил-3-(3-карбоксипропиламино)-4-метоксибензилсульфон,(Е)-2,4,6-триметоксистирил-3-(2-карбоксиэтиламино)-4-метоксибензилсульфон или соль такого соединения. По другим вариантам осуществления изобретения предлагаются способы получения соединений формулы I. В одном таком варианте предлагается способ получения соединения формулы I, включаю-9 008736 щий(1) взаимодействие соединения формулы IIIа или его соли где X2 выбран из группы, состоящей из -NO2 и -NH2, необязательно защищенных химической защитной группой, с соединением формулы XI где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами; и где А представляет собой часть молекулы, содержащую электрофильный реакционноспособный центр, причем указанная часть молекулы выбрана из группы, состоящей из:(a) алкильной группы, содержащей уходящую группу, например такую как галогенид, мезилат или тозилат,(b) группы арилгалогенида или арилпсевдогалогенида,(c) группы карбоновой кислоты, активированной уходящей группой, например, группы хлорангидрида карбоновой кислоты или группы ангидрида карбоновой кислоты,(d) группы сульфоновой кислоты, активированной уходящей группой, например, группы сульфонилхлорида,(e) группы карбаминовой кислоты, активированной уходящей группой, например, группы карбамилхлорида,(f) цианатной группы, например, цианата калия,(g) альдегидной или кетонной группы или ее гидрата, или ее кеталя или ацеталя,(h) группы карбоновой кислоты или группы аминокислоты, где в реакции используют амидсвязывающее вещество,(i) группы, которая представляет собой продукт реакции группы замещенной тиомочевины, и соли 1-метил- или 1-фенил-2-галогенпиридиния, предпочтительно, йодида 2-хлор-1-метилпиридиния, причем данный йодид также известен как реагент Myкаямы,с получением соединения формулы Iа(a) когда -X2 представляет собой -NH2 с защитной группой, удаление указанной защитной группы 2 из -X с получением соединения формулы Ib; или(b) когда -X2 представляет собой -NO2, химическое восстановление указанной -NO2; с получением соединения формулы Ib(3) необязательно взаимодействие указанного соединения формулы Ib или его соли с соединением формулы XI где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами и А является таким, как определено выше; и(4) необязательно удаление указанных защитных групп, защищающих функциональные группы, составляющие R1, с получением соединения формулы I или его соли. В вышеуказанном способе взаимодействия соединений формулы IIIа с соединениями формулы XI и сочетания соединений формулы Ib с соединениям и формулы XI, электрофильное соединение XI во втором взаимодействии может быть таким же или отличающимся от соединения, используемого в первом взаимодействии. Галогениды, которые могут содержать компонент уходящей группы электрофильной функциональной группы А, предпочтительно, представляют собой хлор, бром или йод. Термин "псевдогалогенид" относится к части молекулы, которая ведет себя как галогенид в реакциях аминирования, катализируемых палладием или никелем. Псевдогалогенидные группы включают, например, трифторметилсульфонаты и мезилаты. Группы карбоновых кислот (h) включают, например, аминокислоты, содержащие необязательные защитные группы на любой альфа-амино функциональной группе, амино функциональной группе боковой цепи, функциональной группе альфа карбоновой кислоты, функциональной группе карбоновой кислоты боковой цепи или на других функциональных группах боковых цепей, которые требуют защитную группу. Такие аминокислоты могут представлять собой аминокислоты, встречающиеся в природе, или синтетические аминокислоты, включая аминокислоты либо с R-, либо S-абсолютной конфигурацией. Кроме того, в вышеуказанном способе сочетания соединений формулы IIIа с соединениями формулы XI и сочетания соединений формулы Ib с соединениями формулы XI термин "защитная группа" или"химическая защитная группа" относится к производному химической функциональной группы, которое используют для получения производных химических функциональных групп, которые в противном случае были бы несовместимы с условиями желаемой реакции. Защитная группа придает данной функциональной группе устойчивость к условиям желаемой реакции, и позднее может быть удалена, чтобы регенерировать функциональную группу с удаляемой защитной группой. Одним примером использования защитных групп является обычная реакция аминогруппы первой аминокислоты с карбоксильной группой второй аминокислоты с образованием амидной связи. Однако поскольку каждый реагент содержит как амино, так и карбоксилатную функциональную группу, взаимодействие между ними является (1) неспецифическим в отношении того, какая аминогруппа будет реагировать с какой карбоксильной группой, и (2) объектом полимеризации, поскольку продукт реакции все еще содержит обе реакционноспособные группы. Защитная группа на карбоксилате первой аминокислоты и кислотная защитная группа на аминогруппе второй аминокислоты будут служить для ограничения взаимодействия реагентов до одной желаемой реакции аминогруппы первой аминокислоты с карбоновой кислотой второй аминокислоты и получения продукта, который не будет далее реагировать, поскольку обе оставшиеся реакционноспособные функциональные группы блокированы защитными группами, которые затем можно удалить. Любая химическая функциональная группа, которая составляет R1, может быть необязательно защищена химической защитной группой, если такая защитная группа является применимой в синтезе соединений формулы I. Соответствующие защитные группы для функциональных групп, составляющихR1, включают, например, такие группы, как трет-бутоксикарбонил (t-Boc) или 9-флуоренилметоксикарбонил (Fmoc). Кроме того, в вышеуказанном способе взаимодействия соединений формулы IIIа с соединениями формулы XI и необязательном взаимодействии соединений формулы Ib с соединениями формулы XI,амид-связывающие реагенты (h) являются соединениями, используемыми для сочетания неактивированных карбоновых кислот с аминогруппами, такими как анилиногруппы соединения формулы I, где -X представляет собой NH2 (т.е., где X представляет собой группу формулы (i), у равен 0, R1 представляет собой -Н и R2 представляет собой -Н). Такие амид-связывающие реагенты включают, например, такие реагенты, как диизопропилкарбодиимид и гексафторфосфат О-(7-азабензотриазол-1-ил)-N,N,N',N'тетраметилурония (HATU). После вышеуказанного способа взаимодействия соединений формулы IIIa с соединениями формулыXI и необязательного взаимодействия соединений формулы Ib с соединениями формулы XI, любые защитные группы, используемые в синтезе соединения формулы I, необязательно удаляются. По дальнейшему варианту осуществления изобретения предлагается способ получения соединения формулы IIIа, включающий:(1) химическое восстановление соединения формулы IIа и (2) необязательно алкилирование полученного в результате анилина посредством любого подходящего метода алкилирования амина,с получением соединения формулы IIIа где g равен 0 или 1; каждый R3 независимо выбран из -(C1-С 6)алкила; каждый R4 независимо выбран из группы, состоящей из -Н и -(C1-С 6)алкила;X2 выбран из группы, состоящей из -NO2 и -NH2, необязательно защищенных химической защитной группой,или соли такого соединения. Термин "химически восстанавливая" или "химическое восстановление" относится к химической реакции, где реагент, который восстанавливают, приобретает дополнительные электроны. В вышеуказанном способе -NO2 функциональную группу восстанавливают до -NH2 функциональной группы. Данную реакцию восстановления можно осуществить различными методами, известными специалисту в области синтетической химии. Такие методы включают, например, каталитическое гидрирование с использованием катализатора, такого как, например, палладий или платина, и источника водорода, который может представлять собой, например, введение газообразного водорода, или который можно получать посредством химического генератора водорода, такого как гидразин. Другие методы включают, например, металлы и соли металлов, такие как, например, Sn0, Zn0, Fe0 и SnCl2. Другие реагенты, которые осуществляют данный тип химического восстановления, включают, например, сульфитные реагенты, такие как гидросульфит натрия. Подходящее алкилирование азота анилиногруппы включает:(b) восстановительное аминирование, т.е. реакцию с альдегидом или кетоном в присутствии восстановителя, такого как цианборгидрид натрия или триацетоксиборгидрид натрия. Соединения формулы IIа можно получить способом, включающим конденсацию соединения формулы D с получением соединения формулы IIа- 12008736 где g равен 0 или 1; каждый R3 независимо выбран из -(C1-С 6)алкила; каждый R4 независимо выбран из группы, состоящей из -Н и -(C1-С 6)алкила;X2 выбран из группы, состоящей из -NO2 и -NH2, необязательно защищенных химической защитной группой,или соли такого соединения. В другом варианте предлагается способ получения соединения формулы IV. Способ включает:(1) взаимодействие соединения формулы IIIа с соединением формулы XII где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и где А 1 представляет собой группу карбоновой кислоты с уходящей группой,с получением соединения формулы IVa(a) когда -X2 представляет собой -NH2 с защитной группой, удаление указанной защитной группы 2 из -X с получением соединения формулы IVb; или(b) когда -X2 представляет собой -NO2, химическое восстановление указанной -NO2 в -NH2 с получением соединения формулы IVb(3) необязательно взаимодействие указанного соединения формулы IVb или его соли с соединением формулы XI: где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами; и где А представляет собой часть молекулы, содержащую электрофильный реакционноспособный центр, как определено выше; и(4) необязательно удаление указанных защитных групп, защищающих функциональные группы, составляющие R1, с получением соединения формулы IV или его соли: По другому варианту осуществления изобретения предлагается способ получения соединения фор- 13008736 мулы V. Способ включает:(1) взаимодействие соединения формулы IIIа с где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и где А 2 представляет собой группу карбоновой кислоты; и(b) связывающим реагентом, таким как диизопропилкарбодиимид,с получением соединения формулы Va(a) когда -X2 представляет собой -NH2 с защитной группой, удаление указанной защитной группы 2 из -X с получением соединения формулы Vb; или(b) когда -X2 представляет собой -NO2, химическое восстановление указанной -NO2 в -NH2 с получением соединения формулы Vb(3) необязательно взаимодействие указанного соединения формулы Vb или его соли с соединением формулы XI где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и где А представляет собой часть молекулы, содержащую электрофильный реакционноспособный центр, как определено выше; и(4) необязательно удаление указанных защитных групп, используемых в синтезе, таких как третбутоксикарбонил (t-Boc) или 9-флуоренилметоксикарбонил (Fmoc), с получением соединения формулы Амидсвязывающие реагенты, используемые для сочетания неактивированных групп карбоновой кислоты с ароматическими аминогруппами, такими как 3-аминогруппы соединений формулы I, и аминогруппами, связанными с пептидными R1 заместителями, включают, например, такие реагенты, как диизопропилкарбодиимид (DIC) и гексафторфосфат О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония(HATU). В дальнейшем варианте осуществления изобретения предлагается способ получения соединения формулы VI, включающий:(1) взаимодействие соединения формулы IIIа с соединением формулы XIV где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами; и где А 3 представляет собой сульфонилхлоридную группу,с получением соединения формулы VIa(a) когда -X2 представляет собой -NH2 с защитной группой, удаление указанной защитной группы 2 из -X с получением соединения формулы VIb; или(b) когда -X2 представляет собой -NO2, химическое восстановление указанной -NO2 в -NH2 с получением соединения формулы VIb(3) необязательно взаимодействие указанного соединения формулы VIb или его соли с соединением формулы XI где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами; и где А представляет собой часть молекулы, содержащую электрофильный реакционноспособный центр, как определено выше; и(4) необязательно удаление указанных защитных групп с получением соединения формулы VI или его соли В другом варианте осуществления изобретения предлагается способ получения соединения формулы VII, включающий:(1) взаимодействие соединения формулы IIIа с соединением формулы XV где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами; и где А 4 представляет собой группу, которая является реакционноспособным промежуточным продуктом замещенной тиомочевины, такой как N,N'-бис-(трет-бутоксикарбонил)тиомочевина, и соли 1 метил- или 1-фенил-2-галогенпиридиния, предпочтительно, йодида 2-хлор-1-метилпиридиния,с получением соединения формулы VIIa(a) когда -X2 представляет собой -NH2 с защитной группой, удаление указанной защитной группы 2 из -X с получением соединения формулы VIIb; или(b) когда -X2 представляет собой -NO2, химическое восстановление указанной -NO2 в -NH2 с получением соединения формулы VIIb(3) необязательно взаимодействие указанного соединения формулы VIIb или его соли с соединением формулы XI где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и где А включает часть молекулы, содержащую электрофильный реакционноспособный центр, как определено выше, и(4) необязательно удаление указанных защитных групп с получением соединения формулы VII или его соли В другом варианте осуществления изобретения предлагается способ получения соединения формулы VIII, включающий(1) взаимодействие соединения формулы IIIа с соединением формулы XVI где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и где А 5 представляет собой алкильную группу с уходящей группой,с получением соединения формулы VIIIa(а) когда -X2 представляет собой -NH2 с защитной группой, удаление указанной защитной группы 2 из -X с получением соединения формулы VIIIb; или(b) когда -X2 представляет собой -NO2, химическое восстановление указанной -NO2 в -NH2 с получением соединения формулы VIIIb(3) необязательно взаимодействие указанного соединения формулы VIIIb или его соли с соединением формулы XI где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и где А включает часть молекулы, содержащую электрофильный реакционноспособный центр, как определено выше, и(4) необязательно удаление указанных защитных групп с получением соединения формулы VIII или его соли Подходящие уходящие группы для алкильных групп включают, например, такие группы, как галогениды, мезилаты или тозилаты. В дальнейшем варианте осуществления изобретения предлагается способ получения соединения формулы IX, включающий:(1) взаимодействие соединения формулы IIIа- 17008736 где R2 представляет собой -Н, с соединением формулы XVII где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и где А 6 представляет собой группу, содержащую альдегидную или кетонную группу, ее гидрат или ее кеталь или ацеталь,с получением соединения формулы IХа(a) когда -X2 представляет собой -NH2 с защитной группой, удаление указанной защитной группы 2 из -X с получением соединения формулы IXb; или(b) когда -X2 представляет собой -NO2, химическое восстановление указанной -NO2 в -NH2 с получением соединения формулы IXb(3) необязательно взаимодействие указанного соединения формулы IXb или его соли с соединением формулы XI где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и где А представляет собой часть молекулы, содержащую электрофильный реакционноспособный центр, как определено выше, и(4) необязательно удаление указанных защитных групп с получением соединения формулы IX или его соли В другом варианте осуществления изобретения предлагается способ получения соединения формулы X, включающий:(1) взаимодействие соединения формулы IIIa с соединением формулы XVIII где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, и где(a) если А представляет собой цианатную группу, тогда R1 выбран из группы, состоящей из -Н, (C1C6)алкила и арила,R4 представляет собой -Н и(b) если А представляет собой группу карбаминовой кислоты, активированную уходящей группой,тогда R1 и R4 формулы X являются такими, как определено выше,с получением соединения формулы Ха(a) когда -X2 представляет собой -NH2 с защитной группой, удаление указанной защитной группы 2 из -X с получением соединения формулы Хb; или(b) когда -X2 представляет собой -NO2, химическое восстановление указанной -NO2 в -NH2 с получением соединения формулы Хb(3) необязательно взаимодействие указанного 5-NH2 соединения формулы Хb или его соли с соединением формулы XI где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами; и где А представляет собой часть молекулы, содержащую электрофильный реакционноспособный центр, как определено выше, и(4) необязательно удаление указанных защитных групп с получением соединения формулы X или его соли: В другом варианте предлагается способ получения соединения формулы XX(1) взаимодействие соединения формулы IIIа- 19008736 каждый R3 независимо выбран из -(C1-С 6)алкила; каждый R4 независимо выбран из группы, состоящей из -Н и -(C1-С 6)алкила;X2 выбран из группы, состоящей из -NO2 и -NH2, необязательно защищенных химической защитной группой,или соли такого соединения,с соединением формулы XIX где R1 представляет собой -CHR6R7, R6 представляет собой -СО 2(C1-С 6)алкил, R7 представляет собой Ra и А 8 представляет собой уходящую группу,где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами, с получением соединения формулы ХХа(a) когда -X2 представляет собой -NH2 с защитной группой, удаление указанной защитной группы 2 из -X с получением соединения формулы ХХb; или(b) когда -X2 представляет собой -NO2, химическое восстановление указанной -NO2 в -NH2 с получением соединения формулы ХХb:(3) необязательно взаимодействие указанного соединения формулы ХХb или его соли с соединением формулы XI где одна или несколько функциональных групп, составляющих R1, необязательно защищены химическими защитными группами; и где А представляет собой часть молекулы, содержащую электрофильный реакционноспособный центр, как описано выше; и(4) необязательно удаление указанных защитных групп, защищающих функциональные группы, составляющие R1, с получением соединения формулы ХХс(5) взаимодействие ХХс с водным основанием, предпочтительно с гидроксидом натрия, с получением соединения формулы XX в виде соли карбоновой кислоты, предпочтительно натриевой соли. Соединение формулы XX в виде свободной кислоты можно получить регенерируя свободную кислоту из карбоксилатной соли посредством взаимодействия с одним эквивалентом кислоты, такой как водная НСl,или проводя гидролиз на стадии (5), осуществляя взаимодействие промежуточного соединения ХХс с водным раствором кислоты.- 20008736 Подходящие уходящие группы для алкильных групп, таких как группы, присутствующие в промежуточном соединении XIX, включают, например, такие группы, как галогениды, мезилаты и тозилаты. В еще одном варианте осуществления изобретения предлагается коньюгат формулы I-L-Ab, где I представляет собой соединение формулы I, Ab представляет собой антитело и -L- представляет собой простую связь или линкер, соединяющий ковалентной связью указанное соединение формулы I с указанным антителом. В дальнейшем варианте осуществления изобретения предлагается коньюгат формулы III-L-Ab, гдеIII представляет собой соединение формулы III, Ab представляет собой антитело и -L- представляет собой простую связь или линкер, соединяющий ковалентной связью указанное соединение формулы III с указанным антителом. В предпочтительном подварианте вышеуказанных коньюгатов формул I-L-Ab и III-L-Ab указанное антитело (Ab) представляет собой моноклональное антитело или моноспецифическое поликлональное антитело. В более предпочтительном подварианте вышеуказанных коньюгатов формул I-L-Ab и III-L-Ab указанное антитело (Ab) представляет собой опухолеспецифическое антитело. В еще одном дополнительном варианте осуществления настоящего изобретения предлагается соединение формулы I, из которого получено производное в качестве субстрата для фермента -лактамазы. Также предлагается фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и одно или несколько вышеуказанных соединений формулы I или фармацевтически приемлемую соль такого соединения. Дополнительно предлагается фармацевтическая композиция, включающая фармацевтически приемлемый носитель и по меньшей мере один коньюгат формулы I-L-Ab или III-L-Ab. По другому варианту осуществления изобретения предлагается способ лечения пролиферативных расстройств у индивида, в частности, рака, включающий введение указанному индивиду эффективного количества соединения формулы I или фармацевтически приемлемой соли такого соединения, отдельно или в комбинации с фармацевтически приемлемым носителем. В другом варианте осуществления изобретения предлагается способ лечения пролиферативного расстройства у индивида, в частности, рака, включающий введение указанному индивиду эффективного количества, по меньшей мере, одного коньюгата формулы I-L-Ab или III-L-Ab. В другом варианте осуществления изобретения предлагается способ подавления роста опухолевых клеток у индивида, страдающего от рака, включающий введение указанному индивиду эффективного количества соединения формулы I или фармацевтически приемлемой соли такого соединения, отдельно или в комбинации с фармацевтически приемлемым носителем. В другом варианте осуществления изобретения предлагается способ подавления роста опухолевых клеток у индивида, страдающего от рака, включающий введение указанному индивиду эффективного количества по меньшей мере одного коньюгата формулы I-L-Ab или III-L-Ab. В другом варианте предлагается способ индуцирования апоптоза раковых клеток, более предпочтительно, опухолевых клеток, у индивида, страдающего от рака, включающий введение указанному индивиду эффективного количества соединения формулы I или фармацевтически приемлемой соли такого соединения, отдельно или в комбинации с фармацевтически приемлемым носителем. В другом варианте предлагается способ индуцирования апоптоза раковых клеток, более предпочтительно, опухолевых клеток, у индивида, страдающего от рака, включающий введение указанному индивиду эффективного количества по меньшей мере одного коньюгата формулы I-L-Ab или III-L-Ab, отдельно или в комбинации с фармацевтически приемлемым носителем. Стирилбензилсульфоны характеризуются цис-транс изомерией, причиной которой является присутствие двойной связи. Соединения называют в соответствии с системой Кана-Ингольда-Прелога, IUPAC 1974 Recommendation, Section E: Stereochemistry, Nomenclature of Organic Chemistry, John WileySons,Inc., New York, NY, 4th ed., 1992, p.127-138. Используя данную систему номенклатуры, четыре группы около двойной связи имеют приоритет в соответствии с рядом правил. В таком случае изомер с двумя более высокими по рангу группами на одной и той же стороне от двойной связи обозначают Z (от немецкого слова "zusammen", обозначающего вместе). Другой изомер, в котором две более высокие по рангу группы находятся на противоположных сторонах от двойной связи, обозначают Е (от немецкого слова"entgegen", которое означает "противоположный"). Соединения по настоящему изобретению имеют Е конфигурацию, как показано ниже. Термин "ацил" означает радикал общей формулы -C(=O)-R, где -R представляет собой водород, уг- 21008736 леводород, амино или алкокси. Примеры включают, например, ацетил (-С(=О)СН 3), пропионил(-С(=О)СН 2 СН 3), бензоил (-С(=O)С 6 Н 5), фенилацетил (-С(=O)CH2C6H5), карбоэтокси (-CO2Et) и диметилкарбамоил (-С(=O)N(СН 3)2). Термин "алкил", сам по себе или в виде части другого заместителя, означает, если не указано иное,углеводородный радикал с прямой или разветвленной цепью или циклический углеводородный радикал,включая ди- и мультирадикалы, имеющий указанное число атомов углерода (т.е. C1-С 6 означает от одного до шести атомов углерода) и включает группы с прямой, разветвленной цепью или циклические группы. Примеры включают метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, пентил, неопентил, гексил, циклогексил и циклопропилметил. Наиболее предпочтительным является (C1-С 3)алкил, особенно этил, метил и изопропил. Термин "алкилен", сам по себе или в виде части другого заместителя, означает, если не указано иное, двухвалентный углеводородный радикал с прямой или разветвленной цепью или циклический углеводородный радикал. Термин "алкокси", используемый отдельно или в комбинации с другими терминами, означает, если не указано иное, алкильную группу, имеющую указанное число атомов углерода, как определено выше,связанную с остатком молекулы посредством атома кислорода, такую как, например, метокси, этокси, 1 пропокси, 2-пропокси (изопропокси) и более высокие гомологи и изомеры. Предпочтительной группой является (C1-С 3)алкокси, особенно этокси и метокси. Термин "алкенил", используемый отдельно или в комбинации с другими терминами, означает, если не указано иное, стабильный мононенасыщенный или диненасыщенный углеводородный радикал с прямой или разветвленной цепью или циклическую углеводородную группу, которые имеют указанное число атомов углерода. Примеры включают винил, пропенил (аллил), кротил, изопентенил, бутадиенил, 1,3 пентадиенил, 1,4-пентадиенил, циклопентенил, циклопентадиенил и более высокие гомологи и изомеры. Двухвалентный радикал, полученный из алкена, иллюстрируется -СН=СН-СН 2- в качестве примера. Термин "амин" или "амино" относится к радикалу общей формулы -NRR', где R и R' независимо выбраны из водорода или углеводородного радикала, или где R и R' объединены вместе с образованием гетероцикла. Примеры аминогрупп включают -NH2, метиламино, диэтиламино, анилино, бензиламино,пиперидин, пиперазин и индолин. Термин "карбамил" означает группу -C(=O)NRR', где R и R' независимо выбраны из водорода или углеводородного радикала, или где R и R' объединены вместе с образованием гетероцикла. Примеры карбамильных групп включают -C(=O)NH2 и -С(=O)N(СН 3)2. Термин "карбокси(C1-С 3)алкокси" означает радикал, в котором карбоксигруппа -СООН присоединена к атому углерода алкоксигруппы с прямой или разветвленной цепью, содержащей от одного до трех атомов углерода. Таким образом, радикал содержит вплоть до 4 атомов углерода. Примеры включают-О(СН 2)3 СО 2 Н и -О(СН 2)2 СО 2 Н. Термин "циклоалкил" относится к алкильным радикалам, содержащим цикл. Термин "гетероалкил", используемый отдельно или в комбинации с другим термином, означает, если не указано иное, стабильный радикал с прямой или разветвленной цепью, содержащий указанное число атомов углерода и один или два гетероатома, выбранные из группы, состоящей из О, N и S, и где атомы азота и серы могут быть необязательно окислены, а гетероатом, представляющий собой азот, необязательно может быть кватернизирован. Гетероатом(ы) может располагаться в любом положении гетероалкильной группы, включая участок между остатком гетероалкильной группы и фрагментом, к которому она присоединена, а также присоединен к наиболее отдаленному атому углерода в гетероалкильной группе. Примеры включают -О-СН 2-СН 2-СН 3, -СН 2-СН 2-СН 2-ОН, -CH2-CH2-NH-CH3, -CH2-S-CH2-CH3 и-СН 2 СН 2-S(=O)-CH3. Последовательно могут быть расположены вплоть до двух гетероатомов, например,-CH2-NH-OCH3. Термин "гетероалкенил", используемый отдельно или в комбинации с другим термином, означает,если не указано иное, стабильный мононенасыщенный или диненасыщенный углеводородный радикал с прямой или разветвленной цепью, содержащий указанное число атомов углерода и один или два гетероатома, выбранные из группы, состоящей из О, N и S, и где атомы азота и серы могут быть необязательно окислены, а гетероатом, представляющий собой азот, необязательно может быть кватернизирован. Последовательно могут быть расположены вплоть до двух гетероатомов. Примеры включают -СН=СН-ОСН 3, -СН=СН-СН 2-ОН, -CH2-CH=N-OCH3, -CH=CH-N(CH3)-CH3 и CH2-CH=CH-CH2-SH. Термин "гидроксиалкил" означает алкильный радикал, где один или несколько атомов углерода замещены гидроксигруппой. Примеры включают -СН 2-СН(ОН)СН 3 и -СН 2-СН 2 ОН. Термин "гало" или "галоген" сам по себе или в качестве части другого заместителя, если не указано иное, означает атом фтора, хлора, брома или йода. Термин "ди(C1-С 6)алкиламино(С 2-С 6)алкокси" означает(алкил)2N(СН 2)nO-, где две алкильные цепи,присоединенные к атому азота, независимо содержат от одного до шести атомов углерода, предпочтительно от одного до трех атомов углерода, и n равно целому числу от 2 до 6. Предпочтительно, n равно 2 или 3. Наиболее предпочтительно n равно 2 и алкильные группы представляют собой метил, т.е. группа представляет собой диметиламиноэтоксигруппу, (СН 3)2NCH2CH2O-.- 22008736 Термин "фосфонато" означает -РО(ОН)2 группу. Термин "сульфамил" относится к группе -SO2NRR', где R и R' независимо выбраны из водорода или углеводородного радикала, или где R и R' объединены с образованием гетероцикла. Примеры сульфамильных групп включают -SO2NH2, -SO2N(CH3)2 и -SO2N(C6H5). Термин "ароматический" относится к карбоциклу или гетероциклу, содержащему одно или несколько полиненасыщенных колец, имеющих ароматический характер 4n+2) делокализованных(пи) электронов). Термин "арил", используемый отдельно или в комбинации с другими терминами, если не указано иное, означает карбоциклическую ароматическую систему, содержащую одно или несколько колец (типично одно, два или три кольца), где такие кольца могут быть присоединены в виде боковой группы,такой как дифенил, или могут быть конденсированными, такими как нафталин. Примеры включают фенил, антрацил и нафтил. Термин "арил-(C1-С 3)алкил" означает радикал, где алкиленовая цепь с 1-3 атомами углерода присоединена к арильной группе, например, -СН 2 СН 2-фенил. Аналогичным образом, термин "гетероарил(C1-С 3)алкил" означает радикал, где одна-три углеводородных алкиленовых цепей присоединены к гетероарильной группе, например, -СН 2 СН 2-пиридил. Термин "замещенный арил-(C1-С 3)алкил" означает арил-(C1-С 3)алкильный радикал, в котором арильная группа является замещенной. Термин "замещенный гетероарил-(C1-С 3)алкил" означает гетероарил-(C1-С 3)алкильный радикал, в котором гетероарильная группы является замещенной. Термин "арилен", сам по себе или в качестве части другого заместителя, если не указано иное, означает двухвалентный арильный радикал. Предпочтительными являются двухвалентные фенильные радикалы, в частности, 1,4-двухвалентные фенильные радикалы. Термин "гетероцикл" или "гетероциклический", сам по себе или в качестве части другого заместителя, означает, если не указано иное, незамещенную или замещенную, стабильную моно- или полициклическую гетероциклическую кольцевую систему, которая состоит из атомов углерода и по меньшей мере одного гетероатома, выбранного из группы, состоящей из N, О и S, и где гетероатомы азота и серы могут быть необязательно окислены, а атом азота необязательно может быть кватернизирован. Гетероциклическая система может быть связана, если не указано иное, посредством любого гетероатома или атома углерода, которые дают возможность получения устойчивой структуры. Термин "гетероарил" или "гетероароматический" относится к гетероциклу, имеющему ароматический характер. Примеры неароматических гетероциклов включают моноциклические группы, такие как азиридин,оксиран, тииран, азетидин, оксетан, тиетан, пирролидин, пирролин, имидазолин, пиразолидин, диоксолан, сульфолан, 2,3-дигидрофуран, 2,5-дигидрофуран, тетрагидрофуран, тиофан, пиперидин, 1,2,3,6 тетрагидропиридин, 1,4-дигидропиридин, пиперазин, морфолин, тиоморфолин, пиран, 2,3-дигидропиран,тетрагидропиран, 1,4-диоксан, 1,3-диоксан, гомопиперазин, гомопиперидин, 1,3-диоксепан, 4,7-дигидро 1,3-диоксепин и гексаметиленоксид. Примеры гетероарильных групп включают пиридил, пиразинил, пиримидинил, в частности, 2- и 4 пиримидинил, пиридазинил, тиенил, фурил, пирролил, в частности, 2-пирролил, имидазолил, тиазолил,оксазолил, пиразолил, в частности, 3- и 5-пиразолил, изотиазолил, 1,2,3-триазолил, 1,2,4-триазолил,1,3,4-триазолил, тетразолил, 1,2,3-тиадиазолил, 1,2,3-оксадиазолил, 1,3,4-тиадиазолил и 1,3,4-оксадиазолил. Примеры полициклических гетероциклов включают индолил, в частности, 3-, 4-, 5-, 6- и 7-индолил,индолинил, хинолил, тетрагидрохинолил, изохинолил, в частности, 1- и 5-изохинолил, тетрагидроизохинолил, циннолинил, хиноксалинил, в частности, 2- и 5-хиноксалинил, хиназолинил, 1,4-бензодиоксанил,кумарин, дигидрокумарин, бензофурил, в частности, 3-, 4-, 5-, 6- и 7-бензофурил, 2,3-дигидробензофурил, 1,2-бензизоксазолил, бензотиенил, в частности, 3-, 4-, 5-, 6- и 7-бензотиенил, бензоксазолил, бензотиазолил, в частности, 2-бензотиазолил и 5-бензотиазолил, пуринил, бензимидазолил, в частности, 2 бензимидазолил, бензотриазолил, тиоксантинил, карбазолил, карболинил, акридинил, пирролизидинил и хинолизидинил. Вышеуказанное перечисление гетероциклических и гетероарильных групп предназначено для иллюстрации, но не для ограничения изобретения. Термин "гетероарилен", сам по себе или в качестве части другого заместителя, означает, если не указано иное, двухвалентный гетероарильный радикал. Предпочтительными являются пяти- или шестичленные моноциклические гетероарилены. Более предпочтительными являются гетероариленовые группы, включающие двухвалентные гетероарильные кольца, выбранныеиз пиридина, пиперазина, пиримидина, пиразина, фурана, тиофена, пиррола, тиазола, имидазола и оксазола. Термин "углеводород" относится к любой группе, включающей только атомы водорода и углерода. Термин "замещенный" означает, что атом или группа атомов заменяют водород в качестве заместителя, присоединенного к другой группе. Для арильной и гетероарильной групп термин "замещенный" относится к любому уровню замещения, а именно моно-, ди-, три-, тетра- или пентазамещению, где такое замещение разрешено. Заместители являются независимо выбранными, и замещение может быть в лю- 23008736 бом химически достижимом положении. Когда заместитель представляет собой алкильную или алкоксигруппу, углеродная цепь может быть разветвленной, прямой или циклической, причем прямая является предпочтительной. Термин "антитело", как подразумевается, охватывает не только целые антигенсвязывающие молекулы иммуноглобулинов, но также включает их антигенсвязывающие фрагменты, такие как фрагментыFab, Fab' и F(ab')2, или любой другой фрагмент, сохраняющий антигенсвязывающую способность целого антитела. Термин "гуманизированное антитело" относится к антителу, которое имеет свои области, определяющие комплементарность (CDR), полученные из нечеловеческих образцов иммуноглобулина, а остающаяся часть молекулы антитела получена из человеческого иммуноглобулина. Термин "химерное антитело" означает антитело, включающее вариабельную область и константную область, полученные от различных видов. Термин "гуманизированное химерное антитело" означает химерное антитело, в котором, по меньшей мере, константная область получена из антител человека. Термин "моноспецифическое поликлональное антитело" означает антисыворотку, содержащую разнородные антитела, имеющие специфичность к одному антигену. Используемый термин "эффективное количество" относится к количеству соединения формулы I,которое ингибирует рост опухолевых клеток или, альтернативно, индуцирует апоптоз раковых клеток,предпочтительно опухолевых клеток, приводя к терапевтически полезному и селективному цитотоксическому действию на пролиферативные клетки, при введении пациенту, страдающему от рака или других расстройств, которые проявляют аномальную клеточную пролиферацию. Термин "одновалентная пептидильная группа" относится к пептидному радикалу в качестве заместителя в молекуле формулы I. Такой радикал имеет химическую структуру, которая отличается от структуры соответствующего пептида тем, что структурный компонент пептида, т.е. альфа аминогруппа, аминогруппа боковой цепи, альфа карбоксильная группа или карбоксильная группа боковой цепи, будут образовывать различные функциональные группы при соединении с молекулой, где он должен быть заместителем. Например, когда пептид, такой как показан ниже,является заместителем в соединении формулы I, и указанный пептид взаимодействует с соединением формулы I так, что карбоксильная группа указанного пептида соединяется со свободной аминогруппой соединения формулы I, происходит функциональное удаление Н 2 О, что приводит к образованию амидной связи. В качестве практического результата, соответствующий одновалентный пептидильный заместитель будет таким, как показано слева от пунктирной линии в приведенной ниже формуле вышеуказанного пептида, присоединенного к соединению формулы I Описание чертежа Чертеж показывает действие (Е)-2,4,6-триметоксистирил-3-(карбоксиметиламино)-4-метоксибензилсульфона на рост клеток указанных опухолевых клеточных линий. Значения представлены на графике в виде процента обработанных лекарственным препаратом клеток, остающихся жизнеспособными, по сравнению с клетками такого же типа, которые обработаны ДМСО. Детальное описание изобретения По настоящему изобретению определенные производные замещенных стирилбензилсульфонов селективно обеспечивают гибель различных типов опухолевых клеток, не затрагивая нормальные клетки. Без намерения углубляться в теорию, считается, что соединения воздействуют на путь сигнальной трансдукции МАРК, посредством этого воздействуя на рост и жизнеспособность опухолевых клеток. Данное подавление роста клеток связано с регуляцией ERK и JNK типов МАРК. Без намерения углубляться в теорию, стирилсульфоны по настоящему изобретению могут блокировать фосфорилирующую способность ERK-2. Соединение по изобретению ингибируют пролиферацию опухолевых клеток путем индуцирования гибели клеток. Соединения по изобретению рассматриваются в качестве эффективных против широкого спектра типов рака различного гистологического подтипа и природы. Типы рака, которые можно лечить соединениями по настоящему изобретению, включают, например, типы рака, перечисленные и описанные в- 24008736 включен в данное описание посредством ссылки во всей своей полноте. Например, соединения по изобретению можно использовать для обеспечения гибели первичной или метастатической опухоли или неопластических клеток при раке, по меньшей мере, следующих гистологических подтипов: саркоме (раке соединительной и другой ткани мезодермальной природы), меланоме(раке, происходящем из пигментированных меланоцитов), карциноме (раке эпителиальной природы),аденокарциноме (раке гландулярной эпителиальной природы), раке неврологической природы (глиоме/глиобластоме и астроцитоме) и гематологической неоплазии, такой как лейкемия и лимфома (например, острая лимфобластная лейкемия, хроническая лимфоцитная лейкемия и хроническая миелоцитическая лейкемия). Соединения по настоящему изобретению также можно использовать для обеспечения гибели первичной или метастатической опухоли или неопластических клеток при раке, источник происхождения которого находится, по меньшей мере, в следующих органах или тканях независимо от гистологического подтипа: в молочной железе, тканях мужской или женской мочеполовой системы (например, мочеточнике, мочевом пузыре, простате, яичке, яичнике, шейке матки, матке, влагалище), легких, тканях желудочно-кишечной системы (например, желудке, толстой и тонкой кишке, ободочной кишке, прямой кишке),внешнесекреторных железах, таких как поджелудочная железа и надпочечная железа, тканях рта и пищевода, головном мозге и спинном мозге, почке (почечный), поджелудочной железе, гепатобилиарной системе (например, печени, желчном пузыре), лимфатической системе, гладких и поперечно-полосатых мышцах, кости и костном мозге, на коже и в тканях глаза. Далее, настоящие соединения считаются эффективными при лечении рака или опухолей на любой прогностической стадии развития, определяемой, например, по "Международной классификации опухолей" (также называемой "Римской цифрой") или системе определения стадии: опухоль, лимфоузел, метастаз (TNM). Соответствующие прогностические системы определения стадии и описания стадий данного рака известны и описаны, например, на сайте http: //cancernet.nci.nih. gov/pdq/pdqtreatment.shtml, как указано выше. Соединения не затрагивают нормальные клетки при концентрациях, при которых обеспечивается гибель опухолевых клеток. Соединения также считаются пригодными для лечения нераковых пролиферативных расстройств. Нераковые пролиферативные расстройства характеризуются неконтролируемым ростом клеток с доброкачественным фенотипом, означая, что клетки только уклоняются от нормального контролирования роста, но не могут метастазировать. Нераковые пролиферативные расстройства, которые можно лечить соединениями по настоящему изобретению, включают, но не ограничиваются ими, следующие заболевания: гемангиоматоз новорожденных, вторичный прогрессирующий рассеянный склероз, хронические прогрессирующие миело-дегенеративные заболевания, нейрофиброматоз, ганглионейроматоз, образование келоидов, деформирующий остоз (болезнь Педжета), кистозно-фиброзное заболевание (например,молочной железы или матки), саркоидоз, болезнь Перони и болезнь Дюпюитрена, цирроз, атеросклероз и сосудистый рестеноз. Терапия данного широкого диапазона опухолевых клеток соединениями стирилбензилсульфонов по изобретению ведет к ингибированию клеточной пролиферации и индукции апоптоза клеток. Опухолевые клетки, обрабатываемые соединениями по изобретению, накапливаются в G2/M фазе клеточного цикла. Как только клетки покидают G2/M фазу, оказывается, что они подвергаются апоптозу. Терапия нормальных клеток стирилбензилсульфонами не приводит к апоптозу. Способы получения Промежуточные соединения формулы II по настоящему изобретению, представляющие собой (E)стирил-3-нитробензилсульфоны, можно получить конденсацией Кневенагеля ароматических альдегидов с бензилсульфонилуксусными кислотами. Данные промежуточные соединения формулы II, представляющие собой нитропроизводные, затем можно восстановить до соответствующих анилиновых производных и затем алкилировать атом азота анилиновой группы, получая промежуточные соединения, представляющие собой (E)-стирил-3-аминобензилсульфоны, формулы III. Указанное алкилирование анилина можно осуществить любым методом алкилирования, известным специалисту в данной области. Например, указанный атом азота анилиновой группы можно алкилировать SN2 реакцией с алкильной группой,содержащей уходящую группу, такую как галогенид, тозилат или мезилат. Примеры таких реагентов включают, например, метилйодид и бензилбромид. Другой способ алкилирования атома азота анилиновой группы состоит в восстановительном аминировании альдегидом или кетоном в присутствии соответствующего восстановителя. Подходящие восстановители для данной реакции включают, например, цианборгидрид натрия и триацетоксиборгидрид натрия, которые будут, при слегка кислом рН, селективно восстанавливать иминное промежуточное соединение в присутствии указанного альдегидного или кетонного исходного вещества, давая алкилированный продукт формулы III. Конденсация Кневенагеля описана Reddy et al., в Acta Chim. Hung. 115:269-71 (1984), Reddy et al.,Sulfur Letters 13:83-90 (1991), Reddy et al., Synthesis 4, 322-323 (1984) и Reddy et al., Sulfur Letters 7:4348 (1987), полное описание которых включено в данное описание посредством ссылки. Согласно приведенной ниже схеме 1 бензилтиоуксусную кислоту С получают взаимодействием тиогликолята натрия и бензилгалогенида В. Затем бензилтиоуксусную кислоту С окисляют 30% перокси- 25008736 дом водорода, получая соответствующую бензилсульфонилуксусную кислоту D. Конденсация бензилсульфонилуксусной кислоты D с ароматическим альдегидом Е посредством реакции Кневенагеля в присутствии бензиламина и ледяной уксусной кислоты дает желаемый (Е)-стирил-3-нитробензилсульфон F. Затем (E)-стирил-3-нитробензилсульфон F восстанавливают катализируемым палладием гидрированием с гидратом гидразина в качестве источника водорода, либо Na2S2O4, и затем алкилируют, получая желаемый (Е)-стирил-3-аминобензилсульфон IIIа. Схема 1 Далее следует более детальная состоящая из двух частей методика синтеза промежуточных соединений (Е)-стирилбензилсульфона в соответствии с приведенной выше схемой. Общая методика 1. Синтез (Е)-стирилбензилсульфонов. Часть А. К раствору гидроксида натрия (8 г, 0,2 моль) в метаноле (200 мл) медленно добавляют тиогликолевую кислоту (0,1 моль) и образовавшийся осадок растворяют, перемешивая содержимое колбы. Затем постепенно добавляют соответствующим образом замещенный бензилгалогенид (0,1 моль) и реакционную смесь кипятят с обратным холодильником в течение 2-3 ч. Охлажденное содержимое выливают на толченый лед и нейтрализуют разбавленным раствором хлористо-водородной кислоты (200 мл). Полученную в результате соответствующую бензилтиоуксусную кислоту (0,1 моль) подвергают окислению 30% пероксидом водорода (0,12 моль) в ледяной уксусной кислоте (125 мл), кипятя с обратным холодильником в течение 1 ч. Содержимое охлаждают и выливают на толченый лед. Отделенное твердое вещество перекристаллизовывают из горячей воды, получая соответствующую чистую бензилсульфонилуксусную кислоту, D. Часть В. Смесь бензилсульфонилуксусной кислоты (10 ммоль), соответствующим образом замещенного ароматического альдегида Е (10 ммоль) и бензиламина (200 мл) в ледяной уксусной кислоте (12 мл) кипятят с обратным холодильником в течение 2-3 ч. Содержимое охлаждают и обрабатывают холодным эфиром (50 мл). Осажденный продукт выделяют фильтрованием. Фильтрат разбавляют дополнительным количеством эфира и последовательно промывают насыщенным раствором бикарбоната натрия(20 мл), бисульфита натрия (20 мл), разбавленным раствором хлористо-водородной кислоты (20 мл) и,наконец, водой (35 мл). Выпаривание высушенного эфирного слоя дает стирилбензилсульфоны в виде твердого вещества. В соответствии с альтернативой части А соответствующие бензилсульфонилуксусные кислоты можно получить, заменяя тиогликолевую кислоту тиогликолятом HSCH2COOR, где R представляет собой алкильную группу, обычно (C1-С 6)алкил. Это приводит к образованию алкилбензилтиоацетатного промежуточного соединения (Н) которое затем превращают в соответствующую бензилтиоуксусную кислоту В щелочным или кислотным гидролизом. Стирилбензил-3-аминозамещенные сульфоны по настоящему изобретению получают несколькими реакциями синтеза из общего стирилбензил-3-аминосульфона формулы IIIа. Данные реакции обычно включают сочетание нуклеофильного анилинового азота соединений формулы IIIа с электрофильными группами. Например, взаимодействие с активированными кислотами, такими как хлорангидриды, будет давать амиды формулы IV, как изображено на приведенной ниже схеме 2. Методики синтеза для данного типа взаимодействия даются в приведенных ниже примерах 2, 5, 9 и 10. Схема 2 Дополнительные соединения карбоксамида формулы V можно получить сочетанием промежуточных соединений формулы IIIа с неактивированными карбоксильными группами, используя связывающее вещество, такое как диизопропилкарбодиимид, как изображено на приведенной ниже схеме 3. Детальные методики для данного типа взаимодействия даются в примерах 13, 14 и 15. На схеме 3 Ra выбран из -Н,-СН 3, -(СН 2)3-NH-C(NH2)(=NH), -CH2C(=O)NH2, -CH2COOH, -CH2SH, -(CH2)2C(=O)-NH2, -(CH2)2COOH,-CH2-(2-имидазолила), -CH(CH3)-CH2-CH3, -CH2CH(CH3)2, -(CH2)4-NH2, -(CH2)2-S-CH3, фенила, СН 2 фенила, -CH2-OH, -CH(OH)-CH3, -СН 2-(3-индолила), -СН 2-(4-гидроксифенила), -СН(СН 3)2 и -СН 2-СН 3, и включает соединения, где Ra и R1 объединены с образованием 5- или 6-членного гетероциклического кольца. Примеры гетероциклических колец в данном контексте включают пирролидин, гидроксипирролидин, тиазолидин, пиперидин и гомопиперидин. Схема 3 В аналогичной реакции взаимодействие промежуточных соединений формулы IIIа с сульфонилгалогенидами дает соответствующие соединения сульфонамидов формулы VI, как показано на приведенной ниже схеме 4. Методика синтеза для данного типа взаимодействия дается в примере 1. Схема 4 Взаимодействие соединений формулы IIIа с использованием йодида 2-хлор-1-метилпиридиния(реагент Мукаямы) дает производные гуанидина формулы VII, как показано на приведенной ниже схеме 5. Методика синтеза для данного типа взаимодействия дается в примере 3. Схема 5- 27008736 Также можно осуществить сочетание азота анилиновой группы соединения формулы IIIа с алкилгалогенидными группами с sp3 гибридизацией с получением вторичных или третичных аминоз общей формулы VIII, как изображено на приведенной ниже схеме 6. Методика синтеза для данного типа взаимодействия дается в примере 4. Схема 6 Также можно осуществить сочетание азота анилиновой группы соединений формулы IIIа с альдегидами или кетонами или их гидратами с получением иминов формулы IX, как показано на приведенной ниже схеме 7. Методика синтеза для данного типа взаимодействия дается в примере 12. Схема 7 Азот анилиновой группы соединений формулы IIIа также может быть подвергнут взаимодействию с образованием соответствующих групп мочевины формулы X. Как показано на приведенной ниже схеме 8, незамещенную мочевину можно получить взаимодействием соединений формулы IIIа с цианатом калия. Мочевину, замещенную на периферическом азоте, можно получить, как показано на схеме 8, взаимодействием соединений формулы IIIа с N-замещенными карбамилгалогенидами. Кроме того, взаимодействие с замещенными цианатными группами будет давать однозамещенные мочевины. Методика синтеза для данного типа взаимодействия дается в примере 16. Схема 8 Азот анилиновой группы соединений формулы IIIа также может быть подвергнут взаимодействию с образованием аминокислотных производных формулы XX, где азот анилиновой группы соединенияIIIа представляет собой альфа-аминогруппу аминокислоты. Как показано на приведенной ниже схеме 9,данные аминокислотные производные можно получить взаимодействием соединения формулы III с карбоновой кислотой, имеющей уходящую группу в альфа-положении к карбоксилату. Например, исходным карбоксилатом для соединения примера 4 является метилбромацетат. Пример 22 представляет собой другое соединение, где получают производное по азоту анилиновой группы в виде аминокислоты (аланин). Схема 9- 28008736 В одной конкретной реакции снятия защиты соль соединений карбоновой кислоты формулы XX,предпочтительно соль щелочного металла, более предпочтительно натриевую соль, получают гидролизом производного сложного эфира карбоновой кислоты в водном основании, как показано на приведенной ниже схеме 10. Данный способ более детально описан в примере 4 а. Схема 10 В соединения стирилбензилсульфона по настоящему изобретению можно ввести химические группы в качестве заместителей, чтобы дать возможность конъюгации с молекулой-носителем с целью приращивания антител к стирилсульфонам. Подходящие химические методики получения производных хорошо известны специалисту в данной области. Предпочтительно, производное включает производное карбоновой кислоты. Носитель может включать любую молекулу, достаточно большую, чтобы вызывать иммунную реакцию у соответствующего животного-хозяина. Одним таким предпочтительным носителем является гемоцианин моллюска (KLH). Кроме того, структурные компоненты R1 (такие как пептидильные заместители) соединений по настоящему изобретению сами могут обладать антигенной активностью, достаточной для присоединения антител к стирилсульфонам. Антитела, предпочтительно, моноклональные антитела и моноспецифические поликлональные антитела и, наиболее предпочтительно, опухолеспецифические антитела можно связать ковалентной связью с соединениями по настоящему изобретению. Под "опухолеспецифическим антителом" понимают антитело, которое специфически связывается с опухолевым антигеном, например, антигеном на опухолевой клетке. Ковалентный линкер между соединением формулы I или формулы III и антителом может, в своей простейшей форме, включать простую ковалентную связь, соединяющую соединение формулы I с антителом. В более общем случае, соединение формулы I присоединено к антителу с использованием подходящего бифункционального связывающего реагента. Термин "бифункциональный связывающий реагент", обычно, относится к молекуле, которая содержит две реакционноспособные группы, которые соединены вместе спейсерным элементом. Термин"реакционноспособные группы" в данном контексте относится к химическим функциональным группам,способным взаимодействовать с антителом или соединением формулы I посредством реагирования с функциональными группами на антителе и соединении формулы I или формулы III. Примером ковалентной связи, образованной в виде линкера между соединением формулы I или формулы III и антителом является дисульфидная связь, образованная окислением антитела и соединения формулы I (или формулы III), где R1 представляет собой пептидильную группу, содержащую одну или несколько цистеиновых аминокислот. Цистеиновые остатки можно окислить с образованием дисульфидных звеньев, растворяя 1 мг подходящего соединения формулы I (или формулы III) и 0,5 эквивалента желаемого антитела в 1,5 мл 0,1% (об./об.) 17,5 мМ уксусной кислоты, рН 8,4, с последующей продувкой азотом и затем промывкой 0,01 М K2Fe(CN)6. После инкубации в течение одного часа при комнатной температуре аддукт пептида очищают ВЭЖХ. Другим примером подходящей ковалентной связи, образованной в виде линкера между соединением формулы I (или формулы III) и антителом, является амидная связь, образованная взаимодействием аминогруппы на соединении по изобретению (включая соединение формулы III, где X представляет собой -NH2 (т.е., где X имеет формулу (i), у равен 0, R1 представляет собой -Н и R2 представляет собой -Н),а также аминогруппы на -М-двухвалентных соединяющих группах или на пептидильных R1 заместителях, таких как, например, боковая цепь лизина) с карбоксильной группой, которая формирует часть первичной структуры антитела (Аb) (такую, как, например, глутаминовые или аспаргиновые аминокислотные остатки). Альтернативно, амидную связь можно получить, если реагирующие группы изменены на противоположные, т.е. соединение формулы I может содержать функциональную группу карбоновой кислоты и реагировать с аминофункциональной группой в структуре Аb. Альтернативно, соединение формулы I (или формулы III) и антитело Аb можно ковалентно связать,используя бифункциональный связующий реагент. В одном таком варианте осуществления настоящего изобретения соединение формулы I (или формулы III), где R1 представляет собой пептидильную группу,сочетается с антителом при использовании бифункционального связующего реагента. В другом таком варианте осуществления изобретения соединение формулы I (или формулы III), где X представляет со- 29008736 бой -NH2 (т.е. X имеет формулу (i), у равен 0 и R1 и R2 оба представляют собой -Н), присоединяется к антителу. Например, аддукты можно получить, сначала получая S-(-N-гексилсукцинимидо)модифицированные производные антитела и соединения формулы I методом, описанным Cheronis et al., в J. Med.Chem. 37: 348 (1994) (полное описание которой включено в данное описание посредством ссылки). Nгексилмалеимид, предшественник модифицированного антитела и соединения формулы I, получают изN-(метоксикарбонил)малеимида и N-гексиламина, смешивая два соединения в насыщенном NаНСО 3 при 0 С по процедуре, описанной в Bodanszky and Bodanszky, The Practice of Peptide Synthesis; SpringlerVerlag, New York, pp. 29-31 (1984) (полное описание которой включено в данное описание посредством ссылки). Продукт полученной реакционной смеси выделяют экстракцией этилацетатом, с последующей промывкой водой, сушкой над Na2SO4 и затем концентрированием в вакууме, приводящих к получениюN-гексилмалеимида в виде светло-желтого масла. S-(N-гексилсукцинимидо)модифицированное антитело и соединение формулы I затем получают из цистеинсодержащего пептида и N-гексилмалеимида, смешивая одну часть пептида с 1,5 частями N-гексилмалеимида в диметилформамиде (3,3 мл/мМ пептида), с последующим добавлением до 30 объемов 0,1 М бикарбоната аммония, рН 7,5. Реакция S-алкилирования,осуществляемая таким образом, завершается в течение 30 мин. Получаемый в результате S-(-Nгексилсукцинимидо)модифицированный пептидный мономер очищают препаративной ВЭЖХ с обращенной фазой, с последующей лиофилизацией в виде хлопьевидного белого порошка. Бис-сукцинимидогексанпептидные гетеродимеры (где один пептид представляет собой антитело, а другой пептид представляет собой соединение формулы I, где R1 является пептидильной группой), можно получить методом, описанным Cheronis et al., см. выше из цистеинзамещенных пептидов. Готовят смесь одной части бис-малеимидогексана с двумя частями пептидного мономера в диметилформамиде(3,3 мл/мМ пептида), с последующим добавлением 0,1 М бикарбоната аммония, рН 7,5. Реакционную смесь перемешивают при комнатной температуре, и обычно реакция завершается в течение 30 мин. Полученный в результате бис-сукцинимидогексанпептидный димер очищают препаративной ВЭЖХ с обращенной фазой. После лиофилизации вещество представляет собой хлопьевидный белый порошок. Ковалентно связанные аддукты общей формулы I-L-Ab по настоящему изобретению, или формулыIII-L-Ab, когда связаны с соединением формулы III, можно получить, используя гомобифункциональные связывающие реагенты (где две реакционноспособные группы являются одинаковыми), такие как, например, дисукцинимидилтартрат, дисукцинимидилсуберат, этиленгликольбис-(сукцинимидилсукцинат),1,5-дифтор-2,4-динитробензол ("DFNB"), стильбен 4,4'-диизотиоциано-2,2'-дисульфоновая кислота("DIDS") и бис-малеимидогексан ("ВМН"). Реакция связывания протекает случайным образом между Ab и соединением формулы I, имеющим пептидильную группу в качестве R1. Альтернативно, могут использоваться гетеробифункциональные связывающие реагенты. Такие реагенты, включают, например, N-сукцинимидил-3-(2-пиридилдитио)пропионат ("SPDP"), сульфосукцинимидил-2-(п-азидосалициламидо)этил-1,3'-дитиопропионат ("SASD", Pierce Chemical Company, Rockford,IL), N-малеимидобензоил-N-гидроксисукцинимидиловый сложный эфир ("MBS"), м-малеимидобензоилсульфосукцинимидный сложный эфир ("сульфо-MBS"), N-сукцинимидил(4-йодацетил)аминобензоат ("SIAB") , сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат ("SMCC"), сукцинимидил-4-(п-малеимидофенил)бутират ("SMPB"), сульфосукцинимидил-(4-йодацетил)аминобензоат ("сульфо-SIAB"), сульфосукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат ("сульфо-SMCC") ,сульфосукцинимидил-4-(п-малеимидофенил)бутират ("сульфо-SMPB") , бромацетил-п-аминобензоил-Nгидроксисукцинимидиловый сложный эфир, йодацетил-N-гидроксисукцинимидиловый сложный эфир и аналогичные соединения. Для гетеробифункционального связывания получают производное соединения формулы I (или соединения формулы III), например, с N-гидроксисукцинимидильной частью бифункционального реагента,и полученное в результате производное соединение очищают хроматографией. Затем подходящее опухолеспецифическое Маb подвергают взаимодействию со второй функциональной группой на бифункциональном связывающем реагенте, обеспечивая ориентированную последовательность связывания компонентов желаемого аддукта. Типичные гетеробифункциональные связывающие реагенты для получения белок-белковых коньюгатов содержат химически активный по отношению к аминогруппе N-гидроксисукцинимидный сложный эфир (NHS-эфир) в качестве одной функциональной группы и группу, реакционноспособную по отношении к сульфгидрильной группе, в качестве другой функциональной группы. Сначала эпсилонаминогруппы поверхностных лизиновых остатков Маb, либо соединения формулы I (или соединения формулы III) ацилируют NHS-сложноэфирной группой сшивающего реагента. Остающийся компонент,обладающий свободными сульфгидрильными группами, взаимодействует с группой, реакционноспособной по отношении к сульфгидрильной группе сшивающего реагента с образованием ковалентно сшитого димера. Обычные реакционноспособные по отношению к тиолу группы включают, например, имиды малеиновой кислоты, дисульфиды пиридила и активные галогены. Например, MBS содержит NHSсложный эфир в качестве группы, реакционноспособной по отношению к амину, и группу имида малеиновой кислоты в качестве группы, реакционноспособной по отношению к сульфгидрилу.
МПК / Метки
МПК: A61P 35/00, A61K 31/136, C07C 217/54, C07C 251/08, C07C 251/24
Метки: аминозамещённые, е)-2,6-диалкоксистирил-4-замещённые-бензилсульфоны, пролиферативных, расстройств, лечения
Код ссылки
<a href="https://eas.patents.su/30-8736-aminozameshhyonnye-e-26-dialkoksistiril-4-zameshhyonnye-benzilsulfony-dlya-lecheniya-proliferativnyh-rasstrojjstv.html" rel="bookmark" title="База патентов Евразийского Союза">Аминозамещённые (е)-2,6-диалкоксистирил-4-замещённые-бензилсульфоны для лечения пролиферативных расстройств</a>
Предыдущий патент: Способ загрузки мелкозернистых металлов в электрическую дуговую печь
Следующий патент: Средство для профилактики и лечения конъюнктивитов и кератитов различной этиологии (варианты), способ его применения
Случайный патент: Соединения азаиндазола и способы применения