Хинолинкарбоксамиды в качестве противовирусных агентов
Номер патента: 3945
Опубликовано: 30.10.2003
Авторы: Таисривонгс Сувит, Стробач Джозеф Волтер, Шнуте Марк Э., Тернер Стивен Рональд, Вэйлланкорт Валери А., Такер Джон Алан
Формула / Реферат
1. Соединение формулы I
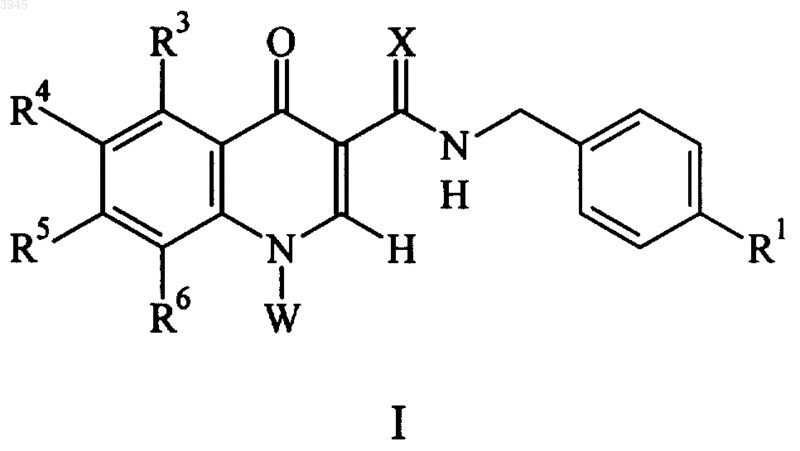
или его фармацевтически приемлемая соль,
где X представляет
a) O или
b) S;
W представляет
a) R2,
b) NR7R8,
c) OR9 или
d) SOiR9;
R1 представляет
a) Cl,
b) F,
c) Br,
d) CN или
e) NO2;
R2 представляет
a) (CH2CH2O)mR10,
b) het, где указанный het связан через атом углерода,
c) C1-7алкил, который может быть частично ненасыщенным и необязательно замещенным одним или несколькими заместителями, выбранными из группы, включающей NR7R8, R11, CN, SOiR9 или OC2-4алкил, который дополнительно замещен het, OR10, OC(=O)арилом или NR7R8, или
d) C3-8циклоалкил, который может быть частично ненасыщенным и необязательно замещенным R11, NR7R8, SOiR9 или C1-7алкилом, необязательно замещенным R11, NR7R8 или SOiR9;
R3 представляет
a) H,
b) галоген или
c) C1-4алкил, необязательно замещенный одним-тремя галогенами;
R4 представляет
a) H,
b) арил,
c) het,
d) SO2NHR12,
e) CONHR12,
f) NR7R8,
g) NHCOR12,
h) NHSO2R12,
i) OC2-7алкил, необязательно замещенный -OH,
j) SC2-7алкил, необязательно замещенный -OH или
k) C1-8алкил, который может быть частично ненасыщенным и необязательно замещен одним или несколькими заместителями, выбранными из группы, включающей N3, OR10, NR7R8, галоген, SOiR9, OR13 или R11;
R5 представляет
a) H,
b) галоген,
c) Cу CR14,
d) NR7R8,
e) SO2NHR12,
f) het или
g) C1-7алкил, необязательно замещенный OH;
R6 представляет
a) H,
b) галоген,
c) SC1-7алкил,
e) C1-7алкокси, необязательно замещенный одним или несколькими галогенами или OH, или
f) C1-7алкил, который может быть частично ненасыщенным и необязательно замещен галогеном, NR10R10, (CH2)nOR13, R11, OC1-7алкилом, который дополнительно замещен het, NR7R8 или SOiR9;
R7 и R8 независимо представляют
a) H,
b) арил,
c) C1-7алкил, который может быть частично ненасыщенным и необязательно замещен одним или несколькими заместителями, выбранными из группы, включающей NR10R10, CONR10R10, R11, SOiR9, галоген, или
d) R7 и R8 вместе с азотом, к которому они присоединены, образуют het;
R9 представляет
a) арил,
b) het,
c) C3-8циклоалкил или
d) C1-7алкил, который может быть частично ненасыщенным и необязательно замещенным одним или несколькими OR10, Oарилом, het, арилом, NR10R10, CN, SH, SOiC1-6алкилом, SOiарилом, галогеном или CONR10R10;
R10 представляет
a) H или
b) C1-7алкил, необязательно замещенный OH;
R11 представляет
a) OR10,
b) Ohet,
c) Oарил,
d) CO2R10,
e) het,
f) арил или
g) CN;
R12 представляет
a) H,
b) het,
c) арил,
d) C3-8циклоалкил или
e) C1-7алкил, необязательно замещенный NR7R8 или R11;
R13 представляет
a) (P=O)(OH)2,
b) (P=O)(C1-7алкокси)2,
c) CO(CH2)nCON(CH3)(CH2)nSO3-M+,
d) аминокислоту,
e) C(=O)арил,
f) C (=O)C1-6алкил, необязательно замещенный NR10R10, или
g) CO(CH2)nCO2H
R14 представляет
a) het,
b) (CH2)nOR13 или
c) C1-7алкил, замещенный одним или несколькими заместителями, выбранными из группы, включающей R11, OC1-7алкил, который дополнительно замещен het, NR7R8 или SOiR9;
арил представляет фенильный радикал или ортоконденсированный бициклический карбоциклический радикал, где по крайней мере одно кольцо является ароматическим;
het представляет четырех- (4), пяти- (5), шести- (6) или семи- (7) членное насыщенное или ненасыщенное гетероциклическое кольцо, имеющее 1, 2 или 3 гетероатома, выбранных из группы, состоящей из кислорода, серы и азота, которое необязательно конденсировано с бензольным кольцом, или любую бициклическую гетероциклическую группу;
где любой арил необязательно замещен одним или несколькими заместителями, выбранными из группы, включающей галоген, OH, CF3, C1-6алкокси и C1-6алкил, который дополнительно может быть замещен одним-тремя SR10, NR10R10, OR10 или CO2R10;
где любой het необязательно замещен одним или несколькими заместителями, выбранными из группы, включающей галоген, OH, CF3, C1-6алкокси, оксо, оксин и C1-6алкил, который дополнительно может быть замещен одним-тремя SR10, NR10R10, OR10 или CO2R10;
i составляет 0, 1 или 2;
m составляет 1, 2 или 3;
n составляет 1, 2, 3, 4, 5 или 6 и
M представляет натрий, калий или литий;
при условии, что R1 не является Cl, Br, F или CN;
когда X представляет O;
R2 представляет C1-7алкил, необязательно замещенный R15;
R3 представляет H, метил или галоген;
R4 представляет H, CONH (C1-7алкил), NR16R17 или C1-7алкил, необязательно замещенный OR10, CN, COOH или NR16N17;
R5 представляет H, галоген, SO2NHR10, NR16R17 или C1-7алкил, необязательно замещенный OR10;
R6 представляет H, галоген, C1-7алкокси или C1-7алкил, необязательно замещенный галогеном, OR10, CO2R10 или NR16R17;
R15 представляет NR16R17, OR10, CN или CO2R10 и
R16 и R17 независимо представляют H или C1-7алкил; или NR16R17 вместе с азотом, к которому они присоединены, образуют 5- или 6-членное кольцо, такое как пирролидин, пиперидин, морфолин или пиперазин.
2. Соединение по п.1, где R1 представляет Cl.
3. Соединение по п.1, где R1 представляет F.
4. Соединение по п.1, где R1 представляет CN или NO2.
5. Соединение по п.1, где R2 представляет (CH2CH2O)mH шыш (CH2CH2O)mC1-4алкил, где m равен 2 или 3.
6. Соединение по п.1, где R2 представляет C3-8циклоалкил, необязательно замещенный R11, NR7R8, SOiR9 или C1-7алкил, необязательно замещенный R11, NR7R8 или SOiR9; где R7, R8, R9, R11 и i такие же, как определено в п.1.
7. Соединение по п.1, где R2 представляет циклопропил.
8. Соединение по п.1, где R2 представляет het, где указанный het связан через атом углерода и является таким же, как определено в п.1.
9. Соединение по п.8, где het представляет тетрагидро-2H-пиранил, пиперидинил, 1-метилпиперидинил или 1,1-диоксотетрагидро-2H-тиопиран.
10. Соединение по п.1, где R2 представляет C2-7алкил, который является частично ненасыщенным и необязательно замещенным NR7R8, R11, SOiR9 или OC2-4алкилом, который дополнительно замещен het, OR10, OC(=O)арилом; где R7, R8, R9, R10 такие же, как определено в п.1.
11. Соединение по п.10, где R2 представляет (Z или E)-CH=CHR10 или C-Cу CR10, где указанный R10 представляет H или C1-7алкил, необязательно замещенный OH.
12. Соединение по п.1, где R2 представляет C1-7алкил, замещенный NR7R8, R11, SOiR9 или OC2-4алкилом, который дополнительно замещен het, OR10, OC(=O)арилом; где R7, R8, R9, R10 и R11 такие же, как определено в п.1.
13. Соединение по п.1, где R2 представляет C1-7алкил, замещенный OC2-4алкилом, который дополнительно замещен het, OH, OC1-4алкилом или OC(=O)арилом.
14. Соединение по п.1, где R2 представляет C1-7алкил, замещенный SOiR9, где R9 и i такие же, как определено в п.1.
15. Соединение по п.1, где R2 представляет C1-7алкил, замещенный SOiR9, где R9 представляет C1-4алкил, необязательно замещенный OH, или R9 представляет фенил, необязательно замещенный Cl, где i равно 0, 1 или 2.
16. Соединение по п.1, где R2 представляет метил.
17. Соединение по п.1, где W представляет NR7R8, где R7 и R8 такие же, как определено в п.1.
18. Соединение по п.1, где W представляет NR7R8, где R7 и R8 вместе с азотом, к которому они присоединены, образуют het, при этом указанный het является таким же, как определено в п.1.
19. Соединение по п.18, где het представляет морфолин, пиперидин, пирролидин, пиперазин или 4-метилпиперазин.
20. Соединение по п.1, где W представляет NR7R8, где R7 и R8 независимо представляют H или C1-4алкил, необязательно замещенный OH.
21. Соединение по п.18, где het представляет морфолин.
22. Соединение по п.1, где W представляет OR9 или SOiR9, где R9 представляет C1-6алкил, который может быть частично ненасыщенным и необязательно замещенным OR10, Oарилом, het, арилом, NR10R10, CN, CONR10R10 или галогеном; где R10 представляет H или C1-4алкил.
23. Соединение по п.1, где R3 представляет H.
24. Соединение по п.1, где R3 представляет CF3 или галоген.
25. Соединение по п.1, где R4 представляет арил или het.
26. Соединение по п.1, где R4 представляет SO2NHR12, CONHR12, NHCOR12 или NHSO2R12, где R12 является таким, как определено в п.1.
27. Соединение по п.1, где R4 представляет C2-8алкил, который является частично ненасыщенным и необязательно замещен OR10, NR7R8, галогеном, SOiR9, OR13 или R11, где R7, R8, R9, R10, R11 и R13 такие, как определено в п.1.
28. Соединение по п.1, где R4 представляет (Z или E)-CH=CHC1-4алкил, необязательно замещенный OH.
29. Соединение по п.1, где R4 представляет -Cу CC1-4алкил, необязательно замещенный OH или OR13, где R13 представляет (P=O)(OH)2, (P=O)(C1-7алкокси)2 или CO(CH2)6CON(CH3)(CH2)nSO3- M+.
30. Соединение по п.1, где R4 представляет C1-8алкил, замещенный OR13, где R13 представляет (P=O)(OH)2, (P=O)(C1-7алкокси)2 или CO(CH2)nCON(CH3)(CH2)6SO3- M+.
31. Соединение по п.1, где R4 представляет C1-8алкил, замещенный SOiR9, где R9 такой, как определено в п.1.
32. Соединение по п.1, где R4 представляет NR7R8, где R7 и R8 такие, как определено в п.1.
33. Соединение по п.1, где R4 представляет C1-8алкил, замещенный NR7R8, где R7 и R8 такие, как определено в п.1.
34. Соединение по п.33, где R7 и R8 вместе с атомом азота, с которым они связаны, образуют het, где het является таким, как определено в п.1.
35. Соединение по п.33, где R7 и R8 независимо представляют C1-6алкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, включающей OH, арил или CN, где арил является таким, как определено в п.1.
36. Соединение по п.1, где R4 представляет C1-8алкил, замещенный N3.
37. Соединение по п.1, где R4 представляет C1-8алкил, замещенный het, где het является таким, как определено по п.1.
38. Соединение по п.1, где R4 представляет 4-морфолинметил.
39. Соединение по п.1, где R4 представляет C1-7алкил, замещенный R11, где R11 является таким, как определено в п.1.
40. Соединение по п.1, где R5 представляет H или C1-7алкил, необязательно замещенный OH.
41. Соединение по п.1, где R6 представляет OC1-7алкил, необязательно замещенный одним или несколькими OH.
42. Соединение по п.1, где R6 представляет галоген.
43. Соединение по п.1, где R6 представляет Cу CC1-7алкил, замещенный одним или несколькими OH, или C2-7алкокси, замещенный одним или несколькими OH.
44. Соединение по п.1, где R6 представляет H или C1-7алкил, необязательно замещенный галогеном, NR10R10, OH, CO2R10 или het; где R10 и het такие, как определено в п.1.
45. Соединение по п.1, где M представляет натрий, калий или литий.
46. Соединение по п.1, где X представляет S; W, R1, R2, R3, R4, R5, R6 такие, как определено по п.1.
47. Соединение по п.1, где X представляет O; R1, R3, R4, R5, R6 такие, как определено в п.1, W представляет NR7R8, OR9, SOiR9 или R2; где R2 представляет
a) (CH2CH2O)nR10,
b) het, где указанный het связан через атом углерода,
c) C1-7алкил, который является частично ненасыщенным и необязательно замещен ОН,
d) C3-8циклоалкил или
e) C1-7алкил, который необязательно замещен одним или несколькими заместителями, выбранными из группы, включающей Ohet, Oарил, SOiR9 или OC2-4алкил, который дополнительно замещен het, OR10 или OC(=O)арилом;
где R7, R8, R9, R10 и n являются такими, как определено в п.1.
48. Соединение по п.1, где X представляет O или S; R1 представляет Cl; R3 представляет H; R5 представляет H; R6 представляет H или F; R4 представляет 4-морфолинилметил и R2 представляет
a) C1-4алкил, замещенный SOiR9, или C1-4алкокси, который дополнительно замещен OH, het, OC1-4алкилом или OC(=O)фенилом,
b) (CH2CH2O)2C1-4алкил,
c) C1-6алкил, который является частично ненасыщенным и необязательно замещен OH,
d) циклопропил,
e) тетрагидро-2H-пиранил,
f) пиперидинил,
g) морфолинил,
h) 1-метилпиперидинил или
i) 1,1-диоксотетрагидро-2H-тиопиран;
где R9 представляет фенил, необязательно замещенный Cl, или R9 представляет C1-6алкил, необязательно замещенный OH.
49. Соединение по п.1, где X представляет O или S; R1 представляет Cl; R3 представляет H; R5 представляет H; R6 представляет H или F; R4 представляет C1-6алкил, который является частично ненасыщенным и необязательно замещенным OH или OR13; или R4 представляет C1-4алкил, замещенный OR13; W представляет NR10R10, циклопропил, (CH2CH2O)2OR10 или C1-6алкил, который может быть частично ненасыщенным и необязательно замещенным OH, морфолинилом, NR10R10; C(=O)OC1-4алкил, где R10 представляет H или C1-4алкил; R13 представляет (P=O)(C1-7алкокси)2, CO(CH2)nCON(CH3)(CH2)nSO3-M+ или (P=O)(OH)2.
50. Соединение по п.1, где X представляет O или S; R1 представляет Cl; R3 представляет H; R5 представляет H; R6 представляет Cу CC1-4алкил, необязательно замещенный OH; R4 представляет H или C1-4алкил, который может быть частично ненасыщенным и необязательно замещенным OH, а W представляет C1-4алкил, необязательно замещенный OH.
51. Соединение по п.1, представляющее собой
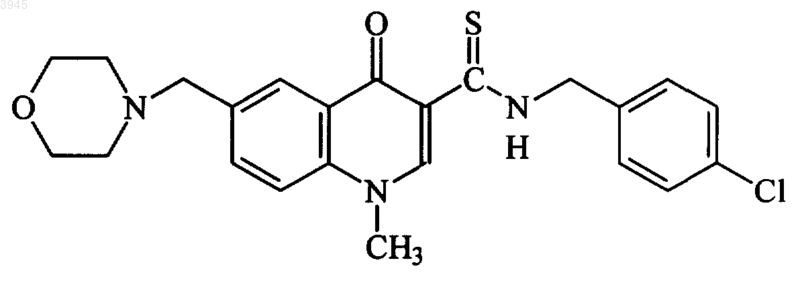
или его фармацевтически приемлемая соль.
52. Соединение по п.1, представляющее собой
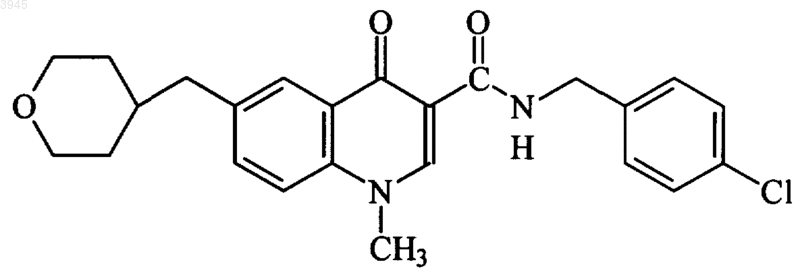
или его фармацевтически приемлемая соль.
53. Соединение по п.1, представляющее собой
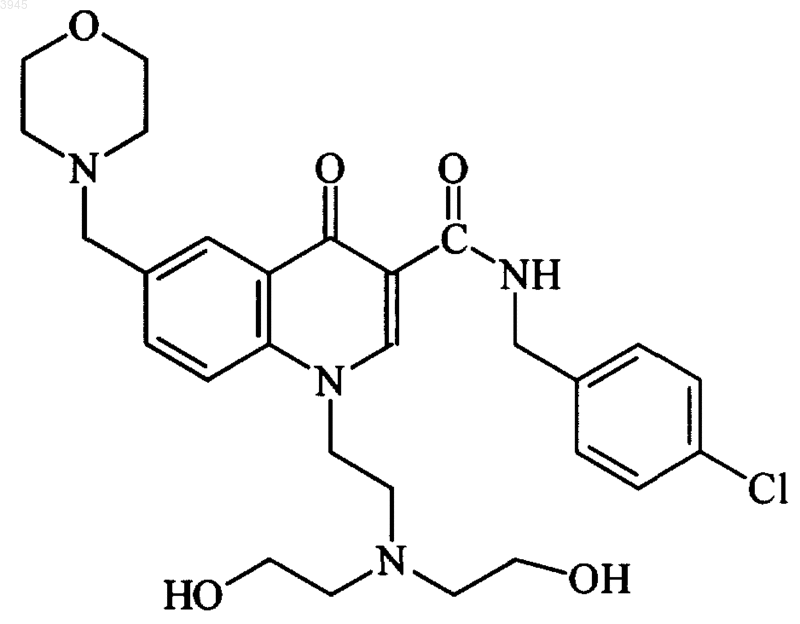
или его фармацевтически приемлемая соль.
54. Соединение по п.1, представляющее собой
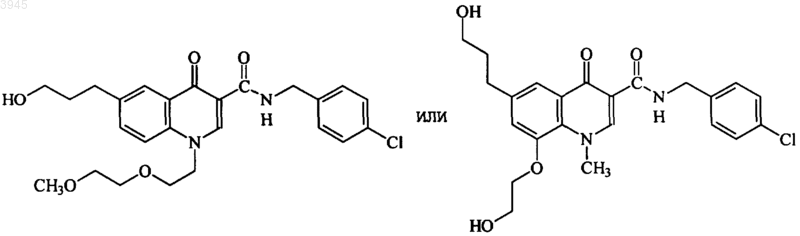
или его фармацевтически приемлемая соль.
55. Соединение по п.1, представляющее собой
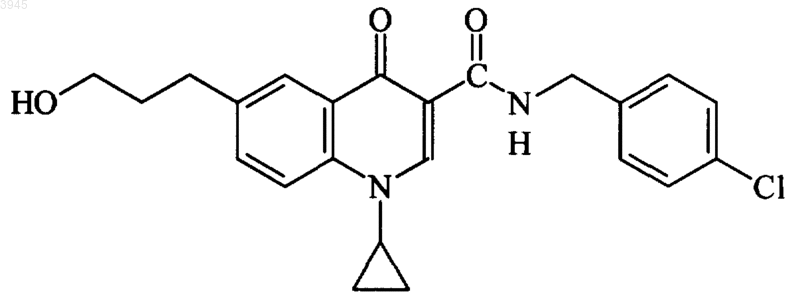
или его фармацевтически приемлемая соль.
56. Соединение по п.1, представляющее собой
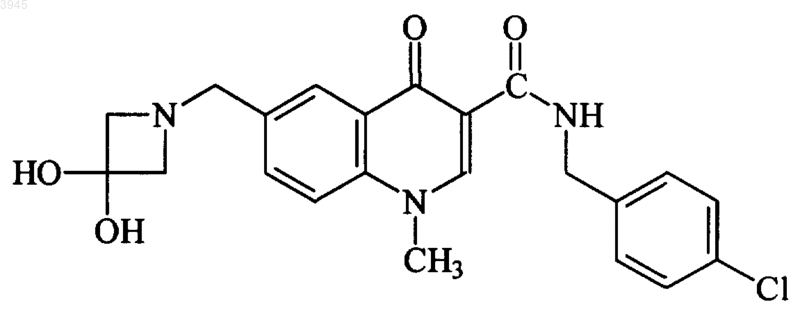
или его фармацевтически приемлемая соль.
57. Соединение по п.1, представляющее собой
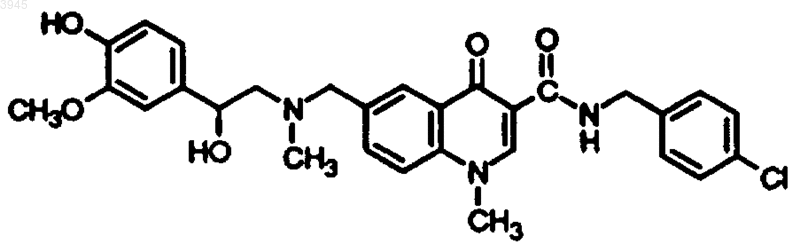
или
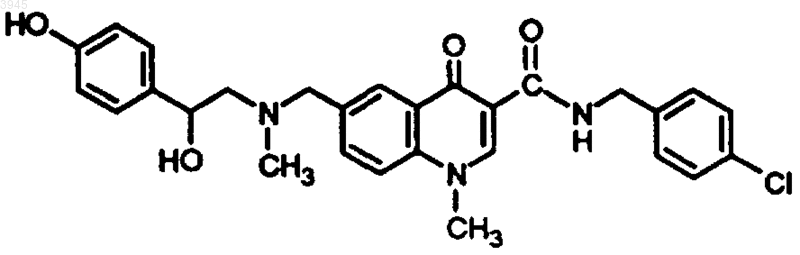
или его фармацевтически приемлемая соль.
58. Соединение по п.1, представляющее собой
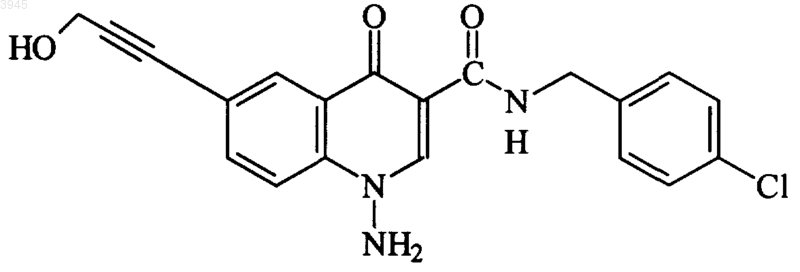
или его фармацевтически приемлемая соль.
59. Соединение по п.1, представляющее собой

или его фармацевтически приемлемая соль.
60. Соединение по п.1, где R2 представляет метил, этил, пропил, изопропил, бутил, трет-бутил, циклопропил, карбоксиметил, (C1-7алкокси)карбонилметил, 2-гидроксиэтил, 2-(2-метоксиэтокси)этил, 3-(2-тетрагидропиранилокси)пропил, 2-морфолиноэтил, 2-(диэтиламино)этил, 2-(диметиламино)этил, 2-пиперидиноэтил, 3-пиперидинопропил, 2-(1-метилпирролидин-2-ил)этил, 2-(диизопропиламино)этил, 2-пирролидин-1-илэтил, 3-(диметиламино)пропил или винил.
61. Соединение по п.1, где R4 представляет 3-гидрокси-1-пропинил, 3-гидроксипропил, гидроксиметил, цис-4-гидрокси-1-бутенил, транс-4-гидрокси-1-бутенил, (2-гидроксиэтил)-(этил)амино, морфолинометил, (CH2)2O(P=O)(OH)2, (CH2)3O(P=O)(трет-бутокси)2, 3-[ди(трет-бутил)фосфорил]пропил, 3-фосфорилпропил, Na+- OS(O)2CH2CH2N(CH3)C(=O)(CH2)6C(=O)O(CH2)3 или Na+-OS(O)2CH2CH2N(CH3)C(=O)-(CH2)6C(=O)OCH2Cу C-.
62. Соединение по п.1, представляющее
(1) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-изопропил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(2) 1-(втор-бутил)-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(3) 1-(втор-бутил)-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-8-метокси-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(4) N-(4-хлорбензил)-6-[3-гидрокси-1-пропенил]-1-[2-(4-морфолинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(5) N-(4-хлорбензил)-8-фтор-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(6) N-(4-хлорбензил)-8-фтор-6-[(Z)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(7) N-(4-хлорбензил)-1-[2-(диэтиламино)этил]-8-фтор-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(8) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-пропил-1,4-дигидро-3-хинолинкарбоксамид;
(9) N-(4-хлорбензил)-1-[2-(диэтиламино)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(10) гидрохлорид N-(4-хлорбензил)-1-[2-(диметиламино)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамида;
(11) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-[2-(1-пиперидинил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(12) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-[3-(1-пиперидинил)пропил]-1,4-дигидро-3-хинолинкарбоксамид;
(13) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(1-метил-2-пирролидинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(14) N-(4-хлорбензил)-1-[2-(диизопропиламино)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(15) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-[2-(1-пирролидинил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(16) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(4-морфолинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(17) N-(4-хлорбензил)-1-[3-(диметиламино)пропил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(18) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-винил-1,4-дигидро-3-хинолинкарбоксамид;
(19) N-(4-хлорбензил)-6-[(E)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(20) N-(4-хлорбензил)-6-[(Z)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(21) N-(4-хлорбензил)-1-циклопропил-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(22) трет-бутил-2-[3-{[(4-хлорбензил)амино]карбонил}-6-(3-гидрокси-1-пропинил)-4-оксо-1(4H)-хинолинил]ацетат;
(23) 2-[3-{[(4-хлорбензил)амино]карбонил}-6-(3-гидрокси-1-пропинил)-4-оксо-1(4H)-хинолинил]уксусная кислота;
(24) N-(4-хлорбензил)-1-(2-гидроксиэтил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(25) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(26) ди(трет-бутил) 3-(3-{[(4-хлорбензил)амино]карбонил}-1-метил-4-оксо-1,4-дигидро-6-хинолинил)пропилфосфат;
(27) 3-(3-{[(4-хлорбензил)амино]карбонил}-1-метил-4-оксо-1,4-дигидро-6-хинолинил)пропилдигидрофосфат;
(28) ди(трет-бутил) 3-(3-{[(4-хлорбензил)амино]карбонил}-1-циклопропил-4-оксо-1,4-дигидро-6-хинолинил)пропилфосфат;
(29) 2-[{8-[3-(3-{[(4-хлорбензил)амино]карбонил}-1-циклопропил-4-оксо-1,4-дигидро-6-хинолинил)пропокси]-8-оксооктаноил}(метил)амино]-1-этансульфонат натрия;
(30) 2-[(8-{[3-(3-{[(4-хлорбензил)амино]карбонил}-1-метил-4-оксо-1,4-дигидро-6-хинолинил)-2-пропинил]окси}-8-оксооктаноил)(метил)амино]-1-этансульфонат натрия;
(31) 2-[(8-{[3-(3-{[(4-хлорбензил)амино]карбонил}-1-метил-4-оксо-1,4-дигидро-6-хинолинил)-2-пропинил]окси}-8-оксооктаноил)(метил)амино]-1-этансульфонат натрия;
(32) 2-[(8-{[3-(3-{[(4-хлорбензил)амино]карбонил}-1-циклопропил-4-оксо-1,4-дигидро-6-хинолинил)-2-пропинил]окси}-8-оксооктаноил)(метил)амино]-1-этансульфонат натрия;
(33) 1-(трет-бутил)-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(34) 2-[{8-[3-(1-(трет-бутил)-3-{[(4-хлорбензил)амино]карбонил}-4-оксо-1,4-дигидро-6-хинолинил)пропокси]-8-оксооктаноил}(метил)амино]-1-этансульфонат натрия;
(35) 2-[(8-{[3-(1-(трет-бутил)-3-{[(4-хлорбензил)амино]карбонил}-4-оксо-1,4-дигидро-6-хинолинил)-2-пропинил]окси}-8-оксооктаноил)(метил)амино]-1-этансульфонат натрия;
(36) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(37) N-(4-цианобензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(38) N-(4-хлорбензил)-1-метил-6-(1,4-оксазепан-4-илметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(39) N-(4-хлорбензил)-1-метил-4-оксо-6-(1,4-тиазепан-4-илметил)-1,4-дигидро-3-хинолинкарбоксамид;
(40) N-(4-хлорбензил)-1-метил-6-(2-окса-5-азабицикло-[2.2.1]гепт-5-илметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(41) N-(4-хлорбензил)-6-(2,3-дигидро-4H-1,4-бензоксазин-4-илметил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(42) 6-(азидометил)-N-(4-хлорбензил)-1-метил-4-оксо-1,4-дигидро-3 -хинолинкарбоксамид;
(43) N-(4-хлорбензил)-1-метил-4-оксо-6-винил-1,4-дигидро-3-хинолинкарбоксамид;
(44) N-(4-хлорбензил)-1-[2-(2-гидроксиэтокси)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(45) N-(4-хлорбензил)-1-{2-[2-(2-метоксиэтокси)этокси]этил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид:
(46) N-(4-хлорбензил)-1-[2-(2-гидроксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(47) N-(4-хлорбензил)-1-[2-(2-этоксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(48) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(2-пропинил)-1,4-дигидро-3-хинолинкарбоксамид;
(49) N-(4-хлорбензил)-1-[2-(этилсульфанил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(50) N-(4-хлорбензил)-1-[3-(метилсульфанил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(51) N-(4-хлорбензил)-1-(4-гидрокси-2-бутинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(52) N-(4-хлорбензил)-6-{[(2-гидрокси-2-фенилэтил)(метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(53) N-(4-хлорбензил)-1-[3-(метилсульфинил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(54) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфанил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(55) N-(4-хлорбензил)-1-[3-(метилсульфонил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(56) N-(4-хлорбензил)-1-[2-(этилсульфинил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
N-(4-хлорбензил)-1-[2-(этилсульфонил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(58) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфинил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(59) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфонил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(60) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[2-(фенилсульфанил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(61) N-(4-хлорбензил)-1-[(метилсульфанил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(62) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(63) N-(4-хлорбензил)-6-[(3-гидрокси-1-азетидинил)метил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(64) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфанил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(65) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидрокси-3-метоксифенил)этил](метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(66) N-(4-хлорбензил)-6-[(3,3-дигидрокси-1-азетидинил)метил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(67) N-(4-хлорбензил)-1-[(метилсульфинил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(68) N-(4-хлорбензил)-1-[(метилсульфонил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(69) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфинил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(70) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфонил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(71) N-(4-хлорбензил)-6-(3-гидроксипропил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(72) N-(4-хлорбензил)-1-[2-(2-метоксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(73) N-(4-хлорбензил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-6-[(4-оксо-1-пиперидинил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(74) N-(4-хлорбензил)-6-{[(цианометил)(метил)амино]метил}-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(75) N-(4-хлорбензил)-6-{[(3R)-3-гидроксипирролидинил]метил}-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(76) N-(4-хлорбензил)-1-[2-(2-метоксиэтокси)этил]-6-[(метилсульфанил)метил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(77) N-(4-хлорбензил)-6-{[[(1R,2S)-2-гидрокси-1-метил-2-фенилэтил](метил)амино]метил}-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(78) N-(4-хлорбензил)-6-{[(2-гидрокси-2-фенилэтил)(метил)амино]метил}-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(79) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(80) 1-2-[2-(трет-бутокси)этокси]этил-N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(81) 1-2-[2-(трет-бутокси)этокси]этил-N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(82) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксю-1,4-дигидро-3-хинолинкарботиоамид;
(83) N-(4-хлорбензил)-8-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(84) N-(4-хлорбензил)-8-(4-гидрокси-1-бутинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(85) N-(4-хлорбензил)-6-{[3-(гидроксиимино)-1-азетидинил]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(86) N-(4-хлорбензил)-1-{2-[2-(4-морфолинил)этокси]этил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(87) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфанил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(88) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфинил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(89) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфонил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(90) N-(4-хлорбензил)-1-[(4-хлорфенокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(91) N-(4-хлорбензил)-1-[(2-метоксиэтокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(92) 2-{[3-{[(4-хлорбензил)амино]карбонил}-6-(4-морфолинилметил)-4-оксо-1(4H)-хинолинил]метокси}этилбензоат;
(93) N-(4-хлорбензил)-1-[(2-гидроксиэтокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(94) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-тетрагидро-2H-пиран-4-ил-1,4-дигидро-3-хинолинкарбоксамид;
(95) N-(4-хлорбензил)-1-(1-метил-4-пиперидинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(96) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(4-пиперидинил)-1,4-дигидро-3-хинолинкарбоксамид;
(97) N-(4-хлорбензил)-1-(1,1-диоксогексагидротиопиран-4-ил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(98) N-(4-хлорбензил)-1-(4-морфолинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(99) N-(4-хлорбензил)-1-(4-метил-1-пиперазинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(100) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(1-пиперидинил)-1,4-дигидро-3-хинолинкарбоксамид;
(101) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(1-пирролидинил)-1,4-дигидро-3-хинолинкарбоксамид;
(102) N-(4-хлорбензил)-1-[(2R)-2-(метоксиметил)пирролидинил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(103) N-(4-хлорбензил)-1-(диметиламино)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(104) 1-амино-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(105) 1-амино-N-(4-хлорбензил)-6-(3-гидроксипропил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(106) N-(4-хлорбензил)-1-(диметиламино)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(107) N-(4-хлорбензил)-1-(диметиламино)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(108) 1-(аллилокси)-N-(4-хлорбензил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(109) N-(4-хлорбензил)-1-метокси-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(110) N-(4-бромбензил)-1-(4-морфолинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(111) N-(4-фторбензил)-1-(4-морфолинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(112) N-(4-хлорбензил)-1-{[2-(4-морфолинил)этокси]метил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(113) N-(4-хлорбензил)-1-{[2-(диметиламино)этокси]метил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(114) N-(4-хлорбензил)-1-{[2-(4-метил-1-пиперазинил)этокси]метил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(115) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-{[2-(1-пиперидинил)этокси]метил}-1,4-дигидро-3-хинолинкарбоксамид;
(116) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-{[2-(1-пирролидинил)этокси]метил}-1,4-дигидро-3-хинолинкарбоксамид;
или его фармацевтически приемлемая соль.
63. Соединение по п.1, представляющее
(1) 1-(втор-бутил)-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(2) 1-(втор-бутил)-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-8-метокси-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(3) N-(4-хлорбензил)-6-[3-гидрокси-1-пропенил]-1-[2-(4-морфолинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(4) N-(4-хлорбензил)-8-фтор-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(5) N-(4-хлорбензил)-8-фтор-6-[(Z)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(6) N-(4-хлорбензил)-1-[2-(диэтиламино)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(7) гидрохлорид N-(4-хлорбензил)-1-[2-(диметиламино)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамида;
(8) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-[2-(1-пиперидинил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(9) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-[3-(1-пиперидинил)пропил]-1,4-дигидро-3-хинолинкарбоксамид;
(10) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(1-метил-2-пирролидинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(11) N-(4-хлорбензил)-1-[2-(диизопропиламино)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(12) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-[2-(1-пирролидинил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(13) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(4-морфолинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(14) N-(4-хлорбензил)-1-[3-(диметиламино)пропил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(15) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-винил-1,4-дигидро-3-хинолинкарбоксамид;
(16) N-(4-хлорбензил)-6-[(E)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(17) N-(4-хлорбензил)-6-[(Z)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(18) N-(4-хлорбензил)-1-циклопропил-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(19) трет-бутил 2-[3-{[(4-хлорбензил)амино]карбонил}-6-(3-гидрокси-1-пропинил)-4-оксо-1(4H)-хинолинил]ацетат;
(20) N-(4-хлорбензил)-1-(2-гидроксиэтил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(21) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(22) 3-(3-{[(4-хлорбензил)амино]карбонил}-1-метил-4-оксо-1,4-дигидро-6-хинолинил)пропилдигидрофосфат;
(23) ди(трет-бутил) 3-(3-{[(4-хлорбензил)амино]карбонил}-1-циклопропил-4-оксо-1,4-дигидро-6-хинолинил)пропилфосфат;
(24) 2-[{8-[3-(3-{[(4-хлорбензил)амино]карбонил}-1-циклопропил-4-оксо-1,4-дигидро-6-хинолинил)пропокси]-8-оксооктаноил}(метил)амино]-1-этансульфонат натрия;
(25) 2-[(8-{[3-(3-{[(4-хлорбензил)амино]карбонил}-1-метил-4-оксо-1,4-дигидро-6-хинолинил)-2-пропинил]окси}-8-оксооктаноил)(метил)амино]-1-этансульфонат натрия;
(26) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(27) N-(4-цианобензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(28) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-пропил-1,4-дигидро-3-хинолинкарбоксамид;
(29) N-(4-хлорбензил)-1-метил-6-(1,4-оксазепан-4-илметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(30) N-(4-хлорбензил)-1-метил-4-оксо-6-(1,4-тиазепан-4-илметил)-1,4-дигидро-3-хинолинкарбоксамид;
(31) 6-(азидометил)-N-(4-хлорбензил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(32) N-(4-хлорбензил)-6-[(4,4-дифтор-1-пиперидинил)метил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(33) N-(4-хлорбензил)-4-гидрокси-6-иод-3-хинолинкарботиоамид;
(34) N-(4-хлорбензил)-6-(2,3-дигидро-4H-1,4-бензоксазин-4-илметил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(35) N-(4-хлорбензил)-1-метил-4-оксо-6-винил-1,4-дигидро-3-хинолинкарбоксамид;
(36) N-(4-хлорбензил)-1-[2-(2-гидроксиэтокси)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(37) N-(4-хлорбензил)-1-{2-[2-(2-метоксиэтокси)этокси]-этил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(38) N-(4-хлорбензил)-1-[2-(2-гидроксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(39) N-(4-хлорбензил)-1-[2-(2-этоксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(40) N-(4-хлорбензил)-1-[2-(этилсульфанил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(41) N-(4-хлорбензил)-1-[3-(метилсульфанил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(42) N-(4-хлорбензил)-1-(4-гидрокси-2-бутинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(43) N-(4-хлорбензил)-6-{[(2-гидрокси-2-фенилэтил)(метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(44) N-(4-хлорбензил)-1-[3-(метилсульфинил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(45) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфанил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(46) N-(4-хлорбензил)-1-[3-(метилсульфонил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(47) N-(4-хлорбензил)-1-[2-(этилсульфинил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(48) N-(4-хлорбензил)-1-[2-(этилсульфонил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(49) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфинил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(50) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфонил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(51) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[2-(фенилсульфанил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(52) N-(4-хлорбензил)-1-[(метилсульфанил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(53) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(54) N-(4-хлорбензил)-6-[(3-гидрокси-1-азетидинил)метил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(55) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфанил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(56) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидрокси-3-метоксифенил)этил](метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
N-(4-хлорбензил)-6-[(3,3-дигидрокси-1-азетидинил)метил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(58) N-(4-хлорбензил)-1-[(метилсульфинил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(59) N-(4-хлорбензил)-1-[(метилсульфонил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(60) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфинил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(61) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфонил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(62) N-(4-хлорбензил)-6-(3-гидроксипропил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(63) N-(4-хлорбензил)-1-[2-(2-метоксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(64) N-(4-хлорбензил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-6-[(4-оксо-1-пиперидинил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(65) N-(4-хлорбензил)-6-{[(3R)-3-гидроксипирролидинил]метил}-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(66) N-(4-хлорбензил)-6-{[[(1R,2S)-2-гидрокси-1-метил-2-фенилэтил](метил)амино]метил}-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(67) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(68) 1-2-[2-(трет-бутокси)этокси]этил-N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(69) 1-2-[2-(трет-бутокси)этокси]этил-N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(70) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарботиоамид;
(71) N-(4-хлорбензил)-8-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(72) N-(4-хлорбензил)-8-(4-гидрокси-1-бутинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(73) N-(4-хлорбензил)-6-{[3-(гидроксиимино)-1-азетидинил]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(74) N-(4-хлорбензил)-1-{2-[2-(4-морфолинил)этокси]этил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(75) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфанил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(76) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфинил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(77) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфонил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(78) N-(4-хлорбензил)-1-[(4-хлорфенокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(79) N-(4-хлорбензил)-1-[(2-метоксиэтокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(80) 2-{[3-{[(4-хлорбензил)амино]карбонил}-6-(4-морфолинилметил)-4-оксо-1(4H)-хинолинил]метокси}этилбензоат;
(81) N-(4-хлорбензил)-1-[(2-гидроксиэтокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(82) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-тетрагидро-2H-пиран-4-ил-1,4-дигидро-3-хинолинкарбоксамид;
(83) N-(4-хлорбензил)-1-(1-метил-4-пиперидинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(84) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(4-пиперидинил)-1,4-дигидро-3-хинолинкарбоксамид;
(85) N-(4-хлорбензил)-1-(1,1-диоксогексагидротиопиран-4-ил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(86) N-(4-хлорбензил)-1-(4-морфолинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(87) N-(4-хлорбензил)-1-(4-метил-1-пиперазинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(88) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(1-пиперидинил)-1,4-дигидро-3-хинолинкарбоксамид;
(89) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(1-пирролидинил)-1,4-дигидро-3-хинолинкарбоксамид;
(90) N-(4-хлорбензил)-1-[(2R)-2-(метоксиметил)пирролидинил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(91) N-(4-хлорбензил)-1-(диметиламино)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(92) 1-амино-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(93) 1-амино-N-(4-хлорбензил)-6-(3-гидроксипропил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(94) N-(4-хлорбензил)-1-(диметиламино)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(95) 1-(аллилокси)-N-(4-хлорбензил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
или его фармацевтически приемлемая соль.
64. Соединение по п.1, представляющее собой
(1) 1-(втор-бутил)-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(2) 1-(втор-бутил)-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-8-метокси-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(3) N-(4-хлорбензил)-6-[3-гидрокси-1-пропенил]-1-[2-(4-морфолинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(4) N-(4-хлорбензил)-8-фтор-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(5) N-(4-хлорбензил)-8-фтор-6-[(Z)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(6) гидрохлорид N-(4-хлорбензил)-1-[2-(диметиламино)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамида;
(7) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-[2-(1-пиперидинил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(8) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-[3-(1-пиперидинил)пропил]-1,4-дигидро-3-хинолинкарбоксамид;
(9) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(1-метил-2-пирролидинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(10) N-(4-хлорбензил)-1-[2-(диизопропиламино)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(11) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-[2-(1-пирролидинил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(12) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(4-морфолинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(13) N-(4-хлорбензил)-1-[3-(диметиламино)пропил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(14) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-винил-1,4-дигидро-3-хинолинкарбоксамид;
(15) N-(4-хлорбензил)-6-[(E)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(16) N-(4-хлорбензил)-6-[(Z)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(17) N-(4-хлорбензил)-1-циклопропил-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(18) трет-бутил 2-[3-{[(4-хлорбензил)амино]карбонил}-6-(3-гидрокси-1-пропинил)-4-оксо-1(4H)-хинолинил]ацетат;
(19) N-(4-хлорбензил)-1-(2-гидроксиэтил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(20) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(21) 3-(3-{[(4-хлорбензил)амино]карбонил}-1-метил-4-оксо-1,4-дигидро-6-хинолинил)пропилдигидрофосфат;
(22) ди(трет-бутил) 3-(3-{[(4-хлорбензил)амино]карбонил}-1-циклопропил-4-оксо-1,4-дигидро-6-хинолинил)пропилфосфат;
(23) 2-[{8-[3-(3-{[(4-хлорбензил)амино]карбонил}-1-циклопропил-4-оксо-1,4-дигидро-6-хинолинил)пропокси]-8-оксооктаноил}(метил)амино]-1-этансульфонат натрия;
(24) 2-[(8-{[3-(3-{[(4-хлорбензил)амино]карбонил}-1-метил-4-оксо-1,4-дигидро-6-хинолинил)-2-пропинил]окси}-8-оксооктаноил)(метил)амино]-1-этансульфонат натрия;
(25) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(26) N-(4-цианобензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(27) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-пропил-1,4-дигидро-3-хинолинкарбоксамид;
(28) 6-(азидометил)-N-(4-хлорбензил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(29) N-(4-хлорбензил)-6-(2,3-дигидро-4H-1,4-бензоксазин-4-илметил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(30) N-(4-хлорбензил)-1-метил-4-оксо-6-винил-1,4-дигидро-3-хинолинкарбоксамид;
(31) N-(4-хлорбензил)-1-[2-(2-гидроксиэтокси)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(32) N-(4-хлорбензил)-1-{2-[2-(2-метоксиэтокси)этокси]этил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(33) N-(4-хлорбензил)-1-[2-(2-гидроксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(34) N-(4-хлорбензил)-1-[2-(2-этоксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(35) N-(4-хлорбензил)-1-[2-(этилсульфанил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(36) N-(4-хлорбензил)-1-[3-(метилсульфанил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(37) N-(4-хлорбензил)-1-(4-гидрокси-2-бутинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(38) N-(4-хлорбензил)-1-[3-(метилсульфинил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(39) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфанил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(40) N-(4-хлорбензил)-1-[3-(метилсульфонил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(41) N-(4-хлорбензил)-1-[2-(этилсульфинил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(42) N-(4-хлорбензил)-1-[2-(этилсульфонил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(43) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфинил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(44) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфонил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(45) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[2-(фенилсульфанил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(46) N-(4-хлорбензил)-1-[(метилсульфанил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(47) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид:
(48) N-(4-хлорбензил)-6-[(3-гидрокси-1-азетидинил)метил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(49) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфанил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(50) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидрокси-3-метоксифенил)этил](метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(51) N-(4-хлорбензил)-6-[(3,3-дигидрокси-1-азетидинил)метил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(52) N-(4-хлорбензил)-1-[(метилсульфинил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(53) N-(4-хлорбензил)-1-[(метилсульфонил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(54) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфинил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(55) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфонил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(56) N-(4-хлорбензил)-6-(3-гидроксипропил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
N-(4-хлорбензил)-1-[2-(2-метоксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(58) N-(4-хлорбензил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-6-[(4-оксо-1-пиперидинил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(59) N-(4-хлорбензил)-6-{[(3R)-3-гидроксипирролидинил]метил}-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(60) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(61) 1-2-[2-(трет-бутокси)этокси]этил-N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(62) 1-2-[2-(трет-бутокси)этокси]этил-N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(63) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарботиоамид;
(64) N-(4-хлорбензил)-8-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(65) N-(4-хлорбензил)-8-(4-гидрокси-1-бутинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид ;
(66) N-(4-хлорбензил)-6-{[3-(гидроксиимино)-1-азетидинил]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(67) N-(4-хлорбензил)-1-{2-[2-(4-морфолинил)этокси]этил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(68) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфанил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(69) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфинил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(70) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфонил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(71) N-(4-хлорбензил)-1-[(2-метоксиэтокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(72) 2-{[3-{[(4-хлорбензил)амино]карбонил}-6-(4-морфолинилметил)-4-оксо-1(4H)-хинолинил]метокси}этилбензоат;
(73) N-(4-хлорбензил)-1-[(2-гидроксиэтокси)метил]-6-(4-морфолинилметил)-4-оксю-1,4-дигидро-3-хинолинкарбоксамид;
(74) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-тетрагидро-2H-пиран-4-ил-1,4-дигидро-3-хинолинкарбоксамид;
(75) N-(4-хлорбензил)-1-(1-метил-4-пиперидинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(76) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(4-пиперидинил)-1,4-дигидро-3-хинолинкарбоксамид;
(77) N-(4-хлорбензил)-1-(1,1-диоксогексагидротиопиран-4-ил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(78) N-(4-хлорбензил)-1-(4-морфолинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(79) N-(4-хлорбензил)-1-(4-метил-1-пиперазинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(80) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(1-пиперидинил)-1,4-дигидро-3-хинолинкарбоксамид;
(81) N-(4-хлорбензил)-1-(диметиламино)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(82) 1-амино-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(83) 1-амино-N-(4-хлорбензил)-6-(3-гидроксипропил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
или его фармацевтически приемлемая соль.
65. Соединение по п.1, представляющее:
(1) N-(4-хлорбензил)-8-фтор-6-[(Z)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(2) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(4-морфолинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(3) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1-винил-1,4-дигидро-3-хинолинкарбоксамид;
(4) N-(4-хлорбензил)-6-[(Z)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(5) N-(4-хлорбензил)-1-циклопропил-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(6) N-(4-хлорбензил)-1-(2-гидроксиэтил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(7) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(8) 3-(3-{[(4-хлорбензил)амино]карбонил}-1-метил-4-оксо-1,4-дигидро-6-хинолинил)пропилдигидрофосфат;
(9) 2-[(8-{[3-(3-{[(4-хлорбензил)амино]карбонил}-1-метил-4-оксо-1,4-дигидро-6-хинолинил)-2-пропинил]окси}-8-оксооктаноил)(метил)амино]-1-этансульфонат натрия;
(10) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(11) N-(4-хлорбензил)-1-метил-4-оксо-6-винил-1,4-дигидро-3-хинолинкарбоксамид;
(12) N-(4-хлорбензил)-1-[2-(2-гидроксиэтокси)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(13) N-(4-хлорбензил)-1-[2-(2-гидроксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(14) N-(4-хлорбензил)-1-[2-(2-этоксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(15) N-(4-хлорбензил)-1-[2-(этилсульфанил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(16) N-(4-хлорбензил)-1-[3-(метилсульфанил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(17) N-(4-хлорбензил)-1-(4-гидрокси-2-бутинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(18) N-(4-хлорбензил)-1-[3-(метилсульфинил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(19) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфанил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(20) N-(4-хлорбензил)-1-[3-(метилсульфонил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(21) N-(4-хлорбензил)-1-[2-(этилсульфинил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(22) N-(4-хлорбензил)-1-[2-(этилсульфонил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(23) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфонил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(24) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[2-(фенилсульфанил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(25) N-(4-хлорбензил)-1-[(метилсульфанил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(26) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(27) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфанил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(28) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидрокси-3-метоксифенил)этил](метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(29) N-(4-хлорбензил)-6-[(3,3-дигидрокси-1-азетидинил)метил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(30) N-(4-хлорбензил)-1-[(метилсульфинил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(31) N-(4-хлорбензил)-1-[(метилсульфонил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(32) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфинил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(33) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфонил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(34) N-(4-хлорбензил)-6-(3-гидроксипропил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(35) N-(4-хлорбензил)-1-[2-(2-метоксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(36) 1-2-[2-(трет-бутокси)этокси]этил-N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(37) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарботиоамид;
(38) N-(4-хлорбензил)-8-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(39) N-(4-хлорбензил)-8-(4-гидрокси-1-бутинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(40) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфанил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(41) N-(4-хлорбензил)-1-([(4-хлорфенил)сульфинил]метил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(42) N-(4-хлорбензил)-1-[(2-метоксиэтокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(43) 2-{[3-{[(4-хлорбензил)амино]карбонил}-6-(4-морфолинилметил)-4-оксо-1(4H)-хинолинил]метокси}этилбензоат;
(44) N-(4-хлорбензил)-1-[(2-гидроксиэтокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(45) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-тетрагидро-2H-пиран-4-ил-1,4-дигидро-3-хинолинкарбоксамид;
(46) N-(4-хлорбензил)-1-(1-метил-4-пиперидинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(47) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(4-пиперидинил)-1,4-дигидро-3-хинолинкарбоксамид;
(48) N-(4-хлорбензил)-1-(1,1-диоксогексагидротиопиран-4-ил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(49) N-(4-хлорбензил)-1-(4-морфолинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(50) 1-амино-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(51) 1-амино-N-(4-хлорбензил)-6-(3-гидроксипропил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
или его фармацевтически приемлемая соль.
66. Соединение, по п.1, представляющее
(5) N-(4-хлорбензил)-1-метил-4-оксо-6-(тетрагидро-2H-пиран-4-илметил)-1,4-дигидро-3-хинолинкарбоксамид;
(5) N-(4-хлорбензил)-1-метил-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарботиоамид;
(5) N-(4-хлорбензил)-8-(2-гидроксиэтокси)-6-(3-гидроксипропил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(5) N-(4-хлорбензил)-1-циклопропил-6-(3-гидроксипропил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(5) 1-{2-[бис(2-гидроксиэтил)амино]этил}-N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
или его фармацевтически приемлемая соль.
67. Соединение по п.1, представляющее
(1) N-(4-хлорбензил)-8-[2-гидрокси-1-(гидроксиметил)этокси]-6-(3-гидроксипропил)-1-метил-4-оксю-1,4-дигидро-3-хинолинкарбоксамид;
(2) N-(4-хлорбензил)-8-фтор-6-(гидроксиметил)-4-оксо-1-[3-(тетрагидро-2H-пиран-2-илокси)пропил]-1,4-дигидро-3-хинолинкарбоксамид;
(3) N-(4-хлорбензил)-6-[этил(2-гидроксиэтил)амино]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(4) N-(4-хлорбензил)-1-циклопропил-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(5) 6-{[бис(2-гидроксиэтил)амино]метил}-N-(4-хлорбензил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(6) N-(4-хлорбензил)-6-{[(2-гидроксиэтил)(метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(7) 6-((бензил(2-гидроксиэтил)амино)метил)-N-(4-хлорбензил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(8) N-(4-хлорбензил)-6-[(4,4-дифтор-1-пиперидинил)метил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(9) N-(4-хлорбензил)-6-{[4-фтор-3,6-дигидро-1(2H)-пиридинил]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
или его фармацевтически приемлемая соль.
68. Соединение по п.1, представляющее
(1) N-(4-хлорбензил)-1-[2-(2-гидроксиэтокси)этил]-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(2) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидроксифенил)этил](метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(3) N-(4-хлорбензил)-6-{[[2-гидрокси-2-(4-гидрокси-3-метоксифенил)этил](метил)амино]метил}-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(4) N-(4-хлорбензил)-6-[(3,3-дигидрокси-1-азетидинил)метил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(5) N-(4-хлорбензил)-8-фтор-6-[(Z)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(6) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(4-морфолинил)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(7) N-(4-хлорбензил)-6-[(Z)-3-гидрокси-1-пропенил]-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(8) N-(4-хлорбензил)-1-циклопропил-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(9) N-(4-хлорбензил)-1-(2-гидроксиэтил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(10) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(11) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-[2-(2-метоксиэтокси)этил]-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(12) N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарботиоамид;
(13) N-(4-хлорбензил)-8-(3-гидрокси-1-пропинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(14) N-(4-хлорбензил)-8-(4-гидрокси-1-бутинил)-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(15) N-(4-хлорбензил)-1-метил-4-оксо-6-(тетрагидро-2H-пиран-4-илметил)-1,4-дигидро-3-хинолинкарбоксамид;
или его фармацевтически приемлемая соль.
69. Соединение по п.1, представляющее
(1) N-(4-хлорбензил)-1-(4-морфолинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(2) 1-амино-N-(4-хлорбензил)-6-(3-гидрокси-1-пропинил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(3) 1-амино-N-(4-хлорбензил)-6-(3-гидроксипропил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(4) N-(4-бромбензил)-1-(4-морфолинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(5) N-(4-фторбензил)-1-(4-морфолинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
или его фармацевтически приемлемая соль.
70. Соединение по п.1, представляющее
(1) N-(4-хлорбензил)-1-{[(4-хлорфенил)сульфанил]метил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(2) N-(4-хлорбензил)-1-{[(4-хлорфенил)сульфинил]метил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(3) N-(4-хлорбензил)-1-[(2-метоксиэтокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(4) 2-{[3-{[(4-хлорбензил)амино]карбонил}-6-(4-морфолинилметил)-4-оксо-1(4H)-хинолинил]метокси}этилбензоат;
(5) N-(4-хлорбензил)-1-[(2-гидроксиэтокси)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(6) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-тетрагидро-2H-пиран-4-ил-1,4-дигидро-3-хинолинкарбоксамид;
(7) N-(4-хлорбензил)-1-(1-метил-4-пиперидинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(8) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-(4-пиперидинил)-1,4-дигидро-3-хинолинкарбоксамид;
(9) N-(4-хлорбензил)-1-(1,1-диоксогексагидро-1l ~6~тиопиран-4-ил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(10) N-(4-хлорбензил)-1-(4-морфолинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(11) N-(4-хлорбензил)-1-[2-(2-гидроксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(12) N-(4-хлорбензил)-1-[2-(2-этоксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид:
(13) N-(4-хлорбензил)-1-[2-(этилсульфанил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(14) N-(4-хлорбензил)-1-[3-(метилсульфанил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(15) N-(4-хлорбензил)-1-(4-гидрокси-2-бутинил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(16) 1-{2-[бис(2-гидроксиэтил)амино]этил}-N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(17) N-(4-хлорбензил)-1-[3-(метилсульфинил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(18) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфанил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(19) N-(4-хлорбензил)-1-[3-(метилсульфонил)пропил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(20) N-(4-хлорбензил)-1-[2-(этилсульфинил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(21) N-(4-хлорбензил)-1-[2-(этилсульфонил)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(22) N-(4-хлорбензил)-1-{3-[(3-гидроксипропил)сульфонил]пропил}-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(23) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[2-(фенилсульфанил)этил]-1,4-дигидро-3-хинолинкарбоксамид;
(24) N-(4-хлорбензил)-1-[(метилсульфанил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(25) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфанил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(26) N-(4-хлорбензил)-1-[(метилсульфинил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(27) N-(4-хлорбензил)-1-[(метилсульфонил)метил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(28) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфинил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(29) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[(фенилсульфонил)метил]-1,4-дигидро-3-хинолинкарбоксамид;
(30) N-(4-хлорбензил)-1-[2-(2-метоксиэтокси)этил]-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(31) 1-{2-[2-(трет-бутокси)этокси]этил}-N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
(32) N-(4-хлорбензил)-1-циклопропил-6-(4-морфолинилметил)-4-оксо-1,4-дигидро-3-хинолинкарбоксамид;
или его фармацевтически приемлемая соль.
71. Фармацевтическая композиция, включающая соединение по п.1 и фармацевтически приемлемый носитель.
72. Способ ингибирования вирусной ДНК полимеразы, включающий контактирование полимеразы с эффективным ингибирующим количеством соединения по п.1.
73. Способ по п.72, где полимераза и соединение контактируют in vitro.
74. Способ по п.72, где полимераза и соединение контактируют in vivo.
75. Способ лечения инфекций вирусов герпеса, включающий введение нуждающемуся в этом пациенту эффективного количества соединения формулы I по п.1.
76. Способ по п.75, где указанные вирусы герпеса представляют вирус простого герпеса типа 1, вирус простого герпеса типа 2, виЁуё varicella zoster, цитомегаловирус, вирус Эпштейна-Барра, вирусы герпеса человека 6, вирусы герпеса человека 7 или вирусы герпеса человека.
77. Способ по п.75, где указанные вирусы герпеса представляют вирус простого герпеса типа 1, вирус простого герпеса типа 2, вирус varicella zoster, цитомегаловирус, вирус Эпштейна-Барра, вирусы герпеса человека 7 или вирусы герпеса человека.
78. Способ по п.75, где указанные вирусы герпеса представляют цитомегаловирус человека.
79. Способ по п.75, где эффективное количество соединения по п.1 вводят перорально, парентерально или местно.
80. Способ по п.75, где эффективное количество соединения по п.1 составляет количество от примерно 0,1 до примерно 300 мг/кг веса тела.
81. Способ по п.75, где эффективное количество соединения по п.1 составляет количество от примерно 1 до примерно 30 мг/кг веса тела.
Текст
1 Область изобретения Настоящее изобретение относится к производным 4-оксо-1,4-дигидро-3-хинолинкарбоксамида. Данные соединения полезны в качестве противовирусных агентов, в частности в качестве агентов против вирусов семейства герпеса. Предпосылки изобретения Вирусы герпеса включают большое семейство двухцепочечных ДНК вирусов. Они также являются источником большинства обычных вирусных заболеваний человека. Известно, что восемь вирусов герпеса, а именно вирус простого герпеса типа 1 и 2 (HSV-1 и HSV-2), вирус ветряной оспы (VZV), цитомегаловирус человека HCMV), вирус Эпштейна-Барра (Epstein-Barr)(EBV) и вирусы герпеса человека 6, 7 и 8 (HHV6, HHV-7 и HHV-8), инфицируют людей.HSV-1 и HSV-2 вызывают герпесные поражения губ и гениталий соответственно. Они также изредка вызывают инфекции глаза и энцефалит. HCMV вызывает врожденные дефекты у младенцев и множество заболеваний у иммунокомпромиссных пациентов, таких как ринит,пневмония и желудочно-кишечные заболевания.VZV является причиной ветряной оспы и опоясывающего лишая. EBV вызывает инфекционный мононуклеоз. Также он вызывает лимфомы у иммунокомпромиссных пациентов и связан с лимфомой Буркита (Burkitt), карциномой носоглотки и болезнью Ходгкинса (Hodgkin). HHV-6 является причиной розеолы и может быть связан с рассеянным склерозом и синдромом хронической усталости. Заболевания, связанные сHHV-7, не ясны, но он может быть вовлечен в некоторые случаи возникновения розеолы.HHV-8 связан с саркомой Капоши (Karposi),полостными лимфомами и множественными миеломами. Соединения настоящего изобретения отличаются от других гидроксихинолиновых противовирусных агентов тем, что заместитель в 4 положении бензиламида настоящего изобретения (например, хлор, бром, циано или нитрозаместитель) обеспечивает значительно улучшенную противовирусную активность. Некоторые соединения формулы (I) также имеют уникальные заместители R4, которые обеспечивают улучшенную противовирусную активность. Описание информации, раскрытой в уровне техники В патенте США 5891878 и WO 97/04775 описаны соединения, о которых сообщается, что они могут использоваться при лечении болезненного состояния, способного модулироваться(управляться) ингибированием продуцирования фосфодиэстеразы IV или фактора некроза опухоли. Предполагается, что ряд соединений, описанных в данных заявках, перекрывается с описанными здесь соединениями формулы I. Однако в данных РСТ заявках не получены конкретные соединения, имеющие 4-замещенную бен 003945 2 замидную группу, имеющуюся в соединениях формулы I настоящего описания. В патенте США 3960868 описаны производные 6-, 7- или 8-циклоалкил-4-оксохинолин 3-карбоновой кислоты, которые, как сообщается, обладают анальгетическими, противовоспалительными, противомикробными и гистаминвысвобождающими свойствами. Структура данных соединений отличается от структуры соединений формулы I тем, что требуется циклоалкильный заместитель в 6, 7 или 8 положении хинолинового кольца. В патенте США 3959363 описаны соединения хинолонкарбоксамида, которые, как сообщается, обладают антивирусной активностью. Структура данных соединений отличается от структуры соединений формулы I, раскрываемых в данном описании тем, что в 3 положении не включен 4-замещенный бензамид, и в 6 положении требуется в качестве заместителя водород или фтор. В патенте США 5175151 описаны соединения хинолона, которые, как сообщается, обладают антигипертензивной и противовирусной активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I тем, что в 3 положении не включен 4-замещенный бензамид, и во 2 положении необходим связанный через кислород заместитель. В заявке на патент Великобритании 1191443 описаны производные хинолина, которые, как сообщается, обладают антивирусной активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I, так как они не включают 4-замещенного бензамида в 3 положении, и для них необходимо наличие конденсированного фуранового гетероциклического кольца в 5,6, 6,7 или 7,8 положении хинолона. В WO 97/14682 описаны производные хинолина, которые, как сообщается, могут использоваться для лечения специфических гормонзависимых заболеваний. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I тем,что в 3 положении не включен 4-замещенный бензамид, в 1 положении требуется галогенаралкил, и в 7 положении требуется ациламиноарильная группа. В патенте США 4786644 описаны 1-арил 3-хинолинкарбоксамиды, которые, как сообщается, могут использоваться для лечения боли и воспаления. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I в 3 положении тем, что здесь не включен 4-замещенный бензамид, и в 1-положении требуется необязательно замещенный фенильный заместитель. В патенте США 4835163 описаны Nалкоксиалкильные производные карбоксамидов хинолона, которые, как сообщается, обладают 3 противосудорожной и психотонической активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I тем, что в 3 положении здесь не включен 4-замещенный бензамид. В патенте США 5096901; заявке на патент Великобритании 2236751 и статье Т.J.Ward etal., Med.Chem.Res. (1993), 4, 267-272 описаны хинолон-3-(азабицикло)карбоксамиды, которые,как сообщается, обладают 5-НТ 3 активностью и могут использоваться для лечения нервнопсихических болезненных состояний. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I необходимостью наличия азабициклосодержащего заместителя в 3 положении. В патенте Японии JP 02124871 описаны соединения хинолона, которые, как сообщается,обладают 5-липоксигеназной активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I в 3-положении тем, что здесь не включен 4-замещенный бензамидный заместитель. В Европейском патенте ЕР 0332930 А 2 описаны соединения хинолона, которые, как сообщается, обладают антибактериальной противовирусной активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I в 3 положении не включен 4-замещенный бензамид, и в 6 положении необходимы в качестве заместителя водород, галоген или нитро. В Chem.Abstracts (1969), 71, 101735q описаны соединения хинолона, которые, как сообщается, обладают противовоспалительной активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I в 3 положении,тем, что здесь не включен 4-замещенный бензамидный заместитель. В патентах США 5051418 и 4908366 описаны соединения 8-цианохинолона, которые,как сообщается, обладают антибактериальной активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I тем, что в 3 положении не включен 4-замещенный бензамид и в 8 положении необходим цианозаместитель. В Европейском патенте ЕР 0370686 описан способ получения промежуточных соединений хинолонкарбоновой кислоты. Структура описанных соединений отличается от структуры раскрытых в данном описании соединений формулы I тем, что в 3 положении не включен 4 замещенный бензамид и в 6 положении необходим фтор в качестве заместителя. В патенте США 4621088 описаны производные хинолонаминокислоты, которые, как сообщается, обладают антиаллергической активностью, активностью в отношении центральной нервной системы и сердечно 003945 4 сосудистой активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I в 3 положении тем, что здесь не включен 4 замещенный бензамид. В патенте США 5328887 описана группа соединений, включая многочисленные соединения хинолона, которые, как сообщается, могут использоваться в качестве флуоресцентнодонорных элементов для применения в термическом переданном состоянии. Отдельное конкретное соединение 4-хинолона, полученное и испытанное в заявке, отличается от раскрытых в данном описании соединений формулы I тем,что в 3 положении не включен 4-замещенный бензамид, во 2 положении имеется фенильный заместитель, в 6-положении имеется водород, а 1 положение является незамещенным. В патенте США 4855291 описаны соединения хинолона, которые, как сообщается, обладают антигипертензивной активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I в 3 положении, где не включен 4-замещенный бензамид. В патенте США 3524858 описаны соединения хинолона, которые, как сообщается, обладают противомикробной активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I тем, что в 3 положении не включен 4-замещенный бензамид и в 6,7 положениях необходим метилендиоксизаместитель. В WO 98/23608 описаны соединения хинолона, которые, как сообщается, обладают интегрин-антагонистической активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I тем, что в 3 положении не включен 4 замещенный бензамид. В патенте США 5026856 описаны соединения изоиндолина, которые, как сообщается,обладают антибактериальной активностью. Структура данных соединений отличается от структуры раскрытых в данном описании соединений формулы I тем, что в 3 положении не включен 4-замещенный бензамид и в 6 положении требуется в качестве заместителя галоген,гидрокси или низший алкокси. В патенте США 5563141 описана группа соединений, которые, как сообщается ингибируют адгезию клеток. Хотя раскрываемое семейство соединений может включать 3 аминокарбонил-4-хинолоны, данные соединения не содержат 4-замещенный бензамид в 3 положении. Все конечные соединения, специально полученные в данном патенте, включают 4-пиридил(пиперазин-1-ил)ьную кольцевую систему. В WO 9932450 описаны соединения следующей общей формулы, которые могут ис 5 пользоваться для лечения герпесных вирусных инфекций. В статье в Liebigs.Ann.Chem., 1987, 871879 описан синтез следующей структуры путем соединения хлорангидрида арилкарбоновой кислоты и амида -гидразидоалкенила. В европейском патенте ЕР 343560 описаны антибактериальные агенты, имеющие следующую структуру В патенте Японии JP 02040379 описаны соединения, полезные в качестве антибактериальных агентов, имеющие следующую общую структуру В патенте США 5412104 описаны следующие соединения общей структуры, как являющиеся полезными в качестве противовирусных агентов против ДНК-содержащих вирусов,таких как вирусы группы герпеса. Краткое изложение сущности изобретения Настоящее изобретение относится к соединению формулы I или его фармацевтически приемлемой соли,где Х представляетa) (СН 2 СН 2 О)mR10,b) het, где указанный het связан через атом углерода,c) C1-7 алкил, который может быть частично ненасыщенным и необязательно замещенным одним или несколькими заместителями, выбранными из группы, включающей NR7R8, R11,CN, SOiR9 или ОС 2-4 алкил, который дополнительно замещен het, OR10, ОС(=O)арилом илиd) С 3-8 циклоалкил, который может быть частично ненасыщенным и необязательно замещенным R11, NR7R8, SOiR9 или С 1-7 алкилом,необязательно замещенным R11, NR7R8, SOiR9;k) C1-8 алкил, который может быть частично ненасыщенным и необязательно замещен одним или несколькими заместителями, выбранными из группы, включающей N3, OR10,NR7R8, галоген, SOiR9, OR13 или R11;a) H,b) галоген,c) SC1-7 алкил,e) C1-7 алкокси, необязательно замещенный одним или несколькими галогенами или ОН илиf) C1-7 алкил, который может быть частично ненасыщенным и необязательно замещен гало 7 геном, NR10R10, (CH2)nOR13, R11, ОС 1-7 алкилом,который дополнительно замещен het, NR7R8 илиa) Н,b) арил,c) C1-7 алкил, который может быть частично ненасыщенным и необязательно замещен одним или несколькими заместителями, выбранными из группы, включающей NR10R10, CONR10R10,R11 , SOiR9, галоген; илиd) C1-7 алкил, который может быть частично ненасыщенным и необязательно замещенным одним или несколькими OR10, О-арилом, het,арилом, NR10R10, CN, SH, SOiС 1-6 алкилом, SOiарилом, галогеном или CONR10R10;c) C1-7 алкил, замещенный одним или несколькими заместителями, выбранными из группы, включающей R11, ОС 1-7 алкил, который дополнительно замещен het, NR7R8 или SOiR9; арил представляет фенильный радикал или ортоконденсированный бициклический карбоциклический радикал, где по крайней мере одно кольцо является ароматическим;het представляет четырех- (4), пяти- (5),шести- (6) или семи-(7)-членное насыщенное или ненасыщенное гетероциклическое кольцо,имеющее 1, 2 или 3 гетероатома, выбранных из группы, состоящей из кислорода, серы и азота,которое необязательно конденсировано с бензольным кольцом или любая бициклическая гетероциклическая группа; где любой арил необязательно замещен одним или несколькими заместителями, выбранными из группы, включающей галоген, ОН,CF3, C1-6 алкокси и C1-6 алкил, который дополнительно может быть замещен одним-тремя SR10,NR10R10, OR10 или CO2R10; где любой het необязательно замещен одним или несколькими заместителями, выбранными из группы включающей галоген, ОН, СF3,C1-6 алкокси, оксо, оксин и C1-6 алкил, который дополнительно может быть замещен однимтремя SR10, NR10R10, OR10 или CO2R10;C1-7 алкил; или NR16R17 вместе с азотом, к которому они присоединены, образуют 5- или 6 членное кольцо, такое как пирролидин, пиперидин, морфолин или пиперазин. В другом аспекте настоящее изобретение также относится к фармацевтической композиции, включающей соединение формулы I или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель,способу лечения или профилактики герпесной вирусной инфекции, включающему введение нуждающемуся в этом млекопитающему соединения формулы (I) или его фармацевтически приемлемой соли, и способу ингибирования вирусной ДНК полимеразы, включающему контактирование (invitro или in vivo) полимеразы с эффективным ингибирующим количеством соединения фор 9 мулы I или его фармацевтически приемлемой соли. Подробное описание изобретения Использованы следующие определения,если не указано другого. Галоген означает фтор,хлор, бром или иод. Алкил, алкокси и т.д. означают как линейные, так и разветвленные группы; но ссылка на индивидуальный радикал, такой как "пропил" охватывает только радикал с линейной цепью, изомер с разветвленной цепью, такой как "изопропил" будет упоминаться особо. Когда алкил может быть частично ненасыщенным, алкильная цепь может включать в цепи одну или несколько (например, 1, 2, 3 или 4) двойных или тройных связей. Арил означает фенильный радикал или ортоконденсированный бициклический карбоциклический радикал, где по крайней мере одно кольцо является ароматическим. Арил необязательно является замещенным одним или несколькими заместителями, выбранными из группы, включающей галоген, ОН, СF3, C16 алкокси и C1-6 алкил, который может быть дополнительно замещен одним-тремя SR10,NR10R10, OR10 или CO2R10;Het означает четырех- (4), пяти- (5), шести(6) или семи-(7)-членное насыщенное или ненасыщенное гетероциклическое кольцо, имеющее 1, 2 или 3 гетероатома, выбранных из группы,включающей кислород, серу и азот, которое необязательно сконденсировано с бензольным кольцом, или Het обозначает любую бициклическую гетероциклическую группу. Het необязательно является замещенным одним или несколькими заместителями, выбранными из группы, включающей галоген, ОН, СF3, C1-6 алкокси, оксо, оксин и C1-6 алкил, который может быть дополнительно замещен одним-тремя"Аминокислота" включает остаток природной аминокислоты (например, Ala, Arg, Asn,Asp, Cys, Glu, Gln, Gly, His, Hyl, Hyp, Ile, Leu,Lys, Met, Phe, Pro, Ser, Thr, Trp, Тyr и Val) в D или L форме, а также неприродных аминокислот (например, фосфосерина, фосфотреонина,фосфотирозина,гидроксипролина,гаммакарбоксиглютамата; гиппуровой кислоты, октагидроиндол-2-карбоновой кислоты, статина,1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты, пеницилламина, орнитина, цитрулина,метилаланина, парабензоилфенилаланина, фенилглицина, пропаргилглицина, саркозина и трет-бутилглицина). Аминокислота может быть подходящим образом связана с остатком соединения формулы I через карбоксильный конец,аминный конец или через любую другую обычную точку присоединения, такую как, например,серу цистеина. В частности, аминокислота может быть подходящим образом связана с остатком соединения формулы I через карбоксильный конец. 10 Млекопитающие означает человека и животных. Специалисту в данной области будет очевидно, что соединения изобретения, имеющие хиральный центр, могут существовать и могут быть выделены в оптически активной и рацемической формах. Некоторые соединения могут проявлять полиморфизм. Следует понимать, что настоящее изобретение охватывает любые рацемические, оптически активные, полиморфные, таутомерные или стереоизомерные формы или их смеси соединения изобретения,которое обладает описанными здесь полезными свойствами, в данной области хорошо известно каким образом получают оптически активные формы (например, разделение рацемической формы способами перекристаллизации, синтезом из оптически активных исходных веществ,хиральным синтезом или с помощью хроматографического разделения с использованием хиральной стационарной фазы), и каким образом определить противовирусную активность с использованием стандартных описанных здесь испытаний или с использованием других подобных испытаний, которые хорошо известны в данной области. Содержание атома углерода в различных углеводородсодержащих фрагментах указано с помощью приставки, обозначающей минимальное и максимальное число атомов углерода во фрагменте, т.е. приставка Ci-j указывает фрагмент, имеющий от целого числа "i" до целого числа "j" атомов углерода, включительно. Так,например, C1-7 алкил относится к алкилу, содержащему от 1 до 7 атомов углерода включительно. Соединения настоящего изобретения обычно названы в соответствии с системой номенклатуры ИЮПАК или CAS. Могут использоваться сокращения, которые хорошо известны обычному специалисту в данной области (например, "Ph" для фенила, "Me" для метила, "Et" для этила, "ч" для часа или часов и "кт" для комнатной температуры). Конкретные и предпочтительные значения,перечисленные ниже для радикалов, заместителей и диапазонов, предназначены только для иллюстрации; они не исключают другие определенные значения или другие значения в рамках определенного интервала для радикалов и заместителей. Конкретно, алкил может представлять метил, этил, пропил, изопропил, бутил, изобутил,втор-бутил, пентил, 3-пентил, гексил, гептил и т.д.; С 3-8 циклоалкил может представлять циклопропил, циклобутил, циклопентил, циклогексил,циклогептил или циклооктил; алкокси может представлять метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси,пентокси, 3-пентокси, гексилокси, 1-метилгексилокси или гептилокси; het может представлять азетидинил, 3,3-дигидрокси-1-азетидинил, пирролидино, пиперидино, морфолино, 11 тиоморфолино или гетероарил; и гетероарил может представлять фурил, имидазолил, триазолил, триазинил, оксазоил, изоксазоил, тиазолил, изотиазоил, пиразолил, пирролил, пиразинил, тетразолил, пиридил (или его N-оксид),тиенил, пиримидинил (или его N-оксид), индолил, изохинолил (или его N-оксид), или хинолил(CH2CH2O)mH или (СН 2 СН 2O)mС 1-4 алкил, где m равен 2 или 3. Конкретным значением R2 является С 3-8 циклоалкил, необязательно замещенный R11,NR7R8, SOiR9 или С 1-7 алкил, необязательно замещенный R11, NR7R8 или SOiR9; где R7, R8, R9,R11 и i такие, как определено выше. Конкретным значением R2 является циклопропил. Конкретным значением R2 является het, где указанный het связан через атом углерода и является таким же, как определено выше. Конкретным значением R2 является тетрагидро-2 Н-пиранил,пиперидинил,1-метилпиперидинил или 1,1-диоксотетрагидро-2 Нтиопиран. Конкретным значением R2 является С 2-7 алкил, который является частично ненасыщенным и необязательно замещенным NR7R8, R11,SOiR9 или OC2-4 алкилом, который дополнительно замещен het, OR10, ОС(=O)арилом; где R7, R8,R9, R10 такие, как определено выше. Конкретным значением R2 является (Z илиE)-CH=CHR10 или C-CCR10, где указанный R10 представляет Н или C1-7 алкил, необязательно замещенный ОН. Конкретным значением R2 является С 2-7 алкил, замещенный NR7R8, R11, SOiR9 или OC2-4 алкилом, который дополнительно замещен het,OR10, ОС(=O)арилом; где R7, R8, R9, R10 и R11 такие, как определено выше. Конкретным значением R2 является C1-7 алкил, замещенный ОС 2-4 алкилом, который дополнительно замещен het, ОН, OC1-4 алкилом или ОС(=O)арилом. Конкретным значением R2 является C1-7 алкил, замещенный SOiR9 , где R9 и i такие, как определено выше. Конкретным значением R2 является С 2-7 алкил, замещенный SOiR9 , где R9 представляет 12 присоединены, образуют het, при этом указанный het является таким, как определено выше. Конкретным значением W является морфолин, пиперидин, пирролидин, пиперазин или 4-метилпиперазин. Конкретным значением W является NR7R8,где R7 и R8 независимо представляют Н или С 1-4 алкил, необязательно замещенный ОН. Конкретным значением W является морфолин. Конкретным значением W является OR9 или SOiR9, где R9 представляет C1-6 алкил, который может быть частично ненасыщенным и необязательно замещенным OR10, Оарилом, het,арилом, NR10R10, CN, CONR10R10 или галогеном; где R10 представляет Н или С 1-4 алкил. Конкретным значением R3 является Н. Конкретным значением R3 является СF3 или галоген. Конкретным значением R4 является арил или het. Конкретным значением R4 являетсяSO2NHR12, CONHR12, NHCOR12 или NHSO2R12,где R12 является таким, как определено выше. Конкретным значением R4 является С 2-8 алкил, который является частично ненасыщенным и необязательно замещен OR10, NR7R8, галогеном, SOiR9, OR13 или R11, где R7, R8, R9, R10,R11 и R13 такие, как определено выше. Конкретным значением R4 является (Z или Е)-СН=СНС 1-4 алкил, необязательно замещенный ОН. Конкретным значением R4 является -С СС 1-4 алкил, необязательно замещенный ОН илиhet, где het является таким, как определено выше. Конкретным значением R4 является C1-8 алкил, замещенный NR7R8, где R7 и R8 независимо представляют C1-6 алкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, включающей ОН, арил или CN, где арил является таким, как определено выше. 13 Конкретным значением R4 является C1-8 алкил, замещенный N3. Конкретным значением R4 является C1-8 алкил, замещенный het, где het является таким,как определено выше. Конкретным значением R4 является 4 морфолинметил. Конкретным значением R4 является С 1-7 алкил, замещенный R11, где R11 является таким,как определено выше. Конкретным значением R5 является Н или С 1-7 алкил, необязательно замещенный ОН. Конкретным значением R6 является ОС 1-7 алкил, необязательно замещенный одним или несколькими ОН. Конкретным значением R6 является галоген. Конкретным значением R6 является ССС 1-7 алкил, замещенный одним или несколькими ОН, или С 2-7 алкокси, замещенный одним или несколькими ОН. Конкретным значением R6 является Н или С 1-7 алкил, необязательно замещенный галогеном, NR10R10, ОН, CO2R10 или het; где R10 и het такие, как определено выше. Конкретным значением М является натрий, калий или литий. Конкретным значением является, когда Х представляет S; W, R1, R2, R3, R4, R5, R6 такие,как определено выше. Конкретным значением является, когда Х представляет О; R1, R2, R3, R4, R5, R6 такие, как определено выше, W представляет NR7R8, OR9,SOiR9 или R2; где R2 представляетa) (CH2CH2O)nR10,b) het, где указанный het связан через атом углерода,c) С 1-7 алкил, который является частично ненасыщенным и необязательно замещен ОН,d) С 3-8 циклоалкил или е) С 1-7 алкил, который необязательно замещен одним или несколькими заместителями,выбранными из группы, включающей Ohet, Оарил, SOiR9 или ОС 2-4 алкил, который дополнительно замещен het, OR10 или ОС(=O)арилом; где R7, R8, R9, R10 и n являются такими, как определено выше. Конкретным значением является, когда Х представляет О или S; R1 представляет Сl, R3 представляет Н, R5 представляет Н, R6 представляет Н или F; R4 представляет 4 морфолинилметил; и R2 представляетSOiR9, или С 1-4 алкокси, который дополнительно замещен ОН,het,ОС 1-4 алкилом или ОС(=O)фенилом,b) (СН 2 СН 2 О)2 С 1-4 алкил,c) C1-6 алкил, который является частично ненасыщенным и необязательно замещен ОН,d) циклопропил, тетрагидро-2 Н-пиранил,пиперидинил, морфолинил, 1-метилпиперидинил или 1,1-диоксотетрагидро-2 Н-тиопиран; гдеR9 представляет фенил, необязательно замещенный Сl, или R9 представляет C1-6 алкил, необязательно замещенный ОН. Конкретным значением является, когда Х представляет О или S; R1 представляет Сl, R3 представляет Н, R5 представляет Н, R6 представляет Н или F; R4 представляет C1-6 алкил, который является частично ненасыщенным и необязательно замещенным ОН или OR13; или R4 представляет С 1-4 алкил, замещенный OR13; W циклопропил,представляет(CH2CH2O)2OR , или C1-6 алкил, который может быть частично ненасыщенным и необязательно замещенным ОН, морфолинилом, NR10R10; С(=O)ОС 1-4 алкил, где R10 представляет Н или С 1-4 алкил; R13 представляет (Р=O)(С 1-7 алкокси)2,или СО(СН 2)nСОN(СН 3)(СН 2)nSO3-M+(Р=O)(ОН)2. Конкретным значением является, когда Х представляет О или S; R1 представляет Сl, R3 представляет Н, R5 представляет Н, R6 представляет ССС 1-4 алкил, необязательно замещенный ОН; R4 представляет Н или С 1-4 алкил, который может быть частично ненасыщенным и необязательно замещенным ОН, а W представляет С 1-4 алкил, необязательно замещенный ОН. Когда алкил является частично ненасыщенным, он может представлять винил, аллил,1-пропенил, 2-пропенил, 1-бутенил, 2-бутенил,3-бутенил, 1,3-бутадиенил, 1-пентенил, 2 пентенил, 3-пентенил, 4-пентенил, 1-гексенил,2-гексенил, 3-гексенил, 4-гексенил, 5-гексенил,этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2 бутинил, 3-бутинил, 1-пентинил, 2-пентинил, 3 пентинил, 4-пентинил, 5-гексен-1-инил, 2 гексинил, 3-гексинил, 4-гексинил или 5 гексинил. Примерами соединений настоящего изобретения являются(130) N-(4-хлорбензил)-6-(4-морфолинилметил)-4-оксо-1-[2-(1-пирролидинил)этокси] метил-1,4-дигидро-3-хинолинкарбоксамид; или его фармацевтически приемлемая соль. На следующих схемах А-АА описано получение соединений настоящего изобретения. Все исходные вещества получают способами,описанными на данных схемах, или аналогичными им способами, которые хорошо известны обычному специалисту в области органической химии. Все целевые соединения настоящего изобретения получают способами, описанными на данных схемах, или аналогичными им способами, которые хорошо известны обычному специалисту в области органической химии. Все переменные, использованные на схемах, являются такими, как определено ниже или как определено в формуле изобретения. Схема А. Этиловый сложный эфир формулы А-1,который представляет собой этил-4-гидрокси-6 иод-3-хинолинкарбоксилат, получают нагреванием 4-иоданилина с диэтилэтоксиметиленмалонатом, первоначально при примерно 150 С,затем в кипящем с обратным холодильником дифениловом эфире. Аминолиз соединения А-1 4-замещенным бензиламином при примерно 160 С дает амид А-2. Катализируемая палладием и медью конденсация А-2 с пропаргиловым спиртом ведет к соединению А-3. Алкилирование азота пиридона осуществляют с использованием карбоната калия и необязательно замещенного галоидного алкила с получением соединения формулы А-4. Альтернативно соединение А-3 частично гидрируют до алкенильного производного, соединения А-5 (Е или Z). Аналогично, 4-хинолоновые структуры формулы А 4 частично гидрируют, получая алкенильные производные формулы А-6 (Е или Z). Алкилирование соединения А-5 необязательно замещенными галоидными алкилами и карбонатом калия также дает соединения формулы А-6. Схема В. Соединение формулы В-1, которое представляет собой 2-фтор-5-иодбензойную кислоту,получают карбонированием аниона 4-фториодбензола, который получают депротонированием 4-фториодбензола с помощью LDA. Взаимодействие кислоты В-1 с карбонилдиимидазолом с последующей обработкой полученного ацилимидазолида этилтриметилсилилмалонатом и дальнейшее декарбоксилирование приводят к кето-сложному эфиру В-2. Кето-сложный эфир превращают в хинолиноны В-3 последовательной обработкой триэтилортоформиатом, амином и трет-бутоксидом калия. Аминолиз сложного эфира осуществляют 4-хлорбензиламином,получая соединения формулы В-4. Конденсацию с пропаргиловым спиртом проводят с использованием катализа палладием и медью,приводя к соединениям формулы В-5. Гидрирование тройной связи с использованием газообразного водорода и платинового катализатора дает гидроксипропил-производные В-6. Схема С. Катализируемое палладием карбонилирование 6-иод-4-гидроксихинолин-3-карбоксамида А-2 дает соответствующий сложный эфир С-1,который затем восстанавливают LAH, получая спирт С-2. Алкилирование азота пиридона алкилбромидом, иодидом или тозилатом (X=I, Br,Тs, R2 такой, как определено ранее) в присутствии карбоната щелочного металла дает соединения общей структуры С-3. Обработка соединения С-3 метансульфонилхлоридом с последующим замещением амином, HNR7R8, где R7 иsitu м-хлорбензойной кислотой, получая дитрет-бутилфосфаты формулы D-2. Обработка фосфатов трифторуксусной кислотой расщепляет трет-бутильные группы, давая фосфорные кислоты формулы D-3. Схема Е. Спирты формулы D-1 конденсируют с триэтиламмониевой солью сулептановой кислоты,которая представляет собой 2-[(7-карбоксигептаноил)(метил)амино]-1-этансульфонат триэтиламмония, с использованием диизопропилкарбодиимида и 4-диметиламинопиридина, получая соответствующие сложные эфиры. Замена триэтиламмониевой соли на ион натрия дает натриевые соли Е-1. 24 Схема F. 4-Иоданилин (F-0) восстановительно алкилируют [(1-этоксициклопропил)окси]триметилсиланом и цианоборгидридом натрия, давая Nциклопропиланилин (F-1). Обработка диэтилэтоксиметиленмалонатом в пиридине дает енамин (F-2), который циклизуют с помощью полифосфорной кислоты в хинолин (F-3). Обработка п-хлорбензиламином при повышенной температуре превращает сложный эфир в амид(F-4). Катализируемое палладием связывание иодида с пропаргиловым спиртом дает F-5. Взаимодействие с платиной и газообразным водородом дает насыщенный пропиловый спирт (F-6). Схема G. 4-Нитробензилбромид обрабатывают морфолином и карбонатом калия в ацетоне, получая 4-(4-нитробензил)морфолин (G-1). Нитрогруппу восстанавливают с помощью платины и газообразного водорода, получая анилин (G-2), который затем обрабатывают [(1-этоксициклопропил)окси]триметилсиланом и цианоборгидридом натрия, давая N-циклопропиланилин (G-3). Взаимодействие с диэтилэтоксиметиленмалонатом в пиридине дает енамин (G-4), который циклизуют с помощью полифосфорной кислоты в хинолин (G-5). Обработка п-хлорбензиламином при повышенной температуре превращает сложный эфир в амид (G-6). Схема Н. Алкилирование N-(4-хлорбензил)-6-иод-4 оксо-1,4-дигидро-3-хинолинкарбоксамида карбонатом калия и трет-бутилбромацетатом дает Н-1. Катализируемое палладием связывание иодида с пропаргиловым спиртом дает Н-2. Взаимодействие с платиной и газообразным водородом дает насыщенный пропиловый спирт(H-3). Обработка трифторуксусной кислотой приводит к свободной кислоте (Н-4). Альтернативно, Н-2 обрабатывают трифторуксусной кислотой, давая Н-5. Схема I. 1-Фтор-4-нитробензол (1-1) превращают в 2-(4-нитроанилино-N-этил)-1-этанол (1-2) нагреванием с N-этилэтаноламином в этаноле. Соединение 1-2 превращают в соответствующий ацетат (1-3) обработкой ацетилхлоридом. Нитрогруппу восстанавливают в свободный амин с использованием палладия-на-угле и газообразного водорода. Полученный анилин обрабатывают диэтилэтоксиметиленмалонатом,получая соединение 1-4. Полученный енамин циклизуют нагреванием в дифениловом простом эфире, получая хинолин (1-5). Соединение 1-5N-алкилируют по атому азота пиридона обработкой йодистым алкилом и карбонатом калия,получая соединение 1-6. Аминолиз сложного диэфира 4-хлорбензиламином дает (1-7). Схема J. 2-Фтор-6-иоданилин конденсируют с диэтилэтоксиметиленмалонатом, а затем нагревают в дифениловом простом эфире, получая этиловый сложный эфир 4-гидроксихинолина (J-1). Аминолиз соединения J-1 4-хлорбензиламином дает соответствующий амид (J-2). Соединение J2 нагревают в присутствии алкоксида, получая соединение J-3. Катализируемая палладием конденсация полученного хинолина с пропаргиловым спиртом дает алкин J-4. Затем азот пиридона J-4 N-алкилируют галоидным алкилом и карбонатом калия, получая 4-хинолоны формулы J-5. Гидрирование соединения J-5 дает гидроксипропильное производное формулы J-6. Схема K. Катализируемое палладием карбонилирование 6-иод-8-фтор-4-гидроксихинолин-3-карбоксамида J-2 дает соответствующий сложный эфир K-1, который затем восстанавливают LAH,получая спирт K-2. Алкилирование азота пиридона галоидным алкилом и карбонатом калия дает соединения формулы K-3. Схема L. Катализируемая палладием конденсация 6 иод-8-фтор-4-гидроксихинолин-3-карбоксамидаJ-2 с пропаргиловым спиртом дает алкин L-1. Атом азота пиридона L-1 затем N-алкилируют галоидным алкилом и карбонатом калия, получая 4-хинолоны формулы L-2. Последующее полугидрирование соединения L-2 дает гидроксиалкенильные производные формулы L-3. Схема М. Обработка соединения С-2 метансульфонилхлоридом с последующей реакцией с морфолином дает соединение М-1. Алкилирование атома азота пиридона алкилбромидом, иодидом или тозилатом (X=I, Br, Ts, R представляет алкил) в присутствии карбоната щелочного металла или, альтернативно, соответствующим алкиловым спиртом в условиях Мицунобу (Mitsunobu) дает соединение формулы М-2. 28 Схема Q. Алкилхлорид N-1 обрабатывают натриевой солью алкилтиола, получая сульфиды общей формулы Q-1 (где R2 и R9 являются такими, как определено выше). Схема N. Обработка соединения С-2 метансульфонилхлоридом дает бензильный хлорид N-1. Обработка соединения N-1 соответствующим первичным или вторичным амином дает соединение формулы С-4, или атом хлора может быть замещен другими нуклеофилами (например,азидом). Схема О. Обработка соединения М-1 тиолсодержащими алкилгалогенидами в присутствии неорганического основания или, альтернативно, соответствующими тиолсодержащими алкиловыми спиртами в условиях Мицунобу (Mitsunobu) дает соединения формулы 0-1 (где R9 является таким, как определено выше). Окисление сульфидов формулы 0-1 м-хлорпербензойной кислотой в присутствии п-толуолсульфоновой кислоты дает соединения формулы 0-2. Схема Р. Соединение А-2 можно ввести во взаимодействие с алкилбромидом, иодидом или тозилатом (X=Br, I, Ts, R представляет алкил) в присутствии карбоната щелочного металла, получая соединения формулы Р-1. Полученные 6-иод-4 хинолоны конденсируют с триалкилалкенилоловом (например, трибутилвинилоловом) при катализе РdСl2(РРh3)2, получая такие соединения, как описываемые формулой Р-2. Схема R. Соединения с 3-тиоамидным заместителем получают из соединения А-2 (см. схему А) взаимодействием с PCl5, получая хлоримидат R1. Последующая обработка хлоримидата R-1H2S дает тиоамид R-2, который алкилируют в условиях Мицунобу (Mitsunobu), получая R-3. Соединение R-3 затем может быть преобразовано в требуемые аналоги с использованием химических аналогов описанных карбоксамидных производных, представленные на схемах А-Е, N,Р или Q.N-(4-Хлорбензил-4-гидрокси-6-иод-3-хинолинкарбоксамид (схема А-2, R=Cl) обрабатывают пентахлоридом фосфора, образуя хинолинкарбоксимидоилхлорид S-1. Его затем обрабатывают сернистым водородом, получая тиоамид S-2. Алкилирование в условиях Мицунобу дает S-3 (где R представляет алкил), который связывают с пропаргиловым спиртом с использованием палладиевого катализатора, получая S4. Схема Т. Катализируемое палладием карбометилирование N-(4-хлорбензил)-4-гидрокси-6-иод-3 хинолинкарботиоамид (S-2) приводит к 6 метиловому сложному эфиру хинолина Т-1. Восстановление в спирт с последующим мезилированием и замещением морфолином дает 6 морфолинметилхинолдин Т-3. Метилирование в условиях Мицунобу дает N-(4-хлорбензил)-1 метил-6-(4-морфолинилметил)-4-оксо-1,4 дигидро-3-хинолинкарботиоамид (Т-4). Схема U. 2-Иоданилин обрабатывают диэтилэтоксиэтиленмалонатом при 130 С. Полученный енамин затем растворяют в Ph2O и нагревают до 250 С, получая этилхинолинкарбоксилат U-1. Конденсация с неразбавленным 4-хлорбензиламином при 180 С дает 4-хлорбензиламид U-2,который метилируют иодметаном, получая N(4-хлорбензил)-8-иод-1-метил-4-оксо-1,4-дигидро-3-хинолинкарбоксамид (U-3). Катализируемое палладием связывание с ацетиленами или алкенами дает соединения общей формулы U-4. Схема V. 4-Нитробензилбромид обрабатывают трифенилфосфином, получая соль фосфония V-1. Депротонирование с образованием реагента Виттига и конденсация с тетрагидропиран-4 оном дает нитробензилиден V-2. Гидрирование до насыщенного амина и конденсация с диэтилэтоксиметиленмалонатом с последующей термической циклизацией полученного енамина дает хинолинкарбоновый сложный эфир V-3. Полученный сложный эфир конденсируют с 4 хлорбензиламином и метилируют, получая V-5. Схема W. Анилин формулы G-2 восстановительно алкилируют замещенным циклогексаноном (W1, Z=O, NMe, NBoc), получая N-алкилированный анилин (W-2, Z=O, NMe, NBoc). Взаимодействие с диэтилэтоксиметиленмалонатом дает енамин (W-3, Z=O, NMe, NBoc), который циклизуют с помощью полифосфорной кислоты в хинолин (W-4, Z=O, NMe, NH). При обработке 4-хлорбензиламином при повышенной температуре сложный эфир превращают в амид (W-5,Z=O, NMe, NH). Аналогично, анилин формулы 30 лированный анилин (W-2; Z=S). Взаимодействие с диэтилэтоксиметиленмалонатом дает енамин (W-3, Z=S). Окисление м-хлорпероксибензойной кислотой дает сульфон (W-2, Z=SO2),который взаимодействует с диэтилэтоксиметиленмалонатом, давая енамин (W-3, Z=SO2), который затем циклизуют с помощью полифосфорной кислоты в хинолин (W-4, Z=SO2). При обработке 4-хлорбензиламином при повышенной температуре сложный эфир превращают в амид (W-5, Z=SO2). Схема X. Восстановительное аминирование 3-бром 4-фторбензальдегида морфолином и триацетоксиборгидридом натрия дает арилбромид Х-1. Галоген-литиевый обмен с последующим ацетилированием N-метокси-N-метилацетамидом дает метилкетон Х-2. Полученный кетон затем превращают в сложный -кетоэфир Х-3 с помощью диэтилкарбоната в основных условиях. Нагревание при кипении с обратным холодильником сложного -кетоэфира Х-3 в триэтилортоформиате и уксусном ангидриде дает промежуточный простой эфир енола, который затем подвергают взаимодействию с выбранным гидразидом. Полученный енамин Х-4 затем циклизуют с использованием нагревания с гидридом натрия в ТГФ, получая соответствующий хинолон-3-сложный эфир Х-5. Непосредственный термолиз сложного эфира с 4-замещенным бензиламином (Х=Сl, Вr, F или CN, R7 и R8 являются такими же, как определено выше) при 190 С дает амиды общей формулы Х-6. 31 Схема Y. Бутилацетатный силилкетенацеталь взаимодействует с 2-хлор-5-иодбензоилхлоридом,давая сложный -кетоэфир Y-1. Нагревание при кипении с обратным холодильником в триэтилортоформиате и уксусном ангидриде дает промежуточный простой эфир енола, который затем подвергают взаимодействию с выбранным гидразидом. Полученный енамин Y-2 (где R7 иR8 являются такими же, как определено выше) затем циклизуют с использованием нагревания с гидридом натрия, получая соответствующий хинолон-3-сложный эфир Y-3. Непосредственный термолиз сложного эфира с 4 хлорбензиламином дает амиды общей формулыY-4. Катализируемое палладием связывание Y-4 с пропаргиловым спиртом дает соединения общей формулы Y-5. Последующее каталитическое гидрирование алкина дает гидроксипропильные производные общей формулы Y-6. Схема Z. Альтернативно, где N1-заместитель представляет амино, N-(4-хлорбензил)-4-гидрокси-6 иод-3-хинолинкарбоксамид (А-2) обрабатывают О-(мезитилсульфонил)гидроксиламином, получая 1-аминохинолон Z-1. Соединение Z-1 затем может быть преобразовано аналогичным образом, подобно описанному выше для общего промежуточного продукта Y-4.(АА-1) нагревают при кипении с обратным холодильником в триэтилортоформиате и уксусном ангидриде, получая промежуточный простой эфир енола, который затем приводят во взаимодействие с выбранными N-алкоксиамином. Полученный енамин АА-2 затем циклизуют с помощью нагревания с гидридом натрия, получая соответствующий хинолон-3 сложный эфир АА-3. Непосредственный термолиз сложного эфира с 4-хлорбензиламином дает амиды общей формулы АА-4. В тех случаях, где соединения являются достаточно основными или кислотными для образования стабильных нетоксичных солей кислоты или основания, подходящим может быть введение соединений в виде солей. Примерами фармацевтически приемлемых солей являются аддитивные соли органических кислот,образованные с кислотами, которые дают физиологически приемлемый анион, например,тозилат, метансульфонат, ацетат, цитрат, малонат, тартрат, сукцинат, бензоат, аскорбат, этоглютарат и глицерофосфат. Также могут быть образованы подходящие неорганические соли,включая такие соли, как гидрохлорид, сульфат,нитрат, бикрабонат и карбонат. Фармацевтически приемлемые соли могут быть получены с использованием стандартных способов, хорошо известных в данной области,например, взаимодействием достаточно основного соединения, такого как амин, с подходящей кислотой, дающей физиологически приемлемый анион. Также могут быть получены соли щелочного металла (например, натрия, калия или лития) или щелочно-земельного металла(например, кальция) карбоновых кислот. Соединения настоящего изобретения могут быть подходящим образом введены в фармацевтическую композицию, содержащую соединение в сочетании с подходящим эксципиентом, композиция может использоваться для борьбы с вирусными инфекциями. Содержащие соединение фармацевтические композиции,подходящие для противовирусного применения,получают способами и содержат эксципиенты,которые хорошо известны в данной области. Обычным известным кратким руководством по таким способам и ингредиентам является(Mark Publ. Co., 15th Ed., 1975). Соединения и композиции настоящего изобретения можно вводить парентерально (например, путем внутривенной, внутрибрюшинной или внутримышечной инъекции), местно, перорально или ректально, в зависимости от того, используют ли препарат для лечения внутренней или внешней вирусной инфекции. Для перорального терапевтического введения активное соединение можно объединять с одним или несколькими эксципиентами и использовать в форме таблеток для проглатывания, буккальных таблеток, пастилок, капсул,эликсиров, суспензий, сиропов, облаток и тому 33 подобного. Такие композиции и препаративные формы должны содержать по меньшей мере 0,1% активного соединения. Процентное соотношение в композициях и препаративных формах может, конечно, изменяться и подходящим образом составлять между от примерно 2 до примерно 60% по весу от данной единичной препаративной лекарственной формы. Количество активного соединения в таких терапевтически полезных композициях таково, что будет достигаться эффективный уровень дозировки. Таблетки, пастилки, пилюли, капсулы и тому подобное также могут содержать следующее: связующие вещества, такие как трагакантовая камедь, аравийская камедь, кукурузный крахмал или желатин; эксципиенты, такие как дикальцийфосфат; дезинтегрирующие агенты,такие как кукурузный крахмал, картофельный крахмал, альгиновая кислота и тому подобное; лубрикант, такой как стеарат магния; и подсластитель, такой как сахароза, фруктоза, лактоза или аспартам, или вкусовой агент, такой как мята перечная, масло грушанки или вишневый ароматизатор. Когда единичная препаративная лекарственная форма представляет капсулу, она может содержать в дополнение к вышеуказанным материалам, жидкий носитель, такой как растительное масло или полиэтиленгликоль. Различные другие материалы могут присутствовать в качестве покрытий или для модификации другим образом физической формы твердой единичной препаративной лекарственной формы. Например, таблетки, пилюли или капсулы могут быть покрыты желатином, воском, шеллаком или сахаром и тому подобным. Сироп или эликсир может содержать активное соединение,сахарозу или фруктозу в качестве подсластителя, метил и пропилпарабены в качестве консервантов, краситель и ароматизатор, такой как вишневый или апельсиновый ароматизатор. Конечно, любой материал, используемый при получении любой единичной препаративной лекарственной формы должен быть фармацевтически приемлемым и по существу нетоксичным в используемых количествах. Кроме того, активное соединение может быть введено в препаративные формы и устройства замедленного высвобождения. Соединения или композиции также можно вводить внутривенно или внутрибрюшинно путем инфузии или инъекции. Растворы активного соединения или его солей могут быть получены в воде, необязательно смешанной с нетоксичным поверхностно-активным веществом. Дисперсии также могут быть получены в глицерине,жидких полиэтиленгликолях, триацетоне и их смесях и в маслах. При обычных условиях хранения и применения данные препаративные формы содержат консервант для предотвращения роста микроорганизмов. Фармацевтические лекарственные формы,подходящие для инъекции или инфузии могут 34 включать стерильные водные растворы или дисперсии, или стерильные порошки, включающие активный ингредиент, который приспособлен для приготовления непосредственно перед употреблением стерильных растворов для инъекций или инфузий, или дисперсии, необязательно инкапсулированные в липосомах. Во всех случаях, окончательная лекарственная форма должна быть стерильной, жидкой и стабильной в условиях получения и хранения. Жидкий носитель или транспорт могут представлять собой растворитель или жидкую дисперсионную среду, включающую, например,воду, этанол, многоатомный спирт (например,глицерин, пропиленгликоль, жидкие полиэтиленгликоли и тому подобное), растительные масла, нетоксичные глицериновые сложные эфиры и их подходящие смеси. Необходимая текучесть может поддерживаться, например,путем образования липосом, поддержанием требуемого размера частиц в случае дисперсий,или за счет использования поверхностноактивных веществ. Профилактика действия микроорганизмов может достигаться с помощью различных антибактериальных и противогрибковых агентов, например, парабенов, хлорбутанола, фенола, сорбитовой кислоты, тримерозаля и тому подобного. Во многих случаях предпочтительно включать изотонические агенты, например, сахара, буферы или хлорид натрия. Пролонгированная абсорбция инъекционных композиций может достигаться посредством применения в композициях агентов, замедляющих абсорбцию, например, моностеарата алюминия и желатина. Стерильные инъекционные растворы могут быть получены введением активного соединения в требуемое количество подходящего растворителя с рядом перечисленных выше других ингредиентов, при необходимости, с последующей стерилизацией фильтрованием. В случае стерильных порошков для получения стерильных инъекционных растворов предпочтительные способы получения представляют собой способы вакуумной сушки и сушки вымораживанием, которые дают порошок активного ингредиента вместе с любым дополнительным желательным ингредиентом, присутствующим в предварительно стерилизованных фильтрованием растворах. Для местного введения настоящие соединения могут применяться в чистой форме, т.е. тогда, когда они представляют собой жидкости. Однако обычно желательно наносить их на кожу в виде композиций и рецептур в сочетании с дерматологически приемлемым носителем, который может быть твердым или жидким. Полезные твердые носители включают тонко измельченные твердые вещества, такие как тальк, глина, микрокристаллическая целлюлоза, диоксид кремния, оксид алюминия и тому подобные. Полезные жидкие носители включа 35 ют воду, спирты или гликоли или смеси водаспирт/гликоль, в которых настоящие соединения могут быть растворены или диспергированы на эффективном уровне, необязательно с добавлением нетоксичных поверхностно-активных веществ. Вспомогательные добавки, такие как ароматизаторы и дополнительные противомикробные агенты могут быть добавлены для оптимизации свойств данного применения. Полученные жидкие композиции могут наноситься из абсорбированных тампонов, применяться для импрегнирования бинтов и других повязок или распыляться на пораженную площадь с использованием распылителей насосного или аэрозольного типа. Загустители, такие как синтетические полимеры, жирные кислоты, соли жирных кислот и сложные эфиры, жирные спирты,модифицированные целлюлозы или модифицированные минеральные вещества, также можно использовать с жидкими носителями для получения намазываемых паст, гелей, мазей, мыл и тому подобного, для применения непосредственно на коже пользователя. Примеры полезных дерматологических композиций, которые могут использоваться для доставки соединений формулы I к коже, известны в данной области, например, см. Jacquet et al.Wortzman (патент США 4820508). Полезные дозировки соединений формулыI могут быть определены путем сравнения их активности in vitro и in vivo на животных моделях. Способы экстраполяции эффективных дозировок от мышей и других животных к человеку известны в данной области, например, см. патент США 4938949. Соединение обычно вводят в виде стандартной (единичной) лекарственной формы,например, содержащей от 5 до 1000 мг, подходящим является от 10 до 750 мг, наиболее подходящим является от 50 до 500 мг активного ингредиента на единичную лекарственную форму. Желательная доза может подходящим образом присутствовать в виде единичной дозы или разделенных доз, вводимых с подходящими интервалами, например, в виде двух, трех, четырех или более субдоз в день. Субдоза сама может быть дополнительно разделена, например, на ряд дискретных произвольно распределенных введений, таких как множественные ингаляции из распылителя или путем введения множества капель в глаз. Для внутренних инъекций композиции могут вводиться перорально или парентерально на уровне дозировки, рассчитанной на свободное основание, примерно от 0,1 до 300 мг/кг, предпочтительно от 1,0 до 30 мг/кг веса тела млекопитающего, и может использоваться для человека в виде единичной лекарственной формы,вводимой от одного до четырех раз в день в ко 003945 36 личестве от 1 до 1000 мг на единичную лекарственную форму. Для парентерального введения или для введения в виде капель, в виде глазных инъекций соединения присутствуют в водном растворе в концентрации от примерно 0,1 до примерно 10%, более предпочтительно от примерно 0,1 до примерно 7%. Раствор может содержать другие ингредиенты, такие как эмульгаторы, антиоксиданты или буферы. Обычно, концентрация соединения(й) формулы I в жидкой композиции, такой как лосьон, будет составлять примерно 0,1-25 вес.%,предпочтительно примерно 0,5-10 вес.%. Концентрация в полутвердой или твердой композиции, такой как гель или порошок, будет составлять примерно 0,1-5 вес.%, предпочтительно примерно 0,5-2,5 вес.%. Точный режим введения соединений и композиций, раскрытых в данном описании,будет обязательно зависеть от потребности индивидуального субъекта, подвергаемого лечению, типа лечения и, конечно, точки зрения практикующего врача. Антивирусная активность соединения данного изобретения может быть определена с использованием фармакологических моделей, которые хорошо известны в данной области или с использованием теста А, описанного ниже. Соединения формулы (I) и их фармацевтически приемлемые соли полезны в качестве противовирусных агентов. Таким образом, они могут использоваться для борьбы с вирусными инфекциями у животных, включая человека. Соединения обычно активны против вирусов герпеса и особенно полезны против вируса ветряной оспы, вируса Эпштейна-Барра, вируса простого герпеса, вируса человеческого герпеса типа 8 (HHV-8) и цитомегаловируса (CMV). Поскольку многие соединения настоящего изобретения продемонстрировали активность против CMV полимеразы, данные соединения могут быть активными против цитомегаловируса за счет данного или другого механизма действия. Таким образом, приведенное ниже описание активности данных соединений противCMV полимеразы не означает ограничения настоящего изобретения специфическим механизмом действия. Тест А. Анализ HCMV полимеразы осуществляют с использованием сцинтилляционного приближенного анализа (SPA), как описано в нескольких ссылках, таких как N.D.Cook et al., Pharmaceutical Manufacturing International, стр. 49-53H-dTTP. Анализы проводят в присутствии и в отсутствие CHAPS, (3-[(3-холамидопропил) диметиламмоний]-1-пропансульфонат) в конечной концентрации 2 мМ. HCMV полимеразу разбавляют в буфере для разбавления фермента,содержащем 50% глицерина, 250 мМ NaCl, 10 мМ HEPES (рН 7,5), 100 мкг/мл БСА и 0,01% азида натрия. HCMV полимеразу, которую экспрессируют в рекомбинантных инфицированных бакуловирусом SF-9 клетках и очищают в соответствии с описанными в литературе методиками, добавляют при 10% концентрации (или 10 мкл) к конечному реакционному объему, т.е. 100 мкл. Соединения разводят в 50% ДМСО и добавляют 10 мкл в каждую лунку. Контрольные лунки содержат эквивалентную концентрацию ДМСО. Если не указано другое, реакции инициируют добавлением 6 нМ биотинилированного поли(dА)-олиго(dT) матрица/праймера к реакционным смесям, содержащим фермент,субстрат и представляющее интерес соединение. Планшеты инкубируют на 25 или 37 С на водяной бане и заканчивают реакцию добавлением 40 мкл/реакцию 0,5 М EDTA (рН 8). Реакции завершают во временных пределах, за время которых введение субстрата является линейным и различается в зависимости от фермента и используемых условий, например, 30 мин дляHCMV полимеразы. 10 мкл стрептавидин-SPA шариков (20 мг/мл в PBS/10% глицерин) добавляют после завершения реакции. Планшеты инкубируют 10 мин при 37 С, затем уравновешивают до комнатной температуры и обсчитывают счетчиком Packard Topcount. Проводят линейные регрессии и рассчитывают IC50 с использованием компьютерного программного обеспечения. Модифицированный вариант вышеуказанного анализа HCMV полимеразы проводят, как описано выше, но со следующими изменениями: соединения разводят в 100% ДМСО до конечного разбавления в буфере для анализа. В предшествующем анализе соединения разводили в 50% ДМСО. К полимеразному буферу добавляют 4,5 мМ дитиотератола (DTT). Также используют другую партию CMV полимеразы,которая оказалась более активна, приводя к более быстрой полимеразной реакции. Результаты испытания представительных соединений формулы I в данном анализе приведены ниже в табл. 1. Таблица 1 Биологические данные Полимераза IC50 (мкМ) Пример 40 Описание предпочтительных вариантов осуществления изобретения Получение 1. N-(4-Хлорбензил)-8-фтор-4 гидрокси-6-иод-3-хинолинкарбоксамид. Смесь 11,85 г 2-фтор-4-иоданилина и 10,81 г диэтилэтоксиметиленмалоната нагревают при 130 С в колбе, оборудованной насадкой ДинаСтарка для сбора образующегося этанола. Затем смесь охлаждают до 75 С и разбавляют гексанами. Полученное твердое вещество собирают и сушат. Затем твердое вещество растворяют в 60 мл дифенилового простого эфира и нагревают при 250 С в течение 3 ч в колбе, оборудованной ловушкой Дина-Старка для сбора этанола. Раствор оставляют охлаждаться до комнатной температуры и полученное твердое вещество собирают и сушат, получая 11,73 г этил 8-фтор-4 гидрокси-6-иод-3-хинолинкарбоксилата. Данное вещество (0,55 г) и 3 мл 4-хлорбензиламина нагревают при 180 С в течение 1 ч. Реакционную смесь охлаждают и выливают в 75 мл диэтилового эфира. Полученное твердое вещество отфильтровывают и перекристаллизовывают из смеси этилацетат/гексаны, получая указанное в заголовке соединение в виде не совсем белого твердого вещества (0,45 г). Физические характеристики следующие: Т.пл. 268-270 С; 1N-(4-Хлорбензил)-8-фтор-4-гидрокси-6 иод-3-хинолинкарбоксамид (2,95 г) из получения 1 и гидрид натрия (60% дисперсия, 520 мг) суспендируют в ДМФ (60 мл) и к смеси добавляют метанол (288 мкл). После нагревания в течение 1 ч при 135 С добавляют дополнительно гидрид натрия (200 мг) и смесь нагревают еще в течение 1 ч. Реакционную смесь оставляют охлаждаться до комнатной температуры и затем выливают в насыщенный водный раствор хлорида аммония (200 мл). Полученный осадок отфильтровывают и промывают водой (20 мл),трет-бутилметиловым простым эфиром (20 мл) и гептаном (20 мл). Сырой продукт очищают(гептан/2 пропанол, 9/1; 4/1), получая 1,68 г (56%) указанного в заголовке соединения в виде белого твердого вещества. Перекристаллизация (уксусная кислота, вода) дает гидрат (1 Н 2 О). Физические характеристики следующие: Т.пл. 241-243 С; 1N-4-(Хлорбензил)-4-гидрокси-6-иод-8 метокси-3-хинолинкарбоксамид (469 мг) из получения 2, иодид меди(I) (57 мг) и бис(трифенилфосфин)палладий(II) хлорид (35 мг) суспендируют в диэтиламине (15 мл). Добавляют пропаргиловый спирт (70 мкл) и смесь оставляют перемешиваться при комнатной температуре в течение 16 ч. Реакционную смесь выливают в воду (50 мл) и экстрагируют этилацетатом (250 мл). Органический слой промывают насыщенным водным раствором хлорида аммония (310 мл) и насыщенным раствором соли (10 мл). Водный слой повторно экстрагируют этилацетатом (20 мл). Объединенные органические слои сушат (MgSO4) и концентрируют. Сырой продукт очищают колоночной хроматографией (дихлорметан/метанол, 50/1; 33/1; 25/1; 20/1), давая 289 мг (73%) указанного в заголовке соединения в виде белого твердого вещества. Физические характеристики следующие: Т.пл. 207-208 С; 1 4-Иоданилин (8,60 г) и диэтилэтоксиметиленмалонат (7,90 мл) нагревают при 130 С в течение 1 ч. Реакционную смесь охлаждают до комнатной температуры и добавляют 60 мл дифенилового простого эфира. Раствор нагревают при 250 С в течение 1,5 ч при удалении этанола с помощью ловушки Дина-Старка. Реакционную смесь охлаждают до комнатной температуры и полученное твердое вещество отфильтровывают, промывают гексанами и сушат, получая 11,20 г этил 4-гидрокси-6-иодхинолин-3-карбоксилата. Смесь данного сложного эфира (0,58 г) и 4-хлорбензиламина (4,0 мл) нагревают при 180 С в течение 1,5 ч. Реакционную смесь охлаждают и выливают в 50 мл диэтилового эфира. Полученное твердое вещество отфильтровывают, растирают в этилацетате и опять фильтруют, получая целевой продукт (0,50 г). Физические характеристики следующие: Т.пл. 297-299 С; 1(0,494 г) в Et2NH (12,9 мл) добавляют CuI (10,8 мг) и (Рh3P)2 РdСl2 (39,7 мг). Для растворения реагентов добавляют ДМФ (2 мл). К данному раствору добавляют пропаргиловый спирт(0,066 мл) и реакционную смесь перемешивают при комнатной температуре в течение 2 дней. Реакционную смесь концентрируют для удаления Et2NH. Полученный остаток распределяют между CH2Cl2 (3 х) и Н 2 О. Коричневое твердое вещество, выпавшее в осадок из CH2Cl2, отфильтровывают и собирают, получая чистый продукт по данным ЯМР. Органические слои объединяют, сушат над Na2SO4 и концентрируют, получая коричневый остаток. Остаток помещают в высокий вакуум для удаления остаточного ДМФ. Остаток адсорбируют диоксидом кремния и хроматографируют, элюируя 2% МеОН в CH2Cl2 и 3% МеОН в CH2Cl2. Фракции, 43 гомогенные по ТСХ, объединяют, конденсируют и перекристаллизовывают из EtOAc/ гексанов, получая кремовое твердое вещество. Две порции давали 325,4 мг (79%) требуемого продукта в виде золотисто-коричневого твердого вещества. Физические характеристики следующие: Т.пл. 248-250 С; 1N-[(4-хлорбензил]-8-фтор-4 гидрокси-6-иод-3-хинолинкарбоксамида из получения 1 (1,0 г), Et3N (0,61 мл), метанол (3,55 мл), Pd(OAc)2 (13,7 мг), и 1,3-бис(дифенилфосфино)пропан (25,2 мг) в ДМСО (12 мл) перемешивают при комнатной температуре до растворения. Газообразный СО(г) медленно барботируют через реакционную смесь в течение 3 ч и смесь нагревают при 70 С в течение ночи. Через реакционную смесь опять барботируют СО(г) в течение 4 ч. Смесь охлаждают до комнатной температуры и разбавляют водой,выпавшее в осадок белое твердое вещество собирают и фильтрат распределяют с CH2Cl2. Водный слой промывают CH2Cl2. Объединенные органические слои сушат (Na2SO4) и конденсируют, получая оранжевый остаток. Остаток помещают в высокий вакуум для удаления остаточного ДМСО. Предварительно собранное твердое вещество объединяют с остатком, растворяют в метаноле и поглощают диоксидом кремния. Сырой (неочищенный) продукт хроматографируют, элюируя смесью 2% метанола/СН 2 Сl2. Фракции, гомогенные по ТСХ, объединяют, конденсируют и перекристаллизовывают из смеси EtOAc/гексаны, получая 0,418 г указанного в заголовке соединения в виде белого твердого вещества. Физические характеристики следующие: Т.пл. 288-290 С; 1 Метил 3-[(4-хлорбензил)амино]карбонил-8-фтор-4-гидрокси-6-хинолинкарбоксилат из получения 6 (150 мг) растворяли в перегранном ТГФ (45 мл). Раствор нагревали до 35 С для переведения исходного вещества в раствор, затем охлаждали до 18 С для добавления LiAlH4LiAlH4 (27,0 мг), поскольку не наблюдалось большого прогресса в завершении преобразования продукта. Полное превращение в продукт достигали через 6,5 ч. Реакционную смесь гасили, добавляя 0,1 мл Н 2 О, 0,1 мл 15% NaOH и 0,1 мл к реакционной смеси. Реакционную смесь фильтровали, чтобы избавиться от выпавшей в осадок соли алюминия. Фильтрат конденсировали, получая зеленый остаток. Зеленый остаток адсорбировали диоксидом кремния и хроматографировали, элюируя 2% МеОН в CH2Cl2 и 3% МеОН в CH2Cl2. Фракции, гомогенные по ТСХ,конденсировали, получая 76,8 мг (55%) требуемого продукта в виде белого твердого вещества. Физические характеристики следующие: Т.пл.263-265 С; 1(30,0 г), Et3N (19,1 мл), МеОН (110,6 мл),Pd(OAc)2 (431 мг) и 1,3-бис(дифенилфосфино)пропан (791,9 мг) в 375 мл безводного ДМФ перемешивают при комнатной температуре до полного растворения всех компонентов. В течение 2 дней медленно барботируют через реакционную смесь СО(г) и реакционную смесь поддерживают при 70 С. Реакционную смесь охлаждают до комнатной температуры. Твердое вещество высаживают в осадок добавлением к реакционной смеси 160 мл 1 н. НСl. Осаждается оранжевое твердое вещество, которое собирают. Твердое вещество растирают с EtOAc, фильтруют и промывают СН 2 Сl2, получая 23,8 г (93%) 45 указанного в заголовке соединения в виде не совсем белого твердого вещества. Физические характеристики следующие: Т.пл. 290-292 С; 1 В высушенной на пламени 3-горлой круглодонной колбе емкостью 1 л метил 3-[(4 хлорбензил)амино]карбонил-4-гидрокси-6 хинолинкарбоксилат из получения 8 (3,0 г) растворяют в 700 мл перегранного ТГФ. Суспензию нагревают до 67 С для растворения исходного вещества. Реакционную смесь оставляют охлаждаться до комнатной температуры и затем охлаждают на ледяной бане до 10 С. В виде одной порции добавляют литийалюминий гидрид (552,2 мг). Реакционную смесь перемешивают при 25 С и контролируют превращение в целевой продукт с помощью масс-спектроскопии. Реакционную смесь гасят добавлением 2 мл H2O, 2 мл 15% NaOH и 2 мл H2O к реакционной смеси. Реакционную смесь фильтруют для удаления соли алюминия, выпавшей в осадок. Фильтрат конденсируют, получая желтозеленый остаток. Остаток адсорбируют на диоксид кремния и хроматографируют, элюируя 2% МеОН в CH2Cl2 (1 л), 3% МеОН в CH2Cl2 (2 л),4% МеОН в CH2Cl2 (2 л), 5% МеОН в CH2Cl2 (1 л), 6% МеОН в CH2Cl2 (1 л) и 7% МеОН вCH2Cl2 (2 л). Требуемый продукт элюируют 47% МеОН в CH2Cl2. Фракции, гомогенные по ТСХ, конденсируют, получая 1,85 г (67%) указанного в заголовке соединения в виде желтых кристаллов. Физические характеристики следующие: Т.пл. 288-289 С; 1(0,11 мл) в 4 мл безводного ДМФ нагревают при 90 С в течение 3 ч. Реакционную смесь охлаждают до комнатной температуры и разбавляютH2O для растворения любых солей и осаждения продукта. Сырой продукт адсорбируют на диоксиде кремния и хроматографируют, элюируя 3% МеОН в CH2Cl2. Фракции, гомогенные по ТСХ,объединяют и конденсируют, давая 154,2 мг(49%) указанного в заголовке соединения в виде белого твердого вещества. Физические характеристики следующие: Т.пл. 168-170 С; 1 Смесь N-(4-хлорбензил)-4-гидрокси-6-(3 гидрокси-1-пропинил)-3-хинолинкарбоксамида из получения 5 (5,48 г) и Pd/C (10%, 0,55 г) в смеси 3:1 CH2Cl2/MeOH (150 мл) помещают в аппарат Парра для гидрирования под давлением 50 фунтов/кв.дюйм (344,738 КПа) H2 и встряхивают в течение 4 ч. Добавляют еще 0,30 г Pd/C и полученную смесь встряхивают в течение 2 ч. Реакционную смесь затем фильтруют через целит, добавляют 0,55 г свежего катализатора и полученную смесь встряхивают в атмосфере H2 в течение 3 ч. Затем реакционную смесь фильтруют через целит и концентрируют в вакууме. Растирание с СНСl3/МеОН дает твердое вещество, которое очищают с помощью ВЭЖХ хроматографии на колонке 0,4625 см ChiralcelOD-H, элюируя EtOH при скорости 0,3 мл/мин,получая 0,383 г N-(4-хлорбензил)-1,4-дигидро 6-[(1Z)-3-гидрокси-1-пропенил]-4-оксо-3-хинолинкарбоксамид (указанное в заголовке циссоединение) и 0,492 г N-(4-хлорбензил)-1,4 дигидро-6-[(1 Е)-3-гидрокси-1-пропенил]-4-оксо 3-хинолинкарбоксамид (указанное в заголовке транс-соединение). Кристаллизация цисизомера из этилацетата давала 0,29 г указанного в заголовке цис-соединения в виде твердого вещества. Кристаллизация транс-изомера из Этил 8-фтор-4-гидрокси-6-иод-3-хинолинкарбоксилат (18,1 г), полученный в качестве промежуточного продукта в получении 1, растворяют в ДМФ (430 мл) и добавляют К 2 СО 3(36,1 г, 261 ммоль) и йодистый метил (3,25 мл,52,3 ммоль). Реакционную смесь нагревают при 95 С в течение 6 ч, затем оставляют перемешиваться при комнатной температуре в течение ночи. Смесь делят на две части. Первую часть выливают в Н 2 О и экстрагируют пятью 100-мл порциями CH2Cl2. Объединенные органические слои промывают пятью 200-мл порциями Н 2 О,сушат над MgSO4, фильтруют и концентрируют в вакууме. Затем повторяют обработку для второй порции реакционной смеси, получая всего 15,8 г указанного в заголовке соединения. Физические характеристики следующие: 1 48 Раствор этил 8-фтор-6-иод-1-метил-4-оксо 1,4-дигидро-3-хинолинкарбоксилата из получения 13 (15,8 г) в п-хлорбензиламине (15,4 мл) нагревают до 190 С. Смесь затем охлаждают до комнатной температуры и добавляют гексан. Полученный осадок собирают фильтрованием,получая указанное в заголовке соединение в виде твердого вещества. Аналитически чистый образец получают перекристаллизацией изN-(4-хлорбензил)-8-фтор-4 гидрокси-6-иод-3-хинолинкарбоксамида из получения 1 (0,466 г) в 15 мл диэтиламина добавляют Cul (0,010 г) и (Рh3P)2 РdСl2 (0,035 г), затем добавляют пропаргиловый спирт (0,058 мл) и реакционную смесь перемешивают в течение ночи при комнатной температуре. Диэтиламин удаляют в вакууме. Остаток распределяют между EtOAc и водой. Нерастворившееся вещество отфильтровывают и сохраняют. Органический слой промывают насыщенным раствором соли,сушат и конденсируют. Остаток объединяют с нерастворившимся веществом и адсорбируют диоксидом кремния и хроматографируют,элюируя 3% MeOH/CH2Cl2. Фракции, гомогенные по ТСХ, объединяют и конденсируют, получая 0,192 г требуемого продукта в виде золотисто-коричневого твердого вещества. Физические характеристики следующие: Т.пл. 277-279 С; 1 В сосуд высокого давления, содержащий 1-фтор-4-нитробензол (5,3 мл), добавляют 2(этиламино)-1-этанол (10,7 г). Реакционную смесь плотно закупоривают и нагревают до 135 С при перемешивании. Через 1 ч реакционную смесь охлаждают до комнатной температуры и концентрируют при пониженном давлении. Остаток сушат в вакууме. Остаток хроматографируют на диоксиде кремния, элюируя этилацетатом. Фракции, содержащие продукт, упаривают, получая 10,1 г 2-(этил-4-нитроанилино)-1 этанола в виде оранжевого твердого вещества. В колбу, содержащую 2-(этил-4-нитроанилино)-1-этанол (4,2 г) и 4-диметиламинопиридин (0,12 г) в пиридине (20 мл), при 0 С с использованием осушительной трубки добавляют по каплям уксусный ангидрид (5,0 мл). Реакционную смесь оставляют нагреваться до комнатной температуры в течение ночи. Реакционную смесь разбавляют этилацетатом и распределяют с насыщенным водным карбонатом натрия. Слои разделяют водную фазу, экстрагируют двумя дополнительными порциями этилацетата. Объединенные органические фазы промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток трижды подвергают азеотропной отгонке с толуолом для удаления остаточного пиридина. Остаток адсорбируют диоксидом кремния и хроматографируют на диоксиде кремния, элюируя 50% этилацетатом в гептане. Фракции, содержащие продукт, упаривают, получая 4,9 г 2-(этил-4-нитроанилино) этилацета в виде желтого масла. В аппарат Парра, содержащий 2-(этил-4 нитроанилино)этилацетат (2,5 г) и этилацетат(25 мл) добавляют 10% палладий-на-угле (0,11 г). Реакционную смесь встряхивают в течение 1 ч под давлением 50 фунтов/кв.дюйм (344,738 КПа) газообразного водорода. Реакционную смесь фильтруют через целит, промывая этилацетатом. Фильтрат концентрируют при пониженном давлении. Остаток обрабатывают диэтилэтоксиметиленмалонатом (2,4 мл) и нагревают при 140 С в токе газообразного аргона. Через 1 ч реакционную смесь охлаждают до комнатной температуры, адсорбируют силикагелем и хроматографируют на диоксиде кремния, элюируя 50% этилацетатом в гептане. Фракции, содержащие продукт упаривают, получая неочищенный диэтил 2-(4-2(ацетилокси)этил](этил)амино]анилинометилен)малонат в виде оранжевого масла. В колбу, содержащую неочищенный диэтил 2-(4-2-(ацетилокси)этил](этил)амино] анилинометилен)малонат (2,2 г) добавляют 50 дифениловый простой эфир (15 мл). Реакционную смесь нагревают от комнатной температуры до 260 С в течение 45 мин в токе газообразного аргона. После выдерживания в течение 1 ч при 260 С горячую реакционную смесь медленно и осторожно добавляют к перемешиваемому диэтиловому эфиру (150 мл). Полученный осадок отфильтровывают и промывают несколько раз гептаном. Остаток адсорбируют диоксидом кремния и хроматографируют на диоксиде кремния, элюируя смесью, содержащей от 3 до 10% метанола в дихлорметане. Фракции, содержащие продукт, упаривают, получая 0,68 г этил 6-2-(ацетилокси)этил](этил)амино]-4-гидрокси-3-хинолинкарбоксилата в виде коричневого твердого вещества. В колбу, содержащую этил 6-2-(ацетилокси)этил](этил)амино]-4-гидрокси-3-хинолинкарбоксилат (0,17 г) в ДМФ (5 мл) добавляют карбонат калия (0,21 г) и иодметан (0,05 мл). Реакционную смесь плотно закупоривают и нагревают до 90 С. Через 3 ч реакционную смесь охлаждают до комнатной температуры, разбавляют дихлорметаном, фильтруют и концентрируют при пониженном давлении. Остаток адсорбируют диоксидом кремния и хроматографируют на диоксиде кремния, элюируя смесью,содержащей от 4 до 8% метанола в дихлорметане. Фракции, содержащие продукт, упаривают,получая 0,22 г указанного в заголовке соединения в виде оранжевого твердого вещества. Физические характеристики следующие: 1H ЯМР (300 МГц, СDСl3) 8,7, 7,6, 7,3, 7,1,4,3, 4,2, 3,8, 3,6, 3,4, 2,0, 1,4, 1,2; Масс-спектр (ESI) m/z 399 (М+К+). Получение 17. N-Циклопропил-4-иоданилин. В колбу, содержащую 4-иоданилин (2,19 г) добавляют метанол (25 мл) и несколько дюжин сухих молекулярных сит (3). Смесь обрабатывают уксусной кислотой (6 мл), после чего [(1 этоксициклопропил)окси]триметилсиланом (2,5 мл). Через 1 ч реакционную смесь осторожно обрабатывают цианоборгидридом натрия (2,8 г) и нагревают при кипении с обратным холодильником в атмосфере азота в течение ночи. Реакционную смесь охлаждают до комнатной температуры, фильтруют и концентрируют при пониженном давлении. Остаток разбавляют этилацетатом и промывают водным гидроксидом натрия (2 н.). Водный слой повторно экстрагируют один раз этилацетатом и объединенные органические слои промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток адсорбируют диоксидом кремния и хроматографируют на диоксиде кремния, элюируя смесью, содержащей от 3 до 9% этилацетата в гептане. Фракции, содержащие продукт, объединяют и упаривают, получая 1,85 г указанного в заголовке соединения в виде золотистокоричневого масла.(0,5 мл). Колбу плотно закрывают и нагревают при 130 С в течение ночи. Реакционную смесь охлаждают до комнатной температуры и подвергают азеотропной отгонке с толуолом при пониженном давлении (3 х). Остаток растворяют в дихлорметане и промывают насыщенным раствором соли, сушат и концентрируют при пониженном давлении. Остаток адсорбируют силикагелем и хроматографируют на диоксиде кремния, элюируя смесью, содержащей от 25 до 75% этилацетата в гептане. Фракции, содержащие продукт, упаривают, получая 0,78 г указанного в заголовке соединения в виде золотистокоричневого твердого вещества. Физические характеристики следующие: 1H ЯМР (300 МГц, СDСl3)7,8, 7,7, 7,0,4,2, 4,1, 3,1, 1,3, 0,9, 0,7; Масс-спектр (ESI) m/z 430 (М+Н+). Получение 19. Этил 1-циклопропил-6-иод 4-оксо-1,4-дигидро-3-хинолинкарбоксилат. В колбу, содержащую диэтил 2[(циклопропил-4-иоданилино)метилен]малонат из получения 18 (0,22 г), добавляют полифосфорную кислоту (1,4 г). Реакционную смесь закрывают и нагревают до 120 С в течение 1 ч. Через 2 ч при 120 С реакционную смесь охлаждают до комнатной температуры, обрабатывают льдом и распределяют между дихлорметаном и насыщенным водным бикарбонатом. Щелочной водный слой экстрагируют двумя дополнительными порциями дихлорметана. Объединенные органические слои промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, давая 0,19 г указанного в заголовке соединения в виде золотисто-коричневого твердого вещества. Физические характеристики следующие: 1 52 плотно закрывают и нагревают при 180 С в течение 1 ч. Реакционную смесь охлаждают до комнатной температуры и распределяют между дихлорметаном, содержащим метанол, и разбавленной соляной кислотой. Водный слой экстрагируют дихлорметаном и объединенные органические слои промывают насыщенным раствором соли, сушат и концентрируют при пониженном давлении. Остаток адсорбируют диоксидом кремния и хроматографируют на диоксиде кремния, элюируя смесью, содержащей от 2 до 6% метанола в дихлорметане. Фракции,содержащие продукт, упаривают, получая 0,10 г указанного в заголовке соединения в виде золотисто-коричневого твердого вещества. Физические характеристики следующие: 1H ЯМР (300 МГц; ДМСО-d6) 10,2, 8,7, 8,6,8,2, 8,0, 7,4, 4,5, 3,7, 3,5, 1,3, 1,1; Масс-спектр (ESI) m/z 479 (М+Н+). Получение 21. 4-(4-Нитробензил)морфолин. В колбу, содержащую 4-нитробензилбромид (21,6 г) в сухом ацетоне (100 мл), добавляют карбонат калия (34,5 г) и морфолин (10 мл). Смесь нагревают при кипении с обратным холодильником в течение ночи с осушительной трубкой. Реакционную смесь распределяют между этилацетатом и водой и разделяют. Щелочной водный слой экстрагируют двумя дополнительными порциями этилацетата. Объединенные органические слои промывают насыщенным раствором соли, сушат и концентрируют при пониженном давлении, давая 21,3 г указанного в заголовке соединения в виде твердого вещества. Физические характеристики следующие: Т.пл. 75-79 С; 1H ЯМР (300 МГц, CDCl3)8,2, 7,6, 3,7,3,6, 2,4. Получение 22. 4-(4-Аминобензил)морфолин. К раствору 4-(4-нитробензил)морфолина из получения 21 (0,89 г) в этилацетате (10 мл) добавляют 5% платину-на-угле (0,04 г). Реакционную смесь встряхивают под давлением газообразного водорода 30 фунтов/кв.дюйм (206,843 КПа) в течение 1 ч. Смесь отфильтровывают,промывая этилацетатом. Фильтрат концентрируют при пониженном давлении, давая 0,71 г указанного в заголовке соединения в виде желтого твердого вещества. Физические характеристики следующие: 1N-циклопропил-4-(4 морфолинилметил)анилин. В колбу, содержащую 4-(4-аминобензил) морфолин из получения 22 (0,96 г), добавляют метанол (12 мл) и несколько дюжин сухих молекулярных сит (3). Смесь обрабатывают ук 53 сусной кислотой (3 мл), а затем [(1-этоксициклопропил)окси]триметилсиланом (1,25 мл). Через 15 мин реакционную смесь осторожно обрабатывают цианоборгидридом натрия (1,4 г) и нагревают при кипении с обратным холодильником в атмосфере азота в течение ночи. Реакционную смесь охлаждают до комнатной температуры, фильтруют, промывая метанолом, и концентрируют при пониженном давлении. Остаток разбавляют диэтиловым эфиром и промывают водным гидроксидом натрия (2 н.). Водный слой повторно экстрагируют один раз диэтиловым эфиром и один раз дихлорметаном. Объединенные органические слои промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток адсорбируют диоксидом кремния и хроматографируют на диоксиде кремния,элюируя смесью, содержащей от 2 до 8% метанола в дихлорметане. Фракции, содержащие продукт, объединяют и упаривают, давая 0,13 г указанного в заголовке соединения в виде розового твердого вещества. Физические характеристики следующие: 1H ЯМР (300 МГц, СDСl3)7,1, 6,8, 3,7,3,4, 2,4, 0,7, 0,5; Масс-спектр (ESI) m/z 233 (М+Н+). Получение 24. Диэтил 2-[циклопропил-4(4-морфолинилметил)анилино]метиленмалонат. В колбу, содержащую N-циклопропил-4(4-морфолинилметил)анилин (0,55 г) из получения 23, добавляют диэтилэтоксиметиленмалонат (0,45 мл) и пиридин (0,33 мл). Колбу плотно закрывают и нагревают при 145 С в течение 2 ч. Реакционную смесь охлаждают до комнатной температуры и подвергают азеотропной отгонке с толуолом при пониженном давлении (3 х). Остаток растворяют в дихлорметане и промывают насыщенным раствором соли, сушат и концентрируют при пониженном давлении. Остаток хроматографируют на диоксиде кремния, элюируя смесью, содержащей от 2 до 6% метанола в дихлорметане. Фракции, содержащие продукт,упаривают, получая 0,77 г указанного в заголовке соединения в виде масла. Физические характеристики следующие: 1 54 но]метиленмалонат из получения 24 (0,77 г) добавляют полифосфорную кислоту (4,4 г). Реакционную смесь плотно закрывают и нагревают до 120 С. Через 1 ч реакционную смесь охлаждают до комнатной температуры. Реакционную смесь осторожно добавляют к интенсивно перемешиваемой смеси дихлорметана и насыщенного водного бикарбоната. Слои отделяют и щелочной водный слой экстрагируют двумя дополнительными порциями дихлорметана. Объединенные органические слои промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток хроматографируют на диоксиде кремния, элюируя смесью, содержащей от 3 до 15% метанола в дихлорметане, давая 0,38 г указанного в заголовке соединения в виде желтого твердого вещества. Физические характеристики следующие: 1(5 мл) добавляют карбонат калия (0,21 г) и третбутилбромацетат (0,11 мл). После перемешивания в течение ночи, реакционную смесь разбавляют дихлорметаном и распределяют с водой. Органическую фазу промывают насыщенным раствором соли, сушат над сульфатом натрия,концентрируют при пониженном давлении и сушат в вакууме, получая 0,26 г указанного в заголовке соединения в виде белого твердого вещества. Физические характеристики следующие: 1(366 мг) из получения 5 и карбонат калия (276 мг) растворяют в ДМФ (5 мл), добавляют 2 бромпропан (470 мкл) и смесь нагревают при 100 С в течение 1 ч. Реакционную смесь остав 55 ляют охлаждаться до комнатной температуры,выливают в воду (25 мл) и экстрагируют этилацетатом (250 мл). Органический слой промывают насыщенным водным раствором соли(10 мл). Водный слой повторно экстрагируют этилацетатом (20 мл). Объединенные органические слои сушат (MgSO4) и концентрируют. Сырой продукт очищают колоночной хроматографией (EtOAc/гептан, от 1/1 до 1/0) и перекристаллизацией (EtOH), получая 70 мг (17%) указанного в заголовке соединения в виде белого твердого вещества. Физические характеристики следующие: Т.пл. 189-191 С разл. 1(366 мг) из получения 5 и карбонат калия (276 мг) растворяют в ДМФ (5 мл). Добавляют 2 иодбутан (575 мкл) и смесь нагревают при 100 С в течение 1 ч. Реакционную смесь оставляют охлаждаться до комнатной температуры,выливают в воду (25 мл) и экстрагируют этилацетатом (250 мл). Органический слой промывают насыщенным водным раствором соли(10 мл). Водный слой повторно экстрагируют этилацетатом (20 мл). Объединенные органические слои сушат (MgSO4) и концентрируют. Сырой продукт очищают колоночной хроматографией (дихлорметан/метанол, 100/1; 50/1; 20/1), давая 80 мг (19%) указанного в заголовке соединения в виде белого твердого вещества. Физические характеристики следующие: Т.пл. 200-201 С разл; 1N-4-Хлорбензил)-4-гидрокси-6-(3 гидрокси-1-пропинил)-8-метокси-3-хинолинкарбоксамид (300 мг) из получения 3 и карбонат калия (310 мг) растворяют в ДМФ (5 мл). Добавляют 2-иодбутан (345 мкл), и смесь нагревают при 120 С в течение 4 ч. Дополнительно добавляют 2-иодбутан (200 мкл) и карбонат калия(100 мг) и смесь нагревают в течение 16 ч. Реакционную смесь оставляют охлаждаться до комнатной температуры, выливают в воду (75 мл) и экстрагируют этилацетатом (350 мл). Органический слой промывают насыщенным водным раствором соли (10 мл). Водный слой повторно экстрагируют этилацетатом (20 мл). Объединенные органические слои сушат (МgSO4) и концентрируют. Сырой продукт очищают колоночной хроматографией (EtOAc/гептан, 30/1; 10/1), давая 60 мг (18%) указанного в заголовке соединения в виде белого твердого вещества. Физические характеристики следующие: Т.пл. 139-142 С разл.; 1(2,28 г) в ДМФ (75 мл) добавляют гидрид натрия (60% дисперсия в масле; 0,600 г) с последующим добавлением 2-бензилоксиэтанола(1,42 мл). Реакционную смесь нагревают до 135 С и перемешивают в течение 1 ч. Реакционную смесь охлаждают до комнатной температуры и выливают в насыщенный водный раствор хлорида аммония (200 мл). Водный слой экстрагируют дихлорметаном (4100 мл). Объединенные органические слои промывают насыщенным раствором соли (50 мл), сушат MgSO4,фильтруют и концентрируют в вакууме. Полученное желтое твердое вещество очищают колоночной хроматографией(дихлорметан/ метанол, 98/2). Фракции, гомогенные по ТСХ, 57 объединяют и концентрируют в вакууме, получая желтое твердое вещество, которое перекристаллизовывают из этанола, получая 1,568 г(53%) промежуточного амида в виде не совсем белого твердого вещества. К суспензии этого вещества (1,149 г) в диэтиламине (24 мл) добавляют иодид меди (0,111 г) и Pd(PPh3)2Cl2 (0,069 г) с последующим добавлением пропаргилового спирта (0,16 мл). Реакционную смесь перемешивают при комнатной температуре в течение 3 дней. Реакционную смесь концентрируют в вакууме и распределяют между H2O (50 мл) и дихлорметаном (50 мл). Водный слой экстрагируют дихлорметаном (350 мл). Объединенные органические слои промывают насыщенным водным раствором хлорида аммония (50 мл),сушат МgSO4, фильтруют и концентрируют в вакууме. Полученное коричневое твердое вещество очищают колоночной хроматографией (дихлорметан/метанол, 98/2). Фракции, гомогенные по ТСХ, объединяют и концентрируют в вакууме, получая золотисто-коричневое твердое вещество, которое перекристаллизовывают из этанола, получая 0,181 г (18%) пропаргилового соединения в виде золотисто-коричневого кристаллического твердого вещества. К раствору этого вещества (0,394 г) в ДМФ (3 мл) добавляют карбонат калия (0,317 г), а затем иодметан(0,14 мл). Реакционную смесь нагревают до 90 С и перемешивают в течение 18 ч. Реакционную смесь концентрируют в вакууме и полученный остаток очищают колоночной хроматографией (дихлорметан; дихлорметан/метанол,98/2). Фракции, гомогенные по ТСХ, объединяют и концентрируют в вакууме, получая желтое твердое вещество, которое перекристаллизовывают из EtOH, получая 0,273 г (67%) Nметилпиридона в виде желтого твердого вещества. Пиридон (0,350 г) растворяют в 1/1 дихлорметан/этанол (100 мл) и гидрируют над 10% Pd/C (53 мг) при 35 фунтах/кв.дюйм(241,316 КПа) в течение 18 ч. Реакционную смесь отфильтровывают через слой целита и фильтрат концентрируют в вакууме. Полученное желтое масло растворяют в метаноле (60 мл) и гидрируют над палладиевой чернью (35 мг) в течение 4 ч. Реакционную смесь фильтруют через слой целита, и фильтрат концентрируют в вакууме. Полученное желтое масло очищают колоночной хроматографией (дихлорметан/метанол, 98/2; 95/5). Фракции, гомогенные по ТСХ, объединяют и концентрируют в вакууме, получая бледно-желтое твердое вещество,которое перекристаллизовывают из этилацетата,получая 0,104 г (35%) указанного в заголовке соединения в виде бледно-желтого твердого вещества. Физические характеристики следующие: Т.пл. 175-179 С;(2,28 г) в ДМФ (75 мл) добавляют гидрид натрия (60% дисперсия в масле; 0,600 г) с последующим добавлением 1,3-дибензилокси-2 пропанола (2,47 мл). Реакционную смесь нагревают до 135 С и перемешивают в течение 2 ч. Реакционную смесь охлаждают до комнатной температуры и выливают в насыщенный водный раствор хлорида аммония (200 мл). Водный слой экстрагируют CH2Cl2 (4100 мл). Объединенные органические слои промывают насыщенным раствором соли (50 мл), сушат MgSO4,фильтруют и концентрируют в вакууме. Полученное коричневое масло очищают колоночной хроматографией (дихлорметан/метанол, 98/2). Смешанные фракции объединяют и повторно очищают (этилацетат/гептан, 1/1). Фракции,гомогенные по ТСХ, объединяют и концентрируют в вакууме, получая желтое твердое вещество, которое перекристаллизовывают из этилацетата, получая 1,701 г (48%) промежуточного амида в виде бледно-желтого твердого вещества. К суспензии этого вещества (1,330 г) в диэтиламине (23 мл) добавляют иодид меди (0,107 г) и Рd(РРh3)2 Сl2 (0,066 г) с последующим добавлением пропаргилового спирта (0,15 мл). Реакционную смесь перемешивают при комнатной температуре в течение 18 ч. Реакционную смесь концентрируют в вакууме. Полученное коричневое твердое вещество очищают колоночной хроматографией (дихлорметан, дихлорметан/метанол, 98/2). Фракции, гомогенные по ТСХ, объединяют и концентрируют в вакууме,получая оранжевое твердое вещество, которое перекристаллизовывают из смеси диэтиловый 59 эфир/этилацетат, получая 0,727 г (61%) пропаргилового производного в виде не совсем белого твердого вещества. К раствору данного вещества (0,500 г) в ДМФ (3 мл) добавляют карбонат калия (0,325 г), затем добавляют иодметан (0,15 мл). Реакционную смесь нагревают до 90 С и перемешивают в течение 18 ч. Реакционную смесь концентрируют в вакууме и остаток очищают колоночной хроматографией (дихлорметан/метанол, 98/2). Фракции, гомогенные по ТСХ, объединяют и концентрируют в вакууме,получая желтое твердое вещество, которое перекристаллизовывают из смеси этилацетат/метанол, получая 0,383 г (75%) Nметилпиридона в виде желтого твердого вещества. Раствор пиридона (0,310 г) в смеси 1/1 дихлорметан/этанол (30 мл) гидрируют над 10%(241,316 КПа) в течение 5,5 ч. Реакционную смесь фильтруют через слой целита и фильтрат концентрируют в вакууме. Полученное желтое масло очищают колоночной хроматографией(дихлорметан/метанол; 98/2, 95/5, 90/10). Фракции, гомогенные по ТСХ, объединяют и концентрируют в вакууме, получая бледно-желтое твердое вещество, которое перекристаллизовывают из смеси этилацетат/метанол, получая 0,050 г (22%) указанного в заголовке соединения в виде белого твердого вещества. Физические характеристики следующие: Т.пл. 120-123 С; 1 К суспензии NaH (60% дисперсия в масле,11,1 мг) в 2,5 мл безводного ДМФ добавляют N(4-хлорбензил)-8-фтор-4-гидрокси-6-(гидроксиметил)-3-хинолинкарбоксамид из получения 7(100 мг). После перемешивания реакционной смеси при комнатной температуре в течение 1520 мин добавляют 2-(3-бромпропокси)тетрагид 003945 60 ро-2 Н-пиран (89,4 мг). Реакционную смесь перемешивают при комнатной температуре в течение 3 дней. Реакционную смесь обрабатывают насыщенным водным раствором NаНСО 3, затем экстрагируют CH2Cl2 (3 х). Объединенные органические слои промывают 15%-ным К 2 СО 3 и Н 2 О (2 х), сушат над Na2SO4 и конденсируют,получая желтый остаток. Остаток хроматографируют, элюируя 2% МеОН в СН 2 Сl2. Фракции,гомогенные по ТСХ, объединяют и конденсируют, давая 34,0 мг (24%) указанного в заголовке соединения в виде белого твердого вещества. Физические характеристики следующие: Т.пл. 148-150 С; 1(0,78 г) и гидрохлорид N-(2-хлорэтил)морфолина (0,52 г). Смесь нагревают при 90 С в течение 2 ч и затем распределяют между водой и хлороформом. Органический слой концентрируют в вакууме, получая коричневое масло. Колоночная хроматография (элюирование 1-7% МеОН/СНСl3) с последующей кристаллизацией из смеси EtOAc/гексан давали указанное в заголовке соединение в виде смеси изомеров. Затем смесь очищают с помощью ВЭЖХ хроматографии на колонке 0,4625 см Chiralcel OD-H,элюируя EtOH при скорости потока 0,5 мл/мин. Это давало 0,161 г смеси алкенов в виде смеси с соотношением приблизительно 2:1 транс:цисизомеров, которые кристаллизовали из этилацетата, получая 13 г указанного в заголовке соединения в виде гидрата. Физические характеристики следующие: Т.пл. 146-148,5 С; 1
МПК / Метки
МПК: A61P 31/12, C07D 215/16, A61K 31/47
Метки: качестве, противовирусных, хинолинкарбоксамиды, агентов
Код ссылки
<a href="https://eas.patents.su/30-3945-hinolinkarboksamidy-v-kachestve-protivovirusnyh-agentov.html" rel="bookmark" title="База патентов Евразийского Союза">Хинолинкарбоксамиды в качестве противовирусных агентов</a>
Предыдущий патент: Способы лечения диабета с помощью пептидных аналогов инсулина
Следующий патент: Бицикло [2.2.1] гептаны и родственные соединения